PENAMBAHAN
ASCORBYL PHOSPHATE
MAGNESIUM
SEBAGAI SUMBER VITAMIN C DAN
IMPLANTASI DENGAN ESTRADIOL-17
β
HENGKY JULIUS SINJAL
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa disertasi dengan judul “ Kajian
Penampilan Reproduksi Induk Ikan Lele (Clarias gariepinus) Betina melalui
Penambahan Ascorbyl Phosphate Magnesium sebagai Sumber Vitamin C pada Pakan
dan Implantasi Estradiol-17
β
”
adalah karya saya sendiri dengan arahan komisi
pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi di
mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan
maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan
dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Bogor, Agustus 2007
Hengky Julius Sinjal
gariepinus) betina melalui Penambahan Ascorbyl Phosphate Magnesium Sebagai
Sumber Vitamin C pada Pakan dan Implantasi Estradiol-17
β
. Komisi
Pembimbing: M. Zairin Jr, R. Affandi, B. Purwantara, dan W. Manalu.
Penelitian ini dilakukan untuk menentukan pengaruh kombinasi
ascorbyl
phosphate magnesium sebagai sumber vitamin C dan implantasi estradiol-17
β
pada
kecepatan pematangan gonad, kualitas telur, dan larva ikan lele (Clarias gariepinus).
Dalam percobaan ini ikan diberikan beberapa kombinasi perlakuan yang terdiri atas 2
faktor, yaitu penambahan ascorbyl phosphate magnesium pada pakan dengan dosis
0, 600, 1200, dan 1800 mg/kg pakan dan implantasi estradiol 17-
β
dengan dosis 00,
250, dan 500
μ
g/kg induk ikan, sehingga jumlah kombinasi perlakuan adalah 12.
Delapan belas ekor induk dengan berat 250–328 gr ditebar ke dalam jaring apung
(3X2X2m) untuk satu perlakuan sehingga terdapat 12 buah jaring apung dengan total
induk ikan berjumlah 216 ekor. Pakan diberikan dua kali sehari secara at satiation.
Pemeriksaan kematangan gonad dilakukan dua minggu sekali dengan
menggunakan metode kanulasi, bersamaan waktunya dilakukan pengambilan sampel
darah dengan menggunakan spuit 2.5 ml yang berheparin untuk keperluan analisis
kandungan estradiol plasma darah. Induk yang telah matang gonad diinjeksi dengan
ovaprim sebanyak 2 kali untuk memacu ovulasi. Telur-telur yang dihasilkan oleh
induk betina ditetaskan di akuarium, kemudian dihitung daya tetas telurnya, dan
persentase larva abnormal yang dihasilkan induk tersebut. Ketahanan larva diuji
dengan memelihara larva sebanyak 100 ekor tanpa diberi makan. Larva diamati setiap
hari dan mortalitasnya dicatat. Jika larva yang hidup tinggal 20 ekor (20%) maka
pengamatan larva diakhiri. Kandungan vitamin C, protein, fosfolipid, lemak, prolin,
dan hidroksiprolin dianalisis pada ovarium, telur, larva 0 hari, dan larva 2 hari.
Berdasarkan evaluasi kombinasi penambahan
ascorbyl phosphate magnesium
dan implantasi estradiol pada induk ikan lele memperlihatkan respons nyata pada
kinerja penampilan reproduksi yang meliputi kecepatan pematangan gonad, indeks
gonad somatik, fekunditas relatif, daya tetas telur, ketahanan hidup larva, dan larva
abnormal yang dihasilkan. Kombinasi yang terbaik untuk mempercepat pematangan
gonad dan memperbaiki kualitas telur dan larva adalah kombinasi penambahan
ascorbyl phosphate magnesium 1200 mg/kg pada pakan dan implantasi estradiol-17
β
dengan dosis 250
μ
g/kg. Dengan semakin meningkatnya penambahan ascorbyl
phosphate magnesium pada pakan menghasilkan peningkatan kandungan vitamin C
pada telur sehingga menghasilkan ketahanan hidup larva yang tinggi dan mengurangi
larva abnormal.
Catfish (Clarias gariepinus) with Supplemeted by Ascorbyl Phosphate
Magnesium as a Source of Vitamin C in Diets and Implanted with
Estradiol-17
β
. Advisors: M. Zairin Jr, R. Affandi, B. Purwantara, dan W. Manalu.
The experiment was conducted to determine the effect of dietary ascorbyl
phospahate magnesium as a source of vitamin C and implanted with estradiol-17
β
on the gonad maturation, egg and larva quality of African Catfish Clarias
gariepinus. Fish were treated by various combinations of dietary dosage of
ascorbyl phosphate magnesium (0, 600, 1200, and 1800 mg/kg of feed) and
estradiol-17
β
(00, 250, and 500
μ
g/kg). Two hundreds sixteen and eighteen pairs of
broodstock fish were used for this experiment. Fish were fed with the experimental
diets two times a day at satiation. The gonad somatic index, egg diameter, fecundity,
hatching rate of the eggs, survival rate, and percentage of abnormal larvae were
determined. Results of the experiment indicated that supplementation of ascorbyl
phosphate magnesium and estradiol-17
β
stimulated gonad development and increased
hatching rate, fecundity and survival rate, and reduced percentage of abnormal larvae.
Combination of ascorbyl phosphate magnesium 1200 mg/kg feed and estradiol-17
β
250
μ
g/kg gave the best reproductive performance.
Key word : African Catfish Clarias gariepinus, Ascorbyl phosphate magnesium,
estradiol-17
β
, reproduction performance
Hak cipta milik Institut Pertanian Bogor tahun 2007
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencamtumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian,
penulisan karya ilmiah, penyusunan laporan, penulisan kritik
atau tinjauan suatu masalah
PENAMBAHAN
ASCORBYL PHOSPHATE
MAGNESIUM
SEBAGAI SUMBER VITAMIN C DAN
IMPLANTASI DENGAN ESTRADIOL-17
β
HENGKY JULIUS SINJAL
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar
Doktor pada
Departemen Budidaya Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
implantasi dengan estradiol-17
β
Nama
: Hengky Julius Sinjal
Nomor Pokok
: C061020041
Disetujui
Komisi Pembimbing
Prof. Dr. Ir. Muhammad Zairin Jr., M.Sc. Dr. Ir. Ridwan Affandi, DEA
Ketua
Anggota
Dr. drh. Bambang Purwantara, M.Sc Prof. Dr. Ir. Wasmen Manalu
Anggota Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana
Ilmu Perairan
Prof. Dr. Ir. H. Enang Harris, MS. Prof. Dr. Ir. Khairil Anwar Notodiputro, MS.
karena hanya dengan berkat anugerah-Nya penulis dapat menyelesaikan penulisan
disertasi ini. Peningkatan produksi perikanan dan peningkatan kualitas dan kuantitas
benih ikan merupakan issue yang mendasari penelitian ini, dengan judul ” Kajian
Penampilan Reproduksi Induk Ikan Lele (Clarias gariepinus) Betina Melalui
Penambahan Ascorbyl Phosphate Magnesium Sebagai Sumber Vitamin C pada Pakan
dan Implantasi Estradiol-17
β
”
Pada kesempatan ini penulis menyampaikan ucapan terima kasih kepada Bapak
Prof. Dr. M. Zairin Jr., M.Sc sebagai ketua komisi pembimbing, Bapak Dr. Ridwan
Affandi, DEA dan Bapak Dr. Drh. Bambang Purwantara, M.Sc, Bapak Prof. Dr. Ir.
Wasmen Manalu sebagai anggota komisi pembimbing yang telah memberikan
nasihat, petunjuk dan bimbingan yang sangat berharga selama proses penelitian
sampai dengan penyelesaian studi. Terima kasih kepada Prof. Dr. Enang Harris, MS.
Ketua Program Studi Ilmu Perairan dan DR. Chairul Muluk mantan Ketua Program
Studi Ilmu Perairan yang terus memberikan motivasi dan nasehat agar penulis cepat
menyelesaikan studi.
Terima kasih dan penghargaan disampaikan kepada pimpinan Universitas Sam
Ratulangi, dan Fakultas Perikanan dan Ilmu Kelautan, Manado yang telah
memberikan kesempatan kepada penulis untuk melanjutkan pendidikan. Terima kasih
dan penghargaan juga disampaikan kepada pimpinan Institut Pertanian Bogor dan
Sekolah Pascasarjana, yang telah menerima penulis untuk belajar dan menyelesaikan
studi di lembaga ini.
Pada kesempatan ini saya sampaikan ucapan terima kasih kepada Departemen
Pendidikan Nasional Republik Indonesia, pemerintaha daerah Sulawesi Utara, dan
yayasan mandiri atas bantuan dana penelitian dan penulisan disertasi.
Terima kasih juga disampaikan kepada Kepala Balai Riset Perikanan Budidaya
Air Tawar, Departemen Kelautan dan Perikanan yang telah mengizinkan penulis
bantuan tenaga teknis lapangan selama saya melakukan penelitian.
Banyak pihak yang telah membantu dan mendukung penulis selama proses
perkuliahan, penelitian sampai penulisan disertasi; oleh karena itu ucapan terima
kasih disampaikan kepada: staf administrasi dan perpustakaan Departemen Budidaya
Perairan: Yuli, Hani, Asep, dan
Dessy
; teknisi laboratorium: Ibu Lina, Bapak Wasjan,
Bapak Ranta. Teman-teman di Program Studi Ilmu Perairan: Suradi, Gunarto
Lantama, Surya Darwisito, Bambang utomo, Yulfiperius, dan Adharto Utiah;
Rekan-rekan di Bogor: Anderson Kumenaung, Orbanus Naharia, Nurdin Jusuf, Ridwan
Lasabuda, Agung Windarto, Alfret Luasunaung, Adnan Wantasen, Edwin Ngangi,
Donata Pandin, Tommy Lolowang, Hasnawaty, Joice Rimper, Jack Mamangkey,
Deny Karwur, Erly Kaligis, Hengky Manoppo, Teo Lasut, Ari Mirah, dan Yosep
Karamoy.
Terima kasih kepada Ayahanda Hendrik Petrus Sinjal (Alm) dan Ibunda
Eleonora Lumintang, adik-adik, kakak-kakak, adik-adik ipar dan kakak-kakak ipar,
atas bantuan doa dan dana dalam penyelesaian studi penulis.
Secara khusus dengan segala ketulusan hati, saya sampaikan terima kasih
kepada istriku dan anakku yang tercinta Joshua Nirai Okinawa Sinjal dan Hideyuki
William Michael Sinjal yang merupakan sumber inspirasi saya dan dengan penuh
pengertian, kesabaran, dan rela ditinggal lama tanpa didampingi secara fisik oleh
penulis sebagai seorang ayah.
Penulis menyadari bahwa apa yang penulis lakukan masih belum memadai
karena keterbatasan waktu dan dana. Oleh karena itu kritik dan saran penyempurnaan
selanjutnya penulis sangat dihargai. Diharapkan apa yang penulis lakukan dapat
bermanfaat dalam memacu perkembangan teknologi pembenihan ikan di Indonesia.
Bogor, Agustus 2007
Penulis dilahirkan di Manado pada tanggal 19 Juli 1958 sebagai anak dari
pasangan Bapak Hendrik Petrus Sinjal (Alm) dan Ibu Eleonora Lumintang. Penulis
menyelesaikan pendidikan sekolah dasar di Manado pada tahun 1970, sedangkan
pendidikan menengah tingkat pertama dan menengah tingkat atas jurusan IPA
diselesaikan masing-masing pada tahun 1973 dan 1976.
Pendidikan sarjana ditempuh pada Program Studi Budidaya Perairan, Fakultas
Perikanan Universitas Sam Ratulangi, Manado masuk pada tahun 1977 dan selesai
pada tahun 1985. Pada tahun 1991 penulis melanjutkan studi ke program Master
Science pada Program Studi Marine Biology, University of the Ryukyus Okinawa
Jepang dan selesai pada tahun 1993. Sejak tahun 1986 penulis telah bekerja sebagai
staf pengajar pada Fakultas Perikanan dan Ilmu Kelautan, Universitas Sam Ratulangi,
Manado. Pada tahun 1995 penulis menikah dengan Ir. Jeane Rimber Indy MSc dan
dikaruniai dua orang anak Joshua Okinawa Nirai Sinjal dan Hideyuki Michael
William Sinjal.
Pada tahun 2002 penulis diberi kesempatan mengikuti program doktor pada
Program Studi Ilmu Perairan, Sekolah Pascasarjana Institut Pertanian Bogor, dengan
bantuan dana beasiswa pendidikan pascasarjana yang diperoleh dari Departeman
DAFTAR GAMBAR...
DAFTAR LAMPIRAN...
xi
xii
I
PENDAHULUAN...
1
Latar Belakang... ...
Perumusan Masalah...
Tujuan dan Manfaat...
Hipotesis...
1
4
6
6
II
TINJAUAN PUSTAKA... 7
Kematangan Gonad Ikan...
Vitelogenesis...
Peranan Vitamin C pada Reproduksi Ikan...
Peranan Estradiol-17
β
pada Reproduksi Ikan...
Kualitas Telur Ikan...
Kerangka Teoretis...
7
10
12
15
17
19
III
METODE PENELITIAN... 22
Waktu dan Tempat Penelitian...
Bahan dan Alat...
Metode Penelitian...
Pelaksanaan Penelitian...
Analisis Data...
22
22
24
26
30
IV
HASIL DAN PEMBAHASAN... 31
Hasil...
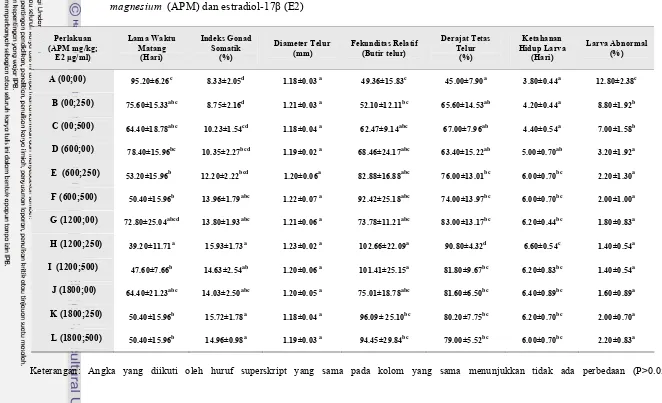
Kecepatan Pematangan Gonad, Indeks Gonad Somatik, Diameter
Telur...
Fekunditas, Daya Tetas Telur, Ketahanan Hidup Larva, dan
Keabnormalan Larva...
Kadar Estradiol-17
β
dalam Plasma Darah...
Kandungan Vitamin C Ovarium, Telur, dan Larva...
Kandungan Protein Telur, dan Larva...
Kandungan Lemak, Telur dan Larva...
Rasio Hidroksiprolin/Prolin Ovarium dan Larva...
Pembahasan...
31
31
37
41
43
46
47
48
50
V
KESIMPULAN DAN SARAN...
69
Tabel Halaman
1
Komposisi pakan dengan penambahan ascorbyl phosphate magnesium 0,
600, 1200, dan 1800 mg/kg pakan...
23
2 Komposisi proksimat pakan dengan penambahan ascorbyl phosphate
magnesium 0, 600, 1200, dan 1800 mg/kg pakan...
24
3
Perlakuan berbagai kombinasi penambahan ascorbyl phosphate magnesium
dan implantasi estradiol-17
β
...
24
4
Kualitas air selama percobaan...
27
1
Proses vitelogenesis pada ikan (Aida et al., 1991)...
16
2 Wadah penelitian yang terbuat dari bambu dengan 12 jaring apung dengan
ukuran 3 X 2 X 2 m yang di atasnya ditutupi dengan jaring...
23
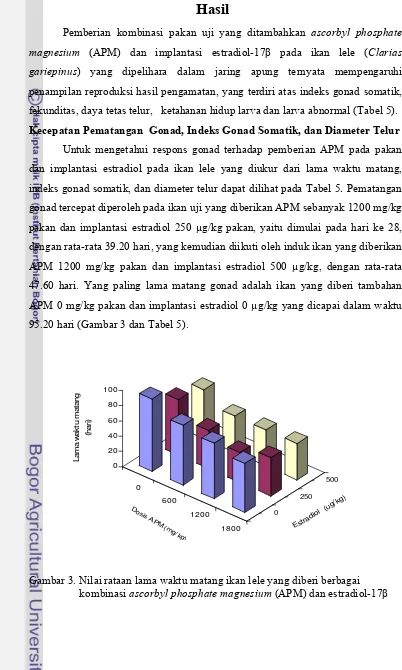
3 Nilai rataan lama waktu matang ikan lele yang diberi berbagai kombinasi
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
31
4 Nilai rataan indeks gonad somatik ikan lele yang diberi berbagai
kombinasi ascorbyl phosphate magnesium (APM) dan hormon
estradiol-17
β
...
34
5 Nilai rataan diameter telur ikan lele yang diberi berbagai kombinasi
ascorbyl phosphate magnesium (APM) dan hormon estradiol-17
β
...
35
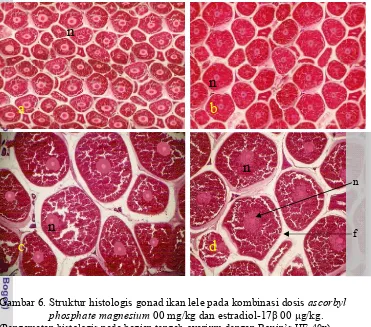
6 Struktur histologi gonad ikan lele pada kombinasi dosis ascorbyl
phosphate magnesium 00 mg/kg dan hormon estradiol-17
β
00
μ
g/ml...
36
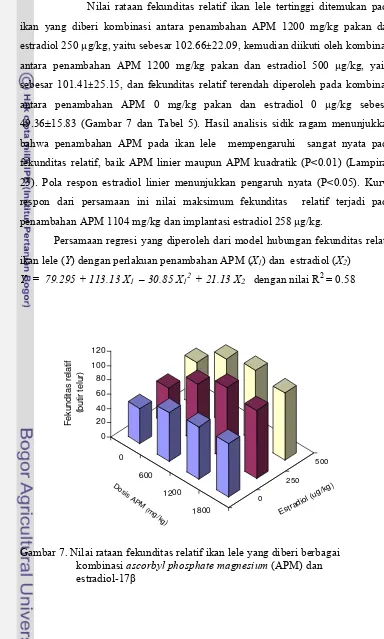
7 Nilai
rataan
fekunditas relatif ikan lele yang diberi berbagai kombinasi
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
37
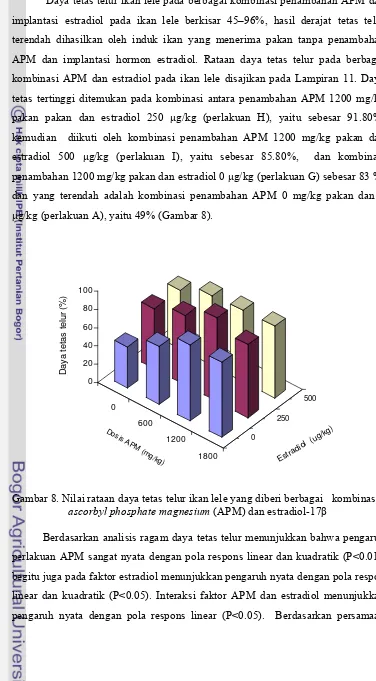
8 Nilai rataan daya tetas telur ikan lele yang diberi berbagai kombinasi
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...;...
38
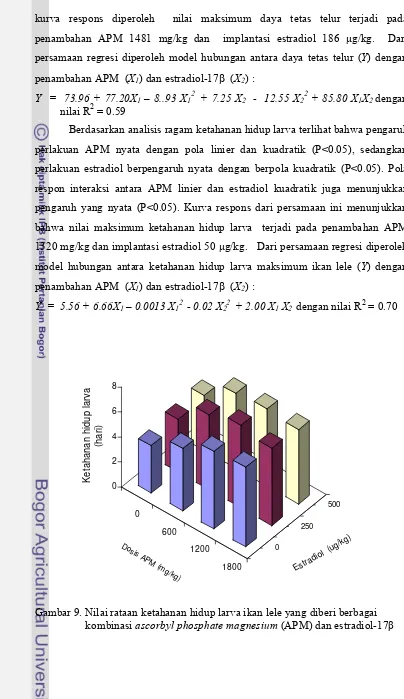
9 Nilai rataan ketahanan hidup larva ikan lele yang diberi berbagai
kombinasi
ascorbyl phosphate magnesium (APM) dan
estradiol-17
β
...
39
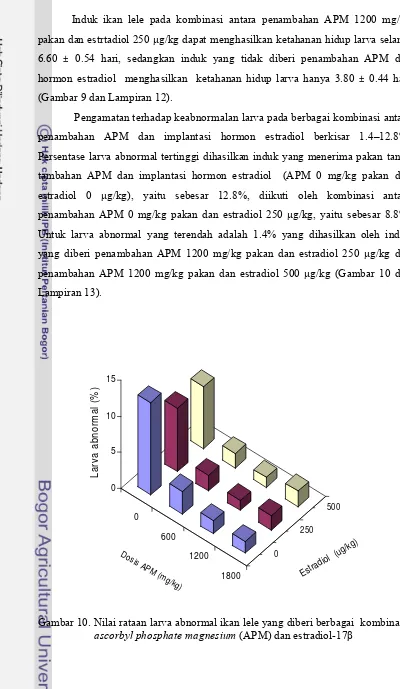
10 Nilai rataan larva abnormal ikan lele yang diberi berbagai kombinasi
ascorbyl phosphate magnesium (APM) dan estradiol 17
β
...
40
11 Gambaran morfologis larva: normal (a) abnormal (b, c, dan, d) dari hasil
penetasan induk ikan lele (Clarias gariepinus)...
41
12 Kadar
estradiol-17
β
plasma darah ikan lele pada berbagai kombinasi
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
selama
percobaan...
42
13 Nilai kandungan vitamin C pada ovarium, telur, larva 0 hari, dan larva 2
hari ikan lele yang diberi berbagai kombinasi ascorbyl phosphate
magnesium (APM) dan estradiol-17
β
...
43
14 Nilai kandungan protein pada telur, larva 0 hari, dan larva 2 hari ikan lele
yang diberi berbagai kombinasi ascorbyl phosphate magnesium (APM)
dan estradiol-17
β
...
45
15 Nilai kandungan vitamin C ovarium ikan lele pada hari ke 0, 42, dan 98
yang diberi berbagai kombinasi ascorbyl phosphate magnesium (APM)
17 Nilai rasio hidroksiprolin/prolin (HP/P) pada telur, larva 0 hari, dan larva
2 hari ikan lele yang diberi berbagai kombinasi ascorbyl phosphate
Lampiran
Halaman
1 Komposisi
vitamin mix dan mineral mix………... 79
2
Cara pembuatan pelet hormon estradiol-17
β
...…... 80
3
Prosedur penyiapan preparat histologi gonad... 81
4 Prosedur
radioimmunoassai……….. 84
5 Prosedur
analisis
lipida nonpolar (Takeuchi, 1988)…..………..……
85
6
Prosedur analisis vitamin C dengan alat HPLC (Schuep et al. 1994).
86
7
Nilai lama waktu matang ikan lele yang diberi berbagai kombinasi
dosis ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
87
8
Nilai indeks gonad somatik ikan lele yang diberi berbagai kombinasi
dosis ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
87
9
Nilai diameter telur ikan lele yang diberi berbagai kombinasi dosis
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
88
10 Nilai fekunditas ikan lele yang diberi berbagai kombinasi dosis
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
88
11
Nilai derajat tetas telur ikan lele yang diberi berbagai kombinasi dosis
ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
89
12
Nilai ketahanan hidup larva ikan lele yang diberi berbagai kombinasi
dosis ascorbyl phosphate magnesium (APM) dan estradiol-17
β
...
89
13 Nilai larva abnormal ikan lele yang diberi berbagai kombinasi dosis
ascorbyl phosphate magnesium (APM) dan hormon estradiol-17
β
...
90
14 Kandungan vitamin C ovarium ikan lele pada hari ke 0, 42, dan 98
yang diberi berbagai kombinasi dosis ascorbyl phosphate magnesium
(APM) dan estradiol-17
β
...
90
15
Nilai rataan kadar estradiol (ng/ml) plasma darah ikan lele yang diberi
berbagai kombinasi ascorbyl phosphate magnesium (APM) dan
estradiol yang diambil setiap dua minggu selama 98 hari...
91
16 Kandungan vitamin C pada ovarium, telur, larva 0, dan larva 2 hari
ikan lele yang diberi berbagai kombinasi ascorbyl phosphate
magnesium (AMP) dan implantasi estradiol-17
β
...
92
17
Kandungan protein pada telur, larva 0, dan larva 2 hari ikan lele yang
diberi berbagai kombinasi ascorbyl phosphate magnesium
(AMP) dan
implantasi estradiol-17
β
...
92
20
Analisis ragam lama waktu matang ikan lele...
94
21
Analisis ragam indeks kematangan gonad ikan lele...
94
22 Analisis
ragam
diameter telur ikan lele...
95
23 Analisis
ragam
fekunditas telur ikan lele...
95
24
Analisis ragam daya tetas telur ikan lele...
96
25
Analisis ragam ketahanan hidup larva ikan lele...
96
26
Analisis ragam larva abnormal ikan lele...
97
27
Analisis ragam kandungan estradiol plasma darah ikan lele
berdasarkan waktu pengamatan...
98
28 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 00 mg/kg dan estradiol 00
μ
g/kg………....
99
29 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 00 mg/kg dan estradiol 250
μ
g/kg…………..…………...
100
30 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 00 mg/kg dan estradiol 500
μ
g/kg………...……….
101
31 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 600 mg/kg dan estradiol 00
μ
g/kg………...
102
32 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 600 mg/kg dan estradiol 250
μ
g/kg……….
103
33 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 600 mg/kg dan estradiol 500
μ
g/kg……….
104
34 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 1200 mg/kg dan estradiol 00
μ
g/kg………..……...
105
35 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 1200 mg/kg dan estradiol 250
μ
g/kg……….…………...
106
36 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 1200 mg/kg dan estradiol 500
μ
g/kg………...
107
37 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 1800 mg/kg dan estradiol 00
μ
g/kg………..……...
108
38 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 1800 mg/kg dan estradiol 250
μ
g/kg……..……….
109
39 Sebaran diameter telur ikan lele yang diberi ascorbyl phosphate
magnesium 1800 mg/kg dan estradiol 500
μ
g/kg……….………..
110
Penguji Luar komisi ujian tertutup: Prof. Dr. Ir. Ing Mokoginta, MS
I.
PENDAHULUAN
Latar Belakang
Salah satu usaha yang mutlak dibutuhkan untuk mengembangkan budi daya ikan
adalah penyediaan benih yang bermutu dalam jumlah yang memadai dan waktu yang
tepat. Selama ini usaha ke arah tersebut telah dilakukan, namun belum berhasil dengan
baik. Kekurangan persediaan benih yang bermutu dalam jumlah dan waktu yang tepat
disebabkan oleh belum optimalnya penanganan induk dan larva yang dihasilkan.
Perbaikan kualitas dan kuantitas telur melalui perbaikan kualitas pakan induk
merupakan alternatif dalam upaya mengatasi masalah tersebut. Kandungan nutrisi
pakan ikan adalah salah satu faktor penentu dalam perkembangan oosit, terutama pada
awal perkembangan telur.
Informasi kebutuhan nutrisi untuk ikan-ikan budi daya yang tersedia umumnya
hanya sebatas kebutuhan nutrien makro, seperti lemak dan protein, sedangkan
informasi kebutuhan mikro nutrien, seperti vitamin dan mineral, masih sangat terbatas.
Selain itu, penggunaan mikro nutrien ini dalam ransum pakan induk hanya mengacu
kepada kebutuhan ransum secara umum untuk pertumbuhan. Dalam kondisi seperti ini,
sulit mengembangkan teknologi produksi benih berkualitas secara massal. Berbagai
penelitian membuktikan bahwa kualitas pakan termasuk nutrien mikro yang
merupakan faktor penting yang berhubungan erat dengan kematangan gonad, jumlah
telur yang diproduksi, dan kualitas telur dan larva (Watanabe 1988).
Kualitas telur merupakan refleksi keadaan kimia nutrisi kuning telur yang sangat
dipengaruhi oleh kesehatan dan gizi pakan yang diterima oleh induk Blaxter (1969).
Beberapa nutrien mikro maupun asam-asam lemak esensial yang terkandung dalam
ransum pakan ikan akan diakumulasikan dalam telur untuk digunakan sebagai energi
maupun senyawa pembentuk jaringan tubuh selama proses perkembangan embrio
(embriogenesis) maupun larva. Saat telur menetas, sumber energi untuk perkembangan
larva ikan sangat bergantung pada material bawaan telur yang telah disiapkan oleh
induk dan fase ini merupakan fase yang paling kritis. Material telur yang mengalami
defisiensi gizi akan menimbulkan gangguan dalam perkembangan larva dan akhirnya
Keberadaan nutrien dalam telur ini merupakan akumulasi nutrien pada fase
pematangan gonad. Secara alamiah proses vitelogenesis memerlukan interaksi faktor
eksternal dan internal. Faktor eksternal yang mempengaruhi vitelogenesis antara lain
temperatur, naik turunnya permukaan air, curah hujan, debit air, feromon, dan pakan.
Pakan induk yang dapat mempengaruhi vitelogenesis adalah pakan yang berkualitas,
yaitu pakan yang mengandung protein, lemak, vitamin E, vitamin C, dan mineral yang
sesuai dengan kebutuhan ikan sebagai bahan pembentuk vitelogenin. Faktor internal
adalah ketersediaan hormon-hormon steroid, gonad terutama estradiol-17β dalam
tingkat yang dapat merangsang vitelogenesis.
Dalam upaya untuk lebih meningkatkan kualitas telur dan larva ikan lele, perlu
diadakan perbaikan pengelolaan reproduksi dengan cara mempercepat kematangan
gonad melalui penggunaan hormon eksogen dan perbaikan nutrisi induk terutama
kebutuhan akan vitamin C. Informasi kebutuhan vitamin C saat siklus reproduksi serta
pengaruhnya pada perkembangan ovarium dan perkembangan larva ikan lele belum
ada, padahal informasi ini sangat bermanfaat dalam penyusunan ransum yang tepat
untuk induk ikan lele sehingga dapat digunakan untuk memperbaiki penampilan
reproduksi ikan tersebut.
Vitamin C merupakan salah satu nutrien mikro yang dibutuhkan oleh induk ikan
dalam proses reproduksi. Hal ini didasarkan pada adanya fluktuasi kandungan vitamin
C ovarium selama berlangsungnya siklus reproduksi pada beberapa spesies ikan dan
udang yang ditangkap di alam seperti pada udang Palaemon serratus (Guary et al.
1975), ikan Carassius carassius (Saeymour 1981), Godus morhua (Agrawal dan
Mahajan 1980; Sandnes dan Braekkan 1981), Oreochromis sp (Azwar 1997).
Kandungan vitamin C dalam ovarium akan meningkat pada awal perkembangannya
dan kemudian menurun pada fase akhir sebelum ovulasi. Ikan tidak mampu
mensintensis vitamin C (Faster dalam Sandnes 1991) sehingga untuk mempertahankan
metabolisme sel, vitamin C mutlak harus diperoleh dari luar tubuh karena tidak terdapat
enzim L-gulonolakton oksidase yang dibutuhkan untuk biosintesis vitamin C
(Dabrowski 2002).
Peran pakan dalam perkembangan gonad penting untuk fungsi endokrin yang
normal. Tingkat pemberian pakan tampaknya mempengaruhi sintesis maupun
karena kekurangan pakan mungkin dapat menyebabkan kadar gonadotropin rendah
yang dihasilkan oleh kelenjar adenohipofisis, respons ovari yang kurang atau mungkin
kegagalan ovari untuk menghasilkan jumlah estrogen yang cukup (Toelihere 1981).
Seperti yang telah dijelaskan di atas, di samping ketersediaan materi baik kualitas
maupun kuantitas untuk mendukung proses reproduksi, kerja hormon juga diperlukan
untuk mempercepat dan meningkatkan proses sintesis vitelogenin dan penyerapannya
oleh telur.
Estradiol-17β merupakan hormon perangsang biosintesis vitelogenin di hati. Di
samping itu estradiol-17β di dalam darah memberikan rangsangan balik terhadap
hipofisis dan hipotalamus ikan. Rangsangan yang diberikan oleh estradiol-17β kepada
hipofisis ikan adalah rangsangan dalam proses pembentukan gonadotropin yang juga
berperan dalam membantu proses penyerapan vitelogenin oleh telur. Vitelogenin yang
disintesis di hati dengan bantuan hormon estradiol-17β disekresikan ke dalam aliran
darah menuju gonad. Oleh karena adanya peranan estradiol-17β pada biosintesis
vitelogenin maka penambahan estradiol-17β melalui implan pada induk ikan
diharapkan dapat meningkatkan ketersediaan estradiol-17β yang optimun untuk
merangsang hati mensintesis dan mensekresi vitelogenin ke dalam darah sehingga
konsentrasi vitelogenin dalam darah akan meningkat. Dengan demikian, penyerapan
vitelogenin oleh oosit akan berjalan dengan lancar.
Dengan melakukan pendekatan-pendekatan di atas maka diharapkan telur yang
dihasilkan akan mempunyai derajat pembuahan dan derajat tetas yang tinggi sehingga
larva yang dihasilkan berkualitas baik dengan ketahanan hidup yang prima. Namun,
usaha-usaha pendekatan tersebut sering dilakukan secara parsial dan tidak bersifat
menyeluruh. Pendekatan yang baik adalah mengkombinasikan antara lingkungan,
pakan, dan hormon. Faktor lingkungan sangat kompleks dan sukar ditiru sehingga
kombinasi antara pakan dan hormonlah yang sangat dimungkinkan, tetapi dengan
memperhatikan faktor lingkungan optimal yang mendukung proses reproduksi.
Dalam upaya meningkatkan kualitas telur yang pada akhirnya dapat
meningkatkan kelangsungan hidup larva ikan, penelitian ini dilakukan dengan
mengkombinasikan pendekatan nutrisi dan hormonal. Di samping itu, kebutuhan
vitamin C induk ikan lele dumbo yang berkaitan dengan akumulasi material telur
demikian, perlu dilakukan penelitian untuk mengevaluasi pengaruh penambahan
ascorbyl phosphate magnesium sebagai sumber vitamin C pada pakan dan hormon
estradiol-17β pada pematangan gonad, kualitas telur, dan ketahanan hidup larva ikan
lele dumbo (Clarias gariepinus). Dengan kombinasi tersebut diharapkan akan lebih
memaksimalkan proses reproduksi sehingga diharapkan materi yang masuk dapat
dengan optimal diserap telur dan pada akhirnya dapat meningkatkan kualitas telur dan
larva.
Perumusan Masalah
Masalah yang dihadapi dalam budi daya ikan lele adalah kurangnya informasi
tentang nutrisi induk. Ketersediaan nutrien induk untuk proses vitelogenesis sangat
bergantung pada kualitas pakan yang diberikan. Material telur yang mengalami
definsiensi gizi akan menimbulkan gangguan pada perkembangan larva dan akhirnya
akan mengalami kematian. Salah satu unsur mikro nutrien yang penting dalam proses
vitelogenesis dan embriogenesis adalah vitamin C. Pada proses vitelogenesis, vitamin
C sebagai donor elektron dalam reaksi hidroksilasi biosintesis hormon steroid yang
diperlukan bagi berlangsungnya proses tersebut. Selain itu, vitamin C juga berfungsi
sebagai anti oksidan yang akan melindungi kolesterol dari kerusakan akibat terjadinya
proses oksidasi sehingga kebutuhan kolesterol untuk proses biosintesis hormon
estrogen dapat terpenuhi. Pada proses embriogenesis, vitamin C berperan dalam
metabolisme lemak, yaitu dalam reaksi biosintesis karnitin, yang berfungsi mentransfer
asam lemak rantai panjang dari sitosol ke mitokondria untuk dikonversi menjadi energi
melalui proses β-oksidasi. Dengan demikian, kebutuhan energi selama proses tersebut
berlangsung dapat dipasok dalam jumlah yang cukup sesuai kebutuhan. Sumber energi
dan nutrien esensial bagi perkembangan larva ikan ketika telur menetas bergantung
pada materi bawaan yang telah dipersiapkan oleh induk.
Vitamin C mempunyai fungsi sebagai kofaktor enzim prolil dan lisin hidroksilase
yang mengkatalis hidroksilasi prolin dan lisin, yang esensial untuk biosintesis jaringan
kolagen yang terdapat pada ovarium dan perkembangan embrio. Kolagen merupakan
penyusun utama dinding dalam kantong ovarium. Kolagen sebagai penyusun dinding
kapiler darah di jaringan termasuk telur. Kapiler darah pada gonad penting dalam
vitamin C telur cepat menurun (Sato et al. 1987) karena pada saat itu terjadi
pembentukan tulang dan jaringan ikat.
Umumnya, spesies ikan tidak mempunyai kemampuan untuk melakukan
biosintesis vitamin C. Ketidakmampuan ikan mensintesis vitamin C disebabkan karena
tidak adanya enzim gulunolakton oksidase yang berperanan dalam mengkonversi
L-gulunolakton ke bentuk 2-keto-L-gunulolakton, sebagai tahap akhir dalam sintesis
vitamin C. Untuk itu kebutuhan vitamin C ikan harus dipasok dari luar.
Selain itu, pemberian pakan yang tidak optimal menyebabkan kurangnya energi
untuk mendukung proses reproduksi, terutama dalam mensintesis hormon-hormon
yang terlibat dalam proses perkembangan telur (vitelogenesis) seperti estradiol-17β.
Estradiol-17β adalah hormon steroid yang disintesis pada lapisan granulosa yang
kemudian bekerja merangsang biosintesis vitelogenin di hati. Sintesis vitelogenin
dirangsang oleh estradiol-17β yang memasuki sistem peredaran darah kemudian
merangsang hati mensintesis dan mensekresi vitelogenin. Konsentrasi estradiol-17β di
dalam plasma darah yang meningkat selama periode pertumbuhan oosit dapat
digunakan sebagai indikator vitelogenesis (Fostier et al. 1978, King dan Pankhurst
2004). Dengan kata lain, estradiol-17β bertanggung jawab dalam sintesis vitelogenin.
Dengan adanya peranan vitamin C dan estradiol-17β seperti tersebut di atas,
perlu diujicobakan peranan tersebut pada ikan uji, agar diperoleh informasi pengaruh
kombinasi ascorbyl phosphate magnesium sebagai sumber vitamin C dan estradiol-17β
pada pematangan gonad dan kualitas telur pada ikan lele dumbo. Informasi ini sangat
penting dalam menyusun suatu ransum yang tepat bagi pemenuhan gizi dan dosis
hormon estradiol-17β untuk induk ikan pada masa reproduksi sehingga telur dan
Tujuan dan Manfaat
Penelitian ini bertujuan untuk:
1. Untuk mendapatkan dosis kombinasi ascorbyl phosphate magnesium dan
estradiol-17β yang optimum dalam pematangan gonad, kualitas telur, dan larva
ikan lele sebagai ikan uji.
2. Untuk melihat pengaruh kombinasi ascorbyl phosphate magnesium dan
estradiol-17β pada penampilan reproduksi induk ikan lele serta keterkaitannya dengan
komposisi vitamin C, protein, lemak, fosfolipid, dan ratio hidroksiprolin/prolin
ovarium, telur, dan larva.
Hasil penelitian ini diharapkan dapat digunakan sebagai dasar dalam manajemen
induk, dengan pemberian pakan dan perlakuan hormonal yang tepat pada induk ikan
sehingga dapat mempercepat pematangan gonad, meningkatkan kuantitas, kualitas
telur, dan ketahanan hidup larva ikan ikan lele.
Hipotesis
Dengan pemberian ascorbyl phosphate magnesium pada pakan dan implantasi
hormon estradiol-17β yang optimal dapat meningkatkan kualitas vitelogenin yang
selanjutnya akan meningkatkan kandungan fosfolipida telur sehingga daya tetas telur
II. TINJAUAN PUSTAKA
Kematangan Gonad Ikan
Kematangan gonad adalah tahapan tertentu perkembangan gonad sebelum dan
sesudah memijah. Selama proses reproduksi, sebagian energi dipakai untuk
perkembangan gonad. Bobot gonad ikan akan mencapai maksimum sesaat ikan akan
memijah kemudian akan menurun dengan cepat selama proses pemijahan berlangsung
sampai selesai. Menurut Effendie (1997), umumnya pertambahan bobot gonad ikan
betina pada saat stadium matang gonad dapat mencapai 10-25 persen dari bobot tubuh
dan pada ikan jantan 5-10 persen. Lebih lanjut dikemukakan bahwa semakin
rneningkat tingkat kematangan gonad, diameter telur yang ada dalam gonad akan
menjadi semakin besar. Pendapat ini diperkuat oleh Kuo et al. (1974) bahwa
kematangan seksual pada ikan dicirikan oleh perkembangan diameter rata-rata telur dan
melalui distribusi penyebaran ukuran telurnya.
Ikan lele (Clarias batrachus) pertama kali matang kelamin pada umur satu tahun
(Chinabut et al. 1991) dengan ukuran panjang tubuh sekitar 20 cm dan ukuran berat
tubuh 100 sampai 200 gram (Mollah dan Tan 1983; Suyanto 1986). Di Thailand, ikan
lele yang hidup di alam memijah pada musim penghujan dari bulan Mei sampai
Oktober (Chinabut et al. 1991).
Perkembangan sel telur (oosit) diawali dari germ cell yang terdapat dalam
lamela dan membentuk oogonia. Oogonia yang tersebar dalam ovarium
menjalankan suksesi pembelahan mitosis dan ditahan pada "diploten" dari profase
meiosis pertama. Pada stadia, ini oogonia dinyatakan sebagai oosit primer
(Harder 1975). Oosit primer kemudian menjalankan masa tumbuh yang meliputi
dua fase. Pertama adalah fase previtelogenesis, ketika ukuran oosit membesar
akibat pertambahan volume sitoplasma (endogenous vitelogenesis), namun
belum terjadi akumulasi kuning telur. Kedua adalah fase vitelogenesis, ketika
terjadi akumulasi material kuning telur yang disintesis oleh hati, kemudian
dibebaskan ke darah dan dibawa ke dalam oosit secara mikropinositosis (Zohar
1991; Jalabert dan Zohar 1982). Peningkatan ukuran indeks gonad somatik atau
saat perkembangan oosit terjadi perubahan morfologis yang mencirikan stadianya.
Menurut Nagahama (1983) stadium oosit dapat dicirikan berdasarkan volume
sitoplasma, penampilan nukleus dan nukleolus, serta keberadaan butiran kuning
telur. Berdasarkan kriteria ini, oosit dapat diklasifikasikan ke dalam beberapa
kelas. Yamamoto dalam Nagahama (1983) membaginya ke dalam 8 kelas, yaitu
stadia kromatin-nukleolus, perinukleolus (yang terdiri atas awal dan akhir
nukleolus), stadium oil drop stadium yolk primer, sekunder, tertier, dan stadium
matang. Sedangkan Chinabut et al. (1991) membagi oosit dalam 6 kelas untuk
Clarias sp, dimana stadia nukleolus dan perinukleolus dikategorikan sebagai
stadium pertama, dan setiap stadium dicirikan sebagai berikut:
-stadium 1 : Oogonia dikelilingi satu lapis set epitel dengan pewarnaan
hematoksilin-eosin plasma berwarna merah jambu, dengan inti
yang besar di tengah.
-stadium 2 : Oosit berkembang ukurannya, sitoplasma bertambah besar, inti
biru terang dengan pewarnaan, dan terletak masih di tengah
sel. Oosit dilapisi oleh satu lapis epitel.
-stadium 3 : Pada stadium ini berkembang sel folikel dan oosit membesar dan
provitilin nukleoli mengelilingi inti.
-stadium 4 : Euvitilin inti telah berkembang dan berada disekitar selaput inti
Stadium ini merupakan awal vitelogenesis yang ditandai dengan
adanya butiran kuning telur pada sitoplasma. Pada stadium ini,
oosit dikelilingi oleh dua lapis sel dan lapisan zona radiata
tampak jelas pada epitel folikular.
-stadium 5 : Stadia peningkatan ukuran oosit karena diisi oleh kuning telur.
Butiran kuning telur bertambah besar dan memenuhi sitoplasma
dan zona radiata terlihat jelas.
-stadium 6 : Inti mengecil dan selaput inti tidak terlihat, inti terletak di tepi.
Zona radiata, sel folikel, dan sel teka terlihat jelas.
Pengetahuan tingkat kematangan gonad sangat penting dan sangat menunjang
keberhasilan dalam membenihkan ikan karena berkaitan erat dengan pemilihan
telur yang terkandung di dalamnya semakin membesar sebagai hasil dari akumulasi
kuning telur, hidrasi, dan pembentukan butir-butir minyak yang berjalan secara
bertahap.
Secara garis besar, perkembangan gonad ikan dapat dibagi menjadi dua tahap,
yaitu tahap pertumbuhan gonad ikan sampai ikan menjadi dewasa kelamin dan
selanjutnya adalah pematangan gamet. Tahap pertama berlangsung mulai dari ikan
menetas hingga mencapai dewasa kelamin dan tahap kedua dimulai setelah ikan
mencapai dewasa, dan terus berkembang selama fungsi reproduksi masih tetap berjalan
normal (Lagler et al. 1977).
Tam et al. (1986) menyatakan bahwa pada saat menjelang ovulasi akan terjadi
peningkatan diameter oosit karena diisi oleh massa kuning telur yang homogen akibat
adanya peningkatan kadar estrogen dan vitelogenin. Sementara itu, menurut Bagenal
(1969), ukuran telur juga berperan dalam kelangsungan hidup ikan. Benih ikan brown
trout yang berasal dari telur yang berukuran besar mempunyai daya hidup yang lebih
tinggi daripada benih ikan yang berasal dari telur yang berukuran kecil. Hal ini terjadi
karena kandungan kuning telur yang berukuran besar lebih banyak sehingga larva yang
dihasilkan mempunyai persediaan makanan yang cukup untuk membuat daya tahan
tubuh yang lebih tinggi dibanding dengan telur-telur yang berukuran kecil.
Woynarovich dan Horvath (1980) menyatakan bahwa induk yang pantas
dipijahkan adalah induk yang telah melewati fase pembentukan kuning telur (fase
vitellogenesis) dan masuk ke fase dorman. Fase pembentukan kuning telur dimulai
sejak terjadinya penumpukan bahan-bahan kuning telur da!am sel telur dan berakhir
setelah sel telur mencapai ukuran tertentu atau nukleolus tertarik ke tengah nukleus.
Setelah fase pembentukan kuning telur berakhir, sel telur tidak mengalami perubahan
bentuk selama beberapa saat, tahap ini disebut fase istirahat (dorman). Menurut Lam
(1985), apabila rangsangan diberikan pada saat ini, maka akan menyebabkan
terjadinya migrasi inti ke perifer, kemudian inti pecah atau melebur pada saat
pematangan oosit, ovulasi (pecahnya folikel), dan oviposisi. Menurut Suyanto (1986),
bilamana kondisi lingkungan tidak cocok dan rangsangan tidak tersedia maka telur
dorman tersebut akan mengalami degenerasi (rusak) lalu diserap kembali oleh lapisan
folikel melalui atresia. Faktor-faktor eksternal lain yang menyebabkan terjadinya atresia
Ukuran sel telur ada hubungannya dengan fekunditas. Makin banyak telur yang
dipijahkan ukuran telurnya makin kecil, misalnya ikan cod (diameternya 1-1,7mm)
produksinya 10 juta telur. Salmon Atlantik yang memiliki diameter telur 5-6 mm,
produksi telurnya 2.000-3.000 butir (Blaxter 1969), sedangkan untuk ikan belut dengan
diameter telur 1–1,5 mm produksinya 2.200–5.400 telur (Sidthimunka 1972).
Vitelogenesis
Sintesis vitelogenin (prekursor kuning telur) di dalam hati disebut vitelogenesis.
Vitelogenin diangkut dalam darah menuju oosit, lalu diserap secara selektif dan
disimpan sebagai kuning telur. Vitelogenin ini berupa glikofosfoprotein yang
mengandung kira-kira 20% lemak, terutama fosfolipid, trigliserida, lipoprotein, dan
kolesterol. Berat molekul vitelogenin untuk beberapa jenis ikan diketahui antara 140-
220 kDa (Tyler 1991; Komatsu dan Hayashi 1997).
Proses oogenesis pada teleost terdiri atas dua fase, yaitu pertumbuhan oosit
(vitelogenesis) dan pematangan oosit. Vitelogenesis merupakan aspek penting dalam
pertumbuhan oosit yang meliputi rangkaian proses (1) adanya sirkulasi estrogen
(estradiol-17β) dalam darah menggertak hati untuk mensintesis dan mensekresikan
vitelogenin yang merupakan prekursor protein kuning telur; (2) vitelogenin diedarkan
menuju lapisan permukaan oosit yang sedang tumbuh; (3) secara selektif, vitelogenin
akan ditangkap oleh reseptor dalam endositosis, dan (4) terjadi translokasi sitoplasma
membentuk badan kuning telur bersamaan dengan pembelahan proteolitik dari
vitelogenin menjadi subunit lipoprotein kuning telur, lipovitelin, dan fosvitin. Adanya
vitelogenin menunjukkan terjadinya akumulasi lipoprotein kuning telur di dalam oosit.
Pada beberapa jenis ikan selama pertumbuhan oosit terjadi peningkatan Indeks Somatik
Gonad (IGS) 1 sampai 20% atau lebih.
Pada ikan betina, ovari berespons terhadap peningkatan konsentrasi gonadotropin
dengan meningkatkan secara tidak langsung produksi estrogen, yakni estradiol-17β
(E2). Estradiol-17β beredar menuju hati, memasuki jaringan dengan cara difusi dan
secara spesifik merangsang sintesis vitelogenin (Ng dan Idler 1983). Aktivitas
vitelogenesis ini menyebabkan nilai indeks hepatosomatik (IHS) dan indeks
Pembesaran oosit disebabkan terutama oleh penimbunan kuning telur. Seperti
pada kebanyakan ikan, kuning telur merupakan komponen penting oosit ikan Teleostei.
Ada tiga tipe material kuning telur pada ikan Teleostei: butiran kecil minyak,
gelembung kuning telur (yolk vesicle) dan butiran kuning telur (yolk globule). Secara
umum, butiran kecil minyak yang kita kenal dengan lipid yang berantai panjang (asam
lemak tidak jenuh) pertama kali muncul di daerah perinuklear dan kemudian berpindah
ke periferi (tepi sel) pada tahap selanjutnya. Urutan kemunculan material kuning telur
bervariasi antarspesies. Pada rainbow trout, butiran kecil muncul segera setelah
dimulainya pembentukan gelembung kuning telur (Yamamoto et al. 1965 dalam
Nagahama 1983).
Fenomena penimbunan material kuning telur oleh oosit ikan dibagi menjadi dua
fase, yakni sintesis kuning telur di dalam oosit atau vitelogenesis endogen dan
penimbunan prekursor (bahan pembentuk) kuning telur yang disintesis di luar oosit
atau vitelogenesis eksogen (Matty 1985). Gelembung kuning telur positif-PAS
(mukopolisakarida atau glikoprotein) umumnya merupakan struktur yang pertama
muncul dalam sitoplasma oosit selama pertumbuhan sekunder oosit, dan pertama kali
muncul di zona terluar dan zona midkortikal pada oosit.
Ketika vitelogenesis berlangsung, sebagian besar sitoplasma telur matang
ditempati oleh banyak gelembung kuning telur yang padat dengan asam lemak dan
dikelilingi oleh selapis membran pembatas. Selama tahap akhir vitelogenesis, globula
kuning telur beberapa ikan Teleostei bergabung satu sama lain membentuk masa
tunggal kuning telur.
Perkembangan gonad ikan betina terdiri atas beberapa tingkat yang dapat
didasarkan atas pengamatan secara mikroskopis dan makroskopis. Secara mikroskopis
perkembangan telur diamati untuk menilai perkembangan ovarium antara lain tebal
dinding indung telur, keadaan pembuluh darah, inti butiran minyak, dan kuning telur.
Secara makroskopis perkembangan ovarium ditentukan dengan mengamati warna
indung telur, ukuran butiran telur, dan volume rongga perut ikan.
Pada ovarium ikan terdapat bakal sel telur yang dilindungi suatu jaringan
pengikat yang bagian luarnya dilapisi peritoneum dan bagian dalamnya dilapisi
epitelium. Sebagian dari sel-sel epitelium akan membesar dan berisi nukleus, yang
akan bervariasi. Pada tahap perkembangan awal, oogonia terlihat masih sangat kecil,
berbentuk bulat dengan inti sel yang sangat besar dibandingkan dengan sitoplasmanya.
Oogonia terlihat berkelompok tapi kadang-kadang ada juga yang berbentuk tunggal.
Sementara itu oogonia terus membelah diri dengan cara mitosis. Pada ikan yang
mempunyai siklus reproduksi tahunan atau tengah tahunan akan terlihat adanya
puncak-puncak pembelahan oogonia. Pada ikan yang memijah sepanjang tahun,
perbanyakan oogonia akan terus menerus sepanjang tahun.
Transformasi oogonia menjadi oosit primer banyak terjadi pada tahap
pertumbuhan yang ditandai dengan munculnya kromosom. Segera setelah itu, folikel
berubah bentuk, dari semula yang berbentuk skuamosa menjadi berbentuk kapsul oosit.
Inti sel terletak pada bagian sentral dibungkus oleh lapisan sitoplasma yang tipis. Pada
perkembangan selanjutnya, oosit membentuk lapisan korion, membran, granulosa,
membran, dan teka. Juga butir-butir lemak mulai terlihat ditumpuk pada sitoplasma
dan bersamaan dengan itu muncul cortical alveoli. Pada saat ini, ketersediaan vitamin
C mutlak diperlukan karena dengan peningkatan kadar asam lemak, kebutuhan vitamin
C semakin meningkat pula. Vitamin C dapat mencegah terjadinya oksidasi pada
unit-unit asam lemak, terutama asam lemak tidak jenuh (Machlin 1990). Butir-butir lemak
ini selanjutnya akan bertambah besar pada vitelogenesis yang diawali dengan
pembentukan vakuola-vakuola yang kemudian diikuti dengan munculnya globula
kuning telur, bersamaan dengan itu oosit membengkak secara menyolok. Kuning telur
pada ikan terdiri atas fosfoprotein dan lipoprotein yang dihasilkan oleh hati kemudian
disalurkan ke dalam peredaran darah.
Peranan Vitamin C pada Reproduksi Ikan
Vitamin C adalah nutrien yang dibutuhkan untuk proses fisiologi hewan,
termasuk ikan (Tolbert 1979 dalam Al Amoudi et al. 1992). Sebagai vitamin yang larut
dalam air, vitamin C disintesis dari asam glukuronat oleh beberapa hewan, namun ikan
tidak dapat mensintesisnya walaupun sel-selnya membutuhkan (Masumoto et al. 1991).
Oleh sebab itu, vitamin C harus tersedia dalam pakan (Faster dalam Sandnes 1991).
Ketidakmampuan ikan mensintesis vitamin C disebabkan oleh tidak adanya enzim
L--gulunolakton oksidase yang berperan dalam konversi L-L--gulunolakton ke bentuk
Variasi kadar vitamin C ovarium pada saat siklus reproduksi dari berbagai
spesies ikan telah dicatat oleh beberapa peneliti sehingga menimbulkan spekulasi
kemungkinan pentingnya senyawa ini saat ovarium berkembang. Kadar vitamin C ikan
karper Krusian (Carassius carassius) saat siklus reproduksi berkisar dari 92 sampai 203
ug/g (Saeymour 1981), ikan cod Atlantik (Gadus morrhua) berkisar dari 80 sampai 203
ug/g (Sandnes dan Braekkan 1981), dan karper India dari 225 sampai 286 ug/g)
(Agrawal dan Mahajan 1980). Cho et al. (1979) mendapatkan bahwa kadar vitamin C
ovarium ikan trout (Oncorhynchus mykiss) mencapai maksimum pada 451 ug/g bobot
basah pada saat akan ovulasi. Dengan memperhatikan indeks gonad somatik, Sandnes
dan Braekkan (1981) mencatat bahwa akumulasi vitamin C tertinggi menjelang GSI
mencapai maksimum, kemudian menurun saat terjadi ovulasi. Pengamatan pada ikan
kod Atlantik memperlihatkan bahwa kandungan vitamin C pada stadia awal
pertumbuhan ovarium adalah 150 ug/g dan tertinggi mencapai 500 ug/g (Sandnes
1984). Menurut Ishibashi et al. (1994), perubahan vitamin C ovarium selama periode
pematangan berkaitan dengan peningkatan ukuran oosit karena akumulasi material
kuning telur. Agrawal dan Mahajan (1980) mencatat bahwa kandungan vitamin C
darah ikan karper India yang ditangkap di alam mencapai titik terendah saat musim
pemijahan, yaitu 17,95-19,65 ug/ml, dan saat pertumbuhan ovarium kadar vitamin C
mencapai kisaran 20,39-25,95 ug/ml. Disimpulkan pula bahwa ada mobilisasi vitamin
C yang diperoleh dari pakan alami ke ovarium saat siklus reproduksi.
Soliman et al. (1986) menyatakan bahwa tingginya kandungan vitamin C saat
ovarium berkembang berkaitan dengan fungsinya sebagai kofaktor enzim prolil dan
lisil hidroksilase yang mengkatalis hidroksilasi prolin dan lisin, dan esensial untuk
perkembangan normal jaringan kolagen yang banyak terdapat dalam ovarium. Kolagen
merupakan penyusun utama dinding dalam kantung ovarium (Sandnes et al. 1984).
Waagbo et al. (1989) telah mengamati adanya akumulasi vitamin C di jaringan
kolagen yang mengitari sel telur sehingga disimpulkan bahwa pada saat gonad
berkembang vitamin C digunakan untuk sintesis kolagen. Pendapat lain dikemukakan
oleh Sandnes (1984) bahwa peningkatan kadar vitamin C dalam siklus reproduksi
berhubungan dengan proses vitelogenesis. Proses ini dikontrol oleh hormon estrogen
yang mampu menstimulasi hati untuk mensintesis protein spesifik, yang kemudian
diakumulasikan pada oosit bersama senyawa lipida. Vitamin C pada ovarium berperan
Penelitian Alava et al. (1993) memperlihatkan bahwa pemberian
askorbil-2-fosfat magnesium, suatu bentuk turunan vitamin C, dalam ransum dapat menstimulasi
perkembangan gonad induk udang Penaeus japonicus betina. Percobaannya dengan
menggunakan pakan yang disuplementasi askorbil-monofosfat magnesium
masing-masing 500, 1000, dan 1500 mg/kg. Setelah pemeliharaan 170 hari, nilai IGS induk
betina mencapai 2.40, 2.51, dan 1.81%, sedangkan nilai IGS induk jantan adalah 0.76,
0.87, dan 0.91%. Untuk kontrol tidak diperoleh data karena induk mati sebelum
berakhimya percobaan. Penelitian Ishibasi et al. (1994) terhadap ikan Japanese parrot
(Oplegnathus fasciatus) memperlihatkan peningkatan indeks gonad somatik dengan
peningkatan dosis vitamin C yang diberikan. Ikan yang menerima pakan dengan
suplementasi vitamin C 0, 300, 1000, dan 3000 mg/kg memperlihatkan nilai IGS
masing-masing 0.5, 0.9, 1.4, dan 2.2 % untuk induk betina, dan 0.4, 0.6, 0.5, dan 0.8
untuk induk jantan. Pengamatan secara mikrokospis terhadap ovarium juga
memperlihatkan persentase induk yang mencapai aktivitas vitelogenesis meningkat
dengan peningkatan dosis vitamin C. Induk yang menerima pakan tanpa suplementasi
vitamin C tidak menunjukkan adanya oosit pada fase vitelogenesis, sedangkan dengan
perlakuan suplementasi vitamin C 300, 1000, dan 3000 mg/kg pakan, jumlah induk
yang ovarinya mencapai stadium vitelogenesis hingga matang adalah 20, 40, dan 80%.
Soliman et al. (1986) mengamati pengaruh asam askorbat pada penampilan reproduksi
ikan Oreochromis mossambicus melaporkan bahwa ikan yang menerima pakan dengan
suplementasi vitamin C biasa 1250 mg/kg memperlihatkan gejala siap mijah lebih
cepat dua minggu dibandingkan induk yang menerima pakan tanpa suplementasi
vitamin C.
Percobaan Priyono et al. (1996) mencatat bahwa ikan bandeng (Chanos chanos
Forskal) yang menerima pakan dengan suplementasi askorbil-2-fosfat magnesium 1500
mg/kg pakan menunjukkan frekuensi bertelur lebih tinggi dibandingkan dengan induk
yang menerima pakan dengan suplementasi 1000 mg/kg pakan, dan tidak ditemukan
induk yang memijah pada kontrol. Vitamin C ovarium induk yang menerima pakan
dengan suplementasi vitamin C lebih tinggi dibandingkan dengan induk yang
menerima pakan tanpa suplementasi vitamin C, namun kadar vitamin C ovarium dapat
mencapai kadar tertentu (Ishibashi et al. 1994). Percobaannya memperlihatkan bahwa
kandungan vitamin C ovarium induk yang menerima pakan dengan suplementasi
vitamin C masing-masing 0, 300, 1000, dan 3000 mg/kg pakan mencapai 70.6, 657.1,
vitamin C dalam ransum yang diterima oleh induk dapat ditransfer ke telur, dan
disiapkan untuk perkembangan embrio. Pengamatannya pada telur ikan Oreochromis
mossambicus dimana induk yang menerima pakan dengan suplementasi vitamin C
1250 mg/kg pakan mengandung vitamin C 201.83 ug/g dan daya tetas telur mencapai
89.33%, sedangkan kandungan vitamin C telur dari induk yang menerima pakan tanpa
vitamin C tidak terdeteksi dan mempunyai daya tetas 56.90%, dan 85% pascalarva
yang dihasilkan mengalami gangguan pertumbuhan tulang belakang. Percobaan
Akiyama et al. (1990) pada ikan sardin (Sardinops sagaxmelanosticia) menunjukkan
bahwa tidak ditemui telur yang menetas dari induk yang menerima pakan dengan
suplementasi vitamin C 80 mg/kg pakan, sedangkan induk yang menerima pakan
dengan suplementasi vitamin C lebih tinggi, yaitu 3200 mg/kg pakan menghasilkan
daya tetas telur lebih baik. Vitamin C yang ditransfer dari induk ke material telur
berperan dalam mendukung perkembangan embrio (Sandnes 1991). Menurut Sandnes
et al. (1984) kandungan vitamin C telur 20 ug/g merupakan batas terendah untuk
perkembangan normal embrio ikan trout.
Peranan Estradiol-17β pada Reproduksi Ikan
Proses vitelogenesis pada ikan melibatkan beberapa hormon, dan pada ikan ada
dua macam hormon gonadotropin yang dihasilkan oleh adenohipofisis yang berperan
sebagai follicle stimulating hormone (FSH) dan luteinizing hormone (LH). Hormon
tersebut adalah FSH (GTH I), yang bekerja merangsang perkembangan folikel melalui
sekresi estradiol-17β pada ovari dan LH (GTH II) yang dibutuhkan untuk proses
pematangan akhir oosit (Nagahama 1983). Gonadotropin yang dihasilkan akan bekerja
pada sel teka sebagai tempat sintesis testosteron. Testosteron yang dihasilkan oleh
lapisan sel teka akan masuk ke dalam lapisan granulosa. Di dalam lapisan granulosa
testosteron diubah menjadi estradiol-17β dengan bantuan enzim aromatase.
Estradiol-17β merupakan perangsang dalam biosintesis vitelogenin di hati. Di
samping itu, estradiol-17β yang terdapat dalam darah memberikan rangsangan balik
terhadap hipofisis dan hipotalamus ikan. Rangsangan yang diberikan oleh estradiol-17β
terhadap hipofisis ikan adalah rangsangan dalam proses pembentukan gonadotropin.
Rangsangan terhadap hipotalamus adalah dalam memacu proses GnRH. GnRH yang
nantinya berperan dalam proses biosintesis estradiol-17β pada lapisan granulosa. Siklus
hormonal terus berjalan di dalam tubuh ikan selama terjadinya proses vitelogenesis
(Nagahama 1983 dan Yaron 1995). Menurut Aida et al. (1991) proses vitellogenesis
pada ikan terjadi seperti pada Gambar 1.
Gambar 1. Proses vitelogenesis pada ikan (Aida et al. 1991)
Beberapa penelitian menunjukkan bahwa peningkatan konsentrasi
estradiol-17β akan meningkatkan konsentrasi vitelogenin darah dan konsentrasi
estradiol-17β tinggi pada saat vitelogenesis pada European sea bass (Dicebtrachus labrax)
(Hassin et al. 1991); salmon (Salmo gairdneri) (Van Bohemen et al. 1981); mas
koki (Pankhurst et al. 1986); jambal siam (Pangasius hypophthalmus) (Indriastuti
2000 dan Monijung 2002). Penelitian untuk melihat hubungan tersebut telah
dilakukan pada ikan trout, Salmo trutta dan rainbouw trout Salmo gairdneri
(Hjartarson et al. 1991), Striped bass Morone sexatilis (Sullivan et al. 1991), dan
Clarias macrocepalus (Tan-Fermin et al. 1997). Sintesis vitelogenin di hati sangat
dipengaruhi oleh estradiol-17β yang merupakan stimulator dalam biosintesis
vitelogenin. Selain itu, sintesis tersebut dipengaruhi juga oleh androgen yang ada
Umpan balik
dalam tubuh ikan (testosteron) dan melalui perubahan androgen menjadi estrogen
oleh enzim aromatase hati (Yaron 1995). Dengan demikian, peningkatan GtH
dapat meningkatkan estradiol, dan pola kandungan estradiol seiring dengan
perkembangan telur (Yaron 1995; Tan-Fermin et al. 1997).
Kualitas Telur Ikan
Kualitas telur adalah kemampuan telur untuk menghasilkan larva yang berdaya
hidup. Kemampuan telur untuk menghasilkan larva yang berdaya hidup dapat
ditentukan dengan beberapa faktor antara lain faktor fisik, kimia, genetik, dan fisiologi
selama terjadi proses awal pada telur. Jika salah satu faktor essensial ini tidak ada,
perkembangan telur akan gagal dalam beberapa stadia. Telur merupakan hasil akhir
dari proses gametogenesis setelah oosit mengalami fase pertumbuhan yang panjang
yang sangat bergantung pada gonadotropin dari pituitari. Perkembangan diameter telur
pada oosit teleostei umumnya karena akumulasi kuning telur.
Ada tiga macam material kuning telur yang berbeda, yaitu 1) oil droplet (butir
minyak), 2) yolk vesicle (vesikula kuning telur), dan 3) yolk globule (bola kecil kuning
telur). Dalam vitelogenesis yang sedang berkembang, sitoplasma telur yang matang
ruangannya diisi oleh bola-bola kecil kuning telur saling bersatu dengan yang lainnya
membentuk menjadi massa kuning telur.
Pembuahan atau fertilisasi adalah proses bergabungnya inti sperma dengan inti
sel telur dalam sitoplasma sehingga membentuk zigot, dimana asosiasi ini merupakan
mata rantai awal dan sangat penting pada proses fertilisasi. Laju pembuahan sering
digunakan sebagai parameter untuk mendeteksi kualitas telur.
Fertilisasi dan proses aktivasi pada telur ikan menjadi penting untuk beberapa
perkembangan embrio. Selama fertilisasi dan aktivasi, pada telur-telur ikan teleost
terjadi reaksi kortikal. Alveoli kortikal melebur dan melepaskan kandungannya
(koloids) dari lapisan kortikal, dan selanjutnya memulai pembentukan ruang perivitelin
(Yamamoto 1961 dalam Kjorsvik et al. 1990). Kortikal alveoli muncul setelah
terjadinya fertilisasi dan reaksi kortikal yang tidak lengkap menunjukkan kualitas telur
yang jelek. Tidak lengkapnya proses aktivasi ini menyebabkan ruang perivitelin
korion telur selama proses aktivasi akibat dari reaksi enzim. Telur yang kualitasnya
bagus memiliki korion yang keras.
Selain hal-hal di atas parameter lain yang dapat juga menjadi patokan kualitas
telur adalah transparansi telur dan distribusi butiran lemak (Mc Evoy 1984). Kualitas
telur yang baik umumnya transparan dan jelas kelihatan serta pembelahan awal yang
simetris.
Selama oogenesis, kuning telur mengakumulasi sejumlah besar granula kuning
telur dan lipid yang terisi pada bagian tengah. Kisaran diameter granula telah diukur
antara 6-24 µm (Linhart et al. 1995). Jumlah dan distribusi lemak (butir lemak) sangat
bervariasi. Ukuran diameternya antara 1-1.5µm, dan diketahui bahwa butir lemak
berfungsi sebagai cadangan energi dan fungsi hidrostatik. Distribusi butir-butir lemak
ini juga menjadi parameter kualitas telur.
Ukuran telur berkorelasi dengan ukuran larva. Larva yang besar lebih tahan tanpa
pakan dibandingkan dengan larva yang kecil yang ditetaskan dari telur yang kecil.
Hubungan positif antara ukuran larva dan ukuran telur telah dilaporkan untuk Salmon
salar, Onchorhynchus mykiss (Kamler 1992), dan turbot (Scopththalmus maximus L)
(Kjorsvik et al. 2003).
Beberapa peneliti menunjukkan bahwa telur yang berukuran besar menghasilkan
kelangsungan hidup yang lebih tinggi. Kamler (1992) mengajukan sebuah persamaan
kelangsungan hidup untuk ikan pelagis laut, laju mortalitas telur dan larva berbanding
terbalik dengan ukuran telur. Bila tidak ada makanan eksternal, larva yang lebih besar
yang berasal dari telur yang besar dapat bertahan hidup lebih lama dibanding larva yang
berasal dari telur yang kecil.
Pada kondisi yang baik seperti di pembenihan, ukuran telur tidak memberikan
dampak secara langsung pada kelangsungan hidup dan pertumbuhan pada ikan
Rainbow trout (Salmo gairdneri: Pitman 1979; Springate dan Bromage 1985), Salmo
salar (Thorpe et al. 1984), catfish Clarias macrocepalus. (Reagen dan Conley 1977),
dan carp (Kirpchnikov 1966 dalam Kjorsvik et al. 1990).
Telur harus mengandung semua nutrien yang diperlukan oleh embrio yang
sedang berkembang dan larva setelah telur dibuahi sampai pada saat ikan dapat
memenuhi keperluannya untuk mengawali konsumsi makanan dari luar. Komposisi
pertumbuhan. Komponen yang diketahui esensial untuk kehidupan organisme
(terutama untuk organisme yang tidak dapat mensintesis nutrien), seperti vitamin C
harus ada dalam pakan dalam jumlah tertentu untuk kebutuhan biologi organisme
tersebut. Oleh karena itu, parameter biokimia kualitas telur dapat digunakan untuk
mengevaluasi kandungan biokimia telur bahkan sebelum fertilisasi.
Materi yang diperlukan selama perkembangan dapat dibagi dua, yaitu 1)
diperlukan secara langsung untuk sintesis jaringan embrionik dan 2) digunakan untuk
energi metabolisme. Jumlah nutrien yang diperlukan jelas bervariasi bergantung pada
beberapa faktor, antara lain waktu inkubasi, ukuran ikan pada waktu menetas, dan
lamanya anak-anak ikan memerlukan persediaan makanan endogen sebelum
menemukan semua keperluan dari sumber lain. Kandungan protein lipid dan
karbohidrat berkorelasi positif dengan kelangsungan hidup larva (Kamler 1992)
Kerangka Teoretis
Secara alami proses vitellogenesis memerlukan interaksi antara faktor eksternal
dan faktor internal. Faktor eksternal yang mempengaruhi vitelogenesis antara lain
temperatur, curah hujan, debit air, feromon, dan pakan. Pakan merupakan komponen
penting dalam proses pematangan gonad karena proses vitelogenesis pada dasarnya
adalah proses akumulasi nutrien dalam sel telur sehingga ketersediaan nutrien pada sel
telur akan menentukan kualitas telur dan pada akhirnya juga pada perkembangan larva.
Di pihak lain, faktor internal yang terpenting adalah tersedianya hormon-hormon
steroid gonad terutama estradiol-17β pada tingkat yang dapat merangsang
vitelogenesis.
Proses perkembangan gonad ikan dimulai dengan adanya respons dari
hipotalamus terhadap sinyal lingkungan, kemudian merangsang pituitari untuk
menghasilkan gonadotropin yang nantinya akan mempengaruhi sintesis testosteron
yang diaromatasi menjadi estradiol-17β. Estradiol-17β merupakan perangsang
biosintesis vitelogenin di hati, dan dapat memberikan umpan balik terhadap hipofisis
serta hipotalamus ikan untuk menghasilkan gonadotropin. Sintesis vitelogenin ini
distimulir oleh estradiol-17β yang masuk ke dalam sistem vaskuler dan merangsang
hati untuk mensintesis dan mensekresi vitelogenin. Selanjutnya vitelogenin ini dilepas
ditimbun sebagai komponen kuning telur. Peningkatan konsentrasi estradiol-17β akan
meningkatkan konsentrasi vitelogenin darah. Hal ini menunjukkan bahwa konsentrasi
estradiol-17β dalam tubuh ikan sejalan dengan perubahan konsentrasi vitelogenin
darah.
Vitamin C mempunyai peranan dalam proses vitelogenesis dan embriogenesis.
Hal ini terjadi karena vitamin C mempunyai peranan penting dalam reaksi hidroksilasi
biosintesis hormon steroid, metabolisme lemak, dan sintesis kolagen (Masumoto et al.
1991; Linder 1992: Piliang 1995).
Vitamin C memainkan peranan penting dalam reaksi hidroksilasi biosintesis
hormon steroid yang diperlukan bagi berlangsungnya proses tersebut. Selain itu,
vitamin C juga berfungsi sebagai antioksidan. Pada proses embriogenesis, vitamin C
berperan dalam metabolisme lemak, yaitu dalam reaksi biosintesis karnitin, yang
berfungsi mentransfer asam lemak rantai panjang dari sitosol ke mitokondria untuk
dikonversi menjadi energi melalui proses β-oksidasi. Dengan demikian, kebutuhan
energi selama proses tersebut berlangsung dapat dipasok dalam jumlah yang cukup
sesuai kebutuhan. Sumber energi dan nutrien esensial bagi perkembangan larva ikan
ketika telur menetas bergantung pada materi bawaan yang telah dipersiapkan oleh
induk.
Vitamin C mempunyai fungsi sebagai kofaktor enzim prolil dan lisil hidroksilase
yang mengkatalis hidroksilasi prolin dan lisin, dan esensial untuk perkembangan
normal jaringan kolagen yang banyak terdapat pada ovarium. Kolagen merupakan
penyusun utama dinding dalam kantong ovarium. Hal inilah yang menyebabkan
adanya fluktuasi kandungan vitamin C ovarium selama berlangsungnya siklus
reproduksi. Selain itu, kolagen dibutuhkan untuk perkembangan embrio dan larva,
karena kolagen merupakan komponen utama pada kulit dan jaringan ikat serta zat-zat
pembentuk tulang dan gigi.
Defisiensi vitamin C pada ikan dapat disebabkan kurang tersedianya
senyawa ini dalam pakan yang diberikan karena mudah larut dalam air dan
hilang selama proses pembuatan pakan. Di samping itu, ikan tidak mampu
mensintesis vitamin C, walaupun sel-selnya membutuhkan vitamin C. Dari
hasil percobaan Azwar (1977) diketahui bahwa ascorbyl phosphate magnesium
oksidasi sehingga bioaktivitasnya sebagai sumber vitamin C dalam pakan tetap
III. BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Instalasi Riset Perikanan Budidaya Air Tawar
(BRPBAT), Depok, Jawa Barat. Penelitian ini dimulai sejak Juni sampai Desember
2005.
Bahan dan Alat
Pakan uji
Selama penelitian, jenis pakan yang digunakan adalah pakan dalam bentuk
pelet dengan komposisi berdasarkan komposisi pakan buatan untuk induk ikan
lele (Khoironi, 2002), kemudian ditambahkan vitamin C yang berupa
ascorbyl
phosphate magnesium
(Showa Denko Jepang) dengan bobot molekul 379,61
serta kandungan asam askorbat 46%. Komposisi pakan uji dan proksimat pakan
dapat dilihat pada Tabel 2 dan 3.
Hewan Uji
Dalam percobaan ini hewan uji yang akan digunakan adalah induk ikan lele
dumbo (
C. gariepinus
) dari hasil pembesaran petani ikan yang ada di Dermaga Bogor.
Induk ikan adalah hasil pemijahan dari satu induk dan berumur 6 bulan. Jumlah ikan
yang digunakan adalah 216 ekor induk ikan lele betina pada tingkat kematangan
gonad II dan 216 ekor ikan jantan. Masing-masing perlakuan mempunyai 18 ekor
ikan. Ukuran panjang dan bobot ikan uji masing-masing 32–38 cm dan 250–328 gram.
Hormon implantasi
Hormon yang digunakan adalah estradiol-17
β
(Sigma Chemical Company) dan
bubuk kolesterol (5-cholesten-3
β
-ol), cocoa butter, alkohol 98%, 2-phenoxyethanol dan
betadine (prosedur selengkapnya pada Lampiran 03).
Wadah
Ikan dipelihara dalam 12 buah jaring terapung yang diletakkan di dalam
kolam dengan ukuran panjang, lebar, dan kedalaman masing-masing 3.0 meter,
untuk mencegah agar ikan uji tidak melompat ke luar wadah (Gambar 2). Untuk
pemijahan digunakan akuarium sebanyak 40 buah dengan ukuran 60 X 50 X 50 cm
yang dilengkapi dengan pipa-pipa aerasi. Akuarium tersebut juga akan digunakan
untuk proses inkubasi, penetasan telur, dan pemeliharaan larva.
[image:40.612.122.507.162.410.2]Gambar 2. Wadah penelitian yang terbuat dari bambu dengan 12 jaring apung
dengan ukuran 3 X 2 X 2 m yang di atasnya ditutupi dengan jaring
Tabel 1. Komposisi bahan pakan dengan penambahan
ascorbyl phosphate
magnesium
(APM) 0, 600, 1200, dan 1800 mg/kg pakan
Persentase
Ascorbyl Phosphate Magnesium
(APM)
Bahan Pakan (%)
0
600
1200
1800
Tepung ikan
23.28
23.28
23.28
23.28
Tepung kedelai
28.08
28.08
28.08
28.08
Pollard
36.29
36.29
36.29
36.29
Minyak ikan
1.37
1.37
1.37
1.37
Minyak jagung
1.37
1.37
1.37
1.37