Lampiran 1. (lanjutan)
29 38 0,435
30 39 0,435
Lampiran 3. Perhitungan Persamaan Regresi
Maka persamaan regresinya adalah y = 0,00738 x – 0,0038025
r = Σ��−(Σ�)(Σ�)/�
[(ΣX2)−(Σ�)2/�][(ΣY2)−(Σ�)2/�]
= 9,8680 −(25)(1,8220 )/6
�(135)–(25)2/6�[(0,7215 )−(1,8220 )2/6]
Lampiran 4. Contoh Perhitungan Kadar Kuning Metanil pada Sampel Berat sampel yang ditimbang = 47,7413 g
Serapan (y) = 0,246
Persamaan regresi y = 0,0738 x – 0,0038 0,246 = 0,0738 x – 0,0038 X = 0246 + 0,0038
0,0738
X = 3,384 mcg/ml
Rumus Perhitungan Kadar Kuning Metanil = ������
��
Di mana K = Kadar total Kuning Metanil dalam sampel (mcg/g) X = Kadar Kuning Metanil setelah pengenceran (mcg/ml) V = Volume Sampel (ml)
Lampiran 4. (lanjutan)
Kadar Total Kuning Metanil = 3,384 ���/��� 50 ��� 25/3,5
47 ,7413 �
= 25,315 mcg/g
Lampiran 5. (lanjutan)
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = 5 diperoleh nilai
t[1-(α/2)],dk= 4,032. Data diterima jika thitung< ttabel thitung = ��−�
��/√6
thitung data 1 = 0,142 thitung data 4 = 0,332 thitung data 2 = 3,665 thitung data 5 = 1,390 thitung data 3 = 3,523 thitung data 6 = 1,438
(Semua Data Diterima)
Lampiran 6. Hasil Analisa Kadar Kuning Metanil dalam Sampel 1. Hasil Analisa Kadar Kuning Metanil dalam Sampel II No. Berat
Lampiran 7. Perhitungan Perolehan Kembali (%) Kadar Kuning Metanil
Keterangan : CF = Kadar sampel yang diperoleh setelah penambahan larutan baku
CA = Kadar sampel yang diperoleh sebelum penambahan larutan baku
C*A = Kadar larutan baku yang ditambahkan
Lampiran 11. Pemerian Kuning Metanil BPFI (Baku Pembanding)
Lampiran 12. Larutan Induk Baku dan Larutan Kurva Kalibrasi
Larutan Induk Baku I (1000 ppm) Larutan Induk Baku II (50 ppm)
Lampiran 13. Benang Wool dan Hasil Ekstraksi Warna
Benang Wool
Hasil Penarikan Warna Sampel I Hasil Penarikan Warna Sampel II
Hasil Penarikan Warna Sampel III Hasil Penarikan Warna Sampel IV
Lampiran 14. Hasil Uji Kualitatif secara Metode Reaksi Warna
Hasil Uji Kualitatif Baku Pembanding
Hasil Uji Sampel I Hasil Uji Sampel II Hasil Uji Sampel III
Lampiran 15. Hasil Uji Kualitatif secara Spektrofotometri Sinar Tampak
Hasil Uji Kualitatif Sampel II secara Spektrofotometri
Lampiran 16. Sampel dan Larutan Uji Sampel
Sampel Sirup (I, II, III, IV dan V)
Lampiran 16. (lanjutan)
Lampiran 17. Alat Spektrofotometer dan Neraca Analitik
Alat Spektrofotometer
DAFTAR PUSTAKA
Aldrich. (1992). Aldrich Chemical Catalogue. Milwaukee: Aldrich Chemical Company. Hal. 1
Anonima, (2014). Aditif Makanan. [Diakses Tanggal 1 September 2014].
Anonimb, (2014). Dye. [Diakses Tanggal 1 September 2014].
Anonimc, (2014). Makanan September 2014].
http://id.wikipedia.org/wiki/Makanan.
Ayuningtyas, S. (2013). Kadar Formalin dan Metanil Yellow dalam Mi Basah yang beredar di Pasaran Secara Kromatografi Cair Kinerja Tinggi. Jurnal Penelitian. Vol. 2(2): 4.
BPOM. (2012). Bahaya Keracunan Metanil Yellow pada Pangan. [Diakses tanggal
25 Agustus 2014].
Cahyadi, W. (2009). Bahan Tambahan Pangan. Edisi Kedua. Jakarta: PT Bumi Aksara. Hal. 1-4, 61-65.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Ke-IV. Jakarta: Departemen Kesehatan Republik Indonesia. Hal. 1066, 1126, 1130-1133, 1183.
Ermer, J., dan McB. Miller, J.H. (2005). Method Validation in Pharmaceutical Analysis. A Guide to Best Practice. Weinheim: Wiley-VCH. Hal. 16.
Gandjar, I.G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 228-229, 241-243, 252-256, 262.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metoda dan Cara Perhitungannya. Jakarta: Departemen Farmasi FMIPA UI. Hal.117-133. Moutinho, I.L.D., Bertges, L.C.,dan Assis, R.V.C. (2007). Prolonged Use of The
Food Dye Tartrazine (FD&C Yellow No. 5) And Its Effects on The Gastric Mucosa of Wistar rats. Braz. J. Biol. 67(1): 141-145.
Munson, J. W. (1991). Pharmaceutical Analysis Modern Methods. Part B. Penerjemah: Harjana. Analisis Farmasi Metode Modern. Parwa B. Surabaya: Universitas Airlangga Press. Hal. 334.
Nath, P.P., Kaushik S. and Panchali T. (2013). Development of a Visible Spectrophotometric Method for the Quantitative Determination of Metanil Yellow in Different Food Samples. Int J Pharm Bio Sci. 4(2): 687.
Sigar, E.S., Gayatri, C., dan Adithya, Y. (2012). Analisis Zat Warna Methanyl Yellow dalam Minuman Sirup di Kawasan Kota Manado. Jurnal Penelitian. FMIPA UNSRAT. Vol. 1(2): 105-106.
Sudjana. (2005). Metode Statistika. Bandung: Penerbit Tarsito. Hal.93, 145, 201, 225.
Wahyuni, I. (2013). Pemeriksaan Kandungan Pemanis dan Pewarna Sintetik dalam Es Lilin Tidak Bermerek dan Tidak Berlabel yang Diproduksi oleh Industri Rumah Tangga “X” Kecamatan Ambulu-Jember. Jurnal Ilmiah. Fakultas Farmasi Universitas Surabaya. Vol. 2(2): 15.
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah metode penelitian deskriptif. Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif Fakultas Farmasi Universitas Sumatera Utara dan di Laboratorium Kimia Farmasi Kuantitatif Fakultas Farmasi Universitas Sumatera Utara.
3.1 Bahan-Bahan 3.1.1 Sampel
Sampel yang digunakan adalah sediaan minuman yang terdapat di pasaran di wilayah Kota Medan.
3.1.2 Pengambilan sampel
Pengambilan sampel didasarkan pada minuman yang pada kemasannya tidak memiliki merek serta tidak mencantumkan nomor izin edar. Metode pengambilan sampel dilakukan secara purposif, yaitu metode pengambilan sampel ditentukan atas dasar pertimbangan bahwa sampel tersebut dapat mewakili sampel lainnya (Sudjana, 2005).
3.1.3 Bahan
Bahan-bahan yang digunakan dalam penelitian ini jika dinyatakan lain adalah berkualitas pro analis (E. Merck), yaitu Eter, Natrium Hidroksida, Asam Asetat, Amoniak, Asam Klorida, Etanol, Akuades dan Benang Wool.
3.2 Alat-Alat
Alat-alat yang digunakan terdiri dariSpektrofotometer UV-Visible (Hitachi U-2900), neraca analitik (Mettler Teledo), bola karet, maat pipet, pipet volume, tabung reaksi, alat-alat gelas seperti gelas ukur, gelas beaker, batang pengaduk, vial, pinset dan penjepit tabung.
3.3 Pembuatan Pereaksi
3.3.1 Pembuatan larutan asam klorida 0,1 N
Dilarutkan 8,3 ml asam klorida 37% b/b ke dalam 1000 ml akuades (Ditjen POM, 1995).
3.3.2 Pembuatan larutan amoniak 10% v/v
Dilarutkan 400 ml amoniak25% b/bdalam 1000 ml akuades(Ditjen POM, 1995).
3.3.3 Pembuatan larutan natrium hidroksida 1% b/v
Dilarutkan 1 g natrium hidroksida kemudian ditambahkan akuades bebas CO2 sampai 100 ml (Ditjen POM, 1995).
3.3.4 Pembuatan larutan asam asetat 10% v/v
3.4 Prosedur Penelitian 3.4.1 Pembuatan larutan uji
Larutan uji dibuat dengan menggunakan metode ekstraksi warna untuk tujuan ekstraksi pemisahan zat warna yang terdapat dalam sampel minuman yaitu:
Digunting benang wool dengan ukuran 15 cm untuk setiap pemakaian masing-masing sampel. Dididihkan dalam akuades kemudian dikeringkan. Dicuci dengan eter untuk menghilangkan kotoran dan lemak. Kemudian dididihkan dengan NaOH 1% dan dibilas dengan akuades.
Ditambahkan 5 ml asam asetat 10% pada masing-masing 50 ml sampel minuman. Dimasukkan benang wool pada sampel dan dididihkan selama 10 menit, kemudian diangkat benang wool (zat warna dalam sampel minuman akan mewarnai benang wool). Dicuci benang wool dengan akuades, kemudian dimasukkan 50 ml amoniak dan dididihkan sampai dilihat warna yang berada dalam benang wool luntur atau telah tertarik dalam larutan basa. Larutan basa yang diperoleh merupakan satu larutan uji dalam berbagai warna kuning yang akan digunakan sebagai cuplikan/larutan uji (Sigar, dkk., 2012).
3.4.2 Analisis kualitatif kuning metanil
Pemeriksaan kualitatif kuning metanil pada sampel menggunakan Metode Reaksi Warna dan Spektrofotometri Sinar Tampak.
3.4.2.1 Metode reaksi warna
Dimasukkan 1 tetes larutan baku pembanding kuning metanil ke dalam tabung reaksi kemudian ditambahkan 1 ml HCl 0,1 N akan terbentuk warna ungu (Nath, et al., 2013).
Kemudian diamati warna yang terjadi pada sampel dan dibandingkan dengan warna yang dihasilkan oleh baku pembanding.
3.4.2.2 Spektrofotometri sinar tampak
Prinsip dari metode ini adalah dengan membandingkan kurva absorbansi yang dihasilkan dari sampel dengan baku pembanding yang diukur dengan spektrofotometer sinar tampak pada panjang gelombang 400-750 nm.
3.4.3 Analisis kuantitatif kuning metanil
Penetapan kadar kuning metanil pada sampel dimulai dengan pembuatan larutan baku pembanding kuning metanil, penentuan panjang gelombang, penentuan waktu kerja, kurva kalibrasi larutan kuning metanil dan penetapan kadar kuning metanil pada sampel.
3.4.3.1 Pembuatan larutan induk baku pembanding
Ditimbang dengan seksama 50 mg pewarna kuning metanil BPFI kemudian dimasukkan ke dalam labu tentukur 50 ml, kemudian ditambahkan etanol sampai garis tanda dan dikocok hingga homogen. Diperoleh larutan dengan konsentrasi 1000 ppm, larutan ini disebut larutan induk baku I (LIB I).
3.4.3.2 Penentuan panjang gelombang maksimum
Dipipet 3 ml dari larutan induk baku II dengan menggunakan maat pipet dan dimasukkan ke dalam labu tentukur 25 ml, lalu ditambahkan etanol sampai garis tanda dan dihomogenkan (konsentrasi 6 ppm). Diukur serapan maksimum pada panjang gelombang 400-750 nm, dengan menggunakan blanko. Sebagai blanko digunakan etanol.
3.4.3.3 Penentuan waktu kerja (operating time)
Dipipet 3 ml dari larutan induk baku II dengan menggunakan maat pipet dan dimasukkan ke dalam labu tentukur 25 ml, lalu ditambahkan etanol sampai garis tanda dan dihomogenkan(konsentrasi 6 ppm). Diukur pada panjang gelombang maksimum yang diperoleh selama 30 menit.
3.4.3.4 Penentuan kurva kalibrasi
Dari larutan induk baku II dipipet sebanyak 1,5 ml; 2 ml; 2,5 ml; 3 ml; dan 3,5 ml dengan menggunakan maat pipet dan dimasukkan ke dalam labu tentukur 25 ml dan masing-masing ditambahkan etanol sampai garis tanda dan dikocok homogen (konsentrasi masing-masing larutan 3 ppm; 4 ppm; 5 ppm; 6 ppm; dan 7 ppm), kemudian diukur serapannya pada panjang gelombang maksimum yang diperoleh dan sebagai blanko digunakan etanol akan diperoleh kurva konsentrasi vs absorban.
3.4.3.5 Penentuan kadar kuning metanil pada sampel
dihomogenkan. Kemudian diukur pada panjang gelombang maksimum 416 nm dan sebagai blanko digunakan etanol. Dilakukan pengulangan sebanyak 6 kali.
Konsentrasi kuning metanil dalam sampel dapat ditentukan berdasarkan persamaan linier kurva kalibrasi y = ax + b, dan kadar kuning metanil dalam sampel ditentukan dengan menggunakan rumus :
Rumus Perhitungan Kadar Kuning Metanil � = ���������
Keterangan : Cs = kadar kuning metanil sesudah pengenceran (mcg/ml) V = volume sampel (ml)
Fp = Faktor pengenceran Bs = Berat sampel (g)
3.5Uji Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi dan Batas Kuantitasi
Validasi dilakukan untuk menjamin bahwa metode analisis yang dilakukan akurat, spesifik, reprodusibel dan tahan kisaran analit yang akan dianalisis. Uji validasi yang digunakan yaitu uji akurasi dengan parameter uji perolehan kembali, uji presisi, batas deteksi dan batas kuantitasi (Harmita, 2004).
3.5.1 Penentuan uji perolehan kembali (recovery)
Uji perolehan kembali dilakukan dengan menambahkan larutan baku kuning metanil berkonsentrasi 50 mcg/ml sebanyak 1,7 ml ke dalam sampel dan dianalisis dengan perlakuan yang sama pada sampel.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali = CF- CA
�∗A ×100%
Keterangan: CF = Kadar sampel setelah penambahan larutan baku (mcg/g) CA = Kadar sampel sebelum penambahan larutan baku (mcg/g) C* A = Kadar larutan baku yang ditambahkan (mcg/g)
3.5.2 Uji ketelitian
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
3.5.3 Penentuan batas deteksi (limit of detection) dan batas kuantitasi (limit of quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (
3.6 Analisis Data secara Statistik
Menurut Sudjana (2005), kadar kuning metanil yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis dengan metode standar deviasi dengan rumus:
�� = �∑(�� − ��)
� −1
Keterangan :
Xi = Kadar sampel (mcg/g)
Untuk mencari t hitung digunakan rumus: �ℎ����� = �� − ��
�� √�⁄
Untuk menentukan kadar kuning metanil di dalam sampel dengan interval kepercayaan 99%, α = 0,01, dk = n-1, dapat digunakan rumus:
Kadar kuning metanil (μ) = X ± (t(α/2, dk) x SD /√�) Keterangan :
X = Kadar rata-rata kuning metanil dalam sampel (mcg/g) SD = Standar Deviasi (mcg/g)
dk = Derajat kebebasan (dk = n-1) α = Interval kepercayaan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pemeriksaan Kualitatif Kuning Metanil pada Sampel
Pada penelitian ini sebelum dilakukan analisis kuantitatif kuning metanil pada sampel, perlu dilakukan identifikasi untuk mengetahui ada tidaknya kuning metanil pada sampel dengan menggunakan metode reaksi warna dan metode spektrofotometri sinar tampak pada sampel diperoleh data dan gambar kurva serapan seperti yang ditunjukkan pada Tabel 4.1, Gambar 4.1 dan Gambar 4.2.
Identifikasi kuning metanil dengan Metode Reaksi Warna dilakukan dengan membandingkan warna yang dihasilkan setelah penambahan HCl 0,1 N dari sampel dengan baku pembanding. Selain identifikasi dengan Metode Reaksi Warna juga digunakan identifikasi dengan Spektrofotometri Sinar Tampak yaitu dengan membandingkan kurva absorbansi pada panjang gelombang 400-750 nm (Gandjar dan Rohman, 2007).
Y X1 X2
Gambar 4.1 Hasil uji kualitatif kuning metanil pada sampel Keterangan : Y = Baku Pembanding
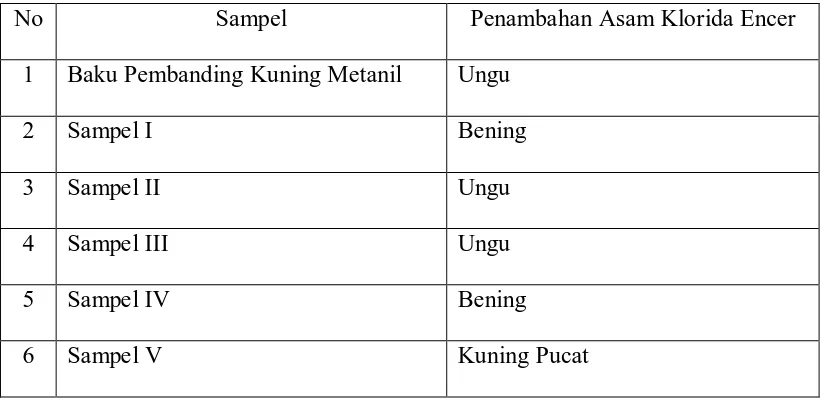
Tabel 4.1 Hasil pemeriksaan kualitatif kuning metanil pada sampel dengan metode reaksi warna
No Sampel Penambahan Asam Klorida Encer
1 Baku Pembanding Kuning Metanil Ungu
2 Sampel I Bening
3 Sampel II Ungu
4 Sampel III Ungu
5 Sampel IV Bening
6 Sampel V Kuning Pucat
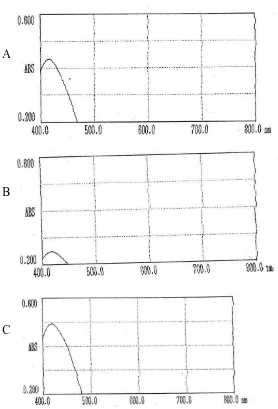
A
B
C
4.2 Penetapan Kadar
4.2.1 Panjang gelombang maksimum larutan baku kuning metanil
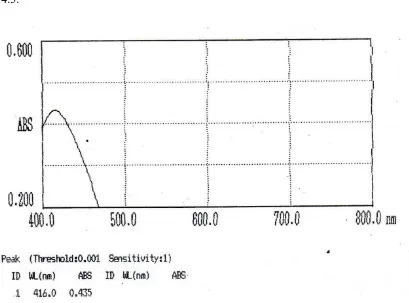
Penentuan panjang gelombang maksimum larutan kuning metanil dilakukan pada konsentrasi 6 ppm dengan rentang panjang gelombang 400-800 nm. Hal ini dilakukan karena larutan kuning metanil merupakan larutan berwarna. Sinar tampak mempunyai panjang gelombang 400-750 nm. Selain itu pengukuran dilakukan pada rentang tersebut karena pada panjang gelombang maksimum kepekaannya juga maksimum dan disekitar panjang gelombang maksimum bentuk kurva absorbansi datar dan pada kondisi tersebut hukum Lambert-Beer akan terpenuhi (Gandjar dan Rohman, 2007). Kurva serapan larutan kuning metanil dapat dilihat pada Gambar 4.3.
Hasil penentuan panjang gelombang maksimum larutan kuning metanil dengan konsentrasi 6 ppm, diperoleh λ maksimum pada 416 nm. Panjang
gelombang maksimum yang diperoleh ini berbeda dengan yang terdapat dalam literatur yaitu 414 nm (Aldrich, 1992). Perbedaan panjang gelombang sebesar 2 nm masih dalam batas toleransi yang diperkenankan menurut Farmakope Indonesia Edisi IV (1995) yaitu lebih kurang 3 nm. Hal ini berarti bahwa panjang gelombang ini dapat diterima untuk analisis kuning metanil pada sampel.
4.2.2 Hasil waktu kerja larutan kuning metanil
Pada penelitian dilakukan penentuan waktu kerja karena kuning metanil merupakan senyawa berwarna dan mudah teroksidasi sehingga semakin lama senyawa tersebut terurai, intensitas warnanya turun dan mempengaruhi absorbansi yang didapat (Gandjar dan Rohman, 2007). Pada penentuan waktu kerja larutan baku kuning metanil diperoleh waktu pengukuran yang stabil dimulai dari menit ke-17 sampai menit ke-27. (Data pengamatan pada Lampiran 1)
4.2.3 Kurva kalibrasi larutan kuning metanil
Gambar 4.4 Kurva kalibrasi larutan kuning metanil dengan berbagai konsentrasi secara spektrofotometri sinar tampak pada panjang gelombang 416 nm
Dari hasil perhitungan persamaan regresi kurva kalibrasi di atas diperoleh persamaan garis y = 0,0738 x – 0,00380246 dengan koefisien korelasi (r) sebesar 0,9996. Dari hasil tersebut dikatakan bahwa terdapat korelasi positif antara kadar dan serapan. Artinya, meningkatnya konsentrasi maka absorbansi juga akan meningkat. Hal ini berarti terdapat 99,96% data yang memiliki hubungan linier (Sudjana, 2005).
4.2.4. Penetapan kadar kuning metanil pada sampel
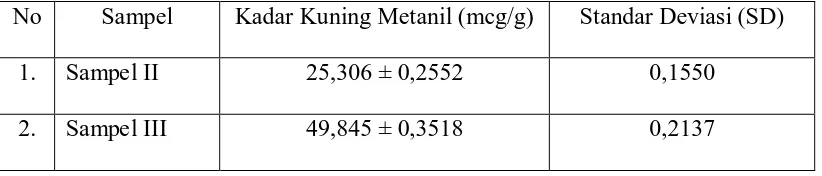
Tabel 4.2 Kadar kuning metanil pada sampel
No Sampel Kadar Kuning Metanil (mcg/g) Standar Deviasi (SD)
1. Sampel II 25,306 ± 0,2552 0,1550
2. Sampel III 49,845 ± 0,3518 0,2137
Dari Tabel 4.2 dapat dilihat bahwa kadar kuning metanil pada sampel II dan III adalah 25,306 mcg/g dan 49,845 mcg/g. Hal ini sangat membahayakan konsumen karena LD50 dari kuning metanil adalah 1000 mg/kg, dalam jumlah kecil akan menyebabkan mual, muntah, sakit perut, diare, demam, lemah, hipotensi dan iritasi saluran cerna (BPOM, 2012). Apabila kadar kuning metanil mencapai LD50 maka akan menyebabkan kanker dan mutasi (Patnaik, 2007).
4.3 Uji Validasi Metode Analisis
Pada penelitian ini dilakukan juga uji validasi metode dengan maksud untuk melihat sejauh mana kebenaran metode yang digunakan. Salah satu uji validasi tersebut adalah uji perolehan kembali. Adapun uji akurasi dengan parameter persen perolehan kembali dan presisi dengan parameter Relatif Standar Deviasi (RSD) dan Standar Deviasi (SD).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Minuman yang berwarna kuning mengandung zat pewarna tekstil kuning metanil.
2. Dari hasil penelitian diperoleh kadar kuning metanil dalam sampel II dan III berturut-turut adalah 25,306 ± 0,2552 mcg/g dan 49,845 ± 0,3518 mcg/g.
5.2 Saran
1. Untuk penelitian selanjutnya, diharapkan untuk memeriksa zat warna kuning metanil pada produk pangan lainnya, seperti tahu, kerupuk, mi basah dan gorengan.
BAB II
TINJAUAN PUSTAKA
2.1 Pangan
Pangan adalah bahan (biasanya berasal dari hewan dan tumbuhan) yang dimakan/diminum oleh makhluk hidup untuk memberikan tenaga dan nutrisi. Pangan yang dibutuhkan manusia biasanya diperoleh melalui bertani atau berkebun yang meliputi sumber hewan dan tumbuhan. Pada umumnya bahan pangan mengandung air, karbohidrat, protein, lemak, vitamin, enzim, pigmen dan lain-lain. Pangan dari sumber tumbuhan yang sering dikonsumsi manusia yaitu buah, sayuran, biji-bijian, kacang-kacangan dan bumbu, sedangkan pangan dari sumber hewan yaitu daging, produk telur dan susu (Anonimc, 2014).
2.2 Bahan Tambahan Pangan (BTP)
Menurut Cahyadi (2009), pada umumnya bahan tambahan terbagi menjadi dua golongan besar, yaitu sebagai berikut:
1. Bahan tambahan pangan yang ditambahkan secara sengaja ke dalam makanan, dengan mengetahui komposisi bahan tersebut dan maksud penambahan itu dapat mempertahankan kesegaran, cita rasa, dan membantu pengolahan, sebagai contoh pengawet, pewarna dan pengeras.
2. Bahan tambahan pangan yang tidak sengaja ditambahkan, yaitu bahan yang tidak mempunyai fungsi dalam makanan tersebut, terdapat secara tidak sengaja, baik dalam jumlah sedikit atau cukup banyak akibat perlakuan selama proses produksi, pengolahan dan pengemasan. Bahan ini dapat pula merupakan residu/kontaminan dari bahan yang sengaja ditambahkan untuk tujuan produksi bahan mentah atau penanganannya yang masih terus terbawa ke dalam makanan yang akan dikonsumsi. Contoh bahan tambahan pangan dalam golongan ini adalah residu pestisida (termasuk insektisida, herbisida, fungisida dan rodentisida) dan antibiotik.
Di Indonesia telah disusun peraturan tentang Bahan Tambahan Pangan yang diizinkan ditambahkan dan yang dilarang (disebut Bahan Tambahan Kimia) oleh Departemen Kesehatan diatur dengan Peraturan Menteri Kesehatan Republik Indonesia Nomor 722/Menkes/Per/IX/88, terdiri dari golongan BTP yang diizinkan di antaranya sebagai berikut:
1. Antioksidan (antioxidant) 2. Antikempal (anticaking agent)
3. Pengatur keasaman (acidity regulator) 4. Pemanis buatan (artificial sweeterner)
5. Pemutih dan pematang telur (flour treatment agent)
6. Pengemulsi, pemantap dan pengental (emulsifier, stabilizer, thickener) 7. Pengawet (preservative)
8. Pengeras (firming agent) 9. Pewarna (colour)
10.Penyedap rasa dan aroma, penguat rasa (flavour, flavour enhancer) 11.Sekuestran (sequestrant)
(pewarna kuning), Dulsin (pemanis sintetis) dan Kalium bromat (pengeras) (Cahyadi, 2009).
Sejak pertengahan abad ke-20 ini, peranan bahan tambahan pangan menjadi semakin penting sejalan dengan kemajuan teknologi produksi bahan tambahan pangan sintetis. Banyaknya bahan tambahan pangan dalam bentuk murni dan tersedia secara komersil dengan harga yang relatif murah akan mendorong meningkatnya konsumsi bahan tersebut bagi setiap individu. Penggunaan bahan tambahan pangan (BTP) dalam proses produksi pangan perlu diwaspadai bersama, baik oleh produsen maupun oleh konsumen. Dampak penggunaannya dapat berakibat positif maupun negatif bagi masyarakat. Penyimpangan dalam penggunaannya akan membahayakan kita, khususnya generasi muda. Di bidang pangan kita memerlukan sesuatu yang lebih baik untuk masa yang akan datang, yaitu pangan yang aman dikonsumsi, lebih bermutu, bergizi dan lebih mampu bersaing dalam pasar global (Cahyadi, 2009).
Zat aditif pangan juga dapat menyebabkan penyakit jika tidak digunakan sesuai dosis, terutama zat aditif pangan sintetis. Penyakit yang biasa timbul dalam jangka waktu lama setelah pengunaan zat aditif pangan adalah kanker dan kerusakan ginjal (Anonima, 2014).
2.3 Pewarna Bahan Pangan
yang menentukan mutu, warna juga dapat digunakan sebagai indikator kesegaran. Baik tidaknya cara pencampuran atau cara pengolahan dapat ditandai dengan adanya warna yang homogen dan merata (Cahyadi, 2009).
Pewarna telah digunakan sejak zaman purbakala. Pewarna biasa diperoleh dari hewan, tumbuhan atau mineral tanpa harus diproses. Umumnya, sumber utama pewarna didapat dari tumbuhan, yaitu dari akar, buah, daun, dan kayu tetapi hanya sedikit yang diperdagangkan. Beberapa pewarna dapat mengendap jika direaksikan dengan garam inert. Secara umum, pewarna terbagi menjadi pewarna alami dan pewarna buatan (sintetis) (Anonimb, 2014).
2.3.1 Pewarna alami
Banyak warna cemerlang yang dijumpai pada hewan dan tumbuhan dapat digunakan sebagai pewarna untuk pangan. Beberapa pewarna alami memberikan nutrisi (karotenoid, riboflavin dan kobalamin), merupakan bumbu (kunir dan paprika) atau pemberi rasa (karamel) ke bahan olahan. Konsumen dewasa ini banyak menginginkan bahan alami dalam diet mereka. Banyak pewarna olahan yang awalnya menggunakan pewarna sintetis berpindah ke pewarna alami. Contohnya penggunaan serbuk beet menggantikan pewarna merah sintetis FD & C No. 2. Beberapa pewarna alami yang berasal dari tumbuhan dan hewan diantaranya klorofil, mioglobin dan hemoglobin, antosianin, flavonoid, tanin, betalain, quinon dan xanthon, serta karotenoid (Cahyadi, 2009).
2.3.2 Pewarna buatan (sintetis)
color. Zat warna yang akan digunakan harus menjalani pengujian dan prosedur
penggunaannya, yang disebut proses sertifikasi. Proses sertifikasi ini meliputi pengujian kimia, biokimia dan toksikologi terhadap zat tersebut (Yuliarti, 2007).
Di Indonesia, peraturan mengenai penggunaan zat pewarna yang diizinkan dan dilarang untuk pangan diatur melalui SK Menteri Kesehatan RI Nomor 722/Menkes/Per/IX/88 mengenai bahan tambahan pangan. Beberapa contoh zat pewarna yang diizinkan yaitu Biru berlian, Eritosin, Hijau FCF, Indigotin dan Tartrazine. Sedangkan contoh pewarna yang dilarang yaitu Rhodamin B, Kuning metanil dan Amaran. Akan tetapi, seringkali terjadi penyalahgunaan pemakaian zat pewarna untuk pangan, misalnya zat pewarna untuk tekstil dan kulit dipakai untuk mewarnai bahan pangan. Hal ini jelas berbahaya bagi kesehatan karena adanya residu logam berat pada zat pewarna tersebut. Timbulnya penyalahgunaan tersebut antara lain disebabkan oleh ketidaktahuan masyarakat mengenai zat pewarna untuk pangan, dan di samping itu harga zat pewarna untuk industri jauh lebih murah dibandingkan dengan harga zat pewarna untuk pangan juga warna dari zat pewarna tekstil lebih menarik (Cahyadi, 2009).
2.4 Kuning Metanil (Methanyl Yellow)
Demi perlindungan terhadap kesehatan dan keselamatan konsumen, Balai POM meminta produsen pangan tidak menggunakan bahan kimia yang dilarang untuk pangan. Demikian juga, Balai POM meminta toko pengencer bahan kimia untuk tidak menjual bahan kimia yang dilarang kepada konsumen. Menurut Yuliarti (2007), monografi dari kuning metanil adalah sebagai berikut:
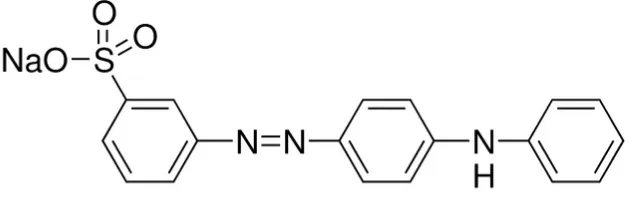
Kuning Metanil (Methanyl Yellow)
Gambar 2.1 Rumus bangun kuning metanil
Nama Kimia : 3-(4-Anilinophenylazo)benzenesulfonic acid sodium salt Nama Lazim : Methanyl Yellow; Acid Yellow 36; C.I. 13065
Rumus Kimia : C18H14N3NaO3S
BM : 375,38
Pemerian : Serbuk kuning kecoklatan
Kelarutan : Larut dalam air, agak larut dalam benzen, eter dan sedikit larut dalam aseton .
Penggunaan : Sebagai pewarna tekstil dan cat.
2.5 Spektrofotometri
panjang gelombang 400-750 nm. Menurut Gandjar dan Rohman (2007), hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan dan berbanding terbalik dengan transmitan. Hukum tersebut dituliskan dengan : A = abc = log 1/T Keterangan : A = absorbans a = koefisien ekstingsi b = tebal sel (cm) c = konsentrasi analit.
Penyerapan radiasi sinar ultraviolet dan sinar tampak oleh spesies atom atau molekul (M) dapat dipertimbangkan sebagai proses 2 langkah; yang pertama adalah melibatkan eksitasi sebagaimana ditunjukkan oleh persamaan berikut:
M + hv M*
Hasil reaksi antara M dengan foton (hv) merupakan partikel yang tereksitasi secara elektronik yang disimbolkan dengan M*. Waktu hidup M* sangat pendek (10-8 – 10-9 detik), dan keberadaannya dapat diakhiri dengan berbagai macam proses relaksasi. Kebanyakan tipe relaksasi melibatkan konversi energi eksitasi menjadi panas, sesuai dengan persamaan berikut:
M* M + panas
Relaksasi juga dapat terjadi dengan terdekomposisinya M* membentuk spesies baru, sebagaimana suatu proses yang disebut dengan reaksi fotokimia. Alternatifnya, relaksasi juga melibatkan emisi radiasi kembali yang dikenal dengan fluorosensi dan fosforesensi (Gandjar dan Rohman, 2007).
tampak yaitu penyerapan oleh transisi elektron ikatan dan elektron anti ikatan, penyerapan oleh transisi elektron d dan f dari molekul kompleks serta penyerapan oleh perpindahan muatan (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), terdapat beberapa hal yang harus diperhatikan dalam analisis dengan spektrofotometri ultraviolet dan cahaya tampak terutama untuk senyawa yang tidak berwarna yang akan dianalisis yaitu:
1. Pembentukan molekul yang dapat menyerap sinar UV-Vis
Cara yang digunakan adalah dengan merubahnya menjadi senyawa lain atau direaksikan dengan pereaksi tertentu sehingga dapat menyerap sinar UV-Vis 2. Waktu kerja (operating time)
Tujuannya ialah untuk mengetahui waktu pengukuran yang stabil. Waktu kerja ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan.
3. Pemilihan panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi maksimal.
4. Pembuatan kurva baku
Dilakukan dengan membuat seri larutan baku dalam berbagai konsentrasi kemudian absorbansi tiap konsentrasi diukur lalu dibuat kurva yang merupakan hubungan antara absorbansi dengan konsentrasi.
5. Pembacaan absorbansi sampel
Instrumentasi untuk Spektrofotometri
Gambar 2.2 Diagram skematis spektrofotometer UV-Vis (Sumber : Gandjar dan Rohman, 2007)
Menurut Gandjar dan Rohman (2007), komponen spektrofotometer ultraviolet/sinar tampak terdiri dari:
a. Sumber Cahaya
Sumber energi radiasi yang biasa untuk daerah ultraviolet dan daerah cahaya tampak adalah sebuah lampu wolfram ataupun lampu tabung discas hidrogen (atau deutrium).
b. Monokromator
Monokromator berfungsi mengubah cahaya polikromatis menjadi cahaya yang monokromatis. Alatnya dapat berupa berupa prisma atau kisi difraksi.
c. Sel
d. Detektor
Peranan detektor adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang. Detektor yang paling sederhana dipakai ialah tabung foto. e. Recorder
Recorder digunakan sebagai perekam absorbansi yang dihasilkan dari pengukuran.
2.6 Validasi
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004). 2.6.1 Perolehan kembali
Uji perolehan kembali dilakukan dengan metode penambahan larutan baku (standard addition method). Dalam metode ini, kadar kuning metanil dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar kuning metanil dalam sampel setelah penambahan larutan standar dengan konsentrasi tertentu. Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali = CF- CA
�∗A ×100%
2.6.2 Uji ketelitian
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan. Menurut Harmita (2004), simpangan baku relatif dapat dihitung dengan rumus di bawah ini:
2.6.3 Penentuan batas deteksi (limit of detection) dan batas kuantitasi (limit of quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama. Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
BAB I PENDAHULUAN
1.1Latar Belakang
Secara luas aditif pangan telah ada lebih dari 2.500 jenis yang digunakan untuk pengawet (preservative) dan pewarna (dye). Zat-zat aditif ini digunakan untuk mempertinggi nilai pangan sebagai konsekuensi dari industrialisasi dan perkembangan proses teknologi pangan (Moutinho, et al., 2007).
Pemerintah melalui Kementerian Kesehatan RI telah menetapkan peraturan terkait jenis pewarna yang diizinkan untuk digunakan pada pangan olahan serta batas maksimum penggunaannya. Hal ini sebagai langkah antisipatif untuk melindungi masyarakat dari bahaya keracunan pewarna yang marak beredar di pasaran. Di Indonesia, penggunaan pewarna pada pangan diatur dalam Peraturan Menteri Kesehatan Nomor 033 Tahun 2012 tentang Bahan Tambahan Pangan (BPOM, 2012).
Namun hingga kini konsumen masih dihadapkan pada masalah terkait penyalahgunaan pewarna pada pangan. Faktanya saat ini di pasaran masih banyak ditemukan pangan yang ditambahkan pewarna non pangan. Tingginya penggunaan bahan kimia yang dilarang untuk pangan, membuat Pemerintah mencanangkan Program Pasar Aman dari Bahan Berbahaya selama tiga tahun, mulai tahun 2013 hingga 2015, salah satunya adalah pewarna kuning metanil (BPOM, 2012).
disimpan sehingga warnanya menjadi tidak menarik. Pewarna sintetis memiliki tingkat stabilitas yang lebih baik sehingga warna lebih cerah meskipun sudah melalui proses pengolahan. Terdapat pewarna sintetis yang diperbolehkan tetapi ada juga yang dilarang seperti pewarna tekstil. Oleh sebab itu, hindari pangan dengan warna kuning yang mencolok, tidak menutup kemungkinan warna yang mencolok tersebut berasal dari pewarna tekstil kuning metanil yang berbahaya bagi kesehatan (Yuliarti, 2012).
Beberapa penelitian telah dilakukan terhadap mi basah di Bogor, Jakarta dan Depok menunjukkan bahwa mi basah di daerah tersebut masih mengandung kuning metanil (Ayuningtyas, 2012). Penelitian yang dilakukan terhadap es lilin berwarna kuning yang diproduksi oleh Industri Rumah Tangga “X” di Surabaya menunjukkan bahwa es lilin tersebut tidak layak diedarkan karena mengandung zat warna kuning metanil (Wahyuni, 2013).
1.2Perumusan Masalah
1. Apakah minuman yang berwarna kuning mengandung zat pewarna tekstil Kuning Metanil?
2. Berapakah kadar Kuning Metanil yang terdapat pada minuman yang ditentukan secara spektrofotometri sinar tampak?
1.3 Hipotesis
1. Minuman yang berwarna kuning mengandung zat pewarna tekstil Kuning Metanil.
2. Zat warna Kuning Metanil yang terdapat pada 9minuman terdapat dalam jumlah tertentu.
1.4Tujuan Penelitian
1. Melakukan uji kualitatif zat warna Kuning Metanil dalam minuman dengan metode reaksi warna.
2. Menentukan kadar zat warna Kuning Metanil dalam minuman dengan metode spektrofotometri sinar tampak.
1.5 Manfaat Penelitian
ANALISIS ZAT WARNA KUNING METANIL DALAM
MINUMAN DI KAWASAN KOTA MEDAN
ABSTRAK
Menurut Peraturan Menteri Kesehatan Nomor 033 Tahun 2012, kuning metanil telah dilarang penggunaannya di dalam makanan dan minuman. Beberapa penelitian menunjukkan bahwa di Indonesia kuning metanil masih digunakan di dalam berbagai produk makanan dan minuman seperti mi basah, es lilin dan minuman sirup. Tujuan penelitian ini adalah untuk melakukan pemeriksaan dan penetapan kadar kuning metanil pada minuman tanpa merek dan izin edar yang terdapat di pasaran Kota Medan.
Metode penelitian ini dilakukan dengan melakukan sampling pada beberapa pasar dan pemeriksaan kualitatif kuning metanil dengan metode reaksi warna dan spektrofotometri sinar tampak. Secara metode reaksi warna dengan menambahkan asam klorida encer akan menghasilkan warna ungu. Secara spektrofotometri sinar tampak diukur serapan maksimumnya pada panjang gelombang 400 - 750 nm. Penetapan kadar dilakukan secara spektofotometri sinar tampak pada panjang gelombang 416 nm.
Hasil penelitian menunjukkan bahwa dari lima sampel yang dilakukan pemeriksaan kualitatif terdapat dua sampel yang mengandung kuning metanil. Kadar kuning metanil pada sampel yang diperiksa adalah 25,306 ± 0,2552 mcg/g untuk Sampel II dan 49,845 ± 0,3518 mcg/g untuk Sampel III.
Dari hasil penelitian di atas dapat disimpulkan bahwa masih terdapat minuman yang berada di beberapa pasar di kota Medan yang menggunakan kuning metanil sebagai pewarnanya.
ANALYSIS OF METHANYL YELLOW DYE IN BEVERAGES
AT MEDAN CITY REGION
ABSTRACT
According to Ministry of Health Rule No. 033 (2012), the methanyl yellow has been prohibited its use in food and beverages. Some researches suggest that in Indonesia the methanyl yellow still be used in various food and beverage products such as noodles, ice lolly and syrup beverages. The objective of this study is to examine and quantitative analysis of methanyl yellow on beverages without brand and marketing authorization in Medan city market .
This research method is done by sampling at several markets and qualitative identification of methanyl yellow is done by color reaction method and visible spectrophotometry. In the color reaction method using dilute hydrochloric acid will be given violet. In visible spectrophotometry is measured at its maximum absorption wavelength 400 - 750 nm. Quantitative analysis was done by visible spectrophotometry maximum wavelength 416 nm.
The results indicated that from five samples done by qualitative identification, there are two samples containing methanyl yellow. Methanyl yellow concentration in Sample II was 25.306 ± 0.2552 mcg/g and Sample III was 49.845 ± 0.3518 mcg/g.
The results indicated that there are beverages in some markets in Medan that use methanyl yellow as dye.
ANALISIS ZAT WARNA KUNING METANIL DALAM MINUMAN
DI KAWASAN KOTA MEDAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
JIMMY ANGGA WINATA NIM 101501082
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
ANALISIS ZAT WARNA KUNING METANIL DALAM MINUMAN
DI KAWASAN KOTA MEDAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
JIMMY ANGGA WINATA NIM 101501082
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ANALISIS ZAT WARNA KUNING METANIL DALAM MINUMAN
DI KAWASAN KOTA MEDAN
OLEH:
JIMMY ANGGA WINATA NIM 101501082
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: 17 Oktober 2014
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas segala limpahan berkat, rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Analisis Zat Warna Kuning Metanil dalam Minuman di Kawasan Kota Medan.
USU yang telah memberikan izin dan fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda dan Ibunda yang telah memberikan cinta kasih yang tidak ternilai dengan apapun, doa yang tulus serta pengorbanan baik materi maupun non materi. Sahabat-sahabat reguler 2010, terimah kasih untuk dorongan, semangat dan kebersamaannya selama ini, serta seluruh pihak yang telah ikut membantu penulis yang tidak dapat disebutkan satu persatu.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, 17 Oktober 2014 Penulis,
ANALISIS ZAT WARNA KUNING METANIL DALAM
MINUMAN DI KAWASAN KOTA MEDAN
ABSTRAK
Menurut Peraturan Menteri Kesehatan Nomor 033 Tahun 2012, kuning metanil telah dilarang penggunaannya di dalam makanan dan minuman. Beberapa penelitian menunjukkan bahwa di Indonesia kuning metanil masih digunakan di dalam berbagai produk makanan dan minuman seperti mi basah, es lilin dan minuman sirup. Tujuan penelitian ini adalah untuk melakukan pemeriksaan dan penetapan kadar kuning metanil pada minuman tanpa merek dan izin edar yang terdapat di pasaran Kota Medan.
Metode penelitian ini dilakukan dengan melakukan sampling pada beberapa pasar dan pemeriksaan kualitatif kuning metanil dengan metode reaksi warna dan spektrofotometri sinar tampak. Secara metode reaksi warna dengan menambahkan asam klorida encer akan menghasilkan warna ungu. Secara spektrofotometri sinar tampak diukur serapan maksimumnya pada panjang gelombang 400 - 750 nm. Penetapan kadar dilakukan secara spektofotometri sinar tampak pada panjang gelombang 416 nm.
Hasil penelitian menunjukkan bahwa dari lima sampel yang dilakukan pemeriksaan kualitatif terdapat dua sampel yang mengandung kuning metanil. Kadar kuning metanil pada sampel yang diperiksa adalah 25,306 ± 0,2552 mcg/g untuk Sampel II dan 49,845 ± 0,3518 mcg/g untuk Sampel III.
Dari hasil penelitian di atas dapat disimpulkan bahwa masih terdapat minuman yang berada di beberapa pasar di kota Medan yang menggunakan kuning metanil sebagai pewarnanya.
ANALYSIS OF METHANYL YELLOW DYE IN BEVERAGES
AT MEDAN CITY REGION
ABSTRACT
According to Ministry of Health Rule No. 033 (2012), the methanyl yellow has been prohibited its use in food and beverages. Some researches suggest that in Indonesia the methanyl yellow still be used in various food and beverage products such as noodles, ice lolly and syrup beverages. The objective of this study is to examine and quantitative analysis of methanyl yellow on beverages without brand and marketing authorization in Medan city market .
This research method is done by sampling at several markets and qualitative identification of methanyl yellow is done by color reaction method and visible spectrophotometry. In the color reaction method using dilute hydrochloric acid will be given violet. In visible spectrophotometry is measured at its maximum absorption wavelength 400 - 750 nm. Quantitative analysis was done by visible spectrophotometry maximum wavelength 416 nm.
The results indicated that from five samples done by qualitative identification, there are two samples containing methanyl yellow. Methanyl yellow concentration in Sample II was 25.306 ± 0.2552 mcg/g and Sample III was 49.845 ± 0.3518 mcg/g.
The results indicated that there are beverages in some markets in Medan that use methanyl yellow as dye.
2.5 Spektrofotometri ... 10
2.6 Validasi ... 14
2.6.1 Perolehan kembali ... 14
2.6.2 Uji ketelitian ... 14
2.6.3 Penentuan batas deteksi (limit of detection) dan batas kuantitasi (limit of quantitation) ... 15
3.4.2 Analisis kualitatif kuning metanil ... 18
3.4.2.1 Metode reaksi warna ... 18
3.4.2.2 Spektrofotometri sinar tampak ... 19
3.4.3 Analisis kuantitatif kuning metanil ... 19
3.4.3.2 Penentuan panjang gelombang
maksimum ... 20
3.4.3.3 Penentuan waktu kerja (operating time) ... 20
3.4.3.4 Penentuan kurva kalibrasi ... 20
3.4.3.5 Penentuan kadar kuning metanil pada sampel ... 20
3.5 Uji Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi dan Batas Kuantitasi ... 21
3.5.1 Uji perolehan kembali (recovery) ... 21
3.5.2 Uji ketelitian ... 22
3.5.3 Penentuan batas deteksi (limit of detection) dan batas kuantitasi (limit of quantitation) ... 23
3.6 Analisis Data secara Statistik ... 23
BAB IV HASIL DAN PEMBAHASAN ... 25
4.1 Pemeriksaan Kualitatif Kuning Metanil pada Sampel ... 25
4.2 Penetapan Kadar ... 29
4.2.1 Panjang gelombang maksimum larutan baku kuning metanil ... 29
4.2.2 Hasil waktu kerja larutan kuning metanil ... 30
4.2.3 Kurva kalibrasi larutan kuning metanil ... 30
4.2.4 Penetapan kadar kuning metanil pada sampel ... 31
DAFTAR TABEL
Tabel Halaman 4.1 Hasil pemeriksaan kualitatif kuning metanil pada sampel
DAFTAR GAMBAR
Gambar Halaman 2.1 Rumus bangun kuning metanil ... 10 2.2 Diagram skematis spektrofotometer UV-Vis ... 13 4.1 Hasil uji kua litatif kuning metanil pada sampel ... 26 4.2 A adalah kurva serapan baku pembanding kuning metanil
(λmaks 416 nm), B adalah kurva serapan Sampel II dari Pasar Glugur (λmaks 417 nm), dan C adalah kurva serapan
Sampel III dari Pasar Sukaramai (λmaks 415 nm) ... 28 4.3 Kurva serapan maksimum larutan kuning metanil dengan
konsentrasi 6 ppm secara spektrofotometri sinar tampak
pada panjang gelombang 400 nm – 800 nm ... 29 4.4 Kurva kalibrasi larutan kuning metanil dengan berbagai
konsentrasi secara spektrofotometri sinar tampak pada