REAKSI PEWARNAAN AgNOR PADA
KARSINOMA SEL SKUAMOSA
RONGGA MULUT
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat guna memperoleh gelar Sarjana Kedokteran Gigi
Oleh :
Michelle Ding
NIM : 100600186
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
Fakultas Kedokteran Gigi
Bagian Biologi Oral
Tahun 2014
Michelle Ding
Reaksi Pewarnaan AgNOR pada Karsinoma Sel Skuamosa Rongga Mulut
xii + 46 halaman
Karsinoma sel skuamosa (KSS) merupakan salah satu jenis kanker yang
ditemukan di rongga mulut. Penyebab KSS adalah multifaktorial. KSS terjadi
akibat dari kerusakan genetik pada kromosom dan gen. Hal ini menyebabkan
perubahan molekular DNA pada nukleolus yang ada pada nukleus sel. Nukleolus
mempunyai bagian kromosom yang dinamakan nucleolar organizer region
(NOR) yang berperan dalam sintesis protein. NOR diamati sebagai titik-titik
hitam di bawah mikroskop cahaya dengan pewarnaan AgNOR. Pada sel normal,
hanya 1-2 titik hitam AgNOR yang diamati. Peningkatan titik-titik hitam AgNOR
mengindikasi perubahan sel normal menuju ke sel displastik/karsinoma dan juga
mencerminkan tingkat keburukan karsinoma. Tujuan penelitian ini adalah untuk
melihat distribusi frekuensi mean AgNOR (mAgNOR) pada nukleus preparat
KSS rongga mulut. Rancangan penelitian ini merupakan deskriptif analitik
dengan pendekatan cross sectional terhadap 30 sampel blok parafin yang
terdiagnosa sebagai KSS rongga mulut yang diperoleh dari Laboratorium
Patologi Anatomi FK USU/RSUP Haji Adam Malik Medan tahun 2009-2013,
Olympus CX21 terhadap 100 nuklei. Hasil penelitian menunjukkan adanya
perbedaan yang signifikan mAgNOR antara KSS sub-tipe diferensiasi baik dan
diferensiasi sedang (p=0,000), dan tidak ditemukan perbedaan yang signifikan
mAgNOR antara sub-tipe keratinisasi KSS (p=0,124), kelompok umur (p=0,964),
jenis kelamin (p=0,053) dan lokasi lesi (p=0,195). Kesimpulan penelitian ini
menunjukkan adanya peningkatan yang signifikan nilai mAgNOR pada KSS
diferensiasi sedang dibandingkan dengan KSS diferensiasi baik, dan tidak
adanya perbedaan yang signifikan nilai mAgNOR antara kelompok sub-tipe
keratinisasi KSS, umur, jenis kelamin dan lokasi lesi.
Kata Kunci: karsinoma sel skuamosa rongga mulut, pewarnaan AgNOR,
diferensiasi KSS
PERNYATAAN PERSETUJUAN
Skripsi ini telah disetujui untuk dipertahankan
di hadapan tim penguji skripsi
Medan, 25 September 2014
Pembimbing: Tanda tangan,
1.Rehulina Ginting, drg., MSi ...
NIP. 19511018 198003 2 001
2.dr. Betty, M.Ked.(PA),Sp.PA ...
TIM PENGUJI SKRIPSI
Skripsi ini telah dipertahankan di hadapan tim penguji
pada tanggal 25 September 2014
TIM PENGUJI
KETUA : Rehulina Ginting, drg., M.Si
ANGGOTA : 1. dr. Betty, M.Ked(PA), Sp.PA
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa yang telah memberikan rahmat dan
karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini sebagai salah satu
syarat untuk mendapatkan gelar Sarjana Kedokteran Gigi di Fakultas Kedokteran
Gigi Sumatera Utara.
Penulis mengucapkan terima kasih kepada Betty, dr., M.Ked. (PA), Sp.PA
selaku dosen pembimbing skripsi yang telah banyak memberikan bimbingan,
motivasi, kritik, saran, serta waktu yang sangat bermanfaat dalam penyelesaian
skripsi ini. Juga tidak lupa ucapan terima kasih kepada Rehulina Ginting, drg., M.Si.,
selaku kepada Departemen Biologi Oral Fakultas Kedokteran Gigi Universitas
Sumatera Utara dan dosen pembimbing skripsi yang juga telah membimbing dan
membantu penulis serta memberikan masukan dalam penyelesaian skripsi ini. Pada
kesempatan ini dengan rendah hati penulis mengucapkan terima kasih kepada yang
terhormat:
1. Prof. Nazruddin, drg., Ph.D., Sp.Ort selaku Dekan Fakultas Kedokteran
Gigi Universitas Sumatera Utara.
2. Sayuti Hasibuan, drg., Sp.PM selaku penasehat akademik yang selama ini
telah banyak memberikan nasehat selama penulis menjalankan pendidikan di Fakultas
Kedokteran Gigi Universitas Sumatera Utara.
3. Seluruh staf pengajar dan pegawai Departemen Biologi Oral FKG USU,
Lisna Unita, drg., M.Kes, Minasari, drg., MM., Yendriwati, drg., M.Kes., Dr. Ameta
Primasari, drg., MDSc., M.Kes dan Yumi Lindawati, drg., selaku para staf pengajar
Departemen Biologi Oral. Ngaisah dan Dani Irma Suryani selaku staf pegawai yang
telah membantu dalam penelitian, memberikan saran dan motivasi dalam
penyelesaian skripsi ini.
4. Seluruh dokter dan staff Departemen Patologi Anatomi FK USU/RSUP H.
5. Teristimewa kepada kedua orang tua penulis tercinta yaitu Michael Ding
dan Karen Lee serta adik penulis Jason Ding yang selalu mendoakan, memberikan
dukungan moril maupun materil, serta motivasi hingga penulis dapat menyelesaikan
penulisan skripsi ini.
6. Sahabat-sahabat terbaik penulis May Eng, Su Yong, Sami Abdul-Wahid,
Shanthi Levanita, Arsila, Titin, dan Kelvin Gohan yang telah memotivasi dan
meluangkan waktu dalam membantu penelitian dan penulisan skripsi ini. Serta
senior-senior dan teman-teman stambuk 2010 yang membuat skripsi di Departemen
Biologi Oral yaitu: Kak Anita, Kak Indira, Kak Tellia, Bang Wanda, Bang Rahmat,
Cindy, Beactris, Joseph, Ervi, Swee Fan, May, Aryani, Josua, Colvin dan Roderick
yang memberikan semangat dan motivasi kepada penulis.
7. Teman-teman stambuk 2010, senior dan junior yang tidak dapat disebutkan
satu per satu atas dukungan dan motivasi yang telah diberikan selama penulisan
skripsi.
Akhir kata, penulis mengharapkan saran dan kritik dalam membangun
kesempurnaan skripsi ini. Semoga skripsi ini dapat memberikan sumbangan pikiran
yang berguna untuk bahan bacaan ke fakultas, dan sebagai pengembangan ilmu yang
bermanfaat bagi masyarakat. Akhirnya tiada lagi yang dapat penulis ucapkan selain
syukur sedalam-dalamnya kepada Tuhan Yang Maha Esa.
Medan, 25 September 2014
Penulis,
(………)
Michelle Ding
DAFTAR ISI
Halaman
HALAMAN JUDUL ...
HALAMAN PERSETUJUAN ...
HALAMAN TIM PENGUJI SKRIPSI ...
KATA PENGANTAR ... iv
2.3.1 Nukleolus ... 16
BAB III METODOLOGI PENELITIAN 3.1 Jenis Penelitian ... 25
3.9.1 Pembuatan Sediaan Mikroskopis dari Blok Parafin ……. . 31
3.9.2 Prosedur Pewarnaan Hematoxylin-eosin ……….. 31
3.9.3 Prosedur Pewarnaan AgNOR ……… 32
3.10 Pengolahan Dan Analisis Data ... 32
BAB IV HASIL PENELITIAN 4.1. Karakteristik Umum Sampel yang Diteliti ... 33
BAB V PEMBAHASAN ... 37
BAB VI KESIMPULAN DAN SARAN ... 42
DAFTAR PUSTAKA ... 43
DAFTAR GAMBAR
Gambar Halaman
1 Gambaran histopatologi KSS berdiferensiasi baik dengan
pewarnaan Hematoksilin Eosin (HE) ... 7
2 Gambaran histopatologi KSS berdiferensiasi sedang dengan
pewarnaan HE ... 8
3 Gambaran histopatologi KSS berdiferensiasi buruk dengan
pewarnaan HE ... 9
4 Skema ilustrasi p53 checkpoint ... 12
5 Bentuk nukleus ... 15
6 Gambaran mikroskopis mukosa normal rongga mulut dengan
pewarnaan AgNOR (100X) ... 20
7 Gambaran mikroskopis KSS rongga mulut yang berdiferensiasi
baik dengan NORs sedikit pada inti (1000X) ... 21
8 Gambaran mikroskopis KSS rongga mulut yang berdiferensiasi
sedang dengan sebagian ukuran NORs pada inti (1000X) ... 21
9 Gambaran mikroskopis KSS rongga mulut yang berdiferensiasi buruk dengan jumlah NORs yang banyak dan beragam pada inti
(1000X) ... 22
10 Gambaran mikroskopis KSS rongga mulut yang tidak berdiferensiasi (undifferentiated) dengan jumlah NORs yang
DAFTAR TABEL
1 Klasifikasi WHO tumor pada kavitas rongga mulut ... 6
2 Sistem penilaian derajat diferensiasi KSS rongga mulut dengan
parameter Bryne ... 10
3 Distribusi frekuensi karateristik umum sampel berdasarkan data
rekam medis sampel yang diteliti ... 33
4 Distribusi frekuensi tampilan mAgNOR pada KSS rongga mulut
berdasarkan jenis sub-tipe keratinisasi ... 34
5 Distribusi frekuensi tampilan mAgNOR pada KSS rongga mulut
berdasarkan jenis diferensiasi ... 35
6 Distribusi frekuensi tampilan mAgNOR pada KSS rongga mulut
berdasarkan umur ... 35
7 Distribusi frekuensi tampilan mAgNOR pada KSS rongga mulut
berdasarkan jenis kelamin ... 35
8 Distribusi frekuensi tampilan mAgNOR pada KSS rongga mulut
DAFTAR SINGKATAN
AgNOR Silver stained Nucleolar Organizer Regions
ARF Alternative Reading Frame
CDK Cyclin-dependent kinases
DNA Deoxyribonucleic acid
EGFR Epidermal growth factor receptor
H&E Hematoxylin & Eosin
IARC International Agency for Research on Cancer
KSS Karsinoma sel skuamosa
NOR Nucleolar organizing region
NORs Nucleolar organizing regions
NPM Nucleophosmin
RNA Ribonucleic acid
rRNA Ribosomal ribonucleic acid
UV Sinar Ultraviolet
DAFTAR LAMPIRAN
Lampiran
1 Alur Pikir
2 Ethical Clearance
3 Contoh Formulir Pemeriksaan Patologi Anatomi
4 Gambar Prosedur Kerja
5 Data Hasil Penelitian
Fakultas Kedokteran Gigi
Bagian Biologi Oral
Tahun 2014
Michelle Ding
Reaksi Pewarnaan AgNOR pada Karsinoma Sel Skuamosa Rongga Mulut
xii + 46 halaman
Karsinoma sel skuamosa (KSS) merupakan salah satu jenis kanker yang
ditemukan di rongga mulut. Penyebab KSS adalah multifaktorial. KSS terjadi
akibat dari kerusakan genetik pada kromosom dan gen. Hal ini menyebabkan
perubahan molekular DNA pada nukleolus yang ada pada nukleus sel. Nukleolus
mempunyai bagian kromosom yang dinamakan nucleolar organizer region
(NOR) yang berperan dalam sintesis protein. NOR diamati sebagai titik-titik
hitam di bawah mikroskop cahaya dengan pewarnaan AgNOR. Pada sel normal,
hanya 1-2 titik hitam AgNOR yang diamati. Peningkatan titik-titik hitam AgNOR
mengindikasi perubahan sel normal menuju ke sel displastik/karsinoma dan juga
mencerminkan tingkat keburukan karsinoma. Tujuan penelitian ini adalah untuk
melihat distribusi frekuensi mean AgNOR (mAgNOR) pada nukleus preparat
KSS rongga mulut. Rancangan penelitian ini merupakan deskriptif analitik
dengan pendekatan cross sectional terhadap 30 sampel blok parafin yang
terdiagnosa sebagai KSS rongga mulut yang diperoleh dari Laboratorium
Patologi Anatomi FK USU/RSUP Haji Adam Malik Medan tahun 2009-2013,
Olympus CX21 terhadap 100 nuklei. Hasil penelitian menunjukkan adanya
perbedaan yang signifikan mAgNOR antara KSS sub-tipe diferensiasi baik dan
diferensiasi sedang (p=0,000), dan tidak ditemukan perbedaan yang signifikan
mAgNOR antara sub-tipe keratinisasi KSS (p=0,124), kelompok umur (p=0,964),
jenis kelamin (p=0,053) dan lokasi lesi (p=0,195). Kesimpulan penelitian ini
menunjukkan adanya peningkatan yang signifikan nilai mAgNOR pada KSS
diferensiasi sedang dibandingkan dengan KSS diferensiasi baik, dan tidak
adanya perbedaan yang signifikan nilai mAgNOR antara kelompok sub-tipe
keratinisasi KSS, umur, jenis kelamin dan lokasi lesi.
Kata Kunci: karsinoma sel skuamosa rongga mulut, pewarnaan AgNOR,
diferensiasi KSS
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Karsinoma sel skuamosa (KSS) adalah suatu neoplasma invasif pada jaringan
epitel rongga mulut dengan berbagai tingkat diferensiasi yang muncul pada
tempat-tempat seperti jaringan mukosa mulut, alveolar, gingiva, dasar mulut, lidah, palatum,
tonsil dan orofaring. KSS cenderung bermetastase dan meluas dengan cepat.1,2
Insidensi KSS dari seluruh jenis keganasan yang terdapat pada rongga mulut
adalah sekitar 95% dan di Indonesia, frekuensi KSS rongga mulut mencapai 3-5%
dari seluruh kanker organ tubuh lainnya.3,4
Penyebab KSS adalah multifaktorial, ada dua faktor predisposisi terjadinya
KSS, yaitu: faktor intrinsik seperti genetik, dan faktor ekstrinsik seperti
mengkonsumsi tembakau, alkohol, infeksi virus, malnutrisi dan sinar matahari.
Risiko terjadi kanker akan meningkat apabila terdapat kombinasi faktor-faktor
predisposisi tersebut, misalnya merokok dengan minum alkohol dan menyirih dengan
tembakau.2,5
KSS dapat terjadi karena kehilangan kontrol pada siklus sel, yaitu control cell
survival, dan control cell motility. Proses terbentuknya KSS merupakan proses
bertahap, yang terjadi karena adanya gangguan fungsi pengatur pertumbuhan
(protoonkogen dan gen penghambat tumor) sehingga terjadi peningkatan produksi
growth factors dan jumlah reseptor permukaan sel, memacu transduksi sinyal
interseluler, dan peningkatkan produksi faktor transkripsi. Sifat letal dari kanker
adalah memiliki kemampuan untuk menginvasi pada jaringan sekitar, dan
menyebar ke seluruh tubuh.6
KSS terjadi akibat dari kerusakan genetik pada kromosom dan gen sehingga
mempengaruhi perubahan molekular DNA.7 Perubahan ini terutamanya terjadi pada nukleolus yang terletak dalam nukleus sel. Nukleolus merupakan tempat sintesis
menggandakan sintesis RNA. Nukleolus dikontrol oleh bagian kromosom yang
mengandung gen tertentu yang dikenal sebagai nucleolar organizer.8
Nukleolus merupakan organel dalam inti sel yang berperanan penting dalam
mengendalikan proliferasi sel dan sintesis protein. Nucleolar organizer regions
(NORs) merupakan segmen DNA dekat nukleolus yang menyandi gen DNA ribosomal
dan berperan dalam sintesis protein untuk proses proliferasi sel.9,10 Terdapat dua jenis protein utama dalam nukleolus yang berperan dalam proliferasi sel yaitu
nucleophosmin (salah satu protein agyrofilik NORs) dan ARF tumor suppressor.11,12 Nucleophosmin diperlukan untuk pemprosesan rRNA dan fungsi utama ARF adalah
menginaktivasi nucleophosmin yang berlebihan.12,13 Protein NORs bersifat argyrofilik yang dapat diamati dengan teknik
pewarnaan perak nitrat. Interaksi akhir perak dengan NOR disebut dengan AgNOR.
Teknik pewarnaan ini menghasilkan tampilan titik-titik hitam dalam nukleus atau inti
sel. Tampilan titik-titik hitam ini mengindikasi terjadinya proliferasi sel yang
menandakan aktivitas transkripsi gen rRNA.14,15,16 Pada sel yang normal akan kelihatan 1-2 titik hitam AgNOR di dalam nukleus sel dan bila sel normal ini menuju
ke sel displastik atau sel karsinoma, jumlah titik hitam AgNOR juga meningkat
karena terjadinya peningkatan transkripsi pada ribosom untuk mensintesis protein
bagi pembelahan sel.15,16 Peningkatan jumlah titik hitam AgNOR menunjukkan keagresifan suatu karsinoma atau tumor. Karsinoma berdiferensiasi buruk
mempunyai jumlah titik hitam AgNOR yang lebih tinggi dibanding dengan karsinoma
berdiferensiasi sedang dan berdiferensiasi baik. Ini merefleksi terdapatnya metabolik
dan aktivitas sel proliferatif tinggi tidak terkontrol, serta kandungan DNA yang
abnormal pada sel karsinoma berdiferensiasi buruk.17,18,19 Selain itu, juga terjadinya penghambatan ARF dari memasuki ke nukleoplasma sehingga hilangnya pengawalan
Berdasarkan permasalahan di atas, maka peneliti ingin melakukan penelitian
untuk melihat tampilan titik-titik hitam AgNOR pada kasus KSS rongga mulut.
Dengan mengkaji ekspresi titik hitam AgNOR pada KSS rongga mulut, dapat
digunakan sebagai upaya memprediksi tingkat keagresifan proliferasi sel kanker.
1.2 Rumusan Masalah
Berdasarkan uraian di atas maka timbul permasalahan yang hendak diteliti
bagaimanakah tampilan titik-titik hitam yang dihasilkan dari pewarnaan AgNOR pada
KSS rongga mulut?
1.3 Tujuan Penelitian
1.3.1 Tujuan Umum
Untuk melihat tampilan titik-titik hitam AgNOR di dalam nukleus sel pada KSS
rongga mulut.
1.3.2 Tujuan Khusus
Untuk melihat tingkat diferensiasi preparat KSS rongga mulut dengan hasil
distribusi frekuensi rata-rata AgNOR (mAgNOR).
1.4 Hipotesis Penelitian
1. H0 : Tidak terdapat perbedaan yang signifikan antara kelompok umur, jenis
kelamin, lokasi lesi, sub-tipe keratinisasi, dan jenis diferensiasi pada KSS rongga
mulut dengan nilai rata-rata titik hitam AgNOR.
2. Hα : Terdapat perbedaan yang signifikan antara kelompok umur, jenis
kelamin, lokasi lesi, sub-tipe keratinisasi, dan jenis diferensiasi pada KSS rongga
1.5 Manfaat Penelitian
1.5.1 Manfaat Teoritis
Hasil yang diperoleh dari penelitian ini diharapkan dapat bermanfaat dalam
mengetahui tampilan titik-titik hitam dan tingkat proliferasi sel dengan pewarnaan
AgNOR pada KSS rongga mulut.
1.5.2 Manfaat Praktis
1. Memberi informasi mengenai pewarnaan AgNOR sebagai suatu teknik untuk
memprediksi prognosa kanker.
2. Memberi informasi mengenai aktivitas proliferasi sel pada sub-tipe KSS
rongga mulut.
3. Data awal untuk penelitian lanjutan tentang KSS rongga mulut.
BAB 2
TINJAUAN PUSTAKA
Mukosa rongga mulut normal dilapisi oleh lapisan epitel skuamosa dan
memiliki perbedaan topografi yang berhubungan dengan karateristik fisik. Mukosa
rongga mulut dapat dibagi atas tiga jenis, yaitu mukosa pengunyahan, mukosa lining
dan mukosa khusus. Mukosa pengunyahan terdiri dari sel epitel yang berkeratinisasi
dan ditemukan pada bagian gingiva, dorsum lidah dan palatal keras. Mukosa lining
terdapat pada bagian dasar mulut, palatal lunak dan sisi ventral/lateral lidah yang
epitelnya adalah tidak berkeratin. Lidah mempunyai mukosa khusus dimana terdiri
dari papila-papila yang berfungsi dalam pengecapan. Mukosa rongga mulut akan
mengalami perubahan seperti hiperplasia atau hiperkeratosis apabila terpapar dengan
bahan-bahan iritan tertentu, dan bila perubahan ini bersifat irreversibel, akan
terjadinya karsinoma.1,20
2.1 KSS Rongga Mulut
KSS rongga mulut merupakan suatu keganasan yang berasal dari epitel, baik
berasal dari mukosa pada dinding rongga mulut, organ dalam mulut atau kelenjar
saliva.2 Sebanyak 95% dari seluruh kanker di rongga mulut adalah karsinoma sel skuamosa rongga mulut. Tingkat prevalensi kanker mulut kebanyakannya ditemukan
di negara seperti India karena penggunaan produk tembakau yang berlebihan. Bagian
rongga mulut yang paling dampak terkena kanker mulut adalah lidah, bibir inferior
dan dasar mulut. Kanker mulut dapat timbul secara denovo atau dari daerah yang
sebelumnya memiliki lesi atau kondisi prekanker, yaitu lesi prakanker yang paling
umum adalah leukoplakia dan kondisi prekanker adalah lichen planus erosif.21,22 KSS rongga mulut merupakan bagian dari kanker di daerah kepala dan leher yang
menempati peringkat keenam kanker terbanyak di dunia dengan distribusi geografis
yang luas dan secara signifikan menyebabkan morbiditas maupun mortalitas.23
Di Indonesia, kanker telah menjadi masalah kesehatan masyarakat yang besar.
penelitian, lebih dari 90% kanker mulut adalah karsinoma epidermoid atau karsinoma
sel skuamosa. Diseluruh dunia diperkirakan 378.000 kasus baru kanker mulut yang
didiagnosa pertahun. Dinegara tertentu, seperti Sri Lanka, India, Pakistan dan
Bangladesh kanker mulut merupakan kanker yang paling sering. Di India kanker
mulut dapat mencapai lebih dari 50% dari semua jenis kanker. Pria mempunyai
tingkatan kanker mulut yang lebih tinggi daripada wanita di dunia yaitu pada laki-laki
4% dan wanita 2%. Di Singapura, insiden kanker rongga mulut tertinggi pada wanita
sebesar 5.8 per 100.000 populasi, sedangkan pada laki-laki yang tertinggi berada di
Perancis yaitu 17.9 per 100.000 populasi.24
2.1.1 Gambaran Histopatologi Sel Skuamosa Rongga Mulut
Menurut World Health Organization (WHO), kode klasifikasi histologi tumor
pada kavitas rongga mulut dan oro-faring pada tahun 2005 dibagi seperti tabel bawah:
Tabel 1. Klasifikasi WHO tumor pada kavitas rongga mulut.25
Malignant epithelial tumours Kode
Menurut kode morfologi dari International Classification of Diseases for
Oncology (ICD-O) (821) dan Systematized Nomenclature of Medicine dimana
jenisnya diberi kode /0 untuk tumor jinak, /3 untuk tumor ganas dan /1 untuk kasus
borderline atau ragu-ragu. KSS rongga mulut secara umum mempunyai gambaran
histopatologi yang tidak berbeda dari KSS kulit maupun organ tubuh lainnya. KSS
rongga mulut ada yang berdiferensiasi baik dimana menyerupai epitel skuamosa
berlapis normal dan menghasilkan keratin dan ada juga KSS rongga mulut yang
berdiferensiasi buruk.25
Berdasarkan derajat diferensiasi KSS rongga mulut, dapat dibagi kepada tiga,
yaitu diferensiasi baik, sedang dan buruk. Gambaran KSS yang berdiferensiasi baik
adalah mengandung sel berkeratin, gambaran keratin seperti tanduk mutiara (pearl
horn formation) dengan ukuran yang bervariasi, pertumbuhan yang lambat, tidak
cepat bermetastase dan mempunyai prognosa yang baik. Pada lesi tipikal, kelompok
sel ganas ini dapat ditemukan secara aktif menginvasi jaringan konektif dengan
bentuk yang tidak teratur (Gambar 1).21,25
Gambar 1. Gambaran histopatologi KSS berdiferensiasi baik dengan pewarnaan Hematoksilin Eosin (HE) (x100). Anak panah: A. Mutiara keratin B. Nukleus sel.25
Gambaran KSS untuk yang diferensiasi sedang, berbeda dari satu dengan yang
lainnya, dimana tersusun secara tipikal, sehingga epitel skuamosa juga kurang jelas.
Laju pertumbuhan sel individu lebih cepat dengan pembelahan mitosis yang lebih
meningkat dan bahkan ukuran bentuknya yang lebih bervariasi (Gambar 2).21,25
Gambar 2. Gambaran histopatologi KSS berdiferensiasi sedang dengan pewarnaan HE (x400). A. Nukleus sel
(anak panah merah).25
Untuk gambaran KSS yang berdiferensiasi buruk, sering sekali menghasilkan
petunjuk sel-sel yang tidak jelas sehingga menimbulkan kesulitan dalam
mendiagnosis. Sel-sel ini menunjukkan kurangnya daya kohesif yang sangat tidak
teratur, pembentukan sel tumor raksasa, adanya anaplasia, peningkatan mitosis, serta
tidak adanya pembentukan keratin (Gambar 3).21,25
Gambar 3. Gambaran histopatologi KSS berdiferensiasi buruk dengan pewarnaan HE (x400). A. Nukleus sel (anak panah merah).25
KSS rongga mulut memiliki kecenderungan besar untuk menghasilkan
metastasis pada kelenjar getah bening. Pada praktek klinis, rencana pengobatan dan
prognosis KSS rongga mulut terutama didasarkan pada tumor primer, metastasis
kelenjar getah bening regional dan sistem pementasan metastasis (TNM). Namun,
sistem ini tidak menyediakan informasi tentang karakteristik biologi dan tingkat
keagresifan klinis tumor yang jelas, dan ini telah menimbulkan suatu sistem penilaian
keganasan KSS rongga mulut yang multifaktorial dikembangkan. Sistem penilaian
pertama KSS rongga mulut telah dikembangkan oleh Broder pada tahun 1927 dan
yang baru-baru ini merupakan sistem penilaian Bryne (1989). Berdasarkan sistem
penilaian Bryne (Tabel 2), terdapat empat parameter yang diperlihatkan untuk menilai
derajat diferensiasi KSS rongga mulut, yaitu derajat keratinisasi, pleomorphism inti,
infiltrasi limfosit dan bentuk invasi tumor. Derajat diferensiasi KSS rongga mulut
akan dinilai dengan memperhitungkan skor dari empat parameter tersebut, yaitu skor
4-8 (diferensiasi baik), skor 9-12 (diferensiasi sedang), dan skor 13-16 (diferensiasi
buruk).21
Tabel 2. Sistem penilaian derajat diferensiasi KSS rongga mulut dengan parameter
Penyebab karsinoma sel skuamosa yang pasti belum diketahui. Penyebabnya
diduga berhubungan dengan bahan karsinogen dan faktor predisposisi. Kanker rongga
mulut memiliki penyebab yang multifaktorial dan suatu proses yang terdiri dari
beberapa langkah yang melibatkan inisiasi, promosi dan perkembangan tumor.
Faktor-faktor etiologi tersebut tidak bekerja secara terpisah, kombinasi dari berbagai
faktor sering ditemukan bersama-sama. Secara garis besar, etiologi kanker rongga
mulut dapat dikelompokkan atas faktor lokal, faktor luar, dan faktor pejamu (host).2,5 Faktor lokal seperti iritasi kronis umumnya dapat menyebabkan kanker seperti
trauma mekanis dari gigitiruan yang tidak pas, restorasi yang tidak tepat, oral hygiene
yang buruk dan tepi-tepi gigi yang tajam. Faktor luar meliputi kebiasaan merokok
dan minum alkohol. Asap rokok mengandung bahan karsinogen (nitrosamine) dan
Terjadinya rangsangan menahun menyebabkan kerusakan jaringan berulang-ulang
sehingga mengganggu keseimbangan sel dan terjadinya displasia. Selain itu, sinar
ultraviolet (UV) seringkali dianggap sebagai faktor penting yang dapat menyebabkan
mutasi gen jika terpapar untuk jangka waktu yang panjang. Infeksi virus dan jamur
yang tidak sembuh-sembuh meskipun telah diobati juga dapat menyebabkan kanker
apabila infeksi tersebut berkelanjutan dalam jangka waktu yang panjang sehingga
memicu terjadinya karsinoma. Faktor host seperti nutrisi yang dikonsumsi dapat
mempengaruhi terjadinya kanker seperti kekurangan zat anti-oksidan seperti Vitamin
A, C dan E. Selain itu, unsur lain seperti usia, jenis kelamin, imunologi dan genetik
seseorang dapat juga meningkatkan risiko terjadinya kanker.2,5
2.1.3 Patogenesis dan Siklus Sel
KSS muncul sebagai akibat dari berbagai kejadian molekular yang
menyebabkan kerusakan genetik yang mempengaruhi kromosom dan gen, yang
akhirnya menuju kepada perubahan DNA. Akumulasi perubahan tersebut memicu
terjadinya disregulasi sel pada batas dimana terjadinya pertumbuhan otonom dan
perkembangan yang invasif. Proses neoplastik mula-mula bermanifestasi secara
intraepitel dekat membran dasar sebagai suatu hal yang fokal, kemudian terjadi
pertumbuhan klonal keratinosit sel yang berubah secara berlebihan, menggantikan
epitelium normal. Setelah beberapa waktu atau beberapa tahun, terjadi invasi
membran dasar jaringan epitel menandakan awal kanker invasif.5,26
Karsinogenesis merupakan proses genetik yang memicu perubahan morfologi
dan tingkah laku seluler. Analisis perubahan di tingkat molekuler dapat menjadi alat
diagnosis utama dan pemandu untuk melakukan perawatan, karena perubahan
morfologis terjadi setelah adanya perubahan genetik. Kanker dan lesi prekanker
rongga mulut berkembang sebagai akibat dari siklus sel yang tidak terkontrol
dikarenakan multiple mutations. Proto-onkogen, Tumor supresor gen (TSG), dan
molekul gatekeeper (cyclins dan CDK) merupakan kelompok gen DNA perbaikan
Siklus sel normal dikendalikan oleh suatu kelompok protein yang secara umum
disebut cyclin. Siklus berlangsung melalui fase mitosis (M), gap-1 (G1), sintesis DNA
(fase S), gap-2 (G2), mitosis (M) dan seterusnya. Sel anak hasil mitosis secara teratur
masuk ke siklus dalam fase G1, sebagian sel anak masuk ke fase istirahat (G0). Sel
pada fase G0 dapat aktif kembali masuk ke fase G1 siklus sel. Masuknya kelompok
sel ke fase istirahat, kemudian aktif kembali menyebabkan proses regenerasi tubuh
berlangsung cepat.27
Masing-masing fase memiliki fungsi untuk mengaktivasi dan melengkapi fase
sebelumnya, dan siklus sel akan berhenti jika fungsinya sudah terganggu. Diantara
G1/S terdapat checkpoint untuk memonitor DNA sebelum replikasi dan G2/M untuk
memonitor DNA setelah replikasi. Checkpoint dilakukan oleh Tumor supresor gen
(TSG) salah satunya gen p53 atau dikenal sebagai master guardian of the genome dan
merupakan unsur utama dalam memelihara keseimbangan genetik. Fungsi gen p53
mendeteksi sintesis DNA yang salah atau kerusakan DNA kemudian menginduksi gen
reparasi DNA serta menginduksi apoptosis.27
Pada gambar di atas (Gambar 4) menunjukkan internal control (checkpoint).
Terdapat dua checkpoint inti, satu terdapat pada masa transisi antara G1/S checkpoint
dan G2/M checkpoint yang berfungsi untuk memeriksa kerusakan DNA, jika
ditemukan adanya kerusakan, maka sirkulasi sel akan melambat, waktu ini akan
digunakan untuk memperbaiki DNA yang rusak, jika tidak dapat diperbaiki maka
jalan untuk terjadinya apoptosis akan aktif dan DNA yang rusak akan dihancurkan.
Gen p53 seharusnya merangsang p21 menekan semua cyclin dependent kinase agar
cyclin tidak bekerja, sehingga siklus sel akan terhenti. Pada saat terhentinya siklus sel
akan memberikan waktu terjadinya perbaikan DNA sehingga dapat dihindari
terbentuknya sel yang mengandung defek DNA.27
2.2 Onkogen
Onkogen merupakan gen pengatur pertumbuhan yang mengalami perubahan
dalam pengaturan jalur transduksi sinyal-sinyal sel. Mutasi gen ini mengakibatkan
terjadinya peningkatan produksi atau fungsi protein dalam sel. Onkogen berperan
penting dalam proses karsinogenesis, tetapi tidak cukup untuk mengubah sel-sel
epitel.7
Beberapa onkogen mempunyai implikasi dalam karsinogenesis rongga mulut.
Penyimpangan reseptor faktor pertumbuhan epidermal proto-onkogen (EGFR / c-erb
1), gen anggota keluarga ras, c-myc, int-2, hst-1, PRAD -1, dan bcl-1 diyakini
berkontribusi terhadap perkembangan kanker.7
Deregulasi faktor pertumbuhan terjadi selama karsinogenesis rongga mulut,
melalui peningkatan produksi dan stimulasi autokrin. Penyimpangan ekspresi dari
Transforming growth factor α (TGF-α) dilaporkan terjadi pada awal karsinogenesis
rongga mulut. Penyimpangan ini terjadi pertama kali pada epitel hiperplastik dan
kemudian pada infiltrasi sel-sel radang karsinoma. TGF-α merangsang proliferasi sel
2.2.1 Gen Penekan Tumor
Onkogen saja tidak cukup sebagai inisiator proses karsinogenesis.
Transformasi sel premalignan menjadi sel ganas terjadi akibat inaktivasi gen penekan
tumor, dan dianggap sebagai penyebab utama dalam perkembangan keganasan. Gen
penekan tumor paling sering diinaktivasi melalui mutasi titik, penghapusan, dan
penyusunan ulang salinan gen.7,26
Salah satu gen penekan kanker adalah gen p53 yang merupakan pelindung
siklus sel. Gen p53 berperan dalam pengaturan siklus sel dengan mengontrol
sejumlah gen termasuk gen apoptosis jika kerusakannya berat. Rekonstitusi jalur
apoptosis oleh p53 dapat terjadi dengan mentransfer gen p53 wild type rekombinan
pada sel kanker yang mengekspresi p53 null atau mutan. Bila sel terluka, p53 dalam
inti memicu sel untuk melakukan “arrest” pada perbatasan G1/S dengan menginduksi
penghambat CDK (cyclin D kinase) dan sistem perbaikan DNA terlebih dahulu
menghilangkan luka tersebut sebelum sel memasuki fase S tanpa adanya DNA yang
rusak. Program “arrest” dan apoptosis ini tergantung pada lingkungan fisiologik
ataupun jenis sel. Oleh karena itu kehilangan fungsi gen p53 ini merupakan penyebab
munculnya malignansi. Inaktivasi gen p53 ini biasanya terjadi dalam dua tahap yakni
inaktivasi pada satu alel oleh mutasi titik atau delesi kecil dan berikutnya adalah
kehilangan alel normal oleh delesi segmen kromosom. Inaktivasi alel pertama dapat
terjadi pada sel somatik maupun sel germ. Gen ini juga disebut “guardian of the cell”.
Sel yang tidak memiliki p53 menunjukkan ketidakstabilan genom dan memperbesar
karsinogenesis.7
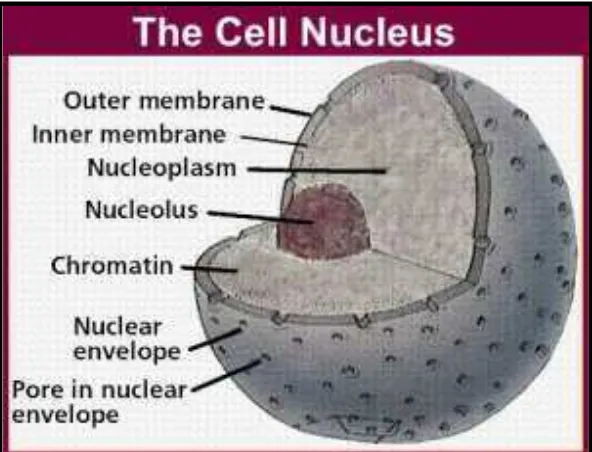
2.3 Nukleus
Nukleus (Gambar 5) sering dikenal sebagai inti sel. Nukleus pertama kali
dikenalkan oleh Brown pada tahun 1831 yang mengamati sel-sel tumbuhan. Struktur
nukleus sel tumbuhan (eukariot) mempunyai inti sel yang jelas ketika diamati, karena
bahan-bahan inti yang ada di dalam nukleus dibatasi oleh membran
nukleus (karyotheca), yaitu struktur membran fosfolipid bilayer mirip dengan
Nukleus memiliki peran yang sangat penting dalam kehidupan sebuah sel.
Peranan nukleus dalam hal ini adalah untuk mengatur dan mengontrol segala aktifitas
kehidupan sel serta membawa informasi genetik yang diturunkan ke generasi
berikutnya. Informasi genetik ini disimpan dalam suatu molekul polinukleutida yang
disebut DNA (Deoxyribonucleic acid). DNA pada umumnya tersebar di dalam
nukleus sebagai matriks seperti benang yang disebut kromatin. Ketika sel akan
memulai membelah, kromatin akan berkondensasi membentuk struktur yang lebih
padat dan memendek yang selanjutnya disebut kromosom. Kromosom tersusun atas
molekul DNA dan protein histon. Struktur di dalam nukleus yang merupakan tempat
berkonsentrasinya molekul DNA adalah nukleolus (anak inti.). Nukleolus berperan
sebagai tempat terjadinya sintesis molekul RNA (Ribonucleic acid) dan ribosom. RNA
merupakan hasil salinan DNA yang akan ditransfer ke sitoplasma untuk
diterjemahkan menjadi rantai asam amino yang disebut protein.28
2.3.1 Nukleolus
Struktur nukleolus (anak inti) pada pengamatan mikroskop elektron terlihat
sebagai sebuah atau lebih bangunan basofilyang berukuran lebih besar dari ukuran
butir-butir kromatin.28
Nukleolus merupakan tempat berlangsungnya transkripsi gen, dimana molekul
rRNA diproses. rRNA adalah salah satu jenis RNA yang merupakan materi penyusun
ribosom. Molekul rRNA yang baru terbentuk, akan segera dikemas bersama protein
ribosom untuk dikeluarkan dari inti sel. Transkripsimolekul rRNA di dalam
nukleolus menjamin pembentukan molekul ribosom pada sitoplasm. Di dalam
nukleolus, terdapat sejumlah potongan-potongan DNA (rDNA) yang ditranskripsi menjadi rRNA secara berulang-ulang, dan berlangsung cepat dengan bantuan
enzim RNA polymerase I. Potongan-potongan DNA tersebut dinamakan nucleolar
organizer. Kandungan RNA dalam nukleolus jika dibanding dengan bagian lain dari
inti sel adalah tidak tetap, yaitu diperkirakan 5%-20%.28,29
2.3.2 Nucleolar Organizing Region (NOR)
Nucleolus organizer region (NOR) atau nucleolar organizer merupakan bagian
kromosom dimana sekitarnya terjadi pembentukan nukleolus.14 Nukleolus organizer regions (NORs) adalah segmen kromosom dienkripsi untuk RNA ribosom (rRNA)
yang hadir pada loop spesifik DNA. NOR telah menerima banyak perhatian baru-baru
ini karena dari pengamatan didapati bahwa frekuensi NOR dalam inti secara
signifikan lebih tinggi dalam sel-sel ganas berbanding sel normal, sel reaktif atau sel
neoplastik jinak sehingga merupakan nilai diagnostik dalam karakterisasi invasi pada
karsinoma. NOR juga berperan dalam estimasi aktivitas selular yang diterapkan pada
berbagai lesi neoplastik atau hiperplastik.30 Daerah ini merupakan bagian tertentu dari kromosom yang berhubungan dengan nukleolus setelah nukleus membagi dan berisi
beberapa salinan tandem gen DNA ribosom. Pada manusia, NOR mengandung gen
5.8S, 18S, 28S rRNA yang berkerumun di lengan pendek kromosom 13, 14, 15, 21
aktif rRNA, yang menimbulkan konstriksi sekunder kromosom metafase. Pada
metafase, sisa protein dari nukleolus sering terkait dengan konstriksi sekunder. Setiap
gen rRNA pada NOR hampir identik secara berurutan, meskipun bervariasi dalam
ukuran karena perbedaan jumlah elemen DNA ulangan dalam bagian ruangan
intergenik umum.32
Dalam komplemen kromosom lengkap selalu ada enam kromosom dengan
terminal nucleolus organizing region (NOR). Dalam kebanyakan kasus, bagian dari
NOR adalah decondensed, dan dari beberapa bagian decondensed ini dibentuk
bersama-sama menjadi nukleolus besar. Nukleolus besar ini mudah terlihat dalam
fase kontras bahkan tanpa pra-perawatan karena struktur khusus dan ukuran besarnya.
Bentuk nukleolus berkisar dari membulat ke irregular. Selain pembentukan nukleolus
dari enam NOR ini, ada juga beberapa nukleolus yang lebih kecil terdiri dari NOR
hanya dua sampai lima nucleolus organizing kromosom.30,33 Nucleolus organizer region (NOR) dapat diidentifikasi melalui teknik argyrofilik (AgNOR) melalui proses
rutin fiksasi formalin parafin.14
NORs juga mengandung zat asam, dan protein non-histon yang mengikat ion
perak dan dapat dilihat secara selektif dengan metode perak pada sampel
sito-histologi. NORs yang dihubungkan dengan protein argyrofilik apabila diwarnakan
dengan perak disebut sebagai “AgNOR”. Sifat biokimia yang tepat dari protein ini
belum didefinisikan, tetapi telah diketahui sebagai B 23, C 23 dan RNA polymerase
dan dikaitkan dengan asam, unsur non-histon.30 Pada mikroskop cahaya, protein AgNOR dapat terlihat sebagai titik-titik hitam yang terletak di dalam nukleolus.14,30 NORs banyak menarik perhatian karena frekuensi muncul pada sel ganas lebih tinggi
daripada sel normal, reaktif atau sel neoplastik jinak.31
2.3.3 Nucleophosmin dan Alternative Reading Frame (ARF)
Nucleophosmin (NPM) atau B23 merupakan sebuah fosfoprotein nukleolar
dalam pengolahan rRNA dan juga merupakan salah satu protein argyrofilik dari
AgNORs. NPM terlibat dalam mengendalikan pertumbuhan sel, diferensiasi sel dan
dalam timbulnya kanker. NPM berperan dalam biogenesis ribosom, dimana
fosforilasi dan modifikasi NPM oleh cyclin E - CDK2 holoenzyme diperlukan untuk
duplikasi sentrosom dan replikasi DNA. NPM merupakan onkogen kuat dan
menyebabkan translokasi kromosom pada leukemia myeloid akut.12,13
ARF merupakan protein yang berperan sebagai gen penekan tumor dalam
nukleolar. Laporan terbaru dari Sherr, Roussel dan Yanping Zhang menunjukkan
bahwa NPM dan ARF berinteraksi secara langsung dalam nukleolus. Laporan data
juga menunjukkan NPM nucleocytoplasmic merupakan kunci utama dalam
mempromosi proliferasi sel. Pengolahan rRNA dipengaruhi oleh pembentukan
kompleks ARF - NPM dalam nukleolus. ARF berinteraksi dengan protein argyrofilik
nucleolar untuk mencegah produksi ribosom dan tumorigenesis, serta
menggarisbawahi potensi onkogenik pada nukleolus.12
Protein shuttling di antara nukleus dan sitoplasma merupakan kunci mekanisme
dalam memastikan perkembangan siklus sel yang tepat. Dalam penelitian
sebelumnya, NPM telah diidentifikasi sebagai target p53-independen novel oleh
protein penekan tumor ARF. Dalam menanggapi sinyal hiperproliferatif karena NPM,
nukleolar ARF mengikat NPM secara efektif dalam menghambat shuttling
nucleocytoplasmic NPM.13 Tanpa sebuah checkpoint ARF utuh, protein nukleolus seperti NPM dapat berubah dan menyebabkan tumorigenesis melalui berbagai fungsi
nukleolarnya.12
2.3.4 Perwarnaan AgNOR
Pemeriksaan kanker pada saat ini banyak dilakukan dengan mengamati
proliferasi dan apoptosis sel. Proliferasi sel dapat dipelajari secara baik dengan
metode “flow-sitometri” atau pelabelan radioisotop dengan Ki-67, PCNA
(Proliferating Cell Nuclear Antigen) dan teknik pewarnaan seperti AgNORs. Metode
AgNOR ini dapat digunakan dalam mengevaluasi morfologi dan kinetika sel, dan
merupakan parameter yang digunakan dalam menilai respon radiasi melalui hasil
Pewarnaan AgNOR (prosedurnya dirujuk pada muka surat 32) ini dengan
mudah dapat dilakukan pada jaringan yang difiksasi dengan formalin, dan digunakan
untuk mengevaluasi morfologi dan kinetika sel dalam biopsi dengan ukuran yang
kecil.16 Marker kanker AgNORs dapat digunakan untuk melakukan pemeriksaan proliferasi melalui bercak AgNORs pada daerah inti atau “Nucleolar Organizer
Regions” (NORs) lengkung DNA ribosom yang ditranskripsikan menjadi RNA
ribosomal dengan bantuan RNA polymerase.31
Pengamatan sejumlah parameter AgNOR (jumlah, ukuran dan distibusi) dapat
digunakan dalam patologi sel kanker untuk kepentingan diagnostik maupun
prognostik.Jumlah, ukuran dan distribusi AgNOR dalam nukleus dapat digunakan
untuk memdeteksi dan memprediksi prognosis sejumlah neoplasia, seperti kandung
kemih, karsinoma faring, dan lesi pada kulit.16,31AgNOR diamati dengan mikroskop cahaya sebagai titik-titik hitam. Pengamatan AgNOR secara kuantifikasi dan
kualitatif lebih tepat dengan menggunakan metode morfometrik, dimana AgNORnya
diperbesarkan dengan skala geometrik tertentu sehingga gambarannya kelihatan lebih
jelas.19
Penelitian menunjukkan AgNOR dapat digunakan untuk menunjukkan adanya
aktifitas biologis pada karsinoma sel skuamosa. AgNOR juga digunakan pada oral
submukus fibrosis untuk memperkirakan perilaku biologis oral submukus fibrosis,
yang dapat dihubungkan dengan gradasi histologi klinis. Ketertarikan para ahli pada protein AgNOR meningkat sekitar tahun 1980-an diikuti dengan observasi bahwa sel
ganas memiliki jumlah AgNOR yang lebih tinggi dibandingkan dengan sel yang jinak
atau sel normal.34 Pada penelitian Salehinejad, dkk. (2007), sel ganas menunjukkan jumlah AgNOR yang lebih banyak dan bentuk tidak beraturan, sedangkan sel jinak
memiliki AgNOR yang lebih sedikit dengan bentuk yang teratur.35 Pada sel normal, hanya satu atau dua titik AgNOR yang dilihat sebagai titik-titik yang padat. Bagi
sel-sel normal (Gambar 6) yang semakin bergerak menuju ke sel-sel displastik dan sel-sel-sel-sel
ganas, jumlah DNA semakin meningkat berserta dengan peningkatan jumlah titik
AgNOR. Sel-sel ganas mempunyai derajat diferensiasi yang berlainan yang dimana
diferensiasi baik (Gambar 7) mempunyai nilai AgNOR yang rendah dibanding dengan
sel ganas yang diferensiasinya sedang (Gambar 8), buruk (Gambar 9) atau
undifferentiated (Gambar 10). Ini karena derajat diferensiasi secara umum
berhubungan dengan tingkat keganasan dan proliferasi sel, sehingga tumor yang
derajat diferensiasinya buruk akan mempunyai tingkat proliferasi yang lebih tinggi
yang tercermin dari nilai AgNOR yang lebih tinggi.36,37,38 Saat ini, berbagai studi dilakukan untuk mengetahui kemungkinan menemukan penanda keganasan dari
titik-titik AgNOR. Hal ini dilakukan karena teknik ini mudah dilakukan, murah, cepat dan
menghasilkan informasi yang akurat tentang perkembangan keganasan.35
Gambar 6. Gambaran mikroskopis mukosa normal rongga mulut
Gambar 7. Gambaran mikroskopis karsinoma sel skuamous (KSS) rongga mulut berdiferensiasi baik dengan NORs yang sedikit terdapat pada inti (1000X). Anak panah biru menunjukkan titik hitam AgNOR.38
Gambar 9. Gambaran mikroskopis karsinoma sel skuamous (KSS) rongga mulut berdiferensiasi buruk dengan jumlah NORs yang banyak dan beragam pada inti (1000X). Anak panah biru menunjukkan titik hitam AgNOR.38
Gambar 10. Gambaran mikroskopis karsinoma sel skuamous (KSS) rongga mulut tidak berdiferensiasi (undifferentiated) dengan jumlah NORs yang banyak dan berkelompok pada inti (1000X). Anak panah biru menunjukkan titik
Perbaikan
Sel epitel rongga mulut
Nukleus
Nukleolus
Nucleolus Organizer Region(NOR)
p53 terhambat sehingga perbaikan
DNA terhambat
NORassociated protein (NORAPs) yang bersifat
asam berhubungan dengan transkripsi RNA
Mutasi gen
ARF normal dan Nucleophosmin
dalam keadaan terkontrol
ARF terhambat masuk ke nukleoplasma
Displasia
Karsinoma rongga mulut
Sel Normal
Perbaikan DNA yang terhambat semakin banyak
Proliferasi
Pewarnaan AgNOR dan pengamatan titik-titik hitam dibawah mikroskop cahaya
Ekspresi Nucleophosmin berlebihan dan mencegah
agregasi NOR yang terjadi secara menetap
Perbaikan
DNA
berhasil (reversible) 2.5 Kerangka Konsep
Sel epitel rongga mulut
Nukleus
Nukleolus
Nucleolus Organizer Region(NOR)
p53 terhambat sehingga perbaikan
DNA terhambat
NORassociated protein (NORAPs) yang
bersifat asam berhubungan dengan
transkripsi RNA
Mutasi gen
ARF normal dan Nucleophosmin
dalam keadaan terkontrol
Displasia
Karsinoma rongga mulut
Pewarnaan AgNOR dan pengamatan titik-titik hitam dibawah mikroskop cahaya
BAB 3
METODOLOGI PENELITIAN
3.1 Jenis Penelitian
Penelitian ini merupakan rancangan deskriptif analitik dengan pendekatan
cross-sectional yang dimana setiap sampel diperiksa satu kali dan pada suatu saat
tertentu.
3.2 Lokasi dan Waktu Penelitian
3.2.1 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Patologi Anatomi Fakultas
Kedokteran USU/RSUP Haji Adam Malik Medan.
3.2.2 Waktu Penelitian
Penelitian ini dimulai dari bulan April 2014 sampai Juni 2014 yang mencakup
pengumpulan data, pengumpulan sampel, penelitian, pengolahan data dan hasil
penelitian.
3.3 Populasi, Sampel, dan Besar Sampel Penelitian
3.3.1 Populasi
Populasi dalam penelitian ini mencakup sediaan blok parafin yang berasal dari
jaringan biopsi rongga mulut yang telah didiagnosa secara histopatologi dengan
pewarnaan H&E KSS rongga mulut pada laboratorium Patologi Anatomi FK
USU/RSUP Haji Adam Malik Medan.
3.3.2 Sampel
Sampel penelitian ini adalah sediaan blok parafin yang berasal dari biopsi
jaringan rongga mulut yang sesuai dengan kriteria inklusi dan ekslusi yang sesuai
3.3.3 Besar Sampel
Penentuan jumlah sampel menggunakan rumus Penaksiran Proporsi Populasi
dengan ketelitian absolut (Absolute Precision) dengan teknik sampling, consecutive
sampling yaitu non-random sampel yang seperti convenience sampling kecuali
consecutive sampling sampel yang tersedia mempunyai kriteria yang telah ditentukan
sampai mencapai besar sampel yang telah ditentukan.38
Jumlah sampel yang diperlukan berdasarkan hasil perhitungan dengan melihat
proporsi yang digunakan pada kasus ini adalah sebesar 50% dengan tingkat kemaknaan 0,05 dan interval kepercayaan 90% dari tabel yang didapatkan Zα = 1,64.
Keterangan:
n = jumlah proporsi
Zα = tingkat kepercayaan (90% Z skor = 1,64)
P = proporsi (seluruh lesi), bila tidak ada dianggap 50% atau 0,5
d = ketepatan (15%)
Hasil perhitungan:
n = 1,642 x 0,5 x 0,5 (0,15)2 n = 29,8
Jumlah minimal sampel yang diperlukan adalah 30 sampel KSS rongga
mulut.
3.4 Kriteria Inkusi dan Ekslusi
3.4.1 Kriteria Inklusi
- Blok paraffin yang telah didiagnosa sebagai KSS rongga mulut.
- Pengambilan spesimen blok paraffin dari tahun 2009-2013.
- Data rekam medis dari tahun 2009-2013 yang terdiri dari: diagnosa
histopatologi, umur pasien, jenis kelamin dan lokasi lesi.
3.4.2 Kriteria Ekslusi
- Blok paraffin KSS rongga mulut yang telah rusak.
3.5Kerangka Operasional
Blok paraffin dari biopsi lesi rongga mulut di Lab Patologi FK USU/RSUP Haji Adam Malik Medan yang didiagnosa secara histopatologi dengan pewarnaan H&E
sebagai KSS rongga mulut
Pemotongan blok parafin
Perhitungan titik-titik hitam dalam nukleus secara acak pada 100 nuklei di
bawah mikroskop cahaya Olympus CX21 (100x)
Hasil Pengamatan mAgNOR
Pewarnaan Hematoxylin-Eosin (HE) Pewarnaan AgNOR
3.6Variabel Penelitian
3.6.1Variabel Bebas
Karsinoma sel skuamosa rongga mulut.
3.6.2Variabel Terikat
Hasil distribusi frekuensi mean titik-titik hitam (NOR) dalam nuklei.
3.6.3Variabel Terkendali
1. Blok paraffin KSS rongga mulut tahun 2009-2013.
2. Processing laboratorium pewarnaan H&E dan histokimia.
3. Data rekam medis pasien dari tahun 2009-2013.
4. Keterampilan operator.
Hasil mean titik-titik hitam (NOR) dalam nukleus pada
tipe differensiasi KSS rongga mulut
Variabel terkendali
- Blok paraffin karsinoma skuamosa sel rongga mulut tahun 2009-2013.
- Processing laboratorium untuk pewarnaan AgNOR.
3.7 Definisi Operasional
Blok paraffin merupakan hasil dari proses embedding jaringan-jaringan
biopsi atau lesi keganasan rongga mulut dari operasi dari tahun 2009-2013 yang
dikirim ke bagian patologi.
KSS rongga mulut adalah keganasan yang berasal dari sel skuamosa
rongga mulut dimana terdapatnya kelainan seluler yang berupa diskontinuitas
membran basalis oleh kelompokan sel-sel tumor yang meluas sampai ke jaringan ikat
dengan ukuran sel beragam, mitosis meningkat, perubahan ukuran dan bentuk inti sel.
Pewarnaan HE merupakan suatu pewarnaan histokimia yang digunakan untuk mewarnai jaringan histologi agar berbagai unsur jaringan jelas terlihat dan
dapat dibedakan. Hasil pewarnaan HE dapat membantu dalam menilai derajat
keganasan suatu karsinoma dengan menilai karakteristik jaringan tersebut.
Derajat diferensiasi KSS dapat dibagi kepada tiga jenis yaitu KSS
berdiferensiasi baik, sedang, dan buruk. Derajat diferensiasi KSS dinilai dengan
sistem Bryne menurut karakteristik morfologi masing-masing kategori. Penilaian
hasil derajat diferensiasi KSS adalah melalui skor, yaitu, skor 4-8 (diferensiasi baik),
skor 9-12 (diferensiasi sedang), dan skor 13-16 (diferensiasi buruk). KSS diferensiasi
baik selalunya mempunyai keratinisasi yang lebih dari >50%, mengandung sel yang
mirip sel matur normal asal jaringan (pleomorphisme sel ringan) dan sel limfosistik
yang banyak. KSS diferensiasi sedang mempunyai keratinisasi yang lebih kurang dari
KSS berdiferensiasi baik atau tidak berkeratin, pleomorphisme sel yang sedang dan
sel limfosistik yang sedang. KSS diferensiasi buruk mayoritasnya tidak berkeratin,
pleomorphisme sel berat, sel mirip primitif dan tidak spesifik serta sel limfosistik
ringan.
Pewarnaan AgNORmerupakan suatu pewarnaan histokimia dimana larutan perak nitrat berikatan pada bagian nucleolar organizing region (NOR) yang bersifat
argyrofilik dan pewarnaan ini merupakan suatu marker atau petanda proliferasi sel.
Penilaian hasil pewarnaan AgNOR adalah tampilan titik-titik kecoklatan atau hitam
pada inti sel epitel yang dilihat dengan menggunakan mikroskop cahaya Olympus
3.8Alat dan Bahan
3.8.1 Alat-alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah sebagai berikut:
1. Mikroskop cahaya Olympus CX21
2. Mikrotom
12.Tissue embedding centre compressor
3.8.2Bahan Penelitian
Bahan penelitian yang digunakan pada penelitian ini adalah:
1. Parafin blok KSS rongga mulut
2. 2% bubuk gelatin
3. 1% asam formiat
4. 50% perak nitrat MERCK
3.9Prosedur Pengambilan dan Pengumpulan Data
Tahap-tahap pengambilan dan pengumpulan data pada penelitian ini adalah
seperti berikut:
3.9.1Pembuatan Sediaan Mikroskopis dari Blok Parafin
Blok paraffin yang telah dikumpulkan, disimpan dalam freezer sampai
cukup dingin, dan kemudian dipotong tipis dengan menggunakan mikrotom dengan
ketebalan 4µm atau 5µm.39 Setiap blok paraffin dipotong sebanyak dua kali untuk masing-masing pewarnaan H&E dan AgNOR. Tempel blok parafin yang telah
dipotong pada gelas objek.
3.9.2Prosedur Pewarnaan Hematoxylin-eosin
Berikut ini adalah penjelasan tentang prosedur pewarnaan H&E39:
1. Setelah difiksasi, preparat dicelupkan dalam hematoxylin selama 5 menit
lalu dibilas dengan air mengalir selama 3 menit.
2. Preparat dicelupkan ke dalam acid alkohol 1% sebanyak 2 kali lalu
dibilas kembali dengan air mengalir selama 3 menit.
3. Lakukan pewarnaan dengan eosin untuk mewarnai nukleus selama 2-3
menit lalu bilas kembali dengan air mengalir selama 3 menit.
4. Kemudian preparat dicelupkan ke dalam alkohol 70%, selama 30 menit,
alkohol 95% selama 3 menit dan alkohol absolut selama 3 menit.
5. Preparat dicelupkan ke dalam xylene selama 3 menit sebanyak 3 kali
pengulangan.
6. Preparat di mounting dengan kanada balsam dan ditutup dengan cover
3.9.3 Prosedur Pewarnaan AgNOR
Berikut ini adalah penjelasan tentang prosedur pewarnaan AgNOR40:
1. Lakukan deparafinasi preparat dengan xylene sebanyak 3 kali
masing-masing 3 menit.
2. Rehidrasi preparat dengan menggunakan absolut alkohol, alkohol 95%
dan alkohol 70% masing-masing selama dua menit, dua menit, satu menit dan
terakhir dengan air aquades selama satu menit.
3. Diperlukan dua larutan, yang pertama larutan A merupakan 2% gelatin
yang ditambahkan dengan 1% asam format.
4. Larutan B merupakan perak nitrat 50%. Larutan pewarnaan diperoleh
dengan mencampur satu bagian dari larutan A dengan dua bagian larutan B dalam
gelas silinder.
5. Larutan pewarnaan dituangkan pada objek gelas. Pewarnaan memerlukan
waktu 30 menit pada suhu ruangan. Selama pewarnaan, sebaiknya menghindari
cahaya matahari langsung.
6. Setelah itu, larutan pewarnaan dibilas dengan air deionisasi sebanyak 3
kali dan dilakukan dehidrasi berurutan dengan menggunakan alkohol bergradasi dan
lakukan mounting.
7. Objek gelas diamati dibawah mikroskop cahaya dengan pembesaran
x100 bersama immersion oil dan titik-titik hitam diperhitungkan dalam nukleus.
8. Setiap hasil pengamatan dicatatkan dan didokumentasikan.
3.10 Pengolahan dan Analisis Data
Pengolahan data dilakukan dengan tabel cross-sectional. Pelaporan data
penelitian adalah dengan memaparkan hasil pengamatan titik-titik hitam AgNOR dalam
BAB 4
HASIL PENELITIAN
Blok parafin yang digunakan oleh peneliti, dikumpulkan dari RSUP Haji
Adam Malik Medan dengan jumlah sampel 30 blok parafin. Sampel penelitian ini
adalah sampel yang memenuhi kriteria inklusi dan ekslusi.
4.1 Karakteristik Umum Sampel yang diteliti
Sampel penelitian yang telah dikumpulkan diambil datanya melalui rekam
medik. Data yang diambil menurut data rekam medis adalah umur, jenis kelamin dan
lokasi lesi (Tabel 3).
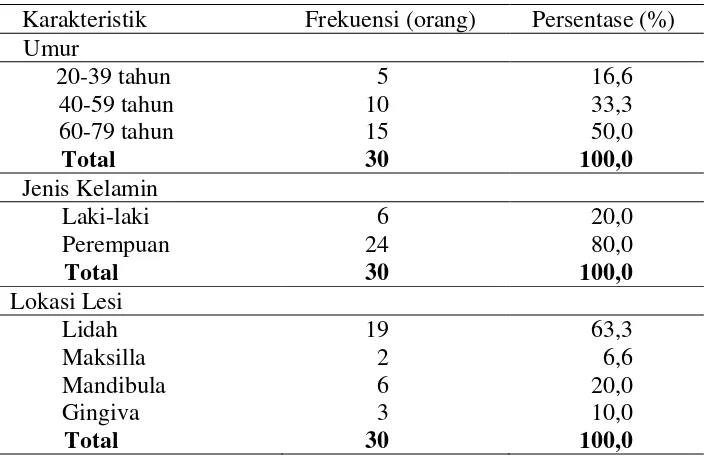
Tabel 3. Distribusi frekuensi karakteristik umum sampel berdasarkan data rekam medis sampel yang diteliti.
Tabel 3 menunjukkan karakteristik umum berdasarkan data rekam medis
KSS rongga mulut yang telah didiagnosa di RSUP Haji Adam Malik Medan.
Berdasarkan umur, KSS rongga mulut tertinggi adalah pada kelompok umur 60 - 79
tahun (50,0%), diikuti kelompok umur 40 - 59 tahun (33,3%) dan terendah
ditemukan pada kelompok umur 20 - 39 tahun (16,6%). Berdasarkan jenis kelamin,
KSS rongga mulut pada wanita (80,0%) lebih tinggi dari laki-laki (20,0%). Lokasi
lesi yang paling tinggi ditemukan pada lidah (63,3%), diikuti mandibula (20%), dan
gingiva (10,0%), sedangkan lokasi lesi terendah adalah maksila (6,6%).
4.2 Distribusi Frekuensi Tampilan mAgNOR pada KSS Rongga Mulut Berdasarkan Sub-tipe Keratinisasi, Jenis Diferensiasi, Umur, Jenis Kelamin dan
Lokasi Lesi.
AgNOR ditemukan sebagai titik-titik hitam di dalam nukleus sel yang dihitung
dalam 100 nukleus sel pada masing-masing 30 sampel KSS rongga mulut, dan
hitungan rata-rata mAgNOR dikelompokkan berdasarkan masing-masing kategori.
Tabel 4. Distribusi frekuensi tampilan mAgNOR pada KSS rongga
tidak ditemukan perbedaan yang signifikan mAgNOR antara KSS berkeratinisasi dan
Tabel 5. Distribusi frekuensi tampilan mAgNOR pada KSS rongga
perbedaan yang signifikan mAgNOR antara KSS diferensiasi baik dan diferensiasi
sedang (p=0,000). Ini berarti semakin menurun atau buruknya derajat diferensiasi
KSS, nilai tampilan titik-titik hitam mAgNOR akan semakin meningkat. Dengan
demikian H0 ditolak.
ditemukan perbedaan yang signifikan mAgNOR antara kelompok umur sampel
penelitian (p=0,964). Ini berarti H0 diterima.
Hasil analisa statistik uji Kruskal-Wallis (Tabel 7), ditemukan bahwa tidak
terdapatnya perbedaan yang signifikan mAgNOR antara laki-laki dan perempuan
(p=0,053). Ini berarti H0 diterima.
Tabel 8. Distribusi frekuensi tampilan mAgNOR pada KSS rongga mulut berdasarkan lokasi lesi.
Lokasi Lesi n mAgNOR ± SD p Lidah
Maksila Mandibula Gingiva
19 2 6 3
4,39±0,75 4,10±0,80 4,86±1,07 3,67±0,55
0,195
Total 30
Uji Kruskal-Wallis, signifikan p < 0,05.
Tabel 8 menunjukkan hasil analisa statistik uji Kruskal-Wallis dimana tidak
ditemukan perbedaan yang signifikan mAgNOR antara masing-masing lokasi lesi di
BAB 5
PEMBAHASAN
Telah dilakukan penelitian terhadap 30 sampel blok parafin yang telah
didiagnosa sebagai karsinoma sel skuamosa (KSS) rongga mulut yang diperoleh dari
data-data rekam medis di Laboratorium Patologi Anatomi RSUP Haji Adam Malik
dan Laboratorium PA FK USU. Blok parafin yang telah dikumpulkan, kemudian di
processing di laboratorium Patologi Anatomi: satu preparat untuk pewarnaan
Hematoxylin-Eosin (HE) dan satu preparat untuk pewarnaan AgNOR. Pewarnaan HE
dilakukan untuk mendiagnosa kembali jaringan sampel tersebut. Sementara itu,
pewarnaan AgNOR bertujuan untuk mendapatkan tampilan titik-titik hitam yang
berperan sebagai suatu metode untuk melihat tingkat keagresifan proliferasi sel
kanker. Pewarnaan AgNOR merupakan suatu pewarnaan histokimia dimana larutan
perak nitrat berikatan pada bagian NOR yang bersifat argyrofilik. Larutan AgNOR
berupa campuran dari satu volume asam format yang ditambah gelatin dan dua
volume perak nitrat. Protein nucleolar organizing regions (NORs) yang bersifat
argyrofilik yang apabila bereaksi dengan perak nitrat akan menghasilkan warna hitam
berupa titik-titik hitam (AgNOR) dalam nukleus sel. Titik-titik hitam yang jelas
kelihatan dihitungkan, sementara gugusan titik-titik hitam diabaikan.14 Hasil pewarnaan HE dan AgNOR diobservasi dengan menggunakan mikroskop cahaya
Olympus CX21 dengan pembesaran 40x dan 100x. Hasil pewarnaan AgNOR
diperoleh melalui perhitungan jumlah titik-titik hitam AgNOR dalam 100 nukleus
sehingga didapatkan rata-rata AgNOR (mAgNOR) dan standar deviasinya. Rancangan
penelitian yang digunakan adalah bersifat deskriptif analitik dengan pendekatan cross
sectional dan dianalisis dengan uji Kruskal-Wallis.
Dari data-data rekam medis lesi rongga mulut yang diperoleh pada penelitian
ini, hanya data umum berupa umur, jenis kelamin dan lokasi lesi yang tersedia dan
diet, pekerjaan atau kondisi rongga mulut yang berhubungan dengan etiologi
terjadinya kanker. Perlunya data-data tersebut ditulis dalam formulir pemeriksaan
patologi rongga mulut (Lampiran 3) sehingga dapat mendukung suatu diagnosa
patologi yang tepat.
Pada penelitian ini diperoleh data distribusi rekam medis karakteristik umum
berupa umur, jenis kelamin dan lokasi lesi (Tabel 3). Lesi KSS pada rongga mulut
yang tertinggi ditemukan pada kelompok umur 60 - 79 tahun (50,0%), diikuti oleh
kelompok umur 40 - 59 tahun (33,3%) dan terendah terdapat pada kelompok umur 20
- 39 tahun (16,6%). Menurut Cawson (2008), 98% dari lesi KSS rongga mulut
terdapat pada kelompok umur di atas 40 tahun,2 dimana sesuai dengan penelitian ini, yaitu kelompok umur yang berisiko tinggi terdapat pada kelompok umur 40 - 79
tahun yaitu sekitar (83,3%), sedangkan kelompok umur yang berisiko rendah terdapat
pada kelompok umur 20 - 39 tahun (16,6%). Peningkatan umur sering dihubungkan
dengan perubahan pada tingkat molekular, selular dan fisiologis, sehingga jaringan
lebih rentan terhadap inisiasi karsinogenesis bila didukung dengan pemaparan
agen/bahan karsinogenik. Di samping itu, pada usia lanjut juga sering timbul
ketidakseimbangan hormon sehingga risiko terjadinya kanker juga meningkat.2,3,5 Berdasarkan jenis kelamin, lesi KSS lebih banyak ditemukan pada perempuan
(80,0%) dibandingkan laki-laki (20,0%). Penelitian ini sesuai dengan penelitian
Ramachandra (2012) di negara India, dimana angka prevalensi pada perempuan lebih
tinggi dibandingkan laki-laki,41 ini mungkin dihubungkan dengan kebiasaan menyirih/menyuntil pada kalangan perempuan, di samping itu mungkin juga
terjadinya ketidakseimbangan hormonal, dimana perempuan sering mengalami
perubahan di rongga mulut setelah mencapai menopause. Lokasi lesi KSS rongga
mulut yang paling banyak ditemukan pada lidah (63,3%) dibandingkan dengan lokasi
lesi lainnya di rongga mulut (36,7%). Hal ini sesuai dengan penelitian yang dilakukan
oleh Neena, dkk. (2011), yang mendapatkan bahwa lidah merupakan lokasi lesi KSS
yang paling banyak terdapat pada rongga mulut (60,4%).21 Insidensi KSS yang tinggi pada lidah mungkin disebabkan oleh beberapa faktor yaitu antaraa lain: iritasi kronis
seperti merokok, minuman alkohol dan menyuntil.2,5 Bagian lidah lateral merupakan bagian yang sering terjadinya kanker. Hal ini dikaitkan dengan struktur histologinya,
dimana epitelnya dilapisi dengan mukosa yang tidak berkeratin. Epitel yang tidak
berkeratin mudah berubah menjadi tipe berkeratin sebagai respon terhadap trauma
gesekan atau kimia, sehingga terjadi hiperkeratinisasi. Perubahan hiperkeratinisasi ini
bersifat reversibel jika sumber traumanya dihilangkan, dan bila trauma kronis terus
berlanjut, akan mengakibatkan terjadinya karsinoma.42
Pewarnaan HE digunakan sebagai pendiagnosa rutin untuk jaringan KSS
dalam menentukan diferensiasi histopatologi. Derajat diferensiasi KSS rongga mulut
dapat dibagi kepada tiga jenis yaitu KSS berdiferensiasi baik, sedang, dan buruk.
Penilaian derajat diferensiasi ini dapat berdasarkan karakteristik sistem penilaian oleh
Broder, Jakobsson, Anneroth, atau Bryne. Sistem penilaian derajat diferensiasi pada
penelitian ini adalah berdasarkan sistem terbaru Bryne, dimana sistem ini mempunyai
parameter morfologi yang adekuat dalam penilaian karakteristik jaringan KSS. Selain
itu, sistem Bryne juga berperan sebagai suatu indikator dalam memprediksi prognosa
KSS.21 Pada penelitian ini, KSS rongga mulut berdiferensiasi baik (63%) lebih banyak ditemukan dibanding dengan KSS berdiferensiasi sedang (37%), tetapi tidak
ditemukan KSS berdiferensiasi buruk. Keratin jenis hiperkeratotik yang ditemukan
pada epitel dari sel tumor merupakan salah satu penanda untuk transformasi
“maglinant” atau kanker. KSS berdiferensiasi baik selalunya menunjukkan
keratinisasi yang lebih banyak dibandingkan dengan KSS berdiferensiasi sedang dan
buruk. KSS berdiferensiasi buruk mayoritas jaringannya tidak berkeratinisasi. KSS
berdiferensiasi baik mempunyai sel yang mirip sel matur normal asal jaringan dan
mempunyai sel limfosistik yang banyak akibat reaksi dari jaringan untuk
memperbaiki sel yang rusak. KSS yang berdiferensiasi sedang dan buruk mempunyai
sel atau inti yang pleomorfik, yaitu ukuran sel yang bervariasi dan besar, serta sering
tidak ditemukan sel limfosistik. Pada KSS berdiferensiasi buruk, adanya ditemukan