UJI BIOAKTIVITAS ZAT EKSTRAKTIF KAYU SUREN
(Toona sureni Merr.) dan KI BONTENG (Platea latifolia BL.)
MENGGUNAKAN BRINE SHRIMP LETHALITY TEST (BSLT)
SRI WAHYUNI MEILANI
DEPARTEMEN HASIL HUTAN
FAKULTAS KEHUTANAN
INSTITUT PERTANIAN BOGOR
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi Uji Bioaktivitas Zat Ekstraktif
Kayu Suren (Toona sureni Merr.) dan Ki bonteng (Platea latifolia BL.)
Menggunakan Brine Shrimp Lethality Test (BSLT) adalah karya saya sendiri dan
belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber
informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak
diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam
Daftar Pustaka di bagian akhir skripsi ini.
Bogor, September 2006
ABSTRAK
SRI WAHYUNI MEILANI. Uji Bioaktivitas Zat Ekstraktif Kayu Suren (Toona sureni Merr.) dan Ki bonteng (Platea latifolia BL.) Menggunakan Brine Shrimp Lethality Test (BSLT). Dibimbing oleh WASRIN SYAFII dan RITA KARTIKA SARI.
Negara Indonesia dikenal dunia memiliki hutan hujan tropika yang kaya akan keanekaragaman flora. Bagian daun dan kulit batang pohon suren (Toona sureni Merr.) telah lama digunakan masyarakat umum sebagai obat tradisional (Sangat el al. 2000). Di hutan alam kawasan Gunung Salak, Jawa Barat ditemukan 112 jenis tumbuhan dari 49 famili yang berpotensi sebagai tumbuhan obat diantaranya ki bonteng (Platea latifolia BL.), karena mengandung senyawa alkaloid, flavonoid dan saponin yang merupakan kelompok senyawa bioaktif (Sugiana 2003). Maka perlu dilakukan penelitian mengenai bioaktivitas dari kedua jenis tersebut agar ditemukan senyawa kimia berkhasiat obat khususnya antikanker. Metode bioassay untuk menguji aktivitas antikanker ekstrak suatu tumbuhan adalah Brine Shrimp Lethality Test (BSLT) dengan menggunakan hewan uji Artemia salina Leach. Penelitian ini dilakukan untuk mengetahui kandungan zat ekstrakif kulit dalam (inner bark) dan bagian teras cabang suren dan ki bonteng yang larut dalam pelarut aseton dan hasil fraksinasinya dengan pelarut n-heksana, etil-asetat serta residu dari ekstrak aseton tersebut serta untuk mengetahui bioaktivitas zat ekstraktif tersebut terhadap A. salina.
Penelitian ini dilakukan dalam beberapa tahapan yaitu ekstraksi serbuk (40-60 mesh) dari inner bark dan bagian teras cabang suren dan ki bonteng dengan menggunakan pelarut aseton dan kemudian fraksinasi dengan pelarut n-heksana dan etil asetat. Kemudian ekstrak dan fraksinya diujikan terhadap larva udang A. salina dan data mortalitas diolah dengan menggunakan analisis probit untuk mendapatkan nilai LC50.
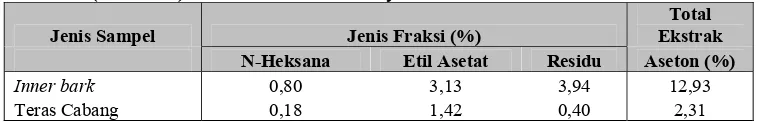
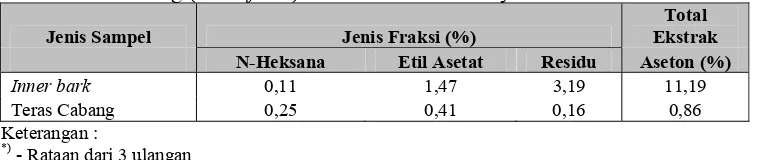
Hasil ekstraksi dan fraksinasi menunjukkan bahwa inner bark suren mengandung 12,93 % ekstrak aseton yang terdiri dari 0,80 % fraksi n-heksana; 3,13 % fraksi etil asetat dan 3,94 % fraksi residu. Sedangkan bagian teras cabangnya mengandung 2,31 % ekstrak aseton dengan 0,18 % fraksi n-heksana; 1,42 % fraksi etil asetat dan 0,40 % fraksi residu. Untuk jenis ki bonteng, inner barknya mengandung 11,19 % ekstrak aseton dengan fraksi n-heksana 0,11 %; fraksi etil-asetat 1,47 % dan fraksi residu 3,19 %. Sedangkan bagian teras cabangnya mengandung 0,90 % ekstrak aseton dengan fraksi n-heksana 0,25 %; fraksi etil-asetat 0,41 % dan fraksi residu 0,16 %.
UJI BIOAKTIVITAS ZAT EKSTRAKTIF KAYU SUREN
(Toona sureni Merr.) dan KI BONTENG(Platea latifolia BL.)
MENGGUNAKAN BRINE SHRIMP LETHALITY TEST (BSLT)
SRI WAHYUNI MEILANI
E24102020
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kehutanan
Pada Fakultas Kehutanan Institut Pertanian Bogor
DEPARTEMEN HASIL HUTAN
FAKULTAS KEHUTANAN
INSTITUT PERTANIAN BOGOR
LEMBAR PENGESAHAN
Judul Penelitian : Uji Bioaktivitas Zat Ekstraktif Kayu Suren (Toona sureni Merr.) dan Ki bonteng (Platea latifolia BL.) Menggunakan Brine Shrimp Lethality Test (BSLT). Nama Mahasiswa : Sri Wahyuni Meilani
NRP : E 24102020
Disetujui,
Komisi Pembimbing
Prof.Dr.Ir.H.Wasrin Syafii, M.Agr Ir. Rita Kartika Sari, M.Si
Ketua Anggota
Diketahui,
Dekan Fakultas Kehutanan
Institut Pertanian Bogor
Prof.Dr.Ir. Cecep Kusmana, MS
Tanggal :
RIWAYAT HIDUP
Penulis dilahirkan di Pekanbaru, Riau pada tanggal 5 Mei 1985. Penulis
merupakan anak kedua dari tiga bersaudara keluarga Wahyono Wassim dan
Tiasari Hasibuan.
Penulis memulai pendidikan di TK Bhayangkari tahun 1989, tahun 1990
masuk Sekolah Dasar Negeri 004 Tembilahan, Kabupaten Indragiri Hilir Propinsi
Riau. Pada tahun 1996 penulis melanjutkan pendidikan ke SLTP Negeri 2
Tembilahan kemudian pada tahun 2002 lulus dari SMU Negeri 2 Tembilahan.
Pada tahun yang sama melalui jalur Undangan Seleksi Masuk IPB (USMI),
penulis diterima di Institut Pertanian Bogor pada Jurusan Teknologi Hasil Hutan,
Fakultas Kehutanan.
Selama mahasiswa, penulis aktif pada Badan Eksekutif Mahasiswa Fakultas
Kehutanan periode tahun 2003-2004 sebagai staff Departemen Kesekretariatan
dan Lembaga Kemahasiswaan Himpunan Profesi Mahasiswa Teknologi Hasil
Hutan (HIMASILTAN) sebagai Kepala Departemen Kesekretariatan periode
2004-2005. Selain itu, penulis juga aktif di berbagai kepanitiaan diantaranya Bina
Corps Rimbawan 2003, Forester Cup 2003, pelepasan wisuda Fakultas Kehutanan
2004 dan KOMPAK THH 2004.
Penulis pernah mengikuti kegiatan Field Trip di PT Trakindo Utama Bekasi,
PT Inhutani II Bekasi, dan Pabrik Pengolahan Gondorukem dan Terpentin (PGT)
Sindang Wangi, Nagrek, Perum Perhutani Unit III Jawa Barat. Pada tahun 2005,
penulis melaksanakan Praktek Pengenalan dan Pengelolaan Hutan (P3H)
kelompok Getas II jalur Baturraden-Cilacap dan Kampus Lapangan UGM, di
Getas, Ngawi, Jawa Timur. Selain itu, pada tahun 2006 penulis melaksanakan
Praktek Kerja Lapang (PKL) di HPHTI PT Arara Abadi (Sinar Mas Group)
Perawang, Kabupaten Siak Propinsi Riau.
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Kehutanan IPB,
penulis melakukan penelitian yang berjudul ”Uji Bioaktivitas Kayu Suren
(Toona sureni Merr.) dan Ki bonteng (Platea latifolia BL.) Menggunakan
Brine Shrimp Lethality Test (BSLT)”, dibawah bimbingan Prof.Dr.Ir.H. Wasrin
PRAKATA
Alhamdulillah, puji dan syukur penulis panjatkan kehadirat Allah SWT
karena atas rahmat dan karunia-Nya penulis dapat menyelesaikan skripsi yang
berjudul ”Uji Bioaktivitas Zat Ekstraktif Kayu Suren (Toona sureni Merr.) dan Ki
bonteng (Platea latifolia BL.) Menggunakan Brine Shrimp Lethality Test (BSLT)”
ini dengan sebaik-baiknya. Skripsi ini disusun sebagai salah satu syarat untuk
memperoleh gelar Sarjana Kehutanan pada Fakultas Kehutanan Institut Pertanian
Bogor.
Pada kesempatan ini, penulis mengucapkan terima kasih yang
sebesar-besarnya kepada :
1. Bapak, mama, bang Febri, adek Rani tercinta, keluarga besar Wassim dan
Dullah Sidik Hasibuan serta bang Neko yang telah memberikan doa, cinta
kasih, perhatian, dukungan, semangat dan motivasinya kepada penulis.
2. Bapak Prof.Dr.Ir.H. Wasrin Syafii, M.Agr selaku pembimbing skripsi 1 dan
Ibu Ir. Rita Kartika Sari, M.Si selaku pembimbing skripsi 2 atas segala
perhatian, masukan, nasehat-nasehat dan bimbingannya.
3. Bapak Drs. Simon Taka Nuhamara, MS selaku dosen penguji dari Departemen
Silvikultur dan Bapak Ir. Edhi Sandra, M.Si selaku dosen penguji dari
Departemen Konservasi Sumberdaya Hutan dan Ekowisata.
4. Seluruh staf dan laboran laboratorium Kimia Hasil Hutan Departemen Hasil
Hutan atas bantuannya selama melaksanakan penelitian.
5. Nura, Fadli dan Ijul atas kerjasamanya selama penelitian.
6. Budi, Ieka, Tia, Nia, Chiput, Irma, Buyung, Rais, Doto dan keluarga besar
THH 39 atas kekompakan serta kebersamaannya selama ± 4 tahun ini.
7. Neni, Vivi, Iera, Andri, Melin dan teman-teman di Puri Fikriyah atas bantuan,
pengertian, dorongan semangat, dan canda tawanya.
8. Seluruh pihak yang telah membantu namun tidak dapat disebutkan satu
persatu.
Bogor, September 2006
DAFTAR ISI
Halaman
PRAKATA ... i
DAFTAR ISI ... ii
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ... v
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Tumbuhan Obat ... 4
Deskripsi Suren (Toona sureni Merr.) ... 4
Deskripsi Ki bonteng (Platea latifolia BL.) ... 5
Ekstraksi ... 5
Senyawa Bioaktif ... 8
Ekstraktif ... 11
Brine Shrimp Lethality Test ... 12
Artemia salina Leach. ... 13
BAHAN DAN METODE Waktu dan Tempat Penelitian ... 15
Bahan dan Alat ... 15
Metode Penelitian ... 16
Uji Bioaktivitas dengan Brine Shrimp Lethality Test ... 19
HASIL DAN PEMBAHASAN Analisis Fisik Inner bark dan Teras Cabang Kayu Suren (Toona sureni Merr.) dan Ki bonteng (Platea latifolia BL.) ... 21
Kandungan Zat Ekstraktif ... 21
Kandungan Zat Ekstraktif Kayu Suren ... 22
Kandungan Zat Ekstraktif Kayu Ki bonteng ... 23
Uji Bioaktivitas Zat Ekstraktif dengan Brine Shrimp Lethality Test ... 28
SIMPULAN Kesimpulan ... 38
Saran ... 49
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Halaman
1. Nilai konstanta dielektrik, titik didih dan sifat kepolaran beberapa pelarut
yang digunakan dalam penelitian ini... 7
2. Jenis kayu dengan diameter berbeda sebagai contoh uji ... 16
3. Hasil analisis fisik kulit cabang kayu suren dan ki bonteng ... 21
4. Hasil analisis fisik bagian teras cabang kayu suren dan ki bonteng ... 21
5. Kandungan rata-rata ekstrak aseton inner bark dan teras cabang suren (T. sureni) serta hasil fraksinasinya ... 23
6. Kandungan rata-rata ekstrak aseton inner bark dan teras cabang ki bonteng (P. latifolia) serta hasil fraksinasinya ... 24
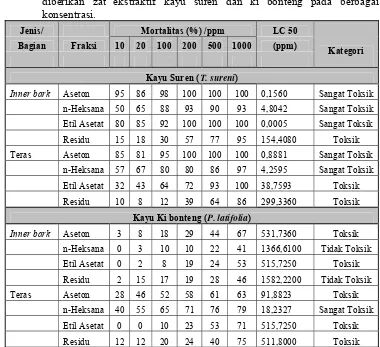
7. Nilai rata-rata mortalitas terkoreksi terhadap larva udang A. salina setelah diberikan zat ekstraktif kayu suren dan ki bonteng pada berbagai konsentrasi ... 29
8. Hasil analisis probit fraksi teraktif ekstrak aseton kayu suren (T. sureni) dan ki bonteng (P. latifolia) ... 30
DAFTAR GAMBAR
Halaman
1. Larva udang Artemia salina Leach ... 13 2. Cabang kayu suren dan ki bonteng sebagai contoh uji ... 15
3. Bagan kerja ekstraksi dan fraksinasi inner bark dan teras
cabang suren dan ki bonteng ... 18
4. Hubungan mortalitas larva udang Artemia salina Leach. dengan
penambahan berbagai konsentrasi ekstrak yang terkandung dalam inner
bark suren ... 31 5. Hubungan mortalitas larva udang A. salina dengan penambahan
berbagai konsentrasi ekstrak yang terkandung dalam teras cabang
suren ... 32
6. Hubungan mortalitas larva udang A. salina dengan penambahan
berbagai konsentrasi ekstrak yang terkandung dalam inner bark
ki bonteng ... 33
7. Hubungan mortalitas larva udang A. salina dengan penambahan
berbagai konsentrasi ekstrak yang terkandung dalam teras cabang
DAFTAR LAMPIRAN
Halaman
1. Nilai persentase kadar air (KA) suren (Toona sureni Merr.) dan
ki bonteng (Platea latifolia BL.) ... 44
2. Nilai persentase kadar ekstrak aseton suren dan ki bonteng ... 45
3. Nilai persentase kadar ekstrak aseton suren dan ki bonteng pada fraksi
n-heksana ... 46
4. Nilai persentase kadar ekstrak aseton suren dan ki bonteng pada fraksi
etil asetat ... 47
5. Nilai persentase kadar ekstrak aseton suren dan ki bonteng pada fraksi
residu ... 48
6. Hasil uji mortalitas aseton inner bark dan teras cabang suren
(Toona sureni Merr.) ... 49
7. Hasil uji mortalitas aseton inner bark dan teras cabang suren
(Toona sureni Merr.) fraksi n-heksana... 50
8. Hasil uji mortalitas aseton inner bark dan teras cabang suren
(Toona sureni Merr.) fraksi etil asetat ... 51
9. Hasil uji mortalitas aseton inner bark dan teras cabang suren
(Toona sureni Merr.) fraksi residu ... 52
10. Hasil uji mortalitas aseton inner bark dan teras cabang ki bonteng
(Platea latifolia BL.) ... 53
11. Hasil uji mortalitas aseton inner bark dan teras cabang ki bonteng
(Platea latifolia BL.) fraksi n-heksana... 54
12. Hasil uji mortalitas aseton inner bark dan teras cabang ki bonteng
(Platea latifolia BL.) fraksi etil asetat ... 55
13. Hasil uji mortalitas aseton inner bark dan teras cabang ki bonteng
(Platea latifolia BL.) fraksi residu ... 56
14. Hasil minitab analisis probit pada suren ... 57
PENDAHULUAN
Latar Belakang
Negara Indonesia dikenal dunia memiliki hutan hujan tropika yang kaya
akan keanekaragaman flora. Diperkirakan flora Indonesia memiliki 30.000-40.000
spesies tumbuhan berbunga. Ini suatu jumlah yang melebihi aneka flora dari
negara-negara tropika lainnya di dunia. Dari jumlah tersebut, terdapat tidak
kurang dari 1.100 spesies tumbuhan yang dapat digunakan sebagai tumbuhan obat
tradisional (Heyne 1987). Menurut Kassahara dan Hemmi (1986), dari 28.000
jenis tumbuhan yang ditemukan di Indonesia, ± 7.000 jenis (7.577 jenis)
diantaranya adalah tumbuhan obat.
Fransworth (1985) dalam Zuhud et al. (1994), menyatakan bahwa 74 % dari 121 bahan aktif obat modern di USA berasal dari pengetahuan obat
tradisional yang berasal dari tumbuhan hujan tropika. Hal ini menunjukkan bahwa
hutan tropika Indonesia sangat potensial mengandung berbagai senyawa bioaktif
yaitu senyawa yang dalam kadar kecil dapat mempengaruhi fungsi fisiologi sel
hidup. Oleh karena itu, keanekaragaman hayati hutan tropika Indonesia adalah
sumber senyawa-senyawa metabolit sekunder (zat ekstraktif) yang tak ternilai
jumlah jenisnya. Senyawa-senyawa ini dapat dimanfaatkan sebagai bahan obat
untuk mengatasi berbagai penyakit bahkan obat modern yang beredar di pasaran
merupakan hasil eksplorasi zat ekstraktif tumbuhan yang terdapat di hutan tropis.
Krisis ekonomi yang melanda serta kesadaran masyarakat untuk back to nature
telah meningkatkan penggunaan tanaman obat baik untuk pencegahan maupun
dalam pengobatannya. Dengan demikian, keanekaragaman tumbuhan obat
tersebut sangatlah mungkin dimanfaatkan demi kesejahteraan umat manusia.
Berdasarkan hasil penelitian Direktorat Aneka Usaha Kehutanan dan
Fakultas Kehutanan IPB tahun 2000 yang dilakukan di Hutan Lindung Gunung
Salak (tidak termasuk kawasan hutan UGI), menunjukkan bahwa kawasan hutan
ini mempunyai potensi yang cukup besar sebagai sumber plasma nutfah tumbuhan
obat. Hal ini dibuktikan dengan ditemukannya 117 jenis dari 60 famili tumbuhan
obat sehingga kemudian kawasan hutan ini ditetapkan sebagai salah satu kawasan
(2003), menyatakan bahwa ditemukan 112 jenis tumbuhan dari 49 famili yang
terdiri dari 62 jenis pohon, 20 jenis herba, 6 jenis perdu, 2 jenis semak, 8 jenis
liana dan 14 jenis epifit yang berpotensi sebagai tumbuhan obat dan diantaranya
adalah ki bonteng. Ki bonteng (Platea latifolia BL.) adalah salah satu jenis
tumbuhan potensial berkhasiat obat yang ditemukan di Gunung Salak karena
bagian kulit batang ki bonteng mengandung senyawa kimia kelompok alkaloid,
flavonoid dan saponin.
Bagian daun dan kulit batang pohon suren (Toona sureni Merr.) telah lama
digunakan masyarakat umum sebagai obat mules, demam, kencing manis dan
gondok (Sangat et al. 2000). Pada screening awal yang dilakukan Kardono et al.
(2002), menunjukkan bahwa ekstrak metanol kulit kayu suren ini mengandung
senyawa bioaktif antidiabetes. Hasil uji fitokimia menunjukkan bahwa bagian
kulit dan kayu suren mengandung senyawa kimia dari kelompok alkaloid,
flavonoid dan saponin. Senyawa-senyawa tersebut merupakan kelompok senyawa
bioaktif. Kelompok senyawa ini diduga memiliki sifat antidiabetes dan antikanker
(Kardono et al. 2002 dan Sajuthi 2001). Oleh karena itu, eksplorasi senyawa bioaktif terhadap kedua jenis tersebut perlu dilakukan dengan harapan ditemukan
senyawa kimia yang berkhasiat obat, khususnya yang bersifat antikanker.
Alasan dipilihnya eksplorasi zat ekstraktif sebagai obat antikanker karena
jumlah penderita kanker yang terus meningkat (penambahan 7 juta orang/tahun),
dan 2/3nya diperkirakan berasal dari negara berkembang termasuk Indonesia
(Kupang Watch 2006).
Untuk melihat adanya kemungkinan efek suatu ekstrak dapat digunakan
penelusuran farmakologis-biologis dengan menguji ekstrak tersebut berdasarkan
suatu metode bioassay (Bruhn 1991). Metode bioassay yang digunakan untuk uji
bioaktivitas zat ekstraktif adalah dengan Brine Shrimp Lethality Test (BSLT)
dengan menggunakan larva udang Artemia salina Leach sebagai hewan uji.
Alasan penggunaan BSLT ini adalah peka, cepat, sederhana dan dapat diulang
tanpa terjadi penyimpangan. Serta metode bioassay ini sering dikaitkan sebagai
metode identifikasi senyawa antikanker yang berasal dari tumbuhan (Wahyuno
50 %) dan hasil BSLT ini berkorelasi positif dengan sifat antikanker
senyawa-senyawa kimia yang dikandung oleh bahan uji (Meyer et al.1982).
Penelitian ini menggunakan kulit dalam (inner bark) dan bagian teras
cabang kayu suren dan ki bonteng. Menurut Fengel dan Wegener (1995), inner
bark kemungkinan mengandung jenis zat ekstraktif maupun komposisi berbeda dengan kulit bagian luarnya sehingga akan mengandung senyawa bioaktif yang
berbeda jenis atau komposisinya. Harun dan Labosky (1985), menyatakan bahwa
ada kemungkinan zat ekstraktif yang terdapat di dalam kayu juga terdapat di
dalam kulit, mengingat pembentukan jaringan kayu dan kulit dimulai dari jaringan
meristem sekunder yang sama. Fengel dan Wegener (1995) juga menyatakan
bagian teras umumnya mengandung lebih banyak zat ekstraktif. Apabila inner
bark dan teras cabang memiliki aktivitas dan kandungan senyawa bioaktif yang tidak berbeda dengan bagian batang maka kita dapat memanfaatkan tanaman
tersebut sebagai obat tanpa melakukan penebangan. Sedangkan untuk
memperoleh ekstrak yang mengandung senyawa kimia dari kelompok alkaloid,
flavonoid, saponin, triterpenoid, dan senyawa bioaktif lainnya dari tumbuhan
dibutuhkan pelarut yang aman, harganya tidak terlalu mahal, toksisitasnya rendah,
daya larutnya tinggi dan tidak terlalu reaktif (Houghton dan Raman 1998). Maka
pelarut aseton dipilih sebagai pelarut dalam penelitian ini, dan untuk memperoleh
fraksi-fraksinya digunakan pelarut n-heksana dan etil-asetat yang mewakili
pelarut yang bersifat non-polar dan polar.
Tujuan
Tujuan penelitian ini adalah untuk mengetahui kandungan zat ekstraktif
kulit dalam (inner bark) dan bagian teras cabang suren (T. sureni) dan ki bonteng
(P. latifolia) yang larut dalam pelarut aseton dan hasil fraksinasinya dengan
pelarut n-heksana, etil asetat dan residunya serta untuk menguji bioaktivitas zat
TINJAUAN PUSTAKA
Tumbuhan Obat
Pengertian tumbuhan obat adalah semua tumbuhan, baik yang sudah
ataupun yang belum dibudidayakan yang dapat digunakan sebagai obat, berkisar
dari yang terlihat mata hingga yang nampak di bawah mikroskop (Hamid et al.
1991). Menurut Zuhud et al. (1994), tumbuhan obat adalah seluruh spesies
tumbuhan obat yang diketahui atau dipercaya mempunyai khasiat obat yang
dikelompokkan menjadi :
Tumbuhan obat tradisional, yaitu spesies tumbuhan yang diketahui
atau dipercaya oleh masyarakat mempunyai khasiat obat dan telah
digunakan sebagai bahan baku obat tradisional.
Tumbuhan obat modern, yaitu spesies tumbuhan yang secara ilmiah
telah dibuktikan mengandung senyawa/bahan bioaktif yang berkhasiat
obat dan penggunaannya dapat dipertanggungjawabkan secara medis.
Tumbuhan obat potensial, yaitu spesies tumbuhan obat yang diduga
mengandung senyawa/bahan aktif yang berkhasiat obat, tetapi belum
dibuktikan secara ilmiah/medis atau penggunaannya sebagai bahan
obat tradisional sulit ditelusuri
Jumlah tumbuhan dan tanaman obat di Indonesia tercatat berkisar antara
ratusan sampai ribuan jenis. Dalam buku “Medicinal Herbs Index in Indonesia”
tercantum 7.577 jenis tumbuhan yang dikenal dan ditemukan di Indonesia,
walaupun tidak seluruhnya berasal dari Indonesia (Heyne 1987).
Deskripsi Suren (Toona sureni Merr.)
Tanaman suren termasuk famili Meliaceae dengan genus Toona. Di
Indonesia tanaman ini dikenal dengan nama suren (Jawa), surian (Kalimantan)
atau mapala/molopaga (Sulawesi). Daerah penyebaran pohon suren di seluruh
Indonesia. Pohon suren memiliki ciri utama warna kayu merah seperti daging
direbus, riap tumbuhnya jelas, susunan pori tata lingkar dan isi porinya berupa
yang berbentuk pohon dengan tinggi mencapai 20 m dan tumbuh baik di dataran
rendah hingga ketinggian 2.000 m dpl.
Sifat dan kegunaan kayu suren adalah berat jenis : rata-rata 0,39
(0,27-0,67); kelas awet : IV/V; kelas kuat : IV. Kegunaan : bahan bangunan ringan
(termasuk lemari), dinding hias, langit-langit, peti teh, kotak cerutu, bangunan
kapal dan perahu dayung, alat musik (antara lain piano), vinir lapisan muka kayu
lapis dan ukiran (Newman et al. 1999).
Suren memiliki kandungan bahan surenon, surenin dan surenolakton yang
berperan sebagai penghambat pertumbuhan, insektisida dan antifeedant
(menghambat daya makan) terhadap larva serangga uji ulat sutera (Dinata 2005).
Suren telah dikenal oleh masyarakat Indonesia sebagai tumbuhan yang berkhasiat
obat. Bagian kulitnya digunakan untuk menyembuhkan berbagai penyakit,
misalnya oleh suku Rejang Lebong (Bengkulu) untuk mules, suku Jawa untuk
demam, suku Bali untuk kencing manis (diabetes mellitus) dan oleh suku Samawa
(NTB) untuk menyembuhkan penyakit gondok (Sangat et al. 2000).
Deskripsi Ki bonteng (Platea latifolia BL.)
Menurut Heyne (1987), ki bonteng termasuk famili Icacinaceae dengan
genus Platea. Nama daerah sunda : Ki kadanca. Pohon ki bonteng dikenal dengan
raksasa rimba karena batangnya berbentuk tiang, perawakan pohon ini sangat
besar dengan tinggi lebih besar dari 40 m, diameter batang setinggi dada 1,50 m
dan terdapat di seluruh pulau Jawa pada ketinggian antara 1.000 dan 1.600 m dpl.
Kayunya yang berbau seperti kumarin, bisa terdapat dalam ukuran yang
sangat besar akan tetapi kayu ini tidak awet di cuaca terbuka. Di daerah Priangan,
ki bonteng dianggap dapat digunakan untuk pekerjaan dibawah atap. Di Jawa
Tengah dan Jawa Timur, walaupun banyak terdapat di sana namun namanya tidak
dikenal oleh masyarakat (Heyne 1987).
Ekstraksi
Ekstraksi kayu meliputi sejumlah besar senyawa berbeda yang dapat
diekstraksi dari kayu dengan menggunakan pelarut polar dan non-polar. Ekstraksi
benzena, etanol, diklorometana atau campuran dari pelarut-pelarut tersebut. Asam
lemak, asam resin, lilin, tannin, dan senyawa berwarna merupakan
senyawa-senyawa yang paling penting yang dapat diekstraksi dengan pelarut. Komponen
utama dari bagian kayu yang dapat larut dalam air terdiri atas karbohidrat, protein
dan garam-garam an-organik (Fengel dan Wegener 1995).
Ekstraksi adalah suatu metode pemisahan komponen-komponen dari suatu
campuran dimana komponen yang larut masuk ke dalam pelarut yang dipakai
sedangkan komponen yang tidak larut akan tertinggal di dalam bahan. Metode
yang paling sederhana yang digunakan untuk mengekstraksi padatan adalah
mencampurkan seluruh bahan dengan pelarut, kemudian memisahkannya dari
padatan yang tidak terlarut (Lehniger dan Baverloo 1976). Hasil ekstraksi yang
diperoleh bergantung pada kandungan ekstrak yang terdapat pada contoh uji dan
jenis pelarut yang digunakan. Hal-hal yang perlu dipertimbangkan dalam
pemilihan pelarut adalah selektivitas, kapasitas, kemudahan untuk diuapkan dan
harga pelarut tersebut. Prinsip kelarutan adalah “like dissolve like”, yaitu (1)
pelarut polar akan melarutkan senyawa polar, demikian juga sebaliknya pelarut
non-polar akan melarutkan senyawa non-polar, (2) pelarut organik akan
melarutkan senyawa organik (Khopkar 1990 dalam Yunita 2004).
Ekstraksi obat dari tumbuhan dengan ekstraksi cair tergolong sebagai jenis
ekstraksi cairan-padat (liquid-solid extraction). Tujuan metode ekstraksi ini
adalah mengeluarkan bahan yang diinginkan dari sel-sel dengan proses difusi.
Prinsip dari cara ini adalah untuk tercapainya keseimbangan konsentrasi bahan
dalam pelarut pada batas yang diinginkan. Hasil ekstraksi dari proses ini
dipengaruhi oleh suhu, pH, ukuran bahan yang akan diekstraksi dan gerakan
pelarut yang terjadi di sekitarnya. Parameter yang juga sangat penting dalam
ekstraksi adalah pemilihan pelarut. Suatu pelarut ideal adalah yang memiliki
selektivitas tinggi yakni untuk memisahkan senyawa dengan bobot molekul
rendah, seperti alkaloid, saponin dan terpentin, pelarut yang paling baik
digunakan adalah alkohol alifatik dengan maksimum 3 atom karbon atau
campuran dari pelarut itu dengan air (Bombardelli 1991).
Tahapan yang harus diperhatikan dalam mengekstraksi jaringan tumbuhan
pengrajangan simplisia, pemilihan pelarut dan kondisi ekstrak, proses
pengambilan pelarut, pengawasan mutu dan pengujian serta usulan proses
ekstraksi yang akan digunakan (Sabel dan Warren 1973). Prosedur klasik untuk
memperoleh kandungan senyawa organik dari jaringan tumbuhan kering adalah
dengan proses ekstraksi berkesinambungan dengan menggunakan sederetan
pelarut yang berbeda tingkat kepolarannya (Harborne 1987). Polaritas sering
diartikan sebagai adanya pemisahan kutub muatan positif dan negatif dari suatu
molekul sebagai akibat terbentuknya konfigurasi tertentu dari atom-atom
penyusunnya. Dengan demikian, molekul tersebut dapat tertarik oleh molekul
yang lain yang juga mempunyai polaritas yang kurang lebih sama. Besarnya
polaritas dari suatu zat pelarut proporsional dengan besarnya konstanta
dielektriknya (Adnan 1997).
Menurut Stahl (1985), konstanta dielektrik (ε) merupakan salah satu
ukuran kepolaran pelarut yang mengukur kemampuan pelarut untuk menyaring
daya tarik elektrostatik antara isi yang berbeda. Kemampuan zat cair melarutkan
zat padat ion sangat bergantung, walaupun tidak semata-mata bergantung pada
tetapan dielektriknya. Dalam penelitian ini digunakan pelarut aseton dikarenakan
pelarut ini memiliki sifat antara lain nilai polaritas dan konstanta dielektrik yang
tinggi, dapat dicampur dengan air dalam berbagai perbandingan dan merupakan
pelarut yang baik (Lestari 2003). Menurut Reichardt (1998), aseton sebagai
pelarut organik lebih aman bagi kesehatan dibandingkan dengan pelarut
kloroform, benzena dan toluena. Pelarut aseton mempunyai toksisitas yang lebih
rendah (1.000 ppm) dibandingkan dengan benzena (8 ppm), kloroform (10 ppm)
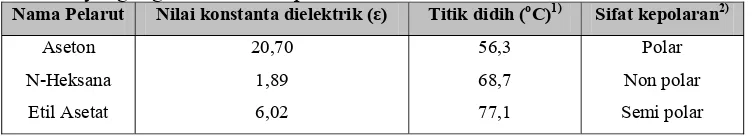
dan toluena (200 ppm). Nilai konstanta dielektrik, titik didih dan sifat kepolaran
beberapa pelarut yang digunakan dalam penelitian ini disajikan dalam Tabel 1.
Tabel 1. Nilai konstanta dielektrik, titik didih dan sifat kepolaran beberapa pelarut yang digunakan dalam penelitian ini
Nama Pelarut Nilai konstanta dielektrik (ε) Titik didih (oC)1) Sifat kepolaran2)
Aseton
Houghton dan Raman (1998)
2)
Senyawa Bioaktif
Senyawa bioaktif merupakan senyawa yang mempunyai aktivitas biologis
terhadap organisme lain atau pada organisme yang menghasilkan senyawa
tersebut. Senyawa bioaktif hampir selalu toksik pada dosis tinggi. Setiap zat
kimia, termasuk senyawa aktif dari tumbuhan pada dasarnya bersifat racun,
tergantung pada penggunaan, takaran, pembuatan, cara pemakaian dan waktu
yang tepat untuk mengkonsumsi. Beberapa tanaman dikenal menghasilkan
senyawa bioaktif yang mempunyai berbagai aktivitas bioaktif termasuk antikanker
yang pada umumnya berupa senyawa-senyawa flavonoid, glikosida, steroid
alkaloid dan terpenoid (Kurz dan Constabel 1998).
Alkaloid
Menurut Harborne (1987), alkaloid sekitar 5.500 jenis telah diketahui dan
merupakan golongan zat tumbuhan sekunder yang terbesar. Tidak ada satupun
istilah ‘alkaloid’ yang memuaskan, tetapi pada umumnya alkaloid mencakup
senyawa bersifat basa yang mengandung satu atau lebih atom nitrogen, biasanya
dalam gabungan, sebagai bagian dari sistem siklik. Alkaloid seringkali bersifat
racun bagi manusia dan banyak mempunyai kegiatan fisiologi yang menonjol
yang secara luas banyak digunakan dalam bidang pengobatan. Alkaloid biasanya
tanpa warna, seringkali bersifat optis aktif, kebanyakan berbentuk kristal tetapi
hanya sedikit yang berupa cairan (misalnya nikotina) pada suhu kamar. Uji
sederhana yang sama sekali tidak sempurna, untuk alkaloid dalam daun atau buah
segar adalah rasa pahitnya di lidah. Misalnya, alkaloid kuinina adalah zat yang
dikenal paling pahit dan pada konsentrasi molar 1x10-3 memberikan rasa pahit yang berarti. Alkaloid dahulu sebagai sumber utamanya hanya berasal dari
tanaman yang berbunga (angiospermae). Tetapi pada dewasa terakhir, ternyata
alkaloid ditemukan juga dalam beberapa jenis hewan baik yang hidup di laut
maupun di darat, berupa serangga, makroorganisme dan tanaman rendah lainnya
(Pandji 1989). Alkaloid dapat ditemukan dalam berbagai bagian tumbuhan seperti
biji, daun, ranting dan kulit kayu. Alkaloid memang jarang ditemukan dalam
jaringan mati. Umumnya alkaloid terakumulasi dalam jaringan yang tumbuh aktif
tumbuhan belum diketahui begitu pasti, walaupun beberapa senyawa ditafsirkan
berperan sebagai pengatur, atau penolak dan pengikat serangga. Sampai saat ini,
penggolongan senyawa alkaloid belum ada yang digunakan secara umum. Hal ini
disebabkan karena alkaloid mempunyai struktur yang banyak jenisnya, sehingga
penggolongan alkaloid berdasarkan strukturnya untuk membedakan jenis yang
satu dengan yang lain sukar dilakukan (Suradikusumah 1989).
Dalam pengobatan, alkaloid memberikan efek fisiologis yang pada
umumnya di susunan syaraf pusat, misalnya sebagai obat anti rasa sakit dan obat
tidur, dalam jumlah besar sangat beracun bagi manusia (Vicker dan Vickery
1981).
Menurut Sumiwi (1992), fungsi alkaloid bagi tumbuhan antara lain
sebagai zat beracun untuk melawan serangga atau hewan pemakan tumbuhan,
faktor pengatur tumbuh, substansi cadangan untuk memenuhi kebutuhan akan
nitrogen dan elemen-elemen lain yang penting bagi tumbuhan dan hasil akhir
reaksi detoksifikasi dari suatu zat yang berbahaya bagi tumbuhan.
Flavonoid
Flavonoid terutama berupa senyawa yang larut dalam air. Mereka dapat
diekstraksi dengan etanol 70% dan tetap ada dalam lapisan air setelah ekstrak ini
dikocok dengan eter minyak bumi. Flavonoid berupa senyawa fenol, karena itu
warnanya berubah bila ditambah basa atau amonia; jadi mereka mudah dideteksi
pada kromatogram atau dalam larutan (Harborne 1987).
Flavonoid mengandung sistem aromatik yang terkonyugasi dan karena itu
menunjukkan pita serapan kuat pada daerah spektrum UV dan spektrum tampak.
Flavonoid umumnya terdapat dalam tumbuhan, terikat pada gula sebagai glikosida
dan aglikon flavonoid yang manapun mungkin saja terdapat dalam satu tumbuhan
dalam beberapa bentuk kombinasi glikosida. Karena alasan itu, maka dalam
menganalisis flavonoid biasanya lebih baik kita memeriksa aglikon yang terdapat
dalam ekstrak tumbuhan yang telah dihidrolisis sebelum memperhatikan
kerumitan glikosida yang mungkin terdapat dalam ekstrak asal (Harborne 1987).
Flavonoid terdapat dalam tumbuhan sebagai campuran, jarang sekali
sering terdapat campuran yang terdiri atas flavonoid yang berbeda kelas.
Antosianin berwarna yang terdapat dalam daun bunga hampir selalu disertai oleh
flavon atau flavonol tanpa warna. Hasil penelitian akhir-akhir ini telah
membuktikan bahwa flavon merupakan ko-pigmen penting, karena sangat
diperlukan untuk menyatakan warna antosianin secara penuh dalam jaringan
bunga. Biasanya antosianin juga terdapat sebagai campuran, terutama dalam
bunga, dan suatu jaringan bunga dapat mengandung sampai sepuluh pigmen yang
berlainan (Harborne 1987). Pada tumbuhan, flavonoid dapat meningkatkan
dormansi, meningkatkan pembelahan sel-sel kalus, sebagai enzim penghambat
pembentukkan protein, menghasilkan zat warna pada bunga, untuk merangsang
serangga, burung dan satwa lainnya untuk mendatangi tumbuhan tersebut sebagai
agen dalam penyerbukan dan penyebaran biji. Dalam dunia pengobatan, beberapa
senyawa flavonoid berfungsi sebagai antibodi, misalnya antivirus dan jamur,
peradangan pembuluh darah dan dapat digunakan sebagai racun ikan (Vickery dan
Vickery 1981).
Saponin
Saponin termasuk dalam golongan senyawa terpenoid dan bagian dari
triterpenoid (diturunkan dari hidrokarbon C30). Saponin merupakan glikosida triterpenoid dan sterol. Senyawa ini merupakan senyawa aktif permukaan yang
bersifat seperti sabun dan dapat dideteksi berdasarkan kemampuannya
membentuk busa yang stabil dan dapat menghemolisis sel darah. Pembentukan
busa yang mantap sewaktu mengekstrak tumbuhan atau pemekatan ekstrak
tumbuhan merupakan bukti adanya saponin. Untuk uji saponin yang sederhana
adalah dengan menggunakan ekstrak alkohol, air dari tumbuhan dalam tabung
reaksi dan perhatikan terbentuknya busa yang tahan lama pada permukaan cairan
(Harborne 1987).
Pada tumbuhan, saponin mempunyai fungsi yang sama dengan
triterpenoid karena mengandung turunan dari senyawa ini, diantaranya dapat
meningkatkan daya kecambah benih dan menghambat pertumbuhan akar,
menghambat pertumbuhan sel-sel tumor pada tumbuhan dan satwa. Saponin
untuk meningkatkan kolesterol serum, sebagai zat antibiotik, tahan jamur, anti
influenza dan peradangan tenggorokan, sebagai bahan dasar untuk mendapatkan
sapogenin yang berguna untuk menghasilkan hormon pertumbuhan pada satwa
dan dapat digunakan sebagai racun ikan (Vickery dan Vickery 1981).
Triterpenoid dan Steroid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam
satuan isoprena dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik,
yaitu skualena. Senyawa ini berstruktur siklik yang nisbi rumit, kebanyakan
berupa alkohol, aldehida atau asam karboksilat. Mereka berupa senyawa tanpa
warna, berbentuk kristal, seringkali bertitik leleh tinggi dan aktif optik, yang
umumnya sukar dicirikan karena tak ada kereaktifan kimianya. Uji yang banyak
digunakan adalah reaksi Lieberman-Burchard (anhidrida asetat-H2SO4 pekat)
yang dengan kebanyakan triterpena dan sterol memberikan warna hijau-biru.
Sterol dianggap senyawa satwa (sebagai hormon kelamin, asam empedu dan
lain-lain), tetapi pada tahun-tahun terakhir ini makin banyak senyawa tersebut yang
ditemukan dalam jaringan tumbuhan. Memang tiga senyawa yang biasa disebut
“fitosterol” mungkin terdapat pada setiap tumbuhan tinggi : sitosterol, stigma
sterol dan kampesterol (Harborne 1987).
Triterpenoid dan turunannya termasuk saponin dan steroid pada tumbuhan
berfungsi sebagai racun serangga, bakteri dan jamur. Steroid dapat meningkatkan
permeabilitas membran sel dan merangsang proses pembungaan. Dalam
pengobatan, senyawa ini berguna sebagai zat antibiotik diantaranya anti jamur,
bakteri dan virus. Steroid dapat merangsang aktivitas hormon estrogen dan
progesteron pada satwa dan manusia. Steroid menjadi sumber energi bagi
mikroorganisme pada pengurai (Vickery dan Vickery 1981).
Ekstraktif
Kayu mengandung endapan yang bervariasi (umumnya bahan organik)
yang gabungannya disebut ekstraneous atau ekstraktif. Bahan tersebut bukan
merupakan bahan penyusun kayu, tetapi terdapat dalam rongga sel dan dinding
lemak, resin, gula, minyak, pati, alkaloid dan tannin. Istilah ekstraktif didasarkan
kepada kemungkinannya (bagian kecil) diekstraksi dari kayu dengan air dingin
atau panas, atau pelarut netral seperti alkohol, benzen, aseton dan lain-lain.
Proporsi ekstraktif bervariasi mulai kurang dari 1 % (sebagai contoh poplar)
hingga lebih dari 10 % (sebagai contoh redwood) berdasarkan berat kering tanur
kayu. Untuk beberapa jenis dari daerah tropis bisa terdapat sekitar 20 %. Adanya
variasi tidak hanya terdapat diantara spesies tetapi juga dalam pohon yang sama
terutama diantara kayu gubal dan kayu teras (Tsoumis 1991).
Menurut Fengel dan Wegener (1995), kandungan ekstraktif dalam kulit
lebih tinggi daripada dalam kayu. Ia tidak hanya tergantung pada spesies tetapi
juga pada pelarut yang digunakan. Keanekaragaman senyawa yang dapat
diekstraksi biasanya membutuhkan serangkaian ekstraksi yang hasilnya
memberikan ciri awal komposisinya.
Hal yang mempengaruhi kandungan zat ekstraktif dalam kayu diantaranya
adalah umur, site (tempat tumbuh), genetik, posisi dalam pohon, jenis pelarut
yang digunakan dan kecepatan pertumbuhan.
Brine Shrimp Lethality Test
Menurut Meyer et al. (1982), uji bioaktivitas menggunakan larva udang
Artemia salina Leach dikenal dengan istilah Brine Shrimp Lethality Test (BSLT). BSLT adalah suatu metode penelusuran untuk menentukan bioaktivitas suatu
ekstrak ataupun senyawa terhadap larva udang dari A. salina. Metode ini
berkembang sebagai salah satu metode bioassay dalam mengisolasi senyawa aktif
yang terdapat dalam suatu ekstrak tanaman. Lebih jauh lagi bioassay ini sering
dikaitkan sebagai metode identifikasi senyawa anti kanker berasal dari tumbuhan.
Uji bioaktivitas dengan menggunakan larva udang memiliki spektrum
farmakologi yang luas, sederhana prosedurnya, cepat, tidak memerlukan biaya
yang besar dan hasilnya dapat dipercaya.
Uji mortalitas larva udang merupakan salah satu metode uji bioaktif pada
penelitian senyawa bahan alam. Penggunaan larva udang untuk kepentingan studi
bioaktivitas sudah dilakukan sejak tahun 1956 dan sejak saat itu telah banyak
jaringan tanaman. Uji ini merupakan uji pendahuluan untuk mengamati aktivitas
farmakologi suatu senyawa. Adapun penerapan untuk sistem bioaktivitas dengan
menggunakan larva udang tersebut, antara lain untuk mengetahui residu pestisida,
anastetik lokal, senyawa turunan morpin, mikotoksin, karsinogenitas suatu
senyawa dan polutan untuk air laut serta sebagai alternatif metode yang murah
untuk uji sitotoksisitas (Hamburger dan Hostettmann 1991).
Senyawa aktif yang memiliki daya bioaktivitas tinggi diketahui
berdasarkan nilai Lethal Concentration 50 % (LC50), yaitu suatu nilai yang menunjukkan konsentrasi zat toksik yang dapat menyebabkan kematian hewan uji
sampai 50 %. Data mortalitas yang diperoleh kemudian diolah dengan probit
analisis yang dirumuskan oleh Finney (1971) untuk menentukan nilai LC50 pada derajat kepercayaan 95 %. Senyawa kimia berpotensi bioaktif jika mempunyai
nilaiLC50 kurang dari 1.000 ppm (Meyer et al. 1982).
Artemia salina Leach.
Menurut Mudjiman (1983), udang renik asin (brine shrimp) atau artemia
adalah udang-udangan tingkat rendah yang hidup sebagai zooplankton yang
menghuni perairan-perairan yang berkadar garam tinggi (salina), baik dekat pantai
maupun jauh di Pedalaman laut. Artemia salina Leach. diklasifikasikan sebagai
berikut :
filum : Arthropoda
kelas : Crustacea
subklas : Branchipoda
ordo : Anostraca
famili : Artemiidae
genus : Artemia
species : Artemia salina Leach.
Gambar 1. Larva A. salina
Keunggulan penggunaan A. salina untuk uji BSLT ini ialah sifatnya yang
peka terhadap bahan uji, waktu siklus hidup yang lebih cepat, mudah dibiakkan
keadaan membran kulitnya yang sangat tipis sehingga memungkinkan terjadinya
difusi zat dari lingkungan yang mempengaruhi metabolisme dalam tubuhnya.
A. salina ditemukan hampir pada seluruh tempat di permukaan perairan di bumi yang memiliki kisaran salinitas 10-20 g/l, hal inilah yang menyebabkannya
mudah dibiakkan. Telur A. salina terlihat seperti partikel-partikel kecil berwarna
coklat dengan diameter kira-kira 0,20 mm. Partikel-partikel tersebut akan naik ke
permukaan dan akhirnya tersapu ke darat oleh angin ketika terjadi penguapan air
pada musim-musim tertentu di wilayah perairan yang memiliki kadar garam
tinggi. Telur-telur tersebut dapat dikumpulkan dan dipisahkan dari pasir dan
kotoran lainnya dengan cara pengayakan. Telur-telur tersebut memiliki resistensi
yang tinggi terhadap kondisi ekstrim dan dapat disimpan dalam waktu yang lama,
jika telur-telur tersebut berada dalam keadaan bebas air. Uji BSLT dengan
menggunakan A. salina dilakukan dengan menetaskan telur-telur tersebut dalam air laut yang dibantu dengan aerasi. Telur A. salina akan menetas sempurna
menjadi larva dalam waktu 24 jam. A. Salina yang baik digunakan untuk uji
BSLT ialah yang berumur 48 jam sebab jika lebih dari 48 jam dikhawatirkan
kematian A. salina bukan disebabkan toksisitas ekstrak melainkan oleh terbatasnya persediaan makanan (Meyer et al. 1982).
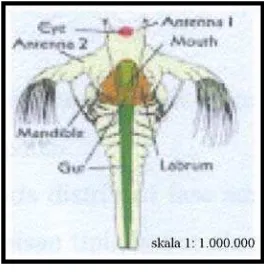
Larva yang baru saja menetas berbentuk bulat lonjong dan berwarna
kemerah-merahan dengan panjang 400 μm dengan berat 15 μg. Anggota badannya
terdiri dari sepasang sungut kecil (anteluena atau antena I) dan sepasang sungut
besar (antena atau antena II). Di bagian depan diantara kedua sungut kecil tersebut
terdapat bintik merah yang berfungsi sebagai mata (oselus). Di belakang sungut
besarnya terdapat sepasang mandibula (rahang) yang kecil, sedangkan di bagian
METODOLOGI PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Hasil Hutan, Fakultas
Kehutanan Institut Pertanian Bogor pada bulan Juni - Agustus 2006.
Bahan dan Alat
Penelitian ini dimulai dengan pengadaan bahan baku yaitu bagian cabang
kayu suren (Toona sureni Merr.) dan ki bonteng (Platea latifolia BL.) yang
berasal dari hutan alam di sekitar Gunung Salak Sukabumi. Secara administrasi
letak lokasi pengadaan bahan baku ini adalah di Wana Wisata Perhutani
Cangkuang, Kecamatan Cidahu, Kabupaten Sukabumi Provinsi Jawa Barat.
Secara geografis terletak pada 06043’58” LS sampai 06045’26” LS dan 106037’41” BT sampai 106040’58” BT pada ketinggian 900 – 1.500 m dpl. Menurut tipe iklim Schmidt dan Fergusson, Gunung Salak termasuk tipe iklim A
sedangkan menurut tipe iklim Mohr termasuk iklim bulan basah sepanjang tahun.
Suhu rata-rata 25,5 oC dan kelembaban udara rata-rata 85,5 % dengan curah hujan rata-rata 3.445 mm/thn (Sugiana 2003). Contoh uji diperoleh dari dua bagian dari
cabang yang diambil, yaitu kulit bagian dalam (inner bark) dan teras cabang kayu
suren dan ki bonteng. Dari dua jenis kayu tersebut diambil masing-masing tiga
bagian cabang dari pohon yang berbeda dengan jenis yang sama. Ketiga bagian
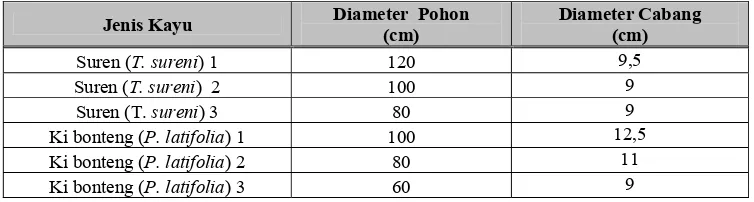
tersebut digunakan sebagai ulangan (Gambar 2). Sedangkan diameter cabang yang
digunakan dalam penelitian ini tertera pada Tabel 2.
Tabel 2. Jenis kayu dengan diameter berbeda sebagai contoh uji
Jenis Kayu Diameter Pohon
(cm)
Diameter Cabang (cm)
Suren (T. sureni) 1 120 9,5 Suren (T. sureni) 2 100 9 Suren (T. sureni) 3 80 9 Ki bonteng (P. latifolia) 1 100 12,5 Ki bonteng (P. latifolia) 2 80 11 Ki bonteng (P. latifolia) 3 60 9
Semua contoh uji dipotong-potong menjadi serpihan dan dikering
udarakan. Apabila sudah kering, kemudian contoh uji digiling dengan
menggunakan hammer mill dan disaring sehingga masing-masing contoh uji berbentuk serbuk dengan ukuran yang seragam (40-60 mesh) sebanyak + 500 g
untuk bagian teras cabang dan + 50 g untuk inner bark.
Bahan lainnya yang digunakan adalah telur A. salina, pelarut netral seperti
aseton, n-heksana dan etil asetat. Peralatan yang digunakan adalah alat pembuat
serbuk (willey mill dan hammer mill), peralatan gelas (labu erlenmeyer, tabung
reaksi, cawan petri, gelas piala, gelas ukur, pipet volumetrik dll), perangkat
ekstraksi, alat timbangan dan rotary evaporator.
Metode Penelitian
Adapun rangkaian metode penelitian dimulai dengan penyiapan serbuk,
ekstraksi dan fraksinasi serta uji bioaktivitas ekstrak dengan Brine Shrimp
Lethality Test (BSLT).
Penyiapan Serbuk
Bagian inner bark suren dan ki bonteng dirajang dan bagian teras cabangnya dipotong-potong sebesar batang korek api lalu dikering udarakan,
kemudian digiling dengan Willey mill dan disaring dengan menggunakan Hammer
Ekstraksi dan Fraksinasi
Serbuk bagian inner bark dan teras cabang kayu suren dan ki bonteng
yang telah diketahui kadar airnya untuk mengoreksi berat serbuk yang digunakan
sehingga diperoleh residu serbuk dengan bobot yang tepat diekstraksi. Teknik
ekstraksi yang dilakukan adalah dengan cara maserasi yaitu dengan merendam
serbuk dalam 1 liter pelarut selama 1 hari. Serbuk inner bark suren dan ki bonteng
sebanyak ± 50 g diekstraksi dengan ± 200 ml aseton dan ± 300 g serbuk teras
cabangnya diekstraksi dengan ± 1.000 ml aseton. Pelarut yang digunakan adalah
aseton teknis yang telah dimurnikan dengan cara penyulingan. Serbuk direndam
dengan menggunakan pelarut aseton hingga seluruh bahan terendam dan lakukan
pengadukan sedikit agar pelarut mengenai seluruh bahan. Perendaman dengan
menggunakan aseton dilakukan berulang-ulang hingga diperoleh larutan yang
tidak berwarna atau jernih (warna pelarut sama seperti warna asalnya). Ekstrak
aseton yang dihasilkan kemudian dipekatkan dengan menggunakan rotary vaccum
evaporator pada suhu 30-40 oC dan selanjutnya dilakukan pengeringan dalam oven pada suhu sekitar 40 oC. Kemudian ditimbang bobotnya untuk mendapatkan kadar ekstrak kasar.
Ekstrak kasar yang diperoleh difraksinasi secara berturut-turut dengan
menggunakan pelarut n-heksana dan etil asetat. Fraksinasi yang dilakukan adalah
dengan cara memasukkan larutan yang telah kental ke dalam funnel separator.
Ekstrak aseton yang dihasilkan dimasukkan ke dalam funnel dan ditambahkan
sebanyak pelarut n-heksana : aquades : aseton (perbandingan 2:1:1). Campuran
dikocok dan dibiarkan hingga terjadi pemisahan, selanjutnya fraksi terlarut dalam
n-heksana dipisahkan dari residunya dan dimasukkan ke dalam labu. Fraksinasi
dengan menggunakan n-heksana dilakukan hingga larutan berwarna jernih dan
selanjutnya fraksi terlarut n-heksana ini dipekatkan dengan menggunakan rotary
vaccum evaporator pada suhu 30-40 oC. Selanjutnya dilakukan pengeringan di oven pada suhu sekitar 40 oC. Kemudian ditimbang bobotnya untuk mendapatkan kadar fraksi terlarut dalam n-heksana
Fraksinasi berikutnya dengan menggunakan pelarut etil asetat. Residu hasil
fraksinasi dengan n-heksana ditambahkan dengan 50 ml etil asetat (perbandingan
seperti fraksi dengan n-heksana. Setelah terjadi pemisahan, fraksi terlarut etil
asetat dimasukkan ke dalam botol yang tertutup rapat. Fraksinasi dilakukan
hingga larutan berwarna jernih. Fraksi yang terpisah dipisahkan menjadi fraksi
pada bagian atas funnel merupakan fraksi etil asetat sedangkan fraksi yang berada
dibagian bawah funnel merupakan residu. Selanjutnya sama dengan fraksi terlarut
n-heksana, fraksi terlarut etil asetat ini dipekatkan dengan menggunakan rotary
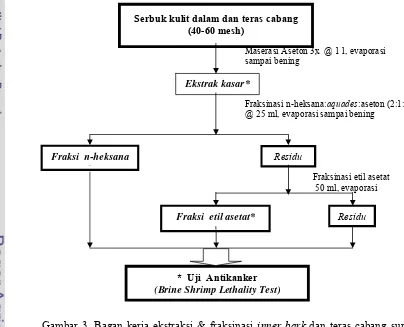
vaccum evaporator pada suhu 30-40 oC. Kemudian dilakukan pengeringan dalam oven pada suhu sekitar 40 oC dan ditimbang bobotnya untuk mendapatkan kadar fraksi terlarut dalam etil asetat. Untuk lebih jelasnya, tahapan fraksinasi dengan
menggunakan pelarut di atas secara skematis dapat dilihat pada Gambar 3 di
bawah ini.
Fraksinasi n-heksana:aquades:aseton (2:1:1) @ 25 ml, evaporasi sampai bening
Gambar 3. Bagan kerja ekstraksi & fraksinasi inner bark dan teras cabang suren dan ki bonteng.
* Uji Antikanker
(Brine Shrimp Lethality Test)
Residu
Fraksi etil asetat* Fraksi n-heksana
*
Residu
Ekstrak kasar*
Penentuan Kadar Ekstraktif
Kandungan zat ekstraktif pada tiap-tiap fraksi dihitung terhadap bobot
kering tanur. Ekstrak aseton, fraksi n-heksana, fraksi etil asetat dan residu yang
telah dikeringkan dalam oven 40 oC ditimbang untuk menghitung kadar ekstraknya.
Mahmudah (2003), menyatakan bahwa kadar ekstraktif dari hasil ekstraksi
dihitung terhadap kering tanur serbuk dengan menggunakan rumus :
Keterangan :
Wa = berat padatan ekstraktif (g) Wb = berat kering tanur serbuk (g)
Uji Bioaktivitas dengan Brine Shrimp Lethality Test (BSLT)
Ekstrak yang diperoleh dari ekstraksi pelarut aseton, n-heksana dan etil
asetat kemudian diuji bioaktivitasnya dengan menggunakan larva udang. Telur
udang ditetaskan di dalam gelas piala ukuran 1 l yang diisi air laut dilengkapi
dengan aerator dan lampu penerangan dan dalam 24 jam telur akan menetas
menjadi larva udang kemudian dilakukan penyiapan larutan ekstrak uji. Pengujian
dilakukan dengan 6 variasi konsentrasi, yaitu 1.000 ppm, 500 ppm, 200 ppm, 100
ppm, 20 ppm dan 10 ppm. Untuk membuat berbagai konsentrasi ekstrak maka
terlebih dulu membuat larutan induk ekstrak 2.000 ppm dengan cara : sebanyak
10 mg ekstrak kering dilarutkan dalam 5 μl aseton dan tambahkan air laut hingga
menjadi 5 ml larutan ekstrak untuk mendapatkan kadar 2.000 ppm larutan induk.
Dari larutan induk ekstrak tersebut dipipet 500, 250, 100, 50, 10, 5 μl ke dalam
vial sehingga konsentrasi ekstrak menjadi 1.000, 500, 200, 100, 20, 10 μg/ml
(ppm) setelah ditambahkan air laut hingga 1 ml. Sebelum dimasukkan larutan
ekstrak dan air laut, terlebih dahulu dimasukkan larva udang sebanyak 10 ekor ke
dalam vial, hal ini dilakukan agar konsentrasi tepat dan udang tidak mendapat
konsentrasi larutan yang terlalu tinggi sebelum penambahan air laut hingga 1 ml.
Setiap ekstrak dari tiap pohon diuji dan ditambah 1 kontrol, sehingga ada 3 contoh
konsentrasi dilakukan pengulangan sebanyak 2 kali sehingga 1 jenis ekstrak
terdapat 6 ulangan.
Setelah 1 hari (24 jam) dilakukan pengamatan dengan cara menghitung
jumlah larva udang yang mati, kemudian dihitung mortalitasnya dengan
menggunakan rumus berikut:
Keterangan :
MA : Mortalitas teramati (%) N1 : Jumlah larva udang awal
N2 : Jumlah larva udang yang mati setelah pengujian
Kemudian nilai mortalitas teramati yang diperoleh dikoreksi dengan
kontrol. Nilai mortalitas terkoreksi ini dapat dihitung dengan menggunakan rumus
dari Abbot (1925) dalam Sari (2002) yaitu :
Keterangan :
MT : Mortalitas teramati yang terkoreksi oleh mortalitas kontrol (%) Ma : Mortalitas teramati (%)
Mk : Mortalitas kontrol (%)
Data yang diperoleh kemudian dianalisis dengan menggunakan probit
analysis method dari minitab release 14 untuk mengetahui Lethal Concentration (LC50)dengan selang kepercayaan 95 %. Apabila LC50 < 30 ppm maka ekstrak sangat toksik dan berpotensi mengandung senyawa bioaktif antikanker. Meyer
(1982), menyebutkan tingkat toksisitas suatu ekstrak :
¾ LC50 ≤ 30 ppm = Sangat toksik
¾ 31 ppm ≤ LC50 ≤ 1.000 ppm = Toksik
¾ LC50 > 1.000 ppm = Tidak toksik.
%
100
100
Mk
x
Mk
Ma
MT
−
−
=
HASIL DAN PEMBAHASAN
Analisis Fisik Inner bark dan Teras Cabang
Kayu Suren (Toona sureni Merr.)dan Ki bonteng (Platea latifolia BL.)
Contoh uji yang dipakai adalah 3 teras serta 3 kulit bagian dalam dari
cabang pohon suren (T. sureni) dan ki bonteng (P. latifolia). Masing-masing
bagian cabang diperoleh dari tiga pohon yang berbeda tetapi masih dalam satu
jenis di lokasi hutan alam di sekitar Gunung Salak Sukabumi. Daun yang berasal
dari pohon suren dan ki bonteng dikirim ke Herbarium Bogoriense, Badan
Penelitian dan Pengembangan Botani Pusat Penelitian dan Pengembangan
Biologi–Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bogor, untuk
mengidentifikasi jenis pohon.
Kulit dalam dan bagian teras dari cabang batang suren dan ki bonteng
setelah dikering udarakan kemudian dipotong-potong/dicacah dan di analisis
secara visual (seperti yang terlihat pada Tabel 3 dan Tabel 4).
Tabel 3. Hasil analisis fisik kulit cabang kayu suren dan ki bonteng
Parameter Hasil Pengamatan
Kulit Suren Kulit Ki bonteng
Bentuk Kulit kayu, persegi panjang (mudah dikuliti)
Kulit kayu, tidak beraturan/serupa serutan (sedikit susah dikuliti)
Warna Outer bark: Coklat muda Inner bark : Kuning kecoklatan
Outer bark: Coklat tua Inner bark : Merah bata Ukuran Tebal kulit + 0,3 – 0,5 cm Tebal kulit + 0,5 – 1,0 cm
Tabel 4. Hasil analisis fisik bagian teras dari cabang kayu suren dan ki bonteng
Parameter Hasil Pengamatan
Teras Suren Teras Ki bonteng
Bentuk Sedikit susah dibedakan dengan kayu gubalnya
Lebih mudah dibedakan dengan kayu gubalnya
Warna Coklat muda Coklat tua (menyerupai merah bata)
Kandungan Zat Ekstraktif
Kadar ekstrak adalah jumlah total ekstrak murni yang didapat pada suatu
proses ekstraksi dalam suatu bahan (tumbuhan). Nilai kadar ekstrak ini
perbandingan jumlah ekstrak dan jumlah pengisi yang terkandung pada setiap
butir obat tersebut.
Warna zat ekstraktif yang larut dalam pelarut aseton pada kayu suren
umumnya berwarna merah kehitaman sedangkan ki bonteng cenderung berwarna
kuning. Sejumlah flavonoid menentukan warna masing-masing kayu, misal
fisetin, morin dan santal, yang lain (butein, sulfuretin, rangsin) menyebabkan
noda-noda warna dalam pulp dari kayu tropika (Fengel dan Wegener 1989).
Beberapa tanaman dikenal menghasilkan senyawa bioaktif termasuk antikanker
yang berupa senyawa-senyawa alkaloid, flavonoid, glikosida, steroid dan
terpenoid. Adanya senyawa alkaloid dan flavonoid, merupakan indikasi
terdapatnya senyawa obat dalam zat ekstraktif tersebut (Kurz dan Constabel
1998).
Kandungan Zat Ekstraktif Kayu Suren (Toona sureni Merr.)
Hasil penelitian ini menunjukkan bahwa ekstraksi dalam pelarut aseton
dari ± 50 g serbuk kulit dalam (inner bark) cabang suren (kadar air 4,62 %)
menghasilkan ekstrak aseton sebesar 5,94 g atau 12,93 % berdasarkan berat
kering tanur (BKT) serbuk kayunya dan tergolong ke dalam kategori kadar
ekstraktif tinggi sedangkan ekstraksi dalam pelarut aseton dari ± 300 g serbuk
kayu teras cabang suren (kadar air 5,66 %) menghasilkan ekstrak aseton sebesar
6,38 g atau 2,31 % berdasarkan BKT serbuk kayunya dan tergolong ke dalam
kategori kadar ekstraktif sedang. Hal ini didasarkan pada klasifikasi kelas
komponen kimia kayu Indonesia (Anonim 1976 dalam Lestari dan Pari 1990)
yang menyatakan bahwa kadar ekstraktif kayu termasuk kelas tinggi jika kadar
ekstraktifnya lebih besar dari 4 %, kelas sedang jika kadar ekstraktif antara 2 %-4
% dan kelas rendah jika kadar ekstraktifnya kurang dari 2 %. Berat serbuk yang
digunakan tidak sama untuk setiap bagian maupun jenisnya dikarenakan
keterbatasan bahan penelitian dan untuk mendapatkan ekstrak
sebanyak-banyaknya (Lampiran 3). Ekstrak aseton yang diperoleh kemudian difraksinasi
secara bertingkat dengan menggunakan pelarut n-heksana dan etil asetat. Hasil
Tabel 5. Kandungan rata-rata ekstrak aseton inner bark dan teras cabang suren (T. sureni) serta hasil fraksinasinya*)
Jenis Sampel Jenis Fraksi (%)
Total Ekstrak
N-Heksana Etil Asetat Residu Aseton (%)
Inner bark 0,80 3,13 3,94 12,93
Teras Cabang 0,18 1,42 0,40 2,31 Keterangan :
*)
- Rataan dari 3 ulangan
- % berat kering tanur (bobot fraksi terhadap bobot awal serbuk)
Berdasarkan Tabel 5 dapat dilihat, hasil fraksinasi ekstrak aseton dari
inner bark suren menunjukkan bahwa jumlah zat ekstraktif fraksi n-heksana, fraksi etil asetat, dan fraksi residu tidak sama dengan ekstrak asetonnya. Hal ini
diduga disebabkan karena adanya zat ekstraktif dari fraksi-fraksi tersebut yang
mudah menguap pada saat dikeringkan, adanya ekstrak yang melekat pada funnel
separator yang sangat sulit untuk diambil dan dikeluarkan. Disamping itu, karena keterbatasan alat maka funnel separator yang digunakan penutupnya kurang rapat
sehingga ada ekstrak yang tercecer. Apabila kita mengabaikan jumlah ekstrak
yang hilang tersebut, maka hasil fraksinasi menunjukkan bahwa fraksi residu
merupakan fraksi dengan nilai kadar tertinggi sebesar 3,94 % namun nilai ini
tidak jauh berbeda dengan fraksi etil asetat sebesar 3,13 % sedangkan terendah
pada fraksi n-heksana sebesar 0,80 %. Dengan demikian dapat dikatakan bahwa
zat ekstraktif inner bark suren sebagian besar merupakan kelompok senyawa
polar dan semi polar.
Hasil fraksinasi untuk teras cabang suren menunjukkan bahwa fraksi etil
asetat dengan nilai kadar tertinggi sebesar 1,42 % diikuti fraksi residu sebesar 0,4
% dan terendah fraksi n-heksana sebesar 0,18 %. Karena etil asetat merupakan
pelarut yang bersifat semi polar (Tabel 1), maka dapat dikatakan bahwa ekstrak
aseton bagian teras cabang suren sebagian besar mengandung zat ekstraktif yang
bersifat semi polar.
Kandungan Zat Ekstraktif Kayu Ki bonteng (Platea latifolia BL.)
Ekstraksi dalam pelarut aseton dari ± 20 gr serbuk inner bark cabang ki
bonteng (kadar air 4,46 %) menghasilkan ekstrak aseton sebesar 1,57 g atau 11,19
kategori tinggi sedangkan ekstraksi dalam pelarut aseton dari ± 500 g serbuk kayu
teras cabang ki bonteng (kadar air 4,46 %) menghasilkan ekstrak aseton sebesar
2,77 g atau 0,86 % (Tabel 6), dan tergolong ke dalam kategori kadar ekstraktif
rendah. Kemudian ekstrak aseton yang diperoleh difraksinasi dan hasil
fraksinasinya dapat dilihat pada Tabel 6.
Tabel 6. Kandungan rata-rata ekstrak aseton inner bark dan teras cabang ki bonteng (P. latifolia) serta hasil fraksinasinya*)
Jenis Sampel Jenis Fraksi (%)
Total Ekstrak
N-Heksana Etil Asetat Residu Aseton (%)
Inner bark 0,11 1,47 3,19 11,19
Teras Cabang 0,25 0,41 0,16 0,86 Keterangan :
*)
- Rataan dari 3 ulangan
- % berat kering tanur (bobot fraksi terhadap bobot awal serbuk).
Berdasarkan Tabel 6 dapat dilihat, hasil fraksinasi ekstrak aseton dari
inner bark ki bonteng menunjukkan bahwa jumlah zat ekstraktif fraksi n-heksana, fraksi etil asetat dan fraksi residu tidak sama dengan ekstrak asetonnya. Hal ini
diduga disebabkan karena adanya zat ekstraktif dari fraksi-fraksi tersebut yang
mudah menguap pada saat dikeringkan, adanya ekstrak yang melekat pada funnel
separator yang sangat sulit untuk diambil dan dikeluarkan. Disamping itu, karena keterbatasan alat maka funnel separator yang digunakan penutupnya kurang rapat
sehingga ada ekstrak yang tercecer. Dengan mengabaikan perbedaan nilai
tersebut, hasil fraksinasi menunjukkan bahwa fraksi residu dari ekstrak aseton
inner bark ki bonteng merupakan fraksi dengan nilai kadar tertinggi sebesar 3,19 % diikuti fraksi etil asetat sebesar 1,47 % dan terendah fraksi n-heksana sebesar
0,11 %. Fraksi residu merupakan fraksi yang bersifat polar. Fraksi ini adalah
fraksi yang tidak larut dalam fraksi n-heksana dan fraksi etil asetat tapi terlarut
dalam campuran air dan aseton yang ditambahkan pada awal fraksinasi. Dengan
demikian dapat dikatakan bahwa zat ekstraktif inner bark ki bonteng sebagian
besar merupakan senyawa polar.
Hasil fraksinasi untuk teras cabang ki bonteng, menunjukkan bahwa nilai
kadar fraksi tertinggi dalam ekstrak aseton adalah fraksi etil asetat sebesar 0,41 %
kemudian fraksi n-heksana sebesar 0,25 % dan terendah fraksi residu sebesar 0,16
aseton pada teras cabang ki bonteng sehingga dapat dikatakan kandungan zat
ekstraktif teras cabang ki bonteng bersifat semi polar.
Tabel 5 dan Tabel 6, menunjukkan bahwa kandungan rata-rata zat
ekstraktif suren dan ki bonteng memiliki perbedaan baik pada inner bark dan
bagian teras cabangnya. Hal ini sesuai dengan yang dikemukakan oleh Tsoumis
(1991), bahwa adanya variasi tidak hanya terdapat diantara spesies tetapi juga
dalam pohon yang sama terutama diantara kayu gubal dan kayu teras. Hasil
ekstraksi secara maserasi (rendaman) dalam pelarut aseton menunjukkan bahwa
kandungan zat ekstraktif dari inner bark suren dan ki bonteng lebih banyak
dibandingkan dengan teras cabangnya. Sjostrom (1998), menyatakan bahwa
kekhasan kulit adalah tingginya kandungan konstituen-konstituen tertentu
(ekstraktif) yang dapat larut seperti pektin dan senyawa-senyawa fenol maupun
suberin. Secara kasar ekstraktif-ekstraktif kulit dapat dibagi menjadi
konstituen-konstituen lipofil dan hidrofil. Kandungan total kedua ekstraktif lipofil dan
hidrofil biasanya lebih tinggi dalam kulit dibandingkan dalam kayu dan bervariasi
dalam batas-batas yang besar diantara spesies-spesies yang berbeda, sekitar 20-40
% berat kering kulit.
Berdasarkan Tabel 5 dan Tabel 6 juga, maka dapat diketahui bahwa inner
bark suren dan ki bonteng memiliki kesamaan fraksi yang dominan yaitu fraksi residu atau fraksi zat tak terlarut dengan kandungan zat ekstraktif tertinggi
sedangkan fraksi n-heksana merupakan fraksi terendah dalam ekstrak aseton
sehingga dapat dikatakan fraksi residu yang bersifat polar mendominasi ekstrak
aseton dari inner bark kedua kayu tersebut. Sjostrom (1998) mengemukakan
bahwa bagian hidrofil kulit yang dapat diekstraksi hanya dengan pelarut-pelarut
organik polar (aseton, etanol dan sebagainya) mengandung jumlah besar
konstituen-konstituen fenol. Untuk teras cabangnya, suren dan ki bonteng juga
memiliki kesamaan fraksi yang dominan yaitu pada fraksi etil asetat yang lebih
bersifat semi polar (Tabel 5 dan Tabel 6).
Zat ekstraktif merupakan hasil metabolisme sekunder dari tumbuhan yang
terus menerus menumpuk dan mengakibatkan kematian sel-sel pada tumbuhan
tersebut. Semakin lama proses ini terjadi maka semakin banyak substansi sisa
bertambah pula kandungan zat ekstraktifnya. Tsoumis (1991), mengemukakan
bahwa proporsi ekstraktif bervariasi mulai kurang dari 1 % (sebagai contoh
poplar) hingga lebih dari 10 % (sebagai contoh red-wood) berdasarkan berat
kering tanurnya dan untuk beberapa daerah tropis bisa terdapat sekitar 20 %.
Riset terhadap 480 sampel Pinus echinata yang hidup pada kondisi dan umur
yang berbeda menunjukkan bahwa umur mempengaruhi jumlah zat ekstraktif
lebih dari pengaruh yang lainnya (Hillis 1987). Pada umumnya zat ekstraktif kayu
terdapat pada bagian teras walaupun terdapat sejumlah kecil pada kayu gubal. Zat
ekstraktif pada pangkal pohon akan lebih banyak dibanding bagian di atasnya. Hal
ini dikarenakan pembentukan kayu teras adalah karena adanya sel yang mati
sedangkan bagian atas sel-selnya sedang aktif membelah. Zat ekstraktif pada kulit
umumnya lebih banyak dari bagian kayunya, hal ini disebabkan kulit kaya akan
konstituen-konstituen tertentu yang dapat larut. Bagian cabang kayu kadang
mengandung lebih banyak zat ekstraktif dibandingkan batangnya. Kayu teras dari
cabang dan akar pada Picea abies mengandung konsentrasi lignan yang lebih
tinggi (4 %-6 % dan 2 %-3 %) dibandingkan pada batang hardwood (0,1 %) dari
pohon yang sama (Ekman 1979 dalam Fengel dan Wegener 1989).
Perbedaan jumlah zat ekstraktif pada kayu menurut Hillis (1987)
dipengaruhi oleh beberapa faktor diantaranya umur, tempat tumbuh, jenis
(genetik), posisi dalam pohon, pelarut yang digunakan dan kecepatan
pertumbuhan. Faktor lain yang mempengaruhi kadar zat ekstraktif pada kayu
adalah ukuran serbuk, frekuensi pengadukan dalam perendaman dan kadar air
serbuk.
Kemampuan tumbuhan untuk mencukupi kebutuhan makanannya sangat
didukung oleh karakteristik daerah tempat dia tumbuh. Semakin baik kondisi
tempat tumbuh (sinar matahari, ketersediaan air, unsur hara, dan sebagainya)
maka semakin banyak makanan yang bisa diproduksi dan semakin baik pula
pertumbuhannya. Dengan demikian, pembentukan metabolit sekunder atau zat
ekstraktif akan semakin banyak pula.
Jenis pelarut yang digunakan dalam proses ekstraksi berperan penting.
Setiap jenis pelarut memiliki karakteristik yang berbeda-beda, tidak ada pelarut
agar lebih banyak maka perlu ditambahkan dua atau lebih jenis pelarut. Zat
ekstraktif mudah larut dalam pelarut netral atau pelarut organik seperti eter,
aseton, benzena, etanol, diklrometana atau campuran larutan tersebut.
Pelarut yang digunakan untuk melarutkan zat ekstraktif pada suatu bahan
tanaman memiliki kemampuan melarutkan (solubility) yang berbeda-beda dan
biasanya dinyatakan dengan konstanta dielektrik. Pelarut dengan konstanta
dielektrik yang tinggi mempunyai kemampuan melarutkan yang lebih besar
dibandingkan pelarut-pelarut yang konstanta dielektriknya lebih kecil. Ekstraktif
kadang berada tersembunyi dibelakang dinding sel tergantung pada derajat
polimerisasi dan insolubitas-nya. Pelarut juga mempunyai batas sampai dia mulai
berkurang daya larutnya. Melalui evaporasi, pelarut yang digunakan untuk
mengekstraksi bahan dapat digunakan lagi akan tetapi daya larutnya diduga
semakin berkurang. Oleh karena itu, jumlah zat ekstraktif yang dapat diekstrak
dari bahan tersebut juga semakin berkurang. Pemakaian ulang pelarut harus
diperhatikan agar bahan dapat terekstrak dengan baik.
Houghton dan Raman (1998), menyatakan bahwa pemilihan pelarut dalam
ekstraksi ditentukan oleh penguapannya, kemudahan untuk terbakar, titik didih,
toksisitas, reaktivitas dan biaya. Titik didih yang terlalu tinggi akan menyebabkan
kerusakan ekstrak pada saat pemisahannya dengan pelarut. Jika pelarut mudah
menguap maka akan menimbulkan efek yang berbahaya bagi operator maupun
lingkungan sehingga potensi berbahaya dari pelarut harus dipertimbangkan.
Pelarut yang mudah terbakar sebaiknya dihindari untuk mencegah hal-hal yang
tidak diinginkan. Pelarut mempunyai toksisitas yang berbeda-beda sehingga dapat
membahayakan bagi operatornya. Terlalu banyak menghirup pelarut dengan
toksisitas tinggi seperti kloroform atau diethil-eter bisa menyebabkan radang
pernafasan dan dapat membius. Pelarut-pelarut yang reaktif seperti pada peroksida
dapat terdekomposisi dan merusak ekstrak. Eksperimen dengan skala besar akan
menggunakan pelarut yang sangat banyak dan menghabiskan biaya yang sangat
tinggi. Oleh karena itu harus dipilih pelarut yang lebih efisien, ekonomis dan
aman.
Ukuran serbuk kayu suren dan ki bonteng yang digunakan dalam