FORMULASI DAN ANALISIS AKTIVITAS ANTIOKSIDAN MINUMAN ISOFLAVON BUBUK
Oleh : YANIASIH
F24101004
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Yaniasih. F24101004. Formulasi dan Analisis Aktivitas Antioksidan Minuman Isoflavon Bubuk. Di bawah bimbingan Dedi Fardiaz dan Noer Laily. 2006
RINGKASAN
Pengembangan produk pangan sekarang tidak hanya ditujukan untuk memperoleh pangan yang berkualitas dari segi rasa, penampilan, harga dan kemudahan bagi konsumen. Muncul tren baru yang disebut pangan fungsional, yaitu pangan yang memiliki manfaat kesehatan. Kacang kedelai merupakan salah satu bahan pangan yang memiliki potensi besar untuk dikembangkan menjadi pangan fungsional. Hal ini terkait dengan adanya kandungan zat antioksidan (isoflavon) dalam kedelai yang bermanfaat dalam mencegah berbagai penyakit yang diakibatkan oleh reaksi oksidasi di dalam tubuh. Formulasi minuman isoflavon bertujuan untuk menghasilkan produk pangan yang berkualitas (segi sensori, kimiawi dan mikrobiologi) serta memiliki manfaat bagi kesehatan (aktivitas antioksidannya tinggi).
Proses pembuatan minuman isoflavon antara lain meliputi optimasi proses pengolahan, formulasi minuman isoflavon, pembuatan susu bubuk dan analisis mutu produk. Hasil optimasi waktu perendaman dalam pembuatan susu kedelai menunjukkan perendaman 12 jam memiliki kualitas sensori (aroma dan warna) yang lebih baik. Penggunaan saringan berhasil menurunkan kandungan total kapang kamir yaitu menjadi sebesar 25 koloni pada ukuran saringan 300 mesh dan 120 koloni pada ukuran saringan 150 mesh yang dapat memenuhi standar SNI.
Formulasi minuman yang tepat berdasarkan uji organoleptik dan aktivitas antioksidannya menghasilkan sampel yang terpilih adalah sampel dengan konsentrasi 30% susu tempe hitam dan ukuran saringan 300 mesh. Formulasi sampel terpilih memiliki kualitas sensori yang disukai panelis dengan skor kesukaan rasa 3.47, aroma 2.67 dan warna 4.0 serta aktivitas antioksidan setara setara 63.19 mg BHA/ml.
Pengeringan formulasi terpilih menjadi minuman isoflavon bubuk dilakukan dengan pengering semprot. Produk minuman isoflavon bubuk yang dihasilkan memiliki aktivitas antioksidan sebesar setara 64.76 mg BHA/ml, kadar isoflavon 212 mg/100g, lemak sebesar 30.18 %, protein 62.91 %, karbohidrat 0.70 %, kadar abu 2.37 %, kadar air 3.84 %, cemaran mikroba sebesar 6.3 x 103 dan kelarutan 90.96%. Dalam memenuhi asupan isoflavon 40mg per hari, konsumsi minuman isoflavon bubuk sebesar 18.87g per saji, memiliki kandungan lemak 5.69g, protein 11.87g, karbohidrat 0.13g dan energi total 99.21 kkal (memenuhi 4.96 % diet 2000 kkal).
FORMULASI DAN ANALISIS AKTIVITAS ANTIOKSIDAN MINUMAN ISOFLAVON BUBUK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi pangan,
Fakultas Teknologi Pertanian, Institut Pertanian Bogor
Oleh : YANIASIH
F24101004
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FORMULASI DAN AKTIVISIDAN
MINUMAN ISOFLAVON BUBUK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor
Oleh : YANIASIH
F24101004
Dilahirkan di Madiun, 13 Juli 1983.
Tanggal lulus : 7 Juni 2006
Bogor, 12 Juni 2006 Menyetujui,
Prof. Dr. Ir. Dedi Fardiaz, MSc Dra. Noer Laily, MSi
Dosen Pembimbing I Dosen Pembimbing II
Mengetahui,
Dr. Ir. Dahrul Syah, MSc.
Ketua Departemen Ilmu dan Teknologi Pangan
RIWAYAT HIDUP
KATA PENGANTAR
Alhamdulillah, puji syukur kepada Allah SWT atas berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi ini. Shalawat dan salam penulis sampaikan kepada Nabi Muhammad SAW beserta seluruh pengikutnya hingga akhir zaman.
Skripsi dengan judul ”Formulasi dan Analisis Aktivitas Antioksidan Minuman Isoflavon Susu Kedelai Bubuk” ini bertujuan untuk membuat formulasi dan mengevaluasi aktivitas antioksidan produk minuman isoflavon bubuk. Produk ini diharapkan dapat menjadi alternatif pangan fungsional yang dapat bermanfaat bagi masyarakat
Penulis menyampaikan terima kasih yang sebesar-besarnya kepada : 1. Kedua orang tua, adik dan seluruh keluarga besar yang selalu memberikan
dukungan, cinta dan doa tiada henti.
2. Prof. Dr. Ir. Dedi Fardiaz, MSc telah membimbing penulis selama mengikuti studi di Departemen TPG.
3. Dra. Noer Laily, MSi yang telah membimbing, mendidik dan mengajarkan banyak hal selama penelitian dan penulisan skripsi.
4. Dr. Ir. Bonny PW Soekarno, MS dan seluruh elemen Badan Pengelola Asrama TPB IPB (senior resident, pegawai, mahasiswa 41 dan 42) yang telah banyak memberikan inspirasi dan motivasi selama 2 tahun ini.
6. Seluruh karyawan, staf dan rekan penelitian di Laboratorium Teknologi Bioindustri BPPT PUSPIPTEK Serpong yang selalu sabar mengingatkan. 7. Sahabat-sahabat luar biasa (Anita, Anna, Wulan, Desi, Ima, Innike, Santi,
Yuni, Dhani, Hasan, Endar, Riyadi, Ibot, Roji, Seno, Asep, Budi) serta seluruh staf pengajar, karyawan dan teman-teman terbaik di TPG, FATETA dan IPB, semoga Allah Swt meridhoi kita semua.
8. Semua pihak yang turut membantu yang tidak bisa disebutkan satu per satu. Semoga skripsi ini dapat bermanfaat bagi semua yang membutuhkan.
Bogor, Juni 2006
DAFTAR ISI
Halaman
KATA PENGANTAR... iv
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... ix
I. PENDAHULUAN ... 1
A. LATAR BELAKANG... 1
B. TUJUAN ... 2
II. TINJAUAN PUSTAKA... 3
A. SUSU KEDELAI ... 3
B. ANTIOKSIDAN... 6
C. ISOFLAVON... 8
III. METODE PENELITIAN... 10
A. BAHAN DAN ALAT ... 10
B. METODE PENELITIAN ... 10
1. Optimasi Proses Pembuatan Minuman Isoflavon ... 11
2. Formulasi Minuman Isoflavon ... 11
3. Pembuatan Susu Bubuk ... 11
4. Analisis Mutu Produk ... 12
IV. HASIL DAN PEMBAHASAN... 16
A. BAHAN BAKU MINUMAN ISOFLAVON ... 16
1. Susu Kedelai ... 17
2. Susu Tempe Hitam ... 19
B. FORMULASI PEMBUATAN MINUMAN ISOFLAVON ... 22
1. Uji Organoleptik ... 22
2. Aktivitas Antioksidan ... 26
C. MINUMAN ISOFLAVON BUBUK ... 28
1. Mutu Mikrobiologi dan Kimiawi ... 28
2. Aktivitas Antioksidan ... 30
3. Isoflavon ... 32
VI. KESIMPULAN DAN SARAN ... 35
A. KESIMPULAN... 35
B. SARAN ... 35
DAFTAR PUSTAKA... 36
LAMPIRAN... 40
DAFTAR TABEL
Halaman
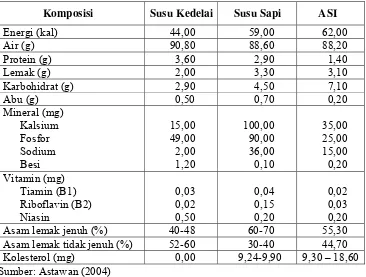
Tabel 1. Komposisi Kimia Susu Kedelai dan Susu Sapi per 100g Bahan... 3
Tabel 2. Syarat Mutu Susu Kedelai Menurut SNI 01-3830-1995... 4
Tabel 3. Syarat Mutu Susu Bubuk Menurut SNI 01-2970-1999... 5
Tabel 4. Formulasi Minuman Isoflavon... 11
Tabel 5. Kualitas Sensori Susu Kedelai Hasil Optimasi Perendaman... 18
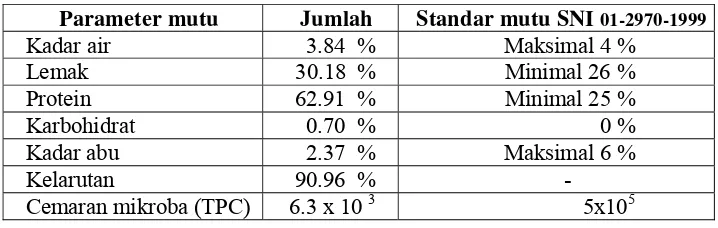
Tabel 6. Mutu Minuman Isoflavon Bubuk... 30
DAFTAR GAMBAR
Halaman
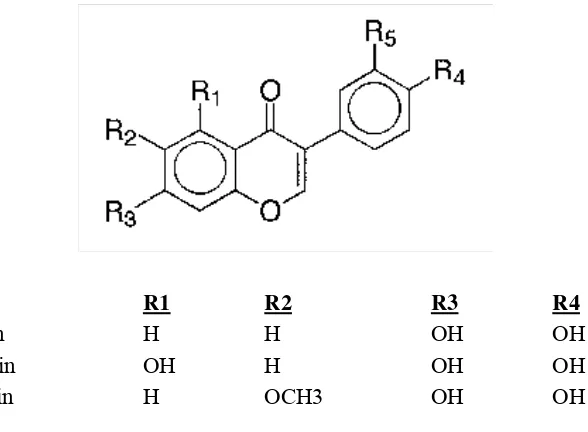
Gambar 1. Struktur Kimia isoflavon kedelai... 9
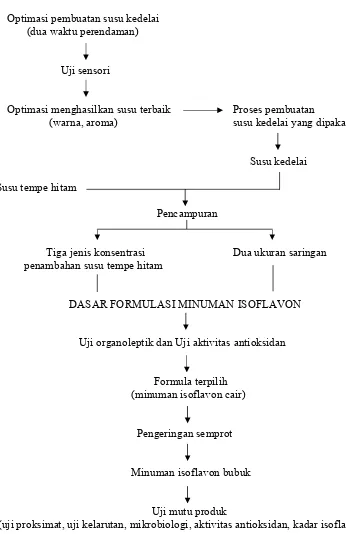
Gambar 2. Diagram alir formulasi dan aktivitas antioksidan minuman isoflavon bubuk ... 16
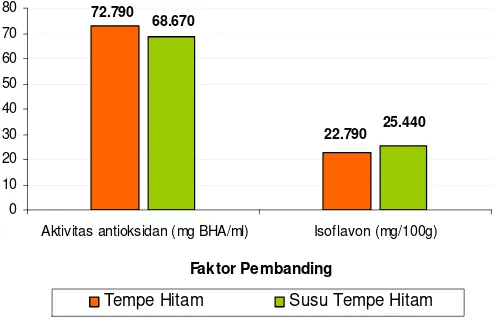
Gambar 3. Perbandingan Aktivitas Antioksidan dan Kadar Isoflavon antara Tempe Hitam dan Susu Tempe Hitam ... 21
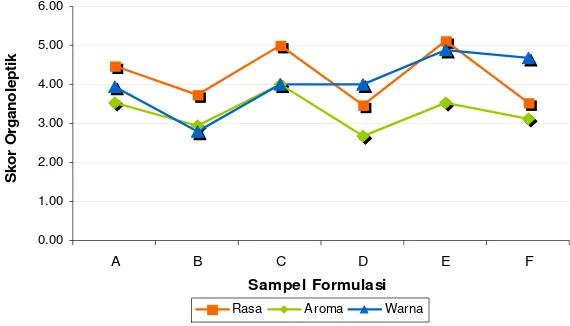
Gambar 4. Grafik Hasil Uji Hedonik terhadap Atribut Rasa, Aroma dan Warna... 24
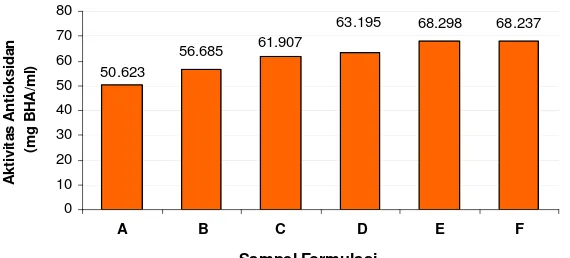
Gambar 5. Aktivitas Antioksidan Sampel Formulasi... 26
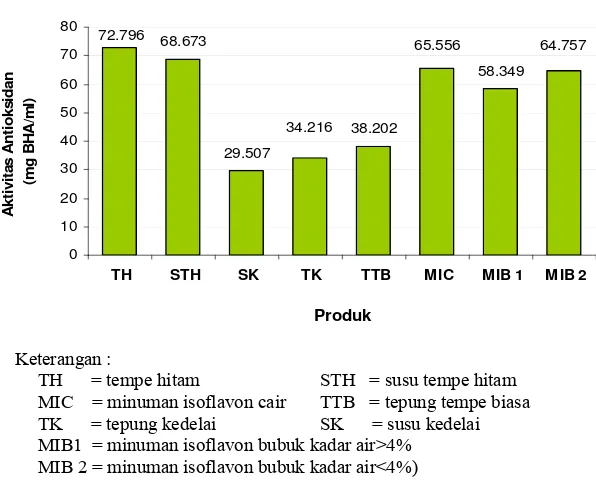
Gambar 6. Aktivitas Antioksidan Beberapa Bahan Pangan... 31
Gambar 7. Kadar Isoflavon Beberapa Bahan Pangan... 34
FORMULASI DAN ANALISIS AKTIVITAS ANTIOKSIDAN MINUMAN ISOFLAVON BUBUK
Oleh : YANIASIH
F24101004
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Yaniasih. F24101004. Formulasi dan Analisis Aktivitas Antioksidan Minuman Isoflavon Bubuk. Di bawah bimbingan Dedi Fardiaz dan Noer Laily. 2006
RINGKASAN
Pengembangan produk pangan sekarang tidak hanya ditujukan untuk memperoleh pangan yang berkualitas dari segi rasa, penampilan, harga dan kemudahan bagi konsumen. Muncul tren baru yang disebut pangan fungsional, yaitu pangan yang memiliki manfaat kesehatan. Kacang kedelai merupakan salah satu bahan pangan yang memiliki potensi besar untuk dikembangkan menjadi pangan fungsional. Hal ini terkait dengan adanya kandungan zat antioksidan (isoflavon) dalam kedelai yang bermanfaat dalam mencegah berbagai penyakit yang diakibatkan oleh reaksi oksidasi di dalam tubuh. Formulasi minuman isoflavon bertujuan untuk menghasilkan produk pangan yang berkualitas (segi sensori, kimiawi dan mikrobiologi) serta memiliki manfaat bagi kesehatan (aktivitas antioksidannya tinggi).
Proses pembuatan minuman isoflavon antara lain meliputi optimasi proses pengolahan, formulasi minuman isoflavon, pembuatan susu bubuk dan analisis mutu produk. Hasil optimasi waktu perendaman dalam pembuatan susu kedelai menunjukkan perendaman 12 jam memiliki kualitas sensori (aroma dan warna) yang lebih baik. Penggunaan saringan berhasil menurunkan kandungan total kapang kamir yaitu menjadi sebesar 25 koloni pada ukuran saringan 300 mesh dan 120 koloni pada ukuran saringan 150 mesh yang dapat memenuhi standar SNI.
Formulasi minuman yang tepat berdasarkan uji organoleptik dan aktivitas antioksidannya menghasilkan sampel yang terpilih adalah sampel dengan konsentrasi 30% susu tempe hitam dan ukuran saringan 300 mesh. Formulasi sampel terpilih memiliki kualitas sensori yang disukai panelis dengan skor kesukaan rasa 3.47, aroma 2.67 dan warna 4.0 serta aktivitas antioksidan setara setara 63.19 mg BHA/ml.
Pengeringan formulasi terpilih menjadi minuman isoflavon bubuk dilakukan dengan pengering semprot. Produk minuman isoflavon bubuk yang dihasilkan memiliki aktivitas antioksidan sebesar setara 64.76 mg BHA/ml, kadar isoflavon 212 mg/100g, lemak sebesar 30.18 %, protein 62.91 %, karbohidrat 0.70 %, kadar abu 2.37 %, kadar air 3.84 %, cemaran mikroba sebesar 6.3 x 103 dan kelarutan 90.96%. Dalam memenuhi asupan isoflavon 40mg per hari, konsumsi minuman isoflavon bubuk sebesar 18.87g per saji, memiliki kandungan lemak 5.69g, protein 11.87g, karbohidrat 0.13g dan energi total 99.21 kkal (memenuhi 4.96 % diet 2000 kkal).
FORMULASI DAN ANALISIS AKTIVITAS ANTIOKSIDAN MINUMAN ISOFLAVON BUBUK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi pangan,
Fakultas Teknologi Pertanian, Institut Pertanian Bogor
Oleh : YANIASIH
F24101004
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FORMULASI DAN AKTIVISIDAN
MINUMAN ISOFLAVON BUBUK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor
Oleh : YANIASIH
F24101004
Dilahirkan di Madiun, 13 Juli 1983.
Tanggal lulus : 7 Juni 2006
Bogor, 12 Juni 2006 Menyetujui,
Prof. Dr. Ir. Dedi Fardiaz, MSc Dra. Noer Laily, MSi
Dosen Pembimbing I Dosen Pembimbing II
Mengetahui,
Dr. Ir. Dahrul Syah, MSc.
Ketua Departemen Ilmu dan Teknologi Pangan
RIWAYAT HIDUP
KATA PENGANTAR
Alhamdulillah, puji syukur kepada Allah SWT atas berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi ini. Shalawat dan salam penulis sampaikan kepada Nabi Muhammad SAW beserta seluruh pengikutnya hingga akhir zaman.
Skripsi dengan judul ”Formulasi dan Analisis Aktivitas Antioksidan Minuman Isoflavon Susu Kedelai Bubuk” ini bertujuan untuk membuat formulasi dan mengevaluasi aktivitas antioksidan produk minuman isoflavon bubuk. Produk ini diharapkan dapat menjadi alternatif pangan fungsional yang dapat bermanfaat bagi masyarakat
Penulis menyampaikan terima kasih yang sebesar-besarnya kepada : 1. Kedua orang tua, adik dan seluruh keluarga besar yang selalu memberikan
dukungan, cinta dan doa tiada henti.
2. Prof. Dr. Ir. Dedi Fardiaz, MSc telah membimbing penulis selama mengikuti studi di Departemen TPG.
3. Dra. Noer Laily, MSi yang telah membimbing, mendidik dan mengajarkan banyak hal selama penelitian dan penulisan skripsi.
4. Dr. Ir. Bonny PW Soekarno, MS dan seluruh elemen Badan Pengelola Asrama TPB IPB (senior resident, pegawai, mahasiswa 41 dan 42) yang telah banyak memberikan inspirasi dan motivasi selama 2 tahun ini.
6. Seluruh karyawan, staf dan rekan penelitian di Laboratorium Teknologi Bioindustri BPPT PUSPIPTEK Serpong yang selalu sabar mengingatkan. 7. Sahabat-sahabat luar biasa (Anita, Anna, Wulan, Desi, Ima, Innike, Santi,
Yuni, Dhani, Hasan, Endar, Riyadi, Ibot, Roji, Seno, Asep, Budi) serta seluruh staf pengajar, karyawan dan teman-teman terbaik di TPG, FATETA dan IPB, semoga Allah Swt meridhoi kita semua.
8. Semua pihak yang turut membantu yang tidak bisa disebutkan satu per satu. Semoga skripsi ini dapat bermanfaat bagi semua yang membutuhkan.
Bogor, Juni 2006
DAFTAR ISI
Halaman
KATA PENGANTAR... iv
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... ix
I. PENDAHULUAN ... 1
A. LATAR BELAKANG... 1
B. TUJUAN ... 2
II. TINJAUAN PUSTAKA... 3
A. SUSU KEDELAI ... 3
B. ANTIOKSIDAN... 6
C. ISOFLAVON... 8
III. METODE PENELITIAN... 10
A. BAHAN DAN ALAT ... 10
B. METODE PENELITIAN ... 10
1. Optimasi Proses Pembuatan Minuman Isoflavon ... 11
2. Formulasi Minuman Isoflavon ... 11
3. Pembuatan Susu Bubuk ... 11
4. Analisis Mutu Produk ... 12
IV. HASIL DAN PEMBAHASAN... 16
A. BAHAN BAKU MINUMAN ISOFLAVON ... 16
1. Susu Kedelai ... 17
2. Susu Tempe Hitam ... 19
B. FORMULASI PEMBUATAN MINUMAN ISOFLAVON ... 22
1. Uji Organoleptik ... 22
2. Aktivitas Antioksidan ... 26
C. MINUMAN ISOFLAVON BUBUK ... 28
1. Mutu Mikrobiologi dan Kimiawi ... 28
2. Aktivitas Antioksidan ... 30
3. Isoflavon ... 32
VI. KESIMPULAN DAN SARAN ... 35
A. KESIMPULAN... 35
B. SARAN ... 35
DAFTAR PUSTAKA... 36
LAMPIRAN... 40
DAFTAR TABEL
Halaman
Tabel 1. Komposisi Kimia Susu Kedelai dan Susu Sapi per 100g Bahan... 3
Tabel 2. Syarat Mutu Susu Kedelai Menurut SNI 01-3830-1995... 4
Tabel 3. Syarat Mutu Susu Bubuk Menurut SNI 01-2970-1999... 5
Tabel 4. Formulasi Minuman Isoflavon... 11
Tabel 5. Kualitas Sensori Susu Kedelai Hasil Optimasi Perendaman... 18
Tabel 6. Mutu Minuman Isoflavon Bubuk... 30
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Kimia isoflavon kedelai... 9
Gambar 2. Diagram alir formulasi dan aktivitas antioksidan minuman isoflavon bubuk ... 16
Gambar 3. Perbandingan Aktivitas Antioksidan dan Kadar Isoflavon antara Tempe Hitam dan Susu Tempe Hitam ... 21
Gambar 4. Grafik Hasil Uji Hedonik terhadap Atribut Rasa, Aroma dan Warna... 24
Gambar 5. Aktivitas Antioksidan Sampel Formulasi... 26
Gambar 6. Aktivitas Antioksidan Beberapa Bahan Pangan... 31
Gambar 7. Kadar Isoflavon Beberapa Bahan Pangan... 34
DAFTAR LAMPIRAN
Lampiran 1. Kurva standar analisis aktivitas antioksidan metode DPPH ... 41
Lampiran 2. Aktivitas antioksidan sampel formulasi ... 42
Lampiran 3. Analisis statistik ANOVA aktivitas antioksidan sampel formulasi ... 43
Lampiran 4. Aktivitas antioksidan bahan/produk pangan ... 45
Lampiran 5. Analisis statistik ANOVA aktivitas antioksidan bahan pangan . 46 Lampiran 6. Kuisioner uji hedonic ………. 48
Lamiran 7. Analisis statistik ANOVA uji organoleptik Hedonik atribut warna ... 48
Lampiran 8. Analisis statistik ANOVA uji organoleptik Hedonik atribut rasa ... 49
Lampiran 9. Analisis statistik ANOVA uji organoleptik Hedonik atribut aroma ... 50
Lampiran 10. Kadar isoflavon metode HPLC ... 51
Lampiran 11. Analisis proksimat minuman isoflavon bubuk ... 52
Lampiran 12. Analisis total kapang ... 53
I. PENDAHULUAN
A. LATAR BELAKANG
Secara tradisional, produk pangan dikembangkan untuk memperoleh pangan yang berkualitas dari segi rasa, penampilan, harga dan kemudahan bagi konsumen. Sekarang muncul tren baru, dimana pengembangan produk pangan banyak dilakukan pada kemungkinan penggunaan produk pangan dalam mengurangi resiko terkena penyakit tertentu (Stephen, 1998). Meningkatnya angka penderita penyakit jantung, kanker dan tekanan darah tinggi di banyak negara serta banyaknya hasil penelitian yang menunjukkan kaitan antara beberapa zat gizi maupun non gizi pangan yang berpotensi mengatasi masalah tersebut menyebabkan tren ini semakin meluas. Dalam mengkonsumsi suatu pangan, masyarakat sekarang tidak hanya menilai dari segi gizi dan rasa suatu produk, tetapi juga mempertimbangkan pengaruh pangan tersebut terhadap kesehatan tubuhnya (Goldberg, 1994).
Perubahan tren produk pangan ke arah potensi pangan bagi kesehatan, memotivasi produsen pangan mengembangkan produk pangan fungsional. Pangan fungsional adalah produk pangan yang menunjukkan adanya manfaat fisiologis atau adanya kemampuan mengurangi resiko penyakit kronis tertentu, disamping fungsi nutrisi dasarnya (Stephen, 1998). Salah satu produk pangan yang banyak dikembangkan sebagai pangan fungsional adalah pangan olahan dari kedelai. Kedelai mengandung beberapa senyawa kimia yang dinamakan phytochemicals yang ternyata mampu mencegah berbagai penyakit, seperti isoflavon, protease inhibitor dan asam fitat yang memiliki kemampuan antioksidan berguna dalam mencegah penyakit kanker (Heinnermen, 2003).
susu masyarakat Indonesia. Kandungan gizi yang tinggi, harga yang relatif lebih murah, proses pengolahan yang mudah dan bebas laktosa (Shurtleff dan Aoyogi, 1984), memungkinkan produk ini untuk lebih dikembangkan di Indonesia.
Pengembangan susu kedelai menjadi produk pangan fungsional yang berkualitas baik dari sisi sensori, kandungan gizi, manfaat kesehatan maupun kemudahan bagi konsumen sekarang banyak dilakukan. Salah satu fokus pengembangan tersebut banyak dikaitkan dengan hasil-hasil penelitian yang menunjukkan adanya kandungan zat antioksidan (isoflavon) dalam susu kedelai yang bermanfaat dalam mencegah berbagai penyakit yang diakibatkan oleh reaksi oksidasi di dalam tubuh (USDA, 1999; Chang, 1998). Selain itu juga terkait dengan kepraktisan konsumsi, distribusi dan penyimpanan sehingga proses pengeringan susu kedelai menjadi bentuk susu bubuk dapat dijadikan sebagai alternatif pilihan.
B. TUJUAN PENELITIAN
II. TINJAUAN PUSTAKA
A. SUSU KEDELAI
Susu kedelai adalah produk pangan olahan berupa ekstrak air dari kacang kedelai (Liu, 1997). Produk ini banyak dikembangkan baik untuk tujuan komersial (industri), tujuan sosial maupun kesehatan. Hal ini disebabkan oleh beberapa nilai lebih yang dimiliki susu kedelai antara lain kandungan gizinya yang tinggi, bebas laktosa, bebas kolesterol, harganya relatif murah, teknologi pembuatannya sederhana dan bisa dijadikan alternatif makanan vegetarian (Shurtleff dan Aoyogi, 1984).
Menurut Liu (1997), susu kedelai memiliki kandungan protein, zat besi, asam lemak tak jenuh dan niasin yang lebih tinggi dibandingkan susu sapi, tetapi kandungan lemak, kalsium dan karbohidratnya lebih rendah. Selain itu susu kedelai tidak mengandung laktosa dan kurang kandungan mineral fosfor, yodium dan sodium. Komposisi susu kedelai, susu sapi dan air susu ibu (ASI) disajikan pada Tabel 1.
Tabel 1. Komposisi Kimia Susu Kedelai dan Susu Sapi per 100g Bahan
Komposisi Susu Kedelai Susu Sapi ASI
Energi (kal) 44,00 59,00 62,00
Standar produk susu kedelai pertama kali ditetapkan di Jepang tahun 1975. Standar produk akhir susu kedelai harus mengandung minimal 3% minyak dan lemak, minimal 10% total padatan dan maksimal 300 mikroorganisme per gram susu kedelai serta tidak terdapat bakteri koliform (Shurtleff dan Aoyogi, 1984). Menurut Haytowitz dan Matthews (1989) susu kedelai minimal mengandung 2% protein, 1% lemak dan 11,5% total padatan dengan pH berkisar antara 6,6-7,0. Di Indonesia, syarat mutu susu kedelai ditetapkan menurut Standar Nasional Indonesia (SNI), yang disajikan dalam Tabel 2.
Tabel 2. Syarat Mutu Susu Kedelai Menurut SNI 01-3830-1995 Kriteria Uji Satuan Persyaratan
Keadaan Bau Rasa Warna
- - -
Normal Normal Normal
pH - 6.5-7.0
Protein % b/b Min 2.0
Lemak % b/b Min 1.0
Total padatan 5 b/b Min 11.5
mendidih, kemudian ditambah pemanis, garam dan flavor untuk mendapatkan citarasa yang lebih baik (Shurtleff dan Aoyogi, 1984).
Perkembangan produksi susu kedelai komersial melahirkan berbagai variasi produk susu kedelai, seperti susu kedelai segar (tanpa penambahan gula), susu kedelai manis dan susu kedelai bubuk. Susu kedelai bubuk dibuat dari susu kedelai segar atau susu kedelai manis kemudian dikeringkan menggunakan pengering semprot (Shurtleff dan Aoyogi, 1984). Menurut Syarief dan Hariyadi (1991), pengeringan susu bubuk dapat menggunakan pengering semprot atau pengering drum. Proses pengeringan ini dapat mempengaruhi sifat fisik dan kimia susu bubuk. Susu yang dikeringkan menggunakan pengering semprot akan menghasilkan partikel 10-15 mikron dan kelarutannya dalam air sempurna hampir sama dengan susu segar. Syarat mutu susu bubuk berdasarkan Standar Nasional Indonesia (SNI) disajikan dalam Tabel 3.
Tabel 3. Syarat Mutu Susu Bubuk Menurut SNI 01-2970-1999
B. ANTIOKSIDAN
Antioksidan secara umum didefinisikan sebagai senyawa yang dapat menunda, memperlambat dan mencegah proses oksidasi lipid. Dalam arti khusus, antioksidan adalah zat yang dapat menunda atau mencegah terjadinya reaksi oksidasi radikal bebas dalam oksidasi lipid (Kochhar dan Rossell, 1990).
Proses oksidasi lipid terjadi dalam tiga tahap yaitu inisiasi, propagasi dan terminasi. Reaksi inisiasi terjadi ketika lemak tidak jenuh berinteraksi dengan oksigen membentuk radikal bebas. Radikal bebas tersebut akan berlanjut mengalami reaksi berantai membentuk radikal bebas-radikal bebas lain dalam tahap reaksi propagasi. Selanjutnya dalam reaksi terminasi, radikal bebas yang bersifat sangat reaktif akan membentuk ikatan yang stabil bila bereaksi dengan senyawa radikal lain (Jadhav et al., 1996). Ketiga tahap reaksi oksidai lipid tersebut adalah sebagai berikut :
Tahap reaksi inisiasi : RH Æ R* + H*
ROOH Æ RO* + HO*
ROOH Æ RO* + ROO* + H2O
Tahap reaksi propagasi : R* + O2 Æ ROO* ROO* + RH Æ ROOH + R* Tahap reaksi terminasi : R* + R* Æ R-R
R* + ROO* Æ ROOR ROO* + ROO* Æ ROOR +O2
Antioksidan sekunder, seperti asam sitrat, asam askorbat, dan esternya, sering ditambahkan pada lemak dan minyak sebagai kombinasi dengan antioksidan primer. Kombinasi tersebut dapat memberi efek sinergis sehingga menambah keefektifan kerja antioksidan primer. Antioksidan sekunder ini bekerja dengan satu atau lebih mekanisme berikut (a) memberikan suasana asam pada medium (sistem makanan), (b) meregenerasi antioksidan utama, (c) mengkelat atau mendeaktifkan kontaminan logam prooksidan, (d) menangkap oksigen. (e) mengikat singlet oksigen dan mengubahnya ke bentuk triplet oksigen.
Berdasarkan sumbernya antioksidan dibagi dalam dua kelompok, yaitu antioksidan sintetik (antioksidan yang diperoleh dari hasil sintesa reaksi kimia) dan antioksidan alami (antioksidan hasil ekstraksi bahan alami). Beberapa contoh antioksidan sintetik yang diijinkan penggunaannya secara luas diseluruh dunia untuk digunakan dalam makanan adalah Butil Hidroksi Anisol (BHA), Butil Hidroksi Toluen (BHT), propil galat, Tert-Butil Hidoksi Quinon (TBHQ) dan tokoferol. Antioksidan tersebut merupakan antioksidan yang telah diproduksi secara sintetis untuk tujuan komersial (Buck, 1991). Antioksidan alami di dalam makanan dapat berasal dari senyawa antioksidan yang sudah ada dari satu atau dua komponen makanan, senyawa antioksidan yang terbentuk dari reaksi-reaksi selama proses pengolahan, serta senyawa antioksidan yang diisolasi dari sumber alami dan ditambahkan ke makanan sebagai bahan tambahan pangan (Pratt,1992).
Penggunaan antioksidan dalam produk pangan sangat bervariasi. Aktivitas antioksidan dalam produk pangan diperngaruhi oleh suhu, komposisi makanan, struktur produk dan keberadaan oksigen (Gordon, 2001). Menurut Coppen (1983), ciri-ciri antioksidan yang dapat digunakan adalah sebagai berikut (a) aman dalam penggunaan, (b) tidak memberi flavor, bau, dan warna pada produk, (c) efektif pada konsentrasi rendah, (d) tahan terhadap proses pengolahan produk (berkemampuan antioksidan yang baik), (e) tersedia dengan harga yang murah.
kardivaskuler, kanker dan penuaan (Nelson et al., 2003). Konsumsi formula antioksidan yang mengandung β-karoten, vitamin E dan selenium organik setiap hari terbukti mengurangi resiko terkena kanker lambung (turun sampai dengan 21%), kanker esofagus resikonya turun sampai 4% dan penurunan tingkat kematian dari penyebab lainnya sampai 9% (Setright, 1993).
C. ISOFLAVON
Isoflavon tergolong kelompok flavonoid yaitu senyawa polifenolik yang banyak ditemukan dalam buah–buahan, sayur-sayuran, dan biji-bijian. Isoflavon adalah flavonoid utama dalam kacang kedelai yang memiliki potensi besar dalam mencegah kanker, osteoporosis, sindrom menopause dan hiperkolesterol (Zubik dan Meydani, 2003).
Kacang kedelai dikenal mengandung beberapa jenis isoflavon yaitu daidzein, glycitein dan genistein yang memiliki daya estrogenik, antifungal dan antioksidan (Fleury et al., 1992). Produk pangan dari kacang kedelai mengandung isoflavon dalam konsentrasi tinggi, terutama dalam bentuk glukosida terkonjugasi (Setchell, 2003). Menurut (Hendrich et al., 1998), kandungan isoflavon dalam kacang kedelai berkisar antara 1-3 mg/g dan pada produk olahannya berkisar antara 0.025-3 mg/g.
Isoflavon kedelai terutama berupa 7-O-monoglukosida-isoflavon, dimana bagian glikosidanya 100 kali bagian aglikonnya. Senyawa antioksidan alami isoflavon dari kedelai tersebut adalah 5,7,5’-trihidroksiisoflavon-7-0-monoglukosida (genistein) 7,4’-dihidroksiisoflavon-7-monoglukosida (daidzein), dan 7,4;-dihidroksi6-metoksi-isoflavon-7-0-monoglukosida (glycitein). Isoflavon lain dari kedelai adalah 6,7,4’-trihidroksiisoflavon yang hanya terdapat pada produk-produk kedelai terfermentasi (Pratt,1992).
R1 R2 R3 R4
Daidzen H H OH OH
Genistein OH H OH OH
Glycitein H OCH3 OH OH
Gambar 1. Soy isoflavones (Harborne, et.all., 1975)
III. METODE PENELITIAN
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan dalam penelitian adalah kacang kedelai, susu tempe hitam, air, maltodekstrin, bufer Tris-HCl, BHA, DPPH, PDA, H2SO4, HgO, K2SO4, H3BO3, NaOH-Na2S2O3 dan PCA.
Alat-alat yang digunakan antara lain timbangan, blender, pompa vakum, saringan, spektrometer, oven, HPLC, alat destilasi, pengering semprot, alumunium foil, kertas saring, pH meter, autoklaf dan peralatan gelas.
B. METODE PENELITIAN
1. Optimasi Proses Pembuatan Minuman Isoflavon
a. Optimasi lama waktu perendaman dalam pembuatan susu kedelai
Bertujuan untuk memperoleh susu kedelai yang memiliki warna dan aroma yang lebih baik. Lama waktu perendaman yang digunakan adalah 2 jam (waktu perendaman yang digunakan dalam pengolahan modern), 8 jam dan 12 jam (metode tradisional di Jepang, Cina, dan Indonesia) (Shurtleff dan Aoyogi, 1984). Setelah direndam, kedelai direbus selama 15 menit. Kedelai yang telah direbus diblender dengan ditambah air (perbandingan kedelai:air adalah 1:5). Kedelai yang sudah diblender kemudian disaring dan susu yang dihasilkan dipasteurisasi pada suhu 90oC selama 15 menit. Susu hasil dua jenis optimasi perendaman tersebut kemudian dibandingkan kualitas rasa, warna dan aromanya. b. Pembuatan susu tempe hitam
c. Optimasi ukuran saringan
Penyaringan minuman isoflavon (campuran susu kedelai dan susu tempe hitam) menggunakan 2 ukuran saringan yaitu 150 dan 300 mesh. Penyaringan diperlukan untuk memperoleh produk yang berkualitas (sensori terkait ukuran partikel dan mikrobiologi). Hasil dua penyaringan dibandingkan kandungan mikrobanya. Penyaringan yang menghasilkan susu dengan kandungan mikroba memenuhi standar mutu digunakan sebagai bagian proses pembuatan minuman isoflavon.
2. Formulasi Minuman Isoflavon
Formulasi pembuatan minuman isoflavon dilakukan dengan membuat campuran dari susu kedelai dengan susu tempe hitam. Formulasi dilakukan berdasarkan perbandingan volume susu kedelai dan susu tempe hitam yang dicampurkan, serta berdasarkan penggunaan variasi ukuran saringan. Penentuan formula terbaik dilakukan dengan uji organoleptik Hedonik dan uji aktivitas antioksidan. Formulasi minuman isoflavon disajikan pada Tabel 4.
Tabel 4. Formulasi Minuman Isoflavon
No Kode Volume susu
kedelai (%)
Volume susu tempe hitam (%)
Ukuran saringan (mesh)
1 A 80 20 150
2 B 80 20 300
3 C 70 30 150
4 D 70 30 300
5 E 60 40 150
6 F 60 40 300
3. Pembuatan Susu Bubuk (Varnam dan Sutherland, 1994)
4. Analisis Mutu Produk
a. Aktivitas antioksidan metode DPPH (Yamaguchi et al., 1998)
Ekstraksi sampel
Sebanyak 10 ml sampel ditambah 90 ml metanol 80%, kemudian dishaker 24 jam, 240 rpm dalam kondisi tertutup alufo. Setelah 24 jam disaring dengan pompa vakum, ditutup rapat, lalu dievaporasi suhu 40oC dengan rotary evaporator sampai volume akhir 9 ml. Volume diatur sampai 10 ml dengan menambahkan metanol 80%, kemudian dimasukkan dalam botol gelap dan simpan dalam freezer.
Analisis aktivitas antioksidan
Sebanyak 800 μl larutan bufer Tris-HCl 100 mM ditambahkan pada 200 μl larutan sampel (atau BHA standar), kemudian ditambahkan 1 ml larutan DPPH 0.2 mM kemudian divortex. Disimpan dalam ruang gelap pada suhu ruang selama 20 menit, kemudian diukur absorbansi pada λ 517 nm.
Aa = Absorbansi DPPH tanpa sampel
Ab = Absorbansi campuran sampel dan DPPH Ac = Absorbansi sampel tanpa DPPH
b. Uji mikrobiologi total kapang dan total mikroba (Fardiaz, 1987)
c. Uji hedonik (Rahayu, 1998)
Sampel diuji tingkat penerimaannya oleh panelis. Uji menggunakan 20-25 panelis agak terlatih. Penerimaan terdiri atas 7 tingkat yaitu sangat suka, suka, agak suka, netral, agal tidak suka, tidak suka dan sangat tidak suka. Data hasil uji dianalisis dengan analisis sidik ragam dan uji lanjut uji Duncan.
d. Uji kelarutan (Apriyantono et al., 1989)
Kertas saring dikeringkan dalam oven 50oC selama 30 menit dan ditimbang. Dilakukan penyaringan terhadap 0.75 g produk yang dilarutkan dalam 100 ml akuades. Kertas saring dikeringkan dalam oven 100oC selama 3 jam kemudian ditimbang.
e. Analisis proksimat
i. Kadar air metode oven vakum (AOAC, 1995)
Cawan alumunium dikeringkan dalam oven bersuhu 100oC selama 15 menit, dinginkan dalam desikator selama 10 menit kemudian timbang (W1). Sebanyak 5 gram contoh ditimbang dalam cawan tersebut (W2). Cawan berisi sampel dipanaskan dalam oven vakum (T = 70oC, 25 mmHg) selama 5 jam atau hingga tercapai berat yang tetap. Selanjutnya didinginkan dalam desikator selama 15 menit, kemudian ditimbang (W3).
(
)
ii. Kadar protein metode Kjedahl (AOAC, 1995)
Sampel ditimbang sebanyak 0,1-0.15 gram lalu dimasukkan ke dalam labu Kjehdahl 30 mL. Di dalam labu ditambahkan 2ml
H2SO4, 40 mg HgO dan 1.9 mg K2SO4. Sampel didihkan selama 1-1.5 jam sampai cairan menjadi jernih, setelah itu didinginkan dengan menambahkan air perlahan-lahan. Isi labu kemudian dipindahkan dalam alat destilasi. Cuci dan bilas labu 5-6 kali dengan 1-2 ml air, air cucian dipindahkan ke alat destilasi. Erlenmeyer 125 ml berisi 5 ml larutan H3BO3 dan 2-3 tetes indikator metil merah-metilen blue, kemudian diletakkan di bawah kondensor. Ujung tabung kondensor terendam dalam H3BO3 kemudian ditambah 8-10 ml NaOH-Na2S2O3 dan didestilasi sampai tertampung kira-kira 15 ml destilat dalam erlenmeyer. Isi erlenmeyer diencerkan sampai 50 ml kemudian dititrasi dengan HCl 0.02 N.
Cawan alumunium dikeringkan dalam oven bersuhu 100oC selama 15 menit. Didinginkan dalam desikator selama 10 menit kemudian dtimbang (W1). Sebanyak 3-5 gram contoh ditimbang dalam cawan tersebut (W2). Cawan berisi sampel dibakar dalam tanur selama 5 jam atau hingga tercapai berat yang tetap. Selanjutnya didinginkan dalam desikator selama 15 menit, kemudian timbang (W3).
iv. Kadar lemak metode destilasi (BSN, 1992)
diekstrak dengan pelarut lemak selama 6 jam. Ekstrak lemak dikeringkan dalam oven pada suhu 105oC, kemudian didinginkan dalam desikator dan ditimbang sampai diperoleh berat yang konstan.
f. Penentuan rendemen (Apriyantono et al., 1989)
g. Kadar isoflavon metode HPLC (Balai Besar Penelitian dan Pengembangan Pasca Panen)
FORMULASI DAN AKTIVITAS ANTIOKSIDAN MINUMAN ISOFLAVON BUBUK
Optimasi pembuatan susu kedelai (dua waktu perendaman)
Uji sensori
Optimasi menghasilkan susu terbaik Proses pembuatan (warna, aroma) susu kedelai yang dipakai
Susu kedelai
Susu tempe hitam
Pencampuran
Tiga jenis konsentrasi Dua ukuran saringan penambahan susu tempe hitam
DASAR FORMULASI MINUMAN ISOFLAVON
Uji organoleptik dan Uji aktivitas antioksidan
Formula terpilih (minuman isoflavon cair)
Pengeringan semprot
Minuman isoflavon bubuk
Uji mutu produk
(uji proksimat, uji kelarutan, mikrobiologi, aktivitas antioksidan, kadar isoflavon)
IV. HASIL DAN PEMBAHASAN
A. BAHAN BAKU MINUMAN ISOFLAVON
1. Susu Kedelai
Susu kedelai merupakan produk pangan yang telah banyak mengalami pengembangan dalam proses pengolahannya, mulai dari pengolahan tradisional sampai pengolahan modern di industri komersial. Prinsip dasar semua proses pengolahan tersebut secara umum adalah sama, yaitu terdiri dari perendaman, penghancuran biji kacang kedelai, penambahan air, proses ekstraksi, pemanasan dan penambahan Bahan Tambahan Pangan (BTP) berupa pemanis dan flavor (Heinnermen, 2003).
Beberapa perbedaan yang muncul sebagai variasi dari proses yang sudah ada, banyak dikembangkan untuk mencapai tujuan-tujuan tertentu dalam produk akhir susu kedelai. Tujuan tersebut antara lain seperti penghematan biaya produksi, peningkatan jumlah rendemen serta peningkatan kualitas sensori. Salah satu variasi yang berbeda adalah dalam proses perendaman yang akan berpengaruh terhadap jumlah rendemen dan kualitas sensori susu kedelai yang dihasilkan (Shurtleff dan Aoyogi, 1984).
Proses pembuatan minuman isoflavon menggunakan variasi waktu perendaman sebagai proses optimasi produk akhir. Optimasi yang dilakukan menggunakan lama perendaman yang berbeda yaitu dua jam dan dua belas jam. Hal ini bertujuan untuk menentukan lama perendaman yang tepat, yang dapat menghasilkan susu kedelai dengan kualitas sensori yang lebih baik.
Hasil penilaian tes panelis menunjukkan perendaman dua belas jam memiliki kualitas sensori yang lebih baik. Menggunakan dua atribut sensori sebagai indikator kualitas yaitu aroma dan warna, perendaman dua belas jam memiliki aroma dengan tingkat aroma langu lebih kecil dan warna yang lebih putih dibandingkan dengan perendaman dua jam. Kualitas sensori hasil optimasi dua waktu perendaman yang dilakukan disajikan pada Tabel 4.
Tabel 5. Kualitas Sensori Susu Kedelai Hasil Optimasi Perendaman
Menurut (Shurtleff dan Aoyogi, 1984), proses perendaman dapat menyebabkan hilangnya sejumlah komponen dalam kedelai karena larut dalam air. Perendaman selama 24 jam akan menyebabkan kehilangan karbohidrat larut air sebesar 73.20%, protein kasar 23.30% dan lemak 2.80%. Kehilangan komponen ini memiliki pengaruh terhadap warna dan aroma susu kedelai yang dihasilkan. Terbentuknya aroma langu disebabkan oleh oksidasi asam lemak. Hilangnya lemak dalam jumlah tertentu selama perendaman akan memperkecil terbentuknya aroma langu. Semakin lama perendaman, jumlah lemak yang hilang dalam kacang kedelai dan larut dalam air, akan semakin besar.
Shurtleff dan Aoyogi (1984) menyatakan proses perendaman juga dapat menghasilkan senyawa volatil 1-okten-3-alkohol yang dapat menyebabkan aroma langu, namun dapat berkurang dalam rangkaian proses pengolahan susu kedelai. Oleh karena itu walaupun perendaman dapat mengurangi jumlah lemak yang teroksidasi menghasilkan aroma langu, namun dengan terbentuknya senyawa lain yang dapat menimbulkan
Waktu perendaman Keterangan Kualitas Sensori
2 jam 8 jam 12 jam
aroma langu juga, menyebabkan perbedaan kualitas sensori produk yang direndam lebih lama tidak terlalu berbeda kualitas sensori aromanya dibandingkan produk yang direndam sebentar.
Lama waktu perendaman selain berpengaruh terhadap aroma juga berpengaruh terhadap kualitas warna produk. Perendaman dalam air dapat membersihkan kotoran pada kulit biji kedelai. Selain itu perendaman produk pangan akan menyebabkan warna produk umumnya memudar menjadi keputih-putihan. Hal ini disebabkan hampir sebagian besar pigmen alami yang terdapat dalam pangan hewani maupun nabati larut dalam air (Winarno, 2002). Proses perendaman kedelai akan melarutkan pigmen sehingga warna kedelai lebih putih dan akan menghasilkan susu yang warnanya lebih putih.
2. Susu Tempe Hitam
Selain susu kedelai, bahan baku lain yang digunakan dalam pembuatan minuman isoflavon adalah susu tempe hitam. Susu tempe hitam dibuat dari tempe hitam yang merupakan produk olahan tempe melalui proses fermentasi. Berdasarkan hasil penelitian sebelumnya, tempe hitam digunakan karena memiliki aktivitas antioksidan yang tinggi dan kadar isoflavonnya juga besar.
Hasil pengukuran aktivitas antioksidan tempe hitam adalah sebesar 65.44 % atau setara 72.79 mg BHA/ml, sedangkan kadar isoflavonnya sebesar 22.79 mg/100g. Pengolahan tempe hitam menjadi susu tempe hitam menghasilkan susu dengan aktivitas antioksidan sebesar 61.22 % atau setara dengan 68.67 mg BHA/ml dan kadar isoflavon 25.44 mg/100g. Pengolahan tempe hitam menjadi produk susu dilakukan dengan penambahan air dua kali berat tempe hitam. Hal ini menyebabkan aktivitas antioksidan susu tempe hitam lebih rendah karena kandungan tempe hitamnya lebih sedikit. Selain itu penurunan aktivitas antioksidan juga disebabkan proses pengholahan tempe menjadi susu menggunakan pemanasan yang mencapai suhu 100oC. Menurut Gordon (2001) aktivitas antioksidan menjadi kurang efektif ketika bahan mengalami pemanasan pada suhu ≥ 100o
C.
isoflavon sedikit lebih tinggi dibandingkan tempe hitam per 100 gram bahan. Perbandingan aktivitas antioksidan dan kadar isoflavon antara tempe hitam dengan susu tempe hitam dapat dilihat pada Gambar 3.
Gambar 3. Perbandingan Aktivitas Antioksidan dan Kadar Isoflavon antara Tempe Hitam dan Susu Tempe Hitam
Penggunaan susu tempe hitam yang merupakan produk fermentasi perlu memperhatikan kandungan total kapang yang mungkin masih ada di dalamnya. Hasil uji total kapang yang dilakukan pada susu tempe hitam menunjukkan jumlah total kapang kamir adalah sebesar 1.1 x 105 koloni. Jumlah ini masih diatas standar susu kedelai yaitu sebesar 300 koloni (Shurtleff dan Aoyogi, 1984). Berdasarkan hasil tersebut, maka perlu adanya optimasi proses pembuatan minuman isoflavon, yang bertujuan untuk mengurangi jumlah total kapang kamir. Optimasi yang dilakukan adalah dengan melakukan penyaringan susu menggunakan dua variasi ukuran yaitu saringan 150 mesh dan 300 mesh.
Hasil optimasi penggunaan saringan menunjukkan total kapang kamir adalah sebesar 25 koloni pada ukuran saringan 300 mesh dan 120 koloni pada ukuran saringan 150 mesh. Kedua jumlah ini memenuhi standar mutu mikrobiologi susu kedelai, sehingga kedua ukuran saringan tersebut dapat digunakan dalam pembuatan minuman isoflavon dan dijadikan dasar formulasi produk minuman isoflavon.
72.790
22.790 68.670
25.440
0 10 20 30 40 50 60 70 80
Aktivitas antioksidan (mg BHA/ml) Isoflavon (mg/100g)
Faktor Pembanding
B. FORMULASI PEMBUATAN MINUMAN ISOFLAVON
1. Uji Organoleptik
Minuman isoflavon merupakan produk pangan fungsional berbahan baku susu kedelai dan susu tempe hitam. Salah satu permasalahan utama dalam pengolahan susu kedelai adalah kualitas aroma dan rasa dari produk yang dihasilkan. Umumnya susu kedelai memiliki aroma langu yang disebabkan oleh enzim lipoksigenase yang ada pada kacang kedelai. Enzim ini akan aktif ketika biji kacang hancur pada proses ekstraksi. Selama ekstraksi terjadi reaksi oksidasi asam lemak tak jenuh yang dikatalis oleh enzim lipoksigenase. Oksidasi akan menghasilkan komponen volatil berupa keton, aldehid dan alkohol yang menimbulkan aroma langu (Shurtleff dan Aoyogi, 1984).
Minuman isoflavon yang berbahan baku kedelai, selain harus meminimalisir terbentuknya aroma langu juga harus mengatasi kemungkinan munculnya rasa pahit yang berasal dari susu tempe hitam yang tinggi kandungan isoflavonnya. Menurut Okubo et al. (1992), isoflavon berupa genistein dan daidzein dapat memberikan kontribusi rasa pahit yang cukup besar. Selama produksi susu, secara alami enzim β -glukosidase akan muncul dan mengubah isoflavon bentuk glukosida menjadi bentuk aglikon (daidzein dan genistein) yang rasanya lebih pahit. (Matsuura et al. 1989).
Keenam formula tersebut adalah formula A susu tempe hitam 20% dengan saringan 150 mesh, formula B susu tempe hitam 20% dengan saringan 300 mesh, formula C susu tempe hitam 30% dengan saringan 150 mesh, formula D susu tempe hitam 30% dengan saringan 300 mesh, formula E susu tempe hitam 40% dengan saringan 150 mesh serta formula F susu tempe hitam 40% dengan saringan 300 mesh.
Penentuan formula yang akan dipilih berdasarkan kualitas sensori, dilakukan menggunakan uji organoleptik. Uji organoleptik dapat dilakukan berdasarkan tingkat kesukaan (uji hedonik) panelis pada produk secara keseluruhan atau lebih spesifik lagi berupa tingkat kesukaan pada kualitas sensori tertentu seperti rasa, aroma, warna, tekstur dan penampakan (Shurtleff dan Aoyogi, 1984).
Pelaksanaan test dapat dilakukan dengan memberikan kepada panelis susu kedelai sebanyak 45 ml pada suhu ruang. Kemudian panelis diminta untuk menilai kesukaan menggunakan skor uji yaitu angka 1 sangat suka, 2 suka, 3 agak suka, 4 netral, 5 agak kurang suka, 6 tidak suka dan 7 sangat tidak suka. Untuk melakukan uji ini minimal menggunakan 12 panelis (Shurtleff dan Aoyogi, 1984)
Uji hedonik dilakukan pada semua sampel formulasi yang berjumlah enam sampel. Panelis yang memberikan penilaiannya sebanyak 30 orang. Uji yang dilakukan bersifat spesifik pada tiga atribut sensori yaitu rasa, warna dan aroma. Skor tingkat kesukaan yang digunakan adalah antara 1 sampai 7.
Hasil uji organoleptik pada atribut sensori aroma dengan uji ANOVA berbeda nyata dengan α = 0.074 pada selang kepercayaan 0.05. Hasil uji hedonik menunjukkan semua sampel A, B, C, D, E, F dapat diterima oleh tingkat kesukaan panelis dengan skor 2.67 sampai 4.0.
Hasil uji organoleptik atribut sensori warna berdasarkan uji ANOVA berbeda nyata antar sampel (α = 0.000 dengan selang kepercayan 5%). Sampel yang paling disukai adalah sampel B (20%, 300 mesh) dengan skor 2.80. Sampel yang masih bisa diterima adalah sampel A (20%, 150 mesh), sampel D (30%, 300 mesh) dan sampel C (30%, 150 mesh) dengan skor kesukaan antara 3.93-4.00. Sampel yang tidak bisa diterima panelis adalah sampel E dan F (40%, 150 dan 40%, 300 mesh) dengan skor 4.67 sampai 4.87.
Keterangan :
A = susu tempe hitam 20% dengan saringan 150 mesh B = susu tempe hitam 20% dengan saringan 300 mesh C = susu tempe hitam 30% dengan saringan 150 mesh D = susu tempe hitam 30% dengan saringan 300 mesh E = susu tempe hitam 40% dengan saringan 150 mesh F = susu tempe hitam 40% dengan saringan 300 mesh.
Gambar 4. Grafik Hasil Uji Hedonik Atribut Rasa, Aroma dan Warna
Hasil keseluruhan uji organoleptik disajikan pada Gambar 4. Berdasarkan hasil tersebut diketahui ketiga atribut sensori yang diuji yaitu rasa, aroma dan warna, memiliki skor yang semakin tinggi dengan
semakin bertambahnya konsentrasi susu tempe hitam. Hal ini menunjukkan semakin besar jumlah susu tempe hitam, rasa produk semakin tidak disukai. Dari enamformula sampel hanya tiga sampel yang atribut rasanya cukup disukai panelis dan dapat dijadikan formula terpilih yaitu sampel dengan skor < 4, yaitu sampel B, D dan F. Atribut aroma secara umum disukai panelis dan keenam formula dapat dipilih. Atribut warna semakin tidak disukai dengan bertambahnya jumlah susu tempe hitam, hanya sampai penambahan sebesar 30% yang warnanya masih disukai panelis, sedangkan untuk jumlah susu tempe hitam > 30 % sudah tidak dapat diterima oleh panelis.
Selain ditentukan oleh jumlah susu tempe hitam, kesukaan panelis pada formula juga ditentukan oleh saringan yang digunakan. Secara umum dengan semakin tinggi konsentrasi jumlah susu tempe hitam yang ditambahkan dalam formulasi, skor kesukaan rasa semakin tinggi yang menunjukkan sampel semakin kurang disukai. Sampel yang menggunakan saringan 300 mesh memiliki skor kesukaan rasa yang lebih rendah yang menunjukkan semakin disukai. Hal ini disebabkan dengan semakin besarnya mesh, semakin kecil lubang saringan, sehingga berpengaruh terhadap jumlah komponen dengan ukuran relatif besar yang tidak lolos saringan 300 mesh. Komponen ini mungkin memiliki pengaruh terhadap rasa pahit susu tempe hitam.
Skor uji hedonik atribut aroma berkisar antara 2.67 sampai 4 yang menunjukkan secara umum semua sampel cukup disukai aromanya oleh panelis. Skor kesukaan aroma tidak berbanding lurus antara penambahan konsentrasi susu tempe hitam maupun semakin besarnya ukuran saringan dengan kenaikan skor uji. Hal ini mungkin disebabkan perubahan aroma tidak terlalu dipengaruhi oleh jumlah maupun ukuran komponen-komponen dalam minuman tersebut.
dengan konsentrasi susu tempe hitam 40% sudah tidak bisa diterima oleh tingkat kesukaan panelis karena warnanya cukup pekat.
Berdasarkan hasil tersebut, sampel yang semua kualitas sensori (rasa, aroma dan warna) disukai panelis adalah sampel D (30%, 300 mesh) dan B (20%, 300 mesh). Kedua sampel ini kemudian dilihat aktivitas antioksidannya. Sampel dengan aktivitas antioksidan terbaik ditetapkan sebagai formulasi terpilih minuman isoflavon.
2. Aktivitas Antioksidan
Kualitas produk minuman isoflavon sangat ditentukan oleh aktivitas antioksidan. Aktivitas antioksidan ini menjadi dasar penentuan formulasi terpilih selain kualitas sensori produk. Salah satu metode yang digunakan untuk mengetahui aktivitas antioksidan adalah dengan metode Radical Scavenging Activity. Dalam metode ini digunakan radikal sintetik dalam pelarut organik pada suhu ruang. Salah satu radikal sintetik yang banyak digunakan adalah 2,2 diphenyl-1-picrylhydrazyl (DPPH).
Metode DPPH mengukur aktivitas antioksidan berdasarkan penurunan absorbansi pada λ 517 nm. Penurunan ini terjadi karena adanya reaksi antioksidan dari sampel yang diukur dengan pereaksi DPPH yang awalnya beerwarna pekat menghasilkan senyawa stabil yang warnanya lebih cerah (Gordon , 2001). Hasil pengukuran aktivitas antioksidan keenam sampel formulasi minuman isoflavon menggunakan metode DPPH disajikan pada Gambar 5.
Keterangan :
A = susu tempe hitam 20% dengan saringan 150 mesh B = susu tempe hitam 20% dengan saringan 300 mesh C = susu tempe hitam 30% dengan saringan 150 mesh D = susu tempe hitam 30% dengan saringan 300 mesh E = susu tempe hitam 40% dengan saringan 150 mesh F = susu tempe hitam 40% dengan saringan 300 mesh.
Gambar 5. Aktivitas Antioksidan Sampel Formulasi
Uji Statistika ANOVA aktivitas antioksidan berbeda nyata antar sampel pada selang kepercayaan 5%. Aktivitas antioksidan semakin tinggi dengan semakin bertambahnya konsentrasi susu tempe hitam. Hal ini sesuai dengan hasil pengukuran aktivitas antioksidan bahan penyusun yang menunjukkan susu tempe hitam memiliki aktivitas antioksidan lebih tinggi dibandingkan dengan susu kedelai. Hal ini mengakibatkan semakin tinggi konsentrasi susu tempe hitam yang ditambahkan dalam formulasi minuman isoflavon, aktivitas antioksidan produk minuman tersebut akan semakin meningkat. Perubahan konsentrasi ini memberikan pengaruh yang lebih dominan terhadap perubahan aktivitas antioksidan dibandingkan dengan perbedaan ukuran saringan. Penggunaan ukuran saringan yang berbeda tidak berpengaruh secara signifikan terhadap aktivitas antioksidan sampel.
Berdasarkan Gambar 5, diketahui sampel yang memiliki aktivitas antioksidan tertinggi adalah sampel E. Namun, walaupun sampel E dan F memiliki aktivitas antioksidan lebih tinggi dari yang lainnya, skor uji
Aktivitas Antioksidan Sampel Formulasi
hedoniknya kurang baik yaitu tidak semua atribut sensori sampel F dapat diterima panelis. Dengan konsentrasi susu tempe hitam 40%, kualitas sensori sampel E dan F kurang diterima panelis terutama warna. Oleh karena itu, berdasarkan uji organoleptik dan aktivitas antioksidan, formulasi menghasilkan formula terpilih yaitu sampel D yang memiliki aktivitas antioksidan cukup tinggi yaitu setara 63.19 mg BHA/ml dan secara organoleptik ketiga atribut sensorinya disukai oleh panelis.
C. MINUMAN ISOFLAVON BUBUK
Minuman isoflavon merupakan produk yang dikembangkan bertujuan untuk menghasilkan pangan yang memiliki manfaat bagi kesehatan. Selain bermanfaat, produk baru ini juga diharapkan memiliki kualitas sensori yang baik, kandungan gizi dasar yang memadai, aman dan mudah dalam penyimpanan serta kemudahan mengkonsumsi. Untuk mencapai tujuan tersebut, maka formula minuman isoflavon terpilih yang berbentuk cair diolah menjadi bentuk bubuk. Menurut Pisecky (1997), susu bubuk dengan kadar air 4% memilki aktivitas air < 0.2 % sehingga umur simpannya menjadi panjang serta dapat menghemat biaya produksi.
Proses pengolahan yang memegang peranan penting dalam pembuatan minuman isoflavon menjadi bentuk bubuk adalah proses pengeringan menggunakan pengering semprot. Prinsip pengeringan semprot adalah dengan menyemprotkan cairan (susu) pada aliran uap panas, air dalam cairan akan menguap meninggalkan tepung kering (Wirakartakusumah et al. 1992).
penyerapan, memberi rasa lembut dan meningkatkan kelarutan Kennedy et al. (1995). Proses pengeringan menggunakan pengering semprot dan penggunaan maltodekstrin sebagai bahan pengisi akan mempengaruhi mutu fisik dan kimia produk.
1. Mutu Mikrobiologi dan Kimiawi
Minuman isoflavon bubuk merupakan produk pangan yang diharapkan dapat menjadi produk pangan fungsional yang dapat diterima masyarakat. Menurut Stephen (1998), pangan fungsional merupakan produk pangan seperti pada umumnya, yang dikonsumsi dalam diet sehari-hari dan memiliki manfaat fisiologis dan mengurangi resiko munculnya penyakit tertentu. Seperti umumnya produk pangan yang lain, mutu pangan fungsional juga terkait dengan kandungan berbagai zat gizi seperti lemak, protein dan karbohidrat di dalamnya.
Analisis proksimat minuman isoflavon menunjukkan kandungan lemak sebesar 30.18 %, protein 62.91 %, karbohidrat 0.70 % dan kadar abu 2.37 %. Nilai ini memenuhi standar susu bubuk SNI yaitu lemak ninimal 26% protein minimal 25% dan kadar abu maksimal 6 %. Selain mutu kandungan lemak, protein dan karbohidrat, salah satu parameter terpenting terkait dengan mutu produk susu kedelai bubuk adalah sifat kelarutan dalam air. Kelarutan yang baik adalah sekitar 85 % karena 15 % kandungan susu kedelai adalah berupa protein yang tidak larut dalam air (Shurtleff dan Aoyogi, 1984). Minuman isoflavon bubuk yang dihasilkan memiliki kelarutan 90.96%. Nilai ini menunjukkan produk yang dihasilkan memiliki kelarutan yang baik.
1997). Menurut Varnam dan Sutherland (1994), untuk menghasilkan susu bubuk dengan kandungan air 2-5%, suhu inlet untuk pengeringan susu bubuk berkisar 180-230oC dan suhu outlet 70-90oC.
Pembuatan minuman isoflavon susu kedelai bubuk menggunakan pengering semprot dengan suhu inlet 180oC dan suhu outlet 70oC. Penggunaan suhu yang relatif rendah ini bertujuan untuk meminimalkan kerusakan isoflavon oleh panas. Menurut Chang (1998), panas dapat menyebabkan perubahan struktur isoflavon. Perubahan struktur akan menurunkan aktivitas antioksidan isoflavon. Penggunaan suhu inlet dan outlet pengering semprot yang relatif rendah ini ternyata menghasilkan susu bubuk dengan kadar air sebesar 6.07%. Kadar air ini belum memenuhi standar mutu SNI yaitu maksimal 4%. Oleh karena itu, bubuk minuman tersebut kemudian di oven selama 4 jam pada suhu 45oC sehingga diperoleh susu bubuk dengan kadar air sebesar 3.84%.
Selain kadar air, kecepatan kerusakan minuman juga dipengaruhi oleh jumlah cemaran mikoba. Mutu Susu Bubuk Menurut SNI 01-2970-1999 mensyaratkan Total Plate Count (TPC) cemaran mikroba maksimal 5x105. Pengukuran TPC produk minuman isoflavon bubuk memiliki cemaran mikroba sebesar 6.3 x 10 3 yang masih memenuhi SNI. Semua parameter mutu minuman isoflavon disajikan dalam Tabel 5.
Tabel 6. Mutu Minuman Isoflavon Bubuk
Parameter mutu Jumlah Standar mutu SNI 01-2970-1999
Kadar air 3.84 % Maksimal 4 %
Lemak 30.18 % Minimal 26 %
Protein 62.91 % Minimal 25 %
Karbohidrat 0.70 % 0 %
Kadar abu 2.37 % Maksimal 6 %
Kelarutan 90.96 % -
2. Aktivitas Antioksidan
Minuman isoflavon merupakan minuman fungsional yang diharapkan memiliki aktivitas antioksidan yang tinggi. Hasil pengukuran aktivitas antioksidan minuman isoflavon bubuk kadar air > 4% adalah setara 58.35 mg BHA/ml, sedangkan minuman isoflavon bubuk kadar airnya < 4% adalah setara 64.76 mg BHA/ml.
Aktivitas antioksidan minuman isoflavon yang kadar airnya > 4% lebih rendah dibandingkan minuman dengan kadar air < 4%. Hal ini disebabkan pada produk dengan kandungan air yang lebih rendah, kadar senyawa lain per jumlah keseluruhan bahan akan lebih besar. Pada susu dengan kadar air < 4% kandungan senyawa yang memiliki aktivitas antioksidan per jumlah total bahan lebih besar dari produk dengan kadar air > 4% sehingga aktivitas antioksidannya juga lebih besar.
Aktivitas antioksidan minuman isoflavon bubuk, baik dengan kadar air>4% maupun <4% lebih rendah dibandingkan dengan minuman isoflavon yang berbentuk cair. Minuman isoflavon cair memiliki aktivitas antioksidan setara dengan 65.56 mg BHA/ml. Penurunan aktivitas antioksidan produk bubuk disebabkan oleh proses pengeringan semprot dan oven yang dapat menyebabkan aktivitas aktioksidan berkurang. Pemanasan dapat mempengaruhi stabilitas dan volatilitas senyawa antioksidan sehingga aktivitasnya menurun (Gordon, 2001). Namun perbedaan aktivitas antioksidan minuman cair dan bubuk ini tidak terlalu besar, sehingga proses pengeringan menjadi bubuk tetap dapat dijadikan pilihan mengingat keuntungan-keuntungan lain dari bentuk minuman bubuk.
bubuk kadar air > 4% (MIB 1), tepung tempe biasa (TTB), tepung kedelai
MIB1 = minuman isoflavon bubuk kadar air>4% MIB 2 = minuman isoflavon bubuk kadar air<4%)
Gambar 6. Aktivitas Antioksidan Beberapa Bahan Pangan
Berdasarkan uji statistik ANOVA pada selang kepercayaan 5%, nilai aktivitas antioksidan dari keenam sampel dapat dibagi dalam tiga kelompok, dimana antar sampel dalam satu kelompok tidak berbeda nyata sedangkan antar sampel yang berbeda kelompok berbeda nyata. Kelompok 1 adalah sampel tepung kedelai dan tepung tempe biasa, kelompok 2 minuman isoflavon bubuk dengan kadar air > 4%, kelompok 3 minuman isoflavon cair dan minuman isoflavon bubuk dengan kadar air %< 4%, serta kelompok 4 susu tempe hitam. Kelompok 3 diketahui minuman isoflavon bubuk dengan kadar air < 4% nilai aktivitas antioksidannya tidak berbeda nyata dengan minuman isofalvon cair, walaupun nilainya lebih rendah. Hal ini menunjukkan proses pengeringan tidak menurunkan kualitas antioksidan minuman isoflavon secara signifikan.
Aktivitas Antioksidan Bahan Pangan
3. Isoflavon
Banyak faktor yang mempengaruhi kandungan isoflavon dalam makanan, antara lain karakteristik bahan mentah, ekstraksi dan proses analisis. Dalam bahan mentah kacang kedelai, terdapat perbedaan kandungan isoflavon yang dipengaruhi oleh varietas, tempat tumbuh dan waktu tumbuh. Berbagai proses analisis juga dapat menghasilkan kandungan isoflavon yang berbeda. Perbedaan analisis biasanya disebabkan oleh standar, alat dan metode ekstraksi yang digunakan. Walaupun ada 12 jenis isoflavon yang telah ditemukan, tidak semua dilaporkan dalam suatu analisis disebabkan oleh kurang baiknya berbagai jenis standar malonil komersil yang ada sehingga hanya jenis isoflavon aglicon (daidzein, genistein dan glyctein) yang dilaporkan jumlahnya (Chang, 1998).
Salah satu alat yang banyak digunakan untuk analisis isoflavon adalah Hight Performance Liquid Chromatogrphy (HPLC). Terkait dengan terbatasnya distribusi sumber bahan pangan yang mengandung isoflavon, metode analisis isoflavon dengan HPLC juga hanya terbatas pada analisis isoflavon kacang kedelai (Lee, 2000).
Tahapan pertama analisis isoflavon menggunakan HPLC adalah persiapan sampel. Sampel porduk yang dianalisis diekstrak dengan metanol 80% (10mg.ml), kemudian ditambah 1.25 mg fluoresin. Selanjutnya sampel di stiring selama 1 jam pada suhu 60oC, kemudian di sentrifugasi selama 10 menit. Hasil supernatan kering yang diperoleh dilarutkan dengan metanol 80% dan heksan, kemudian di evaporasi sampai kering dan disentrifugasi dengan penambahan metanol 80% sampai volume 10 ml selama 2 menit. HPLC yang digunakan adalah deteksi UVV pada 262 nm (Lee, 2000).
terutama ditemukan dalam bentuk genistein, daidzein, glycitein dan glukosidanya yaitu asetil dan malonil glukosida (Chang, 1998).
Kadar isoflavon hasil pengukuran minuman isoflavon bubuk adalah genistein 49 mg/100g, daidzein 56mg/100g dan total isoflavon sebesar 212 mg/100g. Besarnya nilai isoflavon bubuk disebabkan oleh penurunan kadar air dari 96.26% menjadi 3.84 % dan rendemen hasil pengeringan semprot sebesar 9.04%. Hal ini mengakibatkan konversi kandungan isoflavon menjadi lebih besar karena hilangnya sebagian besar kandungan air dalam bahan tersebut sehingga kandungan isoflavon per gram bahan menjadi lebih tinggi.
Menurut Chang (1998), secara umum suhu proses pengolahan makanan akan menyebabkan perubahan struktur kimia isoflavon dalam makanan tersebut. Panas yang terlalu tinggi akan menurunkan kandungan isoflavon antara 57-88 %. Pengolahan minuman isoflavon menjadi bentuk bubuk menggunakan suhu inlet sebesar 180oC. Akibatnya jika dikonversi ke dalam bentuk cair dengan rendemen pengeringan semprot sebesar 9.04 % (b/v), maka untuk membuat 100 ml minuman cair diperlukan 9.04 g minuman bubuk. Hasil konversi 100 ml minuman cair yang dibuat memiliki kandungan isoflavon sebesar 19.16 mg isoflavon. Nilai ini bila dibandingkan dengan minuman isoflavon cair yang kadar isoflavonnya sebesar 24.87 mg/100, maka terjadi penurunan kandungan isoflavon yang disebabkan oleh panas sebesar 22.95 %.
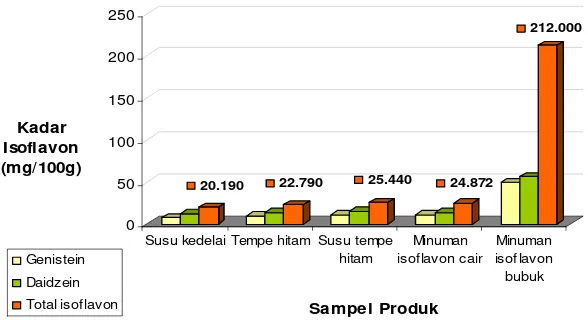
Gambar 7. Kadar Isoflavon Beberapa Bahan Pangan
20.190 22.790 25.440 24.872
212.000
Hasil pengukuran kadar isoflavon pada beberapa bahan pangan disajikan dalam Gambar 7. Berdasarkan Gambar 7 diketahui bahwa minuman isoflavon bubuk memiliki kandungan isoflavon (mg/100g) bahan yang jauh lebih tinggi dibandingkan susu kedelai, tempe hitam, susu tempe hitam dan minuman isoflavon cair.
VI. KESIMPULAN DAN SARAN
A. KESIMPULAN
Proses optimasi pembuatan minuman isoflavon berdasarkan waktu perendaman menunjukkan perendaman 12 jam memiliki kualitas sensori lebih baik (tingkat aroma langu lebih kecil dan warna yang lebih putih) dibandingkan dengan perendaman dua jam. Hasil optimasi penggunaan saringan menunjukkan total kapang kamir adalah sebesar 25 koloni pada ukuran saringan 300 mesh dan 120 koloni pada ukuran saringan 150 mesh.
Penentuan sampel formulasi terpilih adalah berdasarkan uji organoleptik dan aktivitas antioksidannya. Berdasarkan kedua uji tersebut formulasi terpilih adalah sampel D (30%, 300 mesh). Uji organoleptik menunjukkan sampel D memiliki kualitas sensori yang disukai panelis dengan skor kesukaan rasa 3.47, aroma 2.67 dan warna 4.0. Aktivitas antioksidan sampel formulasi adalah sebagai berikut sampel A setara 50.62 mg BHA/ml, sampel B setara 56.69 mg BHA/ml, sampel C setara 61.91 mg BHA/ml, sampel D setara 63.19 mg BHA/ml, sampel E setara 68.29 mg BHA/ml dan sampel F setara 68.24 mg BHA/ml.
Produk minuman isoflavon bubuk yang dihasilkan memiliki aktivitas antioksidan sebesar setara 64.76 mg BHA/ml, kadar isoflavon 212 mg/100g, lemak sebesar 30.18 %, protein 62.91 %, karbohidrat 0.70 %, kadar abu 2.37 %, kadar air 3.84 %, cemaran mikroba sebesar 6.3 x 103 dan kelarutan 90.96%. Dalam memenuhi asupan isoflavon 40mg per hari, konsumsi minuman isoflavon bubuk sebesar 18.87g per saji, memiliki kandungan lemak 5.69g, protein 11.87g, karbohidrat 0.13g dan energi total 99.21 kkal (memenuhi 4.96 % diet 2000 kkal).
B. SARAN
DAFTAR PUSTAKA
AOAC. 1995. Official Methods of Analysis of the Association of Official Analytical Chemistry. AOAC, Inc. Arlington.
Apriyantono, A., D. Fardiaz, N. L. Puspitasari, Sedarnawati, S. Budiyanto. 1989. Analisa Pangan. Pusat Antar Universitas Pangan dan Gizi. IPB. Bogor Badan Standarisasi Nasional. 1992. Cara Uji Makanan dan Minuman. SNI
01-7891-1992. Badan Standarisasi Nasional, Jakarta.
Chang, S. K. C. 1998. Isoflavones from soybean and soy foods. Di dalam : G. Mazza (Ed.). Functional Foods : Biochemical andd Processing Aspects. Technomic Publishing Co. Inc, Basel.
Chen, S. 1989. Preparation of fluids soymilk. Di dalam Liu, K. Soybeans : Chemistry, Technology and Utilization. International Thomson, New York Coppen, P.P 1983. The use of antioxidant. Di dalam: J.C. Allen dan R.J Hamilton
(eds.). Rancidity in Foods. Applied Science Publishers, London.
Direktorat Jendral Peternakan. 2003. Buku Statistik Peternakan. Departemen Pertanian, Jakarta.
Fardiaz, S. 1987. Penuntun Praktikum Mikrobiologi Pangan. Lembaga Sumberdaya Informasi. IPB. Bogor
Fleury, Y. D. H. Welti, G. Philippossian and D. Magnolato. 1992. Soybean (malonyl) isoflavones : Characterization and antioxidant properties. Di dalam : Huang, M., C. Ho and C. Y. Lee (Eds.). Phenolic Compounds in Food and Their Effects on Health II. American Chemical Society, Washington.
Goldberg, I (Ed.). 1994. Functional Food, Designer Food, Pharma Food, Neutraceuticals. Chapman and Hall, New York.
Gordon, M.H 1990. The mechanism of antioxidants action in vitro. Di dalam: B.J.F. Hudson (Ed.). Food Antioxidants. Elsivier Applied Science, London. Gordon, M. H. 2001. Measuring antioxidants activity. Di dalam : Antioxidants in
Foods. J. Pokorny, N. Yanishlei and M. H. Gordon (Eds.). Woodhead Publishing Limited. Cambridge, England.
Hussain, M. 2003. Soy isoflavones in the treatment of prostate cancer. Nutr Cancer : 47(2):111-7.
Jadhav, S. J., S. S. Nimbalkar, A. D. Kulkarni and D. L. Madhavi. 1996. Lipid oxidation in biological and food systems. Di dalam : Madhavi, D. L., S. S. Deshpande and D. K. Salunkhe. Food Antioxidants : Technological, Toxicological and Health Perpecstives. Marcel Dekker, Inc. New York Jogiani. 1992. Mempelajari Pengaruh Ekstraksi Kedelai dan Jenis Bahan Pengisi
terhadap Mutu Susu Kedelai Bubuk yang Dihasilkan. Skripsi. Fakultas Teknologi Pertanian IPB. Bogor
Kennedy, J.F., C. J. Knill and D. W. Taylor. 1995. Maltodekstrin. Di dalam : M. W. Keasley dan S. Z. Dziedzic. (Eds.). Hand Book of Hydrolysis Product and Their Derivates. Blackie Academic and Profesional, London.
Kochar, S.P. dan B. Rossell. 1990. Detection estimation and evaluation of antioxidants in food system. Di dalam : B.J.F. Hudson (ed.). Food Antioxidants. Elvisier Applied Science. London.
Lee. 2000. HPLC analysis of phenolic compounds. Di dalam : L. M. L. Nollet (Ed.). Food Analysis by HPLC. Marcel Dekker, Inc. New York
Lembono, S. 1989. Pembuatan Susu Bubuk Kedelai dengan Alat Pengering Semprot. Skripsi. Fakultas Teknologi Pertanian IPB. Bogor
Liu, K. 1997. Soybeans : Chemistry, Technology and Utilization. International Thomson, New York.
Matsuura, M., A. Obata and D. Fukushima. 1989. Objectionable flavor of soymilk developed during he soaking of soybean and its control. J. Food Sci. 54:602-605
Nda. 2004. Alergi laktosa, konsumsi susu di Indonesia rendah. http:/www.mediaindonesia.co.id. [18 Maret 2004]
Nelson, J. L., P. S. Bernstein, M. C. Schmidt, M. S. Von Tress and E. W. Askew. 2003. Dietary modification and moderate antioxidant supplementation differently affect serum carotenoids, antioxidants level and markers of oxidative stress in older humans. J. Nutr. 133:3117-3123.2003.
Okubo, K., M. Iijima, Y. Kobayashi, M. Yoshikoshi, T. Uchida and S. Kudou. 1992. Components responsiblefor the undesirable taste of soybean seeds. Biosci. Biotech. Biochem. 56:99-103.
Potter, S.M. 1998. Soy protein and isoflavones: their effects on blood lipids and bone density in postmenopausal women. Am J Clin Nutr.: 68(6 Suppl):1375S-1379S
Pratt, D.E. 1992. Natural antioxidants from plant material. Di dalam : M.T. Huang, C.T. Ho, dan C.Y. Lee (eds.). Phenolic Compounds in Food and Their Effects on Health H. American Society, Washington DC.
Rahayu, W.P. 1998. Penuntun Praktikum Penilaian Organoleptik. IPB. Bogor. Ruiz-Larrea, MB. 1997. Antioxidant activity of phytoestrogenic isoflavones. Free
Radic Res. : 26(1):63-70
Setchell, K. D. R, N. M. Brown, P. B. Desai, L. Z. Nechimias, B. Wolfe, A. S. Jakate, V. Creutzinger and J. E. Heubi. 2003. Bioavalibility, disposition and dose-response effects of soy isoflavones when consumed by healthy women at physiologically typical dietary intake. J Nutr. 133:1027-1035.2003
Setright, R. 1993. Get well lve longer, the antioxidant connection. Spunarp Pty, Glenmore Park, Australia : p.1-21
Shuetleff, W dan Aoyogi, A. 1984. Tofu and Soymilk Production. Soyfood Center. Lafayette, California.
Stephen, A. M. 1998. Regulatory aspect of functional products. Di dalam : G. Mazza (Ed.). Functional Foods : Biochemical andd Processing Aspects. Technomic Publishing Co. Inc, Basel.
Syarief, R., dan H. Halid. 1999. Teknologi Pengemasan Pangan. Laboratorium Rekayasa Proses Pangan. PAU Pangan dan Gizi. IPB. Bogor
USDA. 1999. Iowa State University Database on the Isoflavone Content of Foods. Iowa.
Varnam, A. dan J. P. Sutherland. 1994. Milk and Milks Products. Chapman and Hall, London.
Widodo. 2003. Teknologi Proses Susu Bubuk. Lacticia Press, Yogyakarta.
Wirakartakusumah, A., A.Subarna, M.Arpah, D.Syah dan S.I.Budiwati. 1992. Peralatan dan Unit Proses Industri Pangan. PAU Pangan dan Gizi. IPB. Bogor.
Yamamoto, S. 2003. Soy, isoflavones, and breast cancer risk in Japan.. Journal of the National Cancer Institute, Vol. 95, No. 12, 906-913.
Lampiran 2. Aktivitas antioksidan sampel formulasi
µM BHA unit x BM BHA (180.24 g/mol) x 1mol/1000.000µM x 1000mg/1 g x1/ 1 ml (ekstraksi sampel awal)
Keterangan kode sampel :
Kode Volume susu
kedelai (%)
NILAI
1.000 1.000 .232 .953
SAMPEL
Means for groups in homogeneous subsets are displayed. Based on Type III Sum of Squares
The error term is Mean Square(Error) = 47.234. Uses Harmonic Mean Sample Size = 3.000. a.
Alpha = .05. b.
Lampiran 3. Analisis statistik ANOVA
aktivitas antioksidan sampel formulasi
Univariate Analysis of Variance
Between-Subjects Factors
Tests of Between-Subjects Effects
Dependent Variable: NILAI
22066.984a 7 3152.426 66.740 .000
2095034.220 1 2095034.220 44354.218 .000
259.798 2 129.899 2.750 .112
21807.186 5 4361.437 92.337 .000
472.342 10 47.234
of Squares df Mean Square F Sig.
R Squared = .979 (Adjusted R Squared = .964) a.
Post Hoc Tests SAMPEL
ULANGAN
Means for groups in homogeneous subsets are displayed. Based on Type III Sum of Squares
The error term is Mean Square(Error) = 47.234. Uses Harmonic Mean Sample Size = 6.000. a.
Alpha = .05. b.
Lampiran 4. Aktivitas antioksidan bahan/produk pangan