PENGARUH TEMPERATUR TERHADAP PENYERAPAN SO2
OLEH CHILLED WATER PADA SO
2ABSORBER UNIT
CHEMICAL PLANT PT. TOBA PULP LESTARI, Tbk –
PORSEA
KARYA ILMIAH
WYNDA YANNE OKTAVIA
112401084
PROGRAM STUDI DIPLOMA 3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGARUH TEMPERATUR TERHADAP PENYERAPAN SO2
OLEH CHILLED WATER PADA SO
2ABSORBER UNIT
CHEMICAL PLANT PT. TOBA PULP LESTARI, Tbk –
PORSEA
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat memperoleh gelar Ahli Madya.
WYNDA YANNE OKTAVIA 112401084
PROGRAM STUDI DIPLOMA 3 KIMIA DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH TEMPERATUR TERHADAP PENYERAPAN SO2 OLEH CHILLED WATER
PADA SO2 ABSORBER UNIT CHEMICAL PLANT
PT. TOBA PULP LESTARI, Tbk – PORSEA Kategori : KARYA ILMIAH
Nama : WYNDA YANNE OKTAVIA Nomor Induk Mahasiswa : 11240184
Program Studi : DIPLOMA (D3) KIMIA Departement : KIMIA
PERNYATAAN
PENGARUH TEMPERATUR TERHADAP PENYERAPAN SO2 OLEH CHILLED WATER DI SO2 ABSORBER PADA UNIT
CHEMICAL PLANT PT. TOBA PULP LESTARI, Tbk – PORSEA
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2014
PENGHARGAAN
Segala puji dan syukur penulis ucapkan kehadirat Tuhan yang Maha Esa, atas rahmat dan cinta kasih-Nya yang telah dilimpahkan-Nya kepada kita semua, sehingga penulis dapat melaksanakan dan menyelesaikan Karya Ilmiah ini dengan judul PENGARUH TEMPERATUR TERHADAP PENYERAPAN SO2 OLEH CHILLED WATER DI SO2 ABSORBER PADA UNIT CHEMICAL PLANT PT.
TOBA PULP LESTARI, Tbk – PORSEAsesuai dengan waktu yang telah
ditentukan.
Karya ilmiah ini merupakan hasil kerja praktek di PT. TOBA PULP LESTARI, Tbk PORSEA. Karya Ilmiah ini merupakan salah satu persyaratan akademik mahasiswa untuk menyelesaikan pendidikan Diploma – 3 untuk program studi Kimia Industri diFakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Penulis juga menyadari banyak kekurangan dari Karya Ilmiah ini, maka dengan kerendahan hati penulis mengharapkan saran dan kritik yang sifatnya membangun dari berbagai pihak demi penyempurnaan Karya Ilmiah ini.
Penulis juga menyadari Karya Ilmiah ini tersusun dan terselesaikan dengan baik karena ada campur tangan dari berbagai pihak yang mendukung penulis dalam meyelesaikan Karya Ilmiah ini, oleh karena itu penulis mengucapkan terimakasi kepada :
1. Kedua orang tua tercinta dan adik-adik sayayang mendukung dan memotivasi penulis dalam menyelesaikan menyelesaikan Karya Ilmiah ini.
2. Ibu Dr. Yugia Muis, MSiselaku dosen pembimbing dan dosen penasehat akademik, Ibu Dr. Rumondang Bulan Nasution, MS selaku ketua Departement Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, dan Ibu Dra. Emma Zaidar, M.Si selaku ketua Program Study D-3 Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara yang banyak mengarahkan dan membantu penulis dalam menyelesaikan Karya Ilmiah ini.
3. Bapak selaku pembimbing lapangan dan keluarga besar departement chemical plantPT. Toba Pulp Lestari, Tbk yang telah banyak memberikan sumbangan, pikiran, tenaga, dan waktu kepada penulis sewaktu penulis melaksanakan Praktek Kerja Lapangan.
4. Bapak Selaku Learning & Dev. Centre Section Head, para staff di L&D Centre ( Ibu Yanthi Sormin, Bapak Derusman Purba ), dan bapak Jhonny Marpaung selaku staff di LP&C yang telah memberikan kesempatan kepada penulis untuk mengikuti Praktek Kerja Lapangan di PT. Toba Pulp Lestari, Tbk Parmaksian.
5. Kepada sahabat, Desy Hasibuan, Anneke Lumbantoruan, Selly S. Simanjuntak dan ASJ yang cantik-cantik dan sangat jabir tentunya.
Penulis menyadari bahwa tugas akhir ini masih jauh dari sempurna, karena itu segala kritik dan saran yang membangun penulis harapkan dalam sempurnanya tugas akhir ini. Sebagai akhir kata, penyusun mengharapkan semoga Tugas Akhir yang telah disusun ini dapat bermanfaat bagi kita semua khususnya bagi mahasiswa Kimia Industri di Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Medan, Juni 2014 Penullis
ABSTRAK
Telah di lakukan pengamatan di PT. Toba Pulp Lestari, Tbk – Porsea tentang pengaruh temperatur terhadap penyerapan SO2 oleh chilled water pada SO2
absorber. Pengambilan sampel di lakukan sebanyak satu jam sekali setiap harinya. Pada unit gas sulfur dioksida ini, tahap yang menentukan keberhasilan produksi baik dari segi kualitasnya maupun dari segi kuantitasnya adalah tahap penyerapan sulfur dioksida. Penyerapan SO2 pada unit ini menggunakan chilled water (air
dingin yang ditargetkan bertemperatur 8,00 – 8,70 0C). Sesuai dengan pengamatan yang dilakukan, untuk temperatur chilled water sebesar 8,70 0C maka SO2 yang
terserap sebanyak 60,76 kg. Semakin tinggi temperatur chilled water maka penyerapan gas SO2 semakin menurun dan sebaliknya. Penyerapan menggunakan
chilled water dilakukan secara tidak langsung sehingga dapat menurunkan suhu
INFLUENCE OF TEMPERATURE ON THE ABSORPTION OF SO2 BY CHILLED WATER IN SO2 ABSORBER UNIT CHEMICAL PLANT
PT. TOBA PULP LESTARI, Tbk – PORSEA
ABSRACT
Observations have been done in PT. Toba Pulp Lestari Tbk - Porsea on the effect of temperature on the absorption of SO2 by chilled water on SO2 absorber.
Sampling was done by one hour once a day. At the unit's sulfur dioxide gas, which determines the success of the stage production in terms of both quality and quantity terms is the stage of absorption of sulfur dioxide. Absorption of SO2 in
this unit uses chilled water (cold water temperature target from 8.00 to 8.70 0C). In accordance with the observations made, for the chilled water temperature by 8.70 0C then SO2 is absorbed as much as 60.76 kg. The higher the temperature of
the chilled water absorption of SO2 gas decreases and vice versa. Absorption
DAFTAR TABEL
Tabel 2.1 Tabel Perbedaan adsopsi fisika dan kimia Tabel 2.2 Pengaruh Gas SO2 Terhadap Mahasiswa 20
Tabel 4.1 Data Hasil Pengamatan di Lapangan 29 Tabel 4.2 Data Penganalisaan Gas SO2Dalam Air di Laboratorium 30
Tabel 4.3 Hasil Perhitungan SO2Yang Terserap dan SO2Yang Tidak Terserap 33
DAFTAR GAMBAR
Gambar 1. Diagram neraca bahan untuk klorin isian 17
DAFTAR ISI
BAB 2. TINJAUAN PUSTAKA 4
2.1Pembuatan Pulp 4
2.2Sulfur Dioksida (SO2) 9
2.2.1 Sifat-sifat sulfur dioksida 9 2.2.2 Kegunaan Sulfur Dioksida 9 2.2.3 Proses Pembentukan Gas Sulfur Dioksida (SO2) 11
1. Pencairan sulfur 11
2. Pembakaran Sulfur 11
3. Pendinginan pertama gas hasil pembakaran 12 4. Pendingin kedua hasil pembakaran 13 5. Penyerapan Gas Hasil Pembakaran 13 6. Penyimpanan larutan sulfur dioksida 14
2.2.4 Chilled Water 15
1. Trane chiller 15
2. Wiegand chiller 15
2.3 Absorbsi atau Penyerapan Gas 15
2.5.1. Pengertian 15
2.5.2 Neraca Massa Untuk Penyerapan SO2 di Menara Absorbsi 16
2.5 Pencemaran gas sulfur di udara 19
BAB 3. BAHAN DAN METODE 25
3.1. Alat dan Bahan 25
3.1.1. Alat 25
3.1.2. Bahan 26
3.2. Prosedur kerja 27
BAB 4. HASIL DAN PEMBAHASAN 29
4.1. Data 29
4.2. Perhitungan 30
4.3. Pembahasan 38
BAB 5. KESIMPULAN DAN SARAN 42
5.1. Kesimpulan 42
5.2. Saran 45
DAFTAR PUSTAKA
BAB I
PENDAHULUAN
1.1 Latar Belakang
Diera globalisasi ini, dengan kemajuan ilmu pengetahuan dan teknologi yang
semakin canggih kebutuhan kertas semakin bertambah. Indonesia kaya dengan
hutan yang ditumbuhi berbagai jenis kayu, memiliki prospek yang sangat cerah
untuk mendirikan industri pulp dan kertas. Pulp (bubur kertas) merupakan bahan
baku untuk pembuatan kertas yang dapat dibuat dari semua jenis kayu, baik kayu
yang berserat pendek (hardwood) maupun kayu yang berserat panjang (softwood).
Pulp dan kertas merupakan salah satu komiditi andalan yang diharapkan mampu
untuk menunjang perekonomian di Indonesia. Apalagi bahan bakunya banyak
tersedia di bumi Indonesia dan didukung dengan jumlah yang terus bertambah.
Hal inilah yang melatarbelakangi didirikannya PT. Toba Pulp Lestari
Tbk, untuk memenuhi peningkatan kebutuhan akan kertas dan rayon dalam negeri
dan di import dari berbagai negara. PT. Toba Pulp Lestari berlokasi di desa
Sosorladang Porsea, yang berproduksi secara komersial dimulai pada tahun 1989.
Dimana produksi 70% di eksport ke mancanegara, sisanya untuk kebutuhan pasar
domestik. Kapasitas produksi terpasang di pabrik adalah 240.000 ton pulp/tahun.
Bahan baku pabrik ini dihasilkan sendiri oleh Hutan Tanaman Industri (HTI) PT.
bahan baku dalam pembuatan Pulp dan pohon tersebut akan dewasa kira -kira 7-8
tahun kemudian.
Didalam Industri Pulp, chemical plant atau pabrik kimia adalah pabrik
pendukung yang memproduksi bahan kimia untuk pemutihan pulp dan untuk
cairan pemasak. Chemical plant mempunyai pabrik-pabrik yang memproduksi
berbagai jenis bahan kimia yang salah satunya adalah pabrik sulfur dioksida (SO2
-treatment).
Pengolahan gas sulfur dioksida (SO2 Treatment) adalah merupakan salah
satu bagian proses produksi di pabrik kimia yang khusus menghasilkan larutan
sulfurn dioksida (SO2 water).
Proses penyiapan gas sulfur dioksida dilakukan dalam enam tahap utama, yaitu :
1. Pencairan sulfur
2. Pembakaran sulfur
3. Pendinginan pertama gas hasil pembakaran
4. Pendinginan kedua gas hasil pembakaran
5. Penyerapan gas hasil pembakaran
6. Penyiapan larutan sulfur dioksida
Pada unit pengolahan gas sulfur dioksida, tahap yang sangat menentukan
keberhasilan produksi baik dari segi kualitasnya maupun dari segi kuantitasnya
adalah tahap penyerapan sulfur dioksida. Pada tahap ini penyerapan terjadi pada
menara penyerapan (absorber tower). Gas sulfur dioksida yang akan diserap
Gas SO2 diabsorbsi dengan air dingin yang disebut chilled water
sehingga mendapat penyerapan yang lebih tinggi dan dapat disimpan lebih lama
dalam tangki yang berisolasi sehingga tidak terlalu banyak terpengaruh
temperatur udara sekitarnya.
Tetapi kerja dari penyerapan ini tidak selamanya berjalan sempurna,
melainkan ada juga gas SO2 yang tidak terserap yang dipengaruhi oleh temperatur
media penyerapan yaitu chilled water sehingga akan mempengaruhi produk akhir
dari penyerapan.
Sehubungan dengan ditemuinya proses penyerapan yang tidak sempurna
diatas maka penulis tertarik untuk membahasnya dengan judul :
“PENGARUH TEMPERATUR TERHADAP PENYERAPAN SO2 OLEH
CHILLED WATER DI SO2 ABSORBER PADA UNIT CHEMICAL PLANT PT.
TOBA PULP LESTARI, Tbk –PORSEA”
1.2Permasalahan
Pada unit pengolahan gas sulfur dioksida, tahap yang menentukan
keberhasilan produksi adalah media penyerapnya yaitu chilled water. Karena pada
unit ini PT. Toba Pulp Lestari memakai menara penyerap sistem isian.
1.3Tujuan
a. Untuk mengetahui pengaruh temperatur chilled water terhadap penyerapan
SO2
b. Untuk mengetahui kemampuan chilled water terhadap penyerapan SO2 gas
1.4Manfaat
a. Memberikan informasi mengenai penyerapan chilled water terhadap
gas SO2
b. Mengetahui kemampuan kerja dari proses penyerapan chilled water
BAB 2
TINJAUAN PUSTAKA
2.1Pembuatan Pulp
Dalam proses pembuatan pulp ada beberapa tahap yang harus dilakukan,
antara lain sebagai berikut :
1. Penyediaan Bahan Baku
Pada dasarnya kayu yang diolah adalah Eucalyptus. Kemudian di angkut ke
areal pabrik dengan menggunakan truk-truk pengangkut kayu. Kayu yang
ditimbun diumpamakan ke wood room, gelondong-gelondong kayu tersebut
dikulit, dipotong-potong, disaring dan disimpan pada tumpukan serpihan kayu
yang disebut dengan chip.
2. Tahap penyaringan (Screening)
Tujuan dari penyaringan adalah untuk memperbaiki kualitas produksi pulp
dengan proses kimia. Dimana dengan memisahkan serpihan fine dan serpihan
yang memiliki ukuran yang lebih besar, maka chip dengan ukuran yang
diinginkan dapat diperoleh.
3. Tahap pemasakan (Digester)
Digester adalah bejana bertekanan yang didalamnya serpihan kayu dimasak
dengan sejumlah larutan kimia tertentu. Dari hasil pemasakan tersebut
dihasilkan sisa cairan pemasak yang disebut lindi hitam sehingga menjadi
molekul yang lebih kecil yang larut dalam lindi hitam maka didapat pulp yang
4. Tahap pencucian (Washing)
Pencucian ini dilakukan untuk memisahkan serat dari kotoran-kotoran yang
dapat larut dalam air dan untuk menghilangkan sisa-sisa lignin yang masih
terikut pada pulp setelah proses pemasakan dengan penambahan natrium
karbonat. Bila pencucian kurang sempurna maka akan timbul kerugian pada
proses pemutihan sehingga diperlukan bahan pemutih yang besar jumlahnya
dan selain itu timbulnya busa serta lendir yang sangat mengganggu pada proses
pembuatan pulp.
5. Tahap pemutihan (Bleaching)
Bleaching merupakan suatu perlakuan dengan proses kimia terhadap pulp
untuk menghilangkan bahan atau zat pewarna sehingga pulp tersebut memiliki
Brightness yang lebih tinggi. Beberapa tahap pembuatan pulp menjadi putih
dengan bantuan bahan kimia yaitu : Cl2 (Klorin), ClO2 (Klorin Dioksida),
NaOH (Caustic Soda), NaClO (Natrium Hypo Clorit), O2 (Oksigen), SO2
(Sulfur Dioksida), Klor akan bereaksi dengan lignin yang terlarut dalam cairan
lindi hitam yang masuk bersama pulp, dan klor melarutkan sisa-sisa lignin
sehingga didapat pulp yang lebih putih.
6. Tahap pulping (Pulp Machine)
Pulp machine adalah merupakan integrasi dari bagian operasi pabrik pulp. Pulp
machine ini bertujuan untuk mengubah suspensi pulp yang dikirim dari Bleach
pulp menjadi pulp kering dan selanjutnya diproses ke dalam bentuk bal-bal
2.2Sulfur Dioksida (SO2)
2.2.1. Sifat-sifat sulfur dioksida
Sulfur dioksida mempunyai panas pembentukan standar (25 0C) = - 70,86
kkal/grmol. Pada tekanan standar, SO2 murni berupa gas yang tidak berwarna.
Pada prinsipnya, untuk memproduksi SO2 adalah membakar sulfur dengan
oksigen pada temperatur di atas titik didihnya. Konsentrasi gas SO2 yang
dihasilkan tergantung dari temperatur pembakarannya. Semakin tinggi temperatur
pembakaran konsentrasi gas SO2 semakin tinggi. Biasanya sulfur dioksida yang
dihasilkan berbentuk larutan yang diperoleh dengan mengabsorbsi SO2.
Sulfur dioksida adalah senyawa oksida sulfur yang memiliki sifat-sifat
sebagai berikut :
Sulfur dioksida mempunyai unsur-unsur gas baunya tajam. Apabila gas sulfur
dioksida langsung kena pada kulit maka kulit bisa terbakar, sulfur dioksida sangat
membahayakan bagi manusia dan dapat menyebabkan besi-besi berkarat.
(Anonim, 2003)
2.2.2 Kegunaan Sulfur Dioksida
Kegunaan gas sulfur dioksida adalah untuk menetralisir keaktifan dari
Penetralisirannya dilakukan dengan mengubah khlorin aktif menjadi ion khlorin
yang tidak aktif.
Pemakaian dari larutan sulfur dioksida ada pada bagian internal chemical
plant (pabrik kimia0 yaitu proses akhir dechlorination tank. Anolyte (sisa-sisa
larutan garam dari sel) yang berupa natrium hipoklorit (NaOCl) setelah
dielektrolisa yang mengandung 200-225 gr/l NaCl yang masih dapat digunakan
untuk menaikkan konsentrasinya di bak pelarut. Karena larutan sisa tersebut
masih mengandung klorin yang dapat merusak resin pada alat Ion Exchanger,
maka larutan anolyte tersebut harus mengalami pemisahan klorin terlebih dahulu.
Kemudian larutan anolyte tersebutdialirkan ke dalam sebuah tangki yamh
diinjeksikan ke dalmmya steam dan larutan HCl pada pH 1,4-1,6. Adapun fungsi
penambahan tersebut adalah untuk menghidrolisa anolyte dengan reaksi sebagai
berikut :
2 NaOCl + 2 HCl NaCl +NaOCl + Cl2 + H2O
Untuk memastikan dan menyempurnakan reaksi pembebasan klorin pada
anolyte tersebut adalah merupakan hasil dari SO2-plant. Sehingga menghasilkan
reaksi sebagai berikut :
2 NaOCl + SO2 Na2SO4 + Cl2
Dari reaksi tersebut di atas dapat diketahui bahwa sulfur yang terdapat pada
larutan garam selain berasal dari pembentukan garam juga merupakan hasil
oksidasi SO2.
Sedangkan untuk bagian eksternal digunakan pada bleaching plant, zat
pemutih yang ditambahkan pada tahap terakhir proses pemutihan adalah sulfur
menhilangkan dan memutihkan lignin yang masih tersisa dari proses sebelumnya.
Untuk menghentikan kerja dari bahan ClO2, mula-mula diuapkan dan dilarutkan
ke dalam air kemudian ditambahkan ke pabrik pengelatangan sebagai larutan cair
yang encer.
Penambahan sulfur dioksida memegang peranan penting dalam proses
pemutihan pulp dimana sulfur dioksida berfungsi untuk menetralkan ClO2 atau
sisa residu dan mengoksidasi lignin serta menaikkan brightness sehingga
mengurangi pengembalikan warna dari pulp.
2.2.3 Proses Pembentukan Gas Sulfur Dioksida (SO2)
Proses pembentukan gas sulfur dioksida berlangsung dalam 6 tahap utama,
yaitu :
1. Pencairan sulfur
a. Aliran Proses
Sulfur yang berbentuk padat sebanyak 750 kg/hari diumpankan ke tangki
pencairan (melting tank). Temperatur melting tank dijaga pada suhu8
120-130 0C, dengan media pemanas steam bertekanan rendah hal ini dilakukan
mengingat titik lebur sebesar 115,2 0C. Karenanya sulfur pada meltibg tank
tetap dalam keadaan cair dan siap untuk diumpankan ke tangki pembakaran
(furnance). Agar temperatur sulfur tidak mengalami penurunan selama
proses pengumpanan, pada jalur perpipaan dari “melting tank” hingga ke
furnance digunakan jenis pipa “doube pipe” dengan media pemanas steam
bertekanan rendah.
b. Spesifikasi Peralatan
Berat : 1800 kg
Diameter : 1,2 m
Panjang : 3,0 m
Volume : 3,4 m3
Bahan pengisolasi : Rockwool
Ketebalan isolasi : 80 mm
2. Pembakaran Sulfur
a. Aliran Proses
Sulfur yang berfasa cair dikontakkan dengan oksigen dari udara
pembakaran.Untuk meningkatkan kesempurnaan proses pembakaran, sulfur
diumpamakan dengan cara pengabutan (atominasi) dengan bantuan steam.
Hal ini disebabkan dalam keadaan mengkabut, sulfur lebih mudah terbakar
sehingga hasil gas sulfur dioksida lebih mudah sempurna terbentuk.
c. Spesifikasi Peralatan
Nama : Furnance
Berat : 1750 kg
Diameter : 1,5 m
Panjang : 3,3, m
Bahan pengisolasi : Rockwood
Ketebalan isolasi : 25 mm
3. Pendinginan pertama gas hasil pembakaran
a.Aliran proses
Gas hasil pembakaran yang terdiri dari SO2, O2, N2 dan zat-zat impurities
pendingin “mill water” hingga temperatur menurun menjadi 70-75 0C.
Pada lata ini media pendingin dikontakkan secara berlawanan arah
(counter flow) dan untuk meningkatkan transfer panas dilakukan dengan
mensirkulasikan kembali media pendingin mill water ke menara
pendingin.
Kelarutan gas sulfur dioksida dalam mill water pada menara pendingin
sulit untuk dicapai, hal ini disebabkan temperatur operasi yang tidak
memungkinkan untuk melarutkan gas sulfur dioksida.
b.Spesifikasi Peralatan
Nama : SO2gas cooling water
Berat : 500 kg
Diameter : 1,03 m
Tinggi : 6,30 m
4. Pendingin kedua hasil pembakaran
a. Aliran proses
Sistem pendingin dilakukan dengan menggunakan “heat exchanger” jenis
shell and tube. Media pendingin yang diumpamakan secara berlawanan
arah. Maka temperatur akhir gas hasil pendinginan menurun menjadi 15-20
Kondisi di SO2 absorber yaitu :
Konsentrasi SO2 solution : 20 gpl
Tekanan supplay SO2 : 3,4 bar
Temperatur Chilled Water : 8 0C
Flow Chilled Water : 6,2 m3/jam
5. Penyerapan Gas Hasil Pembakaran
a. Aliran Proses
Gas hasil pembakaran setelah melalui pendinginan tahap kedua dengan
temperatur 15-20 0C diumpamakan dari dasar menara absorbsi, sementara
counter flow media penyerap chilled water dialirkan dari puncak menara
dengan sistem semburan (spray). Untuk memperpanjang waktu kontak
antara gas dengan media penyerap, menara absorbsi dilengkapi dengan isian
jenis shuddle packing. Gas SO2 hasil pembakaran akan terserap sementara
gas-gas yang lain seperti O2 sisa, SO2 yang tidak terserap, N2 dan impurities
lainnya akan terbang ke atmosfer melalui cerobong menara. Produk yang
dihasilkan dari proses penyerapan adalah dalam bentuk sulfur dioksida (SO2
water) dengan temperatur akhir 10-15 0C.
b.Spesifikasi Peralatan
Nama : SO2gas absorbation tower
Berat : 260 kg
Diameter : 0,5 m
Tinggi : 9,1 m
6. Penyimpanan larutan sulfur dioksida
Larutan SO2 dengan temperatur sekitar 100C dialirkan ke tangki
penyimpanan. Temperatur fluida dijaga pada 10 0C, hal ini disebabkan pada
temperatur 20 0C gas sulfur dioksida akan memisah dengan air. Untuk
menjaga kondisi variabel operasi tersebut, padat tangki dilengkapi dengan
pengisolasi, sehingga efek transfer panas dapat dicegah.
bSpesifikasi Peralatan
digunakan untuk mengabsorbsi sulfur dioksida dan proses pendinginan pada
alat-alat pendingin tertentu.
Chilled water terdiri dari dua jenis, yaitu :
1. Trane chiller
Yang beroperasi berdasarkan beda tekanan yang menyebabkan pendingin
mengakami penurunan temperatur dan mengambil panas dari air byang hendak
didinginkan.
2. Wiegand chiller
Yang beroperasi juga berdasarkan titik didih yang rendah pada tekanan yang
rendah dengan mengambil panas dari air itu sendiri.
Sistem Chilled water yaitu :
Temperatur Chilled water : 8 – 10 0C
Pemakaian Colling water 270C : 470 m3/jam
Konsumsi Mill water 270C : 63 m3/jam
Total daya listrik penggerak moto : 101 Kw
(Anonim. 2002)
2.3 Absorbsi atau Penyerapan Gas
2.3.1. Pengertian
Menurut Warren L.Mc.Cabe, absorbsi adalah peristiwa terserapnya suatu zat
(absorbat) oleh zat lain (absorbent). Absorbsi merupakan salah satu cara untuk
memisahkan atau mengurangi kadar suatu konstituen dalam fase gas dengan
menggunakan solvent penyerap tertentu secara selektif yang dapat melarutkan
atau menyerap konstituen yang diinginkan. Solvent penyerap harus dipilih secara
tepat baik ditinjau dari sifat-sifat fisik, kimia ataupun harga dan batas-batas
pemakaiannya.
Operasi penyerapan gas yang dijalankan dengan cara mengontakkan campuran
gas dengan cairan tertentu, dengan tujuan salah satu atau beberapa dari komponen
yang terdapat gas tersebut terserap oleh cairan. Pada umumnya, proses
penyerapan dilakukan dalam menara penyerap (absorber) baik yang tersusun dari
sejumlah tray (tray tower) maupun yang berisi sejumlah bahan isian pada
ketinggian tertentu (packed tower).
Absorbsi termasuk pemisahan menurut dasar operasi difusional dimana transfer
massa berlangsung dengan cara difusi antar dua fase yang saling mengadakan
kontak.
a. Memurnikan gas
b. Menghilangkan komponen zat yang berbahaya dan yang tidak diinginkan
c. Mengumpulkan komponen yang berharga
d. Pembentukan persenyawaan kimia dari suatu bahan penyerap dengan suatu
komponen tertentu dari campurannya.
Berdasarkan sifatnya maka peristiwa absorbsi digolongkan dalam dua bagian,
yaitu :
a. Absorbsi fisis
Absorbsi fisis adalah operasi penyerapan suatu zat dengan menggunakan pelarut
(solvent) dan penyerapan berlangsung semata-mata karena pelarutan zat terlarut
(solute) dalam pelarut.
b. Absorbsi kimiawi
Absorbsi kimiawi adalah operasi penyerapan suatu zat dengan pelarut, dimana
peristiwa penyerapan terjadi untuk membentuk suatu zat.
2.3.2. Neraca Massa Untuk Penyerapan SO2 di Menara Absorbsi
Untuk menghitung jumlah perolehan dari larutan hasil absorbsi atau larutan
produk dapat dilakukan dengan metode neraca pada bahan absorbsi.
Menurut Warren L.Mc.Cabe, gas yang mengandung zat terlarut disebut gas
kaya atau gas gemuk (rich gas), masuk ke ruang pendistribusian yang terdapat
dibawah isisan dan mengalir ke atas melalui celah-celah antara isian, berlawanan
arah dengan aliran zat cair. Isian itu memberikan permukaan yang luas untuk
kontak antara zat cair dan gas dan membantu terjadinya kontak yang akrab anatara
kedua fase. Zat terlarut yang ada dalam gas diserap oleh zat cair segar yang masuk
zat pekat antara cairan kuat yang terjadi keluar dari bawah menara absorber
mealalui lubang yang ada dibawah menara. Untuk lebih jelasnya dapat dilihat
pada gambar dibawah ini.
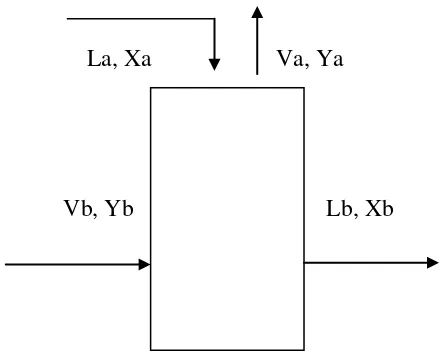
La, Xa Va, Ya
Vb, Yb Lb, Xb
Gambar 1. Diagram neraca bahan untuk klorin isian
Keterangan :
La = laju larutan masuk ke dalam menara
Xa = konsentrasi atau komposisi larutan masuk
Lb = laju larutan produk keluar
Xb = konsentrasi larutan keluar
Va = laju gas keluar
Ya = konsentrasi atau kadar gas keluar
Yb = konsentrasi atau kadar gas masuk
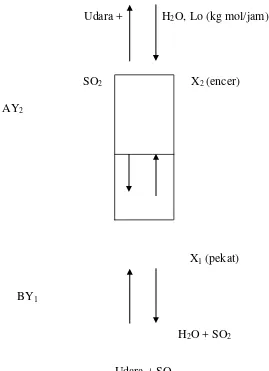
Udara + H2O, Lo (kg mol/jam)
SO2 X2 (encer)
AY2
X1 (pekat)
BY1
H2O + SO2
Udara + SO2
Gambar 2. Diagram proses penyerapan gas SO2 dengan air
X = SO2/H2O (perbandingan mol)
Y = SO2/udara (perbandingan mol)
G = laju udara
Neraca bahan untuk SO2 bila operasinya kontiniu dan keadaan steady
state tercapai adalah :
SO2 keluar = GoY2 + LoX1
Neraca bahannya adalah SO2 masuk sama dengan SO2 keluar yaitu :
GoY1 + LoX2 = GoY2 + LoX1
Go (Y2-Y1) = Lo (X1-X2)
Atau Y2-Y1 = (Lo/Go) (X1-X2)
(Warren L. Mc Cabe, julian C. Smith dkk. 1993)
2.4 Pengertian Adsorpsi menurut Sukardjo
a. Pengertian Adsorpsi
Adsorpsi merupakan suatu proses kimia ataupun fisika yang terjadi ketika suatu
fluida, cairan maupun gas , terikat kepada suatu padatan atau cairan (disebut: zat
penjerap, adsorben) dan akhirnya membentuk suatu lapisan film (disebut: zat
terjerap, adsorbat) pada permukaannya. Berbeda dengan absorpsi yang merupakan
penyerapan fluida oleh fluida lainnya dengan membentuk suatu larutan.
Dengan demikian dapat disimpulkan:
Adsorpsi --> peristiwa penyerapan suatu zat pada permukaan zat lain
Adsorbat à senyawa terlarut yang dapat terserap
Adsorben àpadatan dimana di permukaannya terjadi pengumpulan senyawa yang
diserap
Dalam pengertian lain menyatakan adsorpsi merupakan suatu peristiwa
penyerapan pada lapisan permukaan atau antar fasa, dimana molekul dari suatu
Selain zat padat, adsorben dapat pula zat cair. Karena itu adsorpsi dapat terjadi
Menurut Sukardjo bahwa molekul-molekul pada permukaan zat padat atau zat
cair, mempunyai gaya tarik ke arah dalam, karena tidak ada gaya-gaya yang
mengimbangi. Adanya gaya-gaya ini menyebabkan zat padat dan zat cair,
mempunyai gaya adsorpsi. Adsorpsi berbeda dengan absorpsi. Pada absorpsi zat
yang diserap masuk ke dalam adsorben sedang pada adsorpsi, zat yang diserap
hanya pada permukaan.
Jumlah zat yang diadsorpsi pada permukaan adsorben merupakan proses
berkesetimbangan, sebab laju adsorpsi disertai dengan terjadinya desorpsi. Pada
awal reaksi, peristiwa adsorpsi lebih dominan dibandingkan dengan peristiwa
desorpsi, sehingga adsorpsi berlangsung cepat. Pada waktu tertentu peristiwa
adsorpsi cenderung berlangsung lambat, dan sebaliknya laju desorpsi cenderung
meningkat. Ketika laju adsorpsi adalah sama dengan laju desorpsi sering disebut
sebagai keadaan berkesetimbangan. Waktu tercapainya keadaan setimbang pada
proses adsorpsi adalah berbeda-beda. Hal ini dipengaruhi oleh jenis interaksi yang
terjadi antara adsorben dengan adsorbat. Secara umum waktu tercapainya
kesetimbangan adsorpsi melalui mekanisme fisika (fisisorpsi) lebih cepat
dibandingkan dengan melalui mekanisme kimia atau kemisorpsi
Berdasarkan proses terjadinya ada dua jenis adsorbsi, yaitu Adsorbsi kimia dan
adsorbsi fisika. Berikut masing- masing penjelasannya.
1. adsorpsi fisika (Physisorption)
interaksi yang terjadi antara dasorben dan adsorbat adalah gaya Van der
Walls dimana ketika gaya tarik molekul antara larutan dan permukaan
media lebih besar daripada gaya tarik substansi terlarut dan larutan, maka
substansi terlarut akan diadsorpsi oleh permukaan media. Adsorbsi
fisika ini memiliki gaya tarik Van der Walls yang kekuatannya relatif
kecil. Molekul terikat sangat lemah dan energi yang dilepaskan pada
adsorpsi fisika relatif rendah sekitar 20 kJ/mol.
Contoh :
Adsorpsi oleh karbon aktif. Karbon aktif merupakan senyawa karbon
yang diaktifkan dengan cara membuat pori pada struktur karbon
tersebut. Aktivasi karbon aktif pada temperatur yang tinggi akan
menghasilkan struktur berpori dan luas permukaan adsorpsi yang besar.
Semakin besar luas permukaan, maka semakin banyak substansi terlarut
yang melekat pada permukaan media adsorpsi.
2. adsorpsi kimia (Chemisorption)
Chemisorption terjadi ketika terbentuknya ikatan kimia (bukan ikatan van
Dar Wallis) antarasenyawa terlarut dalam larutan dengan molekul dalam
media. Chemisorpsi terjadi diawali dengan adsorpsi fisik, yaitu partikel
adsorbat tertarik ke permukaan adsorben melalui gaya Van der Walls
atau bisa melalui ikatan hidrogen. Dalam Chemisorbption partikel melekat
kovalen), dan cenderung mencari tempat yang memaksimumkan bilangan
koordinasi dengan substrat.
Contoh : Ion exchange.
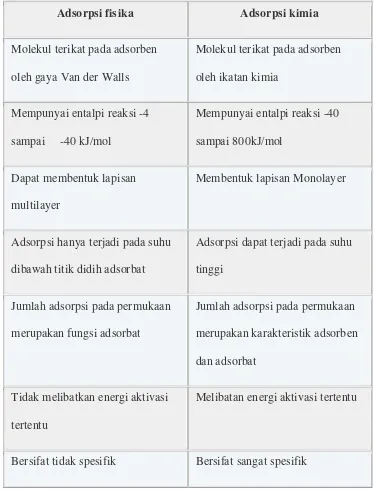
Tabel 2.1 Perbedaan adsorpsi fisika dan kimia
Adsorpsi fisika Adsorpsi kimia
Molekul terikat pada adsorben
oleh gaya Van der Walls
Molekul terikat pada adsorben
Adsorpsi hanya terjadi pada suhu
dibawah titik didih adsorbat
Adsorpsi dapat terjadi pada suhu
tinggi
Bersifat tidak spesifik Bersifat sangat spesifik
2.5 Pencemaran gas sulfur di udara
Udara adalah suatu kesatuan ruangan, dimana makhluk hidup berada di
dalamnya. Udara atmosfer merupakan campuran gas yang terdiri dari sekitar 78%
Nitrogen, 20% oksigen, 0,93% Argon, 0,03% Karbon monoksida dan sisanya
terdiri dari Neon, Helium, Metan dan Hidrogen. Udara dikatakan “normal “ dan
dapat mendukung kehidupan manusia, apabila komposisinya seperti tersebut
diatas. Sedangkan apabila terjadi penambahan gas lain, apalagi yang
menimbulkan gangguan serta perubahan dari komposisi, maka dikatakan udara
sudah tercemar. Pencemaran udara adalah adanya atau masuknya salah satu atau
lebih zat pencemar di udara, dalam jumlah dan waktu tertentu, yang dapat
menimbulkan gangguan pada manusia, hewan, tumbuhan, dan benda-benda
lainnya. (Undang-undang no 4 tahun 1982 tentang pokok-pokok pengelolaan
lingkungan hidup).
Secara umum terdapat 8 parameter pencemar udara yaitu, debu, NH3, Pb,
CO, SO2, hidrokarbon, NOX, dan H2S, yang secara bersamaan maupun
sendiri-sendiri memiliki potensi bahaya bagi lingkungan, yang meliputi dampak bagi
kesehatan masyarakat, hewan, tanaman maupun bagi material (benda) seperti
bangunan, logam dll.
Gas SO2 (sulfur dioksida), merupakan gas polutan yang banyak dihasilkan
dari pembakaran bahan bakar fosil yang mengandung unsur belerang seperti
minyak, gas, batubara, maupun kokas. Disamping SO2, pembakaran ini juga
menghasilkan gas SO3, yang secara bersama-sama dengan gas SO2 lebih dikenal
sebagai gas SOx (sulfur oksida). Akibat utama pencemaran gas sulfur oksida,
pernapasan. Beberapa penelitian menunjukkan bahwa iritasi tenggorokan terjadi
pada konsentrasi SO2 sebesar 5 ppm atau lebih. Bahkan pada beberapa individu
yang sensitive, iritasi sudah terjadi pada paparan 1-2 ppm saja. Untuk penderita
yang mempunyai penyakit kronis pada system pernapasan dan kardiovaskular
dan lanjut usia gas ini merupakan polutan yang berbahaya karena dengan
paparan yang rendah saja ( 0,2 ppm) sudah dapat menyebabkan iritasi
tenggorokan. Lebih lengkap, pada Table 1 ditunjukkan pengaruh SO2 dalam
berbagai kadar (ppm) terhadap kesehatan manusia.
Tabel 2.2 : Pengaruh Gas SO2 Terhadap Manusia
Kadar
20 - Jumlah minimum yang mengakibatkan
iritasi pada mata
- Dapat menyebabkan batuk
- Jumlah maksimum yang diperbolehkan
untuk paparan yang lama
50
-100
- Jumlah maksimum yang dibolehkan untuk
paparan yang singkat ( + 30 menit)
500 Paparan yang singkat
BAB 3
BAHAN DAN METODOLOGI
3.1 Peralatan dan bahan
3.1.1 Alat-alat yang digunakan
a. Di lapangan
1) Sulfur Melting Tank (tangki pencairan sulfur)
Sulfur yang berbentuk padatan sebelum mengalami proses pembakaran
terlebih dahulu dicairkan pada alat ini, dengan menjaga temperatur pada
120-130 oC. Sulfur mencair pada temperatur 114,5 oC dan akan mendidih
pada temperatur 445 oC. Sebagai media pemanas menggunakan steam
bertekanan rendah.
2) Sulfur Pump (pompa sulfur cair)
Yaitu alat untuk mengalirkan cairan sulfur guna diumpankan ke dalam
tungku pembakaran sulfur.
3) Air Blower (penghembusan udara)
Alat ini berfungsi untuk mengalirkan udara pembakaran ke dalam tungku
pembakaran sulfur.
4) Sulfur Furnance (tungku pembakaran sulfur)
Yaitu alat yang berfungsi sebagai tempat terjadinya proses pembakaran
dikontakkan dengan udara pembakaran sehingga menghasilkan gas sulfur
dioksida. Dimana temperatur pembakaran dijaga 700-800 oC.
5) SO2 Gas Cooling Tower (menara pendingin gas SO2)
Gas hasil pembakaran dikirim ke alat ini untuk mengalami pendinginan
pertama dengan media pendingin air, sehingga temperatur turun menjadi
100-75 oC.
6) SO2 Gas Cooler (pendingin gas SO2)
Gas sulfur dioksida yang keluar dari cooli8ng tower selanjutnya
didinginkan dengan alat pendingin, sehingga temperatur gas turun menjadi
15-20 oC.
7) SO2 Absorbtion Tower (median penyerapan gas SO2)
Yaitu sebuah menara penyerap gas sulfur dioksida dengan media penyerap
adalah chilled water, dengan jenis isian “saddle packing”.
8) SO2 Water Storage Tank (tangki penyimpanan larutan SO2)
Larutan SO2 yang merupakan hasil penyerapan di simpan dalam alat ini,
dan siap untuk didistribusikan.
b. Di laboratorium
1. Digital buret
2. Erlenmeyer
3.1.2 Bahan-bahan yang digunakan
a. Di lapangan
1) Sulfur (belerang)
2) Oksigen dari udara pembakaran
b. Di laboratorium
1) SO2 Water
2) Larutan Iodium 0,1 N
3) Larutan Indikator
4) Larutan Natrium Tiosulfat 0,1 N
3.2 prosedur
3.2.1 Di lapangan
Proses pembuatan SO2 di SO2 plant
Dicairkan Sulfur (S) yang dalam bentuk padatan pada alat Sulfur Melting tank (tangki pencairan sulfur) , sebagai media pemanasnya digunakan steam bertekanan rendah.
Dijaga temperatur pada Sulfur Melting Tank(Tangki Pencairan Sulfur) yaitu 130-135 0C, jika digunakan suhu 1450C maka sulfur akan membeku kembali.
Di alirkan sulfur cair dengan bantuan pompa sulfur cair ke tungku pembakaran sulfur (sulfur burner).
Temperatur pembakaran pada sulfur burner dijaga 780 – 805 0C. Didinginkan gas hasil pembakaran di Cooling Tower dengan media pendingin air secara kontak langsung sehingga temperatur gas turun menjadi 75-100 0C.
Didinginkan gas sulfur dioksida yang keluar dari cooling tower dengan menggunakan alat pendingin atau disebut Cooler, sehingga temperatur gas turun menjadi 15- 200 C.
Diserap gas Sulfur dioksida dengan menggunakan menara penyerap (Absorbtion Tower) dengan media penyerap air dimana jenis isian
pada menara penjerap adalah “Saddle Packing”.
Dialirkan larutan SO2 yang terbentuk dari hasil penyerap untuk
3.2.2 Di laboratorium
Prosedur kerja untuk memproleh kadar SO2 adalah sebagai berikut :
a. Dipipet sampel sebanyak 2 ml, dimasukkan ke dalam erlenmeyer
b. Ditambahkan larutan iodium 0,1 N sebanyak 10 ml
c. Kemudian ditambahkan beberapa tetes indikator amilum
d. Lalu dititrasi dengan larutan Natrium Tiosulfat 0,1 N, dicatat volume
(ml) yang dipakai sebagai sebagai A.
Kadar SO2 yang diperoleh :
SO2 =
Dimana :
A = Volume larutan Natrium Tiosulfat
B = Volume sampel
N1 = Normalitas I2
BAB 4
HASIL DAN PEMBAHASAN
4. 1 Hasil
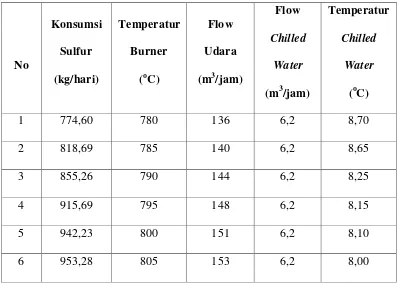
Data-data hasil kerja praktek diambil sekali dalam 24 jam. Data-data tersebut
dibutuhkan untuk pembahasan masalah yang terdapat dilapangan tempat kerta
praktek.
Tabel 4.1. Data Hasil Pengamatan di Lapangan
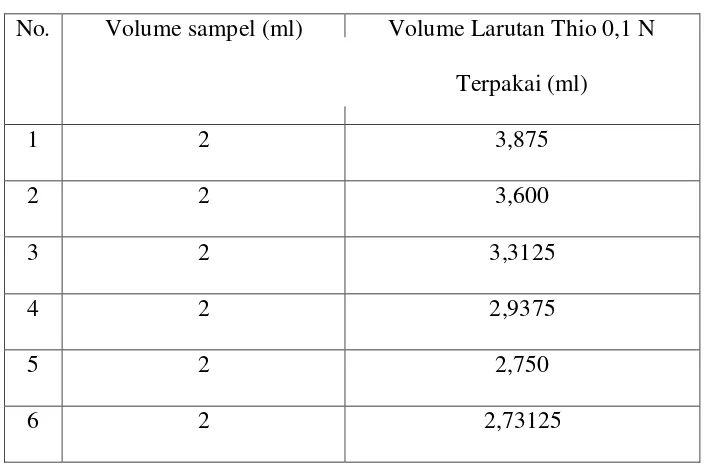
Tabel 4.2. Data penganalisaan Gas SO2 dalam air di Laboratorium
No. Volume sampel (ml) Volume Larutan Thio 0,1 N
Terpakai (ml)
1 2 3,875
2 2 3,600
3 2 3,3125
4 2 2,9375
5 2 2,750
6 2 2,73125
4. 2 Perhitungan
1. Menghitung berat sulfur yang diumpankan
Pemakaian sulfur sebanyak 774,60 kg/hari, maka untuk 1 jam operasi yang
digunakan adalah
S =
= 32,2750 kg/jam
2. Menghitung berat SO2 yang terbentuk :
S + O2 SO2
Mol SO2 = Mol O2 = Mol
= 1,0065 kmol/jam
Berat SO2 yang terbentuk = kmol x BM
= 1,0065 kmol/jam x 64,0628 kg/kmol
= 64,4792 kg/jam
3. Menghitung konsentrasi SO2 dalam air
Melalui penganalisaan di dapat data sebagai berikut :
( A ) Volume larutan Thio = 3,875 ml
( B ) Volume sampel = 2 ml
( N1 ) Normalitas I2 = 0,1 N
( N2 ) Normalitas Thio = 0,1 N
= 9,8 gr/l
4. Menghitung produk SO2 dalam air (SO2 yang terserap)
- Konsentrasi SO2 dalam air : 9,80 gr/l
- Flow Chilled Water : 6,2 m3/jam
Menghilangkan produk SO2 dalam air, dapat memakai rumus sebagai berikut :
SO2 produk (kg/jam) = Flow Chilled Water (m3/ jam) x konsentrasi SO2
dalam air (gr/l)
= 6,2 m3/jam x 1000 ltr/m3 x 9,80 gr/l x 1 kg/ 1000gr
= 60,7600 kg/jam
Maka berat SO2 yang terserap = 60,7600 kg/jam
5. Menghitung SO2 yang tidak terserap (terbuang)
- SO2 yang terserap = 60,7600 kg
Maka SO2 yang tidak terserap :
SO2 yang tidak terserap = SO2 yang terbentuk - SO2 yang terserap
= 64,4792 kg – 60,7600 kg
= 3,7192 kg
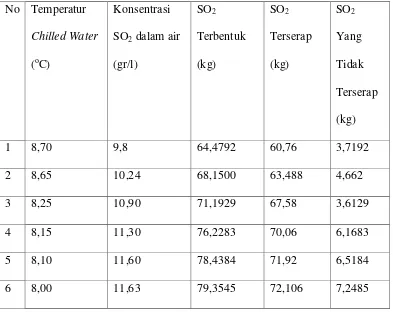
Tabel 4.3 Hasil perhitungan SO2 yang terserap dan SO2 yang tidak terserap
No Temperatur
Dari data-data yang diperoleh berdasarkan hasil pengamatan dan perhitungan,
penyerapan SO2, yakni menentukan temperatur Chilled Water yang tepat agar
diperoleh penyerapan sulfur dioksida yang maksimal. Yaitu dengan
menggunakan teori statistic dengan pendekatan garis regresi menurut
persamaan :
Y = a + bx
Dimana : X adalah temperatur Chilled Water (oC) dan dimana Y adalah SO2
yang terserap.
Untuk memperoleh konstanta a dan b pada persamaan garis regresi linear dapat
dihitung dengan menggunakan rumus :
Untuk mengetahui kuat atau tidaknya hubungan antara x dan y digunakan nilai
koefisien korelasi yang mempunyai batas harga sebesar -1 sampai +1. Rumus
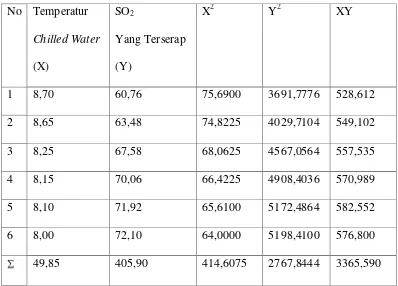
Tabel 4.4 Analisa persamaan Regresi Linear Sederhana
49,85 405,90 414,6075 2767,8444 3365,590
Keterangan :
n = Banyak percobaan
x = Jumlah temperatur Chilled Water
xy = 3365,590
Rumus analisa regresi linear sederhana :
Y = a + bx
= 196, 1955
:
b = -15,4718
Maka persamaan garis regresinya menjadi :
Y = 196,1955 – 15,4718 X
Sedangkan untuk mencari koefisien korelasi ( r ) dari persamaan regresi linier
diatas dapat dicari dengan rumus sebagai berikut :
7. Material Balance SO2 Treatment
Basis perhitungan 1 jam operasi
Flow udara pembakaran = 136 m3/jam
Kebutuhan sulfur = 32,2750 kg/jam
Flow Chilled Water = 6,2 m3/jam
n udara pembakaran = PV/RT
= 5,5587 k-mol
n O2 = (0,21) (5,5587 kmol) x BM O2
= 1,1673 k-mol x BM O2
= 1,1673 kmol x 28,8503 kg/kmol
= 37,3536 kg
n N2 = ( 0,79 ) (5,5587 kmol) x BM N2
= 4,3913 k-mol x BM N2
= 4,3913 kmol x 28,0314 kg/mol
SO2yang terbentuk = x BM SO2
= x 64,0628 kg/mol
= 64,4792 kg/jam
Secara teoritis :
O2 yang terbentuk tiap 1 jam = 32,2750 kg
Sehingga exess O2 = nO2– SO2 yang terbentuk
= 37,3536 kg – 32,2750 kg
= 5,0786 kg
N2 keluar furnace =122,9564 kg
Maka :
SO2 produk (kg/jam) = Flow Chilled Water (m3/ jam) x konsentrasi SO2
dalam air (gr/l)
= 6,2 m3/jam x 1000 ltr/m3 x 9,80 gr/l x 1 kg/ 1000gr
= 60,7600 kg/jam
SO2 yang tidak terserap = SO2 yang terbentuk - SO2 yang terserap
= 64,4792 kg – 60,7600 kg
Flow Chilled Water = 6,2 m3/ jam
= 6200 kg
Sehingga :
Material Balance pada absorption tower adalah
Masuk :
SO2 = 64,4792 kg
O2 = 3,0786 kg
N1 = 122,9564kg
H2O (Chilled Water ) = 6200kg
Total = 6392,5142 kg
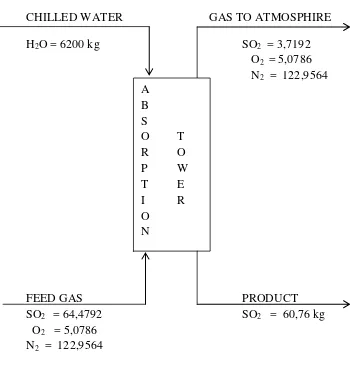
Keluar :
SO2 (yang terserap) = 60,76 kg
SO2 (yang tidak terserap) = 3,7192 kg
O2 yang tidak terserap = 5,0786 kg
N2 yang tidak terserap = 122,9564 kg
H2O (Chilled Water) = 6200 kg
Gambar Proses Penyerapan Gas SO2 di SO2 Absorber
Lestari memakai menara penyerap sistemmenara isian. Jalannya penyerapan ini
adalah dengan mengontakkan kedua fluida secara berlawanan arah di dalam
menara tersebut, dimana dalam proses ini gas SO2 dialirkan dari dasar menara
penyerap. Sedangkan media penyerapnya adalah chilled water yang dispray dari
bagian atas menara dapat memberikan hasil berupa larutan SO2 dengan
konsentrasi yang diharapkan sekitar 9 – 12 gr/l gas SO2 terserap.
Gas SO2 absorbsi dengan air dingin yang disebut chilled water sehingga
mendapat penyerapan yang lebih tinggi dan dapat disimpan lebih lama dalam
dalam tangki yang berisolasi sehingga tidak terlalu banyak terpengaruh
temperatur udara sekitarnya.
Tetapi kerja dari penyerapan ini tidak selamanya berjalan dengan sempurna,
melainkan ada gas SO2 yang tidak terserap sehingga akan mempengaruhi produk
akhir dari penyerapan.
Dan salah satu yang mempengaruhi penyerapan SO2 tersebut adalah temperatur
BAB 5
KESIMPULAN DAN SARAN
5. 1 Kesimpulan
Berdasarkan hasil kerja lapangan serta hasil pembahasan (perhitungan) yang
dilakukan maka dapat ditarik kesimpulan sebagai berikut :
1. Hubungan antara temperatur chilled water terhadap penyerapan SO2 yaitu
semakin tinggi temperatur chilled water maka penyerapan gas SO2
semakin menurun dan sebaliknya.
2. Setelah melihat perhitungan maka temperatur chilled water yang terbaik
untuk penyerapan sulfur dioksida adalah temperatur 8 oC dengan SO2 yang
terserap adalah sebesar 72,106 kg.
5. 2 Saran
Diharapkan pada proses absorbsi SO2 gas menjadi SO2 liquid sebaiknya
temperatur chilled water harus dijaga 8 -10 oC agar penyerapan SO2 lebih
tinggi dan dapat disimpan lebih lama dalam tangki yang berisolasi sehingga
DAFTAR PUSTAKA
Anonim. 2000. Chemical Plant Training Manual. Porsea. PT.Toba Palp Lestari, Tbk.
Anonim. 2002. Standart Technical Procedures. Porsea. PT.Toba Palp Lestari, Tbk.
Anonim. 2003. Chemical plant. Porsea. PT. Toba Pulp Lestari, tbk
Brine,C.J; 1984, Chitin : Accomplishment and Perspectives in Chitin, Chitosan and Related
Enzymes, Academic Press Inc, Orlando, Florida.
Kristanto P, 2002, “Ekologi Industri”, Edisi Pertama, Cetakan Pertama. Jakarta :
Erlangga.
Sukardjo. 2002. Kimia Fisika. Jakarta : Rineka Cipta