GAMBARAN HISTOPATOLOGI
DAN TAMPILAN IMUNOHISTOKIMIA FIBRONEKTIN
PADA SELAPUT KETUBAN PEREMPUAN HAMIL
YANG MENDAPAT ACETYLSALICYLIC ACID (ASA)
DOSIS RENDAH
TESIS
Oleh:
CUT MOURISA
107008005
PROGRAM STUDI MAGISTER ILMU BIOMEDIK
FAKULTAS KEDOKTERAN
GAMBARAN HISTOPATOLOGI
DAN TAMPILAN IMUNOHISTOKIMIA FIBRONEKTIN
PADA SELAPUT KETUBAN PEREMPUAN HAMIL
YANG MENDAPAT ACETYLSALICYLIC ACID (ASA)
DOSIS RENDAH
TESIS
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Magister Biomedik dalam Program Studi Magister Ilmu Biomedik pada Fakultas Kedokteran Universitas Sumatera Utara
Oleh
CUT MOURISA
107008005
PROGRAM STUDI MAGISTER ILMU BIOMEDIK
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
MEDAN
Judul Tesis : GAMBARAN HISTOPATOLOGI DAN TAMPILAN IMUNOHISTOKIMIA
FIBRONEKTIN PADA SELAPUT KETUBAN PEREMPUAN HAMIL YANG MENDAPAT
ACETYLSALICYLIC ACID (ASA) DOSIS RENDAH
Nama Mahasiswa : Cut Mourisa No Induk Mahasiswa : 107008005 Program Studi : Ilmu Biomedik
Menyetujui,
Komisi Pembimbing
Ketua
(Prof. Dr. dr. Rozaimah Zain-Hamid, MS, Sp.FK)
Anggota
(dr. Betty, M.Ked (PA), Sp.PA)
Ketua Program Studi
NIP. 19550807 198503 2 001 (dr. Yahwardiah Siregar, Ph.D)
Dekan
NIP. 19540220 198011 1 001
(Prof. dr. Gontar A Siregar, Sp.PD,KGEH)
Telah diuji pada tanggal :18 Juni 2014
__________________________________________________________________
PANITIA PENGUJI TESIS
Ketua : Prof. Dr. dr. Rozaimah Zain-Hamid, MS, Sp.FK
Anggota : 1. dr. Betty, M.Ked (PA), Sp.PA
2. dr. Makmur Sitepu, Sp.OG(K)
LEMBARAN PERSETUJUAN
Gambaran histopatologi
dan tampilan imunohistokimia fibronektin
pada selaput ketuban perempuan hamil
yang mendapat acetylsalicylic acid (ASA) dosis rendah
Oleh:
Cut Mourisa
107008005
Medan, Juni 2014
Disetujui oleh :
Pembimbing I
Prof. Dr. dr. Rozaimah Zain-Hamid, MS, Sp.FK
Pembimbing II
ABSTRAK
Acetylsalicylic acid (ASA)/aspirin adalah obat yang banyak digunakan dengan berbagai khasiat, diantaranya sebagai antitrombotik (pada dosis rendah yaitu 80-325mg) dengan indikasi pada penatalaksanaan strok, infark miokard, trombosis, sindrom antiphospholipid dan pencegahan pre-eklamsia dan eklamsia selama kehamilan. Pemberian ASA jangka panjang pada perempuan hamil menyebabkan keadaan defisiensi vitamin C melalui mekanisme hambatan absorpsi, transpor, peningkatan ekskresi vitamin C, sehingga mengganggu sintesa protein (kolagen, fibronektin) pada matriks ekstraseluler (MES) selaput ketuban. Penelitian ini bertujuan untuk mengetahui perubahan gambaran struktur histopatologi (ketebalan lapisan amnion-korion) dan tampilan imunohistokimia fibronektin pada selaput ketuban perempuan hamil yang mendapat ASA dosis rendah. Jenis penelitian ini adalah cross sectional dengan menggunakan 81 subjek yang dipilih dengan teknik consecutive sampling. Sebanyak 27 subjek (kelompok kasus) mendapat ASA dosis rendah dan 54 subjek (kelompok kontrol) tanpa ASA
dosis rendah. Pada saat persalinan dilakukan pengambilan selaput ketuban untuk diperiksa. Hasil penelitian menunjukkan selaput ketuban pada kelompok kasus (85,18±15,98) lebih tipis dibandingkan kelompok kontrol (111,68±27,19) (p<0,05). Tampilan imunohistokimia fibronektin pada kelompok kasus (1,85±0,53) lebih lemah dibandingkan kelompok kontrol (2,49±0,63) (p<0,05). Pemberian ASA dosis rendah jangka panjang pada perempuan hamil terbukti menurunkan ketebalan selaput ketuban dan tampilan imunohitokimia fibronektin pada selaput ketuban.
ABSTRACT
Acetylsalicylic acid (ASA)/aspirin, a drug that is widely used, has a variety of properties. One such property permits an antithrombotic use (at low doses are 80-325 mg) indicating treatment of stroke, myocardial infarction, thrombosis, antiphospholipid syndrome and prevention of pre-eclampsia and eclampsia during pregnancy. Long-term use of ASA during pregnancy causes vitamin C deficiency via a mechanism of disturbance absorption, distribution and increased excretion of vitamin C, thereby disrupting the synthesis of proteins (collagen, fibronectin) in the extracellular matrix (ECM) of fetal membranes. This study aims to determine histopathological changes in the structural overview (amnion-chorion layer thickness) and immunohistochemical appearance of fibronectin on the fetal membranes of pregnant women who receive low-dose ASA. This study follows a cross sectional design with 81 subjects selected using a consecutive sampling technique. A total of 27 subjects (cases) received low-dose ASA and 54 subjects (control group) without low-dose ASA. The fetal membranes were collected at experiment end as per results delivery and next were to be examined. The results showed that the fetal membranes in the case group (85.18 ± 15.98) were thinner than the control group (111.68 ± 27.19) (p <0.05). Further, the immunohisto-chemical appearance of fibronectin in the case group (1.85 ± 0.53) was weaker than the control group (2.49 ± 0.63) (p <0.05). The provision of long-term low-dose ASA in pregnant women was shown to decrease the thickness of fetal membranes and weaken the immunohistochemical appearance of fibronectin.
KATA PENGANTAR
Alhamdulillah, segala puji dan syukur ke hadirat Allah SWT atas berkat rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan penelitian yang berjudul “Gambaran Histopatologi dan Tampilan Imunohistokimia Fibronektin Selaput Ketuban pada Perempuan Hamil yang Mendapat Acetylsalicylic Acid (ASA) Dosis Rendah”
Tesis ini merupakan salah satu persyaratan akademik untuk menyelesaikan pendidikan Program Studi Magister Ilmu Biomedik pada Fakultas Kedokteran Universitas Sumatera Utara.
Pada kesempatan ini, penulis mengucapkan terima kasih kepada :
Rektor Universitas Sumatera Utara Prof.Dr.dr. Syahril Pasaribu, DTM&H, M.Sc (CTM), Sp.A(K) dan Dekan Fakultas Kedokteran Universitas Sumatera Utara Prof. dr. Gontar. A. Siregar, Sp.PD-KGEH dan jajarannya atas kesempatan dan fasilitas yang diberikan kepada penulis untuk mengikuti pendidikan pada Program Studi Ilmu Biomedik Fakultas Kedokteran Universitas Sumatera Utara.
Rasa terima kasih yang besar dan tulus kepada Ketua Program Studi S2 Ilmu Biomedik Universitas Sumatera Utara dr. Yahwardiah Siregar Ph.D dan terima kasih tak terhingga serta penghargaan yang setinggi-tingginya kepada ketua komisi pembimbing Prof. Dr. dr. Rozaimah Zain-Hamid, MS, Sp.FK serta anggota komisi pembimbing dr. Betty, M.Ked (PA), Sp.PA yang telah menyediakan waktu, memberikan motivasi, bimbingan dan arahan sehingga penulis dapat menyelesaikan penelitian ini. Terima kasih yang tak terhingga pula penulis sampaikan kepada dr. Makmur Sitepu, Sp.OG(K), dr. Soekimin, Sp.PA yang telah meluangkan waktu untuk memberikan saran dan masukan serta ilmu pengetahuan yang bermanfaat bagi penulis.
pada Fakultas Kedokteran Universitas Sumatera Utara yang begitu banyak membantu penulis dalam menjalani pendidikan.
Persembahan dengan rasa hormat dan terima kasih yang tulus penulis
sampaikan kepada Ayahanda H. T. Zainal Arifin dan Ibunda tersayang Hj. Siti Zainab yang telah melahirkan, membesarkan dan mendidik penulis
sehingga menjadi manusia yang berguna. Teristimewa untuk suami tercinta Meristika Valeri, ST yang selalu memberikan dorongan moril dan materil serta anak-anakku tersayang, Rayyan dan Rifat yang selalu memberikan senyuman dan rasa bahagia sehingga menjadi semangat bagi penulis untuk menyelesaikan pendidikan ini.
Semoga segenap bantuan, bimbingan dan arahan yang telah diberikan kepada penulis mendapat imbalan yang setimpal dari Allah SWT. Akhirnya penulis menyadari dengan keterbatasan yang ada, untuk itu saran dan kritik yang membangun sangat penulis harapkan demi penyempurnaan tulisan ini. Kiranya tulisan ini dapat bermanfaat bagi ilmu pengetahuan di bidang kesehatan dan kita semua. Aamiin.
Medan, Mei 2014 Penulis
DAFTAR RIWAYAT HIDUP
I.DATA PRIBADI
Nama : dr. Cut Mourisa
Tempat/tanggal lahir : Sigli, 23 Mei 1980
Pekerjaan : Staf Bagian Farmakologi dan Terapeutik FK UISU
Alamat : Jl. Garu II B komplek VHI No. 80 Medan
Agama : Islam
Status : Menikah
Telp/HP : 08126906510
II.RIWAYAT PENDIDIKAN
Tahun 1986-1987 : Taman kanak-kanak Aisyiah Sigli
Tahun 1987-1993 : SDN 3 Sigli
Tahun 1993-1995 : SLTPN 1 Sigli
Tahun 1995-1998 : SMAN 1 Sigli
Tahun 1998-2005 : Pendidikan dokter Universitas Syiah Kuala B.Aceh Tahun 2010-sekarang : Peserta Program Magister Ilmu Biomedik FK USU
III.PENGALAMAN KERJA
Tahun 2006 s/d 2007 : PTT di Puskesmas Padang Tiji
DAFTAR ISI
DAFTAR LAMPIRAN... xi
BAB I PENDAHULUAN ... 1
1.1 Latar belakang ... 1.2 Rumusan masalah ... 1.3 Tujuan penelitian... 1.3.1 Tujuan umum ... 1.3.2 Tujuan khusus... 1.4 Hipotesis ... 1.5 Manfaat penelitian ... 1
2.1 Antiphospholipidsyndrome (APS)... 2.2 Antibodi antiphospholipid (aPL) ... 2.3 Pre-eklamsia dan eklamsia... 2.4 Acetylsalicylic acid ... 2.5 Selaput ketuban ... 2.6 Kolagen ... 2.7 Fibronektin ... 2.8 Fibronektin dan vitamin C ... 2.9 Kerangka teori ... 2.10 Kerangka konsep ... 8 BAB III METODOLOGI PENELITIAN ... 22
3.1 Desain penelitian ... 3.2 Lokasi dan waktu penelitian ... 3.3 Populasi dan sampel penelitian ...
3.3.2 Sampel penelitian... 3.3.3 Cara pengambilan sampel... 3.4 Besar sampel ... 3.5 Kriteria inklusi & eksklusi ... 3.5.1 Kriteria inklusi... 3.5.2 Kriteria eksklusi... 3.6 Kerangka operasional ... 3.7 Identifikasi variabel penelitian ... 3.8 Definisi operasional ... 3.9 Bahan & alat penelitian ... 3.10 Prosedur penelitian ... 3.10.1 Pengumpulan data…... 3.10.2 Prosedur perlakuan jaringan ……….. 3.10.3 Prosedur pembuatan sediaan histopatologi……... 3.10.4 Pengukuran ketebalan jaringan ……….. 3.10.5 Prosedur pembuatan sediaan imunohistokimia ….. 3.10.6 Interpretasi tampilan imunohistokimia fibronektin 3.10.7 Keandalan ………... 3.11 Pengolahan dan analisis data ... 3.12 Etik penelitian ... 3.13 Jadwal penelitian...
DAFTAR TABEL
Tabel Halaman
3.1 4.1
4.2
4.3
4.4
Jadwal penelitian ... Rerata dan simpangan baku ketebalan selaput ketuban pada kelompok kontrol dan kelompok kasus………. Rerata dan simpangan baku intensitas pewarnaan imunohistokimia fibronektin pada selaput ketuban kelompok kontrol dan kelompok kasus……… Rerata dan simpangan baku luas tampilan imunohistokimia fibronektin pada selaput ketuban kelompok kontrol dan kelompok kasus……… Rerata dan simpangan tampilan imunohistokimia fibronektin pada selaput ketuban kelompok kontrol dan kelompok kasus.
40
42
44
46
DAFTAR GAMBAR
Gambar Halaman
2.1 Rumus bangun acetylsalicylic acid... 13
2.2 Mikroskopik selaput ketuban pewarnaan HE………. 15
2.3 Struktur mikroskopis selaput ketuban………... 17
2.4 Biosintesa kolagen ………….………... 19
2.5 Kerangka teori ……….. 21
2.6 Kerangka konsep ……….. 22
3.1 Kerangka operasional..………... 28
3.2 Pembuatan gulungan selaput ketuban.………. 33 4.1 Grafik rerata ketebalan selaput ketuban (lapisan amnion
dan korion) pada kelompok kasus dan kontrol………
43
4.2 Grafik rerata kekuatan intensitas pewarnaan
imunohistokimia fibronektin pada kelompok kasus dan kontrol ………..
45
4.3 Grafik rerata luas tampilan imunohistokimia fibronektin pada kelompok kasus dan kontrol ………..
47
4.4 Grafik rerata tampilan imunohistokimia fibronektin pada kelompok kasus dan kontrol ………
DAFTAR SINGKATAN
ACA Anticardiolipin antibody
aCL Anticardiolipin
ASA Acetylsalicylic acid
aPL Antiphospholipid
APS Antiphospholipid syndrome β2GP I Beta-2 glycoprotein I
COX Cyclo-oxygenase
DAB Diamino benzidine
HE Hematoxylin Eosin
IHC Immunohistochemistry
LA Lupus anticoagulant
MES Matriks ekstraseluler
PROM Premature rupture of the membrane/selaput ketuban pecah dini (KPD)
MCI Myocardial infarct
NHS Normal Horse Serum
RGD
Arginin-glisin-Recurrent spontaneous abortion/abortus spontan berulang
Tris Buffered Saline
TTP
Tx A
Tanggal taksiran persalinan
DAFTAR LAMPIRAN
Nomor Judul Halaman
1 Persetujuan komisi etik... 67
2 Lembar penjelasan kepada calon subjek penelitian………. 68
3 Surat persetujuan setelah penjelasan……… 70
4 Profil data subjek penelitian ………. 71
5 Dokumentasi……….………. 73
6 Data Perhitungan Statistik ……….………. 80
ABSTRAK
Acetylsalicylic acid (ASA)/aspirin adalah obat yang banyak digunakan dengan berbagai khasiat, diantaranya sebagai antitrombotik (pada dosis rendah yaitu 80-325mg) dengan indikasi pada penatalaksanaan strok, infark miokard, trombosis, sindrom antiphospholipid dan pencegahan pre-eklamsia dan eklamsia selama kehamilan. Pemberian ASA jangka panjang pada perempuan hamil menyebabkan keadaan defisiensi vitamin C melalui mekanisme hambatan absorpsi, transpor, peningkatan ekskresi vitamin C, sehingga mengganggu sintesa protein (kolagen, fibronektin) pada matriks ekstraseluler (MES) selaput ketuban. Penelitian ini bertujuan untuk mengetahui perubahan gambaran struktur histopatologi (ketebalan lapisan amnion-korion) dan tampilan imunohistokimia fibronektin pada selaput ketuban perempuan hamil yang mendapat ASA dosis rendah. Jenis penelitian ini adalah cross sectional dengan menggunakan 81 subjek yang dipilih dengan teknik consecutive sampling. Sebanyak 27 subjek (kelompok kasus) mendapat ASA dosis rendah dan 54 subjek (kelompok kontrol) tanpa ASA
dosis rendah. Pada saat persalinan dilakukan pengambilan selaput ketuban untuk diperiksa. Hasil penelitian menunjukkan selaput ketuban pada kelompok kasus (85,18±15,98) lebih tipis dibandingkan kelompok kontrol (111,68±27,19) (p<0,05). Tampilan imunohistokimia fibronektin pada kelompok kasus (1,85±0,53) lebih lemah dibandingkan kelompok kontrol (2,49±0,63) (p<0,05). Pemberian ASA dosis rendah jangka panjang pada perempuan hamil terbukti menurunkan ketebalan selaput ketuban dan tampilan imunohitokimia fibronektin pada selaput ketuban.
ABSTRACT
Acetylsalicylic acid (ASA)/aspirin, a drug that is widely used, has a variety of properties. One such property permits an antithrombotic use (at low doses are 80-325 mg) indicating treatment of stroke, myocardial infarction, thrombosis, antiphospholipid syndrome and prevention of pre-eclampsia and eclampsia during pregnancy. Long-term use of ASA during pregnancy causes vitamin C deficiency via a mechanism of disturbance absorption, distribution and increased excretion of vitamin C, thereby disrupting the synthesis of proteins (collagen, fibronectin) in the extracellular matrix (ECM) of fetal membranes. This study aims to determine histopathological changes in the structural overview (amnion-chorion layer thickness) and immunohistochemical appearance of fibronectin on the fetal membranes of pregnant women who receive low-dose ASA. This study follows a cross sectional design with 81 subjects selected using a consecutive sampling technique. A total of 27 subjects (cases) received low-dose ASA and 54 subjects (control group) without low-dose ASA. The fetal membranes were collected at experiment end as per results delivery and next were to be examined. The results showed that the fetal membranes in the case group (85.18 ± 15.98) were thinner than the control group (111.68 ± 27.19) (p <0.05). Further, the immunohisto-chemical appearance of fibronectin in the case group (1.85 ± 0.53) was weaker than the control group (2.49 ± 0.63) (p <0.05). The provision of long-term low-dose ASA in pregnant women was shown to decrease the thickness of fetal membranes and weaken the immunohistochemical appearance of fibronectin.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Acetylsalicylic acid (ASA)/aspirin adalah obat yang banyak digunakan untuk
berbagai indikasi, yaitu sebagai analgesik, antipiretik, anti-inflamasi dan
antitrombotik (bekerja dengan menghambat agregasi trombosit, sehingga obat ini
dapat memperpanjang waktu perdarahan) (Goodman dan Gillman, 2007). Sebagai
antitrombotik, dosis ASA/aspirin yang digunakan adalah dosis rendah (80-325mg)
(Katzung, 2010), dan berguna pada penatalaksanaan strok, infark miokard (MCI),
trombosis(Walsh dan Schwartz-Bloom, 2005) sindrom antiphospholipid dan
pencegahan pre-eklamsia dan eklamsia selama kehamilan(Levine et al., 2002;
WHO, 2011).
Sindrom antiphospholipid (APS) adalah gangguan autoimun yang dapat
menyebabkan trombosis pembuluh darah, abortus berulang akibat adanya
trombosis di pembuluh darah plasenta (Rand, 2002).
Perempuan hamil dengan antibodi aPL
Antibodi antiphospholipid
(aPL) utama yang berhubungan dengan APS adalah antibodi anticardiolipin
(aCL), antikoagulan lupus (LA),danantibodiglikoprotein anti-beta2 I
(anti-beta-2GPI) (McNeil et al., 2002).
positif, mempunyai kecenderungan
mengalami keguguran berulang sebesar 15% pada trimester pertama, dan 21%
pada trimester kedua (Vashisht dan Regan, 2005). APS masih menjadi penyakit
yang sering mengakibatkan keguguran berulang (Rai, 2002). Morbiditas
vasculophaty) dan infark plasenta (Tektonidou, 2004). Pengobatan kombinasi
aspirin/ASA dosis rendah dengan heparin merupakan terapi pilihan (Bates, 2010).
Pemberian ASA/aspirin dosis rendah (50 mg/hari) pada perempuan dengan
riwayatabortus spontan berulang (recurrent spontaneous abortion/ RSA) dengan
atau tanpa antibodi anticardiolipin (ACA) yang positif, dapat menghambat
produksi tromboxan A2 (Tx A2), sehingga menghambat agregasi trombosit
(Tulppala et al., 2000 dan Berg, 2011).
Selain itu pemberian antitrombotik, juga ditujukan untuk menurunkan risiko
terjadinya trombosis, keguguran, dan kehamilan dengan hipertensi, sehingga
pemberian harian ASA/aspirin dosis rendah, merupakan regimen pengobatan pada
kehamilan dengan APS (Branch dan Khamashta, 2003).
ASA/aspirin dosis rendah juga diberikan pada kehamilan dengan atau riwayat
pre-eklamsia (Duley et al., 2007) dikarenakan pre-eklamsia merupakan salah satu
faktor risiko terjadinya trombosis, kelahiran prematur dan kelahiran mati pada
neonatal (Duley et al.,2001;
Pada kehamilan, pembentukan selaput amnion berasal dari jaringan
ekstra-embrio yang terdiri dari bagian fetal (the chorionic plate) dan bagian maternal
(the decidua). Bagian fetal (amnion dan membran korion), memisahkan fetus dari
endometrium (Niknejad et al., 2008).Kolagen merupakan komponen dari
membran yang berfungsi untuk menjaga
Hague et al., 2001). WHO (2011) merekomendasikan
intervensi pemberian ASA/aspirin dosis rendah untuk mencegah terjadinya
pre-eklamsia pada perempuan dengan risiko tinggi sebelum kehamilan 20 minggu.
kekuatan jaringan pada amnion dan
Selaput amnion dan korion manusia terdiri dari beberapa lapisan, dengan
berbagai jenis kolagen (tipe I, III, IV, V, VI) dan glikoprotein non-kolagen
(laminin, nidogen dan fibronektin) yang terdapat didalam matriks ekstraseluler
(MES) (Benirschke dan Kaufmann, 2006).
Lapisan-lapisan pada selaput ketuban akan mempengaruhi ketebalannya, dan
akan memberikan kontribusi terhadap ketahanannya. Namun selaput ketuban yang
tipis belum tentu menyebabkan penurunan ketahanannya, karena ketahanan
selaput ketuban juga dipengaruhi oleh keberadaan dan kondisi (keterikatan)
berbagai komponen penunjang selaput ketuban, seperti kolagen, dan glikoprotein
non-kolagen lainnya, yaitu: laminin, nidogen dan fibronektin. Perubahan pada
membran, termasuk penurunan kadar kolagen, struktur kolagen, peningkatan
aktivitas kolagenolitik, merupakan salah satu faktor risiko untuk terjadinya
ketuban pecah dini/KPD (premature rupture of the membrane/PROM)
(Parry dan Strauss, 1998).
Vitamin C(ascorbic acid) adalah zat yang dibutuhkan untuk pembentukan
kolagen dan stabilitas collagent cross-link,kadar vitamin C jaringan merupakan
mediator penting dalam proses inisiasi ruptur membran sebagai fungsi dari
kolagen cross-link rasio (Myllyharju, 2003). Konsentrasi total vitamin Cpada
perempuan dengan PROM, secara signifikan lebih rendah daripada perempuan
yang mengalami ruptur membran pada saat proses persalinan (Stuart, et al., 2005).
Selain itu, vitamin C mempengaruhi pertumbuhan komponen MES lainnya,
fibronektin dan laminin (Ronchetti et al., 1998). Pemberian vitamin C sebanyak
100 mg/hari pada perempuan hamil, dapat menurunkan risiko terjadinya PROM
Pemberian ASA/aspirin bersama vitamin C (ascorbic acid) mengakibatkan
terjadinya interaksi farmakokinetik pada tahap absorpsi, distribusi dan ekskresi.
Pemberian aspirin pada dosis > 25 mg bersama vitamin C (ascorbic acid) dengan
dosis 50-100 mg menyebabkan hambatan transpor ascorbic acid ke dalam
leukosit (Das dan Nebiogiu, 1999). Obat golongan salisilat juga menghambat
uptake vitamin C kedalam leukosit dan platelet (Levine et al., 1999).
Selain itu ASA/aspirinjuga dapat meningkatkan ekskresi vitamin C melalui
urin dan menurunkan konsentrasi vitamin C platelet (Levine et al., 2006);
menurunkan kadar ascorbic acid leukosit dan menurunkan kemampuan
metabolismenya. (Stargrove et al., 2008).
Berdasarkan uraian di atas, maka akan diteliti pengaruh pemberian ASA/
aspirin dosis rendah (80-100 mg) pada perempuan hamil (mengalami APS atau
pre-eklamsia/eklamsia atauriwayat pre-eklamsia/eklamsia), terhadap gambaran
histopatologi struktur selaput ketuban dan tampilan imunohistokimia fibronektin
pada MES selaput ketuban.
1.2 Perumusan Masalah
Berdasarkan uraian latar belakang diatas, dapat dirumuskan pertanyaan
penelitian sebagai berikut:
1. Apakah pemberian ASA/aspirin dosis rendah (80-100 mg) pada perempuan
hamil (mengalami APS atau pre-eklamsia/eklamsia atau riwayat
pre-eklamsia/eklamsia), dapat menyebabkan penipisan lapisan amnion dan
2. Apakah pemberian ASA/aspirin dosis rendah (80-100 mg) pada perempuan
hamil (mengalami APS atau pre-eklamsia/eklamsia atauriwayat pre-eklamsia/
eklamsia), dapat menyebabkan penurunan tampilan imunohistokimia
fibronektin pada matriks ekstraseluler selaput ketuban (amnion dan korion)?
1.3 Tujuan Penelitian
1.3.1 Tujuan Umum
Untuk mengetahui perubahan gambaran struktur histopatologi dan tampilan
imunohistokimia fibronektin pada matriks ekstraseluler (MES) selaput ketuban
perempuan hamil (mengalami APS atau pre-eklamsia/eklamsia atauriwayat
pre-eklamsia/eklamsia), yang mendapat ASA/aspirin dosis rendah (80-100 mg).
1.3.2 Tujuan khusus
1. Mengetahui pengaruh pemberian ASA/aspirin dosis rendah (80-100 mg)
terhadap gambaran struktur histopatologi (ketebalan lapisan amnion dan
korion) selaput ketuban, pada perempuan hamil (mengalami APS atau
pre-eklamsia/eklamsia atauriwayat pre-eklamsia/eklamsia).
2. Mengetahui pengaruh pemberian ASA/aspirindosis 80 - 100 mg terhadap
kekuatan intensitas pewarnaan imunohistokimia fibronektin pada MES
selaput ketuban perempuan hamil (mengalami APS atau pre-eklamsia/
eklamsia atauriwayat pre-eklamsia/eklamsia).
3. Mengetahui pengaruh pemberian ASA/aspirindosis 80 - 100 mg terhadap
selaput ketuban perempuan hamil (mengalami APS atau pre-eklamsia/
eklamsia atauriwayat pre-eklamsia/eklamsia).
4. Mengetahui pengaruh pemberian ASA/aspirindosis 80 - 100 mg terhadap
tampilan (perkalian kekuatan intensitas pewarnaan dengan luas tampilan
imunohistokimia fibronektin) pada MES selaput ketuban perempuan hamil
(mengalami APS atau pre-eklamsia/eklamsia atauriwayat pre-eklamsia/
eklamsia).
1.4 Hipotesis
Ada perbedaan gambaran histopatologi dan tampilan imunohistokimia
fibronektin selaput ketuban antara perempuan hamil (mengalami APS atau
pre-eklamsia/eklamsia atau riwayat pre-eklamsia/eklamsia) serta mendapat
ASA/aspirin dosis rendah (kelompok kasus), dengan perempuan hamil normal dan
tidak mendapat ASA/aspirin (kelompok kontrol), berupa :
1. Selaput ketuban (amnion dan korion) pada kelompok kasus lebih tipis
dibandingkan selaput ketuban kelompok kontrol.
2. Kekuatan intensitas pewarnaan imunohistokimia fibronektin pada
MES selaput ketuban kelompok kasus lebih lemah dibandingkan
kelompok kontrol.
3. Luas tampilan pewarnaan imunohistokimia fibronektin pada MES
selaput ketuban kelompok kasus lebih lemah dibandingkan kelompok
4. Tampilan (perkalian kekuatan intensitas dengan luas tampilan)
pewarnaan imunohistokimia fibronektin pada MES selaput ketuban
kelompok kasus lebih lemah dibandingkan kelompok kontrol.
1.5 Manfaat Penelitian
Memberikan informasi tentang pengaruh pemberian ASA/aspirin dosis
rendah (80-100 mg) terhadap perubahan gambaran histopatologi dan tampilan
imunohistokimia fibronektin pada MES selaput ketuban perempuan hamil
(mengalami APS atau pre-eklamsia/eklamsia atauriwayat pre-eklamsia/eklamsia),
agar kemungkinan terjadinya ketuban pecah dini (KPD) dapat diprediksi dan
BAB II
TINJAUAN PUSTAKA
2.1 Antiphospholipidsyndrome (APS) 2.1.1 Definisi
Antiphospholipid syndrome (APS) atau Hughes syndrome adalah suatu
kumpulan kondisi yang ditandai dengan trombosis vaskuler (arteri dan atau vena),
dan keguguran (abortus) berulang. Karakteristik laboratorium dari APS adalah
adanya antibodi antiphospholipid (aPL), yaitu lupus anticoagulant (LA), antibodi
anticardiolipin (aCL), antiphosphatidylserine atau beta-2 glycoprotein I / B2GPI
(apolipoprotein H) (Tektonidou, 2004; Keeling et al., 2012). APS merupakan
salah satu penyebab terjadinya abortus (Branch and Khamashta, 2003).
2.1.2 Epidemiologi APS
Frekuensi pasien APS terkini pada populasi umum tidak diketahui,
tetapi 1-5% individu sehat mempunyai antibodi aPL dan antibodi aCL serta
cenderung meningkat pada usia lanjut. Dari sekitar 30-40% pasien SLE dengan
antibodi aPL, 10% menderita APS. Dari hasil penelitian terhadap 100 pasien
dengan trombosis vena dan tanpa riwayat SLE, ternyata ditemukan 24% antibodi
aCL positif dan 15% lupus anticoagulant (LA) positif (Belilos, 2012).
2.1.3 Penatalaksanaan APS
Penanganan ideal untuk kehamilan dengan APS bertujuan untuk: (1)
menurunkan risiko trombosis pada ibu selama kehamilan; (2) upaya pencegahan
Untuk mengobati kondisi ini, dapat diberikan antikoagulan, heparin dan
ASA/aspirin dosis rendah (Branch and Khamashta, 2003).
2.1.4 Profilaksis pasien asimptomatik dengan antibodi aCL positif atau LA
positif
Dalam praktek klinik, pengobatan empiris dilakukan dengan pemberian ASA
(aspirin) dosis rendah (80 mg/hari), walaupun belum ada penelitian prospektif
tentang manajemen profilaksis (Tektonidou, 2004).
2.2 Antibodi Antiphospholipid (aPL)
Antibodi Antiphospholipid (aPL) merupakan autoantibodi yang ditemukan
pada plasma/serum dalam solid-phase immunoassay. Antibodi aPL utama yang berhubungan dengan APS terdiri dari :
(a) Antibodi aCL / antibodi lain yang menyerang bagian negatif fosfolipid :
phosphatidylserine, phosphatidylinositol phosphatidic acid, phosphatidyl
glycerol;
(b) Lupus anticoagulants (LAs), dan
(c) Anti-beta2 glycoprotein I (anti-β-2GPI) (Danowski et al.,2013).
2.3 Pre-eklamsia dan eklamsia
2.3.1 Definisi
Pre-eklamsia adalah sindroma yang spesifik dalam kehamilan yang dapat
menyebabkan perfusi darah ke organ berkurang karena adanya vasospasme dan
pada kehamilan, yang ditandai dengan peningkatan tekanan darah dan proteinuria
(Lowe et al., 2008).
Eklamsia adalah pre-eklamsia yang disertai kejang dan atau koma. Kejang
bisa timbul pada sebelum, selama atau sesudah proses kehamilan. Kejang bisa
juga terjadi pada 48 jam atau lebih sesudah melahirkan, bahkan bisa terjadi
10 hari sesudah kelahiran (Cunningham et al., 2005).
2.3.2 Pencegahan pre-eklamsia dan eklamsia
Pencegahan pre-eklamsia dan eklamsia difokuskan untuk memperbaiki
perubahan patofisiologi yang terjadi. Jalur akhir dari patogenesis terjadinya
pre-eklamsia adalah kerusakan sel endotel, sehingga pencegahan dan pengobatan
ditujukan untuk mengurangi kerusakan sel endotel (pencegahan primer), atau
mengurangi akibat yang muncul dari kerusakan sel endotel (pencegahan sekunder
atau tersier). Beberapa strategi dapat digunakan untuk mencegah pre-eklamsia,
seperti modifikasi diet dan pendekatan farmakologi dengan pemberian ASA/
aspirin dosis rendah (Sofoewan, 2003; Duley et al., 2007). Pemberian ASA/
aspirin dosis rendah, kalsium dan antioksidan, dipercaya efektif untuk
menurunkan risiko pre-eklamsia (Wagner, 2004; Taherian dan Shirvani, 2003).
2.4 Acetylsalicylic acid (ASA)
2.4.1 Uraian umum
Acetylsalicylic acid (ASA) yang nama lainnya aspirin atau asetosal
merupakan derivat asam salisilat dengan rumus molekul C9H8O4 dan berat
non-steroid, dengan khasiat sebagai analgesik, antipiretik dan anti-inflamasi, yang
diperoleh pada penggunaan dosis >325 mg (Goodman and Gilman, 2007).
Namun, pada dosis <325 mg, ASA/aspirin berkhasiat sebagai antitrombotik/
antiplatelet. Dosis efektif ASA sebagai antitrombotik/antiplatelet berkisar antara
80 - 320 mg (Patrono et al., 1980).
Gambar 2.1 Rumus bangun Acetylsalicylic Acid (Goodman and Gilman, 2007)
2.4.2 Farmakokinetik ASA
Setelah pemberian oral, ASA yang tak terionisasi diabsorpsi secara pasif di
lambung dan usus halus. ASA dapat menembus sawar darah otak dan plasenta.
ASA dimetabolisme di hati, dihidrolisis menjadi salisilat dan asam asetat oleh
esterase yang ada di jaringan dan darah. Konjugat hasil metabolisme yang larut
dalam air diekskresikan oleh ginjal (Mycek, 2003).
2.4.3 Farmakodinamik ASA
ASA bekerja dengan menghambat aktifitas enzim siklooksigenase sehingga
menghambat sintesa tromboksan A2 (TXA2) (hambatan agregasi trombosit) serta
ASA menghambat produksi TxA2 dengan mengasetilasi residu serin secara
kovalen yang terletak di dekat active-site cyclo-oxygenase (COX). COX adalah
enzim yang menghasilkan pre-kusor endo-peroksida siklik TxA2, dan TxA2
2.4.4 Interaksi ASA dengan ascorbic acid (vitamin C)
merupakan produk utama COX pada trombosit yang merupakan penginduksi
agregasi trombosit yang labil dan mempunyai sifat vasokonstriktor kuat.
Trombosit tidak mensintesis protein baru, sehingga kerja ASA pada
trombosit-COX bersifat permanen dan bertahan sepanjang usia trombosit yaitu 7-10 hari.
Sehingga pengulangan pemberian dosis ASA menghasilkan efek kumulatif dari
fungsi trombosit (Goodman and Gilman, 2007).
Acetylsalicylic Acid (ASA)/Aspirin dapat meningkatkan ekskresi vitamin C
melalui urin, menurunkan kadar ascorbic acid/vitamin C leukosit dan menurunkan
kemampuan metabolismenya (Stargrove et al., 2008). Pemberian ASA/aspirin
pada dosis > 25 mg bersama vitamin C (ascorbic acid) dengan dosis 50-100 mg
menyebabkan hambatan transpor ascorbic acid ke dalam leukosit (Das dan
Nebiogiu, 1999). Obat golongan salisilat juga menghambat uptake vitamin C
kedalam leukosit dan platelet (Levine et al., 1999).
2.5 Selaput ketuban
2.5.1 Anatomi dan histologi
Selaput ketuban manusia terdiri dari amnion dan non-plasenta korion.
Amnion adalah lapisan terdalam dari selaput ketuban dan berhubungan dengan
pembuluh darah, sehingga bahan nutrisi yang dibutuhkan janin disediakan oleh
cairan ketuban. Walaupun lapisan amnion hanya mengisi sekitar 20% ketebalan
selaput ketuban, namun sangat dominan dalam respon mekanik selaput ketuban
(Oyen et al., 2001), sedangkan korion adalah bagian luar selaput dan memisahkan
selaput amnion dari desidua dan uterus (Benirschke dan Kaufmann, 2006;
Rohen dan Lutjen-Drecoll, 2009)
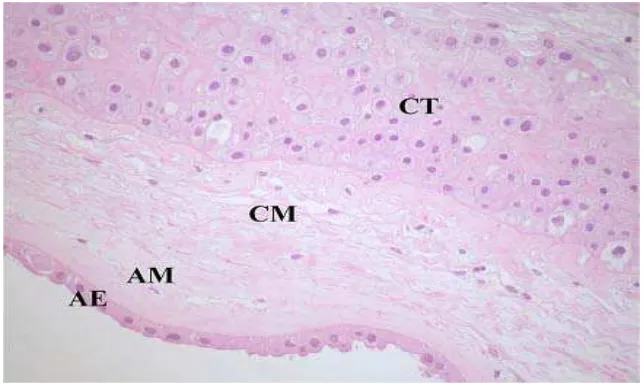
Gambar 2.2 Mikroskopik selaput ketuban pewarnaan Haematoxylin-Eosin (HE) (AE: amniotic epithelial layer, AM: amniotic mesenchymal layer, CM: chorionic mesenchymal layer, CT: chorionic trophoblastic (Parolini et al., 2008)
2.5.2 Amnion
Selaput amnion manusia dapat dibedakan menjadi lima lapisan yaitu :
(1) epithelium amnoinic, (2) basement membrane, (3) compact layer, (4) fibroblas
layer, dan (5) Spongy layer. Lapisan paling dalam adalah epitel amnion; berada
paling dekat dengan janin (Gambar 2.1). Sel epitel mensekresi kolagen tipe III, IV
compact layer disekresi oleh sel-sel mesenkim pada fibroblast layer, yaitu tipe III,
V, VI. Lapisan fibroblast (fibroblast layer) adalah lapisan paling tebal pada
amnion, terdiri dari sel-sel mesenkim dan sebaran sel makrofag dalam matriks
ekstraseluler. Spongy layer/intermediate layer terletak di antara amnion dan
korion dan kaya akan proteoglikan serta mengandung kolagen tipe I, III, dan IV
(Parry and Strauss, 1998). Tebal lapisan epithelium amnoinic adalah 20-30 µm,
sedangkan tebal lapisan basement membrane, compact layer, fibroblast layer
(amnionic mesoderm) adalah 15-30 µm (Baergen, 2005).
2.5.3 Korion
Korion terdiri dari lapisan lapisan retikuler dan basal membran. Korion
menyerupai membran epitel yang khas dengan polaritas mengarah ke bagian
desidua maternal. Pada kehamilan yang lebih lanjut, vili trofoblas pada lapisan
korion akan mengalami regresi. Di bawah lapisan sitotrofoblas terdapat basal
membran dan jaringan ikat chorionic yang kaya akan fibril kolagen. Kolagen pada
lapisan retikular dan basal membran adalah kolagen tipe I, III, IV, V, dan VI.
Walaupun lapisan korion lebih tebal daripada amnion, namun amnion mempunyai
daya regang yang lebih tinggi dibandingkan korion (Parry and Strauss, 1998).
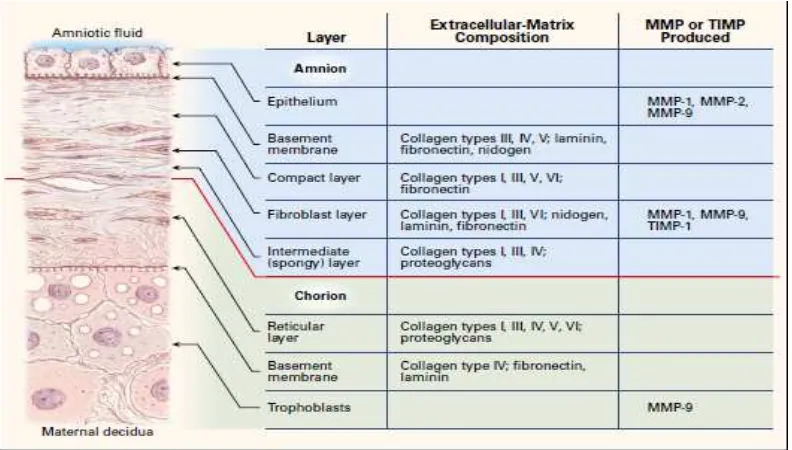
Gambar 2.3 Struktur mikroskopis selaput ketuban (Parry dan Strauss, 1998)
2.6 Kolagen
Kolagen merupakan protein terbanyak dalam tubuh manusia dan
membentuk lebih dari 25% massa protein. Kolagen adalah protein fibrosa dan
salah satu serat jaringan ikat yang dibentuk dari protein berpolimerisasi menjadi
struktur yang panjang. Protein matriks ekstraseluler ini sangat memegang peran
penting dan dirancang untuk memberikan struktur dan ketahanan terhadap
jaringan (Mecham, 2009). Kolagen terdapat pada kulit, tulang, tulang rawan,
jaringan fetal, plasenta, basal membran, dentin, dinding pembuluh darah, sklera,
kornea mata dan jaringan ikat seperti ligamentum dan tendo sehingga menjadikan
jaringan tersebut memiliki daya regang tinggi (Junqueira, 2007). Kolagen yang
terdapat pada amnion terdiri dari kolagen interstisium tipe I, III, V, dan VI, yang
2.6.1 Struktur kolagen
Tropokolagen terdiri dari 3 serat, yang masing-masing mengandung 1000
asam amino yang bersatu membentuk helix triple collagen. Helix triple collagen
memiliki 3,3 residu, salah satunya adalah glisin pada setiap asam amino ketiga
rantai polipeptida dan menghasilkan suatu rangkaian Gly-X-Y yang berulang.
Kolagen juga kaya akan prolin atau hidroksiprolin. Prolin sering menduduki posisi
X, sedangkan hidroksiprolin atau hidroksilisin menduduki posisi Y pada urutan
asam amino. Hidroksiprolin memaksimalkan pembentukan ikatan hidrogen antar
rantai sehingga berperan penting untuk menstabilkan struktur helix triple collagen
(Champe et al., 2010 ; Gordon dan Hahn, 2010).
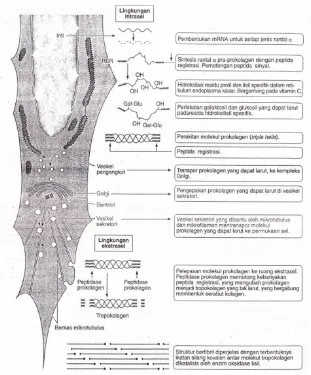
2.6.2 Biosintesa kolagen
Kolagen disintesa sebagai prokolagen yang dibentuk dalam fibroblas
(memproduksi sekitar 5-10% protein totalnya); osteoblas dan kondroblas
kemudian akan disekresi ke dalam matriks ekstraseluler. Kolagen mengandung
hidroksiprolin dan hidroksilisin yang tidak terdapat pada kebanyakan protein yang
lain. Hidroksiprolin memegang peran penting dalam penstabilan struktur helix
triple collagen karena memaksimalkan pembentukan ikatan hidrogen antar rantai
(Champe et al., 2010).
Sintesa diawali dengan pembentukan pro-rantai α, hidroksilasi, glikosilasi, perakitan molekul pro-kolagen, sekresi, pembelahan di luar sel, pembentukan
2.6.3 Hidroksilasi dan vitamin C
Hidroksiprolin dibentuk melalui reaksi hidroksilasi yang dikatalisis oleh
enzim prolil hidroksilase dengan ko-faktor asam askorbat (vitamin C). Defisiensi
asam askorbat menyebabkan gangguan sintesis kolagen akibat defisiensi prolil
dan lisil hidroksilase dan berakibat gangguan stabilitas helix triple collagen
(Murray et al., 2009; dan Osaikhuwuomwan, 2010).
2.7 Fibronektin
2.7.1 Struktur
Fibronektin adalah glikoprotein utama matriks ekstraseluler (MES)
(Korhonen dan Virtanen, 2001). Fibronektin berfungsi mengikat heparin, fibrin,
kolagen, DNA dan permukaan sel. Fibronektin merupakan anggota kelas integrin
transmembran dan berinteraksi dengan reseptor sel, protein ini berperan penting
dalam perlekatan sel pada MES (Murray et al., 2009).
Fibronektin mempunyai tempat khusus untuk berikatan dengan komponen
MES yang lain (berspektrum luas) seperti kolagen, heparin dan proteoglikan
(Robbins et al.,2007).
Pada plasenta manusia, molekul fibronektin terdapat pada lapisan amnion,
membran basal, lapisan korion, desidua, plasenta fibrinoid, vili dan umbilical cord
(Demir-Weuesten, 2002).
Fibronektin terdiri dari fibronektin tipe I, II, dan III, dimana terjadi
pengulangan yang berbeda pada monomer karena differential splicing mRNA
fibronektin, dan lebih dari 20 varian monomer berbeda telah diidentifikasi sampai
saat ini (White, et al., 2008). Fibronektin terbentuk dari dua sub-unit dengan berat
masing-masing sekitar 250kD. Domain ikatan sel mengandung
arginin-glisin-asam aspartat (RGD) yang merupakan sekuensi penting untuk interaksi
sel integrin dan RGD site (Jourdan, 2010).
2.8 Fibronektin dan vitamin C
Jumlah proteoglikan, fibronektin dan protein microfibrillar meningkat
memicu terjadinya penggabungan ['4 C] prolin menjadi protein seluler dan
perubahan parameter pertumbuhan sel dan morfologi. Hanya sejumlah kecil
fibronektin hadir dalam matriks ketika askorbat tidak ditambahkan, meskipun
terdapat jumlah fibronektin yang cukup signifikan dalam serum. Hal ini
menunjukkan bahwa kolagen memberikan tempat yang diperlukan untuk ikatan
fibronektin
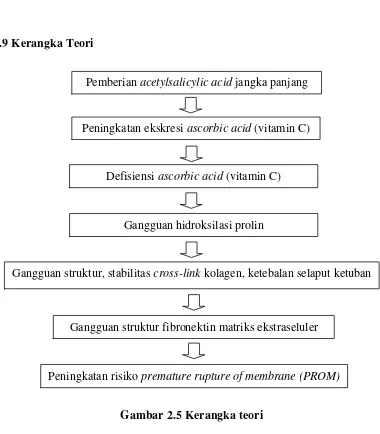
2.9 Kerangka Teori
(Schwartz, et al., 2000).
Gambar 2.5 Kerangka teori
Peningkatan risiko premature rupture of membrane (PROM)
Pemberian acetylsalicylic acid jangka panjang
Peningkatan ekskresi ascorbic acid (vitamin C)
Defisiensi ascorbic acid (vitamin C)
Gangguan struktur, stabilitas cross-link kolagen, ketebalan selaput ketuban Gangguan hidroksilasi prolin
2.10 Kerangka konsep
Gambar 2.6 Kerangka konsep
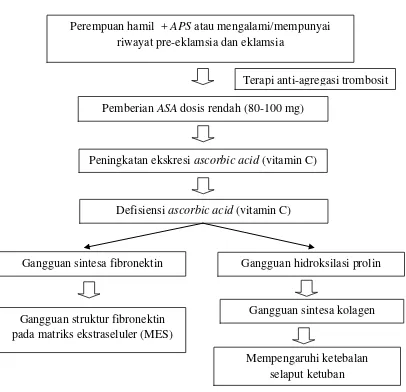
Perempuan hamil dengan APS atau mengalami/mempunyai riwayat
pre-eklamsia dan eklamsia, diberikan salah satu regimen pengobatan ASA/Aspirin
dosis rendah (80-325mg). Pemberian ASA yang terus menerus selama proses
kehamilan dapat menyebabkan defisiensi ascorbic acid (vitamin C) melalui
mekanisme interaksi kedua obat. ASA menurunkan kadar ascorbic acid (vitamin Perempuan hamil + APS atau mengalami/mempunyai
riwayat pre-eklamsia dan eklamsia
Terapi anti-agregasi trombosit
Pemberian ASA dosis rendah (80-100 mg)
Peningkatan ekskresi ascorbic acid (vitamin C)
Defisiensi ascorbic acid (vitamin C)
Gangguan sintesa kolagen Gangguan hidroksilasi prolin Gangguan sintesa fibronektin
Mempengaruhi ketebalan selaput ketuban
Defisiensi ascorbic acid (vitamin C) mempengaruhi pembentukan struktur
kolagen, stabilitas cross-link, struktur fibronektin MES dan ketebalan lapisan
BAB III
METODOLOGI PENELITIAN
3.1 Desain Penelitian
Penelitian ini bersifat deskriptif analitik dengan rancangan penelitian
cross sectional (potong lintang).
3.2 Lokasi dan waktu penelitian
3.2.1 Lokasi penelitian
Pengambilan sampel dilakukan di beberapa praktek spesialis kandungan
di kota Medan. Proses pembuatan dan pembacaan preparat imunohistokimia
dilaksanakan di laboratorium Patologi Anatomi, sedangkan pembacaan preparat
histopatologi (pengukuran ketebalan jaringan) dilaksanakan di Laboratorium
Terpadu Fakultas Kedokteran Universitas Sumatera Utara Medan.
3.2.2 Waktu penelitian
Penelitian dilakukan selama 14 bulan, dari bulan April 2013 sampai Mei
2014 yang mencakup pembacaan proposal, pengumpulan data, pengolahan,
analisis data dan pelaporan hasil.
3.3 Populasi dan sampel penelitian
3.3.1 Populasi penelitian
Semua perempuan hamil (20-45 tahun), yang berobat ke klinik dokter
3.3.2 Sampel penelitian
− Perempuan hamil (20-45 tahun) dengan kehamilan normal dan tidak mendapat
acetylsalicylic acid(ASA).
− Perempuan hamil (20-45 tahun) dengan salah satu diagnosa:
− APS
− Mengalami/mempunyai riwayat pre-eklamsia/eklamsia dan mendapat
acetylsalicylic acid(ASA) dosis rendah (80-100 mg/hari).
3.3.3 Cara pengambilan sampel
Pemilihan sampel penelitian dilakukan dengan metode consecutive
sampling, bagi perempuan hamil yang memenuhi kriteria penelitian (kriteria
inklusi dan eksklusi). Pengambilan sampel akan dihentikan bila jumlah minimal
sampel telah terpenuhi.
3.4 Besar sampel
Untuk membuktikan hipotesis adanya perbedaan gambaran histopatologi
antar subyek, digunakan rumus besar sampel untuk uji analitik komparatif
numerik tidak berpasangan (Dahlan, 2010).
Rumus :
(
)
α= tingkat kemaknaan (ditetapkan peneliti) α= 0,05 zα
β= power of test (ditetapkan peneliti) 80% z = 1,96
β
σ= simpangan baku = 0,3 (penelitian sebelumnya)
= 0,824
(
)
Dari rumus di atas, didapatkan besar sampel minimal adalah 35 orang.
Untuk membuktikan hipotesis adanya perbedaan tampilan imuno-histokimia
fibronektin selaput ketuban antara subjek, digunakan rumus besar sampel untuk
uji analitik komparatif kategorik tidak berpasangan (Dahlan, 2010). Jika kesalahan tipe 1 ditetapkan 5%, hipotesis 1 arah sehingga Zα=1,96, kesalahan tipe II
Dari rumus di atas, didapatkan besar sampel minimal adalah 32 orang.
Berdasarkan kedua rumus yang digunakan, disimpulkan bahwa besar sampel
minimal yang akan diambil untuk menilai perubahan gambaran histopatologi dan
tampilan imunohistokimia pada penelitian ini adalah 35 orang perempuan hamil.
Setelah menjalani proses pengambilan sampel selama 5 bulan, ternyata
jumlah kelompok kasus yang dibutuhkan masih belum memenuhi jumlah sampel
yang dibutuhkan. Sehingga karena keterbatasan waktu dan dana, maka besar
sampel untuk kelompok kasus dihitung kembali dengan cara memperbanyak
kontrol dengan rumus sebagai berikut (Dahlan, 2010).
�′ = �(�+ 1)
n’= besar sampel kasus
n= besar sampel semula
c= jumlah kontrol= 2 (karena direncanakan 2 kontrol/kasus)
n’ = 35(2+1)
2�2
n’ = 105
4 =26,3 27
Dari rumus di atas didapatkan jumlah kasus sebanyak 27 orang, jumlah
kontrol sebanyak 2x27= 54 orang, sehingga total sampel adalah 81 orang.
3.5. Kriteria inklusi dan eksklusi
3.5.1 Kriteria inklusi
− Perempuan hamil (20-45 tahun)
− Usia kehamilan > 37 minggu
− Kehamilan normal (tanpa APS, tidak mengalami/mempunyai riwayat
pre-eklamsia/eklamsia dan tidak mendapat ASAkelompok kontrol
− Kehamilan dengan salah satu diagnosa:
− APS
− Mengalami atau mempunyai riwayat pre-eklamsia/eklamsia dan
mendapat ASA dosis rendah (80-100 mg/hari) sejak trimester
pertama kehamilan dan berhenti pada waktu 2 minggu sebelum
tanggal taksiran persalinan (TTP) kelompok kasus
− Persalinan spontan atau sectiocaesarea
− Sampel jaringan selaput ketuban: berwarna putih dan mengkilat; tanpa
− Bersedia ikut dalam penelitian (bersedia untuk menandatangani
informed consent)
3.5.2 Kriteria eksklusi
− Diabetes mellitus
− Diabetes gestasional
− Perokok
− Kehamilan kembar
3.6 Kerangka operasional
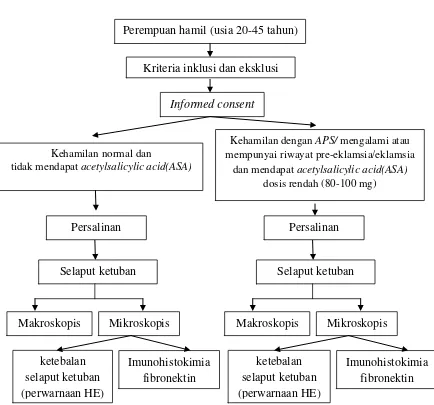
Gambar 3.1 Kerangka operasional
Kehamilan dengan APS/ mengalami atau mempunyai riwayat pre-eklamsia/eklamsia
dan mendapat acetylsalicylic acid(ASA) dosis rendah (80-100 mg)
Informed consent
Kehamilan normal dan tidak mendapat acetylsalicylic acid(ASA)
Perempuan hamil (usia 20-45 tahun)
Kriteria inklusi dan eksklusi
3.7 Identifikasi variabel penelitian
− Variabel bebas : acetylsalicylic acid (ASA) dosis rendah (80-100 mg)
− Variabel tergantung :
− Gambaran histopatologi selaput ketuban ( ketebalan lapisan amnion
dan korion)
− Tampilan imunohistokimia fibronektin selaput ketuban
3.8 Definisi operasional
− Selaput ketuban:
Selaput yang melindungi janin, terdiri atas amnion dan korion; berwarna
putih mengkilat
− Gambaran histopatologi selaput:
Adalah ketebalan lapisan kolagen pada lapisan amnion dan lapisan korion.
− Hasil pengukuran: dinyatakan dalam satuan µm.
− Alat ukur: sediaan histopatologi selaput ketuban, mikroskop Primostar
ZEISS yang dilengkapi kamera Axiocam ERc5s dan software Axiovision
Rel. 4.8.2 (06-2010).
− Skala pengukuran : numerik.
− Lapisan amnion:
Lapisan yang terdiri dari epitel amnion, membran basal, lapisan kompak,
lapisan fibroblas, lapisan intermediat (spongy).
− Lapisan korion:
− Tebal lapisan amnion:
Ketebalan yang diukur dari batas atas epitel amnion sampai batas bawah
lapisan intermediat (spongy).
− Tebal lapisan korion:
Ketebalan yang diukur dari batas bawah lapisan intermediat (spongy)
sampai batas bawah membran basal (batas atas trophoblast).
− Tebal kolagen lapisan amnion:
Ketebalan yang diukur dari batas bawah epitel amnion sampai batas bawah
lapisan intermediat (spongy)
− Tebal kolagen lapisan korion:
Ketebalan yang diukur dari batas bawah lapisan intermediat (spongy)
sampai batas bawah membran basal (batas atas trophoblast).
− Acetylsalicylic acid (ASA) dosis rendah
Acetylsalicylicacid(ASA) dosis 80-100 mg
− Kekuatan intensitas pewarnaan imunohistokimia
Penilaian intensitas tampilan pewarnaan dengan ketentuan : 0 = negatif
1 = lemah 2 = sedang 3 = kuat
− Luas tampilan pewarnaan imunohistokimia
Penilaian luas tampilan pewarnaan dengan ketentuan : 0 = negatif
− Tampilan imunohistokimia
Perkalian kekuatan intensitas pewarnaan dengan luas tampilan pewarnaan
imunohistokimia dengan penilaian skor :
0 = negatif
1-3 = tampilan lemah 4-6 = tampilan sedang 7-9 = tampilan kuat
(modifikasi quantitative method score/Q-score)
− Hasil pengukuran: dinyatakan dalam Q-score.
− Alat ukur: sediaan imunohistokimia (IHC) selaput ketuban, mikroskop
cahaya merk Olympus CX21
− Skala pengukuran : kategorik
3.9. Bahan dan alat penelitian
3.9.1 Bahan penelitian
− Jaringan selaput ketuban
− Larutan neutral buffered formalin, larutan alkohol 70%, 80%, 90%,
95%, 100%, aseton, xylol, parafin, albumin, gliserin, timol, larutan
haematoxylin , larutan eosin, entelan balsam Canada, antibodi fibronektin
14-9869 clone FN-3mouse anti-human
3.9.2 Alat penelitian
purified eBioscience.
− Mikrotom (Leica RM 2245), blade mikrotom (Leica) kaset, cetakan blok
parafin, lemari pendingin, waterbath, hot plate (Thermo), stainning jar,
stanning rack, sengkelit, glas objek, glas penutup, vortex, automatic
+Axiocam ERc5s yang dilengkapi software Axiovision Rel. 4.8.2
(06-2010).
3.10 Prosedur penelitian
3.10.1 Pengumpulan data
1. Perempuan hamil (20-45 tahun) yang mendapatkan acetylsalisilic acid
(ASA) dosis rendah (80-100 mg) yang memenuhi kriteria penelitian
diminta kesediaannya untuk ikut serta dalam penelitian.
2. Subjek yang bersedia ikut serta dalam penelitian, diminta
persetujuannya dalam bentuk informed consent tertulis. Pada calon
subjek penelitian satu persatu diberikan penjelasan secara lisan dan
tulisan tentang tujuan, manfaat dan prosedur penelitian.
3. Pada saat subjek mengalami persalinan, dilakukan pengambilan sampel
selaput ketuban di rumah sakit/klinik tempat subjek melakukan
persalinan untuk dilakukan pemeriksaan makroskopis selaput ketuban.
4. Kemudian dilakukan fiksasi jaringan selaput ketuban dan dibawa ke
laboratorium Patologi Anatomi Fakultas Kedokteran Universitas
Sumatera Utara untuk dilakukan pemeriksaan histopatologi dan
imunohistokimia fibronektin.
3.10.2 Prosedur perlakuan jaringan
Setelah menentukan daerah yang ruptur pada selaput ketuban, dibuat
daerah dengan lebar sekitar 10 cm. Dengan menggunakan forsep, bagian yang
selaput ketuban. Kemudian gulungan jaringan tersebut difiksasi dan dilakukan
pengirisan.
Gambar 3.2 Pembuatan gulungan selaput ketuban (dikutip dari Benirschke and
Kaufmann, 2006)
3.10.3 Prosedur pembuatan sediaan histopatologi
a. Fiksasi
− Jaringan dimasukkan ke dalam larutan neutral buffered formalin,
dan difiksasi selama 18-24 jam.
− Setelah itu, jaringan dimasukkan ke dalam larutan aquadest
selama 1 jam; ini bertujuan untuk penghilangan larutan fiksasi.
b. Dehidrasi
− Potongan jaringan dimasukkan dalam alkohol konsentrasi
bertingkat 70%, 80%, 90% (masing-masing 1 hari) alkohol 95%
selama 2 hari, 2 kali pergantian alkohol 100% selama 2 hari,
2 kali pergantian
c. Penjernihan (clearing)
− Jaringan direndam di dalam larutan xylol sebanyak 20 kali volume
d. Pembenaman/ infiltrasi (Impregnasi)
− Jaringan dimasukkan ke dalam parafin cair dan disimpan di oven
yang bersuhu 60⁰C, selama 3 x 1 jam.
e. Pengecoran (Blocking)
− Parafin dituang secukupnya pada cetakan, kemudian letakkan
jaringan pada dasar cetakan dan beri label.
f. Pengirisan (Sectioning)
− Blok paraffin diiris dengan mikrotom dengan ketebalan potongan ±
5-10 µm
− Atur jarak preparat yang dipegang holder kearah pisau sedekat
mungkin
− Gerakkan rotor pada mikrotom secara ritmis searah jarum jam.
− Buang pita parafin awal yang tanpa jaringan.
− Setelah irisan mengenai jaringan, iris blok paraffin hati-hati.
− Pita paraffin yang diinginkan dipindahkan dengan sengkelit ke atas
air dalam waterbath suhu 55⁰C
− Setelah pita parafin terkembang dengan baik, tempelkan pada kaca
objek yang telah disalut (50 ml albumin + 50 ml gliserin + sedikit
timol dan disimpan pada refrigerator bersuhu 4⁰C)
− Kaca objek yang berisi pita paraffin dibiarkan mengering
g. Pewarnaan dengan Haematoxylin dan Eosin
− Jaringan pada kaca objek dilakukan deparafinisasi dengan xylol
selama 2x2 menit.
− Hidrasi dengan alkohol 100% (selama 2x2 menit); alkohol 95%
(selama 2 menit); 90% (selama 2 menit), 80% (selama 2 menit);
70% (selama 2 menit); air kran (selama 3 menit).
− Inkubasi dalam larutan Haematoxylin Mayer selama beberapa
menit.
− Cuci dalam air kran mengalir selama 15-20 menit.
− Observasi di bawah mikroskop, bila masih terlalu biru cuci lagi
dengan air mengalirbbeberapa menit. Bila sudah cukup warna
lanjutkan dengan counterstaining.
− Counterstaining dengan Eosinworkingsolution beberapa menit.
− Dehidrasi dengan larutan alkohol dengan gradasi peningkatan
persentase dari 70%, 80%, 90%, 95%, 100% (masing-masing
selama 2 menit).
− Inkibasi dengan Xylol 2x masing-masing selama 2 menit.
− Mounting dengan EntellanTM
− Beri label dan biarkan hingga entellan mongering. Hasil pewarnaan
pada inti berwarna biru dan sitoplasma berwarna kemerahan. balsam Kanada dan coverglass.
3.10.4 Pembacaan/interpretasi sediaan (slide) histologi (pengukuran ketebalan jaringan)
ERc5s. Tiap sediaan diperiksa pada 3 area (dengan arah jam 12; teknik Fujikura)
(Benirschke and Kaufmann, 2006) yang masing-masing mewakili tiap lapisan
dari gulungan selaput ketuban.
Prosedur pembacaan dilakukan sebagai berikut: Setelah sediaan
diletakkan di mikroskop, dipilih lapang pandang dengan pembesaran 10 kali. Pada
monitor komputer yang dilengkapi software Axiovision Rel. 4.8.2 (06-2010)
tampak beberapa MENU pilihan. Pada toolbar tampak MENU Live, lalu
ditentukan area yang akan diukur, pilih MENU Snap kemudian Measure. Dari
menu ini dipilih option Length dan dengan menggunakan mouse tarik garis dari
batas bawah epitel aminon sampai batas bawah membran basal korion pada
daerah yang berwarna merah sesuai dengan gambaran kolagen dari pewarnaan
tersebut. Hasil tersebut adalah ketebalan kolagen pada lapisan amnion dan korion.
Data gambar dan hasil pembacaan kemudian disimpan dalam file.
3.10.5 Prosedur pembuatan sediaan (slide) imunohistokimia
1. Dilakukan deparafinisasi sediaan dengan memasukkan sediaan
ke dalam larutan xylol 1, xylol 2 dan xylol 3 selama masing-masing
5 menit
2. Kemudian dilakukan proses rehidrasi untuk menghilangkan sisa xylol
dengan menggunakan larutan alkohol absolut, alkohol 90%, alkohol
80%, alkohol 70% selama masing-masing 4 menit
3. Lalu sediaan dicuci di bawah air mengalir selama 5 menit
4. Masukkan sediaan ke dalam mesin pengering merk PT Link Dako
Epitop Retrieval lalu diatur set up preheat 65 ⁰C, running time 98⁰ C
5. Selanjutnya jaringan pada sediaan dilingkari dengan spidol Pap pen
agar pada saat penetesan antibody atau cairan lainnya tidak keluar
melewati batas lingkaran Pap pen. Kemudian segera dimasukkan ke
dalam larutan Tris Buffered Saline (TBS) pH 7,4 selama 5 menit
6. Kemudian dilakukan blocking dengan peroksidase selama 5-10 menit
dan dicuci TBSpH 7,4 selama 5 menit
7. Selanjutnya dilakukan blocking dengan Normal Horse Serum (NHS
3%) selama 15 menit dan dicuci dengan TBS pH 7,4 selama 5 menit
8. Jaringan pada sediaan ditetesi antibodi primer (antibodi anti-Human
fibronectin purified clone FN-3 eBioscience
9. Lalu dicuci kembali dengan TBS pH 7,4 dan Tween 20 selama
5 menit
) dengan pengenceran
1 : 100 dan di-inkubasi selama 1 jam
10. Selanjutnya jaringan pada sediaan ditetesi Dako Real Envision
Rabbit/Mouse dan inkubasi selama 30 menit dan kembali dicuci
dengan TBSpH 7,4 dan Tween 20 selama 5 -10 menit)
11. Jaringan pada sediaan ditetesi Diamino Benzidine (DAB)+substrat
chromogen solution dengan pengenceran 20 µl DAB: 1000 µl substrat
dan diinkubasi selama 5 menit lalu dicuci kembali dengan air mengalir
12. Selanjutnya dilakukan pewarnaan dengan Hematoxylin selama
10 menit
13. Cuci dibawah air mengalir selama 5 menit dan celupkan sediaan ke
dalam lithium karbonat (5% dalam aqua) selama 2 menit dan cuci
14. Selanjutnya dilakukan proses pengeringan melalui proses dehidrasi
dengan menggunakan alkohol 80%, alkohol 90% dan alkohol absolut
selama masing-masing 5 menit
15. Kemudian dilakukan clearing dengan menggunakan larutan xylol 1,
xylol 2 dan xylol 3, masing-masing 5 menit
16. Selanjutnya dilakukan mounting dan tutup sediaan dengan coverglass
dan sediaan siap untuk dinilai. (Singapore General Hospital/SGH
methode)
3.10.6 Pembacaan/interpretasi sediaan (slide) imunohistokimia (tampilan fibronektin pada jaringan)
Setelah sediaan diletakkan pada mikroskop, dipilih pembesaran 4x untuk
menilai luas tampilan dan pembesaran 100x untuk menilai intensitas pewarnaan.
Penilaian tampilan pewarnaan imunohistokimia fibronektin sebagai berikut:
− Kontrol positif digunakan jaringan human plasenta normal yang berfungsi
sebagai pembanding tampilan warna coklat yang terwarnai dari hasil
pewarnaan imunohistokimia.
− Sediaan yang tertampil warna coklat pada membran sitoplasma dikatakan
positif dan negatif bila tidak tertampil warna coklat.
− Penilaian intensitas pewarnaan dengan cara membandingkan sediaan sampel
penelitian dengan sediaan kontrol.
Intensitas tampilan :
0 = tidak tertampil warna coklat/negatif
Luas tampilan :
1 = luas tampilan warna coklat yang tertampil< 25% 2 = luas tampilan warna coklat yang tertampil 25-50% 3 = luas tampilan warna coklat yang tertampil >50%
Tampilan imunohistokimia :
0 = negatif
1 - 3 = tampilan lemah 4 - 6 = tampilan sedang 7 - 9 = tampilan kuat
3.10.7 Keandalan
− Pengukuran ketebalan selaput ketuban dilakukan oleh peneliti dengan
koefisien variasi < 10%.
− Penilaian/pembacaan sediaan imunohistokimia dilakukan oleh peneliti dan
satu orang ahli patologi anatomi dengan cara tersamar. Inter-rater
reliability (keandalan antar pemeriksa) ditetapkan dengan perbedaan tidak
lebih dari satu tingkat skor.
3.11 Pengolahan dan analisis data
Data dipresentasikan dalam bentuk rata-rata ± simpangan baku (rerata ±
SD). Untuk penilaian perbedaan gambaran histopatologi (rerata ketebalan selaput
ketuban) antara subjek dilakukan uji normalitas dan homogenitas data. Jika data
berdistribusi normal dan homogen maka dilakukan uji t tidak berpasangan. Jika
distribusi data tidak normal atau tidak homogen, dilakukan uji Mann-Whitney.
Untuk penilaian perbedaan tampilan imunohistokimia antara subjek,
uji Chi square, bila syarat tidak terpenuhi lakukan uji Fisher. Semua analisis data
dilakukan dengan menggunakan SPSS versi 20.0.
3.12 Etik penelitian
Penelitian akan dilaksanakan setelah mendapat persetujuan dari Komisi Etik
Penelitian Fakultas Kedokteran Universitas Sumatera Utara.
Kepada calon sampel penelitian, diberikan penjelasan tertulis dan lisan
tentang tujuan, manfaat serta prosedur penelitian. Pasien berhak menolak untuk
ikut serta dalam penelitian, dan bagi pasien yang bersedia ikut serta dimintakan
persetujuan dengan informed consent tertulis. Identitas subjek penelitian
dirahasiakan.
Seluruh biaya yang berhubungan dengan penelitian ditanggung oleh peneliti
dan kepada subjek penelitian diberikan imbalan sesuai kemampuan peneliti.
3.13 Jadwal penelitian
Keseluruhan kegiatan penelitian ini dapat dilihat pada Tabel 3.1
Tabel 3.1 Jadwal penelitian
No Kegiatan Mar
3 Pengolahan dan analisa data xx
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
Berdasarkan penelitian yang telah dilakukan, didapatkan hasil pengukuran
ketebalan selaput ketuban (ketebalan lapisan amnion dan korion) dan tampilan
fibronektin dengan pewarnaan imunohistokimia pada selaput ketuban 2 kelompok
pengamatan, yaitu: kelompok kontrol (tidak mendapat ASA) dan kelompok kasus
(mendapat ASA dosis rendah).
4.1.1 Perbandingan ketebalan selaput ketuban pada kelompok kasus (mendapat ASA dosis rendah) dan kelompok kontrol (tidak mendapat ASA)
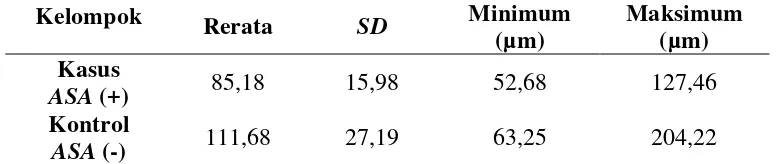
Tabel 4.1 Rerata dan simpangan baku ketebalan selaput ketuban pada kelompok kasus dan kelompok kontrol
Kelompok Rerata SD Minimum
Keterangan: SD (Standard deviation)/simpangan baku
Tabel 4.1 menunjukkan bahwa rerata ketebalan selaput ketuban kelompok
kasus (85,18±15,98) lebih tipis dibandingkan kelompok kontrol (111,68±27,19).
Pada kelompok kasus, selaput ketuban yang paling tipis adalah 52,68 µm dan
yang paling tebal adalah 127,46 µm; sedangkan pada kelompok kontrol,
204,22 µm. Grafik histogram ketebalan selaput ketuban pada masing-masing
kelompok ditampilkan pada Gambar 4.1.
Gambar 4.1 Grafik rerata ketebalan selaput ketuban (lapisan amnion dan korion) pada kelompok kasus dan kontrol (*p<0,05)
Hasil perhitungan analisis statistik terhadap rerata ketebalan selaput
ketuban pada kelompok kasus dan kontrol disajikan pada lampiran 6, dan dapat
dilihat dalam bentuk grafik histogram (Gambar 4.1).
Dari hasil uji normalitas dan homogenitas data, ternyata data dari hasil
penelitian tidak terdistribusi normal dan tidak homogen, sehingga dilakukan
pengulangan transformasi data sebanyak 3 kali, tetapi distribusi data masih tetap
tidak normal. Dengan demikian uji statistik dilakukan dengan uji non- parametrik
Mann Whitney.
Hasil uji statistik Mann Whitney menunjukkan adanya perbedaan yang
bermakna antara tebal selaput ketuban pada kelompok kasus dan kelompok
kontrol (p<0,05).
4.1.2 Perbandingan kekuatan intensitas pewarnaan imunohistokimia fibronektin pada selaput ketuban kelompok kasus (mendapat ASA dosis rendah) dan kelompok kontrol (tidak mendapat ASA)
Tabel 4.2 Rerata dan simpangan baku kekuatan intensitas pewarnaan imunohistokimia fibronektin pada selaput ketuban kelompok kasus dan kontrol
Kelompok Rerata SD Minimum
(skor)
Maksimum (skor)
Kasus
ASA (+)
0,89 0,64 0 2
Kontrol
ASA (-) 1,87 0,65 1 3
Keterangan: SD (Standard deviation)/simpangan baku
Tabel 4.2 menunjukkan bahwa kekuatan intensitas pewarnaan
imunohistokimia fibronektin selaput ketuban pada kelompok kasus (0,89±0,64)
tertampil lebih lemah dibandingkan kelompok kontrol (1,87±0,65). Pada
kelompok kasus, skor kekuatan intensitas pewarnaan yang tertampil paling
rendah adalah 0 dan skor yang paling tinggi adalah 2; sedangkan pada kelompok
kontrol skor kekuatan intensitas pewarnaan yang tertampil paling rendah adalah 1
dan skor yang paling tinggi adalah 3. Grafik histogram kekuatan intensitas
pewarnaan imunohistokimia fibronektin selaput ketuban pada masing-masing
Gambar 4.2. Grafik rerata kekuatan intensitas pewarnaan imunohistokimia fibronektin pada kelompok kasus dan kontrol (*p<0,05)
Hasil perhitungan analisis statistik rerata kekuatan intensitas pewarnaan
imunohistokimia fibronektin pada kelompok kontrol dan kasus, disajikan pada
lampiran 6, dan dapat dilihat dalam bentuk grafik histogram (Gambar 4.2).
Penilaian perbedaan kekuatan intensitas pewarnaan imunohistokimia
fibronektin antar kelompok, tidak memenuhi syarat untuk uji Chi Square maupun
uji Fisher, sehingga analisis data dilanjutkan dengan uji Mann Whitney, yang
menunjukkan adanya perbedaan bermakna antara kekuatan intensitas pewarnaan
imunohistokimia fibronektin selaput ketuban pada kelompok kasus dan kelompok