OPTIMASI DAN EVALUASI MIKROENKAPSULASI
MEDROKSIPROGESTERON ASETAT TERSALUT
POLI(
ε
-KAPROLAKTON)-LILIN LEBAH
GUSLINA ISRIANY
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
GUSLINA
ISRIANY.
Optimasi
dan
Evaluasi
Mikroenkapsulasi
Medroksiprogesteron Asetat Tersalut
Poli(ε
-kaprolakton)-Lilin Lebah. Dibimbing
oleh TETTY KEMALA dan AHMAD SJAHRIZA.
Salah satu teknik menyalut obat dengan suatu material polimer adalah
mikroenkapsulasi. Tujuan enkapsulasi obat adalah mengendalikan pelepasan obat
sehingga
efek
samping
obat
dapat
dikurangi.
Pada
penelitian
ini,
medroksiprogesteron asetat (MPA) disalut oleh
poli(ε
-kaprolakton) (PCL) dan
lilin lebah. Emulsifikasi-penguapan pelarut merupakan metode yang digunakan
untuk membuat mikrokapsul MPA dengan ragam nisbah PCL:lilin lebah 7:3; 8:2;
dan 9:1 dan konsentrasi pengemulsi poli(vinil alkohol) 1%; 2%; dan 3%. Efisiensi
mikrokapsul tertinggi adalah 83.47% pada mikrokapsul dengan nisbah PCL:lilin
lebah 9:1 dan konsentrasi PVA 3%. Kinetika pelepasan MPA mengikuti model
kinetika Korsmeyer-Peppas dengan mekanisme pelepasan obat
super case-II
transport
. Mikrokapsul yang dihasilkan memiliki kisaran ukuran 67
–
144
m
dengan inti yang terdispersi secara homogen pada matriks polimer.
ABSTRACT
GUSLINA ISRIANY. Optimization and Evaluation of Medroxyprogesterone
Acetate (MPA) Microcapsules Coated Poly(
ε
-caprolactone)-Beeswax. Supervised
by TETTY KEMALA and AHMAD SJAHRIZA.
OPTIMASI DAN EVALUASI MIKROENKAPSULASI
MEDROKSIPROGESTERON ASETAT TERSALUT
POLI(
ε
-KAPROLAKTON)-LILIN LEBAH
GUSLINA ISRIANY
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Disetujui
Pembimbing I
Dr Tetty Kemala, SSi, MSi
NIP 19710407 199903 2 001
Pembimbing II
Drs Ahmad Sjahriza
NIP 19620406 198903 1 002
Diketahui
Ketua Departemen Kimia
Prof Dr Ir Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
Tanggal Lulus :
Judul
: Optimasi dan Evaluasi Mikroenkapsulasi Medroksiprogesteron
Asetat Tersalut
Poli(ε
-kaprolakton)-Lilin Lebah
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas berkat limpahan
rahmat dan hidayah-Nya, penulis dapat menyelesaikan karya ilmiah dengan judul
Optimasi dan Evaluasi Mikroenkapsulasi Medroksiprogesteron Asetat Tersalut
Poli
(ε
-kaprolakton)-Lilin Lebah. Salawat serta salam semoga selalu tercurahkan
kepada Nabi Muhammad SAW, keluarganya, dan semoga kita menjadi
pengikutnya hingga akhir zaman.
Penulis mengucapkan terima kasih kepada Ibu Dr Tetty Kemala, SSi, MSi
dan Bapak Drs Ahmad Sjahriza selaku pembimbing yang senantiasa memberikan
arahan, dorongan semangat, dan doa kepada penulis selama melaksanakan
penelitian. Penulis juga mengucapkan terima kasih kepada staf Laboratorium
Anorganik (Pak Syawal, Pak Mulyadi, Pak Caca dan Bu Nurul), serta staf
laboratorium lainnya, yaitu Pak Sabur, Pak Suherman, Bu Nunung, dan Mas Eko
atas bantuan serta masukan selama penelitian berlangsung.
Terima kasih tak terhingga penulis ucapkan kepada Ibu, Ayah, serta
seluruh keluarga, atas doa dan kasih sayangnya. Ucapan terima kasih juga penulis
ucapkan kepada Kak Gina, Kak oji, Kak Bedur, Kak Putri, Kamela, Asa, linda,
Nisa, Ade, Nena, Ryna, Gita, Hafid, Wahyu, Hapsah, Wide, teman-teman kimia
45, dan teman-teman Ikatan Mahasiswa Tapanuli Selatan (Hilda, Dayat, Tagor,
Leman) yang telah membantu memberi masukan dan saran selama pelaksanaan
penelitian. Penulis berharap karya ilmiah ini dapat bermanfaat bagi perkembangan
ilmu pengetahuan.
Bogor, Juli 2012
RIWAYAT HIDUP
Penulis dilahirkan di Padangsidimpuan pada tanggal 11 Agustus 1990 dari
Alm. Muhammad Isrok Harahap, SH dan Hotnitawaty Siregar. Penulis adalah
anak pertama dari 4 bersaudara. Tahun 2008 penulis lulus dari SMA Negeri 1
Padangsidimpuan dan pada tahun yang sama penulis lulus seleksi masuk Institut
Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI) dan
diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE
Bahan dan alat... 1
Metode ... 2
HASIL DAN PEMBAHASAN
Mikroenkapsulasi medroksiprogesteron asetat ... 2
Panjang gelombang maksimum dan kurva standar ... 3
Efisiensi mikrokapsul ... 3
Pelepasan bahan aktif ... 4
Kinetika pelepasan bahan aktif ... 5
Morfologi mikrokapsul ... 5
SIMPULAN DAN SARAN
Simpulan ... 6
Saran ... 6
DAFTAR PUSTAKA ... 6
DAFTAR TABEL
Halaman
1
Komposisi mikrokapsul MPA tersalut paduan PCL-lilin lebah ... 2
2
Parameter pelepasan MPA dari mikrokapsul formula CC ... 5
DAFTAR GAMBAR
Halaman
1
Mikrokapsul MPA tersalut PCL-lilin lebah ... 3
2
Tahap pembentukan mikrokapsul dengan metode emulsifikasi-penguapan
pelarut ... 3
3
Efisiensi mikrokapsul MPA dengan konsentrasi PVA (A) = 1%; (B) = 2%;
dan (C) = 3% ... 4
4
Pelepasan MPA dari mikrokapsul formula CC terhadap waktu (menit) pada
medium asam ... 4
5
Pelepasan MPA dari mikrokapsul formula CC terhadap waktu (menit) pada
medium basa. ... 4
6
Foto mikroskop mikrokapsul kosong dan dengan mikrokapsul MPA pada
perbesaran 10× dan 40× ... 5
7
Foto SEM mikrokapsul MPA pada perbesaran 1200×, 400×, dan 150× ... 6
DAFTAR LAMPIRAN
Halaman
1
Diagram alir penelitian ... 9
2
Spektrum absorbansi MPA ... 10
3
Kurva standar MPA ... 11
4
Efisiensi mikrokapsul MPA tersalut PCL-lilin lebah ... 12
5
Persentase rerata pelepasan MPA dalam uji disolusi dari mikrokapsul
formula CC tersalut PCL-lilin lebah ... 13
6
Pelepasan MPA dalam mikrokapsul formula CC pada waktu t ... 15
PENDAHULUAN
Medroksiprogesteron asetat (MPA) merupakan senyawa aktif kontrasepsi hormon steroid (meliputi kontrasepsi oral, injeksi, dan implan) yang sangat efektif dan digunakan secara luas. Prinsip kerja MPA adalah mencegah ovulasi, mengentalkan lendir serviks, menipiskan selaput lendir rahim, dan menghambat transportasi gamet. Kontrasepsi MPA biasanya dikonsumsi oleh perempuan reproduktif, yaitu 15–49 tahun dan rentang waktu konsumsi obat ini 24–36 jam. Selain dapat menyebabkan penambahan bobot badan, osteoporosis, dan gangguan haid, senyawa ini juga dapat meningkatkan ovulasi jika dikonsumsi lebih dari 36 jam (Diza 2008). Sistem pengantaran obat secara khusus diperlukan MPA untuk mengatasi hal tersebut. Mikroenkapsulasi merupakan proses penyalutan zat aktif padat atau cair dengan suatu material polimer dalam bentuk mikrokapsul (Wang et al. 2006). Di bidang farmasi, teknologi enkapsulasi bertujuan mengurangi rasa pahit obat, memisahkan material yang tidak kompatibel, mencegah kerusakan obat yang diakibatkan oleh uap air dan cahaya, mengurangi risiko iritasi lokal organ atau jaringan yang ditimbulkan obat, mengendalikan pendistribusian obat, serta mengoptimalkan penyerapan obat (Appara et al. 2010; Gowda et al. 2009).
Bahan penyalut mikrokapsul yang banyak digunakan saat ini adalah golongan poliester alifatik yang bersifat degradabel. Salah satunya adalah poli(ε-kaprolakton) (PCL). Poli(ε-kaprolakton) memiliki permeabilitas tinggi, biodegradabel, biokompatibel, dan tidak beracun. Di sisi lain, PCL memiliki kristalinitas yang tinggi dan waktu degradasi yang lama. Pencampuran PCL dengan makromolekul dapat dilakukan untuk mengatasi hal tersebut (Porjazoska et al. 2004).
Lilin lebah merupakan makromolekul yang terdiri atas n-alkana jenuh dan takjenuh, ester rantai panjang, asam lemak, diester, hidroksiester, dan penyusun minor lainnya, seperti flavonoid (Garnier et al. 2002). Lilin lebah dapat digunakan sebagai bahan penyalut mikrokapsul dan memiliki beberapa kelebihan, yaitu stabil pada beberapa nilai pH dan tingkat kelembapan, biokompatibel, tidak imunogenik, tidak beracun, dan tidak menyebabkan peningkatan dosis obat (Ranjha
et al. 2010). Campuran PCL dengan lilin
lebah diharapkan menghasilkan polimer kompatibel yang memiliki permeabilitas dan
waktu degradasi lebih baik, serta mempermudah pencampuran bahan aktif dengan matriks paduan. Bahan aktif yang tidak larut air seperti MPA akan mudah bercampur dengan matriks lilin lebah dan menunjukkan tingkat penyerapan yang baik (Gowda et al. 2009). Selain itu, pencampuran tersebut dapat mengurangi biaya yang dibutuhkan karena lilin lebah relatif lebih murah dibandingkan dengan PCL.
Salah satu metode yang banyak digunakan untuk pengungkungan bahan aktif hidrofobik seperti MPA adalah metode emulsifikasi-penguapan pelarut (Park et al. 2005). Pada metode ini, dibutuhkan pengemulsi seperti poli(vinil alkohol) (PVA) untuk menstabilkan larutan polimer dan obat dengan air. Poli(vinil alkohol) sudah banyak digunakan sebagai pengemulsi dalam pembuatan mikrokapsul tersalut-poliester. Gugus hidroksil (hidrofilik) dari PVA yang bersifat polar akan berikatan dengan molekul air, sedangkan rantai vinilnya (hidrofobik) akan berikatan dengan polimer (PCL-lilin lebah) sehingga emulsi menjadi lebih stabil (Guo et al. 2007). Menurut Kemala et al. (2012), besarnya konsentrasi PVA yang digunakan akan mempengaruhi stabilitas emulsi dan ukuran kapsul. Ukuran kapsul yang seragam meningkatkan efisiensi dan laju disolusi bahan aktif yang telah dikungkung.
Penelitian ini bertujuan membuat mikrokapsul MPA tersalut PCL-lilin lebah, menganalisis efisiensi mikrokapsul MPA, mempelajari pengaruh variasi nisbah PCL:lilin lebah dan konsentrasi pengemulsi terhadap mikrokapsul yang dihasilkan, mempelajari model kinetika pelepasan MPA berdasarkan koefisien determinasi (R2) dengan menggunakan persamaan orde reaksi ke-0, ke-1, dan Korsmeyer-Peppas, serta mempelajari morfologi mikrokapsul.
BAHAN DAN METODE
Bahan dan alatBahan-bahan yang digunakan dalam penelitian ini adalah PCL (Sigma Aldrich, Germany), lilin lebah, PVA (Merck), MPA (BKKBN), diklorometana, etanol 96%, larutan HCl pH 1.2, dan larutan bufer fosfat (NaH2PO4-Na2HPO4) pH 7.4. Alat-alat yang
Metode
Penelitian ini dilakukan dalam beberapa tahapan (Lampiran 1), meliputi pembuatan mikrokapsul MPA, uji efisiensi mikrokapsul MPA, uji disolusi mikrokapsul, dan penentuan kinetika pelepasan obat, serta uji karakteristik mikrokapsul yang dihasilkan dengan mikroskop dan SEM.
Pembuatan mikrokapsul MPA (Dinarvand
et al. 2005)
PCL dan lilin lebah dilarutkan dalam diklorometana kemudian diaduk hingga homogen. Setelah itu, MPA dicampurkan ke dalam larutan paduan tersebut. Campuran kemudian didispersikan ke dalam air yang mengandung PVA menggunakan motor pengaduk, lalu didekantasi hingga mikrokapsul yang terbentuk mengendap. Mikrokapsul yang diperoleh disaring, dicuci dengan akuades, dan dikeringudarakan selama 1 hari. Variasi nisbah PCL:lilin lebah dan konsentrasi PVA yang digunakan dapat dilihat pada Tabel 1.
Tabel 1 Komposisi mikrokapsul MPA tersalut polipaduan PCL-lilin lebah
Formula Nisbah PCL:lilin lebah
Konsentrasi PVA
(%)
AA 7:3 1
AB 8:2 1
AC 9:1 1
BA 7:3 2
BB 8:2 2
BC 9:1 2
CA 7:3 3
CB 8:2 3
CC 9:1 3
Penentuan panjang gelombang maksimum dan pembuatan kurva standar
Panjang gelombang maksimum ( maks)
larutan MPA 10 ppm dalam etanol 96% ditentukan pada rentang panjang gelombang
( ) 240–400 nm menggunakan spekrofotometer UV-Vis. Panjang gelombang
maksimum ( maks) yang diperoleh digunakan
untuk analisis selanjutnya.
Kurva standar dibuat dengan mengukur absorbans larutan MPA dengan konsentrasi 2, 4, 6, 10, 12, 14, 18, dan 20 ppm pada panjang gelombang maksimum. Hasil yang diperoleh merupakan hubungan konsentrasi MPA dengan absorbans.
Efisiensi mikrokapsul (Ibezim et al. 2011)
Sebanyak 2.5 mg mikrokapsul dilarutkan dalam 20 mL etanol 96%, diaduk dengan pengaduk magnetik selama 3 jam, dan filtratnya disaring. Absorbans filtrat dibaca dengan spektrofotometer UV-Vis pada panjang gelombang maksimum. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi MPA dengan bantuan kurva standar.
Uji disolusi secara in vitro (Herdini et al.
2010)
Sebanyak 200 mg mikrokapsul yang diperoleh pada kondisi optimum didisolusi dalam 900 mL medium simulasi (larutan HCl pH 1.2 dan bufer fosfat pH 7.4) menggunakan alat disolusi tipe 2 (tipe dayung). Pengujian dilakukan pada suhu (37 ± 0.5) °C dengan kecepatan pengadukan 100 rpm selama 360 menit. Setiap 15 menit, alikuot diambil sebanyak 10 mL selama 360 menit. Setiap kali pengambilan alikuot, volume medium simulasi yang terambil digantikan dengan medium simulasi yang baru dengan volume dan suhu yang sama. Alikuot disaring dan ditentukan serapan MPA dengan spektrofotometer UV-Vis pada maks. Data
pengukuran yang diperoleh digunakan untuk mempelajari model kinetika pelepasan MPA. Morfologi mikrokapsul
Pengamatan morfologi mikrokapsul dilakukan terhadap 1 formula dengan menggunakan mikroskop cahaya dan SEM. Pengamatan menggunakan SEM dilakukan dengan cara melapisi mikrokapsul dengan emas dan dilihat pada pembesaran 1200×, 400×, dan 150×.
HASIL DAN PEMBAHASAN
Mikroenkapsulasi MPA
Gambar 1 Mikrokapsul MPA tersalut PCL-lilin lebah.
Metode yang digunakan untuk pembuatan mikrokapsul adalah emulsifikasi-penguapan pelarut, yaitu bahan penyalut (PCL dan lilin lebah) dan bahan aktif (MPA) dilarutkan dalam pelarut organik (diklorometana) kemudian didispersikan dalam air yang berisi pengemulsi sehingga terbentuk mikrokapsul (Gambar 2). Obeidat (2009) menyatakan bahwa metode emulsi-penguapan pelarut menghasilkan mikrokapsul dengan mekanisme pelepasan material yang dikungkung secara optimum karena material tersebut terdispersi secara homogen pada matriks polimer sehingga ideal untuk sistem pengantaran bahan aktif.
Gambar 2 Tahap pembentukan mikrokapsul dengan metode emulsifikasi
-penguapan pelarut (Kim et al. 2005).
Diklorometana digunakan sebagai pelarut karena menguap pada suhu 39 °C sehingga penguapan pelarut berlangsung cepat. Bodmeier et al. (1988) dalam Yeo dan Park (2004) menyatakan bahwa diklorometana merupakan pelarut terbaik untuk poliester dibandingkan dengan kloroform atau benzena, dan dapat menghasilkan efisiensi mikrokapsul lebih tinggi.
Pengemulsi yang digunakan adalah PVA yang merupakan polimer ampifilik dan mampu teradsorpsi pada antarmuka (Buttini et al. 2008). Pengemulsi berfungsi menstabilkan emulsi larutan paduan PCL-lilin lebah dan MPA dalam diklorometana dengan air melalui pengikatan gugus hidroksil (hidrofilik) PVA dengan molekul air, dan rantai vinil (hidrofobik) dengan diklorometana (Guo et al. 2007).
Panjang gelombang maksimum dan kurva standar
Panjang gelombang maksimum ( maks)
larutan MPA diperoleh pada 241.6 nm (Lampiran 2). Nilai maks ini tidak berbeda
jauh dengan nilai maks progesteron, yaitu 240
nm (Bilensoy et al. 2006). Penentuan maks
dilakukan pada daerah ultraviolet karena larutan MPA tidak berwarna. Sensitivitas pengukuran yang maksimum diperoleh ketika sampel diukur pada maks (Mikaela 2008).
Persamaan kurva standar yang diperoleh adalah y = 0.0325x + 0.0429 dengan nilai koefisien korelasi (r) 0.9984 (Lampiran 3). Persamaan kurva standar tersebut digunakan dalam perhitungan efisiensi enkapsulasi dan persentase pelepasan MPA. Kurva standar yang digunakan telah memenuhi syarat karena nilai korelasinya lebih besar dari 0.9900. Nilai
r yang tinggi menunjukkan tingkat kesesuaian atau linearitas antara sinyal detektor terukur (respons) dan konsentrasi MPA (analit) dalam sampel, sehingga galat sistematik selama pengukuran dapat diabaikan (Mikaela 2008).
Efisiensi mikrokapsul
Efisiensi mikrokapsul merupakan salah satu parameter yang menunjukkan keberhasilan proses enkapsulasi. Efisiensi menunjukkan persen senyawa aktif (MPA) yang dapat disalut dalam mikrokapsul. Semakin tinggi efisiensi mikrokapsul berarti semakin banyak MPA yang tersalut.
Efisiensi mikrokapsul yang dihasilkan berkisar 51.55–83.47% (Gambar 3). Efisiensi mikrokapsul terendah dihasilkan oleh mikrokapsul formula AA, dan efisiensi tertinggi dihasilkan oleh mikrokapsul formula CC. Perbedaan hasil ini dipengaruhi oleh nisbah paduan PCL-lilin lebah, yaitu 7:3 pada mikrokapsul AA dan 9:1 pada mikrokapsul CC. Lilin lebah yang lebih banyak pada penyalut menyebabkan komponen penyalut dengan bobot molekul rendah bertambah sehingga akan lebih sulit untuk mengungkung MPA. Lilin lebah memiliki bobot molekul sekitar 868 g mol-1. Halder dan Sa (2006) dalam Maulidyawati (2009) menyatakan bahwa salah satu faktor yang menyebabkan tingginya efisiensi mikrokapsul adalah nisbah antara bahan penyalut dan bahan inti. Semakin banyak jumlah penyalut, kemampuannya untuk menahan laju pelepasan semakin besar.
mikrokapsul. Pada nisbah paduan 7:3, dan 9:1, peningkatan konsentrasi PVA menunjukkan peningkatan efisiensi mikrokapsul. Pada nisbah paduan 8:2, hal tersebut tidak terjadi, mungkin disebabkan oleh kecepatan pengadukan yang tidak homogen atau waktu dispersi yang tidak seragam. Efisiensi mikrokapsul tertinggi, yaitu 83.47%, terjadi pada konsentrasi PVA 3%. Data perhitungan efisiensi mikrokapsul untuk semua formula mikrokapsul dapat dilihat pada Lampiran 4.
Gambar 3 Efisiensi mikrokapsul MPA dengan konsentrasi PVA, = 1% = 2% =3%.
Pelepasan Obat
Disolusi adalah proses transfer massa dari permukaan padat ke medium disolusi pada kondisi suhu dan komposisi pelarut terkendali. Menurut Kiortsis et al. (2003) dalam Sinuhaji (2012), proses disolusi obat terdiri atas 3 tahap. Tahap pertama adalah penetrasi media disolusi ke dalam matriks kapsul (hidrasi), tahap kedua adalah pembengkakan dan erosi matriks kapsul, dan tahap ketiga adalah perpindahan senyawa obat keluar dari matriks kapsul yang terhidrasi menuju media disolusi. Proses disolusi dipengaruhi oleh laju alir rata-rata cairan disolusi ke arah lapisan penghubung fase padat-cair, reaksi di lapisan penghubung fase padat-cair, dan difusi molekul obat dari lapisan penghubung fase padat-cair ke medium disolusi (Singhvi & Singh 2011).
Salah satu tujuan mikroenkapsulasi MPA adalah menahan laju pelepasan MPA. Pada penelitian ini, proses disolusi dilakukan secara
in vitro pada medium simulasi cairan lambung
(medium asam larutan HCl pH 1.2) selama 180 menit dan medium simulasi cairan usus (medium basa bufer fosfat pH 7.4) selama 360 menit. Pelepasan obat di lambung biasanya berlangsung selama 3 jam (Setyani 2009). Mikrokapsul yang diuji disolusi adalah mikrokapsul formula CC dengan efisiensi mikrokapsul tertinggi, yaitu 83.47%.
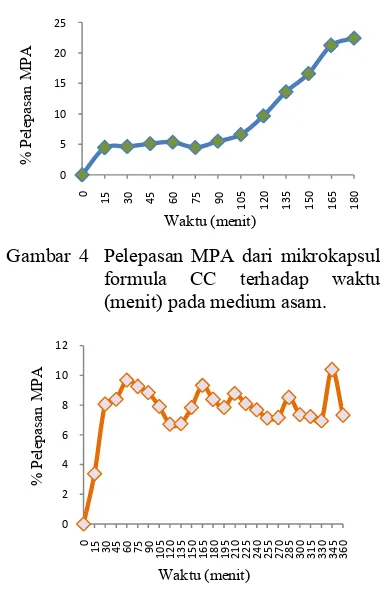
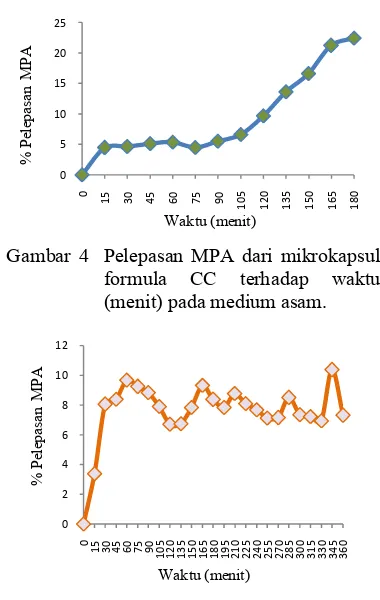
Pelepasan MPA pada medium asam mengalami kenaikan yang konstan hingga menit ke-180 (Gambar 4). Pelepasan MPA di medium basa mengalami kenaikan hingga menit ke-60, lalu pelepasannya mengalami fluktuasi hingga menit ke-360. Penurunan pelepasan MPA pada menit ke-75 hingga menit ke-120 menunjukkan bahwa tidak ada MPA yang terlepas pada rentang waktu tersebut. dan pelepasan MPA kembali terjadi pada menit ke-135 hingga menit ke-165 (Gambar 5). Pada sistem pengantaran obat oral, jumlah pelepasan bahan aktif di lambung (medium asam) diharapkan lebih sedikit karena proses absorpsi nutrisi atau obat berlangsung di usus (Setyani 2009). Pada sistem pengantaran obat implan, jumlah pelepasan bahan aktif di plasma (medium basa) seharusnya konstan atau tidak di atas konsentrasi minimum beracun dan tidak di bawah konsentrasi minimum efektif (Singhvi & Singh 2011).
Gambar 4 Pelepasan MPA dari mikrokapsul formula CC terhadap waktu (menit) pada medium asam.
Gambar 5 Pelepasan MPA dari mikrokapsul formula CC terhadap waktu (menit) pada medium basa. Profil disolusi mikrokapsul CC pada medium basa menunjukkan adanya initial
burst release pada menit ke-15 hingga menit
60 karena pelepasan MPA pada menit ke-60 di medium basa lebih besar, yaitu 9.69% dibandingkan di medium asam, yaitu 5.39%. 0 20 40 60 80 100
7:3 8:2 9:1
% E fi si en si E n k ap su la si
Nisbah PCL-Lilin lebah
0 5 10 15 20 25 0
15 30 45 60 75 90
105 120 135 150 165 180
% P el ep as an M P A Waktu (menit) 0 2 4 6 8 10 12 0
15 30 45 60 75 90
105 120 135 150 165 180 195 210 225 240 255 270 285 300 315 330 345 360
Huang dan Brazel (2001) menyatakan bahwa
initial burst release dapat disebabkan karena
adanya bahan aktif yang tersalut pada permukaan. Hasil uji disolusi mikrokapsul MPA dapat dilihat pada Lampiran 5 dan 6.
Kinetika Pelepasan Obat
Kinetika pelepasan obat dapat menggambarkan laju pelepasan obat dan model pelepasannya. Model kinetika pelepasan MPA ditentukan berdasarkan nilai koefisien determinasi (R2) persamaan orde ke-0, ke-1, dan Koersmeyer-Peppas tertinggi. Kinetika pelepasan MPA (Lampiran 7) dikaji menggunakan data uji disolusi mikrokapsul formula CC pada medium asam (larutan HCl pH 1.2) dan medium basa (bufer fosfat pH 7.4).
Pelepasan MPA dari mikrokapsul formula CC menunjukkan model kinetika Korsmeyer-Peppas karena memiliki nilai R2 yang lebih tinggi dibandingkan dengan model kinetika lainnya, yaitu 0.9951 pada medium asam dan 0.9993 pada medium basa. Nilai n pada model Korsmeyer-Peppas digunakan untuk menentukan mekanisme pelepasan obat. Nilai
n yang lebih besar dari 0.89, yaitu 0.8902 pada medium asam dan 0.9226 pada medium basa (Tabel 2), menunjukkan karakter mekanisme pelepasan obat berdasarkan super
case-II transport yang terjadi karena
penguraian dan erosi polimer (Singhvi & Singh 2011). Ada beberapa proses yang
terjadi pada mekanisme pelepasan obat super
case-II transport, yaitu difusi air ke
mikrokapsul, membesarnya mikrokapsul akibat masuknya air, pembentukan gel, difusi bahan aktif dari matriks polimer, dan rusaknya matriks polimer.
Morfologi Mikrokapsul
Hasil analisis mikrokapsul MPA tersalut PCL-lilin lebah menggunakan mikroskop menunjukkan bahwa mikrokapsul kosong tampak lebih bulat dan transparan dibandingkan setelah penambahan MPA yang tampak lebih gelap (Gambar 6). Hal ini menunjukkan bahwa MPA tersebar pada matriks polimer.
Hasil analisis mikrokapsul MPA dengan SEM menunjukkan bahwa mikrokapsul berbentuk bulat dengan permukaan tidak rata yang disebabkan oleh partikel MPA yang menempel pada permukaan mikrokapsul (Gambar 7). Hal ini menyebabkan initial burst
release atau pelepasan bahan aktif (MPA)
yang berlebih dari matriks polimer (Yeo & Park 2004).
Ukuran mikrokapsul yang dihasilkan pada penelitian ini berkisar 67–144 m. Jain (2000) menyatakan bahwa ukuran mikrokapsul yang baik kurang dari 250 μm. Obeidat (2009) juga menyatakan bahwa umumnya ukuran produk mikroenkapsulasi (mikropartikel) berkisar 1– 1000 μm, sedangkan mikropartikel komersial berkisar antara 3–800 μm.
Tabel 2 Parameter pelepasan MPA dari mikrokapsul formula CC Medium
Disolusi
Orde ke-0 Orde ke-1 Korsmeyer –Peppas
R2 k0 R2 k1 R2 n
Asam 0.8566 0.0164 0.2749 8.4543 0.9951 0.8902
Basa 0.8396 0.0229 0.5239 14.9357 0.9993 0.9226
(a) (b) (c) (d)
(a) (b) (c)
Gambar 7 Foto SEM mikrokapsul MPA pada perbesaran 1200× (a), 400× (b), dan 150× (c).
SIMPULAN DAN SARAN
SimpulanMikrokapsul MPA tersalut PCL-lilin lebah yang dihasilkan berbentuk serbuk, kering, dan berwarna putih. Efisiensi mikrokapsul tertinggi, yaitu 83.47% terdapat pada mikrokapsul dengan nisbah PCL:lilin lebah 9:1 dan konsentrasi PVA 3%. Efisiensi mikrokapsul meningkat dengan meningkatnya nisbah PCL:lilin lebah dan konsentrasi PVA. Kinetika pelepasan MPA mengikuti model kinetika Korsmeyer-Peppas dengan mekanisme pelepasan berdasarkan super
case-II transport. Hasil morfologi mikrokapsul
MPA menunjukkan permukaan tidak rata. Selain itu, ukuran mikrokapsul MPA yang dihasilkan berkisar 67–144 m.
Saran
Perlu dilakukan penelitian lanjutan mengenai disolusi secara in vivo untuk mengetahui pelepasan MPA dalam tubuh dan melihat kompabilitas paduan PCL dan lilin lebah menggunakan DSC, dan variasi kecepatan emulsi maupun dispersi yang lebih tinggi agar diperoleh permukaan mikrokapsul yang rata.
DAFTAR PUSTAKA
Appara B, Shivalingam MR, Reddy YVK, Sunitha N, Jyothibasu T, Shyam T. 2010. Design and evaluation of sustained release microcapsules containing diclofenac sodium. Int J Pharm Biomed Res 3:90–93. Bilensoy EM, Murat S, Hincal AA. 2006.
Effect of drug physicochemical properties on in vitro characteristics of amphiphilic
cyclodextrin nanospheres and
nanocapsules. Journal of
Microencapsulation 23:59–68.
Buttini F, Soltani A, Colombo A, Marriott C, Jones SA. 2008. Multilayer PVA adsorption onto hydrophobic drug substrates to engineer drug-rich microparticles. European journal of
Pharmaceutical sciences. 33: 20–28.
Dinarvand R, Mahmoodi S, Farboud E, Salehi M, Atyabi F. 2005. Preparation of gelatin microspheres containing lactic acid-effect of cross-linking on drug release. Acta
Pharm. 5:57–67.
Diza M. 2008. Perbandingan densitas mineral tulang pada pemakai kontrasepsi
kombinasi dengan depo
medroksiprogesteron asetat untuk jangka panjang di puskesmas mandala medan [tesis]. Medan: Bagian Obstetri dan Ginekologi, Fakultas Kedokteran, Universitas Sumatera Utara.
Garnier N, Olive´ CC, Rolando N, Regert M. 2002. Characterization of archaeological beeswax by electron ionization and electrospray ionization mass spectrometry.
Anal Chem. 74: 4868-4877.
Gowda DV, Ravi V, Shivakumar HG, Hatna S. 2009. Preparation, evaluation and bioavailability studies of indomethacin-bees wax microspheres. J Mater Sci:
Mater Med 20:1447–1456.
Guo X, Zhang L, Qian Y, Zhou J. 2007. Effect of composition on the formation of poly(dl-lactide) microspheres for drug delivery systems: mesoscale simulations.
Chemical Engineering Journal 131:195–
201.
Herdini, Darusman LK, Sugita P. 2010. Disolusi mikroenkapsulasi tersalut gel kitosan-alginat-glutaraldehida. Makara
Huang X, Brazel CS. 2001. On the importance and mechanisms of burst release in matrix-controlled drug delivery systems. Journal
of Controlled Release 73:121–136.
Ibezim EC, Andrade CT, Marcia C, Barretto B, Odimegwu DC, Lima FFD. 2011.
Ionically cross-linked
chitosan/tripolyphosphate microparticles for the controlled delivery of pyrimethamine. Ibnosina Journal of
Medicine and Biomedical Sciences
ISSN:1947–489X.
Jain RA. 2000. The manufacturing techniques of various drug loaded biodegradable poly(lactide-co-glycolide) (PLGA) devices. Biomaterials 21:2475–2490. Kemala T, Budianto E, Soegiyono B. 2012.
Preparation and characterization of microspheres based on blend of poly(lactic acid) and poly(ɛ-caprolactone) with poly(vinyl alcohol) as emulsifier. Arabian
Journal of Chemistry 5:103-108.
Kim BK, Hwang SJ, Park JB, Park HJ. 2005. Characteristics of felodipine-located poly(e-caprolactone) microspheres.
Journal of Microencapsulation 22:193–
203.
Maulidyawati N. 2009. Mikroenkapsulasi ibuprofen dengan penyalut polipaduan poli(asam laktat) dan polikaprolakton [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Mikaela Malm. 2008. Drug analysis bioanalytical method development and validation. Digital Comprehensive Summaries of Uppsala Dissertations from the Faculty of Science and Technology
406:1651–6214.
Obeidat WM. 2009. Recent patents review in microencapsulation of pharmaceuticals using the emulsion solvent removal methods. Recent Patents on Drug Delivery
& Formulation 3:178-192.
Park JH, Ye M, Park K. 2005. Biodegradable polymers for microencapsulation of drugs.
Molecules 10:146–161.
Porjazoska A, Goracinova K, Mladenovska K, Glava M, Simonovska M, Janjevi EI,
Cvetkovska M. 2004. Poly(lactide-co-glycolide) microparticles as systems for controlled release of proteins – Preparation and characterization. Acta Pharm 54:215– 229.
Porjazoska A, Yilmaz OK, Apohan NK, Cvetkovska M, Baysal BM. 2004. Biocompatible polymer blends of poly(D,L-lactic acid-co-glycolic acid) and triblock PCL-PDMS-PCL copolymers: their characterizations and degradations.
Croatica Chemica Acta77:545–551.
Ranjha NM, Khan H, Naseem S. 2010. Encapsulation and characterization of controlled release flurbiprofen loaded microspheres using beeswax as an encapsulating agent. J Mater Sci: Mater Med 21:1621–1630.
Rosida A. 2007. Pencirian polipaduan poli(asam laktat) dengan polikaprolakton [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Setyani YA. 2009. Perilaku disolusi ketoprofen tersalut rangkap dalam gel kitosan-gom guar dengan alginat [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Singhvi G, Singh M. 2011. Review: in-vitro drug release characterization models.
International Journal of Pharmaceutical
Studies and Research 2:77–84.
Sinuhaji PM. 2012. Pelepasan ibuprofen dari mikrokapsul tersalut paduan lilin lebah dan poli(asam laktat) secara in vitro [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Wang W, Liu X, Xie Y, Zhang H, Yu W, Xiong Y, Xie W, Ma X. 2006. Microencapsulation using natural polysaccharides for drug delivery and cell implantation. J. Mater. Chem 16:3252– 3267.
Yeo Y, Park K. 2004. Control of encapsulation efficiency and initial burst in polymeric microparticle system. Archives of
Lampiran 1 Bagan alir penelitian
M I K R O K A P S U L
Karakteristik Mikrokapsul
Penentuan
maksMPA
dan kurva standar
Mikroskop dan SEM
Uji disolusi
Uji efisiensi mikrokapsul
Paduan PCL-lilin lebah dalam
diklorometana (7:3, 8:2, 9:1)
MPA
200 mL akuades
Didispersikan sambil diaduk
dengan pengaduk magnetik
pada kecepatan 1000 rpm
Larutan PVA 1%,
2%, dan 3%
Mekanisme pelepasan MPA
melalui orde ke-0, ke-1, dan
Lampiran 2 Spektrum absorbansi MPA
maks
(nm)
Absorbans
Lampiran 3 Kurva standar MPA
y= 0.0429x+ 0.0325
r= 0.9984
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1
0 5 10 15 20 25
A
b
so
rb
an
s
[MPA] (ppm)
[MPA]
ppm
Absorban
2
0.143
4
0.179
6
0.285
10
0.465
12
0.535
14
0.642
18
0.816
Lampiran 4 Efisiensi mikrokapsul MPA tersalut PCL-lilin lebah
Formula
Bobot
MPA
(g)
a
(g)
b
(g)
c
[MPA]
(ppm)
Efisiensi
Mikrokapsul
(%)
AA
0.1501
0.3080
0.0027
0.178
3.3916
51.55
AB
0.1500
0.2990
0.0025
0.217
4.3007
68.58
AC
0.1501
0.3001
0.0025
0.230
4.6037
73.64
BA
0.1503
0.3448
0.0026
0.177
3.3683
59.44
BB
0.1501
0.3526
0.0028
0.192
3.7179
62.38
BC
0.1501
0.3023
0.0025
0.232
4.6503
74.93
CA
0.1500
0.3091
0.0025
0.199
3.8811
63.98
CB
0.1501
0.3002
0.0025
0.205
4.0210
64.34
CC
0.1502
0.3320
0.0025
0.235
4.7203
83.47
Keterangan :
a
: massa total kapsul yang diperoleh
b
: massa kapsul yang digunakan untuk penentuan efisiensi mikrokapsul
c
: absorban filtrat hasil disolusi kapsul setelah diencerkan 10 kali
Contoh perhitungan (formula AA) :
y = 0.0325x + 0.0429
0.178 = 0.0325x + 0.0429
x = 3.3916
Efisiensi mikrokapsul =
�� × × 1 1000 ×1
1000 × � .� � × ( ) ( )
�� ( )
× 100%
=
3.39161 × 10 × 1 1000 ×
1
1000 × 20 × 0.3080 0.0027
0.1501
× 100%
Lampiran 5 Persentase rerata pelepasan MPA dalam uji disolusi mikrokapsul
formula CC tersalut PCl-lilin lebah
Mikrokapsul dengan medium asam
Waktu
(menit)
Persentase Pelepasan MPA (% b/b)
Rerata Persentase
Pelepasan MPA
(% b/b)
Ulangan 1
Ulangan 2
0
0.00
0.00
0.00
15
6.01
2.91
4.46
30
6.22
3.08
4.65
45
6.83
3.39
5.11
60
6.96
3.82
5.39
75
5.30
3.72
4.51
90
6.27
4.78
5.53
105
7.10
6.17
6.64
120
9.70
9.66
9.68
135
14.08
13.21
13.65
150
16.34
16.86
16.60
165
19.80
22.63
21.22
Lanjutan
Mikrokapsul dengan medium basa
Waktu
(menit)
Persentase Pelepasan MPA (% b/b)
Rerata Persentase
Pelepasan MPA
(% b/b)
Ulangan 1
Ulangan 2
0
0.00
0.00
0.00
15
3.84
2.95
3.40
30
10.30
5.80
8.05
45
8.26
8.50
8.38
60
6.57
12.80
9.69
75
6.38
12.10
9.24
90
8.10
9.60
8.85
105
8.04
7.78
7.91
120
5.68
7.75
6.72
135
5.74
7.75
6.75
150
9.01
6.65
7.83
165
9.61
9.01
9.31
180
9.62
7.11
8.37
195
7.92
7.73
7.83
210
9.61
7.92
8.77
225
8.85
7.34
8.10
240
7.26
8.10
7.68
255
7.09
7.18
7.14
270
8.10
6.19
7.15
285
9.37
7.63
8.50
300
6.90
7.81
7.36
315
7.25
7.18
7.22
330
7.44
6.42
6.93
345
7.63
13.10
10.37
Lampiran 6 Pelepasan MPA dalam mikrokapsul formula CC pada waktu t
Mikrokapsul dengan medium asam (Ulangan I)
Bobot
Mikrokapsul
(g)
Waktu
(menit)
Absorban
[MPA]
ppm
Persentase
Pelepasan MPA
(% b/b)
0.2004
0
0.0000
0.0000
0.00
15
0.0899
1.3380
6.01
30
0.0919
1.3846
6.22
45
0.0977
1.5198
6.83
60
0.0990
1.5501
6.96
75
0.0831
1.1795
5.30
90
0.0924
1.3963
6.27
105
0.1003
1.5804
7.10
120
0.1252
2.1608
9.70
135
0.1670
3.1352
14.08
150
0.1886
3.6387
16.34
165
0.2216
4.4079
19.80
Lanjutan
Mikrokapsul dengan medium asam (Ulangan II)
Bobot
Mikrokapsul
(g)
Waktu
(menit)
Absorban
[MPA]
ppm
Persentase
Pelepasan MPA
(% b/b)
0.2004
0
0.0000
0.0000
0.00
15
0.0603
0.6480
2.91
30
0.0619
0.6853
3.08
45
0.0649
0.7552
3.39
60
0.0690
0.8508
3.82
75
0.0680
0.8275
3.72
90
0.0782
1.0653
4.78
105
0.0914
1.3730
6.17
120
0.1248
2.1515
9.66
135
0.1587
2.9417
13.21
150
0.1936
3.7552
16.86
165
0.2487
5.0396
22.63
Lanjutan
Mikrokapsul dengan medium basa (Ulangan I)
Bobot
Mikrokapsul
(g)
Waktu
(menit)
Absorban
[MPA]
ppm
Persentase
Pelepasan MPA
(% b/b)
0.2006
0
0.0000
0.0000
0.00
15
0.0692
0.8555
3.84
30
0.1309
2.2937
10.30
45
0.1115
1.8415
8.26
60
0.0953
1.4639
6.57
75
0.0935
1.4219
6.38
90
0.1100
1.8065
8.10
105
0.1094
1.7925
8.04
120
0.0868
1.2657
5.68
135
0.0874
1.2797
5.74
150
0.1187
2.0093
9.01
165
0.1244
2.1422
9.61
180
0.1245
2.1445
9.62
195
0.1082
1.7646
7.92
210
0.1244
2.1422
9.61
225
0.1171
1.9720
8.85
240
0.1019
1.6177
7.26
255
0.1003
1.5804
7.09
270
0.1100
1.8065
8.10
285
0.1221
2.0886
9.37
300
0.0985
1.5385
6.90
315
0.1018
1.6154
7.25
330
0.1036
1.6573
7.44
345
0.1055
1.7016
7.63
Lanjutan
Mikrokapsul dengan medium basa (Ulangan II)
Bobot
Mikrokapsul
(g)
Waktu
(menit)
Absorban
[MPA]
ppm
Persentase
Pelepasan MPA
(% b/b)
0.2006
0
0.0000
0.0000
0.00
15
0.0607
0.6573
2.95
30
0.0880
1.2937
5.80
45
0.1138
1.8951
8.50
60
0.1547
2.8485
12.80
75
0.1481
2.6946
12.10
90
0.1243
2.1399
9.60
105
0.1069
1.7343
7.78
120
0.1066
1.7273
7.75
135
0.1066
1.7273
7.75
150
0.0961
1.4825
6.65
165
0.1187
2.0093
9.01
180
0.1005
1.5851
7.11
195
0.1064
1.7226
7.73
210
0.1082
1.7646
7.92
225
0.1027
1.6364
7.34
240
0.1100
1.8065
8.10
255
0.1012
1.6014
7.18
270
0.0917
1.3800
6.19
285
0.1055
1.7016
7.63
300
0.1072
1.7413
7.81
315
0.1012
1.6014
7.18
330
0.0939
1.4312
6.42
345
0.1582
2.9301
13.10
360
0.1019
1.6177
7.26
Contoh perhitungan (mikrokapsul dengan medium basa, ulangan 2, menit ke-15):
% Pelepasan MPA =
�� × ×1 1000 ×
1
1000 × � .
� ( )
× 100%
=
0.65731 × 10 × 1 1000 ×
1
1000 × 900
0.2006
× 100%
Lampiran 7 Kinetika pelepasan MPA dari mikrokapsul formula CC
Medium
Mikrokapsul
Model Kinetika
Persamaan Regresi
R
2
Asam
0
Q = 0.0164
t
+ 0.0678
0.8566
1
Ln[A]
t=
–
8.4543
t
+ 3.1258
0.2749
Korsmeyer-Peppas
Ln(
y
) = 0.8902 Ln(
x
)
–
2.4184
0.9952
Basa
0
Q = 0. 0229
t
+ 0.1191
0.8396
1
Ln[A]
t=
–
14.9357
t
+ 16.9774
0.5239
ABSTRAK
GUSLINA
ISRIANY.
Optimasi
dan
Evaluasi
Mikroenkapsulasi
Medroksiprogesteron Asetat Tersalut
Poli(ε
-kaprolakton)-Lilin Lebah. Dibimbing
oleh TETTY KEMALA dan AHMAD SJAHRIZA.
Salah satu teknik menyalut obat dengan suatu material polimer adalah
mikroenkapsulasi. Tujuan enkapsulasi obat adalah mengendalikan pelepasan obat
sehingga
efek
samping
obat
dapat
dikurangi.
Pada
penelitian
ini,
medroksiprogesteron asetat (MPA) disalut oleh
poli(ε
-kaprolakton) (PCL) dan
lilin lebah. Emulsifikasi-penguapan pelarut merupakan metode yang digunakan
untuk membuat mikrokapsul MPA dengan ragam nisbah PCL:lilin lebah 7:3; 8:2;
dan 9:1 dan konsentrasi pengemulsi poli(vinil alkohol) 1%; 2%; dan 3%. Efisiensi
mikrokapsul tertinggi adalah 83.47% pada mikrokapsul dengan nisbah PCL:lilin
lebah 9:1 dan konsentrasi PVA 3%. Kinetika pelepasan MPA mengikuti model
kinetika Korsmeyer-Peppas dengan mekanisme pelepasan obat
super case-II
transport
. Mikrokapsul yang dihasilkan memiliki kisaran ukuran 67
–
144
m
dengan inti yang terdispersi secara homogen pada matriks polimer.
ABSTRACT
GUSLINA ISRIANY. Optimization and Evaluation of Medroxyprogesterone
Acetate (MPA) Microcapsules Coated Poly(
ε
-caprolactone)-Beeswax. Supervised
by TETTY KEMALA and AHMAD SJAHRIZA.
PENDAHULUAN
Medroksiprogesteron asetat (MPA) merupakan senyawa aktif kontrasepsi hormon steroid (meliputi kontrasepsi oral, injeksi, dan implan) yang sangat efektif dan digunakan secara luas. Prinsip kerja MPA adalah mencegah ovulasi, mengentalkan lendir serviks, menipiskan selaput lendir rahim, dan menghambat transportasi gamet. Kontrasepsi MPA biasanya dikonsumsi oleh perempuan reproduktif, yaitu 15–49 tahun dan rentang waktu konsumsi obat ini 24–36 jam. Selain dapat menyebabkan penambahan bobot badan, osteoporosis, dan gangguan haid, senyawa ini juga dapat meningkatkan ovulasi jika dikonsumsi lebih dari 36 jam (Diza 2008). Sistem pengantaran obat secara khusus diperlukan MPA untuk mengatasi hal tersebut. Mikroenkapsulasi merupakan proses penyalutan zat aktif padat atau cair dengan suatu material polimer dalam bentuk mikrokapsul (Wang et al. 2006). Di bidang farmasi, teknologi enkapsulasi bertujuan mengurangi rasa pahit obat, memisahkan material yang tidak kompatibel, mencegah kerusakan obat yang diakibatkan oleh uap air dan cahaya, mengurangi risiko iritasi lokal organ atau jaringan yang ditimbulkan obat, mengendalikan pendistribusian obat, serta mengoptimalkan penyerapan obat (Appara et al. 2010; Gowda et al. 2009).
Bahan penyalut mikrokapsul yang banyak digunakan saat ini adalah golongan poliester alifatik yang bersifat degradabel. Salah satunya adalah poli(ε-kaprolakton) (PCL). Poli(ε-kaprolakton) memiliki permeabilitas tinggi, biodegradabel, biokompatibel, dan tidak beracun. Di sisi lain, PCL memiliki kristalinitas yang tinggi dan waktu degradasi yang lama. Pencampuran PCL dengan makromolekul dapat dilakukan untuk mengatasi hal tersebut (Porjazoska et al. 2004).
Lilin lebah merupakan makromolekul yang terdiri atas n-alkana jenuh dan takjenuh, ester rantai panjang, asam lemak, diester, hidroksiester, dan penyusun minor lainnya, seperti flavonoid (Garnier et al. 2002). Lilin lebah dapat digunakan sebagai bahan penyalut mikrokapsul dan memiliki beberapa kelebihan, yaitu stabil pada beberapa nilai pH dan tingkat kelembapan, biokompatibel, tidak imunogenik, tidak beracun, dan tidak menyebabkan peningkatan dosis obat (Ranjha
et al. 2010). Campuran PCL dengan lilin
lebah diharapkan menghasilkan polimer kompatibel yang memiliki permeabilitas dan
waktu degradasi lebih baik, serta mempermudah pencampuran bahan aktif dengan matriks paduan. Bahan aktif yang tidak larut air seperti MPA akan mudah bercampur dengan matriks lilin lebah dan menunjukkan tingkat penyerapan yang baik (Gowda et al. 2009). Selain itu, pencampuran tersebut dapat mengurangi biaya yang dibutuhkan karena lilin lebah relatif lebih murah dibandingkan dengan PCL.
Salah satu metode yang banyak digunakan untuk pengungkungan bahan aktif hidrofobik seperti MPA adalah metode emulsifikasi-penguapan pelarut (Park et al. 2005). Pada metode ini, dibutuhkan pengemulsi seperti poli(vinil alkohol) (PVA) untuk menstabilkan larutan polimer dan obat dengan air. Poli(vinil alkohol) sudah banyak digunakan sebagai pengemulsi dalam pembuatan mikrokapsul tersalut-poliester. Gugus hidroksil (hidrofilik) dari PVA yang bersifat polar akan berikatan dengan molekul air, sedangkan rantai vinilnya (hidrofobik) akan berikatan dengan polimer (PCL-lilin lebah) sehingga emulsi menjadi lebih stabil (Guo et al. 2007). Menurut Kemala et al. (2012), besarnya konsentrasi PVA yang digunakan akan mempengaruhi stabilitas emulsi dan ukuran kapsul. Ukuran kapsul yang seragam meningkatkan efisiensi dan laju disolusi bahan aktif yang telah dikungkung.
Penelitian ini bertujuan membuat mikrokapsul MPA tersalut PCL-lilin lebah, menganalisis efisiensi mikrokapsul MPA, mempelajari pengaruh variasi nisbah PCL:lilin lebah dan konsentrasi pengemulsi terhadap mikrokapsul yang dihasilkan, mempelajari model kinetika pelepasan MPA berdasarkan koefisien determinasi (R2) dengan menggunakan persamaan orde reaksi ke-0, ke-1, dan Korsmeyer-Peppas, serta mempelajari morfologi mikrokapsul.
BAHAN DAN METODE
Bahan dan alatBahan-bahan yang digunakan dalam penelitian ini adalah PCL (Sigma Aldrich, Germany), lilin lebah, PVA (Merck), MPA (BKKBN), diklorometana, etanol 96%, larutan HCl pH 1.2, dan larutan bufer fosfat (NaH2PO4-Na2HPO4) pH 7.4. Alat-alat yang
Metode
Penelitian ini dilakukan dalam beberapa tahapan (Lampiran 1), meliputi pembuatan mikrokapsul MPA, uji efisiensi mikrokapsul MPA, uji disolusi mikrokapsul, dan penentuan kinetika pelepasan obat, serta uji karakteristik mikrokapsul yang dihasilkan dengan mikroskop dan SEM.
Pembuatan mikrokapsul MPA (Dinarvand
et al. 2005)
PCL dan lilin lebah dilarutkan dalam diklorometana kemudian diaduk hingga homogen. Setelah itu, MPA dicampurkan ke dalam larutan paduan tersebut. Campuran kemudian didispersikan ke dalam air yang mengandung PVA menggunakan motor pengaduk, lalu didekantasi hingga mikrokapsul yang terbentuk mengendap. Mikrokapsul yang diperoleh disaring, dicuci dengan akuades, dan dikeringudarakan selama 1 hari. Variasi nisbah PCL:lilin lebah dan konsentrasi PVA yang digunakan dapat dilihat pada Tabel 1.
Tabel 1 Komposisi mikrokapsul MPA tersalut polipaduan PCL-lilin lebah
Formula Nisbah PCL:lilin lebah
Konsentrasi PVA
(%)
AA 7:3 1
AB 8:2 1
AC 9:1 1
BA 7:3 2
BB 8:2 2
BC 9:1 2
CA 7:3 3
CB 8:2 3
CC 9:1 3
Penentuan panjang gelombang maksimum dan pembuatan kurva standar
Panjang gelombang maksimum ( maks)
larutan MPA 10 ppm dalam etanol 96% ditentukan pada rentang panjang gelombang
( ) 240–400 nm menggunakan spekrofotometer UV-Vis. Panjang gelombang
maksimum ( maks) yang diperoleh digunakan
untuk analisis selanjutnya.
Kurva standar dibuat dengan mengukur absorbans larutan MPA dengan konsentrasi 2, 4, 6, 10, 12, 14, 18, dan 20 ppm pada panjang gelombang maksimum. Hasil yang diperoleh merupakan hubungan konsentrasi MPA dengan absorbans.
Efisiensi mikrokapsul (Ibezim et al. 2011)
Sebanyak 2.5 mg mikrokapsul dilarutkan dalam 20 mL etanol 96%, diaduk dengan pengaduk magnetik selama 3 jam, dan filtratnya disaring. Absorbans filtrat dibaca dengan spektrofotometer UV-Vis pada panjang gelombang maksimum. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi MPA dengan bantuan kurva standar.
Uji disolusi secara in vitro (Herdini et al.
2010)
Sebanyak 200 mg mikrokapsul yang diperoleh pada kondisi optimum didisolusi dalam 900 mL medium simulasi (larutan HCl pH 1.2 dan bufer fosfat pH 7.4) menggunakan alat disolusi tipe 2 (tipe dayung). Pengujian dilakukan pada suhu (37 ± 0.5) °C dengan kecepatan pengadukan 100 rpm selama 360 menit. Setiap 15 menit, alikuot diambil sebanyak 10 mL selama 360 menit. Setiap kali pengambilan alikuot, volume medium simulasi yang terambil digantikan dengan medium simulasi yang baru dengan volume dan suhu yang sama. Alikuot disaring dan ditentukan serapan MPA dengan spektrofotometer UV-Vis pada maks. Data
pengukuran yang diperoleh digunakan untuk mempelajari model kinetika pelepasan MPA. Morfologi mikrokapsul
Pengamatan morfologi mikrokapsul dilakukan terhadap 1 formula dengan menggunakan mikroskop cahaya dan SEM. Pengamatan menggunakan SEM dilakukan dengan cara melapisi mikrokapsul dengan emas dan dilihat pada pembesaran 1200×, 400×, dan 150×.
HASIL DAN PEMBAHASAN
Mikroenkapsulasi MPA
Gambar 1 Mikrokapsul MPA tersalut PCL-lilin lebah.
Metode yang digunakan untuk pembuatan mikrokapsul adalah emulsifikasi-penguapan pelarut, yaitu bahan penyalut (PCL dan lilin lebah) dan bahan aktif (MPA) dilarutkan dalam pelarut organik (diklorometana) kemudian didispersikan dalam air yang berisi pengemulsi sehingga terbentuk mikrokapsul (Gambar 2). Obeidat (2009) menyatakan bahwa metode emulsi-penguapan pelarut menghasilkan mikrokapsul dengan mekanisme pelepasan material yang dikungkung secara optimum karena material tersebut terdispersi secara homogen pada matriks polimer sehingga ideal untuk sistem pengantaran bahan aktif.
Gambar 2 Tahap pembentukan mikrokapsul dengan metode emulsifikasi
-penguapan pelarut (Kim et al. 2005).
Diklorometana digunakan sebagai pelarut karena menguap pada suhu 39 °C sehingga penguapan pelarut berlangsung cepat. Bodmeier et al. (1988) dalam Yeo dan Park (2004) menyatakan bahwa diklorometana merupakan pelarut terbaik untuk poliester dibandingkan dengan kloroform atau benzena, dan dapat menghasilkan efisiensi mikrokapsul lebih tinggi.
Pengemulsi yang digunakan adalah PVA yang merupakan polimer ampifilik dan mampu teradsorpsi pada antarmuka (Buttini et al. 2008). Pengemulsi berfungsi menstabilkan emulsi larutan paduan PCL-lilin lebah dan MPA dalam diklorometana dengan air melalui pengikatan gugus hidroksil (hidrofilik) PVA dengan molekul air, dan rantai vinil (hidrofobik) dengan diklorometana (Guo et al. 2007).
Panjang gelombang maksimum dan kurva standar
Panjang gelombang maksimum ( maks)
larutan MPA diperoleh pada 241.6 nm (Lampiran 2). Nilai maks ini tidak berbeda
jauh dengan nilai maks progesteron, yaitu 240
nm (Bilensoy et al. 2006). Penentuan maks
dilakukan pada daerah ultraviolet karena larutan MPA tidak berwarna. Sensitivitas pengukuran yang maksimum diperoleh ketika sampel diukur pada maks (Mikaela 2008).
Persamaan kurva standar yang diperoleh adalah y = 0.0325x + 0.0429 dengan nilai koefisien korelasi (r) 0.9984 (Lampiran 3). Persamaan kurva standar tersebut digunakan dalam perhitungan efisiensi enkapsulasi dan persentase pelepasan MPA. Kurva standar yang digunakan telah memenuhi syarat karena nilai korelasinya lebih besar dari 0.9900. Nilai
r yang tinggi menunjukkan tingkat kesesuaian atau linearitas antara sinyal detektor terukur (respons) dan konsentrasi MPA (analit) dalam sampel, sehingga galat sistematik selama pengukuran dapat diabaikan (Mikaela 2008).
Efisiensi mikrokapsul
Efisiensi mikrokapsul merupakan salah satu parameter yang menunjukkan keberhasilan proses enkapsulasi. Efisiensi menunjukkan persen senyawa aktif (MPA) yang dapat disalut dalam mikrokapsul. Semakin tinggi efisiensi mikrokapsul berarti semakin banyak MPA yang tersalut.
Efisiensi mikrokapsul yang dihasilkan berkisar 51.55–83.47% (Gambar 3). Efisiensi mikrokapsul terendah dihasilkan oleh mikrokapsul formula AA, dan efisiensi tertinggi dihasilkan oleh mikrokapsul formula CC. Perbedaan hasil ini dipengaruhi oleh nisbah paduan PCL-lilin lebah, yaitu 7:3 pada mikrokapsul AA dan 9:1 pada mikrokapsul CC. Lilin lebah yang lebih banyak pada penyalut menyebabkan komponen penyalut dengan bobot molekul rendah bertambah sehingga akan lebih sulit untuk mengungkung MPA. Lilin lebah memiliki bobot molekul sekitar 868 g mol-1. Halder dan Sa (2006) dalam Maulidyawati (2009) menyatakan bahwa salah satu faktor yang menyebabkan tingginya efisiensi mikrokapsul adalah nisbah antara bahan penyalut dan bahan inti. Semakin banyak jumlah penyalut, kemampuannya untuk menahan laju pelepasan semakin besar.
mikrokapsul. Pada nisbah paduan 7:3, dan 9:1, peningkatan konsentrasi PVA menunjukkan peningkatan efisiensi mikrokapsul. Pada nisbah paduan 8:2, hal tersebut tidak terjadi, mungkin disebabkan oleh kecepatan pengadukan yang tidak homogen atau waktu dispersi yang tidak seragam. Efisiensi mikrokapsul tertinggi, yaitu 83.47%, terjadi pada konsentrasi PVA 3%. Data perhitungan efisiensi mikrokapsul untuk semua formula mikrokapsul dapat dilihat pada Lampiran 4.
Gambar 3 Efisiensi mikrokapsul MPA dengan konsentrasi PVA, = 1% = 2% =3%.
Pelepasan Obat
Disolusi adalah proses transfer massa dari permukaan padat ke medium disolusi pada kondisi suhu dan komposisi pelarut terkendali. Menurut Kiortsis et al. (2003) dalam Sinuhaji (2012), proses disolusi obat terdiri atas 3 tahap. Tahap pertama adalah penetrasi media disolusi ke dalam matriks kapsul (hidrasi), tahap kedua adalah pembengkakan dan erosi matriks kapsul, dan tahap ketiga adalah perpindahan senyawa obat keluar dari matriks kapsul yang terhidrasi menuju media disolusi. Proses disolusi dipengaruhi oleh laju alir rata-rata cairan disolusi ke arah lapisan penghubung fase padat-cair, reaksi di lapisan penghubung fase padat-cair, dan difusi molekul obat dari lapisan penghubung fase padat-cair ke medium disolusi (Singhvi & Singh 2011).
Salah satu tujuan mikroenkapsulasi MPA adalah menahan laju pelepasan MPA. Pada penelitian ini, proses disolusi dilakukan secara
in vitro pada medium simulasi cairan lambung
(medium asam larutan HCl pH 1.2) selama 180 menit dan medium simulasi cairan usus (medium basa bufer fosfat pH 7.4) selama 360 menit. Pelepasan obat di lambung biasanya berlangsung selama 3 jam (Setyani 2009). Mikrokapsul yang diuji disolusi adalah mikrokapsul formula CC dengan efisiensi mikrokapsul tertinggi, yaitu 83.47%.
Pelepasan MPA pada medium asam mengalami kenaikan yang konstan hingga menit ke-180 (Gambar 4). Pelepasan MPA di medium basa mengalami kenaikan hingga menit ke-60, lalu pelepasannya mengalami fluktuasi hingga menit ke-360. Penurunan pelepasan MPA pada menit ke-75 hingga menit ke-120 menunjukkan bahwa tidak ada MPA yang terlepas pada rentang waktu tersebut. dan pelepasan MPA kembali terjadi pada menit ke-135 hingga menit ke-165 (Gambar 5). Pada sistem pengantaran obat oral, jumlah pelepasan bahan aktif di lambung (medium asam) diharapkan lebih sedikit karena proses absorpsi nutrisi atau obat berlangsung di usus (Setyani 2009). Pada sistem pengantaran obat implan, jumlah pelepasan bahan aktif di plasma (medium basa) seharusnya konstan atau tidak di atas konsentrasi minimum beracun dan tidak di bawah konsentrasi minimum efektif (Singhvi & Singh 2011).
Gambar 4 Pelepasan MPA dari mikrokapsul formula CC terhadap waktu (menit) pada medium asam.
Gambar 5 Pelepasan MPA dari mikrokapsul formula CC terhadap waktu (menit) pada medium basa. Profil disolusi mikrokapsul CC pada medium basa menunjukkan adanya initial
burst release pada menit ke-15 hingga menit
60 karena pelepasan MPA pada menit ke-60 di medium basa lebih besar, yaitu 9.69% dibandingkan di medium asam, yaitu 5.39%. 0 20 40 60 80 100
7:3 8:2 9:1
% E fi si en si E n k ap su la si
Nisbah PCL-Lilin lebah
0 5 10 15 20 25 0
15 30 45 60 75 90
105 120 135 150 165 180
% P el ep as an M P A Waktu (menit) 0 2 4 6 8 10 12 0
15 30 45 60 75 90
105 120 135 150 165 180 195 210 225 240 255 270 285 300 315 330 345 360
[image:32.595.111.302.169.410.2] [image:32.595.320.510.341.641.2]Huang dan Brazel (2001) menyatakan bahwa
initial burst release dapat disebabkan karena
adanya bahan aktif yang tersalut pada permukaan. Hasil uji disolusi mikrokapsul MPA dapat dilihat pada Lampiran 5 dan 6.
Kinetika Pelepasan Obat
Kinetika pelepasan obat dapat menggambarkan laju pelepasan obat dan model pelepasannya. Model kinetika pelepasan MPA ditentukan berdasarkan nilai koefisien determinasi (R2) persamaan orde ke-0, ke-1, dan Koersmeyer-Peppas tertinggi. Kinetika pelepasan MPA (Lampiran 7) dikaji menggunakan data uji disolusi mikrokapsul formula CC pada medium asam (larutan HCl pH 1.2) dan medium basa (bufer fosfat pH 7.4).
Pelepasan MPA dari mikrokapsul formula CC menunjukkan model kinetika Korsmeyer-Peppas karena memiliki nilai R2 yang lebih tinggi dibandingkan dengan model kinetika lainnya, yaitu 0.9951 pada medium asam dan 0.9993 pada medium basa. Nilai n pada model Korsmeyer-Peppas digunakan untuk menentukan mekanisme pelepasan obat. Nilai
n yang lebih besar dari 0.89, yaitu 0.8902 pada medium asam dan 0.9226 pada medium basa (Tabel 2), menunjukkan karakter mekanisme pelepasan obat berdasarkan super
case-II transport yang terjadi karena
penguraian dan erosi polimer (Singhvi & Singh 2011). Ada beberapa proses yang
terjadi pada mekanisme pelepasan obat super
case-II transport, yaitu difusi air ke
mikrokapsul, membesarnya mikrokapsul akibat masuknya air, pembentukan gel, difusi bahan aktif dari matriks polimer, dan rusaknya matriks polimer.
Morfologi Mikrokapsul
Hasil analisis mikrokapsul MPA tersalut PCL-lilin lebah menggunakan mikroskop menunjukkan bahwa mikrokapsul kosong tampak lebih bulat dan transparan dibandingkan setelah penambahan MPA yang tampak lebih gelap (Gambar 6). Hal ini menunjukkan bahwa MPA tersebar pada matriks polimer.
Hasil analisis mikrokapsul MPA dengan SEM menunjukkan bahwa mikrokapsul berbentuk bulat dengan permukaan tidak rata yang disebabkan oleh partikel MPA yang menempel pada permukaan mikrokapsul (Gambar 7). Hal ini menyebabkan initial burst
release atau pelepasan bahan aktif (MPA)
yang berlebih dari matriks polimer (Yeo & Park 2004).
[image:33.595.112.507.496.681.2]Ukuran mikrokapsul yang dihasilkan pada penelitian ini berkisar 67–144 m. Jain (2000) menyatakan bahwa ukuran mikrokapsul yang baik kurang dari 250 μm. Obeidat (2009) juga menyatakan bahwa umumnya ukuran produk mikroenkapsulasi (mikropartikel) berkisar 1– 1000 μm, sedangkan mikropartikel komersial berkisar antara 3–800 μm.
Tabel 2 Parameter pelepasan MPA dari mikrokapsul formula CC Medium
Disolusi
Orde ke-0 Orde ke-1 Korsmeyer –Peppas
R2 k0 R2 k1 R2 n
Asam 0.8566 0.0164 0.2749 8.4543 0.9951 0.8902
Basa 0.8396 0.0229 0.5239 14.9357 0.9993 0.9226
(a) (b) (c) (d)
(a) (b) (c)
Gambar 7 Foto SEM mikrokapsul MPA pada perbesaran 1200× (a), 400× (b), dan 150× (c).
SIMPULAN DAN SARAN
SimpulanMikrokapsul MPA tersalut PCL-lilin lebah yang dihasilkan berbentuk serbuk, kering, dan berwarna putih. Efisiensi mikrokapsul tertinggi, yaitu 83.47% terdapat pada mikrokapsul dengan nisbah PCL:lilin lebah 9:1 dan konsentrasi PVA 3%. Efisiensi mikrokapsul meningkat dengan meningkatnya nisbah PCL:lilin lebah dan konsentrasi PVA. Kinetika pelepasan MPA mengikuti model kinetika Korsmeyer-Peppas dengan mekanisme pelepasan berdasarkan super
case-II transport. Hasil morfologi mikrokapsul
MPA menunjukkan permukaan tidak rata. Selain itu, ukuran mikrokapsul MPA yang dihasilkan berkisar 67–144 m.
Saran
Perlu dilakukan penelitian lanjutan mengenai disolusi secara in vivo untuk mengetahui pelepasan MPA dalam tubuh dan melihat kompabilitas paduan PCL dan lilin lebah menggunakan DSC, dan variasi kecepatan emulsi maupun dispersi yang lebih tinggi agar diperoleh permukaan mikrokapsul yang rata.
DAFTAR PUSTAKA
Appara B, Shivalingam MR, Reddy YVK, Sunitha N, Jyothibasu T, Shyam T. 2010. Design and evaluation of sustained release microcapsules containing diclofenac sodium. Int J Pharm Biomed Res 3:90–93. Bilensoy EM, Murat S, Hincal AA. 2006.
Effect of drug physicochemical properties on in vitro characteristics of amphiphilic
cyclodextrin nanospheres and
nanocapsules. Journal of
Microencapsulation 23:59–68.
Buttini F, Soltani A, Colombo A, Marriott C, Jones SA. 2008. Multilayer PVA adsorption onto hydrophobic drug substrates to engineer drug-rich microparticles. European journal of
Pharmaceutical sciences. 33: 20–28.
Dinarvand R, Mahmoodi S, Farboud E, Salehi M, Atyabi F. 2005. Preparation of gelatin microspheres containing lactic acid-effect of cross-linking on drug release. Acta
Pharm. 5:57–67.
Diza M. 2008. Perbandingan densitas mineral tulang pada pemakai kontrasepsi
kombinasi dengan depo
medroksiprogesteron asetat untuk jangka panjang di puskesmas mandala medan [tesis]. Medan: Bagian Obstetri dan Ginekologi, Fakultas Kedokteran, Universitas Sumatera Utara.
Garnier N, Olive´ CC, Rolando N, Regert M. 2002. Characterization of archaeological beeswax by electron ionization and electrospray ionization mass spectrometry.
Anal Chem. 74: 4868-4877.
Gowda DV, Ravi V, Shivakumar HG, Hatna S. 2009. Preparation, evaluation and bioavailability studies of indomethacin-bees wax microspheres. J Mater Sci:
Mater Med 20:1447–1456.
Guo X, Zhang L, Qian Y, Zhou J. 2007. Effect of composition on the formation of poly(dl-lactide) microspheres for drug delivery systems: mesoscale simulations.
Chemical Engineering Journal 131:195–
201.
Herdini, Darusman LK, Sugita P. 2010. Disolusi mikroenkapsulasi tersalut gel kitosan-alginat-glutaraldehida. Makara
OPTIMASI DAN EVALUASI MIKROENKAPSULASI
MEDROKSIPROGESTERON ASETAT TERSALUT
POLI(
ε
-KAPROLAKTON)-LILIN LEBAH
GUSLINA ISRIANY
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Huang X, Brazel CS. 2001. On the importance and mechanisms of burst release in matrix-controlled drug delivery systems. Journal
of Controlled Release 73:121–136.
Ibezim EC, Andrade CT, Marcia C, Barretto B, Odimegwu DC, Lima FFD. 2011.
Ionically cross-linked
chitosan/tripolyphosphate microparticles for the controlled delivery of pyrimethamine. Ibnosina Journal of
Medicine and Biomedical Sciences
ISSN:1947–489X.
Jain RA. 2000. The manufacturing techniques of various drug loaded biodegradable poly(lactide-co-glycolide) (PLGA) devices. Biomaterials 21:2475–2490. Kemala T, Budianto E, Soegiyono B. 2012.
Preparation and characterization of microspheres based on blend of poly(lactic acid) and poly(ɛ-caprolactone) with poly(vinyl alcohol) as emulsifier. Arabian
Journal of Chemistry 5:103-108.
Kim BK, Hwang SJ, Park JB, Park HJ. 2005. Characteristics of felodipine-located poly(e-caprolactone) microspheres.
Journal of Microencapsulation 22:193–
203.
Maulidyawati N. 2009. Mikroenkapsulasi ibuprofen dengan penyalut polipaduan poli(asam laktat) dan polikaprolakton [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Mikaela Malm. 2008. Drug analysis bioanalytical method development and validation. Digital Comprehensive Summaries of Uppsala Dissertations from the Faculty of Science and Technology
406:1651–6214.
Obeidat WM. 2009. Recent patents review in microencapsulation of pharmaceuticals using the emulsion solvent removal methods. Recent Patents on Drug Delivery
& Formulation 3:178-192.
Park JH, Ye M, Park K. 2005. Biodegradable polymers for microencapsulation of drugs.
Molecules 10:146–161.
Porjazoska A, Goracinova K, Mladenovska K, Glava M, Simonovska M, Janjevi EI,
Cvetkovska M. 2004. Poly(lactide-co-glycolide) microparticles as systems for controlled release of proteins – Preparation and characterization. Acta Pharm 54:215– 229.
Porjazoska A, Yilmaz OK, Apohan NK, Cvetkovska M, Baysal BM. 2004. Biocompatible polymer blends of poly(D,L-lactic acid-co-glycolic acid) and triblock PCL-PDMS-PCL copolymers: their characterizations and degradations.
Croatica Chemica Acta77:545–551.
Ranjha NM, Khan H, Naseem S. 2010. Encapsulation and characterization of controlled release flurbiprofen loaded microspheres using beeswax as an encapsulating agent. J Mater Sci: Mater Med 21:1621–1630.
Rosida A. 2007. Pencirian polipaduan poli(asam laktat) dengan polikaprolakton [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.