OPTIMALISASI AKTIVASI KARBON AKTIF TEMPURUNG
KELAPA DENGAN RAGAM SUHU DAN KONSENTRASI
AKTIVATOR ZnCl
2ARUMI PITALOKA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ARUMI PITALOKA. Optimalisasi Aktivasi Karbon Aktif Tempurung Kelapa
dengan Ragam Suhu dan Konsentrasi Aktivator ZnCl
2.
Dibimbing oleh
CHARLENA dan LISNA ROSMAYATI.
Karbon aktif tempurung kelapa berpotensi sebagai adsorben karena
kemampuan adsorpsi yang tinggi dalam menjerap pengotor. Salah satu
kegunaanya adalah pada indusri migas untuk mengeliminasi kandungan merkuri
(Hg) dalam gas bumi.
Aktivasi karbon aktif dilakukan secara fisika dan kimia.
Aktivasi secara fisika dilakukan dengan memragamkan suhu pemanasan, yaitu
650, 700, dan 800 °C. Aktivasi kimia dilakukan
dengan menggunakan activator
ZnCl
2yang diragamkan dengan konsentrasi 3%, 5%, dan 7% (w/v). Kondisi
optimum aktivasi pada penelitian ini ialah karbon aktif dengan perendaman
aktivator ZnCl
2pada konsentrasi 7% setelah pemanasan suhu 700 °C, ditunjukkan
dengan bilangan iodin sebesar 710.48 mg/g dan daya jerap sebesar 41.96%. Hasil
tersebut didukung dengan analisis metode Brunauer, Emmet, and Teller, adsorben
dengan diameter lebih kecil mempunyai luas permukaan yang lebih besar dan
daya jerap lebih besar. Analisis mikroskop elektron payaran yang di lengkapi
EDXA menunjukkan total volume pori terbanyak, yaitu pada karbon aktif dengan
perendaman ZnCl
2konsentrasi 7% setelah pemanasan. Semakin besar konsentrasi
aktivator kimia ZnCl
2, jumlah pori semakin banyak sehingga, kemampuan karbon
aktif untuk mengadsorpsi suatu adsorben semakin besar.
ABSTRACT
ARUMI PITALOKA. Optimization of Activation on Coconut Shell Activated
Carbon under Various Temperatures and ZnCl
2Concentrations as Activator.
Supervised by CHARLENA dan LISNA ROSMAYATI.
Coconut shell activated carbon could be used as adsorbent for impurities with
high capacity absorption. One of its functions is in the oil and gas indusri to
eliminate mercury (Hg) in natural gas. Activation of the activated carbon was
done by physicals and chemical means. Activation was carried out by heating at
temperatures of 650, 700, dan 800 °C. Chemical activation was performed using
ZnCl
2in concentration of 3%, 5% and 7% (w/v). The optimum conditions in this
study was, immersion in ZnCl
27% after at 700° C, as indicated by its iodine
number of 710.48 mg/g and adsorption capacity of 41.96%. These results are
supported by the method of analysis of Brunauer, Emmett and Teller, that
adsorbent with smaller diameter has larger surface and absorption capacity.
Analysis of electron microscopy microscope equipped with EDXA also showed
the highest total pore volume of the activated carbons was that immersed in ZnCl
27% after heating. The greater the concentration of chemical activators ZnCl
2, the
OPTIMALISASI AKTIVASI KARBON AKTIF TEMPURUNG
KELAPA DENGAN RAGAM SUHU DAN KONSENTRASI
AKTIVATOR ZnCl
2ARUMI PITALOKA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Optimalisasi Aktivasi Karbon Aktif Tempurung Kelapa dengan Ragam
Suhu dan Konsentrasi Aktivator ZnCl
2Nama : Arumi Pitaloka
NIM : G44070042
Disetujui
Pembimbing I
Dr. Charlena, M.Si
NIP 19671222 199403 2 002
Pembimbing II
Dra. Lisna Rosmayati, M.Si
NIP 19680905 199403 2 002
Diketahui
Ketua Departemen Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas berkat limpahan
rahmat dan hidayah-Nya penulis dapat menyelesaikan karya ilmiah dengan judul
Optimalisasi Aktivasi Karbon Aktif Tempurung Kelapa dengan Ragam Suhu dan
Bobot Aktivator ZnCl
2.Salawat serta salam semoga selalu tercurahkan kepada
Nabi Muhammad SAW, keluarganya, dan semoga kita semua menjadi
pengikutnya hingga akhir zaman.
Penulis mengucapkan terima kasih kepada Ibu Dr. Charlena, M.Si dan Ibu
Dra. Lisna Rosmayati, M.Si selaku pembimbing yang senantiasa memberikan
arahan, dorongan semangat, dan doa kepada penulis selama melaksanakan
penelitian. Penulis juga mengucapkan terima kasih kepada
staf Teknogas di
„LEMIGAS‟, Yudha, Risan, Hadi, Bapak Nanang, Bapak Widodo, atas bantuan
serta masukan selama penelitian berlangsung.
Terima kasih tak terhingga penulis ucapkan kepada Papa Ir. Moch.
Dwiyanto, Mama Dra. Sudarmi, Adik Arief, Bude Endang, Om Tris, serta seluruh
keluarga atas doa, nasehat, semangat dan kasih sayangnya. Terima kasih kepada
Narendra Wisnu Cakti atas hati, waktu, pikiran, dan semangatnya selalu
menemani penulis. Kepada Mutia, Feni, Wahyuni, Pertiwi, Siti, Ardita, Dwi Putri,
serta teman-teman seperjuangan di Laboratorium Kimia Anorganik dan Kimia
IPB yang telah membantu memberi masukkan dan saran, penulis mengucapkan
terima kasih.
Penulis berharap karya ilmiah ini dapat bermanfaat bagi pembaca dan
perkembangan ilmu pengetahuan.
Bogor, Desember 2011
RIWAYAT HIDUP
Penulis dilahirkan di Bantul pada tanggal 16 Februari 1990 dari ayah Ir.
Moch. Dwi Yanto dan ibu Dra. Sudarmi. Penulis adalah putri pertama dari dua
bersaudara. Tahun 2007 penulis lulus dari SMAN 3 Tangerang dan pada tahun
yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui
jalur Undangan Seleksi Masuk IPB (USMI) dan diterima di Departemen Kimia,
Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis aktif organisasi IMASIKA sebagai
staf Pengembangan Kimia dan Seni pada tahun 2008/2009 serta menjadi asisten
praktikum Kimia Tingkat Persiapan Bersama (TPB) pada tahun ajaran 2009/2010
dan asisten Kimia Lingkungan 2010/2011. Penulis juga pernah mengajar mata
kuliah Kimia TPB di bimbingan belajar dan privat mahasiswa “Avogadro”. Selain
itu, Penulis sekarang juga sedang menjalankan bisnis di PT. Melia Nature
Indonesia. Bulan Juli
–
Agustus 2009 Penulis melaksanakan magang di Pusat
Penelitian dan Pengembangan Minyak dan Gas Bumi “LEMIGAS”
, bulan
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN
... ……….1METODE
Alat dan Bahan
... 2Lingkup Kerja
... 2Tahap Preparasi
... 2Tahap Aktivasi Karbon
... 2Tahap Lanjutan Aktivasi Karbon
... 2Tahap Pengujian
... 2HASIL DAN PEMBAHASAN
Preparasi Karbon
... 3Aktivasi Karbon
... 4Pengujian Karbon Aktif
... 4SIMPULAN DAN SARAN
Simpulan
... 9Saran
... 9DAFTAR PUSTAKA
... 9DAFTAR TABEL
Halaman
1 Data EDXA massa Zn dan Cl pada karbon aktif suhu optimum 700 °C ... 7
2 Hasil analisis BET pada suhu optimum 700 °C ... 8
DAFTAR GAMBAR
Halaman
1 Struktur grafit ... 4
2 Karbon hasil ayakan 70 mesh ... 4
3 Hubungan ragam konsentrasi ZnCl
2dan suhu 650, 700, dan 800 °C
terhadap
bilangan iodin karbon aktif dengan perendaman ZnCl
2setelah pemanasan
…..
.5
4 Bilangan iodin karbon aktif pemanasan suhu 700 °C dengan
perlakuan
perendaman ZnCl
2setelah pemanasan, perendaman ZnCl
2sebelum pemanasan,
dan perendaman ZnCl
2sebelum dan setelah pemanasan ... 5
5 Daya jerap karbon aktif pemanasan suhu 700 °C dengan
perlakuan perendaman
ZnCl
2setelah pemanasan, perendaman ZnCl
2sebelum pemanasan, dan
perendaman ZnCl
2sebelum dan setelah pemanasan ... 6
6 Pola difraksi sinar-X dispersif energi karbon aktif perendaman ZnCl
2konsentrasi 7% setelah pemanasan ... 7
7 Hasil morfologi karbon aktif perbesaran 50-
20 μm
dengan perendaman ZnCl
2DAFTAR LAMPIRAN
Halaman
1 Bagan alir proses aktivasi karbon aktif ... 12
2 Pembuatan pelarut dan larutan standar ... 13
3 Tabel data analisis penetapan bilangan iodin dan daya jerap karbon aktif ... 14
4 Perhitungan standardisasi larutan dalam penetapan bilangan iodin karbon aktif
perendaman ZnCl
2setelah pemanasan pada suhu 700 °C ... 16
5 Perhitungan bilangan iodin dan daya jerap karbon aktif ... 18
6 Data SEM dan EDXA karbon aktif dengan perendaman
ZnCl
2setelah
pemanasan pada suhu optimum 700 °C ... 19
7 Data hasil BET karbon aktif perendaman ZnCl
2konsentrasi 7% setelah
PENDAHULUAN
Indonesia merupakan negara yang mempunyai areal tanaman kelapa terluas di dunia sekitar ± 3.7 juta ha. Pemanfaatan komoditas kelapa tercatat cukup besar, hampir seluruh bagian kelapa termasuk limbah tempurung kelapa dapat dimanfaatkan menjadi sesuatu yang bernilai ekonomis. Limbah tempurung kelapa menjadi salah satu teknologi alternatif yang menunjang pertumbuhan industri di Indonesia serta menghasilkan nilai tambah cukup besar dengan dilakukan pengolahan menjadi karbon aktif (Prastowo et al. 2008).
Karbon aktif adalah bahan padat yang berpori-pori dan merupakan hasil pembakaran dari bahan yang mengandung 85−95% unsur
C (Chand et al. 2005). Selain tempurung kelapa, karbon aktif dapat dibuat dari semua bahan yang mengandung karbon, diantaranya: residu pabrik kertas, residu pengolahan minyak, kokas dari batubara, minyak bumi (Haryadi et al. 2005), dan limbah kulit singkong (Sudaryanto et al. 2006).
Pemilihan tempurung kelapa sebagai bahan baku karbon aktif atas dasar kualitas karbon yang dihasilkan lebih baik dari pada bahan lain, biayanya relatif lebih murah, dan prosesnya cukup sederhana (Alaerts et al. 1989). Selain itu, pemilihan karbon aktif tempurung kelapa juga didasarkan pada potensinya yang cukup besar. Karbon aktif tempurung kelapa secara luas digunakan dalam berbagai aplikasi dan dimanfaatkan untuk mengatasi permasalahan di berbagai bidang industri (Kismurtono et al. 1999). Khususnya di industri migas, seperti di kepulauan Arun dan Bontang, karbon aktif tempurung kelapa dijadikan adsorben karena adsorpsinya yang tinggi dalam menjerap pengotor (Allwar et al. 2008) sehingga dapat meningkatkan kualitas produksi migas dengan menaikkan harga dan nilai jual produk migas tersebut.
Karbon aktif komersial pada umumnya digunakan sebagai adsorben untuk mengeliminasi kandungan merkuri (Hg) dalam gas bumi. Kehadiran merkuri dalam gas bumi sekalipun dalam jumlah yang kecil dinilai merugikan karena dapat menurunkan umur katalis, menyebabkan korosi pada peralatan dan fasilitas proses di industri migas, khususnya pada pipa penukar panas alumunium (Zeng et al. 2004).
Pemisahan merkuri dapat dilakukan melalui proses adsorpsi, diantaranya dengan
adsorpsi fisik maupun kimia pada konsentrasi merkuri yang rendah dalam kandungan gas bumi. Beberapa metode dan bahan kimia dapat digunakan untuk impregnasi agar dapat memodifikasi karbon aktif untuk meningkatkan kemampuan adsorpsi.
Metode aktivasi yang umum digunakan dalam pembuatan karbon aktif adalah pemanasan (aktivasi secara fisika) dan bahan kimia. Proses aktivasi dilakukan dengan meragamkan perlakuan terhadap suhu aktivasi dan konsentrasi aktivator. Ragam suhu yang digunakan pada penelitian ini yaitu suhu 650, 700, dan 800 °C dialiri gas N2 dengan laju
aliran sebesar 150 cm3/menit STP (Alhamed
2006). Aktivator yang dapat digunakan untuk aktivasi karbon aktif secara kimia adalah hidroksida logam alkali, garam-garam karbonat seperti Na2CO3 dan K2CO3 (Adinata
et al. 2007), garam-garam klorida seperti NaCl, KCl, CaCl2, MgCl2, AlCl3 (Ioannidou
dan Zabaniotou 2007), dan ZnCl2 (Wang et al.
2010), K2HPO4 (Aber et al. 2009), Na2HPO4
(Gercel et al. 2007), dan asam-asam anorganik seperti H2SO4 dan H3PO4 (Gimba et
al. 2009). Penelitian ini menggunakan ZnCl2
sebagai aktivator kimia. Penggunaan ZnCl2
diragamkan berdasarkan konsentrasi 3%, 5%, dan 7% (w/v). Penambahan aktivator ZnCl2
bertujuan untuk membentuk pori baru pada karbon aktif sehingga luas permukaan semakin besar dan meningkatkan kemampuan adsorpsi (Zeng et al. 2004).
Kemampuan adsorpsi dan kualitas dari karbon aktif dapat diketahui melalui pengujian bilangan iodin mengunakan metode American Water Works Association(AWWA) B604-96, metode tersebut didasarkan pada titrasi iodometri. Pencirian lain dilakukan dengan mengukur volume pori dan luas permukaan adsorben dari adsorpsi isoterm nitrogen yang diukur pada 77K menggunakan metode Brunauer, Emmet, and Teller (BET) (Spahis et al. 2008). Morfologi karbon aktif dapat dilihat menggunakan mikroskop elektron payaran (SEM) yang dilengkapi EDXA untuk melihat dan mengukur Cl yang terikat pada atom karbon.
Penelitian ini bertujuan mendapatkan suhu dan konsentrasi aktivator ZnCl2 optimum
2
METODE Alat dan Bahan
Alat-alat yang digunakan untuk aktivasi meliputi oven, tabung baja, tanur, desikator, neraca analitik, pH meter, cawan penguap dengan tutup, ayakan ukuran 70 mesh, alat gelas, pipet volumetrik 10 mL, 25 mL, dan 50 mL, kertas saring Whatman No. 40. Alat untuk pencirian meliputi BET Sorptometer- 201APC dan SEM JEOL JSM-6390LA yang dilengkapi dengan JEOL-EDXA.
Bahan-bahan yang digunakan meliputi karbon tempurung kelapa komersial berasal dari PT AIM TOPINDO daerah Garut, Jawa Barat, larutan ZnCl2, HCl, H2SO4, KI, I2,
Na2S2O7, K2Cr2O7, indikator kanji dan
akuades.
Lingkup Kerja
Penelitian ini dilakukan dalam tiga tahapan, pertama yaitu persiapan sampel dan pembuatan larutan standar, kedua yaitu aktivasi sampel, ketiga yaitu pengujian bilangan iodin (AWWA B604-96) dan pencirian sampel karbon dengan BET dan SEM EDXA. Bagan alir penelitian dapat dilihat pada Lampiran 1.
Tahap Preparasi Persiapan Sampel
Karbon tempurung kelapa komersial dikeringkan pada suhu 60 °C dan digerus hingga menjadi partikel yang lebih kecil dan halus. Selanjutnya, karbon diayak dengan ayakan ukuran 70 mesh.
Tahap Aktivasi Karbon
Serbuk karbon ditimbang sebanyak 100 g, kemudian dikeringkan dalam oven dengan suhu 90 °C selama ± 1 jam. Setelah kering, sampel dimasukkan ke dalam tabung baja dan dipanaskan dengan tanur hingga mencapai suhu 650, 700, dan 800 °C dengan dialiri gas N2 laju aliran sebesar 150 cm3/menit STP.
Selama proses berlangsung laju panas dan aliran nitrogen harus dijaga konstan. Sampel dipertahankan pada suhu 650, 700, dan 800 °C selama 1 jam sebelum didinginkan dibawah aliran N2. Setelah dingin, sampel dicuci secara
berurutan dengan larutan HCl 0.5 N, air hangat kemudian air dingin suhu ruang untuk menghilangkan sisa residu organik dan mineral. Pencucian dengan akuades dilanjutkan sampai air pembilas netral (pH
sekitar 7). Aktivasi secara kimia dengan merendam serbuk karbon tempurung kelapa dalam larutan ZnCl2 3%, 5%, 7% (w/v)
selama ± 24 jam. Pengeringan dilakukan menggunakan wadah cawan penguap didalam oven selama ± 8 jam pada suhu 100 °C. Sampel kemudian dianalisis bilangan iodinnya.
Tahap Lanjutan Aktivasi Karbon
Setelah didapat suhu yang optimum, kemudian dilanjutkan dengan menggunakan perlakuan yang berbeda yaitu perendaman ZnCl2 sebelum aktivasi pemanasan pada suhu
optimum.
Serbuk karbon direndam dengan larutan ZnCl2 3%, 5%, 7% (w/v) selama ± 24 jam.
Campuran (hasil rendaman) dikeringkan dalam pengering oven pada suhu 900 C ± 1
jam. Sampel dimasukkan ke dalam tabung baja dan dipanaskan dengan tanur hingga mencapai suhu optimum dengan dialiri gas N2
150 cm3/menit STP. Sampel tersebut
dipertahankan pada suhu yang telah ditentukan tersebut selama 1 jam. Setelah dingin, sampel dicuci secara berurutan dengan 0.5 N HCl, air hangat, lalu air dingin pada suhu ruang. Sampel dikeringkan dengan cawan penguap dalam oven selama + 8 jam pada suhu 100 °C. Setelah itu, dianalisis bilangan iodinnya.
Tahap lanjutan dengan perlakuan sampel direndam ZnCl2 sebelum dan setelah
pemanasan pada suhu optimum. Sampel direndam kembali dengan dengan larutan ZnCl2 3%, 5%, 7% (w/v) selama ± 24 jam.
Campuran (hasil rendaman) dikeringkan dalam pengering oven pada suhu 100 °C ± 8 jam. Selanjutnya, karbon aktif dianalisis bilangan iodinnya dan dibandingkan dengan hasil karbon aktif perendaman ZnCl2 setelah
pemanasan.
Tahap Pengujian
Penetapan Bilangan Iodin (AWWA B604-96)
3
filtrat hasil saringan dititrasi dengan larutan Na2S2O7 0.1 N yang telah distandardisasi.
Pembuatan pelarut dan larutan standar dalam percobaan ini dapat dilihat pada Lampiran 2. Titrasi dilakukan hingga mendekati titik akhir (berwana kuning muda seulas). Selanjutnya, ditambahkan tiga tetes indikator kanji ke dalamnya dan dititrasi kembali hingga terjadi perubahan warna dari biru tua menjadi hijau muda. Nilai bilangan iodin dihitung dan daya jerap iodin dalam satuan persen.
Nilai bilangan iodin tersebut dapat diketahui dengan tahapan perhitungan menggunakan rumus :
nilai bilangan iodin = dengan:
=
Keterangan :
X/m = miligram iodin yang teradsorbsi pergram karbon
A = normalitas I2 × 12693
B = normalitas Na2S2O7 × 126.93
Kemampuan daya jerap iodin dapat diukur menggunakan rumus:
Daya jerap = × 100%
Keterangan:
b = volume Na2S2O7 pada titrasi blangko
a = volume Na2S2O7 pada titrasi sampel
N = normalitas Na2S2O7
126.9 = bobot atom iodin
Pengukuran Diameter Pori Karbon Aktif dengan Brunauer, Emmet, and Teller (BET)
Pencirian karbon aktif ditentukan dengan adsorpsi N2 pada −196 °C (77K),
menggunakan alat model BET Sorptometer- 201APC (Zabihi et al. 2010). BET berfungsi untuk mendeteksi permukaan area contoh, menggunakan metode adsorpsi gas N2 pada
padatan kemudian data yang diperoleh dihitung menggunakan teori BET.
Berikut persamaan BET:
Keterangan:
Va = volume gas standar keadaan STP (mL)
P = tekanan parsial gas (Pa)
Po = tekanan uap jenuh (Pa)
Vm = volume gas pada lapisan tunggal (mL)
C = tetapan gas
Jika dibuat garfik terhadap P/Po
maka akan diperoleh slope S = dan intersep I =
Harga Vm dapat diperoleh dari S, Vm =
Sehingga luas permukaan spesifik dapat dihitung dengan rumus:
S =
Keterangan:
S = luas permukaan spesifik (m2/g)
Vm = volume gas lapisan tunggal (mL)
m = massa molekul gas (g)
N = bilangan Avogadro (6.022 x 1023 mol-1) τ = luas penampang rata-rata suatu
molekul gas (0.162 nm2 untuk N 2)
(European Pharmacopoeia 2005 ).
Pengukuran Morfologi Karbon Aktif dengan Mikroskop Elektron Payaran (SEM) dan Sinar-X Dispersif Energi (EDXA)
Peralatan yang digunakan adalah SEM JEOL JSM-6390LA yang dilengkapi dengan JEOL-EDXA dan program untuk melihat sampel. SEM adalah jenis mikroskop elektron yang gambar permukaan sampel dengan menembakkan sinar energi tinggi elektron dalam suatu pola raster scan (Prabakaran et al. 2005). Sebagai tahapan persiapan, sampel serbuk karbon direkatkan kedalam wadah khusus lalu dilakukan pengamatan dan pengukuran secara kualitatif dan kuantitatif terhadap sampel yang dianalisis.
HASIL DAN PEMBAHASAN Preparasi Karbon
Karbon yang digunakan dalam penelitian ini berasal dari karbon tempurung kelapa komersial. Tempurung kelapa merupakan bagian dari buah tanaman kelapa (Cocus nuciefera L). Tempurung kelapa tergolong dalam kayu keras, didasarkan pada kandungan airnya yang berkisar 6−9%, dihitung dari
4
untuk karbon aktif maksimum 10% dan kadar abu maksimum 2.5%. Dalam penelitian ini karbon aktif didapatkan kadar air sebesar 6.73% dan kadar abu sebesar 2.08%. Semakin rendah kadar air, luas permukaan karbon semakin besar. Semakin rendah kadar abu, kemurnian dari karbon semakin besar (Zamrudy 2008).
Karbon aktif tersusun dari atom-atom karbon yang berikatan secara kovalen membentuk struktur heksagonal datar pada sebuah atom C pada setiap sudutnya (Gambar 1). Karbon aktif memiliki struktur beragam, di antaranya ada yang berbentuk granular, serbuk, serat, dan monolit (Vargas et al. 2010). Komponennya terdiri atas karbon terikat, abu, air, nitrogen, dan sulfur (Sembiring et al. 2003). Pencirian karbon aktif tempurung kelapa yang baik antara lain memiliki pori mikro yang tinggi, pori makro yang rendah, dan kekerasan cukup tinggi (Suzuki et al. 2007).
Gambar 1 Struktur grafit.
Persiapan sampel karbon dilakukan dengan pemanasan dan pengayakan. Pemanasan pada suhu 60 °C dilakukan untuk menghilanghan uap air (Haryadi et al. 2005). Pengayakan dengan ayakan ukuran 70 mesh dilakukan untuk memperoleh partikel yang lebih kecil dan halus. Hasil pengayakan 70 mesh dapat dilihat pada Gambar 2. Pemilihan ayakan ukuran sampel 70 mesh didasarkan pada penelitian sebelumnya Priagantina (2010), sampel yang memiliki bilangan iodin yaitu dari ukuran 50, 70, 80, dan 100 mesh, paling optimum adalah sampel berukuran 70 mesh. Ukuran partikel karbon akan mempengaruhi kemampuan penjerapan iodin. Partikel yang lebih halus diharapkan memiliki luas permukaan yang besar sehingga meningkatkan kemampuan adsorpsi.
Gambar 2 Karbon hasil ayakan 70 mesh.
Aktivasi Karbon
Aktivasi sampel karbon bertujuan untuk menghilangkan senyawa nonkarbon sehingga diperoleh unsur karbon murni, memperbesar pori dengan cara memecahkan ikatan hidrokarbon atau mengoksidasi molekul-molekul permukaan sehingga karbon mengalami perubahan sifat, baik fisika maupun kimia, yaitu luas permukaannya bertambah besar dan berpengaruh terhadap daya adsorpsi. Proses aktivasi dilakukan dengan meragamkan perlakuan terhadap suhu aktivasi dan konsentrasi aktivator ZnCl2.
Ragam suhu aktivasi karbon 650, 700, dan 800 °C dimaksudkan untuk mengetahui suhu yang optimum untuk karbon aktif tempurung kelapa sebagai adsorben. Pemanasan pada suhu 650, 700, dan 800 °C dengan dialiri gas N2 150 cm3/menit STP dimaksudkan agar
selama karbonisasi, dapat optimal pembentukkan pori karbon dan mencegah dekomposisi bahan organik menjadi CO2 dan
H2O, serta menghindari terjadinya reaksi
karbon dengan O2 (Hu et al. 2009).
Pencucian karbon setelah aktivasi dilakukan untuk menghilangkan sisa residu organik, kontaminan, mineral dan sisa-sisa logam yang tertinggal dalam rongga pori. Oksida logam yang tertinggal didalam pori dapat mempengaruhi daya jerap karbon aktif pada senyawa tertentu (Setianingsih et al. 2008). Kemampuan adsorpsi juga akan meningkat bila pH diturunkan yaitu dengan menambah asam-asam mineral, karena kemampuan asam mineral akan mengurangi ionisasi asam organik tersebut (Sembiring et al. 2003).
Perbedaan konsentrasi ZnCl2 dalam
aktivasi karbon dimaksudkan untuk mengetahui konsentrasi optimum aktivator kimia. Penggunaan ZnCl2 sebagai aktivator
kimia sangatlah penting karena selain dapat menghasilkan pori-pori baru yang mampu meningkatkan kemampuan adsorpsi merkuri, perendaman dengan ZnCl2 juga dapat
menghasilkan terbentuknya ikatan C-Cl dimana gugus Cl tersebut dapat mengikat merkuri (Hg) secara ikatan kimia menjadi HgCl atau HgCl2 (Zeng et al. 2004).
Pengujian Karbon Aktif
Karbon yang telah diaktifkan, akan memiliki pori-pori yang terbuka dan daya jerapnya tinggi. Karbon hasil aktivasi ditentukan bilangan iodin dan daya jerap iodin menggunakan metode AWWA B604-96. Karbon yang telah diaktivasi akan Permukaan dasar
Bagian tepi
Jarak antar lapisan
5
mengadsorpsi iodin yang ditambahkan, sisa iodin yang tidak teradsorpsi oleh karbon akan dititrasi dengan larutan natrium tiosulfat yang telah di standardisasi. Larutan standar dan pelarut yang digunakan ditunjukkan dalam Lampiran 2. Titik akhir titrasi ditandai dengan warna I2 yang hilang yaitu kuning seulas
setelah ditambahkan dengan indikator kanji, berubah dari warna biru tua menjadi tidak berwarna. Volume larutan tiosulfat yang tercatat digunakan untuk menentukan kemampuan karbon aktif tersebut dalam menyerap iodin. Reaksi yang terjadi dalam proses titrasi tersebut (Vogel 1989) :
I2 + 2S2O32- 2I- + S4O6
2-Daya adsorpsi karbon aktif terhadap iodin mengindikasikan kemampuan karbon aktif untuk mengadsorpsi komponen dengan bobot molekul rendah (Suzuki et al. 2007). Hasil penentuan bilangan iodin serta daya jerap setelah aktivasi dengan ragam suhu dan konsentrasi ZnCl2 dapat dilihat pada Lampiran
1.
Gambar 3 menunjukkan hubungan antara konsentrasi ZnCl2, suhu, dan hasil pengujian
bilangan iodin dengan perendaman setelah aktivasi. Semakin tinggi konsentrasi ZnCl2
dan suhu aktivasibilangan iodinnya semakin tinggi. Peningkatan suhu aktivasi mampu meningkatkan daya jerap karbon aktif terhadap iodium. Hal ini disebabkan karena semakin tinggi suhu, maka semakin banyak pelat-pelat karbon yang bergeser yang akan mendorong senyawa hidrokarbon tar dan senyawa organik lainnya untuk keluar pada saat aktivasi (Pari 2004). Karbon aktif dengan kemampuan menyerap iodin yang tinggi berarti memiliki luas permukaan yang lebih besar dan juga memiliki struktur mikropori dan mesopori yang lebih besar (Suzuki et al. 2007). Dalam pekerjaan ini diketahui bahwa aktivasi pada suhu 700 °C merupakan suhu paling optimum dibandingkan suhu 600 °C dan 800 °C.
Terlihat dalam Gambar 3, aktivasi pada suhu 800 °C memiliki nilai bilangan iodin yang lebih kecil dibandingkan pada suhu 700 °C. Hal tersebut disebabkan aktivasi dengan pemanasan pada suhu yang tinggi lebih dari suhu 700 °C akan merusak beberapa dinding pori pada karbon dan menimbulkan oksida logam yang akan menutupi dinding pori pada permukaan karbon (Allwar et al. 2008). Selain itu, pada suhu 800 °C jumlah iodin yang teradsorpsi mengalami penurunan seiring dengan meningkatnya konsentrasi larutan
ZnCl2, karena sifat dari proses adsorpsi
eksotermik (Zeng et al. 2004). Akibatnya adsorben tidak dapat mengadsorpsi iodin dengan maksimal sehingga daya jerapnya menurun.
Gambar 3 Hubungan ragam konsentrasi ZnCl2
dan suhu = 650 °C; = 700 °C; - = 800 °C terhadap bilangan iodin karbon aktif dengan perendaman ZnCl2 setelah pemanasan.
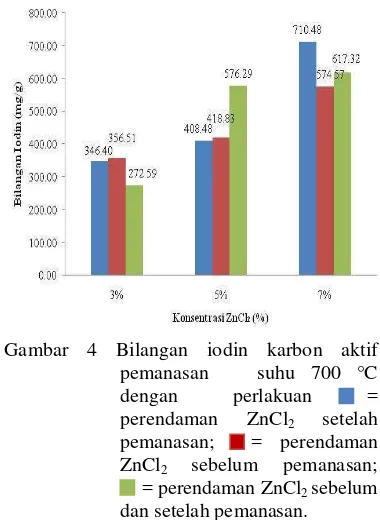
Perlakuan kondisi aktivasi optimum juga dilakukan pada suhu optimum 700 °C dengan membandingkan nilai bilangan iodin karbon aktif yang diberi perlakuan perendaman sebelum pemanasan, perendaman setelah pemanasan, serta perendaman sebelum dan setelah pemanasan. Ragam konsentrasi ZnCl2
juga diterapkan pada setiap perlakuan (Gambar 4).
Gambar 4 Bilangan iodin karbon aktif pemanasan suhu 700 °C dengan perlakuan = perendaman ZnCl2 setelah
pemanasan; = perendaman ZnCl2 sebelum pemanasan;
= = perendaman ZnCl2 sebelum
6
Hasil karbon aktif perendaman ZnCl2
sebelum pemanasan didapat bilangan iodinnya lebih rendah dari perlakuan karbon aktif dengan perendaman ZnCl2 setelah pemanasan
(Lampiran 3), karena pori karbon aktif belum terbuka ketika dilakukan perendaman ZnCl2
terlebih dahulu, sehingga penjerapan iodin kurang maksimal. Sedangkan, hasil aktivasi dengan perendaman ZnCl2 sebelum dan
setelah pemanasan memiliki hasil lebih besar dibandingkan perendaman ZnCl2 sebelum
pemanasan. Hal tersebut dikarenakan ikatan karbon dengan larutan ZnCl2 lebih banyak
dalam produk akan tetapi akan membuat dinding pori dari karbon rapuh karena terbentuk pori yang terlalu banyak sehingga kemampuan menjerap iodin kurang maksimal. Perbandingan dari ketiga perlakuan karbon aktif, yaitu perendaman ZnCl2 setelah
pemanasan, perendaman ZnCl2 sebelum
pemanasan, dan perendaman ZnCl2 sebelum
dan setelah pemanasan ternyata bilangan iodin dan daya jerap lebih maksimal pada kondisi perendaman ZnCl2 setelah pemanasan, karena
karbon yang dihasilkan dari aktivasi kimia lebih tinggi daripada aktivasi fisika (Suzuki et al. 2007). Efek penggunaan bahan kimia mampu meningkatkan jumlah pori-pori. Menurut Zhang et al. (2005), aktivasi karbon aktif tempurung kelapa dengan aktivator ZnCl2 bertujuan untuk menambah porositas
karbon aktif yang akan terbentuk, sehingga luas permukaan lebih besar dan daya jerapnya meningkat. Berikut hubungan daya jerap iodin terhadap konsentrasi larutan ZnCl2 (Gambar
5).
Gambar 5 Daya jerap karbon aktif pemanasan suhu 700 °C dengan perlakuan = perendaman ZnCl2 setelah
pemanasan; = = perendaman ZnCl2 sebelum pemanasan; =
perendaman ZnCl2 sebelum dan
setelah pemanasan.
Konsentrasi aktivator ZnCl2 dari 3%, 5%,
dan 7% pada pemanasan suhu 700 °C terlihat mengalami peningkatan cukup signifikan, semakin besar konsentrasi larutan ZnCl2,
semakin besar bilangan iodin dan daya jerapnya. Hal tersebut dikarenakan ketika aktivasi pemanasan pada suhu 700 °C pori karbon terbentuk dan terbuka dengan sempurna terlihat pada Gambar 7, sehingga ketika dilakukan perendaman ZnCl2 dapat
memenuhi pori tersebut dengan ikatan Cl (Zeng et al. 2004). Karbon aktif dapat mengadsorpsi gas dan senyawa-senyawa kimia tertentu yang sifat adsorpsinya selektif, bergantung pada besar pori-pori dan luas permukaan. Daya jerap karbon aktif sangat besar, yaitu 25–1000% terhadap bobot karbon aktif (Sembiring et al. 2003).
Menurut Pari (2004), besarnya daya jerap terhadap iodin berkaitan dengan terbentuknya pori pada karbon aktif. Selain itu juga berhubungan dengan pola struktur mikropori yang terbentuk dan mengindikasikan besarnya diameter pori karbon aktif tersebut yang mampu dimasuki oleh molekul dengan diameter kurang dari 10Å. Terlihat dari hasil BET ukuran diameter karbon aktif pada penelitian ini lebih dari 100 Å (Tabel 1), sehingga akan mampu mengadsorpsi iodin.
Daya jerap karbon aktif dengan perendaman ZnCl2 setelah pemanasan pada
konsentrasi 3%, 5%, dan 7% berturut-turut 25.41%, 28.20%, dan 41.96%. Semakin meningkatnya konsentrasi ZnCl2, daya jerap
terhadap iodin makin besar . Semakin besar
daya jerap iodin berarti karbon tersebut memiliki luas permukaan dan pori yang lebih besar, sehingga daya jerap paling optimum yaitu konsentrasi ZnCl2 7% dengan
perendaman setelah pemanasan sebesar 41.96% memiliki standar deviasi 0.0000. Hasil penelitian ini memiliki bilangan iodin terbesar yaitu 710.48 mg/g. Bilangan iodin ini telah sesuai dengan standar minimum yang ditetapkan oleh AWWA B604-96 yaitu sebesar 500 mg/g. Selain itu, standar minimum juga ditetapkan oleh SII No.0258-79 yaitu sebesar 20% (200 mg/g).
7
pada kondisi optimum dapat dilihat padaTabel 1.
Tabel 1 Data EDXA massa Zn dan Cl pada karbon aktif suhu optimum 700 °C
Gambar 6 menunjukkan pola difraksi kandungan Zn dan Cl pada permukaan karbon aktif dengan perendaman aktivator ZnCl2
setelah pemanasan pada suhu optimum 700 °C. Terlihat bahwa kandungan Cl terbanyak pada konsentrasi ZnCl2 terbesar yaitu 7%.
Namun, dibandingkan dengan kandungan % massa Zn, % massa Cl lebih sedikit dikarenakan Zn tidak hanya berasal dari ZnCl2, Zn juga diindikasikan berasal dari ZnO
hasil pembakaran pada karbon yang tidak sempurna sehingga bereaksi dengan oksigen. Pola difraksi hasil EDXA pada konsentrasi ZnCl2 lainnya dapat dilihat pada Lampiran 6.
Gambar 6 Pola difraksi sinar-X dispersif energi karbon aktif dengan perendaman ZnCl2 konsentrasi
7% setelah pemanasan.
Hasil analisis SEM untuk melihat morfologi karbon aktif dapat dilihat pada Gambar 6. Terlihat semakin besar konsentrasi ZnCl2 jumlah pori semakin banyak,
kemampuan karbon aktif untuk menjerap semakin besar ditampilkan pada Gambar 7. Total volume pori terbanyak yaitu pada
karbon aktif dengan perendaman ZnCl2
konsentrasi 7% setelah pemanasan (Tabel 2).
Gambar 7 Hasil morfologi karbon aktif perbesaran 50-20 μm dengan perendaman ZnCl2 konsentrasi
3% (a), 5% (b), dan 7% (c) setelah pamanasan.
Pencirian selanjutnya pada penelitian ini menggunakan metode Brunauer, Emmet, dan Teller (BET) yang merupakan teknik untuk memperkirakan luas permukaan sebagai suatu parameter yang erat hubungannya dengan kemampuan adsorpsi suatu adsorben. Persamaan BET digunakan dalam menentukan luas permukaan karbon aktif dari adsorpsi isoterm nitrogen yang diukur pada 77K (Spahis et al. 2008). Analisis BET bertujuan untuk mengetahui karakter fisik dari karbon yang memiliki kemampuan optimum sebagai adsorben. Ciri fisik yang dianalisis yaitu ukuran diameter pori dan total volume pori, sehingga diharapkan luas permukaan akan dapat diperkirakan. Sampel karbon yang akan dianalisis harus bersih dari kontaminan seperti air dan minyak, sehingga perlu dilakukan pembersihan permukaan (degassing) sebelum sampel dianalisis. Proses pembersihan permukaan berlangsung selama 14 jam dengan cara menyimpan sampel dalam sel gelas yang kemudian dipanaskan dengan aliran gas nitrogen dalam kondisi vakum. Hasil analisis BET ditunjukkan pada Tabel 2. Konsentrasi
ZnCl2 (b/v) Massa (%)
(%) Zn Cl
3% 2.42 1.48
5% 1.93 1.60
7% 20.50 4.58
(a)
c (b)
(c)
8
Tabel 2 Hasil analisis BET pada karbon aktif suhu optimum 700 °C
Ragam
Perlakuan Diameter Pori Total Volume Pori
(Å) (cc/g)
3%* tidak
terdeteksi 0.0002618
5%* 228.547 0.001048
7%* 160.242 0.007596
7%** 105.790 0.009671
7%*** 262.725 0.005042 Keterangan: *: perendaman ZnCl2 setelah pemanasan
**: perendaman ZnCl2 sebelum pemanasan ***: perendaman ZnCl2 sebelum dan setelah
pemanasan.
Karbon aktif dari tempurung kelapa biasanya berbentuk granular yang sangat keras
dengan diameter pori berkisar 20−500 Å, tipe pori lebih halus (mesopori), dan digunakan dalam fase gas sebagai penyerap uap (Setianingsih et al. 2008). Tabel 2 menunjukkan analisis BET pada suhu optimum 700 °C yaitu perendaman ZnCl2
konsentrasi 3% setelah pemanasan ukuran diameter pori tidak terdeteksi. Karbon aktif pada perendaman ZnCl2 konsentrasi 5%
setelah pemanasan memiliki diameter pori sebesar 228.547 Å lebih besar dibandingkan dengan diameter pori pada perendaman ZnCl2
konsentrasi 7% setelah pemanasan sebesar 160.242 Å. Diameter pori terbesar yaitu pada karbon aktif dengan perendaman ZnCl2
sebelum dan setelah pemanasan yaitu sebesar 262.725 Å dan diameter terkecil pada karbon aktif perendaman ZnCl2 konsentrasi 7%
sebelum pemanasan sebesar 105.790 Å. Ukuran diameter suatu adsorben yang lebih kecil ternyata lebih efektif dalam proses adsorpsi dibandingkan dengan diameter yang besar. Diameter pori berbanding terbalik dengan luas permukaan. Hal tersebut disebabkan karena adsorben dengan diameter lebih kecil mempunyai luas permukaan yang lebih besar dan menyebabkan daya jerap lebih besar (Purnama dan Setiati 2004). Karbon aktif perendaman ZnCl2 konsentrasi 7%
sebelum pemanasan diharapkan memiliki luas permukaan yang besar.
Total volume pori pada perendaman ZnCl2 konsentrasi 7% setelah pemanasan yaitu
0.007596 cc/g lebih besar dibandingkan dengan konsentrasi ZnCl2 3% dan 5%
(Lampiran 7). Zhang et al. (2005) menyatakan bahwa luas permukaan BET berbanding lurus dengan volume adsorben. Semakin besar luas permukaan, volume pori dan daya jerap semakin besar. Rata-rata
volume pori meningkat seiring dengan meningkatnya konsentrasi larutan ZnCl2
(Zeng et al. 2004).
Hu et al. (2005) menyatakan bahwa karbon aktif sebagai adsorben memiliki porositas tinggi dan luas permukaan yang besar. Luas permukaan karbon aktif berkisar antara 300–2000 m2/g dan volume pori lebih
besar dari 30 cm3/100 g. Total volume pori
terbesar pada karbon aktif perendaman ZnCl2
konsentrasi 7% sebelum pemanasan yaitu 0.009671 cc/g dengan diameter pori terkecil yaitu 105.790 Å. Hasil dari analisis karakter fisik karbon aktif pada penelitian ini didapatkan porositas yang rendah. Hal tersebut diduga preparasi awal karbon aktif kurang maksimal, ketika perendaman ZnCl2
kurang proses pengadukan sehingga penjerapan ZnCl2 kurang maksimum, masih
ada karbon yang tidak teraktifkan sempurna. Karbon aktif juga dibiarkan terlalu lama dalam suhu ruang karena efektivitas dari adsorben tidak akan berlangsung lama.
Kondisi karbon aktif dengan perendaman ZnCl2 setelah pemanasan yang diharapkan
memiliki total volume pori lebih besar ternyata lebih rendah. Hal tersebut diduga ketika dialirkan gas nitrogen (analisis BET) pada pori karbon yang berfungsi untuk membersihkan dan mengosongkan pori, pori karbon masih tertutup dengan oksida logam Zn, sehingga nitrogen tidak dapat masuk kedalam pori dengan sempurna. Keberadaan abu hasil oksida logam yang berlebihan dapat menyebabkan terjadinya penyumbatan pori-pori karbon aktif sehingga luas permukaan karbon aktif menjadi berkurang (Scroder dan Elisabeth2006). Menurut Zeng et al. (2004), Peresapan aktivator ZnCl2 berlebih akan
menurunkan luas permukaan BET sehingga volume pori dari sampel karbon aktif akan semakin kecil dikarenakan penyumbatan porositas internal dengan masuknya molekul ZnCl2. Selain itu juga menyebabkan korosi di
mana karbon aktif yang terbentuk menjadi rusak. Hal tersebut dibuktikan dari hasil EDXA pada Tabel 1 bahwa massa Zn (%) lebih besar daripada massa Cl (%). Terdapat oksida logam ZnO yang cukup banyak pada karbon aktif dengan konsentrasi 3%, 5%, dan 7% dengan perendaman setelah pemanasan (Lampiran 6).
9
menyebabkan korosi pada peralatan dan fasilitas proses di industri migas. Berikut ini merupakan reaksi pengikatan aktivator kimia ZnCl2 pada karbon aktif ketika diaplikasikan
untukmenjerap merkuri menurut Zeng et al. (2004):
ZnCl2 + CnHxOy→ Zn + [Cl2− CnHxOy]
Hg0+ [Cl]ˉ → [HgCl]+ + 2e
Hg0+ 2[Cl]ˉ → [HgCl 2] + 2e
[HgCl2] + 2[Cl]ˉ → [HgCl4]2–
ZnCl2 berikatan dengan karbon , sehingga
gugus dari Cl akan mengisi pori dalam karbon. Cl fungsional grup akan meng adsorpsi kontaminan dalam gas bumi seperti merkuri berbentuk Hg° yaitu merkuri yang teroksidasi dalam bentuk merkuri oksida (HgO). Cl yang ditambahkan berlebih sehingga akan terbentuk ragam kompleks, [HgCl]+, [HgCl
2], dan [HgCl4]2–.
SIMPULAN DAN SARAN
Simpulan
Aktivasi karbon aktif tempurung kelapa yang optimum, yaitu pada perendaman aktivator ZnCl2 dengan konsentrasi 7%
setelah pemanasan pada suhu 700 °C, dengan bilangan iodin sebesar 710.48 mg/g dan daya jerap sebesar 41.96%. Hasil pencirian dengan SEM dan EDXA membuktikan karbon aktif dengan perendaman ZnCl2 konsentrasi 7%
setelah pemanasan memiliki kandungan Cl terbesar, yang nantinya akan digunakan untuk mengikat merkuri dalam gas bumi. Hasil pencirian dengan BET menunjukkan hasil yang berbeda, karbon aktif dengan perendaman ZnCl2 konsentrasi 7% sebelum
pemanasan memiliki total volume pori terbesar berbanding lurus dengan luas permukaan. Semakin besar konsentrasi activator ZnCl2, semakin besar kemampuan
mengadsorpsi suatu adsorben.
Saran
Penelitian lebih lanjut perlu dilakukan untuk menyempurnakan aktivasi karbon aktif menggunakan metode ini dengan memaksimalkan tahapan preparasi, seperti pengadukan saat merendaman ZnCl2 dan
penyimpanan karbon aktif jangan terlalu lama karena karbon aktif mempunyai masa efektivitas. Perlu dilakukan juga pengujian luas permukaan karbon aktif serta adsorpsi merkuri pada gas bumi.
DAFTAR PUSTAKA
Abdullah M, Virgus Y, Nirmin, Khairurrijal. 2008. Sintesis nanomaterial. J Nanosains Nanoteknol 1:33-57.
Aber S, Khataee A, Sheydaei M. 2009. Optimization of activated carbon fiber preparation from Kenaf using K2HPO4 as
chemical activator for adsorption of phenolic compounds. Bioresour Technol 100:6586-6591.
Adinata D, Daud W, Aroua MK. 2007. Preparation and characterization of activated carbon from palm shell by chemical activation with K2CO3.
Bioresour Technol 98:145-149.
Alaerts GJ, Jitjaturun V, Kelderman P. Use of coconut shell based activated carbon for chromium (VI) removal. Water Science Technol 1701-1704.
Alhamed YA. 2006. Activated carbon from dates' stone by ZnCl2 activation. JKAU:
Eng. Sci 17:75–100.
Allwar, Noor M, Asri M. 2008. Textural characteristics of activated carbons prepared from oil palm shells activated with ZnCl2 and pyrolysis under nitrogen
and carbon dioxide. Journal of Physical Science 19:93-104.
[AWWA] American Water Works Association B604. 1996. Granular Activated Carbon.
Chand B, Roop, Meenakshi G. 2005. Activated Carbon Adsorption. New York: Lewis.
European Pharmacopoeia 20926. 2005. Spesific Surface Area by Gas Adsorption.
Gercel O, Ozcan A, Ozcan AS, Gercel HF. 2007. Preparation of activated carbon from a renewable bio-plant of Euphorbia rigida by H2SO4 activation and its adsorption
behavior in aqueous solutions. Appl Surface Sci 253:4843-4852.
Gimba CE, Ocholi O, Egwaikhide PA, Muyiwa T, Akporhonor E. 2009. New raw material for activated carbon. I. Methylene blue adsorption on activated carbon prepared from Khaya senegalensis fruits. Cien Inv Agraria 36:107-114.
10
cotton wood and coconut shell by pyrolisis with ceramic furnace. Indones J Chem 5:121-124.
Hu C, Zhou J, He S, Luo Z, Cen K. 2009. Effect of chemical activation of an activated carbon using zinc chloride on elemental mercury adsorption. Fuel Processing Technology 90:812-817. Ioannidou O, Zabaniotou A. 2007.
Agricultural residues as precursors for activated carbon production. Renewable & Sustainable Energy Reviews 11:1966-2005.
Kismurtono M, Sumarsono, Kurniadi M. 1999. Pembuatan arang aktif dari tempurung kelapa dan kayu lamtorogung dengan cara aktivasi kukus. Di dalam: Prosiding Seminar Nasional III Kimia dalam Pembangunan Hotel Santika, Yogyakarta, 20-21 April 1999. Bandung: LIPI Bandung, hlm 590-599.
[MSDS] Material Safety Data Sheet Number Z2280. 2009. Zinc Chloride.
Pari G. 2004. Kajian Struktur Arang Aktif dari Serbuk Gergaji Kayu sebagai Adsorben Emisi Formaldehida Kayu Lapis [Disertasi Program Doktor]. Bogor: Sekolah Pascasarjana. Institut Pertanian Bogor. Prabakaran K, Balamurunga A, Rajeswari S.
2005. Development of calcium phosphate
bases apatie from Hen‟s eggshell. Bull Mat Sci 28:115-119.
Prastowo B, Allorerung D, Mahmud Z. 2008. Peluang kelapa untuk pengembangan produk kesehatan. Jurnal Pengembangan Inovasi Pertanian 4:298-315.
Priagantina B. 2010. Kondisi optimum pembuatan arang aktif dari tempurung kelapa sebagai adsorben [skripsi]. Bogor: Pusat Pendidikan dan Pelatihan Industri, Akademi Kimia Analisis.
Purnama H, Setiati. 2004. Adsorpsi limbah tekstil sintesis dengan jerami padi. Jurnal Teknik Gelagar 15:1-9.
Scroder, Elisabeth. 2006. Experiment on the Generation of Activated Carbon from Biomass. German: Institute for Nuclear Energy Technologies Forschungs Karlsruhe.
Sembiring, Meiliata T, Sinaga T. 2003. Pengenalan dan proses pembuatan arang
aktif [tesis]. Medan: Sekolah Pascasarjana, Universitas Sumatera Utara.
Setianingsih T, Hasanah U, Darjito. 2008. Study of NaOH- activation temperature influence toward character of mesoporous carbon based on textile sludge waste. Indones J Chem 8:348-352.
Spahis N, Addoun A, Mahmoudi H, Ghaffour N. 2008. Purification of water by activated carbon prepared from olive stones. Desalination 222:519-527.
Sudaryanto Y, et al. 2006. High surface area activated carbons prepared from cassava peel by chemical activation chemical engineering. Widya Mandala Surabaya Catholic University. hlm 734-739.
Suzuki RM, Andrade AD, Sousa JC, Rollemberg. 2007. Preparation and characterization of activated carbon from rice bran. Biores Technol 98:1985-1991. Vargas DP, Giraldo L, Moreno JC. 2010.
Preparation and characterization of activated carbon monoliths with potential application as phenol adsorbents. E-Journal of Chemistry 7:531-539.
Vogel. 1989. Textbook of Macro and Semimicro Qualitative Inorganic Analysis 5th. London: Longman Group Limited. Wang Jun, et al. 2010. Preparation of
activated carbon from a renewable agricultural residue of pruning mulberry shoot. African Biotechnology 9:2762-2767.
Zabihi M, Haghighi AA, Ahmadpour A. 2010. Studies on adsorption of mercury from aqueous solution on activated carbons prepared from walnut shell. Journal of Hazardous Materials 174:251-256. Zamrudy W. 2008. Pembuatan karbon aktif
dari ampas biji jarak pagar (Jatropha curcas Linn). Jurnal Teknologi Separasi 2:1978-1989.
Zeng H, Jin F, Guo J. 2004. Removal of elemental mercury from coal combustion flue gas by chloride-impregnated activated carbon. Fuel 83:143-146.
11
12
Lampiran 1 Diagram alir proses aktivasi karbon aktif
Persiapan sampel
(Karbon digerus dan diayak dengan ukuran 70 mesh)
Aktivasi sampel karbon dengan perendaman aktivator ZnCl
2konsentrasi 3%, 5%, dan 7% (w/v) setelah pemanasan pada
masing- masing perlakuan suhu 650 °C, 700 °C, dan 800°C
Setelah diperoleh suhu optimum, aktivasi lanjutan dilakukan
dengan perlakuan yang berbeda
Aktivasi sampel karbon
dengan perendaman aktivator
ZnCl
2konsentrasi 3%, 5%,
dan 7% (w/v) sebelum
pemanasan pada suhu 700 °C
Pengeringan dalam oven selama 8 jam pada suhu 100 °C
Bilangan iodin
SEM
BET
Aktivasi sampel karbon
dengan perendaman aktivator
ZnCl
2konsentrasi 3%, 5%, dan
7% (w/v) sebelum dan setelah
pemanasan pada suhu 700 °C
13
Lampiran 2 Pembuatan pelarut dan larutan standar
Pembuatan larutan zink klorida 3%
ZnCl
2ditimbang sebanyak 15 gram, kemudian dilarutkan ke dalam labu ukur
500 mL dengan akuades sampai tanda tera dan dihomogenkan.
Pembuatan larutan asam klorida 0.5 N
Sebanyak 41.45 mL larutan HCl 37% dimasukkan ke dalam labu ukur 1000
mL dan diencerkan dengan akuades sampai tanda tera, lalu dihomogenkan.
Pembuatan larutan iodin 0.0471 N
I
2ditimbang sebanyak 5.9 gram dilarutkan dengan akuades dan ditambahkan
KI sebanyak 57.0 gram sedikit demi sedikit sampai larut, kemudian masukkan
ke dalam labu ukur 1000 mL dilarutkan dengan akuades sampai tanda tera
lalu dihomogenkan.
Pembuatan larutan natrium tiosulfat 0.1 N
Na
2S
2O
3•5H
2O ditimbang 25 gram kemudian dimasukkan kedalam labu ukur
1000 mL lalu ditambahkan 0.015 gram Na
2CO
3, kemudian dilarutkan dengan
akuades sampai tanda tera.
Standardisasi natrium tiosulfat
K
2Cr
2O
7ditimbang sebanyak 0.4900 gram, lalu dimasukan ke dalam labu
takar 100 mL. Sebanyak 25 mL larutan K
2Cr
2O
7dimasukkan ke dalam
erlenmeyer kering. Selanjutnya ditambahkan 15 mL HCl pekat dan 10 mL KI
20 %. Titrasi dengan larutan Na
2S
2O
3hingga mendekati titik akhir (hingga
berwarna kuning muda) dan ditambahkan indikator kanji. Kemudian dititrasi
kembali hingga terjadi perubahan warna dari biru tua menjadi hijau muda.
Standardisasi iodium
Sebanyak 25 mL larutan I
2dititrasi dengan larutan Na
2S
2O
3yang telah
14
Lampiran 3 Tabel data analisis penetapan bilangan iodin dan daya jerap karbon
aktif
Data analisis bilangan iodin dan daya jerap karbon aktif dengan perendaman
ZnCl
2setelah pemanasan
Suhu
Konsentrasi ZnCl2 (b/v)
Bobot Sampel
Volume Blanko
Volume Titran
Bilangan Iodin
Daya Jerap
Rata-Rata SD
(°C) (%) (gram) (mL) (mL) (mg/g) (%) (%)
650 °C
3% 0.1011 22.00 20.65 164.06 17.08 16.89 0.2687 22.00 20.68 155.70 16.70
5% 0.1011 22.00 20.60 177.98 17.71 18.02 0.4525 22.00 20.55 191.90 18.35
7% 0.1009 22.00 20.35 248.07 20.92 20.73 0.2687 22.00 20.38 239.70 20.54
700 °C
3% 0.1007 22.00 20.00 346.40 25.41 25.41 0.0000 22.00 20.00 346.40 25.41
5% 0.1009 22.00 19.80 401.51 27.89 28.20 0.4454 22.00 19.75 415.45 28.52
7% 0.1006 22.00 18.70 710.48 41.96 41.96 0.0000 22.00 18.70 710.48 41.96
800 °C
3% 0.1009 22.00 20.15 303.87 23.45 23.45 0.0000 22.00 20.15 303.87 23.45
5% 0.1009 22.00 20.25 275.97 22.19 22.51 0.4454 22.00 20.20 289.92 22.82
7% 0.1008 22.00 20.40 234.36 20.30 20.62 0.4500 22.00 20.35 248.32 20.93
Data analisis bilangan iodin dan daya jerap karbon aktif dengan perendaman
ZnCl
2sebelum pemanasan pada suhu 700 °C
Konsentrasi ZnCl2
(b/v) Sampel Bobot Volume Blanko Volume Titran Bilangan Iodin Daya Jerap Rata-Rata
(%) (gram) (mL) (mL) (mg/g) (%) (%)
3% 0.1009 21.25 19.35 356.51 24.23 24.23
21.25 19.35 356.51 24.23
5% 0.1011 21.25 19.10 425.83 27.36 27.05
21.25 19.15 411.82 26.73
7% 0.1008 21.25 18.60 567.55 33.83 34.15
15
Lanjutan Lampiran 3
Data analisis bilangan iodin dan daya jerap karbon aktif dengan perendaman
ZnCl
2sebelum dan setelah pemanasan pada suhu 700 °C
Konsentrasi ZnCl2
(b/v) Sampel Bobot Volume Blanko Volume Titran Bilangan Iodin Daya Jerap Rata-Rata
(%) (gram) (mL) (mL) (mg/g) (%) (%)
3% 0.1008 21.25 19.65 272.59 20.42 20.42
21.25 19.65 272.59 20.42
5% 0.1005 21.25 18.55 583.33 34.57 34.25
21.25 18.60 569.24 33.93
7% 0.1007 21.25 18.40 624.35 36.42 36.10
16
Lampiran 4 Perhitungan standardisasi larutan dalam penetapan bilangan iodin
karbon aktif perendaman ZnCl
2setelah pemanasan pada suhu 700
°C
Standardisasi natrium tiosulfat
Volume titrasi 1 = 24.80 mL
Volume titrasi 2 = 24.80 mL
Konsentrasi Na
2S
2O
7=
=
= 0.4329 mgek/mL
= 0.1008 mgek/mL
B = konsentrasi Na
2S
2O
7× 126.93
= 0.1008 mgek/mL × 126.93
= 12.7945
Standardisasi larutan iodium
Volume titrasi 1 = 11.70 mL
Volume titrasi 2 = 11.68 mL
Konsentrasi iodium 1
=
Konsentrasi iodium
=
= 0.0472 mgek/mL
Konsentrasi iodium 2
=
= 0.0471 mgek/mL
Konsentrasi iodium rata-rata =
= 0.0471 mgek/mL
A = konsentrasi iodium x 12693
17
Lanjutan Lampiran 4 Perhitungan standardisasi larutan dalam penetapan bilangan
iodin karbon aktif perendaman ZnCl
2sebelum pemanasan
pada suhu 700 °C
Standardisasi natrium tiosulfat
Volume titrasi 1 = 24.65 mL
Volume titrasi 2 = 24.65 mL
Konsentrasi Na
2S
2O
7=
=
= 0.4057 mgek/mL
= 0.1014 mgek/mL
B = konsentrasi Na
2S
2O
7× 126.93
= 0.1014 mgek/mL ×126.93
= 12.8707
Standardisasi larutan iodium
Volume titrasi 1 = 11.35 mL
Volume titrasi 2 = 11.35 mL
Konsentrasi iodium
=
Konsentrasi iodium
=
= 0.0460 mgek/mL
A = konsentrasi iodium ×12693
18
Lampiran 5 Perhitungan bilangan iodin dan daya jerap karbon aktif
Contoh perhitungan bilangan iodin
Sampel 70 mesh dengan suhu pemanasan 700
0C pada konsentrasi ZnCl
27%.
Bobot sampel = 0.1006 gram
Volume titran = 18.70 mL
A
= 597.8403
B
= 12.7945
C
=
=
= 0.0377 mgrek/mL
tidak ada faktor koreksi
=
=
= 710.4828
Bilangan iodin
= D
Bilangan iodin = 710.4828 mg/g
Contoh perhitungan kemampuan daya jerap iodium
Sampel 70 mesh dengan suhu pemanasan 700
0C pada konsentrasi ZnCl
27%.
Bobot sampel = 100.6 miligram
Volume titran = 18.70 mL
Volume blanko = 22.00 mL
Konsentrasi natrium tiosulfat = 0.1008 mgrek/mL
Daya jerap =
x 100 %
Daya jerap =
x 100 %
19
Lampiran 6 Data SEM dan EDXA karbon aktif dengan perendaman ZnCl
2setelah
pemanasan pada suhu optimum 700
0C
Karbon aktif dengan konsentrasi ZnCl
23%
004 004
50 µm50 µm50 µm50 µm50 µm
Title : IMG1 --- Instrument : 6390(LA) Volt : 20.00 kV Mag : x 850 Date : 2011/09/20 Pixel : 512 x 384
0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00 9.00 10.00
keV edx_3%_2
0 100 200 300 400 500 600 700 800 900 1000
Coun
ts
C
O Al
Si
Cl
Cl K K
Zn Zn
Zn Zn
Acquisition Parameter Instrument : 6390(LA) Acc. Voltage : 20.0 kV Probe Current: 1.00000 nA PHA mode : T3
Real Time : 32.02 sec Live Time : 30.00 sec Dead Time : 6 % Counting Rate: 1294 cps Energy Range : 0 - 20 keV
ZAF Method Standardless Quantitative Analysis(Oxide) Fitting Coefficient : 0.6440
Total Oxide : 24.0
20
Lanjutan Lampiran 6
Karbon aktif dengan konsentrasi ZnCl
25%
003
003
50 µm50 µm50 µm50 µm50 µm
Title : IMG1
--- Instrument : 6390(LA) Volt : 20.00 kV Mag : x 650 Date : 2011/09/20 Pixel : 512 x 384
0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00 9.00 10.00
keV edx_5%_2
0 150 300 450 600 750 900 1050 1200 1350 1500
Coun
ts
C
Al Si
Cl Cl
Zn Zn
Zn Zn
Acquisition Parameter Instrument : 6390(LA) Acc. Voltage : 20.0 kV Probe Current: 1.00000 nA PHA mode : T3
Real Time : 32.05 sec Live Time : 30.00 sec Dead Time : 6 % Counting Rate: 1357 cps Energy Range : 0 - 20 keV
ZAF Method Standardless Quantitative Analysis(Oxide) Fitting Coefficient : 0.7057
Total Oxide : 24.0
21
Lanjutan Lampiran 6
Karbon aktif dengan konsentrasi ZnCl
27%
010
010
25 µm25 µm 25 µm 25 µm 25 µm
Title : IMG1
--- Instrument : 6390(LA) Volt : 20.00 kV Mag : x 1,200 Date : 2011/09/20 Pixel : 512 x 384
0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00 9.00 10.00
keV edx_7%_4
0 15 30 45 60 75 90 105 120 135 150 165
Coun
ts
C
Si Cl
Cl Zn
Zn Zn
Zn
Acquisition Parameter Instrument : 6390(LA) Acc. Voltage : 20.0 kV Probe Current: 1.00000 nA PHA mode : T3
Real Time : 30.38 sec Live Time : 30.00 sec Dead Time : 1 % Counting Rate: 257 cps Energy Range : 0 - 20 keV
ZAF Method Standardless Quantitative Analysis(Oxide) Fitting Coefficient : 0.7986
Total Oxide : 24.0
22
Lampiran 7 Data hasil BET karbon aktif perendaman ZnCl
2konsentrasi 7%
23
Lanjutan Lampiran 7 Data hasil BET karbon aktif perendaman ZnCl
2konsentrasi