AGUS WAHYUDI
FTAR
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Adaptasi Bibit Eucalyptus pellita
F. Muell dari Beberapa Asal Sumber Benih Terhadap Cekaman Kekeringan di Persemaian adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Desember 2009
AGUS WAHYUDI. Adaptation of Eucalyptus pellita F. Muell seedling from several seed sources for condition of drought stress in nursery. Under direction of Sri Wilarso Budi R and Omo Rusdiana
The low rate of success in rehabilitation of critical land is the results of various aspects, which among other things is the limited availability of superior planting stocks which are adaptive and productive in such area. Drought stress is one of the limiting factor for the survival and establishment of planting stocks in the field. This research was conducted for (1) obtaining information concerning
groups of E. pellita seed sources which are resistant to drought, (2) learning the
adaptation mechanism of E. pellita seedlings from 10 groups of seed sources for
drought stress condition, (3) learning the role of arbucular mycorrhizae in adaptation mechanism of the plant. Drought stress caused reduction in growth of
height, diameter and total biomass of E. pellita seedlings for all groups of seed
sources which were either inoculated or not inoculated by mycorrhizae. Arbuscular mycorrhizae played some role in increasing plant growth at all condition of drought stresss and also decreasing growth reduction due to drought
stress. The use of arbuscular mycorrhizae in E. pellita seedlings in general,
increased resistance to drought. The highest increase occurred in KBS site I and KBK Perawang. Based on growth parameters and adaptation mechanism, it could
be suggested that groups of E. pellita seed source group which were resistant to
drought condition, were those of KBS Site II, KBK Perawang and APB Bupul Muting.
Keywords : Eucalyptus pellita, survival, drought stress, seed orchard, arbuscular
RINGKASAN
AGUS WAHYUDI. Adaptasi Bibit Eucalyptus pellita F. Muell dari Beberapa
Asal Sumber Benih Terhadap Cekaman Kekeringan di Persemaian. Dibimbing oleh Sri Wilarso Budi R dan Omo Rusdiana.
Salah satu faktor pembatas rendahnya keberhasilan di dalam rehabilitasi lahan kritis kering adalah cekaman kekeringan. Rendahnya keberhasilan tersebut, diperparah lagi dengan adanya pemanasan global yang mengakibatkan tidak
menentunya batas antara musim penghujan dan musim kemarau. E. pellita
merupakan salah satu jenis cepat tumbuh yang multi manfaat dan cocok digunakan sebagai salah satu jenis pilihan dalam rehabilitasi lahan kritis. Sumber benih yang unggul dan pemanfaatan mikoriza merupakan salah satu alternatif untuk meningkatkan keberhasilan rehabilitasi lahan tersebut. Penelitian ini
bertujuan untuk mendapatkan informasi asal sumber benih E. pellita yang adaptif
terhadap cekaman kekeringan, mengkaji mekanisme adaptasi bibit tanaman E.
pellita dari 10 kelompok sumber benih unggul yang telah dibangun, dan mengetahui peranan mikoriza arbuskula dalam mengatasi cekaman kekeringan.
Penelitian dilaksanakan di rumah kaca Fakultas Kehutanan IPB, Bogor. Percobaan menggunakan rancangan faktorial tiga faktor dalam lingkunga n acak lengkap. Faktor pertama asal sumber benih sebanyak 10 kelompok sumber benih, faktor kedua inokulasi mikoriza arbuskula (tanpa mycofer dan dengan mycofer) dan faktor ketiga taraf cekaman kekeringan (100%, 75%, 50% dan 25% air tersedia).
Persentase derajat infeksi akar oleh mikoriza arbuskula pada bibit tanaman E. pellita tidak menunjukkan perbedaan yang nyata antar kelompok sumber benih. Besarnya derajat infeksi akar mengalami penurunan seiring dengan meningkatnya taraf cekaman kekeringan. Hal ini kemungkinan disebabkan pendeknya periode cekaman dan semakin menurunnya suplai karbon hasil fotosintat tanaman kepada mikoriza arbuskula.
Cekaman kekeringan memberikan pengaruh penurunan pertumbuhan bibit
tanaman E. pellita dari 10 kelompok sumber benih ya ng bersimbiosis mikoriza
maupun tanpa mikoriza. Namun demikian, pemberian mikoriza arbuskula membantu tanaman meningkatkan pertumbuhan pada semua tingkatan taraf cekaman kekeringan dibandingkan bibit yang tidak bermikoriza. Mikoriza
arbuskula mampu mengurangi laju penurunan pertumbuhan bibit E. pellita akibat
meningkatnya cekaman kekeringan sampai pada taraf cekaman 75%.
Rata-rata pertumbuhan bibit E. pellita yang tidak bersimbiosis dengan
mikoriza menunjukkan respon berbeda-beda antar kelompok sumber benih. Pada kondisi kapasitas lapang, pertumbuhan bibit yang paling baik berasal dari KBS group D, KBS site II dan KBK Perawang. Sedangkan kelompok sumber benih lainnya sama dalam satu kelompok pertumbuhannya. Cekaman kekeringan
mengakibatkan penurunan pertumbuhan bibit tanaman E. pellita sebesar 60% –
75%. Penurunan pertumbuhan pada sumber benih KBS site II, KBK Perawang dan APB Bupul Muting lebih kecil dibandingkan kelompok sumber benih lainnya.
Hal ini menunjukkan bahwa bibit tanaman E. pellita dari ketiga sumber benih
kondisi kapasitas lapang dan taraf cekaman 75% adalah bibit tanaman yang berasal dari sumber benih KBS group B, KBS group D, KBS site I dan KBK Perawang. Semakin meningkatnya cekaman kekeringan ke taraf cekaman 50% dan 25%, hanya bibit dari KBS site I, KBK Perawang dan APB Bupul-Muting yang masih lebih tinggi dibandingkan sumber benih lainnya.
Mekanisme adaptasi bibit E. pellita terhadap cekaman kekeringan melalui
mekanisme toleransi yaitu pengaturan osmoregulasi dengan peningkatan kadar prolina daun. Kadar prolina daun meningkat seiring dengan meningkatnya taraf cekaman kekeringan. Peningkatan kadar prolina daun akibat meningkatnya taraf
cekaman kekeringan pada bibit tanaman E. pellita bermikoriza lebih rendah
dibandingkan bibit tidak bermikoriza. Hal ini menunjukkan bahwa mikoriza
arbuskula membatu bibit tanamaan E. pellita dalam menghadapi cekaman
kekeringan dengan meningkatkan osmotic adjustment dan juga meningkatkan penyerapan air tanah dibandingkan bibit yang tidak bermikoriza.
Selain me lalui mekanisme toleransi, juga melalui mekanisme penghindaran dengan menjaga status air jaringan. Mekanisme yang muncul dengan meningkatkan penyerapan air tanah oleh akar tanaman dan mengurangi kehilangan air oleh transpirasi. Peningkatan penyerapan air tanah oleh tanaman dengan cara menurunkan nisbah tajuk akar tanaman seiring dengan meningkatnya cekaman kekeringan. Hal ini menunjukkan perkembangan akar tanaman lebih
besar dari perkembangan tajuknya. Selain peningkatan akar tanaman, bibit E.
pellita juga melakukan pengurangan laju transpirasi dengan meningkatkan ketebalan daun.
Kata kunci : Eucalyptus pellita, rehabilitasi, cekaman kekeringan, mikoriza
@ Hak Cipta milik IPB, tahun 2009 Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah
b. Pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
AGUS WAHYUDI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Silvikultur Tropika
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
Nama : Agus Wahyudi
NIM : E451070091
Disetujui :
Komisi Pembimbing
Dr. Ir. Sri Wilarso Budi R, M.S Dr. Ir. Omo Rusdiana, M.Sc
Ketua Anggota
Diketahui :
Ketua Mayor Dekan Sekolah Pascasarjana
Silvikultur Tropika
Prof. Dr. Ir. IGK Tapa Darma, M.S Prof. Dr. Ir. Khairil A. Notodiputro, M.S
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam
penelitian yang dilaksanakan sejak bulan Januari 2009 ini adalah tentang cekaman
kekeringan, dengan judul Adaptasi Bibit Eucalyptus pellita F. Muell dari
Beberapa Asal Sumber Benih Terhadap Cekaman Kekeringan di Persemaian.
Terima kasih penulis ucapkan kepada Bapak Dr. Ir. Sri Wilarso Budi R,
M.S dan Dr. Ir. Omo Rusdiana, M.Sc selaku komisi pembimbing, serta Bapak Dr.
Ir. Prijanto Pamoengkas, M.Sc.F.Trop selaku penguji luar komisi yang telah
memberikan bimbingan dan saran. Di samping itu, penghargaan penulis
sampaikan kepada Bapak Dr. Ir. Arif Nirsatmanto, M. Agr dari Balai Besar
Penelitian Bioteknologi dan Pemuliaan Tanaman Hutan, Yogyakarta yang telah
membantu menyediakan benih E. pellita, serta berbagai pihak yang membantu
dalam penyelesaian karya ilmiah ini. Ungkapan terima kasih juga disampaikan
kepada istri dan anak-anakku serta seluruh keluarga besar, atas segala doa dan
kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2009
Penulis dilahirkan di Sragen, Jawa Tengah pada tanggal 11 Agustus 1977
dari pasangan Sriyanto (alm) dan Wartini. Penulis merupakan putra pertama dari
dua bersaudara.
Pendidikan sarjana ditempuh di Program Studi Budidaya Hutan, Fakultas
Kehutanan UGM, lulus pada tahun 2001. Pada tahun 2007, penulis diterima di
Mayor Silvikultur Tropika pada Program Pascasarjana IPB. Beasiswa pendidikan
pascasarjana diperoleh dari Departemen Kehutanan Republik Indonesia.
Penulis bekerja sebagai peneliti di Balai Penelitian Hutan Penghasil Serat
Kuok-Riau sejak tahun 2004. Bidang penelitian yang menjadi tanggung jawab
DAFTAR ISI
Halaman
DAFTAR TABEL ……… x
DAFTAR GAMBAR ……… xi
DAFTAR LAMPIRAN ... xii
PENDAHULUAN Latar Belakang ……… 1
Tujuan Penelitian ……… 3
Hipotesis ... 3
Manfaat Penelitian ……….. 4
TINJAUAN PUSTAKA Cekaman Kekeringan Tanaman ... 5
Eucalyptus pellita ………..………. 8
Fungi Mikoriza Arbuskula ……….. 10
METODE PENELITIAN Waktu dan Tempat ………. 12
Bahan dan Alat ……… 12
Metodologi ……….. 13
Pelaksanaan Penelitian ... 14
Analisa Data ……… 18
HASIL DAN PEMBAHASAN Derajat infeksi akar bibit E. pellita ...…… 19
Respon pertumbuhan bibit E. pellita terhadap cekaman kekeringan…... 22
Mekanisme adaptasi bibit E. pellita terhadap cekaman kekeringan ... 37
SIMPULAN DAN SARAN Simpulan ………. 47
Saran ……….. 47
DAFTAR PUSTAKA ………. 48
Halaman
1. Rata-rata pertumbuhan Eucalyptus pellita di beberapa lokasi HTI di
Indonesia ... 8
2. Data informasi asal sumber benih Eucalyptus pellita ... 12
3. Kondisi tempat tumbuh asal provenan Eucalyptus pellita ... 13
4. Respon derajat infeksi akar bibit E. pellita dari 10 sumber benih
terhadap inokulasi mikoriza arbuskula dan cekaman kekeringan ... 21
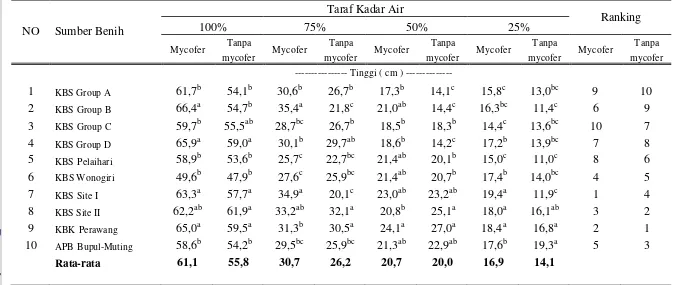
5. Respon pertumbuhan tinggi bibit E. pellita dari 10 sumber benih
terhadap mikoriza arbuskula dan cekaman kekeringa n ... 26
6. Persentase peningkatan pertumbuhan tinggi bibit E. pellita dengan
adanya pemberian mikoriza arbuskula ... 27
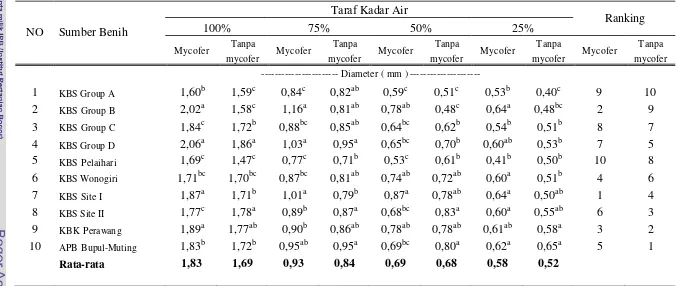
7. Respon pertumbuhan diameter bibit E. pellita dari 10 sumber benih
terhadap mikoriza arbuskula dan cekaman kekeringan ... 29
8. Persentase peningkatan pertumbuhan diameter bibit E. pellita dengan
adanya pemberian mikoriza arbuskula ... 31
9. Respon pertumbuhan biomass total bibit E. pellita dari 10 sumber
benih terhadap mikoriza arbuskula dan cekaman kekeringan ... 34
10. Persentase peningkatan pertumbuhan biomass total bibit E. pellita
dengan adanya pemberian mikoriza arbuskula ... 35
11. Respon prolina daun dan kadar air relatif daun bibit E. pellita dari 10
sumber benih terhadap inokulasi mikoriza arbuskula dan cekaman kekeringan ... 39
12. Respon nisbah tajuk akar dan berat daun spesifik bibit E. pellita dari
DAFTAR GAMBAR
Halaman
1. Kisaran kadar air tanah tersedia pada sepuluh tekstur tanah ... 6
2. Hubungan kisaran kadar air tersedia dengan bahan organik ... 6
3. Peta sebaran alami Eucalyptus pellita ... 8
4. Derajat infeksi akar bibit E. pellita dari 10 sumber benih yang diberi
mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 20
5. Akar bibit tanaman E. pellita yang terinfeksi mikoriza arbuskula ... 22
6. Tanggap morfologi bibit E. pellita umur 5 bulan dari 10 sumber benih
terhadap perlakuan mikoriza dan cekaman kekeringan ... 23
7. Pertumbuhan tinggi bibit E. pellita dari 10 suber benih yang diberi
mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 25
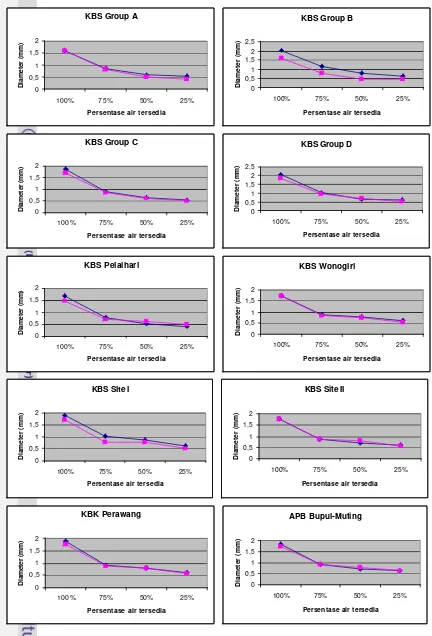
8. Pertumbuhan diameter bibit E. pellita dari 10 suber benih yang diberi
mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 30
9. Pertumbuhan biomass total bibit E. pellita dari 10 suber benih yang
diberi mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 33
10. Kadar prolina daun bibit E. pellita dari 10 suber benih yang diberi
mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 40
11. Kadar air relatif daun bibit E. pellita dari 10 suber benih yang diberi
mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 41
12. Berat daun spesifik bibit E. pellita dari 10 suber benih yang diberi
mycofer dan tanpa mycofer pada beberapa tingkat cekaman kekeringan ... 45
13. Nisbah tajuk akar bibit E. pellita dari 10 suber benih yang diberi
Halaman
1. Tabel hasil analisis anova pada variable pertumbuhan tinggi dan
diameter ……… 53
2. Tabel hasil analisis anova pada variable biomasa total dan nisbah
tajuk akar ………..……… 54
3. Tabel hasil analisis anova pada variable kadar air relatif daun dan
berat daun spesifik ……… 55
4. Tabel hasil analisis anova pada variable kadar prolina daun dan
derajat infeksi akar ………..………. 56
5. Hasil analisis sifat fisik dan kimia media tanam ………..……..…….. 57
6. Hasil perhitungan berat tanah yang harus dipertahankan pada
PENDAHULUAN
Latar Belakang
Lahan kritis atau lahan yang terdegradasi di Indonesia dewasa ini luasnya
telah mencapai 77.8 juta ha, terdiri dari 50 juta ha lahan kritis dalam kawasan
hutan, 27.8 juta ha lahan kritis di luar kawasan hutan (RLPS 2007). Laju
percepatan pertambahan lahan kritis sebesar 1.08 juta ha per tahun sedangkan
realisasi dari kegiatan rehabilitasi lahan kritis selama ini hanya mencapai 700.000
ha per tahun (RLPS 2007). Berdasarkan kondisi tersebut di atas, ada
kecenderungan pertambahan lahan kritis lebih cepat dibandingkan dengan
realisasi rehabilitasinya. Apabila kondisi di atas berlangsung terus maka akan
menimbulkan pengaruh buruk yang luas meliputi aspek lingkungan atau ekologis
maupun aspek ekonomi karena lahan merupakan penyangga kehidupan.
Menurut Njurumana dan Susila (2006) tingginya kegagalan rehabilitasi
lahan kritis merupakan satu kesatuan yang simultan dari berbagai aspek,
diantaranya adalah terbatasnya ketersediaan bibit unggul dan dukungan teknologi
tepat guna yang sesuai dengan kondisi tapak dan agroklimat. Upaya rehabilitasi
lahan kritis banyak mendapatkan kendala berupa kematian jenis-jenis terpilih pada
tingkat awal pertumbuhan (establishment) di lapangan karena kondisi lingkungan
yang panas dan kering (Farida 2000).
Menurut Surata (2007) rehabilitasi lahan kritis di Indonesia Bagian Timur,
khususnya di Propinsi Nusa Tenggara Timur yang umumnya savana kering
mempunyai tingkat keberhasilan yang rendah yaitu kurang dari 20% karena
tingginya tingkat kematian tanaman pada awal penanaman di lapangan. Kematian
ini karena tanaman mengalami kegagalan beradaptasi akibat masalah kekurangan
air, kualitas bibit yang rendah dan kondisi lahan marginal.
Persoalan cekaman kekeringan dan terbatasnya ketersediaan hara bagi
tanaman merupakan realitas permasalahan yang dihadapi dalam upaya rehabilitasi
lahan kritis. Cekaman kekeringan merupakan istilah untuk menyatakan bahwa
tanaman mengalami kekurangan air akibat keterbatasan air dari lingkungannya
yaitu media tanam. Cekaman kekeringan pada tanaman dapat disebabkan
oleh daun akibat laju evapotransporasi melebihi laju absorpsi air walaupun
keadaan air tanah tersedia cukup.
Respon tanaman yang mengalami cekaman kekeringan meliputi perubahan
pada tingkat seluler dan molekuler seperti perubahan akumulasi senyawa
metabolit osmotik terlarut, perubahan metabolisme karbon dan nitrogen sebagai
respon biokimia, dan perubahan ekspresi gen sebagai respon molekuler (Muller &
Whitsitt 1996). Mekanisme adaptasi tanaman untuk mengatasi cekaman
kekeringan adalah dengan pengaturan osmotik sel. Pada mekanisme ini terjadi
sintesis dan akumulasi senyawa organik yang dapat menurunkan potensial
osmotik sehingga menurunkan potensial air dalam sel tanpa membatasi fungsi
enzim serta menjaga turgor sel.
Oleh karena itu diperlukan suatu usaha untuk mencari jenis-jenis yang
toleran dan prospektif pada areal tersebut. Solusi lain yang dapat ditempuh yaitu
memanfaatkan jasad saprofit bagi tanaman yang mampu membantu peningkatan
serapan air dan hara tanaman diantaranya fungi mikoriza arbuskula (FMA).
Penggunaan mikoriza untuk membantu tanaman dalam proses penyerapan air dan
hara yang menjadi faktor pembatas dalam rehabilitasi lahan kritis. Menurut
George et al. (1992) keberadaan mikoriza memberikan kontribusi peningkatan
serapan air oleh tanaman inang selain peran pokoknya meningkatkan serapan
fosfat. Selain itu mikorisa juga mampu meningkatkan efisiensi penggunaan air
oleh tanaman baik pada kondisi kecuk upan air maupun kondisi tercekam
kekeringan (Al Karaki 1998).
Eucalyptus pellita F. Muell (red mahagony) merupakan salah satu jenis
tanaman yang prospektif untuk digunakan dalam rehabilitasi lahan kritis. Produk
hasil dari jenis kayu ini digunakan sebagai kayu pulp, kayu pertukangan dan
daunnya dapat dimanfa atkan sebagai bahan baku minyak atsiri. Jenis ekaliptus ini
dikenal oleh pasar dunia, mempunyai beberapa kelebihan seperti pertumbuhan
cepat, bentuk batang tunggal dan lurus, kualitas kayu bagus dengan berat jenis
yang tinggi dan mudah diolah. Sifat-sifat unggul lainnya yaitu kemampuan
bertunas dan propagasi yang tinggi, toleran terhadap kondisi lingkungan yang
spesifik seperti salinitas, keasaman, hama dan penyakit, suhu rendah (Leksono
3
Untuk me menuhi akan kebutuhan bibit unggul dari jenis-jenis terpilih,
maka perlu dilakukan pembangunan kebun benih. Pembangunan sumber benih E.
pellita dimaksudkan untuk memenuhi kebutuhan akan bibit dalam skala yang
besar dan berkualitas genetik unggul. Keunggulan genetik tersebut adalah dalam
produktivitas tanaman dan daya adaptasinya pada berbagai stress baik biotik dan
abiotik di lapangan. Kebun benih-kebun benih yang telah terbangun berasal dari
beberapa provenan E. pellita yang mempunyai sifat dan karakter lingkungan yang
berbeda-beda untuk tumbuh dan berkembang secara optimal, sehingga perlu
dilakukan suatu penelitian untuk memperoleh informasi dasar tentang pola
kesesuaian lingkungan tempat tumbuh dengan benih-benih yang dihasilkan dari
beberapa kebun benih yang ada.
Tujuan
Untuk memenuhi harapan di atas, penelitian dirancang dengan tujuan
sebagai berikut:
1. Mendapatkan informasi asal sumber benih E. pellita yang toleran terhadap
cekaman kekeringan sebagai sumber benih dalam rehabilitasi lahan kritis di
lahan kering.
2. Mengkaji mekanisme adaptasi bibit tanaman E. pellita terhadap cekaman
kekeringan.
3. Menjelaskan peranan fungi mikoriza arbuskula dalam mekanisme adaptasi
bibit tanaman E. pellita terhadap cekaman kekeringan.
Hipotesis
Hipotesis yang dapat dikemukakan dalam penelitian ini adalah :
1. Adaptasi tanaman E. pellita terhadap cekaman kekeringan ditandai oleh
perubahan pertumbuhan tanaman.
2. Terdapat perbedaan karakter adaptasi tanaman E. pellita dari beberapa asal
sumber benih terhadap cekaman kekeringan.
3. Fungi mikoriza arbuskula meningkatkan kemampuan adaptasi tanaman E.
pellita terhadap cekaman kekeringan melalui peranannya dalam peningkatan
Manfaat
Manfaat yang diharapkan dari penelitian ini adalah :
1. Pengetahuan mekanisme adaptasi tanaman E. pellita terhadap cekaman
kekeringan dapat digunakan sebagai informasi dasar dalam pemuliaan
tanaman tersebut dan informasi kesesuaian sumber benih E. pellita yang
telah dibangun terhadap rencana lokasi penanaman di lapangan.
2. Peran fungi mikoriza arbuskula dalam meningkatkan serapan air dan hara
bagi tanaman E. pellita akan bermanfaat untuk meningkatkan tingkat
TINJAUAN PUSTAKA
Cekaman Kekeringan Tanaman
Cekaman kekeringan merupakan suatu istilah untuk menyatakan tanaman
mengalami kekurangan air akibat keterbatasan air dari lingkungannya yaitu media
tanam. Air merupakan komponen utama tanaman, yaitu membentuk 80 – 90%
bobot segar jaringan yang sedang tumbuh aktif. Air sebagai komponen esensial
tanaman memiliki peranan antara lain : (1) sebagai pelarut, didalamnya terdapat
gas- gas, garam- garam dan zat terlarut lainnya yang bergerak keluar masuk sel, (2)
sebagai pereaksi dalam fotosintesis dan pada berbagai proses hidrolisis, (3) air
esensial untuk menjaga turgiditas yaitu pembesaran sel, pembukaan stomata dan
menyangga bentuk daun-daun muda atau struktur lainnya yang berlignin sedikit
(Levitt 1980).
Cekaman kekeringan akan mengakibatkan rendahnya laju penyerapan air
oleh akar tanaman. Ketidakseimbangan antara penyerapan air oleh akar dan
kehilangan air akibat transpirasi membuat tanaman menjadi layu. Cekaman
kekeringan dapat terjadi karena beberapa hal yaitu : (a) tingginya kecepatan
evaporasi yang melebihi persediaan air tanah ke akar yang akan mengakibatkan
penurunan potensial air, (b) adanya senyawa yang bersifat osmotik, seperti pada
tanah garam, yang dapat menurunkan pengambilan air sehingga terjadi penurunan
potensial osmosis dan tidak cukupnya pengambilan air oleh tanaman yang diserap
dari tanah (Borges 2003).
Status air tanaman pada lingkungan yang mengalami kekeringan dapat
dinyatakan secara kualitatif dan kuantitatif. Pengamatan secara kuantitatif dapat
dilakukan yaitu dengan pengukuran potensial air, potensial osmotik dan
kandungan air pada tanaman misalnya kadar air relatif daun (Repellin et al. 1997).
Pendekatan kualitatif dapat dilakukan dengan pengamatan perubahan warna yang
berkaitan dengan turgor, penggulungan daun, kematian ujung daun, keluarnya
eksudat, penutupan stomata secara prematur di pagi hari dan temperatur kanopi
(Wijana 2001).
Air tersedia adalah air yang ditahan tanah pada kondisi kapasitas lapang
ketersediaannya makin rendah. Air yang ditahan di atas koefisien layu merupakan
air tidak tersedia, terdiri dari sebagian air kapiler dan seluruh air hidroskopis.
Kapasitas lapang merupakan kondisi dimana tebal lapisan air dalam pori-pori
tanah mulai menipis, sehingga tegangan antar air – udara meningkat hingga lebih
besar dari gaya gravitasi, air gravitasi habis dan air tersedia bagi tanaman dalam
keadaan optimal. Kondisi ini terjadi pada tegangan permukaan lapisan air sekitar
1/3 atm atau pF 2,54. Kadar air tersedia umumnya bervariasi tergantung kepada :
tekstur tanah, kadar bahan organik tanah, senyawa kimiawi, kedalam solum,
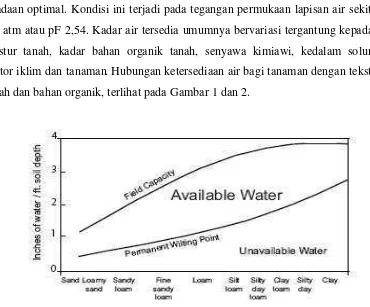
faktor iklim dan tanaman. Hubungan ketersediaan air bagi tanaman dengan tekstur
tanah dan bahan organik, terlihat pada Gambar 1 dan 2.
Gambar 1. Kisaran kadar air tanah tersedia pada sepuluh tekstur tanah
7
Menurut Blum (1996) potensial turgor merupakan faktor utama yang
mempengaruhi pertumbuhan atau perluasan sel. Jika terjadi akumulasi senyawa
osmotik atau perpindahan K+, maka potensial osmotik menurun, sehingga air
berdifusi kedalam sel sehingga potensial turgor meningkat. Beberapa tanaman
dapat mempertahankan tekanan turgor yang tinggi juga pada potensial air yang
agak rendah dengan cara meningkatkan potensial osmotik melalui akumulasi zat
terlarut yang meningkat didalam sel. Proses ini disebut penyesuaian osmotik
(osmotic adjustment) atau regulasi osmotik. Adanya penyesuaian osmotik, berarti
menjaga turgor sel sehingga integritas dan proses fisiologi sitoplasma terjaga.
Penyesuaian osmotik pada tanaman terhadap kondisi kekeringan berperanan
dalam memelihara pemanjangan sel atau perluasan sel melalui pemeliharaan
turgor, memelihara pembukaan stomata, memelihara fotosintesis, sehingga
menjadikan tanaman tetap dapat bertahan hidup pada kondisi kekeringan.
Penyesuaian osmotik terjadi pada tanaman yang mengalami cekaman
kekeringan secara perlahan dan juga pada cekaman medium, namun tidak semua
tanaman dapat mengembangkan penyesuaian osmotik. Penyesuaian osmotik
dipengaruhi oleh laju perkembangan cekaman, tingkat cekaman, kondisi
lingkungan dan perbedaan genotif tanaman. Penyesuaian osmotik melalui
perubahan potensial osmotik dipengaruhi oleh akumulasi senyawa terlarut, ukuran
sel, volume senyawa terlarut, dan ketebalan dinding sel.
Senyawa metabolit yang dihasilkan tanaman sebagai respon terhadap
kondisi kekeringan dan berperan dalam penyesuaian osmotik telah banyak
dilaporkan yang dapat digunakan untuk membedakan tingkat toleransi tanaman
terhadap kekeringan. Nguyen et al. (1997) menyatakan senyawa osmotik terlarut
yang terlibat pada penyesuaian osmotik bervariasi, antara lain gula- gula, asam
organik, asam amino, dan senyawa terlarut kompatibel lainnya. Senyawa osmotik
terlarut yang disintesis dan ditimbun tersebut umumnya segera terjadi ketika
tanaman mengalami kekeringan dengan tingkat kecepatan tergantung pada tingkat
toleransi tanaman terhadap kekeringan tersebut (Kirkham 1990).
Komponen-komponen yang terlibat dalam akumulasi senyawa osmotik tersebut dapat
digunakan sebagai uji sederhana secara kimiawi yang bertujuan untuk mengetahui
Eucalyptus pellita
Eucalyptus pellita F. Muell merupakan pohon yang dapat tumbuh tinggi
mencapai 40 m dan diameter 1 m. Tumbuh alami di Australia yaitu Semenanjung
Cape York, Queensland sampai Cairns dan Townsville bagian utara (12° - 18°
LS) dan bagian selatan Brisbane sampai daerah Batemen, New South Wales (27° -
36° LS). Selain itu juga di Papua Nugini (PNG) dan Papua Tenggara (Hall and
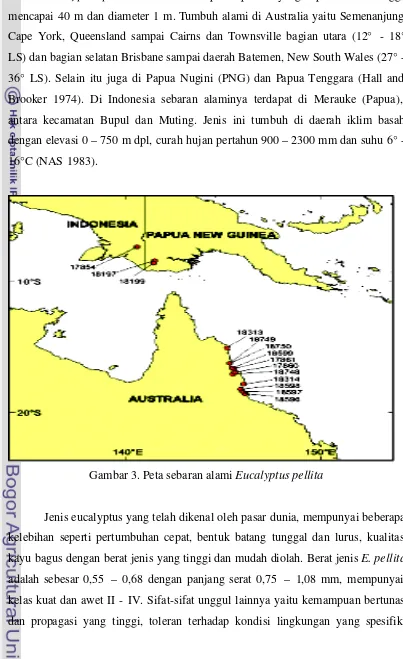
Brooker 1974). Di Indonesia sebaran alaminya terdapat di Merauke (Papua),
antara kecamatan Bupul dan Muting. Jenis ini tumbuh di daerah iklim basah
dengan elevasi 0 – 750 m dpl, curah hujan pertahun 900 – 2300 mm dan suhu 6° -
16°C (NAS 1983).
Gambar 3. Peta sebaran alami Eucalyptus pellita
Jenis eucalyptus yang telah dikenal oleh pasar dunia, mempunyai beberapa
kelebihan seperti pertumbuhan cepat, bentuk batang tunggal dan lurus, kualitas
kayu bagus dengan berat jenis yang tinggi dan mudah diolah. Berat jenis E. pellita
adalah sebesar 0,55 – 0,68 dengan panjang serat 0,75 – 1,08 mm, mempunyai
kelas kuat dan awet II - IV. Sifat-sifat unggul lainnya yaitu kemampuan bertunas
9
(salinitas, keasaman, hama dan penyakit, suhu rendah dll), serta kemudahan dalam
melakukan persilangan untuk program pemuliaan pohon.
E. pellita (red mahagony) merupakan salah satu jenis eucalyptus
mempunyai riap tinggi dan ketahanan terhadap serangan hama dan penyakit lebih
baik dibandingkan dengan jenis-jenis eucalyptus lain, tumbuh baik dan tahan
terhadap pembusuk batang Cryphonectria cubensis (NAS 1983). Di derah tropis,
jenis ini lebih tahan serangan jamur dan serangga pemakan daun dibandingkan
jenis eucalyptus lainnya (Haines and Harwood 1992).
Leksono (2003) menyatakan bahwa E. pellita mempunyai adaptasi yang
tinggi berdasarkan hasil pengamatan pada tanaman di Kalimantan Selatan,
Kalimantan Timur, Sumatera Selatan dan Riau. Sementara jenis E. urophylla, E.
alba dan E. deglupta pada beberapa lokasi HTI menunjukkan pertumbuhan yang
mengecewakan, karena berhenti tumbuh pada umur 2 tahun secara perlahan mati
karena terserang hama dan penyakit. Pertumbuhan dari hasil pengukuran pada
populasi pemuliaan (breeding population) di beberapa lokasi HTI, menunj ukkan
hasil seperti pada Tabel 1. Dari tabel tersebut menunjukkan bahwa E. pellita
mempunyai riap diameter 2.5 – 3.5 cm jika digunakan untuk tujuan pengusahaan
kayu berdaur pendek (4-8 tahun) untuk pulp, kertas atau kayu berdimensi kecil.
Kayu dengan diameter > 20 cm yang dibuat vinir kayu lapis memberikan hasil
yang menggembirakan karena ornamen dan warna kayunya yang bagus (merah
sampai merah tua) meski masih terdapat mata kayu yang cukup banyak karena
umur pohon muda.
Tebel 1. Rata-rata pertumbuhan E. pellita di beberapa lokasi HTI di Indonesia
Lokasi Umur (th) Tinggi (m) Dbh (cm)
Pelaihari, Kalsel 2.0 7.1 7.6
Pulau laut, Kalsel 2.0 7.8 8.0
Pelaihari, Kalsel 2.0
6.0
7.6 20.0
7.7 16.6
Pendopo, Sumsel 2.0
5.0
Fungi Mikoriza Arbuskula
Mikoriza merupakan suatu struktur khas pada sistem perakaran yang
terbentuk karena adanya simbiosis mutualistis antara fungi (myces) dan akar
(rhiza) dari tumbuhan tingkat tinggi (Setiadi 2000). Asosiasi ini saling
menguntungkan bagi kedua pihak, karena fungi memperoleh makanannya dari
tanaman dan sebaliknya tanaman terbantu oleh fungi dalam hal meningkatkan
penyerapan air dan hara.
Mikoriza dapat dikelompokkan ke dalam dua golongan besar berdasarkan
cara infeksinya dan struktur tumbuh pada perakaran tanaman inang, yaitu : (1)
endomikoriza, merupakan struktur mikoriza yang terbentuk sampai ke dalam sel
korteks akar, (2) ektomikoriza, merupakan struktur mikoriza pada lapisan luar
akar yang bentuknya berupa jala hartig. Didalam kelompok endomikoriza terdapat
enam subtipe yaitu mikoriza arbuskula, ektendo, monotropoid, ericoid, dan
orchid.
Fungi mikoriza arbuskula dicirikan oleh adanya pembentukan struktur
haustorial yang bercabang (arbuskula) dalam sel korteks, dan oleh adanya
miselium yang menyebar sampai ke tanah disekitar akar yang disebut sebagai hifa
eksternal atau miselium ekstraradikal. FMA menghasilkan beberapa struktur yaitu
: (a) arbuskula, adalah percabangan dikotomus yang intensif dari hifa intraseluler,
berperan dalam transfer nutrisi antara fungi dan tanaman inang. (b) vesikula,
adalah struktur yang berdinding tipis berisi lipid yang biasanya terbentuk dalam
ruang interseluler, berfungsi sebagai cadangan makanan dan sebagai propagul
reproduktif, (c) sel-sel auksilar yang terbentuk didalam tanah dan dapat
membentuk ”coiled atau knobby” yang fungsinya belum diketahui, (d) spora
aseksual yang berasal dari diferensiasi hifa vegetatif, berupa spora reproduktif
yang dapat dibentuk baik di dalam akar maupun didalam tanah (Brundett et al.
1996).
Asosiasi simbiotik antara fungi mikoriza arbuskula dengan tanaman inang
dimulai dengan berkecambahnya spora yang terdapat dipermukaan akar atau
didaerah rhizoplane atau dengan bertemunya miselium aseptat fungi dengan
sistem perakaran tanaman yang cocok didalam tanah, kemudian melakukan
11
1999). Hifa inter dan intraseluler terbentuk didaerah korteks akar, arbuskula
terbentuk didalam sel, dan vesikel dapat terbentuk baik secara inter maupun
intraseluler. Hifa yang tumbuh didalam akar disebut struktur intraradikal,
sedangkan yang tumbuh diluar akar disebut struktur ekstraradikal. Struktur
ekstraradikal tumbuh menjauhi akar, mengeksplorasi rhizofer, serta melakukan
penye rapan air dan nutrisi (Sukarno 2003).
FMA mempunyai berbagai peran penting dalam peningkatan produktivitas
tanaman melalui peningkatan penyerapan unsur hara, toleransi terhadap kondisi
stress air, toksisitas logam berat dan resistensi terhadap patogen tanah (Killham
1999). Menurut George et al. (1992) bahwa hifa mikoriza dapat menyokong
serapan air oleh tanaman inang. Peningkatan serapan air tersebut diduga
merupakan efek tidak langsung dari mikoriza yakni pengaruhnya terhadap
perbaikan sifat fisik tanah. Keberadaan FMA pada akar tanaman mempengaruhi
kondisi agregasi tanah yang pada gilirannya meningkatkan kemampuan tanah
menahan air, diperoleh bukti bahwa akar tanaman yang terkontaminasi mikoriza
arbuskula mampu meningkatkan penyerapan air menjadi tiga kali lipat (Thomas et
al. 1993). FMA yang menginfeksi sistem perakaran tanaman inang akan
memproduk si jalinan hifa eksternal yang dapat tumbuh secara ekspansif dan
menembus lapisan subsoil sehingga meningkatkan kapasitas akar dalam
penyerapan hara dan air. Volume tanah yang dapat dijelajahi oleh 1 cm akar
bermikoriza dapat mencapai 12-15 cm3 atau 6 -15 kali lebih banyak dibandingkan
akar tanaman yang tak bermikoriza yang hanya sekitar 1-2 cm3 (Cruz et al. 2004).
Menurut Fakuara (1988), bahwa infeksi FMA dipengaruhi oleh berbagai
faktor meliputi : pemupukan, nutrisi tanaman, pestisida, intensitas cahaya, musim
dan kelembaban tanah, pH, kepadatan inokulum dan kerentanan tanaman.
Efektivitas FMA tergantung pada kekesuaian antara faktor jenis FMA, tanaman
dan tanah, serta interaksi ketiga faktor tersebut. Kondisi tanah sangat
mempengaruhi perkembangan FMA, dimana perkembangan asosiasi antara FMA
dengan tanaman inang sangat tertekan pada kondisi ketersediaan N dan P yang
tinggi, demikian juga pH tanah yang dapat mengubah ketersediaan hara maupun
Waktu dan Tempat
Penelitian dilaksanakan di rumah kaca Laboratorium Silvikultur, Fakultas
Kehutanan IPB, sedangkan untuk analisis tanah di Laboratorium Ilmu Tanah IPB.
Analisis peubah pertumbuhan, derajat infeksi akar dan kadar prolina daun
dilakukan di Laboratorium Silvikultur, Fakultas Kehutanan IPB dan Laboratorium
RGCI (Research Group of Crop Improvement), Fakultas Pertanian IPB. Penelitian
dilakukan dari bulan Januari 2009 sampai bulan Juni 2009.
Bahan dan Alat Bahan
Bahan tanam yang digunakan adalah benih E. pellita yang berasal dari 10
sumber benih, koleksi Balai Besar Penelitian Bioteknologi dan Pemulian
Tanaman Hutan, Yogyakarta. Rincian asal sumber benih E. pellita disajikan pada
Tabel 2, dan kondisi tempat tumbuh asal provenan disajikan pada Tabel 3.
Tabel 2. Data informasi asal sumber benih Eucalyptus pellita
No Sumber Benih Provenan Keterangan
1 KBS Grup A, Lipat Kain, Riau South of Kiriwo
5 KBS Pelaihari, Kalsel AUST, IND, PNG Pop tunggal
6 KBS Wonogiri, Jateng AUST, IND, PNG Pop tunggal
7 KBS Site 1, Perawang AUST, IND, PNG Pop tunggal
8 KBS Site 2, Perawang AUST, IND, PNG Pop tunggal
9 KBK, Perawang AUST, IND, PNG Pop tunggal
10 APB Bupul Muting, Merauke – Indonesia
Bupul – Muting ( IND )
Pop tunggal
13
Tabel 3. Kondisi tempat tumbuh asal provenan Eucalyptus pellita
No Provenan Lintang Garis Garis Bujur ( m dpl ) Altitude Curah hujan
( mm/th )
1 Bupul-Muting
(IND)
Media tanam yang digunakan adalah tanah Ultisol yang berasal dari Hutan
Penelitian Haurbentes, Jasinga, Bogor. Sifat-sifat fisika dan kimia media tanah
Ultisol (Lampiran 5). Fungi mikoriza arbuskula yang digunakan adalah Mycofer
berupa campuran jenis Glomus manihotis, Glomus etunicatum, Acaulospora sp
dan Gigaspora sp. Tanaman dipupuk menggunakan pupuk NPK dengan dosis 0,5
g/polybag. Bahan-bahan kimia untuk analisis prolina ( asam sulfosalisilat 3%,
asam ninhidrin, asam glasial, toluen ) dan pengamatan derajat infeksi akar ( KOH
10% w/v, HCl 2%, trypan blue 0.05% w/v, asam laktat, gliserol, dan aquades ).
Alat
Alat yang digunakan adalah polibag ukuran 15 cm x 25 cm, oven,
mikroskop, objek glass, cover glass, spektrofotometer SHIMADZU UV-1201,
penangas air, timbangan 2 kg, timbangan analitik, meteran, kalifer, gelas ukur,
tabung reaksi, mortar, cawan porselin, cutter, kamera dan alat tulis.
Metodologi
Percobaan menggunakan rancangan faktorial tiga faktor dalam lingkungan
acak lengkap. Faktor pertama adalah asal sumber benih E. pellita yang terdiri 10
kelompok sumber benih yaitu : KBS Grup A, Lipat Kain - Riau (A), KBS Grup B,
Lipat Kain - Riau (B), KBS Grup C, Lipat Kain - Riau (C), KBS Grup D, Lipat
1, Perawang (G), KBS Site 2, Perawang (H), KBK, Perawang (I), APB Bupul
Muting, Merauke – Indonesia (J). Faktor kedua adalah cekaman air yang terdiri
atas empat taraf yaitu : 100% kapasitas lapang (K1), 75% kapasitas lapang (K2),
50% kapasitas lapang (K3) dan 25% kapasitas lapang (K4). Faktor ketiga adalah
inokulasi FMA, meliputi : tanpa inokulasi mycofer (M0) dan inokulasi mycofer
(M1). Sehingga diperoleh 80 kombinasi perlakuan dengan 5 ulangan, sehingga
terdapat 400 unit percobaan, masing- masing unit percobaan terdiri 1 tanaman.
Pelaksanaan Penelitian Persemaian benih
Benih E. pellita dikecambahkan dalam bak perkecambahan dengan media
pasir halus yang telah disterilkan dan dipelihara dalam rumah kaca. Pemeliharaan
dilakukan dengan melakukan penyiangan gulma, pembebasan dari hama penyakit
dan penyiraman sampai berumur ± 20 hari, kemudian dipindahkan kedalam
polibag yang berisi tanah Ultisol.
Persiapan media tanam
Tanah Ultisol digunakan sebagai media tanam diambil dari Hutan
Penelitian Haurbentes, Jasinga, Bogor. Tanah disaring dengan menggunakan
saringan berdiameter lubang ± 0,5 cm dan dicampur sampai homogen. Tanah
disterilkan dengan penguapan selama 6 – 7 jam, dikering anginkan selama 1
minggu, kemudian dimasukkan kedalam polibag ukuran 15 cm x 25 cm sebanyak
@ 1 kg/polibag.
Penentuan air tesedia
Air tesedia dalam tanah ditentukan dengan cara mencari selisih antara
kadar air tanah kapasitas lapang dan titik layu permanen. Penetapan kadar air
kapasitas lapang (pF 2,54) menggunakan alat Pressure plate apparatus, dan untuk
penetapan kadar air titik layu permanen (pF 4,20) menggunakan alat Pressure
15
Berdasarkan kadar air tersedia tersebut, penentuan tingkat kadar air dari
masing-masing perlakuan adalah :
Ø 100% air tersedia
Kadar air = (100/100 x kadar air tersedia) + KA titik layu permanen
Ø 75% air tersedia
Kadar air = (75/100 x kadar air tersedia) + KA titik layu permanen
Ø 50% air tersedia
Kadar air = (50/100 x kadar air tersedia) + KA titik layu permanen
Ø 25% air tersedia
Kadar air = (25/100 x kadar air tersedia) + KA titik layu permanen
Penentuan berat tanah dalam polibag
Untuk menentukan jumlah air yang diberikan pada masing- masing
perlakuan, terlebih dahulu dilakukan penetapan berat kering mutlak tanah.
Kemudian dapat ditentukan berat basah tanah masing- masing perlakuan sesuai
dengan persentase kadar air tersedianya, dengan menggunakan rumus :
BB - BK
Kadar air perlakuan ( %) = x 100%
BK
Keterangan : BB = berat basah tanah
BK = berat tanah kering mutlak.
Penyesuaian kadar air tanah untuk masing- masing perlakuan dilakukan setiap 2
hari sekali dan dilakukan koreksi menggunakan pertambahan berat tanaman setiap
2 minggu sekali. Perhitungan berat tanah yang harus dipertahankan pada
masing-masing perlakuan cekaman kekeringan ( Lampiran 6 ).
Penanaman dan Aplikasi FMA
Tanah Ultisol kering udara yang telah disterilkan sebanyak 1 kg tiap
polibag disiapkan sebagai media tanam. Penanaman dilakukan setelah umur
kecambah E. pellita sekitar ± 20 hari, sedangkan pemberian FMA dilakukan
bersamaan dengan pemindahan kecambah kedalam polibag dengan cara
Pemeliharaan tanaman
Pemeliharaan tanaman meliputi penyiraman, pemupukan, penyiangan,
serta pengendalian hama penyakit. Penyiraman dilakukan setiap 2 hari sekali pada
waktu pagi hari dengan cara disiram langsung secara merata pada permukaan pot
sesuai dengan perlakuan taraf kadar air tersedia.
Perlakuan dan pengamatan
Pengamatan dimulai pada saat akan dimulainya perlakuan cekaman
kekeringan yaitu setelah bibit berumur 3 bulan, pengamatan selanjutnya dilakukan
pada waktu bibit berumur 5 bulan.
Peubah atau parameter yang diamati adalah :
1. Tinggi tanaman (cm)
Tinggi tanaman diukur dengan penggaris dari permukaan tanah sampai tunas
apikal tanaman.
2. Diameter tanaman (mm)
Pengukuran diameter tanaman menggunakan kalifer pada posisi 2 cm dari
permukaan tanah.
3. Biomass total ( g )
Biomass total diukur berdasarkan berat kering konstan setelah dilakukan
pengovenan selama 48 jam dengan suhu 80°C.
4. Nisbah tajuk akar
Pengukuran panjang batang dan akar dilakukan dari pangkal batang.
5. Berat daun spesifik (g/cm2)
Berat daun spesifik merupakan nisbah antara berat daun kering konstan
dengan luasnya daun tersebut.
6. Derajat infeksi akar (%).
Pengamatan infeksi akar dilakukan dibawah mikroskop dengan preparat akar
yang telah dipersiapkan dengan metode pewarnaan trypan blue (Brundrett et
al. 1996). Kuantifikasi derajat infeksi FMA dihitung dengan rumus :
Jumlah bidang pandang bermikoriza
Derajat infeksi = x 100%
17
7. Kadar air relatif daun
Pengukuran kadar air relatif dilakukan dengan mengambil bagian daun
tanaman menggunakan pisau dengan ukuran daun 1 cm x 1 cm sebanyak 10
lembar. Bagian daun ini ditimbang berat basahnya, lalu dilakukan perendaman
dalam air selama 24 jam dan kemudian ditimbang berat jenuhnya. Selanjutnya
daun dikering oven pada suhu 80°C selama 48 jam dan diukur bobot
keringnya. Nilai kadar air relatif menggunakan persamaan Prochazkova et al.
(2001) yaitu :
( Wdaun segar – Wdaun kering)
KAR (%) = x 100%
(Wdaun turgit – Wdaun kering)
8. Kadar prolina daun
Prosedur analisis prolina daun dengan metode Bates et al. (1973).
Ø Potongan daun ditimbang sebanyak 0,5 gr, kemudian digerus dan
dihomogenasi dengan 10 mL asam sulfosalisilat 3%.
Ø Bahan tersebut kemudian disentrifugasi pada 9000 rpm selama 15 menit
sehingga diperoleh supernatan.
Ø Supernatan dipipet sebanyak 2 mL, kemudian direaksikan dengan 2 mL
larutan asam ninhidrin dan 2 mL asam asetat glacial dalam tabung
reaksi, kemudian dipanaskan pada penangas air suhu 100oC selama 5
menit.
Ø Setelah 1 jam, kemudian diinkubasi dalam es curah selama 5 menit.
Hasil reaksi selanjutnya diekstraksi dengan 4 mL toluene sehingga
terbentuk kromoform.
Ø Kromoform yang terbentuk diukur absorbsinya dg SHIMADZU
UV-1201 Spectrophotometer pd panjang gelombang 520 nm.
Ø Kandungan prolina dapat dihitung berdasarkan persamaan :
(µg prolina/ml x ml toluen)
Prolina =
(gr contoh)/5
Analisa Data
Data hasil pengukuran dianalisis dengan menggunakan analisis sidik
ragam. Apabila hasil analisis menunjukkan perbedaan ya ng nyata, maka
dilanjutkan dengan uji jarak berganda Duncan (Duncan’s Multiple Range Test –
DMRT). Model linier aditif dalam penelitian ini sebagai berikut :
dimana :
Y ijkl = Nilai pengamatan pada faktor asal sumber benih ke-i, faktor taraf
cekaman air ke-j, inokulasi FMA ke-k dan ulangan ke- l.
µ = Rataan umum
Ai = Pengaruh utama faktor asal sumber benih ke-i
Bj = Pengaruh utama faktor taraf cekaman air ke-j
Mk = Pengaruh utama faktor inokulasi FMA ke-k
(AB)ij = Pengaruh interaksi faktor asal sumber benih ke-i dan faktor taraf
cekaman air ke-j.
(AM)ik = Pengaruh interaksi faktor asal sumber benih ke-i dan faktor
inokulasi FMA ke-k
(BM)jk = Pengaruh interaksi faktor taraf cekaman air ke-j dan faktor inokulasi
FMA ke-k
(ABM)ijk = Pengaruh interaksi faktor asal sumber benih ke-i dan faktor taraf
cekaman air ke-j danfaktor inokulasi FMA ke-k
e
ijk l = Galat percobaan pada faktor asal sumber benih ke-i, faktor tarafcekaman air ke-j, faktor inokulasi FMA ke-k dan ulangan l
( ) ( ) ( ) (
ij ik jk)
ijk ijklk j
i
ijkl
A
B
M
AB
AM
BM
ABM
HASIL DAN PEMBAHASAN
Derajat infeksi akar bibit Eucalyptus pellita
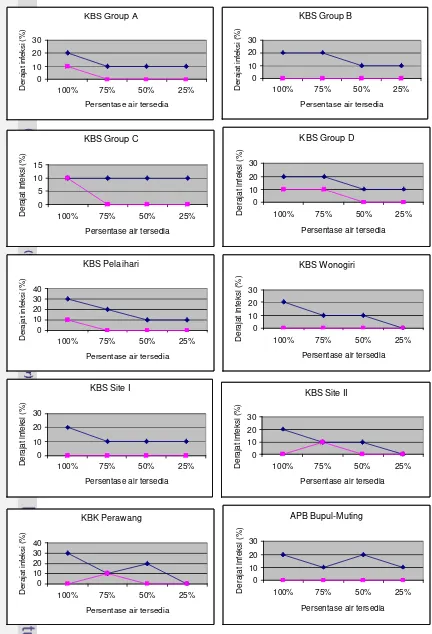
Cekaman kekeringan memberikan dampak penurunan derajat infeksi akar
bibit tanaman E. pellita (Gambar 4), namun pada taraf cekaman kekeringan 75%
dan 50% penurunannya tidak berbeda nyata (Tabel 4). Persentase penurunan
derajat infeksi akar akibat meningkatnya taraf cekaman kekeringan sebesar 38%
(cekaman kekeringan 75% dan 50%) dan 67% (cekaman kekeringan 25%).
Perlakuan tanpa inokulasi mikoriza arbuskula (mycofer) pada media tanam bibit
tanaman E. pellita, ditemukan adanya derajat infeksi akar pada taraf cekaman
kekeringan 100% dan 75%, meskipun infeksi akar tidak terjadi pada semua
kelompok sumber benih. Hal ini kemungkinan disebabkan kurang sterilnya media
tanah dan air yang digunakan dalam penelitian.
Menurut Auge (2000) cekaman kekeringan dapat memberikan pengaruh
peningkatan dan atau penurunan derajat infeksi akar tanaman oleh mikoriza
arbuskula. Derajat infeksi akar suatu tanaman oleh mikoriza dipengaruhi berbagai
faktor meliputi : pemupukan, nutrisi tanaman, pestisida, intensitas cahaya, musim
dan kelembaban tanah, pH, kepadatan inokulum dan kerentanan tanaman (Fakuara
1988). Penurunan derajat infeksi akar seiring meningkatnya cekaman kekeringan
juga terjadi pada tanaman gandum (Al Karaki et al. 1997), tanaman Citrullus
lanatus (Kaya et al. 2003) dan tanaman Citrus tangerine (Wu and Xia 2006).
Penurunan derajat infeksi akar oleh mikoriza arbuskula pada bibit E.
pellita seiring dengan meningkatnya taraf cekaman kekeringan, kemungkinan
dipengaruhi oleh faktor pendeknya periode cekaman kekeringan dan rendahnya
suplai karbon hasil fotosintesis tanaman kepada mikoriza akibat menurunnya
proses fotosintesis. Menurut Bolgiano et al. (1983) singkatnya periode defisit air
dapat menurunkan kolo nisasi pada suatu hubungan asosiasi.
Perbedaan persentase derajat infeksi akar pada bibit E. pellita tidak
menunjukkan perbedaan yang nyata antar kelompok sumber benih pada taraf
cekaman kekeringan 100%, 75% dan 50%. Namun, pada taraf cekaman
kekeringan 25% terdapat bibit yang tidak terinfeksi mikoriza yaitu bibit yang
KBS Group A
Gambar 4 Derajat infeksi akar bibit E. pellita dari 10 sumber benih yang diberi mycofer
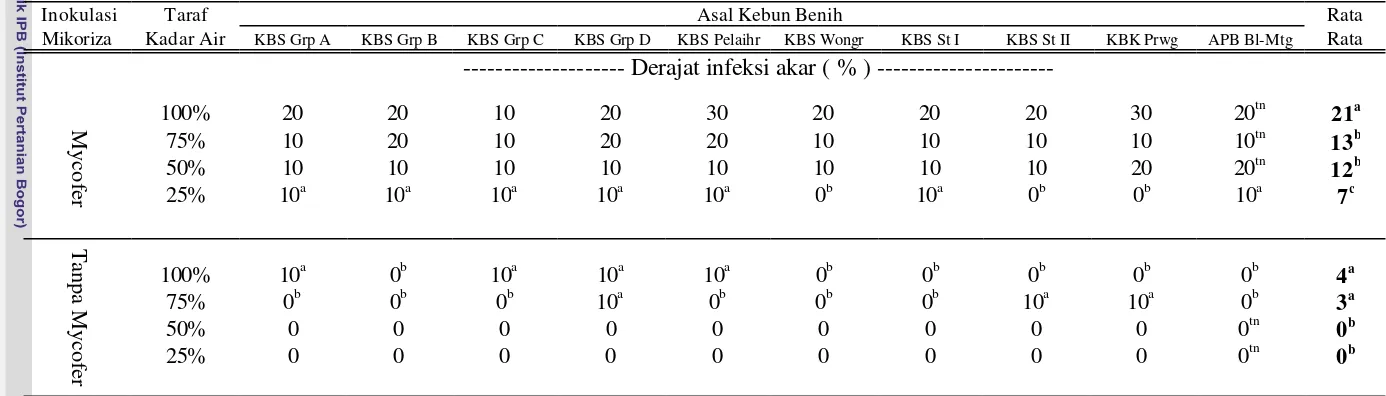
Tabel 4 Respon derajat infeksi akar bibit E. pellita dari 10 sumber benih terhadap inokulasi mikoriza arbuskula dan cekaman kekeringan.
Inokulasi Taraf Asal Kebun Benih Rata
Mikoriza Kadar Air KBS Grp A KBS Grp B KBS Grp C KBS Grp D KBS Pelaihr KBS Wongr KBS St I KBS St II KBK Prwg APB Bl-Mtg Rata
--- Derajat infeksi akar ( % ) ---
Mycofer 100% 20 20 10 20 30 20 20 20 30 20
tn
21a
75% 10 20 10 20 20 10 10 10 10 10tn 13b
50% 10 10 10 10 10 10 10 10 20 20tn 12b
25% 10a 10a 10a 10a 10a 0b 10a 0b 0b 10a 7c
Tanpa Mycofer
100% 10a 0b 10a 10a 10a 0b 0b 0b 0b 0b 4a
75% 0b 0b 0b 10a 0b 0b 0b 10a 10a 0b 3a
50% 0 0 0 0 0 0 0 0 0 0tn 0b
25% 0 0 0 0 0 0 0 0 0 0tn 0b
infeksi akar bibit tanaman E. pellita yang diinokulasi dengan mikoriza arbuskula
(mycofer) tersebut, menurut O’Connor et al. (2001) masuk dalam katagori sedang.
Terdapatnya derajat infeksi akar oleh mikoriza arbuskula pada bibit E.
pellita yang tidak diinokulasi mikoriza pada kelompok sumber benih KBS group
A, KBS group C, KBS group D, KBS site II dan KBK Perawang, kemungkinan
ada bagian propagul dari mikoriza arbuskula yang masuk pada media tanam.
Perbedaan prosentase derajat infeksi akar antar sumber benih E. pellita pada
perlakuan mycofer kemungkinan dipengaruhi oleh perbedaan jenis dan jumlah
eksudat yang dikeluarkan dari masing- masing bibit tanaman. Akar bibit tanaman
E. pellita yang terinfeksi oleh mikoriza arbuskula dapat dilihat pada Gambar 5.
Infeksi yang terjadi dapat berupa adanya hifa dan atau vesikel dalam jaringan
korteks akar bibit tanaman E. pellita tersebut.
Gambar 5 Akar bibit tanaman E. pellita yang terinfeksi mikoriza arbuskula
Respon pertumbuhan bibit E. pellita terhadap cekaman kekeringan
Ketersediaan air merupakan salah satu faktor sangat penting pada fase
pertumbuhan awal bibit dan pemantapan tanaman di lapangan. Pertumbuhan
tanaman pada kondisi cekaman kekeringan adalah signal utama adaptasi suatu
tanaman terhadap cekaman kekeringan. Pertumbuhan tanaman dapat dilihat dari
beberapa parameter, diantaranya : tinggi, diameter dan biomass total tanaman.
Cekaman kekeringan mengakibatkan penurunan pertumbuhan bibit tanaman E.
pellita dari semua kelompok sumber benih, baik yang diinokulasi mikoriza
maupun tidak diinokulasi mikoriza. Tanggap morfologi bibit tanaman E. pellita
umur 5 bulan yang diberi mycofer maupun tanpa mycofer dari beberapa sumber
benih terhadap cekaman kekeringan disajikan pada Gambar 6.
23
Tanggap pertumbuhan tinggi bibit E. pellita terhadap cekaman kekeringan
mengalami penurunan seiring dengan meningkatnya taraf cekaman, pada bibit
yang diinokulasi mikoriza maupun tidak diinokulasi mikoriza (Gambar 7). Bibit
yang diinokulasi mikoriza, pertumbuhan tinggi tanaman pada cekaman kekeringan
50% dan 25% air tersedia menunjukkan perbedaan yang tidak nyata. Pertumbuhan
tinggi bibit yang diinokulasi mikoriza pada umumnya lebih baik dibandingkan
bibit yang tidak diinokulasi mikoriza disemua kondisi cekaman kekeringan,
kecuali taraf cekaman 50% pada beberapa sumber benih (Tabel 5).
Pada kondisi kapasitas lapang, pertumbuhan tinggi bibit E. pellita
menunjukkan tanggap yang berbeda-beda antar kelompok sumber benih. Sumber
benih dari KBS group D, KBS site I, II dan KBK Perawang memiliki
pertumbuhan lebih baik dibandingkan kelompok sumber benih lainnya. Kelompok
sumber benih yang dibangun dari campuran 3 provenan, umumnya lebih baik
pertumbuhannya pada kondisi kapasitas lapang dibandingkan sumber benih dari 1
provenan.
Pemberian mikoriza arbuskula, memberikan peningkatan rata-rata
pertumbuhan tinggi bibit sekitar 9,57% dibanding tanpa mikoriza (Tabel 6).
Peningkatan tetinggi berasal dari KBS group B dan KBS group A masing- masing
sebesar 21,39% dan 14,05%. Rata-rata pertumbuhan tinggi bibit E. pellita setelah
diinokulasi mikoriza, tertinggi berasal dari KBS group B, KBS group D, KBS site
I dan KBK Perawang.
Pertumbuhan tinggi bibit E. pellita pada taraf cekaman kekeringan 75%
mengalami penurunan 50% dibandingkan kondisi kapasitas lapang. Mikoriza
arbuskula membantu tanaman meningkatkan pertumbuhan tinggi di semua
kelompok sumber benih, peningkatan tertinggi berasal dari bibit KBS group B dan
KBS site I masing- masing sebesar 62,39% dan 73,63%. Pertumbuhan tinggi bibit
tanaman E. pellita yang berasal dari KBS group D, KBS site II dan KBK
Perawang menunjukkan lebih baik dibanding kelompok sumber benih lainnya.
Sedangkan pada bibit yang diinokulasi mikoriza KBS group B, KBS site I dan
46
Gambar 7 Pertumbuhan tinggi bibit E. pellita dari 10 sumber benih yang diberi mycofer
Tabel 5 Respon pertumbuhan tinggi bibit E. pellita dari 10 sumber benih terhadap mikoriza arbuskula dan cekaman kekeringan.
NO Sumber Benih
Taraf Kadar Air
Ranking
100% 75% 50% 25%
Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa
mycofer mycofer mycofer mycofer mycofer
--- Tinggi ( cm ) ---
1 KBS Group A 61,7b 54,1b 30,6b 26,7b 17,3b 14,1c 15,8c 13,0bc 9 10
2 KBS Group B 66,4a 54,7b 35,4a 21,8c 21,0ab 14,4c 16,3bc 11,4c 6 9
3 KBS Group C 59,7b 55,5ab 28,7bc 26,7b 18,5b 18,3b 14,4c 13,6bc 10 7
4 KBS Group D 65,9a 59,0a 30,1b 29,7ab 18,6b 14,2c 17,2b 13,9bc 7 8
5 KBS Pelaihari 58,9b 53,6b 25,7c 22,7bc 21,4ab 20,1b 15,0c 11,0c 8 6
6 KBS Wonogiri 49,6b 47,9b 27,6c 25,9bc 21,4ab 20,7b 17,4b 14,0bc 4 5
7 KBS Site I 63,3a 57,7a 34,9a 20,1c 23,0ab 23,2ab 19,4a 11,9c 1 4
8 KBS Site II 62,2ab 61,9a 33,2ab 32,1a 20,8b 25,1a 18,0a 16,1ab 3 2
9 KBK Perawang 65,0a 59,5a 31,3b 30,5a 24,1a 27,0a 18,4a 16,8a 2 1
10 APB Bupul-Muting 58,6b 54,2b 29,5bc 25,9bc 21,3ab 22,9ab 17,6b 19,3a 5 3
Rata-rata 61,1 55,8 30,7 26,2 20,7 20,0 16,9 14,1
27
Cekaman kekeringan 50% menurunkan rata-rata pertumbuhan tinggi
tanaman E. pellita sebesar 65%, baik bibit yang diinokulasi mikoriza maupun
tidak diinokulasi mikoriza. Mikoriza arbuskula tidak dapat mengatasi penurunan
pertumbuhan tinggi akibat meningkatnya cekaman kekeringan. Sekilas mikoriza
membantu tanaman meningkatkan pertumbuhan tinggi dari beberapa kelompok
sumber benih, namun pada sumber benih KBS site I, KBS site II, KBK Perawang
dan APB Bupul-Muting menurunkan pertumbuhan tinggi. Pertumbuhan tinggi
bibit dari sumber benih KBS site II dan KBK Perawang lebih baik dibandingkan
sumber benih lainnya, sedangkan bibit yang diinokulasi mikoriza sumber benih
KBS site I dan KBK Perawang yang paling baik pertumbuhannya.
Cekaman kekeringan 25% secara nyata menurunkan pertumbuhan tinggi
bibit tanaman E. pellita sebesar 70% pada bibit yang bermikoriza maupun tidak
bermikoriza. Namun, rata-rata pertumbuhan bibit bermikoriza lebih tinggi 20%
dibandingkan bibit tidak bermikoriza, kecuali bibit dari APB Bupul Muting.
Pertumbuhan bibit yang berasal dari KBS site II, KBK Perawang dan APB Bupul
Muting memperlihatkan lebih baik dibandingkan lainnya, sedangkan setela h
diberi mikoriza arbuskula bibit dari KBS site I, KBS site II dan KBK Perawang
menunjukkan pertumbuhan lebih baik. Peningkatan pertumbuhan tinggi akibat
pemberian mikoriza arbuskula tertinggi berasal dari sumber benih KBS group B
dan KBS site I masing- masing sebesar 42,98% dan 63,03%.
Tabel 6 Persentase peningkatan pertumbuhan tinggi bibit E. pellita dengan
adanya pemberian mikoriza arbuskula
Sumber Benih Taraf Kadar Air Tersedia
Tanggap pertumbuhan diameter bibit tanaman E. pellita terhadap cekaman
kekeringan menunjukkan penurunan pertumbuhan seiring dengan meningkatnya
taraf cekaman kekeringan yaitu sebesar 50%, 60% dan 70% terhadap kondisi
kapasitas lapang (Tabel 7). Penurunan pertumbuhan ini terjadi pada bibit yang
bermikoriza maupun tidak bermikoriza, namun bila dilihat dari rata-rata
pertumbuhan diameter pada masing- masing taraf cekaman kekeringan, bibit
bermikoriza lebih baik dibandingkan bibit tidak bermikoriza (Gambar 8).
Pertumbuhan diameter pada kapasitas lapang merupakan kondisi optimum
pertumbuhan bibit E. pellita dari 10 kelompok sumber benih. Kelompok sumber
benih KBS group D, KBS site II dan KBK Perawang memiliki pertumbuhan
diameter paling baik dibandingkan kelompok sumber benih yang lainnya. Pada
bibit yang diinokulasi mikoriza pertumbuhan terbaik berasal dari KBS group B,
KBS group D, KBS site I dan KBK Perawang. Peningkatan pertumbuhan
diameter dengan adanya mikoriza arbuskula tertinggi pada KBS group B dan KBS
Pelaihari masing- masing sebesar 27,85% dan 14,97% (Tabel 8).
Pada kondisi cekaman kekeringan 75% kelompok sumber benih yang
pertumbuhannya baik dikondisi kapasitas lapang masih memperlihatkan
pertumbuhan yang baik juga dibandingkan kelompok sumber benih lain.
Kelompok APB Bupul Muting yang pertumbuhannya dibawah KBS group D pada
kondisi kapasitas lapang, memperlihatkan pertumbuhan yang sama baik dikondisi
cekaman kekeringan 75%. Pemberian mikoriza arbuskula meningkatkan
pertumbuhan diameter bibit E. pellita pada semua kelompok sumber benih,
peningkatan tertinggi berasal dari KBS group B dan KBS site I masing- masing
sebesar 43,21% dan 27,85%.
Pertumbuhan diameter bibit E. pellita pada taraf cekaman kekeringan 50%
tidak menunjukkan perbedaan nyata antara bibit yang bermikoriza dengan tidak
bermikoriza. Peningkatan pertumbuhan dengan adanya mikoriza arbuskula
tertinggi berasal dari KBS group B dan KBS group A masing- masing sebesar
62,5% dan 15,69%. Kelompok sumber benih dari KBS group D, KBS Pelaihari,
KBS site II dan APB Bupul-Muting mempunyai pertumbuhan diameter lebih
Tabel 7 Respon pertumbuhan diameter bibit E. pellita dari 10 sumber benih terhadap mikoriza arbuskula dan cekaman kekeringan.
NO Sumber Benih
Taraf Kadar Air
Ranking
100% 75% 50% 25%
Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa
mycofer mycofer mycofer mycofer mycofer
--- Diameter ( mm ) ---
1 KBS Group A 1,60b 1,59c 0,84c 0,82ab 0,59c 0,51c 0,53b 0,40c 9 10
2 KBS Group B 2,02a 1,58c 1,16a 0,81ab 0,78ab 0,48c 0,64a 0,48bc 2 9
3 KBS Group C 1,84c 1,72b 0,88bc 0,85ab 0,64bc 0,62b 0,54b 0,51b 8 7
4 KBS Group D 2,06a 1,86a 1,03a 0,95a 0,65bc 0,70b 0,60ab 0,53b 7 5
5 KBS Pelaihari 1,69c 1,47c 0,77c 0,71b 0,53c 0,61b 0,41b 0,50b 10 8
6 KBS Wonogiri 1,71bc 1,70bc 0,87bc 0,81ab 0,74ab 0,72ab 0,60a 0,51b 4 6
7 KBS Site I 1,87a 1,71b 1,01a 0,79b 0,87a 0,78ab 0,64a 0,50ab 1 4
8 KBS Site II 1,77c 1,78a 0,89b 0,87a 0,68bc 0,83a 0,60a 0,55ab 6 3
9 KBK Perawang 1,89a 1,77ab 0,90b 0,86ab 0,78ab 0,78ab 0,61ab 0,58a 3 2
10 APB Bupul-Muting 1,83b 1,72b 0,95ab 0,95a 0,69bc 0,80a 0,62a 0,65a 5 1
Rata-rata 1,83 1,69 0,93 0,84 0,69 0,68 0,58 0,52
KBS Group A
Gambar 8 Pertumbuhan diameter bibit E. pellita dari 10 sumber benih yang diberi
31
Cekaman kekeringan 25% mengakibatkan penurunan rata-rata
pertumbuhan diameter bibit E. pellita yang diinokulasi mikoriza maupun tidak
sebesar 70% dibandingkan kondisi kapasitas lapang. Mikoriza arbuskula tidak
mampu mengurangi penurunan pertumbuhan diameter bibit E. pellita, namun
secara umum pertumbuhan bibit bermikoriza lebih tinggi dibanding bibit tidak
bermikoriza. Kelompok sumber benih yang pertumbuhan diameternya lebih baik
dibandingkan sumber benih lainnya adalah KBS site II, KBK Perawang dan APB
Bupul Muting. Selanjutnya, untuk bibit yang diinokulasi mikoriza pertumbuhan
terbaik pada taraf cekaman kekeringan 25% adalah KBS group B, KBS site I,
KBK Perawang dan APB Bupul Muting.
Tabel 8 Persentase peningkatan pertumbuhan diameter bibit E. pellita dengan
adanya pemberian mikoriza arbuskula
Sumber Benih Taraf Kadar Air Tersedia
100% 75% 50% 25%
KBS Group A 0,63 2,44 15,69 32,50
KBS Group B 27,85 43,21 62,50 33,33
KBS Group C 6,98 3,53 3,23 5,88
KBS Group D 10,75 8,42 -7,14 13,21
KBS Pelaihari 14,97 8,45 -13,11 -18,00
KBS Wonogiri 0,59 7,41 2,78 17,65
KBS Site I 9,36 27,85 11,54 28,00
KBS Site II -0,56 2,30 -18,07 9,09
KBK Perawang 6,78 4,65 0,00 5,17
APB Bupul-Muting 6,40 0,00 -13,75 -4,62
Tanggap pertumbuhan biomass total tanaman terhadap cekaman
kekeringan pada 10 kelompok sumber benih, baik pada bibit yang bermikoriza
maupun tidak bermikoriza menunjukkan berbeda-beda (Tabel 9). Namun, secara
umum bibit yang bermikoriza mempunyai pertumbuhan biomass total lebih tinggi
dibandingkan bibit yang tidak bermikoriza, pada semua tingkatan cekaman
kekeringan (Gambar 9). Pada bibit yang diinokulasi mikoriza arbuskula, rata-rata
pertumbuhan biomass total pada taraf cekaman kekeringan 50% dan 25% tidak
rata-rata pertumbuhan biomass total pada bibit yang tidak diinokulasi mikoriza
pada taraf cekaman kekeringan 75% dengan 50% dan taraf cekaman kekeringan
50% dengan 25%.
Pertumbuhan biomass total bibit E. pellita pada kondisi kapasitas lapang
(cekaman kekeringan 100%) berbeda-beda setiap asal sumber benih. Bibit yang
berasal dari KBS group D, KBS site II dan KBK Perawang mempunyai
pertumbuhan tertinggi dibandingkan bibit dari kelompok sumber benih lainnya.
Pertumbuhan bibit KBS group B terendah dari semua kelompok sumber benih,
namun tidak berbeda nyata pada kelompok sumber benih dari satu asal provenan
(KBS group A dan C). Bibit E. pellita yang berasal dari KBS group D
pertumbuhannya lebih baik dari APB Bupul Muting meskipun berasal dari
provenan yang sama. Hal ini menunjukkan bahwa kebun benih lebih unggul
genetiknya dibandingkan tegakan benih didalam pertumbuhan biomass total.
Pemberian mikoriza arbuskula secara nyata meningkatkan pertumbuhan
biomass total bibit E. pellita pada semua kelompok sumber benih di kondisi
kapasitas lapang (Tabel 10). Peningkatan pertumbuhan tertinggi berasal dari bibit
KBS group B dan KBS group A, masing- masing sebesar 80,56% dan 39,65%.
Pertumbuhan biomass total setelah diinokulasi mikoriza tidak menunjukkan
perbedaan antar kelompok sumber benih, namun KBS site I dan KBS group D
memiliki nilai tertinggi dibanding lainnya.
Pada taraf cekaman kekeringan 75%, rata-rata pertumbuhan biomass total
mengalami penurunan sebesar 73,89% dibandingkan kondisi kapasitas lapang,
sedangkan bibit yang diinokulasi mikoriza penurunannya 67,72%. Kelompok
sumber benih yang berasal dari provenan campuran memiliki pertumbuhan lebih
tinggi dibandingkan provenan tunggal. Kelompok KBS site II dan KBK Perawang
mempunyai pertumbuha n biomass total lebih baik dibandingkan kelompok
sumber benih lainnya. Pertumbuhan bibit E. pellita setelah diinokulasi mikoriza
pada taraf cekaman kekeringan 75%, secara umum meningkat dibandingkan tanpa
diinokulasi mikoriza. Peningkatan pertumbuhan tertinggi berasal dari KBS group
B sebesar 141,18%, sedangkan bibit dari KBS site II peningkatannya hanya
46
Gambar 9 Pertumbuhan biomass total bibit E. pellita dari 10 sumber benih yang diberi
Tabel 9 Respon pertumbuhan biomass total bibit E. pellita dari 10 sumber benih terhadap mikoriza arbuskula dan cekaman kekeringan.
NO Sumber Benih
Taraf Kadar Air
Ranking
100% 75% 50% 25%
Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa Mycofer Tanpa
mycofer mycofer mycofer mycofer mycofer
--- Biomass total ( g ) ---
1 KBS Group A 3,17tn 2,27c 0,94tn 0,52b 0,45tn 0,34c 0,42tn 0,30c 7 9
2 KBS Group B 3,25 1,80c 1,23 0,51b 0,56 0,38c 0,48 0,31c 4 8
3 KBS Group C 2,54 2,40bc 0,84 0,54b 0,45 0,39c 0,36 0,37b 10 7
4 KBS Group D 3,55 3,46a 1,21 0,65b 0,49 0,47bc 0,47 0,33c 6 6
5 KBS Pelaihari 2,66 2,62b 0,78 0,57b 0,56 0,53b 0,38 0,34bc 5 5
6 KBS Wonogiri 2,37 2,02c 0,93 0,77ab 0,52 0,49bc 0,33 0,23d 9 10
7 KBS Site I 3,55 2,55bc 1,00 0,70ab 0,68 0,55b 0,51 0,35bc 1 4
8 KBS Site II 3,26 3,10a 0,93 0,92a 0,50 0,76a 0,35 0,44b 8 3
9 KBK Perawang 3,46 3,03a 1,03 0,86a 0,66 0,71a 0,52 0,55a 2 2
10 APB Bupul-Muting 2,84 2,63b 0,94 0,61b 0,60 0,74a 0,52 0,55a 3 1
Rata-rata 3,02 2,58 0,98 0,66 0,55 0,54 0,43 0,38
Tabel 11 Respon prolina daun dan kadar air relatif daun bibit E. pellita dari 10 sumber benih terhadap inokulasi mikoriza arbuskula dan cekaman kekeringan.
Inokulasi Taraf Asal Kebun Benih Rata
Mikoriza Kadar Air KBS Grp A KBS Grp B KBS Grp C KBS Grp D KBS Pelaihr KBS Wongr KBS St I KBS St II KBK Prwg APB Bl-Mtg Rata
--- Kadar air re latif daun ( % ) ---
Mycofer 100% 94,35
bcd
88,96d 94,37bcd 91,08cd 95,54abc 96,46ab 96,47ab 97,85a 95,75abc 91,59cd 94,24a
75% 93,06a 86,36b 93,74a 89,85b 86,72b 90,01b 88,45b 88,83b 90,18b 90,92b 89,81ab
50% 91,71a 86,12b 93,51a 87,29b 85,40b 88,34b 86,14b 86,51b 87,87b 82,70b 87,56ab
25% 90,50ab 86,08bc 93,10a 86,71bc 84,70bc 86,68bc 84,75bc 83,94c 86,16bc 81,86c 86,45b
Tanpa Mycofer
100% 93,27ab 87,66c 93,67ab 90,62bc 93,85ab 93,95ab 92,94ab 95,25a 91,03bc 90,30bc 92,25a
75% 90,88bc 84,49c 92,38ab 85,25c 89,64bc 93,16a 89,43bc 92,09ab 86,92c 87,47bc 89,37a
50% 87,09b 82,03c 89,92a 83,55c 83,88c 88,68ab 87,66ab 88,74ab 86,43bc 81,98c 85,99b
25% 86,39a 80,83c 82,69bc 81,96bc 81,98bc 84,70ab 82,73bc 86,29a 81,62c 81,77bc 83,09b
Keterangan : angka yang diikuti satu atau lebih huruf yang sama pada baris yang sama tidak berbeda nyata pada taraf 5% (DMRT)
--- Kadar prolina daun ( mg/g berat basah ) ---
Mycofer 100% 0,80
bc
0,67bc 0,61c 0,62c 0,80bc 1,08a 0,91ab 0,74bc 0,77bc 0,86b 0,79d
75% 1,10ab 0,92bc 0,61c 0,96bc 1,06ab 1,24a 1,23a 1,11ab 1,01ab 1,03ab 1,03c
50% 1,31ab 1,50a 1,30ab 1,02b 1,09b 1,43a 1,31ab 1,34ab 1,34ab 1,59a 1,32b
25% 1,74b 1,66bc 1,68bc 1,22c 1,93ab 2,03ab 1,88b 2,20a 2,02ab 2,22a 1,86a
Tanpa Mycofer
100% 1,05bc 1,36ab 1,34ab 0,95bc 0,77c 1,03bc 1,41a 1,08abc 1,29ab 1,32ab 1,16d
75% 1,34abc 1,68a 1,57ab 1,32bc 0,98c 1,40abc 1,51ab 1,52ab 1,36abc 1,63a 1,43c
50% 2,07a 1,71bc 1,58bc 2,05a 1,90ab 1,40c 1,70bc 1,85ab 1,55bc 1,76abc 1,76b