UIN Syarif Hidayatullah Jakarta
UIN SYARIF HIDAYATULLAH JAKARTA
UJI AKTIVITAS EKSTRAK ETANOL 70% HERBA
KEMANGI (
Ocimum americanum
L.) TERHADAP
KUALITAS SPERMA DAN DENSITAS SEL
SPERMATOGENIK TIKUS SPRAGUE-DAWLEY JANTAN
SECARA
IN VIVO
SKRIPSI
RIAMAYANTI HUTASUHUT
1110102000004
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
UIN Syarif Hidayatullah Jakarta
UIN SYARIF HIDAYATULLAH JAKARTA
UJI AKTIVITAS EKSTRAK ETANOL 70% HERBA
KEMANGI (
Ocimum americanum
L.) TERHADAP
KUALITAS SPERMA DAN DENSITAS SEL
SPERMATOGENIK TIKUS SPRAGUE-DAWLEY JANTAN
SECARA
IN VIVO
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
RIAMAYANTI HUTASUHUT
1110102000004
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
UIN Syarif Hidayatullah Jakarta
HALAMAN PERNYATAAN ORISINALITAS
Skripsi ini adalah hasil karya sendiri, dan semua sumber baik yang dikutip maupun yang dirujuk telah saya nyatakan dengan benar
Nama : RIAMAYANTI HUTASUHUT
NIM : 1110102000004
Tanda Tangan :
Tanggal :
UIN Syarif Hidayatullah Jakarta
HALAMAN PERSETUJUAN PEMBIMBING
NAMA : RIAMAYANTI HUTASUHUT
NIM : 1110102000004
JUDUL : UJI AKTIVITAS EKSTRAK ETANOL 70% HERBA
KEMANGI (Ocimum americanum L.) TERHADAP
KUALITAS SPERMA DAN DENSITAS SEL
SPERMATOGENIK TIKUS SPRAGUE-DAWLEY JANTAN SECARA IN VIVO
Disetujui Oleh :
Pembimbing I
Eka Putri, M. Si., Apt. NIP. 19790517 200901 2 008
Pembimbing II
Dr. Azrifitria, M.Si., Apt. NIP. 19721127 200501 2 004
Mengetahui,
Ketua Program Studi Farmasi Fakultas Kedokteran Dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah
Drs. Umar Mansur, M. Sc., Apt.
UIN Syarif Hidayatullah Jakarta
HALAMAN PENGESAHAN
Skripsi ini diajukan oleh :
Nama : Riamayanti Hutasuhut
NIM : 1110102000004
Program Studi : Farmasi
Judul Skripsi :Uji Aktivitas Ekstrak Etanol 70% Herba Kemangi (Ocimum americanum L.) Terhadap Kualitas Sperma Dan Densitas Sel Spermatogenik Tikus Sprague-Dawley Jantan Secara In Vivo
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
DEWAN PENGUJI
Pembimbing I : Eka Putri, M.Si., Apt. (………)
Pembimbing II :Dr. Azrifitria, M. Si., Apt. (………)
Penguji I : Yardi, M. Si., Apt., Ph. D. (………)
Penguji II : Ismiarni Komala, M. Sc., Apt., Ph. D. (………)
Ditetapkan di :
Tanggal :
UIN Syarif Hidayatullah Jakarta
ABSTRAK
Nama : Riamayanti Hutasuhut
Program Studi : Farmasi
Judul : Uji Aktivitas Ekstrak Etanol 70% Herba Kemangi (Ocimum americanum L.) terhadap Kualitas Sperma Dan Densitas Sel Spermatogenik Tikus Sprague-Dawley Jantan secara In Vivo
Penelitian ini dilakukan untuk menguji aktivitas ekstrak etanol 70% herba
kemangi (Ocimum americanum L.) pada tikus jantan. Ekstrak diberikan secara
oral sekali sehari selama 48 hari terhadap 20 ekor tikus jantan galur
Sprague-Dawley dan dibagi 4 kelompok yaitu kelompok kontrol (Na CMC 0,5%),
kelompok perlakuan dosis rendah (1 mg/kgBB), dosis sedang (10 mg/kgBB) dan
dosis tinggi (100 mg/kgBB). Parameter yang dilakukan meliputi berat testis,
konsentrasi spermatozoa, morfologi sperma, diameter tubulus seminiferus dan
tebal sel germinal.Hasil yang didapat kemudian dianalisis dengan menggunakan
analisis ANOVA satu arah dan dilanjutkan dengan uji Multiple Comparisons.
Hasil penelitian menunjukkan bahwa pemberian ekstrak etanol 70% herba
kemangi dengan dosis I (1 mg/kgBB), II (10 mg/kgBB dan III (100 mg/kgBB),
memberikan peningkatan yang bermakna terhadap diameter tubulus seminiferus
dan tebal germinal dibandingkan dengan kontrol dan pada dosis III (100
mg/kgBB) memberikan peningkatan bermakna terhadap konsentrasi spermatozoa
dibandingkan dengan kontrol (p≤0,05), namun tidak memberikan pengaruh yang
bermakna terhadap berat testis dan morfologi sperma. Dari beberapa hasil
pengamatan tersebut, dapat disimpulkan bahwa ekstrak etanol 70% herba kemangi
dapat mempengaruhi spermatogenesis tikus dan menurunkan kerusakan pada
sperma. Hasil penelitian ini diharapkan dapat dikembangkan sebagai agen
fertilitas.
Kata kunci : Herba kemangi (Ocimum americanum L.), berat testis,
konsentrasi spermatozoa, morfologi sperma, diameter tubulus seminiferus, tebal
sel germinal.
UIN Syarif Hidayatullah Jakarta
ABSTRACT
Nama : Riamayanti Hutasuhut
Program Studi : Farmasi
Judul : Uji Aktivitas Ekstrak Etanol 70% Herba Kemangi (Ocimum americanum L.) terhadap Kualitas Sperma Dan Densitas Sel Spermatogenik Tikus Sprague-Dawley Jantan secara In Vivo
This study was aimed to find out fertility effects of ethanol 70% extract of
Ocimum americanum plants of male rats. The extract was given orally once a day
for 48 days on 20 Sprague-Dawley male rats that were divided four groups:
control group (CMC Na 0,5%), treatment I (1 mg/kgBW), II (10 mg/kgBW) and
III (100 mg/kgBW). The result was analyzed by using One Way ANOVA and by
Multiple Comparisons test and it showed that ethanol 70% extract of Ocimum
americanum plants in dosage 1 mg/kgBW, 10 mg/kgBW and 100 mg/kgBW
significant increase to diameter of seminiferous tubules and germinal cell layer
thickness with control and in dosage 100 mg/kgBW significant increase to sperm concentration (p≤0,05), but it did not significantly increased to weight of testes and sperm morphology. That mean the ethanol 70% of extract of Ocimum
americanum plants influenced the spermatogenesis of rat and decrease damaged
of sperm. It hoped that results of this study can be used to develop a fertility
agent.
Keyword: Ocimum americanum plants, testis weight, sperm concentration,
sperm morphology, diameter of seminiferous tubules, germinal cell layer
thickness.
UIN Syarif Hidayatullah Jakarta
KATA PENGANTAR
Alhamdulillahirobbil’alamin, segala puji bagi Allah SWT yang telah
melimpahkan rahmat, taufik dan hidayah-Nya sehingga penulis dapat
menyelesaikan penelitian dan menyusun skripsi berjudul “Uji Aktivitas Ekstrak Etanol 70% Herba Kemangi (Ocimum americanum L.) terhadap Kualitas Sperma dan Densitas Sel Spermatogenik Tikus Sprague-Dawley secara In Vivo” dengan baik. Shalawat serta salam senantiasa penulis curahkan kepada Nabi
Besar Muhammad SAW beserta keluarga, para sahabat serta para pengikut di
jalan yang diridhoi-Nya.
Penulis menyadari bahwa dalam penelitian sampai penyusunan skripsi ini
tidak akan terwujud tanpa adanya bantuan, bimbingan, dan dukungan dari
berbagai pihak. Oleh karena itu dalam kesempatan ini penulis tidak lupa
mengucapkan terimakasih kepada:
1. Ibu Eka Putri, M.Si., Apt., dan Ibu Dr. Azrifitria, M.Si., Apt., selaku
pembimbing saya, yang dengan sabar memberikan bimbingan, masukan,
dukungan, dan semangat kepada penulis.
2. Bapak Drs. Umar Mansur, M.Sc., Apt selaku Ketua Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. Kedua orang tua tercinta Ibu Nurmalasari Sagala S.Pd dan Bapak Amarullah
Hutasuhut yang senantiasa memberikan kasih sayang, dukungan baik moril
maupun materil, serta doa tanpa henti yang menyertai setiap langkah penulis.
4. Adik tercinta Sefrina Rizkyanti Hutasuhut dan Amri Kurniansyah Hutasuhut
yang dengan sabar senantiasa memberikan dukungan dan motivasi kepada
penulis.
5. Bapak dan Ibu Dosen yang telah memberikan ilmu dan pengetahuan hingga
penulis dapat menyelesaikan studi di jurusan Farmasi FKIK UIN Syarif
Hidayatullah Jakarta.
6. Teman seperjuangan penelitian penulis Auva, Chaya, Annisa Fitriana, Julia,
Mayta, Dita, Suchinda, atas kebersamaan, bantuan serta motivasinya sejak
awal penelitian hingga akhir penyelesaian skripsi ini.
UIN Syarif Hidayatullah Jakarta 7. Sahabat terbaikku Hanny, Chaya dan Citra yang telah memberi dukungan,
motivasi, serta masukan kepada penulis selama pengerjaan skripsi dan selama
di bangku perkuliahan.
8. Teman – teman Farmasi 2010 “Andalusia” atas persaudaraan dan
kebersamaan yang telah banyak membantu dan memotivasi penulis baik
selama pengerjaan skripsi ini maupun selama di bangku perkuliahan.
9. Laboran Farmasi UIN Syarif Hidayatullah Jakarta, Kak Rahmadi, Kak Rani,
Kak Eris, Kak Tiwi, Kak Liken, dan Kak Lisna, yang dengan sabar
membantu penulis mempersiapkan alat dan bahan selama penelitian.
10.Semua pihak yang telah membantu selama penelitian dan penyelesaian
naskah skripsi baik secara langsung maupun tidak langsung yang namanya
tidak dapat penulis sebutkan satu persatu.
Semoga Allah SWT memberikan balasan yang berlipat ganda atas semua
bantuandan dukungan yang diberikan.
Akhir kata dengan segala kerendahan hati, penulis menyadari bahwa
penyusunan skripsi ini masih belum sempurna dan banyak kekurangan. Oleh
karena itu saran serta kritik yang membangun sangat diharapkan.Semoga skripsi
ini dapat bermanfaat bagi penulis pada khususnya dan bagi pembaca pada
umumnya. Amin Ya Robbal’alamin.
Jakarta, Agustus 2014
Penulis
UIN Syarif Hidayatullah Jakarta
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIK
Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah
Jakarta, saya yang bertanda tangan di bawah ini:
Nama : Riamayanti Hutasuhut
NIM : 1110102000004
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan
Jenis Karya : Skripsi
demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya
ilmiah saya, dengan judul :
Uji Aktivitas Ekstrak Etanol 70% Herba Kemangi (Ocimum americanum L.) terhadap Kualitas Sperma Dan Densitas Sel Spermatogenik Tikus Sprague-Dawley Jantan secara In Vivo.
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu
Digital Library Perpustakaan akademik Universitas Islam Negeri (UIN)
Syarif Hidayatullah Jakarta untuk kepentingan akademik sebatas sesuai
dengan Undang-Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya buat dengan
sebenarnya.
Dibuat di : Jakarta
Pada tanggal : 21 Agustus 2014
Yang menyatakan,
(Riamayanti Hutasuhut)
UIN Syarif Hidayatullah Jakarta
DAFTAR ISI
HALAMAN PENRNYATAAN ORISINALITAS ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
BAB 2. TINJAUAN PUSTAKA ...6
2.1. Tanaman Kemangi ...6
2.1.1. Klasifikasi Ilmiah ...6
2.1.2. Nama Lain ...6
2.1.3. Morfologi Tanaman ...7
2.1.4. Ekologi dan Penyebaran Tanaman ...8
2.1.5. Kandungan Kimia Tanaman ...8
2.1.6. Khasiat Tanaman ...8
2.2. Simplisia ...9
2.3. Ekstrak dan Ekstraksi ...9
2.3.1. Ekstrak dengan Menggunakan Pelarut Cara Dingin ...10
2.3.2. Ekstrak dengan Mengguanakan Pelarut Cara Panas ...10
2.4. Tinjauan Hewan Percobaan ...11
2.4.1. Klasifikasi Tikus Putih (Rattus norvegicus) ...11
2.4.2. Biologis Tikus Putih (Rattus norvegicus) ...12
2.5. Sistem Reproduksi Tikus Jantan ...14
2.5.1. Produksi Sperma ...15
2.5.2. Spermatogenesis pada Tikus ...16
2.5.3. Peran Hormon pada Spermatogenesis ...19
BAB 3. METODE PENELITIAN ...21
3.1. Waktu dan Tempat Penelitian ...21
3.2. Alat dan Bahan ...21
3.2.1. Alat Penelitian ...21
3.2.2. Bahan Penelitian...21
3.2.3. Hewan Uji ...22
3.3. Rancangan Penelitian ...22
3.3.1. Besar Sampel ...22
3.3.2. Dosis Perlakuan ...22
3.4. Prosedur Kerja ...23
UIN Syarif Hidayatullah Jakarta
3.4.1. Penyiapan Simplisia dan Pembuatan Ekstrak ...23
3.4.2. Pengujian Parameter Spesifik dan Non Spesifik ...23
3.4.3. Penyiapan Hewan Coba ...24
3.4.4. Pembuatan Preparat ...24
3.4.5. Pengukuran Parameter ...25
3.5. Perencanaan Analisis Data ...28
BAB 4. HASIL PENELITIAN DAN PEMBAHASAN ...29
4.1. Hasil Penelitian ...29
4.1.1. Determinasi Tanaman ...29
4.1.2. Ekstraksi ...29
4.1.3. Pengujian Parameter Ekstrak ...29
4.1.4. Pengukuran Berat Badan Tikus ...30
4.1.5. Pengukuran Berat Testis ...31
4.1.6. Perhitungan Konsentrasi Spermatozoa ...32
4.1.7. Perhitungan Morfologi Sperma ...33
4.1.8. Pengukuran Diameter Tubulus Seminiferus ...35
4.1.9. Pengukuran Tebal Sel Germinal ...36
4.2. Pembahasan ...37
BAB 5. KESIMPULAN DAN SARAN ...46
5.1. Kesimpulan ...46
5.2. Saran ...46
DAFTAR PUSTAKA ...47
ix
UIN Syarif Hidayatullah Jakarta
DAFTAR LAMPIRAN
Lampiran 1. Hasil Determinasi ...55
Lampiran 2. Alat, Bahan dan Kegiatan Penelitian ...56
Lampiran 3. Pemeriksaan Parameter Ekstrak ...58
Lampiran 4. Alur Penelitian ...59
Lampiran 5. Perhitungan Dosis Uji Ekstrak ...60
Lampiran 6. Berat Badan Tikus Jantan ...61
Lampiran 7. Hasil Pengukuran Berat Testis ...63
Lampiran 8. Hasil Perhitungan Konsentrasi Spermatozoa ...64
Lampiran 9. Hasil Perhitungan Morfologi Sperma ...65
Lampiran 10. Hasil Pengukuran Diameter Tubulus Seminiferus ...66
Lampiran 11. Hasil Pengukuran Tebal Sel Germinal ...67
Lampiran 12. Analisis data Berat Testis ...68
Lampiran 13. Analisis Data Konsentrasi Spermatozoa...71
Lampiran 14. Analisis Data Morfologi Sperma ...74
Lampiran 15. Analisis Data Diameter Tubulus Seminiferus ...77
Lampiran 16. Analisis Data Tebal Sel Germinal ...80
Lampiran 17. Gambaran Morfologi Sperma Normal dan Abnormal ...83
Lampiran 18. Gambaran Histologi ...84
UIN Syarif Hidayatullah Jakarta
DAFTAR TABEL
2.1. Data Biologis Tikus ...13
3.1. Rancangan Percobaan...22
3.2. Pengenceran yang Dilakukan dan Kotak yang Dihitung...25
3.3. Cara Pengenceran ...26
3.4. Rumus Konsentrasi Spermatozoa ...27
4.1. Pengujian Parameter Ekstrak...29
4.2. Rerata Berat Badan Tikus Tiap Kelompok ...30
4.3. Rerata Berat Testis Tikus Tiap Kelompok ...31
4.4. Rerata Konsentrasi Spermatozoa Tikus Tiap Kelompok ...32
4.5. Rerata % Morfologi Sperma Abnormal Tikus Tiap Kelompok ...34
4.6. Rerata Diameter Tubulus Seminiferus Tikus Tiap Kelompok ...35
4.7. Rerata Tebal Sel Germinal ...36
UIN Syarif Hidayatullah Jakarta
DAFTAR GAMBAR
Gambar 2.1. Tanaman Kemangi (Ocimum americanum L.) ...6
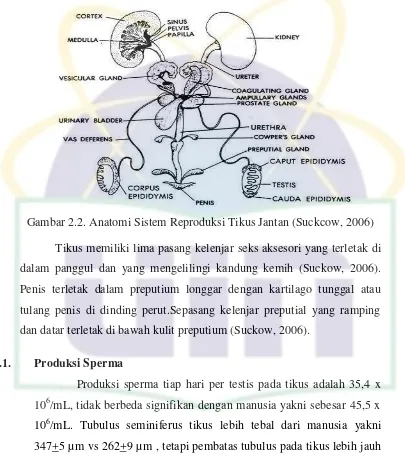
Gambar 2.2. Anatomi Sistem Reproduksi Tikus Jantan ...15
Gambar 2.3. Spermatozoa Tikus ...16
Gambar 2.4. Tahapan dari Siklus Sel Spermatogenesis pada Tikus ...17
UIN Syarif Hidayatullah Jakarta
BAB 1 PENDAHULUAN
1. 1. Latar Belakang
Kasus infertilitas semakin meningkat selama dekade terakhir. Tidak
sedikit pasangan suami istri yang sudah beberapa tahun melangsungkan
pernikahan namun belum juga dikaruniai buah hati. Penyebabnya sangat
bervariasi, dapat karena faktor hormonal, psikologis dan juga patologis
yang dikarenakan penyakit di organ-organ reproduksi pada wanita maupun
pria. Infertilitas tidak hanya dialami oleh wanita. Dalam kasus ini, faktor
pria bertanggung jawab 36%, sedangkan 64% berada pada wanita
(WHO,2011). Penelitian yang dilakukan Arsyad terhadap 246 pasangan
menunjukkan bahwa 48,4% kasus pasangan infertil di Palembang
disebabkan oleh faktor pria (Saputri, 2007).
Kesuburan atau fertilitas pada pria sangat dipengaruhi oleh beberapa
faktor, misalnya adanya gangguan fungsi kelenjar hipotalamus dan
hipofisis yang memproduksi FSH (Follicle Stimulating Hormone) dan LH
(Luteinizing Hormone) atau gangguan pada organ-organ reproduksi,
seperti gangguan pada testis dan epididimis karena penyakit tertentu
(Soenanto dan Kuncoro, 2009).
Salah satu contoh yang mengganggu kesuburan pria lainnya adalah
gaya hidup modern dan paparan lingkungan tertentu. Peningkatan radikal
bebas pada jaringan testis yang memproduksi spermatozoa dapat
menyebabkan kerusakan membran spermatozoa, sehingga mengubah
kestabilan dan fungsi membran. Kemampuan spermatozoa untuk
mengadakan fertilisasi harus didukung oleh membran spermatozoa yang
memiliki integritas (keutuhan) dan fluiditas (kelenturan) optimum
(Agarwal dan Allamaneni, 2004)
Reactive Oxygen Species (ROS) merupakan molekul yang berasal
dari oksigen, yang dibentuk sebagai produk perantara dan termasuk
pengoksidasi kuatdalam tubuh manusia (Halliwel, 1989).ROS adalah senyawa pengoksidasi turunan oksigen yang terdiri atas kelompok radikal
UIN Syarif Hidayatullah Jakarta bebas dan kelompok nonradikal. Spermatozoa membutuhkan ROS pada
konsentrasi rendah untuk menginduksi proses kapasitasi dan reaksi
akrosom, serta berikatan dengan zona pelusida sehingga proses fertilisasi
dapat berlangsung (Sanocka & Kupisz, 2004). Pembentukan ROS secara
berlebihan akan memicu stres oksidatif, berpotensi mengakibatkan toksik
dan merupakan mediator penting terhadap berkurangnya fungsi dan
kualitas spermatozoa (Aitken & Clarkson, 1987). Pembentukan ROS yang
berlebih dapat dihubungkan dengan penurunan motilitas, morfologi
abnormalitas, serta penurunan fertilitas (Potts et al, 2000).
Pencarian obat herbal sebagai agen fertilitas meningkat secara
bermakna (Yakubu et al, 2007). Pemanfaatan tanaman obat atau bahan
alam masih merupakan prioritas untuk diteliti. Selain toksisitasnya yang
rendah, mudah diperoleh, efek yang ditimbulkan juga relatif rendah
(Rusmiati, 2004).Kenyataan menunjukkan bahwa dengan bantuan
obat-obatan yang berasal dari alam tersebut, masyarakat dapat mengatasi
masalah-masalah kesehatan yang dihadapinya, termasuk masalah
infertilitas.
Indonesia merupakan salah satu negara dengan tingkat
keanekaragaman hayati yang tinggi, dimana diseluruh kepulauan nusantara
terdapat lebih dari 30.000 spesies tumbuhan tinggi dari 250.000 spesies
yang terdapat di dunia. Salah satu potensi yang dimiliki oleh tumbuhan,
adalah sebagai sumber bahan kimia berupa metabolit primer maupun
metabolit sekunder, selain itu juga keanekaragaman spesies tumbuhan ini
dapat dijadikan potensi pengembangan obat herbal di Indonesia (Sukandar,
2000).
Salah satu tanaman yang dilaporkan dapat digunakan untuk
mengatasi masalah fertilitas adalah biji karabenguk (Mucuna pruriens).
Mucuna pruriens yang berasal dari India diketahui memilki beberapa
khasiat yaitu antioksidan (Dhanasekaran et al, 2008) dan dapat juga
meningkatkan kualitas sperma pada pria infertil (Shukla et al, 2008). Hasil
UIN Syarif Hidayatullah Jakarta meningkatkan konsentrasi dan motilitas sperma serta menurunkan
morfologi sperma abnormal pada mencit (Pradipta, 2013).
Kemangi (Ocimum americanum L.) sangat populer di Indonesia.Di
daerah Jawa Barat dan daerah-daerah lainnya (Jawa, Sumatera) daun
kemangi sering dikonsumsi sebagai lalapan pelengkap makan dan penguat
aroma dalam makanan. Menurut Kurniawan (2013), secara empiris
kemangi digunakan sebagai afrodisiak karena memiliki kandungan arginin
yang dapat memperkuat daya tahan sperma dan mencegah kemandulan.
Hasil penapisan fitokimia ekstrak etanol 70% herba kemangi (Ocimum
americanum L.) sendiri menunjukkan adanya golongan senyawa seperti
flavonoid, saponin, tanin dan triterpenoid/steroid (Medica dkk, 2004).
Kandungan kimia pada Ocimum americanum L. antara lain : minyak atsiri,
karbohidrat, fitosterol, alkaloid, senyawa fenolik, tanin, lignin, pati,
saponin, flavonoid, terpenoid dan antrakuinon (Sarma dan Babu, 2011).
Hal ini yang melatarbelakangi peneliti untuk melakukan penelitian
tentang fertilitas menggunakan ekstrak herba kemangi (Ocimum
americanum L.).Berbagai penelitian tentang herba kemangi (Ocimum
americanum L.) telah dilakukan, tapi penelitian tentang pengaruh ekstrak
herba kemangi (Ocimum americanum L.) terhadap kualitas sperma dan
densitas selnya belum dilakukan. Untuk membuktikan secara ilmiah, maka
peneliti akan melakukan penelitian uji aktivitas ekstrak herba kemangi
(Ocimum americanum L.) terhadap kualitas sperma yang mencakup profil
morfologi sperma, berat testis dan konsentrasi spermatozoa dan densitas
sel spermatogenik yang mencakup profil histologi diantaranya diameter
tubulus seminiferus dan tebal sel germinal pada tikus jantan.
1. 2. Perumusan Masalah
Berdasarkan dari uraian latar belakang, maka rumusan masalahnya adalah
sebagai berikut:
1. Apakah ada pengaruh pemberian ekstrak etanol herba kemangi
(Ocimum americanum L.) terhadap kualitas sperma yang mencakup
UIN Syarif Hidayatullah Jakarta pada tikus putih (Rattus norvegicus) jantan galur Sprague-Dawley
secara in vivo?
2. Apakah ada pengaruh pemberian ekstrak etanol herba kemangi
(Ocimum americanum L.) terhadap densitas sel spermatogenik yang
mencakup diameter tubulus seminiferus dan tebal sel germinal pada
tikus putih (Rattus norvegicus) jantan galur Sprague-Dawley secara in
vivo?
1. 3. Tujuan Penelitian
Tujuan dari penelitian uji fertilitas ekstrak etanol herba kemangi (Ocimum
americanum L.) pada tikus sehat jantan galur Sprague-Dawley secara in
vivo adalah:
1. Untuk menguji pemberian ekstrak etanol herba kemangi (Ocimum
americanum L.) terhadap kualitas sperma yang mencakup profil
morfologi sperma, berat testis dan konsentrasi spermatozoa pada tikus
putih (Rattus norvegicus) jantan galur Sprague-Dawley secara in vivo.
2. Untuk menguji pemberian ekstrak etanol herba kemangi (Ocimum
americanum L.) terhadap densitas sel spermatogenik yang mencakup
diameter tubulus seminiferus dan tebal sel germinal pada tikus putih
(Rattus norvegicus) jantan galur Sprague-Dawley secara in vivo.
1. 4. Hipotesis
Hipotesis dari penelitian uji fertilitas ekstrak etanol herba kemangi
(Ocimum americanum L.) pada tikus sehat jantan galur Sprague-Dawley
secara in vivo adalah:
1. Pemberian ekstrak ekstrak etanol herba kemangi (Ocimum
americanum L.) dapat meningkatkan kualitas sperma yang mencakup
profil morfologi sperma, berat testis dan konsentrasi spermatozoa
pada tikus putih (Rattus norvegicus) jantan galur Sprague-Dawley
secara in vivo.
2. Pemberian ekstrak etanol herba kemangi (Ocimum americanum L.)
UIN Syarif Hidayatullah Jakarta diameter tubulus seminiferus dan tebal sel germinal pada tikus putih
(Rattus norvegicus) jantan galur Sprague-Dawley secara in vivo.
1. 5. Manfaat Penelitian
Memberikan manfaat kepada masyarakat luas mengenai khasiat
herba kemangi (Ocimum americanum L.) sebagai peningkat kualitas
sperma dan dapat memberikan informasi dalam pengembangan ilmu
UIN Syarif Hidayatullah Jakarta Surawung (Sunda), Selasihputih, kemangi (Indonesia); Maenglak
(Thailand); Rau h[us]ng (Vietnam).
2.1.3. Morfologi Tanaman Kemangi
Kemangi merupakan tanaman tegak, bercabang banyak,
tanaman semusim, herbal aromatik yang tingginya dapat mencapai
0,3-1 m. Batang dan cabangnya berbentuk segi empat, berwarna hijau
kekuningan dan terdapat bulu pada batang terutama pada bagian batang
muda (Siemonsma dan Pileuk, 1994). Bentuk daun sederhana dan
saling berhadapan silang dengan ujung daun berbentuk runcing serta
panjang tangkai daun mencapai 2 cm. Helai daun berbentuk bulat
panjang dengan ukuran panjang daun mencapai 5 cm dan lebar daun
mencapai 2,5 cm (Hadipoentyanti dan Wahyuni, 2008).
Bunga kemangi merupakan bunga majemuk yang panjangnya
dapat mencapai 15 cm, tersusun berhadapan silang dengan 6 bunga
membentuk lingkaran (karangan semu) yang masing-masing terpisah
dengan jarak mencapai 3cm, berbentuk sederhana atau bercabang. Ibu
tangkai bunga dan porosnya berbentuk segi empat. Panjang daun
pelindung pada bunga adalah 2-3 mm berbentuk bulat panjang serta
berbulu. Panjang tangkai bunga mencapai 4 mm, sangat bengkok pada
bagian atas. Kelopak bunga berbelah dua dengan panjang 2-2,5 cm dan
berbulu putih pada bagian luarnya serta berwarna putih. Mahkota bunga
berbentuk tabung berbibir dua dengan ukuran 4 mm dan berwarna
putih. Terdapat 4 benang sari yang berbentuk ramping dengan 2 benang
sari yang lebih panjang.Putik dengan 4 bakal biji dan 4 bakal buah serta
2 kepala putik (Siemonsma dan Piluek, 1994).
2.1.4. Ekologi dan Penyebaran Tanaman
Kemangi sering ditemukan di pinggir jalan, hutan jati, dan
tempat gersang terbuka dekat dengan pemukiman. Tanaman ini lebih
suka tempat yang cerah, terlindung dari angin, tumbuh baik pada
UIN Syarif Hidayatullah Jakarta tanaman ini lebih suka tumbuh pada dataran tinggi, tapi tanaman ini
banyak di tanam di sawah (Siemonsma dan Piluek, 1994).
Kemangi tumbuh secara liar dan dapat di budidayakan di
seluruh Afrika dan Asia yang beriklim tropis. Asal tanaman ini tidak
diketahui secara pasti. DiAsia tenggara telah dilaporkan terdapat
kemangi di Indonesia dan Papua Nugini. Adanya kemangi di Filipina
masih diragukan, namun tanaman ini juga telah dilaporkan terdapat di
Amerika yang beriklim tropis dan beberapa kepulauan di Hindia Barat
(Siemonsma dan Piluek, 1994).
2.1.5. Kandungan Kimia Tanaman
Bahan-bahan kimia yang terkandung diseluruh bagian tanaman
kemangi di antaranya adalah 1,8 sineol, anethol, apigenin fenkhona,
stigmaasterol, triftofan, tannin, sterol dan boron (Dharmayanti, 2003)
Kandungan kimia pada Ocimum americanum L. antara lain :
minyak atsiri, karbohidrat, fitosterol, alkaloid, senyawa fenolik, tanin,
lignin, pati, saponin, flavonoid, terpenoid dan antrakuinon (Sarma dan
Babu, 2011).
Selain itu, daun kemangi juga mengandung minyak atsiri dengan
eugenol sebagai komponen utamanya. Biji kemangi mengandung
saponin, flavonoid dan polifenol (Mangoting dkk, 2005).
2.1.6. Khasiat Tanaman
Secara tradisional, Ocimum spp. dapat digunakan sebagai obat
untuk menyembuhkan beberapa penyakit seperti demam, mengurangi
rasa mual, sakit kepala, sembelit, diare, batuk, penyakit kulit, penyakit
cacing, gagal ginjal, epilepsi dan digunakan sebagai penambah aroma
pada makanan (Nurcahyanti dkk., 2011).
Zat aktif 1,8sineol yang dimiliki kemangi (Ocimum americanum
L.) berkhasiat mampu mengatasi ejakulasi prematur, memperkuat daya
tahan sperma dan mencegah kemandulan pada pria. Sementara apigenin
fenkhona dan eugenol-nya dapat mempermudah ereksi (Dharmayanti,
UIN Syarif Hidayatullah Jakarta Senyawa anethol dan boron dapat merangsang hormon estrogen
pada wanita, sedangkan senyawa eugenol juga dapat membunuh jamur
penyebab keputihan. Zat stigmaasterol dalam kemangi merangsang
pematangan sel telur. Zat triftofan bisa menunda menopause
(Dharmayanti, 2003).
Bijinya memiliki khasiat sebagai peluruh air kencing, peluruh
keringat, mengatasi sembelit, kencing nanah, penyakit mata, pencahar
dan kejang perut (Sudarsono dkk, 2002).
Penelitian yang telah ada menunjukkan bahwa Ocimum spp.
mengandung senyawa yang bersifat insektisida, larvasida, nematisida,
antipiretik, fungisida, antibakteri dan antioksidan (Maryati dkk., 2007).
2.2. Simplisia (Depkes, 2000)
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat
yang belum mengalami pengolahan apapun juga dan kecuali dinyatakan
lain simplisia merupakan bahan yang dikeringkan. Simplisia dapat berupa
simplisia nabati, simplisia hewani dan simplisia pelikan atau mineral.
a. Simplisia nabati adalah simplisia yang berupa tanaman utuh, bagian
tanaman atau eksudat tanaman. Eksudat tanaman ialah isi sel yang
secara spontan keluar dari selnya atau zat-zat nabati lainnya yang
dengan cara tertentu dipisahkan dari tanamannya.
b. Simplisia hewani adalah simplisia yang berupa hewan utuh, bagian
hewan atau zat berguna yang dihasilkan oleh hewan dan belum berupa
zat kimia murni.
c. Simplisia pelikan atau mineral adalah simplisia yang berupa bahan
pelikan atau mineral yang belum diolah atau telah diolah dengan cara
sederhana dan berupa zat kimia murni.
2. 3. Ekstrak Dan Ekstraksi
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi
senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan
UIN Syarif Hidayatullah Jakarta dan massa atau serbuk yang tersisa diperlakukan sedemikian hingga
memenuhi baku yang telah ditetapkan (Depkes RI, 2000).
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat
larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair.
Metode ekstraksi dibagi menjadi tiga cara yaitu: ekstraksi dengan
menggunakan pelarut, destilasi uap dan cara ekstraksi lainnya meliputi
ekstraksi berkesinambungan, superkritikal karbondioksida, ekstraksi
ultrasonik serta ekstraksi energi listrik (Depkes RI, 2000).
2. 3. 1. Ekstraksi dengan Menggunakan Pelarut Cara Dingin 1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau
pengadukan pada temperatur ruangan (kamar). Secara teknologi
termasuk ekstraksi dengan prinsip metode pencapaian konsentrasi
pada keseimbangan. Maserasi kinetik berarti dilakukan
pengadukan yang kontinu (terus-menerus). Remaserasi berarti
dilakukan pengulangan penambahan pelarut setelah dilakukan
penyaringan maserat pertama, dan seterusnya (Depkes RI, 2000).
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru
sampai sempurna (exhaustive extraction) yang umumnya
dilakukan pada temperatur ruangan. Proses terdiri dari tahapan
pengembangan bahan, tahap maserasi antara, tahap perkolasi
sebenarnya (penetesan/penampungan ekstrak), terus menerus
sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali
bahan (Depkes RI,2000).
2. 3. 2. Ekstraksi dengan Menggunakan Pelarut Cara Panas 1. Refluks
Refluks adalah cara ekstraksi dengan pelarut pada
UIN Syarif Hidayatullah Jakarta pelarut terbatas yang relatif konstan dengan adanya pendingin
balik. Umumnya dilakukan pengulangan proses pada residu
pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi
sempurna (Depkes RI, 2000).
2. Soklet
Soklet adalah ekstraksi menggunakan pelarut yang selalu
baru yang umumnya dilakukan dengan alat khusus sehingga
terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan
dengan adanya pendingin balik (Depkes RI, 2000).
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan
kontinu) pada temperatur yang lebih tinggi dari temperatur
ruangan (kamar), yaitu secara umum dilakukan pada temperatur
40 – 50ºC (Depkes RI, 2000).
4. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur
penangas air (bejana infus tercelup dalam penangas air mendidih,
temperatur terukur 96 – 98ºC) selama waktu tertentu (15-20
menit) (Depkes RI, 2000).
5. Dekok
Dekok adalah infus pada waktu yang lebih lama (lebih dari
30 menit) dan temperatur sampai titik didih air (Depkes RI,
2000).
2. 4. Tinjauan Hewan Percobaan
2. 4.1. Klasifikasi Tikus Putih (Rattus norvegicus)
Menurut Krinke (2000) klasifikasi Tikus putih (Rattus
norvegicus) adalah sebagai berikut:
Kingdom : Animalia
Phylum : Chordata
Subphylum : Vertebrata
Class : Mammalia
UIN Syarif Hidayatullah Jakarta
Family : Muridae
Genus : Rattus
Species : norvegicus
2. 4.2. Biologis Tikus Putih (Rattus norvegicus)
Hewan laboratorium atau hewan percobaan adalah hewan yang
sengaja dipelihara dan diternakkan untuk dipakai sebagai hewan model
guna mempelajari dan mengembangkan berbagai macam bidang ilmu
dalam skala penelitian atau pangamatan laboratorik. Tikus termasuk
hewan mamalia, oleh sebab itu dampaknya terhadap suatu perlakuan
mungkin tidak jauh berbeda dibanding dengan mamalia lainnya. Selain
itu, penggunaan tikus sebagai hewan percobaan juga didasarkan atas
pertimbangan ekonomis dan kemampuan hidup tikus hanya 2-3 tahun
dengan lama produksi 1 tahun.
Kelompok tikus laboratorium pertama-tama dikembangkan di
Amerika Serikat antara tahun 1877 dan 1893. Keunggulan tikus putih
dibandingkan tikus liar antara lain lebih cepat dewasa, tidak
memperlihatkan perkawinan musiman, dan umumnya lebih cepat
berkembang biak. Kelebihan lainnya sebagai hewan laboratorium
adalah sangat mudah ditangani, dapat ditinggal sendirian dalam
kandang asal dapat mendengar suara tikus lain dan berukuran cukup
besar sehingga memudahkan pengamatan. Secara umum, berat badan
tikus laboratorium lebih ringan dibandingkan berat badan tikus liar.
Biasanya pada umur empat minggu beratnya 35-40 g, dan berat dewasa
rata-rata 200-250 g, tetapi bervariasi tergantung pada galur. Galur
Sprague Dawley merupakan galur yang paling besar diantara galur yang
lain.
Terdapat beberapa galur tikus yang sering digunakan dalam
penelitian. Galur-galur tersebut antara lain : Wistar, Sprague-Dawley,
Long Evans, dan Holdzman. Dalam penelitian ini digunakan galur
Sprague-Dawley dengan ciri-ciri berwarna putih, berkepala kecil dan
ekornya lebih panjang daripada badannya (Smith dan Mangkoewidjojo
UIN Syarif Hidayatullah Jakarta Dawley. Tikus Sprague Dawley merupakan jenis tikus albino serbaguna
secara ekstensif dalam riset medis. Keuntungan utamanya adalah
ketenangan dan kemudahan penanganannya. Adapun data biologis tikus
sebagai berikut :
Tabel 2.1.Data biologis tikus (Sprague Dawley ® Rat).
Lama hidup 2-3 tahun, dapat sampai 4 tahun
Lama produksi
ekonomis 1 tahun
Lama bunting 20-22 hari
Umur dewasa 40-60 hari
Umur dikawinkan 8-10 minggu (jantan dan betina)
Siklus kelamin Poliestrus
Siklus estrus (berahi 4-5 hari
Lama estrus 9-20 jam
Perkawinan Pada waktu estrus
Ovulasi 8- 11 jam sesudah timbul estrus, spontan
Fertilisasi 7-10 jam sesudah kawin
Implantasi 5-6 hari sesudah fertilisasi
Berat dewasa 300-400 g jantan; 250-300 g betina
Suhu (rektal) 36-39oC (rata-rata 37,5oC)
Pernapasan 65-115/menit, turun menjadi 50 dengan anestesi, naik sampai 550 dalam stres
Denyut jantung 330-480/menit, turun menjadi 250 dengan anestesi, naik sampai 150 dalam stres
Tekanan Darah 90-180 sistol, 60-145 diastol, turun menjadi 80 sistol, 55 diastol dengan anestesi
Konsumsi Oksigen 1,29-2,68 mL/g/jam
Sel darah merah 67,2-9,6 x 106/µL
Konsumsi makanan 15-30 gr/100 gr BB/hari (dewasa)
UIN Syarif Hidayatullah Jakarta
2. 5. Sistem Reproduksi Tikus Jantan
Tikus adalah salah satu hewan penelitian yang paling banyak
digunakan dalam fisiologi reproduksi. Testis dari tikus jantan terdapat
pada dua kantung skrotum yang dipisahkan oleh membran tipis yang
terletak antara anus dan preputium. Testis tersebut kemudian turun antara
hari ke 30 – 40 masa hidupnya dari rongga perut ke kantung skrotum
melalui kanalis inguinal terbuka. Jarakdubur kelamin pada tikus jantan
lebih jauh daripada betina (Suckow, 2006).
Testis terdiri dari tubulus seminiferus yang panjang dan berkelok –
kelok, yang pada epitelnya merupakan tempat berlangsungnya
spermatogenesis. Ujung dari tubulus seminiferus ini kemudian bermuara
menuju epididimis (Barrett et al.,2010).
Epididimis terdiri dari tiga bagian: kaput epididimis yang
membesar diujung proksimal pada testis, yang hampir seluruhnya
terbenam ke dalam lemak; korpus epididimis yang terdapat di sekitar
dorsomedial testis serta kauda epididimis pada ujung distal testis,
merupakan tempat pematangan spermatozoa, yang kemudian bermuara ke
vas deferens (Suckow, 2006).
Diantara tubulus seminiferus di dalam testis terdapat sel Leydig
yang merupakan sel interstisial berfungsi mensekresikan testosteron ke
dalam pembuluh darah (Barrett et al., 2010). Selain sel germinal, di dalam
tubulus seminiferus juga terdapat sel sertoli. Sel ini berperan secara
metabolik dan struktural untuk menjaga spermatozoa yang sedang
berkembang juga memfagosit sitoplasma spermatid yang telah
dikeluarkan. Ukuran sel sertoli sangat besar dengan selubung sitoplasma
yang melimpah yang mengelilingi spermatogoniayang sedang berkembang
(Guyton and Hall, 2006). Sel Sertoli mensekresikan Androgen Binding
Protein (ABP), inhibin, dan Müllerian Inhibiting Substance (MIS). Sel
sertoli mengandung aromatase, enzim yang berperan dalam perubahan
UIN Syarif Hidayatullah Jakarta Gambar 2.2. Anatomi Sistem Reproduksi Tikus Jantan (Suckcow, 2006)
Tikus memiliki lima pasang kelenjar seks aksesori yang terletak di
dalam panggul dan yang mengelilingi kandung kemih (Suckow, 2006).
Penis terletak dalam preputium longgar dengan kartilago tunggal atau
tulang penis di dinding perut.Sepasang kelenjar preputial yang ramping
dan datar terletak di bawah kulit preputium (Suckow, 2006).
2.5.1. Produksi Sperma
Produksi sperma tiap hari per testis pada tikus adalah 35,4 x
106/mL, tidak berbeda signifikan dengan manusia yakni sebesar 45,5 x
106/mL. Tubulus seminiferus tikus lebih tebal dari manusia yakni
347+5 µm vs 262+9 µm , tetapi pembatas tubulus pada tikus lebih jauh
tipis dibanding manusia ( 1,4+1µm vs 15,9+3,4 µm ). Epitel
seminiferus tikus mengandung 40% lebih sel spermatogenik dari
volumenya, dua kali lebih banyak dari epitel seminiferus manusia
(Ilyas, 2007).
Spermatozoa pada tikus lebih panjang dibandingkan dengan
spesies mamalia lainnya, termasuk manusia dan hewan domestik
lainnya dan biasanya panjangnya sekitar 150 – 200 mm. Kepala sperma
pada tikus berbentuk kail hal ini sama seperti pada hewan pengerat
UIN Syarif Hidayatullah Jakarta Gambar 2.3. Spermatozoa Tikus (Krinke, 2000)
2. 5. 2. Spermatogenesis Pada Tikus
Gonosit jantan tetap aktif sampai sebelum pubertas, yaitu
dimana sekitar 50 hari setelah kelahiran. Pada tahap itu mereka mulai
membelah dan menjadi spermatogonium, dan kemudian terus
membelah sampai hewan kehilangan kemampuan untuk memproduksi
UIN Syarif Hidayatullah Jakarta spermiogenesis. Selanjutnya spermatozoa dilepaskan ke dalam lumen
tubulus. Proses pelepasan tersebut dikenal dengan proses spermiasi
(Ilyas, 2007).
Spermatogonium secara garis besar diklasifikasikan ke dalam
tiga jenis: tipe A, tipe intermediet dan tipe B. Tipe spermatogonia A ini
dibagi lagi menjadi tipe AO ( disebut juga sel induk) dan jenis Al-A4.
Tipe spermatogonium AO tetap pada membran basal di tubulus
seminiferus dan memiliki kemampuan untuk membelah menjadi dua sel
anak, salah satunya menjadi spermatogonium A1, yang seterusnya lebih
lanjut dalam proses spermatogenesis, sedangkan yang lainnya sebagai
sel induk. Pada tikus, spermatogonium A1 kemudian memiliki enam
pembelahanmitosis, dan kemudian mereka menjadi spermatosit
prelepton. Kemudian spermatosit dalam fase meiosis, di mana
berkembang melalui leptolene, zygotene dan pachytene menjadi
spermatosit sekunder di komponen adluminal dari sel Sertoli dalam
tubulus seminiferus. Selama fase meiosis, masing-masing spermatosit
menjadi satu dari empat spermatid haploid, yang kemudian memasuki
fase akrosom, selama akrosom berkembang. Kondensasi inti dan
perpanjanganterjadi berikutnya, diikuti oleh fase eliminasi dan
pelepasan sitoplasma.
Pada tikus, 14 tahapan siklus spermatogenesis terjadi di dalam
tubulus seminiferus. Tubulus memiliki susunan ruas, dan setiap
potongan melintang tubula menunjukkan tahapan yang seragam yang
melibatkan empat atau lima generasi di sel germinal dengan sesuai.
Tubulus seminiferus di tikus dikarakterisasi oleh struktur ruas,
sedangkan pada manusia dan hewan domestik lainnya biasanya
menunjukkan pola mosaik di beberapa tahap. Pada tikus, dibutuhkan 12
hari untuk menyelesaikan satu siklus yang terdiri dari 14 tahap.
Spermatogonium tikus membutuhkan empat siklus sampai akhirnya
membentuk spermatozoa, sehingga diperlukan 48 hari untuk
UIN Syarif Hidayatullah Jakarta
2. 5. 3. Peran Hormon Pada Spermatogenesis
Proses spermatogenesis dipengaruhi oleh hormon-hormon
yang dihasilkan oleh organ hipotalamus, hipofisis dan testis sendiri.
Testis memproduksi sejumlah hormon jantan yang kesemuanya disebut
androgen. Yang paling poten dari androgen adalah testosteron. Fungsi
testosteron adalah merangsang pendewasaan spermatozoa yang
terbentuk dalam tubulus seminiferus, merangsang pertumbuhan
kelenjar-kelenjar asesori dan merangsang pertumbuhan sifat jantan
(Partodihardjo,1980).
Spermatogenesis dan pematangan sperma sewaktu bergerak di
sepanjang epididimis dan vas deferens memerlukan androgen.
Androgen juga mengontrol pertumbuhan dan fungsi vesikula seminalis
serta kelenjar prostat. Spermatogenesis hampir seluruhnya terjadi
dibawah pengaruh hormon-hormon yang berasal dari hipofisa, terutama
FSH. Hal ini mirip dengan apa yang terjadi pada ovarium, dimana
terjadi pembentukan folikel di bawah pengaruh FSH. Spermiogenesis
adalah lanjutan spermatogenesis yang berlangsung di bawah peranan
LH dan testosteron. Tanpa testosteron spermatozoa tidak dapat
mencapai pendewasaan yang baik.
Spermatogenesis dimulai pada saat pubertas karena adanya
peningkatan sekresi gonadotropin (FSH dan LH) dari hipofisis anterior.
FSH dianggap merupakan hormon penting untuk menginduksi
spermatogenesis dan untuk merangsang tubulus seminiferus secara
langsung, karena spermatogenesis lengkappada tikus yang
di-hypophysectomise dipulihkan oleh pemberian FSH dalam kombinasi
dengan LH maupun testosteron. Di sisi lain, efek LH pada
spermatogenesis, yang terkadang disebut interstitial cell stimulating
hormone (ICSH) pada pria, karena aksi androgenik pada sel-sel Leydig
di interstitial, dianggap dimediasi oleh androgen, setidaknya pada tikus.
Dalam konteks ini,sekresi LH juga merangsang sintesis testosteron pada
UIN Syarif Hidayatullah Jakarta Aksi FSH pada spermatogenesis diduga diperantarai oleh sel
Sertoli, karena hormon peptida tidak dapat secara langsung mencapai
spermatosit dan spermatid karena barier darah testis, yang terbentuk
selama 16 – 19 hari setelah dilahirkan. Sebaliknya, testosteron dapat
dengan mudah melintasi barier darah testis melalui difusi (dan mungkin
juga melalui beberapa sistem transportasi). Telah dilaporkan bahwa
testosteron pada tikus dewasa yang terdapat dalam cairan interstitial
(lebih dari 50 ng/mL) jauh lebih tinggi dibanding yang terdapat dalam
testis (sekitar 30 ng/mL) maupun yang terdapat pada cairan vena perifer
(<10ng/mL), menunjukkan aksi parakrin atau autokrin dari testosteron
pada spermatogenesis di dalam testis. Adanya reseptor androgen pada
sel germinal masih kontroversial, sementara ini reseptor tersebut telah
ditemukan dalam sel Leydig, sel peritubular, sel Sertoli dan lapisan otot
pembuluh darah pada sebagian arteri dalam testis tikus. Hal ini
menunjukkan bahwa peran testosteron pada spermatogenesis adalah
pada mediasi terakhir. Salah satu peran sel Sertoli adalah memproduksi
protein-pengikat androgen, yang dirangsang oleh FSH dan testosteron
UIN Syarif Hidayatullah Jakarta
BAB 3
METODE PENELITIAN
3.1. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Februari 2014 hingga Juni
2014. Pembuatan ekstrak dilakukan di Laboratorium Penelitian 1,
pemeliharaan dan perlakuan hewan uji di Animal House (MAH) Fakultas
Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri Syarif
Hidayatullah Jakarta. Sedangkan untuk pembuatan preparat histologi
dilakukan di Laboratorium Patologi Universitas Indonesia.
3.2. Alat Dan Bahan 3. 2. 1. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah blender
(Phillips), timbangan analitik (AND GH-202 dan Wiggen Hauser),
vacuum rotaryevaporator (EYELA), botol maserasi, Freeze Dryer
(EYELA FDU-1200), erlenmeyer, beakerglass, batang pengaduk,
spatula, kertas saring, kapas, corong gelas, tabung reaksi, pipet tetes,
oven (Memmert), tanur (Thermo Scientific),aluminium foil, timbangan
hewan (Ohauss), kandang tikus beserta tempat makanan dan minum,
sonde oral, wadah pembiusan, alat bedah minor, kaca objek dan
penutupnya, cawan penguap, mikropipet (Eppendorf Research plus),
mikroskop cahaya (Moticdan Epson) dan Hemositometer Improved
Neubauer (NESCO).
3. 2. 2. Bahan Penelitian
Bahan uji yang digunakan dalam penelitian ini adalah herba
kemangi (Ocimum americanum L.) yang diperoleh dari kebun kemangi
Desa Grogol, Kecamatan Limo, Depok. Kemangi dipanen pada umur 3
bulan, tanpa pestisida dan sistem pengairan menggunakan air hujan dan
air kali di dekat kebun. Selanjutnya kemangi di determinasi di
Herbarium Bogoriensis, LIPI Puslit Biologi, Cibinong Jawa Barat.
Bahan kimia yang digunakan dalam penelitian ini adalah aquades,
UIN Syarif Hidayatullah Jakarta etanol 70%,eter, larutan buffer netral formalin, larutan George, larutan
Eosin Y1%, larutan NaCl, Na CMC, larutan untuk pembuatan preparat
[Hematoksilin-Eosin dan larutan Bouin (asam pikrat,formaldehid 4%,
asam asetat), larutan xilol, Alkohol, Parafin].
3. 2. 3. Hewan Uji
Hewan uji yang akan digunakan dalam penelitian ini adalah
tikus putih jantan strain Sprague-Dawley yang sehat berumur 2,5 – 3
bulan dengan berat badan 180 – 300 gram yang diperoleh dari
peternakan Institut Pertanian Bogor.
3. 3. Rancangan Penelitian 3. 3. 1. Besar Sampel
Penelitian ini bersifat eksperimental yang terbagi dalam 4
kelompok perlakuan yang masing – masing kelompok terdiri dari 5 ekor
tikus putih jantan strain Sprague-Dawley(WHO, 2000).
3. 3. 2. Dosis Perlakuan
Pemberian ekstrak dilakukan selama 48 hari sesuai dengan siklus
spermatogenesis tikus (Krinke, 2000).
Tabel 3.1. Rancangan Percobaan
Kelompok Jumlah
Tikus Perlakuan Keterangan
UIN Syarif Hidayatullah Jakarta
3. 4. Prosedur Kerja
3. 4. 1. Penyiapan Simplisia dan Pembuatan Ekstrak
Kemangi diambil dalam keadaan segar kemudian ditimbang
sebanyak 6 kg kemudian dicuci dengan air mengalir untuk
menghilangkan segala jenis kotoran yang melekat. Setelah pencucian
selesai, kemangi dikering-anginkan untuk mengurangi kadar air dan di
rajang menjadi beberapa bagian. Kemudian dilakukan proses maserasi
selama 72 jam kemudian disaring. Proses maserasi ini diulang hingga
dihasilkan maserat yang lebih bening dibanding maserat awal (pucat).
Ekstrak yang diperoleh dipekatkan dengan vacuum rotary evaporator
sampai diperoleh ekstrak kental. Jika belum kental, ekstrak kemudian di
freeze dry hingga dihasilkan ekstrak yang lebih kental.
3. 4. 2. Pengujian Parameter Spesifik dan Non Spesifik 3. 4. 2.1. Parameter spesifik
Identitas ekstrak.
Deskripsi tata nama :
Nama ekstrak (generik, dagang, paten) Nama latin tumbuhan (sistematika Botani) Bagian tumbuhan yang digunakan
Nama Indonesia tumbuhan (Depkes RI, 2000).
Organoleptik.
Penggunaan pancaindera mendeskripsikan bentuk, warna,bau, rasa.
3. 4. 2.2. Parameter non spesifik
Susut pengeringan
Prosedur : Ekstrak ditimbang secara seksama sebanyak 1 g
sampai 2 g dan dimasukkan ke dalam botol timbang dangkal
bertutup yang sebelumnya telah dipanaskan pada suhu 105ºC selama
30 menit dan telah ditara. Sebelum ditimbang, ekstrak diratakan
dalam botol timbang dengan menggoyangkan botol hingga
merupakan lapisan setebal lebih kurang 5 mm sampai 10 mm. Jika
UIN Syarif Hidayatullah Jakarta pengaduk. Kemudian dimasukkan ke dalam ruang pengering, buka
tutupnya, keringkan pada suhu 105ºC hingga berat tetap. Sebelum
setiap pengeringan, biarkan botol dalam keadaan tertutup mendingin
dalam desikator hingga suhu kamar.Jika ekstrak sulit kering dan
mencair pada pemanasan, ditambahkan 1 g silika pengering yang
telah ditimbang secara seksama, setelah dikeringkan dan disimpan
dalam desikator pada suhu kamar. Campurkan silika tersebut secara
rata dengan ekstrak pada saat panas, kemudian keringkan kembali
pada suhu penetapan hingga berat tetap (Depkes RI, 2000).
Kadar abu
Prosedur: Sebanyak 1 gram ekstrak ditimbang seksama
dimasukkan dalam krus silikat yang sebelumnya telah ditimbang.
Setelah itu ekstrak dipijar dengan menggunakan tanur secara
perlahan-lahan (dengan suhu dinaikkan secara bertahap hingga 600 ±
25ºC, hingga arang habis. Kemudian ditimbang hingga berat tetap
(Depkes, 1980).
3. 4. 3. Penyiapan Hewan Coba
Tikus jantan diaklimatisasi di laboratorium farmakologi selama
1 minggu. Diberi makan dan minum ad libitum serta ditimbang berat
badannya. Ekstrak etanol herba kemangi diberikan secara oral
menggunakan sonde sekali setiap hari yaitu pada pagi hari selama 48
hari dengan dosis seperti yang terterapada tabel rancangan percobaan
(Tabel 1).Pada hari ke-49 masing-masing kelompok diterminasi dengan
eter kemudian dibedah dan diambil testis dan kauda epididimisnya.
3. 4. 4. Pembuatan Preparat
Testis yang telah diambil, difiksasi dalam larutan Bouin,
kemudian didehidrasi dengan etanol seri bertingkat, dan pada akhirnya
ditanamkan dalam parafin wax. Blok parafin dipotong dengan ketebalan 5 μm dan dilakukan pewarnaan dengan hematoksiklin–eosin (Yotarlai
et al., 2011). Pembuatan preparat dilakukan di Laboratorium Patologi
UIN Syarif Hidayatullah Jakarta
3. 4. 5. Pengukuran Parameter 3. 4. 5.1. Berat Testis
Pengukuran berat testis dilakukan dengan cara menimbang
organ testis dengan timbangan analitik kemudian hasil berat testis
tikus yang diberikan perlakuan dibandingkan dengan berat testis
tikus kontrol.
3. 4. 5.2. Perhitungan Konsentrasi Spermatozoa
Perhitungan konsentrasi spermatozoa dilakukan dengan cara
mengambil spermatozoa pada kauda epididimis. Spermatozoa yang
didapat diletakkan pada cawan penguap yang berisi cairan NaCl sebanyak 500 μL. Spermatozoadimasukkan kedalam bilik hitung Neubauer (Hemasitometer) sampai kamar Neubauer terisi rata.
Kemudian dihitung jumlah spermatozoa pada salah satu kamar
hitung Neubauer dan selanjutnya ditentukan pengenceran yang akan
dilakukan dan jumlah kotak yang akan dihitung (Tabel 3.2) (Ilyas,
2007).
Tabel 3.2. Pengenceran yang dilakukan dan kotak yang dihitung
Dari jumlah spermatozoa yang diketahui, maka dilakukan
pengenceran spermatozoa berdasarkan jumlah spermatozoa yang
terhitung (Ilyas, 2007).
No. Jumlah spermatozoa
dalam 1 kotak
Faktor
pengenceran
Kotak kecil
yang dihitung
1 >40 50 kali 5
2 15-40 20 kali 10
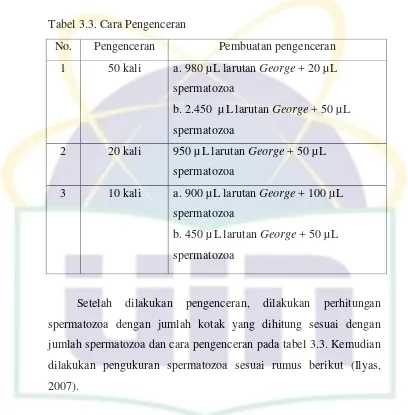
UIN Syarif Hidayatullah Jakarta Tabel 3.3. Cara Pengenceran
Setelah dilakukan pengenceran, dilakukan perhitungan
spermatozoa dengan jumlah kotak yang dihitung sesuai dengan
jumlah spermatozoa dan cara pengenceran pada tabel 3.3. Kemudian
dilakukan pengukuran spermatozoa sesuai rumus berikut (Ilyas,
2007).
Keterangan:
n adalah jumlah spermatozoa yang terhitung. Angka 10.000
merupakan volume kamar hitung Neubauer. Fp merupakan
faktor pengenceran yang dilakukan. Angka 25 menunjukkan
total kotak kecil yang terdapat dalam kamar hitung Neubauer.
k merupakan jumlah kotak kecil yang dihitung pada saat
pengamatan sedangkan vNaCl merupakan volume NaCl
fisiologis (mL) yang digunakan untuk membantu
mengeluarkan spermatozoa dari kauda epididimis.
No. Pengenceran Pembuatan pengenceran
1 50 kali a. 980 µ L larutan George + 20 µL
spermatozoa
b. 2.450 µ L larutan George + 50 µ L
spermatozoa
2 20 kali 950 µ L larutan George + 50 µ L
spermatozoa
3 10 kali a. 900 µ L larutan George + 100 µL
spermatozoa
b. 450 µ L larutan George + 50 µ L
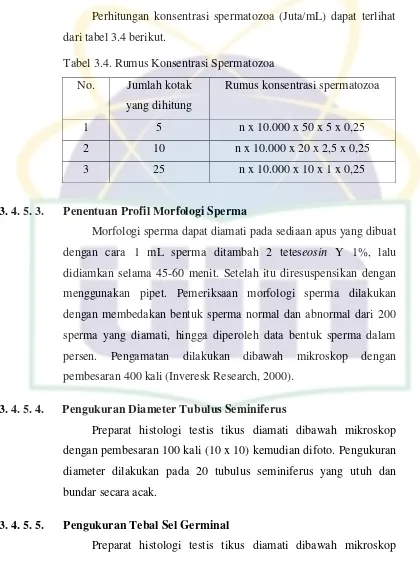
UIN Syarif Hidayatullah Jakarta Perhitungan konsentrasi spermatozoa (Juta/mL) dapat terlihat
dari tabel 3.4 berikut.
Tabel 3.4. Rumus Konsentrasi Spermatozoa
No. Jumlah kotak
yang dihitung
Rumus konsentrasi spermatozoa
1 5 n x 10.000 x 50 x 5 x 0,25
2 10 n x 10.000 x 20 x 2,5 x 0,25
3 25 n x 10.000 x 10 x 1 x 0,25
3. 4. 5. 3. Penentuan Profil Morfologi Sperma
Morfologi sperma dapat diamati pada sediaan apus yang dibuat
dengan cara 1 mL sperma ditambah 2 teteseosin Y 1%, lalu
didiamkan selama 45-60 menit. Setelah itu diresuspensikan dengan
menggunakan pipet. Pemeriksaan morfologi sperma dilakukan
dengan membedakan bentuk sperma normal dan abnormal dari 200
sperma yang diamati, hingga diperoleh data bentuk sperma dalam
persen. Pengamatan dilakukan dibawah mikroskop dengan
pembesaran 400 kali (Inveresk Research, 2000).
3. 4. 5. 4. Pengukuran Diameter Tubulus Seminiferus
Preparat histologi testis tikus diamati dibawah mikroskop
dengan pembesaran 100 kali (10 x 10) kemudian difoto. Pengukuran
diameter dilakukan pada 20 tubulus seminiferus yang utuh dan
bundar secara acak.
3. 4. 5. 5. Pengukuran Tebal Sel Germinal
Preparat histologi testis tikus diamati dibawah mikroskop
dengan pembesaran 100 kali (10 x 10) kemudian difoto. Pengukuran
diameter dilakukan pada 20 tubulus seminiferus yang utuh dan
UIN Syarif Hidayatullah Jakarta
3. 6. Perencanaan Analisis Data
Hasil percobaan yang dianalisis untuk melihat adanya perbedaan
yang nyata pada, berat testis, konsentrasi spermatozoa, profil morfologis
sperma, ukuran diameter tubulus seminiferus dan ketebalan sel germinal
dari masing–masing kelompok perlakuan. Analisis data diolah
menggunakan program pengolahan data statistik SPSS 16 yang meliputi
uji normalitas, uji homogenitas uji parametrik (one-way ANOVA) atau
non parametrik (Kruskal Wallis). Jika hasil dari uji ANOVA maupun
Kruskal Wallis menunjukkan perbedaan yang nyata (p ≤ 0,05) maka
analisis data dilanjutkan menggunakan uji Least Significant Difference
UIN Syarif Hidayatullah Jakarta
BAB 4
HASIL PENELITIAN DAN PEMBAHASAN
4.1. Hasil Penelitian
4. 1. 1. Determinasi Tanaman
Determinasi tanaman dilakukan di Herbarium Bogoriense, Bidang
Botani Pusat Penelitian Biologi-LIPI Bogor. Hasil determinasi
menunjukkan bahwa tanaman sampel uji adalah benar tanaman
kemangi (Ocimum americanum L.) suku Lamiaceae. Surat pernyataan
determinasi dapat dilihat pada Lampiran 1.
4. 1. 2. Ekstraksi
Sebanyak 500 gram serbuk herba kemangi (Ocimum americanum
L.) dimaserasi 70% etanol hingga dihasilkan maserat yang berwarna
pucat (lebih bening daripada maserat awal). Ekstrak yang diperoleh
dipekatkan dengan vacuum rotary evaporator. Ekstrak kental yang
diperoleh sebanyak 30 gram ekstrak kental. Sehingga dihasilkan
rendemen 6%. Perhitungan rendemen dapat dilihat pada Lampiran 3.
4. 1. 3. Pengujian Parameter Ekstrak
Hasil pengujian parameter spesifik dan nonspesifik ekstrak herba
kemangi (Ocimum americanum L.) dapat dilihat pada tabel 4.1.
Tabel 4.1. Pengujian Parameter Ekstrak
Parameter Hasil Pengujian
Parameter Spesifik
a. Identitas ekstrak
Nama lain tumbuhan
Bagian tumbuhan yang digunakan
Nama Indonesia tumbuhan
a. Susut pengeringan 2,277% b. Kadar abu 12,31%
UIN Syarif Hidayatullah Jakarta
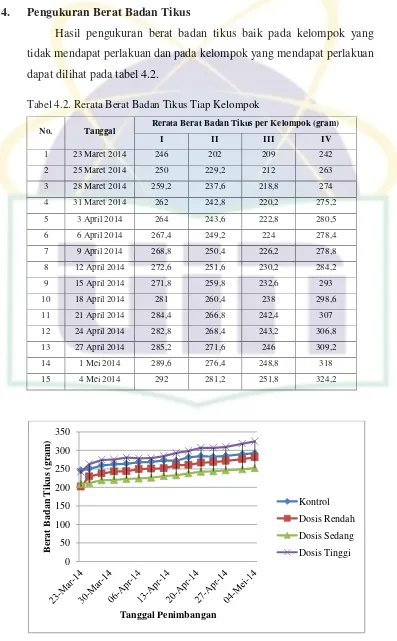
4. 1. 4. Pengukuran Berat Badan Tikus
Hasil pengukuran berat badan tikus baik pada kelompok yang
tidak mendapat perlakuan dan pada kelompok yang mendapat perlakuan
dapat dilihat pada tabel 4.2.
Tabel 4.2. Rerata Berat Badan Tikus Tiap Kelompok
No. Tanggal Rerata Berat Badan Tikus per Kelompok (gram)
I II III IV
Gambar 4.1. Rerata berat Badan Tikus Tiap Kelompok
UIN Syarif Hidayatullah Jakarta
4. 1. 5. Pengukuran Berat Testis
Hasil pengukuran berat testis baik pada kelompok tikus yang
tidak mendapat perlakuan dan pada kelompok yang mendapat perlakuan
dapat dilihat pada tabel 4.3.
Tabel 4.3.Rerata berat testis tikus tiap kelompok
No. Kelompok Rerata Berat Testis (gram) Tiap Kelompok ± SD
1 Kontrol 1,39±0,05 2 Dosis rendah (1 mg/kgBB) 1,39±0,15 3 Dosis sedang (10 mg/kgBB) 1,46±0,12 4 Dosis tinggi (100 mg/kgBB) 1,49±0,19
Gambar 4.2. Hasil rerata berat testis (gram) setelah pemberian ekstrak etanol
70% herba kemangi selama 48 hari
Data rata-rata berat testis diperoleh dengan menimbang
masing-masing testis 20 ekor tikus jantan. Data rata-rata berat testis tikus yang
telah diperoleh selanjutnya dilakukan uji persyaratan. Hasil uji
normalitas Kolmogorov-Smirnov menunjukkan bahwa data berat testis
terdistribusi normal (p ≥ 0,05). Setelah dilakukan uji normalitas,
dilanjutkan uji homogenitas Levene. Hasil uji homogenitas
menghasilkan data homogen (p≥ 0,05). Hasil uji tersebut menunjukkan
nilai signifikan 0,167 (p≥ 0,05). Kemudian dilanjutkan dengan uji BNT
0,0000
Dosis ekstrak herba kemangi (mg/kgBB)
UIN Syarif Hidayatullah Jakarta jenis LSD dimana data yang diperoleh menunjukkan berat testis pada
kelompok dosis rendah, sedang dan dosis tinggi tidak berbeda
bermakna terhadap kelompok kontrol (p ≤ 0,05). Sehingga dapat
disimpulkan bahwa ekstrak etanol 70% herba kemangi tidak dapat
meningkatkan berat testis secara bermakna terhadap kontrol maupun
kelompok tikus lain.
4. 1. 6. Perhitungan Konsentrasi Spermatozoa
Hasil perhitungan konsentrasi spermatozoa pada tiap kelompok
dapat dilihat pada tabel 4.4.
Tabel 4.4. Rerata konsentrasi spermatozoa tikus tiap kelompok
No. Kelompok Rerata Konsentrasi Tiap Kelompok (Juta/mL) ± SD
1 Kontrol 66,625±31,11 2 Dosis rendah (1 mg/kgBB) 71±14,78
3 Dosis sedang (10 mg/kgBB) 81,25±15,31
4 Dosis tinggi (100 mg/kgBB) 104,25±12,11 *
UIN Syarif Hidayatullah Jakarta Gambar 4.3. Hasil rerata konsentrasi spermatozoa setelah pemberian ekstrak etanol
70% herba kemangi selama 48 hari
Data yang telah diperoleh dilakukan uji normalitas dan
homogenitas. Hasil uji normalitas Kolmogorov-Smirnov dan
homogenitas Levene konsentrasi spermatozoa menunjukkan bahwa data
konsentrasi sperma terdistribusi normal (p ≥ 0,05) dan homogen (p ≥
0,05). Data konsentrasi sperma selanjutnya diuji menggunakan
statistika parametric one way Anova (untuk data yang terdistribusi
normal (p ≥ 0,05) dan homogen (p ≥ 0,05)). Hasil uji Anova yang
dilakukan terhadap rata-rata konsentrasi spermatozoa menunjukkan
nilai signifikan 0,036 (p≤ 0,05). Kemudian dilanjutkan dengan uji BNT
jenis LSD dimana data yang diperoleh menunjukkan konsentrasi
spermatozoa pada kelompok dosis tinggi berbeda secara bermakna
terhadap kelompok kontrol (p ≤ 0,05), sedangkan dosis rendah dan
sedang tidak ada perbedaan bermakna dengan kontrol (p ≤ 0,05).
Sehingga dapat disimpulkan jika ekstrak etanol 70% herba kemangi
pada dosis tinggi dapat meningkatkan konsentrasi spermatozoa secara
bermakna terhadap kontrol.
4. 1. 7. Perhitungan Morfologi Sperma
Hasil perhitungan % abnormalitas sperma pada tiap kelompok
dapat dilihat pada tabel 4.5.
0
Dosis ekstrak etanol herba kemangi (mg/kgBB)
UIN Syarif Hidayatullah Jakarta Tabel 4.5. Rerata % morfologi sperma yang abnormal tikus tiap kelompok
No. Kelompok
Rerata % Morfologi Sperma yang Abnormal ± SD
Kepala Sperma Ekor Sperma Total
1 Kontrol 5,9±0,86 2,367±0,355 8,26±1,958
2 Dosis rendah (1 mg/kgBB) 5,31±0,9 2,65±0,87 7,956±1,63
3 Dosis sedang (10 mg/kgBB) 5,158±1,37 2,66±0,578 7,81±1,659
4 Dosis tinggi (100 mg/kgBB) 4,225±1,103 2,335±0,75 6,56±1,335
Gambar 4.4. Hasil rerata persen abnormalitas morfologi sperma setelah
pemberian ekstrak etanol 70% herba kemangi selama 48 hari
Data yang telah diperoleh dilakukan uji normalitas dan
homogenitas. Hasil uji normalitas Kolmogorov-Smirnov dan
homogenitas Levene morfologi sperma menunjukkan bahwa data
morfologi sperma terdistribusi normal (p ≥ 0,05) dan homogen (p ≥
0,05). Data morfologi sperma selanjutnya diuji menggunakan statistika
parametric one way Anova (untuk data yang terdistribusi normal (p ≥
0,05) dan homogen (p ≥ 0,05)). Hasil uji Anova yang dilakukan
terhadap rata-rata morfologi sperma menunjukkan nilai signifikan 0,306
(p ≥ 0,05). Kemudian dilanjutkan dengan uji BNT jenis LSD dimana
data yang diperoleh menunjukkan morfologi sperma pada kelompok
dosis rendah, sedang dan tinggi tidak berbeda secara bermakna terhadap
0
Dosis ekstrak etanol herba kemangi (mg/kgBB)