UIN SYARIF HIDAYATULLAH JAKARTA
Optimasi Formula Mikroemulsi Testosteron Undekanoat
(TU) dengan Kekuatan Sediaan yang Optimum pada
Penggunaan Injeksi Intramuskular
SKRIPSI
SIVIA NURULLIANA SEPTIANINGRUM
108102000025
FAKULTAS KEDOKTERAN & ILMU KESEHATAN
PROGRAM STUDI FARMASI
ii
UIN SYARIF HIDAYATULLAH JAKARTA
Optimasi Formula Mikroemulsi Testosteron Undekanoat
(TU) dengan Kekuatan Sediaan yang Optimum pada
Penggunaan Injeksi Intramuskular
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
SIVIA NURULLIANA SEPTIANINGRUM
108102000025
FAKULTAS KEDOKTERAN & ILMU KESEHATAN
PROGRAM STUDI FARMASI
iii
HALAMAN PERNYATAAN ORISINALITAS
Skripsi ini adalah hasil karya saya sendiri,
dan semua sumber baik yang dikutip maupun dirujuk
telah saya nyatakan dengan benar.
Nama : Sivia Nurulliana Septianingrum
NIM : 108102000025
Tanda Tangan :
iv
HALAMAN PERSERUJUAN PEMBIMBING
Nama : Sivia Nurulliana Septianingrum
NIM : 108102000025
Program Studi : Farmasi
Judul Skripsi : Optimasi Formula Mikroemulsi Testosteron Undekanoat
(TU)
dengan Kekuatan Sediaan yang Optimum pada
Penggunaan
Injeksi Intramuskular
Disetujui oleh :
Pembimbing I Pembimbing II
Dr. Azifitria, M.Si., Apt. Yuni Anggraeni, M.farm., Apt. NIP. 197211272005012004 NIP. 198310282009012008
Mengetahui,
Ketua Program Studi Farmasi
FKIK UIN Syarif Hidayatullah Jakarta
v
HALAMAN PENGESAHAN
Skripsi ini diajukan oleh
Nama : Sivia Nurulliana Septianingrum NIM : 108102000025
Program Studi : Farmasi
Judul Skripsi : Optimasi Formula Mikroemulsi Testosteron Undekanoat (TU)
dengan Kekuatan Sediaan yang Optimum pada Penggunaan
Injeksi Intramuskular
Telah berhasil dipertahankan dihadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Islam Negri (UIN) Syarif Hidayatullah Jakarta.
DEWAN PENGUJI
Pembimbing I : Dr. Azifitria, M.Si., Apt. ( )
Pembimbing II : Yuni Anggraeni, M.Farm., Apt. ( )
Penguji I : Sabrina, M.Farm., Apt. ( )
Penguji II : Drs. Umar Mansur, M.Sc., Apt. ( )
Penguji III : Supandi, M.Si., Apt. ( )
Ditetapkan di : Jakarta
Tanggal : 21 Januari 2013
Mengetahui,
Dekan Fakultas Kedokteran dan Ilmu Kesehatan
UIN Syarif Hidayatullah Jakarta
vi ABSTRAK
Nama : Sivia Nurulliana Septianingrum Program Studi : Farmasi
Judul Skripsi : Optimasi Formula Mikroemulsi Testosteron Undekanoat (TU) dengan Kekuatan Sediaan yang Optimum pada Penggunaan Injeksi Intramuskular.
Mikroemulsi dipilih sebagai pembawa testosteron undekanoat dalam rangka mencari formula alternatif injeksi intramuskular TU. Pada penelitian ini perbandingan campuran minyak (isopropil miristat : minyak jarak : benzil bezoat) untuk meningkatkan solubilisasi testosteron undekanoat diinvestigasi. Selanjutnya, dibuat sediaan mikroemulsi dengan berbagai komposisi minyak, air dan surfaktan dengan perbandingan campuran minyak (20 : 8 : 41) lalu dimasukan ke dalam diagram fase pseudoterner. Formula yang paling stabil dievaluasi meliputi cycling test, uji sentrifugasi, uji pH dan uji ukuran partikel serta dilakukan uji difusi dan dibandingkan dengan sediaan kosolvensi yang beredar di pasaran. Uji difusi menggunakan sel difusi Franz dengan membran otot tikus galur Sprague dawley bagaian biceps femoris serta kompartemen reseptor berisi
phosphate buffer saline pH 7,4. Hasil evaluasi menunjukan sediaan mikroemulsi terpilih adalah formula J yang terdiri dari fase air 3% air dan surfaktan (Tween 80) 28%, serta campuran fase minyak 69% memberikan stabilitas fisik yang baik dengan range pH 6-7 dan ukuran partikel 90,1 nm. Setelah 8 jam pengujian difusi didapatkan Persen TU terpenetrasi pada mikroemulsi dan kosolvensi yang beredar dipasaran secara berturut–turut adalah 1,026 % ; 2,698% dan fluks secara berturut-turut yaitu 63,95 μg/cm2.jam ; 170,476 μg/cm2.jam. Dari hasil uji difusi secara in vitro menunjukan mikroemulsi mempunyai penetrasi yang lebih rendah dibandingkan dengan sediaan kosolvensi yang beredar di pasaran.
Kata kunci : Testosteron Undekanoat, Mikroemulsi, Diagram fase
pseudoterner, sel difusi Franz
vii ABSTRACT
Nama : Sivia Nurulliana Septianingrum Program Study : Pharmacy
Tittle : Optimization and Preparation Testosterone Undecanoate (TU) Microemulsions with Optimum Strength Intramuscular Injection Administration
Microemulsion chosen as the carrier of undekanoat testosterone in order to find an alternative formula of TU intramuscular injection. In this study the mixing ratio of oil (isopropyl myristate: castor oil: benzyl bezoat) to increase solubilization undekanoat testosterone was investigated. Furthermore, microemulsions were made with various compositions of oil, water and surfactant with oil mixture ratio (20: 8: 41) and then inserted into the pseudoterner phase diagram. The most stable formula was evaluated include cycling test, centrifugation test, pH test, particle size test, and then difussion test and compared with cosolvensi preparations in the marketplace. Diffusion test using Franz diffusion cells with membrane strain of
Sprague Dawley rat muscle biceps femoris and the receptor compartment is containing phosphate buffered saline pH 7.4. The result of evaluations shown formula J as the selected microemulsion preparation comprising water phase 3%, and surfactant (Tween 80) 28%, also 69% oil phase mixture gave good physical stability with pH range 6-7 and particle size 90.1 nm. After 8 hours of diffusion tested, percentation of TU in microemulsion and cosolvensi in the marketplace
respectively were 1.026%, 2.698% and flux respectively were 63.95 μg/cm2
.hour; 170.476 μg/cm2.hour. The result of in vitro diffusion test shown that microemulsion had a lower penetration than cosolvensi preparations in the marketplace.
Key Word : Testosterone Undecanoate, Microemulsions, Pseudo-Ternary Phase Diagrams, Franz Diffusions Cell
viii KATA PENGANTAR
ِميِحَرلا ِنم ْحَرلاِه ِمْسِب
Segala puji dan syukur saya panjatkan kepada Allah SWT, atas segala
rahmat dan karunia-Nya yang tidak terhimgga sehimgga saya dapat
menyelesaikan penelitian dan penyusunan skripsi.
Skripsi ini disusun sebagai syarat untuk memperoleh gelar Sarjana
Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri
(UIN) Syarif Hidayatullah Jakarta. Saya menyadari bahwa tanpa bantuan dan
bimbingan dari segala pihak, dari masa perkuliahan sampai pada penyusunan
skripsi ini, kiranya sulit bagi saya untuk menyelesaikan penulisan ini tepat pada
waktunya. Pada kesempatan ini dengan segala kerendahan hati saya
menyampaikan terimakasih yang tulus kepada:
1) Ibu Dr. Azifitria, M.Si., Apt. selaku pembimbing pertama dan Yuni
Anggraeni, M.farm, Apt. sebagai pembimbing kedua yang selalu sabar
membimbing dan memberi saran dalam penyusunan skripsi dan teknis
pengerjaan selama penelitian berlangsung sampai tersusunnya skripsi ini.
2) Bapak Prof. (hc) dr. MK. Tadjudin s.and., selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah
Jakarta.
3) Bapak Drs. Umar Mansur M.Sc., Apt. selaku Ketua Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN)
Syarif Hidayatullah Jakarta.
4) Bapak dan Ibu staf pengajar yang telah memberikan bimbingan dan bantuan
selama saya menempuh pendidikan di Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta.
5) Kedua orang tua saya tercinta Bapak Suroso dan Ibu Rosmalarita atas doa,
nasehat, perhatian, kasih sayang, kesabaran dan pengorbanan baik moral
maupun materil yang diberikan kepada saya.
6) Adik-adik tersayang Hafina Rehana Jannah dan Shalscha Fatimah Az Zahra
yang selalu mendoakan dan menyemangati selama ini.
ix
7) Seluruh karyawan dan laboran khususnya Eris Risenti Amd. yang telah
membantu saya selama penelitian di dalam laboratorium.
8) Ilham Adraviatma S.Kom. atas segala bantuan, saran, semangat dan doa yang
tiada henti kepada saya agar skripsi ini selesai tepat pada waktunya.
9) Teman-teman terbaik (Widya dwi arini, RR. Alvira Widjaya, Indah
Prihandini, Amalia Khairunnisa, Ade Fithrotinnadhiroh, Septi Purnamasari,
Yosseane Widia Kristi) yang tidak bosan untuk memberikan saran dan
semangat dan selalu mendorong saya untuk cepat menyelesaikan skripsi ini.
10)Teman-teman satu perjuangan dalam labolatorium Dina Haryani, Dwi Nur
Astria, dan Mahmudah yang selalu membuat suasana di labolatorium menjadi
hangat seperti keluarga.
11)Teman-teman ALCOOLIQUE yang selalu mewarnai hari-hari selama masa
kuliah (yuni, endah, sinthi, nia, dian, fitri, dewa, ikhsan) dan semuanya yang
tidak dapat disebutkan satu per satu.
12)Seluruh teman-teman farmasi 2008 yang banyak membantu selama masa
perkuliahan maupun selama penelitian serta atas kebersamaan yang tidak akan
terlupa.
Saya berharap Allah SWT, berkenan membalas segala kebaikan semua
pihak yang telah membantu. Penulis menyadari bahwa skripsi ini jauh dari
sempurna, oleh karena itu penulis mengharapkan kritik dan saran untuk
kesempurnaan skripsi ini. Semoga skripsi ini dapat membawa manfaat bagi
pengembangan ilmu.
Jakarta, Januari 2013
Penulis
x
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta, saya yang bertanda tangan di bawah ini:
Nama : Sivia Nurulliana Septianiingrum NIM : 108102000025
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan Jenis Karya : Skripsi
demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya yang berjudul :
Optimasi Formula Mikroemulsi Testosteron Undekanoat (TU) dengan Kekuatan Sediaan yang Optimum Pada Penggunaan Injeksi Intramuskular.
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital Library Perpustakaan akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya buat dengan sebenarnya.
Dibuat di : Jakarta
Pada tanggal : 21 Januari 2013
Yang menyatakan,
(Sivia Nurulliana Septianingrum)
xi DAFTAR ISI
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISININALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN ... v
ABSTRAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
DAFTAR ISI ... xi
2.4 Sediaan Parenteral Intramuskular ... 14
2.5 Uji Difusi ... 15
xii
3.3.2 Bahan ... 23
3.4 Prosedur Kerja ... 23
3.4.1 Percobaan Pendahuluan ... 23
3.4.2 Optimasi Formula Mikroemulsi dengan Variasi Konsentrasi ... 24
3.4.3 Pembuatan Mikroemulsi ... 26
3.4.5.1 Preparasi Cuplikan Uji Difusi dan Penetapan Kadar Sampel Menggunakan KCKT ... 28
3.4.5.2 Penetapan kadar Zat Aktif pada Sediaan Mikroemulsi dan Kosolvensi yang Beredar di Pasaran ... 28
4.1.2 Optimasi Formula Mikroemulsi dengan Variasi Konsentrasi .. 31
4.1.3 Pembuatan Mikroemulsi ... 32
4.1.4 Evaluasi Mikroemulsi Lanjutan ... 32
4.1.4.1 Cycling Test ... 32
4.1.4.2 Uji Sentrifugasi ... 33
4.1.4.3 Uji pH ... 33
4.1.4.4 Uji Ukuran Partikel ... 33
4.1.5 Uji Difusi ... 33
4.1.5.1 Kurva Kalibrasi Testosteron Undekanoat untuk Cuplikan Uji Difusi ... 33
4.1.5.2 Penetapan kadar Zat Aktif pada Sediaan Mikroemulsi dan Kosolvensi yang Beredar di Pasaran ... 34
4.1.5.3 Hasil Uji Difusi Sediaan Mikroemulsi dibandingkan Sediaan Kosolvensi yang Beredar di Pasaran ... 34
4.2. PEMBAHASAN ... 36
BAB 5 KESIMPULAN DAN SARAN ... 46
5.1 Kesimpulan ... 46
5.2 Saran ... 46
DAFTAR PUSTAKA ... 47
xiii DAFTAR TABEL
Tabel 2.1 Kelarutan Testosteron Undekanoat pada Beberapa Pelarut ... 6
Tabel 2.2 Kegunaan IPM dalam Formulasi Farmasetik ... 12
Tabel 3.1 Perbandingan Campuarn Minyak ... 24
Tabel 3.2 Optimasi Formula Mikroemulsi ... 25
Tabel 4.1 Hasil Uji Kelarutan Testosteron Undekanoat dalam Campuran Minyak ... 30
Tabel 4.2 Hasil Optimasi Kecepatan Pengadukan ... 30
Tabel 4.3 Hasil Pengukuran Partikel Mikroemulsi ... 33
Tabel 4.4 Penetapan kadar Zat Aktif pada Sediaan Mikroemulsi dan Kosolvensi yang Beredar di Pasaran ... 34
Tabel 4.5 Persen Jumlah Kumulatif Testosteron Undekanoat yang Terpenetrasi dari Sediaan Mikroemulsi dan Kosolvensi yang Beredar di Pasaran ... 35
Tabel 4.6 Fluks Testosteron Undekanoat dari Sediaan ... 36
xiv DAFTAR GAMBAR
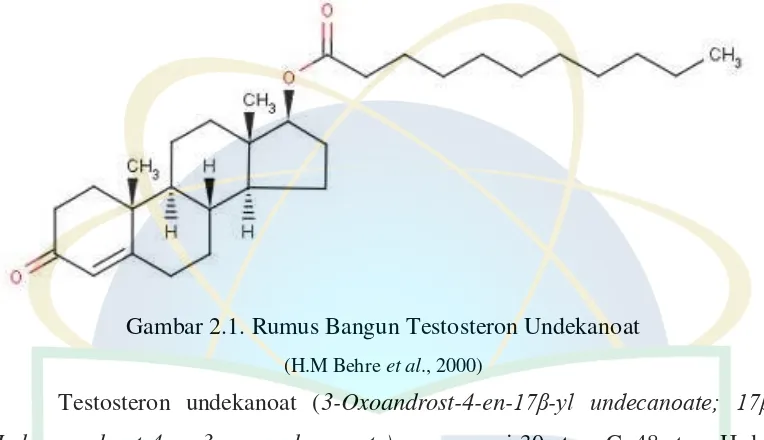
Gambar 2.1 Rumus Bangun Testosteron Undekanoat ... 5
Gambar 2.2 Mekanisme Aksi Testosteron Undekanoat ... 6
Gambar 2.3 Tipe Sistem Dispersi Mikroemulsi ... 9
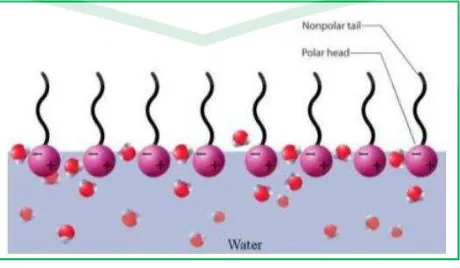
Gambar 2.4 Molekul Surfaktan ... 9
Gambar 2.5 Rumus Bangun Benzil Benzoat ... 11
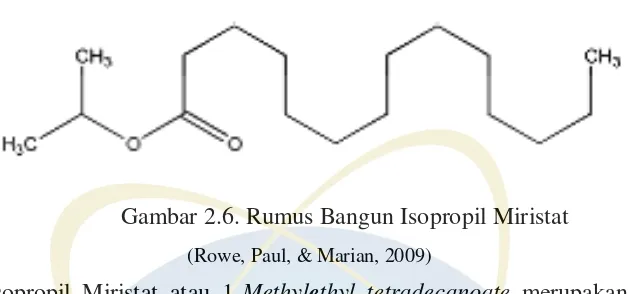
Gambar 2.6 Rumus Bangun Isopropil Miristat ... 12
Gambar 2.7 Ketidakstabilan Emulsi ... 14
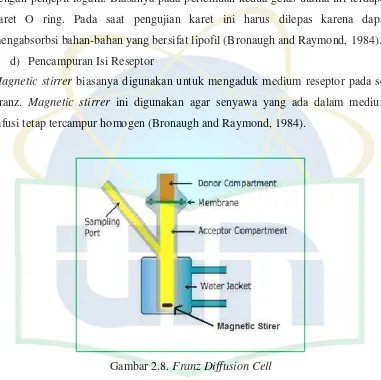
Gambar 2.8 Franz Diffusion Cell ... 17
Gambar 2.9 Solubilisasi Sebagai Reaksi Permukaan ... 21
Gambar 4.1 Diagram Fase pseudoterner ... 31
Gambar 4.2 Hasil Uji Cycling Test Mikroemulsi ... 32
Gambar 4.3 Mikroemulsi Setelah Sentrifugasi ... 33
Gambar 4.4 Kurva Kalibrasi Testosteron Undekanoat ... 34
Gambar 4.5 Grafik Persen Jumlah Kumulatif Testosteron Undekanoat yang Terpenetrasi dalam Sediaan Mikroemulsi dan Kosolvensi yang Bereadar di Pasaran ... 35
Gambar 4.6. Fluks Testosteron Undekanoat dari Sediaan Mikroemulsi dan Sediaan Kosolvensi yang beredar di Pasaran Selama 8 jam ... 36
xv DAFTAR LAMPIRAN
Lampiran 1 Data Konsentrasi dan AUC dari Kurva Kalibrasi ... 51
Lampiran 2 Contoh Perhitungan Jumlah Testosteron Undekanoat yang Terpenetrasi dari Sediaan Komersil Jam ke-3 ... 52
Lampiran 3 Contoh Perhitungan persen Zat Aktif yang Terpenetrasi dari Sediaan Kosolvensi Terhadap Kadar yang diaplikasikannya ... 52
Lampiran 4 Contoh Perhitungan Fluks Testosteron Undekanoat dari Sediaan Mikroemulsi ... 53
Lampiran 5 Perhitungan Kadar testosteron Undekanoat Sebenarnya yang dimasukan ke Dalam Persamaan Regresi Linear Kurva Kalibrasi 1 ... 54
Lampiran 6 Hasil Uji Penetrasi Testosteron Undekanoat dalam Larutan Phosphate Buffer Saline pH 7,4 dari Sediaan Mikroemulsi dan Sediaan Komersi yang Beredar ... 55
Lampiran 7 Gambar Hasil Optimasi Formula ... 56
Lampiran 8 Gambar Alat dan Bahan yang Digunakan ... 57
Lampiran 9 Gambar Hasil Distribusi Ukuran Partikel Sediaan Sebelum Cycling Test ... 58
Lampiran 10 Kromatogram TU dalam Sediaan Mikroemulsi ... 59
Lampiran 11 Kromatogram TU dalam Sediaan Kosolvensi yang Beredar ... 59
Lampiran 12 Kromatogram TU dalam PBS ... 60
Lampiran 13 Kromatogram Blangko Medium PBS ... 60
Lampiran 14 Certificate of Analysis Testosteron Undekanoat ... 61
Lampiran 15 Certificate of Analysis Benzil Benzoat ... 62
Lampiran 16 Certificate of Analysis Minyak Jarak ... 63
1 UIN Syarif Hidayatullah Jakarta BAB 1
PENDAHULUAN
1.1 Latar Belakang
Kelarutan suatu zat berkhasiat memerankan peran penting dalam formulasi
suatu sediaan farmasi (Kim CK, & Park KM, 1999 dalam Rahmawati J., 2004).
Rendahnya kelarutan suatu zat hidrofobik menyebabkan kecilnya penetrasi obat
tersebut dalam tubuh sehingga kegunaan obat menjadi tidak efisien (Lawrence, &
Ress, 2000).
Testosteron undekanoat (3-Oxoandrost-4-en-17β-yl undecanoate) bersifat hidrofobik dengan nilai kelarutan dalam air 0,00052 mg/ml (Saraswati A., 2012)
dan nilai koefisien partisi [n-oktanol/air] (log P) sebesar 6,91+ 0,49 (Azifitria,
2012). Secara klinik testosteron undekanoat (TU) digunakan untuk pengobatan
hypogonadism dan sedang dikembangkan sebagai kontrasepsi hormonal pada pria
(Kamischke A., 2005 dalam Wistuba J., 2005).
Sifat testosteron undekanoat yang sangat hidrofobik menyebabkan
tantangan dalam memformulasikannya. Salah satu sediaan komersil TU yang
beredar di pasaran adalah dalam bentuk kapsul lunak dengan dosis 40 mg tetapi
dosis yang dibutuhkan 80 mg sehingga pasien harus meminum 2 kapsul. Setiap
kapsul mempunyai berat sekitar 777 mg sehingga jika diminum 2 kapsul
menyebabkan ketidaknyamanan pada pasien (Muchow M., 2011). Pemberian
secara oral mempunyai kelemahan dalam hal mempunyai waktu paruh yang
pendek setelah dikonsumsi (Nieschlag E., 2006).
Berdasarkan keterbatasan sediaan oral tersebut maka dikembangkan
formula testosteron undekanoat dalam bentuk injeksi intramuskular. Pemberian
Injeksi intramuskular testosteron undekanoat mempunyai waktu paruh yang
panjang (+ 70 hari) sehingga pemberianya dapat dilakukan setiap 3 bulan
(Zitzmann M., 2006). Pengembangan formulasi obat-obat hidrofobik yang
ditujukan untuk penggunaan parenteral lebih sulit dibanding dengan
pengembangan obat hidrofobik untuk penggunaan oral (Date, A.A. &
UIN Syarif Hidayatullah Jakarta
Injeksi intramuskular testosteron undekanoat yang beredar di pasaran
diformulasi dalam bentuk kosolvensi minyak jarak. Formula testosteron
undekanoat belum berkembang banyak, hanya sebatas penggantian minyak yang
menjadi pembawanya. Di negara China minyak yang digunakan adalah minyak
biji teh. Akan tetapi, penggunaan minyak biji teh mengharuskan penyuntikan
dalam volume besar karena kelarutan testosteron undekanoat kecil pada minyak
biji teh.
Formulasi dengan pembawa minyak mempunyai kelemahan yaitu dapat
menimbulkan nyeri saat disuntikan. Oleh karena itu, formula injeksi testosteron
undekanoat perlu dikembangkan lebih lanjut untuk menghasilkan sediaan yang
dapat mengurangi rasa nyeri saat penyuntikan.
Salah satu teknologi formulasi yang dapat dijadikan sebagai sediaan
parenteral adalah mikroemulsi. Mikroemulsi mempunyai kelebihan yaitu dapat
meningkatkan solubilisasi zat aktif lipofilik dan meningkatkan bioavailibilitas
obat dalam sirkulasi sistemik. Mikroemulsi stabil secara termodinamika,
transparan, viskositasnya rendah, preparasi mudah (Date, A.A. & Nagarsenker,
M.S., 2008) serta mempunyai ukuran partikel yang kecil (10-100 nm) (Myers D.,
2006). Selain itu, peningkatan profil farmakokinetik terlihat pada pengembangan
formulasi paclitaxel yang dibuat dalam bentuk mikroemulsi dibandingkan dengan
kosolven. Nilai Area Under Curve (AUC) mikroemulsi paclitaxel adalah 34,98
gmL-1.h sedangkan dalam kosolven 21,98 gmL-1.h (He L et al., 2003).
Pada penelitian sebelumnya yang dilakukan oleh Retno Kemala Dewi
(2010), testosteron undekanoat dapat dijadikan dalam bentuk mikroemulsi yang
stabil selama 2 bulan penyimpanan. Namun, mikroemulsi yang dibuat
menggunakan ko-surfaktan etanol. Azrifitria (2011) membuat mikroemulsi
testosteron undekanoat dalam bentuk kombinasi dengan MPA. Namun dalam
mikroemulsi tersebut belum diketahui kapasitas maksimal testosteron undekanoat
yang dapat tersolubilisasi. Kemampuan mikroemulsi dalam mensolubilisasi zat
aktif berhubungan dengan volume pemberian. Hal ini dikarenakan pemberian
secara intramuskular harus memenuhi syarat pemberian maksimal untuk sediaan
3
UIN Syarif Hidayatullah Jakarta
volume maksimal akan mengakibatkan nyeri bahkan dapat menyebabkan
nekrosis.
Penelitian yang dilakukan Afrini (2012) memperlihatkan kelarutan
testosteron undekanoat pada beberapa pelarut antara lain isopropil miristat,
minyak jarak, benzil benzoat, tween 80, dan air. Hasilnya menunjukan kelarutan
testosteron undekanoat paling besar pada benzil benzoat dan peningkatan benzil
benzoat dalam sediaan mikroemulsi dapat meningkatkan kelarutan testosteron
undekanoat.
Berdasarkan latar belakang tersebut peneliti tertarik untuk membuat
mikroemulsi TU sesuai dosis klinis 1000 mg dengan memperhatikan volume
maksimal pemberian intramuskular (4 mL) mikroemulsi yang dibuat dengan
komponen isopropil miristat, minyak jarak, benzil benzoat sebagai fase minyak,
tween 80 sebagai surfaktan dan air sebagai fase airnya dengan variasi konsentrasi
fase minyak dan surfaktan. Selanjutnya, mikroemulsi yang dibuat dievaluasi
meliputi cycling test, uji pH, uji sentrifugasi, uji ukuran partikel serta dilakukan
uji difusi secara in vitro yang dibandingkan dengan uji difusi sediaan kosolvensi
yang beredar di pasaran.
1.2 Rumusan Masalah
1. Apakah mikroemulsi yang dibuat dapat meningkatkan solubilisasi
testosteron undekanoat di dalamnya?
2. Bagaimanakah profil uji difusi testosteron undekanoat dalam sediaan
mikroemulsi dan sediaan kosolvensi yang beredar di pasaran?
1.3 Tujuan Penelitian
1. Mendapatkan formula mikroemulsi TU yang dapat meningkatkan
solubilisasi TU.
2. Membandingkan laju difusi hormon testosteron undekanoat dari sediaan
mikroemulsi yang dibuat dengan sediaan kosolvensi yang beredar di
UIN Syarif Hidayatullah Jakarta
1.4 Manfaat Penelitian
Penelitian ini diharapkan mendapatkan formula mikroemulsi testosteron
undekanoat yang dapat meningkatkan solubilisasi testosteron undekanoat
sehingga dapat dibuat sesuai dosis klinis serta mengetahui profil difusi
5 UIN Syarif Hidayatullah Jakarta BAB 2
TINJAUAN PUSTAKA
2.1Testosteron Undekanoat
Gambar 2.1. Rumus Bangun Testosteron Undekanoat
(H.M Behre et al., 2000)
Testosteron undekanoat (3-Oxoandrost-4-en-17β-yl undecanoate; 17β -Hydroxyandrost-4-en-3-one undecanoate) mempunyai 30 atom C, 48 atom H dan
3 atom O (C30H48O3) serta mempunyai bobot molekul 456,7. Secara organoleptis
testosteron undekanoat berbentuk kristal atau serbuk kristal tidak berbau dan tidak
berwarna atau putih serta tidak berasa. Testosteron undekanoat merupakan derivat
testosteron yang berbentuk ester yang dihasilkan melalui esterifikasi testosteron
alami pada posisi 17β.
Panjangnya rantai atom karbon yang dimiliki testosteron undekanoat
menyebabkan hormon ini bersifat sangat hidrofobik. Estserifikasi mengurangi
kepolaran suatu zat namun meningkatkan kelarutan terhadap minyak/lemak.
Kelarutan testosteron undekanoat yaitu sangat mudah larut dalam metanol dan
larut dalam minyak nabati dan etanol. Testosteron undecanoat stabil di bawah
suhu dan temperatur normal.
Berdasarkan penelitian yang sudah dilakukan oleh Saraswati 2012
UIN Syarif Hidayatullah Jakarta
Tabel 2.1 Kelarutan Testosteron Undekanoat pada Beberapa Pelarut
Pelarut TU (mg/mL)*
Benzil Benzoat 544,17096 ± 19,52971 Isopropil Miristat 289,59857 ± 16,90818 Minyak jarak 162,06436 ± 55,68066 Tween 80 37,95878 ± 4,72130
Air 0,00052 ± 0,00012
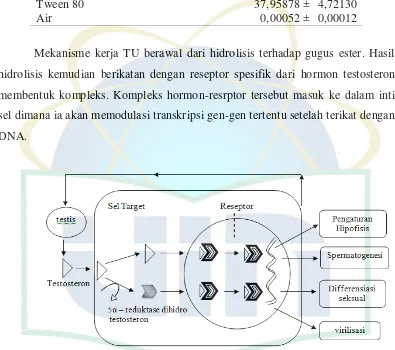
Mekanisme kerja TU berawal dari hidrolisis terhadap gugus ester. Hasil
hidrolisis kemudian berikatan dengan reseptor spesifik dari hormon testosteron
membentuk kompleks. Kompleks hormon-resrptor tersebut masuk ke dalam inti
sel dimana ia akan memodulasi transkripsi gen-gen tertentu setelah terikat dengan
DNA.
Gambar 2.2. Mekanisme Aksi Testosteron Undekanoat
(Ilyas, 2008)
Tujuan utama dari pemberian testosteron adalah mempertahankan
tingginya tingkat serum testosteron jangka panjang pada pria yang ikut dalam
kontrasepsi pria. Hal ini bertujuan untuk menekan spermatogenesis sehingga
terjadi azoospermia atau oligozoospermia berat yang berlangsung lebih lama
namun bersifat aman, efektif, reversibel, dan aseptibel (Ilyas, 2008).
Spermatogenesis memerlukan kerja stimulasi dari kedua hormon
gonadotropin di hipofisis yaitu LH dan FSH. LH berfungsi untuk menstimulasi sel
7
UIN Syarif Hidayatullah Jakarta
agar tetap tinggi di dalam testis yang dibutuhkan untuk spermatogenesis.
Sedangkan FSH berfungsi untuk menginisiasi proses spermatogenesis.
Kontrasepsi hormonal bekerja menghambat sekresi GnRH yang ada pada
hipotalamus sehingga kadar testosteron intra-testikuler menjadi rendah yang
mengakibatkan mengurangi atau mencegah spermatogenesis. Pemberian
testosteron dari luar menyebabkan kadar testosteron dalam darah tetap tinggi
menyebabkan reaksi umpan balik negatif terhadap hipofisis sehingga produksi
FSH dan LH menurun sehingga proses spermatogenesis terhambat.
Bioavailibilitas TU hanya sekitar 7% di dalam tubuh (Muchow, Maincent,
Muller, & Keck 2011) Testosteron ester lambat diabsorbsi ke dalam peredaran
darah dan secara cepat berubah menjadi metabolit aktif yang tidak teresterifikasi.
Ekskresi testosteron 90% melalui urin, 6% melalui feses dalam bentuk asal,
metabolit dan konjugat. Hanya 30% dari 17-ketosteroid yang diekskresi melalui
urin, dengan demikian kadar 17-ketosteroid urin tidak menggambarkan jumlah
sekresi androgen oleh testis tetapi terutama oleh korteks adrenal (Katzung, 2004;
Ilyas, 2008).
2.2 Mikroemulsi
Mikroemulsi adalah sistem dispersi minyak dan air yang secara
termodinamika stabil, transparan atau jernih yang distabilkan oleh lapisan
antarmuka dari molekul surfaktan (El-Laithy, 2003). Mikroemulsi terdiri dari
empat komponen yaitu minyak, air, surfaktan dan kosurfaktan. Hampir semua
penggunaan tunggal surfaktan baik ionik maupun nonionik tidak dapat
menurunkan tegangan antarmuka antara minyak dan air yang mendekati nol. Oleh
karena itu, kosurfaktan dibutuhkan dalam pembuatan mikroemulsi (Kim, &
Cherng-ju, 2004).
Dalam prakteknya, kunci perbedaan antara emulsi dan mikroemulsi adalah
pembentukannya. Emulsi cenderung membentuk dua lapisan di fasa awal
sedangkan mikroemulsi tidak dan mikroemulsi bersifat stabil secara
termodinamik. Selain itu, secara penampilan emulsi terlihat keruh sedangkan
mikroemulsi terlihat jernih dan transparan (Lawrence et al., 2000). Penggunaan
UIN Syarif Hidayatullah Jakarta
Dari segi ukuran droplet (tetesan), emulsi memiliki ukuran diatas 103 nm
sedangkan mikroemulsi memiliki ukuran 10 nm–100 nm (Myers D., 2006).
Mikroemulsi terbentuk dari dua cairan tak tercampurkan yang saling
menguntungkan dimana salah satunya secara spontan terdispersi ke dalam cairan
lainnya dengan bantuan satu atau lebih surfaktan dan kosurfaktan (Rakshit dan
Satya, 2008). Hubungan perilaku fase di dalam mikroemulsi dapat terlihat dengan
bantuan diagram fase (Phase Diagram). Diagram fase ini berguna untuk
menentukan komposisi yang tepat dari fase air, minyak dan surfaktan yang akan
membentuk suatu sistem mikroemulsi. Perilaku fase sederhana sistem
mikroemulsi dapat dipelajari dengan bantuan diagram tiga fase (pseudo-ternary
phase diagram) yang setiap sudut diagram mewakili 100 % tiap komponen
mikroemulsi (air, minyak,surfaktan) (Bakan, J.A., 1995).
Mikroemulsi dapat diberikan secara parenteral. Kelebihan mikroemulsi
jika digunakan untuk parenteral adalah sebagai berikut: a) ukuran droplet yang
kecil sehingga jika masuk ke dalam sirkulasi darah tidak menghambat peredaran
darah, b) stabil secara termodinamika, c) kemampuan mensolubilisasi yang besar,
d) viskositas yang rendah, e) dapat disterilkan dengan filtrasi, f) mengurangi rasa
sakit pada injeksi jika dibandingkan dengan sediaan pelarut campur, g)
mikroemulsi air dalam minyak dapat digunakan untuk penghantaran obat
terkontrol.
2.2.1 Tipe-Tipe Mikroemulsi
Ada tiga tipe sistem dispersi yang dibentuk oleh mikroemulsi yaitu tipe
minyak dalam air (M/A atau O/W), tipe air dalam minyak (A/M atau W/O) dan
tipe kesetimbangan air dan minyak (bicountinous structure). Tipe sistem dispersi
mikroemulsi tersebut terbentuk tergantung komposisi dari komponen mikroemulsi
9
UIN Syarif Hidayatullah Jakarta
Gambar 2.3. Tipe Sistem Dispersi Mikroemulsi
(Lawrence dan Rees, 2000)
Mikroemulsi tipe M/A atau O/W akan terbentuk jika volume fraksi
minyak lebih sedikit dari volume fraksi air. Sebaliknya, mikroemulsi tipe A/M
atau W/O akan terbentuk jika volume fraksi minyak lebih banyak dari volume
fraksi air. Sedangkan mikroemulsi tipe kesetimbangan air dan minyak
(bicountinous structure) akan terbentuk jika volume fraksi minyak sama banyak
dengan volume fraksi air (Lawrence dan Rees, 2000).
2.2.2 Surfaktan
Surfaktan atau zat aktif antarmuka adalah suatu zat yang dapat
menurunkan tegangan antarmuka (Martin, 1993). Surfaktan mempunyai struktur
bipolar yaitu bagian kepala bersifat hidrofilik dan bagian ekor bersifat hidrofobik.
Hal ini menyebabkan surfaktan cenderung berada pada antarmuka antara fase
yang berbeda derajat polaritasnya.
Gambar 2.4. Molekul Surfaktan
(Gevarsio,1996)
Ada empat jenis surfaktan berdasarkan ionisasinya dalam larutan air yaitu
UIN Syarif Hidayatullah Jakarta
Surfaktan anionik adalah molekul yang bermuatan negatif pada gugus
hidrofilik atau aktif permukaan (surface-active), seperti gugus karboksilat sulfat
atau sulfonat. Secara luas, surfaktan ini banyak digunakan karena harganya yang
murah. Namun, surfaktan ini dapat menyebabkan iritasi dan toksik sehingga
hanya digunakan untuk sediaan luar. Surfaktan ini hanya menghasilkan emulsi
A/M. Contoh surfaktan ionik yaitu: Garam Na, K, atau ammonium dari asam
lemak rantai panjang seperti sodium stearat, Sodium lauril sulfat dan sebagainya
(Matheson, 1996; Rosen, 2004).
Surfaktan kationik adalah senyawa yang bermuatan positif pada gugus
hidrofiliknya atau bagian aktif permukaan (surface active). Surfaktan ini memiliki
sifat toksik sehingga cenderung digunakan untuk formula krim antiseptik.
Contohnya surfaktan kationik yaitu cetrimide, cetrimonium bromide
benzalkonium klorida dan quarternery ammonium salt (QUAT) (Matheson, 1996;
Rosen, 2004).
Surfaktan amfoterik adalah surfaktan yang bermuatan positif dan negatif
pada molekulnya, dimana muatannya bergantung kepada pH. Pada pH rendah
akan bermuatan negatif dan pada pH tinggi akan bermuatan positif (Matheson,
1996; Rosen, 2004).
Surfaktan nonionik adalah surfaktan yang tidak bermuatan atau tidak
terjadi ionisasi molekul. Sifat hidrofilik disebabkan karena keberadaan gugus
oksigen eter atau hidroksil. Surfaktan nonionik mempunyai kemampuan
melarutkan senyawa yang kurang larut dan memiliki toksisitas rendah. Contoh
surfaktan nonionik yaitu: Glikol dan gliserol ester, Sorbitan ester, Polysorbate,
PEG, Poloxalkol (Matheson, 1996; Rosen, 2004).
Surfaktan membantu pembentukan emulsi dengan mengabsorpsi pada
antar muka, dengan menurunkan tegangan interfasial dan bekerja sebagai
pelindung agar butir-butir tetesan tidak bersatu. Emulgator membantu
terbentuknya emulsi dengan 3 jalan yaitu (Mayers D., 2006): 1) penurunan
tegangan antar muka (stabilisasi termodinamik), 2) terbentuknya film antar muka
yang kaku (pelindung mekanik terhadap koalesen), 3)Terbentuknya lapisan ganda
11
UIN Syarif Hidayatullah Jakarta
2.2.3 Ko – Surfaktan
Kosurfaktan merupakan molekul kecil bersifat amfifilik, sebuah alkohol
rantai pendek hingga medium (C2-C10). Surfaktan dalam keadaan sendiri tidak
dapat menurunkan tegangan antarmuka air-minyak secara cukup untuk
menghasilkan sebuah mikroemulsi. Penambahan kosurfaktan dapat membantu
menghasilkan tegangan antarmuka mendekati nol. Tegangan antarmuka yang
mendekati nol mengakibatkan diameter globul menjadi sangat kecil. Secara luas
molekul yang dapat berfungsi sebagai kosurfaktan meliputi surfaktan nonionik,
alkohol, asam alkanoat, alkanediol dan alkil amina (Lawrence, 2000).
2.2.4 Komponen Mikroemulsi
2.2.4.1Benzil Benzoat
Benzil benzoat adalah ester dari benzil alkohol dan asam benzoat, dengan
rumus C14H12O2. Sinonim benzil benzoat adalah benzil ester, benzyl benzene
carboxylate, benzylis benzoas, benzil phenylformate, phenylmethyl benzoate.
Benzil benzoat adalah larutan yang jernih dengan bau yang khas. Untuk menjaga
kejernihannya maka benzil benzoat disimpan pada suhu 17oC. Benzil benzoat
larut dalam aseton dan benzen, praktis tidak larut dalam gliserin dan air dan dapat
bercampur dalam kloroform, etanol (95%), eter dan minyak esensial. Benzil
Benzoat merupakan pelarut yang non polar dengan nilai logP 3.7. Benzil benzoat
terutama digunakan sebagai pelarut yang banyak digunakan untuk sediaan
intramuskular dengan kadar 0,01-46% v/v. Selain itu benzil benzoat digunakan
juga pada berbagai macam produk kosmetik seperti sampo, kondisioner, parfum,
pelembab dan cat kuku (Rowe, Paul, & Marian, 2009). Penggunaan benzyl benzot
tidak boleh terlalu tinggi karena akan menyebabkan reaksi anafilaksis.
Gambar 2.5. Rumus Bangun Benzil Benzoat
UIN Syarif Hidayatullah Jakarta
2.2.4.2Isopropil Miristat (IPM)
Gambar 2.6. Rumus Bangun Isopropil Miristat
(Rowe, Paul, & Marian, 2009)
Isopropil Miristat atau 1-Methylethyl tetradecanoate merupakan sebuah
solven yang bersifat lipofilik dengan bobot jenis sama dengan 0,846 – 0,854
g/cm3. Isopropil miristat (IPM) berbentuk cairan bening atau jernih berbau lemah.
IPM larut dalam aseton, kloroform, etanol, etil asetat, lemak, lemak alkohol,
campuran minyak, larutan hidrokarbon, toluen dan lilin. Praktis tidak larut dalam
gliserin, propilenglikol dan air (Rowe, Paul, & Marian, 2009).
Tabel 2.2 Kegunaan IPM dalam Formulasi Farmasetik
Kegunaan IPM Konsentrasi (%)
Deterjen 0,003-0,03
Olic Suspension 0,024
Mikroemulsi < 50
Krim dan Lotio Topikal 1,0 – 10,0
Isopropil miristat (IPM) merupakan pelarut non air pada sediaan parenteral
yang memiliki toksisitas rendah (Rowe, Paul, & Marian, 2009). Selain itu, IPM
tidak menimbulkan aktivitas karsinogenik, mutagenik dan toksisitas akut rendah
dari studi toksisitas secara oral, dermal, inhalasi atau parenteral. IPM tunggal
dapat meningkatkan solubilisasi progesteron 3300 kali dibanding kelarutanya
dalam air. Solubilisasi progesteron dalam IPM dan air berturut – turut adalah 17,0
13
UIN Syarif Hidayatullah Jakarta
2.2.4.3Minyak Jarak (Castrol Oil )
Minyak jarak adalah minyak kental yang berwarna kuning pucat dengan
bau yang sedikit khas dan mempunyai rasa yang sedikit tajam. Minyak jarak
sedikit larut di dalam kloroform, etanol, eter, metanol, sangat mudah larut dalam
etanol (95%) dan petroleum eter, tidak larut dalam minyak mineral kecuali kalau
dicampur dengan minyak nabati. Minyak jarak harus disimpan pada wadah kedap
udara pada suhu tidak lebih dari 15º C (Rowe, Paul, & Marian, 2009).
Minyak jarak biasanya digunakan dalam kosmetik, produk makanan, dan
formulasi farmasetik. Dalam formulasi farmasetik, minyak jarak umumnya
digunakan untuk krim dan salep sediaan topical dengan konsentrasi 5-12,5%.
Namun, minyak jarak juga digunakan pada tablet oral dan formulasi berbentuk
kapsul serta digunakan juga sebagai pelarut pada sediaan injeksi intramuskular.
Penggunaan minyak jarak dalam kosmetik, produk makanan dan formulasi
farmasi umumnya tidak toksik dan tidak mengiritasi jika digunakan sebagai zat
tambahan.
2.2.4.4Tween 80
Tween 80 atau polisorbat 80 merupakan surfaktan nonionik yang memiliki
toksisitas rendah sehingga dapat digunakan untuk penggunaan oral dan parenteral.
Tween 80 berbentuk cairan berwarna kuning dengan bau khas lemah. Tween 80
memiliki bobot jenis 1,08 g/cm3 dan nilai HLB 15 . Nilai HLBnya 14,9. Tween 80
larut dalam etanol dan air. Selain itu, tidak larut dalam minyak mineral dan
minyak nabati. Dalam sediaan farmasetik tween 80 digunakan sebagai agen
pengemulsi, solubilisator, pembasah, dan agen pensuspensi atau pendispersi.
Dosis tween 80 yang dapat digunakan di dalam tubuh selama sehari (acceptable
daily intake) yaitu 25 mg/kgbb (Rowe, Paul, & Marian, 2009).
2.3 Kestabilan Mikroemulsi
Ada empat fenomena yang terjadi jika sebuah emulsi tidak stabil yaitu
flokulasi, creaming, koalesen dan pemisahan sempurna (breaking). Hal tersebut
UIN Syarif Hidayatullah Jakarta
Flokulasi terjadi jika partikel-partikel terdispersi saling berikatan
membentuk kelompok lebih besar, tapi jika dengan pengocokan yang cukup
sediaan akan kembali terdispersi. Terjadinya flokulasi disebabkan oleh kurangnya
jumlah surfaktan dan volume fase terdispersi yang terlalu tinggi.
Creaming adalah pemisahan suatu emulsi ke dalam dua daerah yang
berbeda dimana salah satunya lebih kaya dengan fase dispersi dibandingkan yang
lain. Creaming ini tidak begitu serius karena mudah dihomogen lagi dengan
pengocokan. Creaming mengindikasikan ketidakstabilan pada emulsi sehingga
harus dicegah pembentukanya.
Koalesen terjadi pada kelompok partikel terdispersi yang membentuk
kelompok yang lebih besar lagi dan bersifat irreversibel, hal ini dapat terjadi
akibat keringnya air yang terdapat pada lapisan tipis antarmuka atau pecahnya
lapisan tipis antarmuka.
Breaking adalah proses pemisahan sempurna dari emulsi menjadi
masing-masing komponen cair. Proses pemisahan tersebut terjadi dalam 2 tahap yaitu
flokulasi dan koalesen.
Gambar 2.7. Ketidakstabilan Emulsi
(Im-Emsap W, 2002)
2.4 Sediaan Parenteral Intramuskular
Injeksi intramuskular adalah injeksi volume kecil yang diinjeksikan ke
dalam otot rangka, biasanya pada otot deltoid di bahu atau otot gluteal di bokong.
Suspensi dan larutan berminyak serta injeksi dengan pembawa air dapat diberikan
melalui rute ini. Perbedaan tempat injeksi membuat menyebabkan perbedaan
15
UIN Syarif Hidayatullah Jakarta
volume pemberian maksimal 2ml sedangkan jika diberikan pada otot bagian
gluteeal volume pemberian maksimal adalah 5ml (TPC,92; Lachman 1992) tetapi
biasanya 4 ml.
Persyaratan injeksi intramuskular yaitu dapat diberikan sediaan injeksi
dengan pembawa air ataupun non-air yang dapat bercampur atau tidak dengan air,
suspensi atau larutan koloid, dan emulsi. Tujuan suatu obat diberikan secara
intramuskular adalah mendapatkan efek obat yang tidak terlalu cepat ataupun
untuk sistem depo dimana obat dilepaskan secara lambat sehingga obat dapat
bertahan lama di dalam tubuh seperti contohnya obat-obat KB.
2.5 Uji Difusi
Difusi didefinisikan sebagai suatu proses perpindahan massa molekul
suatu zat yang dibawa oleh gerakan molekular secara acak dan berhubungan
dengan adanya perbedaan konsentrasi aliran molekul melalui suatu batas,
misalnya suatu membran polimer, merupakan suatu cara yang mudah untuk
menyelidiki proses difusi (Martin, 1983).
Difusi adalah proses menjadi difus atau tersebar luas, gerakan molekul
spontan atau partikel dalam larutan, disebabkan gerakan acak suhunya, sehingga
kadarnya sama di seluruh larutan, proses itu tidak memerlukan penambahan
energi terhadap sistem. Pada dasarnya difusi ada 2 macam yaitu difusi aktif dan
difusi pasif. Perbedaan dari keduanya ada pada penggunaan energi. Difusi aktif
memerlukan energy dalam perpindahanya sedangkan difusi pasif tidak
memerlukan energi untuk perpindahan zat. Difusi bebas atau traspor pasif suatu
zat melalui cairan, zat padat, atau melalui membran adalah suatu proses yang
sangat penting dalam ilmu farmasi (Martin, 1983).
2.6 Hukum Fick
Mengacu kepada hukum Fick tentang difusi, jumlah materi M (satuan =
gram atau mol) yang melintasi suatu unit area (satuan = cm2) per satuan waktu
(satuan = detik) dikenal sebagai aliran J, digambarkan sebagai berikut :
UIN Syarif Hidayatullah Jakarta
Pada gilirannya, aliran bersifat proposional terhadap gradien konsentrasi
= −
Di mana dC/dx adalah perubahan konsentrasi dalam sebuah jarak kecil tak
berhingga. Untuk merubah tanda proporsional menjadi tanda sama dengan maka
sebuah konstanta ditambahkan
=−
Yang mana D diketahui sebagai koefisien difusi atau difusifitas (satuan =
cm2/det). Koefisien difusi adalah ukuran laju permeabilitas dari molekul melintasi
suatu area. Tanda negatif menunjukkan bahwa konsentrasi berkurang sebagai
fungsi dari jarak. Bagaimanapun, aliran selalu memiliki nilai positif (Amiji, M.
M., 2003).
2.7 Sel Difusi Statis (Franz Cell)
Franz Cell/ sel difusi statis dengan satu ruang (One Chambered Cell)
pertama kali dibuat oleh Franz. Difusi Franz Cell mungkin adalah sel difusi yang
paling banyak digunakan dan telah tersedia secara komersil (Crown Glass
company, Somerville, New Jersey) selama bertahun-tahun. Hal-hal yang perlu
diperhatikan tentang Sel Difusi Franz adalah sebagai berikut (Bronaugh and
Raymond, 1984):
a) Volume Reseptor
Volume reseptornya dapat dibuat bervariasi dengan diameter peletakan membran.
Volume reseptor Sel Franz tidak harus dimodifikasi seperti pada Flow Through
Cell karena volume reseptor yang relaitf besar (Bronaugh and Raymond, 1984).
b) Pemeliharaan Suhu
Air yang dipanaskan biasanya digunakan untuk mempertahankan suhu fisiologis,
meskipun ada perdebatan mengenai suhu yang sesuai untuk studi difusi. Sel harus
17
UIN Syarif Hidayatullah Jakarta
suhu 37oC disirkulasikan melalui sel Franz untuk menjaga suhu sesuai dengan
keadaan fisiologis tubuh (Bronaugh and Raymond, 1984).
c) Tempat Peletakan Membran
Membran diletakkan diantara pertemuan dua bagian gelas utama dan direkatkan
dengan penjepit logam. Biasanya pada pertemuan kedua gelas utama ini terdapat
karet O ring. Pada saat pengujian karet ini harus dilepas karena dapat
mengabsorbsi bahan-bahan yang bersifat lipofil (Bronaugh and Raymond, 1984).
d) Pencampuran Isi Reseptor
Magnetic stirrer biasanya digunakan untuk mengaduk medium reseptor pada sel
Franz. Magnetic stirrer ini digunakan agar senyawa yang ada dalam medium
difusi tetap tercampur homogen (Bronaugh and Raymond, 1984).
Gambar 2.8. Franz Diffusion Cell
(Pjanovic, Rada, 2009)
2.8 Prosedur dan Alat Pengujian Difusi
Sel dengan konstruksi yang sederhana, seperti yang telah dilaporkan oleh
Aguiar dan Weiner, diduga paling baik untuk pekerjaan difusi. Sel tersebut dibuat
dari gelas atau plastik terang, yang mudah untuk dirakit dan dibersihkan, dan
memberikan kemudahan untuk melihat cairan dan pengaduk yang berputar.
Alat-alat seperti itu dilengkapi dengan Alat-alat untuk mengumpulkan sampel dan uji secara
UIN Syarif Hidayatullah Jakarta
larutan obat. Larutan reseptor dipompa dari tempat yang lebih rendah. Sampel
dikumpulkan dalam suatu tabung di dalam alat pengumpul fraksi otomatis,
kemudian berturut-turut ditentukan kadarnya secara spektrofotometri. Percobaan
bisa dilakukan selama berjam-jam pada kondisi yang terkontrol ini (Martin,
Swarbrick, Cammarata, 1983).
Biber dan Rhodes membuat suatu konstruksi sel difusi tiga kompartemen
dari pleksiglas untuk penggunaan baik dengan membran sintetis maupun
membran biologis yang diisolasi. Obat tersebut dibiarkan berdifusi dari kedua
kompartemen donor sebelah luar ke dalam suatu ruang reseptor pusat. Hasilnya
dapat direproduksi dan dibandingkan dengan hasil penelitian lain. Sel dengan
desain tiga-kompartemen menciptakan pemukaan membran yang lebih besar dan
memperbaiki sensitivitas analitik (Martin, 1983).
Permeasi uap air dan senyawa organik aromatik dari larutan air melalui
lapisan (film) plastik bisa diselidiki dalam sel gelas dengan dua-ruang serupa
dengan desain yang digunakan untuk menyelidiki larutan obat pada umumnya.
Nasim et al. melaporkan tentang permeasi senyawa 19 aromatik dari larutan
dalam air melalui lapisan (film) polietilena. Higuchi dan Auguiar menyelidiki
permeabilitas uap air melalui bahan yang bersalut enterik dengan menggunakan
sel difusi gelas dan ukuran McLeod untuk mengukur perubahan tekanan melewati
lapisan tersebut (Martin, 1983).
Dalam menyelidiki absorpsi melalui kulit, yang biasanya diperoleh dengan
cara autopsi, digunakan kulit manusia atau hewan. Scheuplein menerangkan suatu
sel untuk percobaan penetrasi kulit, dibuat dari Pireks dan terdiri dari dua belahan.
Ruang donor dan ruang reseptor dipisahkan oleh sampel kulit yang ditunjang pada
piring berlubang-lubang dan disekrup kencang di tempatnya. Cairan dalam
reseptor diaduk dengan batang magnet yang dilapis teflon. Alat ini direndam
dalam bejana yang mempunyai temperatur konstan. Sampel diambil secara
periodik dan diuji dengan cara yang sesuai. Untuk senyawa seperti steroida,
penetrasinya lambat. Telah ditemukan metode radioaktif yang diperlukan untuk
menentukan konsentrasi yang rendah tersebut (Martin, 1983).
Wurster et al. mengembangkan suatu sel permeabilitas untuk menyelidiki
19
UIN Syarif Hidayatullah Jakarta
zat yang berpermeasi, termasuk gas, cairan dan gel. Selama percobaan difusi alat
tersebut dijaga pada temperatur konstan dan perlahan-lahan diaduk pada daerah
sekitar membran. Sampel diambil dari ruang reseptor pada waktu-waktu tertentu
dan dianalisis zat yang berpermeasi melalui mebran tersebut (Martin, 1983).
2.9 Solubilisasi
Istilah 'solubilisasi' diperkenalkan oleh McBain untuk menunjukkan
peningkatan kelarutan dari senyawa tertentu, terkait dengan kehadiran surfaktan
misel atau kebalikannya misel dalam larutan. Proses solubilisasi yang paling
populer adalah transfer molekul minyak ke dalam inti surfaktan misel. Dengan
demikian, minyak yang tidak memiliki kelarutan (atau kelarutan terbatas) dalam
fasa air menjadi larut dalam air dalam bentuk tersolubilisasi di dalam misel.
Proses ini memiliki kepentingan khusus untuk menghilangkan kumpulan
minyak dari permukaan padat dan media berpori, dan untuk menghilangkan
campuran minyak yang tersebar di air. Praktik paling penting dari solubilisasi
berkaitan dengan penerapannya dalam kehidupan sehari-hari: detergen dalam
merawat diri dan rumah tangga, juga sama pentingnya dalam berbagai proses
industri (Christian DD., Scamehorn, 1995 dalam Kralchevsk, Peter A., 2005).
Pelaku utama dalam proses solubilisasi yaitu misel dari surfaktan ataupun
kopolimer. Kemampuan mereka untuk menyelimuti minyak adalah hal yang
sangat penting. Penambahan kopolimer yang membentuk campuran misel dengan
surfaktan, adalah cara untuk mengontrol dan meningkatkan kinerja solubilisasi
oleh misel. Mekanisme utama kinetik dari solubilisasi telah dibangun, dengan
keefektifan yang tergantung pada sistem tertentu (Kralchevsk, Peter A., 2005).
Solubilisasi sebagai reaksi massal: disolusi molekul dan difusi minyak
ke dalam fasa air terjadi, dengan penyerapan molekul minyak oleh surfaktan dan
selanjutnya menjadi misel. Mekanisme ini Operatif untuk minyak (seperti
benzena, heksana, dll), yang menunjukkan kelarutan cukup tinggi dalam air
murni. Pertama, molekul minyak larut dari permukaan tetesan minyak ke dalam
air. Kinetika, proses ini dapat ditandai dengan koefisien perpindahan massa.
UIN Syarif Hidayatullah Jakarta
mereka bereaksi dengan misel. Dengan demikian, konsentrasi molekul minyak
bebas berkurang dengan jarak dari antarmuka minyak-air. Dengan kata lain,
solubilisasi terjadi dalam zona terbatas di sekitar tetesan (Kralchevsk, Peter A.,
2005).
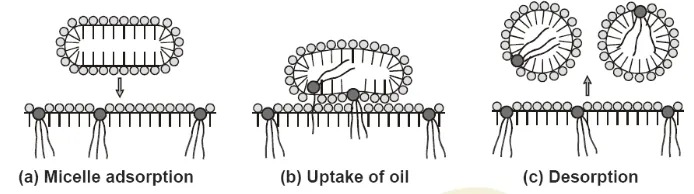
Solubilisasi sebagai reaksi permukaan. Ini adalah mekanisme utama
solubilisasi untuk minyak yang tidak larut dalam air. Pengambilan minyak
tersebut tidak dapat terjadi dalam sebagian besar fasa air. Solubilisasi dapat terjadi
hanya pada antarmuka minyak-air. Mekanisme yang mungkin terjadi termasuk (i)
misel adsorpsi, (ii) minyak yang terselimuti, dan (iii) desorption dari misel yang
mengembang. Sejalan dengan itu, secara teoritis proses ini dapat digambarkan
dengan 3 langkah berturut-turut. Jika misel kosong agregat seperti batang panjang,
di atas solubilisasi mereka biasanya berhenti sejenak untuk agreagat lebih kecil
bulat. Untuk beberapa sistem (terutama solubilizates padat), tahap menengah di
solubilisasi proses mungkin melibatkan penetrasi surfaktan solusi ke fase
berminyak dan pembentukan kristal fase cair pada antarmuka. Untuk beberapa
sistem (kebanyakan solubilisasi padat), tahap menengah dari proses solubilisasi
mungkin melibatkan penetrasi larutan surfaktan ke fase berminyak dan
pembentukan fase kristal cair pada antarmuka (Kralchevsk, Peter A., 2005).
Dalam kasus solubilisasi sebagai reaksi permukaan, mekanisme kinetik
rinci bisa menjadi beraneka ragam. Beberapa penulis mengharapkan bahwa
surfaktan berada di antarmuka sebagai bentuk monomernya. Kemudian, pada fase
pengikatan campuran (atau menggembang) agregat misel terbentuk, akhirnya
terjadi desorbsi. Model ini tampaknya cocok untuk solubilisasi padat, karena
hemimisel dapat terbentuk pada permukanya, bahkan pada konsentrasi surfaktan
di bawah konsentrasi misel kritis (cmc). Konsep lainnya disajikan oleh Plucinski
dan Nitsch, termasuk langkah parsial fusi misel dengan antarmuka dari
minyak-air, diikuti oleh langkah pemisahan. Mekanisme tersebut bisa berlangsung pada
kasus droplet microemulsion, bukan misel, yang bertanggung jawab untuk
21
UIN Syarif Hidayatullah Jakarta
Gambar 2.9. Solubilisasi Sebagai Reaksi Permukaan: Proses dapat dimodelkan Sebagai Urutan Tiga Langkah: (A) Adsorpsi Misel Kosong Pada Antarmuka Minyak-Air; (B) Pengambilan Minyak dicapai Sebagai Reaksi Permukaan: Misel Kosong Mengambil Minyak dan Terbagi Menjadi Beberapa Gembung Misel; (C) Desorption Misel Gembung. Molekul Dengan Tiga Ekor (Solubilizate) Menurut
22 UIN Syarif Hidayatullah Jakarta BAB 3
METODOLOGI PENELITIAN
3.1Alur Penelitian
Formulasi Mikroemulsi Testosteron Undekanoat.
Uji Ukuran Partikel Uji Sentrifugasi
Uji Cyling Test
Mikroemulsi TU Kosolvensi (Produk Pasaran) Pengujian Laju Difusi dengan Franz Diffusion
Cell dengan Medium Posphate Buffer Saline
Dianalisis dengan KCKT Evaluasi Sediaan Mikroemulsi
Uji pH
1.Variasi Konsentrasi Pelarut 2.Diagram fase
23
UIN Syarif Hidayatullah Jakarta
3.2 Lokasi dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Bioavailability Bioequivalence
(PBB), dan Laboratorium Medical Research, Fakultas Kedokteran dan Ilmu
Kesehatan, Universitas Islam Negeri Syarif Hidayatullah Jakarta, Laboratorium
Balai Inkubator Teknologi (BIT) kawasan PUSPIPTEK Serpong. Penelitian
berlangsung selama 8 bulan, terhitung dari bulan Mei 2012 sampai dengan
Desember 2012.
3.3 Alat dan Bahan
3.3.1 Alat
Kromatografi Cair Kinerja Tinggi (Ultimate 3000 Dionex®) yang terdiri
dari pompa, kolom (Dionex®), injektor dan ultraviolet detektor, penyaring
membran 0,45 µ m (Filtrex®), alat-alat gelas (Iwaki Pyrex®), timbangan analitik
(AND GH-202®), pipet mikro (Eppendorf®), lemari pendingin (Sanyo
Medicool®), Oven (France Etuves C 3000®), pengaduk magnetik (Nuova
Stirrer®), hot plate (Advantec SRS710HA), Centrifuge (Eppendrof SH7R),
perangkat alat uji difusi Franz, potongan melintang otot tikus.
3.3.2 Bahan
Testosteron Undekanoat (Jinan Yunxiang Co. Ltd), Benzil Benzoat
(Aldrich Chemistry), Isopropil Miristat (Merck), Castor Oil (Aldrich Chemistry),
Tween 80 (Merck), Aquabidestilata (PT. Ikapharmindo Putramas), Aquadest for
HPLC (Merck), Asetonitril (Merck), Methanol (Merck), Posphate Buffer Saline
(PBS).
3.4 Prosedur Kerja
3.4.1 Percobaan Pendahuluan
Percobaan pendahuluan dilakukan untuk mencari konsentrasi campuran
minyak yang dapat mensolubilisasi testosteron undekanoat sesuai kekuatan yang
paling besar. Selain itu, dilakukan optimasi kondisi pembuatan mikroemulsi yaitu
UIN Syarif Hidayatullah Jakarta
Pencarian konsentrasi campuran minyak dilakukan dengan mencampurkan
semua komponen minyak hingga tercampur homogen. Setelah itu ke dalam
campuran minyak ditambahkan zat aktif sedikit demi sedikit hingga jenuh. Setiap
penambahan zat aktif dilakukan pencatatan jumlah yang ditambahkan. Jumlah zat
aktif yang dapat tersolubilisasi oleh perbandingan campuran minyak adalah
jumlah zat aktif hingga sebelum jenuh. Perbandingan campuran minyak yang
dipilih adalah yang dapat mensolubilisasi zat aktif paling besar. Perbandingan
campuran minyak dapat dilihat pada tabel 3.1.
Tabel 3.1. Perbandingan Campuran Minyak
No IPM Minyak Jarak BB
1 20 8 43
2 20 8 41
3 22 5 44
4 25 5 41
Perbandingan campuran minyak ini didapatkan dari hasil optimasi formula
yang akan jadi mikroemulsi. Formula pada tabel 3.1 merupakan formula yang
dapat membentuk mikroemulsi sehingga selanjutnya ditentukan formula mana
yang dapat meningkatkan solubilisasi testosteron undekanoat paling besar.
Optimasi kondisi yang dilakukan yaitu kecepatan penggadukan dilakukan
pada kecepatan yaitu 100-200rpm, 750 rpm dan 1000-1500rpm. Waktu percobaan
dihitung setelah penambahan air lalu terbentuk mikroemulsi dan dilanjutkan
hingga terlihat adanya kabut-kabut putih yang menandakan pada waktu tersebut
mikroemulsi sudah tidak stabil. Waktu yang terpilih adalah waktu yang dapat
menghasilkan mikroemulsi yang jernih, transparan dan stabil.
3.4.2 Optimasi FormulaMikroemulsi dengan Variasi Kosentrasi
Setelah mendapatkan persentase fase minyak maka dilakukan optimasi dan
digambarkan dengan diagram fase pseudoterner. Diagram fase pseudoterner
membantu mendapatkan konsentrasi optimum fase minyak, surfaktan, kosurfaktan
25
UIN Syarif Hidayatullah Jakarta
stabil. Diagram Fase dibuat dengan variasi konsentrasi minyak dan surfaktan.
Persamaan yang digunakan untuk komposisi diagram fase adalah :
% A (Tween 80)+% B (minyak jarak + IPM + benzil benzoat)+% C (Air) = 100%
% A = Surfaktan %B = Fase minyak %C = Air
Tabel 3.2 Optimasi Formula Mikroemulsi
UIN Syarif Hidayatullah Jakarta
3.4.3 Pembuatan Mikroemulsi
Prosedur pembuatan mikroemulsi dilakukan dengan cara benzil benzoat
dimasukan ke dalam gelas piala, kemudian ke dalamnya ditambahkan IPM dan
minyak jarak. Campuran tersebut diaduk hingga homogen (+ 2 menit). Lalu
ditambahkan komponen lain (Tween 80) sambil diaduk dengan menggunakan
pengaduk magnetik hingga homogen. Aqua bidestilata kemudian ditambahkan ke
dalam campuran sedikit demi sedikit hingga didapatkan larutan yang jernih dan
transparan. Awal penambahan air akan terbentuk gumpalan-gumpalan putih yang
lama kelamaan akan menghilang dan terbentuk mikroemulsi yang jernih.
Penambahan zat aktif dilakukan sebelum penambahan surfaktan. Mikroemulsi
dibuat dengan kekuatan sediaan Testosteron Undekanoat 250 mg/ml.
3.4.4 Evaluasi Mikroemulsi
3.4.4.1 Cycling Test
Sediaan mikroemulsi disimpan pada suhu dingin 4°C selama 24 jam lalu
dikeluarkan dan ditempatkan pada suhu 40°C selama 24 jam (1 siklus). Percobaan
ini dilakukan sebanyak 6 siklus. Kejernihan dan kekeruhan mikroemulsi selama
percobaan dibandingkan dengan sediaan sebelumnya (Azrifitria, 2012).
3.4.4.2 Uji Sentrifugasi
Sediaan mikroemulsi dimasukkan ke dalam tabung sentrifugasi kemudian
dilakukan sentrifugasi pada kecepatan 9000 rpm selama 20 menit (Moreno, MA.,
2001).
3.4.4.3 Uji pH
pH diukur dengan menggunakan pH meter. Pengukuran dilakukan pada
27
UIN Syarif Hidayatullah Jakarta
3.4.4.4 Uji Ukuran Partikel
Ukuran partikel diukur dengan alat DelsaTMNano C (Particle Analyzer).
Sampel yang akan diukur adalah sediaan mikroemulsi suhu ruang dan sediaan
yang telah diuji cycling test. Mikroemulsi didilusi 1:100 dengan aquades sebelum
pengukuran
3.4.5 Uji Difusi
Pengujian dilakukan dengan menggunakan alat uji difusi statis Franz
Cell. Sebanyak 0,5 mL sampel ditempatkan pada kompartemen donor.
Temperatur pada saat pengujian diatur konstan pada suhu 37 + 0,5oC dengan
menggunakan thermostat.
Sebagai barier digunakan potongan melintang otot bagian Biceps Femoris
tikus jantan Sprague-Dawley dengan berat + 380 gram dengan ketebalan otot
yang digunakan 2mm + 0,3 mm dan luas membran 2,46 cm2. Untuk mendapatkan
otot tikus terlebih dahulu tikus dilakukan anestesi menggunakan eter. Selanjutnya
kulit yang melapisi otot dipisahkan dengan perlahan agar otot tidak terluka karena
ditakutkan akan berpengaruh kepada penetrasi zat aktif. Lemak dan pembuluh
darah yang ada pada bagian dalam ataupun luar otot dibersihkan agar tidak
mengganggu penetrasi obat melalui otot. Otot disimpan di dalam lemari pendingin
sebelum digunakan tetapi sebaiknya digunakan otot yang masih segar, otot dapat
digunakan dalam rentan waktu kurang dari 24 jam agar otot masih segar dan tidak
mempengaruhi penetrasi obat
Untuk menciptakan kondisi sink, digunakan medium difusi Phosphate
Buffer Saline sebanyak 21 mL dan diaduk dengan pengaduk magnetik dengan
kecepatan 1500 rpm. Pada interval waktu yang telah ditentukan (1, 2, 3, 4, 5, 6, 7,
8 jam) diambil cuplikan sebanyak 2 ml dengan menggunakan syringe dan segera
digantikan dengan larutan Phosphate Buffer Saline sejumlah volume yang sama.
Uji difusi dilakukan terhadap mikroemulsi dan sediaan kosolvensi yang beredar di
pasaran. Penentuan kadar TU pada sampel dilakukan dengan menggunakan
UIN Syarif Hidayatullah Jakarta
3.4.5.1Preparasi Cuplikan Uji Difusi dan Penetapan Kadar Sampel Menggunakan KCKT
Preparasi sampel cuplikan uji difusi dan penetapan kadar sampel dilakukan
menggunakan KCKT. Cuplikan dari medium uji difusi diambil sebanyak 100 μL,
dimasukkan ke dalam labu ukur 5 mL. Ditambahkan larutan fase gerak hingga 5
ml. Kemudian disaring menggunakan syringe filter lalu dimasukkan ke dalam vial
HPLC. Sampel yang telah dipreparasi diinjeksikan ke dalam instrumen KCKT
dengan fase gerak (Metanol dan Acetonitril (90:10) waktu alir 1,2 mL/menit.
Temperatur kolom ± 25oC. Volume injeksi 20 µL. Detektor UV-Vis diatur pada
panjang gelombang 245 nm (Irma, 2010).
3.4.5.2 Penetapan Kadar Zat Aktif pada Sediaan Mikroemulsi dan Kosolvensi yang Beredar di Pasaran
Penetapan kadar zat aktif dilakukan menggunakan KCKT. Sampel diambil
sebanyak 5 µL dimasukkan ke dalam labu ukur 5 mL. Ditambahkan larutan fase
gerak hingga 5 ml. Kemudian disaring menggunakan syringe filter lalu
dimasukkan ke dalam vial HPLC. Sampel yang telah dipreparasi diinjeksikan ke
dalam instrumen KCKT dengan fase gerak (Metanol dan Acetonitril (90:10)
waktu alir 1,2 mL/menit. Temperatur kolom ± 25oC. Volume injeksi 20 µL.
Detektor UV-Vis diatur pada panjang gelombang 245 nm (Irma, 2010).
3.4.5.3Pembuatan Kurva Kalibrasi
Larutan induk standar testosteron undekanoat dibuat dengan konsentrasi
50 ppm yang dilarutkan di dalam fase gerak Metanol dan Asetonitril (90:10).
Larutan induk dibuat dalam volume 25 mL. Ditimbang 1,25 mg testosteron
undekanoat dan dilarutkan dalam larutan fase gerak metanol dan asetonitril
(90:10) digenapkan hingga 25 mL.
Kurva kalibrasi testosteron undekanoat dibuat dengan mengencerkan
larutan induk testosteron undekanoat 50 ppm menjadi 8 seri konsentrasi yaitu 0,3
– 2,4 ppm lalu diinjeksikan ke dalam instrumen KCKT dengan fase gerak Metanol : Asetonitril (90:10), laju alir 1,2 mL/menit, temperatur kolom 25oC,
volume injeksi 20 µL. detektor UV-Vis diatur pada panjang gelombang 245 nm
29
UIN Syarif Hidayatullah Jakarta
3.4.6 Analisis Data
Data yang dianalisis pada penelitian ini yaitu persentase testosteron
undekanoat yang terakumulasi dan Fluks laju difusi (J).
Persen testosteron undekanoat yang terpenetrasi didapatkan dari jumlah
akumulasi testosteron undekanoat yang terpenetrasi dibagi dengan dosis yang
diplikasikan (125mg) dikali 100%. Jumlah testosteron undekanoat yang
terpenetrasi dihitung dengan rumus:
= { . + =1−1 . }
(Raditya, Iswandana., 2012)
Q = Jumlah akumulatif testosteron undekanoat yang terpenetrasi Cn = Konsentrasi TU(μg/ml) pada sampling Jam ke-n
V = Volume sel difusi Franz = 21 ml
−1
=1 = Jumlah konsentrasi testosteron undekanoat (μg/ml) pada sampling
pertama (jam ke-1) hingga sebelum jam ke-n
S = Volume sampling 2 ml
Kemudian dilakukan perhitungan fluks (kecepatan penetrasi obat tiap
satuan waktu) dengan rumus :
= ×
(Martin, Swarbrick, Cammarata, 1983)
Dimana:
J = Fluks (μg cm-2 jam-1)
M = Jumlah kumulatif testosteron undekanoat yang melalui membran (μg)
S = Luas area difusi (cm2)
30 UIN Syarif Hidayatullah Jakarta
BAB 4
HASIL DAN PEMBAHASAN
4.1 HASIL
4.1.1 Percobaan Pendahuluan
Percobaan pendahuluan dilakukan untuk mencari konsentrasi campuran
minyak yang dapat mensolubilisasi testosteron undekanoat sesuai kekuatan
sediaan yang paling besar. Selain itu, optimasi kondisi pembuatan mikroemulsi
yaitu suhu, kecepatan pengadukan dan waktu pengadukan.
Hasil percobaan pendahuluan kali ini didapatkan perbandingan konsentrasi
campuran minyak yang mensolubilisasi testosteron undekanoat paling besar yaitu
formula 2 dengan perbandingan 20:8:41 (IPM : Minyak Jarak : BB).
Tabel 4.1 Hasil Uji Kelarutan Testosteron Undekanoat dalam Campuran Minyak
Formula IPM Minyak Jarak BB TU yang dapat terlarut (mg)
1 20 8 43 310
2 20 8 41 340
3 22 5 44 331
4 25 5 41 330
Berdasarkan optimasi kondisi pembuatan didapatkan kondisi optimal
pembuatan mikroemulsi yang jernih dan stabil adalah, kecepatan pengadukan +
750 rpm, dengan lama pengadukan + 30 menit.
Tabel 4.2 Hasil Optimasi Kecepatan Pengadukan
Kecepatan (Rpm) Hasil
100-200 Tidak terbentuk mikroemulsi
750 Mikroemulsi yang terbentuk jenih dan transparan
31
UIN Syarif Hidayatullah Jakarta
4.1.2 Optimasi Formula Mikroemulsi dengan Variasi Konsentrasi
Optimasi formula mikroemulsi dilakukan dengan variasi konsentrasi tetapi
persen fase minyak dihitung berdasarkan perbandingan campuran minyak yang
paling besar kemampuan mensolubilisasi testosteron undekanoat yaitu formula 2
(20 : 8 : 41). Besarnya perbandingan lalu dijadikan dalam bentuk 100% sehingga
didapatkan pesentase masing-masing yaitu 12% untuk minyak jarak, 29% untuk
isopropil miristat dan 59% untuk benzil benzoat. Persentase ini digunakan untuk
menghitung jumlah masing-masing minyak dari jumlah minyak yang dibutuhkan
dalam pembuatan mikroemulsi.
Hasil optimasi formula digambarkan dengan digram fase pseudoterner.
Diagram fase pseudoterner dibaut dengan komposisi: A. Surfaktan; Tween 80, B.
Fase minyak; minyak jarak, IPM, benzil benzoat, dan C. air. Diagram fase
pseudoterner dapat dilihat pada Gambar 4.1.
60 70 80 90 100
Gambar 4.1. Diagram fase pseudoterner
Keterangan: Surfaktan (Tween 80) + Minyak (benzil benzoat + IPM + minyak jarak) + Air dengan perbandingan konsentrasi benzil benzoate : IPM : minyak jarak =
41:20:8