xvii INTISARI
Penelitian tentang optimasi formula sediaan krim sunscreen ekstrak kering polifenol teh hijau dengan asam stearat dan Virgin Coconut Oil (VCO) sebagai fase minyak dilakukan untuk mengetahui konsentrasi polifenol teh hijau yang memberikan nilai SPF yang dapat diterima sebagai sunscreen pada penelitian ini, mengetahui dominasi antara asam stearat, VCO, dan interaksinya dalam mempengaruhi sifat fisik dan stabilitas krim sunscreen, serta menemukan area komposisi optimum asam stearat dan VCO yang menghasilkan krim sunscreen dengan sifat fisik dan stabilitas yang baik.
Penelitian ini merupakan penelitian eksperimental dengan desain penelitian secara desain faktorial dua faktor yaitu asam stearat-VCO dan dua level yaitu level tinggi-level rendah. Zat aktif dalam formula krim sunscreen ini adalah polifenol teh hijau. Optimasi dilakukan terhadap sifat fisik krim (daya sebar, viskositas) dan stabilitas krim (pergeseran viskositas) selama penyimpanan 1 bulan. Teknik analisis statistik yang digunakan adalah Yate’s treatment dengan taraf kepercayaan 95%.
xviii ABSTRACT
The aims of formula optimization of green tea polyphenols dry extract sunscreen cream with stearic acid and VCO as the oil phase were to determine the concentration of green tea polyphenols which showed SPF value that can be accepted as sunscreen, to determine the dominant factor among stearic acid, VCO, and its interaction on the physical properties and physical stability of cream, and to determine the optimum composition area of stearic acid and VCO which has good physical properties of cream.
This study was experimental research with two factor stearic acid-VCO and two level high level-low level factorial design. The active ingredient of the formula were green tea polyphenols. The formula were optimized on their physical characteristics (spreadability, viscosity) and their physical stability (viscosity shift over one month storage). The data were analyzed statistically using Yate’s treatment with 95% level of confidence.
The results showed that green tea polyphenols 18,1 mg % had SPF value that can be accepted as sunscreen (5,874). Stearic acid was dominant on determining spreadability, viscosity, and viscosity shift. The superimposed contour plot showed the optimum area of spreadability, viscosity, and viscosity shift. The area was estimated as optimum formula of sunscreen cream on the level studied.
Keywords : green tea polyphenols extract, stearic acid, VCO, factorial design
i
OPTIMASI FORMULA SEDIAAN KRIM SUNSCREEN EKSTRAK KERING POLIFENOL TEH HIJAU (Camellia sinensis L.) DENGAN ASAM
STEARAT DAN VIRGIN COCONUT OIL (VCO) SEBAGAI FASE MINYAK : APLIKASI DESAIN FAKTORIAL
HALAMAN SAMPUL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh:
Lorentius Agung Prasetya NIM : 048114017
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
OPTIMASI FORMULA SEDIAAN KRIM SUNSCREEN EKSTRAK KERING POLIFENOL TEH HIJAU (Camellia sinensis L.) DENGAN ASAM
STEARAT DAN VIRGIN COCONUT OIL (VCO) SEBAGAI FASE MINYAK : APLIKASI DESAIN FAKTORIAL
HALAMAN JUDUL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh:
Lorentius Agung Prasetya NIM : 048114017
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2008
iii Skripsi
OPTIMASI FORMULA SEDIAAN KRIM SUNSCREEN EKSTRAK KERING POLIFENOL TEH HIJAU (Camellia sinensis L.) DENGAN ASA
STEARAT DAN VIRGIN COCONUT OIL (VCO) SEBAGAI FASE MINYAK : APLIKASI DESAIN FAKTORIAL
HALAMAN PERSETUJUAN PEMBIMBING
Yang diajukan oleh: Lorentius Agung Prasetya
NIM : 048114017
telah disetujui oleh
Pembimbing
iv
Pengesahan Skripsi Berjudul
OPTIMASI FORMULA SEDIAAN KRIM SUNSCREEN EKSTRAK KERING POLIFENOL TEH HIJAU (Camellia sinensis L.) DENGAN ASAM
STEARAT DAN VIRGIN COCONUT OIL (VCO) SEBAGAI FASE MINYAK : APLIKASI DESAIN FAKTORIAL
HALAMAN PENGESAHAN
Oleh :
Lorentius Agung Praseya NIM : 048114017
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma pada tanggal : 22 Januari 2008
Mengetahui
Fakultas Farmasi Universitas Sanata Dharma
Dekan
(Rita Suhadi, M.Si., Apt) Pembimbing :
(C.M. Ratna Rini Nastiti, S.Si., Apt)
Panitia Penguji :
Tanda Tangan 1. C.M. Ratna Rini Nastiti, S.Si., Apt ... 2. Sri Hartati Yuliani, M.Si., Apt ... 3. Agatha Budi Susiana Lestari, M.Si., Apt ...
v
HALAMAN PERSEMBAHAN
Kita tidak bisa menjadi bijaksana dengan kebijaksanaan
orang lain, tetapi kita bisa berpengetahuan dengan
pengetahuan orang lain
- Michel De Montaigne-
“Serahkanlah perbuatanmu kepada TUHAN,
maka terlaksanalah segala rencanamu.”
(Amsal 16 : 3)
Karya ini kupersembahkan untuk orang-orang yang
kukasihi
”Jesus Christ”
Ayah, Ibu, Kakak, Adik,
Teman-teman Angkatan 2004,
vi
PERNYATAAN PERSETUJUAN PUBLIKASI
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Lorentius Agung Prasetya
Nomor Mahasiswa : 048114017
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
OPTIMASI FORMULA SEDIAAN KRIM SUNSCREEN EKSTRAK KERING
POLIFENOL TEH HIJAU (Camellia sinensis L.) DENGAN ASAM STEARAT
DAN VIRGIN COCONUT OIL (VCO) SEBAGAI FASE MINYAK : APLIKASI
DESAIN FAKTORIAL
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 22 Januari 2008
Yang menyatakan
(Lorentius Agung Prasetya)
vii PRAKATA
Puji Syukur kepada Tuhan Yang Maha Pengasih dan Penyayang atas
semua berkat dan penyertaan-Nya kepada penulis, sehingga penulis dapat
menyelesaikan laporan akhir ini dengan baik. Laporan akhir ini disusun untuk
memenuhi salah satu persyaratan untuk memperoleh gelar Sarjana Strata Satu
Program Studi Ilmu Farmasi (S.Farm).
Penulis banyak mengalami kesulitan-kesulitan dan masalah dalam
menyelesaikan laporan akhir ini. Tetapi dengan adanya bantuan dari berbagai
pihak, akhirnya penulis dapat menyelesaikan laporan akhir ini. Oleh karena itu
dengan segala kerendahan hati penulis ingin mengucapkan terimakasih atas segala
bantuan yang telah diberikan kepada :
1. “Jesus Christ” for Your LOVE.
2. Rita Suhadi, M.Si., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta.
3. C.M. Ratna Rini Nastiti, S.Si., Apt., selaku dosen pembimbing yang telah
memberikan bimbingan dan pengarahan kepada penulis.
4. Rini Dwiastuti, S.Si., Apt., selaku Dosen yang banyak membantu
terlaksananya penelitian.
5. Sri Hartati Yuliani, M.Si., Apt., selaku dosen penguji yang telah menguji
sekaligus memberi kritik dan saran yang membangun bagi penulis.
6. Agatha Budi Susiana Lestari, M.Si., Apt, selaku dosen penguji atas
viii
7. Romo Drs. Petrus Sunu Hardiyanta, S.J., S.Si. atas masukan yang diberikan.
8. Ayah, ibu, kakak, dan adik atas dukungan dan cinta kasihnya.
9. Ayu, Rudi, Dian ”Sapi”, Desi, Silvia “Cipi”, Dian “DK”, dan Fadjar atas
bantuan, dukungan, dan pertemanan kita.
10.Teman-teman proyek penelitian teh, Dian, Yoyo, Rinta, Ika, Dona, Resty,
Selvi, Tere, dan Feri, atas kerjasama dan kebersamaannya.
11.Teman-teman proyek penelitian wortel dan alga atas kebersamaannya di
laboratorium.
12.Semua anak-anak kost, Theo, Agung, Andri, Frenky, Hendro, dll., untuk
dukungannya.
13.Teman-teman angkatan 2004 terutama kelompok A atas suka duka bersama
dalam praktikum.
14.Pak Musrifin, Mas Agung, Mas Iswandi, Mas Ottok, serta laboran-laboran
yang lain atas bantuannya selama penulis menyelesaikan laporan akhir.
15.Semua pihak yang tidak dapat disebutkan satu persatu yang telah membantu
penulis dalam menyelesaikan laporan akhir ini.
Penulis menyadari bahwa dalam penulisan laporan akhir ini banyak
kesalahan dan kekurangan mengingat keterbatasan kemampuan dan pengetahuan
penulis. Untuk itu penulis mengharapkan saran dan kritik yang membangun dari
semua pihak. Akhir kata semoga laporan ini dapat berguna bagi pembaca
Penulis
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 22 Januari 2008
Penulis
x DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ...v
PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA... vii
PERNYATAAN KEASLIAN KARYA ... ix
DAFTAR ISI...x
DAFTAR TABEL... xiv
DAFTAR GAMBAR ...xv
DAFTAR LAMPIRAN... xvi
INTISARI ... xvii
ABSTRACT... xviii
BAB I. PENGANTAR...1
A. Latar Belakang ...1
B. Perumusan Masalah...3
C. Keaslian Karya ...4
D. Manfaat Penelitian ...4
E. Tujuan Penelitian...4
BAB II. PENELAAHAN PUSTAKA ...6
xi
A. Teh (Camellia sinensis L.) ...6
1. Deskripsi ...6
2. Kandungan kimia teh hijau ...6
3. Manfaat teh hijau ...7
B. Polifenol Teh ...7
C. Ekstrak...8
D. Ekstraksi...9
E. Formulasi ...9
1. Krim ...9
2. Emulgator sabun ...10
3. Asam stearat...10
4. Virgin Coconut Oil ( VCO )...11
F. Sunscreen...11
G. Sun Protection Factor ( SPF )...11
H. Spektrofotometri Ultraviolet ...12
I. Uji Sifat Fisik...13
1. Daya Sebar ...13
2. Viskositas ...14
J. Metode Desain Faktorial ...14
K. Landasan Teori...16
L. Hipotesis ...17
BAB III. METODOLOGI PENELITIAN ...18
xii
B. Variabel Penelitian dan Definisi Operasional ...18
a. Variabel penelitian ...18
b. Definisi operasional ...18
C. Bahan dan Alat ...20
D. Tata Cara Penelitian ...21
1. Penetapan kadar air serbuk teh hijau ...21
2. Ekstraksi polifenol teh hijau ...21
2. Penetapan kadar polifenol dalam ekstrak kering polifenol teh hijau ...22
3. Penentuan nilai SPF secara in vitro...24
4. Optimasi formula krim sunscreen...26
5. Uji sifat fisik dan stabilitas fisik krim sunscreen...28
6. Pengujian tipe krim sunscreen...29
7. Subjective assessment...29
E. Analisis Data dan Optimasi ...29
BAB IV. HASIL DAN PEMBAHASAN ...31
A. Penetapan Kadar Air Serbuk Teh Hijau...31
B. Ekstraksi Polifenol Teh Hijau ...32
B. Penetapan Kadar Polifenol dalam Ekstrak Kering Polifenol Teh Hijau ...34
C. Penentuan Nilai SPF secara In Vitro...37
D. Formulasi ...40
E. Pengujian Tipe Krim ...41
F. Sifat Fisik dan Stabilitas Krim Sunscreen...42
1. Daya sebar...43
xiii
2. Viskositas ...45
3. Pergeseran viskositas ...47
G. Optimasi Formula ...49
H. Subjective Assessment...53
BAB V. KESIMPULAN DAN SARAN ...54
A. Kesimpulan ...54
B. Saran...54
DAFTAR PUSTAKA ...56
LAMPIRAN...59
xiv
DAFTAR TABEL
Tabel I. Kategori nilai SPF ... 12
Tabel II. Rancangan Percobaan desain faktorial dua faktor dan dua level ... 15
Tabel III. Percobaan Desain Faktorial ... 27
Tabel IV. Hasil penetapan kadar air serbuk teh hijau ... 32
Tabel V. Hasil pengukuran absorbansi senyawa hasil reaksi kolorimetri seri kurva baku standar kuersetin... 35
Tabel VI. Hasil perhitungan kadar polifenol dalam ekstrak kering polifenol teh hijau... 37
Tabel VII. Hasil pengukuran SPF in vitro... 39
Tabel VIII. Hasil pengukuran sifat fisik dan stabilitas krim sunscreen...42
Tabel IX. Efek asam stearat, VCO, dan interaksi keduanya dalam menentukan sifat fisik krim sunscreen... 43
Tabel X. Hasil Perhitungan Yate’s treatment pada respon daya sebar ... 44
Tabel XI. Hasil Perhitungan Yate’s treatment pada respon viskositas ... 46
Tabel XII. Hasil Perhitungan Yate’s treatment pada respon pergeseran viskositas... 48
Tabel XIII. Tingkat penerimaan konsumen terhadap krim sunscreen...53
xv
DAFTAR GAMBAR
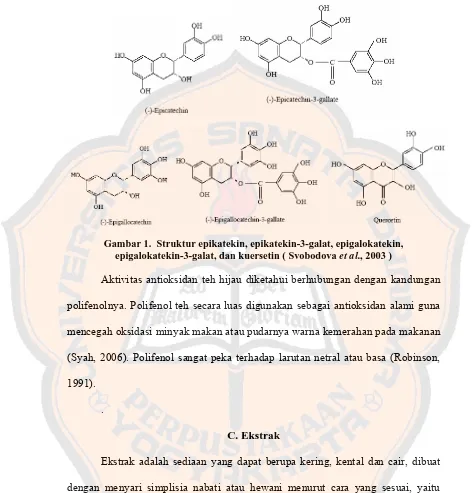
Gambar 1. Struktur epikatekin, epikatekin-3-galat, epigalokatekin,
epigalokatekin-3-galat , dan kuersetin ... 8
Gambar 2. Operating time kuersetin dengan metode Folin-Ciocalteu ... 34
Gambar 3. Panjang gelombang serapan maksimum kuersetin dengan metode Folin-Ciocalteu ... 35
Gambar 4. Hasil scanning spektraUV polifenol teh hijau ... 38
Gambar 5. Struktur epikatekin, epikatekin-3-galat, epigalokatekin, dan epigalokatekin-3-galat dengan sistem kromofor dan gugus auksokrom... 38
Gambar 6. Hasil pengujian tipe krim sunscreen dengan metilen blue... 41
Gambar 7. Hubungan VCO (a) dan asam stearat (b) terhadap daya sebar krim sunscreen... 43
Gambar 8. Hubungan VCO (a) dan asam stearat (b) terhadap viskositas krim sunscreen... 45
Gambar 9. Hubungan VCO (a) dan asam stearat (b) terhadap pergeseran viskositas krim sunscreen... 48
Gambar 10. Contour plot daya sebar krim sunscreen... 50
Gambar 11. Contour plot viskositas krim sunscreen... 51
Gambar 12. Contour plot pergeseran viskositas krim sunscreen... 52
xvi
DAFTAR LAMPIRAN
Lampiran 1. Penetapan kadar air serbuk teh hijau ... 59
Lampiran 2. Penetapan kadar polifenol dalam ekstrak polifenol teh hijau... 61
Lampiran 3. Data SPF polifenol teh hijau... 63
Lampiran 4. Penimbangan, notasi, dan formula desain faktorial... 65
Lampiran 5. Data sifat fisik dan stabilitas krim sunscreen... 66
Lampiran 6. Perhitungan efek sifat fisik dan stabilitas... 68
Lampiran 7. Persamaan regresi... 70
Lampiran 8. Kuesioner subjective assessment... 77
Lampiran 9. Yate’s Treatment... 79
Lampiran 10. Dokumentasi... 85
xvii INTISARI
Penelitian tentang optimasi formula sediaan krim sunscreen ekstrak kering polifenol teh hijau dengan asam stearat dan Virgin Coconut Oil (VCO) sebagai fase minyak dilakukan untuk mengetahui konsentrasi polifenol teh hijau yang memberikan nilai SPF yang dapat diterima sebagai sunscreen pada penelitian ini, mengetahui dominasi antara asam stearat, VCO, dan interaksinya dalam mempengaruhi sifat fisik dan stabilitas krim sunscreen, serta menemukan area komposisi optimum asam stearat dan VCO yang menghasilkan krim sunscreen dengan sifat fisik dan stabilitas yang baik.
Penelitian ini merupakan penelitian eksperimental dengan desain penelitian secara desain faktorial dua faktor yaitu asam stearat-VCO dan dua level yaitu level tinggi-level rendah. Zat aktif dalam formula krim sunscreen ini adalah polifenol teh hijau. Optimasi dilakukan terhadap sifat fisik krim (daya sebar, viskositas) dan stabilitas krim (pergeseran viskositas) selama penyimpanan 1 bulan. Teknik analisis statistik yang digunakan adalah Yate’s treatment dengan taraf kepercayaan 95%.
Diperoleh hasil bahwa polifenol teh hijau dengan konsentrasi 18,1 mg % memberikan SPF yang dapat diterima sebagai sunscreen (5,874). Asam stearat memberikan efek yang dominan dalam menentukan daya sebar, viskositas, dan pergeseran viskositas. Berdasarkan superimposed contour plot dapat diperoleh area optimum untuk daya sebar, viskositas, dan pergeseran viskositas yang diperkirakan sebagai formula optimum krim sunscreen pada level yang diteliti.
xviii ABSTRACT
The aims of formula optimization of green tea polyphenols dry extract sunscreen cream with stearic acid and VCO as the oil phase were to determine the concentration of green tea polyphenols which showed SPF value that can be accepted as sunscreen, to determine the dominant factor among stearic acid, VCO, and its interaction on the physical properties and physical stability of cream, and to determine the optimum composition area of stearic acid and VCO which has good physical properties of cream.
This study was experimental research with two factor stearic acid-VCO and two level high level-low level factorial design. The active ingredient of the formula were green tea polyphenols. The formula were optimized on their physical characteristics (spreadability, viscosity) and their physical stability (viscosity shift over one month storage). The data were analyzed statistically using Yate’s treatment with 95% level of confidence.
The results showed that green tea polyphenols 18,1 mg % had SPF value that can be accepted as sunscreen (5,874). Stearic acid was dominant on determining spreadability, viscosity, and viscosity shift. The superimposed contour plot showed the optimum area of spreadability, viscosity, and viscosity shift. The area was estimated as optimum formula of sunscreen cream on the level studied.
Keywords : green tea polyphenols extract, stearic acid, VCO, factorial design
1
BAB I. PENGANTAR PENGANTAR
A. Latar Belakang
Paparan sinar matahari secara kronik khususnya sinar ultraviolet (UV)
dapat menyebabkan terjadinya eritema, edema, pembentukan sel sunburn,
hiperplasia, penekanan sistem imun, kerusakan DNA, penuaan kulit (photoaging)
seperti kerut serta kehilangan elastisitas, dan melanogenesis pada kulit manusia.
Saat ini, kejadian kerusakan kulit terutama kanker kulit dan malignant melanoma
pada manusia akibat paparan UV semakin banyak dilaporkan (Svobodova,
Psotova, dan Walternova, 2003).
Salah satu cara mencegah terjadinya kerusakan kulit akibat radiasi UV
adalah penggunaan sediaan sunscreen. Bahan sunscreen adalah senyawa kimia
yang menyerap dan atau memantulkan radiasi sehingga melemahkan energi UV
sebelum terpenetrasi ke dalam kulit (Stanfield, 2003). Pada umumnya, sediaan
sunscreen digunakan dengan cara dioleskan pada permukaan kulit, terutama
wajah.
Sediaan sunscreen dapat mengandung bahan fotoprotektif baik fisik,
maupun kimia. Bahan fotoprotektif fisik seperti titanium dioksida (TiO2) dan seng
oksida bekerja dengan cara memantulkan atau menghamburkan sinar UV
sedangkan bahan fotoprotektif kimia seperti p-amino benzoic acid (PABA), ester
PABA, sinamat, salisilat, antranilat, oksibenzon, benzofenon, serta
senyawa-senyawa fenolik bekerja dengan cara mengabsorbsi sinar UV sehingga tidak
caffeic acid, ferulic acid, kuersetin, apigenin, genistein, carnosic acid, silimarin,
polifenol teh, dan tanin (Svobodova et al., 2003).
Teh hijau (Camellia sinensis) telah diketahui mengandung
senyawa-senyawa fenolik seperti epikatekin, epikatekin-3-galat, epigalokatekin, dan
epigalokatekin-3-galat. Keberadaan senyawa fenolik dalam teh digambarkan
sebagai suatu fenol yang mempunyai gugus kromofor dan auksokrom sehingga
dapat menyerap radiasi UV (Svobodova et al., 2003).
Sediaan sunscreen banyak dikembangkan dalam bentuk krim dan lotion.
Krim adalah bentuk sediaan setengah padat yang mengandung satu atau lebih
bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai (Anonim,
1995). Vanishing cream mempunyai keuntungan yaitu mudah dan nyaman
digunakan, dapat menyebar dengan baik, serta dapat dicuci dengan air. Pada
penelitian ini, krim yang dibuat termasuk tipe minyak dalam air, dengan asam
stearat dan Virgin Coconut Oil (VCO) sebagai fase minyak.
Efikasi dan penerimaan pasien terhadap sediaan dipengaruhi oleh sifat
fisik sediaan sehingga diperlukan sediaan yang mempunyai sifat fisik yang baik.
Krim biasanya menggunakan asam stearat sebagai fase minyak. Asam stearat
dalam sediaan krim dapat mengkristal membentuk nongreasy film serta memberi
kenampakan produk yang menarik (Wilkinson dan Moore, 1982). Saat dipanaskan
hingga di atas titik lelehnya (≥54°C) asam stearat meleleh dan saat pendinginan
partikel asam stearat saling berikatan kembali membentuk struktur yang kaku.
Krim tipe stearat dapat mengalami pemadatan (gelation) sehingga diperlukan
penambahan minyak mineral untuk memperbaiki sifat tersebut (Strianse, 1957).
VCO merupakan minyak mineral yang dapat berfungsi sebagai emollient
yang baik untuk sediaan kosmetik. Pada suhu ruang, VCO berwujud cair dan tidak
berwarna (Anonim, 2007). VCO yang ditambahkan ke dalam vanishing cream
basis asam stearat dapat membuat krim lebih plastis dan lebih lembut sehingga
dapat meningkatkan penerimaan konsumen. Asam stearat dan VCO mempunyai
sifat yang berbeda sehingga mempunyai potensi mempengaruhi sifat fisik dan
stabilitas sediaan krim. Oleh karena itu perlu dilakukan penelitian tentang
pengaruh asam stearat dan VCO terhadap sifat fisik dan stabilitas krim.
Metode yang digunakan pada penelitian ini adalah metode desain faktorial.
Metode desain faktorial dapat digunakan untuk mengetahui faktor yang paling
berpengaruh terhadap sifat fisik dan stabilitas dan adakah interaksi antara kedua
faktor tersebut. Selain itu desain faktorial dapat digunakan untuk memprediksi
area komposisi antara asam stearat dan VCO yang menghasilkan krim sunscreen
dengan sifat fisik dan stabilitas yang baik.
B. Perumusan Masalah Permasalahan yang akan diteliti adalah:
1. Berapakah konsentrasi polifenol teh hijau yang dapat memberikan nilai
SPF yang dapat diterima sebagai sunscreen dalam penelitian ini ?
2. Di antara asam stearat, VCO, dan interaksinya, faktor manakah yang
dominan dalam menentukan sifat fisik (daya sebar, viskositas) dan
stabilitas (pergeseran viskositas) krim sunscreen ekstrak kering polifenol
3. Apakah dapat ditemukan area komposisi optimum asam stearat dan VCO
pada superimposed contour plot yang diprediksi sebagai formula optimum
sediaan krim sunscreen ekstrak kering polifenol teh hijau?
C. Keaslian Karya
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian tentang
optimasi formula sediaan krim sunscreen ekstrak kering polifenol teh hijau
(Camellia sinensis L.) dengan asam stearat dan VCO sebagai fase minyak belum
pernah dilakukan.
D. Manfaat Penelitian
Secara teoritis penelitian ini menambah informasi bagi ilmu pengetahuan,
khususnya dalam bidang kefarmasian mengenai aplikasi desain faktorial pada
proses pembuatan krim sunscreen. Secara praktis penelitian ini bermanfaat untuk
mengetahui komposisi asam stearat dan VCO yang menghasilkan krim sunscreen
ekstrak kering polifenol teh hijau dengan sifat fisik dan stabilitas yang baik
E. Tujuan Penelitian Tujuan dari penelitian ini adalah :
1. Untuk mengetahui konsentrasi polifenol teh hijau yang dapat memberikan
nilai SPF yang dapat diterima sebagai sunscreen dalam penelitian ini.
2. Untuk mengetahui dominasi antara asam stearat, VCO, dan interaksi
keduanya dalam mempengaruhi sifat fisik (daya sebar, viskositas) dan
stabilitas (pergeseran viskositas) krim sunscreen ekstrak kering polifenol
teh hijau.
3. Mengetahui area komposisi optimum asam stearat dan VCO pada
superimposed contour plot yang diprediksi sebagai formula optimum
6
BAB II. PENELAAHAN PUSTAKA PENELAAHAN PUSTAKA
A. Teh (Camellia sinensis L.) 1. Deskripsi
Tanaman teh merupakan tanaman semak dengan tinggi 1-2 m, mempunyai
batang tegak, berkayu, bercabang-cabang, ujung ranting dan daun muda berambut
halus. Daun tunggal, bertangkai pendek, letak berseling, helai daun kaku seperti
kulit tipis, bentuknya elips memanjang, ujung dan pangkal runcing, tepi bergerigi
halus, pertulangan menyirip, panjang 6-18 cm, lebar 2-6 cm, warna hijau, dan
permukaan mengkilap. Tanaman ini mempunyai bunga di ketiak daun, tunggal
atau beberapa bunga bergabung menjadi satu, berkelamin dua, garis tengah 3-4
cm, warnanya putih cerah dengan kepala sari berwarna kuning (Arisandi dan
Andriani, 2006).
2. Kandungan kimia teh hijau
Daun teh mempunyai komposisi yang kompleks. Daun teh mengandung
30-40% polifenol yang sebagian besar merupakan katekin. Di dalam teh terdapat
beberapa jenis katekin, yaitu epikatekin (EC), epikatekin galat (ECG),
epigallokatekin (EGC), epigalokatekin galat (EGCG), gallokatekin, dan katekin.
Senyawa epigalokatekin galat merupakan kandungan terbesar di dalam teh hijau
(Syah, 2006).
3. Manfaat teh hijau
Beberapa manfaat teh antara lain sebagai antikanker, antimikroba,
antidiabetes, antioksidan, dan menghambat kerusakan DNA yang diinduksi oleh
radiasi UV (Syah, 2006; Svobodova et al., 2003). EGCG merupakan komponen
aktif teh hijau yang antara lain bermanfaat sebagai antihipertensi, antioksidan,
antikarsinogenesis, antikanker, dan melindungi kulit dari sinar UV (Syah, 2006).
B. Polifenol Teh
Teh dapat dikelompokkan menjadi tiga jenis, yaitu teh hijau, teh hitam,
dan teh hitam. Teh hijau dibuat melalui inaktivasi enzim polifenol oksidase
melalui pemanasan atau penguapan. Teh hitam dibuat melalui proses oksidasi
dengan katalis polifenol oksidase, sedangkan teh oolong diproses melalui
pemanasan dalam waktu singkat setelah penggulungan (Syah, 2006).
Polifenol teh yang terdapat pada teh hitam dan teh hijau dikenal sebagai
epikatekin atau derivat epikatekin. Epikatekin yang terdapat pada teh hijau, antara
lain epikatekin (EC), epikatekin-3-galat, epigalokatekin (EGC), dan
epigalokatekin 3 galat (EGCG) (Svobodova et al., 2003). Teh juga mengandung
Gambar 1. Struktur epikatekin, epikatekin-3-galat, epigalokatekin, epigalokatekin-3-galat, dan kuersetin ( Svobodova et al., 2003 )
Aktivitas antioksidan teh hijau diketahui berhubungan dengan kandungan
polifenolnya. Polifenol teh secara luas digunakan sebagai antioksidan alami guna
mencegah oksidasi minyak makan atau pudarnya warna kemerahan pada makanan
(Syah, 2006). Polifenol sangat peka terhadap larutan netral atau basa (Robinson,
1991).
.
C. Ekstrak
Ekstrak adalah sediaan yang dapat berupa kering, kental dan cair, dibuat
dengan menyari simplisia nabati atau hewani menurut cara yang sesuai, yaitu
maserasi, perkolasi, atau penyeduhan dengan air mendidih. Pembuatan ekstrak
dimaksudkan agar zat berkhasiat yang terdapat dalam simplisia terdapat dalam
kadar yang tinggi sehingga memudahkan untuk pengaturan dosis. Ekstrak kering
harus mudah digerus menjadi serbuk (Anief, 2000).
D. Ekstraksi
Ekstraksi atau penyarian adalah kegiatan penarikan zat yang dapat larut
dari bahan yang tidak dapat larut dengan pelarut cair. Proses penyarian dipisahkan
menjadi : pembuatan serbuk, pembasahan, penyarian, dan pemekatan. Secara
umum, penyarian dilakukan secara infundasi, maserasi, perkolasi, dan destilasi
uap (Anonim, 1986).
Maserasi merupakan cara ekstraksi zat aktif menggunakan cairan
pengekstraksi dengan penggojogan atau pengadukan pada suhu ruangan. Maserasi
kinetik merupakan metode maserasi yang dilakukan pada suhu ruangan dan
mengalami pengadukan secara konstan. Maserasi merupakan metode yang paling
banyak digunakan dalam proses ekstraksi. Metode ini mempunyai keuntungan
yaitu sampel yang dibutuhkan kecil serta dapat dilakukan dengan cara yang sama
seperti teknik dan produksi batch (List dan Schmidt, 1989).
E. Formulasi 1. Krim
Krim adalah bentuk sediaan setengah padat yang mengandung satu atau
lebih bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai (Anonim,
1995 ). Krim dapat bertipe air dalam minyak (A/M) atau minyak dalam air (M/A).
Tipe A/M tidak larut air dan tidak dapat dicuci dengan air, sedangkan tipe M/A
dapat bercampur dengan air, dapat dicuci dengan air, dan tidak berminyak (Allen,
Formula tradisional untuk vanishing cream didasarkan pada jumlah asam
stearat yang besar sebagai fase minyak yang dapat melunak pada suhu tubuh dan
mengkristal pada bentuk yang sesuai sehingga tidak terlihat dalam penggunaan
dan membentuk film yang tidak berminyak. Hal ini merupakan salah satu daya
tarik pada kenampakan produk. Emulgator yang berperan dalam proses tersebut
adalah sabun yang terbentuk secara “in situ“ dengan menambahkan basa yang
cukup untuk bereaksi dengan asam stearat (Wilkinson dan Moore, 1982).
2. Emulgator sabun
Sabun dapat digunakan sebagai emulgator yang sangat efektif
menghasilkan sediaan untuk penggunaan luar. Emulsi yang dihasilkan
mempunyai nilai pH relatif tinggi dan peka terhadap asam dan elektrolit.
Emulgator sabun terbentuk dari reaksi antara alkali, air kapur, atau amina dengan
asam lemak bebas pada fase minyak (Anonim, 1987).
3. Asam stearat
Asam stearat merupakan asam lemak yang terdiri dari campuran asam
stearat (C18H36O2) dan asam palmitat (C16H32O2), dengan kandungan asam stearat
tidak kurang dari 40% dan jumlah kedua asam tersebut tidak kurang dari 90%.
Asam stearat mempunyai bilangan penyabunan 200-220 dan titik leleh > 540 C. Dalam formulasi sediaan topikal, asam stearat berfungsi sebagai emulsifying agent
dan solubilizing agent (Allen, 2005).
4. Virgin Coconut Oil ( VCO )
Virgin Coconut Oil (VCO) merupakan minyak yang diproses dari buah
kelapa tanpa mengalami pemanasan. VCO mempunyai kenampakan bening serta
mengandung banyak asam laurat. VCO mengandung asam lemak rantai menengah
( Medium Chain Fatty Acid/ MCFA) (Timoti, 2005).
Manfaat VCO untuk kesehatan manusia antara lain, mengurangi/
menurunkan resiko kanker dan penyakit degeneratif, mencegah infeksi virus, dan
membantu mengontrol diabetes. Dalam bidang kosmetik, VCO biasa digunakan
dalam krim perawatan wajah (Surtiningsih, 2006).
F. Sunscreen
Sunscreen merupakan bahan kimia yang menyerap atau memantulkan
radiasi sehingga melemahkan energi ultraviolet sebelum terpenetrasi ke kulit
(Stanfield, 2003). Menurut Food and Drug Administration (1999), bahan aktif
sunscreen adalah bahan yang menyerap, memantulkan, atau menghamburkan
radiasi pada daerah UV dengan λ 290-400 nm.
G. Sun Protection Factor ( SPF )
SPF merupakan tingkat perlindungan produk sunscreen terhadap sinar
matahari yang dapat menyebabkan eritema (Stanfield, 2003). SPF merupakan
perbandingan Minimal Erythema Dose (MED) pada kulit manusia yang
Secara in vitro, SPF dapat dihitung berdasarkan persamaan SPF = 10A.
SPF menurut persamaan tersebut didapat dari nilai absorbansi pada panjang
gelombang tunggal, biasanya merupakan puncak absorbansi. Nilai SPF yang
dihasilkan umumnya tinggi, bahkan lebih tinggi daripada yang sebenarnya. Hal ini
disebabkan persamaan tersebut berlaku bila radiasi yang digunakan merupakan
sinar monokromatis, padahal sinar UV matahari merupakan radiasi polikromatis.
Hal ini dapat diatasi dengan memasukkan nilai area di bawah kurva dari grafik
rentang panjang gelombang λn-λ1 sehingga diperoleh persamaan sebagai berikut :
1 n
Area SPF
Log
λ − λ
= ………...(1)
λ1 = 290 nm
λn = panjang gelombang di atas 290 nm yang mempunyai absorbansi 0,05
(Petro, 1981)
Berdasarkan nilai SPF, sunscreen dapat dikelompokkan menjadi produk
proteksi minimal, sedang, ekstra, maksimal, dan ultra.
Tabel I. Kategori nilai SPF SPF Kategori
2 - < 12 Proteksi minimal 12 - < 30 Proteksi sedang 30 + Proteksi tinggi
(Anonim, 1999)
H. Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet merupakan anggota teknik spektroskopik
yang menggunakan sumber radiasi elektromagnetik ultraviolet dekat dengan
instrumen spektrofotometer. Analisis selalu melibatkan pembacaan serapan
radiasi elektronik oleh molekul, atau radiasi elektromagnetik yang diteruskan,
yang disebut serapan (A) tanpa satuan, dan transmitan dengan satuan persen (%
T). Suatu molekul dapat menyerap radiasi elektromagnetik jika mempunyai
kromofor, yaitu gugus penyerap dalam molekul. Molekul yang mengandung
kromofor disebut kromogen. Pada senyawa organik, dikenal pula gugus
auksokrom, yaitu gugus yang tidak menyerap radiasi namun jika terikat pada
kromofor dapat meningkatkan penyerapan oleh kromofor atau mengubah panjang
gelombang penyerapan (Mulja dan Suharman, 1995).
I. Uji Sifat Fisik 1. Daya Sebar
Daya sebar berhubungan dengan sudut kontak antara sediaan dengan
tempat aplikasinya yang mencerminkan kelicinan (lubricity) sediaan tersebut,
yang berhubungan langsung dengan koefisien gesekan. Daya sebar merupakan
karakteristik yang penting dari formulasi sediaan topikal dan bertanggungjawab
untuk ketepatan transfer dosis atau melepaskan bahan obatnya, dan kemudahan
penggunaannya (Garg, Deepika, Sanjay, dan Anil, 2002).
Untuk menilai daya sebar dari sediaan semisolid topikal, faktor-faktor
yang penting dipertimbangkan meliputi karakteristik formulasi, waktu dan
kecepatan shear selama pengolesan dan suhu tempat aplikasi. Kecepatan
penyebaran juga bergantung pada viskositas formulasi, kecepatan penguapan
2. Viskositas
Viskositas adalah suatu pernyataan tahanan dari suatu cairan untuk
mengalir maka makin tinggi viskositas akan makin besar tahanannya.
Penggolongan bahan menurut tipe aliran dan deformasinya dibagi menjadi dua
yaitu sistem Newton dan sistem non-Newton. Tipe alir plastik, pseudoplastik, dan
dilatant termasuk dalam sistem non-Newton (Martin, Swarbick, dan Cammarata,
1993).
J. Metode Desain Faktorial
Desain faktorial merupakan aplikasi persamaan regresi yaitu teknik untuk
memberikan model hubungan antara variabel respon dengan satu atau lebih
variabel bebas. Model yang diperoleh dari analisis tersebut berupa persamaan
matematika (Bolton, 1997). Desain faktorial dua level berarti ada dua faktor
(misal A dan B) yang masing-masing faktor diuji pada dua level yang berbeda,
yaitu level rendah dan level tinggi. Dengan desain faktorial dapat didesain suatu
percobaan untuk mengetahui faktor yang dominan berpengaruh secara signifikan
terhadap suatu respon (Bolton, 1997).
Optimasi campuran dua bahan (berarti ada dua faktor) dengan desain
faktorial (two level factorial design) dilakukan berdasarkan rumus:
Y = b0 + b1(A) + b2(B) + b12 (A)(B)………...(2)
Keterangan
Y = respon hasil atau sifat yang diamati, misalnya waktu alir
(A),(B) = level bagian A, bagian B
b0, b1, b2, b12 = koefisien, dapat dihitung dari hasil percobaan
Pada desain faktorial dua level dan dua faktor diperlukan empat percobaan
(2n =4, dengan 2 menunjukkan level dan n menunjukkan jumlah faktor), yaitu (1) A dan B masing-masing pada level rendah, (a) A pada level tinggi dan B pada
level rendah, (b) A pada level rendah dan B pada level tinggi, (ab) A dan B
masing- masing pada level tinggi. Dari rumus (1) dan data yang diperoleh dapat
dibuat contour plot suatu respon tertentu yang sangat berguna dalam memilih
kondisi yang optimum (Bolton, 1997).
Rancangan percobaan desain faktorial sebagai berikut:
Tabel II. Rancangan Percobaan desain faktorial dengan dua faktor dan dua level
Percobaan Faktor A Faktor B Interaksi
1 - - +
a + - -
b - + -
ab + + +
Keterangan:
Percobaan (1) = faktor A level rendah, faktor B rendah Percobaan a = faktor A level tinggi, faktor B rendah Percobaan b = faktor A level rendah, faktor B tinggi Percobaan ab = faktor A level tinggi, faktor B tinggi (-) = level rendah
(+) = level tinggi
Besarnya efek dapat dicari dengan menghitung selisih antara rata-rata
respon pada level tinggi dan rata-rata respon pada level rendah (Bolton, 1997).
Konsep perhitungannya sebagai berikut:
Efek faktor I =
(
) (
)
21 + − +a b ab
………...(2)
Efek faktor II =
(
) (
)
21 + − +b a ab
Efek faktor Interaksi =
(
) (
)
21 b a
ab+ − +
………...(4).
Dari metode desain faktorial, perhitungan efek ini dapat digunakan
untuk memperkirakan efek yang dominan dalam menentukan respon. Keuntungan
utama desain faktorial adalah bahwa metode ini memungkinkan untuk
mengidentifikasi efek masing- masing faktor, maupun efek interaksi antar faktor
(Muth, 1999).
Keuntungan metode desain faktorial antara lain :
1. Efisiensi yang tinggi
2. Dapat diperoleh informasi dari adanya interaksi yang beragam
3. Hasil percobaan dapat diaplikasikan pada rentang kondisi yang
lebar
Kerugian penggunaan metode desain faktorial :
1. Analisis statistik lebih kompleks
(Ostle, 1956)
K. Landasan Teori
Penggunaan sunscreen merupakan salah satu strategi untuk melindungi
kulit dari pengaruh radiasi sinar UV. Salah satu mekanisme kerja zat aktif
sunscreen adalah menyerap radiasi sinar UV. Teh hijau mengandung polifenol
yang mempunyai kromofor dan auksokrom yang terikat kromofor sehingga dapat
menyerap radiasi UV.
Penerimaan konsumen dipengaruhi oleh sifat fisik sediaan sehingga
diperlukan sediaan yang mempunyai sifat fisik yang baik. Bentuk sediaan yang
diteliti adalah krim sunscreen tipe minyak dalam air (vanishing cream).
Peningkatan konsistensi krim dapat dicapai dengan penggunaan fatty alcohol atau
asam lemak. Asam stearat merupakan asam lemak yang dapat mengkristal dan
membentuk krim dengan kenampakan yang menarik, namun penggunaan dalam
jumlah besar dapat mengakibatkan konsistensi krim sangat tinggi. Selain itu, krim
tipe stearat dapat mengalami pemadatan (gelation) sehingga diperlukan minyak
mineral untuk membuat krim lebih plastis. VCO merupakan minyak mineral yang
berfungsi sebagai emollient yang baik dalam sediaan krim. Pada suhu ruangan
VCO berwujud cair.
Asam stearat dan VCO mempunyai sifat yang berbeda sehingga berpotensi
mempengaruhi sifat fisik dan stabilitas krim. Dalam penelitian ini dilakukan
optimasi komposisi asam stearat dan VCO yang menghasilkan krim sunscreen
ekstrak kering polifenol teh hijau dengan sifat fisik dan stabilitas yang baik.
L. Hipotesis
Ada hubungan antara faktor (asam stearat, VCO, atau interaksinya)
dengan respon sifat fisik dan stabilitas krim sunscreen ekstrak kering polifenol teh
hijau. Hipotesis disusun berdasarkan penggunaan Yate’s treatment dalam analisis
18
BAB III. METODOLOGI PENELITIAN METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian ini termasuk dalam penelitian eksperimental eksploratif dengan
desain penelitian secara desain faktorial.
B. Variabel Penelitian dan Definisi Operasional a. Variabel penelitian
1.Variabel bebas dalam penelitian ini adalah level rendah dan level tinggi asam stearat dan VCO.
2.Variabel tergantung dalam penelitian ini adalah sifat fisik (daya sebar dan viskositas) dan stabilitas (persen pergeseran viskositas).
3.Variabel pengacau terkendali dalam penelitian ini adalah lama penyimpanan dan wadah penyimpanan.
b. Definisi operasional
1. Krim sunscreen ekstrak kering polifenol teh hijau adalah sediaan setengah padat yang berfungsi sebagai penyerap sinar UV yang dibuat dari
ekstrak kering polifenol teh hijau, fase air, dan fase minyak sesuai formula
yang ditentukan, dan dibuat sesuai prosedur pembuatan krim pada
penelitian ini.
2. Ekstrak kering polifenol teh hijau adalah hasil ekstraksi terhadap fase polar teh hijau menggunakan etil asetat yang diuapkan menjadi serbuk
kering.
3. Faktor adalah besaran yang mempengaruhi respon, dalam penelitian ini digunakan 2 faktor, yaitu asam stearat sebagai faktor A dan VCO sebagai
faktor B.
4. Level adalah nilai atau tetapan untuk faktor, dalam penelitian ini terdapat 2 level, yaitu level rendah dan level tinggi. Level rendah asam stearat
dinyatakan dalam jumlah bahan sebanyak 1 g dan level tinggi sebanyak 6
g. Level rendah VCO dinyatakan dalam jumlah bahan sebanyak 3 g dan
level tinggi sebanyak 10 g.
5. Respon adalah besaran yang diamati dalam penelitian ini yaitu daya sebar, viskositas, stabilitas krim yang digambarkan dari persen pergeseran
viskositas yang terjadi setelah satu bulan penyimpanan.
6. Efek adalah perubahan respon yang disebabkan variasi faktor dan level. Besarnya efek dapat dicari dengan menghitung selisih antara rata-rata
respon pada level rendah dan rata-rata pada level tinggi.
7. Contour plot adalah grafik yang merupakan hasil dari respon sifat fisik dan stabilitas krim sunscreen.
8. Superimposed contour plot adalah grafik area pertemuan yang memuat semua arsiran dalam contour plot yang diprediksikan sebagai area
9. Area optimum adalah area kondisi yang menghasilkan krim dengan daya sebar 5 sampai 7 cm, viskositas 50 sampai 65 d Pa.s, persen pergeseran
viskositas (setelah penyimpanan satu bulan) kurang dari 10 %.
C. Bahan dan Alat
Bahan yang digunakan pada penelitian ini adalah serbuk teh hijau yang
berasal dari salah satu produsen teh hijau di Wonosobo, metanol (teknis), metanol
(p.a Merck, Germany), reagen Karl Fischer (p.a Merck, Germany), kloroform
(teknis), etil asetat (teknis), etanol (teknis), akuades, asam stearat (farmasetis),
VCO (Virjint, PT. Vermindo International, Bekasi), setil alkohol (farmasetis),
asam sitrat (farmasetis), trietanolamin, metil paraben, aseton (p.a Merck,
Germany), Na2CO3 (p.a Merck, Germany), kuersetin (p.a Sigma Chem Co, USA),
dan reagen Folin-Ciocalteu (p.a Merck, Germany).
Alat yang digunakan pada penelitian ini adalah Karl Fischer Titrator
Mettler DL 18, timbangan elektrik, shaker, vakum evaporator, seperangkat alat
spektrofotometer UV-Vis Perkin Elmer Lambda 20., spektrofotometer UV
Genesys 10S, timbangan elektrik, vacuum rotary evaporator (Buchi), mikropipet
(Akura 825, Socorex), alat-alat gelas, Mixer (modifikasi Fakultas Farmasi USD),
waterbath, viscotester Rion-Japan VT 04, dan alat uji daya sebar.
D. Tata Cara Penelitian
1. Penetapan kadar air serbuk teh hijau
Penetapan kadar air serbuk teh hijau dilakukan dengan metode Karl
Fischer. Serbuk teh hijau ditimbang 1 g, ditambah 10 mL metanol, lalu didiamkan
selama 1 hari pada suhu kamar. Selanjutnya dilakukan pre-titrasi pada alat dan uji
kebocoran alat, hingga didapat angka drift 10-50. Standarisasi dilakukan dengan
cara menimbang spuit berisi akuades, kemudian sebanyak 1-2 tetes akuades
dimasukkan ke dalam beaker titrator. Bobot akhir akuades dan spuit injeksi
ditimbang. Selisih penimbangan merupakan bobot akuades yang diteteskan. Data
bobot akuades yang diteteskan kemudian dimasukkan ke dalam alat dan dilakukan
titrasi. Alat akan menghitung kesetaraan volume titran dengan bobot akuades.
Sebanyak 1 mL metanol (p.a) dimasukkan ke dalam beaker titrator kemudian
dilakukan titrasi. Hitung kadar air dalam blanko metanol. Sampel sebanyak 1 mL
dimasukkan beaker titrator, dititrasi, kemudian dihitung kadar airnya dengan
rumus:
Kadar air = 100%
) mg ( ditimbang yang
bobot
(mg) metanol blanko
air bobot )
mg (
x − ×
x = angka yang muncul pada alat
2. Ekstraksi polifenol teh hijau
Sebanyak 100 g serbuk teh dengan derajat halus 12/20 dimaserasi
menggunakan pelarut metanol 500 mL dengan bantuan shaker dengan kecepatan
vacuum rotary evaporator sampai volume 100 mL. Selanjutnya ditambahkan 100
mL kloroform dan 100 mL air. Lapisan atas (fase polar) dipisahkan, kemudian
dan diekstraksi dengan etil asetat 2 x 150 mL. Fase atas (etil asetat) dikumpulkan
kemudian diuapkan hingga kering (Nagayama et al., 2002).
2. Penetapan kadar polifenol dalam ekstrak kering polifenol teh hijau a. Larutan stok kuersetin 1 mg/mL
Sebanyak 0,05 g kuersetin standar dilarutkan dengan aseton 75 % dalam
labu ukur 50 mL kemudian diencerkan hingga tanda.
b. Penetapan operating time
Diambil sebanyak 4 mL larutan stok dan encerkan dengan aseton 75 %
dalam labu 10 mL hingga tanda. Sebanyak 0,5 mL larutan tersebut diambil dan
dimasukkan dalam labu ukur 50 mL. Tambahkan pereaksi Folin-Ciocalteu
sebanyak 2,5 mL dan biarkan selama 2 menit. Tambahkan 7,5 mL larutan Na2CO3
kemudian encerkan dengan akuades hingga tanda. Larutan divortex kemudian
absorbansi diukur pada panjang gelombang 726 nm selama 120 menit.
c. Penetapan panjang gelombang serapan maksimum
Diambil sebanyak 4 mL larutan stok dan encerkan dengan aseton 75 %
dalam labu 10 mL hingga tanda. Sebanyak 0,5 mL larutan tersebut diambil dan
dimasukkan dalam labu ukur 50 mL. Tambahkan pereaksi Folin-Ciocalteu
sebanyak 2,5 mL dan biarkan selama 2 menit. Tambahkan 7,5 mL larutan Na2CO3
kemudian encerkan dengan akuades hingga tanda. Larutan divortex selama 30
detik kemudian diinkubasi selama operating time kemudian disentrifuse dengan
kecepatan 4000 rpm selama 5 menit. Absorbansi larutan diukur pada panjang
gelombang 600-800 nm.
d. Penetapan kurva baku
Sebanyak 0,05 g kuersetin standar dilarutkan dengan aseton 75 % sampai
volume 50,0 mL. Buat seri konsentrasi kuersetin 0,2; 0,3; 0,4; 0,5; 0,6; dan 0,7
mg/mL menggunakan aseton 75%. Sebanyak 0,5 mL larutan tersebut diambil dan
dimasukkan dalam labu ukur 50 mL. Tambahkan pereaksi Folin-Ciocalteu
sebanyak 2,5 mL dan biarkan selama 2 menit. Tambahkan 7,5 mL larutan Na2CO3
kemudian encerkan dengan akuades hingga tanda. Larutan divortex selama 30
detik kemudian diinkubasi selama operating time kemudian disentrifuse dengan
kecepatan 4000 rpm selama 5 menit. Absorbansi larutan diukur pada panjang
gelombang serapan maksimum. Replikasi dilakukan sebanyak 3 kali.
e. Penetapan kadar polifenol dalam ekstrak kering polifenol teh hijau
Sebanyak 500 mg ekstrak kering polifenol teh hijau dimasukkan dalam
labu ukur 25 mL kemudian dilarutkan dengan aseton 75 % dan diencerkan hingga
tanda. Sebanyak 1 mL larutan tersebut diambil kemudian dimasukkan dalam labu
ukur 50 mL dan diencerkan dengan akuades hingga tanda. Ambil 0,5 mL larutan
tersebut dan masukkan dalam labu ukur 50 mL. Tambahkan pereaksi
Folin-Ciocalteu sebanyak 2,5 mL dan biarkan selama 2 menit. Tambahkan 7,5 mL
larutan Na2CO3 kemudian encerkan dengan akuades hingga tanda. Larutan
divortex selama 30 detik kemudian diinkubasi selama operating time kemudian
disentrifuse dengan kecepatan 4000 rpm selama 5 menit. Absorbansi larutan
sebanyak 6 kali. Kadar polifenol dalam sampel dihitung menggunakan persamaan
kurva baku sehingga diperoleh konsentrasi polifenol terhitung ekuivalen terhadap
kuersetin.
3. Penentuan nilai SPF secara in vitro a. Larutan stok polifenol teh hijau 30 mg %
Serbuk ekstrak kering polifenol teh hijau ditimbang setara dengan 15 mg
polifenol teh hijau kemudian dilarutkan dengan etanol 90 % dalam labu ukur 50
mL kemudian diencerkan hingga tanda.
b. Penentuan spektra UV ekstrak kering polifenol teh hijau
Diambil larutan stok polifenol teh hijau sebanyak 2 mL dan dimasukkan
dalam labu ukur 10 mL, encerkan dengan etanol 90 % hingga tanda. Spektra UV
larutan diperoleh dengan scanning absorbansi larutan pada panjang gelombang
250-400 nm.
b. Penentuan nilai SPF
Diambil larutan stok polifenol teh hijau sebanyak 2, 4, dan 6 mL dan
encerkan dengan etanol 90 % dalam labu ukur 10 mL sehingga diperoleh larutan
polifenol teh hijau dengan konsentrasi 6; 12; dan 18 mg %. Replikasi dilakukan
sebanyak 3 kali untuk tiap konsentrasi.
Absorbansi (A) masing-masing konsentrasi diukur tiap 5 nm pada rentang
panjang gelombang 290 nm hingga panjang gelombang tertentu di atas 290 nm
yang mempunyai nilai serapan 0,050. Dibuat kurva antara nilai absorbansi
terhadap panjang gelombang. Luas daerah di bawah kurva (AUC) antara dua
panjang gelombang yang berurutan dihitung dengan rumus :
[ AUC ] = [ ( )]
2 ) (
a p p Ap a p
A − + λ −λ −
Ap = absorbansi pada panjang gelombang yang lebih tinggi di antara dua
panjang gelombang yang berurutan
A(p-a) = absorbansi pada panjang gelombang yang lebih rendah di antara dua
panjang gelombang yang berurutan
p
λ = panjang gelombang yang lebih tinggi di antara dua panjang
gelombang berurutan
) (p−a
λ = panjang gelombang yang lebih rendah di antara dua panjang
gelombang berurutan
Seluruh luas daerah di bawah kurva absorbansi dapat dihitung dengan
menjumlahkan semua harga AUC. Harga Sun Protection Factor (SPF) dapat
dihitung dengan rumus :
Log SPF =
1 n AUC
λ −
λ ………...(3)
n
λ = panjang gelombang terbesar di antara panjang gelombang 290 nm
hingga di atas 290 nm yang mempunyai nilai absorbansi 0,050
1
λ = panjang gelombang terkecil ( 290 nm )
4. Optimasi formula krim sunscreen a. Formula Krim Sunscreen
Formula yang digunakan pada penelitian ini mengacu pada formula standar
sunscreen basis krim (Young, 1972) :
Antiviray 8,0
Stearic acid 1,7
Isopropyl myristate 6,0
Abracol PGS 3,5
Triethanolamine 0,8
Distilled water 80,0
Preservative one microspatula-full
Perfume one drop
Pada penelitian ini dilakukan modifikasi formula sehingga diperoleh
formula sebagai berikut :
Polifenol teh hijau 16,07 mg (terhitung ekuivalen terhadap kuersetin)
Asam stearat 1,7 g
VCO 6,0 g
Setil alkohol 3,5 g
Trietanolamin 0,8 g
Akuades 60,0 mL
Asam sitrat 0,5 g
Metil paraben 0,25 g
Perfume q.s
b. Pembuatan krim sunscreen ekstrak polifenol teh hijau
Tabel III. Percobaan Desain Faktorial Formula Komposisi
1 a b ab Polifenol teh hijau (mg)* 15,26 16,34 16,80 17,91
Asam stearat (g) 1 6 1 6
VCO (g) 3 3 10 10
Setil alkohol (g) 3,5 3,5 3,5 3,5
Trietanolamin (g) 0,8 0,8 0,8 0,8
Akuades (mL) 60 60 60 60
Metil paraben (g) 0,25 0,25 0,25 0,25
Asam sitrat (g) 0,5 0,5 0,5 0,5
Perfume q.s. q.s. q.s. q.s.
*Konsentrasi polifenol yang digunakan = 0,022 % b/b terhitung ekuivalen terhadap kuersetin
Asam stearat dan setil alkohol dilelehkan secara terpisah di atas waterbath,
kemudian dicampur dalam keadaan panas. Tambahkan VCO, trietanolamin, dan
metil paraben ke dalam campuran tersebut kemudian diaduk hingga merata.
Masukkan 2/3 bagian akuades ke dalam campuran tersebut dan dicampur
menggunakan mixer dengan kecepatan 300 rpm selama 15 menit. Asam sitrat
yang telah dilarutkan dalam 1/6 bagian akuades ditambahkan ke dalam campuran
sedikit demi sedikit sambil diaduk dengan mixer kecepatan 300 rpm selama 30
menit. Ekstrak kering polifenol teh hijau dilarutkan dalam sisa akuades yang
tersedia kemudian dimasukkan ke dalam campuran tersebut sambil terus diaduk
dengan mixer dengan kecepatan 300 rpm. pH sediaan diuji dengan indikator
5. Uji sifat fisik dan stabilitas fisik krim sunscreen a. Uji daya sebar
Uji daya sebar sediaan krim sunscreen ekstrak kering polifenol teh hijau
dilakukan 48 jam setelah pembuatan dengan cara : krim ditimbang seberat 1 gram,
diletakkan di tengah kaca bulat berskala. Di atas krim diletakkan kaca bulat lain
dan pemberat sehingga berat kaca bulat dan pemberat 125 gram, didiamkan
selama 1 menit, kemudian dicatat penyebarannya (Garg et al., 2002). Replikasi
dilakukan sebanyak 6 kali.
b. Uji Viskositas
Pengukuran viskositas menggunakan alat Viscotester Rion-Japan seri VT
04 dengan cara : krim dimasukkan dalam wadah dan dipasang pada portable
viscotester. Viskositas krim diketahui dengan mengamati gerakan jarum penunjuk
viskositas. Uji ini dilakukan dua kali, yaitu (1) 48 jam setelah krim dibuat dan (2)
setelah disimpan selama 1 bulan. Replikasi dilakukan sebanyak 6 kali (Melani,
Purwanti, dan Soeratri, 2005).
c. Uji Stabilitas
Stabilitas sediaan krim ditunjukkan dengan nilai pergeseran viskositas
yang dihitung dengan rumus :
| jam
48 viskositas
bulan 1 viskositas jam
48 viskositas |
viskositas pergeseran
% = − x 100%
6. Pengujian tipe krim sunscreen
Sebanyak 0,5 g krim sunscreen dimasukkan beaker glass dan diencerkan
dengan 2 mL akuades. Campuran diaduk kemudian ditambah 2 tetes metilen blue.
Warna campuran diamati. Bagian yang berwarna biru menunjukkan fase air
sedangkan bagian yang tidak berwarna merupakan fase minyak.
7. Subjective assessment
Subjective assessment dilakukan dengan membuat kuesioner untuk
memperoleh data tentang tingkat penerimaan konsumen terhadap formula krim
sunscreen ekstrak kering polifenol teh hijau. Kuesioner disebarkan kepada 30
responden. Hasil subjective assessment diinterpretasikan sebagai tingkat
penerimaan konsumen terhadap krim sunscreen ekstrak kering polifenol teh hijau.
E. Analisis Data dan Optimasi
Data yang terkumpul adalah data uji daya sebar, viskositas, dan
pergeseran viskositas. Dengan metode desain faktorial dapat dihitung besarnya
efek asam stearat, VCO, dan interaksinya sehingga dapat diketahui faktor yang
dominan dalam menentukan sifat fisik dan stabilitas. Area komposisi optimum
asam stearat dan VCO diperoleh dari penggabungan contour plot masing-masing
respon yang dikenal dengan superimposed contour plot. Area yang diperoleh
selanjutnya diprediksi sebagai area komposisi yang optimum terbatas pada level
Analisis statistik teknik Yate’s treatment dilakukan untuk mengetahui
signifikansi dari setiap faktor dan interaksi dalam mempengaruhi respon.
Berdasarkan analisis statistik ini, maka dapat ditentukan ada atau tidaknya
hubungan dari setiap faktor dan interaksi terhadap respon. Hal tersebut dapat
dilihat dari harga F hitung dan F tabel. Sebelumnya ditentukan hipotesis terlebih
dahulu, hipotesis alternatif (H1) menyatakan adanya regresi (hubungan) antara
faktor dengan respon, sedangkan H0 merupakan negasi dari H1 yang menyatakan
tidak adanya regresi (hubungan) antara faktor dengan respon. H1 diterima dan H0
ditolak bila harga F hitung lebih besar daripada harga F tabel yang berarti bahwa
faktor berpengaruh signifikan terhadap respon. F tabel diperoleh dari Fα
(numerator, denominator) dengan taraf kepercayaan 95 %. Derajat bebas dan
interaksi (experiment) sebagai numerator yaitu 1, dan derajat bebas experimental
error sebagai denominator yaitu 15, sehingga diperoleh harga F tabel untuk faktor
dan interaksi pada semua respon adalah F0,05(1, 15) = 4,5431.
31
BAB IV. HASIL DAN PEMBAHASAN HASIL DAN PEMBAHASAN
A. Penetapan Kadar Air Serbuk Teh Hijau
Teh hijau yang digunakan dalam penelitian ini berupa serbuk teh berwarna
hijau, berbau khas, serta mempunyai rasa pahit. Sebelum dilakukan ekstraksi,
terlebih dahulu dilakukan penetapan kadar air serbuk teh hijau dengan titrimetri
Karl Fischer. Prinsip penetapan kadar air berdasarkan reaksi kuantitatif air dengan
larutan anhidrat sulfur dioksida dan iodium dengan adanya buffer yang bereaksi
dengan ion hidrogen (Anonim, 1995). Penetapan kadar air dalam serbuk teh hijau
dilakukan untuk mengetahui kandungan air dalam serbuk teh hijau. Kadar air
yang rendah dalam serbuk teh hijau dapat mencegah terjadinya degradasi
enzimatik maupun adanya kontaminasi oleh mikroorganisme.
Sebelum dilakukan penetapan kadar air dalam serbuk teh hijau, terlebih
dahulu dilakukan pre-titrasi, cek kebocoran, dan standarisasi. Pre titrasi bertujuan
untuk menghilangkan air dalam pelarut. Cek kebocoran dilakukan untuk
mengetahui jumlah lembab yang masuk ke dalam titrator. Lembab yang masuk
dapat mempengaruhi hasil penetapan kadar air. Hasil cek kebocoran
diperbolehkan untuk penetapan kadar air bila nilai drift adalah 10-50. Pada
penelitian ini, drift cek kebocoran adalah 25 sehingga diperbolehkan untuk
penetapan kadar air sampel serbuk teh hijau. Standarisasi bertujuan untuk
mengetahui kesetaraan antara volume titran dengan bobot air. Berdasarkan hasil
Untuk penetapan kadar air, serbuk teh hijau ditambah dengan metanol dan
didiamkan selama 24 jam. Hal ini dilakukan untuk menarik air dari serbuk teh
hijau sehingga lebih mudah bereaksi dengan pereaksi Karl Fischer. Berdasarkan
hasil pengujian, kadar air dalam 1 mL blanko metanol adalah 20,89 mg dan kadar
air rata-rata dalam serbuk teh hijau adalah 7,973% b/b (kurang dari 10 %).
Tabel IV. Hasil penetapan kadar air serbuk teh hijau Replikasi Kadar air serbuk teh hijau (% b/b)
1 8,206 2 7,624 3 8,089 Rata-rata 7,973
B. Ekstraksi Polifenol Teh Hijau
Ekstraksi polifenol teh hijau dilakukan dengan cara maserasi yaitu
ekstraksi zat aktif menggunakan cairan pengekstraksi dengan penggojogan atau
pengadukan pada suhu ruangan. Sebelum dilakukan ekstraksi, serbuk diayak
dengan ayakan nomor 12/20 untuk memperoleh derajat halus serbuk yang
seragam.
Penggunaan bahan berupa serbuk teh bertujuan untuk memperluas area
kontak antara bahan dengan cairan penyari sehingga proses penyarian lebih baik.
Pada maserasi, cairan pengekstraksi dapat masuk menembus dinding sel dan
mengakibatkan terjadinya difusi zat aktif dari bahan ke cairan pengekstraksi.
Maserasi mempunyai kelebihan yaitu reprodusibilitas yang baik karena
penggunaan jumlah cairan ekstraksi yang tetap dapat mempertahankan jumlah zat
aktif yang dapat terekstraksi dari bahan sehingga pengulangan proses dapat
menghasilkan zat aktif dalam jumlah yang sama. Alat yang digunakan untuk
maserasi adalah shaker dengan kecepatan penggojogan 150 rpm. Penggojogan
konstan berfungsi untuk meningkatkan efektifitas penyarian.
Cairan pengekstraksi yang digunakan adalah metanol. Pemilihan metanol
sebagai cairan pengekstraksi karena metanol dapat melarutkan senyawa aktif
yaitu polifenol. Metanol sering dipakai untuk ekstraksi flavonoid (Robinson,
1991).
Maserasi dilakukan terhadap 100 g serbuk teh menggunakan metanol
sebanyak 500 mL selama 48 jam. Maserat yang diperoleh dipekatkan hingga 100
mL, kemudian ditambah 100 mL kloroform dan 100 mL akuades. Kloroform
digunakan untuk menghilangkan pigmen yang masih terdapat dalam maserat.
Pigmen perlu dihilangkan untuk meningkatkan penerimaan konsumen terhadap
hasil formulasi.
Lapisan atas diambil sedangkan lapisan bawah yang mengandung pigmen
tidak digunakan. Lapisan atas diekstraksi dengan etil asetat 2 x 150 mL. Etil asetat
digunakan untuk menarik zat aktif dari campuran tersebut karena etil asetat
merupakan pelarut yang baik untuk memisahkan katekin dari senyawa yang lebih
polar seperti karbohidrat (Robinson, 1991). Ekstraksi berulang dengan etil asetat
bertujuan untuk mendapatkan zat aktif yang lebih banyak daripada ekstraksi
tunggal. Lapisan etil asetat dikumpulkan kemudian diuapkan hingga kering.
Penggunaan ekstrak kering mempunyai keuntungan yaitu adanya standarisasi
kandungan air yang rendah. Organoleptis ekstrak kering polifenol teh hijau yaitu
berwarna coklat, bau khas, dan warna pahit.
B. Penetapan Kadar Polifenol dalam Ekstrak Kering Polifenol Teh Hijau Penetapan kadar polifenol dalam ekstrak kering polifenol teh hijau
dilakukan secara kolorimetri metode Folin-Ciocalteu (Lindhorst, 1998). Metode
Folin-Ciocalteu digunakan dalam penetapan kadar polifenol dalam ekstrak kering
polifenol teh hijau karena bersifat spesifik terhadap senyawa fenolik. Prinsip
metode ini adalah pereaksi Folin-Ciocalteu dapat mengoksidasi senyawa fenolik
dalam suasana basa sehingga asam heteropoli fosfomolibdat dan fosfotungstat
dalam pereaksi Folin-Ciocalteu mengalami reduksi menghasilkan kompleks
molibdenum blue (Singleton dan Rossi, 1965). Senyawa yang terbentuk ini dapat
diukur absorbansinya pada panjang gelombang cahaya tampak.
Penetapan operating time bertujuan untuk mengetahui rentang waktu yang
diperlukan oleh senyawa yang terbentuk agar memberikan absorbansi yang stabil,
artinya semua polifenol dalam larutan telah bereaksi dengan pereaksi
Folin-Ciocalteu. Berdasarkan gambar 2, operating time kuersetin dengan metode
Folin-Ciocalteu adalah 40-120 menit.
Gambar 2. Operating time kuersetin dengan metode Folin-Ciocalteu
Penetapan panjang gelombang serapan maksimum bertujuan untuk
mengetahui panjang gelombang saat senyawa memberikan absorbansi yang
maksimum sehingga dapat memberikan sensitifitas yang baik untuk analisis.
Penetapan panjang gelombang serapan maksimum dilakukan dengan larutan
kuersetin konsentrasi 0,4 mg/mL.
Gambar 3. Panjang gelombang serapan maksimum kuersetin dengan metode Folin-Ciocalteu
Berdasarkan gambar dapat disimpulkan bahwa serapan maksimum
kuersetin dengan metode Folin-Ciocalteu terjadi pada panjang gelombang 733,7
nm. Panjang gelombang tersebut selanjutnya digunakan dalam pengukuran
absorbansi pada penetapan kadar polifenol dalam ekstrak kering polifenol teh
hijau.
Pembuatan kurva baku dan penetapan kadar polifenol dalam ekstrak
kering polifenol teh hijau dilakukan dalam 1 proses. Sebelum dilakukan
penetapan kadar polifenol dalam ekstrak kering polifenol teh hijau, terlebih
dahulu dilakukan penetapan kurva baku senyawa standar pembanding kuersetin
ekstrak kering polifenol teh hijau diperlukan senyawa standar pembanding karena
jenis senyawa polifenol dalam teh hijau sangat beragam. Kuersetin digunakan
sebagai senyawa standar karena kuersetin merupakan salah satu jenis polifenol
yang terdapat dalam teh hijau. Persamaan kurva baku yang diperoleh digunakan
untuk perhitungan kadar polifenol dalam ekstrak kering polifenol teh hijau.
Absorbansi senyawa hasil reaksi kolorimetri seri kurva baku kuersetin
yang diukur pada panjang gelombang 733,7 nm ditunjukkan pada tabel V.
Tabel V. Hasil pengukuran absorbansi senyawa hasil reaksi kolorimetri seri kurva baku standar kuersetin
Replikasi 1 Replikasi 2 Replikasi 3 Kadar
(mg %) Absorbansi
Kadar
(mg %) Absorbansi
Kadar
(mg %) Absorbansi 0,198 0,305 0,205 0,316 0,201 0,295 0,297 0,405 0,307 0,425 0,301 0,428 0,397 0,584 0,410 0,521 0,402 0,539 0,496 0,713 0,513 0,669 0,503 0,650 0,595 0,817 0,615 0,737 0,604 0,813 0,694 0,875 0,718 0,821 0,704 0,896
r 0,989 r 0,995 r 0,998
A 0,075 A 0,118 A 0,055
B 1,214 B 1,005 B 1,212
Untuk penetapan kadar polifenol dalam ekstrak kering polifenol teh hijau,
digunakan persamaan kurva baku replikasi 3 (y = 1,212x +0,055) karena kurva
baku tersebut menghasilkan nilai koefisien korelasi (r) paling besar di antara
replikasi yang lain yaitu 0,998. Nilai r tersebut lebih besar daripada nilai r tabel
signifikansi dengan derajat bebas 4 taraf kepercayaan 99 % yaitu 0,917 sehingga
kurva baku tersebut mempunyai hubungan regresi.
Hasil perhitungan kadar polifenol dalam ekstrak kering polifenol teh hijau
dengan persamaan kurva baku terpilih ditunjukkan pada tabel VI.
Tabel VI. Hasil perhitungan kadar polifenol dalam ekstrak kering polifenol teh hijau
Replikasi Absorbansi
Kadar polifenol dalam ekstrak kering polifenol
teh hijau (% b/b)
1 0,342 58,998
2 0,348 60,104
3 0,348 58,991
4 0,347 59,440
5 0,349 59,972
6 0,358 62,052
Rata-rata 59,926 SD 1,142
Dari hasil pengukuran absorbansi dan perhitungan diperoleh kadar
rata-rata polifenol dalam ekstrak kering polifenol teh hijau yaitu (59,926 ± 1,142) %
b/b terhitung ekuivalen terhadap kuersetin.
C. Penentuan Nilai SPF secara In Vitro
Scanning spektra UV yang diserap oleh larutan polifenol teh hijau
bertujuan untuk melihat kemampuan polifenol dalam menyerap radiasi UV.
Larutan dengan konsentrasi polifenol 6 mg % diukur serapannya pada panjang
gelombang sinar UV 250-400 nm. Hasil scanning menunjukkan bahwa polifenol
dapat menyerap radiasi pada panjang gelombang 250-400 nm dengan puncak
Gambar 4. Hasil scanning spektra UV polifenol teh hijau
Struktur polifenol teh hijau mengandung sistem kromofor dan gugus
auksokrom yang terikat pada sistem kromofor. Adanya sistem kromofor dan
gugus auksokrom yang terikat pada sistem kromofor menyebabkan polifenol teh
hijau dapat menyerap radiasi UV.
epikatekin epikatekin-3-galat
Epigalokatekin epigalokatekin-3-galat
Keterangan :
: sistem kromofor
: gugus auksokrom
Gambar 5. Struktur epikatekin, epikatekin-3-galat, epigalokatekin, dan epigalokatekin-3-galat dengan sistem kromofor dan gugus auksokrom
Penetapan nilai SPF ekstrak polifenol teh hijau secara in vitro dilakukan
dengan mengukur area di bawah kurva (AUC) absorbansi terhadap panjang
gelombang antara 290 nm hingga panjang gelombang di atas 290 nm yang
memberikan absorbansi 0,05 (Petro, 1981). Hal ini dilakukan karena radiasi UV
penyebab kerusakan kulit bersifat polikromatis. Penetapan SPF dilakukan
dengan 3 seri konsentrasi larutan polifenol dalam etanol 90% yaitu 6; 12; dan 18
mg %, masing-masing dengan 3 kali replikasi. Nilai SPF secara in vitro diperoleh
menggunakan persamaan :
Log SPF =
1 n
AUC λ − λ
Dari hasil scanning spektra UV terlihat bahwa panjang gelombang serapan
maksimum (277 nm) terletak di luar range panjang gelombang yang akan diukur
untuk penetapan SPF (290-λn). Perhitungan AUC pada range panjang gelombang
tersebut terbatas pada daerah punggung kurva sehingga tidak diperoleh AUC
maksimal.
Hasil perhitungan SPF polifenol teh hijau secara in vitro ditunjukkan pada
tabel VII. Konsentrasi polifenol 6,0 mg % menghasilkan nilai SPF 2, konsentrasi
12,1 mg % menghasilkan SPF 3,687 sedangkan konsentrasi 18,1 mg %
menghasilkan SPF dengan kategori nilai SPF 5,8