METODE DETEKSI UNTUK PENGUJIAN RESPON
KETAHANAN BEBERAPA GENOTIPE CABAI TERHADAP
INFEKSI CHILLI VEINAL MOTTLE POTYVIRUS (ChiVMV)
ENDANG OPRIANA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis “Metode Deteksi untuk Pengujian Respon Ketahanan Beberapa Genotipe Cabai Terhadap Infeksi chilli veinal mottle potyvirus (ChiVMV)” adalah benar merupakan hasil karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, 5 Februari 2009
Endang Opriana A451060081
ABSTRACT
ENDANG OPRIANA. Detection Methods for Evaluastion of Response of Chillipepper Genotypes to chilli veinal mottle potyvirus (ChiVMV) Infection Survey SRI HENDRASTUTI HIDAYAT and SRIANI SUJIPRIHATI.
Chilli veinal mottle potyvirus (ChiVMV) are considered one of the major constraints to chilli production In Indonesia. Preliminary surveys in several provinces in 2005 indicated that ChiVMV were causing disease incidence up to 100%. The use of resistance varieties has become the major focus for controlling ChiVMV. To support breeding activities in developing chillipepper varieties resistace to ChiVMV, rapid and accurate detection method is required. The research was conducted involving three activities: 1) survey to chillipepper growing area to collect field isolates of ChiVMV; 2) evaluation of detection method for ChiVMV, i.e: ELISA, DIBA, and RT-PCR; 3) evaluation of chillipepper genotypes for resistence to ChiVMV.
It was evidenced from the survey that ChiVMV infection has spread widely in chillipepper growing area. Thirteen isolates of ChiVMV were collected and 5 of them showing different symptom types were selected for further studies. Three detection methods tested using 5 different ChiVMV isolates showed variability results in term of their sensitifity. I-ELISA was able to detect ChiVMV at the level of 1: 10.000 (b/w) of leaf extraction; whereas DIBA has less sensitifity with detection level of 1 : 1.000 of leaf extract. However, DIBA requires less amount of antiserum and shorter detection time than I-ELISA. Specific DNA fragment of ChiVMV i.e. 800 bp in size was successfully amplified using RT-PCR. Evaluation of genotypes showed that IPB C1, PBC 521, IPB C10 with highly resistance response and IPB C8, IPB C17, IPB C 14 and Keriting Sumatera with resistence response might be useful for further breeding activities to develop ChiVMV resistance varieties. It was further proved that IPB C99 showed high signal in DIBA when inoculated with the most virulent ChiVMV isolates (CKB) and less virulent isolates (BL) while IPB C521 showed very weak signal in inoculated leaves in DIBA when inoculated with the most virulent ChiVMV isolates (CKB). Its proved that plant response to virus infection definately related to plant genotipes and virulence level of pathogen.
RINGKASAN
ENDANG OPRIANA. Metode Deteksi untuk Pengujian Respon Ketahanan Beberapa Genotipe Cabai Terhadap Infeksi chilli veinal mottle potyvirus
(ChiVMV). Dibimbing oleh SRI HENDRASTUTI HIDAYAT dan SRIANI SUJIPRIHATI.
Chilli veinal mottle potyvirus (ChiVMV) telah menjadi salah satu kendala produksi cabai di Indonesia. Survei yang dilakukan sebelumnya pada tahun 2005 melaporkan kejadian penyakit ChiVMV di lapangan mencapai 100%. Metode pengendalian ChiVMV telah diarahkan dengan penggunaan tanaman tahan. Untuk mendukung kegiatan pemulian tanaman dalam mengembangkan varietas cabai tahan ChiVMV, ketersedian metode deteksi yang cepat dan akurat sangat dibutuhkan. Tiga kegiatan telah dilaksanakan penelitian ini yaitu 1) mengumpulkan isolat ChiVMV dari beberapa sentra tanaman cabai; 2) mengevaluasi metode deteksi yang sesuai untuk ChiVMV yaitu I-ELISA, DIBA dan RT-PCR; 3) menguji respon ketahanan beberapa genotipe cabai terhadap infeksi ChiVMV.
Hasil survei yang telah dilakukan menunjukan bahwa infeksi ChiVMV telah menyebar semakin luas dilapangan. Dari 13 isolat ChiVMV yang berhasil diperbanyak di rumah kaca selanjutnya 5 isolat yang mewakli masing-masing lokasi survei dan memilki karakteristik gejala yang berbeda dipilih untuk pengujian lebih lanjut. Tiga metode deteksi yang dipilih untuk menguji 5 isolat ChiVMV menunjukkan tingkat sensitifitas yang berbeda. I-ELISA mampu mendeteksi ChiVMV hingga taraf pengenceran 1 : 10.000 sedangkan metode DIBA mampu mendeteksi hingga taraf pengenceran 1 : 1.000. Meskipun demikian metode DIBA hanya menggunakan anti serum dalam jumlah yang lebih sedikit dan waktu deteksi yang lebih singkat dari pada I-ELISA. Deteksi ChiVMV dengan RT-PCR berhasil mengamplifikasi fragmen DNA spesifik ChiVMV berukuran 800 bp. Evaluasi beberapa genotipe cabai terhadap infeksi ChiVMV menunjukkan bahwa IPB C1, PBC 521, IPB C10 memberikan respon sangat tahan, sedangkan IPB C8, IPB C17, IPB C14 dan Keriting Sumatera memberikan respon tahan. Ketujuh genotipe cabai tersebut berpotensi digunakan dalam kegiatan pemulian tanaman untuk mendapatkan genotipe cabai tahan ChiVMV. Lebih lanjut diketahui bahwa genotipe IPB C99 yang telah diinokulasi dengan isolat virulen (CKB) dan isolat lemah (BL) tetap menunjukkan signal yang kuat pada membran nitroselulosa, sedangkan genotipe IPB C521 hanya menunjukkan signal pada daun yang diinokulasi. Hal tersebut membuktikan bahwa respon tanaman terhadap infeksi ChiVMV tergantung pada genotipe tanaman dan tingkat virulensi virus.
Hak Cipta Milik Institut Pertanian Bogor, tahun 2009
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
METODE DETEKSI UNTUK PENGUJIAN RESPON
KETAHANAN BEBERAPA GENOTIPE CABAI TERHADAP
INFEKSI CHILLI VEINAL MOTTLE POTYVIRUS (ChiVMV)
ENDANG OPRIANA
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Proteksi Tanaman
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Metode Deteksi untuk Pengujian Respon Ketahanan Beberapa Genotipe Cabai Terhadap Infeksi chilli veinal mottle potyvirus (ChiVMV)
Nama : Endang Opriana
NIM : A451060081
Disetujui
Komisi Pembimbing
Diketahui
PRAKATA
Syukur Alhamdulillah tiada terkira penulis panjatkan ke hadirat Allah SWT. Rabb yang memberi segala kemudahan sehingga akhirnya penulis dapat menyelesaikan penelitian ini. Tesis yang berjudul Metode Deteksi untuk Pengujian Respon Ketahanan Beberapa Genotipe Cabai Terhadap Infeksi chilli veinal mottle potyvirus (ChiVMV) merupakan tugas akhir untuk memperoleh gelar Magister sains pada Sekolah Pascasarjana IPB.
Penelitian dan penulisan tesis ini dibimbing oleh Dr. Ir. Sri Hendrastuti Hidayat, M.Sc dan Prof. Dr. Ir. Sriani Sujiprihati, MS. Terimakasih dan penghargaan sedalam-dalamnya penulis sampaikan atas segala kesabaran, arahan dan bimbingan yang diberikan. Ucapan terimakasih juga disampaikan kepada Badan Penelitian dan Pengembangan Pertanian yang telah mendanai penelitian ini sebagai bentuk kerjasama kemitraan penelitian pertanian dengan perguruan tinggi (KKP3T).
Terimakasih disampaikan kepada Dekan Sekolah Pascasarjana IPB, Ketua Departeman Proteksi Tanaman, Ketua PS Entomologi-Fitopatologi atas kesedian menerima penulis untuk studi di IPB. Dosen-dosen di Jurusan Hama dan Penyakit Tumbuhan Universitas Sriwijaya Dr. Suparman, SHK, Ir. Harman Hamidson, MP, Dr. Chandra Irsan, M.Si, dan Dr. Abdul Mazid, M.Si yang telah memberikan dukungan dan kepercayaan selama ini.
Tanpa mengurangi rasa hormat, ucapan terimakasih juga disampaikan kepada Kepala Laboratorium Virologi Tumbuhan Departemen Proteksi Tanaman atas izin penggunaan bahan dan alat serta rumah kaca Cikabayan. Kepada Kepala Bagian Genetika dan Pemuliaan Tanaman Departemen Agronomi dan Hortikultura atas bantuan bahan genetik dan fasilitas. Kepada Mbak Tuti Susanti Legiastuti, Pak Edi, dan Pak Saefudin atas bantuan pengetahuan teknis yang diberikan selama penelitian dilaksanakan; asisten peneliti di Labdik Pemuliaan Tanaman Mbak Cici atas bantuan pemilihan genotipe cabai.
Yang terakhir namun bukan berarti terakhir di hati, ucapan terimakasih ini diberikan kepada Ibunda Pujiyati dan Ayahanda Syobirin Sulaiman yang tak pernah berhenti memberikan dorongan, semangat, mendoakan dan harapan terbaik kepada penulis selama ini. Kepada saudara dan kerabat Mbak Sri, Titin, Firman dan Putri, Bik cik Yanti dan Ma’ Icat untuk cinta, semangat dan doa. Terimakasih terhangat kepada sahabat terbaik kak Evan Herawan, S.Pi atas segala bantuan, sokongan dan pengorbanan waktu selama ini. Terimakasih untuk energi yang cukup membuat kuat saat lelah dan semangat untuk selalu berharap. Kepada para sahabat dan rekan sejawat Mbak Ipah, Mbak Milah, Mimi, Devi, Mas Khamdan, Pak Rai, Pak Irwan, Pak Jumsu, Bu Ifa, Dila, Dida dan Lara.
Semoga karya tulis ini kelak dapat memberi manfaat bagi ilmu pengetahuan dan masyarakat.
Bogor, Februari 2009
DAFTAR ISI
Reverse Transcription Polymerase Chain Reaction (RT-PCR) ... 13
KOLEKSI ISOLAT LAPANG CHILLI VEINAL MOTTLE POTYVIRUS (ChiVMV) DAN METODE DETEKSI ChiVMV
Survei dan Pengambilan Sampel ... 16
Perbanyakan Isolat Virus ... 17
Diagnosis ChiVMV dengan DAS-ELISA ... 18
UJI KETAHANAN GENOTIPE-GENOTIPE CABAI (Capsicum sp.) TERHADAP ChiVMV
Abstrak ... 37
Pendahuluan ... 37
Bahan dan Metode ... 39
Waktu dan Tempat ... 39
Bahan ... 39
Metode ... 40
Penyemaian Benih ………... 40
Inokulasi ChiVMV pada Genotipe-genotipe Cabai …... 41
Evaluasi Ketahanan Cabai Terhadap Infeksi ChiVMV... 41
Hasil dan Pembahasan ... 42
Simpulan ………. 48
Daftar Pustaka ………. 48
RESPON BEBERAPA GENOTIPE CABAI TERHADAP INFEKSI DUA ISOLAT ChiVMV Abstrak ... 51
Pendahuluan ... 51
Bahan dan Metode ... 53
Waktu dan Tempat ... 53
Bahan ... 53
Metode ... 53
Penyemaian Benih ………... 53
Inokulasi ChiVMV pada Genotipe Cabai ………. 53
Dot Blot Immunobinding Assay (DIBA) ... 54
Hasil dan Pembahasan ... 56
Simpulan ………. 61
Daftar Pustaka ………. 62
PEMBAHASAN UMUM ... 63
SIMPULAN UMUM …... ... 67
DAFTAR TABEL
Halaman
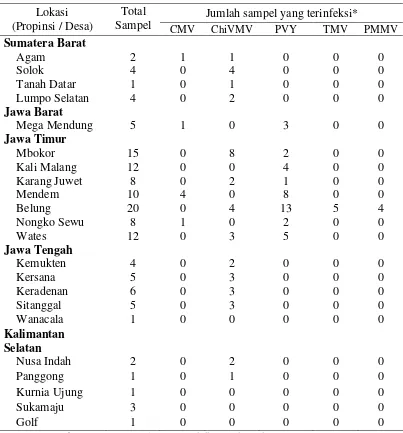
3.1 Deteksi ChiVMV menggunakan metode DAS ELISA pada sampel tanaman cabai asal Sumatera Barat, Jawa Barat, Jawa Timur, Jawa Tengah dan Kalimantan Selatan... 26
3.2 Deteksi beberapa virus pada sampel tanaman cabai ... 27
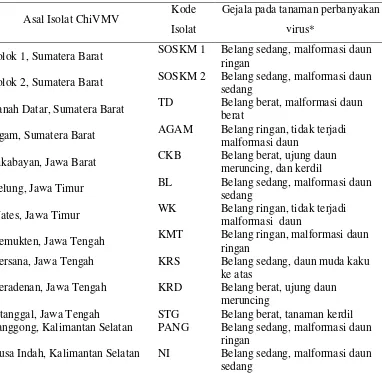
3.3 Isolat-isolat ChiVMV yang berhasil diperbanyak di rumah kaca.... 28
3.4 Rata-rata nilai absorbansi sampel terinfeksi ChiVMV pada berbagai tingkat pengenceran menggunakan metode I-ELISA ... 31
4.1 Daftar genotipe yang dipakai dalam uji ketahanan terhadap infeksi ChiVMV... 40
4.2. Pengelompokan tingkat ketahanan genotipe cabai terhadap infeksi ChiVMV... 41
4.3 Tipe gejala pada 29 genotipe cabai yang diinokulasi dengan ChiVMV... 42
4.4 Respon 29 genotipe cabai yang diinokulasi dengan ChiVMV ... 47
5.1 Genotipe-genotipe cabai yang digunakan dalam uji respon tanaman terhadap isolat ChiVMV... 54
5.2. Penentuan indeks penyakit pada tanaman cabai merah yang terinfeksi beberapa isolat ChiVMV ... 54
5.3 Kejadian penyakit, indeks penyakit dan masa inkubasi tiga genotipe cabai setelah diinokulasi dengan lima isolat ChiVMV ... 56
5.4 Rata-rata skor DIBA pada genotipe IPB C99 yang diinokulasi oleh isolat CKB dan BL ... 58
5.5 Rata-rata skor DIBA pada genotipe IPB C17 yang diinokulasi oleh isolat CKB dan BL ... 59
DAFTAR GAMBAR
Halaman
1.1 Tahap penelitian : Metode deteksi untuk pengujian respon ketahanan beberapa genotipe cabai terhadap infeksi chilli veinal mottle potyvirus (ChiVMV) ... 4
3.1 Keadaan pertanaman cabai di lokasi survei dan pengambilan sampel 24
3.2 Gejala ChiVMV pada tanaman paprika C. annuum var. Grossum .. 29
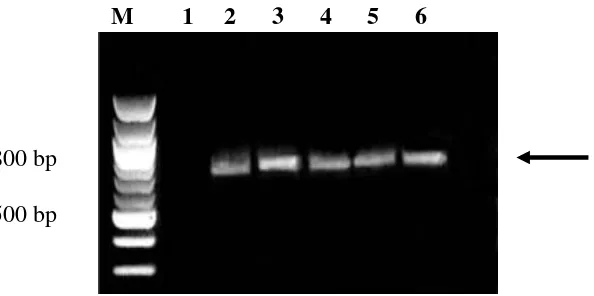
3.3 Hasil amplifikasi RT-PCR dari tanaman cabai terinfeksi beberapa isolat ChiVMV menggunakan primer ChiVMV-F1 dan
ChiVMV-R... 30
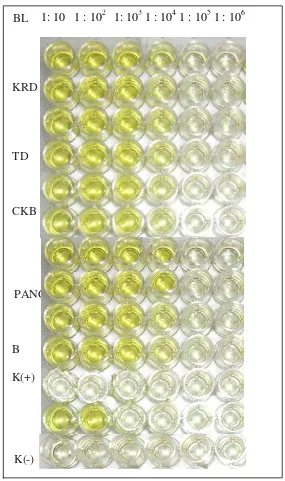
3.4 Reaksi perubahan warna pada plat mikrotiter hasil I-ELISA pada berbagai tingkat pengenceran (1 : 10 hingga 1 : 106) menggunakan lima isolat ChiVMV... 32
3.5 Reaksi perubahan warna pada membran DIBA dengan berbagai tingkat pengenceran sap menggunakan lima isolat ChiVMV... 33
4.1 Tipe gejala yang muncul pada beberapa genotipe cabai pada 14 HSI ... 44
5.1 Posisi letak daun yang diambil untuk dideteksi dengan metode DIBA ... 54
5.2 Penentuan intensitas signal reaksi DIBA pada membran
Nitroselulosa ... 55
5.3 Gejala yang muncul pada genotipe cabai (14 HSI) yang diinokulasi ChiVMV isolat Cikabayan (CKB) dan Malang (BL) ... 57
5.4 Hasil deteksi isolat CKB pada genotipe IPB C99, IPB C17, IPB C521 dengan menggunakan metode deteksi DIBA ... 60
PENDAHULUAN UMUM
Latar Belakang
Cabai (Capsicum spp.) merupakan salah satu komoditas hortikultura penting di Indonesia. Selain memiliki kandungan gizi yang cukup tinggi, cabai juga sangat
potensial secara ekonomi. Menurut data Direktorat Jendral Bina Produksi
Hortikultura, luas panen tanaman cabai adalah luas panen terbesar di antara
tanaman sayuran lainnya yaitu berturut-turut 204.747 ribu hektar untuk tahun
2006 dan 204.048 ribu hektar pada tahun 2007(Biro Pusat Statistik 2007; DBPH
2007).
Produksi cabai di Indonesia masih sangat rendah. Berdasarkan data dari
Balai Penelitian Sayuran (2007), produksi cabai besar nasional hanya mencapai
6.30 ton/ha sedangkan untuk cabai rawit hanya 4.67 ton/ha Jumlah tersebut
belum dapat mengimbangi potensi produksinya yang dapat mencapai 20 ton/ha
(Duriat, 1996). Banyak faktor-faktor pembatas yang dihadapi petani dalam
berusahatani cabai. Beberapa diantaranya adalah harga yang sangat berfluktuasi,
penggunaan benih yang bermutu rendah, memerlukan modal yang besar, dan
banyaknya gangguan serangan hama dan infeksi penyakit mulai dari persemaian
sampai panen. Tanaman cabai merupakan salah satu komoditas yang mengalami
gangguan oleh hama dan penyakit terbanyak. Dilaporkan oleh Ellen et al. (1993), jenis penyakit yang menyerang ada sebanyak 26 macam yang disebabkan oleh
virus, bakteri dan cendawan serta 13 jenis hama serangga.
Menurut Duriat (2003), para pakar virologi seperti Neinhaus (1981) dan
Kalloo (1994) telah mencatat sekitar 13 – 35 jenis virus yang menyerang tanaman
cabai di daerah tropis dan subtropis. Prevalensi penyakit virus dari waktu ke
waktu mengalami perubahan. Balai Penelitian Tanaman Sayuran (Balitsa)
Lembang melaporkan tiga virus utama yaitu cucumber mosaic virus (CMV),
potato virus Y (PVY) dan tobacco etch virus (TEV) berdasarkan hasil survei tahun 1986 dan 1990. Pada tahun 1992 dan 1995 urutan berubah menjadi CMV, chilli veinal mottle potyvirus (ChiVMV) dan PVY (Setiawati 2003).
ChiVMV telah menjadi salah satu kendala utama dalam peningkatan
Berdasarkan hasil penelitian Roff dan Ong (1992), kerugian akibat ChiVMV di
Malaysia dapat mencapai 60% serta menurunkan kualitas buah. Hasil survei yang
telah dilakukan oleh Taufik et al. (2006) menunjukkan kejadian penyakit ChiVMV di Sulawesi Selatan dapat mencapai 100% sedangkan di Jawa Barat
mencapai 50%. Meskipun demikian masih sangat diperlukan survei lebih banyak
dan studi lebih lanjut yang mempelajari penyebaran ChiVMV di Indonesia
terutama di sentra-sentra produksi cabai, mengingat prevalensi ChiVMV yang
sangat tinggi di lapangan.
ChiVMV adalah kelompok Potyvirus yang menyebabkan gejala mosaik berupa belang hijau gelap dan hijau terang pada tulang daun. Pada gejala lanjut,
daun tanaman mengeriting dan kerdil (CABI 2000). ChiVMV juga dapat
menimbulkan gejala yang bervariasi pada daun tanaman cabai yang terinfeksi
tergantung pada kultivar cabai yang ditanam serta waktu infeksi (Chiemsombat
dan Kittipakorn 1996). Gejala pada daun cabai dapat berupa bercak berwarna
hijau tua yang tidak beraturan (belang) dan penebalan tulang daun, permukaan
daun tidak rata, daun menjadi lebih kecil dan kadang diikuti dengan malformasi
daun serta tanaman menjadi kerdil (Siriwong et al. 1995). Gejala mosaik berupa belang yang tampak pada daun disebabkan karena terjadinya penurunan nitrogen
yang terdapat selama sintesis virus dan penurunan tingkat karbohidrat yang kronis
di dalam jaringan tumbuhan (Matthews, 2002).
ChiVMV termasuk jenis virus yang sulit dikendalikan sebab virus ini
ditularkan oleh serangga vektor yaitu Aphid spp. secara non persisten. Karenanya penyebaran virus ini di lapangan terjadi dalam waktu yang cepat dimana virus
ditularkan melalui stilet kutu daun yang mengandung virus dari tanaman sakit dan
menularkannya ke tanaman sehat hanya dalam hitungan menit sampai jam.
Selama ini pengendalian terhadap virus masih terbatas pada penggunaan pestisida.
Pengendalian ini tidak efektif untuk mengendalikan ChiVMV yang ditularkan
secara non persisten oleh kutudaun. Penggunaan tanaman merupakan salah satu
strategi pengendalian sesuai untuk ChiVMV karena metode ini aman bagi
lingkungan, murah dan efektif (Grube et al. 2003).
Terbatasnya pengetahuan tentang keberadaan virus di lapangan dan sulitnya
dibutuhkan ketersediaan metode deteksi yang cepat dan akurat. Untuk mendeteksi
penyakit yang disebabkan oleh virus dapat digunakan berbagai metode. Metode
yang umum digunakan antara lain metode serologi seperti Enzyme Linked Immunosorbent Assay (ELISA) dan Dot Immunobinding Assay (DIBA), atau metode molekuler seperti hibridisasi asam nukleat dan teknik Polymerase Chain Reaction (PCR) (Matthews 1991; Foster dan Taylor 1998; Hull 2002).
Metode deteksi yang memadai merupakan salah satu komponen penting
dalam upaya mencari strategi pengendalian penyakit. Ketersediaan metode deteksi
yang akurat dan sensitif terutama diperlukan dalam kegiatan pemuliaan tanaman
yang ditujukan untuk pengembangan galur-galur tahan penyakit. Pengendalian
penyakit cabai yang disebabkan oleh ChiVMV telah diarahkan melalui perakitan
varietas tahan. Hasil penelitian yang telah dilakukan sebelumnya menunjukkan
bahwa IPB C495, CCA 321, VC211a-3-1-1-1, IPB C122 dan ICPN 7#3
memberikan respon sangat tahan terhadap ChiVMV dengan kejadian penyakit
0% sedangkan Bara dan Tit Super memberikan respon tahan terhadap infeksi
ChiVMV dengan kejadian penyakit 16-22% (Millah 2007; Latifah 2007; Riyanto
2007). Meskipun demikian eksplorasi ketahanan galur-galur cabai tahan ChiVMV
masih perlu terus dilakukan pada berbagai genotipe cabai.
Tujuan Penelitian
Kegiatan dan tahapan penelitian seperti terdapat pada Gambar 1.1 diarahkan untuk
tujuan-tujuan :
1. Mengumpulkan isolat ChiVMV melalui survei ke beberapa daerah sentra
penanaman cabai di Indonesia yaitu di Sumatera Barat, Jawa Barat, Jawa
Tengah, Jawa Timur, dan Kalimantan Selatan.
2. Mengetahui metode deteksi yang tepat untuk ChiVMV.
3. Mempelajari respon beberapa genotipe cabai terhadap infeksi ChiVMV.
Hipotesis Penelitian
1. Terdapat isolat ChiVMV yang memiliki virulensi yang berbeda
2. Genotipe cabai yang diuji terhadap isolat ChiVMV memiliki respon
Gambar 1.1 Tahap penelitian: Metode deteksi untuk pengujian respon ketahanan beberapa genotipe cabai terhadap infeksi chilli veinal mottle potyvirus (ChiVMV).
Survei ChiVMV dan koleksi isolat ChiVMV dari lapang
Hasil: Sebaran ChiVMV dan Isolat ChiVMV dari berbagai lokasi
Evaluasi metode deteksi
ChiVMV dengan ELISA, DIBA dan RT-PCR
Hasil: Metode deteksi yang tepat untuk evaluasi ketahanan genotipe cabai
Evaluasi ketahanan beberapa genotipe cabai terhadap ChiVMV
Hasil: Genotipe cabai dengan respon ketahanan yang berbeda Respon beberapa genotipe cabai
terhadap infeksi 2 isolat ChiVMV
TINJAUAN PUSTAKA
Kemaknaan Tanaman Cabai
Arti Ekonomi Cabai
Cabai merah (C annum L.) merupakan salah satu jenis sayuran yang cukup penting di Indonesia, baik untuk konsumsi di dalam negeri maupun untuk ekspor.
Selain memiliki kandungan gizi yang cukup tinggi, cabai juga sangat potensial
secara ekonomis. Pemanfaatan cabai sebagai bumbu masak, bahan baku berbagai
industri makanan, minuman dan obat-obatan, serta pemasarannya dalam bentuk
segar dan olahan menjadikan komoditas tersebut penting untuk diusahakan
(Durita & Muharam, 2003).
Di Indonesia cabai merah sudah dikembangkan sebagai tanaman
perdagangan dosmestik, dan diusahakan secara intensif di beberapa daerah sentra
produksi baik di Pulau Jawa maupun luar Jawa. Produksi cabai merah tahun 1998
dapat mencapai 452,990 ton terdiri dari 287.576 ton di P. Jawa dan 165.414 ton
hasil dari luar Jawa. Daerah sentra produksi di luar Jawa seperti D.I Aceh, Jambi,
Sumatera Selatan, Bengkulu, Lampung dan Bali. Sedang di luar daerah tersebut
tanaman cabai merah dibudidayakan hanya sekedar permintaan pasar lokal (Duriat
& Muharam, 2003).
Budidaya dan Keragaman Genotipe Cabai
Cabai (Capsicum spp.) merupakan tanaman hortikultura yang dapat ditanam
di segala musim. Genus Capsicum berasal dari dunia baru yang terdiri atas
beberapa spesies, spesies C. annuum dari Meksiko dan spesies lain (C. frutescens,
C.baccatum, C. chinense, dan C. pubescens) berasal dari Amerika Selatan. Oleh
pedagang Portugis dan Spanyol, cabai diintroduksikan ke Asia pada abad ke-16,
dan selanjutnya spesies cabai pedas tersebar paling luas di Asia Tenggara
(Pickersgill 1971; Siemonsma & Piluek 1994).
Lebih dari 100 spesies Capsicum telah diidentifikasi. Lima spesies di
antaranya telah dibudidayakan, yaitu C. annuum, C. chinense, C. frutescens, C.
pubescens, dan C. baccatum (Pickersgill, 1988). Klasifikasi spesies-spesies ini
persilangan antarspesies, dan biji hibrida antarspesies fertil (Heiser & Smith,
1953). C. annuum berbunga tunggal dengan petal berwarna putih bersih. C.
chinense berbunga dua atau lebih per ruas ketiak daundengan warna bunga putih
kehijauan dan penyempitan kelopak yang mencolok. C. frutescens membentuk 1-3
bunga per ruas ketiak daun, warna bunga putih kehijauan tanpa penyempitan pada
kelopak. C.baccatum mempunyai bercak kuning pada petal yang berwarna putih,
dan C. pubescens mempunyai petal ungu dan biji hitam (Pickersgill, 1988).
Penelitian persilangan interspesifik menunjukkan bahwa C. frutescens, C.
pubescens, dan C. chinense dapat disilangkan dengan C. annuum dan
menghasilkan biji yang fertil.
Secara umum cabai merah dapat ditanam di lahan basah (sawah) dan lahan
kering (tegalan) dan dapat dibudidayakan di saat musim hujan dan kering. Cabai
merah dapat tumbuh dengan baik pada daerah yang mempunyai ketinggian
sampai 900 m dari permukaan laut, tanah kaya akan bahan organik dengan pH
6-7, tektur tanah remah (Anonim, 1994).
Pemuliaan cabai pertama dilakukan di Amerika tropis untuk kultivar cabai
manis (Siemonsma & Piluek, 1994). Informasi keragaman genetik merupakan
dasar untuk mengembangkan strategi pemuliaan tanaman (Pickersgill, 1997).
Dalam kasus pembentukan hibrida baru yang tahan terhadap hama dan penyakit,
informasi keragaman genetik dapat digunakan untuk seleksi plasma nutfah dan
pengambilan contoh yang efisien (Prince et al. 1995).
Hama dan Penyakit Tanaman Cabai
Cukup banyak kendala yang dihadapi petani dalah membudidayakan cabai
di lapangan. Salah satu kendala utama rendahnya produksi cabai di Indonesia
adalah adanya gangguan dari hama dan penyakit (Semangun 2000). Prabaningrum
dan Moekasan (1996) melaporkan berbagai hama yang dapat menyerang tanaman
cabai antara lain kutu daun (Myzus persicae Sulz), Thrips (Thrips parvispinus
Karny), lalat buah (Beactrocera dorsalis Hendel), ulat gerayak (Spodoptera litura
(Cchoanephora cucubitarum), penyakit busuk buah (Colletotrichum capsici), CMV, ChiVMV, PVY dan TMV.
Pengendalian Hama dan Penyakit Tanaman Cabai
Tindakan pengendalian dilakukan apabila populasi dan atau tingkat
serangan hama dan penyakit dapat menimbulkan kerugian secara ekonomis, atau
hasil analisis data pengamatan rutin sudah mencapai ambang pengendalian.
Beberapa tindakan pengendalian yang umum dipilih dan digunakan petani cabai
dalam mengendaliakan hama dan penyakit pada cabai antara lain dengan
pengendalian teknik budidaya cabai, pengendalian fisik dan mekanik,
pengendalian biologi, dan aplikasi pestisida. Dari semua teknik pengendalian
tersebut yang paling sering digunakan adalah pengendalian dengan pestisida,
namun sayangnya penggunaan pestisida di Indonesia masih belum tepat sasaran,
tepat dosis, tepat jenis, tepat cara dan tepat waktu. Sehingga seringkali terjadi
kegagalan dalam pengendalian (Setiawan & Muharram 2003).
Untuk penyakit pada cabai yang disebabkan oleh virus, usaha pengendalian
penyakit virus (khususnya dengan pestisida) terutama ditujukan kepada serangga
vektornya, karena sampai saat ini tidak ada pestisida yang terdaftar dan diizinkan
oleh Menteri Pertanian yang dapat mematikan virus (Deptan, 2006).
Dalam mengendalikan serangga vektor virus pada tanaman cabai petani
masih mengandalkan penggunaan pestisida kimia sintetis, namun bila
pemakaiannya tidak bijaksana dikhawatirkan menimbulkan residu pestisida pada
produk buah cabai relatif tinggi, biaya produksi meningkat, bahaya terhadap
kesehatan pekerja, juga menyebabkan pencemaran lingkungan hidup. Di era pasar
bebas saat ini produk cabai yang tidak ramah lingkungan sulit bersaing karena
konsumennya lebih memilih produk pertanian yang bermutu baik dan aman
dikonsumsi (Duriat dan Muharam, 2003).
Seperti telah diuraikan sebelumnya, bahwa penggunaan pestisida dalam
mengendalikan serangga vektor virus seringkali tidak efektif, terutama untuk kutu
daun yang menularkan virus secara non persisten karena jenis vektor tersebut
hanya memiliki masa makan akuisisi yang singkat dan virus dengan waktu yang
singkat sudah dapat di tularkan ke tanaman yang sehat. Dengan demikian
virus yang ada di stilet telah lebih dulu ditularkan ke tanaman sehat melalui
periode makan yang singkat (Matthews, 2002).
Dalam pengendalian penyakit yang disebabkan oleh ChiVMV pada cabai
harus diarahkan pada pengembangan varietas tahan. Namun saat ini belum ada
varietas cabai yang tahan terhadap ChiVMV (Balai Penelitian Tanaman Sayuran,
2005). Walaupun demikian, melalui korespondensi dengan Asian Vegetable Research Development Center (AVRDC) di Taiwan, diketahui bahwa ada beberapa galur cabai yang tahan terhadap isolat virus tertentu.
Sifat-sifat Umum ChiVMV
Biologi, Ekologi dan Keragaman Genetik ChiVMV
ChiVMV adalah salah satu anggota dari kelompok Potyvirus. Asam nukleatnya tersusun dalam untaian RNA utas tunggal positif (ssRNA[+]),
berbentuk benang lentur dengan panjang 750 nm dan diameter 12 nm dan tidak
terbungkus. Namun pada beberapa jenis tumbuhan dan dalam konsentrasi
magnesium yang tinggi, partikel ChiVMV dapat menjadi lebih kaku
(International Taxonomy on Comittee of Viruses, 2002).
ChiVMV pertama kali dilaporkan menginfeksi tanaman cabai di Malaysia
pada tahun 1947 oleh Burnett, selanjutnya berkembang hingga ke Korea, Taiwan,
Thailand, beberapa kawasan di Amerika dan Afrika Selatan sejak tahun 1979
(Ong et al 1979) Selanjutnya ChiVMV telah menjadi salah satu kendala utama dalam peningkatan kualitas tanaman cabai di Asia Tenggara dan Afrika (Moury et al., 2005).
ChiVMV memiliki titik panas inaktivasi (TIV) pada suhu 60oC. Di atas suhu
tersebut, partikel virus akan mengalami lisis. Masa penyimpanan virus in vitro
adalah 7 hari. Seperti kebanyakan anggota kelompok potyvirus yang lain, ChiVMV memiliki struktur khusus yang merupakan ciri infeksi dari grup
potyvirus. Struktur khusus ini disebut badan inklusi yang keberadaannya biasanya menyertai partikel virus pada jaringan tanaman. Badan inklusi ini banyak
ditemukan dalam sitoplasma maupun dalam inti. Pada potyvirus, badan inklusinya berbentuk cakra dan dapat terlihat jelas pada pengamatan melalui
ChiVMV adalah jenis virus yang sulit dikendalikan karena ia ditularkan
secara non persisten di lapangan oleh serangga vektor kutu daun Aphis craccivora, A. gossypii, A. spiraecola, Myzus persicae, Toxoptera citricidus, Hysteroneura setarieae, Rhopalosiphum maidis, Aphis craccivora, A. gossypii, A. spiraecola, Myzus persicae, Toxoptera citricidus, Hysteroneura setarieae, dan
Rhopalosiphum maydis. Selain itu virus juga dapat ditularkan dengan cara inokulasi mekanis pada tanaman sehat dan melalui penyambungan, namun virus
tidak dapat ditularkan melalui benih (Plant Virus Online, 1996).
Periode makan serangga pada tanaman yang sakit (periode akuisisi) yang
optimum untuk virus non persisten adalah 30-60 detik, perpanjangan periode
makan akuisisi tidak meningkatkan efisiensi penularan. Virus dapat ditularkan
segera setelah periode makan akuisisi, daya tular menurun setelah beberapa menit
dan akan berhenti dalam waktu kurang dari 1 jam. Untuk meningkatkan efektifitas
penularan, serangga vektor biasanya dipuasakan selama satu jam sebelum periode
makan akuisisi. Makan akuisisi merupakan periode makan pada tanaman sumber
inokulum (Matthews, 2002).
Kutu daun A. craccivora mendapatkan makanan dengan cara menusukkan stylet pada permukaan daun kemudian menghisap cairan tanaman. Bagian mulut
kutu daun terdiri dari 2 bagian stilet yang lentur. Pada awal proses makan, kutu
daun mensekresikan saliva. Kemudian stylet segera menusuk epidermis daun
kemudian makan dalam waktu tertentu. Penetrasi biasanya berlanjut ke bagian
daun yang lebih dalam dan membentuk tumpukan saliva selama penetrasi
tersebut. Stilet berpindah diantara sel sampai mencapai floem. Proses ini
membutuhkan waktu beberapa menit atau jam. Sekresi saliva ini menularkan
ChiVMV yang ada pada saliva aphid ke tanaman.
Tanaman yang menjadi kisaran inang ChiVMV di lapangan meliputi C. annuum, C. frutescens, Nicandra physalodes, Nicotiana megalosiphon, Physalis floridana, dan N. tabacum. Namun, kondisi lingkungan dan faktor fisiologis tanaman dapat mempengaruhi infeksi ChiVMV pada tanaman. Faktor-faktor
tersebut mencakup umur tanaman, keragaman genetik tanaman inang, posisi daun
pada tanaman, nutrisi tanaman, ketersediaan air, suhu, intensitas cahaya, musim
Gejala ChiVMV
Gejala infeksi virus ChiVMV pada tanaman cabai sangat bervariasi,
tergantung pada strain virus yang menginfeksi dan kultivar tanaman. Untuk
infeksi virus yang berasal dari kelompok Potyvirus seperti ChiVMV, gejala khusus yang diperlihatkan tanaman yang terinfeksi ChiVMV di lapangan adalah
mosaik berupa belang hijau gelap dan hijau terang pada tulang daun. Gejala akan
tampak jelas pada daun muda dan daun kecil. Tanaman yang terinfeksi menjadi
kerdil dan memiliki garis hijau gelap pada batang dan cabangnya. Beberapa bunga
rontok sebelum sempat menjadi buah. Kadang-kadang tanaman masih dapat
memproduksi buah namun dalam jumlah yang sangat sedikit dan permukaan
buah yang agak belang (Matthews, 2002). Infeksi ChiVMV pada fase
pertumbuhan awal mengurangi ukuran daun yang diikuti dengan distorsi, serta
produksi buahnya lebih sedikit dan lebih kecil (Shah & Khalid 2001).
Metode Deteksi dan Karakterisasi Virus Tanaman
Pengamatan gejala penyakit saja tidak cukup untuk mendeteksi dan
mengidentifikasi virus pada tanaman. Hal ini dikarenakan beberapa hal antara lain
beberapa virus dapat menimbulkan gejala yang sama pada tanaman yang sama,
satu virus dapat menghasilkan variasi gejala tergantung strain virusnya, campuran
beberapa virus atau strain virus dapat mempengaruhi gejala. Selain itu, suatu virus
dapat menimbulkan gejala yang berbeda pada tanaman yang berbeda. Kondisi
lingkungan dan iklim juga berpengaruh terhadap tipe gejala yang muncul (Hull
2002).
Sangat diperlukan metode deteksi yang tepat dalam mendeteksi dan
mengidentifikasi virus pada suatu tanaman. Deteksi dan identifikasi virus dapat
dilakukan berdasarkan karakter biologi dan molekuler. Deteksi virus berdasarkan
karakter biologi dapat dengan tanaman indikator, penularan, dan berdasarkan
bentuk partikel. Deteksi dan identifikasi menggunakan karakter molekuler
dilakukan dengan dua cara yaitu berdasarkan sifat protein dengan uji serologi dan
sifat asam nukleat dengan hibridisasi DNA, ekstraksi dsDNA/dsRNA serta
Serologi
Uji serologi dengan memanfaatkan reaksi antigen dan antibodi mempunyai
banyak kegunaan antara lain untuk mengidentifikasi virus penyebab penyakit
tumbuhan, mengukur konsentrasi virus dalam jaringan tumbuhan, mendeteksi
virus tumbuhan dalam tubuh serangga vektor dan untuk mengetahui hubungan
kekerabatan antar virus (Agrios 1997). Deteksi dan identifikasi secara serologi
sudah umum diaplikasikan untuk berbagai virus. Ada beberapa cara yang
digunakan untuk deteksi serologi antara lain ISEM, immunoflourescent staining (Hampton et al. 1990), presipitasi dalam tabung, aglutinasi kloroplas, flokulasi lateks, gel double-diffusion test, DIBA, immunoblotting atau western blotting, danELISA (Harlow & Lane 1999).
Metode serologi yang telah berhasil dikembangkan untuk mendeteksi virus
tumbuhan diantaranya yaitu metode DIBA yang digunakan untuk mendeteksi
ZYMV (Somowiyarjo et al. 1989). Kemudian Abouzid et al. (2002) menggunakan ELISA dan western blotting untuk mendeteksi beberapa protein selubung virus dari genus Begomovirus. Bentuk partikel TYLCV telah berhasil dideteksi dan diidentifikasi oleh Attathom et al. (1990) dengan menggunakan metode ISEM. Deteksi dengan metode immunoflourescent staining juga telah berhasil dilakukan oleh Sudarshana et al. (1997) untuk mengetahui dinamika pergerakan bean dwarf mosaic geminivirus (BDMV) dari sel ke sel pada
Phaseolus vulgaris. Pengujian presipitasi dengan memanfaatkan reaksi difusi antara antigen dan antibodi telah berhasil dilakukan oleh Mahmood et al. (1997) untuk mendeteksi wheat streak mosaic tritimovirus (WSMV).
Metode ELISA merupakan metode serologi yang dapat digunakan untuk
mendeteksi dan mengidentifikasi virus tumbuhan. Dalam metode ini antiserum
dikonjugasikan dengan enzim, sehingga bila ditambahkan substrat enzim maka
kompleks antigen-antibodi dalam jumlah yang sedikit saja dapat tervisualisasi.
Hasil yang diperoleh dapat dianalisis secara kuantitatif dengan spektrofotometer
(ELISA reader). Keuntungan uji ELISA adalah kepekaannya yang sangat tinggi, dapat menguji sampel dalam jumlah banyak secara cepat, penggunaan antiserum
prosedur pengujian yang mudah. Karena keuntungan tersebut, ELISA dengan
cepat menggantikan semua teknik seri diagnostik yang lain (Agrios 1997).
Reverse Transcription Polymerase Chain Reaction (RT-PCR)
Dewasa ini karakterisasi maupun identifikasi virus tumbuhan selain
menggunakan teknik serologi, telah banyak dikembangkan teknik molekuler
melalui analisis sidik jari DNA. Identifikasi virus banyak mengunakan teknik
Polymerase chain reaction (PCR). Teknik PCR dapat mengatasi masalah konsentrasi virus yang rendah, walaupun sampel yang digunakan sedikit dan dapat
berupa bahan segar, beku ataupun kering (Rojas et al. 1993; Wyatt dan Brown 1998). Pengujian dengan teknik PCR memerlukan sepasang primer yang spesifik
yang akan menginduksi pembentukan dan perbanyakan asam nukleat atau untai
DNA dengan bantuan enzim taq polymerase dalam mesin PCR atau thermocycler.
Pemilihan primer yang tepat sangat menentukan keberhasilan identifikasi suatu
jenis virus (Rojas et al. 1993).
PCR adalah suatu metode in vitro untuk menghasilkan sejumlah besar fragmen DNA spesifik dengan panjang dan sekuens yang telah ditentukan dari
sejumlah kecil temlate kompleks. PCR merupakan suatu teknik sangat kuat dan
sensitif yang dapat diaplikasikan dalam berbagai bidang seperti biologi molekuler,
diagnostik, genetika populasi, dan analisis forensik. Teknik DNA rekombinan
telah memberikan perubahan yang revolusioner dalam ilmu genetika karena
memungkinkan dilakukannya isolasi dan karakterisasi gen-gen, mempelajari
secara rinci fungsi dan ekspresi selama proses perkembangan terjadi, atas sebagai
suatu respon terhadap faktor lingkungan. Banyak metode kloning yang terlibat
dapat diakselerasi dan bahkan dielak dengan menggunakan PCR, dan aplikasi
baru dari teknik ini sekarang telah memungkinkan melakukan study yang dahulu
tidak bisa dilakukan (Nasir, 2002).
Polymerase chain reaction mulai berkembang pesat sekitar tahun 1987. Proses PCR pada dasarnya terdiri atas tiga tahap reaksi dengan kondisi suhu yang
berbeda secara berlang dalam beberapa siklus tertentu, yaitu denaturasi, annealing
(penempelan primer) dan ekstensi primer (sintesis DNA). Dengan reaksi
amplikasi DNA secara simultan, maka jumlah DNA sasaran akhir telah
Febrianti (2004) melakukan teknik PCR untuk mendeteksi CMV pada
tanaman lada menggunakan sepasang primer CMV-R dan CMV-F yang dibuat
berdasarkan sekuen CMV-B2 (RNA2) diperoleh ukuran pita 940 bp. Metode PCR
untuk mendeteksi PYMV dengan menggunakan sepasang primer berhasil
mengamplifikasi ukuran pita DNA 450 bp 11 (5’-primer BADNA 2 dan 3’-MYS)
dan 700 bp (primer Badna-T dan SCBV R1) (Lockhart et al. 1997; de Silva et al.
III. KOLEKSI ISOLAT LAPANG CHILLI VEINAL MOTTLE
POTYVIRUS (ChiVMV) DAN METODE DETEKSI ChiVMV
ABSTRAK
Infeksi penyakit yang disebabkan oleh virus dapat mengakibatkan kerugian ekonomi yang cukup tinggi di lapangan. Hal ini disebabkan karena virus dapat menurunkan kualitas dan kuantitas hasil tanaman. Salah satu virus utama pada tanaman cabai yang dapat menimbulkan kerugian hasil panen pada tanaman cabai di Indonesia adalah ChiVMV. Dengan metode purposive sampling, dilakukan survei ChiVMV di beberapa daerah pertanaman cabai di Sumatera Barat, Jawa Barat, Jawa Tengah, Jawa Timur, dan Kalimantan Selatan.
Hasil survei lapang yang dilakukan menunjukkan penyebaran ChiVMV yang sangat luas. Sebanyak 28.8 % sampel survei memberikan reaksi positif terhadap pengujian ChiVMV. Jumlah tanaman terinfeksi ChiVMV tertinggi adalah di Solok dan Tanah Datar (Sumatera Barat) yaitu 100% dan terendah di Megamendung (Jawa Barat), Kali Malang dan Mendem (Jawa Timur), serta Kurnia Ujung, Sukamaju, dan Golf (Kalimantan Selatan) yaitu 0%. Sebanyak tiga belas isolat ChiVMV berhasil dikumpulkan dari lima wilayah survei. Isolat tersebut kemudian diperbanyak dan dipelihara pada cabai paprika (Capsicum annuum var. Grosum). Selanjutnya lima isolat ChiVMV (CKB, KRD, TD, BL dan PANG) dipilih untuk digunakan dalam kajian lebih lanjut.
Hasil deteksi ChiVMV dengan I-ELISA dapat mendeteksi ChiVMV hingga tingkat pengenceran 1 : 10.000, sedangkan deteksi dengan DIBA dapat mendeteksi ChiVMV sampai batas pengenceran 1 : 1000 dengan efisiensi waktu yang lebih singkat dan penggunaan antiserum yang lebih sedikit. Sementara uji molekular dengan RT-PCR berhasil mendapatkan produk DNA spesifik berukuran 800 bp.
Kata kunci: Survei, ChiVMV, Capsicum
PENDAHULUAN
Chilli veinal mottle potyvirus adalah salah satu virus yang banyak menginfeksi pertanaman cabai. Penyakit ini pertama kali dilaporkan menginfeksi
pertanaman cabai di Malaysia (Burnett, 1947). Pada perkembangan selanjutnya,
ChiVMV telah menjadi masalah serius di Korea, Taiwan, Thailand, Indonesia,
Papua New Guinea, Australia, Filipina,China, Bangladesh, India, Nepal, Sri
Penelitian yang dilakukan oleh AVRDC (2000) membuktikan bahwa
ChiVMV merupakan salah satu dari lima penyakit utama pada tanaman cabai
selain cucumber mosaic virus (CMV), layu bakteri, hawar Phytophthora, dan antraknosa. Hasil survei yang dilakukan oleh Green (2004) di 16 negara Asia
melaporkan bahwa ChiVMV dapat menginfeksi pertanaman cabai hingga 30%,
mampu mereduksi hasil panen pada paprika hingga 95% dan pada cabai rawit
hingga 74%. Infeksi virus ini sangat cepat menyebar luas dilapangan karena
ditularkan oleh beberapa spesies kutudaun secara non persisten (Ong et al. 1979).
Infeksi ChiVMV pada tanaman cabai menyebabkan gejala bervariasi. Gejala
pada daun cabai dapat berupa bercak berwarna hijau tua yang tidak beraturan
(belang), penebalan tulang daun, permukaan daun tidak rata, seringkali daun
menjadi lebih kecil dan diikuti dengan malformasi daun (Siriwong et al. 1995; Kittipakorn 1991). Infeksi ChiVMV pada fase pertumbuhan awal mengurangi
ukuran daun yang diikuti dengan distorsi, serta produksi buah yang lebih sedikit
dan lebih kecil (Shah & Khalid 2001).
Beberapa penelitian tentang ChiVMV di Indonesia pada cabai telah
dilakukan. Duriat (1993) dan Taufik (2005) melakukan survei dan karakterisasi
isolat-isolat ChiVMV. Millah (2007), Riyanto (2007), dan Latifah (2007)
melakukan penelitian-penelitian yang berkaitan dengan pengembangan galur
cabai tahan ChiVMV. Namun demikian penelitian tersebut masih perlu
ditindaklanjuti. Survei dan laporan keberadaan ChiVMV di Indonesia masih
belum mencukupi karena lokasi survei masih mencakup daerah tertentu saja.
Selain itu informasi tentang kejadian penyakit ChiVMV di lapangan mungkin
berubah-ubah setiap tahun. Penelitian tentang keberadaan virus ini menjadi
penting untuk dilakukan secara berkala.
Untuk dapat mengetahui keberadaan virus dalam tanaman terinfeksi dengan
tepat diperlukan tindakan deteksi dan identifikasi. Teknik dasar yang sejak lama
dilakukan untuk mendeteksi dan mengidentifikasi virus tanaman biasanya
dilakukan melalui pengamatan partikel dengan mikroskop elektron, pengamatan
gejala, uji kisaran inang dan cara penularan virus. Perkembangan metode deteksi
virus saat ini sudah sangat maju antara lain menggunakan teknik serologi seperti
Immunobinding Assay) yang dikembangkan pada akhir 1970-an (Hull 2002). Teknik serologi ini telah digunakan secara luas dan berkembang pesat untuk
mendeteksi dan mempelajari virus tumbuhan. Deteksi dan identifikasi virus
tumbuhan juga dapat dilakukan dengan beberapa teknik molekular seperti
hibridisasi asam nukleat, ekstraksi dsDNA/dsRNA, dan PCR/RT-PCR (Matthews
2002).
TUJUAN PENELITIAN
Survei dilakukan ke beberapa daerah sentra pertanaman cabai di Sumatera
Barat, Jawa Barat, Jawa Tengah, Jawa Timur dan Kalimantan Selatan untuk
mengumpulkan isolat-isolat ChiVMV. Penelitian juga bertujuan untuk
mengevaluasi beberapa metode deteksi, yaitu I-ELISA, DIBA dan RT-PCR untuk
mengetahui metode deteksi yang paling sesuai untuk ChiVMV.
BAHAN DAN METODE Tempat dan Waktu Penelitian
Survei dan pengambilan sampel tanaman cabai dilakukan di beberapa
daerah sentra penanaman cabai di Sumatera Barat, Jawa Barat, Jawa Tengah,
Jawa Timur dan Kalimantan Selatan. Sampel tanaman sakit dibawa untuk
dilakukan diagnosis virus di Laboratorium Virologi Tumbuhan, Departemen
Proteksi Tanaman. Perbanyakan sumber inokulum dilakukan di rumah kaca
Departemen Proteksi Tanaman di Cikabayan.
Survei dan Pengambilan Sampel dari Lapang
Survei dilakukan untuk melihat kondisi tanaman di lapangan sekaligus
mengumpulkan sampel tanaman cabai yang diduga terinfeksi ChiVMV. Lokasi
survei dilakukan pada beberapa tempat yang merupakan sentra cabai di Sumatera
Barat (Tanah Datar, Solok, Agam), Jawa Barat (Mega Mendung), Jawa Tengah
(Brebes), Jawa Timur (Malang), Kalimantan Selatan (Panggong, Nusa Indah).
Pengambilan sampel di daerah Sumatera Barat dan Kalimantan Selatan dilakukan
dan Dr. Ir. Noor Aidawati M.Si (Staf pengajar Universitas Lambung Mangkurat)
sedangkan pengambilan sampel di lokasi survei di Jawa dilakukan langsung oleh
penulis. Pada setiap lokasi pengambilan sampel dilakukan dengan metode
purposive sampling, metode ini dilakukan dengan mengambil sampel secara acak dengan hanya mengambil bagian tanaman yang menunjukkan gejala khas
ChiVMV. Deskripsi gejala pada tanaman diamati menurut gejala umum yang
muncul akibat infeksi ChiVMV seperti belang, keriting, ujung daun meruncing
dan kerdil. Sampel tanaman tersebut kemudian diuji dengan metode DAS ELISA
dengan menggunakan antiserum ChiVMV, CMV, PVY, PMMV dan ToMV.
Sampel yang terinfeksi hanya oleh ChiVMV selanjutnya ditularkan ke tanaman
paprika (Capsicum annuum var Grosum) untuk perbanyakan isolat virus.
Perbanyakan Isolat Virus
Persiapan Tanaman Inang Sumber Inokulum
Tanaman untuk perbanyakan virus yang digunakan adalah bibit tanaman
paprika C. annuum var. Grosum kultivar Yolo Wonder. Benih disemai pada tanah steril dan ditumbuhkan sampai membentuk 4 - 5 daun (berumur 3 minggu). Bibit
yang sudah siap dipindahkan ke polybag dan ditempatkan pada ruang kedap serangga untuk menghindari serangan hama terutama serangga vektor virus.
Metode inokulasi Virus Secara Mekanis
Inokulasi dilakukan secara mekanis menggunakan cairan perasan tanaman
(sap) sakit. Sap dibuat dari daun tanaman yang terinfeksi ChiVMV tunggal. Daun
tersebut digerus sampai halus dengan menggunakan mortar setelah sebelumnya
ditambahkan bufer fosfat (0.01M; pH 7.0) dengan perbandingan 1:10 (b:v). Daun
tanaman yang akan diinokulasi sebelumnya ditaburi dengan carborundum (600 mesh). Sap kemudian dioleskan pada daun dengan menggunakan kapas steril
dimulai dari bagian pangkal daun ke ujung secara searah dengan tidak mengulangi
pada daerah yang sama. Setelah pengolesan sap selesai, daun tanaman uji disiram
Pengawetan Isolat ChiVMV
Isolat-isolat virus yang telah dikumpulkan dan diperbanyak di rumah kaca
sebagian disimpan dalam bentuk awetan kering agar dapat disimpan dalam waktu
lama dan menghindari hilangnya isolat mengingat banyak faktor yang
mempengaruhi sumber inokulum virus di rumah kaca. Penyimpanan isolat-isolat
virus ini dilakukan dengan metode dehidrasi sesuai dengan prosedur Djikstra dan
Jager (1998). Daun yang positif terinfeksi ChiVMV dicacah dengan silet bebas
virus. Bagian bawah cawan petri diisi dengan kalsium klorida (CaCl2) dengan
perbandingan 1 : 20 (b/b) selanjutnya dilapisi dengan kertas merang atau kertas
saring kemudian bahan yang telah dicacah sebelumnya disebarkan di atas kertas
saring. Cawan petri kemudian ditutup dan direkat dengan parafilm sehingga
menjadi kedap udara. Isolat awetan tersebut disimpan di dalam kulkas bersuhu
4oC untuk pengeringan selama satu minggu. Selanjutnya dipindahkan ke dalam
tabung plastik bertutup yang 1/3 bagian tabung tersebut telah diisi dengan CaCl2.
pada bagian atas ditutup dengan kapas steril. Setelah tabung ditutup dengan
parafilm lalu disimpan pada suhu 4oC. Untuk reaktivasi isolat virus yang telah
disimpan atau jika isolat yang disimpan tersebut akan digunakan untuk inokulasi,
maka ditambahkan 1.9 ml bufer/0.1 g bahan kering yang kira-kira setara dengan
perbandingan 1 : 5 (b/v) bahan segar.
Diagnosis ChiVMV menggunakan Metode Double Antibody Sandwich Enzyme Linked Immunosorbent Assay ( DAS-ELISA)
Deteksi ChiVMV terhadap sampel tanaman hasil survei dan ChiVMV hasil
penularan dilakukan dengan metode DAS ELISA menurut petunjuk dari DSMZ
(Clark, M.F & A.N. Adams, 1977) .
Tahapan uji tersebut diawali dengan tahap coating, yaitu sumuran plat mikrotiter di isi dengan 100 l antiserum CMV atau ChiVMV yang telah
disuspensikan ke dalam bufer coating; dilanjutkan denganinkubasi platmikrotiter pada suhu 30oC-47oC selama 2 jam atau pada suhu 4oC semalam (overnight). Keesokan harinya plat dicuci dengan PBST (phosphate buffer saline tween-20) [8 g NaCL, 02 g KH2PO4, 1,15 g Na2HPO4, 0,2 g KCL, 0,2 g NaN3, 0,5 ml Tween
(general extract buffer) [1,3 g Na2SO3, 20 g PVP- 40, 0,2 g NaN3, 2 g powdered egg albumin, 20 g Tween-20, pH 7,4] yang ditambahkan merkaptoetanol 1% dengan perbandingan 1 : 10 (w:v). Sap tanaman diambil sebanyak 100 l
kemudian dimasukkan kedalam sumuran platmikrotiter. Plat mikrotiter diinkubasi
selama 2 jam pada suhu 37oC. Platmikrotiter kemudian dicuci 5-7 kali dengan
PBST. Selanjutnya enzim konjugat yang dilarutkan dalam ECL bufer (bovine serum albumin 2 g, PVP-40 20 g, NaN3 0,2 g) sebanyak 100 l dimasukkan ke dalam sumuran dan diinkubasi pada suhu 37 oC selama 2 jam, kemudian dibilas
5-7 kali dengan PBST. PNP (P-nitrophenyl-phosphate) yang telah dilarutkan dalam PNP bufer (0.1 g MgCl2, 0.2 g NaN3, 97 ml dietanolamin), dimasukkan sebanyak 100 l kedalam sumuran plat mikrotiter dan diinkubasikan selama 30-60 menit
pada suhu ruang.
Setelah waktu inkubasi tersebut akan terjadi perubahan warna pada cairan
didalam sumuran plat mikrotiter, yaitu warna kuning, yang menandakan reaksi
positif. Reaksi segera dihentikan dengan penambahan 3M NaOH, selanjutnya nilai
absorbansi reaksi dianalisis secara kuantitatif dengan spektrofotometer Microplate reader BIO-RAD Model 550 pada panjang gelombang 405 nm. Pengujian dinyatakan positif jika nilai absorban sampel uji dua kali nilai absorban kontrol
negatif.
Deteksi ChiVMV menggunakan Metode Indirect-Enzyme Linked Immunosorbent Assay (I-ELISA)
Metode I-ELISA dilakukan berdasarkan metode Stack dan Macmillan
(2005). Sampel tanaman terinfeksi ChiVMV digerus dalam bufer coating
(sodium carbonate 0,16 g, sodium bicarbonate 0,29 g, sodium azide 0,02 g,
polyvinylpyrrolidone 2 g yang dilarutkan dalam 100 ml dH2O, pH 9,6) dengan perbandingan 1:10 (b/v). Pada penelitian ini pengenceran sampel tanaman
dilakukan dari 1 : 10 hingga 1: 106. Selanjutnya sampel tersebut dimasukkan ke
dalam masing-masing sumuran pada plat mikrotiter ELISA sebanyak 100 µl
dengan berbagai konsentrasi tergantung uji yang dilakukan dan diinkubasi pada
suhu 4 oC selama semalam. Selanjutnya masing-masing sumuran dicuci sebanyak
dilarutkan dalam bufer ECI (bovine serum albumin 0,2 g, polyvinylpyrrolidone 2 g, sodium azide 0,02 g dan dilarutkan dalam 100 ml PBST, pH 7,4) dengan berbagai konsentrasi tergantung uji yang dilakukan.
Larutan antibodi tersebut kemudian diinkubasi pada suhu 37 oC selama 2
jam. Selanjutnya masing-masing sumuran dicuci kembali dan kemudian diisi
dengan 100 µl konjugat (goat anti rabbit-IgG, Sigma, USA) yang dilarutkan dalam bufer ECI dengan perbandingan 1:1.000. Larutan konjugat tersebut
kemudian diinkubasi pada suhu ruang selama 2 jam. Setelah dicuci, sumuran
diisi dengan 100 µl substrat p-nitrophenyl phosphate (PNP) yang dilarutkan dalam bufer PNP (Magnesium chloride hexahydrate 0,025 g, sodium azide 0,05 g,
diethanolamine 24,25 ml dan dilarutkan dalam 200 ml dH2O, pH 9,8). Setelah diinkubasi pada suhu ruang selama 15 menit dilakukan pengamatan secara
kuantitatif dengan menggunakan ELISA reader pada panjang gelombang 405 nm. Reaksi dihentikan dengan cara menambahkan larutan NaOH 3 M sebanyak 50 µl
ke dalam masing-masing sumuran. Kontrol negatif yang digunakan adalah
tanaman sehat dan bufer .
Deteksi ChiVMV menggunakan Metode Dot Immunobinding Assay (DIBA)
Metode DIBA dilakukan berdasarkan metode Mahmood et al. (1997). Sebelum digunakan membran nitroselulosa (HybondTM-P, Amersham Biosciences UK) direndam dalam metanol 100% selama 10 detik dan dikering anginkan.
Jaringan daun tanaman terinfeksi ChiVMV digerus dalam tris buffer saline (TBS) dengan perbandingan 1:10 (b/v) (TBS: Tris-HCl 0,02 M dan NaCl 0,15M, pH
7,5). Selanjutnya cairan perasan tanaman tersebut diteteskan ke membran
nitroselulosa sebanyak 10 µl setiap sampel dengan berbagai konsentrasi
tergantung uji yang dilakukan. Setelah tetesan sampel kering, membran direndam
di dalam 10 ml larutan blocking non fat milk 2% dalam TBS yang mengandung
Triton X-100 dengan konsentrasi akhir 2%. Membran kemudian diinkubasi pada suhu ruang sambil digoyang dengan kecepatan 50 rpm selama 2 jam dengan
menggunakan EYELA multi shaker MMS. Membran kemudian dicuci 5 kali dengan dH2O, tiap pencucian berlangsung 5 menit sambil digoyang dengan
mengandung antibodi 5 µl ditambah non fat milk dengan konsentrasi akhir 2% dan kemudian membran diinkubasi semalam pada suhu kamar sambil digoyang
dengan kecepatan 50 rpm. Membran kemudian dicuci sebanyak 5 kali dengan
Tween 0,05% dalam TBS (TBST). Selanjutnya membran direndam dalam 5 ml TBS yang mengandung konjugat 5 µl (goat anti rabbit-IgG, Sigma, USA) ditambah non fat milk dengan konsentrasi akhir 2% dan kemudian membran diinkubasi selama 60 menit sambil digoyang dengan kecepatan 50 rpm.
Selanjutnya membran dicuci kembali dengan TBST. Membran kemudian
direndam selama 5 menit dalam 10 ml bufer substrat (Tris-HCl 0,1 M, NaCl 0,1
M dan MgCl2 5 mM) yang mengandung nitro blue tetrazolium (NBT) 66 µl dan
bromo chloro indolil phosphate (BCIP) 30 µl. Bila reaksi positif akan terjadi perubahan warna putih menjadi ungu pada membran nitroselulosa yang telah
ditetesi cairan perasan tanaman dan reaksi dapat dihentikan dengan merendam
membran dengan dH2O
Metode Deteksi ChiVMV menggunakan Metode Reverse Transcription – Polymerase Chain Reaction (RT-PCR)
Tahapan metode deteksi ChiVMV menggunakan metode RT-PCR terdiri
atas tahapan ekstraksi RNA total, transkripsi balik, dan amplifikasi cDNA.
Ekstraksi RNA Total
Metode ekstraksi RNA dilakukan mengikuti metode Qiagen dengan
menggunakan Qiagen plant RNA isolation kit.. Daun tanaman cabai yang sakit (0,1 g) digerus menggunakan pistil dan mortar steril yang didalamnya telah diisi
dengan nitrogen cair hingga menjadi bubuk. Sebanyak 450 µl bufer RLC yang
telah ditambahkan 4,5 µl merkaptoetanol dimasukkan ke dalam hasil gerusan
yang telah menjadi bubuk. Sap yang dihasilkan dimasukkan ke dalam tabung
mikro1,5 ml kemudian dipanaskan di waterbath 56 oC selama 10 menit. Selanjutnya sap dipindahkan ke dalam kolom ungu dan disentrifugasi dengan
kecepatan 13000 rpm selama 2 menit pada suhu ruang. Supernatan yang terbentuk
dipindahkan ke tabung yang baru berukuran 2 ml. Hal ini dilakukan dengan tanpa
ditambahkan ke dalam tabung yang telah diisi supernatan dan dicampurkan
dengan menggunakan pipet.
Proses selanjutnya, sebanyak 200 µl supernatan diambil dan dipindahkan ke
kolom merah jambu. RNA akan tertahan di kolom tersebut dan selanjutnya
disentrifugasi dengan kecepatan 10.000 rpm selama 30 detik. Kolom merah
jambu dipindahkan ke collection tube baru lalu ditambahkan bufer RW 700 µl, kemudian disentrifugasi lagi pada 10.000 rpm selama 30 detik. Selanjutnya kolom
merah jambu dipindahkan lagi ke collection tube baru dan ditambahkan 500 µl bufer RPE lalu disentrifugasi lagi 10.000 rpm selama 30 detik dan diulangi lagi 2
menit. Untuk memastikan bahwa kolom merah jambu bebas etanol, selanjutnya
kolom dipindahkan lagi ke collection tube baru dan disentrifugasi lagi 8000 rpm selama 1 menit. Kolom dipindahkan ke tabung mikro 1.5 ml baru dan
ditambahkan 40 µl water free nuclease ke permukaan saringan dalam kolom sehingga pelet tergenang lalu didiamkan 10 menit. Selanjutnya tabung mikro
disentrifugasi 10.000 rpm selama 1 menit. Hasil ekstraksi disimpan pada suhu
-80oC sampai akan digunakan.
Transkripsi Balik (Reverse Transcription)
Reaksi transkripsi balik ( 25 µl) terdiri atas 9 µl water free nuclease, 2.5 µl bufer RT 10x, 5 µl dNTP 10 mM, 1.5µl oligo d(T) 10 µM, 1 µl RNAseH
Inhibitor, 1 µl MmLV RT, 5 µl RNA sampel ditambahkan kedalam tabung
mikro. Tabung mikro tersebut dimasukkan ke dalam thermal cycler (Gene Amp PCR System 9700) dengan kondisi RT; 25oC selama 5 menit, 37oC selama 90
menit dan 70oC selama 15menit. Hasil akhir dari RT adalah produk cDNA yang
akan digunakan pada reaksi selanjutnya yaitu PCR.
Amplifikasi cDNA
Amplifikasi dilakukan dengan menggunakan pasangan primer yaitu
F1 (5’-TGAGGATCCTGGTGYATHGARAAYGG-3’) dan
ChiVMV-R (5’- gcgggatcctttttttttttttttttt-3’). ChiVMV-Reaksi amplifikasi (50 µl) terdiri atas 30.6 µl
mikro tersebut dimasukkan ke dalam thermal cycler (Gene Amp PCR System 9700). Amplifikasi ChiVMV dilakukan sebanyak 35 siklus mengikuti metode
Reddy (1995) melalui beberapa tahapan yaitu pemisahan utas DNA pada suhu 94 o
C selama 2 menit, penempelan primer pada DNA 55 oC selama 1 menit dan
sintesis DNA pada suhu 72 oC selama 90 detik. Khusus untuk siklus terakhir
ditambah tahapan sintesis selama 15 menit, kemudian siklus berakhir dengan suhu
4 oC.
HASIL DAN PEMBAHASAN Survei dan Pengambilan Sampel dari Lapang
Berdasarkan pengamatan di lapang diketahui bahwa terdapat variasi pola
tanam dan kultivar tanaman cabai yang digunakan (Gambar 3.1). Pada lokasi
pengamatan di Malang, tanaman cabai ditanam secara monokultur pada areal
tanam yang beragam, namun ada juga yang ditanam secara tumpangsari
bersama-sama dengan bawang (Allium cepa L), kubis (Brassica oleraceae L), atau jagung (Zea mays L) seperti di desa Kali Malang, dan Wates. Jenis dan kultivar cabai yang umumnya ditanam oleh petani di Malang antara lain Cabai besar (Hot
Beauty) dan keriting lokal. Pada semua lokasi survei, pola penanaman dilakukan
dengan bedengan dan sebagian areal ditutupi mulsa plastik. Untuk lokasi survei di
daerah Brebes, tanaman cabai umumnya ditanam dengan pola monokultur dengan
sistem bedengan yang sekelilingnya dibuat parit yang digenangi air. Air tersebut
juga digunakan untuk menyiram tanaman. Namun ada juga lahan tanaman cabai
yang ditumpangsari dengan tanaman bawang dan kadang-kadang dengan jagung,
tomat (Solanum lycopersicum L), terong (Solanum melongena L), kacang kedelai (Glycine max (L.) Merr), kacang hijau (Phaseolus radiatus L) dan kacang tanah (Arachis hypogaea L). Kultivar yang umum ditanam di Brebes adalah cabai besar (Tit Segitiga dan Randu) dan cabai keriting (TM 999). Selain itu sebagian petani
telah mengenal sistem pengendalian organisme pengganggu tanaman (OPT)
dengan menanam tanaman penghalang disekeliling tanaman utama. Saat survei di
Brebes dilakukan, gejala ChiVMV tidak ditemukan pada beberapa wilayah
terserang belalang kembara (Locusta migratoria) dan ulat gerayak (Spodoptera litura L), sehingga ada beberapa area tanam yang tanamannya tidak sempat berdaun serta kerdil.
Hasil survei lapang yang telah dilakukan menunjukkan bahwa penyebaran
ChiVMV sangat luas di lapangan. Hasil diagnosis menunjukkan bahwa ChiVMV
hampir selalu berada di pertanaman yang diamati meskipun dengan jumlah infeksi
yang berbeda-beda. Hal ini nampaknya dipengaruhi oleh keadaan iklim, pola
tanam serta jenis kultivar yang ditanam. Pada pertanaman cabai dengan pola
monokultur dalam areal yang luas, serangan virus terlihat lebih parah
dibandingkan pada lahan cabai yang ditanam bersama-sama dengan tanaman
lainnya. Hull (2002) menyatakan bahwa untuk mengurangi kejadian penyakit
virus, dapat dilakukan dengan menanam secara intercropping atau menanam komoditi bersama-sama dengan tanaman sela, misalnya menanam cabai dengan
kacang kedelai atau dengan jagung. Selain itu diperhatikan pemilihan jenis
tanaman serta waktu tanam yang sesuai. Pemilihan jenis tanaman yang tahan akan
mengurangi resiko meluasnya penyebaran virus dan penurunan hasil produksi.
Gambar 3.1 Keadaan pertanaman cabai di lokasi survei dan pengambilan sampel. (A).Tanah Datar, Sumatera Barat; (B). Mega Mendung, Jawa Barat; (C). Brebes, Jawa Tengah; (D). Mendem, Jawa Timur.
A
C
D
Pemilihan waktu tanam yang tepat sangat penting, terutama dalam
hubungannya dengan ketersediaan air, curah hujan serta gangguan hama dan
penyakit. Air diperlukan oleh tanaman cabai sejak awal pertumbuhan tanaman
sampai periode pembungaan dan pembuahan. Kekurangan air pada masa
pertumbuhan vegetatif dan pada masa pembentukan bunga menyebabkan tanaman
cabai tumbuh kerdil dan menurunkan hasil buah, bahkan dapat gagal panen
(Welles 1990). Tetapi lahan yang terlalu lembab juga menyebabkan pertumbuhan
tanaman cabai terhambat. Curah hujan yang tinggi pada saat pembentukan bunga
dan buah dapat menggugurkan bunga dan menyebabkan pembusukan buah
(Sumarni 1996). Sementara pemilihan waktu tanam yang serentak akan
mengurangi terbentuknya sumber inokulum virus yang bertahan di lapangan
karena selalu tersedianya sumber infeksi di lapangan.
Diagnosis Sampel dari Lapang dengan DAS-ELISA
Hasil DAS-ELISA pada 135 sampel bergejala yang dikumpulkan dari 22
lokasi survei menunjukkan 28,88 % sampel terinfeksi ChiVMV. Proporsi jumlah
jumlah sampel yang bereaksi positif terhadap antiserum ChiVMVmenunjukkan
hasil yang beragam pada lokasi survei (Tabel 3.1).
Persentase sampel yang memberikan reaksi positif untuk masing-masing
lokasi survei secara berturut-turut adalah 72,72%, 0%, 55%, 20%, dan 33,33%
(Sumatera Barat, Jawa Barat, Jawa Tengah, Jawa Timur dan Kalimantan Selatan).
Hasil survei yang telah dilakukan juga menunjukkan bahwa ChiVMV dapat
menginfeksi tanaman cabai secara tunggal maupun bersama-sama dengan virus
Tabel 3.1 Deteksi ChiVMV menggunakan metode DAS ELISA pada sampel
Mega Mendung 0/5 (0) Monokultur/ Hot Beauty
Jawa Timur
Mbokor 8/15 (53.33) Monokultur/ Hot Beauty
Kali Malang 0/12 (0) Tumpangsari/ Huang Dong
Karang Juwet 2/8 (25.00) Monokultur/ Hot King
Mendem 0/10 (0) Tumpangsari/ Rawit lokal
Belung 4/20 (20.00) Tumpangsari/ Hot Beauty
Nongko Sewu 0/8 (0) Monokultur/ Hot Beauty
Wates
3/12 (25.00) Tumpangsari/Keriting lokal
Jawa Tengah
Kemukten 2/4 (50.00) Monokultur/Tit Segitiga
Kersana 3/5 (60.00) Tumpangsari/Randu
Keradenan 3/6 (50.00 Tumpangsari/Tit Segitiga
Sitanggal 3/5 (60.00) Monokultur/Tit Segitiga
Kalimantan Selatan
Nilai ditentukan berdasarkan hasil deteksi dengan DAS ELISA, yaitu dengan membandingkan jumlah sampel tanaman bereaksi positif terhadap jumlah sampel total.
- Tidak ada informasi
Hasil penelitian Taufik (2005) melaporkan bahwa ChiVMV seringkali
ditemukan berada bersama-sama dengan CMV di lapangan. Walaupun demikian
deteksi DAS ELISA dengan menggunakan antiserum CMV, ChiVMV, PVY,
TMV dan PMMV menunjukkan bahwa infeksi virus yang dominan di lokasi
Tabel 3.2 Deteksi beberapa virus pada sampel tanaman cabai
* CMV = cucumber mosaic virus; ChiVMV = chilli veinal mottle potyvirus; PVY = potato virus Y; TMV = tobacco mosaic virus; PMMV = pepper mottle mosaic virus.
Perbanyakan Isolat ChiVMV
Dari hasil deteksi dengan DAS ELISA, sampel-sampel yang positif
terinfeksi ChiVMV dengan gejala tunggal kemudian diperbanyak di rumah kaca.
Terdapat 13 isolat ChiVMV yang berhasil diperbanyak di rumah kaca pada
tanaman paprika (C. annuum var. Grossum). Dari ketigabelas isolat tersebut
selanjutnya dipilih 5 isolat yang mewakili masing-masing daerah lokasi survei.