PENETAPAN METODE ANALISIS P TERSEDIA
TANAH ENTISOL
S K R I P S I
MULYANIS RAHMI
030303047
DEPARTEMEN ILMU TANAH
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN METODE ANALISIS P TERSEDIA
TANAH ENTISOL
S K R I P S I
MULYANIS RAHMI
030303047
Skripsi Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana di Fakultas Pertanian Universitas Sumatera Utara, Medan
Dibimbing Oleh
Ir. Mukhlis, MSi Ir. A. B. Sinulingga, SU
Ketua Anggota
DEPARTEMEN ILMU TANAH
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
ABSTRACT
ABSTRAK
RIWAYAT HIDUP
Penulis dilahirkan di Padang Panjang pada tanggal 06 Oktober 1985 dari
ayah Syukri dan Ibu Emy Yustiti. Penulis merupakan anak kedua dari delapan
bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 2 Padang Panjang dan pada
tahun yang sama lulus seleksi masuk Universitas Sumatera Utara (USU) melalui
jalur SPMB. Penulis memilih program studi Ilmu Tanah Departemen Ilmu Tanah,
Fakultas Pertanian.
Selama mengikuti perkuliahan, penulis menjadi asisten mata kuliah agama
Islam, Perancangan Penelitian Tanah dan Analisis Tanah dan Tanaman.
Mengikuti organisasi BKM Al-Mukhlisin (2004-2007), KAM RABBANI FP
USU (2006-2007), Pengajian Al – Bayan dan organisasi Himpunan Mahasiswa
Departemen Ilmu Tanah.
Penulis melaksanakan praktek kerja lapangan di PTPN III Kebun Sei
KATA PENGANTAR
Puji dan Syukur penulis panjatkan kepada Allah SWT karena atas berkah,
rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini.
Judul dari penelitian ini adalah Penetapan Metode Analisis P Tersedia
Tanah Histosol dibawah bimbingan Ir. Mukhlis, MSi dan Ir. A. B. Sinulingga, SU
Terima kasih penulis sampaikan kepada Ir. Mukhlis, MSi
dan Ir. A. B. Sinulingga, SU selaku komisi pembimbing, Dr. Ir. Abdul Rauf, MP
Ir. Bintang Sitorus, MP, Jamilah, SP. MP, Dr. Ir. Hamidah Hanum, MP
dan Ir. Fauzi, MP serta seluruh dosen di Departemen Ilmu Tanah yang banyak
memberikan ilmu dan saran.
Teristimewa ungkapan terima kasih dan rasa hormat penulis sampaikan
kepada ayahanda Syukri Kt. Mudo dan ibunda Emy Yustiti serta seluruh keluarga
besar, Ibu Hj. Nurlena A. M. Pd atas kepercayaan dan doanya. Penghargaan
penulis berikan kepada Yayasan Leuser Indonesia, Keluarga Besar BKM Al
Mukhlisin (ukhti lina, mimi, yani, syam, eci, listia siti, nisa, syari dan ukhtiku
semua) jazakillah khairan katsiro. Bang Anwar dan keluarga, Sri Budiarti SS,
Arliza, Yeni dan Nanda serta seluruh stambuk 2003 atas kebersamaan selama ini.
Keluarga pondok pelangi atas ukhwahnya dan seluruh asisten laboratorium Kimia
dan kesuburan Tanah serta seluruh pihak yang banyak membantu dalam
pelaksanaan penelitian ini. Tanpa mereka semua penulis tidak ada dan bukanlah
siapa – siapa. Semoga skripsi ini bermanfaat.
Medan, November 2007
DAFTAR PUSTAKA ... 26
DAFTAR TABEL
No. Tabel Hal
1. Perlakuan pemberian pupuk P ... 13
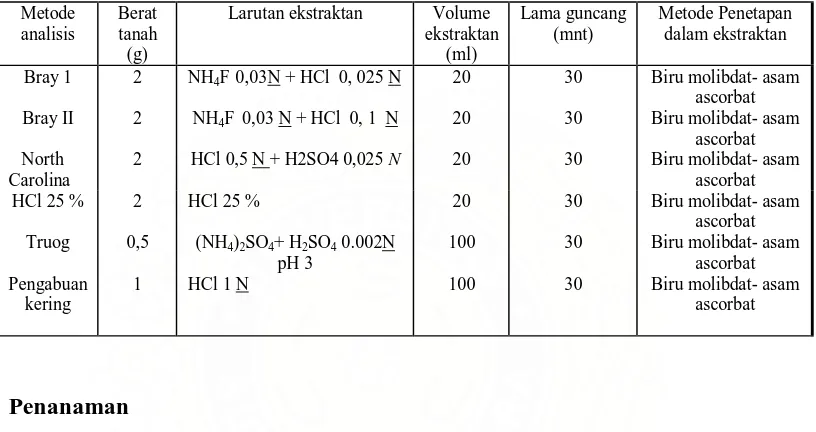
2. Metode analisis P tersedia tanah ... 14
3. Kadar P tersedia tanah 10 hari setelah pemupukan P menggunakan
beberapa metode ... 17
4. Tinggi tanaman, berat kering tajuk dan akar serta serapan P tanaman ... 18
DAFTAR LAMPIRAN
No. Lampiran Hal
1. Analisis awal tanah Entisol ... 28
2. Bagan penelitian di Rumah kaca FP USU……….……..29
3. Perhitungan kebutuhan pupuk P ... 30
4. Rataan kadar P tanah hasil analisis metode Bray I ... 32
5. Daftar sidik ragam kadar P tersedia tanah hasil analisis metode Bray I .. 32
6. Rataan kadar P tersedia tanah hasil analisis metode Bray II ... 33
7. Daftar Sidik Ragam kadar P tersedia tanah hasil analisis metode Bray II . 33 8. Rataan kadar P tersedia tanah hasil analisis metode North Carolina ... 34
9. Daftar Sidik kadar P tersedia tanah hasil analisis metode North Carolina..34
10. Rataan kadar P tanah hasil analisis metode HCl 25 %... 35
11. Daftar sidik ragam kadar P tersedia tanah hasil analisis metode HCl 25 %32 ... 35
12. Rataan kadar P tersedia tanah hasil analisis metode Truog ... 36
13. Daftar Sidik Ragam kadar P tersedia tanah hasil analisis metode Troug... 36
14. Rataan kadar P tersedia tanah hasil analisis metode Pengabuan kering .... 37
15. Daftar sidik ragam kadar P tersedia tanah hasil analisis metode Pengabuan kering ... 37
16. Rataan serapan P tanaman jagung pada masa akhir vegetatif ... 38
17. Daftar sidik ragam serapan P tanaman jagung pada akhir masa vegetatif……… 38
18. Rataan tinggi tanaman jagung pada masa akhir vegetatif ... 39
19. Daftar sidik ragam tinggi tanaman jagung pada akhir masa vegetatif…. ...39
21. Daftar sidik ragam berat kering tajuk tanaman jagung pada akhir masa
vegetatif………. 40
22. Rataan berat kering akar tanaman jagung pada masa akhir vegetatif ... 41
23. Daftar sidik ragam berat kering akar tanaman jagung pada akhir masa vegetatif ………. 41
24. Kriteria penilaian sifat – sifat tanah………42
25. Metode analisis P tersedia tanah metode Bray I……….. 43
26. Metode analisis P tersedia tanah metode Bray II……….. 46
27. Metode analisis P tersedia tanah metode North Carolina………...49
28. Metode analisis P tersedia tanah metode HCl 25 %………...52
29. Metode analisis P tersedia tanah metode Truog……….………. … 55
30. Metode analisis P tersedia tanah metode Pengabuan kering………..58
31. Foto tanaman dan kegiatan ………59
PENDAHULUAN
Latar Belakang
Tanah Entisol merupakan tanah yang baru berkembang sehingga sangat
potensial untuk dijadikan lahan pertanian baik tanaman pangan dan perkebunan.
Meskipun tanah ini sangat potensial, tapi dalam perkembangan tanahnya sangat
bergantung pada bahan induk dan topografi sehingga akan berpengaruh terhadap
kesuburan tanahnya seperti pemadatan, sifat kimia tanah bervariasi dan besarnya
kehilangan air infiltrasi. Sebagai tanah yang baru terbentuk perlu dikaji sifat –
sifat tanah yang dapat mempengaruhi kesuburan tanah dan keberadaan unsur
haranya.
Fosfor (P) merupakan unsur hara esensial yang sangat dibutuhkan oleh
tanaman dalam jumlah besar, sedangkan jumlah P dalam tanah dan tanaman
relatif sedikit dibandingkan unsur hara esensial lainnya. Hal ini disebabkan oleh
unsur P bersifat mobil atau mudah bergerak antar jaringan
(Rosmarkam dan Yuwono, 2002) sehingga mudah mengalami fiksasi. Proses
fiksasi dapat mengakibatkan pemupukan P menjadi tidak maksimal diserap
tanaman. Agar pemupukan P lebih efektif perlu diketahui kadar ketersediannya
didalam suatu jenis tanah.
Ketersedian P tanah entisol dapat diketahui dengan adanya suatu metode
analisis yang dapat menggambarkan dan mendeteksi ketersedian P dalam tanah
yang sebenarnya. P tersedia merupakan P yang dapat diserap oleh tanaman.
sangat sesuai adalah yang memberikan korelasi yang tinggi antara hasil analisis
dengan serapan P tanaman. Korelasi uji tanah dapat menentukan metode analisis
yang sesuai untuk suatu jenis tanah sehingga untuk mengetahui metode analisis P
tersedia yang tepat di tanah entisol maka dilakukan uji korelasi.
Tujuan Penelitian
Untuk menetapkan metode analisis P tersedia tanah yang tepat untuk
tanah Entisol
Hipotesa Penelitian
Metode analisis P tersedia yang tepat untuk tanah Entisol dapat ditentukan
dengan melakukan uji korelasi.
Kegunaan Penelitian
o Sebagai bahan informasi bagi pihak yang membutuhkan.
o Sebagai salah satu syarat untuk meraih gelar sarjana di Fakultas
TINJAUAN PUSTAKA
Tanah Entisol
Konsep pemikiran dari Entisol adalah (recent = umur geologi
Holosin, solum = tanah) adalah tanah mineral yang masih muda
(Holosin), tanah yang baru diendapkan, belum atau masih sedikit mengalami
pelapukan atau berasal dari sisa erosi. Termasuk tanah ini adalah tanah yang
belum memiliki horison pedogenik dan umumnya masih berupa lapisan – lapisan
tanah atau tanah yang hanya memiliki satu atau dua horison pedogenik tertentu
(Hardjowigeno, 1993; Munir, 1996; Subagyo dkk., 2000). Menurut Taksonomi
Tanah, entisol didefinisikan sebagai tanah yang memenuhi syarat bila regim
suhu adalah mesi, isomesik atau lebih panas dan pada waktu kering ditemukan
retakan – retakan sampai selebar 1 cm pada kedalaman 50 cm tapi pada kadar liat
< 39 %, di beberapa sub horison pada kedalaman < 50 cm dan salah satu syarat
dari kriteria berikut ini yaitu bahan sulfidik pada kedalaman < 50 cm dari
permukaan tanah mineral atau mempunyai horison penciri epipedon okhrik,
albik, anthropik, histik atau spodik pada kedalaman lebih dari 2 meter
( Munir, 1996).
Proses pembentukan Entisol dipengaruhi oleh beberapa faktor diantaranya
iklim yang sangat kering sehingga proses pelapukan berjalan lambat, erosi yang
kuat sehingga mampu membawa bahan endapan lebih banyak dari yang dibentuk
melalui proses pedogenik, pengendapan terus – menerus, bahan induk yang sukar
Tanah entisol terdiri dari 5 sub ordo dan 4 diantaranya termasuk dalam
tanah pertanian utama yaitu Aquent yaitu entisol basah yang selalu jenuh air
sehingga drainase terhambat, Fluvent terbentuk dari bahan endapan di dataran
banjir sungai, Psamment, entisol bertekstur pasir atau berlempung dan Orthent
yaitu entisol berpenampang dangkal atau tipis dan berbatu di lereng – lereng
curam (Subagyo dkk., 2000)
Fluvent dan aquents (tanah aluvial) terdapat di dataran-dataran banjir pada
lembah-lembah sungai dan di dataran pantai, yang menerima endapan baru dari
lembah-lembah sungai dan di dataran pantai, yang menerima endapan baru dari
tanah aluvial secara berkala ( Nordin, 2006)
Jenis tanah fluvents penting di dataran banjir di tepi sungai atau danau di
Kalimantan. Tanah-tanah ini umumnya terdapat di sungai-sungai yang
mengangkut endapan yang rawan terhadap banjir dan perubahan aliran sungai.
Kandungan mineral dan kesuburan tanah tropofluvents tergantung pada formasi
geologi di daerah aliran sungai bagian hulu dan topografi daerah sekitarnya. Dua
lingkungan utama yang bertanah aluvial adalah muara sungai dan rawa-rawa
belakangnya (Nordin, 2006).
Tanah-tanah aluvial baru yang berasosiasi dengan air tawar sebagian
besar mendukung hutan-hutan rawa air tawar. Tanah aluvial yang lebih baru ini
umumnya lebih subur dari pada lereng-lereng sekitarnya, tetapi tidak sesubur
tanah aluvial laut atau abu vulkanik Tanah-tanah aluvial di dataran tepi sungai
adalah tanah-tanah yang paling subur dan merupakan habitat yang mudah
tanah muda yang mencolok, umumnya terdapat pada pantai-pantai muda maupun
pantai tua (Nordin, 2006)
Sifat dan Ciri Tanah Entisol
Tanah aquents jenuh air dalam suatu periode yang panjang dalam satu
tahun dengan ciri khas dalam, berwarna abu-abu dan warna lainnya; tingkat
kesuburannya bergantung pada kandungan mineral dan bahan organik endapan
aluvial asalnya. Tanah hydraquents terdapat di rawa pasang surut, tanah ini muda,
lunak, berlumpur dan belum berkembang. Tanah sulfaquents umumnya terdapat
bersama-sama dengan hydraquents. Tanah -tanah ini sangat terbatas untuk tanah
pertanian, karena mengandung pirit yang apabila teroksidasi akan menimbulkan
kondisi yang sangat masam dengan kadar besi dan aluminium sulfat yang cukup
tinggi sehingga bersifat beracun ( Suhardjo dkk., 2000; Noor, 2004; Nordin, 2006)
Kapasitas umum menyimpan zat-zat hara pada tanah-tanah sebagian besar
bergantung pada kandungan humus. Oleh karena itu kandungan zat hara yang
sangat rendah bila lapisan humusnya rendah, misalnya pada tanah-tanah pasir. Di
dalam tanah yang dalamnya satu meter, hampir setengahnya dari basa yang
diserap hanya terdapat dalam lapisan atas sedalam 25 cm (Nordin, 2006).
Kesuburan tanahnya bervariasi bergantung pada bahan induk dan topografi
seperti reaksi tanah antara Aquent dan Fluvent atau Psamment. Reaksi tanah
aquent biasanya masam sampai agak masam (pH 4,7 – 6,6), Fluvent dan Orthent
cenderung masam sampai agak masam (pH 5,0 – 6,5) sedangkan Psamment
lebih masam dari lapisan atas. Kejenuhan basa bervariasi, KTK bervariasi baik
antara horison A maupun C, kandungan P bervariasi sebagian sangat rendah
sampai tinggi pada semua lapisan (Subagyo dkk., 2000; Ritung dan Wahyunto,
2003).
Unsur Hara P
Fosfor (P) merupakan unsur yang diperlukan dalam jumlah besar ( hara
makro) yang berfungsi sebagai penyusun sel hidup, terutama dalam pembelahan
dan pembentukan membran sel, berperan aktif dalam mentranfer energi yakni
merubah ADP menjadi ATP (Hakim dkk., 1996). P diserap tanaman dalam bentuk
ion orthofosfat H2PO4- dan HPO4-2 dan ion ini tidak diikat oleh liat ataupun
koloid organik karena muatannya sama (Rosmarkam dan Yuwono, 2004)
P tanah dapat dibedakan menjadi tak tersedia, potensial tersedia dan segera
tersedia. P segera tersedia adalah bentuk P anorganik di larutan tanah. Bentuk
yang potensial tersedia meliputi bentuk P organik dan beberapa bentuk P
anorganik yang relatif tidak tersedia seperti bentuk P terendapkan (Al – P, Ca – P
dan Mn – P) dan bentuk ini cenderung terakumulasi dalam keadaan stabil dan
dalam keadaan tertentu dapat menjadi tersedia seperti penggenangan pada
tanah sawah (Mukhlis, 2007). Umumnya bentuk P organik ditemukan dalam
bentuk inositol fosfat terutama hexafosfat (60 % dari total P organik). Bentuk –
bentuk lain seperti fosfolipid, asam nukleat, glukosa 1 – fosfat, gliserol fosfat dan
protein fosfat dalam tanah hanya berkisar 2 % dari total P organik
Adanya reaksi – reaksi pelepasan anion P kedalam larutan tanah dan
penjerapan dari larutan tanah berkaitan erat dengan pH larutan tanah dapat
digambarkan dalam kesetimbangan senyawa P di dalam tanah sebagai berikut
+ OH- + OH
-H2PO4- H2O + HPO4-2 H2O + PO4-3
Reaksi ini memperlihatkan bahwa pada kisan pH dari asam sampai basa, larutan
tanah dapat mengandung berbagai bentuk anion P. Pada pH 6,0 larutan tanah di
dominasi bentuk H2PO4- dan HPO4- dan basa di dominasi oleh PO4-3.
(Poerwowidodo, 1992).
Analisis P Tanah
P tersedia dalam tanah dapat diartikan sebagai P tanah yang dapat larut
dalam air dan asam sitrat. Berdasarkan kelarutan dan ketersediannya dalam tanah
maka bentuk P dalam tanah dapat dibedakan ke dalam P yang dapat larut dalam
air merupakan bentuk P yang segera dapat diserap tanaman, bentuk Al – P yang
dapat diekstraksikan dengan NH4F, bentuk Fe – P dapat diekstraksikan oleh
NaOH dan Ca – P yang dapat diekstraksikan oleh campuran Na sitrat dan Na
ditionat (Hakim dkk., 1986).
P tersedia tanah dapat dianalisis dengan berbagai metode. Larutan
ekstraktan yang direkomendasikan cukup banyak, Fixen dan Grove (1990)
mendata beberapa ekstraktan P dalam menetapkan P tersedia tanah yaitu :
- Soltanpour dan Schwab (1977) menggunakan ekstraktan 1 M NH4 HCO3 +
0,005 M DTPA pada pH 7,5
- Bray dan Kurtz (1945) menggunakan ekstraktan 0,03 M NH4 F+ 0,0025 M
- Dyer (1894) menggunakan asam sitrat 1 % pada temperatur konstan
selama 7 hari
- Egner et. al (1960) menggunakan ekstraktan 0,01 M Ca laktat + 0,02 M
HCl
- ISFEIP (1972) menggunakan ekstraktan 0,25 M NaHCO3 + 0,01 M NH4 +
0,01 EDTA pada pH 8,5
- Menlich (1953) menggunakan ekstraktan 0,05 M HCl + 0,0125 M H2So4
- Menlich (1978) menggunakan ekstraktan 0,015 M NH4F + 0,2 M
CH3COOH + 0,2 M NH4Cl + 0,012 M HCl
- Menlich (1984) menggunakan ekstraktan 0,015 M NH4F + 0,2 M
CH3COOH + 0,25 M NH4NO3 + 0,013 M HNO3
- Olsen et. al (1954) menggunakan ekstraktan 0,5 M NaHCO3 pada pH 8,5
- Troug (1930) menggunakan ekstraktan 0,001 M H2SO4 + (NH4)2SO4 pada
pH 3.
Fixen dan Grove (1990) menetapkan bahwa ektraktan yang baik harus
mampu mengekstrak P tersedia tanah, prosedurnya harus bekerja cepat dan tepat
dan nilai uji tanah yang ditentukan harus berkorelasi dengan pertumbuhan
tanaman atau respon P. Pengekstrak tidak menganggu proses analisa, harga bahan
kimia rendah dan mudah dikerjakan (Widjik dkk., 1984) disamping itu metode
tersebut harus menghasilkan angka yang diteliti.
Penelitian korelasi uji tanah dapat menentukan metode ekstraksi yang
sesuai untuk berbagai komoditi pada berbagai jenis tanah. Al – Jabri dkk (1984)
melaporkan bahwa pengekstrak Troug dimodifikasi, HCl 25 %, dan Bray 2
Sitiung untuk tanaman padi gogo. Widjaja- Adhi dan Widjik (1984) melaporkan
metode Bray 1 adalah metode terbaik untuk tanah Hydric dystrandepts untuk
tanaman kentang. Menurut Nursyamsi dan Sutriadi (2002) pengekstrak HCl 25 %
dan Corlwell merupakan pengekstrak terbaik untuk menetapkan status hara P
untuk tanaman kedelai pada Ultisol Deli Serdang, Bray 1 dan Olsen untuk
Inseptisol Subang dan Olsen untuk Vertisol. Nursyamsi dkk (2004) menyatakan
pengekstrak Bray 1 sebagai metode yang terbaik untuk menduga kebutuhan P
tanaman kedelai pada tanah typic Kandiudox. Selanjutnya Iboy (2006)
melaporkan pengekstrak Bray 2 merupakan metode yang terbaik untuk tanah
sawah.
Pengukuran laturan P yang telah terekstrak bisa dilakukan secara
Spektofotometer. Spektrofotometer merupakan instrumen yang digunakan untuk
mengukur transmitan atau adsorban pada berbagai panjang gelombang warna
dengan menggunakan molibdat dan asam ascorbat. Ion orthofosfat dan molibdat
berkondensasi dalam larutan asam heteropoli untuk menghasilkan asam
molibdofosfat heteropoli (asam fosfat molibdat). Asam molidofosfat yang
dihasilkan direduksi dengan hidrazinium sulfat sehingga menghasilkan kompleks
warna biru yang dapat larut. Intensitas warna biru sebanding dengan banyaknya P
yang mula- mula dimasukkan dalam asam heteropoli selektif menghasilkan warna
biru. Intensitas warna biru sebanding dengan banyaknya P yang mula – mula
dimasukkan dalam asam heteropoli. Keuntungan spektrofotometer adalah
memberikan cara sederhana untuk menetapkan kuntitas zat yang sangat kecil dan
merupakan metode yang paling tepat untuk konsentrasi zat – zat terlarut
METODOLOGI PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Rumah Kaca dan Laboratorium Kimia dan
Kesuburan Tanah Fakultas Pertanian Universitas Sumatera Utara, Medan.
Penelitian ini dimulai dari bulan Mei sampai Oktober 2007.
Bahan dan Alat Penelitian
Bahan
- Tanah entisol sebagai media tanam yang diambil secara komposit dari
Desa Air Mancur, Kecamatan Pulau Tiga, Kabupaten Aceh Tamiang
- Pupuk SP – 36 ( 36% P2O5) sebagai sumber pupuk P, Urea (45% N) dan
MOP (60% K2O) sebagai pupuk dasar.
- Benih jagung sebagai tanaman indikator
- Air untuk memenuhi kebutuhan tanah dan tanaman
- Bahan – bahan kimia untuk keperluan analisis di Laboratorium.
Alat
- Cangkul, sekop, dan goni untuk pengambilan contoh tanah entisol
- Polibag sebagai wadah tanah
- Meteran untuk mengukur tinggi tanaman
- Timbangan untuk menimbang tanah, pupuk dan berat kering tanaman
- Alat – alat laboratorium untuk keperluan analisis.
Metode Penelitian
Penelitian menggunakan Rancangan Acak Kelompok (RAK) non faktorial
dengan perlakuan pemberian pupuk P yang terdiri dari 9 taraf (Tabel 1) dan 3
ulangan sehingga didapat 27 satuan percobaan.
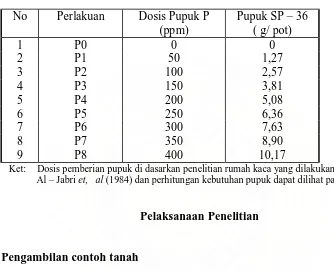
Tabel 1. Perlakuan Pemberian Pupuk P
No Perlakuan Dosis Pupuk P
Ket: Dosis pemberian pupuk di dasarkan penelitian rumah kaca yang dilakukan oleh
Al – Jabri et, al (1984) dan perhitungan kebutuhan pupuk dapat dilihat pada lampiran 3.
Pelaksanaan Penelitian
Pengambilan contoh tanah
Contoh tanah histosol diambil di lokasi yang telah ditentukan secara
komposit. Tanah dimasukkan kedalam polibag 4 kg setara tanah kering oven,
kemudian di beri perlakuan pupuk P sesuai dengan taraf perlakuan (0, 50, 100,
150, 200, 250, 300, 350, dan 400) ppm P dan di inkubasi selama 10 hari, setelah
itu contoh tanah diambil untuk dianalisis kadar P tersedia tanah dengan berbagai
Analisis Awal
Dilakukan analisis awal sifat kimia tanah meliputi % kadar air dan %
kapasitas lapang, pH tanah dengan metode elektrometri, % C organik metode
Walkley & Black, P Tersedia metode Bray II dan KTK metode ekstrak NH4 Oac
(lampiran 1)
Tabel 2. Metode Analisis P tersedia tanah
Penanaman
Setelah diinkubasi selama 10 hari dilakukan penanaman benih sebanyak 3
benih per polibag. Pupuk dasar di berikan pada saat penanaman yang terdiri dari
200 ppm Urea dan 200 ppm MOP. Penjarangan dilakukan setelah tanaman
berumur 2 minggu dengan meninggalkan satu tanaman yang pertumbuhannya
dianggap baik.
Pemeliharaan
Pemeliharaan dilakukan dengan menyiram tanaman setiap hari sampai
tanah dalam keadaan kapasitas lapang melalui pipa yang telah di lobangi sisinya.
Penyiangan gulma dilakukan secara terus menerus dan pemberantasan hama dan
penyakit di lakukan secara preventif dengan menyemprotkan insektisida.
Pemanenan
Pada akhir masa vegetatif (munculnya bunga) diambil contoh daun untuk
dianalisis kadar hara P daun serta berat kering tanaman dimana bagian tajuk dan
akar tanaman dipotong dan diovenkan pada suhu 70 °C selama 24 jam kemudian
ditimbang berat kering tajuk dan akar tanaman.
Pengamatan Parameter
1. Kadar P tersedia (ppm) diukur 10 hari setelah perlakuan
2. Tinggi tanaman (cm) diukur pada akhir masa vegetatif
3. Berat kering tajuk (g) diukur pada akhir masa vegetatif
4. Berat kering akar (g) duikur pada akhir masa vegetatif
5. Serapan P tanaman (mg/ tan) dihitung dari kadar P tanaman dan berat
kering tajuk.
Uji Statistik
Data yang diperoleh melalui analisis pengukuran dengan beberapa metode
pengekstrak, diuji menggunakan uji korelasi. Nilai kadar P tersedia tanah dari
setiap metode ditetapkan sebagai variabel x, sedangkan hasil pengukuran
parameter tanaman ( serapan P tanaman dan berat kering tajuk) sebagai variabel y
sehingga diperoleh nilai koefesien korelasinya yaitu nilai r.
Nilai r diperoleh dari rumus :
Dimana : r = Nilai koefesien relasi
ΧΥ
∑ = jumlah variabel x dikalikan dengan variabel y
n = jumlah perlakuan
SDx = standar deviasi variabel x
SDy = standar deviasi variabel y
Nilai koefesien korelasi r dari masing – masing metode yang tertinggi
HASIL DAN PEMBAHASAN
Hasil
Hasil analisis kadar P tersedia tanah entisol yang diberikan perlakuan
0 – 400 ppm pupuk P yang dianalisis dengan beberapa metode analisis P tersedia,
cenderung menunjukkan peningkatan nyata terhadap semua metode P yang
diujikan (lampiran 4 – 14)
Rataan kadar P tersedia yang teranalisis dari masing – masing metode
memperlihatkan hasil yang beragam (Tabel 3)
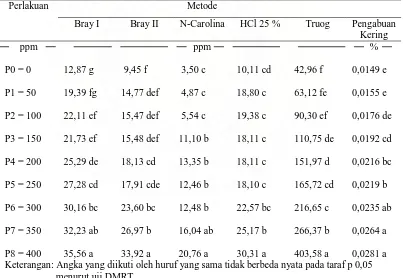
Tabel 3. Kadar P tersedia tanah entisol 10 hari setelah pemupukan
Perlakuan Metode Keterangan: Angka yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf p 0,05
menurut uji DMRT
Dari tabel 3 dapat dilihat bahwa semakin tinggi dosis yang diberikan
masing – masing metode, metode Truog menghasilkan kadar P tersedia yang
relatif lebih tinggi dibanding dengan metode lainnya.
Peningkatan kadar P tersedia akibat pemberian pupuk juga diikuti oleh
tinggi tanaman, berat kering tajuk dan akar serta serapan P tanaman
(lampiran 15 – 23). Rataan tinggi tanaman, berat kering tajuk dan akar serta
serapan P tanaman dapat dilihat pada tabel 4.
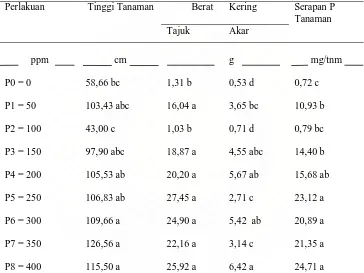
Tabel 4. Tinggi tanaman, berat kering tajuk, berat kering akar dan serapan P
Perlakuan Tinggi Tanaman Berat Kering Serapan P
Keterangan: Angka yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf p 0,05 menurut uji DMRT
Dari tabel 4 dapat dilihat bahwa semakin tinggi dosis pupuk P yang
diberikan akan meningkatkan tinggi tanaman, berat kering akar dan tajuk dan
serapan P tanaman. Peningkatan pemberian dosis pupuk P memberikan pengaruh
yang tidak bebeda nyata terhadap tinggi tanaman. Peningkatan berat kering tajuk
terlihat pada dosis P1 = 50 ppm berat kering akar pada P3 = 150 ppm dan serapan
Pemilihan metode analisis P tersedia tanah Entisol yang tepat adalah
metode yang ekstraktannya mampu mengekstrak bentuk P yang sama dengan
bentuk P yang diserap oleh tanaman. Sehingga untuk menentukan metode analisis
P tersedia yang tepat dilakukan uji korelasi antara kadar P yang terekstrak dari
masing – masing metode dengan berat kering tajuk dan serapan P tanaman.
Hasil uji korelasi antara kadar P tersedia tanah dengan berat kering tajuk
dan serapan P tertera pada tabel 5.
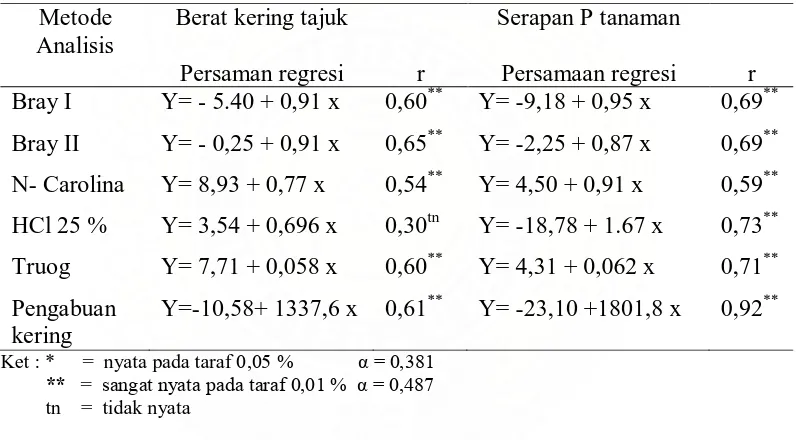
Tabel 5. Persamaan regresi dan koefisien korelasi antara kadar P tersedia tanah dengan berat kering tajuk dan serapam P tanaman.
Metode Analisis
Berat kering tajuk Serapan P tanaman
Persaman regresi r Persamaan regresi r
Bray I Y= - 5.40 + 0,91 x 0,60** Y= -9,18 + 0,95 x 0,69**
Dari tabel 5 dapat dilihat bahwa metode analisis yang tepat adalah
pengabuan kering karena memberikan koefisien korelasi yang tertinggi yakni
r = 0,92 pada serapan P. Pada berat kering tajuk metode analisis Bray II dan
pengabuan kering memiliki koefisien korelasi yang relatif lebih tinggi dari metode
Pembahasan
Kemampuan setiap ekstraktan dari masing – masing metode dalam
mengekstrak P yang terdapat dalam tanah Entisol berbeda – beda, hal ini dapat
dilihat dari nilai kadar P tersedia tanah yang terekstrak dari masing – masing
metode sangat beragam.
Menurut Poerwowidodo (1991) metode Bray I dan Bray II digunakan
untuk menetapkan kandungan P terjerap dan P larut dalam asam dengan
menggunakan larutan pengekstarak NH4F dan HCl yang akan membebaskan ion
– ion F untuk mengikat Al – Fe dan senyawa P dalam larutan asam sehingga ion P
nya dibebaskan.
Metode North Carolina berprinsip bahwa P yang terlarut dalam
asam merupakan ukuran P tersedia didalam tanah – tanah asam dan netral. Pada
metode ini ekstraktan yang digunakan adalah HCl dan SO4, reaksinya menurut
Poerwowidodo (1991) sebagai berikut:
AlPO4 + HCl + H2SO4 PO3-2 + H2O + Al Cl3 + Al2 (SO4)3
FePO4 + HCl + H2SO4 PO3-2 + H2O + Fe Cl3 + Fe2 (SO4)3
selanjutnya,
PO4-3 + 12 MoO4-2 + 27 H+ H7[P (Mo2O7)6] + 10 H2O
H7[P (Mo2O7)6 + vit C Biru molibden
Dari masing – masing metode, metode Truog menggunakan ekstraktan
NH4SO4 menghasilkan kadar P tersedia yang relatif lebih tinggi dibandingkan
dengan ekstraktan lainnya. Hal ini disebabkan karena adanya perbedaan volume
dengan ektraktan 0,5 : 100. Volume ekstraktan yang lebih besar mengakibatkan
factor pengencerannya lebih besar sehingga kadar P menjadi tinggi.
Reaksinya menurut Mukhlis (2007) sebagai berikut
3 NH4SO4 + AlPO4 PO4-3 + NH4 + SO4
3 NH4SO4 + FePO4 PO4-3 + NH4 + SO4
selanjutnya,
PO3- + 12 MoO4-2 + 27 H+ H7[P (Mo2O7)6] + 10 H2O
H7[P (Mo2O7)6 + vit C Biru molibden
Hal ini juga diikuti oleh metode pengabuan kering yang memilki kadar P
tersedia yang relatif tinggi karena perbandingan yang digunakan adalah 1 : 100
dengan ekstraktan HCl. Sebaliknya ekstraktan HCl 25 % mengekstrak P hanya
dalam jumlah yang kecil, karena ekstraktannya kurang mampu mengekstrak P
dari tanah.
Peningkatan kadar P tersedia tanah akibat pemberian pupuk P, diikuti
oleh tinggi tanaman, berat kering tajuk dan akar serta serapan P tanaman. Sebagai
salah satu unsur penting yang diperlukan oleh tanaman, unsur P berfungsi
sebagai penyusun setiap sel hidup, terutama dalam pembelahan sel.
Menurut Hakim dkk (1986) P sangat berperan aktif dalam mentransfer energi di
dalam sel dan meningkatkan efisiensi kerja kloroplas.
Dalam pertumbuhannya tanaman mengalami gejala kekurangan unsur hara
P hal ini dapat dilihat dari tanaman yang kerdil dan munculnya warna ungu yang
dimulai dari pangkal hingga ujung daun. Keadaan ini diduga tidak adanya
mana pertumbuhan dan produksi tanaman ditentukan oleh faktor yang berada
dalam takaran minimum dan akan menjadi faktor pembatas. Menurut
Poerwowidodo ( 1992) jika pasokan P tidak cukup, pembelahan sel menyusut dan
seluruh bagian tanaman akan menjadi kerdil sehingga perkembangan bagian tajuk
dan akar akan terganggu. Perkembangan tajuk dan akar tanaman bergantung pada
ketersedian dan masukkan berbagai hara dalam sistem tanah. Pupuk dasar N dan
K yang diberikan diduga mampu merangsang pertumbuhan akar dan
meningkatkan berat akar tanaman dan pemberian pupuk dasar ini juga mampu
mendorong keseimbangan unsur hara dalan tanah, sehingga unsur P mampu
diserap secara maksimal oleh tanaman. Menurut Poerwowidodo (1992) tidak
adanya keseimbangan hara dalam tanah dapat mempengaruhi penyerapan P oleh
tanaman.
Efisiensi serapan P oleh tanaman dari tanah berkaitan erat dengan tipe
perakaran tanaman. Serapan P menggambarkan jumlah hara yang terdapat dalam
tanaman dan mempunyai hubungan yang erat keadaan hara tanaman yang terdapat
dalam tanah. Menurut Poerwowidodo (1992) tanaman yang berakar serabut
seperti tanaman jagung mempunyai takaran yang luas dalam menyerap hara dan
makanan dari tanah sehingga sangat efisien menyerap P. Dengan bertambahnya
percabangan akar dan perkembangan akar lateral akan meningkatkan penggunaan
dan penyerapan P oleh tanaman
Hasil uji korelasi menunjukkan bahwa metode pengabuan kering
merupakan metode yang tepat untuk tanah entisol, karena memiliki koefisien
korelasi tertinggi dibandingkan dengan metode lainnya yakni r = 0,92. dan secara
dikatakan sebagai metode yang tepat disebabkan ekstraktannya mampu
mengekstrak P pada tanah entisol sesuai dengan jumlah P yang diserap oleh
tanaman. Pemilihan metode ini sebagai metode analisis P tanah entisol didug a
bahan penyusun tanah ini berasal dari jaringan tanaman yang terendapkan dalam
waktu yang lama. Menurut Mukhlis (2007) dalam analisis jaringan tanaman
dapat digunakan metode pengabuan kering yang relatif lebih sederhana, tidak
berbahaya dan lebih murah dibandingkan dekstruksi basah dan hal ini senada
dengan pendapat Fixen dan Grove (1990) yang menetapkan bahwa ekstraktan
yang baik harus mampu mengekstrak P tersedia tanah, prosedurnya cepat dan
tepat dan nilai uji yang ditentukan harus berkorelasi dengan pertumbuhan
KESIMPULAN DAN SARAN
Kesimpulan
1. Metode analisis P tersedia yang tepat untuk tanah entisol adalah
metode pengabuan kering dengan nilai korelasi tertinggi yakni
r = 0,92
2. Kemampuan setiap metode dalam mengekstrak kadar P tersedia tanah
berbeda – beda tergantung pada jenis ektraktan yang digunakan.
Saran
Metode yang telah ada dalam analisis kadar P tersedia tanah entisol
DAFTAR PUSTAKA
Al- Jabri, M., I.M Widjik, S., A. Hamid., Suharto dan M. Supartini. 1984. Pemilihan metode uji P tanah – tanah masam dari Lampung dan Sitiung untuk padi gogo. Jurnal Pemberitaan Penelitian Tanah dan Pupuk.
3: 47 – 52.
Bassett, J., R.C. Denny., G.H. Jeffrey dan J. Mendham. 1994. Buku Ajar Vogel: Kimia Analisis Kuantitatif Anorganik. Edisi ke – 4. Terjemahan A.H.
Pudjaatmaka dan L. Setiono. Penerbit Buku Kedokteran EGC,
Jakarta.
Fixen, P. E dan J. H Grove. 1990. Testing Soil for Phosforous in R. L Westerman (ed) Soil Testing and Plant Analysis, 3rd edition. Soil. Sci. of America Inc. Madison, Wisconsin.
Hakim, N. M. Y Nyakpa, A. M Lubis, M.A Dhiha, S.G Nugroho, M. R Saul, G. B Hong dan H. H Bailey. 1986. Dasar- Dasar Ilmu Tanah. Lampung Pres, Lampung. Hlm
Hardjowigeno, S. 1993. Klasifikasi Tanah dan Pedogenesis. Akapres, Jakarta
. 2003. Ilmu Tanah. Akapres, Jakarta
Hartatik K., K. Idrus., S. Sabiham., S. Djuniwati dan J. Sri- Adiningsih. 2003. Komposisi fraksi – fraksi P pada tanah gambut yang diberi bahan amelioran tanah mineral dan pemupukan P. Jurnal Penelitian Tanah dan Iklim. Puslitbangtanak, Bogor. 21: 15 -27.
Iboy, I.R. 2006. Kajian korelasi beberapa metode analisis fosfat tersedia pada tanah sawah (Skripsi). Jurusan Ilmu Tanah Fakultas Pertanian Universitas Sumatera Utara, Medan. Hlm 42.
Masganti, T., Notohadikusumo., A. Maas dan B. Radjagukguk. 2003. Pengaruh macam senyawa penjerap fosfat dan sumber pupuk P terhadap daya penyedian fosfat bahan gambut. Jurnal Penelitian Tanah dan Iklim. Puslitbangtanak, Bogor. 21: 7 -14.
Mukhlis. 2007. Analisis Tanah dan Tanaman. USU Press, Medan.
Munir, M. 1996. Tanah - Tanah Utama Indonesia karakteristik: klasifikasi dan pemanfaatannya. Pustaka Jaya, Jakarta.
Nordin. 2006. Save our Borneo. http://www. Blogger.com/profile [15 Desember 2007]
Nursyamsi, D. dan M. T. Sutriadi. 2002. Pemilihan metode fosfor pada inseptisol, ultisol dan vertisol untuk kedelai (Glycine max L). Pros. Seminar Nasional Sumber Daya Lahan. Puslitbangtanak, Bogor.
Hlm 283 –292.
Poerwowidodo, M. 1992. Telaah kesuburan tanah. UGM Pres, Jogyakarta
. 1991. Metode selidik tanah, UGM Pres, Jogyakarta
Rosmarkam, A dan N. W. Yuwono. 2002. Ilmu Kesuburan Tanah. Kanisius, Jogyakarta.
Ritiung, S dan Wahyunto. 2003. Kandungan tanah gambut di pulau Sumatera http://www.peat- portal.net/newsmaster [15 desember 2007]
Subagyo, H, N. Suharta dan A.B. Siswanto. 2000. Tanah – tanah pertanian Indonesia dalam Tim Pusat Penelitian Tanah dan Agroklimat (ed) Sumber daya lahan Indonesia dan pengelolaannya. Pusat Penelitian Tanah dan Agroklimat. Badan Litbang Pertanian, Departemen Pertanian.
Hlm 36 - 37, 52
Suhardjo, H, Suratman, T. Prihatini dan S. Ritiung. 2003. Lahan pantai dan pengembangannya dalam Tim Pusat Penelitian Tanah dan Agroklimat (ed) Sumber daya lahan Indonesia dan pengelolaannya. Pusat Penelitian Tanah dan Agroklimat. Badan Litbang Pertanian, Departemen Pertanian. Hlm 113
Widjaja- Adhi dan M. Widjik, S. 1984. Pemilihan dan kalibrasi uji tanah hara P untuk tanaman kentang pada tanah hidric dystranepts. Jurnal Pemberitaan Penelitian Tanah dan Pupuk. 3: 42- 47.
Lampiran 1. Data hasil analisis awal tanah entisol
No Parameter Satuan Hasil Kriteria*
1 pH H2 O - 3,69 sangat masam
2 pH KCl - 3,59 masam
3 P tersedia ppm 6,7 sangat rendah
4 Kl % 92,30 -
5 KA % 53,84 -
6 C- organik % 13,63 sangat tinggi
7
8
B. Organik
KTK
%
me/ 100g
23,49
8,53
-
rendah
Lampiran 2. Bagan penelitian di Rumah kaca FP USU
II I III U
P23p3 P3 P7 P1
P0
P7 P1
P0 P3 P2
P4 P8 P6
P2 P5
P5 P6
P1
P6
P8
P0
P2
P7 P4
Lampiran 4. Rataan kadar P tersedia (ppm) tanah hasil analisis metode Bray I
Perlakuan Blok Total Rataan
I II III
Lampiran 5. Daftar sidik ragam kadar P tersedia tanah hasil analisis metode Bray I
Lampiran 6. Rataan kadar P tersedia (ppm) tanah hasil analisis metode Bray II
Perlakuan Blok Total Rataan
I II III
P0 8,55 8,55 11,27 28,37 9,45
P1 14,76 14,07 15,49 44,32 14,77
P2 15,49 14,76 16,18 46,43 15,47
P3 16,90 15,49 14,07 46,46 15,48
P4 20,55 15,49 18,35 54,39 18,13
P5 14,07 19,83 19,38 53,37 17,91
P6 18,35 27,39 25,07 70,81 23,60
P7 19,83 29,74 31,34 80,91 26,97
P8 27,39 32,15 42,22 101,76 33,92
Total 155,89 177,47 193,82 527,18 19,25
Lampiran 7. Daftar sidik ragam kadar P tersedia tanah hasil analisis metode Bray II
SK dB JK KT F hit F 5 % F 1 %
Perlakuan 8 1321,44 165,18 13,08** 2,59 3,89
Blok 2 80,44 40,22 3,18tn 3,63 6,23
Galat 16 202,00 12,62
Total 26 1603,88
KK= 17,93 %
Lampiran 8. Rataan kadar P tersedia (ppm) tanah hasil analisis metode North Carolina
Perlakuan Blok Total Rataan
I II III
Lampiran 10. Rataan kadar P tersedia (ppm) tanah hasil analisis metode HCl 25 %
Perlakuan Blok Total Rataan
I II III
P0 10,10 11,91 8,33 30,34 10,11
P1 21,29 23,22 11,91 56,42 18,80
P2 23,22 14,47 17,47 58,16 19,38
P3 19,36 19,36 15,61 54,33 18,11
P4 15,61 19,36 19,36 54,33 18,11
P5 17,47 17,47 19,36 54,30 18,10
P6 21,29 25,15 21,29 67,79 22,57
P7 25,15 27,16 23,22 75,53 25,17
P8 30,90 30,90 29,13 90,93 30,31
Total 184,39 192,00 165,68 542,07 20,07
Lampiran 11. Daftar sidik ragam kadar P tersedia tanah hasil analisis metode HCl 25 %
SK dB JK KT F hit F 5 % F 1 %
Perlakuan 8 749,95 93,74 14,73** 2,59 3,89
Blok 2 40,77 20,385 3,20tn 3,63 6,23
Galat 16 101,80 6,36
Total 26 892,52
KK= 12,56 %
Keterangan : * = nyata pada taraf 5 %
Lampiran 12. Rataan kadar P tersedia (ppm) tanah hasil analisis metode Pengabuan Kering
Perlakuan Blok Total Rataan
I II III
Lampiran 14. Rataan kadar P tersedia (ppm) tanah hasil analisis metode Truog
Perlakuan Blok Total Rataan
I II III
Lampiran 16. Rataan serapan P (mg/tnm) tanaman jagung pada akhir masa vegetatif
Perlakuan Blok Total Rataan
I II III
Lampiran 18. Rataan tinggi tanaman (cm) tanaman jagung pada akhir masa vegetatif
Perlakuan Blok Total Rataan
I II III
P0 58,0 76,0 42,0 176,0 58,66
P1 101,3 105,0 104,0 310,3 103,43
P2 42,5 34,0 52,5 129,0 43,00
P3 120,0 50,3 123,4 293,7 97,90
P4 128,0 54,2 134,4 316,6 105,53
P5 76,5 120,0 124,0 320,5 106,83
P6 108,0 90,0 131,0 329,0 109,66
P7 132,6 109,0 138,1 379,7 126,56
P8 101,0 135,0 110,5 346,5 115,50
Total 867,9 773,5 959,9 2601,3 96,34
Lampiran 19. Daftar sidik ragam tinggi tanaman jagung pada akhir masa vegetatif
SK dB JK KT F hit F 5 % F 1 %
Perlakuan 8 17.910,5067 2.238,813 3,76* 2,59 3,89
Blok 2 1.930,3822 965,191 1,62tn 3,63 6,23
Galat 16 9.531,0177 595,688
Total 26 29.371,906
KK= 25,33 %
Lampiran 20. Rataan berat kering tajuk (g) tanaman jagung pada akhir masa vegetatif
Perlakuan Blok Total Rataan
I II III
Lampiran 22. Rataan berat kering akar (g) tanaman jagung pada akhir masa vegetatif
Perlakuan Blok Total Rataan
I II III
Lampiran 25. Metode analisis kadar P tersedia tanah metode Bray I
1. Pereaksi
1. Larutan Amonium Flourida 1N
Larutkan 3,7 g NH4F dengan H2O menjadi 100 ml
2. Larutan HCl 5 N
Larutkan 20,2 ml HCl pekat dengan H2O menjadi 500 ml
3. Larutan Bray I
Larutkan 30 ml larutan NH4F 1N dengan 5 ml HCl 2 N dan jadikan larutan
dengan menambahkan H2O
Campurkan Asam sulfat 5 N, Amonium Molibdat dan Kalium Antimonit
Tartarat, jadikan 2 L dengan menambahkan H2O
9. Pereaksi Fosfat B
Campurkan 1 g sam Ascorbat kedalam 200 ml pereaksi fosfat A
10.Larutan Standard 50 ppm P
11.Larutan standard 0- 0,5- 1,0- 2,0-3,0-4,0-5,0 ppm P
Pipet larutan Standard 50 ppm P masing – masing sebanyak 0 1 2 4
-6- 8 - 10 ml ke dalam labu ukur 100 ml dan penuhkan dengan H2O
2. Cara Kerja
1. Timbang 2 g contoh tanah dan tempatkan pada gelas erlemeyer 250 cc
2. Tambahkan larutan Bray I sebanyak 20 ml, dan goncang pada shaker
selama 30 menit
3. Saring dengan kertas saring Whatman No. 42
4. Pipet filtrat sebanyak 5 ml dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi Fosfat B sebanyak 10 ml. Biarkan selama 5 menit
6. Ukur transmitan pada spectronik dengan panjang gelombang 660 nm
7. Pada saat yang sama pipet juga masing – masing 5 ml larutan standar P 0-
0,5- 1,0 – 2,0- 3,0 – 4,0 – 5,0 ppm P ke tabung reaksi, kemudian
tambahkan 10 ml pereaksi fosfat B
8. Ukur juga transmitan standar pada spectronik dengan panjang gelombang
yang sama yaitu 660 nm.
3. Perhitungan
Nilai adsorben = - log T/ 100
Buat kurva standar P ( 0 – 5 ppm P) sebagai sumbu x dan nilai Adsorben
sebagai sumbu y. Konsentrasi P – larutan ditetapkan dengan menginterpolasikan
nilai adsorben dari sample ke kurva standar ( Kurva standard interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR)
Lampiran 26. Metode analisis kadar P tersedia tanah metode Bray II
1. Pereaksi
1. Larutan Amonium Flourida 1N
Larutkan 3,7 g NH4F dengan H2O menjadi 100 ml
2. Larutan HCl 5 N
Larutkan 20,2 ml HCl pekat dengan H2O menjadi 500 ml
3. Larutan Bray II
Larutkan 30 ml larutan NH4F 1N dengan 20 ml HCl 2 N dan jadikan 1 L
larutan dengan menambahkan H2O
4. Asam Sulfat 5 N
Larutkan 140 ml H2SO4 pekat BD 1,84kg/L dengan H2O hingga volume
larutan menjadi 1000 ml
5. Amonium Molibdat
Larutkan 12 g (NH4)6Mo7O24. 4 H2O dengan H2O hingga volume larutan
menjadi 250 ml
6. Kalium Antimonit Tartarat
Larutkan 1,298 g KSbOC4H4O6 dalam 100 ml H2O
7. Asam Ascorbat
8. Pereaksi Fosfat A
Campurkan Asam sulfat 5 N, Amonium Molibdat dan Kalium Antimonit
Tartarat, jadikan 2 L dengan menambahkan H2O
9. Pereaksi Fosfat B
Campurkan 1 g sam Ascorbat kedalam 200 ml pereaksi fosfat A
11.Larutan standard 0- 0,5- 1,0- 2,0-3,0-4,0-5,0 ppm P
Pipet larutan Standard 50 ppm P masing – masing sebanyak 0 1 2 4
-6- 8 - 10 ml ke dalam labu ukur 100 ml dan penuhkan dengan H2O
2. Cara Kerja
1. Timbang 2 g contoh tanah dan tempatkan pada gelas erlemeyer 250 cc
2. Tambahkan larutan Bray II sebanyak 20 ml, dan goncang pada shaker
selama 30 menit
3. Saring dengan kertas saring Whatman No. 42
4. Pipet filtrat sebanyak 5 ml dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi Fosfat B sebanyak 10 ml. Biarkan selama 5 menit
6. Ukur transmitan pada spectronik dengan panjang gelombang 660 nm
7. Pada saat yang sama pipet juga masing – masing 5 ml larutan standar P 0-
0,5- 1,0 – 2,0- 3,0 – 4,0 – 5,0 ppm P ke tabung reaksi, kemudian
tambahkan 10 ml pereaksi fosfat B
8. Ukur juga transmitan standar pada spectronik dengan panjang gelombang
yang sama yaitu 660 nm.
3. Perhitungan
Nilai adsorben = - log T/ 100
Buat kurva standar P ( 0 – 5 ppm P) sebagai sumbu x dan nilai Adsorben
sebagai sumbu y. Konsentrasi P – larutan ditetapkan dengan menginterpolasikan
nilai adsorben dari sample ke kurva standar ( Kurva standard interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR)
Lampiran 27. Metode analisis kadar P tersedia tanah metode North Carolina
1. Pereaksi
1. Larutan HCl 5 N
Larutkan 20,2 ml HCl pekat dengan H2O menjadi 500 ml
2. Asam Sulfat 5 N
Larutkan 140 ml H2SO4 pekat BD 1,84kg/L dengan H2O hingga volume
larutan menjadi 1000 ml
3. Larutan North Carolina
Larutkan 10 ml HCl dan 5 ml H2SO4 dan ditambahkan H2O menjadi 1 L
4. Amonium Molibdat
Larutkan 12 g (NH4)6Mo7O24. 4 H2O dengan H2O hingga volume larutan
menjadi 250 ml
5. Kalium Antimonit Tartarat
Larutkan 1,298 g KSbOC4H4O6 dalam 100 ml H2O
7. Asam Ascorbat
8. Pereaksi Fosfat A
Campurkan Asam sulfat 5 N, Amonium Molibdat dan Kalium Antimonit
Tartarat, jadikan 2 L dengan menambahkan H2O
12.Pereaksi Fosfat B
Campurkan 1 g sam Ascorbat kedalam 200 ml pereaksi fosfat A
13.Larutan Standard 50 ppm P
14.Larutan standard 0- 0,5- 1,0- 2,0-3,0-4,0-5,0 ppm P
Pipet larutan Standard 50 ppm P masing – masing sebanyak 0 1 2 4
2. Cara Kerja
1. Timbang 2 g contoh tanah dan tempatkan pada gelas erlemeyer 250 cc
2. Tambahkan larutan North Carolina sebanyak 20 ml, dan goncang pada
shaker selama 30 menit
3. Saring dengan kertas saring Whatman No. 42
4. Pipet filtrat sebanyak 5 ml dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi Fosfat B sebanyak 10 ml. Biarkan selama 5 menit
6. Ukur transmitan pada spectronik dengan panjang gelombang 660 nm
7. Pada saat yang sama pipet juga masing – masing 5 ml larutan standar P 0-
0,5- 1,0 – 2,0- 3,0 – 4,0 – 5,0 ppm P ke tabung reaksi, kemudian
tambahkan 10 ml pereaksi fosfat B
8. Ukur juga transmitan standar pada spectronik dengan panjang gelombang
yang sama yaitu 660 nm.
3. Perhitungan
Nilai adsorben = - log T/ 100
Buat kurva standar P ( 0 – 5 ppm P) sebagai sumbu x dan nilai Adsorben
sebagai sumbu y. Konsentrasi P – larutan ditetapkan dengan menginterpolasikan
nilai adsorben dari sample ke kurva standar ( Kurva standard interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR)
Lampiran 28. Metode analisis kadar P tersedia tanah metode HCl 25 %
1. Pereaksi
1. Larutan HCL 25 %
Larutkan 700 ml HCl 37 % menjadi 1L
2. Asam Sulfat 5 N
Larutkan 140 ml H2SO4 pekat BD 1,84kg/L dengan H2O hingga volume
larutan menjadi 1000 ml
3. Amonium Molibda
Larutkan 12 g (NH4)6Mo7O24. 4 H2O dengan H2O hingga volume larutan
menjadi 250 ml
4. Kalium Antimonit Tartarat
Larutkan 1,298 g KSbOC4H4O6 dalam 100 ml H2O
5. Asam Ascorbat
6. Pereaksi Fosfat A
Campurkan Asam sulfat 5 N, Amonium Molibdat dan Kalium Antimonit
Tartarat, jadikan 2 L dengan menambahkan H2O
7. Pereaksi Fosfat B
Campurkan 1 g sam Ascorbat kedalam 200 ml pereaksi fosfat A
8. Larutan Standard 50 ppm P
9. Larutan standard 0- 0,5- 1,0- 2,0-3,0-4,0-5,0 ppm P
Pipet larutan Standard 50 ppm P masing – masing sebanyak 0 1 2 4
2. Cara Kerja
1. Timbang 2 g contoh tanah dan tempatkan pada gelas erlemeyer 250 cc
2. Tambahkan larutan HCl 25 % sebanyak 20 ml, dan goncang pada
shaker selama 30 menit
3. Saring dengan kertas saring Whatman No. 42
4. Pipet filtrat sebanyak 5 ml dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi Fosfat B sebanyak 10 ml. Biarkan selama 5 menit
6. Ukur transmitan pada spectronik dengan panjang gelombang 660 nm
7. Pada saat yang sama pipet juga masing – masing 5 ml larutan standar P
0- 0,5- 1,0 – 2,0- 3,0 – 4,0 – 5,0 ppm P ke tabung reaksi, kemudian
tambahkan 10 ml pereaksi fosfat B
8. Ukur juga transmitan standar pada spectronik dengan panjang
gelombang yang sama yaitu 660 nm.
3. Perhitungan
Nilai adsorben = - log T/ 100
Buat kurva standar P ( 0 – 5 ppm P) sebagai sumbu x dan nilai Adsorben
sebagai sumbu y. Konsentrasi P – larutan ditetapkan dengan menginterpolasikan
nilai adsorben dari sample ke kurva standar ( Kurva standard interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR)
Lampiran 29. Metode analisis P tersedia tanah metode Troug
1. Pereaksi
1. Larutan Asam Sulfat 0,002 N
Larutkan 0,055 ml H2SO4 dengan H2O menjadi 100 ml
2. Larutan Troug
Larutkan 3 g larutan (NH4 )2 SO4 1N dengan H2O dan tambahkan H2SO4
0,002 N set pH menjadi 3,0.
3. Asam Sulfat 5 N
Larutkan 140 ml H2SO4 pekat BD 1,84kg/L dengan H2O hingga volume
larutan menjadi 1000 ml
4. Amonium Molibdat
Larutkan 12 g (NH4)6Mo7O24. 4 H2O dengan H2O hingga volume larutan
menjadi 250 ml
5. Kalium Antimonit Tartarat
Larutkan 1,298 g KSbOC4H4O6 dalam 100 ml H2O
7. Asam Ascorbat
8. Pereaksi Fosfat A
Campurkan Asam sulfat 5 N, Amonium Molibdat dan Kalium Antimonit
Tartarat, jadikan 2 L dengan menambahkan H2O
9. Pereaksi Fosfat B
Campurkan 1 g sam Ascorbat kedalam 200 ml pereaksi fosfat A
10.Larutan Standard 50 ppm P
11.Larutan standard 0- 0,5- 1,0- 2,0-3,0-4,0-5,0 ppm P
Pipet larutan Standard 50 ppm P masing – masing sebanyak 0 1 2 4
-6- 8 - 10 ml ke dalam labu ukur 100 ml dan penuhkan dengan H2O
2. Cara Kerja
1. Timbang 0,5 g contoh tanah dan tempatkan pada gelas erlemeyer 250 cc
2. Tambahkan larutan Troug sebanyak 100 ml, dan goncang pada shaker
selama 30 menit
3. Saring dengan kertas saring Whatman No. 42
4. Pipet filtrat sebanyak 5 ml dan tempatkan pada tabung reaksi
5. Tambahkan pereaksi Fosfat B sebanyak 10 ml. Biarkan selama 5 menit
6. Ukur transmitan pada spectronik dengan panjang gelombang 660 nm
7. Pada saat yang sama pipet juga masing – masing 5 ml larutan standar P 0 -
0,5 - 1,0 – 2,0 - 3,0 – 4,0 – 5,0 ppm P ke tabung reaksi, kemudian
tambahkan 10 ml pereaksi fosfat B
8. Ukur juga transmitan standar pada spectronik dengan panjang gelombang
yang sama yaitu 660 nm.
3. Perhitungan
Nilai adsorben = - log T/ 100
Buat kurva standar P ( 0 – 5 ppm P) sebagai sumbu x dan nilai Adsorben
sebagai sumbu y. Konsentrasi P – larutan ditetapkan dengan menginterpolasikan
nilai adsorben dari sample ke kurva standar ( Kurva standard interpolasi dapat
dilakukan secara mudah dengan menggunakan kalkulator pakai program LR)
Lampiran 30. Metode analisis P tersedia tanah metode Pengabuan kering
1. Pereaksi
1. Asam Chlorida 1 N
Larutkan 4,4 ml HCl pekat dengan H2O menjadi 500 ml.
2. Cara Kerja
1. Timbang 1 g contoh tanah, tempatkan pada crucible dan tutup ( beri tanda
crucible dengan menuliskan di bagian bawah dengan pensil)
2. Tempatkan di Muffle furnance, panaskan pada temperatur 100 o C selama
1 jam, kemudian naikkan pada temperature 200oC selama 2 jam
selanjutnya naikkan pada temperatur 500oC selama 4 jam.
3. Didinginkan, lalu dikeluarkan dari Muffle furnance
4. Tetesi contoh tanah yang telah jadi abu dengan 10 tetes H2O, kemudian
tambahkan 10 ml HCl 1 N
5. Panaskan di hot plate hingga menjelang mendidih
6. saring dengan kertas saring biasa, filtrat di tampung pada labu ukur 100 ml
7. Bilas crucible dengan 10 ml HCl 1N dan tuangkan ke labu ukur.
8. Bilas kertas saring dengan H2O dan penuhkan labu ukur hingga tanda 100
ml
9. Pipet 5 ml cairan dari ekstraksi pengabuan kering tempatkan pada tabung
reaksi
10.Tambahkan 10 ml Reagen Fosfat B biarkan ± 10 menit, kemudian ukur
11.Pada saat yang sama dilakukan pula pada larutan standar 0 – 2 – 4 – 6 – 8
dan 10 ppm dengan cara memipet masing – masing 5 ml dan ditambahkan
10 ml Reagen fosfat B dan ukur pada spectronik.
3. Perhitungan
Lampiran 31. Foto - foto tanaman dan kunjungan suvervisi
Gambar 1. Penulis dan tanaman jagung saat berumur 2 minggu