KEMURNIAN SELULOSA SERABUT AMPAS SAGU
PADA BERBAGAI PERLAKUAN ISOLASI
EGI MARIAH NURPAGI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi yang berjudul Kemurnian Selulosa Serabut Ampas Sagu pada Berbagai Perlakuan Isolasi adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2013
Egi Mariah Nurpagi
ABSTRAK
EGI MARIAH NURPAGI. Kemurnian Selulosa Serabut Ampas Sagu pada Berbagai Perlakuan Isolasi. Dibimbing oleh MUHAMAD FARID dan TUN TEDJA IRAWADI.
Serabut ampas sagu merupakan limbah yang dihasilkan dari industri pengolahan pati sagu dan mengandung 42% selulosa. Selulosa ini diisolasi untuk mendapatkan isolat terbaik melalui beberapa tahapan dan perlakuan, yaitu preparasi dengan dan tanpa penggilingan, pemasakan dengan NaOH dengan dan tanpa pemanasan dengan HCl, serta delignifikasi. Penggilingan dan pemanasan dengan HCl dapat meningkatkan kadar selulosa alfa. Pemanasan dengan HCl dengan dan tanpa penggilingan menghasilkan kadar selulosa alfa berturut-turut sebesar 79.96% dan 74.70%, lebih besar dibandingkan dengan tanpa pemanasan dengan HCl, yaitu berturut-turut sebesar 72.98% dan 63.20%. Spektrum inframerah transformasi Fourier menunjukkan serapan yang tidak jauh berbeda antara isolat selulosa dan selulosa komersial dengan serapan khas ikatan β -glikosida pada bilangan gelombang 894 cm-1. Pemanasan dengan HCl dengan dan tanpa penggilingan dapat meningkatkan indeks kristalinitas dengan menghilangkan sebagian daerah amorf. Termogram diferensial menunjukkan bahwa isolat mulai kehilangan massa pada suhu 98–102 C dan kehilangan massa maksimum terjadi pada suhu 352–377 C.
Kata kunci: isolasi, sagu, selulosa
ABSTRACT
processes and treatments, including preparation with and without grinding, pulping in NaOH with and without heating in HCl, as well as delignification. Grinding and heating in HCl treatment were found to increase the alpha cellulose content. Heating treatment in HCl with and without grinding produced 79.96% and 74.70%, of alpha cellulose, respectively, higher than without heating in HCl that was 72.98% and 63.20%, respectively. Fourier transform infrared spectra of the isolates were not significantly different from a commercial cellulose showing characteristic by β-glycoside absorption at 894 cm-1. Heating in HCl with and without grinding also increased the crystallinity index by removing part of the amorphous region. The differential thermogram showed that the isolates started to lose the mass at around 98–102 °C and lost the maximum weight lost at around 352–377 oC.KEMURNIAN SELULOSA SERABUT AMPAS SAGU
PADA BERBAGAI PERLAKUAN ISOLASI
EGI MARIAH NURPAGI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Kemurnian Selulosa Serabut Ampas Sagu pada Berbagai Perlakuan Isolasi
Nama : Egi Mariah Nurpagi NIM : G44080073
Disetujui oleh
Drs Muhamad Farid, MSi Pembimbing I
Prof Dr Ir Tun Tedja Irawadi, MS Pembimbing II
Diketahui oleh
Prof Dr Ir Tun Tedja Irawadi, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Karya ilmiah ini disusun berdasarkan penelitian yang dilaksanakan pada bulan Mei 2012 hingga Februari 2013 yang berjudul Kemurnian Selulosa Serabut Ampas Sagu pada Berbagai Perlakuan Isolasi.
Terima kasih penulis ucapkan kepada Bapak Drs Muhamad Farid, MSi dan Ibu Prof Dr Ir Tun Tedja Irawadi, MS selaku pembimbing. Di samping itu, penghargaan penulis sampaikan kepada Ibu Dr Henny Purwaningsih Suyuti, MSi, Bapak Mohammad Khotib, MSi, Bapak Novriyandi Hanif, DSc, Ibu Prof Ir Suminar S Achmadi, PhD, dan Bapak Budi Arifin, MSi atas segala diskusi dan saran berkaitan dengan penelitian. Ungkapan terima kasih juga disampaikan kepada Ibu, Ayah, serta keluarga atas segala doa dan kasih sayangnya.
Selain itu, penulis juga mengucapkan terima kasih kepada Ika, Indah, Baim, dan staf analis Laboratorium Terpadu atas bantuan dan masukan selama penelitian. Apresiasi juga penulis ucapkan kepada Ade Irma, Dwi utami, dan Itoh Khitotul Hayati serta teman-teman Kimia 45 atas saran, semangat, dan pengalaman selama studi dan penelitian.
Semoga karya ilmiah ini dapat bermanfaat bagi ilmu pengetahuan.
Bogor, Juli 2013
DAFTAR ISI
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
METODE 1
HASIL DAN PEMBAHASAN 4
Isolasi Selulosa Serabut Ampas Sagu 5
Analisis Komponen Kimia 7
Analisis Gugus Fungsi 8
Analisis Kristalinitas 9
Analisis Termal 10
SIMPULAN DAN SARAN 11
DAFTAR PUSTAKA 11
viii
DAFTAR GAMBAR
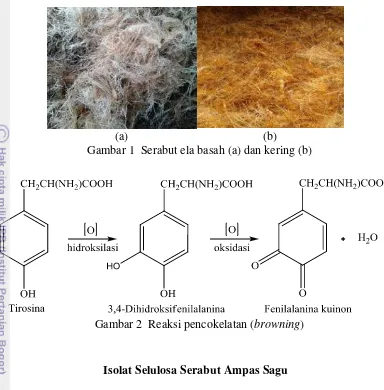
1 Serabut ela: (a) basah (b) kering 5
2 Reaksi pencoklatan (browning) 5
3 Selulosa: a) grinding dengan pemanasan HCl, b) grinding tanpa pemanasan HCl, c) tanpa grinding dan tanpa pemanasan HCl, dan d) tanpa grinding
dengan pemanasan HCl 6
4 Persen rendemen isolat selulosa serabut ampas sagu 7 5 Komposisi kimia selulosa komersial dan isolat selulosa 8 6 Spektrum FTIR selulosa komersial (---), SE1: perlakuan grinding dengan
pemanasan HCl (---), SE2: perlakuan grinding tanpa pemanasan HCl (---), SE3: perlakuan tanpa grinding tanpa pemanasan HCl (---), dan SE4:
perlakuan tanpa grinding dengan pemanasan HCl (---). 9 7 Difraktogram selulosa komersial (---), SE1: perlakuan grinding dengan
pemanasan HCl (---), SE2: perlakuan grinding tanpa pemanasan HCl (---), SE3: perlakuan tanpa grinding tanpa pemanasan HCl (---), dan SE4:
perlakuan tanpa grinding dengan pemanasan HCl (---). 10
DAFTAR LAMPIRAN
1 Pengolahan tepung sagu 14
2 Diagram alir penelitian 14
3 Data tahap dan perlakuan isolasi selulosa serabut ela 16
4 Analisis komponen kimia 18
5 Hasil analisis FTIR 19
6 Difraktogram Selulosa komersial dan isolate selulosa dari serabut ampas
sagu 19
7 Kurva DTA (-) /TGA (---) selulosa komersial dan isolat selulosa dari
1
PENDAHULUAN
Ampas sagu merupakan limbah yang dihasilkan oleh industri pengolahan pati sagu (Lampiran 1). Areal tanaman sagu di Indonesia sekitar 1.4 juta ha, dengan 90% luasan terbesar berada di Papua. Satu hektar lahan sagu menghasilkan 100–200 pohon sagu dan setiap pohon sagu menghasilkan 200–400 kg pati sagu (Bintoro et al. 2010). Jumlah ampas sagu yang dihasilkan bergantung pada kualitas proses pengolahan pati sagu tersebut. Menurut Matitaputty dan Alfons (2006), jumlah ampas sagu yang dihasilkan 6 kali lebih banyak dibandingkan dengan produksi pati sagunya. Sampai saat ini, ampas sagu hanya sebagian kecil digunakan sebagai pupuk, media tanam (Syakir et al. 2009; Bintoro 2008; Leksana 2000), dan pakan ternak (Sangadji 2009). Penimbunan dan pembuangan ampas sagu yang berlebih ini akan mencemari lingkungan karena menimbulkan bau yang tidak sedap (Syakir et al. 2009). Bau ini disebabkan oleh asam-asam organik yang terbentuk dari proses penguraian bahan organik dengan bantuan mikroorganisme pada proses pengenapan (Zaitun et al. 2001).
Ampas sagu (ela) mengandung 58.21% pati, 22.45% selulosa, 11.8% hemiselulosa, 8.95% lignin, dan 1.60% senyawa ekstraktif (Irawadi 2010). Namun, saat ini teknologi proses pengolahan pati sagu telah berkembang sehingga menurunkan keberadaan pati pada ampasnya. Menurut Pushpamalar et al. (2006), selulosa merupakan polimer alami non-pati yang paling banyak terdapat dalam ampas sagu. Jumlahnya yang cukup banyak menjadikan selulosa sebagai bahan baku potensial di berbagai industri. Beberapa kajian tentang pemanfaatan selulosa serabut ela yang dimodifikasi diaplikasikan pada teknologi plastik, membran, dan fase diam kromatografi kolom. Rojali (2011) telah melakukan modifikasi selulosa menjadi selulosa benzoat, sedangkan Setyorini (2011) telah memodifikasi selulosa menjadi selulosa-g-akrilamida sebagai fase diam kromatografi kolom. Oleh karena itu, proses isolasi selulosa dari serabut ela merupakan tahapan yang penting.
Penelitian ini bertujuan mengisolasi selulosa dari ampas sagu melalui beberapa tahap dan perlakuan, yaitu preparasi sampel dengan dan tanpa grinding, proses pulping dengan dan tanpa pemanasan dengan HCl, dan delignifikasi menggunakan peroksida. Selanjutnya, isolat selulosa tersebut dicirikan dan dibandingkan dengan selulosa komersial melalui analisis komponen kimia (selulosa alfa, holoselulosa, dan lignin), analisis gugus fungsi dengan spektrometer inframerah transformasi Fourier (FTIR), analisis kristalinitas dengan difraktometer sinar-X (XRD), dan analisis termal dengan penganalisis termal diferensial/penganalisis termogravimetri (DTA/TGA).
METODE
Alat dan Bahan
2
Prestige-21 Shimadzu, XRD Rigaku D/Max 2500, DTG-60H FC-60A TA-60WS, neraca analitik, dan oven.
Bahan-bahan yang digunakan dalam penelitian ini adalah serabut ela dari industri pati sagu (Tanah Baru, Bogor), selulosa komersial (Sigma-Aldrich), HCl p.a (Merck), NaOH teknis, H2O2 teknis, H2SO4 p.a (Merck), dan KBr untuk spektroskopi IR.
Lingkup Kerja
Penelitian ini terbagi dalam beberapa tahap, yaitu isolasi selulosa (preparasi sampel, pulping, dan delignifikasi), pencirian isolat selulosa (penetapan kadar holoselulosa, α-selulosa, dan lignin), analisis gugus fungsi, analisis kristalinitas, dan analisis termal (Lampiran 2). Empat kombinasi perlakuan isolasi serabut ela ditunjukkan pada Tabel 1.
Tabel 1 Tahap dan perlakuan isolasi serabut ampas sagu
Perlakuan Tahap preparasi Tahap pulping Tahap delignifikasi
Grinding Pemanasan dengan HCl
SE1 √ √ √ selulosa dicirikan yang terdiri atas kadar holoselulosa, kadar selulosa alfa, dan kadar lignin.
Pemasakan (Pulping) (modifikasi Akpabio et al. 2012)
Pulping dilakukan dengan 2 perlakuan. Perlakuan pertama, sampel (E1, E4) ditimbang sebanyak 50 g, dimasukkan ke dalam gelas piala 1 L, dan ditambahkan 1 L HCl 3%. Campuran dipanaskan pada suhu 80 C sambil diaduk selama 1 jam hingga campuran bebas-pati. Setelah 1 jam, dilakukan uji iodin untuk mengamati keberadaan pati dengan mencampurkan 2 tetes larutan iodin ke dalam 2 tetes sampel. Pemanasan dihentikan saat campuran menunjukkan hasil negatif (tidak menimbulkan warna biru). Sampel bebas-pati kemudian disaring dan dicuci hingga bebas asam. Sampel bebas-pati kemudian dikeringkan di bawah sinar matahari hingga kering (E’1, E’4).
3
Delignifikasi (modifikasi Sun et al. 2005)
Sebanyak 20 g sampel hasil pulping (E’1, E2, E3, E’4) ditambahkan dengan 500 mL H2O2 5% pH 12 (dikondisikan dengan NaOH 40%) di dalam gelas piala 1 L. Campuran dipanaskan pada suhu 70–80 C sambil diaduk menggunakan motor pengaduk dengan kecepatan pengadukan 200 rpm, secara bertahap selama 2, 3, dan 3 jam. Pada setiap tahapan, residu disaring sambil dialiri air hingga pH-nya netral. Setelah 8 jam, serabut ela hasil delignifikasi dikeringkan dalam oven pada suhu 60 C sampai kering (SE’1, SE2, SE3, SE’4).
Pencirian Isolat Selulosa
Penetapan Kadar Holoselulosa (ASTM D 1104-56)
Sebanyak 2 g sampel selulosa (isolat SE’1, SE2, SE3, dan SE’4) dimasukkan ke dalam erlenmeyer 250 mL dengan tutup kaca. Sampel ditambahkan 150 mL air suling dan 0.2 mL asam asetat glasial, lalu ditambahkan 1 g NaClO2. Campuran dipanaskan selama 5 jam dengan suhu 70–80 °C dalam penangas air sambil ditambahkan 0.2 mL asam asetat glasial dingin dan 1 g NaClO2 setiap jam dan sering diaduk. Labu didinginkan di dalam air es hingga suhu 10 °C, kemudian campuran disaring menggunakan cawan masir G2 sambil divakum. Residu bebas-ClO2 dicuci dengan air suling hingga berwarna putih, selanjutnya dikeringkan di dalam oven suhu 105 °C hingga bobot tetap, didinginkan dalam desikator, dan ditimbang.
oloselulosa o o on oh ke ing o o selulosa
Penetapan Kadar α-Selulosa (ASTM D 1103-60)
Sebanyak 2 g holoselulosa kering oven dimasukkan ke dalam erlenmeyer 250 mL. Labu dimasukkan ke dalam penangas air untuk menjaga suhu 20 °C dan ditutup dengan cawan petri. Sebanyak 50 mL NaOH 17.5% ditambahkan sambil diaduk selama 1 menit lalu dibiarkan selama 5 menit. Campuran kemudian disaring menggunakan cawan G2 kapasitas 30 mL. Residu dicuci menggunakan larutan NaOH 8.3% dan air suling, dilanjutkan menggunakan 40 mL asam asetat 10%. Residu dicuci hingga bebas asam dengan 1 L air suling panas, lalu dikeringkan dalam oven pada suhu 105 °C selama 6 jam. Setelah didinginkan dalam desikator selama 30 menit, ditimbang hingga bobotnya tetap.
α elulosa o o on oh ke ing o en o o selulosa emiselulosa oloselulosa α elulosa
Penetapan Kadar Lignin (ASTM D 1106-56)
4
air panas di atas penangas air pada suhu 100 °C selama 3 jam, kemudian disaring dan dicuci dengan 100 mL air panas.
Sampel dikeringudarakan kemudian dipindahkan ke dalam gelas piala kecil dan ditambahkan asam sulfat 72% dingin perlahan-lahan sambil diaduk pada suhu 12–15 °C selama 1 menit. Campuran didiamkan selama 2 jam dan suhu dijaga tetap 18–20 °C. Sampel lalu dipindahkan ke dalam erlenmeyer 1 L dan diencerkan dengan air suling 560 mL hingga konsentrasinya 3%, kemudian direfluks selama 4 jam dengan volume tetap. Bahan yang tidak larut disaring dan dicuci dengan air panas hingga bebas asam. Hasilnya dikeringkan dalam oven pada suhu 105° C, didinginkan dalam desikator, dan ditimbang hingga bobotnya tetap.
ignin o o on oh ke ing o en o o lignin
Analisis Spektrum FTIR
Sebanyak 0.01 g sampel selulosa dicampur dengan 0.1 g KBr. Campuran digerus sampai halus dan homogen kemudian dipanaskan dalam oven bersuhu 40
C selama 24 jam. Campuran lalu dianalisis dengan spektrofotometer FTIR IR Prestige–21 Shimadzu dengan resolusi 4 cm-1.
Analisis Kristalinitas dengan Difraktometer Sinar X
Difraksi sinar-X dihasilkan oleh difraktometer Rigaku D/Max 2500. Radiasi yang digunakan adalah Ni-filtered Cu-Kα pada panjang gelom ang .1541 nm. Difraktometer dioperasikan pada 40 kV dan 200 mA. Contoh dipayar pada kisaran 2 = 10–60o. Kristalinitas dihitung berdasarkan
(
)
dengan CI adalah indeks kristalinitas, Iam adalah intensitas puncak fase amorf, dan
I002 adalah intensitas maksimum pada kisi difraksi 002. Analisis Termal dengan TG/DTA
Analisis termal dilakukan dengan DTG-60H FC-60A TA-60WS. Suhu yang digunakan sampai 600 °C dengan laju pemanasan 10 °C menit-1.
HASIL DAN PEMBAHASAN
5
(a) (b)
Gambar 1 Serabut ela basah (a) dan kering (b)
Gambar 2 Reaksi pencokelatan (browning)
Isolat Selulosa Serabut Ampas Sagu
Isolasi selulosa dilakukan dengan beberapa tahapan, yaitu preparasi sampel, pemasakan (pulping), dan delignifikasi. Perlakuan terdiri atas 2 faktor, yaitu preparasi dengan/tanpa grinding dan pulping dengan/tanpa pemanasan dengan HCl. Pemanasan dilakukan dengan menggunakan HCl 3% pada suhu 80 °C. Pemanasan dengan asam encer bertujuan menghidrolisis sebagian besar hemiselulosa menjadi gula dan menghidrolisis pati (Achmadi 1990). HCl dipilih karena ion Cl– yang terbentuk tidak cukup reaktif untuk bereaksi dengan gugus OH selulosa sehingga diharapkan tidak mengganggu komponen nonpati (selulosa) atau menghasilkan reaksi samping. Suhu yang digunakan kurang dari 100 °C untuk menghindari kerusakan bahan. Rendemen pemanasan dengan HCl pada sampel dengan dan tanpa proses grinding berturut- u u se esa 53 (E’1) dan
55 (E’4).
Pemasakan (pulping) bertujuan menghilangkan hemiselulosa dan lignin.
6
se esa 55 (E’1) dan 48% (E2), sedangkan untuk sampel tanpa perlakuan
grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 50% (E’4) dan 51% (E3).
Delignifikasi (pemutihan) merupakan metode penghilangan lignin dengan mendegradasi dan melarutkannya melalui reaksi oksidatif (Achmadi 1990). Tahapan delignifikasi dilakukan dengan menggunakan H2O2 5%. Oksidator ini digunakan karena ramah lingkungan. Hidrogen peroksida bereaksi optimum dalam kondisi basa. Nilai pH optimum untuk penghilangan lignin berkisar 11.5– 11.6 karena H2O2 akan terdisosiasi menjadi anion hidroperoksida dan bereaksi dengan H2O2 menghasilkan radikal •O dan •O2‾ yang merupakan spesi aktif delignifikasi (Fang et al. 2000). Anion ini akan menyerang gugus etilena dan gugus karbonil dari lignin dan mengubahnya menjadi gugus yang tidak berkromofor. Berikut ini mekanisme reaksi pembentukan anion hidroperoksida serta radikal •O dan •O2‾.
H2O2 + HO– HOO– + H2O H2O2 + HOO– HO• + •O2– + H2O
Radikal bebas yang dihasilkan dari dekomposisi hidrogen peroksida berperan dalam proses delignifikasi dan melarutkan hemiselulosa (Pan dan Sano 1999).
Rendemen tahap delignifikasi sampel dengan perlakuan grinding dengan dan tanpa pemanasan dengan HCl berturut- u u se esa 63 (E’ ) dan 42 (E2), sedangkan untuk sampel tanpa perlakuan grinding dengan dan tanpa pemanasan HCl berturut- u u se esa 54 (E’4) dan 47 (E3) (Lampiran 3). Gambar 3 menunjukkan isolat selulosa hasil delignifikasi yang berwarna putih.. Warna putih ini berkaitan dengan jauh berkurangnya gugus kromofor pada lignin yang masih tersisa dalam isolat. Semakin rendah kadar lignin, warna akan semakin putih (Hisyam 2012). Perlakuan dengan grinding dan pemanasan dengan HCl menghasilkan isolat yang paling putih.
Gambar 3 Isolat selulosa dari sampel dengan perlakuan grinding dengan (a) dan tanpa pemanasan dengan HCl (b) serta tanpa perlakuan grinding tanpa (c) dan dengan pemanasan dengan HCl (d)
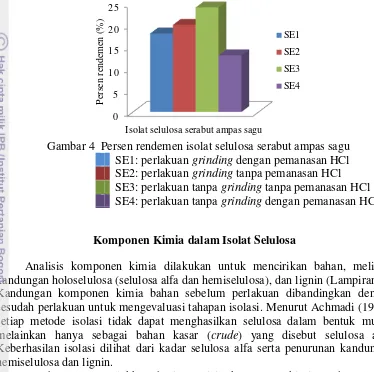
Rendemen total isolat selulosa hasil berbagai perlakuan ditunjukkan pada Gambar 4. Rendemen yang dihasilkan bergantung pada perlakuan yang diberikan selama tahap isolasi. Rendemen total isolat selulosa dari serabut ela dengan
a) (b)
7
perlakuan grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 18% (SE1) dan 20% (SE2), sedangkan yang tanpa perlakuan grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 15% (SE4) dan 24% (SE3). Hal ini menunjukkan bahwa tahapan pemanasan dengan HCl dapat menyebabkan kehilangan bobot sekitar 44–48% dari bobot kering bahan awalnya.
Gambar 4 Persen rendemen isolat selulosa serabut ampas sagu SE1: perlakuan grinding dengan pemanasan HCl SE2: perlakuan grinding tanpa pemanasan HCl SE3: perlakuan tanpa grinding tanpa pemanasan HCl SE4: perlakuan tanpa grinding dengan pemanasan HCl Komponen Kimia dalam Isolat Selulosa
Analisis komponen kimia dilakukan untuk mencirikan bahan, meliputi kandungan holoselulosa (selulosa alfa dan hemiselulosa), dan lignin (Lampiran 4). Kandungan komponen kimia bahan sebelum perlakuan dibandingkan dengan sesudah perlakuan untuk mengevaluasi tahapan isolasi. Menurut Achmadi (1990), setiap metode isolasi tidak dapat menghasilkan selulosa dalam bentuk murni, melainkan hanya sebagai bahan kasar (crude) yang disebut selulosa alfa. Keberhasilan isolasi dilihat dari kadar selulosa alfa serta penurunan kandungan hemiselulosa dan lignin.
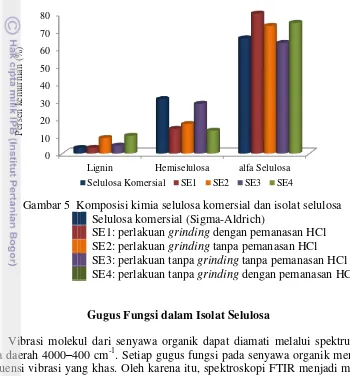
Gambar 5 menunjukkan hasil analisis komponen kimia pada selulosa komersial dan isolat selulosa. Kandungan hemiselulosa menurun oleh pemanasan dengan HCl dan pulping dengan NaOH. Kandungan hemiselulosa isolat pada perlakuan grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 14.09% dan 16.92%, sedangkan pada perlakuan tanpa grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 13.12% dan 28.51%. Menurut Zhang et al. (2010), pemanasan dengan asam dapat menghidrolisis pati dan hemiselulosa menjadi mono- atau oligosakarida yang dapat larut. Sementara itu, tahap delignifikasi, berhasil mengurangi kandungan lignin isolat selulosa hampir 67–90% dari kandungan lignin dalam serabut ela awal (31.09%). Kandungan lignin terendah didapatkan pada perlakuan grinding dengan pemanasan dengan HCl (3.24%).
Parameter keberhasilan isolasi selulosa adalah kadar selulosa alfa. Kandungan selulosa alfa pada perlakuan grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 79.96% dan 72.98%, sedangkan pada perlakuan
0
Isolat selulosa serabut ampas sagu
SE1
SE2
SE3
8
tanpa grinding dengan dan tanpa pemanasan dengan HCl berturut-turut sebesar 74.7% dan 63.2%. Nilai ini meningkat 1.5–1.9 kali dari kandungan selulosa alfa serabut awal, yaitu 41.47%. Berdasarkan analisis komponen kimia, perlakuan
grinding dan pemanasan HCl dapat meningkatkan kadar selulosa alfa. Hal ini berkaitan dengan penurunan kandungan hemiselulosa dan lignin pada isolat yang dihasilkan.
Gambar 5 Komposisi kimia selulosa komersial dan isolat selulosa Selulosa komersial (Sigma-Aldrich)
SE1: perlakuan grinding dengan pemanasan HCl SE2: perlakuan grinding tanpa pemanasan HCl SE3: perlakuan tanpa grinding tanpa pemanasan HCl SE4: perlakuan tanpa grinding dengan pemanasan HCl
Gugus Fungsi dalam Isolat Selulosa
Vibrasi molekul dari senyawa organik dapat diamati melalui spektrum IR pada daerah 4000–400 cm-1. Setiap gugus fungsi pada senyawa organik memiliki frekuensi vibrasi yang khas. Oleh karena itu, spektroskopi FTIR menjadi metode yang sederhana dan cepat untuk menentukan jenis senyawa berdasarkan vibrasi khasnya (Silverstein et al. 2005).
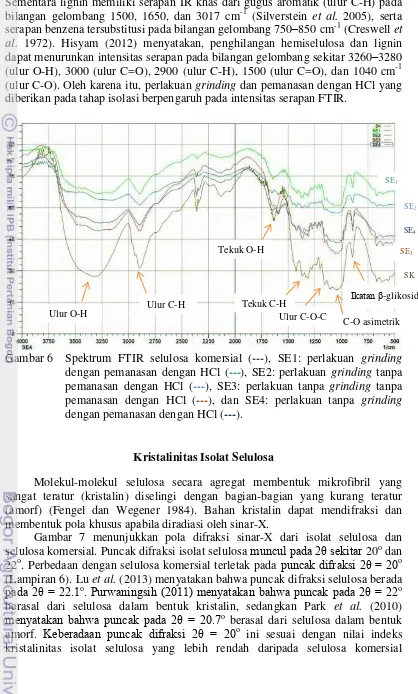
Keberhasilan tahapan isolasi selulosa ditunjukkan oleh kemiripan serapan FTIR isolat selulosa dengan selulosa komersial (Sigma-Aldrich) (Gambar 6). Terdapat serapan pada bilangan gelombang3340 cm-1 (ulur O-H), 2899 cm-1 (ulur C-H), 1639 (tekuk O-H), 1427 cm-1 (tekuk C-H), 1100–1000 cm-1 (ulur C-O-C dan C-O), dan 896 cm-1 (ika an β-glikosida) yang khas untuk selulosa (Lampiran 5) (Abidi et al. 2013; Lanthong et al. 2006).
Isolat selulosa dengan perlakuan grinding dan pemanasan dengan HCl memiliki intensitas serapan lebih rendah dibandingkan dengan tanpa pemanasan dengan HCl. Penurunan intensitas serapan ini disebabkan oleh penurunan kadar hemiselulosa dan lignin pada isolat. Hemiselulosa memiliki gugus fungsi yang hampir sama dengan selulosa, dan dibedakan dengan serapan IR asam uronat
9
Sementara lignin memiliki serapan IR khas dari gugus aromatik (ulur C-H) pada bilangan gelombang 1500, 1650, dan 3017 cm-1 (Silverstein et al. 2005), serta serapan benzena tersubstitusi pada bilangan gelombang 750–850 cm-1 (Creswell et al. 1972). Hisyam (2012) menyatakan, penghilangan hemiselulosa dan lignin dapat menurunkan intensitas serapan pada bilangan gelombang sekitar 3260–3280 (ulur O-H), 3000 (ulur C=O), 2900 (ulur C-H), 1500 (ulur C=O), dan 1040 cm-1 (ulur C-O). Oleh karena itu, perlakuan grinding dan pemanasan dengan HCl yang diberikan pada tahap isolasi berpengaruh pada intensitas serapan FTIR.
Gambar 6 Spektrum FTIR selulosa komersial (---), SE1: perlakuan grinding
dengan pemanasan dengan HCl (---), SE2: perlakuan grinding tanpa pemanasan dengan HCl (---), SE3: perlakuan tanpa grinding tanpa pemanasan dengan HCl (---), dan SE4: perlakuan tanpa grinding
dengan pemanasan dengan HCl (---).
Kristalinitas Isolat Selulosa
Molekul-molekul selulosa secara agregat membentuk mikrofibril yang sangat teratur (kristalin) diselingi dengan bagian-bagian yang kurang teratur (amorf) (Fengel dan Wegener 1984). Bahan kristalin dapat mendifraksi dan membentuk pola khusus apabila diradiasi oleh sinar-X.
Gambar 7 menunjukkan pola difraksi sinar-X dari isolat selulosa dan selulosa komersial. Puncak difraksi isolat selulosa mun ul pada 2θ seki a 20o dan 22o. Perbedaan dengan selulosa komersial terletak pada pun ak dif aksi 2θ 2 o (Lampiran 6). Lu et al. (2013) menyatakan bahwa puncak difraksi selulosa berada pada 2θ 22. o. Pu waningsih (2 ) menya akan ahwa pun ak pada 2θ 22o berasal dari selulosa dalam bentuk kristalin, sedangkan Park et al. (2010) menya akan ahwa pun ak pada 2θ 2 .7o
berasal dari selulosa dalam bentuk amorf. Ke e adaan pun ak dif aksi 2θ 2 o ini sesuai dengan nilai indeks kristalinitas isolat selulosa yang lebih rendah daripada selulosa komersial
10
(37.35%). Perlakuan pemanasan dengan HCl dengan atau tanpa grinding
menurunkan intensitas pun ak dif aksi pada 2θ 2 o (daerah amorf). Oleh karena itu, perlakuan ini menghasilkan indeks kristalinitas yang lebih tinggi (30.86% dan 28.91%) dibandingkan dengan tanpa pemanasan dengan HCl (23.64% dan 25.45%).
Perlakuan dengan grinding juga dapat meningkatkan kristalinitas isolat. Nilai indeks kristalinitas berkaitan dengan penurunan kadar hemiselulosa dan lignin pada selulosa. Menurut Zhang et al. (2010), indeks kristalinitas meningkat pada saat penghilangan lignin dan hemiselulosa. Sebaliknya, pemanasan dengan HCl dapat menurunkan derajat kristalinitas isolat. Menurut Achmadi (1990), HCl dapat menghidrolisis sebagian besar hemiselulosa dan menyerang sebagian selulosa.
Gambar 7 Difraktogram selulosa komersial (---), SE1: perlakuan grinding
dengan pemanasan HCl (---), SE2: perlakuan grinding tanpa pemanasan HCl (---), SE3: perlakuan tanpa grinding tanpa pemanasan HCl (---), dan SE4: perlakuan tanpa grinding dengan pemanasan HCl (---).
Hasil Analisis Termal
Analisis termal didefinisikan sebagai pengukuran sifat-sifat fisis dan kimia material sebagai fungsi suhu. Informasi tersebut dapat menjelaskan perubahan yang terjadi selama selulosa selama proses pemanasan. Degradasi selulosa terjadi dalam beberapa tahap, yaitu proses dehidrasi, dekarboksilasi, dan dekarbonisasi. Kurva DTA/TGA menunjukkan pola degradasi tersebut pada selulosa komersial dan isolat selulosa (Lampiran 7). Dekomposisi selulosa mulai terjadi pada 98–102
11
selulosa) terjadi pada 352–377 C dengan kehilangan massa 85–91%. Perlakuan pemanasan dengan HCl dengan atau tanpa grinding dapat meningkatkan kestabilan termal isolat selulosa.
SIMPULAN DAN SARAN
Simpulan
Selulosa berhasil diisolasi dengan beberapa tahapan dan perlakuan, yaitu preparasi dengan dan tanpa grinding, pulping dengan dan tanpa pemanasan dengan HCl, serta delignifikasi. Parameter keberhasilan isolasi ini ditunjukkan melalui kadar selulosa alfa. Perlakuan grinding dan pemanasan dengan HCl dapat meningkatkan kadar selulosa alfa dari 63.20% menjadi 79.96%. Spektrum FTIR menunjukkan serapan yang tidak jauh berbeda antara isolat selulosa dan selulosa komersial dengan se apan khas selulosa, yai u ika an β-glikosida diperoleh pada bilangan gelombang 894 cm-1. Perlakuan grinding dengan pemanasan dengan HCl menunjukkan indeks kristalinitas paling tinggi (30.86%). Analisis termal menunjukkan bahwa semua isolat mulai kehilangan massa pada suhu sekitar 98– 102 C dan mengalami kehilangan massa maksimum pada suhu sekitar 352–377
C.
Saran
Kajian lanjut perlu dilakukan terkait dengan karakteristik isolat selulosa seperti ukuran partikel, derajat polimerisasi dan derajat keputihan.
DAFTAR PUSTAKA
[ASTM] American Society for Testing Materials. 1975a. Standard test methods for holocellulose in wood. ASTM Standard D 1104-56 (reaffirmed 1972). Philadelphia (US): ASTM.
[ASTM] American Society for Testing Materials. 1975b. Standard test methods for cellulose in wood. ASTM Standard D 1103-60 (reaffirmed 1968). Philadelphia (US): ASTM.
[ASTM] American Society for Testing Materials. 1975c. Standard test methods for lignin in wood. ASTM Standard D 1106-56 (reaffirmed 1966). Philadelphia (US): ASTM.
Abidi N, Cabrales L, Haigler CH. 2013. Changes in the cell wall and cellulose content of developing cotton fiber investigated by FTIR spectroscopy.
12
Aditria R, Cahyono B, Swastawati F. 2013. Identifikasi komponen penyusun asap cair dari ampas sagu dan kulit batang tanaman sagu (Metroxylon sagu
Rottb) serta penentuan senyawa fenolat total dan aktivitas antioksidan.
Chem Info. 1:240-246.
Akpabio UD, Effiong IE, Akpapan AE. 2012. Preparation of pulp and cellulose acetate from nypa palm leaves. Int J Environ Bioeng. 1:179-194.
Bintoro MH. 2008. Bercocok Tanam Sagu. Bogor (ID): IPB Pr.
Bintoro MH, Yanuar M. Purwanto, Amarillis S. 2010. Sagu di Lahan Gambut. Bogor (ID): IPB Pr.
Creswell CJ, Runquist OA, Campbell MM. 1972. Spectrum Analysis of Organic Compound. Minnesota (US): Burgess.
Fang JM, Sun RC, Tomkinson J. 2000. Isolation and characterization of hemicellulose and cellulose from rye straw by alkaline peroxide extraction.
Cellulose. 7:87-107.
Fengel D, Wegener G. 1984. Wood: Chemistry, Ultrastructure, Reactions. New York (US): J Wiley.
Hisyam. 2012. Isolasi selulosa ampas sagu dengan delignifikasi menggunakan hidrogen peroksida [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Ibrahim SF. 2011. Thermal analysis and characterization of some cellulosic fabrics dyed by a new natural dye and mordanted with different mordants.
Int J Chem. 3(2):40-54. doi: 10.5539/ijc.v3n2p40
Irawadi TT. 2010. Teknologi separasi bahan aktif temu lawak menggunakan biopolimer termodifikasi berbasis limbah produksi sagu [laporan penelitian]. Bogor (ID): Lembaga Penelitian dan Pengabdian kepada Masyarakat, Institut Pertanian Bogor.
Lanthong P, Nuisin R, Kiatkamjornwong S. 2006. Graft copolymerization, characterization and degradation of cassava starch-g-acrylamide/itaconic acid superabsorbents. Carbohydr Polym. 66:229-245. doi: 10.1016/ j.carbol.2006.03.006
Leksana YK. 2000. Pemanfaatan limbah ampas sagu untuk budidaya tanaman sayuran [tesis]. Bogor (ID): Institut Pertanian Bogor.
Lu H, Gui Y, Zheng L, Liu X. 2013. Morphological, crystalline, thermal, and physicochemical properties of cellulose nanocrystals obtained from sweet potato residue. Food Res Int. 50:121-128. doi: 10.1016/ j.foodres.2012.10.013.
Matitaputty PR, Alfons JB. 2006. Inovasi teknologi pakan berbahan dasar ela sagu untuk ternak. Di dalam: Hetharia Maris ET, editor. Sagu dalam Revitalisasi Pertanian Maluku, 2006 Mei 29-31; Ambon, Indonesia. Ambon (ID): Badan Penerbit Fakultas Pertanian Universitas Patimura. hlm 100-106. Pan X, Sano Y. 1999. Atmospheric acetic acid pulping of the rice straw.
Holzforschung. 53:49-55.
Park S, Baker J, Himmel M, Parilla P, Jhonson D. 2010. Cellulose crystallinity index: measurement techniques and their impact on interpreting cellulose performance. Biotechnol Biofuel. 3:1-10. Tersedia pada: http://www. biotechnologyforbiofuel.com/conten/3/1/10.
13
Pushpamalar V, Langford SJ, Ahmad M, Lim YY. 2006. Optimization of reaction conditions for preparing carboxymethyl cellulose from sago waste.
Carbohydr Polym. 64:312-318. doi: 10.1016/j.carbpol.2005.12.003
Rojali A. 2011. Sintesis fase diam kromatografi kolom berbasis selulosa benzoate dari serabut ampas sagu [skripsi]. Bogor (ID): Institut Petanian Bogor. Sangadji I. 2009. Mengoptimalkan pemanfaatan ampas sagu sebagai pakan
ruminansia melalui biofermentasi dengan jamur tiram (Pleirotus ostreatus) dan amoniasi [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Setyorini A. 2011. Sintesis dan aplikasi selulosa-g-poliakrilamida sebagai fase diam kromatografi kolom dari serabut ampas sagu [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Sun JX, Xu F, Sun XF, Xiao B, Sun RC. 2005. Physico-chemical and thermal characterization of cellulose from barley straw. Polym Degrad Stability.
88:521-531. doi: 10.1016/j.polymdegradstab.2004.12.013
Silverstein RM, Bassler GC, Morrill TC. 2005. Spectrometric Identification of Organic Compound. Ed ke-7. New York (US): J Wiley.
Syakir M, Bintoro MH, Agusta H. 2009. Pengaruh ampas sagu dan kompos terhadap produktivitas lada perdu. J Litri. 4:168-173.
Zaitun, Saeni MS, Irawadi TT, Djoefrie B. 2001. Pemanfaatan limbah industri tapioka sebagai pupuk cair pada tanaman sayuran [laporan penelitian]. Bogor (ID): Lembaga Penelitian dan Pengabdian kepada Masyarakat, Institut Pertanian Bogor.
Zhang M, Qi W, Liu R, Su R, Wu S, He Z. 2010. Fractionating lignocellulose by formic acid: characterization of major components. Biomass Bioeng.
14
Lampiran 1 Pengolahan tepung sagu
Batang Sagu
Pengupasan kulit dan pemotongan
Kulit batang ---
Pemarutan
Peremasan
Penyaringan
Ampas sagu ---
Pengendapan
Air sisa ---
Pengeringan
Tepung sagu
Keterangan:
15
Lampiran 2 Diagram alir penelitian
Serabut ampas sagu
Dikeringkan Grinding 40 mesh Tanpa grinding
50 g sampel dipanaskan dengan 1 L HCl 3% (80 C, 1 jam)
Uji iodin (negatif)
50 g sampel dipulping dengan 1 L NaOH 20% (80 C, 2 jam)
20 g hasil pulping didelignifikasi dengan 500 mL H2O2 5% pada pH 12 (70 C)
Delignifikasi dilakukan secara bertahap selama 2, 3, 3 jam
SE3 SE4 SE1 SE2
Pencirian isolat selulosa Analisis
komponen kimia
Analisis kristalinitas
Analisis termal
16
Lampiran 3 Rendemen setiap tahap dan perlakuan isolasi selulosa serabut ela
17
Rendemen 55% Rendemen 48% Rendemen 51% Rendemen 50%
Delignifikasi
Rendemen 62% Rendemen 42% Rendemen 47% Rendemen 54%
Perlakuan isolasi dan persen rendemennya
Sampel Perlakuan isolasi Rendemen
18
Lampiran 4 Hasil analisis komponen kimia isolat selulosa dan selulosa komersial
Persen Komposisi (%) Serabut
awal
Selulosa
komersial SE1 SE2 SE3 SE4 Lignin 31.09 3.17 3.24 8.93 4.55 10.20 Hemiselulosa 18.16 31.15 14.09 16.92 28.51 13.12 α-Selulosa 41.47 65.87 79.96 72.98 63.20 74.70 Holoselulosa 70.63 97.02 94.05 89.9 91.71 87.82
Keterangan:
SE1: perlakuan grinding dengan pemanasan dengan HCl SE2: perlakuan grinding tanpa pemanasan dengan HCl
19
Lampiran 5 Interpretasi spektrum FTIR isolat selulosa dibandingkan dengan selulosa komersial
Bilangan gelombang (cm-1)
Serapan Acuan
SE1: perlakuan grinding dengan pemanasan dengan HCl SE2: perlakuan grinding tanpa pemanasan dengan HCl
20
Lampiran 6 Difraktogram isolat selulosa dan selulosa komersial
Selulosa komersial (Sigma-aldrich)
SE1: perlakuan grinding dengan pemanasan dengan HCl
SE2: perlakuan grinding tanpa pemanasan dengan HCl
SE3: tanpa perlakuan grinding dan tanpa pemanasan dengan HCl
21
Lampiran 7 Kurva DTA/TGA isolat selulosa dan selulosa komersial
Selulosa komersial (Sigma-aldrich)
22
lanjutan Lampiran 7
SE2: perlakuan grinding tanpa pemanasan dengan HCl
Kurva
23
lanjutan Lampiran 7
24
RIWAYAT HIDUP
Penulis dilahirkan di Cianjur pada tanggal 16 April 1990 dari Ayah Saepudin Bagus Salam dan Ibu Dedeh Suaebah. Penulis adalah putri keempat dari 4 bersaudara. Tahun 2008, penulis lulus dari SMA Negeri 1 Cilaku, Cianjur dan pada tahun yang sama, penulis lulus seleksi masuk Instititut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI). Penulis memilih Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.