KUANTIFIKASI SENYAWA PENGOTOR ORGANIK PADA
PRODUK BIOETANOL
EKO PRABOWO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
EKO PRABOWO. Kuantifikasi Senyawa Pengotor Organik pada Produk
Bioetanol. Dibimbing oleh ETI ROHAETI dan YOSI ARISTIAWAN.
Salah satu upaya yang dapat dilakukan dalam penghematan konsumsi
minyak bumi ialah penggunaan bahan bakar nabati (BBN)
.
Gasohol adalah salah
satu jenis BBN yang merupakan campuran bensin dengan dengan bioetanol.
Mutu
gasohol
dikendalikan dengan suatu bahan standar yang saat ini masih dalam tahap
pengembangan
.
Penentuan kemurnian bioetanol merupakan tahapan dalam
pengembangan bahan standar. Salah satu bagian dari penentuan kemurnian secara
tidak langsung ialah penentuan pengotor organik. Penelitian ini bertujuan
mendapatkan data pengotor organik pada 2 buah sampel bioetanol menggunakan
kromatografi gas. Metode analisis diverifikasi dengan parameter linearitas,
ketelitian, ketepatan, dan limit deteksi. Hasil analisis pengotor organik
menunjukkan bahwa dalam kedua sampel bioetanol terdapat 8 senyawa pengotor
organik berupa metanol, aseton, 2-propanol, propanol, etil asetat, isobutanol,
1-butanol, dan isoamil alkohol. Sampel 1 memiliki kemurnian sebesar 99.86% dan
konsentrasi metanol sebesar 294.40 ppm, sedangkan sampel 2 memiliki
kemurnian sebesar 99.85% dan konsentrasi metanol sebesar 178.26 ppm. Hasil
tersebut menunjukkan kedua sampel memenuhi syarat SNI 7390:2008 sebagai
bahan dasar pembuatan bahan standar.
Kata kunci: verifikasi metode, kemurnian bioetanol, pengotor organik,
kromatografi gas.
ABSTRACT
EKO PRABOWO. Quantification of Organic Impurity Compounds in Biethanol
Product. Supervised by ETI ROHAETI and YOSI ARISTIAWAN.
One effort in decreasing petroleum consumption is using gasohol. Gasohol
is one of biofuel which is a mixture of gasoline and bioethanol. Gasohol quality is
controlled by reference material which is now in developing process. Purity
assessment of bioethanol is a step in developing the reference material.
Quantification of organic impurity is part of indirect purity assessment. The aim
of this study was to obtain organic impurity data in bioethanol using gas
chromatography. The analysis method was verified based on parameters of
linearity, precision, accuracy, and detection limit. The result shows that organic
impurities in 2 bioethanol samples contain were 8 organic impurities, namely
methanol, acetone, 2-propanol, 1-propanol, ethyl acetate, isobutanol, 1-butanol,
and isoamyl alcohol. The purity of sample 1 was 99.86% and containing
294.40ppm methanol, and that of sample 2 was 99.85% with methanol contain of
178.26 ppm. The results showed that the quality of both samples met SNI
7390:2008 as base material to make reference material.
KUANTIFIKASI SENYAWA PENGOTOR ORGANIK PADA
PRODUK BIOETANOL
EKO PRABOWO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul skripsi : Kuantifikasi Pengotor Senyawa Organik pada Produk Bioetanol
Nama
: Eko Prabowo
NIM
: G44080018
Disetujui
Diketahui
Ketua Departemen Kimia
Prof. Dr. Ir. Tun Tedja Irawadi, M.S
NIP 19501227 197603 2 002
Tanggal Lulus:
Pembimbing I
Dr. Eti Rohaeti, M.S
NIP 19600807 198703 2 001
Pembimbing II
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas limpahan berkat dan
rahmat-Nya sehingga penulis dapat menyelesaikan karya ilmiah dengan judul
“Kuantifikasi Senyawa Pengotor Organik pada Produk Bioetanol”. Penelitian ini
dilakukan dari bulan April sampai Juli 2012 di Laboratorium Kimia Analitik dan
Standar, Pusat Penelitian Kimia, LIPI, Kawasan Puspiptek Serpong.
Penulis mengucapkan terima kasih kepada Dr Eti Rohaeti, MS selaku
pembimbing pertama dan Yosi Aristiawan SSi selaku pembimbing kedua yang
telah memberikan arahan dan dorongan semangat kepada penulis selama
penelitian. Ucapan terima kasih juga diberikan kepada Ibu Eka Sajekti atas
bantuan dan masukan selama penelitian berjalan.
Terima kasih tak terhingga kepada ayah, ibu, dan seluruh keluarga atas doa,
dukungan, dan kasih sayang yang telah diberikan. Penulis juga mengucapkan
terima kasih kepada Viola Monik, Rizki Septiani, Mutiara Wide, Rofiiqoh Inayati,
dan M Wahyu yang telah memberikan bantuan serta dukungan.
Penulis berharap tulisan ini dapat bermanfaat bagi perkembangan ilmu
pengetahuan.
Bogor, Desember 2012
RIWAYAT HIDUP
Penulis dilahirkan di Rejang Lebong Bengkulu pada tanggal 7 Februari
1990 sebagai anak pertama dari tiga bersaudara dari ayah Jalinus dan ibu Suprapti.
Tahun 2008, penulis lulus dari SMA Negeri 1 Curup dan pada tahun yang sama
lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi
Masuk IPB (USMI) pada Departemen Kimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam, IPB.
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE ... 1
Alat dan Bahan ... 1
Metode ... 1
HASIL DAN PEMBAHASAN ... 4
Identifikasi Senyawa berdasarkan kromatogram GC ... 4
Optimasi Pengukuran ... 4
Verifikasi Metode ... 4
Penentuan Pengotor Organik pada Bioetanol ... 6
SIMPULAN DAN SARAN ... 9
Simpulan ... 9
Saran ... 9
DAFTAR PUSTAKA ... 9
DAFTAR TABEL
Halaman
1
Hasil pengujian ketelitian ... 5
2
Pengujian limit deteksi metode ... 5
3 Identifikasi puncak pengotor bioetanol ...
7
DAFTAR GAMBAR
Halaman
1
Kromatogram standar NIST etanol dalam bahan bakar ... 3
2
Kurva regresi linear (a) split 1:200 dan (b) split 1:100 ... 4
3
Kromatogram sampel bioetanol (a) sampel 1 dan (b) sampel 2 ... 7
4
Struktur polidimetilsiloksana ... 8
5
Perbandingan konsentrasi pengotor sampel bioetanol ... 9
DAFTAR LAMPIRAN
Halaman
1
Diagram alir penelitian
...
12
2
Nilai SBR masing-masing
split ratio ...
...
.13
3
Pengujian linearitas ...13
4
Pengujian ketepatan ... 13
5
Jumlah puncak pengotor berdasarkan volume injeksi ... 14
6
Waktu retensi standar senyawa pengotor organik bioetanol ...15
PENDAHULUAN
Jumlah kendaraan bermotor di Indonesia terus mengalami peningkatan. Berdasarkan data dari Badan Pusat Statistik (2010), pada tahun 1987 jumlah kendaraan bermotor Indonesia hanya sebesar 7 981 480. Jumlah tersebut terus meningkat hampir 10 kali lipat pada tahun 2009, yaitu sebesar 70 714 569. Peningkatan jumlah kendaraan bermotor tidak diikuti dengan peningkatan produksi minyak mentah tanah air. Produksi minyak mentah Indonesia pada tahun 1996 sebesar 485 573.80 barel, sedangkan pada tahun 2010 turun menjadi 300 923.30 barel (BPS 2011). Jumlah cadangan minyak bumi Indonesia berdasarkan data Januari 2011 ialah sebesar 7.41 miliar barel, sehingga dengan tingkat produksi saat ini maka cadangan minyak bumi Indonesia akan habis dalam jangka waktu 12 tahun (BPMIGAS 2011). Oleh sebab itu, diperlukan suatu langkah untuk menghemat konsumsi bahan bakar minyak (BBM) dalam negeri.
Penggunaan bahan bakar nabati (BBN)
atau dikenal juga dengan istilah biofuel
merupakan salah satu upaya yang dapat dilakukan untuk mengatasi permasalahan tersebut. BBN merupakan campuran antara BBM dengan bahan bakar alternatif yang
dapat diperbarui. Meskipun tidak
menggantikan secara keseluruhan,
penggunaan bahan tersebut dapat menghemat penggunaan BBM yang berasal dari minyak bumi. Sumber BBN dapat berupa tanaman pertanian terutama kelapa sawit dan jarak pagar yang menghasilkan biodisel serta ketela pohon dan tebu yang menghasilkan bioetanol. Biodisel digunakan sebagai bahan komposisi
solar yang dikenal sebagai biosolar,
sedangkan bioetanol digunakan sebagai
komposisi bensin yang dikenal sebagai gasohol (Balat & Balat 2009). Produksi bioetanol saat ini sudah berkembang ke arah
penggunaan bahan yang mengandung
lignoselulosa berupa hasil hutan dan limbah pengolahan hasil hutan (EREC 2007).
Saat ini penggunaan biosolar secara luas di Indonesia telah dilakukan, namun penggunaan gasohol masih sangat terbatas. Menurut Prihanandana dan Hendroko (2007) program pemanfaatan bioetanol untuk bahan bakar kendaraan bermotor di Indonesia sudah dikaji sejak tahun 1980 hingga pada tingkat pengujian kendaraan dengan bahan bakar gasohol. Namun, rendahnya harga minyak mentah dan naiknya harga bahan baku bioetanol pada saat itu menyebabkan program
tersebut kemudian dihentikan. Saat ini harga minyak mentah dunia terus mengalami peningkatan dan cadangan minyak Indonesia jumlahnya semakin terbatas. Oleh sebab itu, program tersebut dilanjutkan kembali.
Menurut Ballat dan Ballat (2009),
komposisi yang paling umum ialah 10% bioetanol dan 90% bensin yang dikenal dengan istilah E10. Komposisi tersebut tidak
memerlukan modifikasi pada mesin.
Modifikasi pada mesin kendaraan
memungkinkan penggunaan bioetanol dengan proporsi yang lebih banyak. Yuksel dan
Yuksel (2004) melakukan modifikasi
sederhana pada karburator kendaraan dan menghasilkan mesin yang dapat menggunakan komposisi 60% bioetanol dan 40% bensin sebagai bahan bakar. Penggunaan bioetanol sebagai pengganti atau substitusi bensin telah dilakukan di berbagai negara. Amerika Serikat telah memulai program penggunaan bietanol sebagai bahan bakar sejak tahun 1980 dan saat ini Amerika Serikat telah mengembangkan
teknologi kendaraan dengan sistem dual fuel
atau Flexible Fuel Vehicle. Tekonologi ini
memungkinkan penggunaan E85 yang
merupakan komposisi antara 85% bioetanol
dan 15% bensin (Ulmer et al. 2004).
Konsentrasi etanol dalam BBN perlu dianalisis, sebab berpengaruh terhadap
fungsinya sebagai bahan bakar.
Ketidaksesuaian konsentrasi etanol dengan jenis mesin dapat mengakibatkan kerusakan pada mesin kendaraan. Analisis secara kuantitatif etanol BBN membutuhkan bahan standar, namun harga bahan standar tersebut sangat mahal. Oleh sebab itu, perlu dilakukan pengembangan bahan standar tersebut di
dalam negeri. Ketentuan mengenai standar
bioetanol terdenaturasi (bioetanol yang sudah diracuni) sebagai gasohol yang berlaku di Indonesia tercantum dalam SNI 7390:2008 yang menyaratkan biotanol yang digunakan sebagai gasohol harus memiliki konsentrasi
99.5% yang lazim dikenal sebagai fuel grade
ethanol (Prihandana & Hendroko 2007). Kemurnian bioetanol merupakan hal yang sangat penting untuk diperhatikan karena akan
berpengaruh terhadap kinerja mesin
kendaraan. Oleh sebab itu, dibutuhkan data analisis kemurnian bioetanol yang valid sebagai acuan kualitas bioetanol. Penentuan pengotor organik merupakan salah satu tahap
dalam penentuan kemurnian dengan
pendekatan tidak langsung. Penelitian
bertujuan mendapatkan data pengotor organik yang valid dari dua sampel bioetanol
Validitas data dijamin dengan verifikasi metode menggunakan bahan standar yang diakui secara internasional. Hasil analisis pengotor organik tersebut selanjutnya dapat digunakan untuk memutuskan kelayakan bioetanol tersebut sebagai bahan baku standar etanol dalam bahan bakar.
BAHAN DAN METODE
Alat dan Bahan
Alat yang digunakan pada penelitian ini berupa seperangkat alat kromatografi gas GC Shimadzu 17-A, dengan spesifikasi kolom
Equity™ -1 100m×0.25mm, detektor FID, gas
helium, gas nitrogen, gas argon, compressor
udara, dan syringe. Selain itu juga digunakan
alat lain berupa neraca analitik dan alat-alat gelas.
Bahan yang digunakan berupa standar National Institute of Standard and Technology (NIST) etanol 10% dalam bahan bakar yang digunakan dalam proses optimasi pengukuran dan verifikasi metode. Selain itu, digunakan juga standar metanol, etanol, aseton, isopropil alkohol, 1-propanol, 2-butanol, etil asetat, isobutanol, 1-butanol, dan isoamil alkohol yang digunakan untuk penentuan konsentrasi pengotor organik sampel bioetanol. Bahan lain yang digunakan berupa heksana dan dua buah sampel bioetanol yang berasal dari Unit Produksi bioetanol Pusat Penelitian Kimia-LIPI Serpong.
Metode
Metode yang dilakukan pada penelitian mengikuti diagram alir pada Lampiran 1,
meliputi optimasi pengukuran, verifikasi
metode analisis, serta penentuan pengotor organik pada sampel bioetanol.
Optimasi pengukuran (Nuryatini et al.
2011)
Optimasi pengukuran berupa optimasi split
ratio dilakukan dengan cara penginjeksian sebanyak 0.1 µl standar NIST etanol dalam bahan bakar ke dalam sistem GC dengan kondisi sebagai berikut, (1) suhu injektor 300°C, (2) suhu detektor 300°C, (3) oven 40°C selama 10 menit kemudian suhu dinaikkan 30°C/menit sampai 250°C dan ditahan selama 19 menit, (4) gas pembawa
helium dengan laju alir 1 ml/menit. Split ratio
divariasikan dengan nilai 1:50, 1:75, 1:100, 1:125, 1:150, 1:175, 1:200. Injeksi dilakukan masing-masing sebanyak lima kali ulangan
untuk tiap split ratio dan dihitung nilai
simpangan baku relatif (SBR) luas puncak
etanol dari setiap split ratio. Kemudian dipilih
split ratio dengan nilai SBR paling kecil.
Verifikasi metode
Parameter-parameter yang diukur dalam
verifikasi adalah linearitas, ketelitian,
ketepatan, dan limit deteksi. Sebelum
dilakukan verifikasi terlebih dahulu dilakukan preparasi larutan standar NIST.
Preparasi larutan standar NIST.
Larutan standar NIST yang digunakan memiliki konsentrasi etanol 10%. Pembuatan standar dengan konsentrasi yang lebih rendah dilakukan dengan cara mengencerkan standar NIST dengan menggunakan pelarut heksana.
Linearitas. Linearitas diukur dengan cara injeksi 0.1 µl standar NIST etanol dalam bahan bakar dengan konsentrasi 0.5%, 1%, 2%, 4%, 6%, 8%, dan 10% ke dalam sistem GC dan dilakukan sebanyak dua kali pengulangan.
Ketelitian. Ketelitian diukur dengan cara injeksi sebanyak 0.1 µl larutan standar NIST etanol dalam bahan bakar dengan konsentrasi 4% sebanyak tujuh kali ulangan.
Ketepatan. Ketepatan diukur dengan cara menginjeksikan 0.1 µl standar NIST etanol dalam bahan bakar 4% sebanyak tiga kali
ulangan. Konsentrasi etanol kemudian
dihitung dengan menggunakan kurva standar. Ketepatan pengukuran dihitung dengan cara
membandingkan konsentrasi etanol
berdasarkan pengukuran dengan konsentrasi etanol sebenarnya berdasarkan penimbangan.
Limit deteksi. Limit deteksi ditentukan dengan cara menginjeksikan 0.1 µl standar NIST etanol dalam bahan bakar 0.1% ke dalam sistem GC dan dilakukan pengamatan terhadap puncak etanol. Jika masih terdapat puncak etanol diinjeksikan lagi larutan standar
dengan konsentrasi yang lebih kecil.
Penginjeksian dilakukan sampai puncak etanol tidak terdeteksi lagi.
Penentuan pengotor organik pada sampel bioetanol (Wong et al. 2011)
Penentuan pengotor organik pada
bioetanol diawali dengan preparasi larutan standar campuran pengotor. Selanjutnya, dilakukan identifikasi semua kemungkinan pengotor organik pada sampel. Setelah semua
pengukuran konsentrasi tiap pengotor dan penghitungan kemurnian sampel.
Preparasi standar campuran. Standar
campuran dibuat dengan cara mengambil standar metanol, etanol, aseton, isopropil alkohol, 1-propanol, 2-butanol, etil asetat, isobutanol, 1-butanol, dan isoamil alkohol masing-masing sebanyak 1% berdasarkan bobot. Standar-standar tersebut kemudian dicampurkan ke dalam vial dan dilarutkan
menggunakan etanol. Standar dengan
konsentrasi lebih kecil dibuat dengan cara mengencerkan standar campuran stok tersebut menggunakan pelarut etanol.
Identifikasi senyawa pengotor organik
pada produk bioetanol. Sebanyak 0.3 µl
bioetanol diinjeksikan ke dalam sistem GC,
kemudian diamati puncak-puncak pada
kromatogram. Penginjeksian dilakukan lagi dengan menambahkan volume injeksi sampai tidak ada lagi puncak pengotor yang muncul pada kromatogram. Selanjutnya puncak-puncak tersebut diidentifikasi menggunakan standar pengotor bietanol. Volume injeksi yang menghasilkan puncak terbanyak dan volume paling kecil selanjutnya digunakan
untuk pengukuran konsentrasi pengotor
organik pada sampel bioetanol.
Pengukuran Konsentrasi Senyawa
Pengotor Organik dan Penentuan
Kemurnian Sampel. Pengukuran konsentrasi
pengotor organik dilakukan dengan
menggunakan standar eksternal. Standar campuran dari semua pengotor organik disiapkan dengan konsentrasi 15, 50, 100, 150, 300, dan 1000 ppm. Standar pengotor organik dan sampel bioetanol kemudian diinjeksikan ke dalam sistem GC. Konsentrasi pengotor dalam sampel bioetanol kemudian diukur berdasarkan kurva standar eksternal. Pengukuran konsentrasi pengotor organik pada sampel bioetanol dilakukan sebanyak tiga kali ulangan. Konsentrasi total dari semua
pengotor digunakan untuk menghitung
kemurnian sampel.
HASIL DAN PEMBAHASAN
Identifikasi Senyawa berdasarkan kromatogram GC
Bahan standar etanol dalam bahan bakar
yang digunakan berasal dari National Institute
of Standards and Technology (NIST) yang terdiri atas tiga senyawa penyusun, yaitu etanol, isooktana, dan heptana. Kromatogram
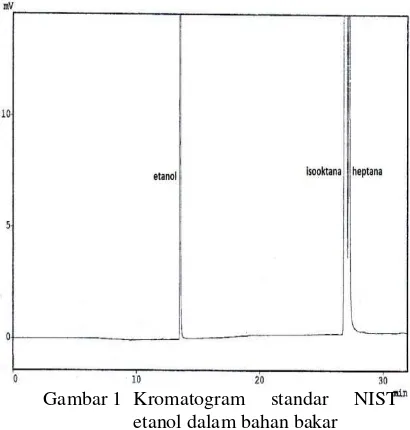
yang dihasilkan dari standar ini dapat dilihat pada Gambar 1.
Waktu retensi puncak suatu senyawa dipengaruhi oleh titik didih senyawa dan kepolaran dari senyawa tersebut. Kolom yang digunakan pada instrumen GC adalah polidimetilsiloksana yang bersifat nonpolar, sehingga senyawa yang bersifat nonpolar akan tertahan lebih lama pada kolom dibandingkan senyawa polar. Etanol memiliki waktu retensi sebesar 13.5 menit. Waktu retensi yang kecil tersebut disebabkan etanol memiliki titik didih yang rendah, yaitu sebesar 78˚C. Selain itu etanol juga bersifat polar, sehingga tidak tertahan terlalu lama pada kolom. Kedua komponen lainnya memiliki titik didih yang lebih besar dibandingkan etanol, yaitu keduanya memiliki titik didih sebesar 99˚C . Kedua komponen tersebut juga merupakan hidrokarbon yang bersifat nonpolar. Oleh sebab itu, kedua komponen tersebut memiliki waktu retensi yang lebih besar dari etanol. Titik didih yang sama tersebut menyebabkan puncak isooktana dan puncak heptana tidak
terpisah dengan baik. Berdasarkan
penginjeksian standar didapatkan waktu retensi isooktana ialah sebesar 26.9 menit. Berdasarkan hasil tersebut didapatkan untuk puncak kedua merupakan puncak isooktana, sedangkan untuk puncak ketiga merupakan puncak heptana. Heptana memiliki struktur yang lebih lurus dibandingkan isooktana,
sehingga sifatnya lebih nonpolar
dibandingkan isooktana. Sifat heptana yang
cenderung lebih nonpolar tersebut
menyebabkan waktu retensi heptana lebih besar dari isooktana.
Gambar 1 Kromatogram standar NIST
Optimasi Pengukuran
Optimasi pengukuran pada percobaan
dilakukan dengan cara mengubah split ratio.
Split ratio merupakan fasilitas pada GC yang memungkinkan pengguna untuk mengatur banyaknya sampel yang masuk ke dalam
kolom. Angka pada split ratio merupakan
perbandingan antara banyaknya sampel yang masuk ke dalam kolom dengan sampel yang
dibuang. Semakin besar nilai split ratio, maka
semakin sedikit sampel yang masuk ke dalam
kolom (Eiceman et al. 2002). Optimasi
pengukuran bertujuan untuk mendapatkan kondisi instrumen yang memberikan puncak etanol yang baik. Puncak yang baik ini ditunjukkan dengan keterpisahannya dengan puncak lain. Selain itu, puncak yang baik juga dapat dilihat dari keterulangan nilai luas puncaknya.
Berdasarkan kromatogram pada Gambar 1, terlihat bahwa puncak etanol sudah terpisah dengan baik dari kedua puncak lainnya. Oleh
sebab itu, optimasi dilakukan untuk
mendapatkan puncak etanol dengan luas puncak yang memiliki keterulangan paling baik (nilai SBR paling kecil). Data nilai SBR dari 5 kali pengulangan tiap variasi split ratio disajikan pada Lampiran 2. Hasil dari
optimasi memperlihatkan bahwa split ratio
1:200 memiliki nilai SBR yang paling kecil, sehingga untuk proses verifikasi metode
digunakan split ratio 1:200.
Verifikasi Metode
Verifikasi metode digunakan untuk
menjamin suatu metode menghasilkan data yang memiliki arti dan dapat dipercaya
(Taverniers et al. 2004). Pada penelitian ini
dilakukan verifikasi untuk menjamin bahwa
hasil analisis pengotor organik yang
didapatkan dengan kolom GC baru bersifat valid. Hasil analisis yang didapatkan harus dapat dipercaya karena data pengotor organik ini akan digunakan untuk menentukan kemurnian dari sampel bioetanol yang selanjutnya akan digunakan sebagai acuan
kualitas dari bioetanol. Verifikasi ini
dilakukan dengan menggunakan standar NIST etanol dalam bahan bakar. Hal ini dilakukan karena pada penelitian selanjutnya akan dikembangkan bahan standar etanol dalam bahan bakar. Verifikasi merupakan pengujian kembali keabsahan suatu metode yang pernah divalidasi sebelumnya. Oleh sebab itu, parameter yang diujikan hanya meliputi pengujian linearitas, ketelitian, ketepatan, dan limit deteksi.
Linearitas
Linearitas merupakan kemampuan
prosedur analisis untuk menghasilkan suatu hasil pengujian yang sebanding dengan konsentrasi analat yang terdapat di dalam
sampel (Chan et al. 2004). Berdasarkan data
optimasi pengukuran didapatkan bahwa split
ratio 1:200 memiliki nilai keterulangan yang
paling baik. Menurut Eiceman et al. (2004)
split ratio yang besar cocok digunakan untuk analat dengan konsentrasi yang besar dan kurang baik untuk konsentrasi kecil. Semakin
besar nilai split ratio semakin banyak pula
sampel yang dibuang. Oleh sebab itu, jika
nilai split ratio yang besar digunakan untuk
menganalisis sampel dengan konsentrasi rendah, maka puncak tidak akan dapat dideteksi.
Pengujian linearitas selain menggunakan split ratio 1:200 dilakukan juga dengan
menggunakan split ratio 1:100. Split ratio
1:100 dipilih karena pada verifikasi
sebelumnya yang dilakukan oleh Nuryatini et
al. (2011), split ratio ini menghasilkan
pemisahan paling baik. Meskipun berdasarkan
hasil optimasi pengukuran, split ratio yang
memiliki keterulangan yang paling baik
setelah split ratio 1:200 ialah split ratio
1:150, namun split ratio tersebut dinilai masih
terlalu besar dan dikhawatirkan menghasilkan respon yang kurang baik. Kurva regresi linear hasil pengujian linearitas untuk kedua nilai split ratio ditampilkan pada Gambar 2, sedangkan data pengujian linearitas
masing-masing split ratio dicantumkan pada
Lampiran 3.
(a)
(b)
Gambar 2 Kurva regresi linear (a) split 1:200 dan (b) split 1:100
y = 8646,x - 4890, R² = 0.998
-5 0 5 10
0 5 10
lu a s p u n ca k (× 1 0 2) konsentrasi (%)
y = 3931,x - 2210, R² = 0.988
-2 0 2 4
0 5 10
Hasil tersebut menunjukkan bahwa split ratio 1:100 memiliki respon yang lebih linear
dari split ratio 1:200. Hal tersebut dapat
dilihat dari nilai R2 split ratio 1:100 sebesar
0.998, sedangkan untuk split ratio 1:200
memiliki nilai R2 hanya sebesar 0.988. Batas
penerimaan linearitas berdasarkan AOAC
(1998) ialah nilai R2 minimal 0.997. Oleh
sebab itu, linearitas dari split ratio 1:100
masih diterima, sedangkan linearitas split
ratio 1:200 tidak diterima. Berdasarkan hasil tersebut, proses verifikasi selanjutnya hanya
dilakukan dengan split ratio 1:100.
Ketelitian
Ketelitian merupakan ukuran kedekatan setiap hasil analisis yang dilakukan berulang kali untuk sampel yang homogen pada kondisi analisis yang sama. Ketelitian diukur dari nilai
simpangan baku relatif (SBR) dari
pengukuran berulang (Chan et al. 2004). Hasil
pengujian ketelitian dapat dilihat pada Tabel 1.
Tabel 1 Hasil pengujian ketelitian
Ulangan luas puncak
1 2 3 4 5 6 7 30283 30203 29717 29672 30621 29982 30520 Rerata Simpangan baku SBR (%) 30142.5714 370.3714 1.2287
Dari hasil pengujian sebanyak 7 kali pengulangan didapatkan nilai RSD sebesar 1.2287%. Berdasarkan AOAC (1998), batas penerimaan ketelitian untuk sampel dengan konsentrasi 1 – 10% ialah maksimum sebesar 1.5%, sehingga pengujian ketelitian yang dilakukan masih diterima. Hasil pengujian
ketelitian tersebut menunjukkan bahwa
metode analisis dapat memberikan hasil analisis dengan keterulangan yang baik.
Ketepatan
Ketepatan merupakan ukuran kedekatan nilai yang diperoleh dari hasil analisis dengan
nilai sebenarnya (Chan et al. 2004). Hasil
pengujian ketepatan disajikan pada Lampiran 4. Berdasarkan hasil tersebut, pengujian
terhadap ketepatan didapatkan sebesar
99.1442%. Batas penerimaan nilai ketepatan untuk sampel dengan konsentrasi 1% – 10%
sebesar 95% – 102% (AOAC 1998), sehingga hasil pengujian ketepatan tersebut masih diterima. Nilai ketepatan yang besar tersebut menunjukkan bahwa nilai yang didapatkan dari pengukuran dengan nilai yang sebenarnya sangat dekat.
Limit deteksi
Limit deteksi ialah konsentrasi analat yang terendah yang masih dapat dideteksi oleh
sistem (Chan et al. 2004). Hasil pengujian
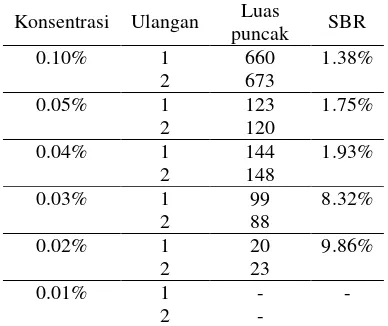
limit deteksi disajikan pada Tabel 2. Hasil pengujian terhadap limit deteksi menunjukkan bahwa limit deteksi sistem ialah sebesar 0.02%. AOAC (1998) menyaratkan nilai SBR yang baik untuk sampel dengan konsentrasi di bawah 0.1% ialah kurang dari 10%. Berdasarkan hasil tersebut, pengujian terhadap konsentrasi tersebut juga masih memiliki keterulangan yang baik.Keterulangan yang baik tersebut menunjukkan bahwa metode analisis masih dapat mendeteksi puncak dengan stabil meskipun dengan konsentrasi kecil.
Tabel 2 Pengujian limit deteksi
Konsentrasi Ulangan Luas
puncak SBR
0.10% 1
2
660 673
1.38%
0.05% 1
2
123 120
1.75%
0.04% 1
2
144 148
1.93%
0.03% 1
2
99 88
8.32%
0.02% 1
2
20 23
9.86%
0.01% 1
2
- -
-
Hasil pengujian linearitas, ketepatan, dan ketelitian yang dilakukan pada penelitian ini lebih baik dari verifikasi yang dilakukan
sebelumnya oleh Nuryatini et al. (2011). Pada
verifikasi sebelumnya menghasilkan nilai ketepatan 98.94% % dan ketelitian 3.7605%. Verifikasi pada tahun sebelumnya yang
menggunakan kolom innowax dengan panjang
Penentuan Pengotor Organik pada Produk Bioetanol
Bioetanol merupakan etanol (C2H5OH)
yang dihasilkan dari fermentasi biomassa yang dapat diperbarui, contohnya hasil pertanian dan hasil hutan (Yunoki & Saito 2009). Bioetanol yang diproduksi dari hasil pertanian yang mengandung pati dan gula disebut sebagai bioetanol generasi pertama, sedangkan bioetanol yang dihasilkan dari bahan yang mengandung lignoselulosa disebut bioetanol generasi kedua (EREC 2007). Saat ini produksi bioetanol dari bahan pangan perlahan-lahan mulai ditinggalkan karena mencuatnya isu mengenai ketahanan pangan. Sebagai gantinya produksi bioetanol saat ini terus diupayakan dari bahan nonpangan, yaitu
dari biomassa yang mengandung
lignoselulosa. Selain potensinya yang sangat besar produksi bioetanol dari biomasa ini juga dapat mengatasi permasalahan pencemaran akibat limbah pabrik yang masih mengandung lignoselulosa (Balat & Balat 2009 ). Bioetanol yang dianalisis pada penelitian ini dihasilkan dari fermentasi tandan kosong kelapa sawit (TKKS). TKKS merupakan limbah dari
pabrik pengolahan kelapa sawit yang
dihasilkan dalam jumlah besar. Bahan ini masih dapat dimanfaatkan sebagai bahan baku pembuatan bioetanol karena mengandung lignoselulosa.
Salah satu syarat bioetanol agar dapat digunakan sebagai gasohol berdasarkan SNI 7390:2008 ialah harus memiliki kemurnian yang sangat tinggi, yaitu sebesar 99.5%. Kemurnian yang tinggi tersebut agar sifat dari campuran bensin dan etanol yang dihasilkan sesuai dengan harapan. Jika konsentrasi pengotor terlalu tinggi, dikhawatirkan akan mengganggu proses pembakaran bahkan dapat merusak mesin kendaraan bermotor (Yuksel & Yuksel 2004). Selain itu, SNI 7390:2008 juga menyaratkan konsentrasi metanol yang terkandung dalam bietanol tidak boleh melebihi 300 ppm. Konsentrasi metanol dalam bioetanol yang akan digunakan sebagai bahan bakar tidak boleh terlalu tinggi karena menurut Prihandana dan Hendroko (2007), metanol bersifat sangat korosif bahkan terhadap alumunium yang biasanya digunakan sebagai pelapis antikarat, sehingga jika konsentrasi metanol terlalu tinggi akan menyebabkan korosi sehingga akan merusak mesin kendaraan bermotor. Sifat korosif ini disebabkan metanol bersifat asam dengan keberadaan air dan memiliki nilai pKa sebesar 15.5 (Fessenden & Fessenden 1997). Sifat
asam ini menyebabkan metanol mudah melepaskan proton dan bereaksi dengan logam. Pengotor organik lain sifat asamnya lebih lemah dibandingkan metanol.
Secara umum, penentuan kemurnian senyawa kimia organik kemurnian tinggi dilakukan dengan pendekatan tidak langsung, yaitu dengan cara mengkuantifikasi semua kemungkinan pengotor yang terdapat pada
sampel. (Wong et al. 2011). Pendekatan tidak
langsung digunakan pada penelitian untuk menentukan kemurnian bioetanol karena pendekatan secara langsung menggunakan kromatografi gas tidak mungkin dilakukan karena konsentrasi bioetanol yang sangat besar. Teknik lain yang dapat dilakukan untuk
menentukan kemurnian etanol secara
langsung ialah dengan metode titrimetri. Metode ini juga tidak dapat digunakan karena hasil yang akan didapat hanya berupa profil dari bioetanol. Berdasarkan SNI 7390:2008 selain menyaratkan kemurnian dari bioetanol, disyaratkan pula batas dari konsentrasi metanol. Oleh sebab itu, penentuan kemurnian bioetanol lebih tepat dilakukan dengan pendekatan secara tidak langsung.
Identifikasi senyawa pengotor organik pada produk bioetanol
Langkah pertama yang dilakukan dalam penentuan pengotor organik pada produk
bioetanol ialah identifikasi semua
kemungkinan senyawa pengotor organik yang terdapat pada sampel. Sebelumnya ditentukan
terlebih dahulu volume injeksi yang
menghasilkan jumlah puncak pengotor
maksimum. Setelah didapatkan jumlah puncak pengotor maksimum, kemudian ditentukan volume injeksi minimum yang menghasilkan jumlah puncak pengotor maksimum tersebut.
Pemilihan volume injeksi minimum
(a)
(b)
Setelah didapatkan
maksimum yang terda
bioetanol, langkah
identifikasi puncak-punca
Puncak tersebut diid
membandingkan waktu
pengotor dengan waktu
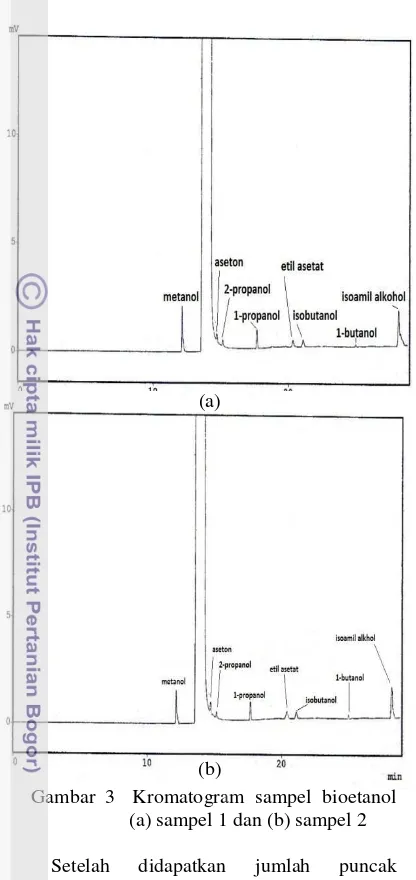
* S1: Sampel 1, S2: Sampel 2 Gambar 3 Kromatogra
(a) sampel 1
no
Waktu retensi (menit)
S1* S2*
1 2 3 4 5 6 7 8 11.9 14.6 15.0 17.5 20.9 22.2 23.8 28.0 12.0 14.7 15.1 17.6 21.1 22.1 24.0
28.1 Iso
an jumlah puncak
dapat dalam sampel
berikutnya ialah
cak pengotor tersebut.
iidentifikasi dengan
u retensi puncak
ktu retensi standar
senyawa pengotor yang um bioetanol yang disajikan Hasil identifikasi menunju sampel memiliki pengoto jenis yang sama. Pengotor sampel berupa metanol, ase propanol, etil asetat, isob dan isoamil alkohol. Hasil i disajikan pada Tabel 3.
Besarnya waktu rete senyawa dipengaruhi ole Selain itu, dipengaruhi j antara senyawa dengan berkaitan dengan kepolaran titik didih suatu senyawa b nilai bobot molekulnya. Se molekul, maka semakin b yang bekerja antar molek Akibatnya semakin ting Namun terdapat pengecual golongan alkohol. Terlih metanol dengan bobot m kecil dari aseton memilik lebih besar dari aseton ya molekul yang lebih besar. karena terdapat ikatan hidro pada alkohol. Ikatan hidro dibandingkan gaya Londo didih alkohol akan tinggi m bobot molekul kecil. Hal te pula pada etil asetat dan Meskipun memiliki bob hampir sama, titik didih eti di bawah isoamil alkoho didih tersebut terjadi kare memiliki ikatan hidrogen Senyawa yang memiliki titi akan memiliki waktu re besar. Hal tersebut dapat di 2-propanol, 1-propanol, iso dan isoamil alkohol. U puncak senyawa-senyawa dengan titik didihnya.
Tabel 3 Identifikasi puncak pengotor sampel ram sampel bioetanol
l 1 dan (b) sampel 2
Senyawa BM (g mol
-1 ) (CRC 1981) Td (ºC) (CRC 1981) K ( Metanol Aseton 2-propanol 1-propanol Etil asetat Isobutanol 1-butanol Isoamil alkohol 32.04 58.08 60.10 60.10 88.11 74.12 74.12 88.15 64.7 56.2 82.5 97.0 77.1 107.9 118.0 131.1
umum terdapat pada pada Lampiran 6. jukkan bahwa kedua tor organik dengan or organik dari kedua aseton, 2-propanol, 1-sobutanol, 1-butanol,
il identifikasi tersebut
tensi puncak suatu oleh titik didihnya. juga oleh interaksi n fase diam yang rannya. Secara umum berhubungan dengan emakin besar bobot besar gaya London lekul suatu senyawa. nggi titik didihnya. ualian untuk senyawa lihat pada Tabel 3 molekul yang lebih liki titik didih yang yang memiliki bobot r. Hal ini disebabkan drogen antar senyawa drogen ini lebih kuat on. Akibatnya titik i meskipun memiliki tersebut dapat dilihat an isoamail alkohol. obot molekul yang etil asetat berada jauh hol. Perbedaan titik rena isoamil alkohol n antar molekulnya. titik didih yang tinggi retensi yang makin dilihat pada senyawa isobutanol, 1-butanol, Urutan munculnya wa tersebut sesuai
Pengecualian terjad metanol, aseton, dan etil a ketiga senyawa tersebut pertambahan titik didi metanol lebih kecil di Padahal metanol memili lebih tinggi dibandingkan juga terjadi pada etil memiliki waktu retensi didasarkan pada titik puncak etil asetat akan k Pada kromatogram puncak waktu retensi sebesar 20. setelah puncak 1-propano Perbedaan waktu rete akibat interaksi senyawa penyusun kolom. Fase di pada penelitian berupa
yang bersifat no
polidimetilsiloksana da
Gambar 4. Senyawa yang kepolaran dengan fase dia kuat, sehingga akan terta kolom. Pada Tabel 3 relatif dari masing-masin polar senyawa nilainya sedangkan semakin no semakin mendekati 0. Ase bersifat nonpolar diba Akibatnya dengan titik rendah aseton tertahan leb
dibandingkan metanol,
retensinya lebih besar dib Hal tersebut juga dapat retensi etil asetat. Me memiliki titik didih yang retensinya besar karena e non polar, sehingga ditah kolom.
Suhu injektor dan suh pada suhu tinggi, yaitu s yang tinggi pada injekto semua senyawa yang ter teruapkan dan dapat dibaw dalam kolom. Suhu detekt dengan tujuan yang sam
Gambar 4 Struktur
adi pada senyawa
il asetat. Waktu retensi t tidak sesuai dengan idih. Waktu retensi dibandingkan aseton. iliki titik didih yang an aseton. Hal tersebut il asetat. Etil asetat si yang besar. Jika k didih, seharusnya keluar setelah aseton. cak etil asetat memiliki 0.8 menit dan muncul nol.
etensi tersebut terjadi wa dengan fase diam diam yang digunakan a polidimetilsiloksana
nonpolar. Struktur
dapat dilihat pada
ng memiliki kesamaan diam akan berinteraksi rtahan lebih lama pada disajikan kepolaran ing senyawa. Semakin a akan mendekati 1, nonpolar maka akan seton cenderung lebih bandingkan metanol. ik didih yang lebih lebih lama pada kolom
l, sehingga waktu
dibandingkan metanol. at dilihat dari waktu Meskipun etil asetat ng rendah tapi waktu etil asetat ini bersifat tahan lebih lama pada
uhu detektor GC diatur sebesar 300ºC. Suhu tor dimaksudkan agar terdapat dalam sampel awa oleh fase gerak ke ektor juga dibuat tinggi ma, yaitu agar semua
senyawa dalam sampel teta dan terdeteksi oleh detekt Pemanasan oven GC temperatur terprogram deng yang ditahan selama 10 me dinaikkan 30˚C permen mencapai 250˚C dan ditah awal harus lebih rendah senyawa yang memiliki rendah, dengan tujuan terkondensasi lagi setelah Suhu akhir diatur pada s tujuan untuk memastikan
yang terkandung dalam
teruapkan.
Pada puncak metanol d terlihat bahwa kedua pun ideal. Kedua puncak terse sangat tajam, sedangkan landai. Kondisi puncak s
dengan istilah tailing. T
karena salah satu sisi pada analat lebih kuat dibandi (Harvey 2000). Hal ini da struktur polidimetilsiloksa pada polidimetilsiloksana sedangkan sisi metil Perbedaan kepolaran ters perbedaan interaksi denga dan isoamil alkohol yang tertahan lebih kuat pa dibandingkan pada sisi m
menyebabkan tailing pad
dan isoamil alkohol.
Kuantifikasi pengotor sam Pengukuran konsentra sampel dilakukan deng standar eksternal. Hasil pengotor sampel disajikan sedangkan data analisis Lampiran 7. Berdasarka terlihat bahwa pengotor sebagian besar berupa
sebesar 26.53% dari
sedangkanuntuk sampel 2 berupa isoamil alkohol, yai dari total pengotor. Selain bahwa sampel 2 memilik yang lebih besar dari s pengotor pada sampel 1 se dan memiliki kemurnian sedangkan sampel 2 men sebesar 1488.96 ppm dan 99.85%. Konsentrasi meta sebesar 249.40 ppm, sedan 2 sebesar 178.26 ppm. ur polidimetilsiloksana
etap dalam bentuk gas ektor (Harvey 2000). dilakukan dengan engan suhu awal 40˚C menit, kemudian suhu enit sampai suhu ahan 19 menit. Suhu ah dari titik didih i titik didih paling senyawa tersebut ah mencapai kolom. suhu tinggi dengan an semua senyawa
lam sampel dapat
l dan isoamil alkohol uncak tersebut tidak rsebut pada sisi kiri an pada sisi kanan seperti ini dikenal Tailing disebabkan a fase diam menahan dingkan sisi lainnya dapat dijelaskan dari ksana. Sisi oksigen na bersifat polar, bersifat nonpolar. rsebut menyebabkan gan analat. Metanol g bersifat polar akan pada sisi oksigen metil. Hal tersebut ada puncak metanol
ampel bioetanol trasi pengotor pada
ngan menggunakan analisis terhadap an pada Gambar 5, s dapat dilihat pada rkan hasil tersebut or pada sampel 1 a isobutanol, yaitu
i total pengotor,
Konsentrasi pengotor organik produk bioetanol dari unit produksi bioetanol yang sama sebelumnya pernah dilaporkan oleh
Nuryatini et al. (2011). Analisis dilakukan
dengan kolom innowax 30 m berdasarkan
metode kalibrasi satu titik dan tidak dilakukan identifikasi jenis pengotornya. Hasil dari analisis tersebut menunjukkan bahwa sampel
mengandung lima pengotor dengan
konsentrasi total sebesar 0.06%. Berdasarkan hasil tersebut terlihat bahwa konsentrasi pengotor organik yang didapatkan dari hasil penelitian ini lebih kecil dari hasil analisis sebelumnya. Hasil yang didapatkan juga lebih akurat karena penentuannya dilakukan dengan menggunakan standar dari masing-masing pengotor. Jenis pengotor yang teridentifikasi
juga lebih banyak dibandingkan hasil
sebelumnya. Hal ini menunjukkan bahwa limit deteksi dengan menggunakan kolom polidimetilsiloksana 100 m lebih kecil dibandingkan dengan menggunakan kolom innowax 30m. Limit deteksi yang lebih kecil ini berkaitan dengan kemampuan kolom polidimetilsiloksana 100 m untuk menampung sampel dalam jumlah yang lebih banyak.
Berdasarkan hasil analisis tersebut,baik sampel 1 maupun sampel 2 masih memenuhi syarat SNI 7390:2008. Kemurnian dari kedua
sampel yang diujikan di atas 99.5% dengan kadar metanol kurang dari 300 ppm. Hasil ini menunjukkan bahwa kedua sampel bioetanol masih layak digunakan sebagai bahan baku untuk membuat standar etanol dalam bahan bakar.
SIMPULAN DAN SARAN
Simpulan
Konsentrasi pengotor organik pada sampel
bioetanol dapat ditentukan dengan
menggunakan kromatografi gas. Metode analisis tersebut telah diverifikasi untuk
menjamin bahwa hasil analisis yang
didapatkan valid dan menghasilkan ketelitian 1.2287%, ketepatan 99.2927%, linearitas 0.998, dan limit deteksi 0.02%. Sampel 1 memiliki kemurnian sebesar 99.86% dan konsentrasi metanol sebesar 294.40 ppm, sedangkan sampel 2 memiliki kemurnian 99.85% dan konsentrasi metanol sebesar 178.26 ppm. Persyaratan bioetanol yang digunakan sebagai gasohol di Indonesia tercantum dalam SNI 7390:2008, yaitu harus memiliki konsentrasi etanol minimum sebesar 99.5% dan memiliki konsentrasi metanol maksimum sebesar 300 ppm. Hasil tersebut menunjukkan bahwa kedua sampel masih memenuhi syarat SNI 7390:2008 untuk digunakan sebagai bahan baku standar etanol dalam bahan bakar.
Saran
Perlu dilakukan pengujian lanjut berupa penentuan konsentrasi pengotor anorganik dan konsentrasi air pada kedua sampel untuk
mengetahui kemurnian sebenarnya dari
sampel tersebut sebelum digunakan sebagai bahan baku untuk membuat standar etanol dalam bahan bakar.
DAFTAR PUSTAKA
[AOAC] Association of Analytical
Communities. 1998. Peer-Verified
Methods Program, Manual on policies and procedures. Arlington: AOAC.
[BPMIGAS] Badan Pelaksana Kegiatan Usaha Hulu Minyak dan Gas Bumi. 2011. Dari minyak, terbitlah gas. Buletin BPMIGAS 73: 2-5.
[BPS] Badan Pusat Statistik. 2010.
Perkembangan Jumlah Kendaraan
Bermotor Menurut Jenis tahun 1987-2009[internet]. [diacu 20 Februari 2012]. 0 1 2 3 4 5 6 k a d a r p en g o to r o rg a n ik ( × 1 0 2p p m )
jenis pengotor organik sampel 1
sampel 2
Tersedia dari http://www.bps.go.id/tab_ sub/view.php?tabel=1&daftar=1&id_suby ek=17¬ab=12
[BPS] Badan Pusat Statistik. 2011. Produksi Minyak Bumi dan Gas Alam, 1996-2010 [internet]. [diacu 20 Februari 2012]. Tersedia dari: http://www.bps.go.id/tab_ sub/view.php?kat=3&tabel=1&daftar=1&i d_subyek=10¬ab=1.
[CRC] Chemical Rubber Company. 1981. Handbook of Chemistry and Physics. Florida: CRC Press.
[EREC] European Renewable Energy
Council. 2007. Bioethanol Production and
Use. Brusel: European Biomass Industry
Association.
Balat M, Balat H. 2009. Recent trends in global production and utilization of
bio-ethanol fuel. Applied Energy 86: 2273–
2282.
Chan CC, Lam H, Lee YC, Zhang XM. 2004. Analytical Method Validation and Instrument Performance Verification. New York: J Willey.
Eiceman GA. 2004. Encyclopedia Anal Chem.
New York: J Willey.
Fessenden RJ, Fessenden JS. Kimia Organik
Jilid 1. Pudjaatmaka AH, penerjemah;
Jakarta: Erlangga. Terjemahan dari:
Organic Chemistry.
Harvey D. 2000. Modern Analytical
Chemistry. New York : Mc Graw Hill.
Nuryatini, Aristiawan Y, Sujarwo, Styarini D. Verifikasi analisis kemurnian bioetanol untuk pembuatan bahan acuan. Di dalam: Prosiding PPI Standardisasi 2011; Jakarta 16 November 2011.
Prihandana P, Hendroko R. 2007. Energi
Hijau Pilihan Bijak Menuju Mandiri Energi. Jakarta: Penebar Swadaya.
Reichardt C. 2003. Solvents and Solvent
Effects in Organic Chemistry. New York: Willey.
Taverniers I, Loose MD, Bockstaele EV. 2004. Trends in quality in the analytical
laboratory. II. Analytical method
validation and quality assurance. Trends
Anal Chem 23: 535-552.
Ulmer JD, Huhnke RL, Bellmer DD, Dwayne D, Cartmell. 2004. Acceptance of
ethanol-blended gasoline in Oklahoma. Biomass
and Bioenergy 27: 437–444.
Wong Siu-kay, Law Tin-yau, Wong Yee-lok. 2011. Purity assessment for 17 -estradiol. Accred Qual Assur 16:245-252. doi: 10.1007/s00769-011-0762-5.
Yuksel F, Yuksel B. 2004. The use of ethanol–gasoline blend as a fuel in an SI
engine. Renewable Energy 29: 1181–
1191.
Yunoki S, Saito M. 2009. A simple method to determine bioethanol content in gasoline using two-step extraction and liquid
scintillation counting. Bioresource
Lampiran 1 Diagram alir penelitian
12
Kondisi optimum
Optimasi pengukuran berupa optimasi
split ratio
(1:50, 1:75, 1:100, 1:200, dan 1:300)
Preparasi standar NIST
etanol dalam bahan bakar
Verifikasi metode analisis
meliputi pengujian
linearitas, ketelitian,
ketepatan, dan limit
deteksi
Pengukuran konsentrasi
pengotor organik sampel
Preparasi standar
campuran
Lampiran 2 Nilai SBR masing-masing
split ratio
split ratio
SBR (%)
1:50
1:75
1: 100
1: 125
1:150
1:175
1:200
4.7675
4.2500
3.1990
3.8996
2.0783
4.3104
1.9221
Lampiran 3 Pengujian linearitas
Konsentrasi
(%)
Luas puncak
Split ratio
1:100
Split ratio
1:200
0.5
1812.7
920.5
1
3862.5
1763.5
2
10336.5
4434
4
28762.33
11996
6
46475.5
24010.5
8
64584
27681.7
10
82293
37562
R² = 0.998
R² = 0.988
Lampiran 4 Pengujian ketepatan
Pengukuran luas puncak deret standar etanol dalam bahan bakar
konsentrasi
luas puncak
1
4536
2
13251
5
38180
8
65887
10
82703
Kurva standar etanol dalam bahan bakar
y = 8713,x - 4400R² = 0.999
0 1 2 3 4 5 6 7 8 9
0 2 4 6 8 10 12
lu
a
s
a
re
a
(×
1
0
4
)
Hasil analisis konsentrasi etanol berdasarkan pengukuran
Ulangan
Luas puncak
Konsentrasi etanol
(%)
1
26281
3.5219
2
26606
3.5586
3
26701
3.5695
Rerata
3.5498
Contoh perhitungan
•
Ulangan 1 : y = 8713 x - 4400
26281 = 8713 x – 4400
26281 + 4400 = 8713 x
x = 3.5219%
•
bobot SRM etanol dalam bahan bakar = 138.266 gram,
bobot larutan = 392.344 gram,
konsentrasi etanol berdasarkan penimbangan =
bobot SRMbobot etanol
×10
.08
%
=
138.266 gram392.344 gram
×10
.08
%
=
3.5523%
•
ketelitian = 1-
konsentrasikonsentrasi sebenarnya-konsentrasi percobaansebenarnya
×100%
= 1-
. . .×100%
= 99.1442%
Lampiran 5 Jumlah puncak pengotor berdasarkan volume injeksi
Volume injeksi (µl)
Jumlah puncak pengotor
Sampel 1
Sampel 2
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0.8
0.9
1.0
3
4
5
6
6
7
8
8
8
8
Lampiran 6 Waktu retensi standar senyawa pengotor
Lampiran 7 Konsentrasi pengotor dan kemurnian sampel
a.
Metanol
Konsentrasi
Luas puncak
15.07
2851
41.71
4139
93.18
4621
159.79
7429
317.18
11906
1001.72
32183
Kurva standar metanol
y = 29,66x + 2468, R² = 0.999
0 0,5 1 1,5 2 2,5 3 3,5
0 200 400 600 800 1000 1200
lu
a
s
a
re
a
(×
1
0
4
)
konsentrasi (ppm)
no
waktu retensi (menit)
senyawa
1
2
3
4
5
6
7
8
9
10
12.0
13.9
14.5
14.9
17.5
20.1
20.8
22.2
24.0
28.1
Konsentrasi metanol pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
11896
317.87
316.09
2
11944
319.49
3
11690
310.92
2
1
9037
221.48
225.93
2
9169
225.93
3
9301
230.38
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 29.66x + 2468
11896 = 29.66x + 2468
x =
(11896 – 2468)
29.66
= 317.87 ppm
Rerata konsentrasi metanol sampel 1 =
317.8
7
+319.4
9
+310.92
3
= 316.09 ppm
b.
Aseton
Konsentrasi
Luas puncak
18.47
458
41.41
832
92.52
1223
158.64
2446
315.42
4872
994.49
15467
Kurva standar aseton
y = 15,48x + 33,04R² = 0.999
0 2 4 6 8 10 12 14 16 18
0 200 400 600 800 1000 1200
lu
a
s
p
u
n
ca
k
(×
1
0
4)
Konsentrasi aseton pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
1224
76.94
77.28
2
1204
75.64
3
1260
79.26
2
1
1277
80.36
80.10
2
1242
78.10
3
1300
81.84
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 15.48x + 33.04
1224 = 15.48x + 33.04
x =
(1224 – 33.04)
15.48
= 76.94 ppm
Rerata konsentrasi aseton sampel 1 =
76.94 +
75.64
+
79.26
3
= 77.28 ppm
c.
2-propanol
Konsentrasi
Luas puncak
13.59
295
37.65
679
84.12
1409
144.24
2807
286.79
4916
904.24
16045
Kurva standar 2-propanol
y = 17,68x + 23,72 R² = 0.999
0 2 4 6 8 10 12 14 16 18
0 200 400 600 800 1000
lu
a
s
p
u
n
ca
k
(×
1
0
4)
Konsentrasi 2-propanol pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
942
51.94
54.31
2
1017
56.18
3
993
54.82
2
1
970
53.52
51.90
2
913
50.30
3
941
51.88
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 17.68x + 23.72
942 = 17.68x + 23.72
x =
(
942
–
23.72
)
17.68
= 51.94 ppm
Rerata konsentrasi 2-butanol sampel 1 =
51.9
4
+ 56.18 + 54.82
3
= 54.31 ppm
d.
1-propanol
Konsentrasi
Luas puncak
15.95
305
44.14
819
98.63
1916
169.13
4054
336.28
7203
1060.28
23941
Kurva standar 1-propanol
y = 22,66x - 142,2 R² = 0.999
0 5 10 15 20 25 30
0 200 400 600 800 1000 1200
lu
a
s
p
u
n
ca
k
(×
1
0
3)
Konsentrasi 1-propanol pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
4442
202.30
202.85
2
4402
200.54
3
4519
205.70
2
1
4235
193.17
193.27
2
4233
193.08
3
4244
193.57
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 22.66x – 142.2
4442 = 22.66x – 142.2
x =
(
4442 +142.2
)
22.66
= 202.30 ppm
Rerata konsentrasi 1-propanol sampel 1 =
202.30 + 200.54 + 205.70
3
= 202.85 ppm
e.
Etil asetat
Konsentrasi
Luas puncak
18.47
428
51.13
744
114.24
1212
195.89
2428
389.49
5049
1228.04
15710
Kurva standar etil asetat
y = 12,77x + 8,704 R² = 0.999
0 2 4 6 8 10 12 14 16 18
0 200 400 600 800 1000 1200 1400
lu
a
s
a
re
a
(×
1
0
3)
Konsentrasi etil asetat pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
2949
230.25
231.66
2
2931
228.84
3
3021
235.89
2
1
2830
220.93
221.24
2
2836
221.40
3
2836
221.40
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 12.77x + 8.704
2949 = 12.77x + 8.704
x =
(
2949-8.704
)
12.77
= 230.25 ppm
Rerata konsentrasi etil asetat sampel 1 =
230.25 + 228.84 + 235.8
9
3
= 231.66 ppm
f.
Isobutanol
Konsentrasi
Luas puncak
15.97
291
44.23
794
98.82
2041
169.46
4331
336.94
7987
1062.35
26414
Kurva standar isobutanol
y = 25,05x - 238,1R² = 0.999
0 5 10 15 20 25 30
0 200 400 600 800 1000 1200
lu
a
s
p
u
n
ca
k
(×
1
0
3)
Konsentrasi isobutanol pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
11296
460.44
459.59
2
11302
460.68
3
11226
457.65
2
1
10779
439.80
439.72
2
10599
432.62
3
10953
446.75
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 25.05x - 238.1
11296 = 25.05x – 238.1
x =
(11296 + 238.1)
25.05
= 460.44 ppm
Rerata konsentrasi isobutanol sampel 1 =
460.44 + 460.68 + 457.65
3
= 459.59 ppm
g.
1-butanol
Konsentrasi
Luas puncak
16.1
357
44.57
807
99.59
2150
170.78
4354
339.56
7956
1070.62
26414
Kurva standar 1-butanol
y = 24,80x - 191,2 R² = 0.999
0 5 10 15 20 25 30
0 200 400 600 800 1000 1200
lu
a
s
p
u
n
ca
k
(×
1
0
2)
Konsentrasi 1-butanol pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
426
24.89
24.97
2
437
25.33
3
421
24.69
2
1
326
20.85
20.56
2
314
20.37
3
316
20.45
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 24.80x – 191.2
426 = 24.80x – 191.2
x =
(426 + 1
91.2
)
24.80
= 24.89 ppm
Rerata konsentrasi 1-butanol sampel 1 =
24.89 +25.33 + 24.69
3
= 24.97 ppm
h.
Isoamil alkohol
Konsentrasi
Luas puncak
15.38
9944
42.56
10157
163.09
15051
324.26
18054
1022.24
36929
Kurva standar isoamil alkohol
y = 26,75x + 9640,R² = 0.996
0 5 10 15 20 25 30 35 40
0 200 400 600 800 1000 1200
lu
a
s
p
u
n
ca
k
(×
1
0
3)
Konsentrasi isoamil alkohol pada sampel
sampel
ulangan
Luas puncak
Konsentrasi
(ppm)
Rerata konsentrasi
(ppm)
1
1
19231
358.54
365.66
2
19328
362.17
3
19705
376.26
2
1
26915
645.79
654.42
2
27121
653.50
3
27401
663.96
Contoh perhitungan
•
Contoh 1 ulangan 1: y = 26.75x + 9640
19231 = 26.75x + 9640
x =
(19231 - 9640)
26.75
= 358.54 ppm
Rerata konsentrasi isoamil alkohol sampel 1 =
358.54 + 362.17 + 376.263
= 365.66 ppm
i.
Pengotor organik sampel
senyawa
Konsentrasi pengotor
(mg/kg)
Konsentrasi pengotor
(mg/l)
Sampel 1
Sampel 2
Sampel 1
Sampel 2
Metanol
316.09
225.93
249.40
178.26
Aseton
77.28
80.10
60.97
63.20
2-propanol
54.31
51.90
42.85
40.95
1-propanol
202.85
193.27
160.05
152.49
Etil asetat
231.66
221.24
182.78
174.56
Isobutanol
459.59
439.72
362.62
346.94
1-butanol
24.97
20.56
19.70
16.22
Isoamil alkohol
365.66
654.42
288.50
516.34
Konsentrasi pengotor total
1366.87
1488.96
Kemurnian bioetanol
99.86%
99.85%
•
Konversi konsentrasi pengotor
Konsentrasi metanol sampel 1 = konsentrasi metanol (mg/kg) × etanol
= 316.09 mg/kg × 0.789 kg/l
= 249.40 mg/l
•
Persentase konsentrasi isobutanol sampel 1 terhadap pengotor total
=
362.621366.87
×100%
•
Persentase konsentrasi isoamil alkohol sampel 2 terhadap pengotor total
=
516.341488.96
×100%
= 34.68 %
•
Kemurnian
Sampel 1 = 100% - jumlah pengotor organik (dalam %)
= 100% - (1366.87 ÷ 10 000)
= 99.86%
Sampel 2 = 100% - jumlah pengotor organik (dalam %)
= 100% - (1488.96 ÷ 10 000)