ISOLASI BAKTERI DARI TANAH TEMPAT PEMBUANGAN
SAMPAH UNTUK PEMBUATAN PUPUK ORGANIK CAIR
SKRIPSI
NOVITYA MAULITA SINAGA
080802037DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI BAKTERI DARI TANAH TEMPAT PEMBUANGAN
SAMPAH UNTUK PEMBUATAN PUPUK ORGANIK CAIR
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana Sains
NOVITYA MAULITA SINAGA
080802037DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
JUDUL : ISOLASI BAKTERI DARI TANAH TEMPAT
PEMBUANGAN SAMPAH UNTUK PEMBUATAN PUPUK ORGANIK CAIR
KATEGORI : SKRIPSI
NAMA : NOVITYA MAULITA SINAGA
NIM : 080802037
PROGRAM STUDI : SARJANA (S1) KIMIA
DEPARTEMEN : KIMIA
FAKULTAS : MATEMATIKA DAN ILMU PENGETAHUAN ALAM
(FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Juli 2012
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dr. Hamonangan Nainggolan, M.Sc Drs. Firman Sebayang, Ms
NIP. 195606241983031002 NIP.195607261985031001
Diketahui/Disetujui Oleh :
Departemen Kimia FMIPA USU
Ketua,
PERNYATAAN
ISOLASI BAKTERI DARI TANAH TEMPAT PEMBUANGAN SAMPAH UNTUK PEMBUATAN PUPUK ORGANIK CAIR
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2012
NOVITYA MAULITA SINAGA
PENGHARGAAN
Bismillahirrahmanirrahim,
Puji Syukur yang tak terhingga penulis ucapkan dengan segala kerendahan hati dan diri kepada Allah SWT, sehingga penulis dapat menyelesaikan skripsi yang berjudul “Isolasi Bakteri Dari Tanah Tempat Pembuangan Sampah Untuk Pembuatan Pupuk Organik Cair” yang disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains (S.Si) Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan.
Kepada Dosen Pembimbing I; Bapak Drs. Firman Sebayang M.S, dan Dosen Pembimbing II; Bapak Dr. Hamonangan Nainggolan, M.Sc yang telah membimbing penulis dengan kesabaran tinggi mulai tahap awal orientasi penelitian sampai tahap akhir selesainya penulisan skripsi ini, kepada Ibu Dr. Rumondang Bulan, M.S selaku ketua Departemen Kimia yang telah mensyahkan skripsi ini..
Penulis menyadari tanpa bantuan dan dukungan berbagai pihak skripsi ini tidak akan terselesaikan. Oleh sebab itu, pada kesempatan ini penulis mengucapkan terima kasih yang sebesar-besarnya kepada kedua orang tua yang selalu sabar membimbing penulis, kepada ayah yang luar biasa Aminuddin Sinaga, mamak yang terhebat Farida Nasution, abang Mansyurddin Sinaga dan adik tersayang M. Khoirul Affan Sinaga. Kepada sahabat-sahabat ku yang terhebat, Arau, Dewi, Elisa, Icha, May, Tiwi, Vany, Wimpy, dan Yayak, terimakasih atas persahabatan manis yang telah terjalin selama ini, atas motivasi dan bantuan moril maupun materil serta cinta yang tak pernah putus dari sahabat-sahabat sekalian. Terimakasih juga saya persembahkan untuk teman-teman dan sepupu yang selalu membantu dan mendukung saya Andre, Arif, Enka, Feri, Christou, Ivo, Okta, Paulus, Rizal, Samuel, bang Aulia, Yunus dan Jaya. Tak lupa teruntuk bang Asril, bang Mirza, kak Nila dan asisten Lab Mikrobiologi, serta laboran laboratorium Biokimia yang selalu sabar membimbing saya. Kepada seluruh pengurus HmI Kom’s Fmipa yang tak bisa saya sebutkan satu persatu namanya, saya juga mengucapkan terimakasih yang sebesar-besarnya atas bantuan teman-teman seperjuangan sekalian. Kepada adik-adik stambuk 2010 dan 2011, Dani, Maimunah, Eli dan Alex, terimakasih atas perhatian dan bantuan adik-adik sekalian.
Penulis juga menyadari dengan kemampuan dan pemahaman terhadap pengetahuan dan pengalaman yang dimiliki bahwa penulisan skripsi ini masih jauh dari kesempurnaan. Harapan kritik dan saran yang bersifat konstruktif sangat penulis harapkan demi kesempurnaan skripsi ini.
ABSTRAK
ISOLATION BACTERIA FROM SOIL OF LOCATED BANISHMENT TRASH FOR MANUFACTURE LIQUID ORGANIC FERTILIZER
ABSTRACT
DAFTAR ISI
1.6. Metodologi Penelitian 5
1.7. Lokasi Penelitian 5
Bab II Tinjauan Pustaka
2.1. Tanah 6
Bab III Metodologi Percobaan
3.1. Alat 20
3.2. Bahan 21
3.3. Prosedur Penelitian 22
3.3.1. Penyedian Sampel Sampah Sayur Pasar 22
3.3.2. Penyedian Sampel Tanah TPA 22
3.3.3.1. Pembuatan Media
3.3.3.1.1. Pembuatan Media Nutrient Agar 22 3.3.3.1.2. Pembuatan Media Skim Milk Agar (SMA) 23 3.3.3.1.3. Pembuatan Media Starch Agar (SA) 23
3.3.3.1.4. Pembuatan Media Margarine 23
.3.3.3.2. Isolasi Bakteri
3.3.3.2.1. Pembuatan Larutan Tanah 10-4 24 3.3.3.2.2. Penanaman Mikroorganisme pada Media 24
3.3.3.2.3. Pembiakan Bakteri 24
3.3.3.2.4. Pembuatan Larutan Standart Mac Varlan 24
3.3.3.2.5.Pembuatan Mac Varlan Bakteri 25
3.3.3.3. Perlakuan Uji Pewarnaan Gram Bakteri 25 3.3.3.4. Perlakuan Uji Potensial Bakteri
3.3.3.4.1. Uji Potensial terhadap Karbohidrat 25 3.3.3.4.2. Uji Potensial terhadap Protein 25
3.3.3.4.3. Uji Potensial terhadap Lemak 26
3.3.3.5. Pembuatan Larutan Bakteri Standart Mac Varlan
sebagai Starter Pembuatan Pupuk Organik 26
3.3.4. Pembuatan Pupuk Organik Cair 26
3.3.5. Pembuatan Pereaksi dan Larutan Standart
3.3.5.1. Pembuatan Pereaksi untuk Penentuan C-Organik
a. Larutan K2Cr2O7 1 N 27
b. Larutan FeSO4 1 N 27
c. Larutan Difenilamin [(C6H5)2NH4] 27 3.3.5.2. Pembuatan Pereaksi untuk Penentuan Nitrogen Metode Kjeldhal
a. Larutan NaOH 40% 27
b. Larutan Indikator Phenolphtalein 28
c. Larutan H3BO3 4% 28
3.3.5.3. Pembuatan Pereaksi dan Larutan Standart untuk Penentuan Posfor sebagai P2O5 Metode Spektrofotometer
a. Larutan HCl 25 % 29
b. Larutan Standart Posfor 100 ppm 29
c. Larutan Amonium Molibdat 4% 30
d. Larutan Asam Askorbat 0,1 M 30
e. Larutan Kalium Antimonil Tartarat 1 mg Sb/mL 30 f. Larutan Seri Standart P dalam ekstrak HCl 0,95 N 30
g. Larutan H2SO4 5 N 30
h. Pembuatan Larutan Campuran Pengkompleks 31 3.3.5.4. Pembuatan Pereaksi Untuk Penentuan Kalium
a. Larutan HCl 25% 31
b. Larutan Kalium 100 ppm 31
c. Larutan Standart Kalium 100 ppm 31
d. Larutan Seri Standart Kalium untuk
Kalibrasi (0,0-5-10-15-20ppm) 32
3.3.6. Penentuan Kadar C-Organik dengan Metode Walkey Black 32 3.3.7. Penentuan Nitrogen dengan metode Kjeldhal 32 3.3.8. Penentuan P-Total Metode Spektrofotometri
3.3.8.1. Preparasi Sampel 32
3.3.8.2. Pembuatan Kurva Kalibrasi 33
3.3.9. Penentuan Kalium Sebagai K2O dengan Metode
Spektrofotometer Serapan Atom SSA 33
3.4. Bagan Penelitian
3.4.1. Skema Pembuatan Starter 3.4.1.1. Skema Pembuatan Media
3.4.1.1.1. Skema pembuatan Media Nutrien Agar 34 3.4.1.1.2. Skema Pembuatan Media Skim Milk Agar 35 3.4.1.1.3. Skema Pembuatan Media Strach Agar 36
3.4.1.1.4. Skema Pembuatan Media Margarin 37
3.4.1.2. Skema Isolasi Bakteri
3.4.1.2.1. Skema Pengenceran Bertingkat 38
3.4.1.2.2. Skema Penanaman Mikroorganisme pada Media 38
3.4.1.2.3. Skema Pembiakan Bakteri 39
3.4.1.3. Skema Uji Pewarnaan Gram Bakteri 40
3.4.1.4. Skema Uji Potensial Bakteri
3.4.1.4.1. Uji Potensial terhadap Karbohidrat 41
3.4.1.4.2. Uji potensial terhadap Protein 41
3.4.1.4.3. Uji Potensial terhadap Lemak 42
3.4.1.5. Skema Pembuatan Larutan Bakteri sp3 Standart
Mac Varlan sebagai Starter Pembuatan Pupuk Organik 42
3.4.2. Skema pembuatan Pupuk Organik Cair 43
3.4.3. Skema Penentuan kadar C-Organik, N, P dan K
3.4.3.1. Skema Penentuan Kadar C-Organik 44
3.4.3.2. Skema Penentuan Kadar Nitrogen Pupuk Organik Cair 45 3.4.3.3. Skema Penentuan Posfor sebagai P2O5 Metode Spektrofometri
3.4.3.3.1. Pembuatan Ekstrak 46
3.4.3.3.2. Pengukuran Absorbansi Larutan Standart P
untuk kurva Kalibrasi Larutan Standart 2 ppm 46 3.4.3.3.3. Skema pengukuran Absorbansi untuk ekstrak
Pupuk Organik Cair 47
3.4.3.4. Skema Penentuan Kalium sebagai K2O dengan
Metode Spektrofotometer Serapan Atom 47
Bab IV Hasil dan Pembahasan 4.1. Hasil
Karbohidrat, Protein, dan Lemak 48 4.1.2. Data Pembuatan Pupuk Organik Cair dengan Menggunakan
Bakteri yang di Isolasi dari Tanah Tempat Pembuangan
Sampah Akhir 49
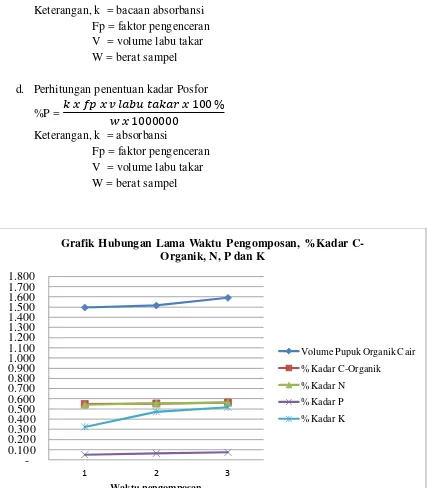
4.1.3. Data Hasil Analisa Kadar C-Organik, N, P dan K dari Pupuk Organik Cair yang Dihasilkan dari Limbah Sayur Pasar Pagi dengan Menggunakan
Bakteri yang Diisolasi dari Pembuangan Sampah Akhir 50 4.1.4. Data Hasil Pengujian Pupuk Organik terhadap tanaman sawi 50 4.2. Pembahasan
4.2.1. Uji Potensial Bakteri dalam mendegradasi Karbohidrat,
Protein dan Lemak 51
4.2.2. Pembuatan Pupuk Organik Cair dari Limbah Sayur Pasar Pagi dengan Menggunakan Bakteri yang Di Isolasi dari Tanah Tempat
Pembuangan Sampah Akhir 51
4.2.3. Analisa Kadar C-Organik, N, P dan K dari Pupuk Organik Cair 52 4.2.4. Pengujian Pupuk Organik Cair terhadap Tanaman 53
Bab V Kesimpulan dan Saran
5.1. Kesimpulan 54
5.2 Saran 54
Daftar Pustaka
DAFTAR TABEL
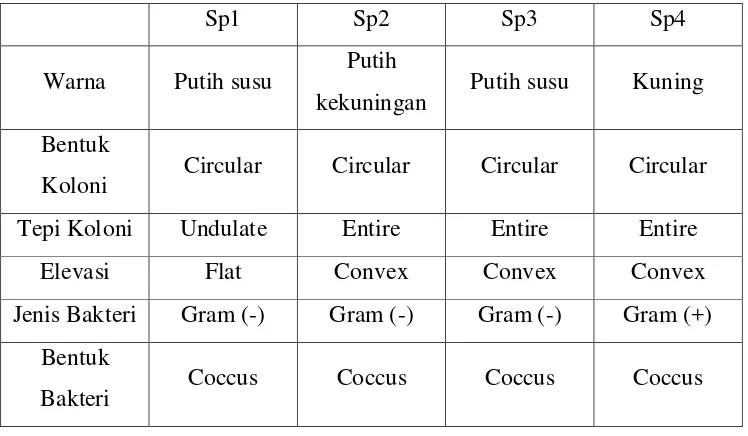
Tabel 4.1. Jenis dan Karakteristik Bakteri Hasil Isolasi dari Tanah
Tempat Pembuangan Sampah Akhir 48
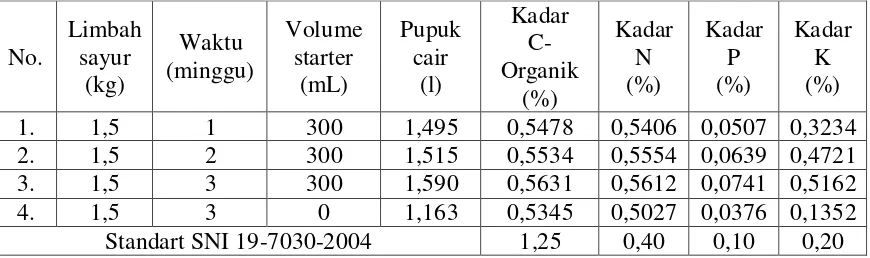
Tabel 4.2. Pengujian Kadar C-Organik, Nitrogen, Posfor, dan Kalium
dari Pupuk Organik Cair 49
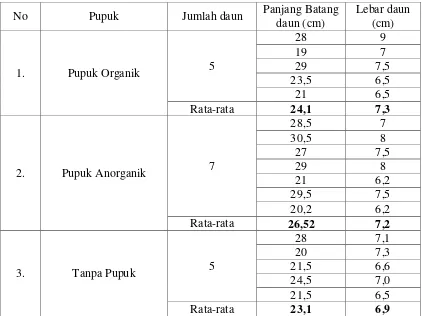
Tabel 4.3. Data Hasil Pengujian Pupuk Organik Cair terhadap
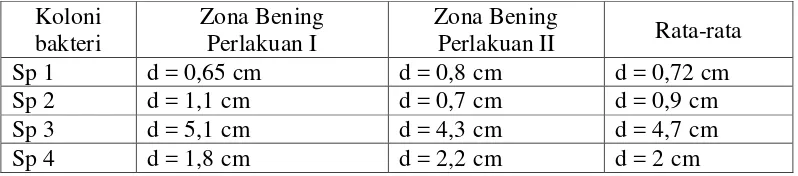
Tanaman Sawi Meliputi Panjang Batang Daun dan Lebar Daun 49 Tabel 1 Data Hasil Uji Potensial Bakteri dalam mendegradasi
Karbohidrat, Protein dan Lemak
DAFTAR GAMBAR
Gambar 1. Tempat Pembuangan Sampah Akhir Tuntungan 59
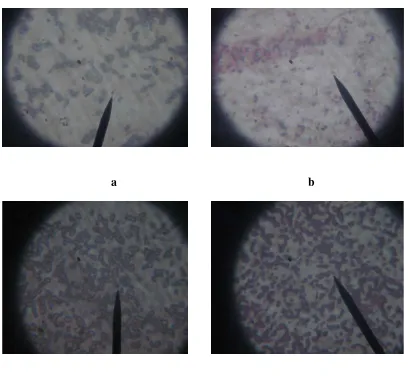
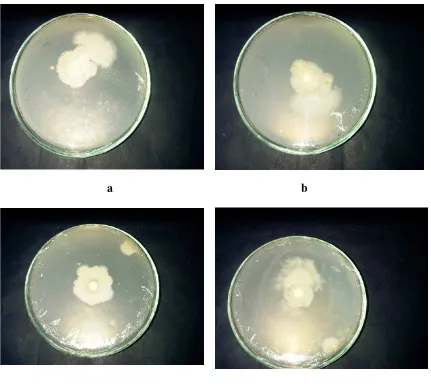
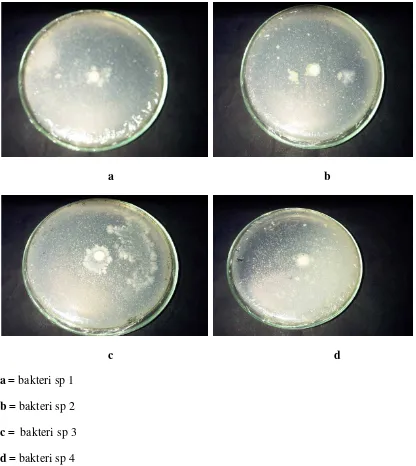
Gambar 2. Bakteri hasil isolasi dari Tanah 60
Gambar 3. Tampakan Mikroskop Hasil Uji Pewarnaan Gram Bakteri 61 Gambar 4. Uji Potensial Bakteri
Gambar 4.1. Uji Potensial Bakteri terhadap Karbohidrat 62
Gambar 4.2. Uji Potensial terhadap Protein 63
Gambar 4.3. Uji Potensial terhadap Lemak 64
Gambar 5. Limbah Sayur Pasar Pagi 65
Gambar 6. Pupuk Organik Cair 65
Gambar 7. Uji Coba Pupuk Organik Cair Pada Tanaman Sawi
Gambar 7.1. Tanaman Sawi dengan Penambahan Pupuk Organik Cair 66 Gambar 7.2. Tanaman Sawi dengan Penambahan Pupuk Anorganik 66
ABSTRAK
ISOLATION BACTERIA FROM SOIL OF LOCATED BANISHMENT TRASH FOR MANUFACTURE LIQUID ORGANIC FERTILIZER
ABSTRACT
BAB I
PENDAHULUAN
1.1. Latar Belakang
Sampah atau waste (Inggris) memiliki banyak pengertian dalam batasan ilmu
pengetahuan. Namun pada prinsipnya, sampah adalah suatu bahan yang terbuang atau
dibuang dari sumber aktifitas manusia maupun alam yang belum memiliki nilai
ekonomis. Bentuk sampah bisa berada dalam setiap fase materi, yaitu padat, cair, dan gas.
Secara sederhana, jenis sampah dapat dibagi berdasarkan sifatnya. Sampah dipilah
menjadi sampah organik dan anorganik. Sampah organik atau sampah basah ialah sampah
yang berasal dari makhluk hidup, seperti dedaunan dan sampah dapur. Sampah jenis ini
sangat mudah terurai secara alami (degradable). Sementara itu, sampah anorganik atau
sampah kering adalah sampah yang tidak dapat terurai (undegradable).
Sumber sampah terbanyak berasal dari pasar tradisional dan pemukiman. Sampah
pasar tradisional, seperti pasar lauk-pauk dan sayur-mayur membuang hampir 95%
sampah organik. Jika ditinjau dari pengolahannya, sampah jenis ini akan lebih mudah
ditangani.
Kompos dan pupuk organik merupakan salah satu produk daur ulang hasil
pengolahan sampah yang dapat dibanggakan dan mudah diaplikasikan. Sampah organik
yang menggunung merupakan bahan baku kompos yang potensial. Di masa mendatang,
penggunaan kompos sebagai sumber nutrisi tanaman akan sangat berarti dan memliki
prospek bisnis yang cerah. Penggunaan kompos tidak hanya sebagai penyedia unsur hara,
produk organik, terutama kompos, mampu menjaga keseimbangan alam(Tim Penulis
PS,2008).
Zat organik dalam sampah terdiri dari bahan-bahan nitrogen, karbohidrat, lemak
dan sabun. Mereka bersifat tidak tetap dan menjadi busuk, mengeluarkan bau-bauan yang
tidak sedap. Sifat-sifat khas sampah inilah yang membuat perlunya pembenahan sampah
dan menyebabkan kesulitan-kesulitan yang sangat besar dalam pembuangannya
(Mahida,1993).
Sampah organik biasanya berasal dari limbah dapur rumah tangga, limbah
restoran, hotel dan sebagainya. Sampah dari bahan organik ini banyak mengandung air
dan serat, dan senyawa organik komplek lainnya. Bahan organik yang berasal dari
tumbuhan maupun hewan merupakan bahan baku yang bagus untuk pupuk organik. Di
samping karena murah dan tidak merusak lingkungan, proses pembuatannya pun mudah.
Hal yang perlu diingat dalam memilih sampah organik untuk diolah menjadi
pupuk yaitu kandungan bahan organik nya. Ada sebagian bahan organik yang bergetah
dan tidak baik untuk bahan baku pupuk organik seperti daun damar, pinus, daun bamboo,
serta daun tembakau.
Berbeda dengan pupuk anorganik yang berasal dari bahan kimia sintesis, pupuk
organik terbuat dari bahan organik seperti sisa-sisa sayuran, kulit buah-buahan, atau
bahan-bahan yang berasal dari tumbuhan atau makhluk hidup lainnya.
Selain dapat menyediakan unsur hara yang dibutuhkan oleh tumbuhan,
penggunaan pupuk organik cair bisa memperbaiki struktur tanah, dan bisa menekan
bakteri yang merugikan dalam tanah. Pupuk organik memiliki beberapa kelebihan
dibandingkan dengan pupuk anorganik. Penggunaan pupuk organik secara terus menerus
terhadap tanah akan memperbaiki kualitas tanah tersebut, baik secara fisik, biologi
meninggalkan residu dalam tanaman sehingga hasil tanaman aman apabila dikonsumsi
manusia(Hidayat,2006).
Pengembalian bahan organik kedalam tanah adalah hal yang mutlak dilakukan
untuk mempertahankan lahan pertanian agar tetap produktif. Dua alasan yang selama ini
sering dikemukakan para ahli adalah: (1) pengolahan tanah yang dangkal selama
bertahun-tahun mengakibatkan menurunnya kandungan C dan N-organik, (2) penggunaan
pupuk kimia seperti urea , KCl, dan TSP telah melampaui batas efisiensi teknis dan
ekonomis sehingga efisiensi dan pendapatan bersih yang diterima petani dari setiap unit
pupuk yang digunakan semakin menurun. Mengingat pentingnya fungsi dan peranan
bahan organik bagi tanah serta makin intensifnya penggunaan pupuk kimia oleh petani
maka sangatlah penting untuk mulai untuk memperhatikan usaha pengembalian bahan
organik ke tanah.
Saat ini fungsi pupuk organik di Indonesia masih sebagai pendamping pupuk
kimia karena adanya target produksi (ton/ha). Masih adanya pendapat bahwa tanaman
yang hanya dipupuk organik sering mengalami defisiensi unsur hara karena kandungan
unsur hara yang diberikan tidak sebanding dengan kebutuhan tanaman ditambah
pelepasan unsur haranya lambat. Padahal, efek pemupukan organik pada pertumbuhan
tanaman cukup menakjubkan. Dari hasil yang dilaporkan di Amerika, efek pemberian
pupuk organik sebanyak 14 ton tiap tahun pada satuan luas tanah selama delapan tahun
masih terasa empat puluh tahun sesudah pemberian pupuk yang terakhir.
Hal ini harus menjadi perhatian bahwa ternyata pupuk organik memegang peranan
penting dalam pembentukan zat hara dalam tanah. Untuk saat ini, penggunaan pupuk
organik sebagai pendamping pupuk kimia diharapkan sebagai tahap awal yang perlu
1.2.Permasalahan
Berdasarkan uraian diatas, yang menjadi permasalahan dalam penelitian ini adalah :
- Bagaimana cara mengisolasi bakteri dari tanah tempat pembuangan sampah akhir
- Apakah bakteri yang di isolasi dari tanah tempat pembuangan sampah dapat
membantu proses pembuatan pupuk organik cair dari limbah sayur pasar pagi
- Berapa kadar unsur C-Organik, Nitrogen, Posfor dan Kalium dari pupuk organik
cair yang dihasilkan dan apakah memenuhi Standart Nasional Indonesia
- Bagaimana pengaruh pupuk organik cair terhadap tanaman
1.3.Pembatasan Masalah
Berdasarkan uraian diatas, maka permasalahan dibatasi pada :
- Bakteri yang digunakan dalam penelitian diisolasi dari tanah yang diambil dari
Tempat pembuangan Sampah Akhir di daerah Tuntungan
- Limbah sayur yang digunakan dalam pembuatan pupuk organik cair diambil dari
Pasar Sore Padang Bulan
- Parameter yang dianalisa adalah unsur C-Organik, Nitrogen, Posfor dan Kalium
- Tanaman yang digunakan untuk pengujian pupuk organik cair diuji coba pada
tanaman sawi hijau
1.4.Tujuan penelitian
Tujuan penelitian ini adalah :
- Untuk mengetahui cara mengisolasi bakteri dari tanah
- Untuk menghasilkan pupuk organik cair dari sampah organik yang diambil dari
Pasar Sore Padang Bulan dengan menggunakan bakteri yang diisolasi dari tanah
Tempat Pembuangan Sampah Akhir dengan variasi waktu yang berbeda dan tanpa
- Untuk mengetahui kandungan unsur C-organik, N, P dan K dari pupuk organik
cair dengan penambahan bakteri dan tanpa penambahan bakteri
- Untuk mengetahui pengaruh pupuk organik cair terhadap tanaman
1.5. Manfaat Penelitian
1. Untuk mengatasi masalah pencemaran lingkungan
2. Untuk menghasilkan pupuk organik cair dengan menggunakan bakteri yang diisolasi
dari tanah serta pemanfaatan limbah sayur dari pasar
3. Sebagai alternatif tambahan yang mudah bagi sektor pertanian
1.6. Metodologi Penelitian
1. Penelitian ini merupakan eksperimen laboratorium
2. Limbah sayur diambil dari Pasar Sore Padang Bulan
3. Bakteri disolasi dari tanah yang diambil dari Tempat Pembuangan Akhir di daerah
Tuntungan
4. Pembuatan pupuk organik cair dari limbah sayur yang difermentasikan dengan bakteri
5. Penentuan C-organik metode Walkey Black
6. Penentuan Nitrogen dilakukan dengan dengan metode Kjehldal
7. Penentuan Posfor sebagai P2O5 dengan Spektrofotometri
8. Penentuan Kalium sebagai K2O dengan Spektrofotometer Serapan Atom (AAS)
9. Pengujian pupuk organik cair terhadap tanaman sawi
1.7. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Mikrobiologi, Laboratorium Biokimia
BAB II
TINJAUAN PUSTAKA
2.1. Tanah
Tanah adalah salah satu benda alam yang terdapat di permukan kulit bumi, yang tersusun
dari bahan-bahan mineral sebagai hasil pelapukan batuan dan bahan-bahan organik,
pelapukan sisa-sisa tumbuhan dan hewan yang merupakan medium atau tempat
tumbuhnya tanaman dengan sifat-sifat tersebut yang terjadi akibat dari pengaruh
kombinasi faktor-faktor iklim, bahan induk, jasad hidup, bentuk wilayah dan lamanya
waktu pembentukan. Tanah mempunyai fungsi yang bermacam-macam. Tanah adalah
tempat tinggal dan hidup berbagai organisme baik manusia, hewan, tumbuhan maupun
mikroorganisme(Yulipriyanto,2010).
Bahan organik tanah adalah semua jenis senyawa organik yang terdapat di
dalam tanah. Termasuk serasah, fraksi bahan organik ringan, biomassa mikroorganisme,
bahan organik terlarut di dalam air, dan bahan organik stabil atau humus. Bahan organik
memiliki peran penting dalam menentukan kemampuan tanah untuk mendukung tanaman,
sehingga jika kadar bahan organik tanah ,menurun kemampuan tanah dalam mendukung
produktifitas tanaman juga menurun(Ansori,2005).
Tanah dihuni oleh bermacam-macam mikroorganisme, mikroorganisme tanah
seperti bakteri dan jamur sangat mempengaruhi kesuburan tanah, oleh karena itu
mikroorganisme merupakan salah satu aspek penting yang berperan dalam pembentukan
suatu ekosistem. Mikroorganisme tanah juga bertanggungjawab atas pelapukan bahan
organik dan pendauran unsur hara, dengan demikian mikroorganisme mempunyai
Di dalam tanah hidup berbagai jasad renik (mikroorganisme) yang melakukan
berbagai kegiatan yang menguntungkan bagi kehidupan makhluk-makhluk hidup
lainnnya atau dengan perkataan lain menjadikan tanah memungkinkan bagi kelanjutan
siklus kehidupan makhluk-makhluk alami(Sutedjo,1996).
Sebuah studi yang dilakukan Antaya dan Callahan (1997), menyebutkan bahwa
aktifitas bakteri berperan penting dalam kesuburan tanah, dimana aktifitasnya selalu
berubah. Kemampuan tanah untuk meningkatkan pertumbuhan tanaman didasarkan pada
keberadaan dan keseimbangan banyak elemen seperti Posfor, Kalsium, Sulfur, dan
Natrium. Bakteri bermanfaat untuk menghancurkan dan mendaur ulang elemen-elemen
ini(Antaya dan Callahn,1997).
Jumlah bakteri yang ada di dalam tanah dipengaruhi oleh berbagai kondisi yang
mempengaruhi pertumbuhannya, seperti temperatur, kelembapan, aerasi dan sumber
energi. Tetapi secara umum populasi yang terbesar terdapat di horison permukaan.
Mikroorganisme tanah lebih banyak ditemukan pada permukaan tanah karena bahan
organik lebih tersedia. Oleh karena itu mikroorganisme lebih banyak berada pada lapisan
tanah yang paling atas(Alexander,1977).
2.2. Bakteri
Bakteri adalah domain yang terdiri dari makhluk hidup yang tidak memiliki membran inti
(prokariota). Bakteri dulu terbagi menjadi Bacteria dan Archaebacteria, namun sekarang
Archaebakteria memiliki domain sendiri yang disebut Archaea. Bakteri memiliki ciri-ciri
antara lain tidak memiliki membran inti, tidak memiliki organel bermembran, memiliki
dinding sel peptidoglikan, dan materi asam nukleatnya berupa plasmid (Postlethwait dan
Hopson, 2006).
Bakteri adalah mikroorganisme bersel tunggal yang tidak terlihat oleh mata, tetapi
dengan bantuan mikroskop, mikroorganisme tersebut akan nampak. Ukuran bakteri
jenisnya. (µ = 1mikron = 0,001 mm). Walaupun terdapat beribu jenis bakteri, tetapi hanya
beberapa karakteristik bentuk sel yang diketemukan yaitu:
1) Bentuk bulat atau cocci (tunggal = coccus)
2) Bentuk batang atau bacilli (tunggal = bacillus)
3) Bentuk spiral atau spirilli (tunggal = spirillum)
4) Bentuk koma atau vibrios (tunggal = vibrio)
Sel-sel ini dapat dijumpai dalam keadaan tunggal, berpasangan, tetrad, kelompok kecil,
gerombolan atau rantai. (Buckle, 2009)
Berdasarkan suhu pertumbuhannya, mikroba dapat dibedakan menjadi tiga golongan :
1) Mikroba psikrofil, dapat tumbuh pada suhu antara 0oC sampai 30oC, dengan suhu
optimum 15oC. Kebanyakan tumbuh ditempat-tempat dingin, baik didaratan ataupun
dilautan.
2) Mikroba mesofil, mempunyai suhu optimum antara 25o- 37oC, dengan suhu minimum
15oC dan suhu maksimum antara 45-55oC. Jasad ini banyak tumbuh dalam saluran
pencernaan , tanah dan perairan.
3) Mikroba termofil, dengan suhu pertumbuhan antara 40o-75oC dengan suhu optimum
55o-60oC. Papertumbuhan antara 40o-75oC dengan suhu optimum 55o-60oC. Pada jasad
termofil dikenal pula stenotermofil( termofil obligat), yaitu mikroba yang dapat
tumbuh baik pada suhu 60oC dan tidak dapat tumbuh pada suhu 30oC dan
euritermofil(termofil fakultatif) yaitu yang mampu tumbuh dibawah 30oC(Nur
Hidayat, 2006).
Bakteri adalah mikroorganisme yang paling dominan di dalam tanah bila
dibandingkan dengan mikroorganisme lain seperti fungi dan protozoa, bakteri dapat hidup
pada seluruh lapisan tanah dan pada kondisi tanah yang berbeda(Widawati dkk,2005).
Pada mulanya bakteri dianggap sebagai golongan mikroorganisme yang sangat
penting dalam berbagai proses yang mempengaruhi fertilitas tanah. Anggapan ini
dihubungkan dengan peristiwa/kejadian dan berkembangbiaknya, sehingga
dihargai maka golongan-golongan mikroorganisme lainnya yang beragam itu harus
mendapatkan perhatian atau dihargai pula peranan pentingnya dalam proses-proses tanah.
Bakteri yang hidup dalam tanah memegang peranan penting dalam
meningkatkan pertumbuhan dan produksi tanaman, sehubungan dengan kemampuannya
dalam mengikat N2 dari udara dan mengubah amonium menjadi nitrat. Termasuk ke
dalam golongan ini yang berbentuk batang (bacil) yang mampu membentuk spora dan
yang tidak membentuk spora, spora pada bakteri bukan alat untuk berkembang biak
melainkan alat untuk mempertahankan diri dari lingkungan yang tidak menyenangkan.
Selain bakteri bacil, terdapat pula bakteri coccus, vibrios, dan spirilla. Bakteri Costvidium
pastorianum adalah bakteri yang dapat memfiksasi/mengikat Nitrogen dalam keadaan
anaerob. Bakteri Azotobakter chrococcum yaitu bakteri yang dapat mengikat Nitrogen
dalam keadaan aerob. Bakteri Nitrobakter yaitu bakteri yang dapat mengubah amonium
menjadi nitrat. Bakteri Radicicolas yaitu bakteri yang dapat bersimbiosa dengan
Leguminosa. Bakteri-bakteri sangat beragam dalam ukuran, bentuk dan
keperluan-keperluan oksigen (aerob dan anaerob), penggunaan energi (autotrof dan heterotrof),
hubungan pada tanaman dan binatang (saprofit dan parasit)(Mul Muyani Sutedjo,1996).
2.3. Isolasi Bakteri
Isolasi bakteri adalah proses mengambil bakteri dari medium atau lingkungan asalnya dan
menumbuhkannya di medium buatan sehingga diperoleh biakan yang murni. Bakteri
dipindahkan dari satu tempat ke tempat lainnya harus menggunakan prosedur aseptik.
Aseptik berarti bebas dari sepsis, yaitu kondisi terkontaminasi karena mikroorganisme
lain. Teknik aseptik ini sangat penting bila bekerja dengan bakteri. Beberapa alat yang
digunakan untuk menjalankan prosedur ini adalah bunsen dan laminar air flow Bila tidak
dijalankan dengan tepat, ada kemungkinan kontaminasi oleh miroorganisme lain sehingga
akan mengganggu hasil yang diharapkan. Teknik aseptik juga melindungi laboran dari
kontaminasi bakteri (Singleton dan Sainsbury, 2006).
Bakteri di alam umumnya tumbuh dalam populasi yang terdiri dari berbagai
diperlakukan dengan pengenceran agar didapat hanya 100-200 bakteri yang ditransfer ke
medium, sehingga dapat tumbuh menjadi koloni yang berasal dari bakteri tunggal. Ada
beberapa metode untuk menginokulasi bakteri sesuai dengan jenis medium tujuannya,
yaitu:
1. Metode gores atau streak plate menggunakan loop ose dan menggoreskannya ke
permukaan medium agar dengan pola tertentu dengan harapan pada ujung goresan,
hanya sel-sel bakteri tunggal yang terlepas dari ose dan menempel ke medium. Sel-sel
bakteri tunggal ini akan membentuk koloni tunggal yang kemudian dapat dipindahkan
ke medium selanjutnya agar didapatkan biakan murni.
2. Metode tuang atau pour plate dilakukan dengan 2 cara, yaitu dengan mencampur
suspensi bakteri dengan medium agar pada suhu 50ºC kemudian menuangkannya
pada petridisk atau dengan menyemprotkan suspensi pada dasar petridisk, kemudian
menuang medium agar keatasnya dan diaduk. Setelah agar mengeras, bakteri akan
berada pada tempatnya masing-masing dan diharapkan bakteri tidak mengelompok
sehingga terbentuk koloni tunggal.
3. Metode sebar atau spread plate dilakukan dengan menyemprotkan suspensi ke atas
medium agar kemudian menyebarkannya secara merata dengan trigalski. Dengan ini
diharapkan bakteri terpisah secara individual, kemudian dapat tumbuh menjadi koloni
tunggal.
4. Metode pemaparan pada udara terbuka adalah metode untuk mengisolasi bakteri
udara. Metode ini sangat simpel, yaitu dengan memaparkan medium pada udara
terbuka, dengan harapan ada bakteri yang menempel dan kemudian akan tumbuh
menjadi koloni (Harley dan Presscot, 2002).
2.3.1. Teknik pewarnan
Banyak senyawa organik berwarna (zat pewarna) digunakan untuk mewarnai
mikroorganisme untuk pemeriksaan mikroskopis. Salah satunya yaitu pewarnaan gram.
Pewarnaan gram masih merupakan salah satu prosedur yang paling banyak digunakan
LARUTAN DAN URUTAN
PENGGUNAANYA
REAKSI DAN TAMPANG BAKTERI
Gram positif Gram negative
1
terbentuk didalam sel ;
sel tetap berwarna ungu
Dinding sel mengalami
sel; sel tetap ungu
Sel tak terpengaruhi,
Uk-Y keluar dari sel; sel
menjadi tak berwarna
Sel menyerap zat pewarna
ini, menjadi merah
(Michael J. Pelczar, 2008)
2.4. Manfaat Pengelolaan Sampah
Sampah apapun jenis dan sifatnya mengandung senyawa kimia yang diperlukan oleh
manusia secara langsung atau secara tidak langsung. Dalam hal ini yang penting sampai
berapa jauh manusia dapat menggunakan dan memanfaatkannya. Penggunaan dan
pemanfaatan sampah untuk manusia sudah lama telah dilakukan, antara lain :
a. Manfaat Sampah
- Pengisi Tanah
Sudah bukan aneh lagi bila kota-kota besar sekarang tumbuh tempat-tempat
pemukiman baru, rumah toko (ruko), kmpleks pembelanjaan baru yang asalnya
dari rawa-rawa atau tempat tanah berair lainnya atau bahkan dari tempat-tempat
- Sumber Pupuk Organik
Kompos adalah sejenis pupuk organik yang sangat dibutuhkan khususnya oleh
petani sayuran. Kompos banyak dibuat dari sampah, walaupun akhir-akhir ini
kehadiran plastik merupakan masalah yang belum sepenuhnya teratasi.
- Sumber Humus
Kehadiran senyawa organik dalam bentuk humus di dalam tanah dapat
mempertahankan sifat fisik tanah. Dengan sifat fisik yang baik, maka
kemampuan tanah menyerap dan mempertahankan air dapat terjadi dengan baik.
- Media Penanaman Jamur
Sampah dapat juga digunakan sebagai media penanaman jamur. Penggunaan
media ini ternyata telah memberikan hasil yang memuaskan. Misalnya, media
jamur merang, jamur “shiitake”, jamur tiram putih tumbuh dengan baik pada
bahan organik pada kompos.
- Penyubur Plankton
Plankton adalah merupakan makanan utama ikan, yang biasanya terdiri dari
hewan dan tanaman bersel tunggal. Kolam ikan yang banyak planktonnya akan
sangat subur. Suburnya plankton ini dapat menyebabkan pertumbuhan yang cepat
pula pada ikan-ikan yang dipelihara, mislanya di kolam-kolam. Suburnya
plankton karena pemasukan bahan-bahan organik dari sampah.
- Bahan Pembuat Biogas
Salah satu manfaat sampah adalah membantu program hemat energi dan dalam
pencarian sumber energi baru. Mengingat bahwa sumber energi yang berbahan
baku bahan bakar fosil merupakan sumber daya alam yang terbatas. Oleh karena
itu, sampah dapat dijadikan alternatif untuk keperluan tersebut.
- Media Produksi PST (Protein Sel Tunggal)
PST adalah protein jenis baru yang dibuat secara tekhnologi dengan
menggunakan mikroorganisme (mikroalgae, jamur dan bakteri). Menurut
perhitungan para ahli, protein sel tunggal akan menjadi sumber protein
penyelamat di masa yang akan datang bila produksi protein secara konvensional
mikroorganisme penghasil PST sangat subur di dalam media yang terbuat
sampah.
- Media Produksi Vitamin
Salah satu jenis mikroorganisme penghasil vitamin (vitamin B12) ternyata sangat
subur pertumbuhannya di dalam media yang dicampur dengan ekstrak sampah.
Telah banyak lembaga penelitian mencoba meneliti lebih lanjut peranan sampah
sebagai bahan media pertumbuhan jasad renik penghasil vitamin.
- Bahan Makanan Ternak
Sampah sebagai bahan makanan ternak secara langsung (yang masih segar) dan
melalui proses fermentasi telah digunakan dimana-mana dengan hasil yang baik
(Lud Waluyo,2009).
2.5. Pupuk
Pupuk adalah material yang ditambahkan pada
mencukupi kebutuhan
dengan baik. Material pupuk dapat berupa baha
Pupuk berbeda dari
pertumbuhan dan perkembangan tanaman, sementara suplemen seperti
membantu kelancaran proses metabolisme. Meskipun demikian, ke dalam pupuk,
khususnya pupuk buatan, dapat ditambahkan sejumlah material
suplemen(id.wikipedia.org/wiki/Pupuk).
Pupuk dapat digolongkan menjadi dua, yakni pupuk organik dan pupuk anorganik.
Pupuk organik adalah pupuk yang terbuat dari sisa-sisa makhluk hidup yang diolah
melalui proses pembusukan (dekomposisi) oleh bakteri pengurai, misalnya pupuk kompos
dan pupuk kandang. Pupuk kompos berasal dari sisa-sisa tanaman, dan pupuk kandang
berasal dari kotoran ternak. Pupuk organik mempunyai komposisi kandungan unsur hara
yang lengkap, tetapi jumlah tiap jenis unsur hara tersebut rendah tetapi kandungan bahan
organik di dalamnya sangatlah tinggi. Sedangkan pupuk anorganik adalah jenis pupuk
kandungan persentase yang tinggi. Contoh pupuk anorganik adalah urea, TSP dan
Gandasil (Novizan, 2007).
2.5.1. Pupuk Organik
Pupuk organik adalah nama kolektif untuk semua jenis bahan organik asal tanaman dan
hewan yang dapat dirombak menjadi hara tersedia bagi tanaman. Dalam Permentan
No.2/Pert/Hk.060/2/2006, tentang pupuk organik dan pembenah tanah, dikemukakan
bahwa pupuk organik adalah pupuk yang sebagian besar atau seluruhnya terdiri atas
bahan organik yang berasal dari tanaman dan atau hewan yang telah melalui proses
rekayasa, dapat berbentuk padat atau cair yang digunakan mensuplai bahan organik untuk
memperbaiki sifat fisik, kimia, dan biologi tanah. Definisi tersebut menunjukkan bahwa
pupuk organik lebih ditujukan kepada kandungan C-organik atau bahan organik daripada
kadar haranya; nilai C-organik itulah yang menjadi pembeda dengan pupuk anorganik.
Bila C-organik rendah dan tidak masuk dalam ketentuan pupuk organik maka
diklasifikasikan sebagai pembenah tanah organik. Pembenah tanah atau soil ameliorant
menurut SK Mentan adalah bahan-bahan sintesis atau alami, organik atau mineral.
Sumber bahan organik dapat berupa kompos, pupuk hijau, pupuk kandang, sisa
panen (jerami, brangkasan, tongkol jagung, bagas tebu, dan sabut kelapa), limbah ternak,
limbah industri yang menggunakan bahan pertanian, dan limbah kota. Kompos
merupakan produk pembusukan dari limbah tanaman dan hewan hasil perombakan oleh
fungi, aktinomiset, dan cacing tanah. Pupuk hijau merupakan keseluruhan tanaman hijau
maupun hanya bagian dari tanaman seperti sisa batang dan tunggul akar setelah bagian
atas tanaman yang hijau digunakan sebagai pakan ternak (Litbang,2006).
Pupuk organik dapat dihasilkan dari bahan-bahan organik di alam. Bahan-bahan
untuk pupuk organik ini dapat ditemukan dari hewan atau tanaman. Satu manfaat yang
didapat dari pupuk organik yaitu kandungan bahan organik alaminya bermanfaat untuk
tanaman dan hewan. Bahan organik dalam pupuk organik membantu meningkatkan
dalam mengikat air dan juga meningkatkan kualitas struktur tanah, dan juga
meningkatkan kemampuan tanah dalam mengikat nutrisi. Manfaat yang lain dari bahan
organik yang terkandung dalam pupuk organik yaitu tidak mengurangi aktifitas-aktifitas
mikroba yang penting dalam tanah(Nnaji,2011).
Syarat-syarat yang dimiliki pupuk organik, yaitu :
a. Zat N atau zat lemasnya harus terdapat dalam bentuk persenyawaan organik, jadi
harus mengalami peruraian menjadi persenyawaan N yang mudah dapat diserap oleh
tanaman-tanaman.
b. Pupuk tersebut dapat dikatakan tidak meninggalkan sisa asam organik didalam tanah.
c. Pupuk tersebut seharusnya mempunyai kadar persenyawaan C organik yang tinggi,
seperti hidrat arang.
Pupuk organik mempunyai fungsi yang penting yaitu untuk menggemburkan
lapisan tanah permukaan (top soil), meningkatkan populasi jasad renik, mempertinggi
daya serap dan daya simpan air, yang keseluruhannya dapat meningkatkan kesuburan
tanah pula (Mul Mulyani Sutedjo,2002).
Pupuk organik sangat penting terutama karena sebagai berikut.
1. Memperbaiki struktur tanah.
Pada waktu penguraian bahan organik oleh organisme di dalam tanah dibentuk produk
yang mempunyai sifat sebagai perekat, yang lalu mengikat butir-butir pasir menjadi
butiran yang lebih besar. Lagipula di dalam tanah tumbuh sistem tali-temali yang terdiri
dari benang-benang jamur yang mengikat bagian tanah menjadi kesatuan.
2. Menaikkan daya serap tanah terhadap air
Bahan organik mempunyai daya absorpsi yang besar terhadap air tanah. Karena itu
pupuk organik sering kali mempunyai pengaruh positif terhadap hasil tanaman, apalagi
pada musim panas yang kering.
3. Menaikkan kondisi kehidupan di dalam tanah
Hal ini terutama disebabkan karena organisme di dalam tanah dapat memanfaatkan
bahan organik sebagai makanan. Berbagai organisme di dalam tanah dapat
memanfaatkan bahan organik sebagai makanan. Berbagai organisme itu di dalam tanah
4. Mengandung zat makanan tanaman
Berbagai zat makanan tanaman hanya sebagian dapat diserap oleh tanaman. Bagian
yang penting daripadanya baru tersedia sesudah terurainya bahan organik itu. Pupuk
organik biasanya menunjukkan pengaruh reaksi reaksi nitrogen yang jelas terlihat.
Pengaruh dari fosfat dan kalium biasanya tidak begitu jelas ( Rinsema, 1993).
3.5.1.1.Kompos
Kompos merupakan hasil akhir suatu proses fermentasi tumpukan sampah, serasah
tanaman ataupun bangkai binatang. Ciri-ciri kompos yang baik adalah berwarna coklat,
berstruktur remah, berkonsistensi gembur dan berbau daun lapuk. Tumpukan bahan
mentah (serasah, sisa tanaman, sampah dapur dan lain sebagainya) bisa menjadi kompos
akibat proses pelapukan dan penguraian, dengan kata lain terjadi perubahan dari sifat fisik
yang baru. Perubahan itu sebagian besar muncul oleh karena adanya kegiatan jasad renik
sehubungan dengan kebutuhan hidup organisme itu. Apa yang diikat oleh jasad renik
demi mencukupi kebutuhan hidupnya, kelak akan dikembalikan lagi apabila jasad renik
itu mati. Terjadi proses penguraian, pengikatan dan pembebasan berbagai zat atau unsur
hara selama berlangsungnya proses pembentukan kompos.
Penjelasan lengkap mengenai proses yang terjadi adalah sebagai berikut :
a. Hidrat arang (selulosa, hemiselulosa, dan lain-lain) diurai menjadi CO2 dan air atau
CH4 dan H2
b. Zat putih telur diurai menjadi amida,assam amino, amoniak, CO2 dan air
c. Berbagai jenis unsur hara, terutama N, disamping P, K dan yang lain sebagai hasil
penguraian, akan terikat dalam tubuh jasad renik. Sebagian yang tidak terikat akan
menjadi persediaan di dalam tanah. Yang terikat dalam tubuh jasad renik tersebut
kelak akan dikembalikan dalam tanah setelah jasad renik itu mati
d. Juga ada unsur hara dari senyawa organik yang akan terbebas menjadi senyawa
anorganik sehingga menjadi persediaan di dalam tanah bagi keperluan perttumbuhan
dan perkembangan tanaman.
Selama berlangsungnya proses tersebut akan terjadi perubahan berat dan isi dari
bahan-bahan pembuatannya. Terjadi pengurangan berat karena adanya penguapan dan
pencucian. Sebagian besar senyawa hidrat arang akan hilang ke udara selama penguapan
(Dipo Yono, 2007).
3.5.1.2. Proses Pengomposan
Sumber bahan organik tanah adalah jaringan tanaman baik yang berupa serasah atau sisa
tanaman yang berupa serasah atau sisa tanaman yang berupa batang, akar, daun, yang
kemudian dirombak oleh mikroorganisme tanah, atau sisa hewan yang berupa kotoran
maupun bangkai hewan. Secara kimiawi bahna organik tanah tersusun atas karbohidrat,
protein lignin dan sejumlah senyawa kecil seperti lemak, lilin dan sebagainya, salah satu
hasil perombakan bahan organik adalah humus, yang mempunyai kapasitas pengikatan
unsur hara dan air yang sangat tinggi, memiliki kekhususan koloidal dan mampu
mengikat air 80-90% dari berat keringnya, bandingkan dengan tanah liat yang hanya
mampu mengikat air 15-20% saja. Humus memberi warna tanah menjadi agak kehitaman
dan sangat bermanfaat bagi pertanian karena mempengaruhi struktur tanah.
Bahan organik dalam tanah sangat berhubungan dengan kecepatan pelapukan
tanah. Bahan organik yang mempunyai C/N rasio yang rendah akan lebih cepat melapuk
dibandingkan bahan organik yang mempunyaiC/N rasio yang tinggi. Untuk cepat lapuk
maka perlu penambahan nitrogen tanah yaitu denga menambahkan bahan organik yang
cepat lapuk. Walaupun demikian peran oksigen yang terkandung dalam tanah sangat
penting, karena berkurangnya kadar oksigen yang terkandung dalam tanah sangat penting,
karena berkurangnya kadar oksigen juga berpengaruh pada aktifitas mikroorganisme
dalam penguraian. Ini berkaitan dengan ketersediaan unsur hara dari bahan organik yang
bisa diserap tanaman (M,Isnaini,2006).
Reaksi-reaksi yang terjadi pada proses pengomposan yaitu :
Reduksi Sulfat :
CH3CHOHCOOH + SO4-2 2CH3COOH + H2S + 2OH
-Reduksi karbon organik secara anaerobik :
(M.Judoamidjojo,A.A.Darwis dan E.G. Said, 1992)
Reaksi Aminasi :
Pupuk cair limbah organik pada dasarnya limbah dari bahan organik bisa dimanfaatkan
menjadi pupuk, limbah cair banyak mengandung unsur hara (N,P,K). Penggunaan pupuk
cair dapat membantu memperbaiki struktur dan kualitas
Pupuk cair organik dalam aplikasi pemupukan lebih merata, sehingga tidak
tedrjadi penumpukan konsentrasi pupuk di satu tempat. Pupuk ini 100 persen larut dan
merata. Pupuk organik cair ini mempunyai kelebihan yaitu dapat secara cepat mengatasi
defisiensi hara dan tidak bermasalah dalam pencucian hara, juga mampu menyediakan
hara secara cepat (Shamsuddin,1994).
2.5.1.3. Pupuk Cair Limbah Organik
Pada dasarnya limbah cair dari bahan organik bisa dimanfaatkan menjadi pupuk. Sama
seperti limbah padat organik, limbah cair banyak mengandung unsur hara (NPK) dan
bahan organik lainnya. Penggunaan pupuk dari limbah ini dapat membantu memperbaiki
struktur dan kualitas tanah. Dari sebuah penelitian di Cina menunjukkan penggunaan
limbah cair organik mampu meningkatkan produksi pertanian 11% lebih tinggi
dibandingkan dengan menggunkan bahan organik lain. Bahkan di Cina penggunaan
pupuk kimia sintetik untuk pupuk dasar mulai tergeser dengan keunggulan pupuk organik
cair.
Petani di Cina mencampurkan limbah organik cair dengan tanah di areal
persawahannya dengan dosis 23 ton/ha setiap hari sebelum melakukan penanaman.
Sedangkan penggunaan pupuk kimia hanya sebagai pupuk lanjutan yang aplikasinya
dicampur dengan pupuk organik dengan perbandingan 1:1. Perbandingan ini mampu
BAB III
METODE PENELITIAN
3.1. Alat
• Gelas ukur Pyrex
• Gelas beaker Pyrex
• Gelas Erlenmeyer Pyrex
• Neraca kaki tiga Ohauss
• Autoklaf Yamato SN210
• Oven Gallenkamp
• Water bath Griffin
• Tabung reaksi pyrex
• Inkubator Fisher scientific
• Hot plate Thermelyne
• Labu takar Pyrex
• Cawan petri pyrex
• Pipet serelogi Pyrex
• Pipet volumetric Pyrex
• Vortex Fisons
• Buret Pyrex
• Spektrofotometric UV-Visibel Simadzu • Spektrofotometri Serapan Atom Shimadzu • Jarum ose
• Glass Object
• H2SO4(p) p.a E. Merck • (NH4)2Fe(SO4)2.6H2O p.a E. Merck
• K2Cr2O7 p.a E. Merck
• NaOH p.a E. Merck
• Fenolftalein p.a E. Merck
• Metil merah p.a E. Merck
• Metil biru p.a E. Merck
• H2C2O4.2H2O p.a E. Merck
• HCl p.a E. Merck
• H3BO3 p.a E. Merck
• H3PO4 p.a E. Merck
• Indikator difenilamin p.a E. Merck
• Selenium p.a E. Merck
3.3 Prosedur Penelitian
3.3.1. Penyediaan sampel sampah sayur pasar
Limbah sayur diambil secara acak dari kios-kios penjual sayur di pasar sore
Padang Bulan.
3.3.2. Penyediaan sampel tanah TPA
Tanah diambil dari Tempat Pembuangan Akhir di daerah Tuntungan.
3.3.3. Pembuatan starter
3.3.3.1. Pembuatan Media
3.3.3.1.1. Pembuatan Media Nutrien Agar
Ditimbang 2 g Nutrient Agar dan dimasukkan kedalam gelas Erlenmeyer 250 mL,
hingga mendidih diatas hot plate, ditutup dengan kapas dan aluminium foil dan dibalut
dengan kertas, dan disterilkan di dalam autoklaf pada suhu 121oC dan tekanan 15 Psi
selama 15 menit.
3.3.3.1.2. Pembuatan Media Skim Milk Agar (SMA)
Ditimbang 1 g susu skim dan dimasukkan kedalam gelas Erlenmeyer 100 mL,
ditambahkan 20 mL akuades dan diaduk hingga larut, kemudian dipanaskan di dalam
Waterbath hingga mendidih dan didinginkan. Ditimbang 2,3 g PCA dan dimasukkan ke
dalam gelas Erlenmeyer 250 mL, ditambahkan 80 mL akuades dan diaduk hingga larut,
dipanaskan diatas hot plate hingga mendidih, dan didinginkan. Dimasukkan larutan susu
skim ke dalam media PCA, diaduk hingga larut, ditutup dengan kapas dan aluminium foil
dan dibalut dengan kertas, dan disterilkan di dalam autoklaf pada suhu 121oC dan tekanan
15 Psi selama 15 menit.
3.3.3.1.3. Pembuatan Media Starch Agar (SA)
Ditimbang 0,3 g Starch Agar dan dimasukkan ke dalam gelas Erlenmeyer 250 mL,
ditambahkan 3 g Agar Swallow, kemudian ditambahkan 100 mL akuades dan diaduk
hingga larut, dipanaskan di atas hot plate hingga mendidih, ditutup dengan kapas dan
aluminium foil dan dibalut dengan kertas, dan disterilkan di dalam autoklaf pada suhu
121oC dan tekanan 15 Psi selama 15 menit.
3.3.3.1.4. Pembuatan Media Margarine
Ditimbang 3 g Margarine dan dimasukkan kedalam beaker glass 250 mL,
dipanaskan hingga meleleh. Ditimbang 3 g Agar Swallow dan dimasukkan kedalam gelas
Erlenmeyer 250 mL, ditambahkan 0,001 g Indikator Fenol Red, ditambahkan 100 mL
akuades dan diaduk hingga larut. Dimasukkan Margarin ke dalam larutan Agar dan
kapas dan aluminium foil dna dibalut dengan kertas, dan disterilkan di dalam autoklaf
pada suhu 121oC dan tekanan 15Psi selama 15 menit.
3.3.3.2. Isolasi Bakteri
3.3.3.2.1. Pembuatan Larutan Tanah 10-1
Ditimbang 1 g tanah Tempat Pembuangan Akhir dan dimasukkan kedalam tabung
reaksi, ditambahkan 9 mL akuades, dan dikocok hingga larut dengan menggunakan
vortex. Dilakukan prosedur yang sama untuk pembuatan Larutan tanah 10-2, dipipet dari
larutan tanah 10-1, dan dilakukan hingga pembuatan larutan tanah 10-6.
3.3.3.2.2. Penanaman Mikroorganisme pada Media
Dipipet larutan tanah 10-4 dan disebar diatas media padat N.A., diinkubasi di
dalam inkubator selama 1-2 hari. Dilakukan perlakuan yang sama untuk larutan tanah 10-5
dan 10-6.
3.3.3.2.3. Pembiakan Bakteri
Diambil koloni bakteri sp 1 menggunakan jarum ose, digoreskan diatas media
padat N.A., diinkubasi didalam inkubator selama 1-2 hari. Dilakukan perlakuan yang
sama untuk larutan tanah 10-5 dan 10-6.
3.3.3.2.4. Pembuatan Standar Mac Varlan
Diukur 0,05 mL BaCl2 0,048 M dan dimasukkan kedalam tabung reaksi,
ditambahkan 9,95 mL H2SO4 0,35 N kemudian ditutup dengan alumunium foil dan
3.3.3.2.5. Pembuatan Mac Varlan Bakteri
Dipipet 10 mL air suling steril kedalam tabung reaksi. Diinokulasi bakteri
kedalam tabung setelah itu divortex dan dilakukan hal yang sama dalam kondisi septic
hingga larutan bakteri sesuai dengan standar Mac Varlan.
3.3.3.3. Perlakuan Uji Pewarnaan Gram Bakteri
Diambil koloni bakteri sp 1 menggunakan jarum ose dan dibuat preparat luas
diatas glass objek, dipanaskan hingga kering menggunakan lampu spiritus, diteteskan 1-2
tetes zat warna kristal violet dan dibiarkan selama 1 menit, kemudian dibilas dengan
akuades, diteteskan 1-2 tetes iodine dan dibiarkan selama 30 detik, dibilas dengan aseton
alkohol dan dibiarkan selama 15 detik, kemudian dibilas dengan akuades, dan diteteskan
1 tetes larutan safranin dan dibiarkan selama 1 menit, dibilas dengan akuades dan
dikeringkan, kemudian diamati dibawah mikroskop. Perlakuan yang sama dilakukan
untuk koloni bakteri sp2, sp3 dan sp4.
3.3.3.4. Perlakuan Uji Potensial Bakteri
3.3.3.4.1. Uji Potensial terhadap Karbohidrat
Dipipet larutan Mac Varlan Bakteri sp 1 dan diteteskan diatas kertas cakram
menggunakan pipet man, diletakkan kertas cakram diatas media padat Starch Agar
diinkubasi di dalam inkubator selama 3 hari Perlakuan yang sama dilakukan untuk
Bakteri sp2, sp3 dan sp4. Uji Potensial dilakukan dengan mengukur zona bening
disekeliling kertas cakram menggunakan jangka sorong.
3.3.3.4.2. Uji Potensial terhadap Protein
Dipipet larutan Mac Varlan Bakteri sp 1 dan diteteskan diatas kertas cakram
menggunakan pipet man, diletakkan kertas cakram diatas media padat Skim Milk Agar
Bakteri sp2, sp3 dan sp4. Uji Potensial dilakukan dengan mengukur zona bening
disekeliling kertas cakram menggunakan jangka sorong.
3.3.3.4.3. Uji Potensial terhadap Lemak
Dipipet larutan Mac Varlan Bakteri sp 1 dan diteteskan diatas kertas cakram
menggunakan pipet man, diletakkan kertas cakram diatas media padat Margarin +agar,
diinkubasi di dalam inkubator selama 3 hari Perlakuan yang sama dilakukan untuk
Bakteri sp2, sp3 dan sp4. Uji Potensial dilakukan dengan mengukur zona bening
disekeliling kertas cakram menggunakan jangka sorong.
3.3.3.5. Pembuatan Larutan bakteri standart Mac Varlan sebagai starter
pembuatan pupuk organik
Diinokulasikan bakteri sp3 kedalam tabung yang berisi 10 mL akuades steril,
kemudian dikocok menggunakan vortex, dan dilakukan hal yang sama sampai larutan
sebanding dengan larutan standart Mac Varlan.
3.3.4. Pembuatan pupuk organik cair
Kedalam wadah plastik dimasukkan sampah sayur yang telah dipotong kecil-kecil,
kemudian ditambahkan 300 mL larutan bakteri sp3 sebagai starter untuk pembuatan
pupuk, diaduk hingga homogen, kemudian ditutup rapat dan dibiarkan hingga terjadi
proses fermentasi, dan dicatat waktu volume pupuk organik cair setelah pengomposan 1
3.3.5. Pembuatan Pereaksi dan Larutan Standart
3.3.5.1. Pembuatan pereaksi untuk penentuan C-organik
a. Larutan K2Cr2O7 1 N
Ditimbang secara kwantitatif kristal K2Cr2O7 sebanyak 12,257 g, dimasukkan
kedalam gelas piala 250 mL, dilarutkan dengan akuades secukupnya, dimasukkan
kedalam labu takar 250 mL, diencerkan hingga garis tanda, dan dikocok sampai
homogen.
b. Larutan FeSO4 1N
Ditimbang secara kwantitatif kristal FeSO4.7H2O sebanyak 69,505 g, dimasukkan
kedalam gelas piala 250 mL, dilarutkan dengan akuades secukupnya, ditambahkan
37,5mL H2SO4(p) secara perlahan-lahan, diaduk hingga larut, dimasukkan kedalam labu
takar 250 mL, ditambahkan akuades hingga garis tanda, didinginkan dan dikocok sampai
homogen.
c. Larutan Difenilamin (C6H5)2NH4)
Ditimbang 0,5 g Kristal difenilamin, dilarutkan dengan 20 mL akuades dalam
gelas piala 250 mL, ditambahkan dengan 100 mL H2SO4(p) secara perlahan-lahan dengan
merendam beaker glass dalam air es, dan diaduk hingga larut seluruhnya.
3.3.5.2. Pembuatan Pereaksi untuk Penentuan Nitrogen Metode Kjeldhal
a. Larutan NaOH 40%
Ditimbang sebanyak 40 g Kristal NaOH, dimasukkan kedalam gelas piala 250mL,
kemudian dilarutkan dengan akuades, dimasukkan kedalam labu takar 100 mL,
b. Larutan Indikator Phenolphtalein
Ditimbang 0,5 g Phenolphtalein, dimasukkan kedalam labu takar 100 mL,
diencerkan hingga garis tanda, dan dikocok sampai homogen.
c. Larutan H3BO3 4%
Ditimbang H3BO3 sebanyak 4 g, dimasukkan kedalam gelas piala 250 mL,
dilarutkan dengan akuades, dimasukkan kedalam labu takar 100 mL, diencerkan hingga
garis tanda dan dikocok sampai homogen.
d. Larutan Indikator Tashiro
Sebanyak 2 bagian indikator metil biru 0,1 % (b/v) dan 1 bagian indikator metil
merah 0,2 % (b/v) dalam etanol.
e. Larutan H2C2O4 0,01 N
Ditimbang kristal H2C2O4.2H2O secara kwantitatif sebanyak 0,63 g, dimasukkan
kedalam gelas piala 250 mL, dilarutkan dengan akuades, dimasukkan kedalam labu takar
1000 mL, diencerkan hingga garis tanda, dan dikocok sampai homogen.
f. Larutan NaOH 0,01 N
Ditimbang kristal NaOH sebanyak 0,4 g, dimasukkan kedalam gelas piala 250mL,
dilarutkan dengan akuades, dimasukkan ke dalam labu takar 1000 mL, diencerkan hingga
g. Larutan HCl 0,1 N
Sebanyak 0,83 mL HCl 37 % dipipet ke dalam labu takar 1000 mL, diencerkan
hingga garis tanda dengan akuades, dan dikocok sampai homogen.
h. Standarisasi Larutan NaOH 0,01 N
Dipipet 10 mL larutan H2C2O4 0,01 N dan dimasukkan ke dalam gelas
Erlenmeyer, ditambahkan 3 tetes indikator Phenolphtalein, kemudian dititrasi dengan
NaOH hingga terjadi perubahan warna menjadi merah lembayung, dilakukan prosedur
yang sama sebanyak 3 kali.
i.Standarisasi HCl 0,1 N
Dipipet 10 mL larutan HCl 0,01 N dimasukkan ke dalam gelas Erlenmeyer,
ditambahkan 3 tetes indikator bromtimul blue, dititrasi dengan NaOH yang telah
distandarisasi hingga terjadi perubahan warna biru menjadi hijau kekuningan, dilakukan
prosedur yang sama sebanyak 3 kali.
3.3.5.3. Pembuatan Pereaksi dan Larutan Standart untuk Penentuan Posfor sebagai
P2O5 metode spektrofotometer
a. Larutan HCl 25%
Dipipet 173,6 mL HCl(p), dimasukkan ke dalam labu takar 250 mL, diencerkan dengan
akuades hingga garis tanda dan dikocok sampai homogen.
b. Larutan Standart Posfor 100 ppm
Ditimbang 0,2195 g kristal KH2PO4 secara kuantitatif, diamsukkan kedaalm gelas
piala 250 mL, dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu takar
c. Larutan Amonium Molibdat 4 %
Ditimbang 1,883 g kristal (NH4)6Mo7O24.4H2O, dimasukkan kedalam gelas piala
50 mL, dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu takar 50
mL, diencerkan dengan akuades hingga garis tanda, dan dikocok sampai homogen.
d. Larutan Asam Askorbat 0,1 M
Ditimbang 0,880 g Kristal C6H8O6, dimasukkan ke dalam gelas piala 50 mL,
dilarutkan dengan akuades secukupnya, dimasukkan kedalam labu takar 50 mL,
diencerkan dengan akuades hingga garis tanda, dan dikocok sampai homogen.
e. Larutan Kalium antimonil Tartarat 1 mg Sb/mL
Ditimbang 0,105 g kristal KSbOC4H4O6.1�2H2O, dimasukkan kedalam gelas piala 50 mL, dilarutkan dengan akuades secukupnya, dimasukkan ke dalam labu takar 50
mL, diencerkan dengan akuades hingga garis tanda, dan dikocok sampai homogen.
f. Larutan Seri standart P dalam ekstrak HCl 0,95 N
Dipipet masing-masing 20 mL akuades dan 11,7 mL HCl 25 % kedalam labu
takar 100 mL, dipipet 2 mL, 4 mL, 6 mL, 8 mL, 10 mL larutan standart 100 ppm secara
kwantitatif, diencerkan deeengan akuades hingga garis tanda, dan dikocok sampai
homogen.
g. Larutan H2SO4 5 N
Dipipet 13,72 mL H2SO4(p), dimasukkan kedalam labu takar 100 mL yang telah
berisi 20 mL akuades, diencerkan dengan akuades hingga garis tanda, didinginkan dan
h. Pembuatan Larutan Campuran pengkompleks
Dipipet 25 mL H2SO4 5 N kedalam labu takar 50 mL, ditambahkan 7,5 mL larutan
(NH4)6Mo7O24 4%, ditambahkan 15 mL larutan asam askorbat o,1 M, ditambahkan 2,5
mL larutan KSbOC4H4O6 0,1 M, dan dikocok sampai homogen.
3.3.5.4. Pembuatan Pereaksi Untuk Penentuan Kalium sebagai K2O dengan Metode
Spektrofotometer Serapa Atom (SSA)
a. Larutan HCl 25%
Dipipet 173,6 mL HCl(p), dimasukkan kedalam labu takar 250 mL, diencerkan
dengan akuades hingga garis tanda dan dikocok sampai homogen.
b. Larutan Kalium 100 ppm
Dilarutkan 1,907 g KCl p.a. dengan akuades dalam labu takar 1000 mL hingga
garis tanda. Larutan ini mengandung 1 mg K/L.
c. Larutan Standart Kalium 100 ppm
Sebanyak 10 mL larutan standart kalium 1000 ppm diencerkan dengan akuades
dalam labu takar 100 mL hingga garis tanda.
d. Larutan Seri Standart Kalium untuk kalibrasi (0,0 – 5 – 10 – 15 – 20 ppm)
Dari larutan standart 100 ppm kalium masing-masing dipipet 0,0 ; 5 ; 10 ; 15;
20mL, kemudian masing-masing diencerkan dengan akuades dalam labu takar 100 mL
3.3.6. Penentuan Kadar C-organik dengan metode Walkey Black
Dipipet sebanyak 1 mL sampel dan dimasukkan kedalam gelas Erlenmeyer 500
mL, ditambahkan 10 mL larutan K2Cr2O7 1N, ditambahkan 5 mL H2SO4(p) secara
perlahan-lahan, kemudian diaduk selama 1 menit dan didiamkan selama 30 menit,
ditambahkan 200 mL akuades, ditambahkan 5 mL H3PO4(p) (85%) dan 1 mL larutan
difenilamin, dititrasi dengan larutan FeSO4 hingga terjadi perubahan warna dari ungu
menjadi hijau.
3.3.7. Pengukuran Nitrogen dengan Metode Kjeldahl
Dimasukkan 20 g sampel kedalam labu kjeldahl 100 mL, ditambahkan 2 g
campuran Selenium dan 25 mL H2SO4(p) , dipanaskan diatas pemanas listrik atau api
pembakar sampai mendidih dan larutan menjadi jernih kehijau-hijauan, ditunggu sampai
larutan dingin, dimasukkan kedalam labu takar 250 mL dan diencerkan dengan akuades,
dipipet 50 mL larutan yang telah diencerkan dan dimasukkan kedalam alat destilasi,
ditambahkan 20 mL NaOH 40 %, didestilasi selama lebih kurang 10 menit, ditampung
destilat didalam 25 mL larutan asam borat 4 % yang telah dicampur dengan indicator,
dibilas ujung pendingin dengan akuades, dititrasi dengan larutan HCl 0,1 N dan dihitung
% Nitrogen.
3.3.8. Penentuan P-Total Metode Spektrofotometri
3.3.8.1. Preparasi Sampel
Dimasukkan 1 mL sampel kedalam gelas Erlenmeyer 250 mL, ditambahkan
dengan 12,5 mL HCl 25 %, dikocok dengan pengaduk stirrer selama 2 jam, disaring
dengan kertas saring whatman no. 40, ditampung ekstrak ke dalam labu takar 100 mL,
3.3.8.2. Pembuatan Kurva Kalibrasi
Dipipet 1 mL masing-masing larutan standart kedalam tabung reaksi, ditambahkan
5 mL akuades, ditambahkan 1 mL larutan campuran, didiamkan selama 15 menit, diukur absorbansinya dengan spektrofotometer, pada λ = 400 nm, dibuat kurva kalibrasi konsentrasi terhadap absorbansi.
3.3.9. Penentuan Kalium sebagai K2O dengan Metode Spektrofotometer Serapan
Atom (SSA)
Sebanyak 5 mL sampel dimasukkan kedalam gelas Erlenmeyer 100 mL,
ditambahkan 12,5 mL HCl 25% , dibiarkan larutan selama 1 malam, kemudian diaduk
dengan pengaduk magnit stirrer selama 2 jam sampai terbentuk suspensi, lalu disaring
dengan menggunakan kertas saring Whatman No. 40, filtrat dimasukkan kedalam takar
100 mL sambil dicuci sebanyak 3 kali dengan akuades, lalu ditambahkan akuades sampai
garis tanda, filtrate disimpan di dalam botol plastic untuk penetapan kadar Kalium, diukur
konsentrasi Kalium menggunakan Spektrofotometer Serapan Atom pada panjang
3.4. Bagan Penelitian
3.4.1. Skema Pembuatan Starter
3.4.1.1. Skema Pembuatan Media
3.4.1.1.1. Skema Pembuatan Media Nutrien Agar
Dimasukkan kedalam gelas Erlenmeyer 250 mL
Ditambahkan 100 mL akuades
Dipanaskan diatas hot plate hingga mendidih
Dididinginkan
Ditutup dengan kapas dan aluminium foil dan
dibalut dengan kertas
Disterilkan didalam autoklaf pada suhu 121oC dan
tekanan 15 Psi selama 15 menit
Hasil
3.4.1.1.2. Skema Pembuatan Media Skim Milk Agar (SMA)
Ditambahkan 20 mL akuades
Diaduk hingga larut
Dimasukkan larutan susu skim kedalam larutan
media PCA
Diaduk hingga larut
Ditutup dengan kapas dan aluminium foil dan
dibalut dengan kertas
Disterilkan didalam autoklaf pada suhu 121oC
dan tekanan 15 Psi selama 15 menit
3.4.1.1.3. Skema Pembuatan Media Starch Agar (SA)
0,3 g Starch Agar
Dimasukkan kedalam gelas Erlenmeyer 250mL
Ditambahkan 3 g agar Swallow
Ditambahkan 100 mL akuades
Diaduk hingga larut
Dipanaskan diatas hot plate hingga mendidih
Didinginkan
Ditutup dengan kapas dan aluminium foil dan
dibalut dengan kertas
Disterilkan didalam autoklaf pada suhu 121oC
dan tekanan 15 Psi selama 15 menit
3.4.1.1.4. Skema Pembuatan Media Margarin
3 g Agar Swallow 3 g Margarin
Dimasukkan kedalam gelas
Erlenmeyer 250 mL
Ditambahkan 0,001 g
indikator Fenol Red
Ditambahkan 100 mL
akuades
Diaduk hingga larut Dimasukkan kedalam
Beaker glass 250 mL
Dipanaskan diatas hot plate
hingga meleleh
Hasil Hasil
Dimasukkan margarin kedalam larutan Agar
Diaduk hingga larut
Dipanaskan diatas hot plate hingga mendidih
Didinginkan
Ditutup dengan kapas dan aluminium foil dan dibalut dengan
kertas
Disterilkan didalam autoklaf pada suhu 121oC dan tekanan
15Psi selama 15 menit
3.4.1.2. Skema Isolasi Bakteri
3.4.1.2.1. Skema Pengenceran Bertingkat
N. B. : Dilakukan prosedur yang sama untuk pembuatan Larutan tanah 10-2, dipipet dari
larutan tanah 10-1, dan dilakukan hingga pembuatan larutan tanah 10-6
3.4.1.2.2. Skema Penanaman Mikroorganisme Pada Media
N.B. : Dilakukan perlakuan yang sama untuk larutan tanah 10-5 dan 10-6 1 g tanah
Dimasukkan kedalam tabung reaksi
Ditambahkan 9 mL akuades
Dikocok hingga larut dengan menggunakan
Vortex
Larutan tanah 10-1
Dipipet sebanyak 1 mL
Disebar diatas media padat NA dengan
menggunakan hockey stick
Diinkubasi dalam inkubator selama 1-2
hari Larutan tanah 10-4
3.4.1.2.3. Skema Pembiakan Bakteri
N.B. : Dilakukan perlakuan yang sama untuk koloni bakteri sp2, sp3 dan sp4. Koloni bakteri sp 1
Diinokulasi pada media padat N.A dengan
metode gores
Diinkubasi didalam inkubator selama 1-2
hari
3.4.1.3. Skema Uji Pewarnaan gram Bakteri
N.B. : Perlakuan yang sama dilakukan untuk koloni bakteri sp2, sp3 dan sp4. Bakteri sp 1
Diambil sebanyak 1 ose
Dibuat preparat luas diatas glass object
Dipanaskan hingga kering menggunakan lampu
spiritus
Diteteskan 1-2 tetes zat warna kristal violet dan
dibiarkan selama 1 menit
Dibilas dengan akuades
Diteteskan 1-2 tetes iodine dan dibiarkan selama
30 detik
Dibilas dengan aseton alkohol dan dibiarkan
selama 15 detik
Dibilas dengan akuades
Diteteskan 1 tetes larutan safranin dan dibiarkan
selama 1 menit
Dibilas dengan akuades
Dikeringkan
Diamati dibawah mikroskop
3.4.1.4. Skema Uji Potensial
3.4.1.4.1. Uji Potensial terhadap karbohidrat
N.B. : - Perlakuan yang sama dilakukan untuk Bakteri sp2, sp3 dan sp4
- Uji Potensial dilakukan dengan mengukur zona bening disekeliling kertas cakram menggunakan jangka sorong
3.4.1.4.2. Uji Potensial terhadap Protein
N.B. : - Perlakuan yang sama dilakukan untuk Bakteri sp2, sp3 dan sp4
- Uji Potensial dilakukan dengan mengukur zona bening disekeliling kertas cakram menggunakan jangka sorong
Larutan Mac Varlan Bakteri sp1
Dipipet dan diteteskan diatas kertas
cakram menggunakan pipet man
Diletakkan kertas cakram diatas media
padat Starch Agar
Diinkubasi di dalam inkubator selama 3
hari
Hasil
Larutan Mac Varlan Bakteri sp 1
Dipipet dan diteteskan diatas kertas
cakram menggunakan pipet man
Diletakkan kertas cakram diatas media
padat Skim Milk Agar
Diinkubasi di dalam inkubator selama 1 x
24 jam
3.4.1.4.3. Uji Potensial terhadap Lemak
N.B. : - Perlakuan yang sama dilakukan untuk Bakteri sp2, sp3 dan sp4
- Uji Potensial dilakukan dengan mengukur zona bening disekeliling kertas cakram menggunakan jangka sorong
3.4.1.5. Skema Pembuatan Larutan bakteri sp3 standart Mac Varlan sebagai starter pembuatan pupuk organik
Larutan Mac Varlan Bakteri sp 1
Dipipet dan diteteskan diatas kertas
cakram menggunakan pipet man
Diletakkan kertas cakram diatas media
padat Margarin Agar
Diinkubasi di dalam inkubator selama 1 x
24 jam
Hasil
Bakteri sp 3
Diinokulasikan kedalam tabung yang berisi 10 mL akuades steril
Dikocok menggunakan vortex
Dilakukan hal yang sama sampai larutan sebanding dengan larutan standart Mac Varlan
3.4.2. Skema Pembuatan Pupuk Organik Cair
Sampah sayur pasar pagi
Dipotong-potong menjadi bagian kecil
Potongan sampah sayur
Dimasukkan kedalam wadah
Disterilkan
Ditambahkan 300 mL larutan bakteri sp3 standart Mac.Varlan
Fermentasi
Catat waktu dan volume
Padatan Cairan
Ditentukan kadar C-organik, Nitrogen, Posfor dan Kalium
3.4.3. Skema Penentuan Kadar C-organik,Nitrogen, Posfor, dan Kalium
3.4.3.1. Skema Penentuan Kadar C-organik
Hasil Larutan Ungu
Dititrasi dengan FeSO4 0,8987 N hingga warna berubah menjadi hijau
Dicatat volume FeSO4 0,8978 N Ditambahkan 10 mL akuades
Ditambahkan 5 mL H3PO4 85%
Ditambahkan 1 mL larutan difenilamin Larutan hijau kekuningan
Ditambahkan 10 mL K2Cr2O7 1 N
Ditambahkan 20 mL H2SO4 (p)
Diaduk selama 1 menit
3.4.3.2. Skema Penentuan Kadar Nitrogen Pupuk Organik Cair
. 1 mL sampel
Hasil
Ditentukan % Nitrogen Larutan Merah Muda
Ditampung didalam gelas Erlenmeyer yang berisi 50 mL H3BO3 3% dan 3 tetes indikator campuran hingga berwarna hijau
Destilat berwarna hijau
Dipindahkan kedalam labu destilasi
Ditambahkan 50 mL akuades
Ditambahkan 3 tetes indikator Phenolphtalein
Ditambahkan NaOH 40%
Dipanaskan Larutan coklat
Ditambahkan 0,3 g Selenium dan H2SO4(p)
3.4.3.3. Skema Penentuan Posfor sebagai P2O5 Metode Spektrofotometri
3.4.3.3.1. Pembuatan Ekstrak
3.4.3.3.2. Pengukuran Absorbansi Larutan Standart P untuk kurva Kalibrasi Larutan standart 2 ppm
1 mL sampel
Ekstrak pupuk organik cair
Dimasukkan kedalam labu takar 100 mL
Ditambahkan akuades hingga garis tanda
Dihomogenkan
Residu Ekstrak pupuk organik cair
Ditambahkan 12,5 mL HCl 25 %
Dikocok selama 2 jam dengan pengaduk dengan kecepatan 20 rpm
Disaring dengan kertas saring whatman n0.40
1 mL larutan standart 2 ppm
Hasil
Diukur absorbansi dengan spektrometer pada λ = 400 nm Larutan berwarna
Dimasukkan ke dalam tabung reaksi
Ditambahkan 5 mL akuades
Ditambahkan 1 mL larutan campuran pengkompleks
3.4.3.3.3. Skema Pengukuran Absorbansi untuk ekstrak pupuk organik cair
3.4.3.4. Skema Penentuan Kalium sebagai K2O dengan metode Spektrofotometer
Serapan Atom
Hasil
Diukur absorbansinya dengan spektrofotometer pada
λ= 400 nm Larutan berwarna biru
Dimasukkan ke dalam tabung reaksi
Ditambahkan 5 mL akuades
Ditambahkan 1 mL larutan campuran pengkompleks
Didiamkan selama 15 menit 1 mL larutan ekstrak pupuk organik
Hasil
Dimasukkan kedalam gelas Erlenmeyer 100 mL
Ditambahkan 40 mL HNO3(p)
Dipanaskan hingga suhu 80oC hingga HNO3 menguap
Didinginkan
Diencerkan dengan akuades hingga volume 100 mL
Disaring dengan kertas saring Whatman no. 42
Diukur pH 3,5-5
Dimasukkan kedalam labu takar 50 mL hingga garis tanda