PENETAPAN KADAR KALIUM, KALSIUM DAN
NATRIUM PADA BIJI, DAGING BUAH DAN DAUN
LABU KUNING (
Cucurbita moschata
D.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
VERONIKA P. S. GINTING
NIM 101501147
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALIUM, KALSIUM DAN
NATRIUM PADA BIJI, DAGING BUAH DAN DAUN
LABU KUNING (
Cucurbita moschata
D.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
VERONIKA P. S. GINTING
NIM 101501147
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALIUM, KALSIUM DAN
NATRIUM PADA BIJI, DAGING BUAH DAN DAUN
LABU KUNING (
Cucurbita moschata
D.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
VERONIKA P. S. GINTING
NIM 101501147
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 29 November 2014
Medan,
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Prof. Dr. Sumadio Hadisahputra, Apt. NIP 195311281983031002
Pembimbing I,
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Pembimbing II,
Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Panitia Penguji,
Prof. Dr. Ginda Haro, M.Sc., Apt. NIP 195108161980031002
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Esa yang telah memberikan kasih, rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul “Penetapan kadar kalium, kalsium dan natrium pada biji, daging buah dan daun labu kuning (Cucurbita moschata D.) secara Spektrofotometri serapan atom”. Skripsi ini disusun untuk melengkapi salah satu syarat memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyampaikan terima kasih kepada Bapak Dekan Fakultas Farmasi Prof. Dr. Sumadio Hadisahputra, Apt., yang telah memberikan fasilitas kepada penulis sehingga dapat menyelesaikan pendidikan. Kepada Bapak Drs. Fathur Rahman Harun, M.Si., Apt., dan Bapak Dr. Muchlisyam M.Si.,Apt., yang telah membimbing penulis dengan sabar sehingga penulisan skripsi ini dapat diselesaikan. Kepada Ibu Dra. Masria Lasma Tambunan, M.Si., Apt., selaku penasihat akademik yang telah memberikan nasihat dan arahan kepada penulis selama masa perkuliahan dan Bapak/Ibu Pembantu Dekan, Bapak dan Ibu staf pengajar Fakultas Farmasi USU atas ilmu yang telah diberikan. Kepada Bapak Dr. Ginda Haro, M.Sc., Apt., Ibu Tuti Pardede, M.Si., Apt., dan Ibu Dra. Sudarmi, M.Si., Apt., selaku dosen penguji yang telah memberikan saran, arahan, kritik dan masukan kepada penulis dalam penyelesaian skripsi ini.
dukungan baik moril maupun materil, serta kerabat-kerabat dan sahabat-sahabat penulis atas motivasi dan segala bantuan dalam penyelesaian skripsi ini.
Penulis menyadari bahwa penulisan skripsi ini masih jauh dari sempurna, untuk itu penulis mengharapkan kritik dan saran yang membangun dari semua pihak demi kesempurnaan skripsi ini. Harapan penulis semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan khususnya di bidang Farmasi.
Medan, 29 November 2014 Penulis,
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM PADA BIJI, DAGING BUAH DAN DAUN
LABU KUNING (Cucurbita moschata D.) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Labu kuning atau waluh (Cucurbita moschata) yang termasuk dalam suku Cucurbitaceae merupakan salah satu tanaman yang penting untuk dikonsumsi karena mempunyai kandungan gizi yang tinggi dan lengkap. Tanaman ini kaya akan vitamin A, B dan C, mengandung mineral seperti kalium, kalsium, natrium, besi, fosfor serta mengandung karbohidrat dan protein. Daun, daging buah dan biji labu kuning mengandung kalium, kalsium dan natrium yang berperan menurunkan risiko hipertensi. Oleh karena itu, penelitian ini bertujuan untuk mengetahui kadar kalium (K), kalsium (Ca) dan natrium (Na) pada daun, daging dan biji serta untuk mengetahui perbedaan kadar ketiga mineral tersebut.
Metode penelitian yang dilakukan secara deskriptif dengan pengambilan sampel biji, daging buah dan daun labu kuning (Cucurbita moschata) dan dilakukan destruksi kering. Penetapan kadar dilakukan dengan menggunakan alat spektrofotometer serapan atom untuk kalium pada panjang gelombang 766,5 nm, kalsium 422,7 nm dan natrium 589,0 nm menggunakan nyala udara-asetilen. Dilakukan juga uji nyala dengan kawat Ni/Cr dan uji kristal (kritalisasi) untuk mengidentifikasi mineral secara kualitatif.
Hasil penelitian menunjukkan kadar kalium dalam biji adalah (376,15 ± 12,05) mg/100 g, daging buah (394,86 ± 5,02) mg/100 g, dan daun (478,61 ± 1,53) mg/100 g, kadar kalsium dalam biji (6,54 ± 0,09) mg/100 g, daging buah (18,66 ± 0,10) mg/100 g dan daun yaitu (36,29 ± 0,18) mg/100 g dan kadar natrium dalam biji (17,92 ± 0,37) mg/100 g, daging buah (14,33 ± 4,03) mg/100 g dan daun adalah (20,90 ± 0,28) mg/100 g.
Dari hasil penelitian dapat disimpulkan bahwa kadar kalium, kalsium dan natrium pada biji, daging buah dan daun berbeda secara signifikan pada interval kepercayaan 95% dan kadar tertinggi adalah kadar kalium yang terdapat pada daun.
DETERMINATION OF POTASSIUM, CALCIUM AND SODIUM CONCENTRATION IN SEEDS, FLESHES AND LEAVES OF PUMPKIN (Cucurbita moschata D.) BY ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Pumpkin or squash (Cucurbita moshata) belonging to Cucurbitaceae family is one among the plants that important to consume. Pumpkin has been grown for the purpose of consumption as vegetable or as a medicine. The leaves, flesh and seed are very useful for a healthy life. Leaves, fleshes and seeds can decrease the hypertension risk. For that reason, the purpose of this research was to determine the potassium (K), calcium (Ca) and sodium (Na) level and the differences among that three minerals on seed, flesh and leaves.
The method that used in this research was descriptive, sampling from seeds, fleshes and leaves of pumpkin (Cucurbita moschata) using dry ashing. To determine the three minerals level were using atomic absorption spectrophotometry for potassium at a wavelength 766.5 nm, for calcium 422.7 nm and sodium 589.0 nm which using air-acetylene flame. Furthermore, the investigation for that three mineral was done by cristalization and flame test wtih Ni/Cr.
The result showed that the concentration of potassium in seeds was (376.15 ± 12.05) mg/100 g, fleshes was (394.86 ± 5.02) mg/100 g, and leaves (478.61 ± 1.53) mg/100 g, the level of calcium in seed was (6.54 ± 0.09) mg/100 g, fleshes was (18.66 ± 0.10) mg/100 g and leaves was (36.29 ± 0.18) mg/100 g, the concentration of sodium in seed was (17.92 ± 0.37) mg/100 g, fleshes was (14.33 ± 4.03) mg/100 g and leaves was (20.90 ± 0.28) mg/100 g.
Based on the result the levels of potassium, calcium and sodium in seeds, fleshes and leaves are significant difference with 95% confidence level and the highest level is potassium in leaves.
DAFTAR ISI
Halaman
JUDUL ….. ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA . ... 4
2.1 Uraian Tumbuhan ... 4
2.1.1 Tumbuhan Labu Kuning ... 4
2.1.1.1 Sistematika Tumbuhan ... 4
2.1.1.2 Morfologi Tumbuhan ... 5
2.1.1.3 Kandungan Kimia ... 5
2.2 Mineral ... 6
2.2.1 Kalsium ... 6
2.2.2 Kalium ... 7
2.2.3 Natrium ... 8
2.3 Spektrofotometri Serapan Atom ... 9
2.3.1 Instrumentasi SSA ... 10
2.4 Validasi Metode Analisis ... 13
BAB III METODE PENELITIAN ... 16
3.1 Tempat dan Waktu Penelitian ... 16
3.2 Bahan-Bahan ... 16
3.2.1 Sampel ... 16
3.2.2 Pereaksi ... 16
3.3 Alat-alat ... 16
3.4 Identifikasi Sampel ... 17
3.5 Pembuatan Pereaksi ... 17
3.5.1 Larutan HNO3 (1:1) ... 17
3.5.2 Larutan H2SO4 1 N ... 17
3.5.3 Larutan HCL 2N ... 17
3.5.4 Larutan asam pikrat 1% b/v ... 17
3.6 Prosedur Penelitian ... 17
3.6.1 Pengambilan Sampel ... 17
3.6.2 Penyiapan Sampel ... 18
3.6.3 Proses Destruksi Kering ... 18
3.6.5 Analisis Kualitatif ... 18
3.6.5.1 Kalsium ... 18
Uji dengan Reaksi Nyala ... 18
Uji kristal kalsium dengan asam sulfat 1N .. 18
3.6.5.2 Kalium ... 18
Uji dengan Reaksi Nyala ... 18
Uji kristal kalium dengan asam pikrat ... 19
3.6.5.3 Natrium ... 19
Uji dengan Reaksi Nyala ... 19
Uji kristal natrium dengan asam pikrat ... 19
3.6.6 Analisis Kuantitatif ... 19
3.6.6.1 Kalium ... 19
Pembuatan kurva kalibrasi kalium ... 19
Penetapan kadar kalium dalam sampel ... 20
3.6.6.2 Kalsium ... 21
Pembuatan kurva kalibrasi kalsium ... 21
Penetapan kadar kalsium dalam sampel ... 22
3.6.6.3 Natrium ... 22
Pembuatan kurva kalibrasi natrium ... 22
Penetapan kadar natrium dalam sampel ... 22
3.6.7 Analisis Data Secara Statistik ... 23
3.6.7.1 Penolakan Hasil Pengamatan ... 23
3.6.8 Pengujian Beda Nilai Rata-Rata Antar Sampel ... 24
3.6.10 Simpangan Baku Relatif ... 25
3.6.11 Penentuan Batas Deteksi dan Batas Kuantitasi ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Identifikasi Sampel ... 27
4.2 Analisis Kualitatif ... 27
4.3 Analisis Kuantitatif ... 28
4.3.1 Kurva kalibrasi kalium, kalsium, dan natrium ... 29
4.3.2 Analisis kadar kalsium, kalium, dan natrium pada biji, daging dan daun labu kuning ... 30
4.3.3 Analisis Data Secara Statistik ... 33
4.3.4 Uji Perolehan Kembali (Recovery) ... 33
4.3.5 Batas Deteksi dan Batas Kuantitasi ... 34
4.3.6 Simpangan Baku Relatif ... 35
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Halaman Tabel 4.1 Hasil Analisis Kualitatif dalam Sampel Biji, Daging dan
Daun Labu Kuning yang Telah Didestruksi . ……… 27 Tabel 4.2 Hasil Analisis Kadar Kalsium, Kalium dan Natrium dalam
Sampel ………..….. 31 Tabel 4.3 Persen Uji Perolehan Kembali (recovery) Kadar Kalsium,
Kalium dan Natrium ………..……….… 34 Tabel 4.4 Batas Deteksi dan Batas Kuantitasi Kalsium, Kalium dan
Natrium ...………..………..… 35 Tabel 4.5 Nilai Simpangan Baku dan Simpangan Baku Relatif
DAFTAR GAMBAR
DAFTAR LAMPIRAN
Halaman Lampiran 1 Bagan Alir Proses Destruksi Kering ... 40 Lampiran 2 Bagan Alir Proses Pembuatan Larutan Sampel ... 43 Lampiran 3 Perhitungan Kalibrasi Kalsium dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 44 Lampiran 4 Perhitungan Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi
dan Koefisien Korelasi (r) ... 46 Lampiran 5 Perhitungan Kalibrasi Natrium dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi
dan Koefisien Korelasi (r) ... 48 Lampiran 6 Hasil Analisis Kadar Kalsium, Kalium, dan Natrium
dalam Daun Labu Kuning ... 50 Lampiran 7 Contoh Perhitungan Kadar Kalsium, Kalium, dan
Natrium dalam Biji, Daging dan Daun Labu Kuning ... 51 Lampiran 8 Perhitungan Statistik Kadar Kalium, Kalsium dan
Natrium dalam Daun Labu Kuning ... 53
Lampiran 9 Hasil Analisis Kadar Kalsium, Kalium, dan Natrium
Dalam Daun Labu Kuning . ... 58 Lampiran 10 Contoh Perhitungan Kadar Kalsium, Kalium dan Natrium
Dalam Daging Buah Labu Kuning ... 59 Lampiran 11 Perhitungan Statistik Kadar Kadar Kalium, Kalsium dan
Natrium Dalam Daging Buah Labu Kuning ... 61 Lampiran 12 Hasil Analisis Kadar Kalsium, Kalium, dan Natrium
Dalam Biji Labu Kuning ... 66 Lampiran 13 Contoh Perhitungan Kadar Kalsium, Kalium dan Natrium
Dalam Biji Labu Kuning ... 67 Lampiran 14 Perhitungan Statistik Kadar Kadar Kalium, Kalsium
Lampiran 15 Hasil Analisis Kadar Kalium pada Daging Buah
Setelah Penambahan Larutan Baku ... 75 Lampiran 16 Contoh Perhitungan Uji Perolehan Kembali Kadar
Kalium, Kalsium dan Natrium dalam Daging Buah
Labu Kuning ... 77 Lampiran 17 Perhitungan Simpangan Baku Relatif (RSD) Kadar
Kalium, Kalsium dan Natrium dalam Daging Buah
Labu Kuning ... 80 Lampiran 18 Perhitungan Batas Deteksi dan Batas Kuantitasi ... 83 Lampiran 19 Hasil Pengujian Beda Nilai Rata-Rata Kadar
PENETAPAN KADAR KALIUM, KALSIUM DAN NATRIUM PADA BIJI, DAGING BUAH DAN DAUN
LABU KUNING (Cucurbita moschata D.) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Labu kuning atau waluh (Cucurbita moschata) yang termasuk dalam suku Cucurbitaceae merupakan salah satu tanaman yang penting untuk dikonsumsi karena mempunyai kandungan gizi yang tinggi dan lengkap. Tanaman ini kaya akan vitamin A, B dan C, mengandung mineral seperti kalium, kalsium, natrium, besi, fosfor serta mengandung karbohidrat dan protein. Daun, daging buah dan biji labu kuning mengandung kalium, kalsium dan natrium yang berperan menurunkan risiko hipertensi. Oleh karena itu, penelitian ini bertujuan untuk mengetahui kadar kalium (K), kalsium (Ca) dan natrium (Na) pada daun, daging dan biji serta untuk mengetahui perbedaan kadar ketiga mineral tersebut.
Metode penelitian yang dilakukan secara deskriptif dengan pengambilan sampel biji, daging buah dan daun labu kuning (Cucurbita moschata) dan dilakukan destruksi kering. Penetapan kadar dilakukan dengan menggunakan alat spektrofotometer serapan atom untuk kalium pada panjang gelombang 766,5 nm, kalsium 422,7 nm dan natrium 589,0 nm menggunakan nyala udara-asetilen. Dilakukan juga uji nyala dengan kawat Ni/Cr dan uji kristal (kritalisasi) untuk mengidentifikasi mineral secara kualitatif.
Hasil penelitian menunjukkan kadar kalium dalam biji adalah (376,15 ± 12,05) mg/100 g, daging buah (394,86 ± 5,02) mg/100 g, dan daun (478,61 ± 1,53) mg/100 g, kadar kalsium dalam biji (6,54 ± 0,09) mg/100 g, daging buah (18,66 ± 0,10) mg/100 g dan daun yaitu (36,29 ± 0,18) mg/100 g dan kadar natrium dalam biji (17,92 ± 0,37) mg/100 g, daging buah (14,33 ± 4,03) mg/100 g dan daun adalah (20,90 ± 0,28) mg/100 g.
Dari hasil penelitian dapat disimpulkan bahwa kadar kalium, kalsium dan natrium pada biji, daging buah dan daun berbeda secara signifikan pada interval kepercayaan 95% dan kadar tertinggi adalah kadar kalium yang terdapat pada daun.
DETERMINATION OF POTASSIUM, CALCIUM AND SODIUM CONCENTRATION IN SEEDS, FLESHES AND LEAVES OF PUMPKIN (Cucurbita moschata D.) BY ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Pumpkin or squash (Cucurbita moshata) belonging to Cucurbitaceae family is one among the plants that important to consume. Pumpkin has been grown for the purpose of consumption as vegetable or as a medicine. The leaves, flesh and seed are very useful for a healthy life. Leaves, fleshes and seeds can decrease the hypertension risk. For that reason, the purpose of this research was to determine the potassium (K), calcium (Ca) and sodium (Na) level and the differences among that three minerals on seed, flesh and leaves.
The method that used in this research was descriptive, sampling from seeds, fleshes and leaves of pumpkin (Cucurbita moschata) using dry ashing. To determine the three minerals level were using atomic absorption spectrophotometry for potassium at a wavelength 766.5 nm, for calcium 422.7 nm and sodium 589.0 nm which using air-acetylene flame. Furthermore, the investigation for that three mineral was done by cristalization and flame test wtih Ni/Cr.
The result showed that the concentration of potassium in seeds was (376.15 ± 12.05) mg/100 g, fleshes was (394.86 ± 5.02) mg/100 g, and leaves (478.61 ± 1.53) mg/100 g, the level of calcium in seed was (6.54 ± 0.09) mg/100 g, fleshes was (18.66 ± 0.10) mg/100 g and leaves was (36.29 ± 0.18) mg/100 g, the concentration of sodium in seed was (17.92 ± 0.37) mg/100 g, fleshes was (14.33 ± 4.03) mg/100 g and leaves was (20.90 ± 0.28) mg/100 g.
Based on the result the levels of potassium, calcium and sodium in seeds, fleshes and leaves are significant difference with 95% confidence level and the highest level is potassium in leaves.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Labu kuning atau waluh adalah salah satu tanaman pangan yang mempunyai kandungan gizi yang tinggi dan lengkap. Labu kuning kaya dengan air, vitamin, antioksidan, dan karoten (provitamin A) yang memelihara tubuh dan mencegah penuaan dini. Labu kuning kaya akan vitamin A, B dan C, mineral seperti kalium, kalsium, natrium, besi, zinc, selenium serta mengandung karbohidrat. Labu kuning dapat dikonsumsi sebagai sayuran segar atau dimasak serta dibekukan atau dikalengkan (Fang, 2008).
Labu Kuning juga dikenal dari bijinya yang kaya akan lemak, protein, thiamin, niacin dan berbagai macam mineral (magnesium, zink, kalium) dan ketika diubah menjadi bentuk serbuk obat dapat berperan sebagai antiinflamsi, diuretik, dan emulgator yang dapat membantu dalam pengobatan demam, sakit telinga, inflamasi bagian perkemihan. Selain itu, biji labu ini sangat popular sebagai makanan ringan seperti kuaci (Henriques, et al., 2012; Amin, 2013).
hiperkalemia yang menyebabkan aritmia jantung, konsentrasi yang lebih tinggi lagi yang dapat menimbulkan henti jantung atau fibrilasi jantung (Fitriani, 2012).
Kekurangan asupan kalsium dalam tubuh menyebabkan abnormalitas tubuh manusia menyebabkan abnormalitas metabolism terutama pada usia dini, gangguan pertumbuhan seperti tulang kurang kuat, mudah bengkok,dan rapuh .Namun kelebihan kalsium juga dapat beresiko terhadap tubuh seperti menyebabkan batu ginjal, kanker prostat dan penumpukan kalsium di dalam pembuluh darah (Fitriani, 2012 ).
Natrium adalah kation utama dalam darah dan cairan ekstraselular yang mencakup 95% dari seluruh kation. Oleh karena itu, mineral ini sangat berperan dalam pengaturan cairan tubuh, termasuk tekanan darah dan keseimbangan asam-basa (Barasi, 2009).
Penetapan kadar kalsium, kalium dan natrium pada penelitian ini dilakukan dengan menggunakan spektrofotometri serapan atom, karena pelaksanaannya relatif cepat dan sederhana, batas deteksi kurang dari 1 ppm (Gandjar dan Rohman, 2007), bahan yang digunakan sedikit dan spesifik untuk setiap logam tanpa dilakukan pemisahan pendahuluan (Khopkar, 1985).
1.2Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut:
b. Apakah terdapat perbedaan kadar kalium, kalsium dan natrium pada biji daging buah dan daun labu kuning?
1.3Hipotesis
Hipotesis dalam penelitian ini adalah:
a. Biji, daging buah dan daun labu kuning mengandung kalium, kalsium dan natrium dalam jumlah tertentu.
b. Terdapat perbedaan kadar yang signifikan kalium, kalsium dan natrium pada biji, daging buah dan daun labu kuning.
1.4Tujuan Penelitian
a. Untuk menentukan kadar kalium, kalsium dan natrium yang terdapat pada biji, daging buah dan daun labu kuning.
b. Untuk mengetahui perbedaan kadar kalium, kalsium dan natrium antara biji, daging buah dan daun labu kuning.
1.5Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel
2.1.1 Tumbuhan Labu kuning
Tanaman labu kuning banyak dibudidayakan di Negara-negara Afrika, Amerika, India dan Cina, dapat tumbuh di dataran rendah maupun dataran tinggi. Labu kuning adalah salah satu tanaman yang banyak tumbuh di Indonesia. Penanamannya tidak sulit, baik pembibitannya, perawatannya, hasilnya cukup memberikan nilai ekonomis untuk masyarakat (Safitri, 2011).
Labu kuning ini termasuk dalam suku Cucurbitaceae. Labu kuning terdiri atas 5 spesies yaitu, Cucurbita ficifolia, Cucurbita maxima, Cucurbita mixta, Cucurbita moschata, dan Cucurbita pepo. Dari kelima spesies tersebut Cucurbita moschata adalah spesies yang paling banyak ditemui di iklim tropis (Safitri, 2011).
2.1.1.2 Sistematika Tumbuhan
Menurut Pandey (1969), sistematika tumbuhan labu kuning adalah sebagai berikut:
Kingdom : Plantae
Genus : Cucurbita
Spesies : Cucurbita moschata Duch
2.1.1.3 Morfologi tumbuhan
Tanaman Labu kuning berasal dari Benua Amerika yaitu Peru atau Meksiko dan termasuk kedalam family Cucurbitaceae. Tanaman labu kuning termasuk tanaman berbentuk semak yang tumbuh merambat atau menjalar ditanah dengan panjang batang dapat mencapai 12 m dan berbentuk segi lima (Smith, 2002).
Buah Labu kuning berbentuk bulat, berukuran besar dan berwarna kuning kecoklatan. Selain buahnya, daunnya berbentuk ginjal atau lekuk jantung berukuran besar yaitu 20 cm x 30 cm berwarna hijau gelap dengan permukaan daun dipenuhi bulu halus (Smith, 2002).
Bunganya berwarna kuning atau hijau muda berbentuk terompet dan dari bunga ini akan terbentuk buah labu kuning yang berwarna hijau saat masih muda dan berwarna kecoklatan saat sudah tua. Ukuran pertumbuhan labu kuning cepat sekali mencapai 350 gr per hari. Buahnya mempunyai berat rata-rata 2 – 3 kg. Labu kuning yang baik untuk dikonsumsi adalah sudah tua dengan tanda warna kulit yang cokelat atau cokelat kehijauan (Smith, 2002).
2.1.1.4 Kandungan kimia
Bagian tumbuhan yang sering digunakan adalah buah, biji, dan daun. Labu kuning mengandung Vitamin A, C, E, B1 (tiamin) β-karoten, α-karoten, zat besi, serat, kalium, kalsium, magnesium, natrium dan gula (Safitri, 2011).
Daun labu kuning dapat dijadikan sayur dan dibeberapa negara daun labu kuning digunakan untuk pengobatan lambung dan sakit kuning. Buahnya dimanfaatkan sebagai makanan bayi dan dijadikan sebagai bahan dasar pembuatan roti dan bijinya dapat digunakan kuwaci (Safitri, 2011).
2.2 Mineral
Mineral terdapat di dalam tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan. Keseimbangan mineral di dalam tubuh diperlukan untuk pengaturan kerja enzim, pemeliharaan keseimbangan asam basa, pemeliharaan kepekaan otot dan saraf terhadap rangsangan. Kalsium merupakan komponen pembentukan tulang dan gigi (Almatsier, 2001).
2.2.1 Kalsium
Tubuh kita mengandung lebih banyak kalsium daripada mineral lain. Diperkirakan 2% berat badan orang dewasa atau sekitar 1,0 – 1,4 kg terdiri dari kalsium. Meskipun pada bayi kalsium hanya sedikit (25 – 30 g), setelah usia 20 tahun secara normal akan terjadi penempatan sekitar 1.200 g kalsium dalam tubuhnya. Sebagian besar kalsium terkonsentrasi dalam tulang rawan dan gigi, sisanya terdapat dalam cairan tubuh dan jaringan lunak (Winarno, 1995).
Kalsium merupakan komponen penyusun tulang dan gigi tetapi juga memegang peranan penting yaitu transmisi impuls, relaksasi dan kontraksi, memberikan kekerasan dan ketahanan terhadap pengeroposan, bersama fosfor membentuk matriks tulang yang dipengaruhi oleh vitamin D (Budiyanto, 2001).
seperti tulang kurang kuat, mudah bengkok, dan rapuh. Pada orang dewasa dengan usia di atas 50 tahun, yang asupan kalsiumnya kurang dapat mengakibatkan tulang menjadi rapuh dan mudah patah yang dikenal sebagai osteoporosis ( Almatsier, 2001).
Namun, bila kelebihan kalsium juga dapat beresiko terhadap tubuh seperti menyebabkan batu ginjal, kanker prostat, sulit buang air besar (konstipasi) dan penumpukan kalsium di pembuluh darah. Kalsium dieksresikan lewat urin serta feses dan untuk mencegah kehilangan ini diperlukan kalsium melalui makanan. Kalsium tambahan diperlukan dalam keadaan tertentu seperti pada masa pertumbuhan mulai dari anak-anak hingga usia remaja,dan pada saat hamil untuk memenuhi kebutuhan janin. (Budiyanto, 2001; Winarno, 1995).
2.2.2 Kalium
Seperti halnya natrium, kalium mudah sekali diserap tubuh; diperkirakan 90% dari yang dicerna akan diserap dalam usus kecil. Kekurangan kalium jarang sekali disebabkan kekurangan kalium dari ransum. Gejala kekurangan kalium biasanya pelunakan otot. Karena itu diperlukan konsumsi kalium yang tinggi yaitu dengan perbandingan nitrogen 6:1 (pada badan normal hanya memerlukan perbandingan 4:1). Dalam keadaan lapar gizi, banyak sekali kalium hilang dari otot. Dalam waktu puasa terjadi kekurangan kalium dan terjadi toleransi glukosa yang abnormal (Winarno, 1995).
2.2.3 Natrium
Natrium adalah kation utama dalam darah dan cairan ekstraseluler, yang mencakup 95% dari seluruh kation. Oleh karena itu, mineral ini sangat berperan dalam pengaturan cairan tubuh,termasuk tekanan darah dan keseimbangan asam-basa. Perubahan kadar natrium dapat mempengaruhi tekanan darah, tetapi tidak dengan sendirinya menyebabkan tekanan darah tinggi. Meskipun demikian, terdapat cukup banyak bukti yang mendukung anggapan bahwa mengurangi asupan natrium dapat menurunkan tekanan darah (Barasi, 2009).
Natrium harus terdapat dalam jumlah yang cukup pada makanan agar kecukupan Na ini dapat terjamin tubuh sendiri dapat mengatur kadar Na tubuh dan mengeluarkan kelebihan Na melalui urine akan tetapi pada penyakit tertentu Na tetap bertahan dalam tubuh dengan jumlah yang berlebihan, pada keadaan ini diperlukan pembatasan masukan Na. Ekskresi Na terutama terjadi lewat urine dan air penuh dalam keadaan normal kandungan Na tubuh dipertahankan oleh sinyal pada kadar yang selalu tetap (Budiyanto, 2001).
2.3 Spektroskopi Serapan Atom
Spektroskopi serapan atom digunakan untuk analsis kunatitatif unsur -unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok untuk analisis kelumit logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya sedikit. Dalam garis besarnya prinsip spektroskopi serapan atom sama saja dengan spektrofotometri sinar tampak dan ultraviolet. Perbedaan terletak pada bentuk spektrum, cara pengerjaan sampel peralatannya (Ganjar dan Rohman, 2007).
mana pada transisi elektronik suatu atom bersifat spesifik. Dengan menyerap suatu energi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan ke tingkat eksitasi. misalkan, suatu unsur Na mempunyai konfigurasi elektron 1s2, 2s2, 2p6, dan 3s1. Tingkat dasar untuk elektron valensi 3s1 ini dapat mengalami eksitasi ke tingkat 3p dengan energi 2,2 eV atau ke tingkat 4p dengan energi 3,6 eV yang masing-masing bersesuaian dengan panjang gelombang 589,3 nm dan 330, 2 nm. Keberhasilan analisis dengan SSA ini tergantung pada proses eksitasi dan cara memperoleh garis resonansi yang tepat. Temperatur nyala harus sangat tinggi (Gandjar dan Rohman, 2007).
2.3.1 Instrumentasi SSA
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca bertutup yang mengandung suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon) dengan tekanan rendah (10-15 torr). Neon biasanya lebih disukai karena memberikan intensitas pancaran lampu yang lebih rendah. Salah satu kelemahan penggunaan lampu katoda berongga adalah satu lampu digunakan untuk satu unsur, akan tetapi saat ini telah banyak dijumpai suatu lampu katoda berongga kombinasi; yakni satu lampu dilapisi dengan beberapa unsur sehingga dapat digunakan untuk analisis beberapa unsur sekaligus.
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu : dengan nyala (flame) dan dengan tanpa nyala (flameless) (Gandjar dan Rohman, 2007).
a. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Pada cara spektrofotometri emisi atom, nyaa ini berfungsi untuk mengeksitasikan atom dari tingkat dasar ke tingkat yang lebih tinggi. Sumber nyala yang paling banyak digunakan adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi (Ganjar dan Rohman, 2007).
b. Tanpa nyala (flameless)
Teknik atomisasi dengan nyala dinilai kurang peka, oleh karena itu muncullah suatu teknik atomisasi yang baru yakni atomisasi tanpa nyala.
Sistem pemanasan dengan tanpa nyala ini dapat melalui 3 tahap yaitu : pengeringan (drying) yang membutuhkan suhu yang relative rendah; pengabuan (ashing) yang membutuhkan suhu yang lebih tinggi karena menghilangkan matriks kimia dengan mekanisme volatilasi atau pirolisis; dan pengatoman (atomizing). Pada umumnya waktu dan suhu pemanasan tanpa nyala dilakukan dengan cara terprogram (Gandjar dan Rohman, 2007).
3. Monokromator
dalam monokromator juga terdapat suatu alat yang digunakan untuk memisahkan radiasi resonansi dan kontinyu yang disebut chopper (Gandjar dan Rohman, 2007).
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman. Biasanya digunakan tabung penggandaan foton (photomultiplier tube). Ada 2 cara yang dapat digunakan dalam sistem deteksi yaitu: (a) yang memberikan respon terhadap radiasi resonansi dan radiasi kontinyu; (b) hanya memberikan respon terhadap radiasi resonansi (Gandjar dan Rohman, 2007).
5. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai sistem pencatatan hasil. Hasil pembacaan dapat berupa angka atau berupa kurva dari suatu recorder yang menggambarkan absorbansi atau intensitas emisi.
Menurut Gandjar dan Rohman (2007), yang dimaksud dengan gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel . Gangguan yang dapat terjadi yaitu:
1. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala.
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi di dalam nyala.
3. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di dalam nyala.
Adanya gangguan-gangguan di atas dapat diatasi dengan menggunakan cara-cara sebagai berikut :
a. Penggunaan nyala/suhu atomisasi yang lebih tinggi
Suhu tinggi sering menyebabkan pembentukan atom-atom gas bebas, contoh alumunium oksida lebih mudah berdisosiasi di dalam nyala asetilen-nitrogen oksida daripada di dalam nyala asetilen-udara. Gangguan kalsium-alumunium yang bersal dari pembentukan kalsium aluminat juga dapat dihindari dengan bekerja pada suhu yang lebih tinggi daripada nyala asetilen-nitrogen oksida (Hendayana dkk, 1994).
b. Penambahan senyawa penyangga.
Suhu nyala asetilen-udara dapat menyebabkan ionisasi unsur seperti unsur-unsur logam alkali: kalsium, stronsium, dan barium. Ionisasi unsur yang ditentukan dapat dikurangi dengan zat penahan ionisasi; biasanya berupa larutan yang mengandung kation dengan potensial ionisasi lebih rendah daripada analit (Hendayana dkk, 1994).
Gangguan utama dalam absorpsi atom adalah efek matriks yang mempengaruhi proses pengatoman. Baik jauhnya disosiasi menjadi atom-atom pada suatu temperature tertentu laju proses bergantung sekali pada komposisi keseluruhan dari sampel (Gandjar dan Rohman, 2007).
2.4 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Menurut Harmita (2004), beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan dapat ditentukan dengan dua cara yaitu metode simulasi dan metode penambahan baku.
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya) (Harmita, 2004).
konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan dalam sampel dapat ditemukan kembali (Harmita, 2004). Menurut Miller (2005), parameter ini memenuhi syarat jika nilainya berada pada rentang 80 - 120%.
b. Keseksamaan (presisi)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen (Harmita, 2004).
Nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per billion (ppb) RSDnya adalah tidak lebih dari 32% (Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
diterima Secara statistik linearitas dari kurva kalibrasi dinyatakan dalam koefisien korelasi (r). Koefisien korelasi yang lebih besar dari 0, 99 menyatakan adanya hubungan yang linear (Harmita, 2004; Watson, 2005).
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara Medan pada bulan Mei 2014 – Agustus 2014.
3.2 Bahan–Bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah biji, daging buah dan daun labu kuning yang diambil secara purposif di Desa Samura, Kecamatan Kabanjahe, Kabupaten Karo, Sumatera Utara.
3.2.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini kecuali akua demineralisata, berkualitas pro analisa keluaran E. Merck yaitu asam nitrat (65% b/v), asam sulfat (96% v/v), asam pikrat, etanol (96% v/v), asam klorida (37% v/v), larutan baku kalium 1000 µg/ml, larutan baku kalsium 1000 µg/ml dan larutan baku natrium 1000 µg/ml.
3.3 Alat–Alat
3.4 Identifikasi Sampel
Identifikasi sampel dilakukan oleh bagian Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi-LIPI Bogor.
3.5 Pembuatan Pereaksi
3.5.1 Larutan HNO3 (1:1)
Sebanyak 500 ml larutan HNO3 (65% b/v) diencerkan dengan 500 ml
akua demineralisata (Helrich, 1990).
3.5.2 Larutan H2SO4 1 N
Sebanyak 3 ml larutan H2SO4 (96% v/v) diencerkan dengan akuades
hingga 100 ml (Ditjen POM, 1979).
3.5.3 Larutan HCL 2N
Sebanyak 17 ml asam klorida pekat (37% v/v) diencerkan dengan air suling sampai 100 ml (Depkes, 1978).
3.5.4 Larutan Asam Pikrat 1% b/v
Sebanyak 1 gram asam pikrat dilarutkan dalam akuabides hingga 100 ml (Ditjen POM, 1979).
3.6 Prosedur Penelitian
3.6.1 Pengambilan Sampel
3.6.2 Penyiapan Sampel
3.6.2.1 Daun Muda Labu Kuning
Daun yang digunakan adalah daun muda (pucuk daun) yang berwarna hijau muda yang dicuci bersih dengan air mengalir, dirajang, ditiriskan hingga air cuciannya kering, kemudian diblender sampai halus dan ditimbang sebanyak ± 1000 gram.
3.6.2.2 Daging Buah Labu Kuning
Daging buah labu kuning dicuci dengan air mengalir, ditiriskan hingga air cuciannya kering kemudian dirajang dan diparut dengan parutan stainless steel, setelah itu ditimbang ± 1000 gram.
3.6.2.3 Biji Labu Kuning
Biji labu kuning dicuci bersih dengan air mengalir agar lendirnya hilang, ditiriskan hingga air cuciannya kering lalu diblender sampai halus setelah itu ditimbang ± 1000 gram.
3.6.3 Proses Destruksi Kering
Sampel yang telah dihaluskan ditimbang seksama sebanyak 25 gram dalam krus porselen, diarangkan di atas hot plate, lalu diabukan dalam tanur dengan temperatur awal 100℃ dan perlahan–lahan temperatur dinaikkan hingga suhu 500℃ dengan interval 25℃ setiap 5 menit. Pengabuan dilakukan selama 60 jam (dihitung saat suhu sudah 500℃), lalu setelah suhu tanur ±27℃, krus porselen dikeluarkan dan dibiarkan hingga dingin pada desikator. Abu ditambahkan 5 ml HNO3 (1:1), kemudian diuapkan pada hot plate sampai
interval 25℃ setiap 5 menit. Pengabuan dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator (Horwitz, 2000).
3.6.4 Pembuatan Larutan Sampel
Sampel hasil destruksi dilarutkan dalam 5 ml HNO3 (1:1), lalu
dipindahkan ke dalam labu tentukur 50 ml, dibilas krus porselen dengan 10 ml akua demineralisata sebanyak tiga kali dan dicukupkan dengan akua demineralisata hingga garis tanda. Kemudian disaring dengan kertas saring Whatman No. 42,5 ml filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian filtrat selanjutnya ditampung ke dalam botol (Horwitz, 2000). Larutan ini digunakan untuk analisis kualitatif dan kuantitatif terhadap logam kalsium, kalium dan natrium yang terkandung di dalamnya.
3.6.5 Analisis Kualitatif
3.6.5.1 Kalsium
Uji dengan Reaksi Nyala
Kawat Ni/Cr dibersihkan dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat kalsium akan terbentuk warna merah bata pada nyala tersebut (Vogel, 1979).
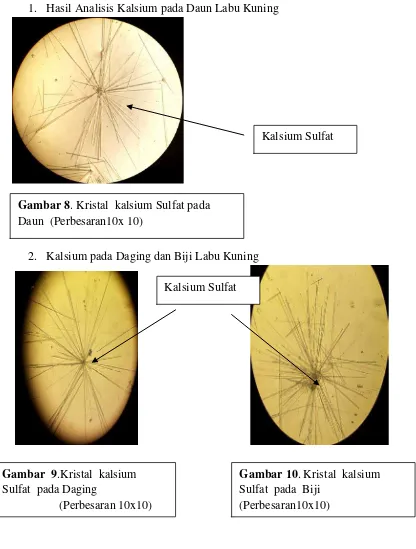
Uji Kristal Kalsium dengan Asam Sulfat 1 N
3.6.5.2 Kalium
Uji dengan Reaksi Nyala
Kawat Ni/Cr dibersihkan dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian kawat dicelupkan ke dalam sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat kalium akan terbentuk warna ungu pada nyala bunsen (Vogel, 1979).
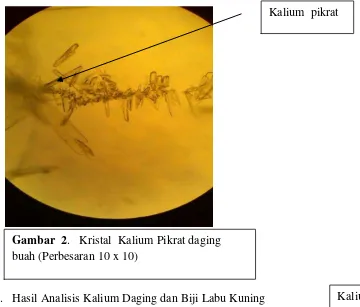
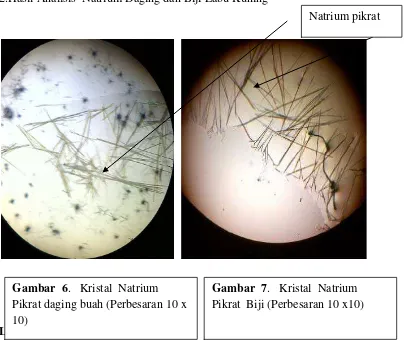
Uji Kristal Kalium dengan Asam pikrat
Larutan zat diteteskan 1-2 tetes pada object glass kemudia ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati dibawah mikroskop. Jika terdapat kalium, akan terlihat kristal berbentuk jarum–jarum besar (Vogel, 1979).
3.6.5.3 Natrium
Uji dengan Reaksi Nyala
Kawat Ni/Cr dicelupkan ke dalam HCl pekat kemudian dipijar pada nyala bunsen hingga tidak memberikan warna khusus pada nyala bunsen Kemudian, kawat dicelupkan ke dalam sampel dan dipijar. Jika terdapat natrium, akan dihasilkan warna kuning keemasan pada nyala bunsen (Vogel, 1979).
Uji Kristal Natrium dengan Asam Pikrat
3.6.6 Analisis Kuantitatif
3.6.6.1 Kalium
Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalsium (1000 µg/ml) sebanyak 2 ml dimasukkan kedalam labu tentukur 100 ml lalu diencerkan dengan akua demineralisata hingga garis tanda. Dari larutan tersebut (20 µg/ml) dipipet masing-masing 5,0 ml; 10,0 ml; 15,0 ml; 20,0 ml; dan 25,0 ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akua demineralisata hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 2 µg/ml; 4 µg/ml; 6 µg/ml; 8 µg/ml; dan 10 µg/ml, lalu dilakukan pengukuran pada panjang gelombang 766,5 nm dengan tipe nyala udara-asetilen.
Penetapan Kadar Kalium dalam Sampel
Larutan sampel hasil dekstruksi dipipet sebanyak 0,1 ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akua demineralisata hingga garis tanda (Faktor pengenceran = 50/0,1 = 500 kali). Larutan diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 766,5 nm dengan tipe nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel dihitung berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.6.6.2 Kalsium
Pembuatan Kurva Kalibrasi Kalsium
hingga garis tanda. Dari larutan tersebut (20 µg/ml) dipipet masing-masing 5,0 ml; 10 ml; 15 ml; 20 ml; dan 25 ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akua demineralisata hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 2,0 µg/ml; 4,0 µg/ml; 6,0 µg/ml; 8,0 µg/ml; dan 10,0 µg/ml, lalu dilakukan pengukuran pada panjang gelombang 422,7 nm dengan tipe nyala udara-asetilen.
Penetapan Kadar Kalsium dalam Sampel
Larutan sampel hasil destruksi dipipet sebanyak 1 ml dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan dengan akua demineralisata hingga garis tanda (Faktor pengenceran = 50/1 = 50 kali). Lalu diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm dengan tipe nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel dihitung berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.6.6.3 Natrium
Pembuatan Kurva Kalibrasi Natrium
µg/ml; dan 1 µg/ml, lalu dilakukan pengukuran pada panjang gelombang 589,0 nm dengan tipe nyala udara-asetilen.
Penetapan Kadar Natrium dalam Sampel
Larutan sampel hasil dekstruksi dipipet sebanyak 0,5 ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan akua demineralisata hingga garis tanda (faktor pengenceran = 50/0,5 = 250 kali). Larutan diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 589,0 nm dengan tipe nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku natrium. Konsentrasi natrium dalam sampel dihitung berdasarkan persamaan garis regresi dari kurva kalibrasi.
Menurut Gandjar dan Rohman (2007), kadar logam kalsium, kalium dan natrium dalam sampel dapat dihitung dengan cara sebagai berikut:
(g) Sampel Berat
n pengencera Faktor
x (ml) Volume x
(µ g/ml) i
Konsentras (µ g/g)
Logam
Kadar =
3.6.7 Analisis Data Secara Statistik
3.6.7.1 Penolakan Hasil Pengamatan
Menurut Sudjana (2005), kadar kalsium, kalium dan natrium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis dengan metode standar deviasi dengan rumus sebagai berikut:
SD =
(
)
1 -n
X -Xi 2
Keterangan : Xi = Kadar sampel
−
X = Kadar rata-rata sampel n = Jumlah ulangan Untuk mencari t hitung digunakan rumus:
t hitung =
�Xi−X �
n
SD
/
dan untuk menentukan kadar mineral di dalam sampel dengan interval kepercayaan 99%, α = 0.01, dk = n-1, dapat digunakan rumus:
Kadar Mineral : µ = X ± (t(α/2, dk) x SD / √n ) Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = Interval kepercayaan
n = Jumlah ulangan
3.6.8 Pengujian Beda Nilai Rata-Rata Antar Sampel
Untuk mengetahui perbedaan nilai rata-rata kadar kalium, kalsium dan natrium antar sampel dilakukan analisis statistik menggunakan Statistical Product Services Solution (SPSS) uji ANOVA dengan taraf kepercayaan 95%, dengan menggunakan uji tambahan yaitu uji Tukey.
3.6.9 Uji Perolehan Kembali (Recovery)
2005). Larutan baku yang ditambahkan yaitu 10ml larutan baku kalium (konsentrasi 1000 µg/ml), 0,5 ml larutan baku kalsium (konsentrasi 1000 µg/ml) dan 0,5 ml larutan baku natrium (konsentrasi 1000 µg/ml) .
Daging buah labu kuning yang telah diparut lalu ditimbang secara seksama sebanyak 25 gram di dalam krus porselen, lalu ditambahkan 10 ml larutan baku kalium (konsentrasi 1000 µg/ml), 0,5 ml larutan baku kalsium (konsentrasi 1000 µg/ml) dan 0,5 ml larutan baku natrium (konsentrasi 1000 µg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali= CF- CA x 100%
Keterangan :
CA = Kadar logam dalam sampel sebelum penambahan baku
CF = Kadar logam dalam sampel setelah penambahan baku
C*A = Kadar larutan baku yang ditambahkan
3.6.10 Simpangan Baku Relatif
Menurut Harmita (2004), keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan.
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah:
RSD = ×100%
X SD
Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.6.11 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (
X
SY ) =
(
)
2 2
− −
∑
nYi Y
Batas deteksi (LOD) =
slope X SY x
3
Batas kuantitasi (LOQ) =
slope X SY x
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Sampel
Hasil identifikasi sampel yang dilakukan oleh bagian Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi LIPI-Bogor terhadap tumbuhan labu kuning adalah jenis Cucurbita moschata D., suku Cucurbitaceae. Hasil identifikasi sampel dapat dilihat pada lampiran 20 halaman 92.
4.2 Analisis Kualitatif
[image:45.595.115.512.496.672.2]Analisis kualitatif dilakukan untuk mengetahui ada atau tidaknya ion-ion kalium, kalsium dan natrium dalam sampel. Data dapat dilihat pada Tabel 4.1 dan Lampiran 22, halaman 94 - 96.
Tabel 4.1 Hasil Analisis Kualitatif dalam Biji, Daging dan Daun Labu Kuning
No. Logam yang
dianalisis Pereaksi Hasil Reaksi Hasil
1. K
Uji Nyala Ungu +
Asam pikrat 1% b/v Kristal Jarum
Panjang +
2. Ca
Uji Nyala Merah Bata +
Asam sulfat 1N +
etanol 96% Kristal jarum +
3. Na Uji Nyala Kuning keemasan +
Asam pikrat 1% b/v Kristal jarum halus + Keterangan :
Tabel 4.1 menunjukkan bahwa larutan sampel yang diperiksa mengandung logam kalium, kalsium dan natrium. Sampel positif mengandung logam kalium karena memberikan warna nyala ungu saat dibakar mengunakan kawat Ni/Cr dan menghasilkan kristal jarum panjang dengan penambahan asam pikrat 1% b/v. Positif mengandung logam kalsium karena memberikan warna nyala merah bata saat dibakar mengunakan kawat Ni/Cr serta dengan penambahan asam pikrat 1N memhasilkan Kristal jarum dan mengandung logam natrium karena menghasilkan kristal berupa jarum halus dengan penambahan asam pikrat 1% b/v serta memberikan warna nyala kuning keemasan saat dibakar mengunakan kawat Ni/Cr. Berdasarkan hasil reaksi warna nyala maupun reaksi kristal dari masing-masing ketiga logam tersebut membuktikan larutan sampel mengandung logam kalium, kalsium dan natrium. Hal ini sejalan dengan logam kalium yang dianalisis secara spektrofotometri serapan atom pada panjang gelombang 766,5 nm, kalsium pada panjang gelombang 422,7 nm dan natrium pada panjang gelombang 589 nm.
4.3 Analisis Kuantitatif
4.3.1 Kurva kalibrasi Kalsium, Kalium dan Natrium
Kurva kalibrasi larutan baku kalsium, kalium dan natrium dapat dilihat pada Gambar 4.1 - 4.3.
Gambar 4.1 Kurva Kalibrasi Kalium
[image:47.595.115.497.124.263.2]
Gambar 4.2 Kurva Kalibrasi Kalsium
[image:47.595.116.494.397.667.2]
Dari gambar 4.1, 4.2, 4.3 di atas dapat dilihat bahwa kurva kalibrasi kalium, kalsium dan natrium menunjukkan ada hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalium sebesar 0,9993, kalsium sebesar 0,9995 dan natrium sebesar 0,9992. Nilai r ≥ 0,95 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (Konsentrasi) dan Y (Absorbansi) (Watson, 2005). Perhitungan hasil pengukuran absorbansi larutan baku kalsium, kalium dan natrium dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 3 sampai dengan Lampiran 5, halaman 45 - 49 .
4.3.2 Kadar Kalium, Kalsium dan Natrium pada Biji, Daging dan Daun Labu Kuning
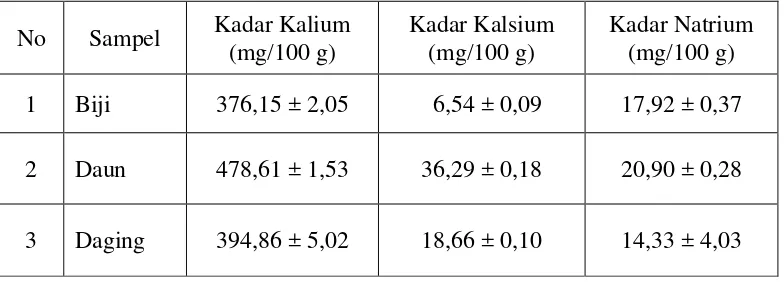
Tabel 4.2 Hasil Analisis Kadar Kalsium, Kalium dan Natrium dalam Biji, Daun dan Daging Labu Kuning
No Sampel Kadar Kalium (mg/100 g)
Kadar Kalsium (mg/100 g)
Kadar Natrium (mg/100 g) 1 Biji 376,15 ± 2,05 6,54 ± 0,09 17,92 ± 0,37 2 Daun 478,61 ± 1,53 36,29 ± 0,18 20,90 ± 0,28
3 Daging 394,86 ± 5,02 18,66 ± 0,10 14,33 ± 4,03
Dari Tabel 4.2 dapat diperoleh kesimpulan bahwa biji, daun dan daging mengandung mineral kalium, kalsium dan natrium. Dari ketiga mineral tersebut kalium memiliki kadar mineral yang paling tinggi dibandingkan dengan kalsium dan natrium. Dari tabel juga dapat dilihat terdapat perbedaan kadar mineral kalium, kalsium dan natrium pada biji, daging buah dan labu kuning yang berbeda secara signifikan. Kadar kalium dalam daun lebih tinggi dibandingkan kadar kalium yang terkandung dalam daging dan biji. Kadar kalsium dalam daun juga lebih tinggi dibanding dengan yang terkandung pada biji dan daging buah. Kadar natrium dalam daun paling tinggi jika dibandingkan dengan kadar natrium di biji dan daging buah.
[image:49.595.114.506.126.267.2]Sedangkan kadar kalium dan kalsium yang paling rendah ditemukan pada biji hal ini terjadi karena biji tidak dikupas terlebih dahulu dari kulit luarnya. Di mana, kulit luar dari biji labu kuning sedikit mengandung mineral seperti kalium, kalsium dan natrium. Sedangkan kadar natrium yang paling rendah ditemukan pada daging buah labu kuning. Jika dilihat dari hasil analisis kadar kalium maka daun paling berpotensi untuk dapat menurunkan risiko hipertensi dibandingkan dengan daging buah dan biji.
Dalam penelitian ini tipe nyala yang digunakan untuk ketiga logam tersebut adalah udara – asetilen. Suhu yang dicapai oleh nyala tergantung pada gas-gas yang digunakan, misalnya udara – asetilen 2200oC, dinitrogen oksida – asetilen sebesar 3000oC sedangkan udara – propana 1800oC. Biasanya untuk logam kalium dan natrium nyala yang digunakan adalah udara – propana sedangkan untuk kalsium adalah dinitrogen oksida – asetilen namun karena keterbatasan alat maka ketiga logam tersebut diukur dengan tipe nyala udara – asetilen (Gandjar dan Rohman, 2007).
Kalsium dalam cairan ekstrasel dan intrasel memegang peranan penting dalam mengatur fungsi sel, seperti transmisi saraf, kontraksi otot, penggumpalan darah dan menjaga permeabilitas membran sel. Fungsi kalsium dapat meningkatkan fungsi transport membran dan transmisi ion melalui membran organel sel, di mana kebutuhan maksimum perharinya 2500 mg (Almatsier, 2001).
diatur oleh kalium guna menjaga cairan tidak keluar dari sel. Bila jumlah natrium di dalam sel meningkat secara berlebihan maka air akan masuk kedalam sel, akibatnya sel akan membengkak. Inilah yang menyebabkan terjadinya pembengkakan/edema dalam jaringan tubuh (Almatsier, 2001).
Sebanyak 95% natrium tubuh berada di dalam cairan ekstraselular. Bersama natrium, kalium memegang peranan dalam pemeliharaan keseimbangan cairan dan elektrolit serta keseimbangan asam basa. Bersama kalsium, kalium berperan dalam transmisi saraf dan relaksasi otot. Kalium berperan dalam pertumbuhan sel. Tekanan darah normal memerlukan perbandingan antara natrium dan kalium yang sesuai di dalam tubuh. (Almatsier, 2011).
4.3.3 Analisis Data Secara Statistik
Dilakukan juga uji statistik One Way Annova untuk mengetahui apakah kadar kalium, kalsium dan natrium yang terdapat pada daun, daging dan biji labu kuning perbedaan secara signifikan. Dari Tabel hasil analisis dapat dilihat bahwa signifikansi < 0,05 sehingga Ho ditolak dan H1diterima, hal ini berarti terdapat perbedaan yang signifikan rata – rata kadar kalium, kalsium dan natrium pada biji, daging buah dan dan daun labu kuning. Hasil uji statistik dapat dilihat pada Lampiran 19 halaman 86 - 91.
4.3.4 Uji Perolehan Kembali (Recovery)
Tabel 4.3 Persen Uji Perolehan Kembali (recovery) kadar kalium, kalsium dan natrium
Mineral yang
dianalisis Recovery (%) Rentang % recovery
K 111,92
80-120
Ca 114,20
Na 106,69
Dari Tabel 4.3 di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) secara berurutan adalah mineral kalium 111,92%, untuk kandungan kalsium 114,20% dan untuk kandungan natrium 106,69%. Persen recovery tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kalsium, kalium dan natrium dalam sampel. Hasil uji perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80-120% (Miller, 2005). Hasil uji perolehan kembali (recovery) kadar kalsium, kalium dan natrium setelah penambahan masing-masing larutan baku dan contoh perhitungan dapat dilihat pada Lampiran 17, halaman 80 - 82.
4.3.5 Batas Deteksi dan Batas Kuantitasi
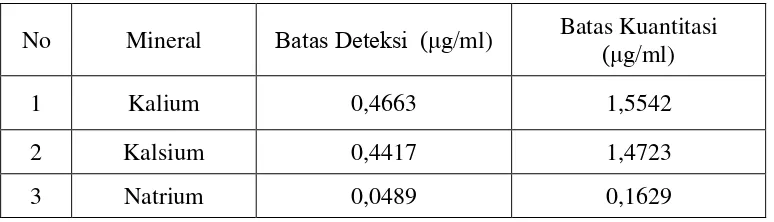
Tabel 4.4 Batas Deteksi dan Batas Kuantitasi
No Mineral Batas Deteksi (μg/ml) Batas Kuantitasi (μg/ml)
1 Kalium 0,4663 1,5542
2 Kalsium 0,4417 1,4723
3 Natrium 0,0489 0,1629
Dari Tabel 4.4 di atas dapat dilihat bahwa batas deteksi untuk pengukuran kalium, kalsium dan natrium masing-masing sebesar 0,4663 μg/ml, 0,4417 μg/ml dan 0,0489 μg/ml, sedangkan batas kuantitasinya sebesar 1,5542 μg/ml, 1,4723 μg/ml dan 0,1629 μg/ml.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi. Perhitungan batas deteksi dan batas kuantitasi dapat dilihat pada Lampiran 18,
halaman 83 - 85.
4.3.6 Simpangan Baku Relatif
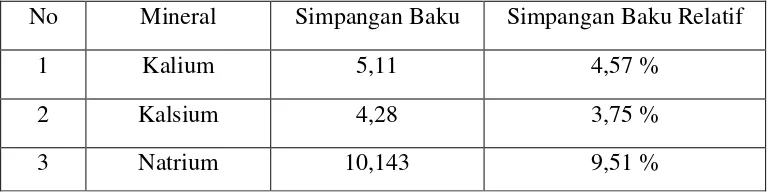
Tabel 4.5 Nilai simpangan baku dan simpangan baku relatif kalium, kalsium dan natrium
No Mineral Simpangan Baku Simpangan Baku Relatif
1 Kalium 5,11 4,57 %
2 Kalsium 4,28 3,75 %
3 Natrium 10,143 9,51 %
Dari Tabel 4.5 tersebut dapat dilihat simpangan baku relatif sebesar 4,57% untuk mineral kalsium; 3,75% untuk mineral natrium 9,51% .Simpangan baku kalium 5,11, kalsium 4,28 dan natrium 10,143.
Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per billion (ppb) RSDnya adalah tidak lebih dari 32%.
[image:54.595.113.499.126.224.2]BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan bahwa:
1. Biji, daging labu dan daun kuning memiliki kandungan mineral kalium, kalsium dan natrium.
Berdasarkan hasil analisis labu kuning secara spektrofotometri serapan atom menunjukkan bahwa kadar kalium padabiji (376,15 ± 2,05) mg/100 g, daging buah (395,65 ± 5,03) mg/100 g dan daun (478,61 ± 1,53 ) mg/100 g. Kadar kalsium pada biji (6,54 ± 0,087) mg/100 g, daging buah (18,66 ± 0,10) mg/100 g dan daun (36,29 ± 0,18) mg/100 g. Kadar natrium pada biji (17,92 ± 0,37) mg/100 g, daging buah (14,33 ± 4,03) mg/100 g dan daun (20,90 ± 0,28) mg/100 g.
2. Hasil uji statistik menunjukkan terdapat perbedaan yang signifikan antara kadar kalium, kalsium dan natrium yang terdapat pada biji, daun dan daging labu kuning dengan tingkat kepercayaan 95%.
5.2 Saran
1. Disarankan kepada masyarakat untuk mengkonsumsi daun, daging dan biji labu kuning karena mengandung mineral yang dibutuhkan tubuh.
DAFTAR PUSTAKA
Almatsier, S. (2001). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 228 - 238, 241-243.
Amin, T. (2013). Research Article Cucurbita Mixta (Pumpkin) seeds- A General Overview On Their Health Benefits. International Journal of Recent Scientific Research. 6(4): 846-854.
Barasi, M. (2009). At a Glance: Ilmu Gizi. Penerjemah: Hermin. Jakarta: Penerbit Erlangga. Hal. 52-53.
Bassett, J., Denney, R. C., Jeffery, G. H., dan Mendham, J. (1994). Vogel’s Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. Penerjemah: Hadiyana Pudjaatmaka dan L. Setiono. (1994). Buku Ajar Vogel Kimia Analisis Kuantitatif Anorganik. Edisi Keempat. Jakarta: Penerbit Buku Kedokteran EGC. Hal. 557-559.
Budiarto, E. (2004). Metodologi Penelitian Kedokteran. Jakarta: Penerbit Buku Kedokteran EGC. Hal. 46.
Budiyanto, M.A.K. (2001). Dasar-Dasar Ilmu Gizi. Edisi Kedua. Cetakan I. Malang: UMM-Press. Hal. 59.
Depkes RI. (1978). Materi Medika Indonesia. Jilid 2. Jakarta: Departemen Kesehatan Republik Indonesia. Hal. 150.
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Hal. 744.
Fang, S.E. (2008). Physico-chemical and Organoleptic Evaluations Of Wheat Bread Substituted with Different Percentage Of Pumpkin Flour (Cucurbita moschata). Journal of Science. 1(3): 112 – 134.
Fitriani, N.L.C. (2012). Penentuan Kadar Kalium (K) dan Kalsium (Ca) Dalam Labu Siam (Sechium edule) Serta Pengaruh Tempat Tumbuhnya. Jurnal Akademia Kimia. 1(4): 174 - 180.
Gandjar, I. G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan IV. Yogyakarta: Pustaka Pelajar. Hal. 298, 305-312, 319.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3). 117 – 122, 127 - 130.
Henriques, F, Raquel G. dan Maria J. B. (2012). Chemical Properties of Pumpkin Dried by Different Methods. Croation Journal of Food Technology, Biotechnology and Nutrition. 7(1-2): 98-105.
Horwitz, K. (2000). Official Methods of The Association of Official Analytical Chemist. Edisi Ketujuhbelas. Arlington: AOAC International. Hal. 42. Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: A.
Saptorahardjo. (2008). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Hal. 283, 298.
Miller, J.H.McB. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Hal. 171.
Pandey, B.P. (1969). Taxonomy of Angiosperms. New Delhi: S.Chand and Company Ltd. Hal.171.
Safitri, R. (2011). Penggunaan Buah Labu Kuning (Cucurbita moschata Durch) Dalam Sediaan Krim Pelembab. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara.
Smith, Y.E. (2002). Terapi Sayuran. Jakarta: Prestasi Pustaka. Hal. 153 – 154. Sudjana. (2005). Metode Statistika. Edisi VI. Bandung: Tarsito. Hal. 93, 168,
239.
Vogel, A.I. (1979). Textbook of Macro and Semimicro Qualitative Inorganic Analysis. Edisi Kelima. Bagian I. Penerjemah: Setiono dan Hadyana Pudjaatmaka. (1990). Analisis Anorganik Kualitatif Makro dan Semimikro. Jakarta: PT. Kalman Media Pustaka. Hal. 262, 263, 301, 307.
Watson, G. (2005). Pharmaceutical Analysis. Penerjemah: Winny R, Syarief. (2010). Analisis Farmasi. Jakarta: Penerbit Buku Kedokteran EGC.
Hal. 18.
Winarno, F.G. (1995). Kimia Pangan dan Gizi. Jakarta: PT. Gramedia. Hal. 345.
Yamaguchi, M., dan Rubatzky, V.E. (2007). Sayuran Dunia 2: Prinsip, Produksi dan Nilai Nutrisi. Jakarta: Agromedia Pustaka. Hal. 54, 76. Zaitun. (2012). Pemanfaatan Buah Labu Kuning Sebagai Bahan Dasar dalam
Lampiran 1. Bagan Alir Destruksi Kering
`
Buah Labu Kuning
Ditimbang sebanyak 25 gram di atas krus Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan–lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering
Hasil
Dilakukan selama 62 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dipotong melintang
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dipisahkan biji dan dagingnya
Sampel yang telah dihaluskan
Biji Daging buah
Diiuci bersih dengan air mengalir
Diblender Biji
Lampiran 1. (Lanjutan)
Ditimbang sebanyak 25 gram di atas krus Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan–lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering
Hasil
Dilakukan selama 32 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Sampel yang telah dihaluskan Daging buah
Dikupas kulitnya
Dicuci bersih dengan air mengalir
Dikeringkan dengan cara diangin-anginkan Dipotong kecil-kecil
Lampiran 1. (Lanjutan)
Daun Labu kuning
Ditimbang sebanyak 25 gram di atas krus Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan–lahan temperature dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering
Hasil
Dilakukan selama 50 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dicuci bersih dengan air mengalir
Dihaluskan dengan blender Sampel yang telah dihaluskan
Lampiran 2. Bagan Alir Pembuatan Larutan Sampel
Sampel yang telah didestruksi
Dilarutkan dalam 5 mL HNO3 (1:1)
Dipindahkan ke dalam labu tentukur 50 mL Dibilas krus porselen sebanyak tiga kali dengan 10 ml akuademineralisata. Dicukupkan dengan akuademineralisata hingga garis tanda
Dimasukkan ke dalam botol Larutan sampel
Disaring dengan kertas saring Whatman No. 42
Filtrat
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan Atom pada λ 422,7 nm untuk kadar kalsium, pada 766,5 nm untuk kadar kalium, dan pada λ 589,0 nm untuk kadar natrium
Lampiran 3. Perhitungan Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No. Konsentrasi (µg/ml) (X)
Absorbansi (Y)
1. 0,0000 0,0044
2. 2,0000 0,0672
3. 4,0000 0,1142
4. 6,0000 0,1649
5. 8,0000 0,2197
6. 10,0000 0,2770
No. X Y XY X2 Y2
1. 0,0000 0,0044 0,0000 0,0000 0,000000
2. 2,0000 0,0672 0,1344 4,0000 0,004516
3. 4,0000 0,1142 0,4568 16,0000 0,013042
4. 6,0000 0,1689 1,0134 36,0000 0,028527
5. 8,0000 0,2197 1,7576 64,0000 0,048268
6. 10,0000 0,2770 2,7700 100,0000 0,076729
∑ 30,0000
X = 5,0000
0,8470
Y = 0,141167
6,1322 220,0000 0,171082
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)
Lampiran 3. (Lanjutan)
Y = a X + b b = Y − aX
= 0,141167 – (0,02710)(5,0000) = 0,005667
Maka persamaan garis regresinya adalah: Y = 0,02710X + 0,005667
=
(
)(
)
(
)
Lampiran 4. Perhitungan Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No. Konsentrasi (µg/ml) (X)
Absorbansi (Y)
1. 0,0000 -0,0042
2. 2,0000 0,1260
3. 4,0000 0,2459
4. 6,0000 0,3584
5. 8,0000 0,4630
6. 10,0000 0,5767
No. X Y XY X2 Y2
1. 0,0000 -0,0042 0,0000 0,0000 0,00000
2. 2,0000 0,1260 0,2520 4,0000 0,015876
3. 4,0000 0,1260 0,9836 16,0000 0,060466
4. 6,0000 0,2459 2,1504 36,0000 0,128450
5. 8,0000 0,3584 3,7040 64,0000 0,214369
6. 10,0000 0,4630 5,7670 100,0000 0,332582
∑ 30,0000
X = 5,0000
0,5767
Y = 0,1691
12,8570 220,0000 0,751400
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)( )
Lampiran 4. (Lanjutan)
Y = a X + b b = Y − aX
= 0,2950 – (0,0572)(5,0000) = 0,009
Maka persamaan garis regresinya adalah: Y = 0,0572 X + 0,009
=
(
)(
)
(
)
Lampiran 5. Perhitungan Kalibrasi Natrium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No. Konsentrasi (µg/ml) (X)
Absorbansi (Y)
1. 0,0000 0,0000
2. 0,2000 0,0406
3. 0,4000 0,0739
4. 0,6000 0,1072
5. 0,8000 0,1424
6. 1,0000 0,1728
No. X Y XY X2 Y2
1. 0,0000 0,0000 0,00000 0,0000 0,000000
2. 0,2000 0,0406 0,00812 0,0400 0,001648
3. 0,4000 0,0739 0,02956 0,1600 0,005461
4. 0,6000 0,1072 0,06432 0,3600 0,011492
5. 0,8000 0,1424 0,11392 0,6400 0,020277
6. 1,0000 0,1728 0,17280 1,0000