TESIS Oleh
SONY 117006032/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENURUNAN KADAR LEMAK DAN MINYAK LIMBAH CAIR INDUSTRI BIODISEL DENGAN METODE ELEKTROLISIS DAN ADSORBSI
MENGGUNAKAN KARBON AKTIF
TESIS
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains dalam Program Studi Ilmu Kimia pada Sekolah Pascasarjana
Universitas Sumatera Utara
Oleh
SONY 117006032/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
Judul Tesis : PENURUNAN KADAR LEMAK DAN MINYAK LIMBAH CAIR INDUSTRI BIODISEL DENGAN METODE ELEKTROLISIS DAN ADSORBSI MENGGUNAKAN KARBON AKTIF
Nama Mahasiswa : SONY Nomor Pokok : 117006032 Program Studi : Ilmu Kimia
Menyetujui Komisi Pembimbing
Pembimbing I Pembimbing II
(Prof. Dr. Zul Alfian, M.Sc) (
Ketua Anggota
Prof. Dr. Harry Agusnar, M.Sc, M.Phill)
Ketua Program Studi Dekan
Telah diuji pada
Tanggal : 22 Juli 2014
PANITIA PENGUJI TESIS
KETUA : Prof.Dr. Zul Alfian, M.Sc
ANGGOTA : 1. Prof. Dr. Harry Agusnar, M.Sc, M.Phill 2. Prof. Harlem Marpaung, M.Sc
PERNYATAAN
PENURUNAN KADAR LEMAK DAN MINYAK LIMBAH CAIR INDUSTRI BIODISEL DENGAN METODE ELEKTROLISIS DAN ADSORBSI
MENGGUNAKAN KARBON AKTIF
TESIS
Dengan ini saya menyatakan bahwa dalam tesis ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan sepanjang pengetahuan saya tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain kecuali secara tertulis diacu dalam naskah dan disebutkan sumbernya dalam daftar pustaka.
Medan, Juli 2014
Penulis
PENURUNAN KADAR LEMAK DAN MINYAK LIMBAH CAIR INDUSTRI BIODISEL DENGAN METODE ELEKTROLISIS DAN ADSORBSI
MENGGUNAKAN KARBON AKTIF ABSTRAK
Penelitian tentang pengolahan limbah cair industri biodisel dengan proses elektrolisis dan adsorbsi menggunakan karbon aktif (KA) cangkang kelapa sawit telah dilakukan. Penelitian meliputi pembuatan karbon aktif, karakterisasi dan penggunaanya sebagai adsorben pada pengolahan limbah cair. Pada tahap pertama limbah cair dielektrolisis untuk menurunkan pH menjadi ≤ 2, kemud ian tahap kedua limbah cair diadsorbsi dengan karbon aktif dan difiltrasi menggunakan kertas saring, tahap berikutnya limbah cair kembali dielektrolisis kembali untuk menaikkan kembali pH ± 7. Dari penelitaian ini didapat lama proses elektrolisis untuk mendapatkan pH limbah 2 adalah selama 50 menit untuk 200 mL sampel limbah cair. Hasil uji limbah cair industri biodisel pada kondisi optimum didapat kadar lemak dan minyak (L & M) 12 ppm dan Kebutuhan Oksigen Kimiawi (KOK) 47 ppm.
REDUCTION OIL AND GREASE CONTENT OF BIODIESEL WASTEWATER INDUSTRY BY ELECTROLISYS METHOD AND ADSORBTION
USING ACTIVATED CARBON
ABSTRACT
Research on biodiesel wastewater treatment by electrolysis and adsorption using activated carbon (AC) of oil palm shell has been done. The study includes the manufacture of activated carbon, characterization and its use as an adsorbent in wastewater treatment. In the first stage wastewater electrolyzed to lower the pH ≤ 2, then the second stage wastewater adsorbed with activated carbon and filtered using filter paper, the next stage of wastewater re-electrolyzed back to raise the pH of ± 7. From this study obtained long process of electrolysis to get waste pH 2 is for 50 minutes for a 200 mL sample of wastewater. Test results of biodiesel wastewater in optimum condition obtained oil and grease content (O & G) 12 ppm and Chemical Oxygen Demand (COD) ppm 47.
KATA PENGANTAR
Bismillahirrahmanirrahim
Puji Syukur yang tak terhingga penulis ucapkan dengan segala kerendahan hati dan diri kepada Allah SWT, Sang Khaliq yang senantiasa mencurahkan segala nikmat Iman, Islam
dan Ihsan, serta Shalawat dan salam kepada Nabi Allah sebagai patron insan terbaik ; Rasulullah Muhammad sehingga penulis mampu menyelesaikan penelitian hingga selesainya penulisan tesis ini dengan sebaik mungkin. Tesis ini berjudul “PENURUNAN KADAR LEMAK DAN MINYAK LIMBAH CAIR INDUSTRI BIODISEL MENGGUNAKAN METODE ELEKTROLISIS DAN ADSORBSI MENGGUNAKAN KARBON AKTIF”. Tesis ini merupakan salah satu syarat untuk memperoleh gelar Magister Sains (M.Si) Fakultas Matematika dan Ilmu Pengetahuan Alam Universias Sumatera Utara Medan.
Keberhasilan dari penelitian dan penulisan tesis ini tidak terlepas dari bantuan berbagai pihak yang terlibat secara langsung maupun tidak langsung dan telah memberikan dukungan baik secara moril maupun materil. Dalam kesempatan ini penulis ingin menyampaikan terima kasih yang tidak terhingga kepada :
Orangtua penulis, buat Ayahanda Sunarto dan Ibunda Ngatinem yang selalu sabar
dan mendoakan, memberi perhatian, dan menjadikan inspirasi di setiap langkah hidup kami. Kepada kakak saya tersayang Sriyani dan adik saya tersayang Yunita yang selalu memotivasi dan menginspirasi disetiap langkah hidup kami. Istri penulis Khairina safitri, S.Si, yang senantiasa mendoakan dan menjadi teman untuk berbagi, beserta ibunda Khairotun Nisaiah, S.Pd, abangda Khairi Saputra, ST, adik-adik kami Irmaliyani, S.Pd dan Widya Faridayanti.
Bapak Prof. Dr. dr. Syahril Pasaribu, DMT&H, M.Sc, (CTM), Sp.A(K) dan Dr. Sutarman, M.Sc selaku Rektor Universitas Sumatera Utara dan Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Bapak Prof.Basuki Wirjosentono, MS, Ph.D dan Dr. Hamonangan Nainggolan, M.Sc selaku ketua program studi dan sekretaris Pascasarjana Ilmu Kimia. Bapak dan Ibu dosen Pascasarjana Ilmu Kimia yang telah membimbing dan memotivasi serta memberi disiplin ilmu selama penulis menjalani studi.
Kak Lely selaku tata usaha Pascasarjana Ilmu Kimia. Rekan-rekan penulis diprogram Pascasarjana Ilmu Kimia yang telah berbagi banyak ilmu yang bermanfaat.
Sahabat terbaik yang selalu mengerti, membantu, dan berbagi dalam suka dan duka, Benny Hudaya, S.Si, Rivan,S.Si dan Hendi Surya Lubis, S.Si. Semua saudara dan teman-teman yang selalu mendoakan yang terbaik kepada penulis yang tidak dapat disebutkan satu persatu, yang telah dengan sabar mendengarkan segala keluh kesah dan memberikan masukannya kepada penulis.
Penulis menyadari bahwa tesis ini masih banyak kekurangan. Oleh karena itu, kritik dan saran yang membangun dari pihak pembaca sangat diharapkan penulis demi kesempurnaan tesis ini. Akhir kata semoga tesis ini bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan untuk massa yang akan datang.
Medan, Juli2014 Penulis
RIWAYAT HIDUP
DATA PRIBADI
Nama Lengkap berikut gelar : Sony, S.Si
Tempat dan Tanggal Lahir : Solo, 10 Maret 1987
Alamat Rumah : Jl. Melati No. 5 DSN I. Helvetia, Kec. Labuhan Deli. Kab. Deli Serdang. Sumatera Utara
Telepon/HP : +6281397979181
Email : sony_soenarto@yahoo.co.id
Nama Ayah : Sunarto
Nama Ibu : Ngatinem
DATA PENDIDIKAN
DAFTAR ISI
Halaman
ABASTRAK i
ABSTRACT ii
KATA PENGANTAR iii
RIWAYAT HIDUP v
DAFATR ISI vi
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
DAFTAR SNGKATAN xi
BAB 1. PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Perumusan Masalah 3
1.3 Pembatasan Masalah 4
1.4 Tujuan Penelitian 4
1.5 Manfaat Penelitian 4
1.6 Metode Penelitian 4
1.7 Lokasi Penelitian 4
BAB 2. TINJAUAN PUSTAKA 5
2.1 Limbah 8
2.2 Karbon Aktif 11
2.4 Elektrolisis 19
2.5 Elektrolisis Air 22
2.6 Elektrolisis Larutan Metanol 24
BAB 3. METODE PENELITIAN 25
3.1 Alat dan Bahan 25
3.1.1 Alat 25
3.1.2 Bahan 25
3.2 Prosedur Penelitian 26
3.2.1 Pembuatan Arang Aktif 26
3.2.2 Penentuan Kadar Air Karbon Aktif 26
3.2.3 Uji Adsorbsi Metilen Biru dengan Karbon Aktif 27 3.2.3.1 Pembuatan Larutan Standar Metilen Biru 27
3.2.3.2 Penentuan λ Maksimum 27
3.2.3.3 Adsorbsi Metilen dengan Karbon Aktif 27
3.2.4 Uji Adsorbsi Karbon Aktif Terhadap Iodine (ASTM D4607-94) 28
3.2.5 Penentuan Kadar Lemak dan Minyak 28
3.2.6 Uji Adsorbsi Lemak dan Minyak menggunakan Karbon Aktif 28 3.2.7 Uji Penurunan pH dengan Proses Elektrolisis 29
3.2.8 Pembuatan Jembatan Garam 29
3.2.9 Deadsorbsi Lemak dan Minyak dalam Karbon Aktif 29
3.3 Bagan Penelitian 30
BAB 4. HASIL DAN PEMBAHASAN 37
4.1 Analisis Limbah Cair Industri Biodisel 37
4.2 Karakterisasi Karbon Aktif 37
4.2.2 Uji Adsorbsi KArbon Aktif Terhadap Metilen Biru 38 4.2.3 Uji Adsorbsi KArbon Aktif Terhadap Iodin 40
4.3 Penentuan Kondisi Optimum 41
4.3.1 Penentuan pH Optimum 41
4.3.2 Penentua Waktu kontak Optimum 41
4.4 Isoterm Adsorbsi Freunlich 42
4.5 Penurunan Liabah Cair Industri Biodisel 43
4.6 Adsorbsi Minyak dan Lemak 43
4.7 Deadsorbsi dan Uji Pemakaian Kembali Arang aktif 45
BAB 5. KESIMPULAN DAN SARAN 47
5.1 Kesimpulan 47
5.2 Saran 47
DAFTAR PUSTAKA 48
DAFTAR TABEL
Nomor Judul Halaman
Tabel 2.1 Baku Mutu Air Limbah 9
Tabel 4.1 Hasil Analisis Limbah Cair Industri Biodisel 37 Tabel 4.2 Hasil Analisis Kadar Air Karbon Aktif 38
Tabel 4.3 Uji adsorbsi Metilen Biru 40
Tabel 4.4 Uji Adsorbsi Iodin 40
Tabel 4.5 Isoterm adsorbsi Freunlich 42
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar 2.1 Bagan proses pembuatan biodisel 5
Gambar 2.2 Raksi esterifikasi asam lemak dengan katalis asam 7 Gambar 2.3 Mekanisme reaksi transesterifikasi trigliserida dengan
katalis basa 8
Gambar 2.4 Mekanisme aktivasi arang aktif dengan larutan H3PO4 15 Gambar 2.5 Hasil analisa SEM karbon aktif dari tempurung
kelapa sebelum dan setelah aktivasi dengan NaOH 15
Gambar 2.5 Oksidasi elektrolisis air 21
Gambar 4.1 Kurva Panjang Gelombang Optimum metilen Biru 38
Gambar 4.2 Kurva Kalibrasi Metilen Biru 39
Gambar 4.3 Pengaruh pH Terhadap Adsorbsi Minyak dan Lemak 41
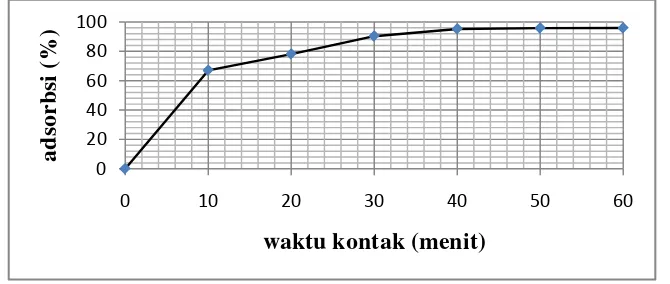
Gambar 4.4 Pengaruh Waktu Kontak 41
Gambar 4.5 Kurva Isoterm Adsorbsi Freunlich 42
DAFTAR LAMPIRAN
Nomor Judul Halaman
DAFTAR SINGKATAN
MEAL : Metil Ester Asam Lemak
KA : Karbon Aktif
ASTM : American Standart for Testing and Material L&M : Lemak Dan Minyak
KOK : Kebutuhan Oksigen Kimiawi O&G : Oil & Grease
PENURUNAN KADAR LEMAK DAN MINYAK LIMBAH CAIR INDUSTRI BIODISEL DENGAN METODE ELEKTROLISIS DAN ADSORBSI
MENGGUNAKAN KARBON AKTIF ABSTRAK
Penelitian tentang pengolahan limbah cair industri biodisel dengan proses elektrolisis dan adsorbsi menggunakan karbon aktif (KA) cangkang kelapa sawit telah dilakukan. Penelitian meliputi pembuatan karbon aktif, karakterisasi dan penggunaanya sebagai adsorben pada pengolahan limbah cair. Pada tahap pertama limbah cair dielektrolisis untuk menurunkan pH menjadi ≤ 2, kemud ian tahap kedua limbah cair diadsorbsi dengan karbon aktif dan difiltrasi menggunakan kertas saring, tahap berikutnya limbah cair kembali dielektrolisis kembali untuk menaikkan kembali pH ± 7. Dari penelitaian ini didapat lama proses elektrolisis untuk mendapatkan pH limbah 2 adalah selama 50 menit untuk 200 mL sampel limbah cair. Hasil uji limbah cair industri biodisel pada kondisi optimum didapat kadar lemak dan minyak (L & M) 12 ppm dan Kebutuhan Oksigen Kimiawi (KOK) 47 ppm.
REDUCTION OIL AND GREASE CONTENT OF BIODIESEL WASTEWATER INDUSTRY BY ELECTROLISYS METHOD AND ADSORBTION
USING ACTIVATED CARBON
ABSTRACT
Research on biodiesel wastewater treatment by electrolysis and adsorption using activated carbon (AC) of oil palm shell has been done. The study includes the manufacture of activated carbon, characterization and its use as an adsorbent in wastewater treatment. In the first stage wastewater electrolyzed to lower the pH ≤ 2, then the second stage wastewater adsorbed with activated carbon and filtered using filter paper, the next stage of wastewater re-electrolyzed back to raise the pH of ± 7. From this study obtained long process of electrolysis to get waste pH 2 is for 50 minutes for a 200 mL sample of wastewater. Test results of biodiesel wastewater in optimum condition obtained oil and grease content (O & G) 12 ppm and Chemical Oxygen Demand (COD) ppm 47.
BAB 1 PENDAHULUAN
1.1Latar Belakang
Cadangan energi fosil dunia yang semakin menipis serta pencemaran lingkungan yang disebabkan oleh pembakaran atau penggunaan energi fosil tersebut memaksa masyarakat dunia mencari alternatif bahan bakar pengganti bahan bakar fosil.Salah satu bahan bakar alternatif yang dikembangkan diberbagai Negara adalah bahan bakar hayati yang dapat diperbaharui seperti bioetanol, biogas dan biodisel.Indonesia sebagai salah satu Negara dengan lahan perkebunan kelapa sawit yang cukup luas tentunya merupakan sebuah Negara yang berpotensi sebagai penghasil biodiesel sebagai bahan bakar hayati yang berasal dari tanaman kelapa sawit.Menurut data dari kementrian ESDM, total produksi biodiesel nasional mencapai 1.654.260 kiloliter pada tahun 2012.Potensi tersebut tentunya diikuti dengan tumbuh dan berkembangnya industri penghasil biodiesel, yang tentunya diikuti pula dengan bertambahnya kuantitas limbah yang dihasilkan, khususnya limbah cair dari proses produksi biodiesel tersebut. Pengolahan limbah yang tepat dan efisien tentunya sangat diperlukan untuk menjaga lingkungan tetap lestari dengan biaya yang seefisien mungkin.
Telah dilakukan berbagai metode pengolahan limbah dari industri pembuatan biodiesel. Seperti metoda eletrokoagulasi, yang menghasilkan flok pada proses pengolahanya yang kemudian dipisahkan dari limbah cair (Srirangsan et al., 2009), metode biologis dengan menggunakan ragi yang mengandung bakteri Rhodotorula mucilaginosabesertanutrien untuk perkembangan bakteri tersebut seperti sumber nitrogen ( ammonium sulfat, ammonium klorida atau urea), ektrak ragi, KH2PO4 dan MgSO4 . 7H2O (Suehara et al., 2005), metoda kimia, dengan penambahan bahan pengendap serta gabungan metode kimia dan metoda elektrokoagulasi (Ngamlerdpokin.,et al., 2011). Pada metoda elektrokoagulasi kimia maupun metode elektrokoagulasi menghasilkan endapan yang memerlukan pengolahan lanjutan sehingga membutuhkan biaya yang lebih besar.
Oksidasi Elektrolisis air pertama sekali dikembambanngkan di jepang (shimizu& hirusawa, 1992). Oksidasi air dilakukan dengan mengalirkan larutan garam encer dalam sebuah sel lektrolitik, dimana anoda dan katoda dipisahkan oleh sebuah membran, dan dengan menghubungkan elektroda dengan sebuah sumber arus DC. Ion dengan muatan negative seperti ion klorida dan ion hidroksida dalam larutan garam akan bergerak ke anoda untuk menyumbangkan elektron dan menghasilkan gas oksigen, gas klorin, ion hipoklorin, asam hipoklorid dan asam klorida. Ion dengan muatan positf seperti H+ dan Na+akan bergerak ke katoda untuk menangkap elektron dan menghasilkan gas H2 dan sodium hidroksida. Dua jenis larutan yang dihasikan dari proses oksidasi elektrolisis yang dihasilkan secara simultan yaitu larutan dengan pH rendah antara 2.3-2.7 pada anoda dan larutan dengan pH tinggi 10.0-11.5 pada katoda.
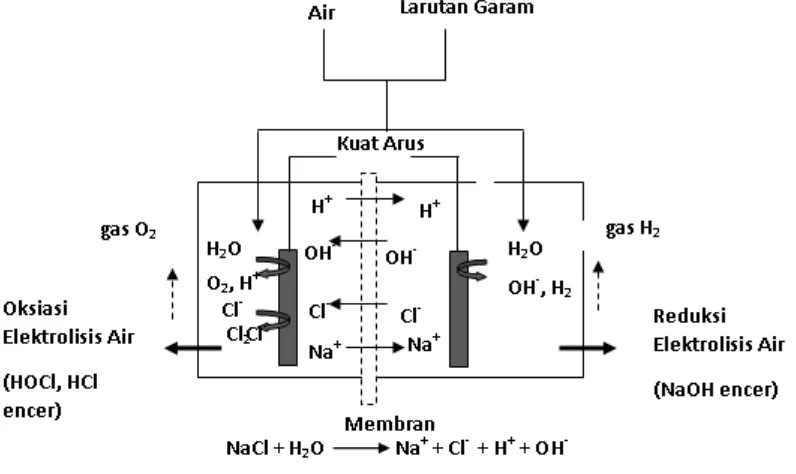
Prinsip oksidasi elektrolisis air adalah sebagai berikut:
Kutup positif : 2H2O 4H+ + O2 + 4e-
2NaCl Cl2 + 2e + 2Na+
Kutup Negatif : 2H2O +2e- 2OH- + H2 2NaCl + 2OH- 2NaOH + Cl
-(Huang, Hung, Hsu & Hwang, 2007) Adanya asam yang dihasilkan dari proses oksidasi elektrolisis air tersebut maka memungkinkan konsep tersebut digunakan untuk mengasamkan limbah cair industri biodiesel.
Berlimpahnya cangkang kelapa sawit sebagai hasil dari industri minyak kelapa sawit mendorong keinginan untuk meningkatkan nilai ekonomi bahan tersebut.Salah satu upaya yang dilakukkanan adalah pengolahancangkang kelapa sawit menjadi karbon aktif.Karbon aktif telah banyak digunakan dalam berbagai kegunaan termasuk sebagai bahan pengolahan limbah cair industri.
Dari beberapa alasan diatas maka dalam penelitian ini peneliti akan meneliti penggunaan proses elektrolisis untuk menurunkan pH limbah cair industri biodiesel dan karbon aktif sebagai bahan adsorben untuk menyerap minyak dan lemak dari limbah cair industri biodiesel, yang diharapkan dapat menjadi suatu metode dan bahan yang efisien dalam pengolahan limbah cair dari industri pembuatan biodiesel.
1.2Perumusan Masalah
-Apakah karbon aktif dari cangkang kelapa sawit dapat mengadsorbsi kandungan lemak dan minyak dari limbah cair industri biodisel.
-Apakah proses elektrolisis dapat menurunkan pH limbah cair industri biodisel
1.3Pembatasan Masalah
1.4Tujuan Penelitian
Tujuan penelitian ini adalah menurunkan kadar lemak dan minyak dari limbah cair industri biodisel dengan menggunakan proses elektrolisis untuk menurunkan pH dan karbon aktif sebagai adsorben minyak dan lemak.
1.5Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi dan temuan tentang pengolahan limbah cair industri biodisel yang lebih ekonomis dan meminimalkan penggunaan bahan kimia dalam pengolahan limbah cair tersebut.
1.6Metodologi Penelitian
Penelitian ini merupakan eksperimental laboratorium. Dengan melihat pengaruhwaktu elektrolisis dalam menurunkan pH limbah cair industri biodisel dan kuantitas karbon aktif dalam penurunan kadar lemak dan minyakdari limbah cairindustri pembuatan biodiesel.
1.7Lokasi Penelitian
BAB 2
TINJAUAN PUSTAKA
Untuk menghasilkan biodiesel minyak nabati atau lemak hewani direaksikan dalam reaksi kimia yang biasa disebut transesterifikasi.
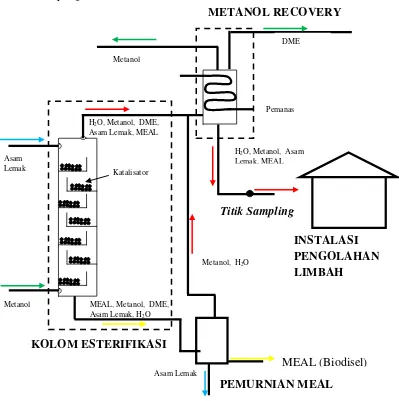
Gambar 2.1 Bagan proses pembuatan biodiesel
Dalam reaksi tersebut, minyak nabati atau lemak hewani direaksikan dengan suatu alkohol (biasanya methanol) dengan dengan adanya suatu katalis (biasanya suatu basa) untuk menghasilkan suatu alkil ester yang sesuai ( atau untuk methanol
dihasilkan metal ester) dari campuran asam lemak yang terdapat dalam minyak nabati atau lemak hewani.
Methanol direaksikan dengan asam lemak dalam kolom esterifikasi, dimana metanol diuapkan dengan pemanasan pada suhu sebelum diaspirasikan melalui bagian bawah kolom esterifikasi sementara itu asam lemak di aspirasikan kedalam kolom esterifikasi melalui bagian atas dari kolom esterifikasi. Dalam kolom esterifikasi terdapat katalisator heterogen yang memebantu mempercepat reaksi esterifikasi. Suhu didalam kolom di jaga pada kisaran antara 115-125oC. dengan pemanasan kolom tersebut air sebagi hasil samping reaksi esterifikasi
Methanol direaksikan dengan asam lemak dan katalisator dalam sebuah kolom pada suhhu 115-125o C. uap methanol direspirasikan melalui bagian bawah kolom esterifikasi, sedangkan asam lemak diaspirasikan melalui bagian atas kolom esterifikasi. Dalam kolom esterifikasi terjadi reaksi :
RCOOH + CH3OH RCOOCH3 + H2O
CH3OH + CH3OH CH3-O-CH3 + H2O
Pemansan pada reaktor esterifikasi selain bertujuan mempercepat reaksi esterifikasi juga bertujuan menguapkan air dan sisa methanol yang tidak bereaksi serta dimetil eter. Pada prakteknya tidak hanya methanol dan air yang teruapkan keluar dari bagian atas kolom esterifikasi, tetapi metl ester asam lemak (MEAL) dan asam lemak juga sedikit juga ikut keluar dari bagian atas kolom esterifikasi.
diharapkan bebas dari methanol, MEAL, dan asam lemak. Tetapi pada kenyataanya air yang dihasilkan tetapa mengandung methanol, MEAL dan asam lemak dan membentuk emulsi dan sulit dipisahkan dengan metode diatas.
Biodiesel dapat di produksi dari berbagai sumber- sumber yang umum baik digunakan. Diantaranya sumber tersebut adalah minyak nabati ( seperti kedelai, biji kapas, kelapa, kacang, bunga matahari, bijicoklat) dan dari lemak hewani serta limbah minyak (biasanya minyak bekas penggorengan). Pemilihan sumber bahan baku biodiesel biasanya dipengaruhi oleh sebagian besar dari letak geograpis. Tergantung dari keaslian dan kualitas sumber bahan baku biodiesel, dapat dilakukan perubahan dalam proses produksi jika dibutuhkan.
Metanol biasa digunakan sebagai alkohol dalam proses pembuatan biodiesel hal ini dikarenakan methanol cenderung lebih murah jika dibandingkan dengan jenis alkohol yang lain, akan tetapi alkohol yang lain seperti etanol dan iso propanol menghasilkan kualitas biodiesel yang lebih baik. Produk yang dihasilkan sering kali disebut sebagai metal ester asam lemak (MEAL) sebagai ganti dari sebutan biodiesel. Walaupun jenis lakohol lain yang digunakan tetapi hasilnya biasa disebut juga sebagai biodiesel (Gerhard., dkk. 2005)
Proses pembuatan biodiesel dengan biaya yang ralatif lebih murah dapat dilakukan dengan menggunakan bahan baku destilat asam lemak dari minyak kelapa sawit. Destilat asam lemak merupakan residu dari pengolahan dan pemurnian minyak kelapa sawit. Destilat asam lemak direaksikan dengan metanol dengan katalis asam berupa asam sulfat (chongkong., dkk, 2007)
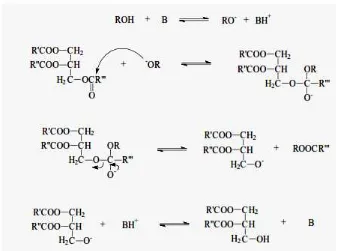
(Schuchardt, dkk., 1997) Gambar 2.3 Mekanisme reaksi transesterifikasi trigliserida dengan katalis basa
2.1 Limbah
Limbah padat suatu industri adalah merupakan bahan sisa dari suatu proses yang dilakukan dalam suatu industri yang tidak dapat digunakan atau dimanfaatkan lagi oleh industri tersebut sehingga perlu dikeluarkan dari industri tersebut (Hiroshi, 2000).
Bahan berbahaya dan beracun yang biasa disebut B3 adalah zat, energi, dan/atau komponen lain yang karena sifat, konsentrasi, dan/atau jumlahnya, baik secara langsung maupun tidak langsung, dapat mencemarkan dan/atau merusak lingkungan hidup, dan/atau membahayakan lingkungan hidup, kesehatan, serta kelangsungan hidup manusia dan makhluk hidup lain. (UU No.23, 2009).
Agar tidak mencemari lingkungan maka limbah dari pembuatan biodiesel harus sesuai dengan peraturan menterinegaralingkungan hidup no. 10 tahun 2009 tentang baku mutu air limbah bagi usah adan /atau kegiatan industry oleokimia dasar :
Tabel 2.1. Baku mutu air limbah
Parameter Kadar Maksimum Satuan
BOD 125 mg/Liter
dan membentuk emulsi. Karena adanya asam lemak dalam limbah tersebut biasanya pH dari limbah tersebut asam ± pH 5.
RCOOH + CH3OH RCOOCH3 + H2O
Telah banyak dilakukan berbagi penelitian mengenai pengolahan limabah cair dari industri pembuatan biodisel, diantaranya :
1. Pengolahan secara biologis.
Suehara dkk, telah melakukkan penelitian tentang pengolahan limbah cair dari produksi biodisel dengan metode biologis, mereka menggunakan Rhodotorula mucilaginosa, yang merupakan ragi minyak yang biodegredable dan dengan penambahan bebebrapa sumber nutrien diantaranya urea sebagai sumber nitrogen, ekstrak ragi, KH2PO4 dan MgSO4. 7H2O. pH diatur pada 6,8 dan penambahan konsentrasi ekstrak ragi optimum pada 1 g/L limbah cair. Dalam penelitian yang dilakukan mereka juga mengencerkan limbah untuk menurunkan kadar padatan karena bakteri dari tidak dapat tumbuh jika kadar padatan dari limbah melebihi kadar 2,14g/L. Efisiensi biodegradasi dari minyak dan lemak yang dilaporkan mereka lebih dari 98%. (Suehara, dkk. 2005).
2. Pengolahan Secara kimia
3. Elektrokoagulasi
Pengolahan limbah cair dari industri pembuatan biodisel juga dapat dilakukan dengan metoda elektrokoagulasi. Dari uji terhadap variasi jenis elektroda (Fe, Fe-C, C-Fe-C, Al-C dan Al-Al), didapat elektroda dengan hasil optimum pada pasangan elektroda Al-C, dengan arus 8,32 mA/cm2, dengan pH awal 6, metoda elektrokoagulasi ini dapat menurunkan nilai COD 55,7 %, minyak dan Lemak 97,8% dan total padatan terlarut 97,5 %. Endapan yang diperoleh dari metode juga lebih sedikit jika dibandingkan dengan metode konvensional (Saringsan, dkk., 2009).
2.2 Karbon Aktif
Karbon aktif merupakan karbon amorf dari pelat-pelat datar disusun oleh atom-atom C yang terikat secara kovalen dalam suatu kisi heksagonal datar dengan satu atom C pada setiap sudutnya yang luas permukaan berkisar antara 300 m2/g hingga 3500 m2/g dan ini berhubungan dengan struktur pori internal sehingga mempunyai sifat sebagai adsorben (Taryana.,2002).
Berlimpahnya tempurug kelapa sawit sebagai hasil dari industri minyak kelapa sawit mendorong keinginan untuk meningkatkan nilai ekonomi bahan tersebut.Salah satu upaya yang dilakukan adalah perosesan tempurung kelapa sawit menjadi karbon aktif. Bahan karbon aktif ini banyak digunakan dalam industri khususnya di bidang perminyakan,pengolahan air,industri gas, makanan dan minuman,obat-obatan dan industri kimia.
pori-pori arang aktif, mengakibatkan luas permukaan semakin besar. Dengan demikian kecepatan adsorpsi bertambah.Untuk meningkatkan kecepatan adsorpsi, dianjurkan agar menggunakan karbon aktif yang telah dihaluskan.( Puspita, D., 2008)
Arang aktif tersusun dari suatu jaringan pori-pori yang rumit dan dapat dibagi menjadi dua bagian menurut ukuranya :
a. Makropori adalah pori-pori arang aktif deengan diameter lebih besar dari 500 Å. Pori-pori ini merupakan kapiler yang besar yang menyebar keseluruh bagian partikel.
b. Mikropori adalah arang aktif dengan diameter antara 10-500 Å dan merupakan cabang dari makropori.
Secara umum susunan pori-pori yang ada dalam karbon aktif berhubungan dengan permukaan luar dari partikel. Pori mikro merupakan cabang dari pori transisi dan dapat menyerap pelarut dan adsorbat dengan ukuran yang lebih kecil (Samuel, 1983).
Secara umum proses pembuatan karbon aktif dari tempurung kelapa sawit dilakukan dalam tiga tahap proses yaitu tahap persiapan, tahap karbonisasi, dan tahap aktivasi. Tahap persiapan dilakukan dengan pembersihan tempurung dari serabut dan sisa daging buah yang menempel di tempurung, dipanaskan dalam oven pada suhu 110oC selama satu jam.
Tahap karbonisasi dilakukan dengan memasukkan sejumlah tempurung kedalam peralatan furnace pada suhu antara 300-500 oC selama kurang lebih 3 jam. Tahap aktivasi dilakukan dengan perendaman dalam aktifatorkimia (NaCl, NaOH, dan HCl) dengan konsentrasi 2 % selama 1-4 jam (Singgih, 2010).
Tahap I, pada suhu 100 -120o C terjadi penguapan air dan sampai pada suhu 270o C mulai terjadi peruraian selulosa. Distilat mengandung asam organik dan sedikit metanol. Asam asetat terbentuk pada suhu 200-270o C.
Tahap II, pada suhu 270 – 310o C reaksi eksotermik berlangsung dimana terjadi peruraian selulosa secara intensif menjadi larutan piroligant, gas kayu dan sedikit tar. Asam merupakan asam organik dengan titik didih rendah seperti asam asetat sedangkan gas yang dihasilkan terdiri dari CO dan CO2.
Tahap III, pada suhu 310 – 500o C terjadi peruraian lignin, lebih banyak dihasilkan tar sedangkan larutan piroligant menurun, gas CO2 menurun sedangkan gaas CO dan CH4 dan H2 meningkat.
Tahap IV, pada suhu 500-1000o C merupakan tahap pemurnian arang atau kadar karbon (Sudrajat, 1994).
Faktor faktor yang mempengaruhi proses karbonisasi adalah :
1. Waktu karbonisasi, bila waktu karbonisasai diperpanjang maka reaksi pirolisa semakin sempurna sehingga hasil arang menurun tetapi cairan dan gas makin meningkat. Waktu karbonisasi berbeda – beda tergantung pada jenis dan jumlah bahan yang akan diolah menjadi karbon aktif. Misalnya, untuk pengolahan tempurung kelapa menjadi karbon aktif dibutuhkan waktu selama 3 jam (BPPI Bogor, 1980), sekam padi kira-kira 2 jam( Joni, dkk., 19965) dan tempurung kemiri 1 jam ( Bardi & Mun’im, 1999).
Aktivasi adalah perubahan secara fisik dimana luas permukaan dari karbon meningkat dengan tajam dikarenakan terjadinya penghilangan senyawa tar dan senyawa sisa-sisa pengarangan (Shreve, 1997). Daya serap karbon aktif akan semakin kuat bersamaan dengan meningkatnya konsentrasi dari aktivator yang ditambahakan. Hal ini memberikan pengaruh yang kuat untuk mengikat senyawa-senyawa tar keluar melewati mikro pori-pori dari karbon aktif sehingga permukaan dari karbon aktif tersebut semakin lebar dan luas yang mengakibatkan semakin besar pula daya serap karbon aktif tersebut.Metode yang dapat diguakan adalah, Aktivasi kimia, pada cara ini proses aktivasi dilakukan dengan mempergunakan bahan kimia sebagai bahan aktivator. Aktivasi arang ini dilakukan dengan merendam arang kedalam larutan kimia, misalnya ZnCl2, HNO3, KCl dan lain-lain, sehingga bahan kiia akanmeresap dan membuka permukaan arang yang semula tertutup oleh deposit tar. Aktivasi secara fisika, pada aktivasi ini menggunakan suhu tinggi dalam proses akivasi. Karbon atau arang dipanaskan pada suhu tinggi didalam sistem tertutup sambil dialiri gas inert. Dengan pemanasan yang tinggi tersebut terjadi reaksi lanjutan pemecahan atau penguraian sisa deposit tar dan senyawa hidrokarbon sisa karbonisasi yang keluar dari permukaan karbon akobat pemanasan pada suhu tigngi dan adanya aliran gas inert, sehingga akan dihasilkan karbon dengan luas permukaan yang cukup luas (Tutik & Fauziah, 2001).
Ada bebrapa faktor yanng mempengaruhi dalam proses aktivasi diantaranya : 1. Waktu aktivasi/ waktu perendaman, perendaman dengan bahan aktivasi ini
2. Konsentrasi aktivator, semakin tinggi konsentrasi larutan kimia yang digunakan sebagai aktovator maka semakin semakin kuat pengaruh larutan tersebut mengikat senyawa-senyawa tar sisa karbonisasi untuk kelluar melewati mikro pori-pori dari karbon sehingga permukaan karbon semakin porous yang mengakibatkan semakin besar daya serap karbon aktif tersebut. Mekanisme aktivasi arang dengan larutan H3PO4 ditunjukkan dalam gambar dibawah ini :
Gambar 2.5. Mekanisme aktivasi arang aktif dengan larutan H3PO4.
Arang atau karbon semakin banyak mempunyai mikro pori-pori setelah dilakukan aktivasi, hal ini karena aktivator telah menikat senyawa – senyawa tar sisa karbonisasi keluar dari mikropori arang, sehingga permukaanya semakin porous (Tutik & Faizah, 2001)
(Singgih, 2010) Gambar 2.4. Hasil analisa SEM karbon aktif dari tempurung kelapa sebelum dan
Dua jenis perbedaan yang dipertimabangkan dalam pembuatan dan penggunaan karbon aktif adalah, untuk penggunaan pada fase cair karbon aktif yang digunakan biasanya digunakan yangmemiliki berat molekul kecil dan halus seperti serbuk. Sedangkan jika digunakan dalam fase atau pemurnian gas biasanya digunakan karbon aktif dengan berat dan ukuran yang lebih besar seperti berbentuk butiran atau seperti pil (Othmer, 1992).
Cangkang kelapa sawit merupakan bahan baku yang baik dalam pembuatan karbon aktif , memiliki tingkat porositas yang tinggi dengan aktivasi menggunakan asam pospat. Luas permukaan maksimum dengan BET pada suhu 700o C adalah 1915 cm2 g-1 . Distribusi ukuran pori dari karbon aktif didominasi oleh struktur mesopori. Modifikasi dengan uap air dan asam nitrat menghasilkan permukaan oksigen yang lebih luas dan menggandung gugus fungsi pada permukaanya berupa gugus fungsi asam (Allwar, 2012).
Perpaduan antara aktivasi kimia dan aktivasi fisika pada pembuatan karbon aktif dari cangkang kelapa sawit menghasilkan karbon aktif yang diaktivasi dengan menggunakan H3PO4 memiliki luas permukaan dan volume mikropori yang lebih tinggi jika dibandingkan dengan karbon aktif yang diaktifasi dengan menggunakan ZnCl2 dan aktivasi secara fisika. Penggunaan sedikit ZnCl2 dan H3PO4 menghasilkan beberapa pori dengan ukuran kecil, hal tersebut dapat dikembangkan agar merata dengan menggunakan ekstra aktivasi secara fisika. Penggunaan aktifasi kimia dan fisika menghasilkan distribusi permukaan pori yang lebih merata. Dengan demikian pengunaan metode ini sangat baik digunakan untuk menggatur dan mengembangkan mikropori yang seragam dimana peningkatan kapasitas adsorbsi dari karbon aktif merata paddasemua permukaan karbon aktif (Arami.,daud.,Majli, 2010).
tinggi menggunakan aktifasi kimia, dengan KOH sebagai bahan pengaktifasi. Karbon aktif yang dihasilkan menunjukkan bahwa dihasilkan mikropori padasuhu redah dan mesopori pada suhu tinggi. Luas permukaan maksimum dengan metode BET dan volume dari mikropori karbon aktif yang dihasilkan adalah brturut turut yaitu 2301 m2g-1 dan 0.55 cm3g-1, dimana karbonbon aktif tersebut dihasilkan dari proses pemanasan pada suhu 800 oC. pengaruh penggunaan bahan kimia pada pembuatan karbn aktif adalah meningkatkan permukaan dengan gugus fungsi. Hasil yang didapat dengan menggunakan asam nitrat sebagai bahan dalam pembuatan meningkatkan gugus oksigen padapermukaan karbon aktif (Allwar, 2012).
2.3 Adsorbsi
Adsorbsi merupakan proses pengikatan suatu molekul baik dalam bentuk gas atau gas kedalam suatu padatan. Suatu bahan yang dapat menyerap dan mengikat suatu molekul disebut sebagai adsorben, dan zat yang diserap oleh adsorben adalah adsorbat. Proses adsorbsi biasanya dilakukan dengan cara mengontakkan adsorbat dengan adsorben, sehingga komponen larutan/gas terserap pada permukaan adsorben.
Proses adsorbsi dibagi sebagai berikut :
a. Adsorbsi fisika, terjadi apabila molekul adsorbat ditahan secara fisika oleh molekul adsorben dengan adanya gayua Van Der Waals. Adsorbsi ini terjadi karena adanya gaya tarik menarik antara molekul adsorben dengan molekul adsorbat. Pada proses adsorbsi ini adsorbat tidak terjadi perubahan kimia dan tiak menenmbus ke dalam kristal adsorben.
b. Adsorbsi kimia, proses adsorbsi ini terjadi karena adanya pertukaran elektron pada permukaan. Adsorbsi jenis ini terjadi akibat adanya interaksi kimia antara adsorben dengan bahan adsorbat. Adsorbsi secara kimia berlangsung searah (Treybal, 1981).
ketika sistem mencapai kesetimbangan; yaitu ketika tingkat adsorpsi zat terlarut ke permukaan adsorben adalah sama dengan laju desorpsinya dari permukaan adsorben. Oleh karena itu,tidak ada adsorpsi lanjut terjadi.
Beberapa hubungan matematis telah dikembangkan untuk menggambarkan distribusi kesetimbangan zat terlarut antarafase padat dan fase cair pada suhu konstan dan dengan demikian membantu dalam interpretasi proses adsorpsi. Model yang paling banyak digunakan adalah Langmuir dan isoterm Freundlich.keduanya berguna untuk menggambarkan kapasitas adsorpsi dari adsorben tertentu.
2.3.1 Isoterm Adsorbsi Langmuir
Persamaan Langmuir untuk system padat-cair biasanya ditulis seperti persamaan berikut ini :
�� =
KL:Ce
1 + bCe
Dimana qe adalah jumlah adsorbat per satuan berat adsorben (mg /g), Ce adalah konsentrasi adsorbat dalam larutan pada kesetimbangan setelah adsorbsi selesai (mg /L), KL adalah jumlah berat zat terlarut terserap/unit adsorben dalam membentuk monolayer lengkap di permukaan (mg /g), dan badalah konstanta terkait dengan energi atau entalpi adsorpsi. Bentuk persamaan linear Langmuir di tulis sebagai berikut :
�= 1 1 + bC0
di mana Co adalah konsentrasi adsorbat awal (mg /L) dan b adalah konstanta Langmuir terkait dengan energia dsorpsi (L /mg). Nilai r menunjukkan bentuk adsorpsi isoterm adsorpsi untuk mengetahui apakah kurang baik(r>1), linear(r =1), baik (0 <r <1), atautidak reversibel((r =0).
2.3.2 Isoterm Adsorbsi Freundlich
Isotherm Adsorbsi Freundlich dapat diterapkan untuk adsorpsi nonideal pada permukaan heterogen serta multilayer penyerapan dan dinyatakan oleh persamaan berikut:
�� =����1/� Persamaan garis linearnya adalah :
log�� = log��+1 � �����
Dimana Kf adalah konstanta kesetimbangan Freundlich yang menunjukkan kapasitas serap dan n adalah indikasi konstanta Freundlich dari afinitas adsobat untuk permukaan adsorben, qe adalah jumlah adsorbat per satuan berat dari adsorben (mg /g), Ce adalah konsentrasi adsorbat dalam larutan pada kesetimbangan setelah adsorbsi selesai (mg /L) (K.Okiel et al, 2010).
2.4 Elektrolisis
positif ) bermuatan positif.spesi (ion, molekul, atau atom) tertentu dalam dalam larutan akan mengambil elektron dari katoda,sementara spesi lainya melepas elektron ke anoda.selanjutnya elektron akan daialirkan ke katoda melalui sumber arus searah. Elektrolit kuat mempunyaidaya hantar yang relatif baik meskipun konseantrasi relatif kecil, sedangkan elektrolit lemah mempunyaidaya hantar yang relatif buruk meskipun konsentrasinya relatif besar. Pada proses elektrolisis selain jenis larutan, jenis elektroda juga mempengaruhi hasil elektrolisis. Disini elektroda diplih berdasarkan kemampuanya untuk menghantarkan listrik ( bersifat konduktor). Maka elektroda yang dipilih adalahn bersifat logam. Jenis elektroda kita pilih berdasarkan deret volta dan segiekonomis.
Elektrolit adalah suatu zat terlarut atau terurai kedalam bentuk ion-ion dan selanjutnya lrutan menjadi konduktor elektrik.Umumnya, air adalah pelarut yang baik untuk senyawa ion dan mempunyai sifat menghantarkan listrik. Air murni adalah elektrolit yang buruk (Brady, 199)
Berdasarkan penelitian yang pernah dilakukan faktor-faktor yang mempengaruhi proses elektrolisis yaitu kerapatan arus listrik, waktu, tegangan, kadar keasaman (pH), ketebalan plat dan jarak antar elektroda (Putero, 2008). Contoh diagram sederhana elektrolisis,
(Huang, Hung, Hsu & Hwang, 2007) Gambar 2.5. Oksidasi elektrolisis air
Secara umum proses elektrolisis terdiri dari beberapa bagian yaitu: a. Sumber Arus
Sumber arus yang dimaksud adalah sumber arus searah. b. Elektroda
Elektroda berfungsi sebagai penghantar arus listrik dari adaptor menuju larutan elektrolit sehingga terjadi proses elektrolisis.
akan terbentuk, konduktivitas listrik, ketahanan dan harga faktor, serta kesesuaian dengan desain sel atau sistem (Artadi, 2007).
2.5 Elektrolisis Air
Sejarah elektrolisis air dimulai pada revolusi industri pertama , pada tahun 1800 , ketikaNicholson dan Carlisle tokoh yang pertamamenemukan kemampuan untuk mendekomposisi air. Pada tahun 1902 lebihdari 400 industri elektrolisis air yang telah beroperasi dan pada tahun 1939 telah beroprasi pabrik elektrolisis air berkapasitas besar pertama dengan kapasitas 10.000 Nm3 H2 / jam. Pada tahun 1948 , electroliser bertekanan untuk industri pertama kali dproduksi olehdiproduksi oleh Zdansky / Lonza . Pada tahun 1966 ,sistem elektrolit padat dari bahan polimer dibuat dibangun oleh General electrik , dan pada tahun 1972, oksida padat unit elektrolisis airdikembangkan . Elektrolisis dengan sistem alkali dimulai pada tahun 1978 . Saat ini telah dikembangan membran pertukaran proton , digunakan untuk unit elektrolisis air dan sel bahan bakar , yang diproduksi oleh DuPont dan produsen lain , sejalan dengan perkembanganbidang teknologi oksida padat pada suhu tinggi dan optimalisasi serta rekonstruksi elektrolisis air pada sistem alkali(Kreuter, 1998).
Faraday mempelajari hubungan antara jumlah listrik yang digunakan pada elektrolisis dengan massa produk yang dihasilkan. Hukum faraday pertama mengenai elektrolisis menyatakan bahwa jumlah perubahan kimia yang terjadi pada proses elektrolisis bergantung pada jumlah muatan listrik yang melalui sel lektrolisis tersebut. Hukum faraday kedua menyatakan bahwa dalam elektrolisis jumlah muatan listrik yang sama akan menghasilkan jumlah ekuivalen yag sama pula tanpa bergantung jenis zat yang terlibat dalam reaksi lektrolisis.
maka sejumlah muatan listrik sebesar satu faraday (satu faraday sama dengan 1 mol elektron = 96500 coulomb per mol e-) yang lewat melaui sel akan menyebabkan perubahan senyawa yang terlibat dalam reaksi tersebut sesuai dengan koefisienya (dalam satuan mol).
Reaksi oksidasi air yang terjadi pada anoda suatu sel elektrolisis :
2 H2O O2(g) + 4H+ + 4e
-Persamaan diatas didasarkan atas pembentukan 4 mol elektron, apabila ditulis berdasarkan pembentukan satu mol elektron, maka akan diperoleh :
½ H2O ¼ O2(g) + H+ + e
-Dengan demikian, apabila muatan listrik 1 faraday dilakukan pada ssel elektrolisis diatas, maka berdasarkan hukum faraday kedua perubahan yang terjadi adalah ½ mol air (9 gram) berubah menjadi ¼ mol O2 (8 gram) dan 1 mol H+ (1 gram). Jadi, untuk reaksi reduksi, satu ekuivalen dapat didefenisikan sebagai koefisien reaksi dari species yang bersangkutan apabila reaksi berdasarkan perpindahan 1 mol elektron. Jadi untuk reaksi diatas, 1 ekuivalen adalah sama denngan ½ mol H2O, ¼ mol O2, dan 1 mol H+.
Karena arus listrik sebesar 1 ampere menyatakan perpindahan muatan sebesar 1 coulomb perdetik, maka :
A x t = C
A = arus (ampere)
t = waktu (det)
Dengan menggunakan persamaan diatas, massa senyawa yang diendapkan selama proses elektrolisis berlangsung dapat ditentukan (Bird, 1993)
2.6 Elektrolisis Larutan Metanol
Jika air membutuhkan minimum beda potensial teoritis sebesar 1.23 V untuk dielektrolisis, larutan methanol hanya membutuhkan beda potensial teoritis sebesar 0.02 V untuk dapat dielektrolisis dan menghasilkan hydrogen. Prinsip elektrolisis larutan methanol mengikuti reaksi berikut :
Anoda : CH3OH + H2O CO2 + 6H+ 6e-
Katoda : 6H+ 6e- 3H2
Sehingga secara keseluruhan reaksinya adalah :
BAB 3
METODE PENELITIAN
3.1 Alat dan Bahan 3.1.1. Alat
− Peralatan gelas Pyrex
− Timbangan elektrik Metler Toledo
− Hot plate stirer IKA
− Oven Memert
− Colorimeter HACH
− Spcektrofotometer UV-Visible Perkin Elmer
− pH meter Hanna
− Rotari evaporator Hadolp
− Power Suplay − Elektroda karbon
− Peralatan Kromartrogafi Gas Agilent
3.1.2. Bahan − Arang aktif
− NaCl p.a (E.Merck)
3.2 Prosedur Penelitian 3.2.1 Pembuatan Karbon Aktif
- Cangakang kelapa sawit dikeringkan dalam oven pada suhu 110oC selama 24 jam - Didinginkan
- Dihaluskan
- Dikarbonisasi pada suhu 400oC dalam tanur listrik selama 1 jam - didinginkan
- Ditimbang 20 g karbon hasil karbonisasi dan dimasukkan kedalam labu alas - Ditambahkan 200 mL KOH (1:1/KOH:karbon)
- Dipanaskan pada suhu 80O C dan diaduk selama 2 jam - Disaring dengan pompa vakum
- Dikeringkan dalam oven pada suhu 120Oselama 24 jam - Dikarbonisasi kembali pada suhu 800OC selama 45 menit - Didinginkan
- Dicuci dengan akuades dan HCl 0.1 M sampai pH 7 - Dikeringkan pada suhu 120O C selama 24 jam - Didinginkan dan disimpan dalam desikator
3.2.2 Penentuan kadar air karbon aktif (ASTM D 2867-91-1991) - Dipanaskan cawan porselin dalam oven pada suhu 140o C selama 1 jam - Didinginkan dalam desikator selama 30 menit
- Ditimbang hingga berat konstan - Dimasukkan 5 g karbon aktif
- Dipanaskan dalam oven pada suhu 1050 C selama 3 jam - Didinginkan dalam desikator selama 30 menit
- Ditimbang hingga berat konstan
3.2.3 Uji Adsorbsi Karbon Aktif Terhadap Metilen Biru 3.2.3.1 Pembuatan Larutan Standar Metilen Biru
3.2.3.1.1Pembuatan Larutan Standar Metilen Biru 100 ppm - Ditimbang 0,01 g serbuk metilen biru
- Dimasukkan kedalam gelas beaker 50 mL - Dilarutkan dengan akuades
- Dimasukkan kedalam labu takar 100 mL
- Ditambahkan dengan akuades sampai garis tanda
3.2.3.1.2Pembuatan Larutan Standar Metilen Biru 25 ppm - Dipipet sebanyak 25 mL larutan standar metilen biru 100 ppm - Dimasukkan kedalam labu takar 100 mL
- Ditambahkan akuades sampai garis tanda
3.2.3.1.3Pembuatan Larutan Standar Metilen Biru 1; 2; 3; 4; & 5 ppm - Dipipet sebanyak 1; 2; 3; 4; dan 5 mL larutan standar metilen biru 25 ppm - Dimasukkan kedalam labu takar 25 mL
- Ditambahkan akuades sampai garis tanda
3.2.3.2 Penentuan λ Maksimum Metilen Biru
Larutan standar metilen biru 10 ppm diukur absorbansinya dengan spektrofotometer Ultra violet pada panjang gelombang 610-680 nm.
3.2.3.3 Adsorbsi metilen biru Menggunakan karbon aktif (JIS K 1470-1991)
- 0,1 g karbon aktif dimasukkan dalam gelas beaker 250 mL - Ditambahkan 200 mL larutan standar metilen biru 50 ppm - Diaduk dengan pengaduk maknetik selama 24 jam
- Ditentukan kadar metilen biru dalam filtrat dengan spektrofotometer UV Visibel pada panjang gelombang 660 nm
3.2.4 Uji Adsorbsi Karbon Aktif Terhadap Iodin (ASTM D4607-94) - Ditimbang 0.1 g arang aktif dan dimasukkan kedalam Erlenmeyer
- Ditambahkan 5 mL HCl 5% dan diaduk - Dididihkan kemudian didinginkan - Ditambahkan 10 mL larutan iodin 0.1 N - Diaduk selama 4 menit
- Disaring
- Filtrat dititrasi dengan larutan Na2S2O3 0.1 N dan dengan menggunakan indikator amilum
3.2.5 Penentuan Kadar Lemak dan Minyak - 100 mL limbah dimasukkan kedalam corong pisah - Ditambahkan H2SO4 1: 1 sampai pH ≤ 2
- Diekstraksi dengan 100 mL N-Heksana - Didiamakan sampai terbentuk dua lapisan
- Diekstraksi kembali lapisan bawah dengan 100 mL N-Heksana
- Dilewatkan ekstrak melalui kertas saring dengan kristal natrium sulfat diatasnya dan ditampung dalam labu alas
- Diuapkan pelarut N-heksana dengan rotari evaporator - Dikeringkan dalam oven selama 30 menit
- Didinginkan dalam desikator - Ditimbang
3.2.6 Uji Adsorbsi Arang Aktif Tehadap Lemak dan Minyak Dalam Limah Cair Industri Biodisel
- Ditambahakan berat tertentu arang aktif
- Diaduk dengan maknetik stirer selama 40 menit - Disaring
- Dianalisis kadar lemak dan minyak dari filtrat
3.2.7 Uji Penurunan pH dengan Proses Elektrolisis - Dirangkai peralatan elektrolisis
- Dinyalakan sumber arus
- Diatur kuat arus pada 10 Ampere
- Diamati dan dicatat perubahan pH setiap 10 menit sampai pH 2
3.2.8 Pembuatan jembatan Garam - Ditimbang 3 g tepung agar
- Dimasukkan kedalam gelas beaker 250 mL - Ditambahkan 100 ml NaCl jenuh
- Dipanaskan sambil diaduk sampai mendidih - Dituangkan kedalam pipa U
- Didinginkan sampai terbentuk gel
3.2.9 Deadsorbsi lemak dan minyak dalam karbon aktif
- Dikeringkan karbon aktif setelah digunakan dalam adsorbsi dalam oven pada suhu 105o C selama 1 jam
- Direndam dalam 100 mL methanol sambil diaduk selama 30 menit - Disaring
3.3 Bagan Penelitian
3.3.1 Bagan rencana penelitian secara umum
Skema 3.1. Bagan penelitian Pembuatan Karbon Aktif
Karbon Aktif + Minyak / lemak
3.3.2 Pembuatan Karbon Aktif
3.3.3 Penentuan Kadar Air Arang Aktif
Cangkang Kelapa Sawit
Dikeringkan dalam oven pada suhu ± 110oC selama 24 jam
Didinginkan
Dihaluskan
Dikarbonisasi dalam tanur listrik pada suhu 400o C
selama 1 jam Didinginkan
Di tambahkan 200 mL KOH (1:1/ KOH:karbon)
Dipanaskan pada suhu 80 O C dan diaduk selama 2 jam
Disaring dengan pompa vakum
Arang Aktif
Dikeringkan dalam oven pada suhu 120 O C selama 24 jam
Dikarbonisasi kembali pada suhu 800O C selama 45 menit
Didinginkan
Dicuci dengan akuades dan HCl 0.1 M sampai pH 7
Dikeringkan dalam oven pada suhu 120O C selama 24 jam
Didinginkan dan disimpan dalam desikator
Ditimbang 2 g hasil karbonisasi dan dimasukkan dalam labu alas
5 g karbon Aktif
Dimasukkan kedalam cawan porselin yang telah dikeringkan dan ditimbang
Dipanaskan dalam oven pada suhu 105oC selama 3 jam
Didinginkan dalam desikator selama 30 menit
Ditimbang hingga berat konstan
3.3.4 Uji Adsorbsi Arang Arang Aktif Terhadap Metilen Biru 3.3.4.1Pembuatan larutan standar metilen biru
3.3.4.1.1 Pembauatan larutan standar metilen biru 100 ppm
3.3.2.1.1 Pembauatan larutan standar metilen biru 25 ppm
3.3.2.1.1 Pembauatan larutan standar metilen biru 1, 2, 3, 4, dan 5 ppm
0,01 g serbuk metilen biru
Dimasukkan kedalam gelas beaker 50 mL
Dilarutkan dengan akuades
Dimasukkan kedalam labu takar 100 ml
Ditambahkan akuades sampai garis tanda
100 ppm metilen biru
25 mL larutan standar metilen biru 100
Dimasukkan kedalam labu takar 100 mL
Ditambahakan akuades sampai garis tanda
25 ppm metilen biru
Dimasukkan kedalam labu takar 25 mL
Ditambahakan akuades sampai garis tanda 1, 2, 3, 4, dan 5 mL larutan standar metilen biru 25 ppm
3.3.2.1.2 Adsorbsi metilen biru menggunakan karbon aktif (JIS K 1470-1991)
3.3.5 Uji Adsorbsi Arang Arang Aktif Terhadap Iodin (ASTM D4607-94)
0,1 g Karbon aktif
Dimasukkan kedalam gelas beaker 250 mL
Ditambahkan 200 mL metilen biru 50 ppm
Diaduk dengan penganduk maknetik selama 24 jam
Disaring
Ditentukan kadar metilen biru dalam filtrat dengan
spektofotometer UV Visibel pada panjang gelombang 660 nm
Hasil
0,1 g Karbon aktif
Dimasukkan kedalam erlenmeyer
Ditambahkan 5 mL HCl 5% dan diaduk
Dididihkan kemudian didinginkan
Ditambahkan 10 mL larutan iodine 0,1 N
Diaduk selama 4menit dan disaring
Hasil
3.3.6 Penentuan Kadar Lemak dan Minyak
3.3.7 Uju Adsorbsi Arang Aktif terhadap Lemak dan Minyak
200 mL Limbah
Dimasukkan kedalam gelas beaker
Ditambahkan H2SO4 1 : 1 sampai pH ≤ 2
Ditambahkan berat tertentu aktif
Diaduk dengan maknetik stirer selama 40 menit
Disaring
Dianalisa kadar lemak dan minyak
Hasil
100 mL Limbah
Dimasukkan kedalam corong pisah
Ditambahkan H2SO4 1 : 1 sampai pH 2
Diekstraksi dengan 100 mL N-Heksana
Didiamkan sampai terbentuk dua lapisan
Diekstrasi kembali lapisan bawah dengan 100 mL N-Heksana
Dilewatkan ekstrak melalui kertas saring dengan kristal Natrium sulfat diatasnya dan ditampung dalam labu takar
Diuapkan pelarut N-Heksana dengan rotari evaporator
Hasil
Dikeringkan dalam oven selama 30 menit
3.3.8 Uji Penurunan pH dengan Proses Elektrolisis
3.3.9 Pembuatan jembatan garam
3 g Tepung agar
Dimasukkan kedalam gelas beaker 250 mL
Ditambahkan 100 mLNaCL jenuh
Dipanaskan dan diaduk sampai mendidih
Dituangkan kedalam pipa U dan didinginkan samapai terbentuk gel
Hasil
Dimasukkan kedalam beaker gelas
Dirangkai peralatan Elektrolisis
Dinyalakan sumber arus
Diatur kuat arus pada 10 Ampere
Diamati perubahan pH setiap 10 menit sampai pH 2 200 mL Limbah
3.3.10 Deadsorbsi Lemak dan Minyak dalam Karbon Aktif
Dikeringkan dalam lam oven pada suhu 105oC selama 1 jam
Direndam dalam 100 ml metanol dan diaduk selama 30 menit
Disaring
Dikeringkan kembali dalam oven pad suhu 105oC selama 1 jam
Didinginkan dan disimpan dalam desikator Karbon Aktif Bekas
BAB 4
HASIL DAN PEMBAHASAN 4.1 Analisis Limbah Cair Industri Biodisel
Analisis limbah cair industri biodisel meliputi analisis pH, kadar metanol, kadar lemak dan minyak, kadar COD dan turbiditi. Analisis kadar metanol ditentukan dengan kromatografi gas. Analisis kadar lemak dan minyak ditentukan dengan metode gravimetri, sedangakan analisis kadar COD dan turbiditi ditentukan dengan metode spectrofotometer. Hasil analisa limbah cair industri biodisel diberikan dalam tabel 4.1 berikut :
Tabel 4.1 Hasil Analisa limbah Cair Industri Biodisel
Parameter Metode Hasil
pH 5,8
Metanol (%) Kromatografi 0.87
Lemak dan Minyak (ppm)
Gravimetri 885
COD (ppm) Spectrofotometri 15680
4.2 Karakterisasi Karbon Aktif
Karakterisasi karbon aktif meliputi penentuan kadar air, uji adsorbsi terhadap metilen biru, dan uji adsorbsi terhadap larutan iodin.
4.2.1 Penentuan Kadar Air
Tabel 4.2 Kadar Air Karbon Aktif
Parameter Metode Hasil
Kadar Air (%) Gravimetri
3,19 % (Pengulangan 1) 3,00 % (Pengulangan 2) 3,20 % (Pengulangan 3)
Rata-rata = 3,13 %
Dari data diatas didapat kadar air karbon aktif dari cangkang kelapa sawit dalam penelitian ini masih sesuai dengan standar nasional indonesia SNI 06-3730-1995 yaitu maksimum 4,5 %.
4.2.2 Uji Adsorbsi Karbon Aktif Terhadap Metilen Biru a. Penentuan panjang gelombang (λ) maksimum
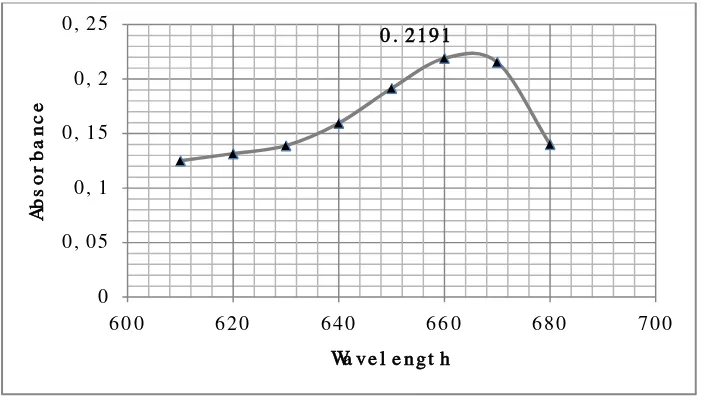
Penentuan panjang gelombang (λ) maksimum ini diperoleh dengan cara mengukur larutan metilen biru 10 ppm pada berbagai variasi panjang gelombang yaitu 610-680 nm dengan menggunakan spektrofotometer perkin elmer lamda 25. Data pengukuran ditunjukkan dalam gambar berikut :
Gambar 4.1 kurva penentuan λ maksimum 0. 2191
600 620 640 660 680 700
Dari gambar diatas terlihat bahawa panjang gelombang maksimum untuk metilen biru yaitu pada 660 nm yang ditunjukkan dengan nilai absorbansi yang lebih besar jika dibandingkan dengan absorbansi pada panjang gelombang lainya.
b. Pembuatan kurva kalibrasi metilen biru
Kurva kalibrasi ditentukan dengan mengukur absorbansi berbagai konsentrasi larutan metilen biru pada panjang gelombang 660 nm. Grafik hasil pengukuran ditunjukkan pada grafik dibawah ini:
Gambar 4.2 kurva kalibrasi Metilen Biru Dari kurva kalibrasi diatas didapat persamaan garis lurus sebagai berikut: y = 0,0224x + 0,0007
c. Penentuan adsorbsi metilen biru
Penentuan adsorbsi dilakukan dengan mengontakkan 0.1 g karbon aktif dengan 200 mL larutan standar metilen biru 50 ppm, selama 24 jam, kemudian ditentukan kadar metilen biru sebelum dan setelah dikontakkan dengan karbon aktif. Data penentuan adsorbsi metilen biru ditunjukkan dalam table 4.4 dibawah ini:
Tabel 4.3 Penentuan Adsorbsi Metilen Biru
Parameter Metode Hasil
Adsorbsi metilen biru (mg/g) Spektrofotometri
74 (Pengulangan 1) 74 (Pengulangan 2) 72 (Pengulangan 3)
Rata-rata = 73 mg/g
4.2.3 Uji Adsorbsi Karbon Aktif Terhadap Iodin
Uji adsorbsi Iodin dengan karbon aktif dilakukan dengan menggunakan 50 mL larutan iodin 0, 1 N yang dikontakkan dengan 0,1 g karbon aktif selama 15 menit kemudian disaring dan di tentukan kembali konsentrasi larutan iodin dengan metode volumetri. Data daya serap karbon aktif terhadap larutan iodin di tunjukkan dalam tabel 4.5 berikut:
Tabel 4.4 Penenuan Adsorbsi Iodin
Parameter Metode Hasil
Daya serap iodin
(mg/g) Gravimetri
975,6 (Pengulangan 1) 994,6 (Pengulangan 2) 984,4 (Pengulangan 3)
Rata-rata = 984,8 mg/g
4.3 Penentuan Kondisi Optimum Adsorbsi Lemak dan Minyak 4.3.1 Penentuan pH Optimum
Penentuan pH optimum adsorbsi minyak dan lemak dari limbah cair dilakukan dengan memvariasikan pH limbah cair yang kemudian di kontakkan dengan karbon aktif. Hasil penentuan pH optimum terlihat pada grafik dibawah ini :
Gambar 4.3 Pengaruh pH terhadap adsorbsi minyak dan lemak 4.3.2 Penentuan Waktu Kontak Optimum
Waktu kontak optimum ditentukan dengan mengontakkan limbah cair biodisel dengan karbon aktif dengan berbagai variasi waktu pengadukan. Data waktu kontak optimum ditunjukkan dalam grafik dibawah ini:
4.4Isoterm Adsorbsi Freunlich
Untuk menentukan kuantitas karbon aktif sebagai adsorben minyak dan lemak dalam limbah industry biodisel dapat diunakan persamaan isotherm adsorbsi freunlich, data penentuan isotherm adsorbsi ditunjukkan dalam table 4.6 dibawah ini:
Table 4.5 Isoterm adsorbsi freunlich
Berat
Gambar 4.5 Kurva Isoterm Adsorbsi Freunlich
Dari uji isoterm adsorbsi freunlich didapat nilai log K = 0.934 dan 1/n = 0.095 dengan demikian didapat persamaan freunlich sebagai berikut :
log��
1,50 1,70 1,90 2,10 2,30
log q
e
Dimana, qe = berat lemak dan minyak yang terserap dalam karbon aktif (mg), m = berat karbon aktif (g),Ce = kadar lemak dan minyak dalam kesetimbangan setelah adsorbsi.
4.5Penurunan pH Limbah Cair Biodisel dengan Elektrolisis
Elektrolisis digunakan untuk menurunkan pH limbah cair industri menggunakan elektroda karbon dengan dimensi Panjang x Lebar x Tebal, 10 x 2 x 0,03 cm. Jembatan garam NaCl. Sumber arus searah 10 Ampere. Dalam percobaan digunakan 1000 mL air limbah cair dengan pH awal ± 5 yang dibagi dalam 5 wadah masing-masing 200 mL yang di elektrolisis pada kutup positif. Data penerunan pH limbah cair biodisel ditunjukkan dalam Grafik dibawah ini.
Gambar 4.6 Kurva Penuruan pH limbah Cair Industri Biodisel
4.6Adsorbsi kandungan lemak dan minyak dalam limbah cair industri dengan karbon aktif
Adsorbsi lemak dan minyak dalam limbah cair biodisel menggunakan karbon aktif dengan berat sesuai dengan perhitungan persamaan freunlich , dan dikontakkan selama 40 menit serta diaduk dengan pengaduk elektrik pada 350 rpm. Limbah cair pembuatan biodisel yang digunakan adalah limbah cair yang telah diturunkan pHnya dengan proses elektrolisis pada sub bab sebelumnya. Setelah adsorbsi dengan karbon aktif limbah cair industry dielektrolisis kembali dengan menempatkan pada kutup
negatif untuk menaikkan kembali pH dari limbah cair tersebut.Berikut data peningkatan pH dengan proses elektrolisis.
Gambar 4.7 Kurva peningkatan pH limbah cair setelah elektrolisis kembali
Hasil analisa limbah cair industri biodisel sebelum dan sesudah di lakukan pengolahan dengan proses elektrolisis dan adsorbsi dengan karbon aktif ditunjukkan dalam tabel dibawah ini.
Tabel 4.6 Hasil Analisis Limbah Cair Industri Biodisel Setelah Elektrolis dan Adsorbsi Menggunakan Karbon Aktif
Parameter Metode Sebelum
perlakuan
COD (ppm) Spectrofotometri 17850 27
Turbiditi (NTU) Spectrofotometri 850 0
Data diatas menunjukkan bahwa kadar pH, COD dan kadar lemak dan minyak dari limbah cair industri diatas telah memenuhi Peraturan menteri negara lingkungan hidup tahun 2009 mengenai baku mutu limbah industry oleokimia dasar.
Jika dibandingkan dengan penelitian yang telah dilakukan sebelumnya mengenai pengolahan limbah cair indurtri biodiesel ada bebrapa hal yang dihasilkan lebih baik dari penelitian ini, diantaranya: pada pengolahan secara kimia dengan penambahan zat pengendap maupun pengolahan secara biologis dengan menggunakan bakteri keduanya menggunakan beberapa bahan kimia seperti urea, KH2PO4 dan MgSO4. 7H2O sebagai sumber nutrient bagi bakteri pengurai tersebut, sedangkan pada penelitian ini hanya digunakan garam NaCl sebagai jembatan garam. Selain itu jika dibandingkan dengan metode elektrokoagulasi, pada metode elektrokoagulasi dihasilkan endapan hasil koagulasi sehingga perlu dilakukan pengolahan lebih lanjut sedangkan pada penlitian ini dihasilkan karbon aktif bekas adsorbsi lemak dan minyak yang dapat di deadsorbsi kembali menggunakan methanol sehingga dapat digunakan kembali.
4.7Uji deadsorbsi dan pemakaian kembali karbon aktif dari cangkang kelapa sawit
Hasil analisis uji adsorbsi terhadap lemak dan minyak dengan menggunakan karbon aktif setelah deadsorbsi ditunjukkan dalam table 4.8 berikut.
Tabel 4.7 Perbandingan Adsorbsi Karbon aktif bekas dan baru
BAB 5
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan penelitian mengenai penurunan kadar lemak dan minyak limbah cair industri pembuatan biodiesel dengan proses elektrolisis dan adsorbsi menggunakan karbon aktif yang telah dilakukan dapat disimpulkan bahwa, kadar lemak dan minyak dalam limbah cair industri pembuatan biodiesel dapat diturunkan dengan menggunakan elektrolisis untuk penurunkan pH limbah cair dari pH awal 5 menjadi pH 2, dengan waktu elektrolisis selama 50 menit dan karbon aktif yang digunakan dalam penelitian ini dapat mengadsorbsi kandungan lemak dan minyak dalam limbah cair industri biodiesel sehingga limbah cair hasil pengolahan sesuai dengan peraturan menteri lingkungan hidup nomor 10 tahun 2009 tentang baku mutu air limbah bagi usaha dan/atau kegiatan industri oleokimia dasar.
5.2 Saran
DAFTAR PUSTAKA
Abechi, S.,E., Gimba C.,E., Uzairu, A., Dallatu, Y.,A. 2013. Preparation and Characterization of Activated Carbon from Palm KernelShell by Chemical Activation.Research Journal of Chemical Sciences, Vol. 3(7), 54-61
Allwar, 2012. Characteristics of Micro- and Mesoporous Structure and Surface Chemistry of Activated Carbons Produced by Oil Palm Shell.
International Conference on Chemical, Ecology and Environmental Sciences.
Allwar , 2012. Characteristics of Pore Structures and Surface Chemistry of Activated Carbons by Physisorption, Ftir And Boehm Methods.Journal of Applied Chemistry. Volume 2. 10-15.
Arami, A., Daud, W.M.A., Majlli, M.S., 2010. Production of Palm Shell Based Activated Carbon With More Homogeniouse Pore Zise Ditribution. Journal of Applied Sciences 10 (24) , 3361-3366.
Anh T. P., Thosio S., 2012. Efficient Hydrogen from Aqueous Methanol in a proton Exchange Membrane Electrolyzer with Porous Metal Flow Fields. International Journal of Automitive Engineering 3(2012) 125-130.
Bird, T. 1993. Kimia Fisik Untuk Universita. Jakarta: Gramedia Pustaka Utama Congkhong, S., Tongurai, C., Chetpattananondh, P., Bunyakan, C.,
2007
.
Biodiesel production by esterification of palm fatty acid distillate . Biomass & Energy.Fessenden, R. J., Fessenden, J. S., 1995. Kimia Organik. Jilid 2, Jakarta. Penerbit Erlangga.
Gerhard, K., Gerpen, J.V., Jurgen, K. 2005. The Biodiesel Handbook. AOCS PRESS. Champaign, Illinois.
Schuchardt, U.,Sercheli, R., Vargas, R.M. 1997. Transesterification of vegetable oils: A review. J. Braz. Chem. Soc., Vol. 9, No. 1, 199-210.
Harsanti, E., S. 2011. Arang Aktif Meninngkatkan Kualitas Lingkungan. Agroinovasi Edisi 6.
Huang, Y. R., Shiau, C. Y., Hung, Y. C., & Hwang, D. F. 2007. Application of Electrolyzed water in the Food Industry. Journal Food Control, 19, 329– 345.
Kreuter W., Hofmann H., 1998. Electrolysis: the important energy transformer in a world of sustainable energy. Int J. Hydrogen Energy 28(8), 661-666 Ngamlerdpokin, K., Kumjadpai, S., Chatanon, P., Tungmanee, U.,
Chuenchunchom, S., Jaruwat, P., Lertsathitphongs, P., Hunsom, M. 2011. Remediation of Biodiesel wastewater by-Chemical-and Electro-Coagulation: A comparative Study. Journal of Environment Management. 2454-2460.
Okiel, K., El-Sayed, M., El-Kady, M.Y., 2011. Treatment of Oil-Water Emulsions by Adsorbtion onto Activated Carbon, Bentonite and Deposited Carbon. Egyptian Journal of petroleum. 20. 9-15.
Othmer, K. 1992. Encyclopedia OfChemical Technology. 2nd Edition Vol. 4, John Willy and Sons.
Peraturan Menteri Negara Lingkungan Hidup Nomer 10 Tahun 2009, Baku Mutu Air Limbah Bagi Usaha dan/atau Kegiatan industri Oleokimia Dasar. Puspita, D. 2008. Penurunan Konsentrasi Total Suspended Solid (TSS) pada
Limbah Laundry Dengan Menggunakan Reaktor Biosand Filter Disertai Dengan Reaktor Activated Carbon. Yogyakarta.
Sahira,J., Mandira, A., Prasad, P.B., Ram, P.R. Effects of Activating Agent on the Activated Carbon Prepared from Lapsi Seed Stone. Research Journal of Chemical Sciences, Vol. 3(5), 19-24.
Samuel, D., 1983. Chemistry Of Water Treatment. Better Work Publisher
Singgih, H., & Ratnawati. 2010. Pembuatan Arang Aktif dari tempurung Kelapa Sawit dengan Metode Aktivasi Kimia. Jurnal Sains Materi Indonesia, Vol 12, No. 1: 12-16.
Sreve, R., N. 1977. Chemical Process Industries. McgrowHill Kogasha.
Srirangsan, A., Ongwande, M., Chavalparit, O. 2009. Treatment of biodiesel Wastewater by Electrocoagulation Process. EnvironmentAsi: 15-19. Standard Methods for the Examination of Water & Wastewater.21th
Sudradjat, R. Tresnawati, D. dan Setiawan, D. 2004. Pembuatan Arang Aktif Dari Tempurung Biji Jarak Pagar (Jatropha curcas L.). Bogor.
Suehara, K., Kawamoto, Y, Fujii, E., Kohda, J., Nakano, Y., Yano, T. 2005. Biodiesel Treatment of Wastewater Discharged from Biodiesel Fuel Plant with Alkaly-Cstslyzed Transesterification. Journal of Bioscience and Bioengineering.Vol 100. No. 4: 437-442.
Taryana, M.2002. Arang Aktif ( Pengenalan dan Proses Pembuatanya). Skripsi Jurusan Teknik Industri, FT-USU.
Treybal, R., E. 1981. Mass Transfer Operation.McGrawHill.Third Edition. Tokyo.
Lampiran 1.
Perhitungan penentuan kadar air karbon aktif cangkag kelapa sawit
Penentuan kadar air ditentukan dengan rumus :
�������� (%) =��������������� − ���������������������������
��������������� ����
Pengulangan 1
=5,3000−5,1311
5,3000 x 100 = 3,19 %
Pengulangan 2
=5,3000−4,8510
5,3000 x 100 = 3,00 %
Pengulangan 3
=5,3000−4,8625
5,3000 x 100 = 3,20 %
Lampiran 2.
Perhitungan penentuan adsorbsi iodin pada karbon aktif cangkang kelapa sawit
Standarisasi larutan Na2S2O3 0,1 N Penentuan konsentrasi Iodin Awal
Penentuan konsentrasi Iodin Setelah Adsorbsi
Berat Iodin terserap per gram karbon Aktif (mg/g)
Lampiran 3.
Penentuan Persamaan garis regresi kurva kalibrasi metilen biru
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis: y = ax + b
Dimana : a = Slope b = Intercept
selanjutnya harga slope (a) dapat ditentukan dengan menggunakan metode least square sebagai berikut:
Maka persamaan garis yang diperoleh adalah :
Koefisien korelasi untuk kurva kalibrasi metilen biru adalah :
r = Σ(xi−x)(yi−y)
[Σ(xi−x)2Σ(yi−y)2]1/2=
0,3928
0,3924= �,���� Berat Metilen biru terserap per gram karbon Aktif (mg/g)
Lampiran 4.
Penentuan persamaan garis regresi Isoterm Adsorbsi freunlich
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
Persamaan garis regresi untuk isotherm adsorbsi freunlich dapat diturunkan dari persamaan garis:
y = ax + b Dimana : a = Slope b = Intercept
selanjutnya harga slope (a) dapat ditentukan dengan menggunakan metode least square sebagai berikut: Maka persamaan garis yang diperoleh adalah :
�= �,�����+�,���� Maka didapat nilai :
Koefisien korelasi untuk kurva isotherm adsorbsi freunlich adalah :
r = Σ(xi−x)(yi−y)
[Σ(xi−x)2Σ(yi−y)2]1/2=
0,1379
0,1397= �,����
Penentuan Kuantitas karbon aktif yang digunakan untuk adsorbsi lemak dan minyak
log��
� = 0.9346 + 0.0952 log��
Jika kadar lemak dan minyak dari limbah cair industry biodiesel adalah 542 mg/L dan diharapkan konsentrasi residu lemak dan minyak dalam limbah cair adalah 5 mg/L maka karbon aktif yang ditambahkan adalah:
log(542−5)
� = 0.9346 + 0.0952 log 5
log(537)
� = 0.9346 + (0.0952 � 0,6990)
log537
� = 1,0011
� = 537