AKTIVITAS ANTIOKSIDAN EKSTRAK PELEPAH POHON
AREN (
Arenga pinnata
Merr.)
NUR FITRIANI MOKOGINTA
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Aktivitas Antioksidan Ekstrak Pelepah Pohon Aren (Arenga pinnata Merr.) adalah benar karya saya dengan arahan pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Penelitian ini merupakan bagian dari penelitian Program Kreativitas Mahasiswa dengan judul Khasiat Limbah Abu Pelepah Aren sebagai Inhibitor Tirosinase dalam Bedak Dingin yang didanai oleh Direktorat Jenderal Pendidikan Tinggi. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Januari 2014
Nur Fitriani Mokoginta
ABSTRAK
NUR FITRIANI MOKOGINTA. Aktivitas Antioksidan Ekstrak Pelepah Pohon Aren (Arenga pinnata Merr.). Dibimbing oleh SULISTIYANI dan SYAEFUDIN. Pelepah aren telah dilaporkan mengandung senyawa tanin, namun belum ada informasi ilmiah mengenai potensinya sebagai antioksidan. Oleh karena itu, penelitian ini bertujuan menguji aktivitas antioksidan ekstrak pelepah aren (Arenga pinnata Merr.) secara in vitro. Penelitian ini menggunakan pelarut air, etanol 70% dan etanol 96%. Pelepah aren diekstraksi dengan pelarut air menggunakan metode perebusan, sedangkan ekstraksi dengan pelarut etanol 70% dan etanol 96% dilakukan dengan cara maserasi. Senyawa bioaktif dalam ekstrak ditentukan secara fitokimia. Aktivitas antioksidan ekstrak pelepah aren ditentukan dengan metode serapan radikal 1,1-difenil-2-pikrilhidrazil (DPPH) dan kandungan total fenoliknya diukur secara kolorimetri dengan metode Folin-Ciocalteu. Hasil penelitian menunjukkan bahwa ekstrak pelepah aren mengandung senyawa saponin, tanin dan fenol, serta steroid dan triterpenoid. Analisis aktivitas antioksidan menunjukkan bahwa baik ekstrak etanol 70% maupun ekstrak etanol 96% pelepah aren berpotensi sebagai antioksidan alami. Aktivitas antioksidan dan total fenolik yang tertinggi terdapat pada ekstrak etanol 96% (IC50 = 2.57 μgL-1; 3.75 GAE mgg-1).
Kata kunci: antioksidan, DPPH, pelepah aren, fitokimia, fenolik
ABSTRACT
NUR FITRIANI MOKOGINTA. Antioxidant Activity of Stem Sugar Palm Extract (Arenga Pinnata Merr.). Supervised by SULISTIYANI and solvent by boiling method and by maceration in ethanol 70% and 96% solvents. Bioactive compounds in the extracts were determined by phytochemical method. Antioxidant activity of stem sugar palm extracts were determined by 1,1-diphenyl-2-picrylhydrazyl radical absorption method (DPPH) and the content of the total phenolic measured in colometric with Folin-Ciocalteu method. The result showed that the stem sugar palm extracts contained saponin, tannin and phenol, and steroids and triterpenoid. Analysis of antioxidant activity showed that both ethanol 70% and 96% stem sugar palm extracts were potential as natural antioxidant. The highest antioxidant activity and the total phenolic value were showed by ethanol 96% extract (IC50 = 2.570 μgL-1; 3.75 GAE mgg-1).
AKTIVITAS ANTIOKSIDAN EKSTRAK PELEPAH POHON
AREN (
Arenga pinnata
Merr.)
NUR FITRIANI MOKOGINTA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Aktivitas Antioksidan Ekstrak Pelepah Pohon Aren (Arenga pinnata Merr.)
Nama : Nur Fitriani Mokoginta NIM : G84090086
Disetujui oleh
drh Sulistyani, MSc, PhD Pembimbing I
Syaefudin, SSi, MSi Pembimbing II
Diketahui oleh
Dr Ir I Made Artika, MAppSc Ketua Departemen
PRAKATA
Puji dan syukur hanya kepada Allah SWT atas segala nikmat dan karunia yang telah dilimpahkan-Nya, sehingga penelitian ini dapat diselesaikan. Shalawat beriring salam senantiasa penulis haturkan kepada Rasulullah SAW sebagai pembimbing dan teladan seluruh umat manusia. Penelitian ini dilaksanakan di Laboratorium Biokimia, Departemen Biokimia FMIPA IPB pada bulan Maret sampai Juni 2013, dengan judul “Aktivitas Antioksidan Ekstrak Pelepah Pohon Aren (Arenga pinnat Merr.)”.
Penulis mengucapkan terima kasih yang sebesar-besarnya pada drh Sulistyani, MSc, PhD dan Syaefudin, SSi, MSi atas bantuan dan bimbinganya sehingga penulis dapat menyelesaikan penelitian ini sebaik mungkin. Penulis juga mengucapkan terima kasih kepada pihak Direktorat Jenderal Pendidikan Tinggi yang telah mendanai penelitian ini hingga selesai, kepada kedua orang tua dan kak Rahmat atas segala doa dan dukungannya, serta teman-teman Biokima dan Staf Departemen Biokimia khususnya kak Yafet, kak Shelly, Yayuk Kartika, Azra Zahra NI, Mina Ervani, Andal Yakinudin, Dessy Amalia, Waliyudin, Pratiwi Hamsah, Kasita, Kharisma Panji, Novilia Eka dan mba Eli atas segala bantuan dan saran yang telah diberikan.
Penulis sangat menyadari sepenuhnya bahwa karya tulis penelitian ini secara ilmiah masih jauh dari kesempurnaan dan kekurangan dalam penyajiannya. Oleh karena itu, penulis sangat mengharapkan saran dan kritik yang membangun agar karya tulis penelitian selanjutnya menjadi lebih baik. Penulis berharap karya tulis penelitian ini dapat bermanfaat bagi pembaca dan perkembangan ilmu pengetahuan.
DAFTAR ISI
PENDAHULUAN 1
METODE 2
Bahan dan Alat 2
Prosedur Penelitian 2
HASIL 4
Kandungan Ekstrak Pelepah Aren 4
Pengujian Aktivitas Antioksidan dengan Metode DPPH 5
Total Fenolik 5
PEMBAHASAN 6
Kandungan Ekstrak Pelepah Aren 6
Aktivitas Antioksidan Ekstrak Pelepah Aren 7 Kandungan Fenol dalam Ekstrak Pelepah Aren 8
SIMPULAN 9
DAFTAR PUSTAKA 9
LAMPIRAN 12
DAFTAR TABEL
1 Hasil rendemen ekstrak pelepah aren 4
2 Hasil analisis fitokimia pelepah aren 5
3 Aktivitas antioksidan pada ekstrak pelepah aren dan standar α-tokoferol
berdasarkan nilai IC50 5
DAFTAR GAMBAR
1 Pohon aren (Arenga pinnata Merr.) 2
2 Kurva korelasi antara nilai total fenolik dan IC50 6
DAFTAR LAMPIRAN
1 Diagram alir penelitian 12
2 Contoh perhitungan rendemen 12
3 Gambar fitokimia ekstrak pelepah aren 12
4 Kurva standar asam galat 13
5 Contoh perhitungan total fenolik 13
6 Contoh perhitungan Aktivitas antioksidan 14
PENDAHULUAN
Perubahan gaya hidup masyarakat dewasa ini seringkali menjadi faktor penyebab munculnya beragam penyakit. Sebagian besar penyakit yang ditimbulkan merupakan akibat dari aktivitas dan terbentuknya radikal bebas secara berlebihan. Berbagai penelitian ilmiah mengungkapkan bahwa radikal bebas memiliki efek yang negatif bagi kesehatan tubuh apabila jumlahnya terlalu banyak karena dapat merusak berbagai jaringan tubuh, sel, DNA dan enzim-enzim tertentu (Supiyanti 2010; Panjaitan et al. 2011). Gaya hidup yang tidak sehat seperti konsumsi makanan instan dan minuman beralkohol, merokok, terpapar bahan-bahan kimia dan radiasi sinar matahari dapat meningkatkan produksi radikal bebas di dalam tubuh. Akibatnya radikal bebas merusak jaringan normal sehingga sistem kekebalan tubuh menurun dan tubuh mudah terserang penyakit.
Tubuh membutuhkan antioksidan untuk menjaga keseimbangan radikal bebas agar tidak mengakibatkan munculnya berbagai penyakit degeneratif dan penuaan dini. Antioksidan telah dikenal memiliki kemampuan meredam radikal bebas dengan cara memberikan atom hidrogennya sehingga dapat merubah radikal bebas menjadi non radikal. Selain itu, antioksidan juga dapat menurunkan reaktivitas radikal bebas sehingga tidak terjadi reaksi dengan molekul lain (Chanwitheesuk et al. 2004). Secara alami, tubuh memproduksi antioksidan untuk melindungi tubuh dari kerusakan yang dapat terjadi akibat kelebihan radikal bebas. Akan tetapi dalam keadaan tertentu tubuh tidak mampu menyeimbangkan radikal bebas di dalam tubuh (Jain et al. 2004). Oleh karena itu, dibutuhkan antioksidan tambahan dari luar baik itu antioksidan alami atau pun antioksidan buatan.
Umumnya penggunaan antioksidan alami lebih sering dimanfaatkan oleh masyarakat karena mudah diperoleh dan memiliki efek samping yang lebih kecil dibandingkan antioksidan buatan. Antioksidan alami dapat diisolasi dari tanaman jika mengandung senyawa yang dapat menangkal radikal bebas seperti flavonoid dan fenolik (Gupta dan Sharma 2006). Salah satu tanaman yang dapat dimanfaatkan sebagai antioksidan alami adalah pelepah tanaman aren (Gambar 1). Tanaman aren atau yang dikenal dengan sebutan enau merupakan sumber daya hayati yang diduga memiliki kemampuan antioksidan dan mudah ditemukan di seluruh wilayah Indonesia. Tanaman ini telah banyak dimanfaatkan oleh masyarakat seperti pada tepung pelepahnya dimanfaatkan sebagai obat tradisional penghilang gatal dan bekas luka pada kulit, serta penggunaan abu pelepahnya sebagai kosmetik tradisional (Sangi et al. 2012).
Gambar 1 Pohon Aren (Arenga pinnata Merr.)
(Sumber: Efendi 2009)
METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah pelepah aren, akuades, etanol 70%, etanol 96%, kertas saring, 1,1-difenil-2-pikrilhidrazil (DPPH), senyawa α-tokoferol, asam galat, pereaksi Follin Ciocalteu 10%, pereaksi Meyer, pereaksi Wagner, pereaksi Dragendroff, pereaksi asam Liebermann-Burchard, Na2CO3 7.5%, dan FeCl3 1% bb/v.
Alat yang digunakan adalah oven Eyela NDO-700, rotary evaporator Eyela OSB-2100, shaker, dan spektofotometer UV-VIS Genesys 10w thermo scientific.
Prosedur Penelitian
Preparasi Sampel
Pelepah pohon aren yang digunakan adalah pelepah yang sudah berusia tua yang ditandai dengan terlepasnya pelepah dari pohon dan berwarna coklat kehitaman. Pelepah tersebut dipotong dengan ukuran 2 cm. Kemudian pelepah digiling menjadi serbuk dengan ukuran 20 mesh sampai 60 mesh.
Ekstraksi Pelepah Aren
Ekstraksi dengan pelarut Air (modifikasi dari Harjadi 1993). Serbuk pelepah aren berukuran 20-60 mesh sebanyak 80 g ditambahkan air dengan perbandingan 1:10. Ekstraksi dengan air panas dilakukan pada temperatur 100 oC selama kurang lebih 1 jam. Selanjutnya ekstrak air disaring dan filtratnya dikeringkan dengan menggunakan rotary vaccum evaporator pada suhu 50°C-80°C hingga diperoleh ekstrak kasar kering.
dan didiamkan selama 24 jam. Maserat dipisahkan dan proses diulang 2 kali dengan jenis dan jumlah pelarut yang sama. Perbandingan sampel dan pelarut yang digunakan dalam maserasi adalah 1:10 (b:v). Filtrat yang diperoleh dipekatkan dengan rotavapor pada suhu 50 °C - 80 °C. Kemudian hasil pemekatan dihitung rendemennya dan disimpan dalam lemari es pada suhu 4 °C.
Uji Fitokimia (Modifikasi Harbone 1987)
Uji Alkaloid. Sebanyak 50 mg ekstrak ditambahkan 3 mL kloroform dan 3 tetes amoniak. Fraksi kloroform dipisahkan dan diasamkan dengan 10 tetes H2SO4 2 M. Fraksi asam diambil kemudian ditambahkan pereaksi Meyer, Wagner, Dragendroff. Senyawa alkaloid ditandai dengan terbentuknya endapan putih oleh pereaksi Meyer, endapan coklat oleh pereaksi Wagner, dan endapan merah oleh pereaksi Dragendroff. Sebagai kontrol positifnya digunakan daun tapak dara (Catharantus roseus).
Uji Steroid/triterpenoid. Sebanyak 50 mg ekstrak ditambah asam asetat anhidrida sampai terendam dalam tabung reaksi dan dipanaskan selama 5 menit. Setelah dipanaskan, campuran ekstrak didinginkan, kemudian ditambahkan
satu tetes H2SO4 pekat melalui sisi tabung. Warna hijau yang terbentuk menandakan adanya steroid dan warna merah menandakan adanya triterpenoid. Sebagai kontrol positif digunakan daun som jawa (Talinum paniculatum (Jacq). Gaertn).
Uji Flavonoid. Sebanyak 50 mg ekstrak ditambahkan metanol 30% sampai terendam dan dipanaskan selama 5 menit. Setelah dipanaskan, ekstrak disaring sehingga diperoleh filtratnya. Filtrat ekstrak kemudian ditambahkan satu tetes NaOH 10%. Warna merah pada filtrat menandakan adanya flavonoid. Sebagai kontrol positifnya digunakan buah harendong (Melastoma affine D. Don). Uji Saponin (Uji Busa). Sebanyak 50 mg ekstrak dimasukan dalam gelas piala kemudian ditambahkan 50 ml air panas dan didihkan selama 5 menit, setelah itu disaring dan filtratnya digunakan untuk pengujian. Uji saponin dilakukan dengan pengocokan 10 mL filtrat dalam tabung reaksi tertutup selama 10 detik kemudian dibiarkan selama 10 menit. Terbentuknya busa ketika larutan dikocok menandakan adanya saponin. Sebagai kontrol positif digunakan biji buah klerak (Sapindus rarak).
Uji Tanin dan Fenol. Sebanyak 102 mg ekstrak ditambahkan 2 mL air kemudian dididihkan selama beberapa menit. Lalu disaring dan filtratnya ditambah 1 tetes FeCl3 1% (bb/v). Warna biru tua atau hitam kehijauan menunjukkan adanya tanin. Sebagai pembanding digunakan daun teh (Camelia sinensis).
Pengukuran Aktivitas Antioksidan Ekstrak Pelepah Aren dengan Metode 1,1-difenil-2-pikrilhidrazil (DPPH)
panjang gelombang 517 nm. Kontrol positif yang digunakan adalah α-tokoferol pada berbagai konsentrasi ( 1, 2.5, 5, 7.5, dan 10 μgL-1) dan kontrol negatifnya yaitu larutan DPPH dengan etanol sebagai blanko. Nilai absorbansi yang diperoleh digunakan untuk mendapatkan persamaan regresi Y = a + b ln x dan nilai IC50. Adapun aktivitas persen penangkapan radikal DPPH (%) dihitung dengan rumus :
% inhibisi = x 100% Keterangan:
A0 = absorbansi kontrol negatif/absorbansi larutan DPPH tanpa sampel A = absorbansi sampel
Pengukuran Total Fenolik (Javanmardi et al. 2003)
Sebanyak 0.2 ml ekstrak pelepah aren dengan konsentrasi 500 μgL-1, 2.5 ml reagen Folin-Ciocalteu 10% dan 2 ml Na2CO3 7.5% dicampurkan dan diinkubasi selama 15 menit pada suhu 45°C. Absorban larutan diukur menggunakan spektrofotometer pada panjang gelombang 765 nm. Total fenolik ekstrak pelepah aren diekspresikan sebagai miligram (mg) asam galat ekuivalen per gram bobot ekstrak kering (GAE mgg-1 ekstrak pelepah aren). Sebagai standar digunakan asam galat pada berbagai konsentrasi (0, 20, 40, 60, 80, 100 μgL-1).
HASIL
Kandungan Ekstrak Pelepah Aren
Rendemen ekstrak diperoleh dari hasil pembagian bobot ekstrak dan bobot sampel terkoreksi. Hasil perhitungan rendemen yang diperoleh menunjukkan seberapa banyak senyawa bioaktif pelepah aren yang terekstrak pada pelarut sehingga dapat dianalisis lanjut. Berdasarkan hasil pengujian rendemen pada Tabel 1 diketahui bahwa ketiga ekstrak memiliki rendemen yang kecil. Ekstrak etanol 96% memiliki persentase rendemen yang paling tinggi, yaitu sebesar 0.022% sedangkan rendemen terkecil diperoleh dari ekstrak air, yaitu 0.002%.
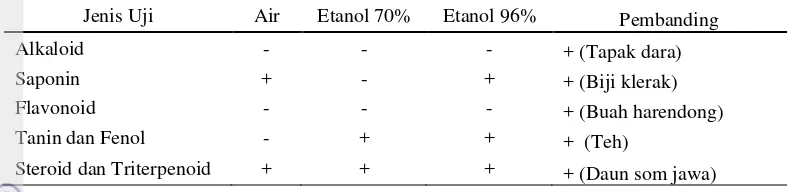
Berdasarkan hasil analisis fitokimia dapat diketahui bahwa ketiga ekstrak tidak mengandung senyawa alkaloid dan flavonoid. Senyawa steroid dan triterpenoid ditemukan dalam semua ekstrak yang diujikan, senyawa saponin hanya ditemukan pada ekstrak air dan ekstrak etanol 96%, serta senyawa tanin dan fenol hanya ditemukan pada ekstrak etanol 70% dan ekstrak etanol 96% (Tabel 2).
Tabel 1 Hasil rendemen ekstrak pelepah aren
Sampel Pelarut Kadar air
Tabel 2 Hasil analisis fitokimia pelepah aren
Pengujian Aktivitas Antioksidan dengan Metode DPPH
Aktivitas antioksidan pelepah aren diketahui dari nilai IC50 yaitu konsentrasi sampel yang mampu memberikan persen penangkapan radikal bebas sebanyak 50% dengan kontrol melalui persamaan garis (Rosiyana 2012). Hasil pengujian nilai IC50 rata-rata ekstrak etanol 96% sebesar 2.570 μgL-1 dan ekstrak etanol 70% sebesar 3.999 μgL-1 (Tabel 3). Jika dibandingkan dengan kontrol
positifnya yaitu α-tokoferol yang memiliki nilai IC50 sebesar 3.389 μgL-1, nilai IC50 rata-rata ekstrak etanol 96% lebih kecil dari α-tokoferol dan nilai IC50 ekstrak etanol 70% lebih besar dari nilai IC50 α-tokoferol. Artinya ekstrak etanol 96% adalah yang terbaik karena dapat menangkal 50% radikal bebas pada konsentrasi lebih kecil yaitu 2.570 μgL-1 dibandingkan dengan etanol 70%.
Tabel 3 Aktivitas antioksidan pada ekstrak pelepah aren dan standar α-tokoferol berdasarkan nilai IC50
Berdasarkan data absorbansi dari pengukuran total fenolik diperoleh persamaan garis yaitu y = 0.0704x – 0.0509 dengan r2 sebesar 98.83%. Persamaan tersebut digunakan untuk menghitung total fenolik pelepah aren. Hasil pengujian total fenolik pelepah aren dengan pelarut yang berbeda menunjukkan perbedaan kuantitas. Hasil yang diperoleh menunjukkan bahwa total fenolik ekstrak etanol 70% memiliki kandungan fenol sebesar 3.533 GAE mgg-1 dan ekstrak etanol 96% memiliki kandungan fenol sebesar 3.749 GAE mgg-1. Berdasarkan hasil tersebut dapat diketahui bahwa ekstrak terbaik adalah ekstrak etanol 96% karena memiliki kandungan fenol lebih tinggi dibandingkan ekstrak etanol 70% (Lampiran 5).
Berdasarkan analisis data statistik secara bivarian, total fenolik dan aktivitas antioksidan memiliki korelasi yang berbanding terbalik artinya semakin kecil nilai IC50 maka semakin besar nilai total fenolnya (Gambar 2). Hal ini ditunjukkan oleh koefisien total fenolik dan IC50 yang bernilai negatif pada analisis statistik yaitu -0.724. Korelasi tersebut bersifat signifikan secara statistika karena nilai p-value sebesar 0.028 berada di bawah 0.05 (Lampiran 8).
Gambar 2 Kurva korelasi antara nilai total fenolik dan IC50 (n = 3) Keterangan: a) ekstrak etanol 70% dan b) ekstrak etanol 96%
PEMBAHASAN
Kandungan Ekstrak Pelepah Aren
Pelepah aren memiliki senyawa bioaktif seperti tanin dan fenolik yang berperan sebagai antioksidan alami. Senyawa bioaktif ini dapat diidentifikasi melalui beberapa tahapan penting di antaranya ekstraksi, fitokimia, dan pengukuran fenolik secara kualitatif. Ekstraksi pelepah aren dilakukan dengan menggunakan pelarut air, etanol 70%, dan etanol 96%. Ekstraksi dengan pelarut etanol 70% dan etanol 96% dilakukan dengan metode maserasi yaitu perendeman pada suhu ruang karena sifatnya yang volatil atau mudah menguap. Jika ekstraksi dilakukan pada pelarut volatil dengan suhu tinggi dapat menyebabkan hasil ekstraksi kurang maksimal (Eleanore 2013). Sementara itu, ekstraksi dengan pelarut air dilakukan dengan metode perebusan pada suhu tinggi yaitu 100 0C selama 15 menit agar hasil ekstraksi maksimal. Pemanasan pelepah aren akan mengakibatkan terjadinya pelunakan komponen matrik pelepah sehingga senyawa bioaktif dalam pelepah aren akan keluar dan terlarut dalam pelarut air.
Tahapan selanjutnya dalam penelitian ini adalah analisis komponen kimia pada ekstrak pelepah aren. Analisis fitokimia dilakukan secara kualitatif untuk mengidentifikasi senyawa bioaktif yang terkandung dalam ekstrak pelepah aren seperti senyawa alkaloid, saponin, flavonoid, tanin, fenol, steroid dan triterpenoid. Perbedaan jenis pelarut yang digunakan dalam ekstraksi akan memberikan pengaruh yang berbeda pada hasil uji fitokimia karena pada setiap pelarut memiliki tingkat kepekatan yang berbeda dalam identifikasi zat bioaktif pada sampel pelepah aren (Anwariyah 2011; Egwaikhide dan Gimba 2007).
Hasil fitokimia secara umum menunjukkan ekstrak pelepah aren mengandung senyawa saponin, tanin dan fenol, serta steroid dan triterpenoid. Hal ini menunjukkan bahwa senyawa yang terkandung dalam ekstrak pelepah aren bersifat polar sehingga larut dalam pelarut polar seperti air dan etanol (Javanmardi
et al. 2003). Namun, pada ekstrak etanol 70% senyawa saponin tidak ditemukan. Diduga hal ini karena kandungan senyawa saponin yang terekstrak sedikit dalam pelarut etanol 70% sehingga pada pengujiaan tidak dapat diidentifikasi. Selain itu, senyawa tanin dan fenol tidak ditemukan pada ekstrak air karena sifat fisik senyawa tanin dan fenol yang kurang tahan panas dan mudah menguap selama perebusan (Molyneux 2003). Hal ini juga telah dibuktikan dalam penelitian Grafianita (2011) bahwa senyawa fenol dalam sampel menjadi berkurang akibat pemanasan dan kadar fenolnya menurun seiring lamanya waktu pemanasan. Oleh karena itu, senyawa tanin dan fenol tidak dapat diidentifikasi dalam analisis fitokimia karena diduga telah terdegradasi atau menguap.
Senyawa fitokimia dalam ekstrak pelepah aren seperti tanin dan triterpenoid juga ditemukan dalam ekstrak tepung gabah pelepah aren dari penelitian Sangi et al. (2012). Dalam penelitian tersebut, ekstraksi tepung hanya menggunakan pelarut etanol. Pengujian fitokimia ekstrak etanol tepung gabah pelepah aren juga menemukan adanya senyawa alkaloid. Namun senyawa alkaloid dalam penelitian ini tidak ditemukan pada ekstrak simplisia pelepah aren.
Aktivitas Antioksidan Ekstrak Pelepah Aren
Analisis aktivitias antioksidan ekstrak pelepah aren diukur dengan metode DPPH. Radikal bebas DPPH merupakan radikal sintetik yang bersifat peka terhadap cahaya, oksigen, dan pH namun stabil pada suhu ruang dan larut dalam pelarut polar seperti metanol dan etanol (Molyneux 2003). Uji antioksidan dengan metode peredaman DPPH ini dilakukan lebih lanjut dengan mengukur sejauh mana reaksi peredaman DPPH berlangsung. Pengukuran dilakukan secara spektrofotometri dengan mengukur serapan dari sampel yang telah direaksikan dengan larutan DPPH pada panjang gelombang 517 nm dan hasilnya diinterpretasikan dengan nilai inhibitor concentration (IC50) (Yuhernita dan Juniarti 2011).
Adapun pembanding yang digunakan dalam penelitian ini adalah α -tokoferol yang merupakan karateristik utama dari vitamin E. Vitamin ini merupakan antioksidan larut lemak yang baik untuk kesehatan tubuh manusia karena berperan melindungi fosfolipid dalam membran dari degradasi oksidatif
peroksil (hasil peroksida lipid) menjadi radikal tokoferol yang kurang reaktif, sehingga tidak mampu merusak rantai asam lemak (Sareharto 2010). Oleh karena
itu, α-tokoferol dapat digunakan sebagai pembanding dalam pengukuran aktivitas antioksidan dengan metode DPPH.
Hanani et al. (2005) menginformasikan bahwa suatu bahan yang memiliki aktivitas antioksidan adalah jika memiliki nilai IC50 kurang dari 200 μgL-1. Berdasarkan literatur tersebut, hasil analisis aktivitas antioksidan diketahui bahwa baik ekstrak etanol 70% maupun ekstrak etanol 96% memiliki kemampuan antioksidan. Hal ini ditunjukkan dengan nilai IC50 yang kecil dari kedua ekstrak yaitu 3.999 μgL-1 pada ekstrak etanol 70% dan 2.570 μgL-1 pada ekstak etanol 96%. Nilai IC50 pada ekstrak etanol 96% menunjukkan aktivitas antioksidan yang
lebih tinggi dibandingkan ekstrak etanol 70% dan kontrol positifnya α-tokoferol (IC50 = 3.389 μgL-1). Hasil analisis statistika aktivitas antioksidan ekstrak etanol 70% dan ekstrak etanol 96% adalah berbeda nyata artinya perbedaan jenis pelarut atau konsentrasi pelarut yang digunakan berpengaruh nyata terhadap aktivitas antioksidan ekstrak pelepah aren (Lampiran 8).
Hasil penelitian Alfarabi (2010), melaporkan bahwa nilai IC50 ekstrak etanol 70% (85.82 μgL-1) daun sirih lebih tinggi dibandingkan dengan nilai IC50
α-tokoferol (2.12 μgL-1). Jika dibandingkan dengan hasil penelitian ini terdapat persamaan bahwa ekstrak etanol 70% juga memiliki nilai IC50 yang lebih tinggi
dibandingkan dengan α-tokoferol. Selain itu, dapat diketahui bahwa nilai IC50 α -tokoferol dalam penelitian ini memiliki nilai yang tidak berbeda jauh dengan nilai IC50 α-tokoferol pada penelitian Alfarabi dan memiliki aktivitas antioksidan yang kuat karena nilai IC50 nya kurang dari 200 μgL-1.
Kandungan Fenol dalam Ekstrak Pelepah Aren
Analisis total fenolik dalam ekstrak pelepah aren ditentukan berdasarkan kemampuan senyawa fenolik dalam ekstrak yang bereaksi dengan asam fosfomolibdat-fosfotungstat dalam reagen Folin-Ciocalteu (kuning) mengalami perubahan warna menjadi warna biru (Suryanto dan Wehantouw 2009). Berdasarkan hasil pengujian total fenolik, kandungan fenol tertinggi terdapat dalam ekstrak etanol 96%. Hal ini sebanding dengan aktivitas antioksidan ekstrak etanol 96% yang lebih tinggi dibandingkan dengan ekstrak etanol 70% dan
kontrol positifnya α-tokoferol. Menurut Maisuthisakul et al. (2007), senyawa fenolik memiliki gugus hidroksil yang mampu menghambat reaktivitas dari radikal bebas sehingga semakin tinggi kadar fenolik, maka semakin kecil nilai IC50 atau aktivitas antioksidannya semakin besar. Hasil analisis statistika kandungan fenol dalam ekstrak pelepah aren menunjukkan adanya perbedaan secara nyata antara ekstrak etanol 70% dan ekstrak etanol 96% artinya perbedaan pelarut yang digunakan berpengaruh terhadap kuantitas senyawa fenol.
Pengaruh kadar senyawa fenol dalam aktivitas antioksidan telah dilaporkan oleh Ismail et al. (2012) yang menyatakan bahwa biji pinang yaki dengan nilai total fenolik sebesar 85.92 GAE mgg-1 memiliki aktivitas antioksidan yang lebih besar dibandingkan kulit buah pinang yaki yang memiliki nilai total fenol sebesar 3.16 GAE mgg-1. Selain itu, penelitian Dewi (2012) melaporkan kandungan fenolik daun salam yang tinggi didukung dengan nilai IC50 yang rendah dibandingkan kandungan fenolik dan nilai IC50 dari daun jati belanda.
SIMPULAN
Ekstrak etanol 70% maupun ekstrak etanol 96% pelepah aren berpotensi sebagai antioksidan alami. Hasil penelitian ini menunjukkan adanya senyawa metabolit sekunder dalam ekstrak pelepah aren seperti saponin, steroid dan triterpeonoid, serta tanin dan fenol. Selain itu, diketahui bahwa total fenolik GAE dan aktivitas antioksidan tertinggi terdapat pada ekstrak etanol 96%.
DAFTAR PUSTAKA
Alfarabi M. 2010. Kajian antidiabetogenik ekstrak daun sirih merah (Piper crocatum) in vitro [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Anwariyah S. 2011. Kandungan fenol, komponen fitokimia dan aktivitas antioksidan lamun (Cymodocea rotundata) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Aqil F, Ahmad I, Mehmood Z. 2006. Antioxidant and free radical scavenging properties of twelve traditionally used Indian medicinal plants. Turk J Biol. 30:177-183.
[BPOM RI] Badan Pengawas Obat dan Makanan Republik Indonesia. 2005.
Gerakan Nasional Minum Temulawak. Jakarta: BPOM RI.
Chanwitheesuk A, Teerawutgulrag A, Rakariyatham N. 2004. Screening of antioxidant activity and antioxidant compounds of some edible plants of Thailand. J Food Chem 92:491-497
Dewi R. 2012. Aktivitas antioksidan dan sitotoksis metabolit sekunder daun salam (Syzygium polyanthum Wight.) dan daun jati Belanda (Guazuma ulmifolia
Lamk.) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Egwaikhide PA, Gimba CE. 2007. Analysis of the phytochemical content and anti-microbial activity of plectranthus glandulosis whole plant. Middle-East J Scie Res. 2(3-4):135-138.
Eleanore Y. 2013. Analisis fitokimia dan aktivitas antioksidan ekstrak daun sengon (Paraserianthes falcataria (L) Nielsen) menggunakan metode DPPH [skripsi]. Bogor (ID): Institut Pertanian Bogor
Gravianita. 2011. Kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia temulawak (Curcuma xanthorrhiza Roxb.) pada berbagai teknik pengeringan [skripsi]. Surakarta (ID): Universitas Sebelas Maret
Hanani E, Mun’im A, Sekarini R. 2005. Identifikasi senyawa antioksidan dalam spons Callyspongia sp dari kepulauan seribu. Ilmu Kefarmasian. 2 (3):127-133.
Harborne. 1987. Metode Fitokimia. Kosasih Padmawinata, penerjemah. Bandung: Penerbit ITB.
Harjadi W. 1993. Kimia Organik Suatu Kuliah Singkat. Ed-11. Achmadi S, penerjemah; Jakarta:Erlangga. Terjemahan dari: Organic Chemistry.
Ismail J, Runtuwene MRJ, Fatimah F. Penentuan total fenolik dan uji aktivitas antioksidan pada biji dan kulit buah pinang yaki (Areca vestiaria Giseke). J Ilmiah Sains 12(2): 84-88
Javanmardi J, Stushnoff C, Locke E, Vivanco JM. 2003. Antioxidant activity and total phenolic content of Iranian Ocimum accessions. J Food Chem 83:547-550.
Jain K, Katarina S, Guruprasad K.N. 2004. Effect of UV-B radiation on
antioxidant enymes and its modulation by bensoquinone and α-tocopherol in cucumber cotyledons. Current Sci 87(1):87-90.
Maisuthisakul P, Suttajit M, Pongsawatmanit R. 2007. Assessment of phenolic content and free radical-scavenging capacity of some Thai indigenous plants.
Food Chemistry. 100:1409-1418.
Medica. 2009. Manfaat pembudidayaan aren (Arenga pinnata (Wurmb.) Merr), tanaman perkebunan multiguna yang ramah lingkungan dan bernilai ekonomi tinggi. Di dalam: Rivaie AA, editorial. Pusat Penelitian dan Pengembangan Perkebunan, hal 27.
Molyneux P. 2003. The use of the stable free radical dyphenylpicrylhydrazil (DPPH) for estimating antioxidant activity. J Sci and Technol. 26:211-219. Panjaitan TD, Prasetyo B, Limantara L. 2011. Peranan karetenoid alami dalam
menangkal radikal bebas di dalam tubuh. Ma Chung Res Cent 79-86.
Prabawati SY, Setiawan AF, Agustina AF. 2012. Sintesis senyawa 1,4-Bis [(2-hidroksi-3-metoksi-5-formaldehid-fenil)-metil] piperazin dari bahan dasar vanilin dan uji aktivitasnya sebagai zat antioksidan. Kaunia 8(1):30-43
Rafi M, Widyastuti N, Suradikusumah E, Darusman LK. 2012. Antioxidant activity, fenolic concentration and total flavonoid of six Indonesia herbs. J Trad Med 18(1):29-34
Rosiyana AN. 2012. Aktivitas antioksidan dan penghambatan α-Glukosidase dan nanopartikel ekstrak kulit mahoni (Swietenie macrophylla King) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Sangi MS, Momuat LI, Kumaunang M. 2012. Uji toksisitas dan skrining fitokimia tepung gabah pelepah aren (Arenga pinnata). J Ilmiah Sains 12(2):127-134 Sareharto TP. 2010. Kadar vitamin E rendah sebagai faktor risiko peningkatan
bilirubin serum pada neonatus [tesis]. Semarang (ID): Ilmu Kesehatan Anak, Universitas Diponegoro.
Sihombing PA. 2007. Aplikasi ekstrak kunyit (Curcuma domestica) sebagai bahan pengawet mie basah [skripsi]. Bogor (ID): Institut Pertanian Bogor Suryanto E, Wehantouw F. 2009. Aktivitas penangkapan radikal bebas dari
ekstrak fenolik daun sukun (Artacarpus atilis F.). Chem Prog 2(1):1-7. Supiyanti W, Wulansari ED, Kusmita L. 2010. Test of antioxidant activity and
determination of total anthocyanin content in rind of mangosteen (Garcinia Mangostana L). Obat Tradisional 15(2):64-70.
Efendi DS. 2009. Aren, sumber energi alternatif. Warta 31(2):1-3.
Yuhernita, Juniarti. 2011. Analisis senyawa metabolit sekunder dari ekstrak metanol daun surian yang berpotensi sebagai antioksidan. Makara Sains
15(1):48-52.
Zeuthen P, Sørensen LB. 2003. Food Preservation Techniques. CRC Press, Cambridge England.
LAMPIRAN
Lampiran 1 Diagram alir penelitian
Lampiran 2 Contoh perhitungan rendemen % Rendemen =
=
-
= 0.002%
Lampiran 3 Gambar fitokimia ekstrak pelepah aren
Jenis Uji Air Etanol 70% Etanol 96% Pembanding
Alkaloid :
- Meyer
- Wagner
- Dragendorf
Saponin
Preparasi sampel
Analisis Fitokimia
Analisis Antioksidan dengan metode DPPH
Pengukuran total fenolik Ekstraksi
(Akuades, etanol 70% dan etanol 96%)
Flavonoid
Tanin dan Fenol
Steroid dan Triterpenoid
Lampiran 4 Kurva standar asam galat
Lampiran 5 Contoh perhitungan total fenolik
1. Total fenolik ekstrak
Persamaan kurva standar asam galat : y = 0,0704 x – 0,0509 Absorbansi rata-rata = 0,0704 x – 0,0509 (total fenolik) 0,260 = 0,0704 x – 0,0509 (total fenolik)
Total fenolik =
= 4.4169 mgL-1 x faktor pengenceran = 4.4169 mgL-1 x 4
= 17.665 mL-1
y = 0,0704x - 0,0509 R² = 0,9883
0,000 0,100 0,200 0,300 0,400
0 (Blanko) 20 40 60 80 100
Abs
o
rba
n
[asam galat] μgL-1
Kurva standar asam galat
2. Total fenolik GAE
Total fenolik GAE (C) = c (V/m) Keterangan:
c = konsentrasi total fenolik dari kurva standar V = volume ekstrak
m = berat ekstrak
Diketahui: c = 17.665 mgL-1, V = 10 ml = 0.01 L, m = 0.050 g Total fenolik GAE (C) = 17.665 mgL-1 (0.01 L/0.050 g)
= 3.533 mgg-1
Lampiran 6 Contoh perhitungan aktivitas antioksidan 1. % Inhibisi
% inhibisi =
x 100%
=
x 100% = 3.152%
2. IC50
Y= 22.82x – 27.408
(% inhibisi) = 22.82x – 27.408 (IC50) IC50 =
=
= 3.3921 μgL
Lampiran 8 Analisis statistika aktivitas antioksidan (IC50) ekstrak pelepah aren
Means for groups in homogeneous subsets are displayed.
a. Uses Harmonic Mean Sample Size = 3,000.
Lampiran 9 Analisis statistika kandungan total fenol ekstrak pelepah aren ANOVA
Means for groups in homogeneous subsets are displayed.
Lampiran 10 Analisis statistik korelasi antara IC50 dan total fenolik Descriptive Statistics
Mean Std. Deviation N
Perlakuan 3,00 1,464 15
IC50 3,3956 ,82876 9
Total_fenol 3,632828 ,1009532 9
Correlations
Perlakuan IC50 Total_fenol
Perlakuan Pearson Correlation 1 ,200 -,359
Sig. (2-tailed) ,605 ,343
N 15 6 6
IC50 Pearson Correlation ,200 1 -,724*
Sig. (2-tailed) ,605 ,028
N 6 6 6
Total_fenol Pearson Correlation -,359 -,724* 1
Sig. (2-tailed) ,343 ,028
N 6 6 6
*. Correlation is significant at the 0.05 level (2-tailed).
RIWAYAT HIDUP
Penulis dilahirkan di Pomalaa, Sulawesi Tenggara pada tanggal 05 April 1991 dari Bapak Harsono Mokoginta dan Ibu Misnawati Syahrir. Penulis adalah anak pertama dari 2 bersaudara. Penulis lulus dari SMAN 01 Pomalaa pada tahun 2009 dan pada tahun yang sama penulis lulus seleksi masuk di Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor (IPB) melalui jalur beasiswa utusan daerah (BUD).
Selama mengikuti perkuliahan, penulis aktif dalam organisasi Community of Research and Education in Biochemistry (CREBS) sebagai anggota divisi metabolisme (tahun 2011-2012) dan sebagai bendahara (tahun 2012-2013), Ikatan Kekeluargaan Mahasiswa Indonesia Sulawesi Selatan (IKAMI Sulsel), dan Ikatan Kekeluargaan Pelajar Mahasiswa Sulawesi Tenggara (IKPM Sultra), serta aktif dalam berbagai kepanitiaan seperti Lomba Karya Ilmiah Populer (LKIP) tahun 2010-2011 sebagai sekertaris kegiatan, Workshop Kesehatan dan Keselamatan Kerja (K3) di Laboratorium (2011), dan Masa Perkenalan Departemen (MPD) tahun 2011. Penulis juga pernah menjadi Asisten Praktikum Biokimia Umum (2011-2013) dan asisten praktikum Instrumen Biokimia (2013). Selain itu, penulis juga pernah melaksanakan praktek lapang selama bulan Juli-Agustus tahun 2012 di Pusat Studi Biofarmaka Bogor dengan judul laporan ilmiah Validasi Metode Analisis Logam Timbal (Pb) dalam Tanaman Kunyit (Curcuma domestica) dengan Spektrofotometer Serapan Atom. Tahun 2013, penulis pernah mendapatkan dana Program Kreativitas Mahasiswa bidang Penelitian (PKM-P) dari Dikti dengan judul Khasiat Limbah Pelepah Pohon Aren (Arenga pinnata