KORELASI
SHORT FORM
-36 DENGAN SKALA
EASTERN
COOPERATIVE ONCOLOGY GROUP
DALAM MENILAI
KUALITAS HIDUPPADA PASIEN LIMFOMA NON
HODGKIN YANG MENDAPAT KEMOTERAPI REGIMEN
CYCLOPHOSHAMIDE, DOXORUBICIN, VINCRISTINE,
DAN
PREDNISONE
TESIS
Oleh
DIKA IYONA SINULINGGA
NIM : 087101016
DEPARTEMEN ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
MEDAN
KORELASI
SHORT FORM
-36 DENGAN SKALA
EASTERN
COOPERATIVE ONCOLOGY GROUP
DALAM MENILAI
KUALITAS HIDUP PADA PASIEN LIMFOMA NON
HODGKIN YANG MENDAPAT KEMOTERAPI REGIMEN
CYCLOPHOSPHAMIDE, DOXORUBICIN, VINCRISTINE,
DAN
PREDNISONE
TESIS
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Magister Kedokteran Klinik dan Spesialis Penyakit Dalam pada Fakultas Kedokteran Universitas Sumatera
Utara
Oleh
DIKA IYONA SINULINGGA
087101016
DEPARTEMEN ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA
MEDAN
Judul Tesis : Korelasi Short Form-36 Dengan Skala Eastern Cooperative Oncology Group Dalam Menilai Kualitas Hidup Pada Pasien Limfoma Non Hodgkin Yang Mendapat Kemoterapi Regimen Cyclophosphamide, Doxorubicin, Vincristine, dan Prednisone Nama Mahasiswa : Dika Iyona Sinulingga
Nomor Induk Mahasiswa : 087101016
Program Studi : Spesialis Ilmu Penyakit Dalam
Menyetujui, Komisi Pembimbing
Ketua
Dr. Dairion Gatot, SpPD-KHOM
Anggota
Dr. Savita Handayani, SpPD
Sekretaris Departemen Sekretaris Program Studi
Dr. RefliHasan, SpPD, SpJP(K)
NIP. 19610403 198709 1 001 NIP. 19680504 199903 1 001 Dr. ZainalSafri, SpPD, SpJP
Telahdiuji
PadaTanggal :4 September 2014
PANITIA PENGUJI TESIS
Ketua : Prof. dr. Lukman Hakim Zain, SpPD-KGEH Anggota : dr. Mabel Sihombing, SpPD-KGEH
PERNYATAAN ORISINALITAS
Tesis ini adalah hasil karya penulis sendiri, dan semua sumber baik yang dikutip
maupun dirujuk telah penulis nyatakan dengan benar
Nama : Dika Iyona Sinulingga
NIM : 087101016
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademik Universitas Sumatera Utara, saya yang bertanda tangan di bawah ini :
Nama :DikaIyonaSinulingga
NIM :087101016
Program Studi :Ilmu Penyakit Dalam Jenis Karya :Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-eksklusif (Non-exclusive Royalty Free Right) atas tesis saya yang berjudul :“KorelasiShort Form-36 Dengan Skala Eastern Cooperative Oncology Group Dalam Menilai Kualitas Hidup Pada Pasien Limfoma Non Hodgkin Yang Mendapat Kemoterapi Regimen Cyclophosphamide, Doxorubicin, Vincristine, dan Prednisone”beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non-eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalihmedia/formatkan, mengelola dalam bentuk database, merawat dan mempublikasikan tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemilik hak cipta.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di : Medan
Pada tanggal : 15 Agustus 2014 Yang menyatakan,
KATA PENGANTAR
Puji syukur yang tak terhingga senantiasa penulis panjatkan kehadirat Tuhan yang Maha Esa, atas karunia, petunjuk, kekuatan dan kemudahan sehingga penulis dapat menyelesaikan tesis ini. Penulis sangat menyadari bahwa tanpa bantuan dari semua pihak, tesis ini tidak mungkin dapat penulis selesaikan. Oleh karena itu perkenankanlah penulis mengucapkan terima kasih serta penghargaan yang setinggi-tingginya kepada semua pihak yang telah membantu penulis dalam menyelesaikan tesis ini, baik secara langsung maupun tidak langsung. Rasa hormat, penghargaan dan ucapan terima kasih sebesar-besarnya penulis sampaikan kepada:
1. dr. Salli Roseffi Nasution, SpPD-KGH dan dr. Refli Hasan, SpPD, SpJP(K)
selaku Kepala dan Sekretaris Departemen Ilmu Penyakit Dalam FK-USU yang telah memberikan kesempatan pada penulis untuk mengikuti pendidikan serta senantiasa membimbing, memberi dorongan dan kemudahan selama penulis menjalani pendidikan.
2. dr. Zainal Safri, SpPD, SpJP dan dr. Ilhamd, SpPD selaku Ketua dan Sekretaris Program Studi Ilmu Penyakit Dalam FK-USU yang telah dengan sungguh-sungguh membantu, membimbing, memberi dorongan dan membentuk penulis menjadi dokter Spesialis Penyakit Dalam yang siap mengabdi pada nusa dan bangsa.
3. Khusus mengenai karya tulis ini, penulis mengucapkan terima kasih yang sebesar-besarnya kepada dr. Dairion Gatot, SpPD-KHOM dan dr. Savita Handayani, SpPD selaku pembimbing tesis, yang telah memberikan bimbingan dan kemudahan bagi penulis selamamelaksanakan penelitian, juga telah banyak meluangkan waktu dan dengan kesabaran membimbing penulis sampai selesainya karya tulisini. Terima kasih yang tak terhingga penulis ucapkan.
4. dr. Zulhelmi Bustami, KGH (Alm), Dr. dr. Dharma Lindarto, SpPD-KEMD selaku mantan Kepala Program Studi dan mantan Sekretaris Program StudiIlmu Penyakit Dalam FK-USU, saat penulis diterima sebagai peserta Program Pendidikan Dokter Spesialis. Terima kasih atas kesempatan, dukungan dan bimbingan yang telah diberikan.
6. Para Guru Besar :Prof. dr. Harun Rasyid Lubis, SpPD-KGH, Prof. dr. Bachtiar Fanani Lubis, SpPD-KHOM,Prof. dr. Habibah Hanum, SpPD-KPsi, Prof. dr. PengarapenTarigan, SpPD-KGEH, Prof. dr. Sutomo Kasiman, SpPD, SpJP(K), Prof. dr. Azhar Tanjung, SpPD-KP-KAI, SpMK, Prof. dr. OK. Moehadsyah, SpPD-KR, Prof. dr. Lukman Hakim Zain, SpPD-KGEH, Prof. dr. M. Yusuf Nasution, SpPD-KGH, Prof. dr. Abdul Majid, Sp.PD-KKV, AIF, Prof. dr. Azmi S. Kar, SpPD-KHOM, Prof. dr. Gontar Alamsyah Siregar, SpPD-KGEH, Prof. dr. Harris Hasan, SpPD, SpJP(K), Prof. dr. Harun Al Rasyid Damanik, SpPD, SpGK, yang telah memberikan bimbingan dan teladan selama penulis menjalani pendidikan.
7. Seluruh staf pengajar Departemen Ilmu Penyakit Dalam FK USU, para guru penulis : Prof. dr. Lukman Hakim ZainSpPD-KGEH,dr. Rustam Effendi Y.SSpPD-KGEH, dr. Zulhelmi Bustami, SpPD-KGH (Alm), dr. Salli Roseffi Nasution, SpPD-KGH, dr. Abdurrahim Rasyid Lubis, SpPD-KGH, dr. R. Tunggul Ch. Sukendar, SpPD-KGH (Alm), dr. Refli Hasan, SpPD, SpJP(K), dr. Zainal Safri, SpPD, SpJP, Dr. dr. Dharma Lindarto, KEMD, dr.Mardianto, SpPD-KEMD, dr. Santi Syafril, SpPD-SpPD-KEMD, dr. Sri Maryuni Sutadi, SpPD-KGEH, dr. Betthin Marpaung, KGEH (Alm), dr. Mabel Sihombing, SpPD-KGEH, Dr. dr. Juwita Sembiring, SpPD-SpPD-KGEH, dr. Leonardo Basa Dairi, Sp.PD-KGEH, dr. Dairion Gatot, KHOM, dr. Yosia Ginting, KPTI, Dr. dr. Umar Zein, KPTI, DTM&H, dr. Armon Rahimi, SpPD-KPTI,dr. Alwinsyah Abidin, SpPD-KP, dr. E.N. Keliat, SpPD-KP, dr. Zuhrial Zubir, SpPD-KAI, dr. Pirma Siburian, SpPD-KGer, Dr. dr. Blondina Marpaung, SpPD-KR, dr. Tambar Kembaren, SpPD, dr. Sugiarto Gani, SpPD, dr. Savita Handayani, SpPD serta para guru lainnya yang tidak dapat penulis sebutkan satu persatu, yang dengan kesabaran dan perhatiannya senantiasa membimbing penulis selama mengikuti pendidikan. Penulis haturkan rasa hormat dan terima kasih yang tak terhingga.
8. Seluruh staf pengajar di Divisi Hemato-Onkologi Medik Departemen Ilmu Penyakit Dalam: Dr. Dairion Gatot, SpPD-KHOM, Dr. Savita Handayani, SpPD, Dr. Soegiarto Gani, SpPD, dan Dr. Heny S. Lubis, SpPD yang telah memberikan banyak bantuan kepada penulis dalam melakukan penelitian ini.
memberikan fasilitas dan kesempatan yang seluas-luasnya kepada penulis dalam menjalani pendidikan.
10. Rektor Universitas Sumatera Utara, Dekan dan Ketua TKP-PPDS Fakultas Kedokteran Universitas Sumatera Utara yang telah memberikan kesempatan kepada penulis untuk mengikuti Program Pendidikan Dokter Spesialis Ilmu Penyakit Dalam di Fakultas Kedokteran Universitas Sumatera Utara.
11. Dr. TaufikAshar, MKM, selaku pembimbing statistik yang telah banyak meluangkan waktu untuk membimbing dan berdiskusi dengan penulis dalam penyusunan tesis ini.
12. Teman-teman seangkatan penulis yang memberikan dorongan semangat : dr. Siti Taqwa Lubis, MKed(PD), SpPD, dr. Lisa Yuliyanti, dr. Aini Pertiwi, dr. Yuswita Santi Siregar, MKed(PD), SpPD, dr. Rachmat S. W. Siregar, dr. Hendrik Sarumpaet, dr. Tawarta Keliat, dr. Arief Banu Pradipta, dr. Arif Budiman, dr. Andre Marpaung, MKed(PD), SpPD serta seluruh rekan seperjuangan peserta PPDS Ilmu Penyakit Dalam FK-USU, khususnya dr. Ester M. Silalahi, Mked(PD),yang telah memberikan banyak dukungan dengan persahabatan, kerja sama serta berbagi dalam suka dan duka dalam menjalani kehidupan sebagai residen.
13. Partner penelitian dr. MawaddahFitria, SpPDdandokterruangan di RS H. Adam Malik Medan dan RS Pirngadi Medan yang membantumengumpulkan sampel penelitian.
14. Seluruh perawat/paramedis di berbagai tempat di mana penulis pernah bertugas selama pendidikan, terima kasih atas bantuan dan kerja sama yang baik selama ini. 15. Para pasien yang telah bersedia ikut dalam penelitian ini sehingga penulisan tesis
ini dapat terwujud.
16. Syarifuddin Abdullah, Lely HusnaNasution, Deni, Yanti, Wanti, Tika, Tanti, ErjanGintingdan seluruh pegawai administrasi Departemen Ilmu Penyakit Dalam FK-USU, yang telah banyak membantu memfasilitasi penulis dalam menyelesaikan tugas pendidikan.
mertua sayaAbdul Muluk Dalimunthe, SH dan Tiasri Hasibuan yang telah mendukung, membimbing, menyemangati, dan menasehati agar kuat dalam menjalani pendidikan, saya ucapkan terimakasih yang setulus-tulusnya.
Teristimewa, penulis menyampaikan terimakasih yang sedalam – dalamnya kepada suami tercinta, Mahyarudin Dalimunthe, ST, M.Eng dan anak-anakku
tercinta Qalesya Aiko Dalimunthe dan Rakhshan Hideaki Dalimunthe atas cinta kasih yang tulus, pengertian, perhatian, kesabaran, dukungan moril dan materil serta telah mendukung, mendoakan, sertamemberikansemangatbagipenulis.Semogaapa yang kitacapaiinidapatmemberikankebahagiaandankesejahteraanbagikitadandiberkati Allah SWT. Kepada saudarakandung penulis,Dini Bahraini Sinulingga, SH, LLM, Debi
DwiyonaSinulingga, ST, dandr. R.
DisfahanYonandaSinulinggasertasegenapkeluargabesarpenulisyang telah banyak memberikan bantuan moril, semangat dan doa tanpa pamrih selama pendidikan, terimakasihku yang takterhinggauntuksegalanya.
Akhirnya dengan segala kerendahan hati, penulis sampaikan pula terima kasih kepada semua pihak yang tidak dapat penulis sebutkan satu persatu, yang telah membantu baik secara langsung maupun tidak langsung selama pendidikan maupun dalam penyelesaian tesis ini.
Semoga Tuhan Yang MahaEsa senantiasa memberikan limpahan rahmat dan karuniaNya kepada kita semua dan semoga penelitian ini dapat bermanfaat bagi kita dan masyarakat.
Medan, Agustus 2014
Penulis,
Abstrak
KORELASISHORT FORM-36 DENGAN SKALA EASTERN COOPERATIVE ONCOLOGY GROUP DALAM MENILAI KUALITAS HIDUP PADA PASIEN LIMFOMA NON HODGKIN YANG MENDAPAT KEMOTERAPI REGIMEN CYCLOPHOSPHAMIDE, DOXORUBICIN, VINCRISTINE, DAN PREDNISONE
DikaIyonaSinulingga, Savita Handayani1, Dairion Gatot1 1
Fakultas Kedokteran Universitas Sumatera Utara/RSUP.H.Adam Malik Medan Divisi Hemato Onkologi Medik Departemen Ilmu Penyakit Dalam
Latar Belakang --- Penilaian kualitas hidup telah menjadi peralatan yang vital,tidakhanyadalampemantauanhasilterapipadapasiendenganberbagaimodalitasterapi, tetapijugakarenatelahterbuktisecarasignifikanmempengaruhimorbiditasdanmortalitas.Baik instrumen yang bersifat umum maupun yang bersifat khusus telah digunakan dalam penilaian kualitas hidup pada pasien limfoma non hodgkin (LNH). Padapenelitianini, kami menganalisisduainstrumen yang bersifatumum - Skala Status Performa ECOG (The Eastern Cooperative Oncology Group) danSurveiKesehatan SF-36 (Short Form-36) padapasienlimfoma non hodgkin yang mendapatkemoterapi regimen CHOP (Cyclophosphamide, Doxorubicin, Vincristine, Prednisone).
Tujuan --- Untukmengetahuiapakahsurvey kesehatan SF-36 berkorelasidenganskala status performa ECOG padapasienlimfoma non hodgkin yang mendapatkemoterapi regimen CHOP.
Bahan dan Cara --- Penelitian cross sectional dilakukan pada bulan Oktober 2012 hingga Desember 2013. Pengambilan sampel penelitian dilakukan secara consecutive sampling pada penderita LNH yang memenuhi kriteria inklusi dan tidak memenuhi kriteria eksklusi. Dilakukan penilaian kualitas hidup dengan menggunakan SF 36 dan skala ECOG setelah kemoterapi siklus keenam.
0,0001). Dengan nilai cut-off ≥ 54,66SF-36 menunjukkan performa diagnostik yang baik untuk memprediksi skala ECOG yang baik dengan sensitifitas 94,7%, spesifisitas 100%, PPV 100%, NPV 66,67%, LR (+) ~, LR (-) 0,05, akurasi diagnostik 95,23%, dan AUC 98,7% (95% CI: 0% - 100%; p = 0,027).
Kesimpulan ---SF 36 berkorelasi dengan skala ECOG dan memiliki diagnostik yang sangat baik dalam memprediksi skala ECOG, sehingga SF 36 dapat menjadi pilihan alternatif dalam menilai kualitas hidup pada pasien limfoma non hodgkin yang mendapat kemoterapi regimen CHOP.
Abstract
CORRELATION BETWEEN SHORT FORM-36 AND EASTERN COOPERATIVE ONCOLOGY GROUP SCALE IN ASSESSING NON HODGKIN LYMPHOMA PATIENTS’ QUALITY OF LIFE RECEIVING CYCLOPHOSPHAMIDE, DOXORUBICIN, VINCRISTINE, AND PREDNISONE
CHEMOTHERAPY
DikaIyonaSinulingga, Savita Handayani1, Dairion Gatot1 1
Division of Hematology and Medical Oncology, Department of Internal Medicine, Faculty of Medicine, University of Sumatera Utara, Medan
Background --- Health-related quality of life’s (HRQOL) assessment has become a vital tool not only in the monitoring of treatment outcomes in patients on various modalities of therapy but also because it has been established to significantly influence morbidity and mortality. Both generic and disease-specific instruments have been used in the assessment of HRQOL in non hodgkin lymphoma (NHL) patients. In this study, we analyze two generic instruments - The Eastern Cooperative Oncology Group (ECOG) Performance Status Scaleand Health SurveyShort Form-36 (SF-36)in NHL patients receiving Cyclophosphamide, Doxorubicin, Vincristine, and Prednisone (CHOP) chemotherapy.
Objectives--- To find out the the correlation between SF-36 and ECOG scale in NHL patients receiving CHOP chemotherapy.
Materials and Methods ---Cross sectional research was conducted from October 2012 up to December 2013. Samples were selected consecutively to NHL patients that met the inclusion criteria. SF-36 and ECOG scale was assessed after CHOP chemotherapy cycle 6.
54,66,with sensitivity 94,7%, specificity 100%, PPV 100%, NPV 66,67%, LR (+) ~, LR (-) 0,05, accuracy 95,23%, and AUC 98,7% (95% CI: 0% - 100%; p = 0,027).
Conclusion --- SF 36 correlates with ECOG scaleand has a very good diagnostic in predicting ECOG scale, therefore SF 36 can be used as an alternative choice in assessing quality of life in patients receiving CHOP chemotherapy .
DAFTAR ISI
2.2.1. SurveiKesehatan SF 36 ... 14
2.2.2. Skala ECOG……….. .. 19
BAB III METODE PENELITIAN ... 21
3.1. DesainPenelitian ... 21
3.2Waktu dan tempatpenelitian... 21
3.3 Populasi dan Sampel ... 21
3.4 Besar Sampel ... 21
3.5 KriteriaInklusi ... 22
3.7 DefinisiOperasional ... 22
3.8 KerangkaOperasional ... 23
3.9 BahandanProsedurPenelitian……… .... 23
3.10 Analisis Data ………... . 24
3.11 EthicalClearance dan InformedConsent ... 24
BAB IV HASIL ... 25
4.1 KarakteristikSubjekPenelitian ... 25
4.2 Hasil Penelitian ... 26
BAB V PEMBAHASAN……… 32
BAB VI KESIMPULAN DAN SARAN ... 35
6.1 Kesimpulan ... 35
6.2 Saran ... 35
DAFTAR TABEL
Halaman
Tabel 2.1.1 KlasifikasiLimfomaMenurutKlasifikasi REAL dan WHO ... 6
Tabel 2.1.2 Stadium LimfomaMenurut Ann Arbor ... 9
Tabel 2.1.3 KriteriaResponLimfoma ... 12
Tabel 2.2.1.1 Pertanyaan yang Mewakili 8 DimensiKuesioner SF-36 ... 16
Tabel 2.2.1.2 SkorKuesioner SF-36 ... 17
Tabel 2.2.2.1 Skala ECOG………. 19
Tabel 4.1.1 KarakteristikDasarSubjekPenelitian ... 25
Tabel 4.2.1 DistribusiRerata, Simpangan Baku, danHasilUjiNormalitas Data ... 26
Tabel 4.2.2 Korelasi Spearman SF 36 danSkala ECOG ... 27
Tabel 4.2.3 KorelasiUsiadengan SF 36 ... 28
Tabel 4.2.4 HubunganKarakteristikdengan SF 36 ... 28
DAFTAR GAMBAR
DAFTAR SINGKATAN
LNH : Limfoma Non Hodgkin
CHOP : Cyclophosphamide, Vincristine, Doxorubicin, Prednisone SF 36 : Short Form 36
ECOG : The Eastern Cooperative Oncology Group HRQOL: Health Related Quality of Life
QOL : Quality of Life
WHO : World Health Organization
REAL : Revised European American Lymphoma Classification CD 20 : Cluster Differentiation 20
IPI : International Prognostic Index
DAFTAR LAMPIRAN
Halaman
LAMPIRAN 1. SuratPersetujuanKomiteEtikPenelitian ... 40
LAMPIRAN 2. SuratPenjelasanKepadaSubjek ... 41
LAMPIRAN 3. SuratPersetujuanSetelahPenjelasan ... 43
LAMPIRAN 4. KertasKerjaProfilPesertaPenelitian ... 44
LAMPIRAN 5. Cara PemberianKemoterapi Regimen CHOP ………. .. 50
LAMPIRAN 6. SF-36 SurveiKesehatan ………... .. 51
LAMPIRAN 7. DaftarRiwayatHidup ... 57
LAMPIRAN 8. HasilStatistik ... 60
Abstrak
KORELASISHORT FORM-36 DENGAN SKALA EASTERN COOPERATIVE ONCOLOGY GROUP DALAM MENILAI KUALITAS HIDUP PADA PASIEN LIMFOMA NON HODGKIN YANG MENDAPAT KEMOTERAPI REGIMEN CYCLOPHOSPHAMIDE, DOXORUBICIN, VINCRISTINE, DAN PREDNISONE
DikaIyonaSinulingga, Savita Handayani1, Dairion Gatot1 1
Fakultas Kedokteran Universitas Sumatera Utara/RSUP.H.Adam Malik Medan Divisi Hemato Onkologi Medik Departemen Ilmu Penyakit Dalam
Latar Belakang --- Penilaian kualitas hidup telah menjadi peralatan yang vital,tidakhanyadalampemantauanhasilterapipadapasiendenganberbagaimodalitasterapi, tetapijugakarenatelahterbuktisecarasignifikanmempengaruhimorbiditasdanmortalitas.Baik instrumen yang bersifat umum maupun yang bersifat khusus telah digunakan dalam penilaian kualitas hidup pada pasien limfoma non hodgkin (LNH). Padapenelitianini, kami menganalisisduainstrumen yang bersifatumum - Skala Status Performa ECOG (The Eastern Cooperative Oncology Group) danSurveiKesehatan SF-36 (Short Form-36) padapasienlimfoma non hodgkin yang mendapatkemoterapi regimen CHOP (Cyclophosphamide, Doxorubicin, Vincristine, Prednisone).
Tujuan --- Untukmengetahuiapakahsurvey kesehatan SF-36 berkorelasidenganskala status performa ECOG padapasienlimfoma non hodgkin yang mendapatkemoterapi regimen CHOP.
Bahan dan Cara --- Penelitian cross sectional dilakukan pada bulan Oktober 2012 hingga Desember 2013. Pengambilan sampel penelitian dilakukan secara consecutive sampling pada penderita LNH yang memenuhi kriteria inklusi dan tidak memenuhi kriteria eksklusi. Dilakukan penilaian kualitas hidup dengan menggunakan SF 36 dan skala ECOG setelah kemoterapi siklus keenam.
0,0001). Dengan nilai cut-off ≥ 54,66SF-36 menunjukkan performa diagnostik yang baik untuk memprediksi skala ECOG yang baik dengan sensitifitas 94,7%, spesifisitas 100%, PPV 100%, NPV 66,67%, LR (+) ~, LR (-) 0,05, akurasi diagnostik 95,23%, dan AUC 98,7% (95% CI: 0% - 100%; p = 0,027).
Kesimpulan ---SF 36 berkorelasi dengan skala ECOG dan memiliki diagnostik yang sangat baik dalam memprediksi skala ECOG, sehingga SF 36 dapat menjadi pilihan alternatif dalam menilai kualitas hidup pada pasien limfoma non hodgkin yang mendapat kemoterapi regimen CHOP.
Abstract
CORRELATION BETWEEN SHORT FORM-36 AND EASTERN COOPERATIVE ONCOLOGY GROUP SCALE IN ASSESSING NON HODGKIN LYMPHOMA PATIENTS’ QUALITY OF LIFE RECEIVING CYCLOPHOSPHAMIDE, DOXORUBICIN, VINCRISTINE, AND PREDNISONE
CHEMOTHERAPY
DikaIyonaSinulingga, Savita Handayani1, Dairion Gatot1 1
Division of Hematology and Medical Oncology, Department of Internal Medicine, Faculty of Medicine, University of Sumatera Utara, Medan
Background --- Health-related quality of life’s (HRQOL) assessment has become a vital tool not only in the monitoring of treatment outcomes in patients on various modalities of therapy but also because it has been established to significantly influence morbidity and mortality. Both generic and disease-specific instruments have been used in the assessment of HRQOL in non hodgkin lymphoma (NHL) patients. In this study, we analyze two generic instruments - The Eastern Cooperative Oncology Group (ECOG) Performance Status Scaleand Health SurveyShort Form-36 (SF-36)in NHL patients receiving Cyclophosphamide, Doxorubicin, Vincristine, and Prednisone (CHOP) chemotherapy.
Objectives--- To find out the the correlation between SF-36 and ECOG scale in NHL patients receiving CHOP chemotherapy.
Materials and Methods ---Cross sectional research was conducted from October 2012 up to December 2013. Samples were selected consecutively to NHL patients that met the inclusion criteria. SF-36 and ECOG scale was assessed after CHOP chemotherapy cycle 6.
54,66,with sensitivity 94,7%, specificity 100%, PPV 100%, NPV 66,67%, LR (+) ~, LR (-) 0,05, accuracy 95,23%, and AUC 98,7% (95% CI: 0% - 100%; p = 0,027).
Conclusion --- SF 36 correlates with ECOG scaleand has a very good diagnostic in predicting ECOG scale, therefore SF 36 can be used as an alternative choice in assessing quality of life in patients receiving CHOP chemotherapy .
BAB I PENDAHULUAN
1.1. Latar Belakang
Kualitas hidup terkait kesehatan sering didefinisikan sebagai “nilai yang diberikan
untuk durasi kehidupan sebagaimana telah diubah oleh gangguan, status fungsional,
persepsi, dan kesempatan sosial yang dipengaruhi oleh penyakit, trauma, terapi, atau
kebijakan”. Penilaian kualitas hidup telah menjadi peralatan yang vital, tidak hanya dalam
pemantauan hasil terapi pada pasien dengan berbagai modalitas terapi, tetapi juga karena
telah terbukti secara signifikan mempengaruhi morbiditas dan mortalitas.1
Penilaian kualitas hidup terkait kesehatan adalah penting, sebagaimana ia
menentukan seberapa dekat modalitas terapi mencapai prinsip fundamental dalam
memperpanjang hidup, menghilangkan tekanan, mengembalikan fungsi dan mencegah
disabilitas, yang secara konsekuen akan menyebabkan hidup yang lebih produktif dan
efektif. Hal ini terkait, sebagaimana definisi WHO mengenai kesehatan membawa pusat
perhatian terhadap perlunya pendekatan holistik untuk terapi.1
Baik instrumen yang bersifat umum atau yang spesifik untuk penyakit tertentu
telah digunakan dalam penilaian kualitas hidup terkait kesehatan pada pasien limfoma non
hodgkin dengan berbagai modalitas terapi. Setiap instrumen tersebut memiliki kelebihan
dan kekurangan tertentu, tetapi secara umum memiliki korelasi yang baik.1,2
Limfoma non hodgkin merupakan neoplasma hematopoietik yang paling sering
ditemukan, menempati urutan ketujuh dari seluruh kanker. Limfoma non hodgkin
ditemukan 5 kali lebih banyak dari limfoma Hodgkin. Saat ini jumlah penderita limfoma
non Hodgkin semakin bertambah, hal ini mungkin berkaitan dengan deteksi dini ataupun
infeksi HIV.
Pada
penelitian ini, kami menganalisis dua instrumen yang bersifat umum - Skala Status
Performa ECOG (The Eastern Cooperative Oncology Group) dan Survei Kesehatan SF-36
(Short Form-36) pada pasien limfoma non hodgkin yang mendapat kemoterapi regimen
CHOP (Cyclophosphamide, Doxorubicin, Vincristine, Prednisone).
3,4
Hodgkin yang berobat ke Instalasi Rawat Jalan RSUP. H. Adam Malik selama periode 1
Januari – 31 Desember 2009 berjumlah 60 orang.
Pemilihan terapi untuk limfoma non Hodgkin bergantung kepada stadium tumor,
fenotipe (sel B, T, atau NK), histologi (low, intermediate, atau high grade), gejala, status
performa pasien, umur, dan faktor komorbid. Kemoterapi dengan regimen CHOP
diindikasikan pada pasien limfoma non hodgkin dengan intermediate hingga high grade.
Kemoterapi diberikan sebanyak 6-8 siklus terapi. Pemberian regimen CHOP juga bisa
dikombinasikan dengan antibodi monoklonal seperti Rituximab. Penelitian yang
membandingkan efektivitas regimen-regimen kemoterapi pada limfoma maligna
menyimpulkan sampai saat ini regimen CHOP yang lebih murah dan lebih sederhana
dibandingkan dengan regimen-regimen lain yang merupakan terapi terpilih, seperti
m-BACOD, ProMACE, dan MACOP-B.4,5
Skala Status Performa ECOG merupakan skala peringkat yang digunakan dokter
yang menjamin penilaian objektif status klinis pasien. Skala status performa ECOG secara
original didesain untuk menilai progresivitas penyakit pasien, menilai bagaimana penyakit
mempengaruhi kemampuan aktivitas sehari-hari pasien, dan menentukan terapi yang paling
cocok serta prognosisnya. Saat ini ECOG kemungkinan merupakan instrumen kualitas
hidup terkait kesehatan yang paling sering digunakan, bersamaan dengan Karnofsky.
ECOG terdiri dari 6 skala, mulai dari 0 hingga 5. Skala 0 berarti aktif secara penuh, bisa
melakukan aktivitas sebagaimana sebelum terkena penyakit tanpa hambatan. Skala 1
berarti terbatas dalam melakukan aktivitas berat tetapi masih bisa rawat jalan dan bisa
melakukan pekerjaan yang ringan seperti pekerjaan rumah tangga atau pekerjaan kantor
yang ringan. Skala 2 berarti bisa rawat jalan dan mampu untuk merawat diri sendiri tetapi
tidak mampu melakukan pekerjaan dan < 50% waktu harus berbaring. Skala 3 berarti
hanya mampu merawat diri sendiri dan > 50% waktu harus berbaring. Skala 4 berarti harus
berbaring terus menerus, dan 5 berarti meninggal. Beberapa kelemahannya adalah fakta
bahwa skornya tidak tergantung pada penilaian pasien dan fakta bahwa status mental tidak
dinilai.
Kualitas hidup bersifat multidimensional sehingga dalam sebuah studi yang
sensitif dalam menilai kualitas hidup. Hal ini dimungkinkan oleh karena skala ECOG
sangat tergantung oleh penilaian dokter, dan hanya melihat kemampuan fisik saja.Karena
itu, alat ukur kualitas hidup seharusnya bersifat multidimensional yang menyinggung aspek
fisik, sosial dan emosional, simpel, mudah dimengerti dan dijawab oleh semua pasien dan
harus divalidasi.10,11
Short Form-36 (SF-36) merupakan salah satu kuesioner untuk mengukur fungsi
kesehatan fisik dan mental. SF-36 terdiri dari 36 butir pertanyaan yang menggambarkan 8
sub skala, yaitu fungsi fisik, hambatan kerja yang dialami oleh karena masalah fisik, nyeri
pada tubuh, persepsi kesehatan secara umum, vitalitas, fungsi sosial, hambatan kerja oleh
karena masalah emosional, dan kesehatan mental. Dua skor kesimpulan yang digambarkan
oleh SF-36 adalah komponen fisik dan komponen mental. SF-36 biasa digunakan untuk
mengukur kualitas hidup di antara pasien-pasien dengan penyakit kronik, membandingkan
antara pasien-pasien penyakit kronik dengan tingkat keparahan tertentu, serta mengukur
kualitas hidup setelah terapi tertentu.12,13,14
Beberapa penelitian terdahulu, yang dilakukan oleh Sutrisno, dkk di Bali,
mendapatkan korelasi yang kuat antara kualitas hidup yang dinilai dengan menggunakan
EORTC QLQ C-30 dan skala ECOG. Yost, dkk mendapatkan korelasi yang sedang antara
kualitas hidup yang dinilai dengan FACT-G dan skala ECOG.10
1.2. Perumusan Masalah
Pada penelitian ini, kami
menganalisis korelasi SF-36 dengan skala ECOG, sehingga diharapkan jika ditemukan
korelasi yang kuat, SF-36 dapat digunakan bersama dengan ECOG dalam menilai kualitas
hidup pada pasien limfoma non hodgkin yang mendapat kemoterapi regimen CHOP secara
lebih komprehensif.
Apakah survey kesehatan SF-36 berkorelasi dengan skala ECOG pada pasien
limfoma non hodgkin yang mendapat kemoterapi regimen CHOP?
1.3. Hipotesis
Survey kesehatan SF-36 berkorelasi dengan skala ECOG pada pasien limfoma
1.4. Tujuan Penelitian
Untuk mengetahui apakah survey kesehatan SF-36 berkorelasi dengan skala
ECOG pada pasien limfoma non hodgkin yang mendapat kemoterapi regimen CHOP.
1.5. Manfaat Penelitian
1. Dengan diketahuinya hubungan antara survey kesehatan SF-36 dengan skala ECOG,
diharapkan SF-36 dapat digunakan sebagai instrumen yang komprehensif dan tepat
bersama dengan skala ECOG dalam menilai kualitas hidup pada pasien limfoma non
hodgkin yang mendapat kemoterapi regimen CHOP.
2. Sebagai data dasar bagi penelitian selanjutnya
1.6. Kerangka Konsep
Penilaian dokter
Kualitas Hidup Pasien limfoma non Hodgkin
post kemoterapi CHOP 6 siklus
Skala Eastern Cooperative Oncology Group (ECOG Scale)
Survey Kesehatan
Short Form 36 (SF 36)
BAB II
TINJAUAN PUSTAKA
2.1.Limfoma Non Hodgkin
Limfoma non Hodgkin merupakan sekelompok keganasan yang berasal dari sistem
kelenjar getah bening, yang biasanya menyebar ke seluruh tubuh. Diagnosis limfoma non
Hodgkin ditegakkan berdasarkan konfirmasi patologis melalui pemeriksaan biopsi jaringan.
Patogenesis terjadinya limfoma non Hodgkin adalah translokasi kromosom dan perubahan
molekuler, seperti t(14;18)(q32;q21), t(11;14)(q13;q32), dan lainnya. Beberapa virus juga
dipercaya mempengaruhi patogenesis terjadinya limfoma non Hodgkin, oleh karena
kemampuan mereka untuk menginduksi stimulasi antigen dan disregulasi sitokin, yang
akhirnya menyebabkan stimulasi, proliferasi, dan limfomagenesis sel B dan sel T yang tak
terkontrol. Virus-virus ini antara lain yaitu virus Epstein Barr, hepatitis C, human T cell
leukemia virus type 1 (HTLV-1).3
Morfologi limfoma non Hodgkin kompleks dan bervariasi. Sejak tahun 1960-an,
bermunculan berbagai metode klasifikasi. Dengan perkembangan biologi, imunologi, dan
genetika molekuler, formula klasifikasi yang baru akan lebih sesuai dengan klinis. Pada
waktu mendiagnosis penyakit ini, harus jelas diklasifikasikan termasuk jenis yang mana,
barulah dapat membantuk dokter untuk memilih strategi pengobatan yang tepat.3,4
Formulasi kerja merupakan suatu sistem klasifikasi limfoma non Hodgkin yang
dikemukakan pada tahun 1982. Klasifikasi ini terutama didasarkan kepada kriteria morfologi
(pola pertumbuhan kelenjar limfe dan karakteristik sitologi sel tumor) serta sifat progresivitas
biologik (tingkat keganasan rendah, sedang, dan tinggi). Kekurangan dari klasifikasi ini
adalah belum dapat membedakan asal tumor dari sel B atau sel T. Selain itu karena belum
memanfaatkan teknik imunologi dan genetika molekuler, belum dapat mengidentifikasi jenis
tertentu yang penting. Namun demikian, karena penggunaannya secara klinis sudah relatif
lama dan klasifikasinya sederhana, maka masih memiliki nilai referensi tertentu.3,4
World Health Organization (WHO) pada tahun 2001 mengklasifikasikan limfoma
limfoma yang berasal dari sel T dan NK. Kedua golongan besar ini memiliki banyak entitas
penyakit, setiap entitas penyakit memiliki epidemiologi, etiologi, dan ciri klinis yang khas,
mereka seringkali bereaksi berbeda terhadap terapi.15,16
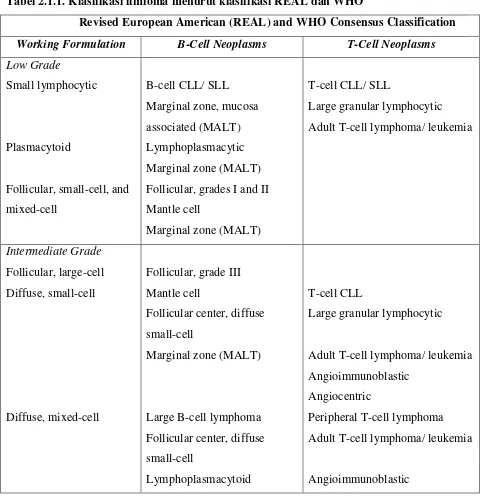
Klasifikasi limfoma dapat dilihat pada tabel di bawah ini:3
Tabel 2.1.1. Klasifikasi limfoma menurut klasifikasi REAL dan WHO
Revised European American (REAL) and WHO Consensus Classification Working Formulation B-Cell Neoplasms T-Cell Neoplasms
Low Grade
Follicular, grades I and II
Mantle cell
Marginal zone (MALT)
T-cell CLL/ SLL
Large granular lymphocytic
Adult T-cell lymphoma/ leukemia
Intermediate Grade
Adult T-cell lymphoma/ leukemia
Angioimmunoblastic
Angiocentric
Peripheral T-cell lymphoma
Adult T-cell lymphoma/ leukemia
Diffuse, large-cell
Marginal zone (MALT)
Mantle cell
Diffuse large B-cell lymphoma
Angiocentric
Intestinal T-cell lymphoma
Peripheral T-cell lymphoma
Adult T-cell lymphoma/ leukemia
Angioimmunoblastic
Diffuse large B-cell lymphoma
Precursor B-cell lymphoblastic
Burkitt Lymphoma
Peripheral T-cell lymphoma
Adult T-cell lymphoma/ leukemia
Angioimmunoblastic
Manifestasi klinis limfoma non Hodgkin bervariasi, karena jaringan limfatik tersebar
luas dalam tubuh. Jaringan limfatik di bagian manapun dapat menjadi lesi primer atau dalam
perjalanan penyakit mengalami invasi. Kelainan di bagian tubuh berbeda dapat menunjukkan
manifestasi berbeda. Selain itu limfoma non Hodgkin stadium lanjut dapat menginvasi
jaringan di luar limfatik, maka gejalanya pun lebih rumit lagi. Berikut adalah gejala dan
tanda yang dapat dijumpai pada pasien limfoma non Hodgkin:
1. Limfadenopati
15,16,17
Yang tampil dengan gejala pertama berupa pembesaran kelenjar limfe superfisial
menempati lebih dari 60% pasien, di antaranya yang mengenai kelenjar limfe bagian
leher (60-80%), aksila (6-20%), inguinal (6-12%). Pembesaran kelenjar limfe sering
asimetri, konsistensi padat dan kenyal, serta tidak nyeri.
Terjadi pada stadium lanjut, hepatomegali dan gangguan fungsi hati. Sebagian
pasien dapat menderita ikterus obstruktif akibat limfadenopati portal atau akumulasi
cairan empedu intrahepatik.
3. Kelainan skeletal
Pada limfoma non Hodgkin sering ditemukan invasi ke sumsum tulang
4. Destruksi kulit
Kelainan kulit ada yang spesifik dan non spesifik. Kelainan spesifik adalah invasi
kulit limfoma malignum, tampil bervariasi, massa, nodul, plak, ulkus, papul, dan makula.
Ada kalanya berupa eritroderma maligna. Yang non spesifik hanya transformasi dari
dermatitis biasa, berupa pruritus, prurigo, herpes zoster, iktiosis akuisita, dan lain-lain.
5. Kelainan sistem neural
Yang sering ditemukan adalah paralisis neural, sefalgia, serangan epileptik,
peninggian tekanan intrakranial, kompresi spinal, dan paraplegia.
6. Gejala sistemik
a. Demam
Demam dapat berupa demam ireguler, atau demam rekuren periodik spesifik
(Pel-Ebstein), penyebab demam mungkin terkait dengan masuknya sel tumor ke dalam
sirkulasi.
b. Keringat malam
c. Penurunan berat badan
Dalam 6 bulan berat badan turun lebih dari 10% tanpa penyebab yang spesifik
Untuk memastikan diagnosis, prosedur pemeriksaan lengkap harus dilakukan,
mencakup: anamnese yang teliti, khususnya perhatikan ada atau tidaknya simptom B,
pemeriksaan fisik lengkap, khususnya perhatikan area limfatik dan cincin Waldeyer faring,
ukuran hati dan limpa serta ada tidaknya nyeri tekan tulang.3,18
Pemeriksaan laboratorium yang diperlukan adalah pemeriksaan hematologi lengkap,
urinalisa rutin, feses rutin, laju endap darah, elektrolit darah, fungsi hati dan ginjal, biokimia
rutin mencakup gula darah, LDH serum, fosfatase alkali, asam urat, dan lainnya merupakan
Pemeriksaan radiologik yang diperlukan mencakup pemeriksaan foto toraks. Foto
toraks terutama bertujuan melihat kelenjar limfe di daerah hilus paru, mediastinum,
subkarina dan mamaria internal, sekaligus melihat ada atau tidaknya invasi ke paru. Bila
terdapat nyeri tulang, dilakukan foto di bagian tulang yang nyeri.3,18
Pemeriksaan CT yang dianjurkan adalah pemeriksaan CT scan toraks yang lebih peka
dari pemeriksaan foto toraks biasa, yang dianjurkan sebagai pemeriksaan rutin pra terapi
limfoma. Pemeriksaan USG, CT atau MRI abdomen termasuk salah satu yang diperlukan
sebelum terapi, untuk menemukan lesi rongga abdomen. Sementara pemeriksaan MRI untuk
sistem saraf pusat dan foto tulang tidak dianjurkan sebagi pemeriksaan rutin.
Pemeriksaan-pemeriksaan tersebut hanya dilakukan bila timbul gejala.3,18
Kriteria klasifikasi stadium klinis masih menggunakan patokan yang ditentukan oleh
Ann Arbor, dapat dilihat pada tabel di bawah ini:
Stadium
3,4
Tabel 2.1.2. Stadium Limfoma menurut Ann Arbor
Lingkup terkena
I Mengenai satu region kelenjar limfe (I), atau satu lokasi ekstranodal (IE)
II Mengenai dua regio lebih kelenjar limfe, tetapi semuanya masih di satu sisi
diafragma (II), atau selain itu juga terdapat invasi organ ekstranodal
terlokalisasi di sisi yang sama (IIE)
III Terdapat invasi regio kelenjar limfe di atas dan bawah diafragma (III),
dapat disertai invasi organ ekstranodal terlokalisasi (IIIE) atau disertai
invasi limpa (IIIS) atau kedua-duanya terkena (IIIES)
IV Invasi jaringan atau organ ekstranodal difus atau diseminata, tidak perduli
ada atau tidak ada invasi kelenjar limfe
Penulisan stadium juga dilengkapi dengan:3,4
B: terdapat simptom B (demam ≥ 38˚C), keringat malam, atau dalam 6 bulan berat badan
turun lebih dari 10% tanpa etiologi lain yang dapat menjelaskan)
E: satu organ ekstranodal di area dekat kelenjar limfe
X: terdapat massa besar (bulky disease)
Metode terapi terpenting pada limfoma non Hodgkin adalah kemoterapi, terutama
terhadap tingkat keganasan sedang dan tinggi. Radioterapi juga memiliki peranan tertentu
dalam terapi limfoma non Hodgkin. Terapi terhadap limfoma non Hodgkin berkaitan erat
dengan subtipe patologiknya. Dewasa ini klasifikasi patologik umumnya memakai sistem
klasifikasi baru menurut WHO tahun 2001, tetapi klasifikasi kerja masih berguna sebagai
rujukan. Setiap pasien paska terapi 2-3 siklus dan setelah selesai terapi harus diperiksa
menyeluruh, untuk menilai hasil terapi serta menentukan strategi terapi selanjutnya.
1. Limfoma agresif (intermediate/ high grade)
19
Rekomendasi terapi:
Stadium Terapi
IA, IIA non bulky (< 10 cm), termasuk E
I-II (bulky), III, IV
3-4 siklus CHOP diikuti IFRT (3000cG
dalam 10 fraksi) atau 6-8 siklus CHOP ±
radioterapi
6-8 siklus CHOP, pada daerah bulky dapat
diberikan radioterapi
2. Limfoma indolen
1. Stadium I dan II: radioterapi 3500 – 4000 cGy
2. Stadium III dan IV:
- tanpa terapi
- indikasi terapi: adanya gejala sistemik, pertumbuhan tumor yang cepat, adanya
- kemoterapi tunggal:
• Chlorambucil 4-6 mg/m2/hari PO
• Fludarabine 25 mg/m2/hari IV selama 5 hari setiap 4 minggu
• Cladribine 0,14 mg/kgBB IV drip 2 jam/ hari selama 5 hari, setiap 4
minggu atau 0,1 mg/kgBB/hari infus kontinu selama 7 hari, setiap 4
minggu
- kemoterapi kombinasi:
kemoterapi kombinasi dapat digunakan bila diperlukan respon terapi yang
cepat
- antibodi monklonal
Rituximab merupakan anti CD 20 dengan efek sitotoksik melalui aktivasi
komplemen, antibody-dependent cytotoxic cells dan efek langsung terhadap
signal intraseluler
Indikasi: penderita low grade atau follicular CD 20 positif limfoma non
Hodgkin yang relaps atau refrakter.
Dosis: 375 mg/m2 IV hari 1, 8, 15, dan 22
- Interferon α
Indikasi: follicular lymphoma (respon 40-60%)
Dosis: 2 – 3 juta unit 3 kali seminggu
- Radioterapi
Indikasi: paliatif: bulky disease dan untuk mengatasi nyeri atau obstruksi
“limited” stadium III (asimtomatik, < 5 lokasi yang terlibat, tanpa bulky
disease)
3. Limfoma relaps
Penderita dengan status performance yang baik direkomendasikan untuk stem cell
transplantation atau transplantasi alogenik. Pada sebagian besar penderita dapat
dipertimbangkan regimen terapi relaps konvensional. Pada penderita dengan status
performance kurang baik dapat diberikan monoterapi paliatif (mitoxantrone, etoposide,
Setelah selesai menjalani kemoterapi, maka pasien limfoman non Hodgkin kembali
dievaluasi. Berikut adalah tabel yang menunjukkan pemantauan keberhasilan kemoterapi
pada limfoma non Hodgkin.
Kategori Respon
20
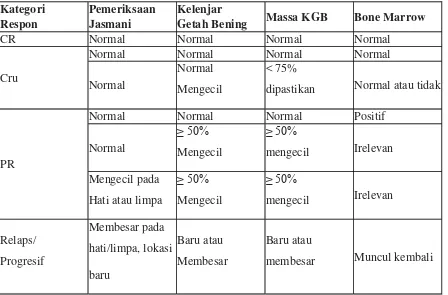
Tabel 2.1.3. Kriteria respon limfoma Pemeriksaan
Jasmani
Kelenjar
Getah Bening Massa KGB Bone Marrow
CR Normal Normal Normal Normal
Cru
Normal Normal Normal Normal
Normal
Normal
Mengecil
< 75%
dipastikan Normal atau tidak
PR
Normal Normal Normal Positif
Normal
membesar Muncul kembali
2.2.Kualitas Hidup
Kualitas hidup menurut World Health Organization (WHO) adalah persepsi
seseorang terhadap kedudukannya dalam konteks kehidupan berdasarkan nilai budaya dan
sistem dimana mereka hidup dan hubungannya dalam mencapai target sasaran.21 Ukuran
kualitas hidup saat ini banyak digunakan untuk melengkapi penilaian obyektif secara klinis
atau ukuran penyakit secara biologis untuk menilai kualitas pelayanan, pemeliharaan
kesehatan, keefektifan suatu tindakan intervensi, dan analisis penggunaan biaya.22,23
Banyak faktor yang mempengaruhi kualitas hidup seseorang, seperti faktor
terkait satu sama lain dalam menentukan kualitas hidup seseorang, namun yang akan
dibahasi di bidang kesehatan hanya kualitas hidup terkait kesehatan (health related quality of
life/ HRQOL). Banyak definisi tentang kualitas hidup terkait kesehatan, salah satunya adalah
yang didefinisikan oleh Cella dan Tulsky sebagai penilaian seseorang terhadap derajat fungsi
dan kepuasannya sekarang dibandingkan dengan apa yang diharapkan.24
Kualitas hidup penting untuk diketahui, karena pengukuran fisiologis, yang
memberikan informasi kepada dokter, pada kenyataannya tidak selalu memberikan informasi
kepada pasien. Misalnya, hasil pemeriksaan laboratorium yang tidak selalu mewakili
kapasitas organ pasien. Pasien lebih mengutamakan kapasitas fungsional dan
kesejahteraannya. Alasan lain mengapa kualitas hidup penting untuk diketahui adalah adanya
perbedaan kemampuan adaptasi seseorang terhadap penyakit. Misalnya, pada kasus
seseorang dengan sakit sendi yang sama, dapat memberikan status fungsional dan status
emosional yang berbeda. Sehingga pada kasus seperti ini, seorang pasien masih bisa bekerja
sedangkan pasien yang lain sudah berhenti bekerja.24,25
Penilaian kualitas hidup dilakukan dengan berbagai instrumen dan umumnya
dilakukan pada berbagai macam penyakit seperti diabetes, gangguan ginjal, hipertensi, asma,
AIDS, dan kanker. Penilaian kualitas hidup pada penderita kanker seperti limfoma non
Hodgkin merupakan hal yang penting dalam memberikan informasi untuk mengambil
keputusan dalam hal pengobatan, mengamati timbulnya efek samping yang tidak diinginkan,
dan untuk mengetahui kapan sebaiknya dilakukan tindakan intervensi untuk memperbaiki
kualitas hidupnya.21,26,27
Terdapat beberapa instrumen untuk menganalisis kualitas hidup yang meliputi
persepsi fisik, psikologi, dan hubungan sosial pasien, seperti Medical Outcomes Study
36-Item Short Form Health Survey (SF-36), Sickness Impact Profile, Karnofsky Scales, ECOG
Performance Scale dan lain-lain. SF-36 telah banyak digunakan dalam mengevaluasi kualitas
hidup pasien penderita penyakit-penyakit kronis. SF-36 adalah salah satu instrumen untuk
menilai kualitas hidup, sederhana, mudah, dan secara luas telah dipakai untuk mengevaluasi
kualitas hidup pada penyakit-penyakit keganasan.
2.2.1. Survei Kesehatan SF-36
SF-36 merupakan instrumen non spesifik yang biasanya digunakan pada
hampir semua penelitian penyakit kronis dan bisa juga digunakan untuk menilai
kualitas hidup pada populasi yang sehat. SF-36 telah terbukti dapat dipakai untuk
menilai kualitas hidup penderita penyakit kronis termasuk limfoma non Hodgkin.21
SF-36 ini telah diterjemahkan dalam bahasa Indonesia dan telah divalidasi.
Beberapa penelitian di Indonesia yang menggunakan skor yang baru yang belum
diterjemahkan dan divalidasi, bahkan menggunakan SF-36 sebagai baku emas,
termasuk penelitian Perwitasari di Yogyakarta yang menggunakan European
Organization for Research and Treatment of Cancer Quality of Life
Questionnaire-C30 (EORTC QLQ-Questionnaire-C30), yang meneliti mengenai pengukuran kualitas hidup pasien
kanker sebelum dan sesudah kemoterapi dengan EORTC QLC-C30 di RSUP Dr.
Sardjito Yogyakarta.30,31,32
SF-36 berisi 36 pertanyaan yang terdiri dari 8 skala antara lain:
1. Fungsi fisik (Physical Functioning)
21,22
Terdiri dari 10 pertanyaan yang menilai kemampuan aktivitas seperti berjalan,
menaiki tangga, membungkuk, mengangkat, dan gerak badan. Nilai yang rendah
menunjukkan keterbatasan semua aktivitas tersebut, sedangkan nilai yang tinggi
menunjukkan kemampuan melakukan semua aktivitas fisik termasuk latihan
berat.
2. Keterbatasan akibat masalah fisik (Role of Physical)
Terdiri dari 4 pertanyaan yang mengevaluasi seberapa besar kesehatan fisik
mengganggu pekerjaan dan aktivitas sehari-hari lainnya. Nilai yang rendah
menunjukkan bahwa kesehatan fisik menimbulkan masalah terhadap aktivitas
sehari-hari, antara lain tidak dapat melakukannya dengan sempurna, terbatas
dalam melakukan aktivitas tertentu atau kesulitan di dalam melakukan aktivitas.
Nilai yang tinggi menunjukkan kesehatan fisik tidak menimbulkan masalah
terhadap pekerjaan ataupun aktivitas sehari-hari.
3. Perasaan sakit/ nyeri (Bodily Pain)
Terdiri dari 2 pertanyaan yang mengevaluasi intensitas rasa nyeri dan pengaruh
rendah menunjukkan rasa sakit yang sangat berat dan sangat membatasi
aktivitas. Nilai yang tinggi menunjukkan tidak ada keterbatasan yang disebabkan
oleh rasa nyeri.
4. Persepsi kesehatan umum (General Health)
Terdiri dari 5 pertanyaan yang mengevaluasi kesehatan termasuk kesehatan saat
ini, ramalan tentang kesehatan dan daya tahan terhadap penyakit. Nilai yang
rendah menunjukkan perasaan terhadap kesehatan diri sendiri yang memburuk.
Nilai yang tinggi menunjukkan persepsi terhadap kesehatan diri sendiri yang
sangat baik.
5. Energi/ Fatique (Vitality)
Terdiri dari 4 pertanyaan yang mengevaluasi tingkat kelelahan, capek, dan lesu.
Nilai yang rendah menunjukkan perasaan lelah, capek, dan lesu sepanjang
waktu. Nilai yang tinggi menunjukkan perasaan penuh semangat dan berenergi.
6. Fungsi sosial (Social Functioning)
Terdiri dari 2 pertanyaan yang mengevaluasi tingkat kesehatan fisik atau masalah
emosional yang mengganggu aktivitas sosial normal. Nilai yang rendah
menunjukkan gangguan yang sering. Nilai yang tinggi menunjukkan tidak
adanya gangguan.
7. Keterbatasan akibat masalah emosional (Role Emotional)
Terdiri dari 3 pertanyaan yang mengevaluasi tingkat dimana masalah emosional
mengganggu pekerjaan atau aktivitas sehari-hari lainnya. Nilai yang rendah
menunjukkan masalah emosional mengganggu aktivitas termasuk menurunnya
waktu yang dihabiskan untuk beraktivitas, pekerjaan menjadi kurang sempurna,
dan bahkan tidak dapat bekerja seperti biasanya. Nilai yang tinggi menunjukkan
tidak adanya gangguan aktivitas karena masalah emosional.
8. Kesejahteraan mental (Mental Health)
Terdiri dari 5 pertanyaan yang mengevaluasi kesehatan mental secara umum
termasuk depresi, kecemasan, dan kebiasaan mengontrol emosional. Nilai yang
rendah menunjukkan perasaan tegang dan depresi sepanjang waktu. Nilai yang
Skala SF-36 yang terbagi atas 8 dimensi tersebut dapat dikumpulkan menjadi
2 komponen besar, dimana persepsi kesehatan umum, energi, fungsi sosial, dan
keterbatasan akibat masalah emosional disebut sebagai dimensi “Kesehatan Mental”
(Mental Component Scale), sementara fungsi fisik, keterbatasan akibat masalah fisik,
perasaan sakit/ nyeri, persepsi kesehatan umum dan energi disebut sebagai dimensi
“Kesehatan Fisik” (Physical Component Scale). Masing-masing skala dinilai 0-100,
dimana semakin tinggi skor menunjukkan semakin baiknya kualitas hidup pasien.21,33
Penghitungan hasil skor kualitas hidup terkait kesehatan dengan kuesioner
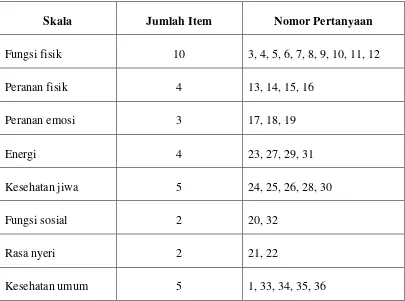
SF-36 menggunakan daftar nilai seperti yang tersebut dalam tabel di bawah ini.
Untuk skor akhir, dilakukan perhitungan rata-rata pada masing-masing pertanyaan
yang menunjukkan dimensi yang diwakilinya seperti pada tabel di bawah sehingga
hasil akhirnya akan menunjukkan skor masing-masing dimensi yaitu skor dimensi
fungsi fisik, peranan fisik, rasa nyeri, kesehatan umum, fungsi sosial, energi, peranan
emosi, dan kesehatan jiwa.21,34,35
Skala
Tabel 2.2.1.1. Pertanyaan yang mewakili 8 dimensi kuesioner SF-36
Jumlah Item Nomor Pertanyaan
Tabel 2.2.1.2. Skor kuesioner SF-36
No Pertanyaan No Respon Skor
1, 2, 20, 22, 34, 36 1 100
2 75
3 50
4 25
5 0
3, 4, 5, 6, 7, 8, 9, 10, 11, 12 1 0
2 50
3 100
13, 14, 15, 16, 17, 18, 19 1 0
2 100
21, 23, 26, 27, 30 1 100
2 80
4 40
5 20
6 0
24, 25, 28, 29, 31 1 0
2 20
3 40
4 60
5 80
6 100
32, 33, 35 1 0
2 25
3 50
4 75
5 100
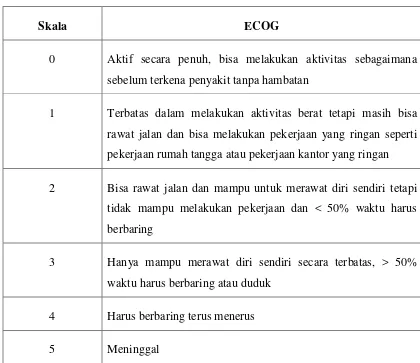
Skala ECOG dikembangkan pada tahun 1960, merupakan skala 6 poin yang
simpel, berkisar dari normal (0) hingga meninggal (5). Skala ECOG telah secara luas
digunakan dalam penelitian dan praktek klinis di bidang onkologi.6
Pada awalnya pengukuran untuk status performa adalah dengan
menggunakan skor Karnofsky yang diperkenalkan oleh David A. Karnofsky pada
tahun 1948 untuk menilai pasien yang mendapat kemoterapi nitrogen mustard pada
karsinoma paru primer. Tetapi kemudian penggunaan skala ECOG lebih disukai oleh
karena lebih mudah dan lebih simpel.6,7
Berikut adalah tabel skala ECOG:
Skala
8,9
Tabel 2.2.2.1 Skala ECOG
ECOG
0 Aktif secara penuh, bisa melakukan aktivitas sebagaimana
sebelum terkena penyakit tanpa hambatan
1 Terbatas dalam melakukan aktivitas berat tetapi masih bisa
rawat jalan dan bisa melakukan pekerjaan yang ringan seperti
pekerjaan rumah tangga atau pekerjaan kantor yang ringan
2 Bisa rawat jalan dan mampu untuk merawat diri sendiri tetapi
tidak mampu melakukan pekerjaan dan < 50% waktu harus
berbaring
3 Hanya mampu merawat diri sendiri secara terbatas, > 50%
waktu harus berbaring atau duduk
4 Harus berbaring terus menerus
BAB III
METODE PENELITIAN
3.1 Desain Penelitian
Penelitian dilakukan dengan desain cross sectional (potong lintang)
3.2. Waktu dan Tempat Penelitian
Penelitian dilakukan mulai 1 Oktober 2012 s/d 31 Desember 2013, di ruang rawat penyakit
dalam rumah sakit-rumah sakit di kota Medan.
3.3. Populasi dan Sampel
Populasi adalah semua penderita limfoma non Hodgkin.
Sampel adalah semua populasi penderita limfoma non Hodgkin yang dirawat di rumah
sakit-rumah sakit di kota Medan.
3.4. Besar Sampel
Perkiraan besar sampel 21 orang
Rumus yang digunakan:
n =
n =
n = 20,5
n = besar sampel minimum
α = tingkat kesalahan, ditetapkan sebesar 5% = 1,96
Sen = sensitivitas yang diinginkan, ditetapkan sebesar 80%
p = prevalensi limfoma non hodgkin, sebesar 75%
3.5. Kriteria Inklusi
- Pasien yang baru terdiagnosis limfoma non Hodgkin dan mendapat kemoterapi regimen
CHOP sebanyak 6 siklus
- Usia ≥ 18 tahun
3.6. Kriteria Eksklusi
- Pasien yang sudah pernah mendapat kemoterapi sebelumnya
- Pasien yang mendapat kemoterapi regimen CHOP < 6 siklus
3.7. Definisi Operasional
3.7.1. Limfoma Non Hodgkin
Limfoma non Hodgkin adalah semua pasien baru usia ≥ 1 8 tahun yang telah
ditegakkan diagnosisnya berdasarkan pemeriksaan histopatologi, belum pernah
mendapat kemoterapi sebelumnya, dan memenuhi syarat untuk dilakukan
kemoterapi dengan regimen CHOP.
3.7.2. Kemoterapi regimen CHOP
Kemoterapi regimen CHOP adalah pengobatan antikanker yang terdiri atas
Cyclophosphamide 750 mg/m2 intravena hari pertama, Doxorubicin 50 mg/m2
intravena hari pertama, Vincristine 1,4 mg/m2 intravena hari pertama, dan
Prednisone 100 mg per oral hari pertama sampai hari kelima. Kemoterapi diberikan
sebanyak 6 siklus, dengan selang waktu 21 hari.
3.7.3. SF-36
Short Form 36 adalah instrumen untuk mengukur kualitas hidup yang berisi 36 butir
pertanyaan, dijawab secara langsung oleh pasien.
3.7.4. Skala ECOG
Skala ECOG adalah instrumen untuk mengukur kualitas hidup yang terdiri atas 6
3.8. Kerangka Operasional
3.9. Bahan dan Prosedur Penelitian
Seluruh subjek diberikan penjelasan tentang tujuan,prosedur,manfaat serta resiko dalam
menjalani penelitian ini, kemudian menandatangani informed consent.
3.9.1. Pemeriksaan kualitas hidup dengan menggunakan SF-36
Pemeriksaan dilakukan dengan menanyakan 36 butir pertanyaan kepada pasien
pada 21 hingga 28 hari setelah dilakukan kemoterapi siklus keenam. Pertanyaan
terlampir.
3.9.2. Pemeriksaan kualitas hidup dengan menggunakan skala ECOG
Pemeriksaan dilakukan dengan melihat dan menilai langsung kondisi pasien pada
21 hingga 28 hari setelah dilakukan kemoterapi.
3.9.3 Kemoterapi regimen CHOP
SF-36
Pasien limfoma non Hodgkin post kemoterapi CHOP 6 siklus
ECOG - Usia
- Jenis Kelamin
- Pendidikan
- Stadium
Kemoterapi regimen CHOP dilakukan sebanyak 6 siklus dengan interval 21 hari.
Cara pemberian kemoterapi terlampir.
3.10. Analisis Data
- Untuk melihat gambaran karakteristik, berupa usia, pendidikan, jenis kelamin, stadium,
skor SF 36, skala ECOG dan respon terapi disajikan dalam bentuk tabulasi dan
dideskripsikan
- Untuk melihat distribusi SF 36 dan skala ECOG digunakan uji normalitas Shapiro Wilk
- Untuk melihat korelasi SF 36 dengan skala ECOG dan usia digunakan uji korelasi
Spearman
- Untuk melihat korelasi SF 36 dengan jenis kelamin digunakan uji T test independen
- Untuk melihat korelasi SF 36 dengan tingkat pendidikan, stadium, dan respon terapi
digunakan uji Kruskal Wallis
- Untuk melihat kemampuan SF 36 dalam memprediksi ECOG digunakan analisis
Receiver Operating Characteristic (ROC).
- Pada penelitian ini juga dilakukan uji diagnostik dengan mencari nilai sensitifitas,
spesifisitas, Positive Predictive Value (PPV), Negative Predictive Value (NPV), Positive
Likelihood Ratio (LR+), Negative Likelihood Ratio (LR-), rasio kemungkinan positif, dan
rasio kemungkinan negatif.
- Analisa statistik dilakukan dengan software SPSS versi 19.0
- Untuk semua uji statistik p < 0,05 dianggap bermakna dalam statistik
3.11. Ethical Clearance dan Informed Consent
Ethical clearence (izin untuk melakukan penelitian) diperoleh dari Komite Penelitian
Bidang Kesehatan Fakultas Kedokteran Universitas Sumatera Utara yang ditanda tangani
oleh Prof. Dr. Sutomo Kasiman, Sp.PD, Sp.JP (K).
Informed consent diminta secara tertulis dari subjek penelitian yang bersedia untuk ikut
dalam penelitian setelah mendapatkan penjelasan mengenai maksud dan tujuan penelitian
BAB IV HASIL
4.1. Karakteristik Subjek Penelitian
Telah dilakukan penelitian dengan cara potong lintang di ruang rawat Penyakit Dalam
RSUP H. Adam Malik Medan dan R.S. Pirngadi Medan pada bulan Oktober 2012 –
Desember 2013. Secara keseluruhan, terdapat 21 orang pasien limfoma non hodgkin yang
diikutsertakan dalam penelitian ini. Karakteristik klinis berupa jenis kelamin, usia, stadium,
derajat ECOG serta respon terapi dapat dilihat pada tabel 4.1.1
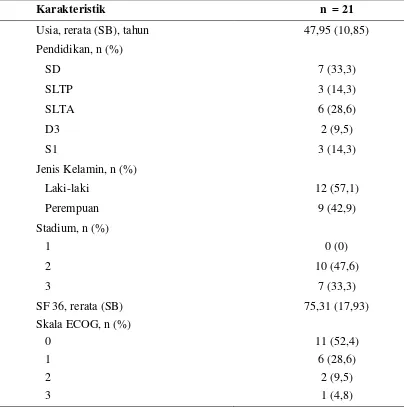
Tabel 4.1.1 Data Karakteristik Dasar Subjek Penelitian
Karakteristik n = 21
Usia, rerata (SB), tahun 47,95 (10,85)
4
Selama periode penelitian diperoleh dua puluh satu subjek. Rerata usia responden 47,95
tahun (SB=10,85 tahun). Jenis kelamin lelaki terdapat sebanyak 12 orang (57,1%). Stadium
limfoma non hodgkin pada pasien yang terbanyak adalah stadium 2 sebanyak 10 orang
(47,6%). Rerata skor SF 36 adalah 75,31 (SB = 17,93). Hasil skala ECOG terbanyak adalah
skala 0 yaitu sebanyak 11 orang (52,4%). Sebagian besar responden merupakan pasien
yang complete response sebanyak 17 orang (81%).
4.2. Hasil Penelitian
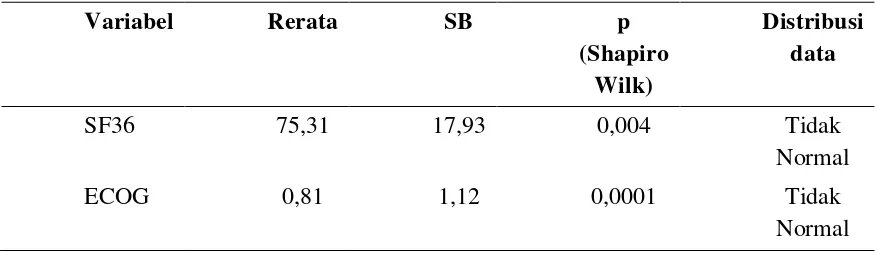
Tabel 4.2.1. Distribusi Rerata, Simpangan Baku, dan Hasil Uji Normalitas Data
Variabel Rerata SB p
Dari hasil uji normalitas data menggunakan uji Shapiro Wilk ditemukan seluruh variabel
tidak berdistribusi normal (p<0,05), sehingga uji yang dipakai untuk menetukan korelasi
antara SF36 dan ECOG menggunakan uji korelasi Spearman.
p R
SF36 - ECOG 0,0001 -0,744
Physical Health - ECOG 0,0001 -0,739
Mental Health - ECOG 0,0001 -0,739
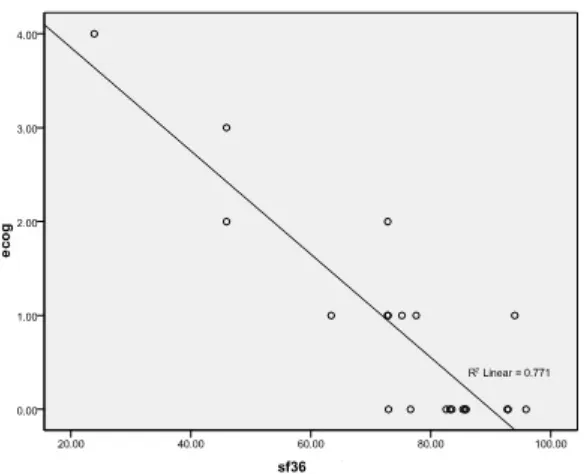
Dari analisis menggunakan uji korelasi Spearman diperoleh korelasi yang signifikan antara
SF36 dan ECOG (p=0,0001, p<0,05). Nilai korelasi (r) menunjukkan -0,744 yang berarti
terdapat korelasi yang kuat antara skor SF36 dan ECOG. Nilai r yang bertanda negatif
menunjukkan bahwa semakin tinggi skor SF36 maka akan semakin rendah ECOG. Hal
serupa juga ditunjukkan oleh masing-masing komponen, baik komponen fisik maupun
komponen mental.
Gambar 4.2.1. Grafik Scatter Plot Korelasi Skor SF 36 dengan Skala ECOG
Dari hasil analisis menggunakan uji korelasi Spearman ditemukan tidak ada korelasi yang
signifikan antara usia dan SF 36 dengan nilai p = 0,218 (p > 0,05).
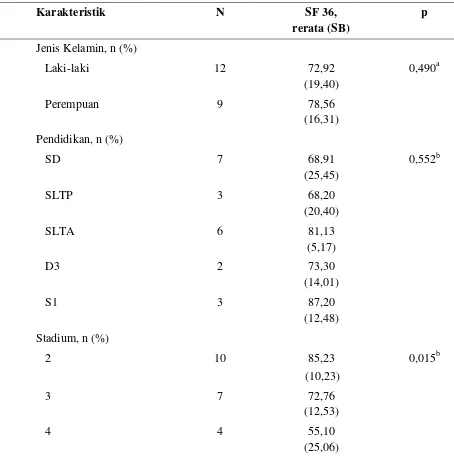
Tabel 4.2.4. Hubungan karakteristik dengan SF 36
Respon Terapi, n (%)
Complete response 17 81,97
(9,04)
0,014
Partial response
b
3 54,90
(15,50)
Progressive disease 1 23,90
a
T test independent, b Kruskal Wallis
Skor SF 36 pada perempuan lebih tinggi dibanding laki-laki yaitu 78,56 (SB=16,31)
berbanding 72,92 (SB=19,40). Namun, tidak ada perbedaan signifikan rerata skor SF 36
berdasarkan jenis kelamin (p=0,490) dengan uji t independent.
Bila dilihat skor SF 36 berdasarkan pendidikan, maka skor SF 36 tertinggi berada pada
kelompok responden dengan pendidikan S1 yaitu sebesar 87,20 (SB=12,48), tapi tidak
berbeda secara signifikan bila dibandingkan dengan rerata skor dengan tingkat pendidikan
yang lain (p=0,552).
Berdasarkan stadium limfoma non hodgkin ditemukan perbedaan yang signifikan untuk
rerata skor SF 36 (p=0,015). Skor SF 36 tertinggi berada pada kelompok pasien pada
stadium 2 dengan skor sebesar 85,23 (SB=10,23) dan terendah pada kelompok pasien
stadium 4 yaitu 55,10 (SB=25,06).
Rerata skor SF 36 terlihat signifikan berdasarkan respon terapi (p=0,014). Skor tertinggi
pada kelompok pasien yang mengalami complete response yaitu sebesar 81,97 (SB=9,04).
Kurva ROC dari Skor SF 36 terhadap ECOG
Skor SF36 dalam studi ini memiliki kemampuan untuk memprognosis skor ECOG. Dari
hasil analisis menggunakan kurva ROC diperoleh bahwa area di bawah kurva (AUC) ROC
Gambar 4.2.3. Kurva Sensitifitas dan Spesifisitas Skor SF 36 terhadap ECOG
Berdasarkan kurva sensitifitas dan spesifisitas pada gambar 4 maka diperoleh nilai Cut Off
untuk Skor SF36 adalah 54,66. Dengan menggunakan cut off point 54,66 maka didapatkan
nilai sensitivitas skor SF36 adalah 94,7% dan spesifisitas 100%.
Tabel 4.2.5. Sensitivitas, spesifisitas, positive dan negative predictive value dari skor SF36 terhadap Skala ECOG
ECOG Sensi Spesi
Baik Buruk tifitas fisitas NPP NPN RKP RKN Acc
Skor SF 36 ≥ 54,66 18 0 94,7% 100% 100% 66,67% ~ 0,05 95,23%
< 54,66 1 2
Nilai Prediksi Positif (PPV) SF36 adalah sebesar 100% dan Nilai Prediksi Negatif (NPV)
adalah 66,7%. Sedangkan untuk rasio kemungkinan positif adalah ~ dan rasio
kemungkinan negatif adalah 0,05. Akurasi diagnostik sebesar 95,23%.
BAB V PEMBAHASAN
Kualitas hidup pasien merupakan topik yang saat ini banyak diteliti dan diminati dalam
praktek dan penelitian klinis. Penilaian kualitas hidup pada penyakit keganasan menjadi alat
yang vital, tidak hanya dalam mengevaluasi hasil terapi, tetapi juga secara signifikan dapat
mempengaruhi morbiditas dan mortalitas.1
Pengukuran kualitas hidup dapat menggunakan berbagai macam instrumen. Beberapa
hanya pada penyakit tertentu. Pengukuran bisa dilakukan oleh dokter maupun pasien. Skala yang
sudah sering digunakan dalam penilaian kualitas hidup pada penyakit keganasan oleh dokter
adalah skor Karnofsky dan skala ECOG. Skala ECOG lebih disukai mengingat penggunaannya
yang mudah dan simpel sehingga tidak memakan waktu lama. Sensitifitas dan spesifisitas kedua
skala ini juga hampir sama, sebagaimana dikemukakan oleh Hollen dkk.1,2
Kualitas hidup bersifat multidimensional sehingga dalam sebuah studi yang dilakukan
oleh Bottomley dkk menyatakan bahwa skala ECOG ternyata tidak cukup sensitif dalam menilai
kualitas hidup. Hal ini dimungkinkan oleh karena skala ECOG sangat tergantung oleh penilaian
dokter, dan hanya melihat kemampuan fisik saja.2 Pada penelitian ini kami menggunakan survey
kesehatan SF 36 dalam menilai kualitas hidup pasien limfoma non hodgkin yang mendapat
kemoterapi regimen CHOP sebanyak 6 siklus. Pada penelitian ini ditemukan korelasi yang kuat
antara SF 36 dengan skala ECOG. Semakin tinggi SF 36 maka akan semakin rendah skala
ECOG. Korelasi yang kuat ini ditemukan pada kedua komponen, yaitu komponen fisik dan
komponen mental. Hasil yang serupa juga dikemukakan oleh penelitian yang dilakukan oleh
Sutrisno, dkk di Bali yang mendapatkan korelasi yang kuat antara kualitas hidup yang dinilai
dengan menggunakan EORTC QLQ C-30 dan skala ECOG. Yost, dkk mendapatkan korelasi
yang sedang antara kualitas hidup yang dinilai dengan FACT-G dan skala ECOG.7,36
Usia dinyatakan sebagai salah satu indeks prognostik untuk pasien limfoma non hodgkin,
dimana usia < 60 tahun skornya 0, sedangkan ≥ 60 tahun, skornya 1. Semakin kecil skor maka
resiko semakin rendah. Smith, dkk melaporkan bahwa usia berkorelasi negatif dengan komponen
fisik SF-36, dimana semakin tua usia maka komponen fisik akan semakin rendah. Sebaliknya,
usia berkorelasi positif dengan komponen mental SF-36, dimana semakin muda usia maka
komponen mental akan semakin rendah. Penelitian lain yang dilakukan oleh Kouroukis, dkk
melaporkan bahwa umur tidak secara nyata mempengaruhi penilaian pasien limfoma non
hodgkin terhadap kualitas hidupnya yang diukur dengan menggunakan skala SELF. Pada
penelitian ini setelah diuji secara statistik didapatkan tidak adanya korelasi usia dengan kualitas
hidup yang dinilai dengan SF 36. Hasil yang didapat kemungkinan disebabkan oleh karena pada
penelitian ini hanya 2 orang subjek yang berusia ≥ 60 tahun, sehingga tidak didapatkan hasil
yang bermakna, tetapi sebagaimana diketahui, seperti yang juga dikemukakan oleh Kouroukis,
usia muda yang cenderung memiliki pengharapan yang lebih tinggi akan kualitas hidup yang
baik, sehingga hasil yang menunjukkan bahwa seharusnya usia muda mempunyai kualitas hidup
yang lebih baik tidak didapat.37
Penelitian yang dilakukan oleh Sutrisno, dkk mendapati bahwa jenis kelamin tidak
berhubungan dengan kualitas hidup yang diukur dengan menggunakan instrumen EORTC QLQ
C-30. Hal ini sesuai dengan penelitian ini, dimana setelah diuji secara statistik didapatkan skor
SF 36 pada perempuan lebih tinggi dibanding laki-laki. Namun, tidak berbeda secara
signifikan.10
Penilaian kualitas hidup sangat terkait dengan tingkat pendidikan seseorang. Semakin
tinggi tingkat pendidikan, maka kualitas hidup seseorang akan semakin baik. Smith, dkk
melaporkan bahwa tingkat pendidikan berkorelasi dengan komponen fisik SF-36 dimana pasien
yang tidak kuliah didapati skor komponen fisiknya lebih rendah. Pada penelitian ini didapatkan
skor SF 36 tertinggi berada pada kelompok responden dengan pendidikan S1, tetapi tidak
berbeda secara signifikan bila dibandingkan dengan rerata skor SF 36 dengan tingkat pendidikan
yang lain. Hal ini mungkin disebabkan bahwa kualitas hidup yang dinilai dengan SF 36 tidak
hanya tergantung kepada tingkat pendidikan saja, tetapi juga hal-hal lain, seperti stadium, respon
terapi, dan lain-lain.10
Penelitian yang dilakukan oleh Sutrisno, dkk mendapatkan bahwa stadium penyakit
limfoma non hodgkin berkorelasi negatif dengan kualitas hidup yang diukur dengan
menggunakan EORTC QLQ C-30. Hal yang memang sudah established, dimana stadium
penyakit berbanding terbalik dengan kualitas hidup, dimana makin rendah stadium penyakit,
maka kualitas hidup pasien semakin baik. Balderas Pena, dkk melaporkan, tanpa melihat
pemberian kemoterapi atau tidak, penurunan kualitas hidup yang berkaitan dengan semakin
tingginya stadium adalah penurunan fungsi emosional dan fungsi kognitif. Balderas Pena, dkk
menggunakan instrumen Global Health Status. Pada penelitian ini, ditemukan perbedaan yang
signifikan untuk rerata skor SF 36. Skor SF 36 tertinggi berada pada kelompok pasien pada
stadium 2 dan terendah pada kelompok pasien stadium 4.10,38
Doorduijn, dkk melaporkan bahwa selama follow up kualitas hidup secara signifikan
lebih baik pada pasien lanjut usia dengan complete response atau partial remission dibandingkan
pasien yang progressive disease. Doorduijn, dkk menggunakan instrumen EuroQol 5D, EORTC