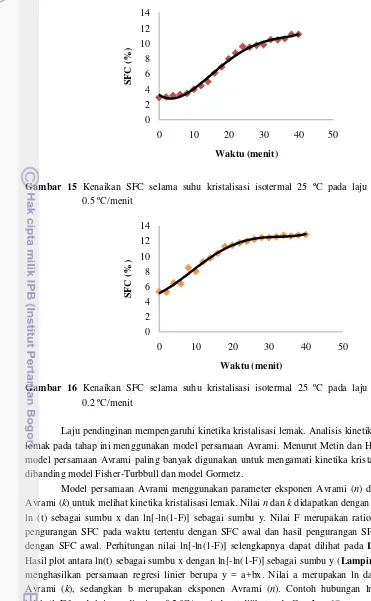
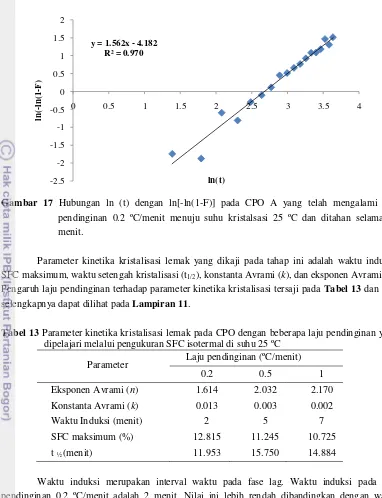
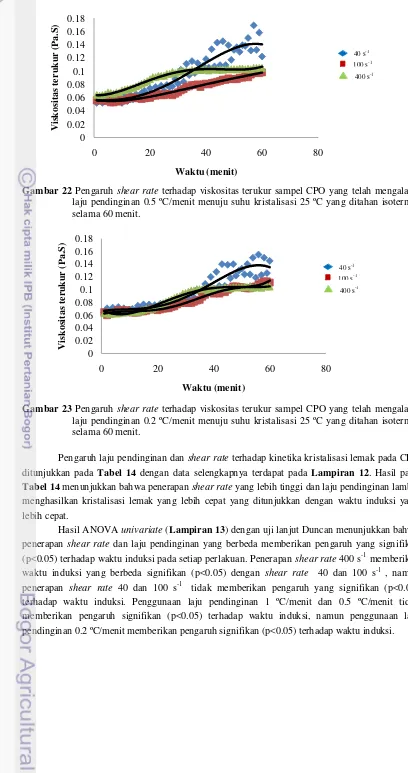
STUDY OF FAT CRYSTALLIZATION PROPERTIES OF CRUDE PALM OIL
Hanna Mery Aulia, Nur Wulandari
Department of Food Science and Technology, Faculty of Agricultural Engineering
and Technology, Bogor Agricultural University, IPB Darmaga Campus, PO BOX
220, Bogor, West Java, Indonesia
Phone: +62 856 92225790, e-mail: hanna_mery@yahoo.com
ABSTRACT
Indonesia is the biggest crude palm oil (CPO) producer in the world. Study on fat crystallization of CPO is needed to improve the knowledge of CPO handling during storage and transportation. The aim of this study is to characterize fat crystallization properties of CPO related to storage and transportation. Solid fat content (SFC) of CPO were decreased in higher temperature. After four weeks storage, SFC of CPO were increased at 20 ºC and 25 ºC, but were decreased at 30-40 ºC. CPO crystallized in slow cooling rate (0.2 ºC/minute) had higher SFC, meanwhile CPO crystallized in faster cooling rate (0.5 ºC/minute and 1 ºC/minute) had lower SFC. CPO which crystallized under slow cooling resulted higher Avrami constant (k) and lower Avrami exponent (n) than CPO which crystallized under fast cooling. The Avrami constant on cooling rate 0.2 ºC/minute, 0.5ºC/minute, and 1 ºC/minute were 0.013, 0.003, and 0.002 respectively. CPO which crystallized under fast cooling had higher induction time and crystallization half time. The Avrami exponent on cooling rate 0.2 ºC/minute, 0.5 ºC/minute, and 1 ºC/minute was 1.614, 2.032, and 2.170 repectively. Faster crystallization occured on higher shear rate. CPO which crystallized under higher shear rate had longer induction time than lower shear rate.
1
I.
PENDAHULUAN
A.
LATAR BELAKANG
Indonesia merupakan negara penghasil minyak sawit kasar (crude palm oil/CPO)terbesar
di dunia. Luas lahan perkebunan kelapa sawit Indonesia meningkat setiap tahunnya. Data Gabungan Pengusaha Kelapa Sawit Indonesia (GAPKI) menunjukkan bahwa volume ekspor CPO Indonesia tahun 2010 mencapai 15.656.349 ton, naik 0.8% dibanding ekspor 2009 yang sebesar 15.528.851 ton. Dengan meningkatnya volume ekspor CPO Indonesia, maka upaya penanganan CPO selama penyimpanan dan transportasi perlu terus dilakukan agar daya saing CPO Indonesia semakin meningkat.
Salah satu permasalahan yang sering terjadi dalam proses penyimpanan dan transportasi CPO adalah terjadinya kristalisasi lemak. Proses kristalisasi lemak pada CPO mengakibatkan terbentuknya fraksi stearin dengan titik leleh tinggi dan fraksi olein dengan titik leleh rendah. Komposisi CPO terdiri dari 50% asam lemak jenuh dan 50% asam lemak tidak jenuh yang mengakibatkan minyak sawit akan mengalami kristalisasi pada suhu rendah dan terpisah menjadi fraksi stearin dan olein (Deffense 1985).
Kristalisasi lemak merupakan salah satu parameter penting dalam rekayasa proses penyimpanan dan transportasi CPO. Kristalisasi lemak pada CPO terjadi apabila suhu transportasi atau penyimpanan tidak sesuai yang membuat lemak pada CPO memadat dan kemudian membentuk kristal. Suhu penyimpanan dan transportasi yang dipilih harus dapat meminimalkan pembentukan kristal dan kerusakan mutu CPO.
Codex Alimentarius Commision (CAC) (2005) merekomendasikan suhu maksimal dalam
transportasi CPO sebesar 55 ºC dan suhu penyimpanan maksimal 40 ºC. Hal ini menyebabkan perlu adanya pemanasan dari proses penyimpanan sebelum transportasi. Pembentukkan kristal lemak selama proses penyimpanan dan transportasi menggunakan pipa akan merugikan. Kristal lemak yang terbentuk selama transportasi akan menyumbat pipa sehingga laju alirnya akan terhambat. Proses pemanasan perlu dilakukan agar kristal lemak yang terbentuk meleleh sehingga laju alir CPO kembali lancar. Proses pemanasan untuk melelehkan kristal lemak memerlukan energi dan biaya tambahan. Untuk mengefisiensikan pemanasan dan meminimalkan kristal yang terbentuk diperlukan informasi yang cukup mengenai kristalisasi lemak pada CPO.
Kristalisasi lemak terjadi pada proses pendinginan lemak hingga mencapai suhu tertentu saat terbentuk kristal. Kristalisasi lemak dapat dibagi menjadi dua tahap, yaitu pembentukan nuklei dan perkembangan kristal (Ariana & Purboyo 1995). Lemak yang mengalami kristalisasi membentuk molekul/atom yang rigrid, beraturan (highly ordered) dan berbentuk tiga dimensi
(Nawar 1985).
Kristalisasi lemak merupakan proses yang kompleks. Parameter-parameter proses seperti suhu, gaya geser, agitasi, dan laju aliran produk sangat menentukan terjadinya kristalisasi (Man et al. 1989). Tinjauan terhadap beberapa hasil penelitian sebelumnya tentang kristalisasi
minyak/lemak menunjukkan bahwa proses kristalisasi minyak/lemak sangat dipengaruhi oleh faktor suhu, laju pendinginan, serta gaya geser yang diterapkan.
Penelitian yang terkait dengan sifat kristalisasi minyak sawit telah dilakukan oleh beberapa peneliti antara lain Graef et al. (2008; 2009), Braipson dan Gibon (2007); serta Tarabukina et al.
2 telah mengalami pemurnian (refined bleached deodorized palm oil/RBDPO), sedangkan penelitian
mengenai karakteristik kristalisasi CPO belum banyak dilakukan.
Miskandar et al. (2003) serta Metin dan Hartel (2005) menyatakan bahwa adanya
komponen minor atau kotoran yang terdapat di dalam minyak sawit kasar sangat besar pengaruhnya pada proses kristalisasi yang terjadi, sehingga fenomena kristalisasi antara minyak sawit yang telah mengalami pemurnian sangat berbeda dengan yang terjadi pada minyak sawit kasar. Dengan demikian, kajian sifat kristalisasi yang fokus pada sampel CPO perlu dilakukan.
Pada penelitian ini dilakukan kajian terhadap sifat kristalisasi lemak pada CPO. Parameter-parameter yang mempengaruhi kristalisasi lemak yaitu suhu, laju pendinginan, dan
shear rate akan dikaji pada pada penelitian ini.
B.
TUJUAN
Penelitian ini bertujuan memperoleh data dan informasi lengkap mengenai karakteristik kristalisasi minyak sawit kasar atau crude palm oil (CPO), beserta parameter kinetika
kristalisasinya.
C.
MANFAAT
3
II.
TINJAUAN PUSTAKA
A.
MINYAK SAWIT KASAR/ CRUDE PALM OIL (CPO)
1. Botani Kelapa Sawit
Tanaman kelapa sawit (Elaeis guinneensis Jacq) merupakan tumbuhan tropis
golongan palma yang termasuk tanaman tahunan. Kelapa sawit (Elaies guinneensis Jacq)
adalah tanaman perkebunan berupa pohon batang lurus dari famili Palmae. Tanaman tropis yang dikenal sebagai penghasil minyak nabati ini berasal dari Benua Amerika. Brazil dipercaya sebagai tempat dimana pertama kali kelapa sawit tumbuh (Lubis 1992).
Kelapa sawit dapat tumbuh dengan baik pada daerah tropika basah di sekitar 15 ºLintang Utara- 15 ºLintang Selatan pada ketinggian 0-500 m di atas permukaan laut (Lubis 1992). Curah hujan minimum untuk pertumbuhan kelapa sawit adalah 1000-1500 mm/tahun dan terbagi rata sepanjang tahun. Suhu optimum pertumbuhan tanaman kelapa sawit sebesar 26 oC dengan kelembaban rata-rata 75%. Tanaman kelapa sawit dapat tumbuh pada
bermacam-macam tanah, dengan syarat gembur, aerasi dan drainase baik, dan kaya akan humus pada pH optimum 5.5-7 (LITPAN 1992).
Menurut Naibaho (1998), tanaman kelapa sawit sudah mulai menghasilkan buah pada usia 24-30 bulan dan mencapai puncaknya setelah 12-15 tahun. Buah yang pertama keluar masih dinyatakan dalam buah pasir yang memiliki arti belum dapat diolah dalam pabrik karena masih mengandung kadar minyak yang rendah. Buah sawit berukuran kecil antara 12-18 gram/butir yang duduk pada bulir. Setiap bulir terdiri dari 10-18 butir tergantung pada kesempurnaan penyerbukan. Beberapa bulir bersatu membentuk tandan.
Saat ini terdapat empat tipe atau varietas kelapa sawit yang biasa ditanam oleh petani ataupun perusahaan sawit. Menurut Ketaren (2005), keempat varietas tersebut dibedakan berdasarkan ketebalan tempurung seperti terlihat pada Tabel 1.
Tabel 1 Beda tebal tempurung dari berbagai tipe kelapa sawit. Tipe Tebal Tempurung (mm) Macrocarya >5
Dura 3-5
Tenera 2-3
Pisifera <2
Sumber : Ketaren (2005)
Buah sawit mempunyai warna bervariasi dari hitam, ungu, hingga merah tergantung bibit yang digunakan. Buah terdiri dari tiga lapisan, yaitu eksokarp, mesokarp, dan endokarp. Penampang melintang buah kelapa sawit dapat dilihat pada Gambar 1.
4
Gambar 1. Penampang melintang buah kelapa sawit.
Penggunaan kelapa sawit sangat luas, yaitu 90% digunakan untuk bahan pangan dan 10% untuk bahan non-pangan. Komponen dalam minyak sawit yang digunakan sebagai bahan pangan adalah minyaknya, baik minyak sawit maupun minyak inti sawit.
2. Teknologi Produksi CPO
Pengolahan buah kelapa sawit menjadi CPO melalui beberapa stasiun proses, yaitu: a. Stasiun penerimaan buah (fruit reception)
Stasiun ini berfungsi menerima buah sawit yang telah dipanen dari kebun. Pada stasiun ini dilakukan penimbangan terhadap buah sawit. Untuk menghindari kerusakan akibat penimbunan tandan buah segar (TBS), maka TBS harus segera diproses (Corley & Tinker 2003)
b. Stasiun perebusan (sterilizer)
Buah yang telah ditimbang selanjutnya direbus dengan menggunakan uap panas. Proses sterilisasi umumnya dilakukan pada bejana tekan horizontal (Basiron 2005). Proses sterilisasi dilakukan dengan uap bertekanan 3 kg/cm2 pada suhu 143 ºC selama satu jam
(Basiron 2005 dan Corley & Tinker 2003). Perebusan yang terlalu lama dapat menyebabkan penurunan kadar minyak dan pemucatan kernel, namun perebusan yang terlalu cepat menyebabkan buah tidak dapat rontok dari tandannya. Tujuan perebusan pada tahapan produksi CPO adalah mematikan enzim lipase yang menyebabkan kenaikan asam lemak bebas (ALB), mempermudah pelepasan buah dari tandan dan inti dari cangkang, memperlunak buah sehingga mempermudah saat proses penebahan, dan mengkoagulasikan protein sehingga memudahkan saat pemurnian minyak (Basiron 2005).
c. Stasiun penebahan (threshing station)
Buah yang telah distrerilisasi selanjutnya dikirim ke stasiun penebahan untuk dipisahkan dari tangkainya (Corley & Tinker 2003). Menurut Basiron (2005) ada dua metode pemisahan buah dari tangkai, yaitu dengan getaran dan pukulan. Namun saat ini pemisahan buah dari tangkainya sudah menggunakan drum yang berputar dengan kecepatan 20-25 rpm. Brondolan buah sawit yang keluar dari bagian bawah drum ditampung oleh sebuah conveyor
lalu diangkat dengan fruit elevator untuk dikirim ke bagian digesting dan pressing.
d. Stasiun kempa (pressing station)
Pada stasiun ini daging buah dan biji diekstrak atau diperas sehingga menghasilkan minyak. Proses ekstraksi dilakukan pada suhu 90-100 ºC selama 20 menit (Basiron 2005).
Mesokarp
Tempurung
5 e. Stasiun pemurnian minyak (clarification station)
Minyak kasar hasil pengepresan mengandung 66% minyak, 24% air, dan 10% padatan (Basiron 2005). Menurut Corley dan Tinker (2003) proses pemurnian minyak bertujuan mendapatkan kadar air, kadar kotoran, dan ALB yang sesuai dengan standar. Tahapan proses di stasiun klarifikasi adalah tahap penyaringan crude oil dengan vibrating screen, tahap pemisahan minyak pada tangki, tahap pemurnian minyak, tahap pengambilan
minyak dari sludge, dan tahap pengurangan kadar air.
B.
SIFAT FISIKO KIMIA MINYAK SAWIT
1. Sifat Kimia Minyak Sawit
Menurut Naibaho (1998) tanaman kelapa sawit menghasilkan dua jenis minyak nabati, yaitu minyak sawit dan minyak inti sawit. Kedua jenis minyak tersebut mempunyai perbedaan karakteristik seperti tersaji pada Tabel 2. Minyak sawit merupakan hasil ekstraksi daging buah (mesokarp) dari tanaman Elaeis guinneensis. Minyak inti sawit merupakan hasil
pengepresan endokarp dari tanaman Elaeis guinneensis.
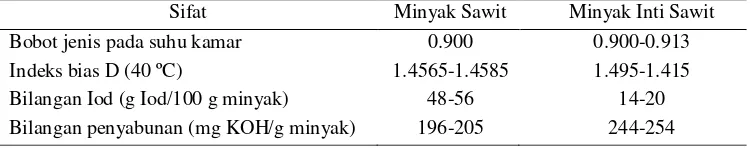
Tabel 2 Sifat fisiko kimia minyak sawit kasar dan minyak inti sawit
Sumber : Ketaren (2005)
Bilangan Iod menggambarkan derajat ketidakjenuhan suatu lemak yang dihitung berdasarkan perbandingan asam lemak jenuh dan tidak jenuh penyusun lemak tersebut. Data pada Tabel 2 menunjukan bilangan Iod minyak sawit dan minyak inti sawit adalah 48-56 dan 14-20 g Iod/100 g minyak. Perbedaan ini terjadi karena asam lemak penyusun kedua minyak tersebut berbeda. Asam lemak dominan penyusun minyak sawit adalah 47% asam palmitat dan 41% asam oleat (Basiron 2005). Keseimbangan antara asam lemak jenuh dan asam lemak tidak jenuh penyusun minyak sawit menyebabkan bilangan Iod minyak sawit berkisar 48-56 g Iod/100 g minyak. Minyak inti sawit tersusun atas 48% asam laurat, 16% asam miristat, dan 15% asam oleat (Pantrazis & Basiron 2002). Asam lemak dominan penyusun minyak inti sawit adalah asam laurat yang merupakan asam lemak jenuh. Hal inilah yang menyebabkan bilangan Iod minyak inti sawit rendah yaitu berkisar 14-20 g Iod/100 g minyak.
Menurut Ketaren (2005), bilangan penyabunan adalah jumlah alkali yang dibutuhkan untuk menyabunkan sejumlah minyak. Bilangan penyabunan dinyatakan dalam miligram kalium hidroksida yang dibutuhkan untuk menyabunkan satu gram minyak atau lemak. Kalium hidroksida akan bereaksi dengan asam lemak membentuk garam asam lemak. Bilangan penyabunan minyak sawit lebih rendah daripada bilangan penyabunan minyak inti sawit karena pada minyak sawit terdapat komponen yang tidak tersabunkan. Menurut Lin (2002) dalam minyak sawit terdapat komponen yang tidak dapat disabunkan seperti sterol, pigmen, dan hidrokarbon.
CPO tersusun atas 50% asam lemak jenuh dan 50% asam lemak tidak jenuh. Keseimbangan antara asam lemak jenuh dan asam lemak tidak jenuh menyebabkan CPO lebih stabil terhadap oksidasi dibanding minyak nabati lainnya dan CPO berwujud semisolid
6 pada suhu ruang (Basiron 2005). Menurut Rohani et al. (2006), komponen utama dalam CPO
adalah triacylglicerol (TAG) yaitu sebesar 95%. TAG merupakan kombinasi dari gliserol dan
tiga asam lemak. Komposisi asam lemak dan TAG penyusun minyak sawit dapat dilihat pada Tabel 3 dan Tabel 4
Tabel 3 Asam lemak penyusun minyak sawit.
Jenis asam lemak Komposisi (%) Asam kaprat (C10:0) 1-3 Asam laurat (C12:0) 0.1-1 Asam miristat (C14:0) 0.9-1.5 Asam palmitat (C16:0)
Asam palmitoleat (C16:1)
41.8-46.8 0.1-0.3 Asam stearat (C18:0) 4.2-5.1 Asam oleat (C18:1) 37.3-40.8 Asam linoleat (C18:2) 9.1-11.0 Asam linolenat (C18:3) 0-0.6 Asam arakhidonat (C20:0) 0.2-0.7
Sumber : Basiron (2005)
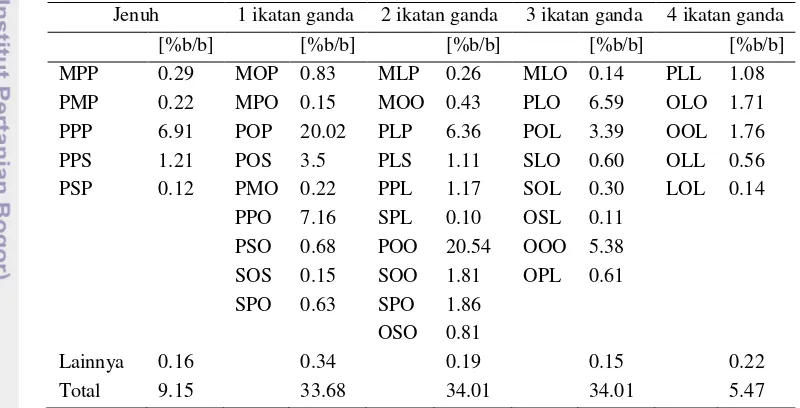
Tabel 4 Komposisi TAG penyusun minyak sawit
Jenuh 1 ikatan ganda 2 ikatan ganda 3 ikatan ganda 4 ikatan ganda [%b/b] [%b/b] [%b/b] [%b/b] [%b/b] MPP 0.29 MOP 0.83 MLP 0.26 MLO 0.14 PLL 1.08 PMP 0.22 MPO 0.15 MOO 0.43 PLO 6.59 OLO 1.71 PPP 6.91 POP 20.02 PLP 6.36 POL 3.39 OOL 1.76 PPS 1.21 POS 3.5 PLS 1.11 SLO 0.60 OLL 0.56 PSP 0.12 PMO 0.22 PPL 1.17 SOL 0.30 LOL 0.14
PPO 7.16 SPL 0.10 OSL 0.11 PSO 0.68 POO 20.54 OOO 5.38 SOS 0.15 SOO 1.81 OPL 0.61 SPO 0.63 SPO 1.86
OSO 0.81
Lainnya 0.16 0.34 0.19 0.15 0.22
Total 9.15 33.68 34.01 34.01 5.47
M : asam lemak miristat P: asam lemak palmitat S: asam lemak stearat O: asam lemak oleat L : asam lemak linolenat
Sumber : Gee (2007)
CPO memiliki dua komponen asam lemak terbesar yaitu asam palmitat dan asam oleat. Kandungan asam palmitat pada minyak sawit sebesar 41.8-46.8%, sedangkan asam oleat sebesar 37.3-240.8% (Basiron 2005). Asam palmitat adalah asam lemak jenuh rantai panjang yang memiliki titik cair (melting point) yang tinggi, yaitu 64 ºC (Belitz & Grosch
1999). Kandungan asam palmitat yang tinggi membuat minyak sawit tahan terhadap oksidasi. Asam oleat adalah asam lemak tidak jenuh dengan rantai panjang C18 dan memiliki dua ikatan
7 Selain kandungan asam lemak terdapat juga komponen minor pada minyak sawit yang mempengaruhi kualitasnya. Kandungan komponen minor pada CPO dapat dilihat pada
Tabel 5. Kandungan komponen minor mempunyai peranan penting dalam kestabilan minyak
walaupun kandungannya hanya 1%. Faktor lain yang menentukan kualitas minyak sawit adalah bau, flavor, dan warna. Menurut Ketaren (2005), asam lemak dan TAG tidak berwarna. Bau khas minyak sawit ditimbulkan oleh gugus beta ionone dari karotenoid. Bau menyimpang pada minyak sawit terbentuk akibat kerusakan asam lemak rantai pendek.
Tabel 5 Kandungan komponen minor pada CPO
Komponen minor Kandungan (ppm)
Karoten 500-700
Tokoferol dan tokotrienol 600-1000
Sterol 326-527
Ubiquinone 10-80
Squalene 200-500
Phospolipid 5-130
Triterpene alkohol 40-80
Metil sterol 40-80
Alifatik alkohol 100-200
Sumber : Lin (2002)
CPO mempunyai warna merah yang diakibatkan oleh adanya karotenoid. CPO mengandung 500-700 ppm karotenoid (Basiron 2005). Karotenoid yang terdeteksi terdiri dari α-karoten, -karoten, dan likopen dalam jumlah yang sedikit sekali (Muchtadi & Sugiyono 1992). Karotenoid sangat larut dalam minyak. Bila minyak dihidrogenasi maka warna merah dari karotenoid akan berkurang. Karotenoid memiliki sifat tidak stabil pada suhu tinggi. Pada minyak sawit, kandungan karotenoid jarang dihilangkan sepenuhnya karena merupakan pro vitamin A (Winarno 1992). Menurut Hartley (1987) terdapat dua jenis warna buah sawit yang berbeda, satu berwarna merah dan lainnya berwarna oranye. Kedua warna buah tersebut memberikan kandungan karoten yang berbeda. Pada buah yang berwarna merah, total karoten di dalam mesokarp kering berkisar 207 mg per 100 gram, dan total karoten dalam minyak berkisar 2560 ppm, sedangkan untuk buah yang berwarna oranye, total karoten di dalam mesokarp hanya 89 mg per 100 gram, dan total karoten dalam minyak hanya 1100 ppm.
Perbedaan lain antara minyak sawit dengan minyak nabati lainnya adalah adanya kandungan tokoferol dan tokotrienol. Menurut Law dan Thiaharajan (1989), tokoferol dan tokotrienol (vitamin E) ditemukan dalam produk minyak sawit berkisar dari 600-1000 ppm dengan komposisi 83% tokotrienol dari total vitamin E. Menurut Basiron (2005) kandungan tokoferol dan tokotrienol pada minyak sawit yang telah dimurnikan akan berkurang sebesar 50%. Tokoferol dan tokotrienol sangat penting bagi kesehatan karena befungsi sebagai antioksidan alami (pengikat radikal bebas).
2. Sifat Fisik Minyak Sawit
Sifat fisik minyak sawit yang penting untuk diketahui antara lain densitas, indeks refraktif, slip melting point (SMP), dan solid fat content (SFC). Menurut Winarno (1992),
8 penyusunnya. Komposisi asam lemak pada CPO beraneka ragam yang masing-masing memiliki titik leleh berbeda-beda sehingga titik leleh CPO merupakan suatu kisaran.
Menurut Lin (2002), SFC merupakan jumlah kandungan lemak padat yang terdapat pada suatu lemak. Lemak padat dihasilkan dari proses kristalisasi. Nilai SFC sering digunakan untuk menggambarkan daya oles (spreadability) suatu bahan pangan pada suhu tertentu.
Karakteristik fisik minyak sawit yang diteliti oleh Lin (2002) dan Basiron (2005) tersaji pada Tabel 6.
Tabel 6 Karakteristik fisik minyak sawit
Karakteristik Kisaran Rata-rata Indeks Refraktif (50 ºC) 1.4544-1.4550(a) 1.4548(a)
1.455-1.456(b) 1.455(b)
Densitas (50 ºC) 0.8896-0.8910(a) 0.8899(a) 0.888-0.889(b) 0.889(b)
Slip Melting Point (ºC) 32-40 (a)
31.1-37.6(b) 34.2(b) Solid Fat Content (SFC)
5 ºC 50.7-68(b) 60.5(b)
10 ºC 46.1-60.8(a) 53.7(a) 40.0-55.2(b) 49.6(b)
15 ºC 33.4-50.8(a) 39.1(a) 27.2-39.7(b) 34.7(b)
20 ºC 21.6-31.3(a) 26.1(a) 14.7-27.9(b) 22.5(b)
25 ºC 12.1-20.7(a) 16.3(a) 6.5-18.5(b) 13.5(b)
30 ºC 6.1-14.3(a) 10.5(a) 4.5-14.1(b) 9.2(b)
35 ºC 3.5-11.7(a) 7.9(a) 1.8-11.7(b) 6.6(b)
40 ºC 0.0-8.3(a) 4.6(a) 0.0-7.5(b) 4(b)
45 ºC 0.7(b)
Sumber : (a)Lin (2002) (b)Basiron (2005)
SFC menunjukkan banyaknya kandungan lemak padat pada suatu lipid. Menurut Basiron (2005), kandungan TAG menentukan SFC CPO. Pada suhu 10 ºC, SFC CPO mencapai 50% dan akan berkurang menjadi separuhnya saat suhu 20 ºC. Penambahan 10% diacylgliserol (DAG) akan
9
C.
KRISTALISASI LEMAK
1. Mekanisme Kristalisasi Lemak
Pada proses pengolahan produk pangan berbasis lemak, sangat penting untuk mengontrol kristalisasi lemak untuk mendapatkan jumlah, ukuran, polimorfisme, dan fase dispersi kristal yang diinginkan. Pada produk pangan berbasis lemak, kristalisasi lemak sangat dipengaruhi oleh kristalisasi TAG, namun kristalisasi komponen lemak lainnya yaitu DAG, monoacylglicerol (MAG), dan fosfolipid juga turut berperan besar.
Menurut Winarno (1992), bila suatu lemak didinginkan, hilangnya panas akan memperlambat gerakan molekul-molekul dalam lemak, sehingga jarak antar molekul lebih kecil. Jika jarak antar molekul tersebut mencapai 5Ǻ, maka akan timbul gaya tarik menarik antar molekul. Akibat adanya gaya ini, radikal-radikal asam lemak dalam molekul lemak akan tersusun berjajar dan saling bertumpuk serta membentuk ikatan kristal.
Pemadatan lemak akibat proses kristalisasi merupakan proses yang tidak sederhana. Parameter-parameter proses seperti suhu, gaya geser, agitasi, dan laju aliran produk sangat menentukan terjadinya kristalisasi (Man et al. 1989). Faktor-faktor tersebut juga menentukan
bentuk struktur kristalin produk berlemak. Menurut Lawler dan Dimick (2002), proses kristalisasi dari larutan membutuhkan kondisi lewat jenuh (supersaturation), dilanjutkan
dengan kondisi lewat dingin (supercooling), sehingga akan terjadi pembentukan inti
(nucleation) dan pertumbuhan kristal (crystal growth).
Menurut Metin dan Hartel (2005), driving force untuk terjadinya kristalisasi adalah
adanya perbedaan suhu aktual (T) di bawah suhu titik leleh (melting temperature, Tm) TAG.
Pada lemak alami, terjadi interaksi yang kompleks diantara campuran TAG dengan jenis asam lemak dan titik leleh yang berbeda. Hal ini menyebabkan lemak alami memiliki kisaran titik leleh yang lebar. Beberapa peneliti menggunakan titik leleh TAG tertinggi sebagai acuan driving force kristalisasi. Bila lemak didinginkan di bawah titik leleh dari
komponen TAG dengan titik leleh tertinggi, akan terdapat rasio antara lemak padat terhadap lemak cair yang tergantung pada kondisi campuran TAG, yang dikenal dengan kandungan lemak padat (solid fat content/SFC).
Menurut Lawler dan Dimick (1998), saat bulk minyak dikristalisasi, massa minyak
tidak terkristalisasi secara serempak. Pada kenyataannya, kristalisasi dimulai pada sisi-sisi tertentu saat suhu mencapai tingkat yang mampu membentuk inti kristal. Dengan demikian, saat lemak yang dilelehkan mengalami pendinginan, akan terbentuk produk dengan tekstur granular akibat kristalisasi yang terjadi secara bertahap (gradual) pada setiap gliserida.
Kristalisasi pada lemak alami diawali dengan pembentukan kristal yang tipis dan berupa platelet yang cukup panjang, dan dilanjutkan dengan agregasi kristal lemak
membentuk spherulites dari ukuran beberapa mikron hingga 300 mm. Bila kristalisasi terjadi
sangat lambat, kristal spherulites yang sangat besar akan terbentuk. Sebaliknya, pendinginan
yang cepat pada suhu rendah akan menghasilkan kristal yang halus dan acak. Dengan demikian, laju pendingian merupakan faktor yang paling penting dalam menentukan mikrostruktur kristal lemak (Metin & Hartel 2005).
Menurut Richard et al.(2000), lemak yang telah dilelehkan memiliki kecenderungan
10
2. Faktor-Faktor yang Mempengaruhi Kristalisasi Lemak
Parameter yang mempengaruhi kristalisasi lemak juga akan mempengaruhi kinetika kristalisasinya. Parameter yang mempengaruhi kristalisasi lemak meliputi komposisi TAG, laju pendinginan, agitasi, suhu kristalisasi, dan komponen minor pada lemak.
a. Laju Pendinginan (Cooling Rate)
Kristalisasi lemak sangat dipengaruhi oleh laju pendinginan. Pendinginan cepat menyebabkan nukleasi terjadi pada suhu yang lebih rendah dibanding dengan pendinginan lambat. Laju pendinginan juga berpengaruh pada laju nukleasi, yang mempengaruhi ukuran kristal. Pendinginan cepat sampai suhu rendah menyebabkan laju nukleasi cepat dan mengakibatkan pembentukan kristal kecil. Ketika lemak didinginkan dengan lambat, kristal terbentuk dengan ukuran yang lebih besar. Laju pendinginan juga mempengaruhi mikrostruktur kristal (Metin & Hartel 2005)
Pada laju pendinginan cepat, akan terbentuk kristal-kristal lemak yang lebih kecil dan seragam dibandingkan bila pendinginan dilakukan pada laju lambat. Bila pada lemak terlalu banyak kristal-kristal kecil (dari tipe kristal α), struktur lemak akan menjadi terlalu rapat. Kapiler antar padatan akan menyempit, dan mengakibatkan kristal-kristal saling mengunci dengan cairan yang ada di sekelilingnya (Che & Swe 1995).
Menurut Lawson (1995), ketika MAG didinginkan secara cepat, kristal pertama yang terbentuk adalah bentuk α. Bentuk kristal ini akan berubah secara irreversible
menjadi bentuk ‟ yang lebih stabil. Pada akhirnya kristal ‟ akan berubah menjadi bentuk kristal yang merupakan bentuk kristal paling stabil.
Pada proses pendinginan minyak dan lemak yang dilakukan secara mendadak, terjadi pembentukan kristal campuran dari TAG yang bertitik leleh tinggi dan rendah (Man et al. 1989). Di lain pihak, pendinginan cepat yang dibantu dengan proses
pengadukan menyebabkan terjadinya kristalisasi TAG bertitik leleh tinggi dan rendah pada waktu yang bersamaan (Borwanker et al. 1992). Pengadukan dan agitasi juga dapat
memperlunak tekstur produk dan menurunkan kadar lemak padat (solid fat content/SFC)
selama penyimpanan (Herrera & Hartel 2000).
b. Komponen Minor
Menurut Metin dan Hartel (2005), komponen minor yang dapat mempengaruhi kristalisasi lemak adalah lemak yang lebih polar seperti DAG, MAG, asam lemak bebas, fosfolipid, dan sterol. Kehadiran komponen ini mempercepat proses kristalisasi lemak tetapi pada keadaan lain dapat menghambat.
Adanya komponen-komponen pengotor lain selain lemak (impurities), akan
berpengaruh terhadap terjadinya kristalisasi (Miskandar et al. 2003). Menurut Timms
(1997), adanya kotoran dalam minyak biasanya menyebabkan penurunan laju nukleasi. Diasumsikan bahwa kotoran tersebut mengotori sisi pertumbuhan kristal pada inti kristal. Sejumlah kecil pengotor dapat menurunkan laju nukleasi hingga beberapa kali lipat. Metin dan Hartel (2005) menyebutkan bahwa adanya pengotor pada crude oil akan
11
c. Komposisi TAG
Lemak alami mengandung beberapa jenis TAG dengan asam lemak yang berbeda panjang rantainya, dan derajat kejenuhannya. Basiron (2005) mengemukakan bahwa minyak sawit mengandung kombinasi asam-asam lemak dengan panjang rantai dan derajat ketidakjenuhan yang berbeda, dan di dalamnya terkandung TAG dengan titik leleh yang rendah dan tinggi. Kristalisasi minyak sawit pada pendinginan yang terkontrol diikuti dengan proses separasi akan menghasilkan fase cairan bertitik leleh rendah (olein), dan fase padat bertitik leleh tinggi (stearin), dengan rasio olein terhadap stearin sekitar 7:3 (Ong et al. 1995).
CPO mengandung 4-8% DAG, yang dapat membentuk campuran eutectic
dengan TAG, yang menghasilkan kadar padatan yang rendah dan dapat memperlambat laju kristalisasi. MAG dalam CPO kurang dari 1% dan tidak memberikan pengaruh yang nyata terhadap proses kristalisasi (Basiron 2005).
d. Agitasi
Kecepatan pengadukan umumnya mempengaruhi nukleasi dan pertumbuhan kristal. Namun, pengaruh laju pengadukan sangat kompleks karena terkadang sulit untuk mengetahui perbedaan pengadukan dan laju pendinginan pada kristalisasi. Menurut Metin dan Hartel (2005), agitasi menaikkan nukleasi karena adanya mekanisme penggangguan terhadap supply energi. Laju pendinginan lambat dan agitasi lambat pada lemak
menghasilkan kenaikan sejumlah kristal sehingga cakupan pelelehan meningkat. Laju agitasi tinggi menghasilkan laju kristalisasi yang tinggi pula dan kristal lemak yang kecil.
e. Suhu Kristalisasi
Parameter yang paling penting dalam mempengaruhi kristalisasi lemak adalah suhu kristalisasi dimana lemak membeku di bawah titik lelehnya. Ketika suhu kristalisasi dinaikkan, maka suhu nukleasi meningkat dan waktu induksi untuk kristalisasi bertambah. Pada lemak alami dimana panjang rantai asam lemaknya berbeda, kristal lemak dapat terbentuk jika panjang rantai dan titik lelehnya berdekatan (Metin & Hartel 2005).
3. Kinetika Kristalisasi Lemak
Pengetahuan mengenai kinetika kristalisasi lemak penting untuk menentukan parameter proses (suhu kristalisasi dan laju pendinginan) yang tepat agar dihasilkan produk dengan jumlah, ukuran, dan polimorfisme kristal lemak yang diinginkan. Pemodelan kinetika kristalisasi lemak telah dilakukan, yaitu model Avrami dan model Fisher-Turnbull. Model Fisher-Turnbull melihat nukleasi berdasarkan pada perubahan energi (Metin & Hartel 2005). Menurut Himawan et al. (2006), model Avrami banyak digunakan untuk melihat kinetika
kristalisasi lemak saat isotermal. Model Avrami menggambarkan laju kristalisasi dan mekanisme pembentukan inti kristal lemak (nucleation). Menurut Metin dan Hartel (2005),
persamaan Avrami (Persamaan 1), banyak digunakan untuk menggambarkan proses nukleasi dan pertumbuhan kristal lemak.
1− � = exp[−���] (1)
12
F adalah fraksi kristal yang terbentuk selama waktu kristalisasi t (menit), k adalah
laju kristalisasi konstan yang ditentukan terutama oleh suhu kristalisasi, dan n adalah
eksponen Avrami.
Eksponen Avrami (n) adalah fungsi dari dimensi pertumbuhan kristal, dan
menggambarkan mekanisme nukleasi dan pertumbuhan kristal secara detail (Tabel 7). Metin dan Hartel (1998) menggunakan model persamaan Avrami untuk melihat kinetika kristaliasi lemak pada cocoa butter,lemak susu, dan milk fat fraction. Eksponen Avrami (n) untuk cocoa butter,lemak susu, dan milk fat fraction masing-masing bernilai 4,3, dan 2. Nilai eksponen
Avrami (n) bernilai 4, 3, dan 2 menunjukkan pembentukan inti secara heterogenous nucleation, instantaneous nuclei, dan high nucleation rate.
Tabel 7. Hubungan antara mekanisme pertumbuhan kristal lemak dengan eksponen Avrami
(n)
Mekanisme pertumbuhan kristal Nilai konstanta n** Polyhedral
Plate-like
Silinder
4 3 2 ** n = indeks persamaan Avrami.
Sumber : Toro et al. (2002).
Nilai k secara langsung berhubungan dengan waktu setengah kristalisasi (t1/2). Laju
kristalisasi (k) sangat dipengaruhi oleh suhu kristalisasi. Menurut Martini et al.(2002), suhu
kristalisasi yang tinggi menyebabkan driving force kristalisasi rendah sehingga laju kristalisasi
rendah. Selain itu, laju kristalisasi mempunyai hubungan terbalik dengn waktu induksi dan waktu setengah kristalisasi. Waktu induksi merupakan waktu ketika fraksi kristal yang terbentuk bertambah secara cepat dari fraksi kristal awal (Metin & Hartel 1998). Waktu setengah kristalisasi (t1/2) menunjukkan jumlah waktu dalam menit yang dibutuhkan untuk
membentuk 50% fraksi kristal (Martini et al. 2002).
4. Polimorfisme Lemak
Pada minyak alami banyak terkandung berbagai jenis TAG dengan panjang asam lemak dan derajat ketidakjenuhan yang berbeda. Perbedaan komposisi ini menyebabkan terjadinya proses kristalisasi yang sangat kompleks. Dalam pembentukan latis (lattice)
kristal, molekul TAG dapat mengalami beberapa bentuk kristal yang sangat ditentukan oleh kondisi proses, dan fenomena ini dikenal dengan polimorfisme (Metin & Hartel 2005). Sifat kristalisasi TAG yang mencakup laju kristalisasi, ukuran kristal, morfologi, dan total kristalinitas dipengaruhi oleh polimorfisme. Polimorfisme dipengaruhi oleh struktur molekul TAG, dan faktor eksternal seperti suhu, tekanan, laju kristalisasi, adanya pengotor, dan laju geser.
Menurut Metin dan Hartel (2005) terdapat tiga kategori bentuk polimorfik lemak yaitu α, dan . Bentuk α paling tidak stabil dengan titik leleh dan panas laten peleburan paling rendah, sedangkan bentuk bersifat paling stabil. Setiap polimorfik memiliki short spacings atau spasi pendek (jarak antara gugus asil paralel pada TAG), sifat dan ukuran yang
13 Tabel 8 Identifikasi bentuk polimorf lemak berdasarkan analisis difraksi sinar X pada spasi
pendek (short spacings), sifat, dan ukuran.
Bentuk
polimorf Sel unit
(a) Garis dan spasi pendek
(Ǻ)(a) Sifat
(b) Ukuran
(µm)(b) α Heksagonal Satu garis tebal dan sangat
lebar pada 4.15 Rapuh, transparan, pipih
5
„ Ortorombik Dua garis tebal pada 4.2
dan 3.8 Jarum halus 1
Triklinik Sebuah garis tebal pada 4.6 Besar-besar dan
berkelompok
kadang-kadang 100 Sumber : (a)Metin dan Hartel (2005) (b) Fenema (1976) dalam Winarno (1992)
Metin dan Hartel (2005) mengemukakan bahwa bentuk polimorfik yang paling tidak stabil biasanya terbentuk lebih dahulu pada lemak cair yang lewat dingin karena energi permukaannya yang lebih rendah. Laju transformasi polimorfik pada lemak alami yang mengandung banyak TAG berjalan sangat lambat. Bentuk α terjadi saat lemak mengalami pendinginan cepat, dan segera berubah menjadi bentuk . Bentuk dan dapat bertahan pada waktu yang cukup panjang (beberapa jam atau hari). Untuk beberapa lemak tidak terjadi perubahan dari bentuk menjadi seperti yang terjadi pada lemak sawit. Menurut Sato dan Ueno (2005), perubahan bentuk polimorfisme dari α menjadi yang paling stabil terjadi secara irreversible. Laju perubahan polimorfisme yang terbentuk sangat bergantung
pada waktu dan suhu. Laju perubahan polimorfisme kristal lemak dapat dilihat pada Gambar 2.
Gambar 2 Laju perubahan polimorfik kristal lemak (Marangoni & McGauley 2003)
Setiap lemak atau minyak mempunyai bentuk polimorf kristal lemak yang berbeda-beda. Menurut Marangoni dan McGauley (2003), cocoa butter mempunyai enam bentuk kristal lemak
14
D.
KRISTALISASI MINYAK SAWIT
Menurut Smith (2001), komposisi minyak sawit yang terdiri dari beraneka ragam TAG membuat minyak sawit tidak mengkristal pada suhu tertentu. Parameter untuk melihat terjadinya kristalisasi lemak pada minyak sawit salah satunya adalah solid fat content (SFC). SFC merupakan
jumlah kandungan lemak padat pada suatu lipid. Nilai SFC mempunyai hubungan terbalik dengan suhu yang berarti semakin tinggi suhu akan menghasilkan SFC yang semakin kecil. Kurva hubungan suhu dengan SFC RBDPO ditunjukkan oleh Gambar 3.
Gambar 3 Kurva hubungan suhu dengan SFC pada sampel RBDPO (Smith 2001)
Tarabukina et al. (2009) telah melakukan pengujian profil kristalisasi lemak RBDPO
dengan menggunakan instrumen Differential Scanning Calorimetry (DSC) pada beberapa laju
pendinginan (10, 5, dan 0.5 oC/menit). Laju pendinginan ternyata berpengaruh nyata terhadap
entalpi kristalisasi dan waktu terjadinya kristalisasi tahap pertama. Melalui Gambar 4 dapat diketahui bahwa pada laju pendinginan yang lambat akan terjadi peningkatan suhu peak
kristalisasi.
Gambar 4 Termogram DSC pada pendinginan CPO dari 70 oC hingga -30 oC pada beberapa
laju pendinginan (-10, -5, dan -0.5 oC/menit). Berat masing-masing sampel 11.1,
9, dan 11.4 mg (Tarabukina et al. 2009).
Pengaruh laju pendinginan terhadap sifat kristalisasi CPO telah dikaji oleh Chong et al.
15 sensitivitas tinggi. Pengujian dilakukan pada laju pendinginan 0.1 dan 0.4 °C/menit, dari titik lelehnya hingga suhu -20 °C, untuk mengetahui bentuk penataan TAG sebagai fungsi dari suhu dan perlakuan panas. Pada laju pendinginan lambat, TAG CPO mengkristal secara bertahap dalam 2 struktur lamellar dengan panjang ikatan rangkap dua 41.9 Å dan panjang ikatan rangkap tiga
6β.8 Å yang menumpuk, yang menunjukkan tipe kristal ‟. Hasil tersebut berkorelasi dengan dua puncak eksotermik pada suhu 26 and 8 °C. Pada CPO terjadi transisi tak dapat balik kristal ‟
yang ditentukan oleh waktu. Proses ini terjadi pada suhu yang rendah, namun hanya terjadi pada populasi TAG yang sangat sedikit. Pemanasan bertahap pada laju pemanasan 1 °C/min menunjukkan tidak adanya penataan ulang struktur kristalin saat belum mencapai suhu pelelehan akhir. Hal ini mengindikasikan bahwa sebagian besar sistem berada pada kondisi ekuilibrium.
Chong et al. (2007) juga mengemukakan bahwa kristalisasi CPO pada 0.4 oC/menit
menunjukkan pembentukan struktur-struktur tambahan. Terdapat temuan yang tidak diduga yaitu adanya dua garis yang terkait dengan struktur 2L (bilayered) dan titik isobestic pada 4.42 Å.
Dengan analisis yang sangat hati-hati, kedua garis tersebut dapat dipisahkan, dan keberadaan keduanya terkait dengan fenomena epitaxy/eutectic, yang ditunjukkan dengan munculnya susunan
3L (trilayered) pada waktu yang sama dengan saat rusaknya susunan 2L dan saat terjadinya titik isobestic. Munculnya bentuk kristal dan ‟ secara bersamaan pada suhu yang tinggi
menunjukkan bahwa seluruh sistem tersebut tidak berada dalam domain tiga fase, tetapi lebih menyerupai tiga fase (kristal + ‟ + cairan) dimana tidak seluruh molekul TAG dapat tepat tersusun ke dalam struktur tunggal ‟. Hal ini sepertinya terkait dengan terjadinya pemisahan fase granular seperti yang terjadi pada margarin.
Vuillequez et al. (2010) telah mempelajari pengaruh laju perubahan suhu (q = -0.5
°C/menit hingga -50 °C/menit) terhadap pembentukan fase RBDPO pada suhu rendah, dengan menggunakan analisis kalorimetri dan optik. Hasil penelitiannya menunjukkan bahwa laju pendinginan merubah polimorfisme TAG. Diperoleh dua fraksi yaitu fraksi cair dan fraksi padat yang mengandung fraksi cair TAG. Laju sentrifugasi dalam pemisahan fraksi olein dan stearin tidak berpengaruh pada jumlah fraksi yang diperoleh. Fraksi padat RBDPO lebih sensitif terhadap pengaruh laju pendinginan. Dengan mengubah laju pendinginan q, diketahui bahwa q = -3
oC/menit menjadi batas antara laju pendinginan lambat dan laju pendinginan cepat. Pada laju
pendinginan lambat, TAG memiliki waktu yang cukup untuk berinteraksi. Sebaliknya pada laju pendinginan cepat, TAG tidak memiliki waktu yang cukup untuk mengatur diri dalam konformasi yang lebih stabil. Hasil mikrograf menunjukkan bahwa kristal yang dihasilkan berupa spherulites,
dengan ukuran kristal berbeda pada laju pendingian yang berbeda.
Graef et al. (2008) telah mengembangkan metode reologi baru untuk memantau
terjadinya kristalisasi RBDPO pada gaya geser tertentu. Metode tersebut dapat dibagi menjadi 2 tahap yaitu tahap 1 berupa pemberian gaya geser pada waktu tertentu dan kristalisasi dimonitor dengan mengukur viskositas terukur sebagai fungsi waktu isotermal. Pada tahap 2, gaya geser dihentikan dan osilasi diterapkan selama 30 detik dan dicatat sudut modulus dan fasenya. Sudut modulus dan fase tersebut dicatat sebagai karakteristik sampel yang dikristalisasi pada gaya geser dan waktu tertentu. Prosedur ini dilakukan pada beberapa waktu pemberian gaya geser di tahap pertama, dan sudut modulus kompleks dan fase diplotkan sebagai fungsi waktu isotermal pada beberapa gaya geser yang berbeda. Hasil tersebut kemudian dibandingkan dengan data kristalisasi yang diperoleh dari time resolved X-ray diffraction and polarized light microscopy.
Selain itu Graef et al. (2009) juga telah mempelajari pengaruh gaya geser terhadap sifat
16 kristalisasi primer. Selain itu, adanya perlakuan gaya geser yang mengawali tahap kristalisasi statis juga sangat berpengaruh pada pengembangan mikrostruktur kristal RBDPO.
Gambar 5 Viskositas terukur RBDPO pada kristalisasi selama 30 menit pada beberapa laju
geser dan suhu kristalisasi 25 oC (Graef
et al. 2008).
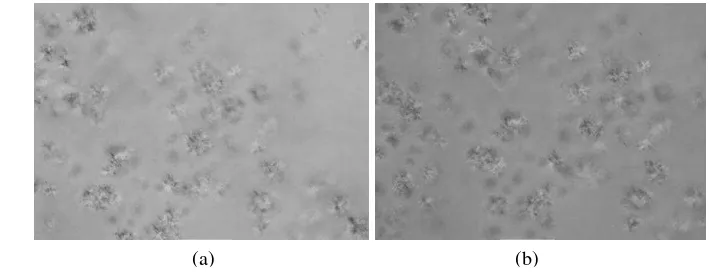
Pengaruh gaya geser terhadap kristal lemak yang terbentuk pada sampel RBDPO juga diamati oleh Graef et al. (2009) secara mikroskopi dengan mikroskop polarisasi cahaya (polarized light microscope/PLM) (Gambar 6). Pada laju geser yang semakin meningkat (1, 10 dan 100s-1)
yang diterapkan selama 30 menit, dan dilanjutkan proses kristalsasinya selama 30 menit berikutnya, akan dihasilkan ukuran kristal yang lebih besar. Agregat kristal pada laju geser yang lebih besar juga dihubungkan dengan kristal-kristal baru yang berperan dalam membentuk struktur jaringan lemak padat.
Gambar 6 Bentuk kristal lemak RBDPO yang dipotret menggunakan mikroskop polarisasi
cahaya yang dikristalisasi pada suhu 25 oC selama 60 menit pada beberapa laju
geser (g) 1 s-1, (h) 10 s-1, dan (i) 110 s-1 (Graef
17
III.
METODOLOGI PENELITIAN
A.
BAHAN DAN ALAT
Bahan utama yang digunakan pada penelitian ini adalah CPO yang berasal dari lima perusahaan kelapa sawit di Indonesia, yaitu PT. Sinar Meadow Internasional Indonesia Jakarta (CPO A), PT. Perkebunan Nusantara (PTPN) VIII Banten (CPO B), PTPN XIII Perkebunan Gunung Meliau Kalimantan Barat (CPO C), dan PTPN XIII Perkebunan Ngabang Kalimantan Barat (CPO D), dan PT. Wilmar Internasional Riau (CPO E). Bahan lain yang digunakan dalam analisis kimia adalah n-heksana, larutan NaOH 0.1 N, ethanol 95%, indikator fenolftalein, kristal kaliumhidrogenftalat (KHP), sikloheksana, larutan Wijs, larutan KI 15%, larutan Na2S2O7 0.1 N,
indikator pati, dan air destilata.
Peralatan yang digunakan untuk mengukur karakteristik kristalisasi lemak CPO adalah
Nuclear Magnetic Resonance (NMR) Analyzer Bruker Minispec PC 100 untuk mengukur kadar
lemak padat (solid fat content/SFC), Haake Viscometer RV20 (Karlsruhe, Jerman) untuk
menerapkan shear rate, serta mikroskop polarisasi Olympus CX untuk mengamati mikrostruktur
kristal lemak. Peralatan yang digunakan untuk analisis kimia adalah oven, penyaring vakum, spektrofotometer, gelas piala, buret, erlenmeyer, pipet mohr, dan labu takar.
B.
METODE PENELITIAN
Sifat kristalisasi lemak CPO dipelajari melalui empat tahap penelitian, yaitu (1) analisis mutu dan profil SFC CPO, (2) kajian perubahan nilai SFC selama penyimpanan, (3) kajian pengaruh laju pendinginan terhadap SFC kinetika kristalisasi dan mikrostruktur kristal lemak, dan (4) kajian pengaruh laju pendinginan dan shear rate terhadap kinetika kristalisasi lemak.
1. Analisis Mutu dan Profil SFC CPO
Kajian analisis mutu CPO ditujukan untuk mengetahui kualitas lima CPO berdasarkan parameter yang ditetapkan dalam SNI 01-2901-2006. Sampel CPO yang digunakan merupakan sampel yang baru dihasilkan industri pengolah CPO, serta belum mengalami proses transportasi dan penyimpanan dalam waktu yang lama. Dengan demikian, diharapkan komposisi kimia dan kondisi kristal lemak di dalamnya belum mengalami perubahan akibat terjadinya pelelehan dan kristalisasi lemak yang berulang.
Analisis mutu CPO yang digunakan dilakukan berdasarkan atribut mutu yang ditetapkan dalam standar spesifikasi CPO menurut Standar Nasional Indonesia (SNI) 01-2901-2006yang mencakup warna visual jingga kemerah-merahan, kadar air dan kotoran (maksimal 0.5%), kadar asam lemak bebas (sebagai asam palmitat, maksimal 0.5%), dan bilangan Iod (50-55 g Iod/100 g).
Salah satu parameter sifat fisik yang penting dalam mempelajari kristalisasi lemak adalah nilai solid fat content (SFC) atau kandungan lemak padat. Profil SFC CPO pada
beberapa suhu diukur berdasarkan metode IUPAC 2.150 ex 2.323 1987 untuk non tempering fat menggunakan Nuclear Magnetic Resonance (NMR) Bruker Minispec 100 NMR Analyzer
(Gambar 7). Sebelum dilakukan pengukuran terlebih dahulu dilakukan pretreatment. Prosedur
stabilisasi atau pretreatment sangat menentukan jumlah dan tipe kristal lemak yang terbentuk
18
Gambar 7 Nuclear Magnetic Resonance (NMR) yang digunakan untuk mengukur
kandungan lemak padat (SFC) CPO.
Sampel CPO diisikan ke dalam tabung NMR setinggi + 2.5 cm. Sebelum dianalisis, sampel CPO dipanaskan pada suhu 80 oC selama 30 menit agar meleleh sempurna untuk
meyakinkan homogenitasnya. Kemudian sampel yang telah meleleh dipertahankan pada suhu 60 oC selama 5 menit. Selanjutnya sampel disimpan pada suhu 0 oC selama 60 menit.
Sebelum dilakukan pengukuran SFC, sampel dipertahankan dulu pada masing-masing suhu pengukurannya selama 30-35 menit. SFC sampel CPO diukur pada suhu yang berbeda yaitu pada kisaran suhu 5 oC hingga suhu saat SFC bernilai 0%, dengan kenaikan suhu pada setiap
pengukuran sebesar 5 oC, yaitu suhu 25, 30, 35, 40, 45, 50, 55 , dan 60 ºC. Pengujian profil
SFC CPO dilakukan secara triplo.
2. Kajian Perubahan Nilai SFC selama Penyimpanan
Menurut Brulenno et al. (2003), nilai SFC pada produk berlemak akan berubah
selama penyimpanan akibat pengaruh suhu dan lama penyimpanan. Pengujian terhadap perubahan SFC CPO selama penyimpanan perlu dilakukan untuk mengetahui perubahan fraksi lemak padat CPO selama penyimpanan akibat pengaruh suhu dan waktu penyimpanan. Pengaruh suhu dan lama penyimpanan terhadap perubahan SFC CPO dipelajari dalam penelitian ini dengan mensimulasikan kondisi penyimpanan sesuai dengan rekomendasi Codex Alimentarius Commision (CAC) (2005).
Sampel CPO (CPO A) dimasukkan ke dalam tabung NMR setinggi + 2.5 cm. Sampel dipanaskan sampai 55 ºC dengan kenaikan suhu 5 ºC/hari. Setelah sampel mencapai suhu 55 ºC, sampel tersebut disimpan pada suhu 20, 25, 30, 35, dan 40 ºC selama 4 minggu. Sampel diukur nilai SFC-nya setiap minggu. Pengujian perubahan SFC terhadap suhu dan waktu penyimpanan dilakukan secara duplo.
3. Kajian Pengaruh Laju Pendinginan terhadap Nilai SFC, Kinetika Kristalisasi, dan
Mikrostruktur Kristal Lemak.
Menurut Wiking et al. (2009), salah satu parameter yang mempengaruhi kristalisasi
lemak adalah laju pendinginan. Laju pendinginan mempengaruhi kinetika kristalisasi dalam hal mekanisme pembentukan nuklei dan laju kristalisasi (Campos et al. 2002). Pada penelitian ini
ingin diketahui pengaruh laju pendinginan terhadap nilai SFC CPO, kinetika kristalisasi lemak, dan mikrostruktur kristal lemak
Sampel CPO (CPO A) sebelumnya dimasukkan ke dalam tabung NMR setinggi +2.5 cm. Sampel tersebut kemudian dipanaskan dalam water bath hingga mencapai suhu saat
SFC bernilai 0% yaitu suhu 55 ºC selama 30 menit. Selanjutnya suhu water bath diturunkan
19 dipertahankan hingga diperoleh nilai SFC tetap. Pengukuran SFC dilakukan setiap 2 menit sekali. Pengujian pengaruh laju pendinginan terhadap kristalisasi lemak dilakukan secara triplo
Kinetika kristalisasi dipelajari menggunakan model Avrami dengan parameter laju kristalisasi (k) dan koefisien Avrami (n) (Metin & Hartel 2005). Nilai n dan k dihitung dari
bentuk linier persamaan Avrami (Persamaan 2), sebagai slope dan intercept pada ln t = 0. F
adalah fraksi kristal yang terbentuk selama waktu kristalisasi t (menit).
ln(−ln 1− � = ln � +�[ln � ] (2)
Nilai k secara langsung berhubungan dengan waktu setengah kristalisasi (t1/2). Waktu
setengah kristalisasi dihitung dengan persamaan Arhenhius.
(t1/2)n= 0.693/k (3)
Menurut Martini et al. (2002), nilai fraksi kristal ditentukan saat SFC pada waktu
tertentu dinormalisasi dengan nilai SFC maksimal yang diperoleh pada kondisi percobaan tersebut. Untuk memperoleh parameter yang memberikan ketepatan yang tinggi pada persamaan Avrami, digunakan analisis regresi linier.
Untuk mengetahui morfologi dan distribusi ukuran kristal lemak sampel CPO yang terbentuk selama perlakuan, dilakukan pengamatan kristal lemak di bawah mikroskop sinar polarisasi (polarized light microscopy) sesuai dengan metode yang dilakukan oleh Martini et al. (2002).
Sampel CPO yang telah mengalami laju pendinginan tertentu dan telah mencapai suhu kristalisasi isotermal (25 ºC) diteteskan di atas kaca preparat. Kaca preparat yang telah berisi sampel disimpan pada ruangan yang bersuhu 25 ºC selama 25 menit. Setelah itu kaca preparat diletakan di bawah mikroskop polarisasi cahaya untuk melihat pembentukan kristal lemak. Kaca preparat didiamkan kembali pada suhu 25 ºC tanpa diangkat dari mikroskop polarisasi cahaya selama 10 menit. Pengamatan kristal lemak dilakukan pada menit ke-35 untuk melihat pertambahan jumlah dan perubahan ukuran kristal lemak.
4. Kajian Pengaruh Laju Pendinginan dan Shear Rate terhadap Kinetika Kristalisasi
CPO akan mengalami perubahan proses kristalisasi akibat adanya pengaruh shear rate
selama transportasi. Sifat kristalisasi lemak selama transportasi ditentukan oleh laju pendinginan dan shear rate. Untuk mengkaji kedua faktor tersebut, dilakukan pengujian
dengan pendekatan sesuai kondisi transportasi, yang dicobakan dengan menggunakan Haake
Rotoviscometer RV20 (Gambar 8).
Gambar 8 Haake Rotoviscometer RV 20 yang digunakan untuk menerapkan perlakuan laju
20 Sampel CPO dipanaskan dari suhu 25 oC sampai suhu 55 ºC pada
shear rate 5 s-1
dengan laju kenaikan suhu 1ºC/menit. Selanjutnya suhu sampel dipertahankan selama 10 menit dan kemudian diturunkan suhunya hingga mencapai suhu kristalisasi 25 oC, dengan perlakuan
laju pendinginan dan shear rate tertentu. Setelah mencapai 25 ºC, suhu sampel dipertahankan
selama 60 menit untuk melihat fenomena kristalisasi yang terjadi melalui pengamatan kenaikan nilai viskositas terukur. Perlakuan laju pendinginan dan shear rate yang diterapkan dapat
dilihat pada Tabel 9.
Tabel 9 Perlakuan pengaruh laju pendinginan dan laju geser terhadap proses kristalisasi Perlakuan Laju pendinginan Shear rate (s-1)
1 1 40
2 1 100
3 1 400
4 0.5 40
5 0.5 100
6 0.5 400
7 0.2 40
8 0.2 100
9 0.2 400
C.
METODE ANALISIS
1. Kadar Air (BSN 2006)
Kadar air dianalisis berdasarkan SNI 01-2901-2006 tentang minyak sawit kasar dan dihitung sebagai berat yang hilang setelah contoh uji dipanaskan pada suhu 103±2 ºC selama 3 jam atau 130±2 ºC selama 30 menit. Mula-mula cawan alumunium dikeringkan pada oven 103±2 ºC selama 15 menit, kemudian didinginkan dalam desikator lalu ditimbang. Minyak yang akan menjadi sampel uji dilelehkan pada suhu 50 ºC sambil diaduk hingga rata. Minyak tersebut lalu ditimbang 5-10 g dan dimasukkan dalam cawan alumunium. Cawan yang berisi sampel dipanaskan dalam oven 103±2 ºC selama 3 jam, kemudian segera dimasukkan ke dalam desikator dan didinginkan selama 15 menit. Setelah dingin, cawan tersebut ditimbang sampai diperoleh berat yang konstan. Kadar air dihitung dengan rumus:
− ( 1− 2)
� 100 %
Keterangan :
W : bobot contoh sebelum dikeringkan (g)
W1 : bobot contoh dan cawan sesudah dikeringkan (g)
W2 : bobot cawan kosong kering (g)
2. Kadar Kotoran (BSN 2006)
21 mL pelarut ditambahkan ke dalam sampel uji dan dipanaskan pada penangas air, sambil digoyang-goyangkan sampai minyak larut semua. Sampel uji kemudian disaring dengan menggunakan alat penyaring. Pencucian dilakukan beberapa kali dengan menggunakan pelarut sampai kertas Whatman No. 41 bersih dari minyak. Kertas Whatman No. 41 kemudian dikeringkan ke dalam oven suhu 103±2 ºC selama 30 menit dan didinginkan dalam desikator selama 15 menit. Kertas Whatman No. 41 kemudian ditimbang hingga diperoleh berat yang konstan. Kadar kotoran dihitung dengan rumus :
− ( 1− 2)
� 100
Keterangan :
W : bobot contoh (g)
W1 : bobot alat penyaring setelah dikeringkan (g)
W2 : bobot alat penyaring kering (g)
3. Kadar Asam Lemak Bebas (BSN 2006)
Kadar asam lemak bebas dianalisis berdasarkan SNI 01-2901-2006 tentang minyak sawit kasar dan dihitung sebagai persentase berat (b/b) dari asam lemak bebas yang terkandung dalam CPO dimana berat molekul asam lemak bebas tersebut dianggap sebesar 256 (sebagai asam palmitat). Sampel yang akan diuji dipanaskan pada suhu 60-70oC dan diaduk hingga
homogen. Sampel sebanyak 5 g dilarutkan dalam 50 mL ethanol 95% yang telah dinetralkan lalu dipanaskan sampai suhu 40 ºC. Ke dalam larutan tersebut ditambahkan indikator fenolftalein 1% sebanyak 1-2 tetes. Larutan tersebut dititrasi menggunakan NaOH 1N sambil digoyang-goyang hingga mencapai titik akhir yang ditandai dengan perubahan warna menjadi merah muda yang stabil minimal 30 detik. Asam lemak bebas dinyatakan sebagai asam palmitat dihitung dengan rumus :
Kadar ALB (%) = 25.6x�x Keterangan :
V : volume titrat yang digunakan (mL) N : normalitas larutan titrat (N) W : berat contoh (g)
25.6 : konstanta untuk menghitung kadar asam lemak bebas sebagai asam palmitat
4. Bilangan Iod
Bilangan Iod dianalisis berdasarkan SNI 01-2901-2006 tentang minyak sawit kasar dan dinyatakan sebagai gram Iod yang diserap per 100 g minyak. Mula-mula sampel yang akan diuji dilelehkan pada suhu 60-70 oC sambil diaduk hingga rata. Contoh uji tersebut lalu
22 Bilangan Iod = 12.69 � ( 2− 1)
Keterangan
N : normalitas larutan natrium tiosulfat 0.1 N (N)
V2 : volume natrium tiosulfat yang digunakan pada penetapan blanko (mL)
V1 : volume natrium tiosulfat yang digunakan pada penetapan contoh (mL)
W : berat contoh (g)
12.69 : konstanta untuk menghitung bilangan Iod.
5. Analisis Statistik
Data yang diperoleh dari hasil pengukuran selanjutnya dilakukan uji secara statistik. Pengujian statistik menggunakan program SPSS 16.0 dengan uji Pearson correlation two tailed untuk mengetahui korelasi antar faktor, ANOVA one way, dan ANOVA univariate
23
IV.
HASIL DAN PEMBAHASAN
A.
ANALISIS MUTU CPO
CPO merupakan minyak nabati berwarna jingga kemerah-merahan yang diperoleh dari hasil pengempaan (ekstraksi) daging buah tanaman Elaeis guinneensis (BSN 2006). Mutu CPO
ditentukan oleh karakteristik kimia dan fisik. Karakteristik kimia yang dikaji pada penelitian ini sesuai dengan standar yang ditetapkan dalam SNI 01-2901-2006 meliputi kadar kadar air dan kotoran, kadar asam lemak bebas (ALB), dan bilangan Iod, sedangkan karakteristik fisik yang dikaji adalah profil solid fat content (SFC) CPO. Selain itu juga dilakukan analisis korelasi antara
karakteristik kimia dengan nilai SFC yang didapatkan. Beberapa penelitian sebelumnya menyebutkan bahwa terdapat hubungan antara sifat kimia suatu minyak dengan profil SFC-nya. Bilangan Iod dan ALB memiliki hubungan terbalik dengan SFC (Basiron 2005; Foubert et al.
2004). Menurut Metin dan Hartel (2005) kadar kotoran memiliki hubungan searah terhadap SFC.
1. Analisis Mutu Kimia CPO
Kualitas CPO ditentukan oleh beberapa parameter yaitu kadar air dan kotoran, kadar ALB, dan bilangan Iod. Mutu CPO di Indonesia diatur dalam SNI 01-2901-2006 tentang minyak sawit kasar. Hasil pengujian mutu CPO tersaji pada Tabel 10 dengan data lengkap pada Lampiran 1.
Tabel 10 Hasil analisis mutu lima CPO dari beberapa lokasi di Indonesia
Nilai yang diikuti oleh huruf yang berbeda pada kolom yang sama menunjukkan perbedaan yang signifikan (p<0.05)
Sumber : *BSN (2006)
Hasil analisis mutu kimia CPO pada Tabel 10 menunjukkan semua sampel CPO yang dianalisis tidak memenuhi standar mutu yang telah ditetapkan dalam SNI 01-2901-2006 tentang minyak sawit kasar. Hal ini diakibatkan oleh proses produksi yang tidak terkontrol dan adanya penimbunan CPO di Pabrik Kelapa Sawit (PKS) yang menyebabkan terjadinya penurunan mutu CPO.
Uji statistik ANOVA one way dengan uji lanjut Duncan dilakukan untuk melihat
apakah terdapat perbedaan karakteristik mutu kimia antar sampel CPO yang digunakan. Hasil ANOVA one way dengan uji lanjut Duncan (Lampiran 2) menunjukkan bahwa kelima sampel memiliki karakteristik yang berbeda-beda. Perbedaan karakteristik dari kelima sampel CPO dimungkinkan akibat perbedaan kematangan buah saat pemanenan dan proses produksi yang diterapkan oleh masing-masing perusahaan.
Sampel CPO Parameter
Kadar air & kotoran (%) ALB (%) Bilangan Iod (g/100g)
A 0.33(a) 5.80(a) 50.38(a)
B 0.68(b) 3.88(b) 51.30(ab)
C 0.67(b) 3.84(b) 52.47(b)
D 0.67(b) 4.58(c) 54.15(c)
E 5.39(c) 4.60(c) 50.79(a)
24 Kadar air merupakan persentase kandungan air dengan kandungan bahan kering pada suatu bahan. Kadar kotoran merupakan jumlah bahan-bahan yang tidak larut dalam minyak seperti mineral. Kadar air dan kadar kotoran disebut juga sebagai kadar kemurnian CPO. Hasil pengujian kadar air dan kadar kotoran pada Tabel 10 menunjukkan kadar air dan kadar kotoran setiap sampel CPO bervariasi dan hanya CPO A saja yang memenuhi standar dalam SNI 01-2901-2006. Banyaknya sampel CPO yang tidak memenuhi syarat diakibatkan oleh pemanenan buah sawit yang dilakukan saat lewat matang dan kontaminasi dari tangki penyimpanan atau alat pengolahan minyak sawit. Buah yang dipanen saat lewat matang akan memiliki kadar air yang tinggi. Menurut Naibaho (1998) kotoran pada CPO terjadi akibat adanya kontaminasi dari tangki penampungan CPO. CPO C memiliki kadar air dan kadar kotoran tertinggi yaitu 4.84%. Kadar air dan kadar kotoran yang tinggi dapat menyebabkan kerusakan CPO. Kadar air yang tinggi akan memicu terjadinya reaksi hidrolisis yang menghasilkan ALB pada CPO. Mineral seperti Cu dan Fe dapat mengkatalisis reaksi oksidasi lemak sehingga akan terbentuk senyawa peroksida yang akan menyebabkan ketengikan pada minyak (CAC 2005).
Asam lemak bebas (ALB) merupakan salah satu parameter kerusakan pada produk minyak atau lemak. Hasil analisis menunjukkan kelima sampel CPO tidak memenuhi standar ALB yang ditetapkan dalam SNI 01-2901-2006 yaitu batas maksimal ALB pada CPO adalah 0.5%. Namun ALB dari CPO tersebut masih memenuhi standar yang ditetapkan dalam SNI CPO sebelum revisi 2006 (SNI 01-2901-1992) yaitu maksimal 5% dan hanya CPO A yang melebihi 5%.
Nilai ALB yang tinggi menandakan minyak atau lemak sudah mengalami kerusakan. ALB terbentuk ketika asam lemak terpisah dari TAG, DAG, atau MAG akibat adanya reaksi kimia atau enzimatis (Rohani et al. 2006). Menurut Codex Alimentarius Commision (CAC) (2005) nilai ALB yang tinggi diakibatkan oleh reaksi hidrolisis. Reaksi
hidrolisis dipicu oleh adanya air dalam minyak. Hidrolisis lemak akan menghasilkan gliserol dan ALB yang menyebabkan ketengikan pada minyak. Proses reaksi hidrolisis TAG dapat dilihat pada Gambar 9.
Gambar 9 Reaksi hidrolisis menghasilkan Asam Lemak Bebas (ALB) (Ketaren 2005)
Proses tahapan sterilisasi pada produksi CPO dilakukan dengan suhu 135 ºC. Proses tersebut bertujuan mematikan enzim lipase sehingga kenaikkan ALB akibat reaksi enzimatis dapat dicegah (Rohani et al. 2006). Kenaikan ALB juga diakibatkan oleh suhu penyimpanan
25 akan menghasilkan ALB dan rendemen yang rendah. Pemanenan yang dilakukan saat buah lewat masak akan menghasilkan ALB dan rendemen yang tinggi.
Bilangan Iod menunjukkan derajat ketidakjenuhan suatu lemak atau minyak. Menurut Ketaren (2005) bilangan Iod menyatakan jumlah gram Iod yang digunakan untuk mengadisi 100 gram lemak/minyak. Bilangan Iod ditentukan dengan perbandingan antara asam lemak jenuh dan asam lemak tidak jenuh penyusun suatu lemak atau minyak. Komposisi minyak sawit kasar terdiri dari 50% asam lemak jenuh dan 50% asam lemak tidak jenuh (Basiron 2005). Oleh karena itu bilangan Iod pada minyak sawit adalah 50-55 g Iod/100 g sampel (BSN 2006). Hasil analisis menunjukkan bahwa kelima sampel CPO mempunyai bilangan Iod yang sesuai dengan yang ditetapkan dalam SNI.
2. Analisis Profil SFC CPO
SFC menunjukkan banyaknya kristal lemak dalam suatu lipid, yang dihitung sebagai fungsi dari suhu (Zaliha et al. 2003). Suhu pengukuran yang diterapkan adalah 5-60 oC untuk
mendapatkan nilai SFC hingga 0%. Pengukuran SFC CPO menggunakan lima sampel CPO dari beberapa daerah di Indonesia untuk mendapatkan kisaran nilai SFC CPO pada suhu tertentu. Pengukuran SFC CPO menggunakan alat Nuclear Magnetic Resonance (NMR)
yang mengukur kandungan lemak padat berdasarkan kecepatan mobilitas elektron yang berbeda pada fase padat dan cair. Resonansi elektron akan menginduksi signal yang akan dipancarkan oleh alat NMR sehingga akan mewakili jumlah fase cair ataupun padat pada sampel (Satiawihardja et al. 2001).
Dalam analisis SFC, dilakukan proses pretreatment terlebih dahulu pada sampel
yang akan diujikan. Pada preatreatment atau prosedur stabilisasi, CPO terlebih dahulu
dipanaskan sampai 80 ºC selama 30 menit untuk meyakinkan homogenitasnya serta menghilangkan ingatan mengenai kristal dan disimpan pada suhu 0 ºC selama 60 menit untuk memastikan terbentuknya kristal lemak. CPO dipertahankan pada suhu pengukuran selama 30 menit. Hal ini dimaksudkan agar kristal yang terbentuk telah stabil.
Hasil pengujian pada Gambar 10 dan Tabel 11 menunjukkan bahwa nilai SFC CPO berbanding terbalik dengan suhu pengukuran. Hal ini sesuai dengan penelitian yang dilakukan oleh Salimon dan Abdullah (2009) bahwa semakin tinggi suhu pengukuran, maka nilai SFC akan menurun. Data mengenai nilai SFC selengkapnya dapat dilihat pada Lampiran 3. Bentuk kurva profil SFC CPO yang didapatkan pada penelitian ini sesuai dengan kurva SFC minyak sawit (RBDPO) oleh Smith (2001) (Gambar 2 ).
26 Gambar 10 dan Tabel 11 menunjukkan bahwa nilai SFC kurang dari 10% pada suhu di atas 40 ºC. Nilai SFC yang rendah menandakan bahwa kristal lemak pada CPO sudah meleleh akibat pengaruh suhu. Titik leleh merupakan faktor penting dalam kristalisasi lemak karena lemak akan mengkristal apabila suhu berada di bawah titik lelehnya. Titik leleh minyak sawit adalah kisaran dari nilai-nilai yang menunjukkan gliserida penyusunnya yang terdiri dari asam-asam lemak dengan titik cair yang berbeda (Satiawihardja et al. 2001).
Menurut Himawan et al. (2006), titik leleh minyak sawit adalah 40 ºC.
Hasil pengujian profil SFC minyak sawit pada penelitian ini menunjukkan nilai yang berbeda dengan hasil pengujian yang dilakukan oleh Zaliha et al. (2003). Perbedaan ini
diakibatkan kedua penelitian menggunakan sampel minyak sawit yang berbeda. Pada penelitian Zaliha et al. (2003) digunakan sampel refined bleached deodorized palm oil
(RBDPO) yang telah mengalami pemurnian, sedangkan pada penelitian ini menggunakan CPO yang masih menggandung kadar kotoran dan komponen minor. Menurut Metin dan Hartel (2005) adanya komponen minor dan kotoran pada minyak sawit kasar turut berperan dalam proses kristalisasi lemak pada CPO. Adanya kotoran mendukung terjadinya kristalisasi sehingga nilai SFC semakin besar. Hal inilah yang menyebabkan nilai SFC pada penelitian yang dilakukan oleh Zaliha et al.(2003) pada suhu 40 ºC sudah mencapai 0%, sedangkan
pada penelitian ini masih berkisar 4.69-9.63%. Nilai SFC minyak sawit yang didapatkan pada penelitian ini cenderung sama dengan nilai SFC pada penelitian yang dilakukan oleh Himawan et al. (2006) kecuali nilai SFC pada suhu 10 dan 15 ºC.
Tabel 11 Pengaruh perubahan suhu terhadap profil SFC CPO*
*Pengukuran dilakukan menggunakan lima sampel CPO
Faktor penting yang mempengaruhi nilai SFC salah satunya adalah slip melting point (SMP). SMP merupakan suhu saat lemak pada pipa kapiler mulai meleleh. Menurut
Goh dan Ker (1991), SMP lemak dapat ditentukan ketika SFC menunjukan nilai di bawah 5%. Data SFC pada Tabel 11 menunjukan penurunan nilai SFC hingga di bawah 5% terjadi antara suhu 35-40 ºC yang menandakan SMP CPO 35-40 ºC. Kisaran SMP CPO yang didapatkan pada penelitian ini berada dalam kisaran SMP yang diteliti oleh Lin (2002). Lin (2002) menyebutkan SMP minyak sawit berkisar 32-40 ºC.
Suhu (ºC) Kisaran SFC (%) Rata-rata
5 48.03-50.44 49.02
10 43.17-46.98 45.15
15 32.45-38.45 35.65
20 23.81-30.08 27.18
25 14.55-20.16 17.41
30 9.13-14.63 11.78
35 6.36-11.43 8.36
40 4.59-9.36 6.76
45 4.53-7.85 5.81
50 4.11-7.18 5.22
55 4.06-7.01 4.88
27 Faktor lain yang mempengaruhi kristalisasi lemak adalah komposisi triacylglicerol
(TAG) pada suatu lemak atau minyak. CPO mengandung banyak TAG dengan asam lemak yang berbeda panjang rantainya, derajat kejenuhannya, dan letak gliserolnya (Basiron 2005). SFC pada suhu di atas 40 ºC sudah tidak mengalami penurunan yang besar karena asam lemak penyusun CPO telah meleleh. Asam lemak dominan pada CPO adalah asam palmitat dengan panjang rantai C16. Asam palmitat memiliki titik leleh yang tinggi yaitu 64 ºC
(Ketaren 2005). Hal inilah yang menyebabkan SFC CPO pada suhu 60 ºC berkisar 3.5-6.8% belum mencapai 0%.
3. Korelasi Mutu Kimia CPO dengan SFC CPO
Untuk mengetahui adanya hubungan antara mutu kimia dengan SFC dilakukan analisis Pearson correlation. Analisis Pearson correlation dilakukan untuk setiap parameter
kimia dengan nilai SFC pada suhu 25 ºC. Suhu 25 ºC dipilih karena analisis mutu kimia hanya dilakukan pada suhu ruang (25 ºC).
Hasil analisis Pearson correlation pada penelitian ini (Lampiran 4) menunjukkan bahwa tidak ada hubungan antara nilai SFC dengan bilangan Iod, kadar asam lemak bebas, dan kadar air. Ada atau tidaknya korelasi antar kedua faktor ditentukan dengan nilai Pearson correlation dan signifikansinya. Nilai Pearson correlation untuk bilangan Iod dengan SFC
bernilai 0.269 dengan signifikansi lebih besar dari 0.05 yang menandakan korelasi antar kedua faktor tersebut cukup namun tidak signifikan. Kadar asam lemak bebas dengan SFC mempunyai nilai Pearson correlation -0.328 dengan signifikansi lebih besar dari 0.05 yang
berarti korelasi antar kedua fakor cukup dan berbanding terbalik namun tidak signifikan. Nilai Pearson correlation untuk kadar air dengan SFC bernilai 0.621 dengan signifikansi
lebih besar dari 0.05 yang berarti korelasi antara kedua faktor kuat namun tidak signifikan. Penelitian sebelumnya yang dilakukan oleh Basiron (2005) dan Foubert et al. (2004)
menyebutkan bahwa terdapat hubungan antara bilangan Iod dan kadar asam lemak bebas dengan nilai SFC. Menurut Basiron (2005), bilangan Iod mempunyai korelasi negatif dengan SFC yaitu semakin rendah bilangan Iod maka nilai SFC akan semakin tinggi. Bilangan Iod yang rendah menandakan kandungan asam lemak jenuh lebih banyak daripada asam lemak tidak jenuh dalam suatu lemak. Asam lemak jenuh memiliki titik leleh lebih tinggi dibanding dengan asam lemak tidak jenuh. Rantai jenuh yang panjang memiliki konformasi goyang yang memanjang sehingga struktur ini dapat dikemas dengan cukup teratur seperti dalam kristal (Hart 2003). Menurut Foubert et al. (2004), kandungan ALB yang tinggi
menyebabkan struktur lemak menjadi tidak beraturan dan memiliki titik leleh lebih rendah. Selain itu Wright et al. (2000) juga menyebutkan adanya asam lemak bebas pada suatu lemak
menyebabkan titik lelehnya lebih rendah sehingga kandungan lemak padatnya lebih rendah. Pada penelitian ini tidak terlihat adanya korelasi antara bilangan Iod dan kadar asam lemak bebas dengan SFC. Hal ini karena kisaran bilangan Iod yang digunakan pada penelitian ini kecil (50-55 g Iod/100 g sampel) sesuai dengan persyaratan SNI 01-2901-2006. Basiron (2005) menggunakan sampel dengan kisaran bilangan Iod yang lebih besar (24-50 g Iod/100 g sampel). Selain itu bilangan Iod dan kadar asam lemak bebas yang bervariasi pada setiap sampel penelitian ini menyebabkan tidak dapat dilihatnya pengaruh dari salah satu faktor saja.
Hasil analisis Pearson correlation antara kadar kotoran dengan SFC menunjukkan
adanya korelasi antar keduanya. Pearson correlation yang bernilai 0.789 dengan signifikansi
28 semakin tinggi kadar kotoran maka nilai SFC akan semakin besar. Keberadaan kotoran dapat mempercepat terjadinya kristalisasi. Metin dan Hartel (2005) menyatakan adanya kotoran dapat mengurangi energi bebas untuk pembentukkan inti (nukleasi) sehingga nukleasi lebih mudah terjadi. Kotoran akan menghubungkan fase padat dan fluida lewat jenuh (supersaturated) sehingga terjadi interaksi yang menyebabkan terbentuknya inti kristal.
Berdasarkan hasil analisis korelasi yang telah dilakukan dapat ditarik kesimpulan bahwa tidak terlihat adanya korelasi antara nilai SFC CPO dengan bilangan Iod, kadar asam lemak bebas, dan kadar air. Korelasi antara SFC CPO dengan mutu kimia hanya terlihat pada kadar kotoran. Kadar kotoran CPO mempunyai hubungan searah dengan nilai SFC CPO yang berarti semakin tinggi kadar kotoran akan menghasilkan nilai SFC yang semakin tinggi pula.
B.