SINTESIS HIDROGEL ANTIBAKTERI BERBASIS
KARBOKSIMETIL SELULOSA-ASAM SUKSINAT-AgNO
3DYAH PERMATA SARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Sintesis Hidrogel Antibakteri Berbasis Karboksimetil Selulosa-Asam Suksinat-AgNO3 adalah benar
karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
DYAH PERMATA SARI. Sintesis Hidrogel Antibakteri Berbasis Karboksimetil Selulosa-Asam Suksinat-AgNO3. Dibimbing oleh BETTY MARITA
SOEBRATA dan HENNY PURWANINGSIH.
Hidrogel berbasis karboksimetil selulosa (CMC) memiliki potensi yang baik untuk digunakan sebagai penutup luka. CMC direaksikan dengan asam suksinat (AS) sebagai agen pengikat silang dan AgNO3 sebagai zat antibakteri. Penelitian
ini bertujuan menyintesis hidrogel antibakteri berbasis CMC-AS-AgNO3,
mempelajari ciri-ciri, dan potensinya sebagai zat antibakteri. CMC yang digunakan berasal dari selulosa bakteri. CMC tersebut memiliki nilai kadar air sebesar 9%, pH 4.6, dan derajat substitusi sebesar 0.24. Campuran CMC dan asam suksinat ditambah AgNO3 dengan ragam konsentrasi 0.2%, 0.4%, dan 0.6%.
Peningkatan konsentrasi AgNO3 mengakibatkan peningkatan kemampuan
pembengkakan hidrogel. Peningkatan konsentrasi AgNO3 juga meningkatkan zona
inhibisi CMC-AS-AgNO3 terhadap bakteri Escherichia coli dan Staphylococcus
aureus. Zona inhibisi terluas dihasilkan oleh CMC-AS-AgNO3 0.6% dengan
diameter zona inhibisi sebesar 17 mm terhadap bakteri E. coli dan 12 mm terhadap bakteri S. aureus. Hidrogel CMC-AS-AgNO3 dicirikan menggunakan
mikroskop elektron payaran dan difraktometer sinar-X.
Kata kunci: antibakteri, CMC-AS-AgNO3, hidrogel, zona inhibisi
ABSTRACT
DYAH PERMATA SARI. Synthesis of Antibacterial Hydrogels Based on Carboxymethyl Cellulose-Succinic Acid-AgNO3. Supervised by BETTY
MARITA SOEBRATA and HENNY PURWANINGSIH.
Hydrogels based on carboxymethyl cellulose (CMC) are potential to be used as wound dressing. CMC was reacted with succinic acid as a cross linker and AgNO3 as an antibacterial substance. The aims of the experiment are to synthesis
antibacterial hydrogels based on CMC-AS-AgNO3, to study its characteristic, and
its potential of antibacterial substance. CMC was prepared from bacterial cellulose, with moisture content of 9%, pH 4.6, and degree of substitution 0.24. To the CMC and succinic acid, AgNO3 were added with concentration of 0.2%,
0.4%, and 0.6%. The increasing concentration of AgNO3 caused increasing of
swelling behavior. The increasing concentration of AgNO3 also caused increasing
the inhibition zone towards Escherichia coli and Staphylococcus aureus. The wider inhibition zone was produced by CMC-AS-AgNO3 0.6% with diameter of
17 mm towards E. coli and 12 mm towards S. aureus. The CMC-AS-AgNO3 was
characterized using scanning electron microscopy and X-ray diffraction methods. Key words: antibacterial, CMC-AS-AgNO3, hydrogels, inhibition zone
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
SINTESIS HIDROGEL ANTIBAKTERI BERBASIS
KARBOKSIMETIL SELULOSA-ASAM SUKSINAT-AgNO
3DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2014
Judul Skripsi : Sintesis Hidrogel Antibakteri Berbasis Karboksimetil Selulosa-Asam Suksinat-AgNO3
Nama : Dyah Permata Sari NIM : G44100039
Disetujui oleh
Betty Marita Soebrata, SSi, MSi Pembimbing I
Dr Henny Purwaningsih, SSi, MSi Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah yang berjudul “Sintesis Hidrogel Antibakteri Berbasis Karboksimetil Selulosa-Asam Suksinat-AgNO3”. Karya ilmiah ini disusun berdasarkan
penelitian yang dilakukan penulis di Laboratorium Kimia Fisik, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) IPB dan Laboratorium Pusat Studi Biofarmaka Lembaga Penelitian dan Pengabdian Kepada Masyarakat-Institut Pertanian Bogor (LPSB LPPM-IPB) dari Maret sampai Juli 2014.
Terima kasih penulis ucapkan kepada Ibu Betty Marita Soebrata, SSi, MSi dan Ibu Dr Henny Purwaningsih, SSi, MSi selaku pembimbing yang telah memberi saran, bimbingan, serta nasihat sehingga penelitian ini dapat diselesaikan. Di samping itu, penghargaan dari penulis disampaikan kepada Ibu Nunuk selaku staf Laboratorium Mikrobiologi LPSB IPB dan segenap staf Laboratorium Kimia Fisik, Departemen Kimia, FMIPA IPB yang telah membantu selama penelitian ini berlangsung. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, serta seluruh keluarga, atas segala doa dan kasih sayangnya. Tak lupa rasa terima kasih juga disampaikan kepada Candra Perangin-angin, Alfian Hadi, Oki Defrimika, Nanda Yuditya, dan seluruh teman-teman Kimia 47 yang tidak dapat disebutkan satu-persatu yang telah memberikan semangat, nasihat, dan bantuannya selama penelitian ini berlangsung.
Semoga karya ilmiah ini bermanfaat.
Bogor, November 2014
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 2
Alat dan Bahan 2
Metode Penelitian 3
HASIL DAN PEMBAHASAN 6
Karboksimetil Selulosa 6
Karboksimetil Selulosa-Asam Suksinat-AgNO3 7
Pencirian CMC Hasil Sintesis 8
Kemampuan Pembengkakan (Swelling) 9
Identifikasi Gugus Fungsi 11
Morfologi CMC-AS-AgNO3 12
Aktivitas Antibakteri 14
SIMPULAN DAN SARAN 16
Simpulan 16
Saran 16
DAFTAR PUSTAKA 17
LAMPIRAN 19
DAFTAR TABEL
1 Pencirian CMC hasil sintesis 9
2 Perbandingan pola difraksi hasil analisis dengan JCPDS-ICDD 14
3 Zona inhibisi CMC-AS-AgNO3 15
4 Rasio aktivitas antibakteri 16
DAFTAR GAMBAR
1 Struktur unit berulang dalam CMC 1
2 Struktur kimia asam suksinat 2
3 Metode difusi agar 6
4 Mekanisme reaksi pembentukan CMC 7
5 Hasil sintesis CMC 7
6 Reaksi esterifikasi CMC dengan asam suksinat 8
7 Film dengan berbagai komposisi a) CMC-AS, b) CMC-AS-AgNO3 0.2%,
c) CMC-AS-AgNO3 0.4%, d) CMC-AS-AgNO3 0.6% 8
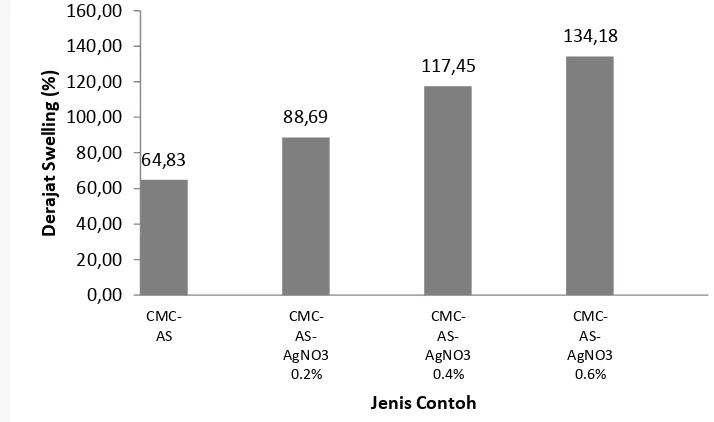
8 Derajat swelling hidrogel 10
9 Spektrum FTIR 11
10Analisis morfologi CMC-AS-AgNO3 0.6% a) perbesaran 100×, b)
perbesaran 1000×, c) morfologi CMC dengan penambahan nanopartikel
perak 12
11Pola difraksi sinar-X CMC-AS-AgNO3 0.6% 13
12Pola difraksi (a) CMC-AS (b) CMC-AS-AgNO3 0.6% 14
13Hasil uji aktivitas antibakteri a) pada bakteri uji E. coli, b) pada bakteri
uji S. aureus 15
DAFTAR LAMPIRAN
1 Diagram alir penelitian 19
2 Kadar air CMC hasil sintesis 19
3 pH larutan CMC 1% 20
4 Penentuan derajat substitusi CMC 20
5 Derajat swelling CMC-AgNO3 21
6 Spektrum FTIR standar selulosa bakteri 22
7 Spektrum FTIR standar CMC 22
23
PENDAHULUAN
Hidrogel dapat didefinisikan sebagai jejaring polimer tiga dimensi yang dapat menyerap air maupun cairan biologis dan memiliki kemampuan mengembang tanpa larut di dalam air (Defader et al. 2009). Berdasarkan sifatnya yang dapat menyerap air dalam jumlah yang besar dan biokompatibilitasnya yang baik, hidrogel banyak dimanfaatkan sebagai penutup luka, sistem pelepasan obat, kosmetik, maupun pertanian. Hidrogel dapat dibuat menggunakan polimer sintetik di antaranya polivinil pirolidon, asam poliakrilat, dan polietilena glikol, maupun polimer alam seperti alginat, kitosan, karaginan, dan selulosa (Gulrez et al. 2011).
Karboksimetil selulosa (CMC) (Gambar 1) merupakan senyawa turunan selulosa yang diperoleh dari reaksi selulosa dengan senyawa monokloroasetat (Tomasino 1992). Karboksimetil selulosa banyak dimanfaatkan untuk keperluan biomedis karena memiliki keunggulan dalam hal biokompatibilitas dan biodegradabilitasnya, serta ketersediaan bahan bakunya, yaitu selulosa yang sangat melimpah di alam (Hashem et al. 2013). Selulosa yang digunakan sebagai bahan baku dapat bersumber dari selulosa bakteri seperti nata de coco. Selulosa bakteri mempunyai kekhasan sifat struktural dan fisikokimiawi dibandingkan dengan selulosa kayu (Yoshinaga et al. 1997).
Gambar 1 Struktur unit berulang dalam CMC
2
Gambar 2 Struktur kimia asam suksinat
Hidrogel memiliki sifat yang ideal sebagai penutup luka karena bersifat moist wound healing,yang berarti dapat mempertahankan kelembapan lingkungan di sekitar luka sehingga dapat mempercepat penyembuhan luka (Perwitasari et al. 2012). Penutup luka yang baik harus memiliki zat antibakteri (antibiotika) untuk mencegah tumbuhnya bakteri penyebab infeksi. Infeksi dapat memperberat kerusakan jaringan sehingga luka menjadi sukar pulih. Impregnasi antibakteri ke dalam penutup luka dapat memberikan hasil yang baik karena zat antibakteri yang ada dapat dilepaskan secara perlahan-lahan ke tempat luka untuk membunuh bakteri yang ada pada luka tersebut (Darwis et al. 2005).
Penelitian yang mengarah pada pengembangan hidrogel sebagai penutup luka dan sekaligus bersifat antibakteri telah banyak dilakukan. Istiqomah et al. (2012) telah meneliti pembuatan hidrogel kitosan-glutaraldehida untuk aplikasi penutup luka secara in vivo. Perwitasari et al. (2012) telah mencirikan secara in vitro dan in vivo komposit alginat-polivinil alkohol-ZnO berukuran nano sebagai penutup luka antibakteri. Hashem et al. (2013) telah meneliti pembuatan hidrogel dari CMC dan ZnO yang memiliki aktivitas antibakteri terhadap bakteri gram positif dan negatif.
Pada penelitian ini dibuat hidrogel menggunakan CMC dan asam suksinat serta penambahan zat antibakteri berupa logam perak. Perak telah dikenal luas sebagai senyawa yang dapat membunuh mikrob dengan efektif, seperti bakteri gram positif maupun negatif, dan bakteri super resisten (Ashe 2011). CMC-AS-AgNO3 diuji aktivitas antibakterinya terhadap Escherichia coli dan
Staphylococcus aureus untuk mengetahui besarnya penghambatan yang ditimbulkan terhadap kedua bakteri tersebut.
Penelitian ini bertujuan menyintesis hidrogel CMC-AS-AgNO3 dengan
penambahan asam suksinat sebagai agen pengikat silang, menentukan pengaruh nisbah komposisinya, serta ciri-ciri dan potensinya sebagai zat antibakteri. Penelitian ini dilaksanakan dari bulan Maret hingga Juli 2014 di Laboratorium Kimia Fisik, Departemen Kimia, FMIPA IPB dan Laboratorium Pusat Studi Biofarmaka, Lembaga Penelitian dan Pengabdian Kepada Masyarakat-Institut Pertanian Bogor (PSB LPPM-IPB).
METODE
Alat dan Bahan
3 inkubator, ruang laminar (Aneka Lab), autoklaf, penangas air, oven, ultrasonik, desikator, neraca analitik, blender, ayakan 100 dan 400 mesh, kertas alumunium, kempa hidraulik, mikropipet, dan alat-alat kaca. Bahan-bahan yang digunakan adalah nata de coco, isopropanol p.a (Merck), NaOH 35% (b/v) (Merck), asam monokloroasetat p.a (Merck), metanol 80%, metanol absolut p.a (Merck), asam suksinat p.a (Merck), asam asetat teknis (Bratachem), AgNO3 p.a (Merck), NaOH
0.3 M (Merck), HCl 0.3 M (Merck), induk bakteri Escherichia coli dan Staphylococcus aureus (IPB Culture Centre Lab Mikrobiologi), agar hara (NA), kaldu hara (NB), agar soya tripton (TSA), kaldu soya tripton (TSB), kloramfenikol 1000 ppm, tetrasiklin 1000 ppm, akuabides, dan akuades.
Metode Penelitian
Tahapan penelitian yang dilakukan meliputi pembuatan CMC dan CMC-AS-AgNO3, pencirian CMC, pencirian, dan pengujian antibakteri
CMC-AS-AgNO3 (Lampiran 1).
Pencucian Nata de Coco
Nata de Coco dicuci dengan air keran hingga bersih, kemudian direndam di dalam ember plastik selama 3 hari dan setiap hari air rendaman diganti. Setelah itu, nata direbus sampai mendidih pada suhu 110 °C selama 10-20 menit. Setelah direbus, lembaran nata ditekan menggunakan kempa hidraulik hingga hampir seluruh air keluar. Selulosa bakteri yang berbentuk lembaran tipis dikeringkan di bawah sinar matahari, lalu dihancurkan dengan blender. Serbuk halus berukuran 60 mesh disaring dengan ayakan (Awalludin 2004).
Pembuatan CMC dinetralkan dengan asam asetat pada suhu kamar. Campuran disaring kembali, lalu CMC dicuci dengan metanol absolut dan dikeringkan pada suhu 55 °C hingga kering. CMC yang diperoleh dihaluskan hingga berukuran 100 mesh (Awalludin 2004).
Pembuatan CMC-AS-AgNO3
Sebanyak 3 g CMC, 1.5 g asam suksinat, dan AgNO3 (0.2, 0.4, 0.6% (b/v))
4
Penentuan Derajat Substitusi CMC
Sebanyak 0.5 g serbuk kering CMC ditimbang, dimasukkan ke dalam Erlenmeyer 250 mL dan ditambahkan 100 mL akuades, kemudian diaduk. Sebanyak 25 mL NaOH 0.3 M ditambahkan dan campuran dipanaskan di atas penangas air selama 15 menit. Setelah larutan homogen, ditambahkan indikator fenolftalein sebanyak 3 tetes, selanjutnya larutan dititrasi menggunakan HCl 0.3 M. Titik akhir titrasi tercapai ketika terjadi perubahan warna larutan dari merah muda menjadi tidak berwarna. Titrasi dilakukan 3 kali ulangan (Hong 2013).
Derajat substitusi (DS) dari CMC dapat diketahui melalui persamaan berikut:
Kandungan Karboksimetil (%CM) = DS =
Keterangan:
V0 = Volume HCl yang digunakan saat titrasi blangko (mL) Vn = Volume HCl yang digunakan saat titrasi sampel (mL)
M = Molaritas HCl yang digunakan (M) m = Massa sampel (g)
162 g/mol = Massa molar dari satu unit anhidroglukopiranosa (AGU) 59 g/mol = Massa molar dari –CH2COOH
Penentuan Kadar Air CMC
5
Kemampuan Pembengkakan (Swelling)
Lembaran CMC-AS-AgNO3 berukuran 1 cm2 ditimbang dengan teliti (A),
kemudian direndam di dalam cawan petri berisi akuades. Lembaran direndam selama 24 jam, setelah itu hidrogel dikeluarkan dari cawan petri, dan air pada permukaan hidrogel dihilangkan dengan tissue, kemudian hidrogel ditimbang kembali dengan teliti (B) (Modifikasi Darwis et al. 2010). Derajat pembengkakan atau swelling dihitung dengan persamaan berikut:
Derajat swelling (%) = × 100%
Identifikasi Gugus Fungsi dengan Spektroskopi FTIR
Selulosa bakteri, CMC, dan CMC-AS dilakukan pengujian gugus fungsi dengan spektroskopi inframerah transformasi Fourier (FTIR). Sebanyak 0.02 g sampel dihaluskan secara hati-hati dengan 0.1 g KBr kemudian dipanaskan dalam oven pada suhu 60 °C selama 12 jam. Setelah itu dicetak dalam bentuk pelet. Kemudian dilakukan pengukuran menggunakan alat FTIR pada bilangan gelombang 500-4000 cm-1.
Analisis Morfologi dengan Mikroskop Elektron Payaran (SEM)
Lembaran CMC-AS-AgNO3 0.6% dilakukan pengujian bentuk
morfologinya dengan menggunakan Mikroskop Elektron Payaran atau Scanning Electron Microscopy (SEM). Sampel berukuran 1 cm2 dilapisi dengan lapisan tipis logam emas, kemudian dianalisis menggunakan SEM.
Pola Difraksi CMC-AS-AgNO3 dengan Difraktometer Sinar-X (XRD)
Lembaran CMC-AS-AgNO3 0.6% dilakukan pengujian pola difraksinya
dengan menggunakan difraktometer sinar-X. Sumber sinar yang digunakan adalah radiasi sinar Cu dengan panjang gelombang 1.5406 Å dan sudut difraksi antara 10°-80° dengan kecepatan 2°/menit.
Uji Aktivitas Antibakteri CMC-AS-AgNO3
Metode uji antibakteri diadaptasi dari metode Garriga et al. (1993) dengan menggunakan teknik difusi agar yang telah dimodifikasi. Pertama-tama, alat-alat dan bahan yang akan digunakan seperti cawan petri, kertas cakram, akuades harus disterilkan terlebih dahulu di dalam autoklaf pada suhu 121 °C selama 15 menit.
Kultur mikroba uji harus disegarkan terlebih dahulu. Inokulasi bakteri dimulai dengan menyiapkan media cair NB untuk bakteri Escherichia coli sebanyak 10 mL (13 g/1000 mL) dan TSB untuk bakteri Staphylococcus aureus sebanyak 10 mL (30 g/1000 mL), bakteri disegarkan dengan menginokulasikan satu ose kultur murni E. coli dari agar miring NA ke dalam medium cair NB secara aseptik, hal yang sama juga dilakukan dengan menginokulasikan satu ose kultur murni S. aureus dari agar miring TSA ke dalam medium cair TSB secara aseptik. Kultur uji kemudian diinkubasi selama 18 jam untuk bakteri E. coli dan 24 jam untuk bakteri S. aureus pada suhu 37 °C.
6
dihomogenkan dengan pengaduk magnetik di atas penangas air hingga larutan berubah menjadi bening. Media ini disterilkan menggunakan autoklaf pada suhu 121 °C selama 15 menit. Media NA dan TSA steril didinginkan sampai suhu 45-50 °C.
Kultur uji segar diinokulasikan sebanyak 100 µL ke dalam 100 mL media NA dan TSA. Setelah kultur bercampur dengan media, media cair dituangkan ± 20 mL ke dalam cawan petri. Setelah campuran media dan kultur uji membeku, sampel CMC-AS-AgNO3 yang dibentuk cakram berukuran 6 mm diletakkan di
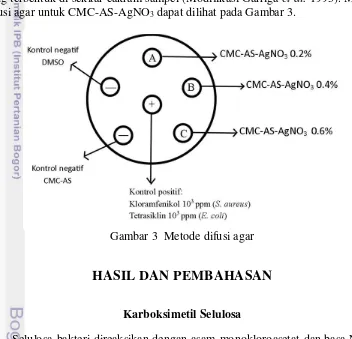
atas media agar tersebut, selain sampel digunakan juga kontrol negatif berupa CMC-AS dan DMSO, serta kontrol positif berupa kloramfenikol 1000 ppm untuk bakteri S. aureus dan tetrasiklin 1000 ppm untuk bakteri E. coli. Cawan petri tersebut diinkubasi pada suhu 37 °C selama 18 jam untuk bakteri E. coli dan 24 jam untuk bakteri S. aureus. Areal penghambatan diukur berdasarkan zona bening yang terbentuk di sekitar cakram sampel (Modifikasi Garriga et al. 1993). Metode difusi agar untuk CMC-AS-AgNO3 dapat dilihat pada Gambar 3.
Gambar 3 Metode difusi agar
HASIL DAN PEMBAHASAN
Karboksimetil Selulosa
7
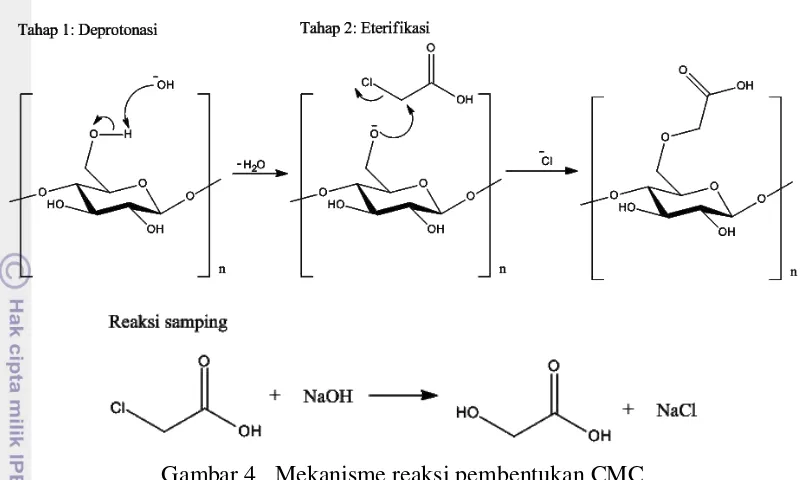
Gambar 4 Mekanisme reaksi pembentukan CMC
Reaksi samping berupa NaCl dan asam glikolat dapat dipisahkan melalui pencucian dengan metanol dan penetralan menggunakan asam asetat (Aprilia 2009). Asam monokloroasetat yang ditambahkan secara berlebih pada polimer selulosa menghasilkan CMC sebesar 3-4 kali berat selulosa awal. Hal ini menunjukkan bahwa gugus-gugus hidroksil yang terdapat pada selulosa telah bereaksi dengan gugus-gugus karboksimetil menghasilkan rantai eter antara selulosa dan karboksimetil. Hasil sintesis CMC diperoleh berupa serbuk padatan halus berwarna putih kekuningan yang ditunjukkan oleh Gambar 5.
Gambar 5 Hasil sintesis CMC
Karboksimetil Selulosa-Asam Suksinat-AgNO3
8
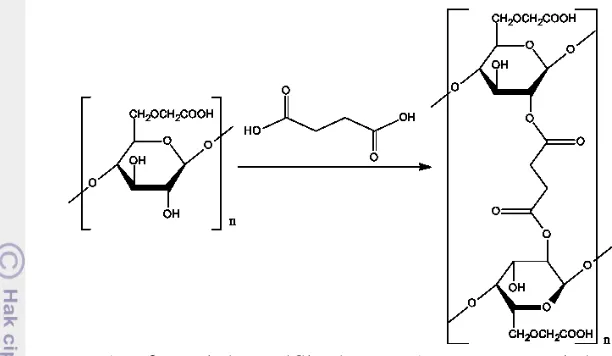
Gambar 6 Reaksi esterifikasi CMC dengan asam suksinat
Campuran CMC-asam suksinat (CMC-AS) menghasilkan larutan kental berwarna kekuningan. Perbandingan CMC dan asam suksinat yang digunakan menentukan sifat fisik dan kimia hidrogel yang dihasilkan, karena memengaruhi banyaknya ikatan silang yang terbentuk. Campuran CMC-AS kemudian ditambahkan larutan AgNO3 dengan variasi konsentrasi sebesar 0.2%, 0.4%, dan
0.6% (b/v). Menurut Kim & Kim (2013), perak dapat menunjukkan aktivitas antibakteri yang baik pada konsentrasi di atas 0.1% dan tidak lebih dari 6%, konsentrasi perak di atas 6% dapat menyebabkan toksisitas. Campuran larutan CMC, asam suksinat, dan AgNO3 menghasilkan larutan kental berwarna putih
susu, selanjutnya larutan tersebut dicetak pada pelat kaca, dan dikeringkan pada suhu 55 °C. Gambar 7 menunjukkan film yang dihasilkan.
Gambar 7 Film dengan berbagai komposisi a) CMC-AS, b) CMC-AS-AgNO3
0.2%, c) CMC-AS-AgNO3 0.4%, d) CMC-AS-AgNO3 0.6%
Pencirian CMC Hasil Sintesis
9 10.00%. Bahan organik tersebut dapat disimpan dalam jangka waktu yang lama karena lebih tahan terhadap kontaminan mikrob. Menurut SNI 06-3736-1995, CMC merupakan senyawa yang memiliki rentang pH antara 6-8.5. Berdasarkan hasil pengukuran, CMC hasil sintesis memiliki pH sebesar 4.57 (Lampiran 3), hasil ini tidak berada pada rentang pH CMC berdasarkan literatur, hal ini mungkin disebabkan proses penetralan yang tidak sempurna. Proses penetralan dilakukan pada CMC hasil sintesis yang belum murni. Hasil sintesis masih berupa campuran antara CMC, asam glikolat, dan NaCl (Aprilia 2009). Campuran ini dapat dipisahkan dengan melakukan pencucian hasil sintesis menggunakan metanol dan penetralan dengan asam asetat, namun pada penelitian ini proses pemurnian CMC tersebut belum maksimal. Menurut Aprilia (2009) CMC stabil pada rentang pH 2-10. Tabel 1 menunjukkan pencirian dari CMC hasil sintesis dibanding dengan CMC mutu 1.
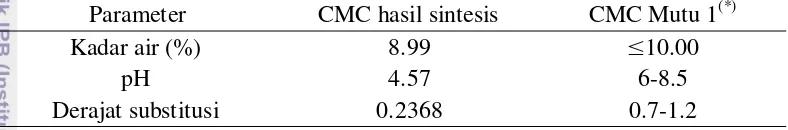
Tabel 1 Pencirian CMC hasil sintesis
Parameter CMC hasil sintesis CMC Mutu 1(*)
Kadar air (%) 8.99 ≤10.00
pH 4.57 6-8.5
Derajat substitusi 0.2368 0.7-1.2
(*) SNI 06-3736-1995
Derajat substitusi merupakan ukuran rerata dari banyaknya gugus hidroksil yang digantikan menjadi gugus eter karboksilat pada pembentukan CMC. Derajat substitusi ini mempengaruhi sifat kelarutan CMC yang dihasilkan, semakin banyak gugus karboksimetil maka CMC memiliki gugus fungsi yang lebih mudah berikatan dengan air. Setiap monomer selulosa memiliki dua gugus hidroksil sekunder yang terikat pada 2 dan 3, serta satu gugus hidroksil primer pada C-6. Secara teoritis 3 buah gugus hidroksil yang terdapat pada monomer selulosa tersebut dapat digantikan dengan gugus karboksimetil menghasilkan CMC dengan derajat substitusi sebesar 3. Namun pada berbagai pengujian dihasilkan derajat substitusi antara 0.2-1.2. Hal ini disebabkan karena reaksi dipengaruhi oleh halangan sterik dari polimer selulosa serta asam monokloroasetat yang digunakan. Selama proses karboksimetilasi gugus hidroksil pada C-6 menunjukkan reaktivitas paling tinggi diikuti oleh C-2 dan C-3 (Aprilia 2009). CMC hasil sintesis yang diperoleh memiliki derajat substitusi rerata sebesar 0.2368 (Lampiran 4). CMC dengan derajat substitusi sebesar 0.2368 tidak larut sempurna di dalam air, sehingga masih terdapat sebagian kecil CMC yang tidak dapat larut. Ditinjau dari segi kualitas, CMC dengan kemurnian yang tinggi merupakan CMC yang memiliki nilai kadar air tidak lebih dari 10.00%, derajat substitusi antara 0.7-1.2, dan nilai pH antara 6-8.5 (SNI 06-3736-1995). Dengan demikian, CMC yang dihasilkan dari penelitian ini belum termasuk CMC dengan mutu terbaik.
Kemampuan Pembengkakan (Swelling)
10
sifat tersebut hidrogel sangat ideal digunakan sebagai penutup luka, karena hidrogel yang telah menyerap air maupun cairan biologis lain dapat mempertahankan kelembaban sekitar luka sehingga mempermudah pembentukan sel-sel dan jaringan baru sehingga dapat mempercepat penyembuhan luka.
Kemampuan pembengkakan ini dipengaruhi oleh beberapa faktor, di antaranya adalah banyaknya ikatan silang yang terbentuk dan banyaknya komposit atau zat lain yang ditambahkan. Ikatan silang dalam polimer menghasilkan struktur tiga dimensi, struktur inilah yang membuat hidrogel dapat mempertahankan bentuknya walaupun banyak molekul air yang masuk. Namun, peningkatan ikatan silang dapat menurunkan absorbsi air ke dalam rongga-rongga polimer, hal ini disebabkan karena semakin banyak ikatan silang yang terbentuk maka struktur polimer akan semakin rapat sehingga kemampuan difusi air ke dalam jaringan polimer berkurang dan menyebabkan derajat swelling hidrogel relatif turun. Komposisi CMC dan asam suksinat yang digunakan merupakan komposisi yang relatif baik karena menghasilkan hidrogel dengan ikatan silang yang cukup untuk mempertahankan struktur tiga dimensi hidrogel. Penambahan komposit berupa logam perak dapat menaikkan kemampuan pembengkakan hidrogel, hal ini disebabkan karena kemampuan dari logam perak yang dapat menempel pada hidrogel sehingga dapat meningkatkan porositas dan ruang kosong di antara jaringan hidrogel yang berakibat dapat menyerap lebih banyak air (Hebeish et al. 2013). Derajat swelling CMC-AS dan CMC-AS-AgNO3
disajikan pada Gambar 8.
Gambar 8 Derajat swelling hidrogel
Hidrogel CMC-AS-AgNO3 0.6% memiliki nilai derajat swelling tertinggi
11 yang digunakan tidak larut sempurna di dalam air sehingga ikatan silang yang terbentuk belum maksimal.
Identifikasi Gugus Fungsi
Identifikasi gugus fungsi dengan FTIR dilakukan pada beberapa tahap penelitian, yang pertama adalah analisis gugus fungsi pada selulosa bakteri yang digunakan sebagai bahan baku pembuatan CMC, yang kedua adalah CMC hasil sintesis, dan CMC-AS. Analisis ini didasarkan pada penyerapan radiasi elektromagnetik oleh sejumlah sampel pada bilangan gelombang antara 4000-400 cm-1.
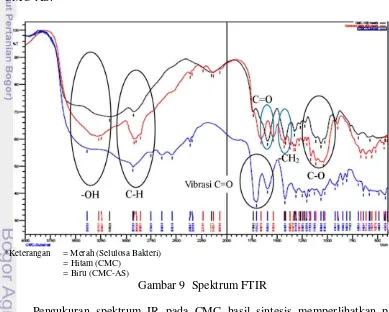
Selulosa bakteri yang dianalisis memperlihatkan pencirian pita serapan dari gugus fungsi dan ikatan yang terdapat pada molekul selulosa. Pita serapan pada panjang gelombang 3244.27 cm-1 mengindikasikan adanya gugus –OH. Pita serapan pada 2920 cm-1 mengindikasikan adanya vibrasi C-H, serta pita serapan pada panjang gelombang 1037.70 cm-1 menunjukkan vibrasi C-O. Spektrum IR selulosa bakteri tersebut memiliki kemiripan gugus fungsi dengan selulosa bakteri standar (Parthibanka et al. 2011) (Lampiran 6). Gambar 9 menunjukkan spektrum FTIR yang diperoleh pada pengukuran selulosa bakteri, CMC hasil sintesis, dan CMC-AS.
*Keterangan = Merah (Selulosa Bakteri) = Hitam (CMC)
= Biru (CMC-AS)
Gambar 9 Spektrum FTIR
Pengukuran spektrum IR pada CMC hasil sintesis memperlihatkan pita serapan pada panjang gelombang 3163.26 cm-1 yang mengindikasikan adanya gugus –OH. Pita serapan pada panjang gelombang 2924.09 cm-1 menunjukkan vibrasi C-H. Pita serapan pada panjang gelombang 1593.20 cm-1 menunjukkan
gugus karbonil, dan pada panjang gelombang 1060.85 cm-1 merupakan vibrasi
12
yang diidentifikasi sebagai gugus C=O dan pada daerah bilangan gelombang 1415.75 cm-1 yang diidentifikasi sebagai –CH2. Hal tersebut menunjukkan bahwa
selulosa telah memiliki gugus karboksimetil. Spektrum IR yang dihasilkan pada pengukuran CMC hasil sintesis menunjukkan adanya kemiripan gugus fungsi yang ada pada CMC standar (Mohkami & Talaeipour 2011) (Lampiran 7).
Pengukuran spektrum IR CMC-AS memperlihatkan adanya gugus –OH yang ditunjukkan oleh pita serapan pada panjang gelombang 3387 cm-1. Pada
panjang gelombang 2931.80 cm-1 adalah vibrasi C-H. Pita serapan pada panjang
gelombang 1701.22 cm-1 merupakan vibrasi dari gugus karbonil. Pergeseran gugus karbonil pada CMC dan CMC-AS dari pita serapan pada panjang gelombang 1593.20 cm-1 ke panjang gelombang 1701.22 cm-1 menunjukkan
adanya ikatan silang yang terbentuk antara CMC dengan asam suksinat (Hashem et al. 2013). Gugus fungsi yang dimiliki oleh spektrum IR sampel CMC-AS menyerupai gugus fungsi yang dimiliki spektrum IR CMC-AS menurut penelitian yang dilakukan oleh Hashem et al. 2013. Hal ini mengindikasikan bahwa proses ikatan silang antara CMC dan asam suksinat telah berhasil dilakukan.
Morfologi CMC-AS-AgNO3
Analisis menggunakan mikroskop elektron payaran (SEM) adalah teknik analisis untuk mengetahui morfologi, bentuk, ukuran, serta porositas dari hidrogel. Gambar 10 menunjukkan mikrograf dari CMC-AS-AgNO3 0.6%. Pada
Gambar 10a terlihat cuplikan CMC-AS-AgNO3 0.6% pada perbesaran 100×
menunjukkan bahwa AgNO3 tidak terdistribusi secara merata di antara CMC-AS,
gambar berwarna terang merupakan distribusi logam AgNO3, sedangkan gambar
berwarna gelap merupakan CMC-AS. Distribusi yang tidak merata dapat disebabkan karena larutan belum homogen. Pada Gambar 10b cuplikan CMC-AgNO3 0.6% pada perbesaran 1000× memperlihatkan kristal AgNO3 yang
terdapat di permukaan film.
Gambar 10 Analisis morfologi CMC-AS-AgNO3 0.6% a) perbesaran 100×, b)
13 Analisis lebih jauh mengenai morfologi film yang dihasilkan tidak dapat dilakukan karena permukaan film dengan perbesaran 1000× sebagian besar menunjukkan distribusi kristal, oleh karena itu pori-pori dari film yang dihasilkan tidak dapat diamati. Hebeish et al. (2013) melaporkan morfologi dari CMC yang ditambahkan komposit berupa nanopartikel perak menghasilkan penampang nanopartikel perak yang berbentuk bola (Gambar 10c).
Difraktogram CMC-AS-AgNO3
Hasil pengukuran CMC-AS dan CMC-AS-AgNO3 0.6% menggunakan
difraksi sinar-X menghasilkan difraktogram yang khas. Difraktogram yang dihasilkan dari CMC-AS-AgNO3 0.6% dibandingkan dengan standar dari
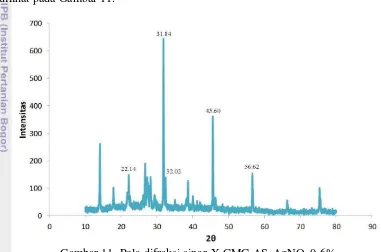
program PCPDFWIN database Joint Committee on Powder Diffraction Standards-International Centre for Diffraction Data (JCPDS-ICDD) untuk mengetahui jenis logam yang terbentuk. Difraktogram yang dihasilkan dapat dilihat pada Gambar 11.
Gambar 11 Pola difraksi sinar-X CMC-AS-AgNO3 0.6%
Perbandingan pola difraksi sinar-X CMC-AS-AgNO3 0.6% menunjukkan
bahwa terdapat beberapa kesesuaian dengan database PCPDFWIN No. 73-1861 (Lampiran 8) yang merupakan kristal AgNO2 dengan sistem ortorombik.
Puncak-puncak AgNO2 pada difraktogram terletak pada 2θ: 22.14; 31.84; 32.02; 45.60;
dan 56.62°. Perubahan bentuk AgNO3 yang ditambahkan sebelumnya menjadi
AgNO2 dapat disebabkan karena adanya pemberian panas mencapai suhu 70 °C
pada proses ultrasonikasi maupun pada proses pengeringan film. Tabel 2 menunjukkan perbandingan pola difraksi hasil analisis CMC-AS-AgNO3 0.6%
14
Tabel 2 Perbandingan pola difraksi hasil analisis dengan JCPDS-ICDD
CMC-AS-AgNO3 0.6% JCPDS-ICDD AgNO2
2θ (°) Intensitas 2θ (°) Intensitas
22.12 149 22.386 837
31.84 643 29.132 999
32.02 128 30.633 195
45.60 360 45.84 428
56.62 153 55.183 72
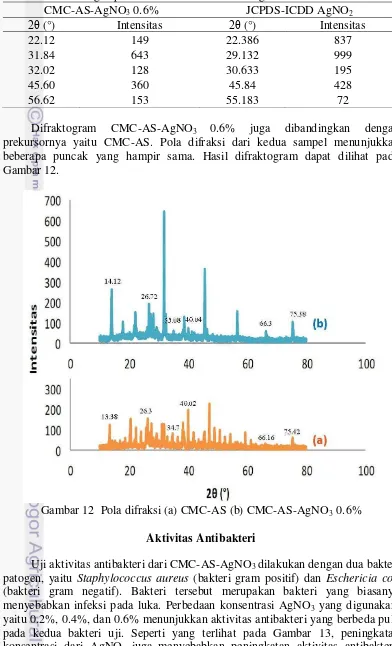
Difraktogram CMC-AS-AgNO3 0.6% juga dibandingkan dengan
prekursornya yaitu CMC-AS. Pola difraksi dari kedua sampel menunjukkan beberapa puncak yang hampir sama. Hasil difraktogram dapat dilihat pada Gambar 12.
Gambar 12 Pola difraksi (a) CMC-AS (b) CMC-AS-AgNO3 0.6%
Aktivitas Antibakteri
Uji aktivitas antibakteri dari CMC-AS-AgNO3 dilakukan dengan dua bakteri
patogen, yaitu Staphylococcus aureus (bakteri gram positif) dan Eschericia coli (bakteri gram negatif). Bakteri tersebut merupakan bakteri yang biasanya menyebabkan infeksi pada luka. Perbedaan konsentrasi AgNO3 yang digunakan,
15 Gambar 13 menunjukkan dengan jelas zona inhibisi yang terbentuk akibat penambahan CMC-AS-AgNO3 seperti yang terlihat juga pada antibiotik standar
seperti kloramfenikol dan tetrasiklin pada kedua bakteri uji.
Gambar 13 Hasil uji aktivitas antibakteri a) pada bakteri uji E. coli, b) pada bakteri uji S. aureus
Tabel 3 Zona inhibisi CMC-AS-AgNO3
Sampel Zona inhibisi (mm)
E. coli S. aureus
Kontrol - DMSO 0.00 0.00
Kontrol - (CMC-AS) 15.25 10.52
A (0.2%) 15.74 11.27
B (0.4%) 16.21 11.77
C (0.6%) 17.27 11.94
Kontrol + (*) 21.91 16.72
(*) Kontrol + (E. coli) : Tetrasiklin 1000 ppm
Kontrol + (S. aureus) : Kloramfenikol 1000 ppm
Diameter zona inhibisi CMC-AS-AgNO3 pada bakteri E. coli maupun pada
bakteri S. aureus mengalami peningkatan seiring dengan meningkatnya konsentrasi perak (Tabel 3). Sampel CMC-AS-AgNO3 lebih toksik terhadap
bakteri E. coli, hal ini dibuktikan dengan diameter zona inhibisi terhadap bakteri E. coli lebih besar dibandingkan dengan bakteri S. aureus. Bakteri E. coli merupakan bakteri gram negatif yang mengandung peptidoglikan lebih sedikit dibandingkan dengan S. aureus yang merupakan bakteri gram positif. Peptidoglikan adalah polimer-polimer dan protein penyusun dinding sel dari bakteri, sehingga E. coli memiliki dinding sel yang lebih tipis dari pada S. aureus yang menyebabkan E. coli lebih mudah diserang oleh senyawa antibakteri (Adji 2008). Kontrol negatif CMC-AS menunjukkan adanya aktivitas antibakteri, namun nilai zona inhibisi yang dihasilkan lebih kecil dibanding dengan CMC-AS-AgNO3. Analisis lebih lanjut dapat dilakukan untuk mempelajari aktivitas
16
Tabel 4 Rasio aktivitas antibakteri
Sampel CMC-AS-AgNO3 0.6% memiliki rasio aktivitas antibakteri sebesar 0.7882
dibanding dengan kontrol antibiotik standar untuk bakteri uji E. coli dan 0.7141 untuk bakteri uji S. aureus. Hidrogel CMC yang berpotensi sebagai penutup luka juga dapat dihasilkan dengan penambahan logam-logam selain perak, yaitu seng dan titanium. Hadi (2014) melaporkan CMC-AS-ZnO 0.5% memiliki rasio aktivitas antibakteri sebesar 0.8180 dibanding dengan kontrol positif antibiotik standar untuk bakteri uji E. coli dan 0.5838 untuk bakteri uji S. aureus. Perangin-angin (2014) melaporkan CMC-AS-TiO2 0.5% memiliki rasio aktivitas antibakteri
sebesar 0.8138 dibanding dengan kontrol antibiotik standar untuk bakteri uji E. coli dan 0.7590 untuk bakteri uji S. aureus. Hasil tersebut menunjukkan bahwa hidrogel berbasis karboksimetil selulosa dengan penambahan logam memiliki potensi sebagai antibakteri.
SIMPULAN DAN SARAN
Simpulan
CMC berhasil disintesis dari bahan dasar selulosa bakteri. CMC yang dihasilkan merupakan CMC kualitas 2 yang memiliki derajat substitusi sebesar 0.2368 dan pH sebesar 4.57. Hidrogel yang berpotensi sebagai penutup luka dapat dibuat dari campuran CMC, asam suksinat, dan AgNO3. Paduan CMC-AS-AgNO3
berpotensi sebagai penutup luka yang baik karena memiliki aktivitas antibakteri dan bersifat dapat mempertahankan kelembaban sekitar luka. CMC-AS-AgNO3
dengan penambahan AgNO3 sebesar 0.6% menunjukkan kemampuan
pembengkakan terbaik sebesar 134.16% dan aktivitas antibakteri terbaik dengan zona inhibisi sebesar 17.27 mm untuk bakteri E. coli dan 11.94 mm untuk bakteri S. aureus.
Saran
17
DAFTAR PUSTAKA
Adji K. 2008. Evaluasi kontaminasi bakteri pathogen pada ikan segar diperairan teluk semarang [tesis]. Semarang (ID): Program Pasca Sarjana, Universitas Diponegoro.
Aprilia L. 2009. Preparasi produk nata de pina dan aplikasi pengikatannya terhadap logam kobalt (II) [skripsi]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Ashe B. 2011. A detail investigation to observe the effect of zinc oxide and silver nanoparticles in biological system [tesis]. Orissa (IN): Fakultas Teknologi, Institut Teknologi Nasional.
Awaluddin A. 2004. Karboksimetilasi selulosa bakteri [skripsi]. Bogor (ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Darwis D, Erlinda T, Hardiningsih L, Chosdu R. 2005. Uji daya antimikroba dan
sifat fisiko-kimia penutup luka hidrogel steril radiasi yang mengandung ekstrak buah mengkudu (Morinda citrifolia L.). J. Ilmiah AI & R 1(1):38-47 Darwis D, Hardiningsih L, Nurlidar F. 2010. Modifikasi penutup luka hidrogel
hasil iradiasi sinar gamma dengan madu: karakteristik sifat fisika-kimia hidrogel PVP madu. Seminar Nasional Keselamatan Kesehatan dan Lingkungan VI; 2010 Jun 15-16; Jakarta, Indonesia.
Defader NC, Ganguli S, Sattar MA, Haque ME, Akhtar F. 2009. Synthesis of superabsorben acrylamide/kappa-carrageenan blend hydrogel by gamma radiation. Malay Polym J 4(2): 27-45.
Fessenden RJ, Fessenden JS. 1986. Kimia Organik Jild 2. Pudjaatmaka AH, penerjemah. Jakarta: Erlangga. Terjemahan dari Organic Chemistry Part 2. Garriga M, Hugas M, Aymerich T, Monfort JM. 1993. Bacteriocinogenic activity
of Lactobacilli from fermenter sausages. J App Bact 75:142-148.
Gulrez SKH, Al-Assaf S, Phillips GO. 2011. Hydrogels: methods of preparation, characterisation, and aplications, progress in molecular and environmental bioengineering - Dari Analysis and Modeling to Technology Applications, Prof. Angelo Carpi (Ed.), ISBN: 978-953-307-268-5, InTech, Tersedia pada: http://www.intechopen.com/books/progress-in-molecular-and- environmental-bioengineeringfrom-analysis-and-modeling-to-technology- applications/hydrogels-methods-of-preparation-characterisationand-applications
Hadi A. 2014. Sintesis hidrogel antibakteri berbasis karboksimetil selulosa-ZnO [skripsi], siap terbit. Bogor (ID): Institut Pertanian Bogor.
Hashem M, Sharaf S, El-Hady MMA, Habeish A. 2013. Synthesis and characterization of novel carboxymethylcellulose hydrogels and carboxymethylcellulose-hydrogel-ZnO-nanocomposites. Carbohyd Polym 94(2013): 421-427.
Heibeish A, Hashem M, Abd El-Hady MM, Sharaf S. 2013. Development of cmc hydrogels loaded with silver nan0-particles for medical applications. Carbohyd Polym 92(2013): 407-4013.
18
Istiqomah N, Izak D, Sumarsih S. 2013. Pembuatan Hidogel Kitosan-Glutaraldejid untuk Aplikasi Penutup Luka secara In Vivo. Jurnal Fisika dan Terapannya 1(1): 104-116.Kim YS, Kim JY, penemu; Cellulose Concepts, Llc. 2013 Apr 2. Methods for producing silver-bonded antimicrobial moist wound dressings and moist wound dressings produced by the methods. Paten Amerika Serikat US 8409608 B2.
Mohkami M, Talaeipour M. 2011. Investigation of the chemical structure of carboxylated and carboxymethylated fibers from waste paper via XRD and FTIR analysis. BioResources 69(2): 1988-2003.
Parthiban K, Manikandan S, Ganesapandian S. 2011. Production of cellulose I microfibrils from Rhizobium sp. and its wound healing activity on mice. AJAS 4(3): 247-254.
Pavia DL, Lampman GM, Kriz GS, Vyvyan JR. 2009. Introduction to Spectroscopy. Ed ke-4. Washington (US): Thomson Learning.
Perangin-angin C. 2014. Sintesis hidrogel antibakteri berbasis karboksimetil selulosa-TiO2 [skripsi], siap terbit. Bogor (ID): Institut Pertanian Bogor.
Perwitasari FLR, Aminatun, Sumarsih S. 2012. Karakterisasi in vitro dan in vivo komposit alginat-poli vinil alkohol-ZnO nano sebagai wound dressing antibakteri. Di dalam: Samian, Yuwana YGY, editor. Peran Fisika Dan Terapannya Sebagai Modal Pengembangan Kemandirian Bangsa Di Bidang Pendidikan, Industri, dan Kedokteran. Seminar Nasional Fisika Terapan III; 2012 Sept 15; Surabaya, Indonesia. Surabaya (ID): Universitas Airlangga. hlm 115-118.
[SNI 06-3736-1995]. 1995. Natrium Karboksimetil Selulosa Teknis. Jakarta: Badan Standarisasi Nasional.
Tomasino C.1992. Chemistry and Technology of Fabric Preparation and Finishing. Raleigh: North Carolina state University.
Wijayani A, Ummah K, Tjahjani S. 2005. Characterization of carboxymethyl cellulose (CMC) from Eichornia crassipes (Mart) Solms. Indo J Chem 5(3): 228-231.
19
LAMPIRAN
Lampiran 1 Diagram alir penelitian
20
Lampiran 3 pH larutan CMC 1%
Ulangan pH pH
1 4.58
4.57
2 4.57
3 4.57
Contoh Perhitungan
Rerata pH CMC = =
= 4.57
Lampiran 4 Penentuan derajat substitusi CMC
Ulangan Bobot CMC Volume HCl %CM Substitusi Derajat Awal Akhir Terpakai
Blangko 0.0000 0.00 24.30 24.30
1 0.5228 23.60 45.70 22.10 7.5750 0.2247 2 0.5053 1.80 23.90 22.10 7.8373 0.2332 3 0.5043 23.90 45.75 21.85 8.4358 0.2526
Rerata 0.2368
Contoh Perhitungan Molaritas HCl induk: -HCl 32% (b/b)
-Bobot Jenis 1,160 g/mL M =
=
= 10.1699 M HCl 0.3 M V1M1 = V2M2
100 mL × 0.3 M = V2 × 10.1699 M
V2 = 2.94 mL
Konsentrasi HCl sebenarnya: V1M1 = V2M2
100 mL × M1 = 3 mL × 10.1699 M
21
Lampiran 5 Derajat swelling CMC-AgNO3
22
Lampiran 6 Spektrum FTIR standar selulosa bakteri
Gugus fungsi Panjang gelombang
-OH 3412
-CH 2922
C-O-C 1034
Lampiran 7 Spektrum FTIR standar CMC
Gugus fungsi Panjang gelombang
-OH 3587
-CH 2876
C=O 1636
C-O-C 994
23
RIWAYAT HIDUP
Penulis dilahirkan di Tangerang pada tanggal 10 Juli 1992 dari ayah Rasimin dan ibu Siti Kanah. Penulis adalah putri kedua dari dua bersaudara. Tahun 2010 penulis lulus dari SMA Negeri 47 Jakarta dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB dan diterima di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.