SELEKSI DAN KARAKTERISASI BAKTERI ENDOFIT
UNTUK MENEKAN KEJADIAN PENYAKIT LAYU BAKTERI
(Ralstonia solanacearum) PADA TANAMAN TOMAT
IKA DAMAYANTI
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
ABSTRAK
IKA DAMAYANTI. Seleksi dan Karakterisasi Bakteri Endofit untuk Menekan Kejadian Penyakit Layu Bakteri (Ralstonia solanacearum) pada Tanaman Tomat. Dibimbing oleh ABDJAD ASIH NAWANGSIH.
Ralstonia solanacearum merupakan salah satu bakteri penyebab layu pada tanaman tomat. Tanaman yang terserang menunjukkan gejala layu mendadak bahkan dapat menimbulkan kematian. Penelitian ini bertujuan untuk mengetahui keragaman jenis bakteri endofit yang ada dalam batang tanaman tomat sehat dan menseleksi bakteri endofit tersebut sebagai kandidat agens hayati dan pemacu pertumbuhan tanaman tomat. Bakteri endofit diisolasi dari batang tanaman tomat sehat yang berasal dari wilayah Bogor, Cipanas dan Lembang, kemudian diseleksi keefektifannya dalam menghambat populasi R.solanacearum dengan metode dual culture berdasarkan pembentukan zona penghambatan. Isolat bakteri endofit yang tidak menghasilkan zona hambatan kemudian diuji kemampuan penekanannya dalam media cair. Masing-masing tiga jenis isolat bakteri endofit yang memberikan penekanan terbaik berdasarkan kedua pengujian tersebut, yaitu yang memiliki diameter zona hambatan terbesar dan penekanan populasi
SELEKSI DAN KARAKTERISASI BAKTERI ENDOFIT
UNTUK MENEKAN KEJADIAN PENYAKIT LAYU BAKTERI
(Ralstonia solanacearum) PADA TANAMAN TOMAT
IKA DAMAYANTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Pertanian
pada Departemen Proteksi Tanaman
Fakultas Pertanian
di Insitut Pertanian Bogor
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul : Seleksi dan Karakterisasi Bakteri Endofit untuk
Menekan Kejadian Penyakit Layu Bakteri (Ralstonia
solanacearum) pada Tanaman Tomat
Nama : Ika Damayanti
NRP : A34050855
Menyetujui
Pembimbing
Dr. Ir. Abdjad Asih Nawangsih, M.Si
NIP 19650621 198910 2 001
Mengetahui
Ketua Departemen Proteksi Tanaman
Dr. Ir. Dadang, M.Sc
NIP 19640204 199002 1 002
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, pada tanggal 7 Agustus 1988. Penulis adalah
anak tunggal dari pasangan Joko Susilo (alm) dan Neneng Masani. Penulis
memulai pendidikan formalnya di TK Elsyifa Ciganjur, lalu melanjutkan ke
jenjang Sekolah Dasar di MI Hidayatul Anam Jakarta pada tahun 1999. Penulis
melanjutkan pendidikan menengah pertama di SLTP Negeri 218 pada tahun 1999
– 2002 dan menamatkan pendidikan lanjutan tingkat atas di SMA Negeri 38
Jakarta pada tahun 2005. Pada tahun yang sama, penulis diterima di Institut
Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasisawa Baru (SPMB).
Kemudian pada tahun 2006, penulis menjadi mahasiswa pada Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas rahmat dan
hidayah-Nya sehingga skripsi yang berjudul ”Seleksi dan Karakterisasi Bakteri
Endofit untuk Menekan Kejadian Penyakit Layu Bakteri (Ralstonia
solanacearum) pada Tanaman Tomat” ini dapat diselesaikan dengan baik.
Dalam penyusunan skripsi ini penulis banyak mendapat bantuan dari
berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih yang
sebesar-besarnya kepada :
1. Orang tua penulis, ibunda Neneng Masani serta ayahanda Joko Susilo
(alm) dan Suparman yang telah memberikan dukungan baik secara moril
maupun materil dalam penyusunan skripsi ini.
2. Dr. Ir. Abdjad Asih Nawangsih, M.Si selaku dosen pembimbing skripsi
yang telah telah banyak meluangkan waktunya memberikan bimbingan,
saran, motivasi dan pengarahan kepada penulis.
3. Dr. Ir. Dadan Hindayana sebagai dosen penguji yang telah memberikan
tambahan masukan untuk menyempurnakan isi skripsi ini.
4. Nenek dan kakek tercinta serta keluarga besar lainnya yang telah
memberikan dukungan moril kepada penulis.
5. I Made Rajiv Permadi yang telah memberikan semangat dan bantuan
mulai dari pelaksanaan penelitian hingga penyelesaian skripsi ini.
6. Teman-teman satu bimbingan yaitu Methy, Fitriani, Hakim serta
teman-teman dalam satu laboratorium bakteriologi tumbuhan yang tidak dapat
disebutkan satu persatu.
7. Seluruh staf dan rekan-rekan di lingkungan Departemen Protesi Tanaman.
8. Damar, Memes, Yanti, Uli Khusna, Hardi, Triva, Tety, Farah, Kadek, kak
Ujang, Huda, pak Mput serta pihak-pihak lain yang tidak bisa disebutkan
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh
karena itu kritik dan saran sangat diharapkan. Semoga skripsi ini dapat bermanfaat
bagi pembaca, khususnya dalam bidang proteksi tanaman.
Bogor, Februari 2010
DAFTAR ISI
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 3
Hipotesis ... 3
Manfaat Penelitian ... 3
TINJAUAN PUSTAKA ... 4
Arti Penting Tanaman Tomat ... 4
Penyakit Layu Bakteri pada Tomat oleh Ralstonia solanacearum... 4
Pengendalian Biologi (Biological control) ... 6
Rhizobakteri Pemacu Pertumbuhan Tanaman (PGPR) ... 7
Bakteri Endofit sebagai Agens Hayati ... 8
BAHAN DAN METODE ... 11
Tempat dan Waktu Penelitian ... 11
Bahan dan Alat ... 11
Metode Penelitian ... 11
Isolasi dan pemeliharaan bakteri endofit ... 11
Isolasi bakteri patogen (R. solanacearum) ... 13
Peremajaan bakteri endofit, patogen dan PGPR ... 13
Penyiapan suspensi dan penentuan konsentrasi bakteri endofit, patogen dan PGPR ... 14
Uji hipersensitif ... 14
Uji antagonis secara in vitro... 14
Uji in planta... 15
Karakterisasi bakteri endofit... 17
Analisis data ... 18
HASIL DAN PEMBAHASAN ... 19
Isolasi Bakteri Endofit Asal Bogor, Cipanas dan Lembang ... 19
Uji Reaksi Hipersensitif ... 20
Uji Penghambatan Pertumbuhan R. solanacearum secara in vitro ... 22
Metode dual culture ... 22
Uji penghambatan pertumbuhan R. solanacearum pada media cair ... 24
Keefektifan Bakteri Endofit dalam Menekan Kejadian Penyakit Layu Bakteri dan Kemampuan Pemacu Pertumbuhan Tanaman ... 27
Kejadian penyakit (KP) ... 27
Karakterisasi Bakteri Endofit ... 31
KESIMPULAN DAN SARAN ... 33
Kesimpulan ... 33
Saran ... 33
DAFTAR PUSTAKA ... 34
DAFTAR TABEL
1 Jumlah bakteri endofit yang berhasil diisolasi dari tanaman tomat
sehat dan mekanisme antibiosis yang dihasilkan ... 19 2 Daftar kode isolat bakteri endofit ... 20 3 Sifat patogenisitas isolat-isolat bakteri endofit asal Bogor,
Cipanas dan Lembang ... 21 4 Rerata diameter zona hambatan yang dihasilkan oleh isolat-isolat
kandidat agens hayati pada media King’s B agar... 23 5 Karakteristik isolat-isolat bakteri endofit yang digunakan dalam
pengujian kemampuan penghambatan populasi R. Solanacearum
pada King,s B cair ... 26 6 Pengaruh aplikasi bakteri endofit terhadap kejadian penyakit layu
bakteri R. Solanacearum pada tanaman tomat ... 27 7 Pengaruh aplikasi bakteri endofit terhadap tinggi tanaman tomat .... 30 8 Karakter fisiologi dan biokimia beberapa jenis bakteri endofit
SELEKSI DAN KARAKTERISASI BAKTERI ENDOFIT
UNTUK MENEKAN KEJADIAN PENYAKIT LAYU BAKTERI
(Ralstonia solanacearum) PADA TANAMAN TOMAT
IKA DAMAYANTI
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
ABSTRAK
IKA DAMAYANTI. Seleksi dan Karakterisasi Bakteri Endofit untuk Menekan Kejadian Penyakit Layu Bakteri (Ralstonia solanacearum) pada Tanaman Tomat. Dibimbing oleh ABDJAD ASIH NAWANGSIH.
Ralstonia solanacearum merupakan salah satu bakteri penyebab layu pada tanaman tomat. Tanaman yang terserang menunjukkan gejala layu mendadak bahkan dapat menimbulkan kematian. Penelitian ini bertujuan untuk mengetahui keragaman jenis bakteri endofit yang ada dalam batang tanaman tomat sehat dan menseleksi bakteri endofit tersebut sebagai kandidat agens hayati dan pemacu pertumbuhan tanaman tomat. Bakteri endofit diisolasi dari batang tanaman tomat sehat yang berasal dari wilayah Bogor, Cipanas dan Lembang, kemudian diseleksi keefektifannya dalam menghambat populasi R.solanacearum dengan metode dual culture berdasarkan pembentukan zona penghambatan. Isolat bakteri endofit yang tidak menghasilkan zona hambatan kemudian diuji kemampuan penekanannya dalam media cair. Masing-masing tiga jenis isolat bakteri endofit yang memberikan penekanan terbaik berdasarkan kedua pengujian tersebut, yaitu yang memiliki diameter zona hambatan terbesar dan penekanan populasi
SELEKSI DAN KARAKTERISASI BAKTERI ENDOFIT
UNTUK MENEKAN KEJADIAN PENYAKIT LAYU BAKTERI
(Ralstonia solanacearum) PADA TANAMAN TOMAT
IKA DAMAYANTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Pertanian
pada Departemen Proteksi Tanaman
Fakultas Pertanian
di Insitut Pertanian Bogor
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul : Seleksi dan Karakterisasi Bakteri Endofit untuk
Menekan Kejadian Penyakit Layu Bakteri (Ralstonia
solanacearum) pada Tanaman Tomat
Nama : Ika Damayanti
NRP : A34050855
Menyetujui
Pembimbing
Dr. Ir. Abdjad Asih Nawangsih, M.Si
NIP 19650621 198910 2 001
Mengetahui
Ketua Departemen Proteksi Tanaman
Dr. Ir. Dadang, M.Sc
NIP 19640204 199002 1 002
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, pada tanggal 7 Agustus 1988. Penulis adalah
anak tunggal dari pasangan Joko Susilo (alm) dan Neneng Masani. Penulis
memulai pendidikan formalnya di TK Elsyifa Ciganjur, lalu melanjutkan ke
jenjang Sekolah Dasar di MI Hidayatul Anam Jakarta pada tahun 1999. Penulis
melanjutkan pendidikan menengah pertama di SLTP Negeri 218 pada tahun 1999
– 2002 dan menamatkan pendidikan lanjutan tingkat atas di SMA Negeri 38
Jakarta pada tahun 2005. Pada tahun yang sama, penulis diterima di Institut
Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasisawa Baru (SPMB).
Kemudian pada tahun 2006, penulis menjadi mahasiswa pada Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas rahmat dan
hidayah-Nya sehingga skripsi yang berjudul ”Seleksi dan Karakterisasi Bakteri
Endofit untuk Menekan Kejadian Penyakit Layu Bakteri (Ralstonia
solanacearum) pada Tanaman Tomat” ini dapat diselesaikan dengan baik.
Dalam penyusunan skripsi ini penulis banyak mendapat bantuan dari
berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih yang
sebesar-besarnya kepada :
1. Orang tua penulis, ibunda Neneng Masani serta ayahanda Joko Susilo
(alm) dan Suparman yang telah memberikan dukungan baik secara moril
maupun materil dalam penyusunan skripsi ini.
2. Dr. Ir. Abdjad Asih Nawangsih, M.Si selaku dosen pembimbing skripsi
yang telah telah banyak meluangkan waktunya memberikan bimbingan,
saran, motivasi dan pengarahan kepada penulis.
3. Dr. Ir. Dadan Hindayana sebagai dosen penguji yang telah memberikan
tambahan masukan untuk menyempurnakan isi skripsi ini.
4. Nenek dan kakek tercinta serta keluarga besar lainnya yang telah
memberikan dukungan moril kepada penulis.
5. I Made Rajiv Permadi yang telah memberikan semangat dan bantuan
mulai dari pelaksanaan penelitian hingga penyelesaian skripsi ini.
6. Teman-teman satu bimbingan yaitu Methy, Fitriani, Hakim serta
teman-teman dalam satu laboratorium bakteriologi tumbuhan yang tidak dapat
disebutkan satu persatu.
7. Seluruh staf dan rekan-rekan di lingkungan Departemen Protesi Tanaman.
8. Damar, Memes, Yanti, Uli Khusna, Hardi, Triva, Tety, Farah, Kadek, kak
Ujang, Huda, pak Mput serta pihak-pihak lain yang tidak bisa disebutkan
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh
karena itu kritik dan saran sangat diharapkan. Semoga skripsi ini dapat bermanfaat
bagi pembaca, khususnya dalam bidang proteksi tanaman.
Bogor, Februari 2010
DAFTAR ISI
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 3
Hipotesis ... 3
Manfaat Penelitian ... 3
TINJAUAN PUSTAKA ... 4
Arti Penting Tanaman Tomat ... 4
Penyakit Layu Bakteri pada Tomat oleh Ralstonia solanacearum... 4
Pengendalian Biologi (Biological control) ... 6
Rhizobakteri Pemacu Pertumbuhan Tanaman (PGPR) ... 7
Bakteri Endofit sebagai Agens Hayati ... 8
BAHAN DAN METODE ... 11
Tempat dan Waktu Penelitian ... 11
Bahan dan Alat ... 11
Metode Penelitian ... 11
Isolasi dan pemeliharaan bakteri endofit ... 11
Isolasi bakteri patogen (R. solanacearum) ... 13
Peremajaan bakteri endofit, patogen dan PGPR ... 13
Penyiapan suspensi dan penentuan konsentrasi bakteri endofit, patogen dan PGPR ... 14
Uji hipersensitif ... 14
Uji antagonis secara in vitro... 14
Uji in planta... 15
Karakterisasi bakteri endofit... 17
Analisis data ... 18
HASIL DAN PEMBAHASAN ... 19
Isolasi Bakteri Endofit Asal Bogor, Cipanas dan Lembang ... 19
Uji Reaksi Hipersensitif ... 20
Uji Penghambatan Pertumbuhan R. solanacearum secara in vitro ... 22
Metode dual culture ... 22
Uji penghambatan pertumbuhan R. solanacearum pada media cair ... 24
Keefektifan Bakteri Endofit dalam Menekan Kejadian Penyakit Layu Bakteri dan Kemampuan Pemacu Pertumbuhan Tanaman ... 27
Kejadian penyakit (KP) ... 27
Karakterisasi Bakteri Endofit ... 31
KESIMPULAN DAN SARAN ... 33
Kesimpulan ... 33
Saran ... 33
DAFTAR PUSTAKA ... 34
DAFTAR TABEL
1 Jumlah bakteri endofit yang berhasil diisolasi dari tanaman tomat
sehat dan mekanisme antibiosis yang dihasilkan ... 19 2 Daftar kode isolat bakteri endofit ... 20 3 Sifat patogenisitas isolat-isolat bakteri endofit asal Bogor,
Cipanas dan Lembang ... 21 4 Rerata diameter zona hambatan yang dihasilkan oleh isolat-isolat
kandidat agens hayati pada media King’s B agar... 23 5 Karakteristik isolat-isolat bakteri endofit yang digunakan dalam
pengujian kemampuan penghambatan populasi R. Solanacearum
pada King,s B cair ... 26 6 Pengaruh aplikasi bakteri endofit terhadap kejadian penyakit layu
bakteri R. Solanacearum pada tanaman tomat ... 27 7 Pengaruh aplikasi bakteri endofit terhadap tinggi tanaman tomat .... 30 8 Karakter fisiologi dan biokimia beberapa jenis bakteri endofit
DAFTAR GAMBAR
1 Hasil pengujian keefektifan sterilisasi permukaan dengan cara
menggulirkan potongan batang pada permukaan medium NA;
sterilisasi belum sempurna dengan adanya pertumbuhan bakteri (a),
sterilisasi sudah sempurna (b) ... 12
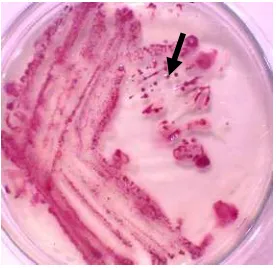
2 Biakan murni R. solanacearum pada medium TZC; koloni tunggal
yang virulen (tanda panah) bagian tengah berwarna merah muda
dikelilingi lendir berwarna putih ... 13
3 Gejala uji HR positif, bagian daun yang disuntik mengalami
nekrosis (tanda panah) ... 22
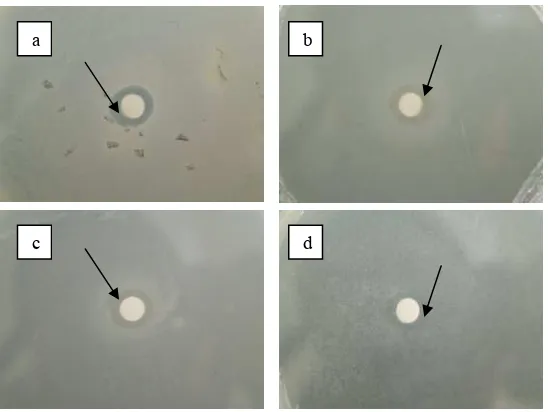
4 Berbagai macam zona hambatan (tanda panah) yang dihasilkan oleh
beberapa bakteri endofit; isolat BC4 (a), isolat AC8 (b), isolat BC5 (c)
dan isolat BC10 (d)... 24
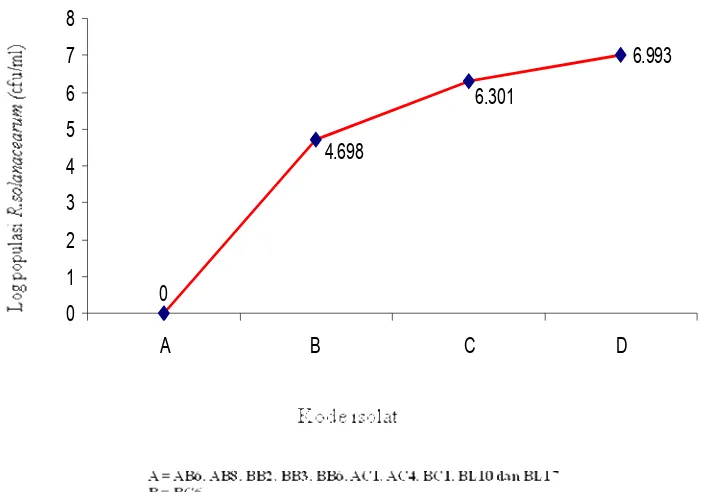
5 Grafik hubungan antara log populasi R. solanacearum dengan isolat
bakteri endofit ... 25
6 Gejala penyakit layu bakteri pada tomat, perbandingan tanaman
sehat dan sakit (a), daun bagian bawah layu dan terkulai (b), terbentuk
akar adventif (tanda panah) (c) serta batang tanaman tumbuh
tinggi dan kurus (d) ... 29
7 Bentuk pertumbuhsn isolat bakteri endofit yang digunakan dalam
pengujian secara in planta; AC1 (a), BC4 (b), BC5 (c), BC10 (d),
DAFTAR LAMPIRAN
1 Hasil analisis ragam kejadian penyakit layu bakteri pada tanaman
tomat pada pengamatan 4 - 6 MST ... 37
2 Hasil analisis ragam pertumbuhan tinggi tanaman tomat pada
pengamatan 2 - 6 MST ... 38
3 Karakter morfologi isolat bakteri endofit yang digunakan dalam
pengujian secara in planta ... 39
4 Persiapan media tanam; tanah dan kompos dicampur sebelum
disterilisasi (a), sterilisasi media tanam (b) dan (c), pencampuran
media tanam steril dengan suspensi R. solanacearum (d)... 40
5 Penyemaian benih tomat pada pot tray (a), bibit tanaman yang
direndam dalam suspensi bakteri endofit (b)... 41
6 Keadaan pertanaman tomat di rumah kaca... 42
7 Pertumbuhan tanaman tomat setelah diaplikasikan dengan bakteri
endofit... 42
8 Gejala penyakit layu bakteri : terbentuk akar adventif (a) dan
PENDAHULUAN
Latar Belakang
Tomat merupakan salah satu tanaman hortikultura yang penting di
Indonesia. Buahnya dapat dikonsumsi dengan berbagai cara, antara lain dimakan
secara langsung, diolah menjadi jus buah, sebagai pelengkap bumbu dapur dan
sebagainya. Tomat kaya akan vitamin C, vitamin A, zat besi (Fe) dan potasium
(Supriati & Siregar 2009). Tanaman ini dapat ditanam di berbagai daerah dengan
ketinggian tempat yang beragam, mulai dari dataran rendah hingga dataran tinggi.
Menurut BPS (2006) dari data Dirjen Bina Hortikultura, produksi tomat nasional
meningkat dari 594.022 ton pada tahun 2002 menjadi 629.743 ton pada tahun
2006.
Selama masa pertumbuhannya, tanaman yang termasuk dalam famili
Solanaceae ini banyak mendapatkan gangguan baik dari hama maupun patogen
tanaman yang dapat menurunkan tingkat produksinya. Penyakit penting yang
sering menyerang adalah penyakit layu bakteri yang disebabkan oleh Ralstonia
solanacearum (Djafruddin 2004; Semangun 2004; Pracaya 2007). Penyakit layu
telah lama dikenal sebagai penyakit yang paling merugikan tanaman cabai dan
tomat yang dilaporkan pada tahun 1921 dan 1922 di Madiun dan Kediri (Van Hall
1922; 1923 dalam Semangun 2004) serta Irian Jaya (Anonim 1987, 1988dalam
Semangun 2004). Patogen ini merupakan bakteri penyebab penyakit yang cukup
penting di daerah tropis, subtropis dan daerah bersuhu hangat (Jeung et al. 2007)
serta menyerang lebih dari 50 famili tanaman (Denny & Hayward 2001), seperti
tomat, kentang, lada, tembakau, terung, pisang, jahe dan kacang (Jeung et al.
2007; Walker 1957; Aeny 2001; Handayani 2005).
R. solanacearum menyebar melalui air tanah, benih yang terinfeksi atau
terkontaminasi, luka yang terbentuk pada saat pemindahan tanaman, melalui
alat-alat pertanian yang terkontaminasi (Denny & Hayward 2001), dengan bantuan
nematoda penghuni akar dalam penetrasinya (Walker 1957) serta lubang alami
atau stomata (Handayani 2005). Patogen menginfeksi pada bagian akar, bergerak
secara sistemik melalui xylem, berpindah menuju ruang antar sel (Walker 1957)
dengan menghasilkan polimer sakarida yang dapat menyumbat jaringan hingga
menyebabkan tanaman menjadi layu (Walker 1957). Tanaman tomat yang
terinfeksi patogen ini menyebabkan daun menjadi terkulai ke bawah (layu) dan
sistem pembuluh menjadi coklat, batang tanaman akan terus tumbuh tinggi dan
kurus (Walker 1957), terbentuk lebih banyak akar adventif di permukaan batang
(Walker 1957) sampai pada ruas tempat terbentuknya bunga pertama (Semangun
2004).
Berbagai pengendalian yang telah dilakukan antara lain kimia seperti
penggunaan bakterisida, penggunaan varietas yang resisten dan prosedur sanitasi
lahan (Sigee 1993), pengapuran pada lahan terinfestasi, rotasi tanaman dengan
tanaman non-Solanaceae (Wiryanta 2002 dalam Khoirunnisya 2009), menanam
tanaman dari varietas yang resisten terhadap penyakit layu bakteri dan mencabut
tanaman terserang (Tim Bina Karya Tani 2008 dalam Khoirunnisya 2009) serta
pengendalian hayati menggunakan Bacillus subtilis (Nawangsih 2006),
Pseudomonas fluorescens (Nawangsih 2006; Ratdiana 2007).
Selain pengendalian di atas, pada dasawarsa terakhir diketahui bahwa
bakteri endofit yang biasa bersimbiosis dengan tanaman juga dapat menjadi
sumber strain yang menjanjikan dibandingkan dengan bakteri rizosfer karena
kurangnya kompetisi dengan bakteri lain dalam apoplast (Sigee 1993). Hubungan
simbiosis antara bakteri endofit dengan tanaman dapat bersifat netral, mutualisme
atau komensalisme (Bacon & Hinton 2006). Bakteri endofit mendapatkan nutrisi
dari hasil metabolisme tanaman dan memproteksi tanaman dalam melawan
patogen, sedangkan tanaman mendapatkan derivat nutrisi dan senyawa aktif yang
diperlukan selama hidupnya ( Tanaka et al. 1999 dalam Simarmata et al. 2007).
Cara kerja bakteri endofit sebagai agens pengendali hayati antara lain :
memproduksi bahan campuran anti mikroba; kompetisi ruang dan nutrisi;
kompetisi mikro nutrisi seperti zat besi dan produksi siderofor; serta dapat
menyebabkan tanaman inang menjadi resisten (Bacon & Hinton 2006).
Keanekaragaman spesies bakteri endofit merefleksikan banyaknya cara kerja yang
mungkin terjadi untuk melawan patogen, yang memungkinkan patogen
memproduksi senyawa antibiotik untuk melawan bakteri endofit tersebut (Bacon
bakteri endofit juga dapat berperan sebagai pemacu pertumbuhan tanaman,
terutama yang menghasilkan hormon pertumbuhan seperti etilen, auksin dan
sitokinin (Bacon & Hinton 2006).
Tujuan
Penelitian ini bertujuan untuk mengetahui keragaman jenis bakteri endofit
yang ada dalam batang tanaman tomat sehat dan menseleksi bakteri endofit
tersebut sebagai kandidat agens hayati untuk menekan populasi Ralstonia
solanacearum penyebab layu bakteri secara in vitro dan in planta, serta
mengetahui peranannya sebagai pemacu pertumbuhan tanaman tomat.
Hipotesis
Bakteri endofit dapat menekan populasi Ralstonia solanacearum penyebab
penyakit layu bakteri pada tomat dan dapat berperan sebagai pemacu
pertumbuhan tanaman.
Manfaat
Sebagai salah satu teknik penendalian hayati dalam menekan penyakit
layu bakteri, Ralstonia solanacearum pada tanaman tomat yang ramah
TINJAUAN PUSTAKA
Arti Penting Tanaman Tomat
Tomat (Lycopersicon esculentum Mill.) adalah komoditas hortikultura
yang penting di Indonesia dan merupakan salah satu jenis sayuran yang banyak
digemari orang karena rasanya enak, segar dan sedikit asam (Sihotang 2008) serta
multiguna karena banyak digunakan sebagai sayuran, bumbu masak, buah meja,
penambah nafsu makan, minuman, bahan pewarna makanan, bahan kosmetik,
obat-obatan (Pudjiatmoko 2008), makanan yang diawetkan (saus tomat) dan
minuman (jus) (Sihotang 2008). Menurut BPS (2006) dari data Dirjen Bina
Hortikultura, produksi tomat nasional meningkat dari 594.022 ton pada tahun
2002 menjadi 629.743 ton pada tahun 2006.
Tomat sangat bermanfaat bagi tubuh karena mengandung vitamin dan
mineral yang diperlukan untuk pertumbuhan dan kesehatan (Supriati & Siregar
2009). Sebagai sumber vitamin, tomat kaya akan vitamin C yang berguna untuk
meningkatkan kekebalan tubuh serta mengobati berbagai macam penyakit, seperti
sariawan; vitamin A untuk mencegah dan mengobati xeropthalmia pada mata; zat
besi (Fe) untuk pembentukan sel darah merah; serat untuk membantu penyerapan
makanan dalam pencernaan; serta potasium yang bermanfaat untuk menurunkan
tekanan darah tinggi (Supriati & Siregar 2009).
Tomat termasuk jenis tanaman perdu semusim, berbatang lemah dan
basah, daunnya berbentuk segitiga, bunganya berwarna kuning, hijau waktu muda
dan kuning atau merah waktu tua, berbiji banyak, berbentuk bulat pipih, putih
atau krem serta kulit biji berbulu (Sihotang 2008). Tanaman ini dapat tumbuh
pada ketinggian tempat 0 sampai 1.250 m di atas permukaan laut dengan suhu
optimal untuk pertumbuhannya adalah 23°C pada siang hari dan 17°C pada
malam hari, menyukai tanah dengan tingkat keasaman netral terutama yang
mengandung humus, gembur, sarang dan berdrainase baik (Sihotang 2008).
Penyakit Layu Bakteri pada Tomat oleh Ralstonia solanacearum
Ralstonia solanacearum sebelumnya dikenal dengan Pseudomonas
Pseudomonas (Denny & Hayward 2001) dan mampu hidup dalam tanah untuk
periode yang lama (Walker 1957). Bakteri ini merupakan salah satu bakteri
penyebab penyakit layu yang penting di wilayah tropis, subtropis, dan daerah
beriklim hangat (Jeung et al. 2007). R. solanacearum menyerang ratusan spesies
tanaman (Kaur & Mukerji 1999; Denny & Hayward 2001) dan lebih dari 50
famili (Denny & Hayward 2001), termasuk famili Solanaceae dan tanaman
pertanian lainnya yang bernilai ekonomi, seperti tomat, kentang, lada, tembakau,
terung, pisang, jahe, dan kacang (Jeung et al. 2007; Walker 1957; Aeny 2001;
Handayani 2005). Patogen ini bahkan tidak jarang dapat menyebabkan kematian
pada inangnya (Denny & Hayward 2001).
Penyakit layu telah lama dikenal sebagai penyakit yang paling merugikan
tanaman cabai dan tomat yang dilaporkan pada tahun 1921 dan 1922 di Madiun
dan Kediri (Van Hall 1922, 1923 dalam Semangun 2004) serta Irian Jaya
(Anonim 1987, 1988 dalam Semangun 2004). Kerugian mencapai 80% pada
pertanaman jahe atau bahkan dapat menggagalkan panen (Aeny 2006). Di Taiwan
dilaporkan kehilangan hasil oleh Ralstonia solanacearum berkisar antara 5%
sampai 55% pada musim panas, bahkan di India kehilangan hasil mencapai 10%
sampai 100% (AVRDC 2005 dalam Sasmito 2007).
Sebagai patogen tular tanah, Ralstonia solanacearum menginfeksi pada
bagian akar, bergerak secara sistemik melalui xylem, bersifat nonmotil pada
tanaman, namun pada media pertumbuhan bersifat motil (Kersten et al. 2001) dan
menyebabkan gejala layu yang seringkali hingga letal (Denny & Hayward 2001).
Bakteri menyebar melalui air tanah, benih yang terinfeksi atau terkontaminasi,
luka yang terbentuk pada saat pemindahan tanaman, melalui alat-alat pertanian
yang terkontaminasi (Denny & Hayward 2001), dengan bantuan nematoda
penghuni akar dalam penetrasinya (Walker 1957) serta lubang alami atau stomata
(Handayani 2005).
Agrios (2005) mengemukakan bahwa bakteri masuk dalam pembuluh
xylem dan menyebar ke seluruh bagian tanaman. Dari jaringan xylem bakteri
berpindah menuju ruang antar sel (Walker 1957) dari parenkim di dalam korteks
dan jaringan gabus, kemudian merusak dinding sel dengan menghasilkan polimer
layu (Walker 1957). Sel-sel tanaman yang rusak tersebut kemudian terisi dengan
masa lunak bakteri (ooze) dan sisa-sisa sel tanaman sehingga menyebabkan
terhambatnya translokasi hara dan mineral dari dalam tanah. Respon fisiologi dari
perubahan inang tergantung tingkat serangannya (Walker 1957). Tanaman tomat
yang terinfeksi patogen ini menyebabkan daun menjadi terkulai ke bawah (layu)
dan sistem pembuluh menjadi coklat, batang tanaman akan terus tumbuh tinggi
dan kurus (Walker 1957), terbentuk lebih banyak akar adventif di permukaan
batang (Walker 1957) sampai pada ruas tempat terbentuknya bunga pertama
(Semangun 2004).
Jika batang, cabang, atau tangkai daun dibelah akan tampak berkas
pembuluh berwarna coklat, empulur sering juga berwarna kecoklatan (Anonim
1976 dalam Semangun 2004). Pada stadium penyakit yang lanjut, bila batang
dipotong, dari berkas pembuluh akan keluar massa bakteri seperti lendir berwarna
putih susu. Lendir akan lebih banyak keluar bila potongan batang ditaruh di
tempat yang lembab. Jika potongan batang sakit dimasukkan ke dalam gelas yang
berisi air jernih, setelah ditunggu beberapa menit akan terlihat benang-benang
putih halus, yang akan putus bila gelas digoyang. Benang putih tersebut adalah
massa bakteri. Adanya massa lendir ini dapat dipakai untuk membedakan
penyakit layu bakteri dengan layu fusarium. Karena adanya lendir ini penyakit
layu bakteri sering juga disebut “penyakit lendir” (Semangun 2004).
Pengendalian Biologi (Biological control)
Menurut Cook & Baker (1974dalam Yudiarti 2007) pengendalian biologi
adalah pengurangan inokulum atau aktivitas patogen penghasil penyakit atau
parasit baik dalam bentuk dorman dengan satu atau banyak organisme yang
dilakukan secara alami atau dengan cara memanipulasi lingkungan, inang, atau
antagonis. Aktivitas penghasil penyakit yang dimaksud yaitu : pertumbuhan,
kemampuan menginfeksi, keganasan patogen atau akivitas penghasil penyakit,
atau dapat pula berupa proses dari infeksi, perkembangan gejala dan reproduksi
patogen. Sedangkan menurut Subagiya (2006 dalam Sasmito 2007), pengendalian
hayati pada dasarnya adalah usaha untuk memanfaatkan dan menggunakan musuh
memanfaatkan hubungan antagonis antara patogen dan inang baik secara langsung
(antibiosis, kompetisi, parasitisme) maupun secara tidak langsung (introduksi
mikroorganisme) (Janse 2005).
Di dalam pengendalian secara biologi terdapat beberapa komponen antara
lain : organisme patogen, organisme antagonis, agen biologi yang berpotensi
untuk mengganggu proses kehidupan dari patogen tanaman; Inang, berperan
secara langsung untuk menekan atau mengakhiri patogenesis atau reproduksi dari
patogen dengan berbagai mekanisme ketahanan tanaman (Cook & Baker 1974
dalam Yudiarti 2007).
Berbeda dengan pengendalian kimia, pengendalian secara biologi sangat
potensial dengan sasaran yang spesifik, yaitu patogen, tidak merusak lingkungan,
dan tidak menimbulkan efek fitotoksisitas (Sigee 1993).
Rizobakteri Pemacu Pertumbuhan Tanaman (PGPR)
Rhizobakteri pemacu pertumbuhan tanaman atau Plant Growth Promoting
Rhizobacteria (PGPR) adalah kelompok bakteri menguntungkan yang agresif
menduduki (mengkolonisasi) rizosfer (lapisan tanah tipis dengan ketebalan 1-2
mm di sekitar zona perakaran) (Husein at al. 2007), berperan penting dalam
meningkatkan pertumbuhan tanaman (Podile & Kishore 2006), perlindungan hasil
panen, meningkatakan kesuburan lahan (Wahyudi 2009), sebagai tambahan bagi
kompos serta mempercepat proses pengomposan (Irmawan 2008). Secara
langsung, PGPR merangsang pertumbuhan tanaman dengan menghasilkan
hormon pertumbuhan, kelarutan fosfat anorganik (Podile & Kishore 2006) dan
meningkatkan asupan nutrisi (Wahyudi 2009). Pertumbuhan tanaman ditingkatkan
secara tidak langsung karena PGPR menghasilkan senyawa anti mikroba yang
menekan pertumbuhan populasi patogen penyebab penyakit tumbuhan dan
mikroorganisme lain yang dapat merusak lingkungan rizosfer (Wahyudi 2009;
Podile & Kishore 2006). Strain PGPR yang telah dikenal secara luas yaitu
Pseudomonas sp dan Bacillus sp. (Wahyudi 2009).
Menurut Irmawan (2008), Aplikasi PGPR mampu mengurangi kejadian
dan keparahan penyakit. Beberapa bakteri PGPR yang diinokulasikan pada benih
yang membuat bakteri PGPR mampu mengurangi keparahan dari penyakit
dumping-off (Pythium ultimum) di tanaman. Beberapa bakteri PGPR mampu
memproduksi racun bagi patogen tanaman, misalnya bakteri Bacillus subtilis
mampu melawan cendawan patogen. Kelebihan lain dari PGPR diantaranya :
menambah fiksasi nitrogen di tanaman kacang-kacangan; memacu pertumbuhan
bakteri fiksasi nitrogen bebas; meningkatkan ketersediaan nutrisi lain seperti
phospat, belerang, besi dan tembaga; memproduksi hormon tanaman; menambah
bakteri dan cendawan yang menguntungkan, mengontrol hama dan penyakit
tumbuhan dengan memproduksi siderofor, kitinase, selulase, antibiotika, sianida
(Soesanto 2008).
Penerapan PGPR pada rizosfer sangat dikaitkan dengan kemampuannya
mengkoloni perakaran tanaman. PGPR harus mampu menyelubungi sepanjang
permukaan akar. Karena keaktifan pengkolonian akar tersebut, akar menyerap
produk mikroba yang secara langsung mempengaruhi pertumbuhan dan fisiologi
akar, disamping mempengaruhi invasi patogen (Soesanto 2008).
PGPR juga memiliki beberapa kekurangan, seperti : kekonsistenan
pengaruh bakteri PGPR di laboratorium dengan di lapangan kadang-kadang
berbeda, bakteri ini harus dapat diperbanyak dan diproduksi dalam bentuk yang
optimum baik vialibilas maupun biologinya selama diaplikasikan di lapangan, dan
beberapa bakteri PGPR harus dilakukan reinokulasi setelah diaplikasikan di
lapangan seperti Rhizobia. Tantangan lainnya berkaitan dengan regulasi atau
kebijakan suatu negara. Di beberapa negara, kontrol terhadap produksi agens
antagonis ini sangat ketat, walaupun produk tersebut tidak berefek negatif pada
manusia (Irmawan 2008).
Bakteri Endofit sebagai Agens Hayati
Menurut Bacon & Hinton (2006), bakteri endofit adalah bakteri yang
mengkolonisasi jaringan tanaman sehat tanpa menyebabkan gejala atau luka pada
inangnya. Bakteri ini juga dapat hidup pada bagian tanaman seperti akar, batang,
daun dan buah (Simarmata et al. 2007; Bacon & Hinton 2006). Keberadaannya
terjadi secara alami, dapat berasosiasi dengan tanaman dalam jangka waktu yang
2006). Oleh karena itu, bakteri endofit hanya dapat dideteksi dengan mengisolasi
pada media agar, namun jumlahnya tidak dapat ditentukan secara pasti (Bacon &
Hinton 2006). Bakteri endofit dapat bersifat obligat ataupun fakultatif dalam
mengkolonisasi inangnya. Meskipun bakteri ini memiliki kisaran inang yang luas,
namun ada beberapa bakteri endofit yang hanya dapat berasosiasi dengan inang
dari famili tertentu (Bacon & Hinton 2006). Simbiosis antara tanaman dengan
bakteri endofit bersifat netral, mutualisme atau komensalisme (Bacon & Hinton
2006). Simbiosis mutualisme antara bakteri endofit dan tanaman, dalam hal ini
bakteri endofit mendapatkan nutrisi dari hasil metabolisme tanaman dan
memproteksi tanaman dalam melawan patogen, sedangkan tanaman mendapatkan
derivat nutrisi dan senyawa aktif yang diperlukan selama hidupnya ( Tanaka et al.
1999 dalam Simarmata et al. 2007).
Bakteri endofit mengkolonisasi relung hidup yang sama dengan patogen
tetapi tidak menimbulkan kerusakan pada inangnya (Sigee 1993). Bakteri ini
dapat berperan sebagai agens pengendali hayati jika bakteri endofit telah
berasosiasi dengan tanaman sebelum patogen menyerang tanaman tersebut (Bacon
& Hinton 2006). Cara kerja bakteri endofit sebagai agens pengendali hayati antara
lain : memproduksi bahan campuran anti mikroba; kompetisi ruang dan nutrisi;
kompetisi mikro nutrisi seperti zat besi dan produksi siderofor; serta dapat
menyebabkan tanaman inang menjadi resisten (Bacon & Hinton 2006).
Keanekaragaman spesies bakteri endofit merefleksikan banyaknya cara kerja yang
mungkin terjadi untuk melawan patogen, yang memungkinkan patogen
memproduksi senyawa antibiotik untuk melawan bakteri endofit tersebut (Bacon
& Hinton 2006).
Selain sebagai agens pengendali hayati, hampir semua spesies bakteri
endofit juga dapat berperan sebagai pemacu pertumbuhan tanaman, terutama yang
menghasilkan hormon pertumbuhan seperti etilen, auksin dan sitokinin (Bacon &
Hinton 2006). Bakteri ini juga dapat meningkatkan kandungan zat besi dalam
tanah, fosfor dan nitrogen bagi tanaman (Bacon & Hinton 2006). Menurut Xu,
Griffith, Patten, & Glick (1998 dalam Bacon & Hinton 2006), efek dari
pertumbuhan tanaman tidak terjadi secara langsung. Jika ada patogen yang
daripada memacu pertumbuhan. Mekanisme kerja seperti ini juga terjadi jika
terjadi tekanan abiotik pada tanaman seperti saat musim kering atau musim
dingin. Lazarovits et al. (1997 dalam Bacon & Hinton 2006) menambahkan,
bakteri endofit secara tidak langsung dapat memacu pertumbuhan tanaman
dengan menambah jumlah produksi fitohormon dan ketersediaan mineral.
Beberapa contoh bakteri endofit yang bersifat antagonis terhadap patogen
diantaranya : Bacillus subtilis, mampu menekan penyakit layu bakteri oleh
Ralstonia solanacearum; Pseudomonas fluorescens; Pseudomonas putida, mampu
menekan pertumbuhan patogen tular tanah; Agrobacterium radiobacter, mampu
mengendalikan Agrobacterium tumifaciens secara efektif; Erwinia Herbicola,
untuk mengendalikan penyakit pascapanen; Serratia marcescens, menghasilkan
prodigiosin yang efektif untuk mengendalikan nematoda Caenorhabditis elegans
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan dan Rumah
Kaca University Farm, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut
Pertanian Bogor. Penelitian dimulai dari bulan Mei sampai Desember 2009.
Bahan dan Alat
Bakteri endofit yang digunakan dalam penelitian ini diisolasi dari batang
tanaman tomat sehat yang berada di wilayah Bogor, Cipanas dan Lembang.
Sebagai pembanding dalam pengujian, digunakan isolat PGPR antara lain
Pseudomonas fluorescens RH4003, Bacillus cereus L32 dan Bacillus Subtilis
AB89, yang merupakan koleksi Laboratorium Bakteriologi Tumbuhan,
Departemen Ptoteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor.
Selain itu, digunakan pula bakteri patogen Ralstonia solanacearum yang diisolasi
dari tanaman tomat yang terserang layu bakteri pada areal pertanaman tomat di
Bogor. Benih tomat yang digunakan untuk pengujian di lapangan yaitu varietas
Arthaloka, yang disemai pada pot tray berukuran 30 cm x 50 cm dengan 50
lubang tanam, selanjutnya dipindah tanam pada polybag berdiameter 20 cm.
Media tanam yang digunakan yaitu campuran antara pupuk kompos dan tanah
steril dengan perbandingan 1:1.
Metode Penelitian
Isolasi dan pemeliharaan bakteri endofit
Sumber bakteri endofit berasal dari tanaman tomat sehat yang berada di
daerah Bogor, Cipanas dan Lembang. Sampel tanaman sehat yang dipilih yaitu
yang berada diantara tanaman tomat yang terserang parah layu bakteri.
Selanjutnya tanaman dibersihkan dengan air mengalir hingga bersih,
dipotong-potong sepanjang 5 cm dengan memisahkan batang bagian bawah dan atas.
Potongan batang tersebut kemudian disterilisasi permukaan dengan merendamnya
alkohol 70% selama tiga puluh detik, lalu dibilas dengan aquades steril sebanyak
dua kali dan dikeringkan menggunakan kertas saring steril. Setelah batang kering,
ujung-ujung batang dibakar dengan spirtus dan dipotong masing-masing
sepanjang satu sentimeter pada kedua ujungnya. Bagian tengah dihaluskan pada
mortar steril dan diencerkan dengan larutan buffer fosfat (PBS) sebanyak 5 ml.
Suspensi kemudian diencerkan secara berseri hingga 10-5 dan dilakukan
pencawanan (plating) secara duplo masing-masing sebanyak 50 μl pada media
NA (Nutrient Agar). Setelah diinkubasikan pada suhu ruang selama 24-48 jam,
koloni bakteri yang terbentuk masing-masing dipisahkan dan dipindahkan pada
media cawan agar yang baru sehingga diperoleh isolat yang murni. Isolat bakteri
endofit yang telah murni kemudian disimpan pada aquades steril pada suhu ruang
untuk penyimpanan jangka pendek dan pada gliserol 20% dengan suhu -40C untuk
penyimpanan jangka panjang.
Sebagai kontrol, batang yang belum dihaluskan digulirkan pada bagian
tengah media NA dalam cawan petri dan diinkubasikan selama 24-48 jam. Hal ini
dilakukan untuk menguji keefektifan sterilisasi permukaan. Jika terdapat
kontaminasi maka bakteri hasil plating tidak dapat digunakan dan sterilisasi
permukaan harus diulang (Gambar 1).
Gambar 1 Hasil pengujian keefektifan sterilisasi permukaan dengan cara menggulirkan potongan batang pada permukaan medium NA; sterilisasi belum sempurna dengan adanya pertumbuhan bakteri (a), sterilisasi sudah sempurna (b)
[image:34.612.133.503.431.584.2]Isolasi bakteri patogen (Ralstonia solanacearum)
Bakteri patogen yang digunakan berasal dari areal pertanaman tomat yang
terserang layu bakteri. Hal ini dimaksudkan agar bakteri patogen masih memiliki
tingkat virulensi yang tinggi, karena masih fresh sehingga dapat memberikan hasil
yang nyata pada saat pengujian. Ooze yang berasal dari bagian batang bawah
(akar) yang dipotong kemudian disebar pada media TZC dalam cawan petri dan
diinkubasikan selama 48 jam. Bakteri patogen kemudian disimpan pada suhu
ruang dalam aquades steril dan dalam gliserol 20% pada suhu -40C. Koloni
patogen yang digunakan yaitu koloni tunggal berwarna merah muda dan
dikelilingi lendir yang berwarna keputihan seperti pada Gambar 2.
Gambar 2 Biakan murni R. solanacearum pada medium TZC; koloni tunggal yang virulen (tanda panah) bagian tengah berwarna merah muda dikelilingi lendir berwarna putih
Peremajaan bakteri endofit, patogen, dan PGPR
Sebelum digunakan untuk pengujian, bakteri endofit, patogen, dan PGPR
diremajakan terlebih dahulu pada media King’s B Agar. Penandaan bagi tiap
calon bakteri endofit didasarkan atas daerah asal tanaman diambil dan bagian
batang yang diambil ekstraknya. Bakteri PGPR berperan sebagai pembanding
bagi bakteri endofit pada pengujian terhadap bakteri patogen. Agens pembanding
ini berasal dari koleksi ketua peneliti yang diisolasi dari perakaran tomat dan
disimpan dalam gliserol 20%. Bakteri-bakteri PGPR tersebut antara lain
Pseudomonas fluorescens RH4003, Bacillus cereus L32 dan Bacillus subtilis
[image:35.612.246.384.284.418.2]Penyiapan suspensi dan penentuan konsentrasi bakteri endofit, patogen, dan PGPR
Bakteri yang disimpan dalam stok diremajakan pada media King’s B Agar
(KBA) dan diinkubasikan selama 24 jam. Setelah 24 jam, dibuat suspensinya dan
dilakukan pengenceran berseri. Masing-masing hasil pengenceran diambil 100µl
untuk diplating secara duplo pada media King’s B Agar dan diinkubasikan selama
24 jam. Sisa hasil pengenceran diukur nilai absorbansinya dengan
spektrofotometer dengan panjang gelombang 560-660 nm. Hasil plating yang
telah diinkubasikan dihitung populasinya (jumlah koloni tunggal) agar diketahui
kerapatan populasinya.
Uji hipersensitif
Uji hipersensitif bakteri endofit dilakukan untuk mengetahui patogenesitas
bakteri endofit dengan menggunakan daun tembakau sehat. Suspensi bakteri
endofit disuntikkan pada daun tembakau masing-masing sebanyak 2 ml dengan
tiga kali ulangan untuk setiap bakteri endofit. Kemudian diinkubasi selama 24 jam
sampai 48 jam dan dilakukan pengamatan terhadap perubahan yang terjadi pada
daun tembakau. Bakteri yang menunjukkan reaksi negatif yaitu tidak timbul
gejala nekrosis dapat digunakan untuk pengujian selanjutnya.
Uji antagonis secara in vitro
Pengujian dilakukan dengan metode ”dual culture” dan dalam dua tahap.
Tahap pertama yaitu dengan melihat zone hambatan yang dihasilkan bakteri
endofit pada media King’s B Agar yang mengandung Ralstonia solanacearum.
Tahap kedua, bakteri endofit yang tidak menghasilkan zone hambatan diuji pada
media King’s B cair 10% yang mengandung Ralstonia solanacearum.
Pada tahap pertama, media KBA yang belum padat dengan suhu 500C
sampai 550C dicampurkan dengan 1 ml suspensi Ralstonia solanacearum lalu
divortex dan dituang pada cawan petri. Setelah padat, kertas saring steril yang
telah dicetak berbentuk bulatan kecil diletakkan pada bagian tengah media,
ditetesi dengan suspensi bakteri endofit sebanyak 20 ul dengan kerapatan 108-109
kontrol, di atas kertas saring diteteskan aquades steril sebanyak 20 ul. Sedangkan
untuk pembanding, diteteskan bakteri PGPR masing-masing sebanyak 20 ul.
Kemudian diinkubasikan selama 24 jam sampai 48 jam. Zona bening yang
terbentuk lalu diukur panjang diameternya.
Bakteri endofit yang tidak menghasilkan zona bening kemudian diuji
dengan King’s B cair (KBB) 10%. Sebanyak 50 ml KBB 10% ditambahkan 1 ml
suspensi bakteri endofit dan 1 ml suspensi Ralstonia solanacearum. Sebagai
kontrol, dicampurkan 1 ml aquades steril dan 1 ml suspensi Ralstonia
solanacearum. Kemudian, diinkubasikan pada suhu ruang dan digoyang pada
rotary shaker selama 24 jam. Hasil inkubasi diencerkan secara berseri dengan
metode ”longkang”, yaitu hanya pengenceran genap saja (10-4, 10-6, 10-8) yang
diplating secara duplo pada media KBA dan diinkubasikan selama 24 jam. Setelah
masa inkubasikan, dilakukan perhitungan populasi Ralstonia solanacearum.
Bakteri endofit yang mampu melakukan penekanan paling baik terhadap
Ralstonia solanacearum dan membentuk zone hambatan paling besar akan
digunakan pada pengujian secara in planta.
Uji in planta
Pengujian secara in planta untuk melihat peran bakteri endofit dalam
memacu pertumbuhan tanaman (PGPR) dan kemampuannya menekan kejadian
penyakit layu bakteri oleh Ralstonia solanacearum (sebagai agens antagonis).
Pada pengujian pertama, media tanam pada polybag tidak diinfestasikan
R.solanacearum. Digunakan satu tanaman untuk tiap bakteri endofit dan diulang
sebanyak sepuluh kali. Sedangkan pada pengujian kedua, media tanam pada
polybag diinfestasikan R. solanacearum sebanyak 50 ml untuk tiap polybag dan
digunakan 10 tanaman uji untuk setiap pelakuan dengan tiga kali ulangan.
Terdapat tujuh macam perlakuan, enam diantaranya menggunakan bakteri endofit
dan sebagai kontrol menggunakan aquades steril. Adapun tahapannya sebagai
berikut :
1. Persiapan media tanam dan tanaman uji
Media tanam berupa tanah dan kompos dengan perbandingan 1:1
pada pot tray berukuran 30 cm x 50 cm dengan jumlah lubang tanam
sebanyak 60 lubang. Media tanam yang sudah steril diisikan ke dalam pot
tray untuk kemudian ditanami benih tomat Arthaloka sebanyak empat
benih (biji) per lubang tanam. Bibit yang telah berumur satu minggu
setelah tanam (MST) kemudian dicabut, dibersihkan akarnya, dan
direndam pada suspensi bakteri endofit dan aquades steril untuk kontrol
selam 12-14 jam untuk kemudian dipindahtanamkan ke polybag
berukuran 1 kg. Polybag diisi dengan media tanam steril sekitar 500 gr
atau kira-kira ½ dari tinggi polybag, 250 gr di atasnya media tanam yang
terinfestasi patogen Ralstonia solanacearum, dan ditimbun dengan 250 gr
media tanam steril setelah dilakukan pindah tanam.
2. Persiapan suspensi bakteri patogen dan endofit
Bakteri patogen yang digunakan dalam pengujian kejadian
penyakit (KP) berjumlah enam bakteri dan aquades steril sebagai kontrol.
Tiga macam bakteri dari hasil pengujian zona bening dengan kriteria
panjang diameter zona bening yang lebih besar, pertumbuhan bakteri yang
baik dan cepat, serta berwarna khas. Ketiga bakteri yang lainnya berasal
dari pengujian penghambatan patogen dengan media cair. Adapun kriteria
yang dipilih yaitu mampu memberi penekanan yang besar terhadap
pertumbuhan patogen, berwarna khas, dan bakteri endofit tersebut tumbuh
sangat baik dan cepat. Suspensi bakteri endofit dan Ralstonia
solanacearum yang digunakan untuk perlakuan memiliki kerapatan 109
-1010 cfu/ml. Suspensi patogen yang telah dishaker kemudian diencerkan
sebanyak 10-1 dan dicampurkan pada tanah steril secara merata sebanyak
50 ml untuk tiap polybag. Sedangkan suspensi bakteri endofit digunakan
untuk perendaman bibit sebelum pindah tanam masing-masing direndam
dalam suspensi bervolume 50 ml/bakteri endofit, serta untuk penyiraman
sesaat setelah pindah tanam dengan volume masing-masing 50
ml/tanaman. Suspensi ini sebelumnya diencerkan terlebih dahulu sebanyak
10-1. Bakteri endofit yang digunakan antara lain AC 1, BC 4, BC 5, BC 10,
3. Perlakuan dan pindah tanam
Bibit yang berumur kurang lebih satu minggu setelah tanam (MST)
direndam dengan suspensi bakteri endofit masing-masing 50 ml/bakteri
endofit selama 12-14 jam kemudian dipindahtanamkan pada media tanam
yang berada pada polybag. Media tanam steril digunakan untuk perlakuan
tinggi dan bobot tanaman, sedangkan media tanam yang mengandung R.
solanacearum untuk pengujian kejadian penyakit (KP). Bibit yang telah
dipindahtanamkan lalu disiram dengan suspensi bakteri endofit sesuai
perlakuan masing-masing sebanyak 50ml/tanaman. Setelah itu, dilakukan
pengamatan kejadian penyakit (KP) dan pemacu pertumbuhan (tinggi
tanaman dan bobot basah) setiap minggunya. Jika kejadian penyakit pada
salah satu perlakuan sudah menduduki posisi teratas (paling banyak) untuk
ketiga ulangannya maka pengamatan dihentikan dan pada saat itu bobot
basah tanaman pada pengujian pemacu pertumbuhan ditimbang. Jumlah
tanaman yang digunakan pada pengujian kejadian penyakit yaitu 10
tanaman/perlakuan dengan tiga kali ulangan dan satu tanaman untuk
perlakuan pemacu pertumbuhan dengan ulangan sebanyak sepuluh kali.
Kejadian penyakit (KP) dapat dihitung dengan rumus :
Keterangan :
KP = kejadian penyakit layu bakteri pada tanaman tomat
n = jumlah tanaman yang terserang patogen
N = jumlah tanaman uji untuk tiap ulangan
Karakterisasi bakteri endofit
Pengujian terhadap sifat-sifat fisiologi dan biokimia dilakukan pada empat
macam bakteri endofit (AC1, BC4, BL10 dan BL17) sampai tingkat genus dan
spesies di Laboratorium Bakteriologi Hewan, Departemen Kedokteran Hewan,
Analisis data
Rancangan percobaan yang digunakan adalah Rancangan Acak Kelompok
(RAK) dengan kelompok sebagai ulangan. Kemudian data yang diperoleh
dianalisis menggunakan analisis ragam (anova) dengan menggunakan program
Statistical Analysis System (SAS) versi 9.0 dan dilanjutkan uji DMRT dengan
taraf nyata 5%. Nilai dugaan untuk data hilang diperoleh dengan rumus sebagai
berikut (Gomez & Gomez 1995).
Keterangan :
X = dugaan data yang hilang
t = banyaknya perlakuan
r = banyaknya ulangan
Bo = jumlah nilai pengamatan dari ulangan dimana terdapat data yang
hilang
To = jumlah nilai pengamatan dari perlakuan dimana terdapat data yang
hilang
Go = jumlah umum dari semua pengamatan X = rBo + tTo – Go
HASIL DAN PEMBAHASAN
Isolasi Bakteri Endofit Asal Bogor, Cipanas, dan Lembang
Bakteri endofit yang digunakan dalam penelitian ini berasal dari tiga
tempat yang berbeda dalam satu propinsi Jawa Barat. Bogor, dengan ketinggian
tempat antara 190 m hingga 330 m dpl (Pemkot Bogor 2009) mewakili area
pertanaman tomat dataran rendah; Cipanas dengan ketinggian 850 m dpl (Pemkot
Bogor 2009) mewakili area pertanaman tomat dataran menengah; dan Lembang
dengan ketinggian antara 1.300 m sampai 2.084 m dpl (Pemda Bandung 2009)
mewakili area pertanaman tomat dataran tinggi.
Bakteri endofit yang berhasil diisolasi diberi kode berdasarkan daerah asal
sampel tanaman diambil dan bagian batang yang diisolasi. Sebagai contoh, ”AB”
merupakan isolat bakteri endofit yang diisolasi dari bagian batang atas tanaman
tomat asal Bogor dan ”BB” sebaliknya. Jumlah bakteri endofit yang berhasil
diisolasi sebanyak 49 isolat, 17 diantaranya diisolasi dari tanaman asal Bogor, 18
isolat dari Cipanas, dan 14 isolat dari Lembang. Masing-masing bakteri endofit
memiliki ciri fisik yang berbeda satu sama lain (Tabel 1). Masing-masing bakteri
endofit memiliki ciri fisik yang berbeda satu sama lain.
Tabel 1 Jumlah bakteri endofit yang berhasil diisolasi dari tanaman tomat sehat dan mekanisme antibiosis yang dihasilkan
Asal isolat Jumlah isolat Zona hambatan Tidak ada zona hambatan
Bogor 17 7 10
Cipanas 18 8 10
Lembang 14 2 12
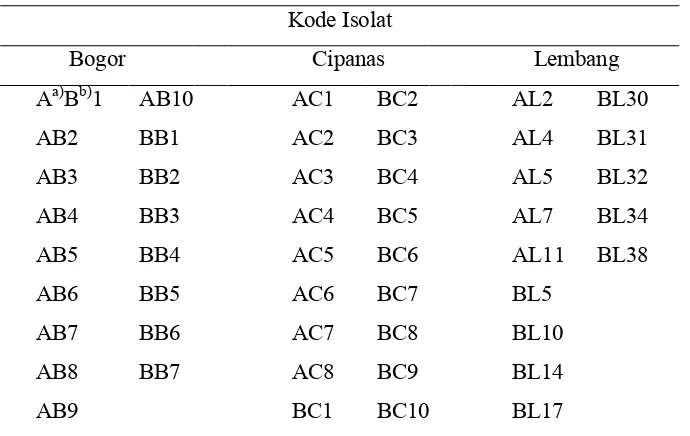
[image:41.612.133.507.479.595.2]Tabel 2 Daftar kode isolat bakteri endofit
Kode Isolat
Bogor Cipanas Lembang
Aa)Bb)1 AB10 AC1 BC2 AL2 BL30
AB2 BB1 AC2 BC3 AL4 BL31
AB3 BB2 AC3 BC4 AL5 BL32
AB4 BB3 AC4 BC5 AL7 BL34
AB5 BB4 AC5 BC6 AL11 BL38
AB6 BB5 AC6 BC7 BL5
AB7 BB6 AC7 BC8 BL10
AB8 BB7 AC8 BC9 BL14
AB9 BC1 BC10 BL17
a) Bagian batang dari sampel tanaman : B = batang bawah (pangkal batang), A = batang atas (pertengahan tinggi tanaman).
b) Asal sampel tanaman: L = Lembang, C = Cipanas, B = Bogor.
Uji Reaksi Hipersensitif
Untuk mengetahui sifat patogenisitas dari tiap isolat maka dilakukan uji
hipersensitif (HR). Bakteri endofit yang tidak menimbulkan gejala nekrosis
manandakan reaksi negatif atau non patogen dan dapat digunakan untuk pengujian
selanjutnya yaitu uji zona bening dan uji penghambatan pertumbuhan patogen
pada media cair.
Tabel 3 menunjukkan hasil uji HR bahwa terjadi reaksi positif pada
bakteri asal Bogor dengan kode isolat AB7 dan BB2. Bagian daun yang disuntik
dengan isolat AB7 dan BB2 warnanya berubah menjadi kuning dan akhirnya
mengering (nekrosis). Sedangkan 15 bakteri endofit lainnya tidak menimbulkan
gejala apapun setelah diaplikasikan sehingga dapat digunakan kembali untuk
pengujian selanjutnya.
Berbeda dengan isolat asal Bogor, isolat asal Cipanas lebih banyak
menimbulkan reaksi positif pada uji HR, antara lain isolat dengan kode AC4,
AC5, AC6, AC7, dan BC2. Gejala nekrosis terjadi pada isolat AC5, AC6, dan
AC7. Sedangkan AC4 dan BC2 menimbulkan pengubingan pada area yang
dengan isolat BL38. Dengan demikian, 13 isolat asal Lembang lainnya dapat
[image:43.612.134.492.154.547.2]digunakan pada pengujian berikutnya.
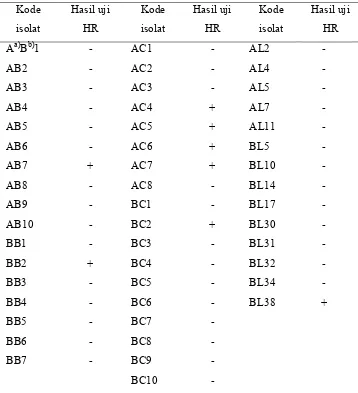
Tabel 3 Sifat patogenisitas isolat-isolat bakteri endofit asal Bogor, Cipanas dan Lembang
Kode
isolat
Hasil uji
HR
Kode
isolat
Hasil uji
HR
Kode
isolat
Hasil uji
HR
Aa)Bb)1 - AC1 - AL2
-AB2 - AC2 - AL4
-AB3 - AC3 - AL5
-AB4 - AC4 + AL7
-AB5 - AC5 + AL11
-AB6 - AC6 + BL5
-AB7 + AC7 + BL10
-AB8 - AC8 - BL14
-AB9 - BC1 - BL17
-AB10 - BC2 + BL30
-BB1 - BC3 - BL31
-BB2 + BC4 - BL32
-BB3 - BC5 - BL34
-BB4 - BC6 - BL38 +
BB5 - BC7
-BB6 - BC8
-BB7 - BC9
-BC10
-a) Bagian batang dari sampel tanaman : B = batang bawah (pangkal batang), A = batang atas (pertengahan tinggi tanaman).
Gambar 3 Gejala uji HR positif, bagian daun yang disuntik mengalami nekrosis (tanda panah)
Uji Penghambatan Pertumbuhan R. solanacearum secara in vitro
Metode Dual Culture
Uji penghambatan pertumbuhan Ralstonia solanacearum dengan metode
dual culture dengan pembentukkan zona bening dimaksudkan untuk mengetahui
besarnya penghambatan bakteri endofit terhadap pertumbuhan bakteri patogen
berdasarkan panjang diameter zona bening yang terbentuk. Semakin panjang
diameter zona bening yang terbentuk, semakin besar pula tingkat penekanannya
terhadap pertumbuhan patogen. Pengujian dilakukan secara duplo untuk tiap
bakteri endofit, sehingga diameter yang didapat merupakan rata-rata dari hasil
penjumlahan duplo tersebut. Isolat asal Bogor yang memiliki diameter terpanjang
yaitu AB10 dengan panjang diameter 0,3 cm, disusul AB9 dan BB1 sepanjang 0,2
cm, dan AB2, AB4, BB5, serta BB7 dengan panjang 0,1 cm, sedangkan bakteri
lainnya tidak menghasilkan zona bening sama seperti kontrol.
Pada Tabel 4 terlihat bahwa delapan isolat asal Cipanas membentuk zona
bening (zona hambatan) dengan diameter rata-rata terpanjang sebesar 0,5 cm pada
isolat BC4; 0,45 cm pada isolat AC8 dan BC5; AC3, BC7 dan BC10 sebesar 0,4
cm; serta AC2 dan BC9 dengan panjang diameter sebesar 0,3 cm. Dari hasil yang
didapat isolat asal Cipanas memiliki zona hambatan yang lebih besar
dibandingkan isolat asal Bogor dan Lembang. Isolat asal lembang hanya
berjumlah dua yang membentuk zona hambatan yaitu BL14 sebesar 0,2 cm dan
BL32 sebesar 0,15 cm. Dengan kata lain, isolat asal Cipanas lebih besar
untuk dijadikan sebagai bakteri antagonis untuk melawan patogen dalam menekan
penyakit layu bakteri di areal pertanaman tomat. Berbagai bentuk zona hambatan
yang dihasilkan oleh isolat bakteri endofit disajikan pada Gambar 4.
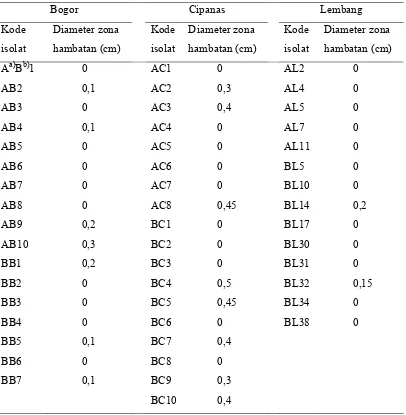
Tabel 4 Rerata diameter zona hambatan yang dihasilkan oleh isolat-isolat kandidat agens hayati pada media King’s B agar
Bogor Cipanas Lembang
Kode
isolat
Diameter zona
hambatan (cm)
Kode
isolat
Diameter zona
hambatan (cm)
Kode
isolat
Diameter zona
hambatan (cm)
Aa)Bb)1 0 AC1 0 AL2 0
AB2 0,1 AC2 0,3 AL4 0
AB3 0 AC3 0,4 AL5 0
AB4 0,1 AC4 0 AL7 0
AB5 0 AC5 0 AL11 0
AB6 0 AC6 0 BL5 0
AB7 0 AC7 0 BL10 0
AB8 0 AC8 0,45 BL14 0,2
AB9 0,2 BC1 0 BL17 0
AB10 0,3 BC2 0 BL30 0
BB1 0,2 BC3 0 BL31 0
BB2 0 BC4 0,5 BL32 0,15
BB3 0 BC5 0,45 BL34 0
BB4 0 BC6 0 BL38 0
BB5 0,1 BC7 0,4
BB6 0 BC8 0
BB7 0,1 BC9 0,3
BC10 0,4
a) Bagian batang dari sampel tanaman : B = batang bawah (pangkal batang), A = batang atas (pertengahan tinggi tanaman).
[image:45.612.136.542.179.594.2]Gambar 4 Berbagai macam zona hambatan (tanda panah) yang dihasilkan oleh beberapa bakteri endofit; isolat BC4 (a), isolat AC8 (b), isolat BC5 (c) dan isolat BC10 (d)
Uji Penghambatan Pertumbuhan R. solanacearumpada Media Cair
Isolat bakteri endofit yang tidak menghasilkan zona hambatan pada
metode dual culture kemudian digunakan dalam uji penghambatan pertumbuhan
patogen pada media cair. Namun, hanya lima isolat bakteri dari tiap wilayah yang
memiliki kriteria tertentu saja yang akan diuji. Kriteria tersebut antara lain bakteri
harus tumbuh dengan cepat dan jumlah koloninya banyak pada media agar,
memiliki warna yang khas dan mencolok, bentuk yang unik, dan ciri khas tertentu
yang berbeda dengan isolat lainnya. Adapun isolat-isolat yang diuji antara lain :
AB6, AB8, BB2, BB3, BB6, AC1, AC4, BC1, BC6, BC8, BL5, BL10, BL17,
BL38 dan AL2.
Tiap isolat yang diuji memperlihatkan penekanan yang berbeda terhadap
pertumbuhan populasi R. solanacearum. Berdasarkan hasil yang diperoleh,
bakteri endofit yang mampu menekan populasi R. solanacearum dengan
kerapatan dibawah 104 cfu/ml antara lain AB6, AB8, BB2, BB3 dan BB6.
Kemampuan penekanan yang sama juga terjadi pada bakteri endofit asal Cipanas,
yaitu AC1 dan AC4, diikuti oleh bakteri endofit asal Lembang, BL10 dan BL17.
a
d b
[image:46.612.192.466.92.298.2]Meskipun isolat asal Bogor mampu menekan pertumbuhan R.
solanacearum populasi dibawah 104 cfu/ml, namun bakteri endofit ini tumbuh
sangat sedikit pada media agar sehingga tidak memenuhi syarat fisik yang telah
ditentukan sebelumnya. Penekanan paling baik terhadap populasi R.
solanacearum terjadi pada isolat asal Cipanas dengan kode isolat AC1. Bakteri
endofit ini mampu menekan populasi patogen hingga dibawah 104 cfu/ml dan
dapat tumbuh sangat baik pada media agar. Isolat asal Cipanas lainnya seperti
AC4 tidak tumbuh sedikitpun pada media agar, BC1 tumbuh sangat sedikit, BC6
dan BC8 kurang baik dalam memberikan penekanan terhadap pertumbuhan R.
solanacearum, karena patogen masih dapat tumbuh bersamaan dengan kedua
isolat ini masing-masing dengan kerapatan 5.104 cfu/ml pada isolat BC6, 2.108
cfu/ml pada isolat BC8 dan 9,85.106 cfu/ml pada isolat BL38. Hubungan antara
[image:47.612.136.489.360.606.2]log populasi R. solanacearum dengan bakteri endofit yang diuji disajikan pada
Gambar 5.
Gambar 5 Grafik hubungan antara log populasi R. solanacearum dengan isolat bakteri endofit
6.993 6.301
4.698
0 0
1 2 3 4 5 6 7 8
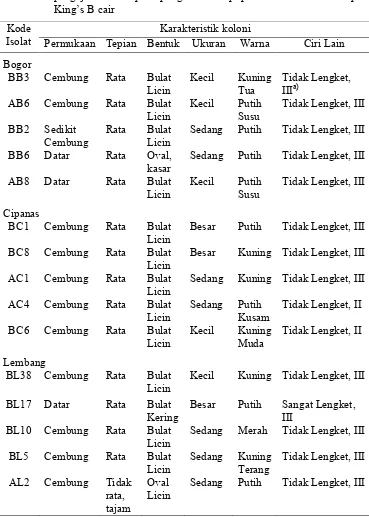
Tabel 5 Karakteristik isolat-isolat bakteri endofit yang digunakan dalam pengujian kemampuan penghambatan populasi R. solanacearum pada King’s B cair
Karakteristik koloni Kode
Isolat Permukaan Tepian Bentuk Ukuran Warna Ciri Lain
Bogor
BB3 Cembung Rata Bulat
Licin
Kecil Kuning
Tua
Tidak Lengket, IIIa)
AB6 Cembung Rata Bulat
Licin
Kecil Putih
Susu
Tidak Lengket, III
BB2 Sedikit Cembung
Rata Bulat
Licin
Sedang Putih Tidak Lengket, III
BB6 Datar Rata Oval,
kasar
Sedang Putih Tidak Lengket, III
AB8 Datar Rata Bulat
Licin
Kecil Putih
Susu
Tidak Lengket, III
Cipanas
BC1 Cembung Rata Bulat
Licin
Besar Putih Tidak Lengket, III
BC8 Cembung Rata Bulat
Licin
Besar Kuning Tidak Lengket, III
AC1 Cembung Rata Bulat
Licin
Sedang Kuning Tidak Lengket, III
AC4 Cembung Rata Bulat
Licin
Sedang Putih Kusam
Tidak Lengket, II
BC6 Cembung Rata Bulat
Licin
Kecil Kuning
Muda
Tidak Lengket, II
Lembang
BL38 Cembung Rata Bulat
Licin
Kecil Kuning Tidak Lengket, III
BL17 Datar Rata Bulat
Kering
Besar Putih Sangat Lengket, III
BL10 Cembung Rata Bulat
Licin
Sedang Merah Tidak Lengket, III
BL5 Cembung Rata Bulat
Licin
Sedang Kuning Terang
Tidak Lengket, III
AL2 Cembung Tidak
rata, tajam
Oval Licin
Sedang Putih Tidak Lengket, III
[image:48.612.134.503.103.620.2]Keefektifan Bakteri Endofit dalam Menekan Kejadian Penyakit Layu Bakteri dan Kemampuan Pemacu Pertumbuhan Tanaman
Kejadian Penyakit (KP)
Masing-masing tiga isolat bakteri endofit hasil pengujian dengan metode
dual culture dan dengan media cair digunakan untuk pengujian penekanan
kejadian penyakit layu bakteri yang disebabkan oleh R. solanacearum. Sebagai
kontrol digunakan aquades steril dalam perendaman bibit dan penyiraman
tanaman.
Tabel 6 Pengaruh aplikasi bakteri endofit terhadap kejadian penyakit layu bakteri
Ralstonia solanacearum pada tanaman tomat
Kejadian penyakit (%) Kode isolat
4 MSTa) 5 MST 6 MST
Kb) 3,33ae) 70,0a 83,33a
Ac)Cd) 1 0,00a 50,0ab 53,33ab
BC 4 0,00a 33,33ab 33,33b
BC 5 0,00a 50,00ab 53,33ab
BC 10 10,00a 23,33b 40,00b
BL 10 6,67a 36,67ab 43,33ab
BL 17 6,67a 36,67ab 46,67ab
a) MST = Minggu Setelah Tanam. b) K = Kontrol.
c) Bagian batang dari sampel tanaman : B = batang bawah (pangkal batang), A = batang atas (pertengahan tinggi tanaman).
d) Asal sampel tanaman: L = Lembang, C = Cipanas, B = Bogor.
e) Angka yang diikuti huruf yang berbeda pada kolom yang sama berbeda nyata (uji selang ganda Duncan α = 0,05).
Berdasarkan Tabel 6, kejadian penyakit tidak berbeda nyata pada
pengamatan 4 MST. Namun, pada pengamatan 5-6 MST perbedaan yang nyata
terjadi pada tiap perlakuan, dengan persen kejadian penyakit pada tanaman
kontrol berturut-turut sebesar 70% dan 83,33%. Pada 5 MST bakteri BC10
memberikan penekanan yang baik terhadap serangan patogen R. Solanacearum
dengan persen kejadian penyakit sebesar 23,33%, sedangkan pada minggu
[image:49.612.131.491.292.482.2]dengan kejadian penyakit berturut-turut sebesar 33,33% dan 40%. Dari hasil yang
diperoleh dapat diketahui bahwa telah terjadi simbiosis antara bakteri endofit dan
tanaman tomat dengan mekanisme yang berbeda satu sama lain dalam melawan
patogen R. Solanacearum. Menurut Bacon & Hinton (2006), keanekaragaman
spesies bakteri endofit merefleksikan banyaknya cara kerja yang mungkin terjadi
untuk melawan patogen, yang memungkinkan patogen memproduksi senyawa
antibiotik untuk melawan bakteri endofit tersebut.
Menurut Sigee (1993), agens pengendali hayati sanggup untuk membatasi
pertumbuhan dan aktifitas bakteri fitopatogen dengan dua langkah, yaitu dengan
memproduksi substansi anti mikrobial serta berkompetisi atas ruang dan nutrisi
yang spesifik pada permukaan tanaman.
Gejala penyakit layu bakteri yang muncul pada tanaman bervariasi,
beberapa tanaman memperlihatkan layu pada daun dan tanaman hingga daun
berwarna coklat dan terkulai ke bawah yang dimulai dari daun paling bawah.
Tanaman lainnya tidak langsung menunjukkan gejala layu dengan daun yang
terkulai ke bawah, akan tetapi batang memanjang dan kurus, serta munculnya
banyak akar adventif di permukaan batang sampai pada ruas tempat terbentuknya
bunga pertama (Semangun 2004; Walker 1957).
Sebagai patogen tular tanah, Ralstonia sola