PRA RANCANGAN PABRIK PEMBUATAN
METANOL DENGAN PROSES GASIFIKASI BATUBARA
DENGAN KAPASITAS 70.000 TON/TahunTUGAS AKHIR
Diajukan untuk memenuhi persyaratan Ujian Sarjana Teknik Kimia
Oleh : STEPHANIE
030405035
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PENGESAHAN
PRA RANCANGAN PABRIK PEMBUATAN
METANOL DENGAN PROSES GASIFIKASI BATUBARA DENGAN KAPASITAS 70.000 Ton/Tahun
TUGAS AKHIR
Diajukan untuk memenuhi persyaratan Ujian Sarjana Teknik Kimia
Oleh : STEPHANIE
030405035
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
2008
Diketahui/disetujuiKoordinator TA
(Dr.Eng.Ir.Irvan, MSi) NIP : 132 126 842
Diketahui/disetujui Dosen Pembimbing I
(Ir. Indra Surya, MSc) NIP : 131 836 666
Diketahui / disetujui Dosen Pembimbing II
INTISARI
Methanol merupakan salah satu senyawa yang dapat digunakan sebagai bahan baku lem kayu lapis dan pencampur bahan bakar minyak. Indonesia sendiri hanya memilki satu pabrik metanol, sehingga kebutuhan metanol dalam negri harus di impor. Pembuatan metanol dalam perancangan pabrik ini, menggunakan bahan baku dari batubara yang di gasifikasi menjadi gas Hidrogen dan Karbonmonoksida yang mana merupakan bahan baku pembuatan metanol .
Metanol yang diproduksi 70.000 ton/tahun dengan 330 hari kerja dalam 1 tahun dengan menggunakan bahan baku batubara 75.080,5286 ton/tahun. Lokasi pabrik direncanakan di daerah Mariana, Musi Banyuasin, Sumatera Selatan dengan luas daerah 17.200 m2, tenaga kerja yang dibutuhkan berjumlah 193 orang dengan bentuk badan usaha Perseroan Terbatas (PT) yang dipimpin oleh seorang direktur utama dengan struktur organisasi sistem garis.
Hasil analisa ekonomi Pabrik Metanol adalah sebagai berikut : Modal Investasi : Rp 3.159.552.438.000,- Biaya Produksi per tahun : Rp 1.486.442.571.000,- Hasil Jual Produk per tahun : Rp. 2.188.147.500.000,- Laba Bersih per tahun : Rp 500.618.124.000,-
Profit Margin : 31,91 %
Break Event Point : 60 %
Return of Investment : 21,04 %
Pay Out Time : 4,75 tahun
Return on Network : 26,41 %
Internal Rate of Return : 34,42 %
KATA PENGANTAR
Rasa Hormat dan Syukur penulis naikkan ke hadirat Tuhan Yang Maha Kuasa atas kasih dan perkenaanNya penulis dapat menyelesaikan Tugas Akhir yang berjudul:
PRA RANCANGAN PABRIK
PEMBUATAN METANOL DARI BARUBARA
DENGAN PROSES GASIFIKASI
KAPASITAS PRODUKSI 70.000 TON/TAHUN
Tugas akhir ini disusun untuk melengkapi tugas-tugas dan merupakan salah satu syarat untuk mengikuti ujian sarjana pada Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
Dalam menyelesaikan tugas akhir ini penulis banyak menerima bantuan, bimbingan dan dukungan dari berbagai pihak, oleh karena itu penulis mengucapkan terima kasih kepada :
1. Ibu Ir. Renita Manurung, MT., Ketua Jurusan Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara
2. Bapak M. Hendra Ginting, ST. MT., Sekretaris Jurusan Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara
3. Bapak Dr.Eng Ir. Irvan, M.Si, Koordinator Tugas Akhir Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
4. Bapak Indra Surya, Msc., selaku dosen pembimbing dalam penyusunan tugas akhir ini.
5. Ibu Ir. Kartini Noor Hafni, MT., selaku co-dosen pembimbing dalam penyusunan tugas akhir ini.
6. Bapak dan Ibu dosen serta pegawai Program Studi Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
7. Orangtua dan Saudara Penulis, yang telah banyak memberikan dukungan moril dan materil kepada penulis.
9. Benny, orang yang paling sabar yang selalu memberikan semangat dan bantuan yang tak terkira pada penulis.
10.Teman-teman mahasiswa/i Teknik Kimia terkhusus stambuk 2003 yang telah memberikan banyak dukungan kepada penulis.
11.Sahabat-sahabat seperjuangan penulis; Boby B.S, dan Ennophati. Gass truss!! Penulis menyadari bahwa Tugas Akhir ini memiliki kekurangan, untuk itu dibutuhkan saran yang membangun dari semua pihak demi penyempurnaannya.
Semoga karya ini dapat bermanfaat bagi pembacanya, terutama mahasiswa/i Teknik Kimia, Fakultas Teknik, Sumatera Utara.
Medan, Desember 2008 Penulis,
DAFTAR ISI
Halaman
KATA PENGANTAR ...i
INTISARI ... iii
DAFTAR ISI ... iv
DAFTAR GAMBAR ... x
5.1.8 Membran (G502) ... V-3 5.1.9 Tangki Penyimpanan Larutan Monoetanolamin (F-104) ... V-4 5.2 Unit Sintesa ... V-4 5.2.1 Steam Methane Reformer (R-701) ... V-4 5.2.2 Expander (G-504) ... V-4 5.2.3 Cooler (E-602) ... V-5 5.2.4 Absorber (D-801) ... V-5 5.2.5 Exchanger (E-603) ... V-6 5.2.6 Cooler (E-604) ... V-6 5.2.7 Stripper (D-802) ... V-7 5.2.8 Kompresor (G-505) ... V-7 5.2.9 Reaktor Metanol (R-702) ... V-7 5.2.10 Cyclone (H-11) ... V-8 5.2.11 Screw Conveyor (J-203) ... V-8 5.2.12 Pompa Absorber (L-901) ... V-8 5.2.13 Pompa Stripper (L-902) ... V-9 5.2.14 Pompa MEA (L-903) ... V-9 5.3 Pemisahan Produk Utama dan Produk Samping ... V-9 5.3.1 Kompresor (G-503) ... V-9 5.4 Unit Penyempurnaan Produk ... V-10 5.4.1 Tangki Penyimpanan Metanol (F-104) ... V-10 5.4.2 Kondensor (E-605) ... V-10 5.4.3 Separator (D-803)... V-11 BAB VI INSTRUMENTASI DAN KESELAMATAN KERJA ... VI-1 6.1 Instrumentasi ... VI-1 6.1.1 Tujuan Pengendalian ... VI-3 6.1.2 Jenis – jenis Pengendalian dan Alat Pengendali
6.2.3 Pengukuran Terhadap Keselamatan ... VI-16 6.2.4 Hal – hal Yang Perlu Diperhatikan dalam Perencanaan
7.4.11 Sand Filter (SF) ... VII-17 7.4.12 Pompa Sand Filter (PU-06) ... VII-18 7.4.13 Tangki Utilitas-01 (TU-01) ... VII-18 7.4.14 Pompa Cation Exchanger –01 (PU-07) ... VII-18 7.4.15 Tangki Pelarutan H2SO4 (TP-03)) ... VII-18
7.4.16 Pompa H2SO4 (PU-10) ... VII-19
9.1.4 Bentuk Organisasi Fungsionil dan Staf ... IX-3 9.2 Manajemen Perusahaan ... IX-3 9.3 Bentuk Hukum Badan Usaha ... IX-4 9.4 Uraian Tugas, Wewenang, dan Tanggung Jawab ... IX-6 9.4.1 Rapat Umum Pemegang Saham (RUPS) ... IX-6 9.4.2 Dewan komisaris ... IX-6 9.4.3 Direktur ... IX-6 9.4.4 Staf Ahli ... IX-7 9.4.5 Sekretaris ... IX-7 9.4.6 Manajer Produksi ... IX-7 9.4.7 Manajer Teknik ... IX-7 9.4.8 Manajer Umum dan Keuangan ... IX-8 9.4.9 Manajer Pembelian dan Pemasaran ... IX-8 9.5 Sistem Kerja ... IX-8 9.6 Jumlah Karyawan dan Tingkat Pendidikan ... IX-10 9.7 Sistem Penggajian ... IX-11 9.8 Tata Tertib ... IX-13 9.9 JAMSOSTEK dan Fasilitas Tenaga Kerja ... IX-14 BAB X ANALISIS EKONOMI ... X-1 10.1 Modal Investasi ... X-1 10.1.1 Modal Investasi Tetap / Fixed Capital Investment (FCI)... X-1 10.1.2 Modal Investasi Tak Langsung / Indirect Fixed
DAFTAR GAMBAR
Gambar 6.1 Diagram Balok Sistem Pengendalian Feedback... VI-4 Gambar 6.2 Sebuah loop Pengendalian ... VI-5 Gambar 6.3 Reaktor ... VI-11 Gambar 6.4 Tangki Cairan ... VI-11 Gambar 6.5 Tangki Gas ... VI-11 Gambar 6.6 Cooler dan Heater ... VI-11 Gambar 6.7 Absorber ... VI-13 Gambar 6.8 Ekspander ... VI-13 Gambar 6.9 Pompa ... VI-13 Gambar 6.10 Instrumentasi pada Kompresor ... VI-14 Gambar 6.11 Stripper... VI-14 Gambar 6.12 Bucket Elevator ... VI-14 Gambar 6.13 Membran (ASU) ... VI-15 Gambar 6.14 Belt Conveyor ... VI-15 Gambar 6.15 Screw Conveyor ... VI-15 Gambar 8.1 Tata Letak Pabrik Metanol ... VIII-5 Gambar 9.1 Bagan Struktur Organisasi Perusahaan-Pabrik Pembuatan
Metanol Dengan Proses Gasifikasi Batubara ... IX-17 Gambar LE.1 Break Event Point Pabrik Pembuatan Metanol dengan Proses
DAFTAR TABEL
Tabel 2.1 Perbandingan jenis-jenis gasifier(A.G.A.Z, Habib, 2008) ... II-7 Tabel 6.1 Daftar Penggunaan Instrumentasi Pada Pra Rancangan Pabrik
INTISARI
Methanol merupakan salah satu senyawa yang dapat digunakan sebagai
bahan baku lem kayu lapis dan pencampur bahan bakar minyak. Indonesia sendiri
hanya memilki satu pabrik metanol, sehingga kebutuhan metanol dalam negri harus
di impor. Pembuatan metanol dalam perancangan pabrik ini, menggunakan bahan
baku dari batubara yang di gasifikasi menjadi gas Hidrogen dan Karbonmonoksida
yang mana merupakan bahan baku pembuatan metanol .
Metanol yang diproduksi 70.000 ton/tahun dengan 330 hari kerja dalam 1
tahun dengan menggunakan bahan baku batubara 75.080,5286 ton/tahun. Lokasi
pabrik direncanakan di daerah Mariana, Musi Banyuasin, Sumatera Selatan dengan
luas daerah 17.200 m2, tenaga kerja yang dibutuhkan berjumlah 193 orang dengan bentuk badan usaha Perseroan Terbatas (PT) yang dipimpin oleh seorang direktur
utama dengan struktur organisasi sistem garis.
Hasil analisa ekonomi Pabrik Metanol adalah sebagai berikut :
Modal Investasi : Rp 3.159.552.438.000,-
Biaya Produksi per tahun : Rp 1.486.442.571.000,-
Hasil Jual Produk per tahun : Rp. 2.188.147.500.000,-
Laba Bersih per tahun : Rp 500.618.124.000,-
Profit Margin : 31,91 %
Break Event Point : 60 %
Return of Investment : 21,04 %
Pay Out Time : 4,75 tahun
Return on Network : 26,41 %
Internal Rate of Return : 34,42 %
Dari hasil analisa aspek ekonomi dapat disimpulkan bahwa pabrik pembuatan
BAB I
PENDAHULUAN
1.1 Latar Belakang
Dewasa ini semua industri diarahkan untuk menggunakan teknologi yang minim akan polusi dan hemat biaya untuk operasional, salah satu jenis proses teknologi tersebut adalah proses gasifikasi. Teknologi gasifikasi ini juga merupakan teknologi yang hemat biaya. Dapat dikatakan demikian karena, proses konversi batubara menjadi gas dapat dilakukan dengan alat yang bernama gasifier, dimana dapat disesuaikan dengan kebutuhan yang diinginkan (Sukandarumidi,2006). Gasifikasi merupakan satu upaya pengkonversian batubara padat menjadi gas, seperti H2, CO, CO2, CH4, N2 dan H2S. Gas-gas ini selanjutnya
akan mengalami proses purifikasi sebelum disintesa menjadi senyawa kimia baru yang secara luas dibutuhkan dalam kehidupan manusia, salah satunya adalah metanol.
Metanol (CH3OH) merupakan salah satu senyawa kimia yang dapat
diproduksi melalui proses gasifikasi. Metanol (CH3OH) adalah senyawa kimia
yang banyak digunakan dalam berbagai sektor kehidupan, seperti sektor kesehatan sektor kosmetik dan lain-lain. Metanol (CH3OH) bertindak sebagai bahan baku
dalam memproduksi senyawa hidrokarbon yang berguna sebagai bahan bakar atau senyawa organik yang biasa digunakan untuk menaikkan nilai oktan suatu bahan bakar, seperti metil t- butil eter (MTBE) ( US Patent 5472986, 1995).
Permintaan industri dunia akan metanol lebih dari 32 juta ton per tahun dan mengalami peningkatan permintaan lebih dari 3% tiap tahunnya (
. Indonesia merupakan salah satu
BAB II
TINJAUAN PUSTAKA
2.1 Sejarah Metanol
Dalam proses pengawetan mayat, orang Mesir kuno menggunakan
berbagai macam campuran, termasuk di dalamnya metanol, yang mereka peroleh
dari pirolisis kayu. Metanol murni, pertama kali berhasil diisolasi tahun 1661 oleh
Robert Boyle, yang menamakannya spirit of box, karena ia menghasilkannya
melalui distilasi kotak kayu. Nama itu kemudian lebih dikenal sebagai pyroxylic spirit (spiritus). Pada tahun 1834, ahli kimia Perancis Jean-Baptiste Dumas dan Eugene Peligot menentukan komposisi kimianya. Mereka juga memperkenalkan
nama methylene untuk kimia organik, yang diambil dari bahasa Yunani methy = "anggur") + hwl_ = kayu (bagian dari pohon). Kata itu semula dimaksudkan untuk menyatakan "alkohol dari (bahan) kayu".
Kata metil pada tahun 1840 diambil dari methylene, dan kemudian
digunakan untuk mendeskripsikan "metil alkohol". Nama ini kemudian disingkat
menjadi "metanol" tahun 1892 oleh International Conference on Chemical Nomenclature. Suffiks [-yl] (indonesia {il}) yang digunakan dalam kimia organik untuk membentuk nama radikal-radikal, diambil dari kata methyl.
Pada tahun 1923, ahli kimia Jerman, Matthias Pier, yang bekerja untuk
BASF mengembangkan cara mengubah gas sintesis (syngas / campuran dari
karbon dioksida and hidrogen) menjadi metanol. Proses ini menggunakan katalis
zinc chromate (seng kromat).
Penggunaan metanol sebagai bahan bakar mulai mendapat perhatian ketika
krisis minyak bumi terjadi di tahun 1970-an karena ia mudah tersedia dan murah.
Masalah timbul pada pengembangan awalnya untuk campuran metanol-bensin.
Untuk menghasilkan harga yang lebih murah, beberapa produsen cenderung
mencampur metanol lebih banyak. Produsen lainnya menggunakan teknik
pencampuran dan penanganan yang tidak tepat. Akibatnya, hal ini menurunkan
digunakan sebagai bahan bakar bersih. Mobil-mobil dengan bahan bakar fleksibel
yang dikeluarkan oleh General Motors, Ford dan Chrysler dapat beroperasi
dengan setiap kombinasi etanol, metanol dan bensin. (Sheldiez, 2007)
2.2 Gambaran Metanol
Senyawa alkohol yang paling sederhana dan umum digunakan adalah
metanol. Metanol yang juga dikenal sebagai metil alkohol, wood alcohol atau spiritus, adalah senyawa kimia yang dapat disusun dari tiga unsur kimia yaitu
unsur oksigen, karbon, dan hidrogen dengan rumus kimia CH3OH. Metanol
diproduksi secara alami oleh metabolisme anaerobik oleh bakteri. Hasil proses
tersebut adalah uap metanol (dalam jumlah kecil) di udara. Setelah beberapa hari,
uap metanol tersebut akan teroksidasi oleh oksigen dengan bantuan sinar matahari
menjadi karbon dioksida dan air. Reaksi kimia metanol yang terbakar di udara dan
membentuk karbon dioksida dan air adalah sebagai berikut:
2 CH3OH + 3 O2→ 2 CO2 + 4 H2O
Pada keadaan atmosfer ia berbentuk cairan yang ringan, mudah menguap,
tidak berwarna, mudah terbakar, dan beracun dengan bau yang khas (berbau lebih
ringan daripada etanol). Ia digunakan sebagai bahan pendingin anti beku, pelarut,
bahan bakar dan sebagai bahan additif bagi etanol industri.
Api dari metanol biasanya tidak berwarna. Oleh karena itu, kita harus
berhati-hati bila berada dekat metanol yang terbakar untuk mencegah cedera
akibat api yang tak terlihat. Karena sifatnya yang beracun, metanol sering
digunakan sebagai bahan additif bagi pembuatan alkohol untuk penggunaan
industri; Penambahan "racun" ini akan menghindarkan industri dari pajak yang
dapat dikenakan karena etanol merupakan bahan utama untuk minuman keras
(minuman beralkohol).
Metanol kadang juga disebut sebagai wood alcohol karena ia dahulu
merupakan produk samping dari distilasi kayu. Saat ini metanol dihasilkan
melului proses multi tahap. Secara singkat, gas alam dan uap air dibakar dalam
tungku untuk membentuk gas hidrogen dan karbon monoksida. Kemudian, gas
katalis untuk menghasilkan metanol. Tahap pembentukannya adalah endotermik
dan tahap sintesisnya adalah eksotermik.
Saat ini, gas sintesis umumnya dihasilkan dari metana yang merupakan
komponen dari gas alam. Terdapat tiga proses yang dipraktekkan secara
komersial, yaitu: (Sheldiez, 2007)
1. Pada tekanan sedang 1 hingga 2 MPa (10-20 atm) dan temperatur tinggi
(sekitar 850 °C), metana bereaksi dengan uap air (steam) dengan katalis
nikel untuk menghasilkan gas sintesis menurut reaksi kimia berikut:
CH4 + H2O → CO + 3 H2
Reaksi ini, umumnya dinamakan steam-methane reforming atau SMR,
merupakan reaksi endotermik dan limitasi perpindahan panasnya menjadi
batasan dari ukuran reaktor katalitik yang digunakan.
2. Metana juga dapat mengalami oksidasi parsial dengan molekul oksigen
untuk menghasilkan gas sintesis melalui reaksi kimia berikut:
2 CH4 + O4 → 2 CO2 + 4 H2
reaksi ini adalah eksotermik dan panas yang dihasilkan dapat digunakan
secara in-situ untuk menggerakkan reaksi steam-methane reforming.
3. Ketika dua proses tersebut dikombinasikan, proses ini disebut sebagai
autothermal reforming. Rasio CO and H2 dapat diatur dengan
menggunakan reaksi perpindahan air-gas (the water-gas shift reaction):
CO + H2O → CO2 + H2,
untuk menghasilkan stoikiometri yang sesuai dalam sintesis metanol.
Karbon monoksida dan hidrogen kemudian bereaksi dengan katalis kedua
untuk menghasilkan metanol. Saat ini, katalis yang umum digunakan
adalah campuran tembaga, seng oksida, dan alumina, yang pertama kali
digunakan oleh ICI di tahun 1966. Pada 5-10 MPa (50-100 atm) dan
temperatur 250 °C, ia dapat mengkatalisis produksi metanol dari karbon
CO + 2 H2→ CH3OH
Sangat perlu diperhatikan bahwa setiap produksi gas sintesis dari metana
menghasilkan 3 mol hidrogen untuk setiap mol karbon monoksida, sedangkan
sintesis metanol hanya memerlukan 2 mol hidrogen untuk setiap mol karbon
monoksida. Salah satu cara mengatasi kelebihan hidrogen ini adalah dengan
menginjeksikan karbon dioksida ke dalam reaktor sintesis metanol, dimana ia
akan bereaksi membentuk metanol sesuai dengan reaksi kimia berikut:
CO2 + 3 H2→ CH3OH + H2O
Walaupun gas alam merupakan bahan yang paling ekonomis dan umum
digunakan untuk menghasilkan metanol, bahan baku lain juga dapat digunakan.
Ketika tidak terdapat gas alam, produk petroleum ringan juga dapat digunakan. Di
Afrika Selatan, sebuah perusahaan (Sasol) menghasilkan metanol dengan
menggunakan gas sintesis dari batu bara.
2.3 Gasifikasi Batu Bara
Gasifikasi adalah proses yang dilakukan pada suhu dan tekanan yang
tinggi untuk menghasilkan campuran gas (gas sintetis) dengan mereaksikan steam,
oksigen, dan material yang mengandung karbon. Produk terdiri dari karbon
monoksida, karbon dioksida, hidrogen, metana, dan gas-gas lain, dalam
perbandingan yang tergantung pada reaktan tertentu dan kondisi operasi
(temperatur dan tekanan) yang dilakukan dalam reaktor, dan tahap perlakuan yang
dilalui gas-gas tersebut untuk selanjutnya meninggalkan gasifier. Bahan-bahan
kimia yang sama dapat juga digunakan dalam gasifikasi kokas (batu bara) yang
diturunkan dari petroleum dan sumber yang lain. Reaksi batu bara dan arang batu
bara dengan udara atau oksigen untuk menghasilkan panas dan karbon dioksida
dapat disebut sebagai gasifikasi, tapi lebih cocok dikatakan sebagai proses
pembakaran. Tujuan dasar dari beberapa konversi adalah produksi gas alam
sintesis sebagai bagian bahan bakar gas dan gas-gas sintesis untuk produksi
Panas
Hampir dalam semua proses, flow diagram proses secara umum adalah
sama. Batu bara disiapkan melalui penghancuran dan pengeringan, pra perlakuan
jika diperlukan untuk mencegah pembentukan caking, dan kemudian digasifikasi
dengan uap air dari udara atau oksigen dan steam. Gas yang dihasilkan
didinginkan dan dibersihkan dari debu-debu arang, hidrogen sulfida, dan CO2
sebelum memasuki tahapan proses yang dikehendaki untuk mencocokkan
komposisinya untuk penggunaan akhir yang dikehendaki.
Dasar reaksi kimia secara umum untuk seluruh gasifikasi batu bara adalah
batu bara dan arang batu bara (1-3) dan reaksi gas (4-5):
Batu bara gas (CO, CO2, H2, CH4) + char ... (1)
C (arang) + H2O CO + H2 (endotermis) ... (2)
2C (arang) + 3/2 O2 CO2 + CO (eksotermis) ... (3)
CO + H2O H2 + CO2 (sedikit eksotermis) ... (4)
CO + 3H2 CH4 + H2O (eksotermis) …..(5)
Gasifikasi batubara pada dasarnya merupakan suatu proses perubahan
menjadi gas yang lebih mudah terbakar dengan klasifikasi berdasarkan nilai panas
(heating value) yaitu low-btu (180-350 Btu/scf), medium-btu (250-500 Btu/scf),
high-btu (950-1000 Btu/scf). Perubahan batubara menjadi gas yang mudah terbakar terjadi melalui beberapa proses kimia dalam reaktor gasifikasi. Tahap
awal setelah batubara mendapat perlakuan awal (ukuran butir diperkecil hingga
ukuran butir tertentu), sebagai feed stock, mengalami pemanasan sampai
temperatur reaksi dan mengalami pirolisa atau pembaraan.
Pembakaran yang terjadi disini adalah pembakaran tidak sempurna
(partial combustion) dengan rasio batubara lebih besar dari stoikiometri reaksi atau oksigen dibuat tidak mampu mengkonversi seluruh karbon menjadi
karbondioksida. Dalam reaktor gasifikasi, produk gasifikasi yaitu CO dan H2,
bercampur dengan produk pirolisa. Distribusi berat dan komposisi berat gas yang terjadi dipengaruhi oleh beberapa kondisi antara lain temperatur, kecepatan
Panas gasifikasi cenderung diklasifikasikan berdasarkan nilai panas, tetapi
dapat pula digolongkan berdasarkan atas transportasi dan kondisi sistem reaksi
dalam reaktor yaitu, fixed bed, fluidized bed dan entrained bed.
a. Fixed Bed
Pada proses gasifikasi cara ini, gravitasi menguasai sistem
partikel-partikelnya tidak dapat bergerak dan membentuk suatu tumpukan atau solid bed.
Penghembusan gas pereaksi uap dan O2 dari bawah berlawanan dengan arah
suplai partikel batubara ukuran 3-30 mm dengan residence time 1-5 jam. Gas yang dihasilkan dari proses ini dialirkan dari atas sementara abu yang dihasilkan di
keluarkan dari bagian bawah.
Pada gasifikasi dengan menggunakan proses Fixed Bed terdapat empat zona reaksi, yaitu: (Naskahta, 2005)
1. Zona Devolatisasi
Pada zona ini terjadi penguapan air dan zat-zat volatil yang terkandung
dalam batubara
2. Zona Gasifikasi
Pada zona ini steam yang dialirkan dan CO2 yang terbentuk dari
pembakaran sempurna, bereaksi dengan batubara pada suhu tinggi dan
membentuk gas sintesis yang terdiri dari CO2, H2, dan N2.
3. Zona Pembakaran
Pada zona ini O2 yang masuk bereaksi dengan sebagian batubara
membentuk CO2 dan H2O yang diperlukan dalam reaksi gasifikasi.
4. Zona Abu
Zona ini adalah tempat penampungan abu yang dihasilkan, baik hasil
reaksi pembakaran maupun hasil gasifikasi.
b. Fluidized Bed
gaya gravitasi sehingga batubara yang diinjeksikan dari atas dalam bentuk serbuk
berukuran antara 0,1-5 mm berada dalam keadaan melayang dan juga berakibat
permukaan reaksi menjadi lebih luas sehingga reaksi lebih cepat dengan residence time 15-50 detik. Pada reaktor fluidized bed O2 dan steam alirkan melalui bagian
bawah, sedangkan gas yang dihasilkan di alirkan ke bagian bawah reaktor dan abu
dialirkan ke samping bagian bawah reaktor.
c. Entrainned Bed
Pada proses ini, steam dan O2 bercampur dengan kecepatan sedemikian
tinggi sehingga membuat partikel-partikel solid batubara terbawa oleh gas
(transport pneumatic) yang masuk dari bagian atas. Dalam hal ini diperkenalkan istilah partikel cloud (bukan dinamakan bed lagi). Untuk partikel batubara disebut
dengan powder coal dengan ukuran partikel lebih kecil dari 0,5 mm dengan
residence time antara 1-5 detik. Pada reaktor ini, gas yang dihasilkan dialirkan ke samping bagian bawah reaktor sedangkan abu dikeluarkan dari bagian dasar
reaktor.
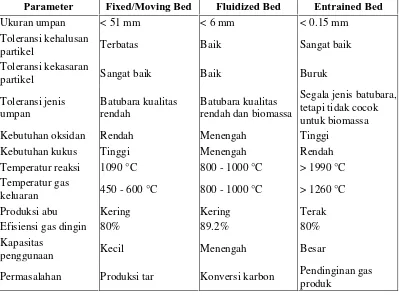
Tabel 1 Perbandingan jenis-jenis gasifier (A.G.A.Z, Habib, 2008)
Parameter Fixed/Moving Bed Fluidized Bed Entrained Bed
Ukuran umpan < 51 mm < 6 mm < 0.15 mm
Toleransi kehalusan
partikel Terbatas Baik Sangat baik
Toleransi kekasaran
partikel Sangat baik Baik Buruk
Toleransi jenis umpan
Batubara kualitas rendah
Batubara kualitas rendah dan biomassa
Segala jenis batubara, tetapi tidak cocok untuk biomassa
Kebutuhan oksidan Rendah Menengah Tinggi
Kebutuhan kukus Tinggi Menengah Rendah
Temperatur reaksi 1090 °C 800 - 1000 °C > 1990 °C Temperatur gas
keluaran 450 - 600 °C 800 - 1000 °C > 1260 °C
Produksi abu Kering Kering Terak
Efisiensi gas dingin 80% 89.2% 80%
Kapasitas
penggunaan Kecil Menengah Besar
2.4 Batubara
Batubara merupakan nama umum yang digunakan untuk mengekspresikan
mineral hitam yang terbentuk dari tumbuh-tumbuhan pada masa lampau, bersifat
padat, berwarna gelap dan dapat dibakar. Batubara sebagian besar mengandung
karbon dan sejumlah kecil hidrogen, nitrogen, oksigen, dan sulfur. (Brady, George
S.,dkk, ).
Pembentukan batubara dimulai sejak Carboniferous Period (Periode
Pembentukan Karbon atau Batu Bara) yang dikenal sebagai zaman batubara
pertama. Zaman batubara pertama ini berlangsung antara 360 juta sampai 290 juta
tahun yang lalu. Mutu dari setiap endapan batubara ditentukan oleh suhu dan
tekanan serta lama waktu pembentukan, yang disebut sebagai ‘maturitas organik’.
batubara tersebut mudah terbakar dan menghasilkan kalori tinggi, disebut
batubara, tetapi apabila batubara tersebut tidak mudah terbakar dan mengasilkan
kalori rendah disebut sebagai batubara muda.
Batubara merupakan salah satu jenis bahan bakar pembangkit energi.
Batubara dapat pula dipergunakan tidak sebagai bahan bakar, tetapi dipergunakan
sebagai reduktor pada proses peleburan timah, industri ferro-nikel, industri besi
dan baja, sebagai bahan pemurnian pada industri kimia (dalam bentuk karbon
aktif), sebagai bahan pembuatan kalsium karbida (dalam bentuk kokas atau semi
kokas). Pemanfaatan batubara dalam industri semen, batubara yang dibakar akan
menyisakan abu. Abu batubara tersebut akan bercampur dengan klinker dan akan
berpengaruh pada kualitas semen. Pada proses pembakaran bata, kandungan abu
batubara yang terlalu banyak akan menyumbat celah-celah susunan antar bata,
berakibat akan menggangu penyebaran panas sebagai hasil pembakaran.
Proses pembentukan batubara terdiri dari dua tahap yaitu tahap biokimia
(penggambutan) dan tahap geokimia (pembatubaraan). Tahap penggambutan
(peatification) adalah tahap dimana sisa-sisa tumbuhan yang terakumulasi tersimpan dalam kondisi reduksi di daerah rawa dengan sistem pengeringan yang
buruk dan selalu tergenang air pada kedalaman 0,5 – 10 meter. Material tumbuhan
NH3 untuk menjadi humus. Selanjutnya oleh bakteri anaerobik dan fungi diubah
menjadi gambut.
Tahap pembatubaraan (coalification) merupakan gabungan proses biologi, kimia, dan fisika yang terjadi karena pengaruh pembebanan dari sedimen yang
menutupinya, temperatur, tekanan, dan waktu terhadap komponen organik dari
gambut. Pada tahap ini persentase karbon akan meningkat, sedangkan persentase
hidrogen dan oksigen akan berkurang. Proses ini akan menghasilkan batubara
dalam berbagai tingkat kematangan material organiknya mulai dari lignit, sub
bituminus, bituminus, semi antrasit, antrasit, hingga meta antrasit.
Berikut adalah beberapa penggolongan batubara secara umum dan
berdasarkan nilai kalor batubara.
1. Klasifikasi secara Umum
Secara umum batubara digolongkan menjadi 3 tingkatan yaitu, anthracite, bituminous coal dan sub bituminous coal, lignite dan peat (gambut).
a. Anthracite
Warna hitam, sangat mengkilat, kompak, kandungan karbon sangat tinggi,
kandungan sulfur sangat sedikit. Kandungan air sangat sedikit dan kandungan
abu sangat sedikit.
b. Bituminous/sub bituminous coal
Warna hitam mengkilat, kurang kompak, kandungan karbon relatif tinggi,
nilai kalor tinggi, kandungan air sedikit, kandungan abu sedikit dan
kandungan sulfur sedikit.
c. Lignite/peat (brown coal)
Warna hitam, sangat rapuh, kandungan karbon sedikit, nilai kalor rendah,
kandungan air tinggi, kandungan abu banyak dan kandungan sulfur banyak.
2. Klasifikasi berdasarkan atas nilai kalor
b. Batubara tingkat menengah (moderate rank) meliputi low volatile bituminous coal, high volatile coal.
c. Batubara tingkat rendah (low rank) meliputi sub bituminous coal dan lignit.
2.5 Sifat – sifat Bahan Baku dan Produk 2.5.1 Bahan Baku
A. Batubara ( Subbituminous)
1) Mengandung :
- C (Carbon) : 76,24%
- H (Hidrogen) : 4,85%
- N (Nitrogen) : 1,34%
- S (Sulfur) : 1,38%
- O (Oxigen) : 4,84%
- Ash(Abu) : 8,02%
- Air : 2,82%
2) Ukuran butiran :
- kurang dari 2,38 mm : 19,84%
- 2,38 – 32 mm : 75,49%
- 32 – 50 mm : 4,53%
- lebih dari 50 mm : 0,14%
2.5.2 Produk
A. Hidrogen (H2)
1) Sifat Fisika:
1. Wujud : Gas
2. Densitas : 0,08988 g/L (0oC, 101, 325 kPa)
3. Titik Leleh : 14,01 K
4. Titik Didih : 20,28 K
5. Titik Kritis : 13, 8033 K, 7, 042 kPa
2) Sifat Kimia:
1. Gas hidrogen sangat mudah terbakar dan akan terbakar pada
konsentrasi serendah 4% H2 di udara bebas. Hidrogen terbakar menurut
persamaan kimia:
2 H2(g) + O2(g) → 2 H2O(l) + 572 kJ (286 kJ/mol)
2. H2 bereaksi secara langsung dengan unsur-unsur oksidator. Ia bereaksi
dengan spontan dan hebat pada suhu kamar dengan
menghasilkan hidrogen halida berupa
H2(g)+ Cl2(s) → 2 HCl(g)
B. Karbonmonoksida (CO)
1) Sifat Fisika :
1. Wujud : Gas
2. Densitas : 1, 250 g/L (0oC, 101, 325 kPa)
3. Titik Leleh : 68 K
4. Titik Didih : 81 K
5. Momen Dipol : 0,112−31 C·m)
2) Sifat Kimia :
1. CO adalah
untuk menghasilkan CO dari dehidrasi asam format.
2.CO juga merupakan hasil sampingan dari reduksi bijih logam oksida
dengan karbon:
MO + C → M + CO ΔH = 131 kJ/mol
C. Karbondioksida (CO2)
1) Sifat Fisika:
1. Wujud : Gas
2. Densitas : 1, 98 g/L (0oC, 101, 325 kPa)
3. Titik Leleh : 216 K
4. Titik Didih : 195 K
5. Momen Dipol : Nol
6. Viskositas : 0, 07 cP pada -78oC
2) Sifat Kimia:
1. CO2 dapat dihasilkan melalui pembakaran dari semua bahan bakar yang
mengandung karbon, seperti
contohnya reaksi antara metana dan oksigen:
CH4 + 2 O2→ CO2 + 2 H2O
2.
→ 2 CO2 + 2 C2H5OH
D. Metana (CH4)
1) Sifat Fisika:
1. Berat Molekul : 16,04 gr/gmol
2. Nilai Bakar : 995 Btu/ft3 (pada 600F, 30in Hg) 3. Titik Didih : -161,40C
4. Titik Lebur : -182,60C
2) Sifat Kimia:
1. Dapat bereaksi dengan golongan halogen. Reaksi:
CH4 + X2 CH3X + HX ; X = F, Cl, Br, I
2. Radical Exchanges Reaction
CH4 + Cl- CH- + HCl + 14 KJ
3. Radical Extermination Reaction
2 Cl- Cl2 + 239 KJ
CH- + Cl- CH3Cl + 339 KJ
2 CH3- CH3CH3 + 347 KJ
E. Nitrogen (N2)
1) Sifat Fisika:
1. Fase : Gas
2. Berat Molekul : 28 gr/gmol
3. Densitas : 1, 251 g/L (0oC, 101, 325 kPa)
4. Titik Didih : 77, 36 K
5. Titik Lebur : 63, 15 K
6. Titik Kritis : 126, 21 K, 3, 39 MPa
7. Struktur Kristal : Heksagonal
2) Sifat Kimia:
1. Nitrogen bereaksi dengan elemen litium pada keadaan STP
menghasilkan litium nitrit. Reaksi:
6 Li + N2 2 Li3N
2. Nitrogen bereaksi dengan magnesium menghasilkan magnesium nitrit.
Reaksi:
3. Jika nitrogen bereaksi spontan dengan regensia, bentuk tranformasinya
disebut dengan fiksasi nitrogen.
F. Hidrogen Sulfida (H2S)
1) SifatFisika:
1. Berat molekul : 34,076 gr/gmol
2. Densitas : 0,79 gr/l (600F, 14,7 psia)
3. Titik didih : -60,280C
4. Titik Beku : -85,50C
5. Tekanan kritis : 1,304 psia
2) Sifat Kimia:
1. Hidrogen sulfida merupakan
aqueous (mengandung air) menjad+ dan
hidrosulfid HS−:
H2S → HS− + H+
−7 mol/L
pKa = 6.89.
2. Hidrogen sulfida merupakan
terkait dengan2O) karen
golongan yang sama di
G. Metanol (CH3OH)
1) Sifat Fisika:
1. Fase : Cairan jernih pada suhu kamar
2. Berat Molekul : 32 gr/gmol
3. Titik didih : 65 oC
4. Titik lebur : -97 oC
6. Densitas pada : 0,796 gr/ml (0oC, 101, 325 kPa) 7. Tekanan kritis : 78,5 atm
8. Temperatur kritis : 240 oC
(Perry, 1997; Othmer, 1981)
2) Sifat Kimia:
1. Tidak memiliki sifat adisi yang kuat
2. Klor dan brom dapat mensubstitusi atom H dari metanol
3. Sulfonasi dengan asam sulfat berasap membentuk metanol sulfonat
4. Bereaksi dengan Na membentuk gas H2 dan garam Na metanolat
5. Termasuk golongan senyawa kimia beracun
6. Oksidasi dengan oksiditor kuat (KMnO4 dalam asam) menghasilkan
asam formiat dan dapat teroksidasi lebih lanjut membentuk CO2 dan
H2O
7. Merupakan pelarut yang baik untuk senyawa organik
(Othmer, 1981)
H. Air (H2O)
1) Sifat Fisika:
1. Tidak berbau, berasa, dan tidak berwarna
2. Berbentuk heksagonal dalam keadaan padat
3. Berat molekul : 18 gr/gmol
4. Titik beku : 0 oC ( pada 1 atm)
5. Densitas : 995,68 kg/m3
6. Viskositas : 8,949 mP (pada kondisi standar, 1 atm)
7. Koefisien difusi : 2,57 x 10-5 cm2/dt 8. Konstanta disosiasi : 10-4
9. Panas ionisasi, : 55,71 Kj/mol
2) Sifat Kimia:
1. Bereaksi dengan karbon menghasilkan metana, hidrogen, karbon
dioksida, monoksida membentuk gas sintetis (dalam proses gasifikasi
batubara)
2. Bereaksi dengan kalsium, magnesium, natrium dan logam-logam reaktif
lain membebaskan H2
3. Air bersifat amfoter
4. Bereaksi dengan kalium oksida, sulfur oksida membentuk basa kalium
dan asam sulfat.
5. Dengan anhidrid asam karboksilat membentuk asam karboksilat.
(Othmer, 1981 )
I. Udara (O2)
1) Sifat Fisika:
1. Fase : Gas
2. Berat Molekul : 32 gr/gmol
3. Titik didih : 90,20 K
4. Titik lebur : 54,36 K
5. Kalor Peleburan : 0,444 Kj/mol
6. Kalor Penguapan : 6,82 Kj/mol
7. Kapasitas Kalor : 29,378 J/mol.K
8. Densitas : 1,429 gr/L (0oC, 101, 325 kPa)
2) Sifat Kimia :
1. Dapat bereaksi dengan metana menghasilkan karbondioksida dan air.
Reaksi:
CH4 + 2 O2→ CO2 + 2 H2O
2. Dapat membakar gas hidrogen berkonsentrasi 4% di udara bebas.
Reaksi:
2 H2(g) + O2(g) → 2 H2O(l) + 572 kJ (286 kJ/mol)
J. Monoetanolamine (MEA)
1) Sifat Fisika:
1. Fase : Cairan tidak berwarna
2. Berat Molekul : 61,06 gr/mol
3. Titik Beku : 10,5 0C
4. Spesifik Gravity : 1,017
5. Titik Didih : 170 0C
6. Densitas : 2,1 g/liter ( pada 00C, 1 atm)
7. pH : 12
2) Sifat Kimia:
1. Bereaksi dengan selulosa nitrat menghasilkan api dan beresiko timbul
ledakan
2. Terurai jika dipanaskan dan menghasilkan racun serta gas pengkorosi
termasuk N2O
3. Sangat reaktif terhadap asam kuat dan oksidator kuat
2.6 Deskripsi Proses
Proses produksi metanol adalah salah satu proses petrokimia yang paling
sederhana dengan fasilitas produksi yang aman dan terpercaya dalam
pengoperasiannya. Secara umum, pembuatan metanol untuk tujuan komersial
meliputi 3 tahapan utama, yaitu persiapan gas umpan dengan proses gasifikasi
batu bara, sintesis metanol (proses utama) dan penanganan produk akhir
(Schmidt, 2005);
1. Persiapan gas umpan dengan proses gasifikasi batu bara.
Tahap ini meliputi produksi gas hidrogen melalui proses gasifikasi batu
Pada proses gasifikasi besarnya perbandingan O2 terhadap batubara
(kg/kg) adalah sebesar 0,23 dan batubara terhadap steam (kg/kg) sebesar 1,175.
Reaktor yang digunakan adalah jenis fixed bed dengan proses lurgi untuk
menghasilkan H2 dalam jumlah yang paling besar. Ukuran partikel batubara
adalah 3- 30 mm dengan subbituminous coal sebagai bahan baku pada temperatur gasifikasi 8000C dan tekanan 13 atm (Swargina, 2006). Besarnya waktu tinggal dalam reaktor gasifikasi adalah 1 jam (Sukandarrumidi, 2006).
Tahapan selanjutnya adalah pemisahan zat-zat pengotor dan racun katalis
dari aliran gas hidrogen. Zat racun katalis berupa karbon monoksida, karbon
dioksida, dan hidrogen sulfida (H2S). Tahapan purifikasi zat racun katalis tersebut
diawali dengan konversi metana oleh steam menjadi karbon monoksida dan
hidrogen yang berlangsung dalam steam methane reformer (SMR). Karbon
monoksida hasil gasifikasi dan konversi metana dalam aliran gas kemudian
diubah menjadi hidrogen dan karbon dioksida dengan menggunakan yang
melibatkan steam dan katalis Cu-Zn. Karbon dioksida dan H2S dalam aliran gas
kemudian diumpankan dalam absorber dengan monoetanolamine 20% sebagai
absorben, dimana seluruh hidrogen sulfida (H2S) dalam aliran gas terserap.
2. Proses utama
Gas sintesis yang di hasilkan dari gasifier memiliki kondisi yaitu tekanan 13 atm dan temperatur 8000C (1073 K). Reaksi berlangsung cepat dengan waktu tinggal 10 detik dan konversi 99% (Indala,2001). Jenis reaktor yang digunakan
adalah jenis fixed bed dengan katalis multikomponen. (Walas, 1988).
3. Penanganan Produk akhir
Gas metanol bersama dengan hidrogen dan nitrogen yang tidak terkonversi
dan gas inert didinginkan sehingga terjadi kondensasi gas metanol menjadi cairan
metanol sementara gas yang tidak terkonversi dan inert masih berada dalam fase
gas. Proses ini berlangsung pada temperatur 250C.
Metanol cair yang dihasilkan disimpan dalam tangki penyimpanan
sebelum didistibusikan atau digunakan untuk proses selanjutnya. Gas sisa dari
reaksi yang sebagian besar merupakan hidrogen dan nitrogen disimpan dalam
Metanol cair yang dihasilkan disimpan dalam tangki penyimpanan
sebelum didistibusikan atau digunakan untuk proses selanjutnya. Gas sisa dari
reaksi yang sebagian besar merupakan hidrogen dan nitrogen dialirkan ke IGCC
digunakan sebagai turbin gas (Gary, 2006).
4. Unit Pengolahan Limbah
Limbah dari suatu pabrik harus diolah sebelum dibuang ke lingkungan
atau atmosfer, karena limbah tersebut mengandung bermacam-macam zat yang
dapat membahayakan alam sekitar maupun manusia itu sendiri. Demi kelestarian
lingkungan hidup, maka setiap pabrik harus mempunyai unit pengolahan limbah.
Dalam pra rancangan pabrik pembuatan metanol dari batu bara dengan
proses gasifikasi ini tidak menghasilkan limbah cair melainkan limbah padat.
Adapun sumber limbah padat pabrik pembuatan metanol ini meliputi fly ash.
Fly ash yang dihasilkan dari pembuatan metanol ini apabila dibuang langsung ke lingkungan lambat laun akan membentuk gas metana yang dapat
menyebabkan ledakan, oleh karena itu diperlukan penanganan terhadap limbah
Fly ash. Fly ash dapat dimanfaatkan menjadi campuran beton, campuran aspal,
dan batako, 2006).
Dalam pra rancangan pabrik pembuatan metanol dari batu bara dengan
proses gasifikasi ini, limbah padat yang dihasilkan direncanakan akan dijual ke
BAB III
NERACA MASSA
Kapasitas produksi : 70.000 ton/tahun
Basis perhitungan : 1 jam operasi
Satuan operasi : kg/jam
Dibawah ini merupakan neraca bahan pada masing-masing alat proses
pada pra rancangan pabrik pembuatan metanol dari batubara dengan proses
gasifikasi.
1. Unit Pemisah Udara (ASU) (G-502)
Komponen Laju alir masuk Laju alir keluar
(3) (4) (6)
N2 7183,6632 7083,5324 94,79864
O2 2182,1856 8,1024 2180,36889
Total 9365,8488 9365,8488
2. Crusher (C-301)
Komponen Laju alir masuk Laju alir keluar
(8) (9)
Batubara 9.479,86472 9.479,86472
3. Gasifier (B-401)
Komponen Laju alir masuk Laju alir keluar
(6) (10) (11) (12) (13)
Batu bara - 9.479,86472 - - -
Steam - - 11.138,84105 - -
Oksigen 2180,36889 - - - -
H2 - - - - 802,99564
CO - - - - 5188,58722
CO2 - - - - 13589,15701
CH4 - - - - 1647,17055
N2 94,79864 - - 576,50969
H2S - - - - 350,02374
Ash - - - 739,42945 -
Total 22893.8733 22893.8733
4. Steam Methane Reforming (R-701)
Komponen Laju alir masuk Laju alir keluar
(13) (14)
(15)
H2 802,99564 - 1358,915701
CO 5188,58722 - 7782,880834
CO2 13589,15701 - 13589,15701
CH4 1647,17055 - 164,7170547
N2 576,50969 - 576,5096915
H2S 350,02374 - 350,0237413
H2O - 1667,760179 -
5. Absorber (D-801)
Komponen Laju alir masuk Laju alir keluar
(17) (18) (19) (27)
H2 1358,915701 - 1358,915701
CO 7782,880834 - 7782,880834
CO2 13589,15701 13542,95388 46,20313386
CH4 164,7170547 - 164,7170547
N2 576,5096915 - 576,5096915
H2S 350,0237413 350,0237413 -
MEA (20%) - 31808,92214 31808,92214 -
Total 55631,12617 55631,12617
6. Stripper (D-802)
Komponen Laju alir masuk Laju alir keluar
(21) (22) (24)
CO2 13542,95388 13542,95388 -
H2S 350,0237413 350,0237413 -
MEA (20%) 31.808,92214 - 31.808,92214
H2O 2085,83096 - 37.544,95728
7. Reaktor Metanol (R-702)
Komponen Laju alir masuk Laju alir keluar
(28) (30) (31)
H2 1358,915701 - 251,9565602
CO 7782,880834 - 77,82880834
CO2 46,2031338 - 0,462031338
CH4 164,7170547 - 164,7170547
N2 576,5096915 - 576,5096915
CH3OH - - 8839
H2O - - 18,71226922
ZnCr-Cu - 14731,66667 14731,66667
Total 24660,89309 24660,89309
8. Cyclone (H-111)
Komponen Laju alir masuk Laju alir keluar
(31) (29) (32)
H2 251,9565602 - 251,9565602
CO 77,82880834 - 77,82880834
CO2 0,462031338 - 0,462031338
CH4 164,7170547 - 164,7170547
N2 576,5096915 - 576,5096915
CH3OH 8839 - 8839
H2O 18,71226922 - 18,71226922
ZnCr-Cu 14731,66667 14731,66667 -
9. Tangki Separator (D-803)
Komponen Laju alir masuk Laju alir keluar
(34) (35) (36)
H2 251,9565602 251,9565602 -
CO 77,82880834 77,82880834 -
CO2 0,462031338 0,462031338 -
CH4 164,7170547 164,7170547 -
N2 576,5096915 576,5096915 -
CH3OH 8839 - 8839
H2O 18,71226922 - 18,71226922
BAB IV
NERACA ENERGI
Basis perhitungan : 1 jam operasi
Satuan operasi : kJ/jam
Temperatur basis : 25oC
1. Gasifier (B-401)
No Komponen Panas Masuk Panas Keluar
1. Umpan 10.667.440,13
2. Produk 115.977.014,2
3. Steam 107.636.475,4
4. Udara 1.771.636,15
5. Ash -555.265,1805
Total 116.532.279,4 116.532.279,4
2. Heater (E-601)
No Komponen Panas Masuk Panas Keluar
1. Umpan 47.010,57898
2. Produk 4.383.097,46
3. Steam 4.336.086,081
Total 4.383.097,46 4.383.097,46
3. Steam Methane Reformer (R-701)
No Komponen Panas Masuk Panas Keluar
1. Umpan 38.298.540,64
2. Produk 5.815.439,23
3. ∆ Hr 32.483.101.41
4. Cooler (E-602)
No Komponen Panas Masuk Panas Keluar
1. Umpan 5.815.439,23
2. Produk 528.588,4451
3. Air Pendingin 4.807.983,535
Total 5.336.571,98 5.336.571,98
5. Heat Exchanger (E-603)
No Komponen Panas Masuk Panas Keluar
1. Umpan 3.332.029,447 58.102.028,55
2. Produk 105.609.974,6 50.839.975,5
Total 108.942.004 108.942.004
6. Cooler (E-604)
No Komponen Panas Masuk Panas Keluar
1. Umpan 50.839.975,5
2. Produk 3.177.470,993
3. Air Pendingin 47.664.504,51
Total 50.839.975,5 50.839.975,5
7. Reaktor Metanol (R-702)
No Komponen Panas Masuk Panas Keluar
1. Umpan 4.433.909,471
2. Produk 18.009.449,13
3. ∆ Hr -13.408.163,71
4. Air pendingin 167.375,949
8. Kondensor (E-605)
No Komponen Panas Masuk Panas Keluar
1. Umpan 18.009.449,13
2. Produk 273.041,7956
3. Air pendingin 17.736.407,33
BAB V
SPESIFIKASI PERALATAN
Proses pembuatan metanol dari batubara dengan proses gasifikasi, dapat dibagi
menjadi 4 unit proses, yaitu:
1. Unit Persiapan Bahan Baku
2. Sintesa
3. Pemisahan Produk Utama dan Produk Samping
4. Penyempurnaan Produk
Di bawah ini merupakan alat-alat proses yang digunakan pada tiap-tiap unit
proses.
5.1 Unit Persiapan Bahan Baku
5.1.1 Gudang batu bara (F-101)
Fungsi = Tempat penyimpanan batu bara sebelum diproses
selama 30 hari
Bentuk = Prisma segi empat beraturan
Jumlah = 1 Unit
Bahan Konstruksi = Beton
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300 C = 303 K
Tinggi Gudang = 10,439 m
Panjang = Lebar = 20,878 m
5.1.2 Crusher (C-301)
Fungsi = Memperkecil ukuran batubara hingga 3-30 mm
Jenis = Roll Crusher
Jumlah unit = 1 Unit
Bahan Konstruksi = Carbon Steel SA-283 Grade C
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300C = 303 K
5.1.3 Bucket Elevator (J-201)
Fungsi = Mengangkat batubara dari gudang ke Crusher
Jenis = Spaced-Bucket Centrifugal-Discharge Elevator
Jumlah unit = 50 Unit
Bahan Konstruksi = Malleable-Iron
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300C = 303 K
Daya = 0,0574 Hp
5.1.4 Belt Conveyor (J-202)
Fungsi = Mengangkat batubara dari Crusher ke Gasifier
Jenis = Belt Conveyor
Bahan Konstruksi = Carbon Steel SA-283 Grade C
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300C = 303 K
Daya = ¾ Hp
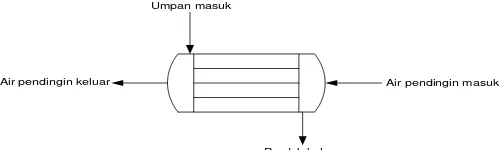
5.1.5 Gasifier (B-401)
Fungsi = Membakar batubara menjadi gas produser (H2,CO,CO2,
CH4, N2, dan H2S) dengan bantuan steam dan
O2.
Jenis = Fixed bed ellipsoidal
Jumlah = 2 Unit
Bahan Konstruksi = Stainless steel, type-430F
Kondisi Operasi = - P = 13 atm = 191,048 psi
- T = 8000C = 1073 K
Tinggi Tangki = 17,654 m
Volume = 989,811 m3
Tebal Dinding Tangki = 1 5/8 in
5.1.6 Kompresor Udara (G-501)
Fungsi = Menaikkan tekanan udara sebelum masuk ke membran
pemisah
Jenis = Multistage Rreciprocating Compressor
Jumlah = 1 Unit dengan 3 stages
Bahan Konstruksi = Carbon steel
Kondisi Operasi = - P = 1 atm = 101,325 kPa
- T = 1150C = 388 K
Daya yang dibutuhkan= 1107,64 Hp
5.1.7 Heater (E-601)
Fungsi = Memanaskan udara umpan membran
Jenis = 1-2 shell and tube
Jumlah unit = 1
Kondisi Operasi = Fluida Dingin:
- Tmasuk = 300 C
- TKeluar = 4480 C
Fluida Panas:
- Tmasuk = 6000 C
- TKeluar = 3000 C
Diameter tube = ¾ in
Pitch (PT) = 1 in triangular pitch
Jenis tube = 18 BWG
Passes = 6
Jumlah tube = 172
Panjang tube = 15 ft
5.1.8 Membran (G-502)
Fungsi = Memisahkan oksigen dari udara
Jumlah = 1 Unit
Bahan Konstruksi = Carbon steel SA-283 Grade C
5.1.9 Tangki Penyimpanan Larutan Monoetanolamin (F-104)
Fungsi = Wadah Penyimpanan MEA untuk kebutuhan 1 hari
Bentuk = Silinder vertikal dengan alas datar dengan tutup
ellipsoidal
Jumlah = 1 Unit
Bahan Konstruksi = Carbon Steel SA-285 Grade C
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 380C = 311 K
Tinggi Tangki = 20,175 m
Volume = 1989,7332 m3
Tebal Dinding Tangki = 1 in
Tebal Tutup Tangki = 1 in
5.2 Unit Sintesa
5.2.1 Steam Methane Reformer (R-701)
Fungsi = Mengkonversi CH4 menjadi CO dan H2 dengan
bantuan steam
Jenis = Fixed bed ellipsoidal
Jumlah = 1 Unit
Bahan Konstruksi = Stainless steel, type-430F
Kondisi Operasi = - P = 13 atm = 191,048 psi
- T = 8000C = 1073 K
Tinggi Reaktor = 5,8364 m
Volume = 35,7637 m3
Tebal Dinding Reaktor= 7/16 in
Tebal Tutup Reaktor = 7/16 in
5.2.2 Ekspander (G-504)
Fungsi = Menurunkan tekanan produk Steam Methane Reformer
sebelum masuk ke Absorber
Jenis = Single Stage Expander
Bahan Konstruksi = Carbon steel
Kondisi Operasi = - Pmasuk = 13 atm = 1.317,225 Kpa
- PKeluar = 1 atm = 101,325 Kpa
Daya = 2.022,19 Hp
5.2.3 Cooler (E-602)
Fungsi = Mendinginkan gas produk Steam Methane Reformer
Jenis = 2-4 shell and tube
Jumlah unit = 1
Kondisi Operasi = Fluida Dingin:
- Tmasuk = 300 C
- TKeluar = 600 C
Fluida Panas:
- Tmasuk = 5000 C
- TKeluar = 380 C
Diameter tube = 1 ¼ in
Pitch (PT) = 1 9/16 in square pitch
Passes = 4
Jenis tube = 16 BWG
Jumlah tube = 425
Panjang tube = 30 ft
5.2.4 Absorber (D-801)
Fungsi = Menyerap Gas CO2 dan H2S
Jenis = Packed tower , berbentuk silinder dengan 2 head
ellipsoidal
Jumlah = 1 Unit
Bahan Konstruksi = Carbon steel SA-283 Grade C
Kondisi Operasi = - P = 1 atm = 14,696 psi
- T = 380C = 311 K
Tinggi Absorber = 2,0602 m
Tebal Tutup Tangki = 1/8 in
5.2.5 Exchanger (E-603)
Fungsi = Mempertukarkan panas antara aliran bawah Stripper
dengan aliran bawah Absorber
Jenis = 2-4 shell and tube
Jumlah unit = 1
Kondisi Operasi = Fluida Dingin:
- Tmasuk = 380 C
- TKeluar = 1000 C
Fluida Panas:
- Tmasuk = 1120 C
- TKeluar = 1000 C
Diameter tube = 1 in
Pitch (PT) = 1 ¼ in square pitch
Passes = 4
Jenis tube = 8 BWG
Jumlah tube = 376
Panjang tube = 25 ft
5.2.6 Cooler (E-604)
Fungsi = Mendinginkan MEA kembali ke Absorber
Jenis = 3-6 shell and tube
Jumlah unit = 1
Kondisi Operasi = Fluida Dingin:
- Tmasuk = 300 C
- TKeluar = 750 C
Fluida Panas:
- Tmasuk = 1000 C
- TKeluar = 380 C
Diameter tube = 1 in
Jenis tube = 18 BWG
Passes = 4
Jumlah tube = 632
Panjang tube = 36 ft
5.2.7 Stripper (D-802)
Fungsi = Melucuti gas CO2dan H2S dari larutan MEA
Jenis = Fixed bed ellipsoidal
Bentuk = Berdiri Tegak
Jumlah = 1 Unit
Bahan Konstruksi = Carbon steel SA-283 Grade C
Kondisi Operasi = - P = 1 atm = 14,696 psi
- T = 1150C = 388 K
Tinggi Stripper = 4,8768 m
Tebal Dinding Tangki = 3/16 in
Tebal Tutup Tangki = 1/8 in
Tebal Dinding Jaket = 3/16 in
5.2.8 Kompresor (G-505)
Fungsi = Menaikkan tekanan gas masuk ke reaktor sekaligus
menaikkan suhu gas umpan dari 311 K menjadi 450 K
Jenis = Multi Stage Reciprocating Compressor
Bahan Konstruksi = Carbon steel
Kondisi Operasi = - Pmasuk = 1 atm = 101,325 Kpa
- PKeluar = 52 atm = 5.268,9 Kpa
Daya = 5623,01 Hp
5.2.9 Reaktor Metanol (R-702)
Fungsi = Tempat terjadinya reaksi pembuatan metanol
Jenis = Fixed bed ellipsoidal
Jumlah = 1 Unit
Kondisi Operasi = - P = 50 atm
- T = 2500C = 523 K
Tinggi Reaktor = 4,7391 m
Volume = 19,145 m3
Tebal Dinding Reaktor= 1 7/8 in
Tebal Tutup Reaktor = 1 7/8 in
Tebal Dinding Jaket = ¼ in
5.2.10 Cyclone (H-111)
Fungsi = Untuk Menangkap katalis yang keluar dari Reaktor
Jenis = Cyclone Separator
Jumlah unit = 1 Unit
Bahan Konstruksi = Carbon Steel
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300C = 303 K
Tinggi = 1,1495 ft
Lebar = 0,4598 ft
Diameter = 1,8392 ft
5.2.11 Screw Conveyor (J-203)
Fungsi = Mengangkat Katalis ke Reaktor
Jumlah unit = 1 Unit
Bahan Konstruksi = Malleable-iron
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300C = 303 K
Kapasitas = 3,2667 kg/jam
Daya = 3,0759 Hp
5.2.12 Pompa Absorber (L-901)
Fungsi = Memompa MEA bersama gas yang terserap menuju
Stripper
Bahan Konstruksi = Commercial Steel
Kondisi Penyimpanan = - T = 380C = 311 K
Daya = 2 Hp
5.1.13 Pompa Stripper (L-902)
Fungsi = Memompa MEA dari Stripper menuju Absorber
Jenis = Pompa sentrifugal
Bahan Konstruksi = Commercial Steel
Kondisi Penyimpanan = - T = 380C = 311 K
Daya = 1 Hp
5.1.14 Pompa MEA (L-903)
Fungsi = Memompa MEA dari tangki penyimpanan menuju
Absorber
Jenis = Pompa sentrifugal
Bahan Konstruksi = Commercial Steel
Kondisi Penyimpanan = - T = 380C = 311 K
Daya = 3,245 Hp
5.3 Pemisahan Produk Utama dan Produk Samping
5.3.1 Kompresor (G-503)
Fungsi = menurunkan tekanan produk membran sebelum masuk
ke Intergated Gasification Combined Circle (IGCC).
Jenis = Single Stage Expander
Jumlah = 1 Unit dengan 1 stages
Bahan Konstruksi = Carbon steel
Kondisi Operasi = - Pmasuk = 13 atm = 1.317,225 Kpa
- PKeluar = 1 atm = 101,325 Kpa
5.4 Unit Penyempurnaan Produk
5.4.1 Tangki Penyimpanan Metanol (F-104)
Fungsi = Wadah Penyimpanan MEA untuk kebutuhan 1 hari
Bentuk = Silinder vertikal dengan alas datar dengan tutup
ellipsoidal
Jumlah = 5 Unit
Bahan Konstruksi = Carbon Steel SA-285 Grade C
Kondisi Penyimpanan = - P = 1 atm = 14,696 psi
- T = 300C = 303 K
Tinggi Tangki = 15,9198 m
Volume = 984,9943 m3
Tebal Dinding Tangki = 5/8 in
Tebal Tutup Tangki = 5/8 in
5.4.2 Kondensor (E-605)
Fungsi = Mendinginkan gas produk keluaran reactor pembuatan
metanol
Jenis = 2-4 shell and tube
Jumlah unit = 1
Kondisi Operasi = Fluida Dingin:
- Tmasuk = 300 C
- TKeluar = 650 C
Fluida Panas:
- Tmasuk = 2500 C
- TKeluar = 350 C
Diameter tube = 1 in
Pitch (PT) = 1 ¼ in square pitch
Passes = 4
Jenis tube = 18 BWG
Jumlah tube = 430
5.4.3 Separator (D-803)
Fungsi = memisahkan metanol dari gas impuritis lainnya.
Bentuk = silinder vertikal dengan alas dan tutup ellipsoidal.
Bahan = Carbon steel, SA – 285 Gr. C
Jumlah = 1 unit
Kondisi Operasi = - Temperatur (T) = 30 0C
- Tekanan ( P) = 1 atm = 14,696 psia
Volume Tangki = 15,3353 m3
Tinggi Tangki = 4,4 m
Tebal Tangki = 3/16 in
BAB VI
INSTRUMENTASI DAN KESELAMATAN KERJA
6.1 Instrumentasi
Instrumentasi merupakan salah satu bagian yang penting dalam suatu pabrik.
Instrumentasi adalah peralatan yang dipakai di dalam suatu proses control yang
digunakan untuk mengatur jalannya suatu proses sehingga diperoleh hasil yang
diinginkan. Dengan adanya alat kontrol atau pengendali yang baik, maka dapat
diketahui dan dikoreksi segala kesalahan ataupun penyimpangan proses yang
mungkin terjadi, karena pada dasarnya, tujuan pengendalian tersebut adalah agar
kondisi proses di pabrik mencapai tingkat kesalahan (error) yang paling minimum sehingga produk dapat dihasilkan secara optimal (Perry dan Green, 1999).
Variabel – variabel yang biasanya dikontrol atau diukur oleh alat-alat
instrumentasi, antara lain:
1. Variabel Utama:
• Indikator dan kendali temperatur yaitu alat untuk mengetahui dan
mengendalikan suhu operasi agar sesuai dengan yang diinginkan.
• Indikator dan kendali tekanan yaitu alat untuk mengetahui dan
mengendalikan tekanan operasi agar sesuai dengan yang diinginkan.
• Indikator dan kendali ketinggian yaitu alat untuk mengetahui dan
mengendalikan ketinggian cairan agar sesuai dengan yang diinginkan.
• Pengendali aliran yaitu alat untuk mengendalikan/mengatur aliran sesuai dengan yang diinginkan
Pengukuran nilai keempat variabel di atas menggunakan bantuan sensor
untuk mendeteksi nilai masing-masing variabel proses.
2. Variabel Tambahan:
• Konsentrasi : - Cairan (pH)
- Gas
• Kepadatan (density) dan spesific gravity
• Kekeruhan zat cair (turbidity) dan derajat warna zat cair (clarity) • dan masih banyak lagi.
Untuk pengukuran nilai variabel proses di atas dapat digunakan sebuah
penganalisis (analyzer).
Menurut sifatnya konsep dasar pengendalian proses ada dua jenis, yaitu:
1. Pengendalian secara manual
Tindakan pengendalian yang dilakukan oleh manusia. Sistem pengendalian
ini merupakan sistem yang ekonomis karena tidak membutuhkan begitu banyak
instrumentasi dan instatalasinya. Namun pengendalian ini berpotensi tidak praktis
dan tidak aman karena sebagai pengendalinya adalah manusia yang tidak lepas
dari kesalahan.
2. Pengendalian secara otomatis
Berbeda dengan pengendalian secara manual, pengendalian secara otomatis
menggunakan instrumentasi sebagi pengendali proses, namun manusia masih
terlibat sebagai otak pengendali. Banyak pekerjaan manusia dalam pengendalian
secara manual diambil alih oleh instrumentasi sehingga membuat sistem
pengendalian ini sangat praktis dan menguntungkan.
Pada dasarnya sistem pengendalian terdiri dari :
1. Sensing Elemen (Primary Element)
Elemen yang merasakan (menunjukkan) adanya perubahan dari harga
variabel yang diukur.
2. Elemen pengukur (measuring element)
Elemen pengukur adalah suatu elemen yang sensitif terhadap adanya
perubahan temperatur, tekanan, laju aliran, maupun tinggi fluida. Perubahan ini
merupakan sinyal dari proses dan disampaikan oleh elemen pengukur ke elemen
pengontrol.
3. Elemen pengontrol (controlling element)
Elemen pengontrol yang menerima sinyal kemudian akan segera mengatur
perubahan-perubahan proses tersebut sama dengan nilai set point (nilai yang diinginkan). Dengan demikian elemen ini dapat segera memperkecil ataupun
4. Elemen pengontrol akhir (final control element)
Elemen ini merupakan elemen yang akan mengubah masukan yang keluar
dari elemen pengontrol ke dalam proses sehingga variabel yang diukur tetap
berada dalam batas yang diinginkan dan merupakan hasil yang dikehendaki.
Pengendalian peralatan instrumentasi dapat dilakukan secara otomatis dan
semi otomatis. Pengendalian secara otomatis adalah pengendalian yang dilakukan
dengan mengatur instrumen pada kondisi tertentu, bila terjadi penyimpangan variabel
yang dikontrol maka instrumen akan bekerja sendiri untuk mengembalikan variabel
pada kondisi semula, instrumen ini bekerja sebagai controller. Pengendalian secara semi otomatis adalah pengendalian yang mencatat perubahan-perubahan yang terjadi
pada variabel yang dikontrol. Untuk mengubah variabel-variabel ke nilai yang
diinginkan dilakukan usaha secara manual, instrumen ini bekerja sebagai pencatat
(recorder) atau petunjuk (indicator).
Faktor-faktor yang perlu diperhatikan dalam instrumen – instrumen adalah
(Peters dan Timmerhaus, 2004) :
1. Range yang diperlukan untuk pengukuran 2. Level instrumentasi
3. Ketelitian yang dibutuhkan
4. Bahan konstruksinya
5. Pengaruh pemasangan instrumentasi pada kondisi proses
6.1.1 Tujuan Pengendalian
Tujuan perancangan sistem pengendalian dari pabrik pembuatan methanol
dari gasifikasi batubara adalah sebagai keamanan operasi pabrik yang mencakup :
− Mempertahankan variabel – variabel proses seperti temperatur dan tekanan tetap berada dalam rentang operasi yang aman dengan harga toleransi yang
kecil.
− Mendeteksi situasi berbahaya kemungkinan terjadinya kebocoran alat
6.1.2 Jenis – Jenis Pengendalian dan Alat Pengendali ( Instrumen )
Sistem pengendalian yang digunakan pada pabrik ini menggunakan dan
mengkombinasikan beberapa tipe pengendalian sesuai dengan tujuan dan
keperluannya :
1. Feedback control
Perubahan pada sistem diukur (setelah adanya gangguan), hasil pengukuran
dibandingkan dengan set point, hasil perbandingan digunakan untuk
mengendalikan variabel yang dimanipulasi.
2. Feedforward control
Besarnya gangguan diukur (sensor pada input), hasil pengukuran digunakan untuk mengendalikan variabel yang dimanipulasi.
3. Adaptive control
Sistem pengendalian yang dapat menyesuaikan parameternya secara otomatis
sedemikian rupa untuk mengatasi perubahan yang terjadi dalam proses yang
dikendalikannya, umumnya ditandai dengan adanya reset input pada controller
(selain set point pada input dari sensor) 4. Inferential control
Seringkali variabel yang ingin dikendalikan tidak dapat diukur secara
langsung, sebagai solusinya digunakan sistem pengendalian di mana variabel
yang terukur digunakan untuk mengestimasi variabel yang akan dikendalikan,
variabel terukur dan variabel tak terukur tersebut dihubungkan dengan suatu
persamaan matematika.
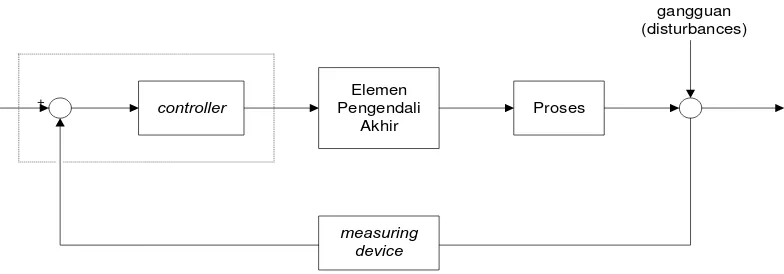
Pengendalian yang banyak digunakan adalah jenis feedback (umpan balik) berdasarkan pertimbangan kemudahan pengendalian. Diagram balok untuk sistem
pengendalian ini secara umum dapat dilihat pada Gambar 6.1 berikut ini :
controller
Elemen Pengendali
Akhir
Proses
measuring device +
[image:57.595.125.517.601.738.2]gangguan (disturbances)
Pengukuran nilai keempat variabel di atas menggunakan bantuan sensor
untuk mendeteksi nilai masing – masing variabel proses. Sedangkan variabel proses
yang lain termasuk dalam kategori tertentu karena variabel itu tergantung kebutuhan
akan proses yang melibatkannya. Variabel proses tersebut antara lain :
1. Konsentrasi
2. Kepadatan (density) dan spesific gravity
3. Kelembaban (humidity) dan kadar air (moisture)
4. Kekeruhan zat cair (turbidity) dan derajat warna zat cair (clarity)
Untuk pengukuran nilai variabel proses di atas dapat digunakan sebuah
[image:58.595.120.529.279.463.2]penganalisis (analyzer).
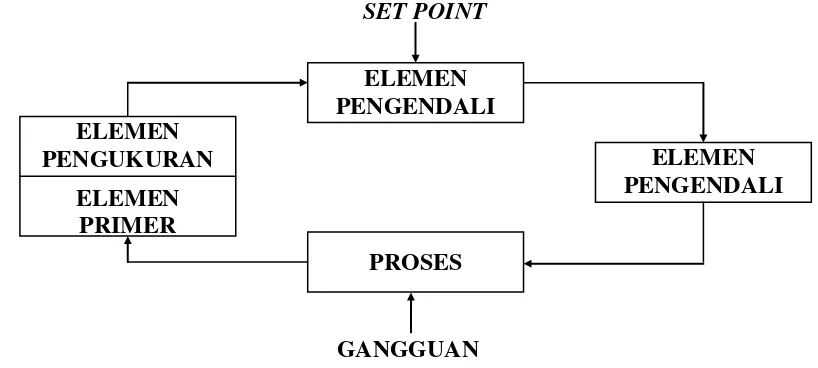
Gambar 6.2 Sebuah loop Pengendalian
Dari gambar di atas dapat dijelaskan bahwa dalam proses terdapat variabel
proses yang diantisipasi oleh elemen primer sebagai nilai perubahan proses misalnya
naik turunnya level suatu tangki, tinggi rendahnya temperatur, cepat lambatnya aliran
fluida, dan tinggi rendahnya tekanan dalam suatu tangki. Variabel proses ini bersifat
relatif atau dalam kondisi berubah – ubah. Sensor diterjemahkan sebagai harga
pengukuran.
Pada dasarnya sistem pengendalian terdiri dari (Considine,1985) :
a. Elemen Primer (Primary Element)
Elemen Primer berfungsi untuk menunjukkan kualitas dan kuantitas suatu
variabel proses dan menerjemahkan nilai itu dalam bentuk sinyal dengan
ELEMEN PENGENDALI
PROSES ELEMEN
PENGUKURAN
ELEMEN PRIMER
ELEMEN PENGENDALI
GANGGUAN
menggunakan transducer sebagai sensor. Ada banyak sensor yang digunakan
tergantung variabel proses yang ada.
− Sensor untuk temperatur, yaitu bimetal, thermocouple, termal mekanik, dll.
− Sensor untuk tekanan, yaitu diafragma, cincin keseimbangan, dll.
− Sensor untuk level, yaitu pelampung, elemen radioaktif, perbedaan tekanan, dll.
− Sensor untuk aliran atau flow, yaitu orifice, nozzle dll.
b. Elemen Pengukuran (Measuring Element)
Elemen Pengukuran berfungsi mengonversikan segala perubahan nilai yang
dihasilkan elemen primer yang berupa sinyal ke dalam sebuah harga pengukuran
yang dikirimkan transmitter ke elemen pengendali.
− Tipe Konvensional
Tipe ini menggunakan prinsip perbedaan kapasitansi.
− Tipe Smart
Tipe smart menggunakan microprocessor elektronic sebagai pemroses sinyal.
c. Elemen Pengendali (Controlling Element)
Elemen pengendali berfungsi menerima sinyal dari elemen pengukur yang
kemudian dibandingkan dengan set point di dalam pengendali (controller). Hasilnya berupa sinyal koreksi yang akan dikirim ke elemen pengendali menggunakan
processor (computer, microprocessor) sebagai pemroses sinyal pengendalian. Jenis elemen pengendali yang digunakan tergantung pada variabel prosesnya.
Alat-alat kontrol yang biasa dipakai pada peralatan proses antara lain :
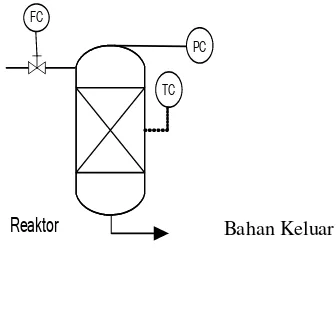
1. Temperature Controller (TC)
Adalah alat/instrumen yang digunakan sebagai alat pengatur suhu atau pengukur
sinyal mekanis atau listrik. Pengaturan temperatur dilakukan dengan mengatur
jumlah material proses yang harus ditambahkan/dikeluarkan dari dalam suatu
proses yang sedang bekerja.
Prinsip kerja :
Rate fluida masuk atau keluar alat dikontrol oleh diafragma valve. Rate fluida ini memberikan sinyal kepada TC untuk mendeteksi dan mengukur suhu sistem pada
2. Pressure Controller (PC)
Adalah alat/instrumen yang dapat digunakan sebagai alat pengatur tekanan atau
pengukur tekanan atau pengubah sinyal dalam bentu