UJI EFEKTIFITAS CHITOSAN UNTUK MENGENDALIKAN PENYAKIT JAMUR AKAR PUTIH (Rigidoporus microporus (Swart: Fr) van Ov.)
PADA TANAMAN KARET (Hevea brasiliensis Muell. Arg.) DI LABORATORIUM
S K R I P S I
Oleh:
RONALD HARIANTO H. 040302037
HPT
DEPARTEMEN ILMU HAMA DAN PENYAKIT TUMBUHAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI EFEKTIFITAS CHITOSAN UNTUK MENGENDALIKAN PENYAKIT JAMUR AKAR PUTIH (Rigidoporus microporus (Swart: Fr) van Ov.)
PADA TANAMAN KARET (Hevea brasiliensis Muell. Arg.) DI LABORATORIUM
Skripsi Sebagai Salah Satu Syarat Untuk Dapat Memperoleh Gelar Sarjana di Departemen Ilmu Hama dan Penyakit Tumbuhan Fakultas Pertanian
Universitas sumatera Utara Medan Ir. Aidi Daslin Sagala, MS
DEPARTEMEN ILMU HAMA DAN PENYAKIT TUMBUHAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
ABSTRAK
Ronald Harianto H. “ Uji Efektifitas Chitosan Untuk Mengendalikan Penyakit Jamur Jamur Akar Putih (Rigidoporus microporus (Swart: Fr) van Ov.) Pada Tanaman Karet ( Hevea brasiliensis Muell.Arg.) di Loboratorium“ dengan komisi pembibing Bapak Dr. Ir. Hasanuddin, MS selaku ketua dan Ibu Ir. Syamsinar Yusuf, MS selaku anggota, Bapak Ir. Aidi Daslin Sagala, MS, selaku pembimbing lapangan. Penelitian ini dilaksanakan di Laboratorium Prokteksi Tanaman Balai Penelitian Perkebunan Karet Sungei Putih dari bulan Mei 2009 sampai dengan Januari 2010. Tujuan Penelitian ini adalah Untuk mengetahui efektifitas chitosan terhadap jamur Rigidoporus microporus (Swartz:Fr.) van ov. dan untuk mendapatkan fungisida alami dalam mengendalikan penyakit jamur akar putih (JAP) pada tanaman karet (Hevea
brasiliensis Muell. Arg.). Penelitian menggunakan Racangan Acak Lengkap
ABSTRACT
Ronald Harianto H “Uji Efektifitas Chitosan Untuk Mengendalikan Penyakit Jamur Jamur Akar Putih (Rigidoporus microporus (Swart: Fr) van Ov.) Pada Tanaman Karet ( Hevea brasiliensis Muell.Arg.) di Loboratorium“
under the supervision of conceling team Dr. Ir. Hasanuddin, as a chairman, Ir. Syamsinar Yusuf, MS as member, Ir Aidi Daslin Sagala, MS as field
supervisor. This research was conducted at Laboratory of Crops Protection of Rubber Plantation Research Center of Sungai Putih since May 2009 up to January 2010. The objective of this research is to study the chitosan effectiveness for
Rigidoporus microporus fungus diseases and to obtain the natural fungicide in
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa karena atas berkat dan rahmat-Nya penulis dapat menyelesaikan skripsi ini tepat pada waktunya.
Adapun judul dari skripsi ini adalah “UJI EFEKTIFITAS CHITOSAN UNTUK MENGENDALIKAN PENYAKIT JAMUR AKAR PUTIH (Rigidoporus microporus (Swart: Fr) van Ov.) PADA TANAMAN KARET (Hevea brasiliensis Muell. Arg.) DI LABORATORIUM” yang merupakan salah satu syarat untuk dapat memperoleh gelar sarjana di Departemen Ilmu Hama dan Penyakit Tumbuhan Fakultas Pertanian Universitas Sumatera Utara, Medan.
Penulis mengucapkan terima kasih kepada Bapak Dr. Ir. Hasanuddin, MS
dan Ibu Ir. Syamsinar Yusuf, MS selaku Komisi Pembimbing serta kepada Bapak Ir. Aidi Daslin Sagala, MS dan Ibu Zaida Fairuzah, SP selaku
Pembimbing di Lapangan yang telah banyak membantu penulis dalam menyelesaikan skripsi ini
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis mengharapkan kritik dan saran yang sifatnya membangun demi kesempurnaan skripsi ini di masa mendatang.
Akhir kata penulis mengucapkan terima kasih dan semoga skripsi ini dapat bermanfaat bagi kita semua.
Medan, Maret 2010
DAFTAR ISI
Biologi Penyebab Penyakit ... 5Gejala Serangan ... 7
Faktor-Faktor yang Mempengaruhi JAP ... 9
Pengendalian Penyakit JAP ... 11
Chitosan ... 13
BAHAN DAN METODE Tempat dan Waktu Penelitian ... 16
Bahan dan Alat ... 16
Metode Penelitian ... 16
Pelaksanaan Penelitian Persiapan Chitosan ... 17
Persiapan Bahan Inokulasi ... 19
Pembuatan Potato Dextrose Agar ... 19
Media PDA yang Terdapat Senyawa Chitosan ... 19
Media PDA yang Terdapat Larutan Fungisida ... 19
Parameter Pengamatan
Luas Pertumbuhan Koloni R. microporus ... 20 Pengamatan Miselium dan Warna Koloni Jamur ... 21 HASIL DAN PEMBAHASAN
Luas Pertumbuhan Koloni Jamur Rigidoporus microporus ... 22 Pengamatan Miselium dan Warna Koloni Jamur
Rigidoporus microporus ... 25 KESIMPULAN DAN SARAN
DAFTAR TABEL
No. Judul Halaman
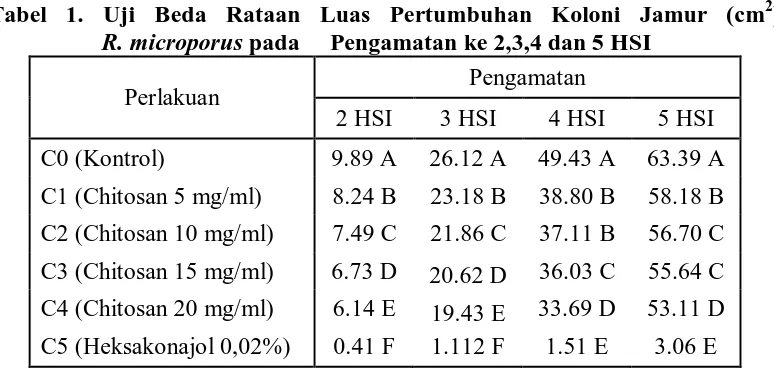
1. Rataan Luas Pertumbuhan Koloni Jamur R. microporus
DAFTAR GAMBAR
No. Judul Halaman
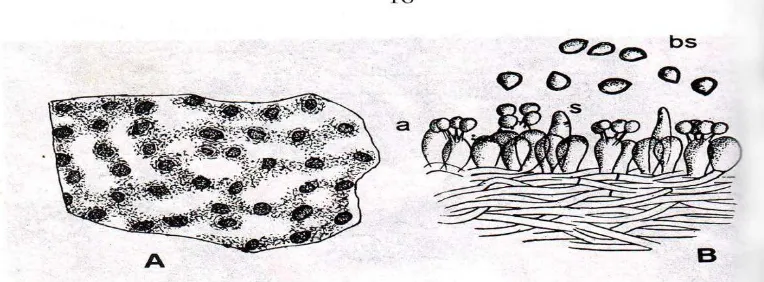
1. Badan Buah R. microporus ... 6
2. Basidium dan Basidiospora R. microporus ... 7
3. Rizomorf R. microporus ... ... 8
4. Foto Chitosan ... .. ... 15
5. Alat Planimeter ... ... 21
DAFTAR LAMPIRAN
No Judul Halaman
1. Bagan penelitian di laboratorium ... 31 2. Foto Luas Pertumbuhan Koloni Jamur R. microporus
Pada 1 HSI, 2,3,4,5 dan 6 HSI ... 33 3. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus
Pada Uji Efektifitas Chitosan 2 HSI (cm2) ... 35 4. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus
Pada Uji Efektifitas Chitosan 3 HSI (cm2) ... 37 5. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus
Pada Uji Efektifitas Chitosan 4 HSI (cm2) ... 39 6. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus
ABSTRAK
Ronald Harianto H. “ Uji Efektifitas Chitosan Untuk Mengendalikan Penyakit Jamur Jamur Akar Putih (Rigidoporus microporus (Swart: Fr) van Ov.) Pada Tanaman Karet ( Hevea brasiliensis Muell.Arg.) di Loboratorium“ dengan komisi pembibing Bapak Dr. Ir. Hasanuddin, MS selaku ketua dan Ibu Ir. Syamsinar Yusuf, MS selaku anggota, Bapak Ir. Aidi Daslin Sagala, MS, selaku pembimbing lapangan. Penelitian ini dilaksanakan di Laboratorium Prokteksi Tanaman Balai Penelitian Perkebunan Karet Sungei Putih dari bulan Mei 2009 sampai dengan Januari 2010. Tujuan Penelitian ini adalah Untuk mengetahui efektifitas chitosan terhadap jamur Rigidoporus microporus (Swartz:Fr.) van ov. dan untuk mendapatkan fungisida alami dalam mengendalikan penyakit jamur akar putih (JAP) pada tanaman karet (Hevea
brasiliensis Muell. Arg.). Penelitian menggunakan Racangan Acak Lengkap
ABSTRACT
Ronald Harianto H “Uji Efektifitas Chitosan Untuk Mengendalikan Penyakit Jamur Jamur Akar Putih (Rigidoporus microporus (Swart: Fr) van Ov.) Pada Tanaman Karet ( Hevea brasiliensis Muell.Arg.) di Loboratorium“
under the supervision of conceling team Dr. Ir. Hasanuddin, as a chairman, Ir. Syamsinar Yusuf, MS as member, Ir Aidi Daslin Sagala, MS as field
supervisor. This research was conducted at Laboratory of Crops Protection of Rubber Plantation Research Center of Sungai Putih since May 2009 up to January 2010. The objective of this research is to study the chitosan effectiveness for
Rigidoporus microporus fungus diseases and to obtain the natural fungicide in
PENDAHULUAN
Latar Belakang
Karet (Hevea brasiliensis Muell. Arg.) berasal dari Brazilia, Amerika Selatan. Akan tetapi meskipun telah diketahui penggunaannya oleh Colombus dalam pelayarannya ke Amerika Selatan pada akhir abad ke -15 dan bahkan oleh penjelajah-penjelajah berikutnya pada awal abad ke-16, sampai saat ini masih belum menarik perhatian orang – orang Eropa (Dijkman, 1986). Tanaman karet mulai diperkebunkan di Indoneisia sejak tahun 1900-an. Di Sumatera Utara pada tahun 1903 dan di Jawa tahun 1906 (Semangun, 2000).
Sistem perkebunan karet muncul pada awal abad ke- 19 akan tetapi sistem perkebunan di Asia Tenggara tidak terjadi sebelum akhir abad ke- 19, ketika pertumbuhan permintaan menuntut perluasan sumber penawaran. Sistem ini
diperkenalkan oleh beberapa ahli tumbuh-tumbuhan dari Inggris (Spillance, 1989).
sekitar 786 juta U$ dolar, yang menduduki peringkat kedua terbesar setelah sawit (Sinaga, 2004). Propinsi yang memiliki perkebunan karet terluas pada tahun 2004 adalah Sumatera Selatan. Yakni mencapai 671.920 ha. Dari total areal perkebunan karet di Indonesia tersebut 84,5% diantaranya merupakan kebun milik rakyat, 8,4% milik swasta dan hanya 7,1% milik negara (Andoko dan Setiawan, 2006).
Di dalam budidaya tanaman karet Hevea penyakit akar putih adalah penyakit yang merugikan diantara penyakit- penyakit akar yang di kenal. Bahkan bagi daerah karet tertentu, seperti Jawa Timur dan Sumatera Utara, penyakit akar
putih merupakan penyakit yang terpenting diantara penyakit yang ada (Semangun, 2000).
Jamur akar putih (JAP) disebabkan oleh jamur Rigidoporus lignosus (Klotszch) Imazeki (Syn, R. microporus) adalah jamur saprofit penghuni tanah, tetapi bila bertemu dengan akar tanaman akan berubah menjadi parasit (parasit fakultatif). JAP bertahan dalam tanah dengan membentuk rizomorf. Sekali tanah terkontaminasi oleh JAP seterusnya tanah tersebut dihuni oleh JAP dan menjadi ancaman setiap tanaman baru. Peremajaan yang berulang-ulang akan menyebabkan akumulasi sumber penyebab JAP dalam tanah (Soepena, 1995).
Pengendalian penyakit jamur akar putih dapat dilakukan dengan aplikasi fungisida, belerang dan Trichoderma sp. yang diaplikasikan secara total maupun secara selectif. Titik berat pengendalian jamur akar putih diprioritaskan untuk mempertahankan populasi. Dengan pengendalian JAP diharapkan tingkat kematian pohon karet dapat dikendalikan, populasi bisa dipertahankan sehingga produktifitas bisa meningkat seiring dengan umur tanaman (Suhandi, 2004).
Chitosan adalah polisakarida linier dengan komposisi glukosamin. Chitosan banyak digunakan dalam biomedis komersional. Chitosan sebenarnya serat yang didapat dari polisakarida dari kerang, udang, kepiting dan lain-lain. Chitosan bersifat larut dalam larutan asam organik, tetapi tidak larut dalam pelarut organik dan dalam larutan yang memiliki pH 6,5. Pelarut chitosan yang baik adalah asam asetat (CH3COOH) (Prasetiyo dan Yusuf, 2005).
Tujuan Penelitian
Untuk mengetahui efektifitas chitosan terhadap jamur Rigidoporus
microporus (Swartz:Fr.) van ov. dan untuk mendapatkan fungisida alami dalam
mengendalikan penyakit jamur akar putih (JAP) pada tanaman karet (Hevea brasiliensis Muell. Arg.).
Hipotesis Penelitian
• Chitosan pada media agar dapat menekan pertumbuhan jamur
Rigidoporus microporus di laboratorium.
• Konsentrasi chitosan mempengaruhi pertumbuhan jamur Rigidoporus
microporus di laboratorium.
Kegunaan Penelitian.
• Sebagai salah satu syarat untuk dapat memperoleh gelar sarjana di Departemen Hama dan Penyakit Tumbuhan Fakultas Pertanian Universitas Sumatera Utara, Medan.
TINJAUAN PUSTAKA
Biologi Penyebab Penyakit
Penyakit akar putih disebabkan oleh jamur yang lazimnya disebut jamur akar putih (JAP). Nama ilmiah jamur ini adalah Rigidoporus lignosus (Klotzsch) Imazeki atau Rigidoporus microporus (Swartz: Fr.)Van ove., Poliporus lignosus Klotzsch, meskipun sampai sekarang jamur ini sering dikenal dengan nama
Fomes lignosus (Klotzsch) Bres (Semangun, 2000).
Menurut Alexopoulus and Mins (1979) penyakit Jamur Akar Putih (JAP) dapat diklasifikasikan sebagai berikut:
Divisio : Mycetaceae Sub Divisio : Amestigomycots Kelas : Basidiomycetes Ordo : Homobasidiomycetes Famili : Polyperales
Genus : Rigidoporus
Spesies : Rigidoporus microporus (Swartz: Fr.) Van overeem
Permukaan bawah berwarna jingga, tepihnya berwarna kuning jernih atau putih kekuningan. Jika menjadi tua atau kering tubuh buah menjadi suram, permukaan atasnya cokelat kekuningan pucat dan permukaan bawahnya cokelat kemerahan (Semangun, 2000).
Gambar 1. Badan buah jamur Rigidoporus microporus
Menurut Steinmann (1925) dalam Semangun (2000) lapisan atas tubuh buah yang berwarna muda terdiri atas benang-benang jamur yang terjalin rapat. Dibawahnya terdapat lapisan pori kemerahan atau kecokelatan dengan garis tengah 45-80 μm , panjang berbeda-beda umumnya 0,7-1,0 μm.
Diameter sporofor pada umumnya 10 cm tetapi pada keadaan yang sesuai untuk pertumbuhan dapat mencapai 30 cm dengan tebal 1,5 cm, bagian tepi sporofor lebih tipis, selanjutnya sporofor ini menghasilkan basidiospora. Basidiospora bulat, tidak berwarna, dengan garis tengah 2,8-5,0 μm, banyak
Gambar 2. Rigidoporus lignosus. A. Pori; B. basidium (a) dengan basidiospora (bs) dan
sistidium (s). (menurut A. Steinmann, 1925 dalam Semangun, 2000)
Rigidoporus microporus jamur yang bersifat parasit fakultatif, artinya
dapat hidup sebagai saprofit yang kemudian menjadi parasit. Jamur R. microporus tidak dapat bertahan hidup apabila tidak ada sumber makanan. Bila belum ada inang jamur ini bertahan di sisa-sisa tunggul (Liyanage, 1976).
Gejala Serangan
Gejalah serangan JAP pada tanaman karet ditandai dengan adanya perubahan pada warna daun. Daun berwarna hijau kusam, permukaan daun lebih tebal dari yang normal. Setelah itu daun- daun menguning dan rontok. Pada pohon dewasa gugurnya daun, yang disertai dengan matinya ranting menyebabkan pohon mempunyai mahkota yang jarang. Ada kalanya tanaman membentuk bunga/ buah lebih awal (Semangun, 2000 dan Rahayu, dkk., 2006).
yang baru saja mati tetap keras, berwarna cokelat, kadang-kadang agak kekelabuan. Pada pembusukan yang lebih jauh, kayu berwarna putih atau krem, tetapi padat dan kering, meskipun di tanah basah kayu yang terserang dapat busuk dan hancur (Basuki dan Wisma, 1995 dan Semangun, 2000).
Gambar 3. Rizomorf pada permukaan akar karet yang terserang Rigidoporus microporus
Pada tanaman muda gejalanya mirip dengan tanaman yang mengalami kekeringan. Daun-daun berwarna hijau kusam dan lebih tebal dari yang normal. Daun tersebut akhirnya menjadi cokelat dan mengering. Pohon akhirnya tumbang dengan daun yang masih menggantung. Ada kalanya pohon tiba-tiba tumbang tanpa menimbulkan gejala kematian tajuk, karena akar tanaman telah busuk dan mati. Apabilah leher akar tanaman yang terserang dibuka, akan tampak rizomorf jamur berwarna putih, baik diakar tunggang ataupun di akar lateral. Akar- akar tersebut akan busuk dan tanaman akan mati (Sinulingga, 1989).
Faktor-Faktor yang Mempengaruhi Penyakit JAP
Jamur akar putih (JAP) dapat menyerang tanaman karet pada bermacam-macam umur. Penyakit akar putih terutama timbul pada kebun-kebun muda. Pada umumnya gejala mulai tampak pada tahun-tahun ke-2. Sesudah tahun ke-5 atau ke-6 infeksi-infeksi baru mulai berkurang, meskipun dalam kebun-kebun tua penyakit dapat berkembang terus (Semangun, 2000). JAP dapat mematikan tanaman karet yang berumur 3 tahun dalam waktu 6 bulan dan tanaman karet umur 6 tahun dalam waktu 12 bulan (Basuki, 1981 dalam Yusuf, dkk 1992).
Penyebaran JAP yang paling efektif yaitu melalui kontak akar. Apabila akar-akar tanaman sehat saling bersinggungan dengan akar tanaman karet yang sakit, maka rizomorf JAP akan menjalar pada tanaman yang sehat kemudian menuju leher akar dan selanjutnya menginfeksi akar lateral lainnya. Tanaman yang terinfeksi ini akan menjadi sumber infeksi pada tanaman jirannya, sehingga perkembangan penyakit semakin lama semakin meluas (Sujatno, dkk., 2007).
Setelah patogen menginfeksi tanaman, perkembangan selanjutnya bergantung pada pH, kandungan bahan-bahan organik, kelembapan dan aerase tanah. R. micropous dapat tumbuh baik pada kelembapan diatas 90%, kandungan bahan organik tinggi serta aerase yang baik. Apabila kondisi ini sesuai, patogen dapat menjalar sejauh 30 cm dalam waktu 2 minggu (Sinulingga dan Eddy, 1989).
merupakan medium penularan JAP dan akar-akar yang terinfeksi merupakan sumber penularan lebih lanjut (Soepena, 1984).
Infeksi patogen lebih mudah terjadi melalui luka dan lentisel, walaupun penetrasi secara langsung mungkin terjadi. Pada tanaman karet yang sering di temukan bagian leher akar pecah dan ini merupakan tempat yang baik bagi infeksi jamur. Patogen kemudian ke bagian yang lebih dalam dari akar. Tanaman akan mengadakan pertahanan seperti pembentukan kambium dan gabus, akan tetapi hal ini sering tidak dapat menahan perkembangan lanjut patogen. Serangan lebih tingggi akan ditemukan pada tanaman okulasi dibandingkan dengan tanaman biji. Hal ini disebabkan pada bagian okulasi ada bagian-bagian yang luka, sehingga memudahkan patogen untuk mengadakan infeksi (Sinulinggga, 1989).
Menurut Basuki (1986) dalam Semangun (2000) pembongkaran karet-karet tua secara mekanis dengan alat-alat berat memberikan hasil yang lebih baik, karena hannya meninggalkan sedikit sumber infeksi di dalam tanah. Sebaliknya diketahui pada peremajaan yang hanya dilakukan dengan peracunan pohon-pohon karet tua akan menyebabkan terjadinya banyak infeksi pada tanaman muda kelak.
Di Sumatera Utara kebun-kebun yang terletak di tanah podsolik merah kuning kurang menderita kerugian dari jamur akar putih, daripada yang terdapat di tanah aluvial. Ini disebabkan karena tanah tersebut lebih masam, sehingga
Rigidoporus tidak dapat berkembang dengan baik. Selain itu di tanah yang lebih
masam terdapat jamur Trichoderma koningii Oud., yang menjadi antagonis bagi
Pengendalian Penyakit JAP
Pengendalian JAP ditujukan untuk memusnakan sumber infeksi dan mencegah terbentuknya penyakit pada tanaman karet muda serta meluasya dari satu tanaman ke tanaman yang lain (Yusuf, dkk., 1992).
Menurut Semangun (2000) pengendalian dapat dibagi menjadi dua kelompok kegiatan, yaitu: membersikan sumber infeksi, sebelum dan sesudah penanaman karet dan dan mencegah meluasnya penyakit dalam kebun.
1. Membersikan sumber infeksi
Sumber infeksi berasal dari pohon-pohon hutan yang sakit, atau tunggul-tunggul pohon hutan yang terinfeksi, sedang pada peremajaan berasasl dari pohon karet tua yang sakit atau tunggul-tunggul tua pohon yang sakit. Tunggul-tunggul yang terdapat di kebun harus dibongkar. Jika pembongkaran tunggul tidak dapat dilakukan, untuk mempercepat pembusukan akar dilakukan peracunan tunggul (stump poisoning) dan peracunan pohon. Agar tunggul yang baru tidak dapat diinfeksi oleh spora R. microporus, sehabis penebangan bidang potongan harus segera ditutup dengan obat penutup luka (Semangun, 2000).
Untuk penyulaman, tanaman yang tidak bisa diselamatkan lagi, harus segera dibongkar dan sisa-sisa akar harus disingkirkan dan bekas lubang harus diberi 250 g serbuk belerang atau ZA. Tanah bekas lubang tanam harus disingkirkan dan dibuat lubang tanam yang baru (40 x 40 x 30) cm. Bibit yang ditanam harus bibit stump tinggi, disekitar bibit stump ditaburkan serbuk belerang atau ZA untuk melindungi bibit dari serangan JAP (Pinem dan Yusuf, 2004).
Pengendalian secara biologis merupakan tindakan dengan penggunaan agensia hayati, pengendalian ini paling mudah, murah dan ramah lingkungan (Hamdan, 2007).
Banyak jenis Bio-fungisida yang diteliti para ahli untuk menekan pertumbuhan JAP, misalnya Trichoderma sp. Pada pembibitan dengan dosis 50 g/pohon, dilapangan pada pohon yang sudah terserang diberikan 100 g/pohon (TBM). Sedang pada pohon yang sudah menghasilkan dibuat parit keliling dengan radius 0,5 m dari pangkal pohon yang akan diisi Trico-sp dan ditutup kembali dengan tanah (Ilahang, dkk., 2007).
Pengendalian jamur akar putih dapat juga dilakukan dengan bakteri
Pseudomonas aeruginosa dimana bakteri ini dapat menekan pertumbuhan
miselium R. microporus (Hasanuddin, 1999).
2. Mencegah meluasnya penyakit dalam kebun
pembukaan leher akar. Pembukaan leher akar ini bertujuan agar pangkal dari akar tunggang dan akar-akar samping tidak tertutup tanah, karena jamur R. microporus tidak dapat berkembang dengan baik pada akar-akar yang berada di luar tanah (Semangun, 2000).
Pegendalian jamur akar putih sebaiknya dilakukan dengan kombinasi antara cara kimia dan cara biologis, walaupun cara kimia menunjukkan hasil yang lebih efektif daripada biologis. Pada aplikasi per pohon, pengobatan secara kimia misalnya dengan pengaplikasian fungisida Bayleton dengan dosis 5 cc/L air. Dengan membuat parit isolasi agar campuran Bayleton tersebut dapat terserap ke dalam perakaran tanaman. Aplikasi berdasarkan umur tanaman dengan dosis 250 ml/pohon (umur <1 tahun), 500 ml/pohon (umur 2-3 tahun) dan 1000 ml/pohon (>3 tahun) (Ilahang, dkk., 2007).
Chitosan
Chitosan pertama kali ditemukan oleh ilmuwan Perancis, Ojier pada tahun 1823. Ojier meneliti chitosan hasil ekstrak kerak binatang berkulit keras, seperti udang, kepiting, dan serangga (Luthfi, 2006).
Gambar 4. Chitosan
Proses pembuatan chitosan pertama-tama kulit udang dicuci dengan air mengalir selanjutnya dicuci dengan air panas kemudian di jemur sampai kering. Selanjutnya kulit udang diblender lalu dicuci dengan larutan asam klorida untuk menghilangkan kerak kapur (demineralisasi) selanjutnya di cuci dengan larutan NaOH untuk menghilangkan protein (deproteinisasi) Prasetiyo dan Yusuf (2005). Chitosan digunakan untuk kesehatan untuk penyakit diabetes dan hipertensi. Ternyata di dalam zat kerak udang terdapat unsur butylosar yang bermanfaat bagi tubuh manusia. Butylosar yang telah didapatkan itu hanya larut dalam asam encer dan cairan tubuh manusia. Dengan demikian, butylosar dapat diserap oleh tubuh, zat ini juga mempunyai muatan positif yang kuat, dan dapat mengikat muatan negatif dari senyawa lain. Selain itu, zat ini tidak mudah mengalami degradasi secara biologis dan tidak beracun (Linawati, 2008).
kepiting atau eksokleton udang (Wilson and Ell Ghaouth, 1993). Chitosan melindungi buah dan sayuran melalui dua mekanisme, fisik dan kimiawi. Secara fisik, chitosan membentuk lapisan film yang membungkus permukaan produk dan mengatur pertukaran gas dan kelembaban. Secara kimiawi, chitosan bersifat fungisidal dan merangsang respon resistensi pasca panen pada jaringan tanaman. Aktifitas antifugal dan merangsang ketahanan dari chitosan menjanjikan kemungkinan yang baik untuk pengendalian penyakit tanaman ( Pamekas, 2007).
Chitosan (sebuah polymer dari beta- 1,4- glucosamin residues) adalah sebuah deacetyl jadian dari kitin yang memberikan sifat antifugal yang berperan untuk memancing/mendapatkan ketahanan tanaman yang potensial untuk melawan jamur patogen (Roblin, 2008). Allan dan Hadwiger melaporkan bahwa cithosan (1000 µg/ml) efektif dan mengurangi pertumbuhan dari beberapa jamur yang telah diuji. Efek penghambatan dari chitosn juga telah didemostrasikan dengan jamur tular tanah (soil borne) (El Ghaouth, at al., 1992).
Efek pemberian chitosan terhadap tingkat kerusakan buah strawberry yang diinokulasi dengan suspensi spora Botrytis cinerea atau Rhizopus stolonifer kemudian diberi dengan larutan chitosan (10 atau 15 mg/ml), setelah 14 hari disimpan kerusakan yang disebabkan oleh B. cinerea atau R. stolonifer sangat nyata pengurangannya dengan pemberian chitosan. Chitosan sangat efektif menghambat pertumbuhan spora dan perpanjangan germtube dari B. cinerea atau
R. stolonifer pada media. Mekanisme dari chitosan mengurangi pembusukan/
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian dilakukan di Laboratorium Proteksi Tanaman Balai Penelitian Tanaman Karet Sungei Putih, dengan ketinggian ± 80 meter dari permukaan laut. Penelitian dilaksanakan pada bulan Mei 2009 sampai dengan Desember 2010.
Bahan dan Alat
Adapun bahan yang digunakan adalah Isolat jamur Rigidoporus microporus, PDA (Potato Dektrose Agar), kulit udang , aquadest steril dan bahan-bahan kimia seperti alkohol 96%, HCl 37%, NaOH 40 g/mol, Fungisida Anvill 50 SC (Heksakonazol).
Adapun alat yang digunakan adalah autoclave untuk sterilisasi alat, becker glass, gelas ukur, gunting, erlenmeyer, deck glass, blender, hand spayer, planimeter, hot plate, cork borer, incubator, panci, timbangan, cawan petri, kompor, bbelender, oven, lampu bunsen, mikroskop, jarum inokulasi, batang pengaduk, pinset, toples, saringan, dan kain muslin.
Metode Penelitian
Penelitian ini dilakukan dengan menggunakan Rancangan Acak Lengkap (RAL) Non faktorial yang terdiri dari 6 perlakuan dan 3 ulangan.
C2 = Chitosan sebanyak 10 mg/ml C3 = Chitosan sebanyak 15 mg/ml C4 = Chitosan sebanyak 20 mg/ml
C5 = Fungisida Anvill 50 SC ( heksakonazol) dengan konsentrasi 0,02% Jumlah ulangan adalah :
(t-1)(r - 1) ≥ 15 (6-1)(r - 1) ≥ 15 6 (r-1) ≥ 15 6 r ≥ 21 r ≥ 3.2 r = 3
Jumlah perlakuan = 6 Jumlah ulangan :
Replikasi = 3 (Duplikasi sebanyak 3 kali) Jumlah keseluruhannya = 54
Pelaksanaan Penelitian Persiapan Chitosan
Chitosan dibuat berdasarkan metode yang digunakan oleh Prasetiyo dan
Yusuf (2005) yaitu :
a. Demineralisasi
direbus selama 10 menit. Setelah direbus, kulit udang ditiriskan dan dikeringkan. Kulit udang yang sudah kering digiling sampai menjadi serbuk. Setelah itu, serbuk kulit udang dicampur dengan asam klorida (HCL) 1 N dengan perbandingan 10 : 1 (1000 ml : 100 gr). Larutan tersebut diaduk secara merata selama 1 jam, lalu dipanaskan pada suhu 900 C selama 1 jam. Residu padatan dicuci dengan air sampai pH netral. Selanjutnya, residu padatan ini dikeringkan dalam oven pada suhu 800 C selama 24 jam.
b. Deproteinasi
Kulit udang yang telah dimineralisasi dicampur dengan larutan NaOH 3,5% dengan perbandingan pelarut dan kulit udang sebesar 6 : 1 (600 ml : 100 gr). Larutan tadi diaduk secara merata selam 1 jam, lalu dipanaskan pada suhu 900 C selama 1 jam. Setelah itu, larutan disaring dan didinginkan hingga diperoleh residu padatan, residu padatan ini dicuci dengan air sampai pH netral dan dikeringkan pada suhu 800 C selama 24 jam.
c. Deasetilisasi Khitin Menjadi Chitosan
Persiapan Bahan Inokulasi
Inokulum R. microporus diperoleh dari isolasi langsung tanaman karet yang terserang patogen jamur akar putih. Dalam hal ini yang dibiakkan adalah bagian akar yang terserang, kemudian ditumbuhkan dalam media PDA. Hasil biakan tersebut, dibiakkan kembali hingga menjadi biakan murni.
Pembuatan Potato Dextrose Agar (PDA)
Kentang dikupas dan dicuci bersi lalu ditimbang sebanyak 250 gram seterusnya dipotong kecil-kecil, kemudian potongan kentang direbus dengan aquadest sebanyak 500 ml selama 1-1½ jam. Kemudian disaring ekstraknya dengan kain muslin dan dibuat volume menjadi 500 ml lalu ditambahkan 20 gram dextrose dan 20 gram agar lalu dipanaskan hingga homogen, lalu ditambahkan aquadest streril hingga volume menjadi 1 liter. Selanjutnya dituang kedalam tabung reaksi dengan volume 15 ml/ tabung reaksi, kemudian ditutup dengan kapas yang dilapisi dengan alumeniumfoil, lalu dimasukkan kedalam autoclave untuk disterilisasi selama 15 menit degan suhu 1210 C dan tekanan 1,5 atm. Setelah disterilisasi kemudian PDA didinginkan hingga diperoleh suhu 400 C (hangat kuku).
Medium PDA yang terdapat Senyawa Chitosan
petri. Setelah semua perlakuan selesai, kemudian disimpan ke dalam inkubator selama satu malam.
Medium PDA yang terdapat Larutan Fungisida
Tabung reaksi yang telah berisi PDA sebanyak 15 ml kemudian ditambahkan larutan fungisida sebanyak 400 µ l/ tabung reaksi, kemudian tabung reaksi digoyang-goyang agar larutan fungisida tercampur rata dengan PDA . Setelah tercampur rata kemudian langsung dituang ke dalam cawan petri. Setelah perlakuan selesai, kemudian disimpan ke dalam inkubator selama satu malam. Hal yang sama juga dilakukan untuk perlakuan kontrol dimana yang membedakannya adalah dalam perlakuan kontrol penambahan larutan fungisida 400 µ l tidak dilakukan
Pelaksanaan Inokulasi
Campuran PDA dan chitosan serta campuran PDA dan Fungisida tersebut ditumbuhkan jamur R. microporus yang berasal dari biakan murni R. microporus berumur 7 hari dengan menggunakan cork borer (diameter 4 mm), diambil dari tepi koloni yang diletakkan tepat di tengah cawan petri. Hal yang sama juga dilakukan pada perlakuan kontrol. Lalu cawan petri diinkubasikan dalam kotak incubator pada suhu ruangan.
Parameter Pengamatan
Luas Pertumbuhan Koloni R. microporus
1. Diamati pertumbuhan luas koloni jamur R. Microporus secara periodik pada perlakuan kontrol, perlakuan chitosan dan fungisida. Diukur mulai hari kedua sampai dengan hari ke lima, dengan interval waktu pengamatan 1 hari.
2. Digambar di cawan petri dibagian belakang dengan menggunakan spidol permanent.
3. Hasilnya digambar di kertas minyak trasparan.
4. Dihitung luas pertumbuhan koloni jamur menggunakan alat plani meter (gambar 5).
Gambar 5. Alat Planimeter
Pengamatan Miselium dan Warna Koloni Jamur
HASIL DAN PEMBAHASAN
1. Luas Pertumbuhan Koloni Jamur Rigidoporus microporus
Data Pengamatan luas pertumbuhan koloni jamur R. microporus dapat dilihat pada lampiran 3-6. Hasil analisis statistik menggunakan daftar sidik ragam dan Uji Jarak Duncan (UJD) pada taraf 1 % menunjukkan bahwa pertumbuhan luas koloni jamur R. microporus pada pengamatan 2-5 HSI (Hari Setelah Inokulasi) menunjukkan hasil yang berbeda sangat nyata. Hasilnya dapat dilihat pada tabel 1 berikut ini:. Keterangan: Angka-angka yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata
pada taraf 0,01 % menurut uji jarak Duncan
53,11 cm2. dengan demikian semakin tinggi konsentrasi chitosan semakin baik untuk menghambat pertumbuhan koloni jamur.
Pada pengamatan 2 HSI luas pertumbuhan koloni jamur pada perlakuan C1 (chitosan 5 mg/ml aquadest steril) adalah 8,24 cm2 berbeda sangat nyata terhadap perlakuan C2 (chitosan 10 mg/ml aquadest steril) 7,49 cm2, C3 (chitosan 15 mg/ml aquadest steril) 6,73 cm2 dan C4 (chitosan 20 mg/ml aquadest steril) 6,14 cm2. Pada pengamatan 3 HSI luas pertumbuhan koloni jamur pada perlakuan C1 (chitosan 5 mg/ml aquadest steril) adalah 23,18 cm2 berbeda sangat nyata
terhadap perlakuan C2 (chitosan 10 mg/ml aquadest steril) 21,86 cm2,, C3 (chitosan 15 mg/ml aquadest steril) 20,62 cm2 dan C4 (chitosan 20 mg/ml
aquadest steril) 19,43 cm2. Pada pengamatan 4 HSI luas pertumbuhan koloni jamur pada perlakuan C1 (chitosan 5 mg/ml aquadest steril) adalah 38,80 cm2 tidak berbeda nyata dengan perlakuan C2 (chitosan 10 mg/ml aquadest steril) 37,11 cm2 dan berbeda sengat nyata terhadap perlakuan C3 (chitosan 15 mg/ml aquadest steril) 36,03 cm2 dan C4 (chitosan 20 mg/ml aquadest steril) 33,69 cm2.
Pada pengamatan 5 HSI luas pertumbuhan koloni jamur pada perlakuan C1 (chitosan 5 mg/ml aquadest steril) adalah 58,18 cm2, berbeda sangat nyata
koloni jamur yang terendah adalah pada perlakuan C5 (Fungisida Anvill 50 SC 2 ml/l aquadest steril).
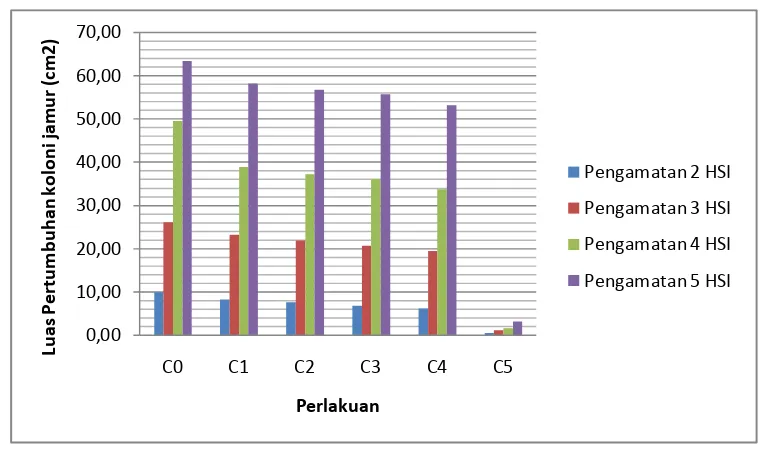
Untuk lebih jelasnya dapat dilihat pada gambar Histogram berikut ini:
Gambar 6. Histogram pertumbuhan luas koloni jamur R. Microporus
Dari hasil penelitian yang dilakukan, bahwa penghambatan luas pertumbuhan koloni jamur diakibatkan karena senyawa chitosan mempunyai kemampuan untuk menghambat pertumbuhan koloni. Hal ini sesuai dengan literatur El Ghaouth et al. (1992), yang menyatakan bahwa chitosan mengandung
enzim β 1 ,3- glukanase yang dapat menurunkan jumlah kitin pada dinding hifa
2. Pengamatan Miselium dan Warna Koloni Jamur Rigidoporus microporus
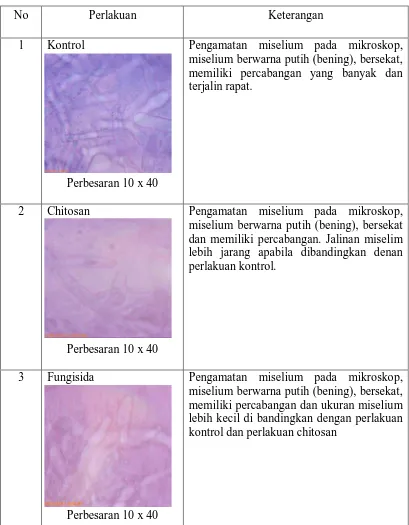
Hasil pengamatan dari jamur R.microporus dari masing-masing perlakuan diperoleh bentuk miselium dan warna koloni yang berbeda. Tertera pada tabel berikut:
Tabel 2. Pengamatan miselium pada tiap Perlakuan
No Perlakuan Keterangan 1 Kontrol
Perbesaran 10 x 40
Pengamatan miselium pada mikroskop, miselium berwarna putih (bening), bersekat, memiliki percabangan yang banyak dan terjalin rapat.
2 Chitosan
Perbesaran 10 x 40
Pengamatan miselium pada mikroskop, miselium berwarna putih (bening), bersekat dan memiliki percabangan. Jalinan miselim lebih jarang apabila dibandingkan denan perlakuan kontrol.
3 Fungisida
Perbesaran 10 x 40
Tabel 3. Pengamatan Warna Koloni Jamur Rigidoporus microporus No Perlakuan Keterangan
1 Kontrol Pada media tampak belakang berwarna putih. Sedangkan tampak depan, terdapat kumpulan miselium berwarna putih jernih. Pertumbuhan miselium terjalin dengan rapat. Koloni jamur memenuhi cawan petri pada hari ke 4-5.
2 Chitosan Pada media tampak belakang berwarna putih, lama-kelamaan menjadi kuning kecokelatan. Sedangkan tampak depan, terdapat kumpulan miselium berwarna putih. Koloni jamur memenuhi cawan petri pada hari ke 5-6.
KESIMPULAN DAN SARAN
Kesimpulan
1. Pada pengamatan luas koloni jamur R. microporus untuk perlakuan chitosan berbeda sangat nyata terhadap perlakuan kontrol dan fungisida anvill 50 SC
2. Luas koloni jamur R. microporus pada 5 HSI tertinggi terdapat pada perlakuan kontrol yaitu sebesar 63,39 cm2 dan yang terendah terdapat pada perlakuan fungisida anvill yaitu sebesar 3.06 cm2.
3. Pada perlakuan chitosan, luas pertumbuhan koloni jamur R. microporus yang tertinggi terdapat pada perlakuan C1 (chitosan 5 mg/ml aquadest steril) yaitu sebesar 58,18 cm2 dan yang terendah terdapat pada perlakuan C4 (chitosan 20 mg/ml aquadest steril) yaitu 53,11 cm2.
4. Bentuk miselium dan warna koloni jamur R. microporus berbeda pada setiap perlakuan.
Saran
Perlu dilakukan penelitian lanjutan mengenai perbandingan chitosan kulit
udang dengan chitosan dari sumber lain, untuk mengendalikan jamur
DAFTAR PUSTAKA
Alexopoulus, C. J., and C. J., Mims. 1979. Introductory Mycology. 3rd edition. John Willey and Sons, New York. pp: 355, 365.
Andoko, A., dan Setiawan, D.H., 2006. Petunjuk Lengkap Budidaya Karet, Kanisius, Yogyakarta, hal: 11-12.
Baroni, T.J., 2007 Rigidoporus microporus.
Basuki, dan Wisma, S., 1995. Pengenalan dan Pengendalian Penyakit Akar Putih Pada tanaman Karet, hal: 1-5. dalam Kumpulan Lokakarya Pengendalian Penyakit Penting Tanaman Karet. Pusat Penelitian Karet, Sungei Putih. Dijkman, M.J., 1986. Havea: Thirty Years of Research in the Far East. University
of Miami- Press, Coral Gables, Florida, pp: 3-5.
El Ghaouth, A., Arul, J., Granier, J., and Asselin, A., 1992. Antifugal Activity of Chitosan on Two Postharvest Pathogens of Strawberry Fruits. Februari 2009.
Fairuzah, Z., Rahayu, S.T.S., Suryaman, S., dan Zaini, A., 2008. Laporan Pengujian Efectivitas Biotani Terhadap Perkembangan Jamur Akar Putih (JAP). Pusat Penelitian Karet, Sungei Putih, hal: 3-5.
Hamdan, 2007. Pengendalian Organisme Pengganggu Tumbuhan (OPT) Jamur Akar Putih (JAP) Pada Tanaman Karet. remove this watermark,diakses 19 Januari 2009.
Hasanuddin, 1999. Efektivitas Medium Pertumbuhan Pseudomonas aeruginosa Sebagai Penghasil Senyawa Antagonis Terhadap Pertumbuhan Miselium
R. microporus Penyebab Penyakit Akar Putih. hal: 653-657. dalam
Prosiding Kongres Nasional XV dan Seminar Ilmiah PFI, Purwokerto. Ilahang, Budi, Wibawa, G., dan Joshi, L., 2007. Status dan Pengendalian Penyakit
Jamur Akar Putih pada Sistem Wanatani Berbasis Karet Unggul di Kalimantan Barat.
Linawati, 2008. Chitosan: Limbah Kulit Udang untuk Diabetes dan Hipertensi.
Liyanage, A.S., 1976. Control of White Rott Disease Caused by Rigidoporus
(Fomes) lignosus. Bull. Rubb. Res. Inst. Srilangka V: No. 1. pp: 24-29.
Luthfi, 2006.Chitosan dan Cara Pembuatannya.
http//luthfi web.id/2006/12/01/chitosan. diakses 10 Januari 2009.
Pamekas, T., 2007. Potensi Ekstrak Cangkang Kepiting Untuk Mengendalikan Penyakit Pasca Panen Antraknosa pada Buah Cabai merah. Universitas Bengkulu, Bengkulu. Vol (10) No. 1, hal: 72-75.
Pamekas, T., Rogis, A., dan mucharromah 2007. Karakteristik dan Uji Efikasi Bahan Senyawa Alami Chitosan pathogen Pasca Panen Antraknosa
Colletotricum musae. Universitas Bengkulu, Bengkulu. Vol (9) No. 1,
2007 hal: 58-63.
Pinem, M.I., dan Yusuf, S., 2004. Buku Ajar Penyakit Tanaman Perkebunan. USU-Press, Medan, hal: 1-4.
Prasetiyo, K.W., dan Yusuf, S., 2005. Mencegah dan Membasmi Rayab Secara Ramah Lingkungan dan Kimiawi, Agromedia Pustaka, Tangerang, hal: 52-58.
Rahayu, S., Sujatno, dan Pawirosoemardjo, S., 2006. Management Pengendalian Penyakit Jamur Akar Putih pada Tanaman Karet, hal: 258-260, 265. dalam Prosiding Lokakarya Nasional Budidaya Tanaman Karet. Pusat Penelitian Karet, Sungei Putih.
Roblin, G., 2008. Early Events Induced by Chitosan on Plant Cells. 12 Februari, 2009.
Semangun, H., 2000. Penyakit – Penyakit Tanaman Perkebunan di Indonesia. Gadjah Mada University -Press, Yogyakarta, hal 11-30.
Sinaga, M. S., 2004. Strategi Pengelolaan Penyakit Penting Tanaman Karet di Indonesia pada Masa Mendatang. hal: 12 dalam Prosiding Pertemuan Teknis Strategi Pengelolaan Penyakit Tanaman Karet untuk Mempertahankan Potensi Produksi Mendukung Industri Perkaretan Indonesia tahun 2020. Palembang, 6 – 7 Oktober 2004, Pusat Penelitian Karet, Sembawa.
Sinulingga, W., 1989. Pengendalian Biologi Penyakit Cendawan Akar Putih Pada Tanaman Karet. Pusat Penelitian Karet, Sungei Putih, hal: 8-15.
Soepena, 1984., Penyakit Akar Tanaman Karet, Pusat Penelitian Karet, Sungei Putih, hal: 1-6.
, 1995.,Pengendalian Penyakit Jamur Akar putih Secara Biologis dengan Bio-Fungicide Saco-P pada Tanaman Karet, hal: 4-12. dalam Kumpulan Makalah Lokakarya Pengendallian Penyakit Penting Tanaman Karet. Pusat Penelitian Karet, Sungei Putih.
Spillance, J.J., 1989. Komoditi Karet: Peranannya dalam Perekonimian Indonesia. Kanisius, Yogyakarta, hal: 14
Suhandi, N., 2004. Pengendalilan Penyakit Jamur Akar Putih Untuk Mempertahankan populasi tanaman dan peningkatan produksi di PT. Brahma Binabakti, Jambi, hal: 153-155 dalam Prosiding Pertemuan Teknis Strategi Pengelolaan Penyakit Tanaman Karet untuk Mempertahankan Potensi Produksi Mendukung Industri Perkaretan Indonesia tahun 2020. Palembang, 6 – 7 Oktober 2004, Pusat Penelitian Karet, Sembawa.
Sujatno, Rahayu, S.T.S., Nugroho, P.A., dan Bukit, E., 2007. Evaluasi Pengaruh Penanaman ubi Kayu Terhadap pertumbuhan tanaman karet tahun tanam 2006 di Kebun Sungei Putih, PTPN-3, Balai Penelitian Karet, Sungei Putih, hal: 3-4.
Wilson, C.L., and A. El Ghaouth. 1993. Multifaceted Biological Control of Postharvest Disease of fruit and Vegetables. dalam Karakteristik dan Uji Efikasi Bahan Senyawa Alami Chitosan pathogen Pasca Panen Antraknosa
Colletotricum musae. Pamekas, dkk., 2007.
Wilson, et al., 1994. Potential of Induced Resistace to Control Postharvest disease of fruit and Vagetables. dalam Karakteristik dan Uji Efikasi Bahan Senyawa Alami Chitosan pathogen Pasca Panen Antraknosa Colletotricum
musae. Pamekas, dkk., 2007.
Keterangan:
Jumlah Petridish : 54 Jumlah Ulangan:
Replikasi : 3 Duplikasi : 3
Lampiran 2. Foto Luas Pertumbuhan Koloni Jamur Rigidoporus microporus
Gambar Pertumbuhan Koloni Jamur Gambar Pertumbuha KoloniJamur
R. microporus 1 HSI R. microporus 2
HSIGambar Pertumbuhan Koloni Jamur Gambar Pertumbuhan Koloni Jamur
Gambar Pertumbuhan Koloni Jamur Gambar Pertumbuhan Koloni Jamur
Lampiran 3. Data Pengamatan Luas Pertumbuhan Koloni Jamur R.microporus Pada Uji Efektifitas Chitosan 2 HSI (cm2)
Perlakuan
Ulangan
I II III
Replikasi
Total Rataan Replikasi Total Rataan Replikasi Total Rataan
1 2 3 1 2 3 1 2 3
Uji Jarak Duncan SY 0.06
P 2 3 4 5 6 7
SSR 0,01 4.32 4.55 4.68 4.76 4.81 4.92 LSR0,01 0.25 0.26 0.27 0.27 0.27 0.28 Perlakuan C5 C4 C3 C2 C1 C0 Rataan 0.41 6.14 6.73 7.49 8.24 9.89
.A .B
.C .D
Lampiran 4. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus Pada Uji Efektifitas Chitosan 3 HSI (cm2)
Perlakuan
Uji Jarak Duncan
SY 0.22 0.17
P 2 3 4 5 6 7
SSR 0,01 4.32 4.55 4.68 4.76 4.81 4.92 LSR 0,01 0.95 1.00 1.03 1.04 1.05 1.08 Perlakuan C5 C4 C3 C2 C1 C0 Rataan 1.11 19.43 20.62 21.86 23.18 26.12
.A .B
.C .D
Lampiran 5. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus Pada Uji Efektifitas Chitosan 4 HSI (cm2)
Perlakuan
Uji Jarak Duncan SY 0.37
P 2 3 4 5 6 7
SSR 0,01 4.32 4.55 4.68 4.76 4.81 4.92 LSR0,01 1.59 1.68 1.73 1.75 1.77 1.81 Perlakuan C5 C4 C3 C2 C1 C0 Rataan 1.51 33.69 36.03 37.11 38.80 49.43
.A B
.C .D
Lampiran 6. Data Pengamatan Luas Pertumbuhan Koloni Jamur R. microporus Pada Uji Efektifitas Chitosan 5 HSI (cm2)
Ulangan
Uji Jarak Duncan
SY 0.28 1.86 51.85 54.35 55.39 56.85 62.03
P 2 3 4 5 6 7
SSR 0,01 4.32 4.55 4.68 4.76 4.81 4.92 LSR0,0
1 1.19 1.26 1.29 1.31 1.33 1.36 Perlakuan C5 C4 C3 C2 C1 C0 Rataan 3.06 53.11 55.64 56.70 58.18 63.39
.A .B
C .D