39
LAMPIRAN 1
DATA BAHAN BAKU
L1.1 HASIL ANALISA KADAR AIR DAUN KATUK
Pada penelitian ini digunakan daun katuk (Sauropus androgynus (L) Merr) sebagai bahan baku. Adapun analisa yang dilakukan pada bahan baku daun katuk adalah analisa kadar air. Analisa dilakukan di Laboratorium Proses Industri Kimia Departemen Teknik Kimia USU.
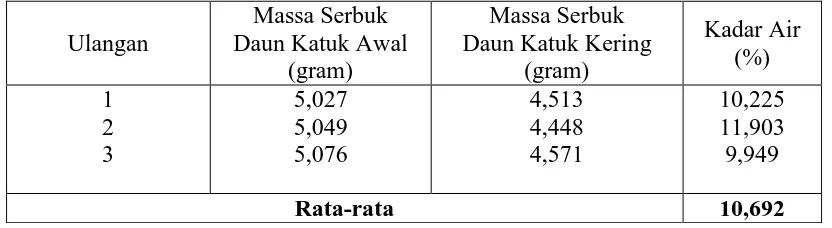
Tabel L1.1 Data Hasil Analisa Kadar Air Daun Katuk
Ulangan
Massa Serbuk Daun Katuk Awal
(gram)
Massa Serbuk Daun Katuk Kering
(gram)
Kadar Air (%)
1 2 3
5,027 5,049 5,076
4,513 4,448 4,571
10,225 11,903 9,949
40
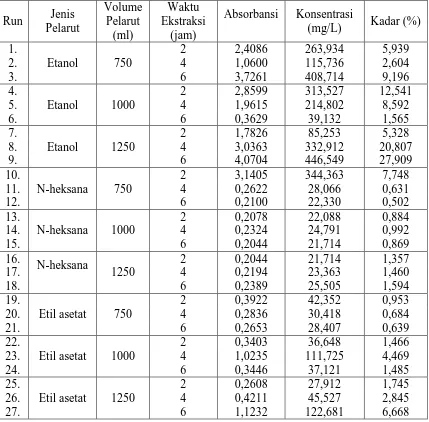
L1.2 ANALISA RENDEMEN EKSTRAK DAUN KATUK
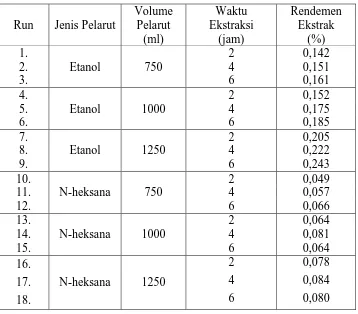
Tabel L1.2 Data Hasil Analisa Rendemen Ekstrak Daun Katuk
41
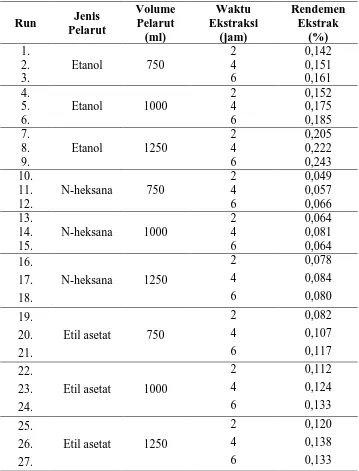
L1.3 ANALISA ABSORBANSI EKSTRAK DAUN KATUK
Tabel L1.3 Data Hasil Analisa Absorbansi Ekstrak Daun Katuk
42
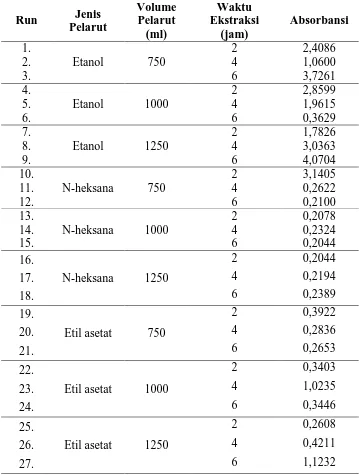
L1.4 ANALISA KADAR FLAVONOID TOTAL EKSTRAK DAUN KATUK
Tabel L1.4 Data Hasil Analisa Kadar Flavonoid Total Ekstrak Daun Katuk
43
LAMPIRAN 2
CONTOH PERHITUNGAN
L2.1 PERHITUNGAN KADAR AIR SERBUK DAUN KATUK
Sebelum dilakukan proses ekstraksi maka terlebih dahulu dilakukan analisa kadar air serbuk daun katuk agar diperoleh keseragaman kadar air bahan baku. Kadar air bahan baku yaitu ± 10%.
100%
Data serbuk daun katuk ulangan 1 Massa awal : 5,027 gram Massa kering akhir : 4,513 gram
100%
Penentuan kadar air serbuk daun katuk dilakukan dengan ulangan sebanyak 3 kali. Perhitungan kadar air ulangan selanjutnya dilakukan sama dengan contoh perhitungan di atas. Adapun hasil perhitungan kadar air serbuk daun katuk keseluruhan dapat dilihat pada tabel L2.1.
44
L2.2 PERHITUNGAN RENDEMEN EKSTRAK DAUN KATUK
100%
Contoh perhitungan rendemen ekstrak untuk sampel pada jenis pelarut etanol, volume pelarut 750 ml dan waktu ekstraksi 2 jam.
Massa sampel : 50 gram
Perhitungan rendemen ekstrak sampel selanjutnya sama dengan contoh perhitungan di atas. Adapun hasil perhitungan rendemen ekstrak sampel keseluruhan dapat dilihat pada tabel L2.2.
45
L2.3 PERHITUNGAN BAHAN KIMIA YANG DIGUNAKAN 2.3.1 Pembuatan Larutan AlCl3 10%
Massa AlCl3 : 1 gram
Volume aquades : 10 ml
Sebesar 1 gram AlCl3 padatan dilarutkan dengan aquades sebanyak 10 ml.
2.3.2 Pembuatan Larutan Na-asetat 1 M
Molaritas Na-asetat : 1 M Volume larutan : 10 ml Berat molekul Na-asetat : 98 gr/mol
gr
46
L2.4 PERHITUNGAN KADAR FLAVONOID TOTAL EKSTRAK DAUN KATUK
Perhitungan kadar flavonoid total dilakukan berdasarkan persamaan yang diperoleh dari kurva standar. Kurva standar yang digunakan menggunakan larutan quercetin yang biasanya digunakan untuk mengidentifikasi flavonoid total. Hasil kurva standar quercetin pada konsentrasi 1, 2, 3, 4, 5, 6 dan 7 ppm dapat dilihat pada tabel L2.3.
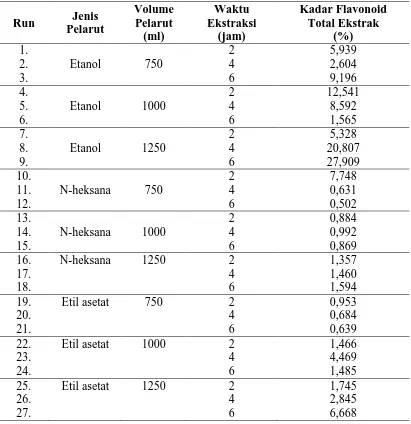
Tabel L2.3 Data Absorbansi Larutan Quercetin [17] Konsentrasi (ppm) Absorbansi
1 2 3 4 5 6 7
0,0160 0,0254 0,0331 0,0421 0,0539 0,0625 0,0693
Data pada tabel 2.3 diplotkan pada kurva sehingga diperoleh gambar seperti pada gambar L2.1.
Gambar L2.1 Hubungan antara Absorbansi dengan Konsentrasi Quercetin yang Dinyatakan dalam mg/L (ppm)
[17]
47 Dimana : y = absorbansi
x = konsentrasi flavonoid total
Persamaan regresi ini akan digunakan untuk menghitung konsentrasi flavonoid total ekstrak daun katuk.
Contoh perhitungan konsentrasi flavonoid total ekstrak untuk sampel pada jenis pelarut etanol, volume pelarut 750 ml dan waktu ekstraksi 2 jam dengan absorbansi (y) 2,4086.
y = 0,0091x + 0,0068 2,4086 = 0,0091 (x) + 0,0068 0,0091 (x) = 2,4018
x = 263,934 ppm = konsentrasi flavonoid total
Setelah diperoleh konsentrasi flavonoid total ekstrak, dilakukan perhitungan kadar flavonoid total ekstrak dengan persamaan sebagai berikut.
100%
Dimana : x = Konsentrasi flavonoid total Fp = Faktor pengenceran
w = Massa sampel v = Volume sampel
Contoh perhitungan kadar flavonoid total ekstrak untuk sampel pada jenis pelarut etanol, volume pelarut 750 ml dan waktu ekstraksi 2 jam.
48
Perhitungan kadar flavonoid total sampel selanjutnya sama dengan contoh perhitungan di atas. Adapun hasil perhitungan kadar flavonoid total sampel keseluruhan dapat dilihat pada tabel B.4.
49
LAMPIRAN 3
DOKUMENTASI PENELITIAN
L3.1 OVEN PADA PROSES PENGERINGAN
Gambar L3.1 Foto Oven Pada Proses Pengeringan
L3.2 HASIL PENGERINGAN DALAM OVEN
50
L3.3 P HASIL AYAKAN DAUN KATUK KERING
Gambar L3.3 Foto Sampel Daun Katuk Halus
L3.4 PROSES EKSTRAKSI DAUN KATUK
51
L3.5 PROSES FILTRASI EKSTRAK DAUN KATUK
Gambar L3.5 Gambar Proses Filtrasi Ekstrak Daun Katuk
L3.6 HASIL EKSTRAKSI DAUN KATUK
Gambar L3.6 Gambar Hasil Filtrasi Ekstrak Daun Katuk
L3.7 ALAT SPEKTOFOTOMETER
36
DAFTAR PUSTAKA
[1] Ameliawati, Dwi Astuti . "Pemanfaatan daun katuk sebagai ingredient fungsional dalam formulasi biskuit." Skripsi Program Diploma Fakultas Teknik UNM, Malang 2012, hal 2.
[2] Sidauruk, Bernard David. 2008. Produksi Air Susu Induk Babi dengan Penambahan Ekstrak Daun Katuk dalam Ransum pada Taraf dan Waktu Pemberian yang Berbeda. Program Studi Teknologi Produksi Ternak, Fakultas Peternakan, IPB, Bogor.
[3] Agus Budiyanto, Yulianingsih. " Pengaruh Suhu Dan Waktu Ekstraksi Terhadap Karakter Pektin Dari Ampas Jeruk Siam (Citrus Nobilis L)." Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian. Bogor., 2008.
[4] Agung Endro Nugroho, Abdul Malik, Suwidjio Pramono. " Total phenolic and flavonoid contents, and in vitro antihypertension activity of purified extract of Indonesian cashew leaves (Anacardium occidentale L.)." Jurnal International Food Research, 20(1), 2013 : 299 - 305
http://www.ifrj.upm.edu.my
[5] Dewi Maulida, Naufal Zulkarnaen. " Proses Antioksidan Likopen dari Buah Tomat dengan Menggunakan Solven Campuran n-heksana, Aseton dan Etanol. ." Tugas Akhir Program Sarjana. Jurusan Teknik Kimia Fakultas Teknik, Universitas Semarang. 2010.
[6] Cut Zuhra Fatimah, Juliati Br. Tarigan, Herlince Sihotang. " Aktivitas Antioksidan Senyawa Flavonoid Dari Daun Katuk (Sauropus Androgunus (L) Merr.)." Jurnal Biologi Sumatera Vol. 3 No. 1, Departemen Kimia FMIPA – USU, Januari 2008.
[7] Ana Andari. “Uji Aktivitas Ekstrak Daun Katu Sebagai Antioksidan Pada Minyak Kelapa.” Skripsi Program Sarjana Sains , Yogyakarta,2010.
[8] Muhammad Haris. Penentuan Kadar Flavonoid Total dan Aktifitas Antioksidan dari Daun Dewa dengan Spektrofotometer UV-Visibel. Fakultas Farmasi, Universitas Andalas. Padang .2011.
[9] Nuri Andarwulan, Ratna Batari, Diny Agustini Sandrasari, Braddley Bolling, Hanny Wijaya . “Flavonoid Content And Antioxidant Activity Of Vegetables From Indonesia” .Journal Food Chemistry. 121, 2010 : 1231 – 1235
http://www.elsevier.com/locate/foodchem
37
[11] Ahmad Ramadhan Eka, Haries Aprival Phaza " Pengaruh Konsentrasi Etanol, Suhu dan Jumlah Stage Pada Ekstraksi Oleoresin Jahe (Zingiber Officinale Rosc) Secara Batch”, Artikel Teknik Kimia, Fakultas Teknik, Universitas Diponegoro. 2010.
[15] Mohamed Ali Ar-Farsi and Chang Yong Lee . " Optimization of phenolics and dietary fibre extraction from date seeds". Journal of Food Science and Technology, Cornell University, Geneva, New York, USA.. 108, 2008 : 977 - 985
[16] Unin. “ kajian ekstrak biji mengkudu (Morinda Citrifolia L.) menggunakan pelarut organik ” Skripsi Sarjana Teknologi Pertanian. Bogor. September 2003. [17] Ratna Djamil, Wahyudi PS, Wahono S, M. Hanafi. “Antioxidant Activity Of Flavonoid From Andredera Cordifolia (Ten) Steenis Leaves”. Journal Of Research Farmasi, Moksha Publishing House, 3 (9), 2012 : 241 – 243
[18] Dwi Handayani, Abdul Mun’im, Anna S. Ranti. “ Optimation Of Green Tea Waste Axtraction Using Microwave Assisted Extraction To Yield Green Tea Extract”. Journal Of Farmacy. 19 (1), 2014. 29 – 35.
[19] Wei Liu, et al.” Optimization of Total Flavonoid Compound Extraction from Gynura medica Leaf Using Response Surface Methodology and Chemical Composition Analysis”. Journal Of Moleculer Sciences, 11, (2010) : 4750 – 4760. http:// www.mdpi.com/journal/ijms
[20] Bambang Irawan dan Bakti Jos. “Peningkatan Mutu Minyak Nilam Dengan
Ekstraksi Dan Destilasi Pada Berbagai Komposisi Pelarut” Jurnal Seminar Kimia
dan Proses, AKIN St. Paulus dan Teknik Kimia Universitas Diponegoro. 2010. [21] Petrus Darmawan. "Pengaruh Jenis Pelarut terhadap Rendemen Terhadap Minyak Bunga Cengkeh Mengggunakan Metode Ekstraksi Soxhletasi." Jurnal Teknik Kimia . Universitas Setia Budi, Surakarta, 2009.
38
[23] Nyi Gustina Mas Rosmeini Anica “ Sifat Aktivitas Ekstrak, Fraksi Pelarut, dan Senyawa Flavonoid Daun Sukun (artocarpus altilis) terhadap Enzim α-Glukosidase sebagai Antidiabetes.” Jurnal MIPA,Institude Pertanian Bogor, Bogor, 2012.
[24] Susiana Prasetyo, Henny Sunjaya, Yohanes Yanuar N.. " Pengaruh Rasio Massa Daun Suji / Pelarut, Temperatur Dan Jenis Pelarut Pada Ekstraksi Klorofil Daun Suji Secara Batch Dengan Pengontakan Dispersi." Jurusan Teknik Kimia, Fakultas Teknologi Industri Universitas Katolik Parahyangan, Bandung Mei. 2012. [25] Sabri Sudirman. “ Aktivitas Antioksidan dan Komponen Bioaktif kangkung
Air “Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan,
IPB, Bogor. 2011
[26] Yudhi Romansyah. “ Kandungan Senyawa Bioaktif Antioksidan Karang Lunak Alami dan Transplantasi di Perairan Pulau Pramuka, Kepulauan Seribu “. Departemen Ilmu dan Teknologi Kelautan, Fakultas Perikanan dan Ilmu Kelautan, IPB, Bogor. 2011.
16
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian ini dilakukan di Laboratorium Proses Industri Kimia, Jurusan Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan dan Laboratorium Pengujian Balai Teknik Kesehatan Lingkungan (BTKL) Sumatera Utara, Medan. Penelitian ini dilakukan selama 6 bulan.
3.2 BAHAN DAN PERALATAN 3.2.1 Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah : 1. Daun katuk
2. Etanol (C2H5OH)
3. N-heksana (C6H14)
4. Etil asetat (CH3COOC2H5)
5. Aluminium klorida (AlCl3)
17
3.2.3 Rangkaian Peralatan Penelitian
Gambar 3.1 Rangkaian Peralatan Penelitian
Keterangan gambar : 1. Statif
2. Klem
18
3.3 RANCANGAN PERCOBAAN
Penelitian ini menggunakan metode percobaan dengan Rancangan Acak Lengkap (RAL) faktorial dengan dua variabel bebas yaitu jenis pelarut, waktu ekstraksi dan volume pelarut pada prosedur ekstraksi. Menggunakan metode percobaan RAL ini diperoleh 27 kombinasi perlakuan, yaitu :
Tabel 3.1 Kombinasi Perlakuan pada Rancangan Percobaan
19
3.4 PROSEDUR PENELITIAN
3.4.1 Prosedur Pembuatan Serbuk Daun Katuk
1. Sampel (daun katuk segar) dipotong-potong sehingga ukurannya lebih kecil kemudian dibersihkan dari pengotor menggunakan air bersih lalu ditiriskan di atas tampah yang dialasi kain kering.
2. Sampel yang telah berukuran kecil dan bersih ditimbang sebanyak 2000 gram kemudian dikeringkan di dalam oven pada suhu 40 oC selama 4 hari.
3. Setelah kering, sampel dihaluskan menggunakan blender.
4. Sampel yang telah halus diayak dengan menggunakan ayakan berukuran 140 mesh sehingga diperoleh serbuk daun katuk.
[5].
3.4.2 Prosedur Analisa Kadar Air Serbuk Daun Katuk
1. Cawan aluminium dikeringkan di dalam oven pada suhu 100 oC selama 15 menit kemudian didinginkan di dalam desikator selama 10 menit lalu cawan ditimbang.
2. Serbuk daun katuk sebanyak ± 5 gram dimasukkan ke dalam cawan porselen lalu dikeringkan di dalam oven pada suhu 100 oC selama 6 jam kemudian didinginkan dalam desikator lalu ditimbang beratnya.
3. Serbuk daun katuk kembali dikeringkan dalam oven selama 30 menit lalu ditimbang kembali beratnya.
4. Perlakuan nomor 3 diulangi terus hingga diperoleh berat kering yang relatif konstan (dianggap konstan jika selisih berat kering yang ditimbang
). gram 0,0003
5. Kadar air dari serbuk daun katuk ditentukan menggunakan persamaan
20
3.4.3 Prosedur Ekstraksi Daun Katuk
1. Serbuk daun katuk ditimbang sebanyak 50 gram kemudian dimasukkan ke dalam beaker glass.
2. Pelarut etanol ditambahkan sebanyak 750 ml ke dalam beaker glass lalu diaduk.
3. Campuran dimasukkan ke dalam labu leher empat. 4. Peralatan ekstraksi dirangkai (seperti pada gambar 3.1).
5. Magnetic stirrer dimasukkan ke dalam labu leher tiga dan diatur kecepatannya sebesar 7 rpm.
6. Hot plate dinyalakan dan diatur suhunya sebesar 60 oC. 7. Ekstraksi dibiarkan berlangsung selama 2 jam.
8. Setelah waktu ekstraksi tercapai, hot plate dimatikan dan hasil ekstraksi dituang ke dalam beaker glass.
9. Ekstrak diambil dengan cara filtrasi yaitu hasil ekstraksi disaring menggunakan kertas saring kemudian filtrat ditampung ke dalam beaker glass dan residu yang tersaring di kertas saring dibuang.
10.Hasil filtrasi berupa filtrat, dipekatkan menggunakan rotary evaporator dengan suhu 70 oC.
11.Prosedur dilakukan kembali dengan sampel yang sesuai dengan kombinasi perlakuan (seperti pada tabel 3.1).
[5].
3.4.4 Prosedur Penentuan Rendemen Ekstrak
1. Massa sampel serbuk daun katuk yang digunakan untuk proses ekstraksi dicatat yaitu sebesar 50 gram.
2. Ekstrak pekat yang dihasilkan dari proses ekstraksi daun katuk ditimbang. 3. Persentase rendemen ekstrak ditentukan menggunakan persamaan
21
3.4.5 Prosedur Penentuan Kadar Flavonoid Total Ekstrak
1. Penentuan kadar flavonoid total ekstrak dilakukan dengan menggunakan 2 ml ekstrak.
2. Larutan AlCl3 10% sebanyak 0,1 ml, larutan Na-asetat 1 M sebanyak 0,1 ml
dan aquadest sebanyak 2,8 ml ditambahkan pada larutan . 3. Campuran dikocok homogen lalu dibiarkan selama 30 menit. 4. Serapan campuran diukur pada panjang gelombang 415 nm. 5. Kadar flavonoid total dihitung menggunakan persamaan linear.
22
3.5 FLOWCHART PENELITIAN
3.5.1 Prosedur Pembuatan Serbuk Daun Katuk
Gambar 3.2 Flowchart Prosedur Pembuatan Serbuk Daun Katuk Mulai
Daun katuk segar dipotong kecil-kecil
Dicuci bersih dan ditimbang sebanyak 2000 gram
Dikeringkan di dalam oven pada suhu 40 oC selama 4 hari
Dihaluskan menggunakan blender
Diayak dengan ayakan 140 mesh
Tidak Apakah sampel
sudah berukuran 140
23
3.5.2 Prosedur Analisa Kadar Air Serbuk Daun Katuk
Gambar 3.3 Flowchart Prosedur Analisa Kadar Air Serbuk Daun Katuk Mulai
Dikeringkan cawan aluminium di dalam oven pada suhu 100 oC selama 15 menit
Didinginkan di dalam desikator selama 10 menit lalu ditimbang beratnya
Ditimbang serbuk daun katuk sebanyak ± 5 gram dan dimasukkan ke dalam cawan aluminium
Dikeringkan di dalam oven pada suhu 100 oC selama 6 jam lalu didinginkan dalam desikator
Ditimbang beratnya
Dikeringkan dalam oven selama 30 menit kemudian ditimbang beratnya
Tidak Apakah berat
kering sudah konstan ?
Ya Ditentukan kadar air bahan
24
3.5.3 Prosedur Ekstraksi Daun Katuk
Mulai
Ditimbang sampel sebanyak 50 gram dan dimasukkan ke dalam beaker glass
Ditambahkan pelarut etanol sebanyak 750 ml ke dalam beaker glass lalu diaduk
Dimasukkan campuran ke dalam labu leher tiga
Dirangkai peralatan ekstraksi (seperti pada gambar 3.1)
Dimasukkan magnetic stirrer ke dalam labu leher tiga dan diatur kecepatannya sebesar 7 rpm
Dinyalakankan hot plate dan diatur suhunya sebesar 60 oC Ya Dibiarkan ekstraksi berlangsung selama 2 jam
Setelah waktu ekstraksi tercapai, dimatikan hot plate dan hasil ekstraksi dituang ke dalam beaker glass
Difiltrasi hasil ekstraksi menggunakan kertas saring kemudian filtrat ditampung ke dalam beaker glass dan residu dibuang
Dipekatkan filtrat menggunakan rotary evaporator sehingga diperoleh filrat pekat
Apakah masih ada kombinasi perlakuan sampel
25
3.5.4 Prosedur Penentuan Rendemen Ekstrak
Gambar 3.5 Flowchart Prosedur Penentuan Rendemen Ekstrak Gambar 3.4 Flowchart Prosedur Ekstraksi Daun Katuk
24 Mulai
Dicatat massa sampel yang digunakan untuk proses ekstraksi yaitu sebesar 50 gram
Ditimbang ekstrak pekat yang dihasilkan dari proses ekstraksi daun katuk
Dihitung persentase rendemen ekstrak
26
3.5.5 Prosedur Penentuan Kadar Flavonoid Total Ekstrak
Mulai
Penentuan kadar flavonoid total ekstrak dilakukan dengan mengganti larutan standar kuersetin menggunakan 2 ml ekstrak
Larutan AlCl3 10% sebanyak 0,1 ml,
larutan Na-asetat 1 M sebanyak 0,1 ml dan aquadest sebanyak 2,8 ml ditambahkan pada larutan standar
kuersetin
Campuran dikocok homogen lalu dibiarkan selama 30 menit
Serapan campuran diukur pada panjang gelombang 415 nm
Kadar flavonoid total dihitung menggunakan persamaan linear
Selesa
27
BAB IV
HASIL DAN PEMBAHASAN
Pada bab ini akan dibahas hasil penelitian pengaruh waktu reaksi (dengan variasi 2, 4, 6 jam), volume pelarut (dengan variasi 750, 1.000, 1.200 ml), dan jenis pelarut (dengan variasi etanol, n-heksana, dan etil asetat) dengan menggunakan ekstraksi padat cair.
Pembahasan dibagi atas dua bagian yaitu pembahasan pengaruh waktu reaksi, volume pelarut, dan jenis pelarut terhadap rendemen ekstrak daun katuk. Dan pengaruh waktu reaksi, volume pelarut, dan jenis pelarut terhadap kadar flavonoid.
4.1 PENGARUH WAKTU REAKSI, VOLUME PELARUT, DAN JENIS PELARUT TERHADAP RENDEMEN EKSTRAK DAUN KATUK 4.1.1 Jenis Pelarut Etanol, N-heksana dan Etil Asetat
Pada percobaan ini digunakan daun katuk 50 gram dengan volume pelarut 750, 1.000, dan 1.250 ml, dengan jenis pelarut etanol, N-heksana dan etil asetat dan variasi waktu ekstraksi 2, 4, 6 jam (hasil percobaan pada tabel L1.2 ).
28
dapat dilihat bahwa semakain lama waktu ekstraksi maka rendemen yang diperoleh semkain meningkat. Pada jenis pelarut etanol semakin lama waktu reaksi makakadar rendemen yang diperoleh semakin meningkat. Pada volume 750 ml diperoleh hasil rendemen dari 0,142% hingga 0,161%, volume 1000 ml diperoleh dari 0,152% hingga 0,185%, dan untuk volume 1250 diperoleh dari 0,205 hingga 0,243%. Dari hasil data yang diperoleh bahwa waktu ekstraksi terbaik adalah pada waktu 6 jam dengan volume pelarut 1250 ml yaitu sebesar 0,243%.
Sedangkan untuk jenis pelarut n-heksana dapat dilihat bahwa sedmakin lama waktu reaksi maka kadar rendemen yang diperoleh semakin besar. Pada volume 750 ml diperoleh hasil rendemen dari 0,049% hingga 0,066%, volume 1000 ml diperoleh dari 0,064% dan untuk volume 1250 diperoleh dari 0,078 hingga 0,080%.
Untuk jenis pelarut etil asetat dapat dilihat bahwa semakin lama waktu rekasi maka rendemen yang dihasilkan semakin besar. Dapat dilihat bahwa volume 750 ml diperoleh hasil rendemen dari 0,082% hingga 0,117%, volume 1000 ml diperoleh dari 0,112% hingga 0,133%, dan untuk volume 1250 diperoleh dari 0,120% hingga 0,133%.
29
ketiga jenis pelarut yang digunakan yaitu etanol, n-heksana dan etil asetat diketahui bahwa jenis pelarit yang paling polar adalah etanol dan n-heksana.
Beberapa peneliti seperti Agus Budiyanto dengan judul penelitian “pengaruh suhu dan waktu ekstraksi terhadap karakter pektin dari ampas jeruk bahwa Kenaikan waktu ekstraksi mempengaruhi meningkatnya rendemen yang dihasilkan”. Semakin lama waktu ekstraksi, rendemen pektin yang dihasilkan semakin besar [3] dan (Dwi Handayani, Abdul Mun’im and Anna S. Rantidengan judul “optimasi ekstraksi ampas teh hijau (camellia sinensis) menggunakan metode microwave assisted extraction untuk menghasilkan ekstrak teh hijau”. Berdasarkan variasi waktu, untuk rendemen didapatkan hasil semakin lama waktu ekstraksi, rendemen yang didapatkan semakin banyak [18]. Waktu ekstraksi merupakan faktor yang akan berpengaruh secara signifikan terhadap efisiensi ekstraksi dari tanaman obat atau sayuran yang dapat dimakan [22]. Penelitian yang dilakukan Menurut penelitian sebelumnya yang dilakukan oleh Mandana Bimark dan juga penelitian yang dilakukan Darmawan bahwa senyawa alkohol seperti heksana dapat mempengaruhi hasil ekstraksi berdasarkan kepolaran dari larutan itu sendiri [21].
Menurut penelitian sebelumnya yang dilakukan oleh Bambang Irawan dan Jos,” pada grafik hubungan antara waktu reaksi dengan rendemen menunjukkan bahwa semakin lama waktu reaksi, maka rendemen yang dihasilkan semakin tinggi. Hal ini disebabkan proses pencampuran antara pelarut ke dalam bahan baku, dimana kelarutan komponen-komponen serbuk akan akan berjalan perlahan sebanding dengan kenaikan waktu” [20].
Dari hasil percobaan diatas dapat disimpulkan bahwa waktu reaksi terbaik adalah waktu 2 jam dan volume pelarut 1.250 ml dengan jenis pelarut etanol. Untuk mengetahui perbandingan standar kadar rendemen ekstrak daun katuk dengan hasil yang diperoleh dapat dilihat pada tabel 4.1 berikut ini.
Jenis Pelarut Kadar Rendemen (%) Hasil Penelitian
(Pengaruh waktu Ekstraksi, Volume Pelarut dan Jenis Pelarut terhadap Rendemen dan Kadar Flavonoid Total pada Ekstraksi Daun Katuk)
Hasil Literatur [27]
Etanol 0,243 0,275
N-heksana 0,084 0,08
30
4.2 PENGARUH WAKTU REAKSI, VOLUME PELARUT, DAN JENIS PELARUT TERHADAP FLAVONOID.
4.2.1 Jenis Pelarut Etanol, N-heksana dan Etil Asetat
Pada percobaan ini digunakan daun katuk 50 gram dengan volume pelarut 750, 1.000, dan 1.250 ml, dengan jenis pelarut etanol, N-heksana dan etil asetat dan variasi waktu ekstraksi 2, 4, 6 jam (hasil percobaan pada tabel L1.4 ).
Gambar 4.2 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap Kadar Flavonoid dengan Jenis Pelarut Etanol, N-heksana dan Etil Asetat Gambar 4.4 menunjukkan hubungan waktu reaksi terhadap kadar flavonoid dengan jenis pelarut etanol dengan waktu ekstraksi 2 jam, 4 jam, dan 6 jam dengan variasi volume pelarut 750 ml, 1000 ml, 1250 ml. Dari grafik diperoleh bahwa pada volume 750 ml diperoleh hasil kadar flavonoid total dari 5,939% hingga 9,196%, volume 1000 ml diperoleh dari 12,541% hingga 1,565%, dan untuk volume 1250 diperoleh dari 5,328 hingga 27,909%. Dari grafik 4.2 dapat dilihat bahwa semakin lama waktu reaksi kadar flavonoid yang diperoleh semakin meningkat. semakin tinggi kadar total flavonoid yang dihasilkan berarti antioksidan yang dihasilkan dari ekstrak daun katuk itu tinggi. Pada jenis pelarut etanol dengan variasi waktu ekstraksi 2 jam, 4 jam, dan 6 jam diperoleh nilai kadar flavonoid total yang fluktuatif, dimana pada saat pada volume 750 ml dengan waktu 2 jam mengalami penurunan yang derastis menuju volume 1250 ml dengan nilai rendemen 5,939% menjadi 5,328% namun pada saat volume 1000 mengalami puncaj nilai rendemen yaitu 12,541%. Sedangkan untuk waktu 4 jam mengalami penaikan rendemen yang sangat signifikan bebentuk hgaris lurus. Dan untuk wakti 6 jam voleme pelarut terhadap rendemen diperoleh hasil yang fluktuatif dimana sama hal nya dengan
31
waktu 2 jam namun pada volume ini mencapai nilai volume pelarut terhadap rendemen tertinggi yaitu pada volume 1250 dengan waktu 6 jam dari 9,196% menjadi 27,909%. Sehingga diperoleh hasil rendemen tertinggi pada volume 1.250 ml dengan waktu 6 jam. dan jenis pelarut etanol dengan waktu ekstraksi 2 jam, 4 jam, dan 6 jam dengan variasi volume pelarut 750 ml, 1000 ml, 1250 ml. Dari grafik diperoleh bahwa pada volume 750 ml diperoleh hasil kadar flavonoid total dari 7,748% hingga 0,502%, volume 1000 ml diperoleh dari 0,884% hingga 0,869%, dan untuk volume 1250 diperoleh dari 1,357 hingga 1,594%. Untuk mengetahui pengaruh waktu ekstraksi terhadap kadar flavonoid dengan jenis pelarut Etanol pada serbuk kering daun katuk, dilakukan sejumlah percobaan Pada pelarut etanol dengan variasi volume pelarut (v) 750 ml diperoleh grafik semakin meningkatnya kadar flavonoid total secara fluktuatif. Sedangkan untuk variasi volume pelarut 1000 ml diperoleh kadar flavonoid total mengalami penurunan yang tidak terlalu signifikan, dan untuk variasi volume pelarut 1250 ml diperoleh kadar total flavonoid yang meningkat yaitu dengan diperolehnya kadar flavonoid total tertinggi yaitu 27,9 %.
Pada jenis pelarut N-heksanal dengan variasi waktu ekstraksi 2 jam, 4 jam, dan 6 jam diperoleh nilai kadar flavonoid total yang fluktuatif, pada volume 750 ml dan waktu ekstraksi 2 jam kadar flavonoid yang sangat tinggi yaitu dengan kadar flavonoid 7,748% sedangkan untuk waktu ekstraksi 4 jam dan 6 jam diperoleh kadar flavonoid yang rendah yaitu masing masing kadar flavonoid total adalah 0,631% dan 0,502%. Dan pada volume 1.000 ml pada waktu ekstraksi 2 jam diperoleh masing-masing kadar flavonoid total sebesar 0,884%, 0,992%,dan 0,869%. Dan pada volume 1.250 ml pada waktu ekstraksi 2 jam diperoleh masing-masing kadar flavonoid total sebesar 1,357%, 1,460%,dan 1,594%. Pada jenis pelarut N-heksana ini sangat tidak diinginkan karena diperoleh grafik yang tidak beraturan yaitu diperoleh nilai nilai falvonoid tertinggi pada volume 750 ml dengan waktu 2 jam. namun yang dapat dilihat sesuai teori yaitu pada waktu 6 jam yaitu dengan volume pelarut masing-masing berurutan mengalami kenaikan sesuai dengan teori. Hal ini disebabkan beberapa faktor yaitu adanya kesalahan pada saat melakukan ekstraksi yaitu salah satunya waktu ekstraksi yang berlebihan pada saat proses ekstraksi dilakukan. Hal
ini disebabkan dipengaruhi kepolaran suatu pelarut. Seperti yang dilakukan oleh
32
flavonoid total 1,5 %. Sedangkan untuk variasi volume pelarut 1000 ml dan 1250 ml diperoleh kadar flavonoid total yang hamper tidak mengalami peningkatan kadar flavonoid total.
33
Pada jenis pelarut etil asetat dengan variasi waktu ekstraksi 4 jam mengalami penurunan nilai kadar total flavonoid, sedangkan untuk waktu ekstraksi 2 jam dan 6 jam diperoleh kadar total flavonoid mengalami kenaikan hasil kadar total flavonoid. Sedangkan untuk waktu 4 jam diperoleh volume pelarit dan kadar flavonoid yang tidak beraturan namun pada saat waktu 6 jam volume pelarut meningkat seiring dengan meningkatnya waktu ehinggda diperoleh kadar flavonoid sebesar 7,668%. Apabila telah diperoleh kadar flavonoid total dari bahan yang diekstrak dan mempunyai titik maksimum pada waktu reaksi tertentu, sehingga ekstraksi dilakukan dengan menggunakan waktu ekstraksi dan jenis pelarut lainnya sehinga diperoleh kadar total flavonoid dari masing-masing variabel. Setelah senyawa polifenol pada ekstrak diperoleh, maka polifenol (flavonoid) yang dihasilkan dapat digunakan sebagai antioksidan yang digunakan untuk menetralisir radikal bebas pada antioksidan dan kemudian akan menghasilkan nilai bilangan peroksida. Menurut penelitian sebelumnya yang dilakukan oleh Mandana Bimark,”semakin banyak volume pelarut, maka semakin besar rendemen hasil dari ekstrak”. Dengan demikian maka volume pelarut digunakan untuk menentukan nilai rendemen tertinggi untuk senyawa flavonoid [22]. Akan tetapi jika volume pelarut terlalu banyak digunakan maka kadar rendemen akan turun karena semakin banyak pelarut digunakan dan semakin waktu reaksi akan semakin akan menyebabkan perubahan sifat dan komposisi dari ekstrak sehingga mudah menguap dan akhirnya terkondensasi [20].
Dari hasil percobaan ini sesuai dengan penelitian sebelumnya bahwa jenis pelarut terbaik pada proses ekstraksi adalah pelarut etanol dengan waktu maksimum ekstraksi adalah 6 jam, semakin lama waktu ekstraksi maka rasio pelarut akan semakin padat karena adanya proses penguapan pada pelarut [3]. Untuk mengetahui perbandingan standar kadar flavonoid total ekstrak daun katuk dengan hasil yang diperoleh dapat dilihat pada tabel 4.1 berikut ini.
Jenis Pelarut
Kadar Flavonoid Total (%) Hasil Penelitian
(Pengaruh waktu Ekstraksi, Volume Pelarut dan Jenis Pelarut terhadap Rendemen dan Kadar Flavonoid Total pada Ekstraksi Daun Katuk)
Hasil Literatur [27]
Etanol 27,90 30,33
N-heksana 7,748 6,277
34
BAB V
KESIMPULAN
5.1 KESIMPUAN
Adapun kesimpulan yang diperoleh pada penelitian ini adalah sebagai berikut:
1. Pengaruh waktu ekstraksi terhadap rendemen ekstrak daun katuk terbaik pada proses ekstraksi daun katuk diperoleh pada watu ekstraksi 6 jam dengan pelarut etanol dan volume pelarut 1250 jam yaitu sebesar 0,24%.
2. Pengaruh volume pelarut terhadap rendemen pada ekstraksi daun katuk terbaik diperoleh pada volume pelarut 1250 ml dengan jenis pelarut etanol yaitu sebesar 0,243%
3. Pengaruh jenis pelarut terhadap rendemen ekstraksi daun katuk diperoleh adalah jenis pelarut etanol pada waktu 6 jam yaitu sebesar 0,243%
4. Pengaruh waktu ekstraksi terhadap kadar flavonoid terbaik pada proses ekstraksi daun katuk diperoleh pada watu ekstraksi 6 jam dengan pelarut etanol dengan volume pelarut 1250 jam yaitu sebesar 27,909%.
5. Pengaruh volume pelarut terhadap kadar flavonoid terbaik pada proses ekstraksi daun katuk menjadi flavonoid diperoleh pada pelarut etanol dengan volume pelarut 1.250 ml, pada waktu 6 jam yaitu sebesar 27,909%.
6. Pengaruh waktu ekstraksi terhadap kadar flavonoid terbaik pada proses ekstraksi daun katuk menjadi flavonoid diperoleh pada watu ekstraksi 6 jam dengan pelarut etanol dengan volume pelarut 1250 jam yaitu sebesar 27,909%.
7. Pengaruh waktu ekstraksi, volume pelarut, dan jenis pelarut terhadap rendemen diperoleh waktu ekstraksi terbaik pada saat 6 jam dengan volume pelarut 1250 ml dengan jenis pelarut etanol.
35
5.2 SARAN
Adapun saran yang dapat diberikan setelah melakukan penelitian ini adalah sebagai berikut:
1. Untuk penelitian berikutnya diharapkan dapat mencari cara untuk menghilangkan kandungan zat warna yang masih terdapat di dalam antioksidan daun sirih seperti menggunakan karbon aktif atau bahan lainnya yang mampu mengurangi kadar warna antioksidan.
6
BAB II
TINJAUAN PUSTAKA
2.1 TANAMAN KATUK (Sauropus androgynus (L) Merr)
Katuk (Sauropus androgynus (L) Merr) merupakan tanaman yang tumbuh subur di Indonesia, diketahui mengandung senyawa aktif yang memiliki aktifitas antioksidan dengan menangkap radikal bebas hidroksil yang diuji dengan metode Deoxyribose. Katuk termasuk tanaman jenis perdu berumpun dengan ketinggian
3-5 m. Batangnya tumbuh tegak dan berkayu. Jika ujung batang dipangkas, akan tumbuh tunas-tunas baru yang membentuk percabangan. Daunnya kecil-kecil mirip daun kelor, berwarna hijau. Katuk termasuk tanaman yang rajin berbunga. Bunganya kecil-kecil, berwarna merah gelap sampai kekuning-kuningan, dengan bintik-bintik merah. Bunga tersebut akan menghasilkan buah berwarna putih yang di dalamya terdapat biji berwarna hitam [7]. Tanaman katuk dapat dilihat pada gambar 2.1 berikut ini.
Gambar 2.1 Tanaman Katuk (Sauropus androgynus (L) Merr) [7]
7
lemak, vitamin, mineral, saponin, flavonid dan tanin. Beberapa senyawa kimia yang terdapat dalam tanaman katuk diketahui berkhasiat obat [6].
Tanaman katuk banyak dimanfaatkan sebagai sayuran atau lalapan dan dipercaya masyarakat mampu melancarkan air susu ibu (ASI) dan mempercepat pemulihan tenaga bagi orang sakit. Tanaman katuk juga bermanfaat sebagai tanaman obat keluarga (TOGA), bahan makanan dan sebagai tanaman hias. Rebusan daun katuk memberikan rasa yang agak asam dan manis, air perasan daun katuk digunakan juga untuk memberi warna pada makanan, disamping itu air rebusan daun dan akarnya digunakan sebagai obat demam, diuretika dan meningkatkan ASI [6].
2.2 FLAVONOID
Flavonoid adalah senyawa yang paling fenolat tanaman. Dalam studi tersebut, kandungan total flavonoid ditentukan dengan menggunakan metode dimodifikasi berdasarkan prosedur Chang et al. (2002) divalidasi oleh Mujahid (2011) menggunakan rutin sebagai standar acuan. Pada prinsipnya, prosedur ini berkaitan dengan pembentukan kompleks antara flavonoid dan AlCl3 yang menghasilkan solusi berwarna kuning. Absorbansi diukur dengan spektrofotometer pada panjang gelombang maksimum 415 nm. Total kandungan flavonoid adalah setara dengan rutin di miligram per gram bahan kering fraksi [25].
8
Konsisten dengan literatur, nilai Total fenol yang sangat berkorelasi dengan DPPH, ABTS dan sianida besi mengurangi kekuatan antioksidan nilai dengan nilai R dari 0,77, 0,79, 0,85, masing-masing (P <0,01). Konten flavonoid tidak berkorelasi dengan antioksidan aktivitas di DPPH, ABTS, dan mengurangi tes daya. Flavonoid konten berkorelasi negatif dengan penghambatan oksidasi lipid (R =0,78, P = 0,005). Hal ini mempengaruhi juga bisa dikaitkan dengan logam atau konstituen pro-oksidan lainnya di ekstrak. ABTS, DPPH, dan besi mengurangi langkah-langkah kekuatan antioksidan yang sangat berkorelasi (R> 0,9000, P <0,0001) satu sama lain, dengan peringkat yang berbeda perintah kapasitas antioksidan. Hasil ini menyoroti kontribusi fenolat dalam vitro aktivitas antioksidan sayuran dan kebutuhan untuk menganalisis keragaman tes antioksidan untuk peringkat aktivitas antioksidan [9].
2.3 EKSTRAKSI
Ekstraksi merupakan proses pemisahan dua zat atau lebih dengan menggunakan pelarut yang tidak saling bercampur. Berdasarkan fase yang terlibat, terdapat dua jenis ekstraksi yaitu:
1. yaitu ekstraksi cair-cair dan 2. ekstraksi padat-cair.
Pemindahan komponen dari padatan ke pelarut pada ekstraksi padat-cair melalui tiga tahapan, yaitu difusi pelarut ke pori-pori padatan atau ke dinding sel, di dalam dinding sel terjadi pelarutan padatan oleh pelarut, dan tahapan terakhir adalah pemindahan larutan dari pori-pori menjadi larutan ekstrak. Ekstraksi padat-cair dipengaruhi oleh waktu ekstraksi, suhu yang digunakan, pengadukan, dan banyaknya pelarut yang digunakan. Terdapat dua macam ekstraksi padat-cair, yaitu dengan cara sokhlet dan perkolasi dengan atau tanpa pemanasan (Sabel & Warren 1973 dalam Muchsony 1997). Menurut Brown (1950) dalam Muchsony (1997), metode lain yang lebih sederhana dalam mengekstrak padatan adalah dengan mencampurkan seluruh bahan dengan pelarut, lalu memisahkan larutan dengan padatan tak terlarut [10].
Penjelasan tentang faktor-faktor yang mempengaruhi ekstraksi yaitu :
9
Persiapan bahan baku sebelum proses ekstraksi mencakup pengeringan bahan dan pengecilan ukuran bahan hingga mencapai ukuran yang tepat sesuai dengan keperluan ekstraksi. Ukuran partikel bahan merupakan salah satu faktor yang berpengaruh terhadap keberhasilan proses ekstraksi. Semakin kecil ukuran partikel, semakin besar luas bidang kontak antara padatan dan pelarut, serta semakin pendek jalur difusinya, yang menjadikan laju transfer massa semakin tinggi [10]. Selain itu, waktu yang diperlukan komponen untuk keluar dari bahan menjadi lebih singkat sehingga proses ekstraksi dapat berlangsung lebih cepat. Teknik pengecilan ukuran bahan dapat dilakukan dengan cara pengirisan, penghancuran atau penggilingan dengan mesin. Partikel bahan setelah pengecilan sebaiknya berukuran seragam untuk mempermudah difusi pelarut ke dalam bahan. Bahan yang teralu halus juga dapat menggumpal sehingga sukar ditembus pelarut. Oleh karena itu ukuran partikel yang baikk untuk proses ekstraksi adalah serbuk dengan ukuran 0,5 nm [11].
Pengeringan bahan sampai kadar air tertentu juga merupakan salah satu perlakuan pendahuluan terhadap bahan sebelum proses ekstraksi. Pengeringan juga dapat mempermudah proses pengecilan ukuran dan meningkatkan mutu ekstrak dengan menghindari adanya air dalam ekstrak. Kadar air yang tinggi dapat menyebabkan hasil ekstrak mengandung komponen larut air seperti pati dan gula. Umumnya tumbuhan dikeringkan pada suhu kamar dengan suhu kurang dari 30
o
C dan terhindar dari sinar matahari langsung. Radiasi sinar ultraviolet akibat pengeringan dengan matahari langsung dapat menyebabkan terjadinya perubahan komposisi senyawa penyusun bahan [11].
2.3.2 Pemilihan Jenis Pelarut
10
didapat. Pelarut yang banyak digunakan dalam proses ekstraksi dengan pelarut adalah aseton, etanol, metanol, etil asetat, kloroform, heksana dan etilen diklorida [27].
2.3.3 Perbandingan Jumlah Pelarut dan Bahan
Semakin besar volume pelarut yang digunakan dibandingkan jumlah bahan yang diekstrak maka rendemen yang dihasilkan juga semakin besar. Semakin banyak pelarut yang ditambahkan maka semakin besar kemampuan pelarut untuk melarutkan bahan sehingga semakin banyak komponen bahan yang dapat terekstrak oleh pelarut. Rendemen hasil ekstraksi akan terus meningkat hingga larutan menjadi jenuh. Setelah titik jenuh larutan, tidak akan terjadi peningkatan rendemen dengan penambahan pelarut [27].
2.3.4 Pengaturan Kondisi Ekstraksi
Lama ekstraksi menentukan jumlah komponen yang dapat diekstrak dari bahan. Lama ekstraksi berhubungan dengan waktu kontak antara bahan dan pelarut. Semakin lama waktu ekstraksi maka kesempatan untuk bersentuhan antara bahan dan pelarut semakin besar sehingga kelarutan komponen bioaktif dalam larutan akan meningkat.
Proses pengadukan larutan merupakan salah satu faktor penting dalam proses ekstraksi untuk mempercepat pelarutan zat padat dan meningkatkan laju difusi bahan terlarut. Pergerakan pelarut disekitar bahan akibat pengadukan dapat mempercepat kontak bahan dengan pelarut dan memindahkan komponen dari permukaan bahan ke dalam larutan dengan jalan membentuk suspensi serta melarutkan komponen tersebut ke dalam media pelarut. Pengadukan dapat dilakukan dengan cara mekanis, penyemprotan udara atau dengan kombinasi keduanya [11].
11
2.4 JENIS PELARUT
Sebagai tenaga pemisah, solven harus dipilih sedemikian hingga kelarutannya terhadap salah satu komponen murninya adalah terbatas atau sama sekali tidak saling melarutkan. Karenanya, dalam proses ekstraksi akan terbentuk dua fase cairan yang saling bersinggungan dan selalu mengadakan kontak. Fase yang banyak mengandung diluen disebut fase rafinat sedangkan fase yang banyak mengandung solven dinamakan ekstrak. Terbentuknya dua fase cairan, memungkinkan semua komponen yang ada dalam campuran terbesar dalam masing – masing fase sesuai dengan koefisien distribusinya, sehingga dicapai keseimbangan fisis. Pemisahan kedua fase seimbang dengan mudah dapat dilakukan jika density fase rafinat dan fase ekstrak mempunyai perbedaan yang cukup. Tetapi jika density keduanya hampir sama proses pemisahan semakin sulit, sebab campuran tersebut cenderung untuk membentuk emulsi. Dibidang industri, ekstraksi sangat luas penggunaannya terutama jika larutan yang akan dipisahkan tediri dari komponen – komponen :
1. Mempunyai sifat penguapan relatif yang rendah. 2. Mempunyai titik didih yang berdekatan.
3. Sensitif terhadap panas.
4. Merupakan campuran azeotrop.
Adapun pelarut (solven yang sering digunakan digunakan pada penelitian adalah sebagai berikut :
2.4.1 Etanol
Etanol (disebut juga etil-alkohol atau alkohol saja), adalah alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Karena sifatnya yang tidak beracun bahan ini banyak dipakai sebagai pelarut dalam dunia farmasi dan industri makanan dan minuman. Etanol merupakan jenis pelarut polar.
12 6. Soluble in water : insoluble 7. Density : 0,7991 gr/cc 8. Temperatur kritis : 243,1 oC 9. Tekanan kritis : 63,1 atm
Etanol banyak digunakan dalam penelitian sebelumnya sebagai bahan pelarut dengan berbagai variasi sampel, temperature, dan juga jenis proses ekstraksinya . Seperti pada penelitianyang dilakukan oleh Dewi Maulida yaitu proses antioksidan likopen dari buah tomat dengan menggunakan solven campuran n-heksana, aseton dan etanol [6] dan juga penelitian yang dilakukan oleh Gustina yaitu tentang kajian ekstrak biji mengkudu menggunakan pelarut organik, dan masih banyak lagi penelitian yang menggunakan etanol sebagai bahan pelarut untuk ekstraksi [12].
2.4.2 N-heksana
Heksana adalah senyawa hidrokarbon alkana dengan rumus kimia C6H14 (isomer utama n-heksana memiliki rumus CH3(CH2)4CH3. Awalan heks- merujuk pada enam karbon atom yang terdapat pada heksana dan akhiran -ana berasal dari alkana, yang merujuk pada ikatan tunggal yang menghubungkan atom-atom karbon tersebut. N Hexana merupakan jenispelarut non polar.
Karakteristik n – heksana :
13
benzena dapat digunakan untuk mengekstraksi minyak dari kopra (Kustanti, F., dan Ajianni, M. Y., 2000). Sedangkan solven campuran antara heksana dan isopropanol dapat digunakan dalam penurunan kadar limbah sintetis asam phosphat dengan ekstraksi cair – cair [5]. Dalam penggunaan heksana sebagai solven sudah banyak dilakukan banyak peneliti diantaranya yang dilakukan oleh Budi Nugroho yaitu heksana sebagai bahan pengekstraksi yaitu pengaruh suhu ekstraksi terhadap kandungan kurkuminoid dan air serbuk temulawak [15], juga dilakukan oleh aunin tentang kajian ekstrak minyak biji mengkudu dengan menggunakan pelarut organik [16], Ana Andari tentang Uji Aktivitas Ekstrak Daun Katuk Sebagai Antioksidan Pada Minyak Kelapa [7] dan Dewi Maulida tentang proses antioksidan likopen dari buah tomat dengan menggunakan solven campuran n-heksana, aseton dan etanol [5].
2.4.3 Etil Asetat
Etil Asetat dengan rumus C3OH merupakan turunan dari alkohol yang
dapat digunakan sebagai pelarut, dan sifatnya yang tidak beracun sehingga sering digunakan dalam kehidupan sehari-hari khususnya dunia farmasi.
Karakteristik metanol :
1. Berat molekul :102,18 g/mol 2. Titik didih : 64,5 0C 3. Melting poin : -86 0C
4. Specific gravity : 0,7257 (20 0C)
14
2.6 ANALISIS EKONOMI
Pada penelitian ini dilakukan suatu analisis ekonomi yang sederhana,
sehingga dapat diketahui biaya operasional pembuatan ekstrak flavonoid sebagai antioksidan pada minyak kelapa dengan bahan baku daun katuk. Proses pembuatannya menggunakan proses ekstraksi. Berikut rincian biaya yang digunakan dengan menggunakan proses tersebut :
1. Biaya Bahan Baku
Adapun bahan yang digunakan untuk pembuatan ekstrak flavonoid sebagai antioksidan pada minyak kelapa dengan bahan baku daun katuk antara lain, daun katuk, etanol 96% (C2H5OH), etil asetat (CH3COOC2H5), N-heksana (C6H14) dan
aluminium klorida (AlCl3). Pada tabel 2.3 akan ditampilkan rincian biaya bahan
baku.
Tabel 2.3 Rincian Biaya Bahan Baku
Bahan Jumlah Harga (Rp) Biaya Total (Rp)
Proses pembuatan ekstrak flavonoid sebagai antioksidan pada minyak kelapa dengan bahan baku daun katuk terdiri dari proses ekstraksi. Pada tabel 2.4 akan ditampilkan rincian biaya proses.
Tabel 2.4 Rincian Biaya Proses
Jumlah Waktu Harga (Rp) Biaya
15
Total biaya operasional merupakan biaya bahan baku ditambah dengan biaya proses pada pembuatan ekstrak flavonoid sebagai antioksidan pada minyak kelapa dengan bahan baku daun katuk.
Total biaya operasional = biaya bahan baku + biaya proses = Rp 1.081.000 + Rp 852.672
= Rp 1.933.672
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Berkembangnya pengetahuan manusia dalam pembuatan berbagai bahan makanan dan bahan obat – obatan dapat meningkatkan pemanfaatan bahan yang lebih mudah diperoleh dan diolah. Untuk mengurangi pemakaian bahan kimia sebagai dasar pembuatannya maka diperlukan bahan alami yang banyak mengandung nilai gizi dan vitamin, yaitu seperti sayur – sayuran dan buah – buahan. Untuk sayur – sayuran yang mengandung banyak nilai gizi, vitamin, dan kalsium adalah seperti daun katuk, daun nilam, tomat, daun sirsak dan sebagainya. Namun dalam hal ini yang diopergunakan adalah daun katuk, dimana daun katuk (Sauropus Androgiuns) merupakan salah satu jenis sayuran dengan nilai gizi tinggi" Kandungan gizi yang dimiliki daun katuk antara lain kalsium (233 g/100 gr), fosfor (98 mg/100 g) , zat besi (3,5 mg/100 g), vitamin A (203 mg/100 g), dan vitamin C (164 mg/100 g)" Keunggulan lain yang dimiliki oleh daun katuk adalah kandungan klorofilnya yang tinggi sehingga sering dimanfaatkan sebagai pewarna alami makanan [1].
Tumbuhan ini dapat dijumpai hampir di semua tempat di Indonesia. Di dalam daun katuk banyak terdapat minyak atsiri, sterol, saponin, flavonoid, triterpin, asam-asam organik, asam-asam amino, alkaloid dan tanin. Zuhra dkk, 2008, telah menguji aktivitas antioksidan senyawa flavonoid dari daun katuk dan menunjukkan hasil bahwa flavonoid dari daun katuk (Sauropus androgunus (L) Merr) memiliki kemampuan sebagai antioksidan yang kuat [2].
2
seperti jantung penyakit, stroke, dan beberapa jenis kanker (Cutler et al., 2008; Geleijnse, Launer, Hofman, Pols, & Witteman, 1999; Keli, Hertog, Feskens, & Kromhout, 1996). Fraksi flavonoid dari Chromolaena odorata yang antipiretik pada tikus (Owoyele et al., 2008). Demikian pula, flavonoid yang mengandung sayuran seperti S. androgynus (L) Merr dan P. indica (Kurang.) kurang memiliki kegunaan antipiretik di tradisional Indonesia obat. Oleh karena itu, analisis potensi asupan flavonoid dan aktivitas antioksidan dari sayuran ini waran penyelidikan lebih lanjut untuk mekanisme (s) dari tindakan dari Indonesia menggunakan obat tradisional sayuran ini [3].
Flavonoid yang terkandung dalam daun katuk dapat digunakan sebagai antioksidan yang bermanfaat sebagai radikal bebas. Dalam aplikasinya adalah antioksidan pada minyak kelapa, dimana Secara alamiah antioksidan dalam minyak nabati mudah terdegradasi pada saat pengolahan ataupun penyimpanan karena adanya kandungan oksigen berlebih, maka sengaja ditambahkan kedalam minyak kelapa antioksidan sintetik. Antioksidan sintetik merupakan antioksidan yang disintesis dari senyawa fenolik dengan tambahan zat kimia. Untuk menghindari efek antioksidan yang berbahaya maka cara yang paling aman adalah penggunaan antioksidan alami. Oleh karena itu, perlu dilakukan penelitian untuk menggali potensi senyawa bahan alam yang memiliki aktivitas antioksidan yang mudah diperoleh dalam jumlah besar, stabil pada suhu tinggi dan tanpa efek samping [3].
Pemanfaatan flavonoid dalam kehidupan sehari – hari dapat kita gunakan pada minyak, khususnya minyak kelapa. Setelah mengetahui bahwa minyak kelapa mudah mengalami oksidasi sehingga memerlukan antioksidan, penggunaan antioksidan sintetik yang berbahaya, dan kandungan flavonoid daun katuk dapat berfungsi sebagai antioksidan, maka perlu dilakukan penelitian yang memanfaatkan ekstrak daun katuk sebagai antioksidan pada minyak kelapa
3
Tabel 1.1 Penelitian pemanfaatan bahan alam sebagai antioksida
Peneliti Judul Penelitian Hasil Penelitian
Agun
Penelitian ini bertujuan untuk mengevaluasi efek antihipertensi in vitro
ekstrak daun mete
(PECL) menggunakan teknik organ terisola si, dan menentukan total fenolik dan flavonoid isi. Hasil penelitian menunjukkan bahwa Efek penghambatan PECL yang 25,72 ± 8,19% dan 39,60 ± 3,50% (p <0,05), Selain itu, PECL terkandung total fenolik dari 19,78 ± 0,62% dan total flavonoid dari 1,97 ± 0,04% yang setara dengan asam galat [4] Dewi
antioksidan dilakukan dengan menggunakan metode analisa spektrofotometri UV-VIS. Dari hasil penelitian ini menunjukkan bahwa kondisi optimum operasi ekstraksi lycopene adalah pada perbandingan F/s, 4 : 1 pada suhu operasi 70˚C dan 90 menit untuk variabel waktu ekstraksi. Pada kondisi ini lycopene yang terekstrak sebesar 5,14 mg/100gram atau sebesar 40,15% [5].
Daun katuk dibersihkan dan dikeringkan kemudian dihaluskan dengan blender lalu ditimbang. Diekstraksi dengan alkohol. Dari hasil penelitian ini bilangan
4
1.2 PERUMUSAN MASALAH
Adapu perumusan masalah dalam penelitian ini adalah sebagai berikut: 1. Bagaimana pengaruh waktu reaksi, volume pelarut, dan jenis pelarut dari
daun katuk yang digunakan sebagai atioksidan pada minyak kelapa. 2. Bagaimana pengaruh pemilihan waktu reaksi, volume pelarut, dan jenis
pelarut pada proses penentuan kadar flavonoid untuk diaplikasikan sebagai antooksidan pada minyak kelapa.
1.3 TUJUAN PENELITIAN
Adapun tujuan dari penelitian ini adalah sebagai berikut:
1. Untuk mengetahui Bagaimana pengaruh waktu reaksi, volume pelarut, dan jenis pelarut dari daun katuk yang digunakan sebagai atioksidan pada minyak kelapa.
2. Untuk mengetahui dan menghasilkan jenis pelarut, volume pelarut dan waktu ekstraksi terbaik terhadap rendemen ekstrak daun katuk dan kadar total flavonoid yang terkandung pada daun katuk.
1.4 MANFAAT PENELITIAN
Adapun manfaat dari penelitian ini adalah :
1. Sebagai informasi tentang pemanfaatan daun katuk sebagai antioksidan pada minyak kelapa.
2. Penelitian ini diharapkan dapat memberikan informasi kepada masyarakat bahwa antioksidan dari daun kauk dapat digunakan sebagai antioksidan pada minyak kelapa.
5
1.5 RUANG LINGKUP PENELITIAN
Penelitian ini dilakukan di Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan.
Bahan baku utama yang digunakan adalah daun katuk yang diperoleh dari pasar tradisional.
Penelitian ini di laksanakan dengan tiga tahapan yaitu proses pembuatan serbuk daun katuk, analisa kadar air serbuk daun katuk dan proses ekstraksi daun katuk.
1. Proses Pembuatan Serbuk Daun Katuk Massa total daun katuk segar : 18 kg Temperatur pengeringan : 40 oC Waktu pengeringan : 4 hari
Ukuran ayakan : 140 mesh
2. Proses Analis Kadar Air Serbuk Daun Katuk Basis kering serbuk daun katuk : ±10 % 3. Proses Ekstraksi Daun Katuk
Massa serbuk daun katuk : 50 gram (basis kering)
Jenis pelarut : etanol, n-heksana dan etil asetat Volume pelarut : 750, 1000, 1250 ml
Kecepatan pengadukan : 7 rpm Temperatur ekstraksi : 60 oC
Waktu ekstraksi : 2, 4 dan 6 jam Temperatur pemekatan filtrat : 70 oC
Analis yang dilakukan dalam penelitian ini adalah :
1. Analis kadar air serbuk daun katuk dengan menggunakan oven. 2. Penentuan rendemen ekstrak.
vi
ABSTRAK
Ekstraksi adalah pemisahan suatu zat dari campurannya, dengan pembagian sebuah zat terlarut antara dua pelarut yang tidak dapat tercampur untuk mengambil zat terlarut tersebut dari satu pelarut ke pelarut yang lain. Dalam penelitian ini, zat yang diekstrak dari daun katuk adalah antioksidan berupa zan flavonoid yang akan digunakan sebagai antioksidan pada minyak kelapa. Tujuan dari penelitian ini adalah mengetahui Bagaimana pengaruh waktu reaksi, volume pelarut, dan jenis pelarut dari daun katuk yang digunakan sebagai atioksidan pada minyak kelapa, dan juga mengetahui dan menghasilkan jenis pelarut, volume pelarut dan waktu ekstraksi terbaik terhadap rendemen ekstrak daun katuk dan kadar total flavonoid yang terkandung pada daun katuk. Dalam penelitian ini, daun katuk diekstrak dengan menggunakan pelarut etanol, n-heksan dan etil asetat hasil ekstrak akan dicari hasil rendemen dan kadar flavonoidnya. Hasil yang diperoleh pada penelitian ini adalah bahwa waktu ekstraksi terbaik 6 jam dengan volume pelarut 1250 ml dengan jenis pelarut terbaik adalah etanol.
.
vii
ABSTRACT
Extraction is the separation of a substance from a mixture thereof, with the distribution of a solute between two solvents which can not be mixed to take the solute from one solvent to another solvent. In this study, a substance extracted from the leaves katuk are antioxidants such as flavonoids substances to be used as antioxidants in coconut oil. The purpose of this study was know how to influence the reaction time, the volume of the solvent, and the type of solvent used as a leaf katuk atioksidan in coconut oil, and also determine and produce the type of solvent, solvent volume and the best extraction time on the yield katuk leaf extract and total flavonoid content in leaves katuk. In this study, leaves katuk extracted by using ethanol, n-hexane and ethyl acetate extract to search results yield and the level of flavonoids. The results obtained in this study is that the best extraction time of 6 hours with a volume of 1250 ml of solvent with the best kind of solvent is ethanol.
17
PENGARUH WAKTU EKSTRAKSI, VOLUME PELARUT,
DAN JENIS PELARUT TERHADAP RENDEMEN DAN
KADAR FLAVONOID TOTAL PADA EKSTRAKSI
DAUN KATUK (Sauropus androgynus (L) Merr)
SKRIPSI
Oleh
IKA HERAWATI HASIBUAN
090405006
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
18
PENGARUH WAKTU EKSTRAKSI, VOLUME PELARUT,
DAN JENIS PELARUT TERHADAP RENDEMEN DAN
KADAR FLAVONOID TOTAL PADA EKSTRAKSI
DAUN KATUK (Sauropus androgynus (L) Merr)
SKRIPSI
Oleh
IKA HERAWATI HASIBUAN
090405006
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
i
PERNYATAAN KEASLIAN SKRIPSI
Saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul :
PENGARUH WAKTU EKSTRAKSI , VOLUME PELARUT, DAN JENIS PELARUT, TERHADAP RENDEMEN DAN KADAR TOTAL FLAVONOID PADA EKSTRAKSI DAUN KATUK (SAUROPUS
ANDROGYNUS (L) MERR) SEBAGAI ANTIOKSIDAN PADA MINYAK
KELAPA
dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini adalah hasil karya saya kecuali kutipan-kutipan yang telah saya sebutkan sumbernya.
Demikian pernyataan ini diperbuat, apabila dikemudian hari terbukti bahwa ini bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima sanksi sesuai dengan aturan yang berlaku.
Medan, Juni 2015
iii
PRAKATA
Segala puji dan syukur kepada Tuhan Yang Maha Kuasa atas segala berkat dan karunia - Nya sehingga penulis dapat menyelesaikan laporan proposal yang berjudul “ Pengaruh Waktu Ekstraksi , Volume Pelarut, dan Jenis pelarut,
terhadap Rendemen dan Kadar Total Flavonoid pada Ekstraksi Daun Katuk (Sauropus androgynus (l) Merr) Sebagai Antioksidan pada Minyak Kelapa ”. Pada kesempatan ini penulis juga mengucapkan terima kasih kepada. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Selama melakukan penelitian hingga penulisan skripsi ini, penulis banyak mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ibu Prof. Dr. Ir. Rosdanelli. H, M.T selaku Dosen Pembimbing yang telah bersedia meluangkan waktu untuk memberi pengarahan, diskusi dan bimbingan serta persetujuan sehingga skripsi ini dapat selesai dengan baik. 2. Dr. Ir. Taslim, M. Si dan Dr. Eng. Rondang Tambun, ST, MT, selaku Dosen
Penguji yang telah memberikan saran dan masukan yang membangun dalam penulisan skripsi ini.
3. Bapak Dr.Eng.Ir. Irvan, MT., selaku ketua Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
4. Ibu Ir. Renita Manurung, MT., selaku koordinator penelitian.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, 2015
iv
DEDIKASI
v
RIWAYAT HIDUP PENULIS
Nama : Ika Herawati Hasibuan NIM : 090405006
Tempat/tgl lahir : Lobu Jelok, 18 Januari 1991 Nama orang tua : Umar Hasibuan
Alamat orang tua :
Desa Siuhom, Kec. Angkola Barat, Kab. Tapanuli Selatan, Sumatera Utara
Asal Sekolah :
SD Negeri 145582 Siuhom tahun 1997 – 2003 SMP Negeri 1 Angkola Barat tahun 2003-2006 SMA Negeri 1 Angkola Barat tahun 2006-2009 Beasiswa yang diperoleh :
Beasiswa BBM tahun 2009
Pengalaman Organisasi :
CSG periode 2011-2012 sebagai Sekretaris Bidang Dakwah
HIMATEK periode 2012 – 2013 sebagai Anggota Bidang Kreativitas dan Minat
vi
ABSTRAK
Ekstraksi adalah pemisahan suatu zat dari campurannya, dengan pembagian sebuah zat terlarut antara dua pelarut yang tidak dapat tercampur untuk mengambil zat terlarut tersebut dari satu pelarut ke pelarut yang lain. Dalam penelitian ini, zat yang diekstrak dari daun katuk adalah antioksidan berupa zan flavonoid yang akan digunakan sebagai antioksidan pada minyak kelapa. Tujuan dari penelitian ini adalah mengetahui Bagaimana pengaruh waktu reaksi, volume pelarut, dan jenis pelarut dari daun katuk yang digunakan sebagai atioksidan pada minyak kelapa, dan juga mengetahui dan menghasilkan jenis pelarut, volume pelarut dan waktu ekstraksi terbaik terhadap rendemen ekstrak daun katuk dan kadar total flavonoid yang terkandung pada daun katuk. Dalam penelitian ini, daun katuk diekstrak dengan menggunakan pelarut etanol, n-heksan dan etil asetat hasil ekstrak akan dicari hasil rendemen dan kadar flavonoidnya. Hasil yang diperoleh pada penelitian ini adalah bahwa waktu ekstraksi terbaik 6 jam dengan volume pelarut 1250 ml dengan jenis pelarut terbaik adalah etanol.
.
vii
ABSTRACT
Extraction is the separation of a substance from a mixture thereof, with the distribution of a solute between two solvents which can not be mixed to take the solute from one solvent to another solvent. In this study, a substance extracted from the leaves katuk are antioxidants such as flavonoids substances to be used as antioxidants in coconut oil. The purpose of this study was know how to influence the reaction time, the volume of the solvent, and the type of solvent used as a leaf katuk atioksidan in coconut oil, and also determine and produce the type of solvent, solvent volume and the best extraction time on the yield katuk leaf extract and total flavonoid content in leaves katuk. In this study, leaves katuk extracted by using ethanol, n-hexane and ethyl acetate extract to search results yield and the level of flavonoids. The results obtained in this study is that the best extraction time of 6 hours with a volume of 1250 ml of solvent with the best kind of solvent is ethanol.
viii
DAFTAR ISI
Halaman
PERNYATAAN KEASLIAN SKRIPSI i
PENGESAHAN UNTUK UJIAN SKRIPSI ii
PRAKATA iii
DEDIKASI iv
RIWAYAT HIDUP PENULIS v
ABSTRAK vi 1.3 TUJUAN PERCOBAAN 4 1.4 MANFAAT PERCOBAAN 4 1.5 RUANG LINGKUP PERCOBAAN 5
BAB II TINJAUAN PUSTAKA 6 2.1 TANAMAN KATUK (Sauropus androgynus (L) Merr) 6 2.2 FLAVONOID 7 2.3 EKSTRAKSI 8 2.3.1 Perlakuan Pendahuluan Terhadap Bahan 9 2.3.2 Pemilihan Jenis Pelarut 9 2.3.3 Perbandingan Jumlah Pelarut dan Bahan 10
2.3.4 Pengaturan Kondisi Ekstraksi 10
2.4 JENIS PELARUT 11
2.4.1 Etanol 11
ix
4.1 PENGARUH WAKTU EKSTRAKSI, VOLUME PELARUT, DAN JENIS PELARUT TERHADAP RENDEMEN EKSTRAK DAUN KATUK 27 4.1.1 Jenis Pelarut Etanol 29
4.1.2 Jenis Pelarut N-heksana 30
x
4.2 PENGARUH WAKTU EKSTRAKSI, VOLUME PELARUT, DAN JENIS PELARUT TERHADAP RENDEMEN EKSTRAK
DAUN KATUK 34
4.2.1 Jenis Pelarut etanol 34
4.2.2 Jenis Pelarut N-heksana 36
4.2.3 Jenis Pelarut Etil Asetat 38
BAB V KESIMPULAN DAN SARAN 41
5.1 KESIMPULAN 41
5.2 SARAN 42
DAFTAR PUSTAKA 43
LAMPIRAN 1 46
LAMPIRAN II 50
xi
DAFTAR GAMBAR
Halaman Gambar 2.1 Tanaman Katuk (Sauropus androgynus (L) Merr) 6
Gambar 3.1 Rangkaian Peralatan Penelitian 18
Gambar 3.2 Flowchart Pembuatan Serbuk Daun Katuk 22 Gambar 3.3 Flowchart Analisa Kadar Air Serbuk Daun Katuk 23 Gambar 3.4 Flowchart Proses Ekstraksi Daun Katuk 24 Gambar 3.5 Flowchart Penentuan Rendemen Ekstrak Daun Katuk 25 Gambar 3.6 Prosedur Penentuan Kadar Flavonoid Total Ekstrak Daun Katuk 26 Gambar 4.1 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap
Rendemen dengan Jenis Pelarut Etanol 27
Gambar 4.2 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap
Rendemen dengan Jenis Pelarut N-heksana 28
Gambar 4.3 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap Rendemen dengan Jenis Pelarut Etil Asetat 29 Gambar 4.4 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap
Kadar Flavonoid dengan Jenis Pelarut Etanol 30 Gambar 4.5 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap
Kadar Flavonoid dengan Jenis Pelarut N-heksana 31 Gambar 4.6 Grafik Pengaruh Waktu Ekstraksi dan Volume Pelarut terhadap
Kadar Flavonoid dengan Jenis Pelarut Etil Asetat 32
Gambar L3.1 Foto Oven pada Proses Pengeringan 56
Gambar L3.2 Foto Sampel Daun Katuk Kering 56
Gambar L3.3 Foto Sampel Daun Katuk Halus 57
Gambar L3. 4 Foto Proses ekstraksi Daun Katuk 57
Gambar L3.5 Foto Proses Filtrasi ekstrak Daun Katuk 58 Gambar L3.6 Foto Hasil filtrasi Ekstrak Daun Katuk 58
xii
DAFTAR TABEL
xiii
DAFTAR LAMPIRAN
Halaman
LAMPIRAN 1 DATA BAHAN BAKU 46
LAMPIRAN 2 CONTOH PERHITUNGAN 50
![Tabel L2.3 Data Absorbansi Larutan Quercetin [17]](https://thumb-ap.123doks.com/thumbv2/123dok/891200.596950/8.595.193.444.219.337/tabel-l-data-absorbansi-larutan-quercetin.webp)