GLUKOSA STEARAT SEBAGAI PENGEMULSI, DETERGEN,
DAN PEMBUSA
SEKAR INDRASWARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Glukosa Miristat, dan Ester Glukosa Stearat sebagai Pengemulsi, Detergen, dan Pembusa. Dibimbing oleh KOMAR SUTRIAH dan HENNY PURWANINGSIH.
Surfaktan nonionik mempunyai fungsi dan aplikasi yang sangat luas terutama untuk industri perawatan diri seperti sabun dan sampo serta industri detergen. Pencirian surfaktan nonionik perlu dilakukan untuk mengetahui kemampuannya yang utama. Pencirian yang dilakukan yaitu penentuan tegangan permukaan dan antarmuka, nilai HLB (hydrophile lypophile balance), stabilitas emulsi, daya detergensi, stabilitas busa, dan nilai pH. Surfaktan nonionik yang digunakan adalah ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat. Hasil pencirian menunjukkan nilai KMK (konsentrasi misel kritis) ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat berturut-turut adalah 0.0027, 0.0026, dan 0.0024% (b/v). Tegangan antarmuka pada KMK yang terbaik dicapai oleh ester glukosa miristat sebesar 15.33 dyne/cm. Nilai HLB ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat berturut-turut adalah 8.75, 8.30, dan 7.25. Berdasarkan nilai HLB dan pengujian yang telah dilakukan terbukti
bahwa ketiga ester glukosa lebih cenderung kepada emulsi oil in water (o/w). Stabilitas
emulsi o/w terbaik diperlihatkan oleh ester glukosa stearat. Daya detergensi terbaik diperlihatkan oleh ester glukosa miristat. Stabilitas busa terbaik diperlihatkan oleh ester glukosa laurat. Nilai pH tertinggi dicapai oleh ester glukosa miristat sebesar 6.82. Nilai pH terendah dicapai oleh ester glukosa stearat sebesar 6.40.
ABSTRACT
SEKAR INDRASWARI. Characterization of Glucose Laurate Ester, Glucose Myristate Ester, and Glucose Stearate Ester Nonionic Surfactant as Emulsifier, Detergent, and Foaming Agent. Supervised by KOMAR SUTRIAH and HENNY PURWANINGSIH.
GLUKOSA STEARAT SEBAGAI PENGEMULSI, DETERGEN,
DAN PEMBUSA
SEKAR INDRASWARI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM : G44201050
Menyetujui:
Pembimbing I, Pembimbing II,
Drs. Komar Sutriah, M.S. Henny Purwaningsih, S.Si., M.Si.
NIP 131950979
NIP 132311914
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuann Alam Institut Pertanian Bogor
Dr.Ir. Yonny Koesmaryono, M.S.
NIP 131473999
Alhamdulillahirabbil’aalamiin, penulis panjatkan kepada Allah SWT yang telah memberikan kesabaran dan kekuatan, hingga akhirnya penulis dapat menyelesaikan skripsi ini. Skripsi ini disusun berdasarkan hasil penelitian yang dilaksanakan mulai Desember 2005 hingga Maret 2006 di Laboratorium Kimia Fisik dan Lingkungan dan Laboratorium Kimia Organik FMIPA IPB. Penelitian ini merupakan penelitian lanjutan untuk mencirikan produk-produk ester glukosa yang telah disintesis lebih dulu oleh peneliti yang berbeda-beda. Adapun judul skripsi ini adalah Pencirian Surfaktan Nonionik Ester Glukosa Laurat, Ester Glukosa Miristat, dan Ester Glukosa Stearat sebagai Pengemulsi, Detergen, dan Pembusa.
Ucapan terima kasih penulis sampaikan kepada Drs. Komar Sutriah, M.S. dan Henny Purwaningsih, S.Si., M.Si atas segala bimbingan, dorongan semangat, dan ilmu yang diberikan kepada penulis selama penelitian dan penyusunan skripsi ini. Prof. Dr. Ir. Tun Tedja Irawadi, M.S. dan Proyek Hibah A2 yang telah mendanai penelitian ini. Terima kasih tak terhingga kepada keluarga besar Rahmat Sutomo dan Suradji, bapak, ibu, Mas Andis, adik-adik tersayang (Gandes, Gomo, dan Abadi) atas do’a serta kasih
sayangnya yang tulus ikhlas dan tiada henti kepada penulis. Terima kasih juga tak lupa
penulis ucapkan kepada Pak Sabur, Ibu Yenni, Pak Mail, Pak Nano, Om Eman, dan Ibu Enung atas segala fasilitas dan kemudahan yang telah diberikan. Penghargaan yang tak terhingga tak lupa penulis sampaikan kepada Drs. M. Farid, Kak Khotib, Mbak Helva, Kak Budi, tim surfaktan (Ega, Ika, Agung, Kak Ibe, dan terutama Rini) atas kerjasama dan persahabatan yang indah selama penelitian, warga Cidangiang 49 (Ani, Maya, dan
terutama Woro), warga Green House (Aning, Lia, dan Nita) serta kepada teman-teman
Kimia 38 atas persahabatan selama ini. Woro Januarti atas persahabatan yang telah terjalin selama 8 tahun, do’a, dorongan semangat serta kerelaannya mendengarkan keluhan dan tangisan penulis selama satu tahun terakhir. Sri, Dila, Anis, Tina, Santi, Epi, Aci, Nersy, Dina, Rian, dan Tati atas do’a dan ukhuwah yang teramat indah. Serta kepada semua pihak yang secara langsung maupun tidak langsung telah membantu penulis menyelesaikan karya ilmiah ini yang tidak dapat disebutkan satu per satu.
Semoga karya ilmiah ini bermanfaat.
Bogor, Mei 2006
Penulis dilahirkan di Semarang pada tanggal 10 Juli 1984 dari ayah Ismail Bambang Suharto dan ibu Werdi Yudiningsri. Penulis merupakan putri kedua dari lima bersaudara.
Tahun 2001 penulis lulus dari SMU Negeri 4 Semarang dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan penulis menjadi asisten praktikum mata kuliah
Kimia Bahan Alam untuk Program Studi D3 Analisis Kimia pada tahun ajaran 2005/2006, Kimia Fisik untuk Program Studi D3 Analisis Kimia pada tahun ajaran 2005/2006, Kimia Fisik 2 untuk Program Studi Kimia pada tahun ajaran 2005/2006, serta Kimia Lingkungan untuk Program Studi Kimia pada tahun ajaran 2005/2006. Penulis juga aktif dalam kepengurusan DKM Al-Ghifari periode 2002-2003 dan 2003-2004. Pada bulan Juli hingga Agustus 2004 penulis melaksanakan Praktik Lapangan di LIPI Biologi Bogor dan menulis Laporan Ilmiah dengan judul Degradasi Senyawa Nitril Alifatik oleh
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Surfaktan ... 1
Ester Asam Lemak-Karbohidrat ... 2
Tegangan Permukaan ... 2
Tegangan Antarmuka ... 2
HLB ... 3
Emulsi ... 3
Detergen ... 4
Busa ... 4
pH ... 4
BAHAN DAN METODE Bahan dan Alat ... 4
Metode... 4
HASIL DAN PEMBAHASAN Tegangan Permukaan dan Nilai KMK ... 6
Tegangan Antarmuka ... 6
Nilai HLB ... 7
Stabilitas Emulsi ... 7
Daya Detergensi ... 8
Stabilitas Busa ... 9
Nilai pH ... 9
SIMPULAN DAN SARAN Simpulan... 9
Saran ... 10
DAFTAR PUSTAKA ... 10
DAFTAR TABEL
Halaman
1 Nilai HLB dan aplikasinya berdasarkan konsep Griffin ... 3
2 pH ester glukosa... 9
DAFTAR GAMBAR
Halaman 1 Tegangan permukaan ester glukosa ... 62 Tegangan antarmuka ester glukosa... 7
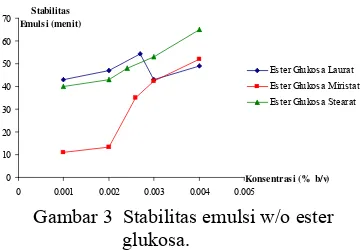
3 Stabilitas emulsi w/o ester glukosa ... 7
4 Stabilitas emulsi o/w ester glukosa ... 8
5 Daya detergensi ester glukosa laurat ... 8
6 Daya detergensi ester glukosa miristat ... 8
7 Daya detergensi ester glukosa stearat ... 9
8 Stabilitas busa ester glukosa ... 9
DAFTAR LAMPIRAN
Halaman 1 Pengukuran tegangan permukaan ester glukosa ... 132 Pengukuran tegangan antarmuka ester glukosa ... 15
3 Penentuan nilai HLB ester glukosa ... 16
4 Pengukuran stabilitas emulsi ester glukosa ... 17
5 Pengukuran daya detergensi ester glukosa ... 19
PENDAHULUAN
Surfaktan (surface active agent) adalah senyawa kimia yang jika terdapat pada konsentrasi rendah dalam suatu sistem maka akan mempunyai sifat teradsorpsi pada permukaan dan antarmuka pada sistem tersebut. Salah satu fungsi surfaktan di antaranya menurunkan tegangan permukaan. Aplikasi surfaktan sangat luas terutama untuk industri produk-produk perawatan diri seperti sabun dan sampo serta industri detergen. Surfaktan dapat dihasilkan dari minyak bumi (petrokimia) dan minyak-lemak (oleokimia). Penggunaan oleokimia sebagai bahan baku surfaktan belum seumum petrokimia, sehingga perlu pengembangan lebih lanjut, mengingat beberapa kelebihan oleokimia dibandingkan petrokimia, diantaranya mudah terurai secara biologis dan dapat diperbaharui.
Salah satu oleokimia yang berpotensi sebagai bahan baku surfaktan adalah minyak sawit. Terlebih lagi Indonesia dikenal sebagai negara produsen minyak sawit terbesar kedua di dunia setelah Malaysia. Pemanfaatan minyak sawit sebagai bahan baku surfaktan juga dapat memberikan nilai tambah terhadap minyak sawit tersebut. Minyak sawit dipilih sebagai bahan baku surfaktan karena komponen asam lemak penyusun trigliseridanya, yaitu asam lemak C16-C18 mampu berperan terhadap sifat detergensinya, sedangkan asam lemak C12-C14 berperan terhadap efek pembusaan.
Ester asam lemak-karbohidrat merupakan suatu surfaktan nonionik berbasis minyak nabati dan karbohidrat yang memperlihatkan ciri-ciri yang baik diantaranya mudah terdegradasi, tidak menimbulkan iritasi, dan digunakan sebagai formula dalam industri detergen, farmasi, makanan, dan kosmetik (Obaje 2005). Pemanfaatan surfaktan jenis ini memiliki keunggulan yang mampu bersaing dengan surfaktan jenis lain seperti LAS (Linear Alkil Sulfonat) dan ABS (Alkil Benzena Sulfonat) yang lebih umum digunakan saat ini.
Pencirian ester asam lemak-karbohidrat perlu dilakukan sebelum diaplikasikan lebih lanjut, untuk mengetahui kemampuannya yang utama sebagai surfaktan nonionik. Pencirian itu antara lain, penentuan tegangan permukaan dan antarmuka, nilai HLB, stabilitas emulsi, daya detergensi, daya busa, dan nilai pH. Penelitian ini bertujuan mencirikan ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat serta mengetahui pengaruh panjang rantai karbon
asam lemak terhadap sifat-sifatnya sebagai surfaktan nonionik.
TINJAUAN PUSTAKA
Surfaktan
Surfaktan merupakan molekul amfifilik yang terdiri atas gugus hidrofilik yang mempunyai afinitas tinggi terhadap air dan gugus lipofilik yang mempunyai afinitas tinggi terhadap minyak (Dickinson & Mc Clements 1996). Kehadiran kedua gugus yang berbeda ini menyebabkan surfaktan cenderung berada pada antarmuka antara fasa yang berbeda derajat polaritas dan ikatan hidrogen seperti minyak dan air. Pembentukan lapisan tipis pada antarmuka ini akan menurunkan energi antarmuka dan menyebabkan sifat-sifat khas molekul surfaktan (Georgiou et al. 1992). Surfaktan dapat berfungsi sebagai detergen, wetting agent (zat pembasah), pengemulsi, bahan pendispersi, foaming agent
(zat pembusa), dan sebagainya (Swern 1997). Sifat-sifat surfaktan adalah dapat menurunkan tegangan permukaan dan tegangan antarmuka, meningkatkan kestabilan partikel terdispersi, dan mengontrol formulasi emulsi, misalnya
oil in water (o/w) atau water in oil (w/o). Di samping itu, surfaktan akan terserap ke dalam permukaan partikel minyak atau air sebagai penghalang yang akan mengurangi atau menghambat penggabungan (koalesensi) dari partikel yang terdispersi (Rieger 1985). Surfaktan dapat dikelompokkan berdasarkan sumber bahan baku pembuatnya, struktur ion, nilai HLB, serta unsur dan gugus fungsi.
Swern (1997) membagi surfaktan menjadi empat kelompok:
1. Surfaktan kationik, merupakan surfaktan yang bagian pangkalnya berupa gugus hidrofilik dengan ion bermuatan positif (kation). Umumnya merupakan garam-garam amonium kuaterner atau amina.
2. Surfaktan anionik, merupakan surfaktan yang gugus hidrofobiknya dihubungkan dengan ion bermuatan negatif (anion). Umumnya berupa garam natrium, akan terionisasi menghasilkan Na+ dan ion surfaktan yang bermuatan negatif.
tidak membawa muatan elektron, tetapi mengandung heteroatom yang menyebabkan terjadinya momen dipol.
4. Surfaktan amfoterik, mengandung gugus yang bersifat anionik dan kationik seperti pada asam amino. Sifat surfaktan ini tergantung pada kondisi media dan nilai pH.
Surfaktan berbasis bahan alami dapat dibagi menjadi empat kelompok: (1) berbasis minyak-lemak seperti monogliserida, digliserida, dan poligliserol ester, (2) berbasis karbohidrat seperti alkil poliglukosida, dan n-metil glukamida, (3) ekstrak bahan alami seperti lesitin dan saponin, (4) biosurfaktan yang diproduksi oleh mikroorganisme seperti ramnolipid dan soforolipid.
Ester Asam Lemak-Karbohidrat
Ester asam lemak-karbohidrat merupakan surfaktan nonionik yang memiliki kemampuan yang baik dalam mengaktifkan permukaan dan mudah didegradasi. Jenis surfaktan ini dapat digunakan sebagai zat tambahan untuk produk makanan, kosmetik, farmasi, dan bahan pembersih. Sintesis konvensional senyawa ini telah dilaporkan oleh beberapa peneliti dengan metode yang berbeda-beda terutama pada beberapa dekade belakangan ini sejak ester tersebut dapat dipreparasi dari senyawa alami yang dapat diperbaharui dan tidak habis terpakai seperti karbohidrat dan asam lemak (Kasori et al. 1999).
Ester asam lemak-karbohidrat yang digunakan dalam penelitian ini adalah ester glukosa laurat yang disintesis dari GPA (glukosa pentaasetat) dan metil laurat (C12), ester glukosa miristat dari metil miristat (C14), dan ester glukosa stearat dari metil stearat (C18). Ketiga ester asam lemak-karbohidrat ini disintesis dengan metode bebas pelarut.
Tegangan Permukaan
Tegangan permukaan merupakan sifat cairan yang membuatnya berperilaku seolah-olah permukaannya terkurung dalam lapisan yang elastis. Sifat ini timbul karena adanya ketidakseimbangan gaya antara molekul di permukaan cairan dan molekul di badan cairan. Molekul di badan cairan mengalami interaksi yang sama dari molekul-molekul lain di semua sisi, sedangkan molekul di permukaan hanya dipengaruhi oleh molekul-molekul di bawahnya dan di sampingnya.
Sifat tegangan permukaan berpengaruh terhadap pembentukan tetesan cairan, busa sabun, dan meniskus, begitu juga dengan kenaikan cairan dalam pipa kapiler, dan kemampuan cairan untuk membasahi permukaan (Butt et al. 2003 diacu dalam Jaya 2005).
Terdapat beberapa metode pengukuran tegangan permukaan di antaranya dengan metode kenaikan kapiler, metode sudut kontak, metode tekanan gelembung, metode berat tetes, dan metode tensiometer du Noüy. Metode cincin du Noüy berdasarkan pada penentuan gaya yang diperlukan untuk menarik cincin Pt-Ir dari permukaan cairan (Holmberg et al. 2003). Cincin yang tergantung pada neraca torsi ditarik dari cairan dengan memutar kawat torsi. Gaya yang diperlukan untuk memutuskan lapisan tipis cairan didefinisikan sebagai
F = 4πRγ
dengan R adalah jari-jari cincin dan γ adalah tegangan permukaan. Alat tensiometer du Noüy mempunyai faktor koreksi sebesar
R
dengan r adalah jari-jari kawat, R jari-jari cincin, P nilai tegangan permukaan terukur, C keliling cincin, d rapat massa untuk fluida di atas, dan D adalah rapat massa untuk fluida di bawah. Untuk mendapatkan nilai tegangan permukaan yang sebenarnya, maka tegangan permukaan yang terukur harus dikalikan dengan faktor koreksi di atas.
Tegangan Antarmuka
pengukuran tegangan antarmuka dapat dilakukan menggunakan metode cincin du Noüy.
HLB (Hydrophile Lypophile Balance)
Nilai HLB merupakan sejumlah urutan angka yang mewakili kecenderungan hidrofilik dan lipofilik dari suatu surfaktan. Nilai ini bergantung pada perbandingan bagian hidrofilik dan lipofilik. HLB adalah konsep untuk memilih pengemulsi. Sistem HLB pertama kali diperkenalkan oleh William C. Griffin (Holmberg et al. 2003).
Umumnya HLB digunakan hanya untuk surfaktan nonionik. Nilai HLB berkisar antara 1 dan 20. Pengemulsi dengan HLB rendah larut dalam minyak dan meningkatkan emulsi air dalam minyak (w/o). Pengemulsi dengan HLB tinggi larut dalam air dan akan meningkatkan emusi minyak dalam air (o/w). Nilai HLB berdasarkan konsep Griffin dan aplikasinya dapat dilihat dalam Tabel 1.
Tabel 1 Nilai HLB dan aplikasinya berdasarkan konsep Griffin Nilai HLB Aplikasi
3 – 6 Pengemulsi w/o
Penentuan nilai HLB sebagai berikut:
a. Pengemulsi yang bagian hidrofiliknya hanya mengandung gugus polioksietilena
5 E HLB=
dengan E adalah kadar gugus polioksietilena (%).
b. Pengemulsi senyawa turunan tall oil, rosin, beeswax, dan lain-lain
5 P E HLB= +
dengan E adalah kadar gugus polioksietilena (%) dan P adalah kadar alkohol polihidroksi (%). c. Pengemulsi ester asam lemak dari
alkohol polihidroksi
⎟
dengan S adalah bilangan penyabunan ester dan A adalah bilangan netralisasi asam lemak. d. Campuran pengemulsi A dan B
B bobot pengemulsi A dan B.
B
Emulsi
Emulsi adalah dispersi dari satu cairan dalam cairan lain yang tidak saling bercampur. Dua jenis emulsi yang paling umum adalah emulsi minyak dalam air (o/w) dan emulsi air dalam minyak (w/o). Faktor-faktor yang memengaruhi emulsifikasi di antaranya adalah jenis pengemulsi, suhu, perbandingan volume dari kedua fase cairan, dan sifat-sifat dinding wadah.
Stabilitas emulsi merupakan suatu sistem ketika tetesan mempertahankan sifat awalnya karena penggabungan tetesan-tetesan dicegah oleh energi penghalang yang cukup besar. Pada umumnya energi penghalang dibangun oleh lapisan pengemulsi yang terbentuk pada permukaan tetesan-tetesan (Heusch et al. 1987). Faktor yang dapat memengaruhi stabilitas emulsi antara lain tolakan elektrik dan rintangan sterik, sedangkan faktor yang dapat memengaruhi destabilisas emulsi diantaranya pembentukan krim, flokulasi, sedimentasi, dan koalesensi (Holmberg et al. 2003).
Bahan yang umum digunakan sebagai penstabil emulsi adalah surfaktan karena surfaktan hampir terserap irreversibel pada antarmuka. Tolakan sterik di antara bagian-bagian surfaktan dalam medium pendispersi berpengaruh penting dalam stabilisasi ini. Rantai hidrokarbon dihalangi dalam pergerakan termalnya jika dua tetesan air saling mendekati terlalu rapat dan gugus kepala hidrofiliknya didehidrasi sehingga terjadi kontak yang rapat. Akibatnya tolakan hidrasi menstabilkan emulsi (Holmberg et al. 2003).
mengukur ukuran partikel. Derajat stabilitas emulsi biasanya ditunjukkan oleh perubahan nilai yang diukur dengan metode ini pada beberapa interval waktu (Holmberg et al. 2003).
Detergen
Detergen merupakan zat yang ditambah-kan ke dalam air untuk meningkatditambah-kan daya pembersihnya. Detergen juga dapat diartikan sebagai senyawa yang menyebabkan zat nonpolar dapat larut dalam air (Daintith 1994). Daya detergensi adalah kemampuan surfaktan untuk mengikat minyak dan mengangkat kotoran pada permukaan kain (Holmberg et al. 2003).
Faktor-faktor yang memengaruhi daya detergensi adalah komposisi pengotor secara kimia dan fisik, temperatur pada saat proses pencucian, durasi setiap tahap pencucian, jenis dan proses mekanisasi yang digunakan, jumlah pengotor yang terdapat dalam sistem, serta jenis dan jumlah detergen yang digunakan. Daya detergensi juga dipengaruhi oleh tingkat kesadahan air. Semakin tinggi kesadahan air, maka daya detergensi akan semakin menurun (Lynn 1993).
Busa
Busa merupakan dispersi gelembung dalam cairan (Daintith 1994). Salah satu fenomena khas dari larutan surfaktan adalah kemampuannya dalam membentuk busa. Busa akan terbentuk jika larutan surfaktan diaduk atau dialiri udara. Busa adalah gas yang terjebak oleh lapisan tipis cairan yang mengandung sejumlah molekul surfaktan yang teradsorpsi pada lapisan tipis tersebut. Dalam gelembung, gugus hidrofobik surfaktan akan mengarah ke gas, sedangkan bagian hidrofiliknya akan mengarah ke larutan (Holmberg et al. 2003).
Kemampuan pembentukan busa dari surfaktan akan berubah dengan bertambahnya jumlah air dan perubahan suhu. Stabilitas suatu busa ditentukan oleh tingkat elastisitas lapisan tipisnya. Pada umumnya surfaktan yang memiliki daya busa yang tinggi akan memiliki daya bersih yang juga tinggi. Akan tetapi surfaktan nonionik walaupun daya busanya relatif rendah, ternyata mempunyai daya bersih yang tinggi dibandingkan dengan surfaktan anionik yang berdaya busa tinggi (Holmberg et al. 2003).
pH
pH berarti ’potensial hidrogen’. Skala ini diperkenalkan oleh S.P. Sorensen pada tahun 1909. pH merupakan skala logaritmik untuk menyatakan keasaman atau kebasaan suatu larutan. pH larutan dapat didefinisikan sebagai –log10C, dengan C adalah konsentrasi ion hidrogen dalam mol dm-3. Larutan netral pada suhu 25 °C mempunyai konsentrasi ion hidrogen 10-7 mol dm-3, sehingga pH-nya adalah 7. pH di bawah 7 menyatakan larutan asam, sedangkan pH di atas 7 menyatakan larutan basa (Daintith 1994).
Nilai pH suatu surfaktan perlu diketahui untuk aplikasi lebih lanjut. Umumnya surfaktan yang bersifat netral lebih disukai daripada surfaktan yang bersifat asam atau basa.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah ester glukosa laurat, ester glukosa miristat, ester glukosa stearat yang diperoleh dari hasil sintesis Russiana, Prihanjani, dan Sari 2006, xilena, piridina, benzena, iod, KI, dan akuades.
Alat-alat yang digunakan adalah aerator, Cole-Parmer surface tensiometer 20, pH meter HM-20J DKK-TOA Corporation, turbidimeter produksi Hach Company 2100P, ultrasonic
homogenizer T8. 10 IKA®-WERRE, dan
peralatan gelas.
Metode
Penelitian ini dilakukan di Laboratorium Kimia Fisik dan Lingkungan dan Laboratorium Kimia Organik, Departemen Kimia FMIPA IPB.
Pengukuran Tegangan Permukaan Metode du Noüy (ASTM D_1331 2000). Peralatan dan wadah sampel yang digunakan harus dibersihkan terlebih dahulu dengan larutan asam sulfat-kromat dan dibilas dengan akuades, lalu dikeringkan. Wadah yang digunakan biasanya terbuat dari bahan gelas dengan diameter lebih dari 6 cm. Cincin platinum yang digunakan pada alat Tensiometer du Noüy mempunyai keliling 5.9450 cm.
Posisi alat diatur agar horizontal dengan
sinar matahari, dan panas. Larutan surfaktan dengan variasi konsentrasi yaitu 0.0010, 0.0020, 0.0030, 0.0040, 0.0050, 0.0060, 0.0070, 0.0080, 0.0090, 0.0100% (b/v), dimasukkan ke dalam gelas piala dan diletakkan di atas dudukan pada tensiometer. Suhu cairan diukur dan dicatat. Selanjutnya cincin platinum dicelupkan ke dalam sampel (lingkaran logam tercelup kurang lebih 3 mm), dengan cara memutar kawat torsi. Skala Vernier Tensiometer diatur pada posisi nol dan jarum penunjuk harus berada pada posisi berhimpit dengan garis pada kaca. Selanjutnya kawat torsi diputar perlahan-lahan. Proses ini diteruskan sampai lapisan tipis cairan tepat putus. Saat cairan tepat putus, skala dibaca dan dicatat sebagai nilai tegangan permukaan. Pengukuran dilakukan hingga diperoleh paling sedikit lima kali pembacaan tidak jauh berbeda.
Pengukuran Tegangan Antarmuka (ASTM_D, 1331 2000)]. Metode penentuan tegangan antarmuka hampir mirip dengan pengukuran tegangan permukaaan. Untuk pengukuran cairan yang mengandung dua fasa yang berbeda, yaitu fasa polar berisi surfaktan dengan variasi konsentrasi antara 0.0010% (b/v) dan 0.0040% (b/v), dan fasa nonpolar berupa xilena dengan perbandingan volume 1:1. Larutan surfaktan terlebih dahulu dimasukkan ke dalam wadah sampel, kemudian cincin platinum dicelupkan ke dalamnya (lingkaran logam tercelup kurang lebih 3 mm), setelah itu secara hati-hati xilena ditambahkan ke dalam larutan surfaktan sehingga sistem terdiri atas dua lapisan. Kontak antara cincin dan xilena sebelum pengukuran harus dihindari. Setelah tegangan antarmuka mencapai ekuilibrium, yaitu benar-benar terbentuk dua lapisan terpisah yang sangat jelas, pengukuran dapat dilakukan dengan cara yang sama dengan pengukuran tegangan permukaan.
.
Penentuan Nilai HLB (Hidrophile-Lipophile Balance) (Gupta et al. 1983 di dalam Kuang et al. 2000). HLB ditentukan dengan
metode water number method. Larutan
surfaktan yang mengandung 1 g surfaktan dalam 25 mL campuran piridina dan benzena (95:5 (v/v)), dititrasi dengan akuades sampai kekeruhan permanen. Nilai HLB dari sampel surfaktan diperoleh dengan interpolasi pada kurva kalibrasi.
Pengukuran Kestabilan Emulsi (Modifikasi ASTM 2000). Kestabilan emulsi diukur untuk
emulsi o/w (minyak dalam air) dan w/o (air dalam minyak) antara air dan xilena. Larutan surfaktan yang akan diukur mempunyai konsentrasi 0.0010−0.0040% (b/v). Kestabilan emulsi o/w diukur dengan cara sebanyak 9.5 mL larutan surfaktan dimasukkan ke dalam tabung reaksi khusus, kemudian dicampur dengan 0.5 mL xilena. Campuran dikocok selama 5 menit menggunakan ultrasonic homogenizer. Pengukuran kestabilan emulsi dilakukan setelah 24 jam. Tinggi emulsi yang tersisa dan tinggi emulsi total larutan diukur. Kestabilan emulsi w/o diukur dengan cara sebanyak 9.5 mL xilena dimasukkan ke dalam tabung reaksi khusus, kemudian ditambah dengan 0.5 mL larutan surfaktan. Campuran dikocok selama 5 menit menggunakan
ultrasonic homogenizer. Lamanya pemisahan fase antara xilena dan larutan surfaktan diukur.
Daya Detergensi (Lynn 1996 di dalam Martini 2003). Larutan surfaktan dengan variasi konsentrasi antara 0.0010% (b/v) dan 0.0040% (b/v) diukur kekeruhannya dan dicatat sebagai nilai T1. Kain putih dengan jenis dan ukuran berbentuk bujur sangkar dengan luas 25 cm2 direndam dalam 100 mL akuades selama 30 menit. Setelah itu, kain diangkat dan ditiriskan selama 30 menit, kemudian akuades hasil rendaman diukur kekeruhannya dan dicatat sebagai nilai T2. Kain putih dengan jenis dan ukuran yang sama direndam dalam larutan pengotor bumbu rendang dengan konsetrasi 5% (b/v) selama 30 menit. Setelah itu, kain ditiriskan selama 30 menit, kemudian kain direndam dalam larutan surfaktan sebanyak 100 mL selama 30 menit. Kekeruhan larutan surfaktan diukur setelah perendaman dan dicatat sebagai nilai T3.
Pembusaan (Modifikasi Hui 1996 di dalam Martini 2003). Larutan surfaktan dengan variasi konsentrasi antara 0.0010% (b/v) dan 0.0040% (b/v) dimasukkan ke dalam tabung reaksi, kemudian dialiri udara selama 1 menit dengan aerator. Selanjutnya diamati pembentukan busa yang terjadi. Waktu terbentuknya busa dicatat sebagai lama pembusaan.
HASIL DAN PEMBAHASAN
Tegangan Permukaan dan Nilai KMK
Pengukuran tegangan permukaan larutan ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat pada berbagai konsentrasi dilakukan menggunakan metode du Noüy. Pada metode ini tegangan permukaan sebanding dengan gaya yang diperlukan untuk menarik cincin hingga lapisan tipis pada cincin tepat putus. Pengukuran tegangan permukaan sangat penting dilakukan untuk menentukan besarnya nilai KMK (Konsentrasi Misel Kritis) dari masing-masing larutan. Nilai KMK inilah nantinya yang akan digunakan untuk pencirian sifat-sifat fisik lebih lanjut karena pada saat KMK tercapai banyak terjadi perubahan sifat-sifat fisik dari suatu larutan (Holmberg et al. 2003).
Misel adalah gerombol kecil molekul yang gugus nonpolarnya (hidrokarbon) berada di bagian tengah dan gugus hidrofiliknya berada di bagian luar tersolvasi oleh molekul air (Daintith 1994). KMK adalah konsentrasi pada saat misel mulai terbentuk (Holmberg et al. 2003). Nilai KMK yang diperoleh untuk ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat berturut-turut adalah 0.0027% (b/v), 0.0026% (b/v), dan 0.0024% (b/v). Perbedaan ini dapat terjadi karena panjang rantai hidrokarbon pada setiap jenis ester berbeda-beda. Semakin panjang rantai hidrokarbon maka semakin kecil nilai KMK karena jumlah molekul yang diperlukan untuk mencapai kejenuhan pada permukaan dengan luas permukaan yang sama semakin sedikit (Ferrer et al. 2002). Nilai KMK diperolah dari perpotongan dua garis pada kurva hubungan antara konsentrasi dan tegangan permukaan masing-masing ester glukosa (Lampiran 1).
Gambar 1 menunjukkan bahwa dengan semakin tinggi konsentrasi maka tegangan permukaan akan semakin rendah. Pada tiga konsentrasi pertama (0.0010, 0.0020, dan 0.0030% b/v) setiap jenis ester, tegangan permukaan turun cukup drastis. Namun setelah KMK tercapai, penurunan tegangan permukaan hanya sedikit. Hal ini dikarenakan pada konsentrasi di atas KMK, hampir seluruh molekul telah membentuk misel dan hanya sedikit yang dapat teradsorpsi di permukaan. Akibatnya, surfaktan tidak lagi efektif dalam menurunkan tegangan permukaan (Holmberg
et al. 2003). Nilai tegangan permukaan
masing-masing larutan dapat dilihat dalam Lampiran 1 .
0 0.002 0.004 0.006 0.008 0.01 0.012
Konsentrasi (% b/v) Tegangan
Permukaan (dyne/cm)
Ester Glukosa Laurat Ester Glukosa Miristat Ester Glukosa Stearat
Gambar 1 Tegangan permukaan ester glukosa.
Tegangan Antarmuka
Pengukuran tegangan antarmuka dilakukan pada lima konsentrasi, yaitu dua konsentrasi di bawah KMK, konsentrasi pada saat KMK, dan dua konsentrasi di atas KMK. Pengukuran ini menggunakan dua larutan yang tidak saling bercampur satu sama lain. Larutan ester glukosa sebagai fase polar, sedangkan sebagai fase nonpolarnya digunakan xilena. Pengukuran ini masih menggunakan metode du Noüy. Cincin du Noüy diatur sehingga berada pada batas kedua larutan yang tidak saling bercampur tersebut. Besarnya tegangan antarmuka sebanding dengan gaya yang diperlukan untuk menarik cincin hingga lapisan tipis pada cincin yang terbentuk pada batas dua larutan tepat putus. Seperti halnya tegangan permukaan, tegangan antar muka larutan ester glukosa juga bergantung kepada besarnya konsentrasi dan panjang rantai hidrokarbon. Berdasarkan Ferrer et al. (2002) seharusnya dengan semakin bertambahnya panjang rantai hidrokarbon maka semakin kecil tegangan antarmuka ester glukosa pada KMK. Namun dari hasil penelitian ini terjadi penyimpangan pada ester glukosa stearat yang justru memberikan hasil lebih tinggi dibandingkan kedua jenis ester glukosa lainnya (Lampiran 2).
0
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Tegangan
Antarmuka (dyne/cm)
Ester Glukosa Laurat Ester Glukosa Miristat Ester Glukosa Stearat
Gambar 2 Tegangan antarmuka ester glukosa.
Nilai HLB
Penentuan nilai HLB dari ketiga ester glukosa diperlukan untuk mengetahui kesesuaiannya sebagai pengemulsi. Metode yang digunakan adalah titrimetri, dengan akuades sebagai titran dan larutan surfaktan yang mengandung 1 g surfaktan dalam 25 ml campuran piridina dan benzena (95:5 v/v) sebagai titrat. Kepala polar dari ester glukosa yang bersifat hidrofilik akan tarik menarik dengan molekul air yang juga bersifat polar dan ion nitrogen dari molekul piridina yang bersifat semi polar. Ekor hidrokarbon ester glukosa yang bersifat hidrofobik akan tarik menarik dengan molekul benzena yang nonpolar dan cincin heterosiklik aromatik molekul piridina. Titik akhir titrasi dicapai pada saat kekeruhan permanen, karena pada saat kekeruhan permanen larutan telah jenuh dan molekul ester glukosa sudah tidak dapat berikatan dengan molekul air maupun piridina dan benzena.
Nilai HLB dari ketiga ester glukosa diperoleh melalui perhitungan pada persamaan linear y = 0.2551x – 3.5487. Persamaan linear tersebut diperoleh dari kurva standar yang didapat dari pengukuran Tween-20 (polioksietilena sorbitan monolaurat), Tween-80 (polioksietilena sorbitan mono-oleat), dan GMS (gliserol monostearat) murni dengan menganggap nilai HLBnya sesuai dengan literatur (Jaya 2005).
Hasil pengukuran nilai HLB ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat berturut-turut adalah 8.75, 8.30, dan 7.25 (Lampiran 3). Panjang rantai hidrokarbon memengaruhi nilai HLB ester glukosa, semakin panjang rantai hidrokarbon suatu ester glukosa maka semakin rendah nilai HLBnya. Hal ini disebabkan karena HLB merupakan nilai yang bergantung pada perbandingan antara rantai hidrofilik dan lipofilik suatu molekul surfaktan. Semakin
panjang rantai hidrofilik maka semakin tinggi nilai HLB. Sebaliknya semakin panjang rantai lipofilik (hidrokarbon) maka semakin rendah nilai HLB.
Berdasarkan konsep Griffin maka ester glukosa laurat dan ester glukosa miristat dapat diaplikasikan sebagai pengemulsi o/w, sedangkan ester glukosa stearat sebagai
wetting agent. Oleh karena itu, diperlukan pencirian lebih lanjut untuk mengetahui aplikasi yang lebih tepat dari ketiga ester glukosa.
Stabilitas Emulsi
Pengukuran stabilitas emulsi dilakukan dengan mencampurkan dua zat yang berbeda polaritasnya. Pada penelitian ini digunakan xilena sebagai fase nonpolar, sedangkan larutan ester glukosa sebagai fase polar. Dilakukan dua perbandingan volume antara larutan ester glukosa dengan xilena, yaitu 0.5:9.5 (mL) dan 9.5:0.5 (mL), untuk melihat dan membuktikan jenis emulsi yang telah diramalkan sebelumnya melalui nilai HLB. Perbandingan 0.5:9.5 adalah pengemulsi w/o, sedangkan 9.5:0.5 adalah pengemulsi o/w. Kedua larutan yang tidak saling bercampur ini dihomogenkan dengan ultrasonic homo-genizer pada kecepatan sedang selama 5 menit.
Berdasarkan Gambar 3 dan 4 dapat dilihat bahwa emulsi o/w lebih stabil dibandingkan emulsi w/o. Emulsi o/w dapat bertahan selama lebih dari 24 jam, sedangkan emulsi w/o hanya dapat bertahan selama beberapa menit saja. Hal ini membuktikan bahwa ester glukosa laurat dan ester glukosa miristat merupakan pengemulsi o/w dan sejalan dengan nilai HLB kedua ester glukosa tersebut.
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Stabilitas
Emulsi (menit)
Ester Glukosa Laurat Ester Glukosa Miristat Ester Glukosa Stearat
0
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Stabilitas
Emulsi (% )
Ester Glukosa Laurat Ester Glukosa Miristat Ester Glukosa Stearat
Gambar 4 Stabilitas emulsi o/w ester
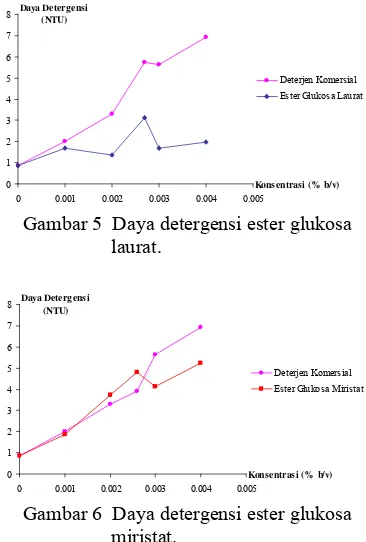
Gambar 5, 6, dan 7 memperlihatkan daya detergensi ester glukosa miristat adalah yang tertinggi dibandingkan dua jenis ester glukosa lainnya. Bahkan pada KMK daya detergensi ester glukosa miristat lebih tinggi dari detergen komersial. Daya detergensi terendah diperlihatkan oleh ester glukosa laurat (Lampiran 5). Hal ini disebabkan karena panjang rantai hidrokarbon memengaruhi daya detergensi. Lynn (1993) melaporkan bahwa surfaktan dengan rantai hidrofobik antara 12 dan 16 atom karbon memperlihatkan daya detergensi optimum, sedangkan surfaktan dengan rantai karbon lebih dari 16 daya detergensinya akan menurun. Hal ini juga sejalan dengan nilai HLB yang telah ditentukan sebelumnya. Berdasarkan konsep Griffin daya detergensi optimal dicapai pada nilai HLB 12 (Lynn 1993).
glukosa.
Stabilitas emulsi sebanding dengan konsentrasi, semakin tinggi konsentrasi, maka stabilitas emulsi juga akan semakin tinggi (Friberg 1993). Akan tetapi stabilitas emulsi w/o ester glukosa laurat dan stabilitas emulsi o/w ketiga ester glukosa memperlihatkan ketidaksesuaian dengan teori di atas. Hal ini dapat disebabkan pengaruh kemurnian yang rendah. Mengingat kisaran titik leleh yang cukup besar yaitu 100 °C-110 °C, 115 °C-122 °C, dan 96 °C-112 °C berturut-turut untuk ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat (Russiana 2006; Prihanjani 2006; Sari 2006).
Stabilitas emulsi juga bergantung pada panjang rantai hidrokarbon dari asam lemak yang digunakan. Pada umumnya stabilitas emulsi meningkat dengan bertambahnya panjang rantai hidrokarbon. Hal ini berkaitan dengan halangan sterik yang timbul akibat panjangnya rantai hidrokarbon (Holmberg et al. 2003). Namun hasil penelitian ini tidak sejalan dengan teori di atas. Hal ini dapat terjadi karena pengaruh ketidakmurnian seperti yang telah dijelaskan sebelumnya.
Stabilitas emulsi tertinggi sebesar 13.64% dicapai oleh ester glukosa stearat pada konsentrasi 0.0040% (b/v) (Lampiran 4). Nilai ini menunjukkan bahwa ester glukosa stearat cukup baik apabila akan diaplikasikan sebagai pengemulsi o/w. Pengukuran stabilitas emulsi perlu dilakukan untuk aplikasi lebih lanjut. Surfaktan yang sesuai sebagai pengemulsi o/w banyak digunakan pada industri produk-produk perawatan diri, sedangkan surfaktan yang sesuai sebagai pengemulsi w/o banyak digunakan pada industri makanan.
Daya Detergensi
Uji detergensi dilakukan untuk mengetahui kemampuan ester asam lemak-karbohidrat untuk membersihkan kotoran berlemak pada suatu kain. Pada pengukuran daya detergensi ini selain ketiga jenis ester
glukosa, juga digunakan detergen komersial sebagai pembanding.
Daya detergensi sebanding dengan konsentrasi surfaktan, semakin tinggi konsentrasi maka semakin tinggi pula daya detergensinya, terlebih lagi jika KMK telah dicapai. Semakin tinggi konsentrasi di atas KMK maka misel yang terbentuk semakin banyak sehingga kotoran yang dapat terikat oleh misel juga akan semakin banyak (Lynn 1993). Gambar 5, 6, dan 7 memperlihatkan perilaku yang menyimpang dari teori di atas karena pengaruh ketidakmurnian.
0
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Daya Detergensi
(NTU)
Deterjen Komersial Ester Glukosa Laurat
Gambar 5 Daya detergensi ester glukosa laurat.
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Daya Detergensi
(NTU)
Deterjen Komersial Ester Glukosa Miristat
0
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Daya Detergensi
(NTU)
Deterjen Komersial Ester Glukosa Stearat
Gambar 7 Daya detergensi ester glukosa stearat.
Stabilitas Busa
Uji pembusaan dimaksudkan untuk mengetahui kemampuan surfaktan dalam menghasilkan busa. Surfaktan dengan stabilitas busa yang baik diperlukan dalam industri produk-produk perawatan diri seperti sabun dan sampo. Stabilitas busa sangat bergantung kepada elastisitas lapisan tipis cairan antar busa (lamela) yang diantaranya dapat dihasilkan dengan cara teradsorpsinya surfaktan pada lapisan cairan (Holmberg et al. 2003).
Gambar 8 memperlihatkan bahwa ketiga jenis ester glukosa hanya dapat mempertahankan busa selama beberapa jam saja, bahkan untuk ester glukosa stearat hanya beberapa menit (Lampiran 6). Rendahnya daya busa disebabkan karena gugus hidrofobik dari ketiga ester glukosa mempunyai struktur meruah sehingga adsorbsinya di permukaan tidak tersusun dengan baik.
0
0 0.001 0.002 0.003 0.004 0.005
Konsentrasi (% b/v) Stabilitas Busa
(jam)
Ester Glukosa Laurat Ester Glukosa Miristat Ester Glukosa Stearat
Gambar 8 Stabilitas busa ester glukosa.
Ester glukosa laurat memiliki stabilitas busa terbaik dibandingkan dua jenis ester glukosa lainnya karena ester glukosa laurat memiliki gugus hidrofobik yang terpendek. Semakin panjang gugus hidrofobik (rantai hidrokarbon) suatu ester asam lemak, maka stabilitas busanya akan semakin rendah karena strukturnya akan semakin meruah (Durian & Weitz 1993).
Surfaktan nonionik lebih tepat jika diaplikasikan sebagai anti busa, terlebih lagi jika merupakan pengemulsi o/w. Karena bahan yang mudah terdispersikan dalam air akan menurunkan elastisitas lamela, sehingga busa akan semakin cepat pecah.
Nilai pH
Nilai pH tertinggi dicapai oleh ester glukosa miristat, sedangkan nilai pH terendah dicapai oleh ester glukosa stearat (Tabel 2). Pengukuran pH penting dilakukan untuk mengetahui keasaman suatu surfaktan. Pada umumnya surfaktan yang digunakan dalam industri produk-produk perawatan diri bersifat netral. Ester glukosa miristat cukup baik jika akan diaplikasikan dalam industri produk-produk perawatan diri, karena nilai pH-nya mendekati netral.
Tabel 2 pH ester glukosa
Jenis pH Ester Glukosa Laurat 6.62
Ester Glukosa Miristat 6.82 Ester Glukosa Stearat 6.40
SIMPULAN DAN SARAN
Simpulan
Berdasarkan pencirian yang telah dilakukan ester glukosa stearat cukup baik apabila akan diaplikasikan sebagai pengemulsi o/w, sedangkan ester glukosa miristat dapat diaplikasikan sebagai detergen.
Saran
Perlu dilakukan pemurnian lebih lanjut terhadap ketiga ester glukosa agar diperoleh hasil yang lebih baik dalam pencirian. Perlu dilakukan uji wetting agent untuk ketiga ester glukosa. Uji toksisitas perlu dilakukan untuk mengetahui keamanan ketiga ester glukosa apabila akan diaplikasikan dalam industri makanan.
DAFTAR PUSTAKA
Adamson WA. 1982. Physical Chemistry of Surfaces. Canada: J Willey.
ASTM D_1331. 2000. Standard Test Methods Surface and Interfacial Tension of Surface
Active Agents and Emulsions. Annual
Book of ASTM Standards, Vol. 15. USA: Easton, MD.
Daintith J. 1994. Kamus Lengkap Kimia. SS Achmadi, penerjemah; Marias, Sitohang DP, editor, Jakarta: Erlangga. Terjemahan dari: A Concise Dictionary of Chemistry.
Dickinson E, Mc Clements. 1996. Advance in Food Colloids. New York: Chapman and Hall.
Durian DJ, Weitz DA. 1993. Foams. Di dalam: Kroschwitz JI, editor. Encyclopedia of Chemical Technology. Ed ke-4. Volume ke-11. New York: Wiley Interscience. hlm. 783-802.
Ferrer M et al. Comparative surface avtivities of di- and trisaccharide fatty acid esters. J Langmuir 18:667-673.
Friberg SE, Steven J. 1993. Emulsions. Di dalam: Kroschwitz JI, editor.
Encyclopedia of Chemical Technology. Ed ke-4. Volume ke-9. New York: Wiley Interscience. hlm. 393-412.
Georgiou G, Lin SC, Sharma MM. 1992. Surface Active Compounds from Microorganisms. J Biol 10:60-65.
Heusch R, Bayer AG, Leverkusen. 1987.
Emulsions. Volume ke-A9. Ullmann’s Encyclopedia of Industrial Chemistry. New York: Federal Republic of Germany.
Holmberg K, Jönsson B, Kronberg B, Lindman B. 2003. Surfactants and Polymers in Aqueous Solution. Ed ke-2. Chichester: J Wiley.
Jaya HS. 2005. Profil stabilitas emulsi fraksi ringan minyak bumi dalam air dengan penambahan surfaktan nonionik. [Skripsi]. Bogor: Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Kasori Y, Kashiwa K, penemu; Mitsubishi Chemical Corporation. 1999. Method for producing a sucrose fatty acid ester. US Patent 5,908,922.
Kuang D, Obaje OJ, Ali AM. 2000. Synthesis and characterization of acetylated glucose fatty esters from palm and palm kernel oil fatty methyl esters. J Oil Palm Res. 12(2):14-19.
Lynn J. 1993. Detergency. Di dalam: Kroschwitz JI, editor. Encyclopedia of Chemical Technology. Ed ke-4. Volume ke-7. New York: Wiley Interscience. hlm. 1072-1099.
Martini Y. 2003. Kajian pengaruh jenis dan konsentrasi katalis pada proses produksi surfaktan sukrosa ester dari metil ester minyak inti sawit. [Skripsi]. Bogor: Jurusan Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Obaje OJ, penemu; URAH Resources. 2005. Trans-acidolysis Process for the Preparation of Carbohydrate Fatty-Acid Esters. US Patent 6,846,916.
Prihanjani M. 2006. Sintesis ester glukosa miristat melalui interesterifikasi antara metil miristat dan glukosa pentaasetat. [Skripsi]. Bogor: Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Rieger MM. 1985. Surfactants in cosmetics.
Russiana IB. 2006. Sintesis ester glukosa laurat dari metil laurat dan glukosa pentaasetat. [Skripsi]. Bogor: Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sari I. 2006. Sintesis ester glukosa stearat melalui reaksi interesterifikasi dengan metode bebas pelarut. [Skripsi]. Bogor: Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lampiran 1 Pengukuran tegangan permukaan ester glukosa
Tegangan permukaan ester glukosa laurat Konsentrasi
(% b/v)
Densitas (g/mL)
Tegangan Permukaan Terukur (dyne/cm)
Mean circumference = 5.9450 R/r = 53.2561920
T = 28 ºC
d = densitas udara = 0.0012 g/mL D = densitas sampel
Contoh Perhitungan
Tegangan permukaan larutan ester glukosa laurat 0.0010% (b/v)
R
Tegangan permukaan ester glukosa miristat Konsentrasi
(% b/v)
Densitas (g/mL)
Lanjutan Lampiran 1
Tegangan permukaan ester glukosa stearat Konsentrasi
(% b/v)
Densitas (g/mL)
Tegangan Permukaan Terukur (dyne/cm)
Prerata
(dyne/cm) Fr
Lampiran 2 Pengukuran tegangan antarmuka ester glukosa
Tegangan antarmuka ester glukosa laurat Konsentrasi
(% b/v)
Densitas (g/mL)
Tegangan Antarmuka Terukur (dyne/cm)
Mean circumference = 5.9450 R/r = 53.2561920
T = 28 ºC
d = densitas xilena = 0.8802 g/mL D = densitas sampel
Contoh Perhitungan
Tegangan antarmuka larutan ester glukosa laurat 0.0010% (b/v)
R
Tegangan antarmuka ester glukosa miristat Konsentrasi
(% b/v)
Densitas (g/mL)
Tegangan Antarmuka Terukur (dyne/cm)
Tegangan antarmuka ester glukosa stearat Konsentrasi
(% b/v)
Densitas (g/mL)
Lampiran 3 Penentuan nilai HLB ester glukosa
Penentuan kurva standar HLB
Jenis Surfaktan V akuades terpakai (mL) HLB Perubahan Warna
Tween-80 (PA) 69.4 15.0 Kuning muda menjadi keruh
Tween-20 (PA) 81.9 16.7 Kuning muda menjadi keruh
GMS 29.6 3.8 Tidak berwarna menjadi putih
Berdasarkan pada tabel di atas dibuat persamaan garis. Volume akuades yang terpakai sebagai sumbu x dan nilai HLB sebagai sumbu y. Nilai HLB ester glukosa laurat, ester glukosa miristat, dan ester glukosa stearat diperoleh dengan interpolasi ke dalam persamaan garis y = 0.2551 x – 3.5487 (Jaya 2005).
y = 0.2551x - 3.5487 R2 = 0.9881
0 2 4 6 8 10 12 14 16 18 20
0 10 20 30 40 50 60 70 80 90 Volume Akuades Terpakai (mL)
HL
B
Penentuan HLB ester glukosa laurat
Ulangan Bobot
(g)
V akuades terpakai
(mL) HLB Perubahan Warna
1 1.0009 48.25 8.80 Kuning menjadi kuning keruh
2 1.0016 48.00 8.70 Kuning menjadi kuning keruh
Rerata 8.75
Penentuan HLB ester glukosa miristat
Ulangan Bobot
(g)
V akuades
terpakai (mL) HLB Perubahan Warna
1 1.0010 46.50 8.30 Kuning menjadi kuning keruh
2 1.0070 46.50 8.30 Kuning menjadi kuning keruh
Rerata 8.30
Penentuan HLB ester glukosa stearat
Ulangan Bobot
(g)
V akuades terpakai
(mL) HLB Perubahan Warna
1 1.0004 42.25 7.20 Tidak berwarna menjadi putih keruh
2 1.0013 42.50 7.30 Tidak berwarna menjadi putih keruh
Lampiran 4 Pengukuran stabilitas emulsi ester glukosa
Stabilitas emulsi w/o ester glukosa
Stabilitas Emulsi (menit) Jenis Konsentrasi
(% b/v) Ulangan I Ulangan II
Stabilitas Emulsi Rerata
(menit)
Ester glukosa laurat
0.0040 50.00 48.00 49.00
Ester glukosa miristat
0.0040 52.00 52.00 52.00
Ester glukosa stearat
0.0040 65.00 65.00 65.00
Stabilitas emulsi o/w ester glukosa laurat
Ulangan I Ulangan II emulsi rerata
(%)
Stabilitas emulsi o/w ester glukosa miristat
Ulangan I Ulangan II
Lanjutan Lampiran 4
Stabilitas emulsi o/w ester glukosa stearat
Ulangan I Ulangan II
Konsentrasi
(% b/v) Tinggi awal (cm)
Tinggi akhir (cm)
Stabilitas emulsi
(%)
Tinggi awal (cm)
Tinggi akhir
(cm)
Stabilitas emulsi
(%)
Stabilitas emulsi rerata
(%)
0.0000 3.30 0.00 0.00 3.30 0.00 0.00 0.00
0.0010 3.50 0.30 8.57 3.40 0.30 8.82 8.70
0.0020 3.30 0.35 10.61 3.30 0.35 10.61 10.61
0.0024 2.70 0.35 12.96 2.60 0.35 13.46 13.21
0.0030 2.70 0.30 11.11 2.60 0.35 13.46 12.29
0.0040 3.30 0.45 13.64 3.30 0.40 13.64 13.64
Contoh perhitungan
Stabilitas emulsi o/w ester glukosa laurat 0.0030% (b/v)
%
100
awal
tinggi
akhir
tinggi
emulsi
Stabilitas
=
×
100% 50
. 2
30 .
0 ×
=
Lampiran 5 Pengukuran daya detergensi ester glukosa
Daya detergensi ester glukosa laurat Konsentrasi
(% b/v) Ulangan
Turbiditas (T1) (NTU)
Turbiditas (T3) (NTU)
Daya detergensi (NTU)
1 0.61 2.54
2 0.60 2.55
0.0010
Rerata 0.60 2.54
1.68
1 0.49 2.24
2 0.49 2.22
0.0020
Rerata 0.49 2.23
1.37
1 0.55 3.97
2 0.55 3.97
0.0027
Rerata 0.55 3.97
3.11
1 0.36 2.52
2 0.36 2.54
0.0030
Rerata 0.36 2.53
1.67
1 0.43 2.85
2 0.42 2.85
0.0040
Rerata 0.42 2.85
1.99
Daya detergensi ester glukosa miristat Konsentrasi
(% b/v) Ulangan
Turbiditas (T1) (NTU)
Turbiditas (T3) (NTU)
Daya detergensi (NTU)
1 0.62 2.70
2 0.62 2.71
0.0010
Rerata 0.62 2.70
1.85
1 0.57 4.57
2 0.57 4.59
0.0020
Rerata 0.57 4.58
3.72
1 1.24 5.66
2 1.24 5.64
0.0026
Rerata 1.24 5.65
4.79
1 0.73 5.00
2 0.73 5.00
0.0030
Rerata 0.73 5.00
4.14
1 0.67 6.11
2 0.67 6.11
0.0040
Rerata 0.67 6.10
Lanjutan Lampiran 5
Daya detergensi ester glukosa stearat Konsentrasi
(% b/v) Ulangan
Turbiditas (T1) (NTU)
Turbiditas (T3) (NTU)
Daya detergensi (NTU)
1 0.74 2.03
2 0.74 2.03
0.0010
Rerata 0.74 2.03
1.17
1 0.31 1.44
2 0.31 1.44
0.0020
Rerata 0.31 1.44
0.58
1 1.16 2.88
2 1.16 2.88
0.0024
Rerata 1.16 2.88
2.02
1 0.33 2.29
2 0.33 2.29
0.0030
Rerata 0.33 2.29
1.43
1 0.41 4.26
2 0.41 4.27
0.0040
Rerata 0.41 4.26
3.40
Daya detergensi deterjen komersial Konsentrasi
(% b/v) Ulangan
Turbiditas (T1) (NTU)
Turbiditas (T3) (NTU)
Daya detergensi (NTU)
1 0.26 2.86
2 0.26 2.87
0.0010
Rerata 0.26 2.86
2.00
1 0.37 4.15
2 0.37 4.16
0.0020
Rerata 0.37 4.15
3.29
1 0.42 4.54
2 0.42 4.55
0.0024
Rerata 0.42 4.54
3.68
1 0.56 4.76
2 0.56 4.77
0.0026
Rerata 0.56 4.76
3.90
1 0.57 6.59
2 0.59 6.60
0.0027
Rerata 0.58 6.59
5.73
1 0.80 6.36
2 0.80 6.36
0.0030
Rerata 0.80 6.36
5.62
1 0.91 7.80
2 0.91 7.80
0.0040
Rerata 0.91 7.80
Lanjutan Lampiran 5
Turbiditas akuades
Ulangan Turbiditas (T2) (NTU) 1 0.86 2 0.86 Rerata 0.86
Contoh perhitungan
Daya detergensi ester glukosa laurat 0.0010% (b/v) OD (Original Dirt) = T2 − T1
= 0.86 − 0.60 = 0.26
Daya detergensi = T3 − OD − T1 = 2.54 − 0.26 − 0.6 = 1.68
Lampiran 6 Pengukuran stabilitas busa ester glukosa
Lama pembusaan (jam) Jenis Konsentrasi (% b/v)
Ulangan I Ulangan II
Stabilitas Busa Rerata (jam)
0.0010 4.50 4.52 4.51
0.0020 6.13 6.12 6.12
0.0027 7.15 7.20 7.17
0.0030 8.13 8.13 8.13
Ester glukosa laurat
0.0040 9.60 9.63 9.61
0.0010 1.67 1.68 1.67
0.0020 2.30 2.33 2.31
0.0026 2.57 2.57 2.57
0.0030 2.92 2.97 2.91
Ester glukosa miristat
0.0040 3.72 3.70 3.71
0.0010 11.98 12.00 11.99
0.0020 18.78 18.83 18.80
0.0024 21.40 21.43 21.41
0.0030 23.97 24.00 23.98
Ester glukosa stearat
0.0040 43.83 43.97 43.90