TOKSIKOPATOLOGI HATI MENCIT (
Mus musculus
) PADA
PEMBERIAN PARASETAMOL
HEIRMAYANI
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
ABSTRAK
HEIRMAYANI. Toksikopatologi Hati Mencit (Mus musculus) Pada Pemberian Parasetamol. Dibimbing oleh DEWI RATIH AGUNGPRIYONO dan SRI ESTUNINGSIH.
Parasetamol adalah obat yang digunakan secara meluas di masyarakat. Digolongkan obat yang berlabel bebas terbatas, bisa dibeli secara bebas. Penggunaannya kadang menyalahi aturan pakai yang tertera pada pembungkus obat tersebut. Penelitian ini bertujuan untuk mempelajari efek parasetamol dosis normal optimum selama 6 minggu pada organ hati mencit. Hasil yang diperoleh diharapkan dapat melengkapi informasi dasar tentang toksikopatologi hati akibat obat-obatan kimiawi. Penelitian ini menggunakan 36 ekor mencit yang diberi 500 mg/ 50 kgBB parasetamol intragastric. Parameter histopatologi hati yang dipakai adalah dengan menghitung persentase sel yang mengalami degenerasi dan yang mengalami nekrosa pada kelompok yang diberi parasetamol. Data yang diperoleh dianalisa menggunakan analisis sidik ragam acak lengkap (ANOVA) dilanjutkan dengan uji Tukey (α = 0,05). Hasil penelitian menunjukkan bahwa sejalan dengan pertambahan waktu, pemberian parasetamol dosis normal optimum menyebabkan terjadinya peningkatan lesio kematian hepatosit berupa nekrosa sementara lesio degeneratifnya menurun.
Kata kunci : Parasetamol, hepatotoksikopatologi, toksikopatologi hati
ABSTRACT
HEIRMAYANI. Toxicopathology of mice liver (Mus musculus) received paracetamol. Under the direction of DEWI RATIH AGUNGPRIYONO and
SRI ESTUNINGSIH.
Paracetamol is drugs that common used widely by many people. Paracetamol classify as limited free labling drugs so that everybody can it without prescription. Many people use this drug sometimes were not follow the direction written on the label. The aim of this research was to study the effect of normal optimum dose of paracetamol for 6 weeks application within mice liver. Thirty six mice were used in this research and given 500 mg/ 50kgBW of paracetamol intragastrically. Histopathology parameters that used to evaluate the hepatocytes lesion is to count the percentage of lesion degeneration and necrosis exist. The data then were analysed statistically using Analysis of Variance (ANOVA), continued by Tukey test (α = 0,05). The result showed, as the time of paracetamol application increase, there were also increase of necrosis hepatocytes percentage while the percentage of degeneration hepatocytes were decreased.
TOKSIKOPATOLOGI HATI MENCIT (
Mus musculus
) PADA
PEMBERIAN PARASETAMOL
HEIRMAYANI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Toksikopatologi Hati Mencit (Mus musculus) Pada Pemberian Parasetamol
Nama : Heirmayani
NRP : B04103128
Disetujui
Pembimbing Skripsi I Pembimbing Skripsi II
Drh. Dewi Ratih Agungpriyono, PhD. Dr. Drh. Sri Estuningsih, MSi. NIP. 131 760 839 NIP. 131 878 929
Diketahui
Wakil Dekan FKH IPB
Dr. Drh. I Wayan Teguh Wibawan, MS. NIP. 131 129 090
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Judul yang dipilih dalam
penelitian yang dilaksanakan sejak bulan Februari sampai bulan Juli 2007 ini
adalah Toksikopatologi Hati Mencit (Mus musculus) Pada Pemberian
Parasetamol.
Terima kasih penulis ucapkan kepada Ibu Drh. Dewi Ratih Agungpriyono,
PhD dan Ibu Dr. Drh. Sri Estuningsih, MSi selaku pembimbing, Bapak Drh.
Hernomoadi Huminto, MVS selaku dosen penguji serta Bapak Dr. Drh. Eko
Sugeng Pribadi, MS yang telah banyak memberikan saran. Di samping itu, ucapan
terima kasih penulis sampaikan kepada Bapak dan Ibu Dosen beserta staf di
Bagian Patologi, Departemen Klinik, Reproduksi dan Patologi Fakultas
Kedokteran Hewan Institut Pertanian Bogor yang telah membantu dalam
pelaksanaan penelitian ini.
Terima kasih tak terhingga dan penuh hormat penulis ucapkan kepada
Bapak Enceng Suherman dan Mama Nuryani tercinta yang selalu mengasuh,
mendidik dan membimbing dengan penuh kasih sayang serta senantiasa
mendo’akan dan memberikan dorongan penuh baik moril maupun materil sampai
saat ini. Keluarga di Jakarta (Ndhe, Aa, De ira, Nenek, Engki, Om, Ante dan
semua sepupuku), terima kasih telah memberikan semangat, perhatian dan warna
dalam senyum cerianya. Achmad Isfar Shaffan Adlim dan Erly Pratita, terima
kasih atas kesabaran dan pengertian yang diberikan selama ini serta pelajaran
tentang hidup dan kedewasaan. Tak lupa penulis ucapkan terima kasih kepada
teman-teman seperjuangan Au, Ika, Reny, Bayu atas bantuannya selama ini serta
seluruh teman-teman angkatan 40, kosan Zulfa dan teman-teman yang tidak dapat
disebutkan namanya satu-persatu.
Semoga karya ilmiah ini dapat bermanfaat bagi para pembaca.
Bogor, Juli 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 21 Februari 1986 sebagai anak
pertama dari empat bersaudara, anak dari pasangan Enceng Suherman dan
Nuryani.
Tahun 2003 penulis lulus SMU Negeri 49 Jakarta dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis memilih Fakultas Kedokteran Hewan.
Selama mengikuti perkuliahan, penulis pernah aktif menjadi anggota
Ikatan Mahasiswa Kedokteran Hewan Indonesia (2004/2005), Himpunan Minat
Profesi Satwa Liar (2004/2005), Himpunan Minat Profesi Ornithologi dan Unggas
(2005/2006) serta Forum Ilmiah Mahasiswa (2005/2006). Praktik lapangan yang
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... i x PENDAHULUAN ... 1
TINJAUAN PUSTAKA Hati ... 3
Karakteristik dan data biologis mencit ... 8
Parasetamol (asetaminofen) ... 10
BAHAN DAN METODE Waktu dan tempat penelitian ... 16
Alat dan bahan ... 16
Metode penelitian ... 16
HASIL DAN PEMBAHASAN ... 19
KESIMPULAN DAN SARAN ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Halaman
1. Derajat Keparahan Lesio Hepatosit Mencit Pada Pemberian
Parasetamol Dosis Normal Optimum Dalam Waktu 6 Minggu ... 20
2. Derajat Keparahan Perubahan Hepatosit Mencit Pada Vena Porta (VP) Dan Vena Sentralis (VS)
Akibat Pemberian Parasetamol Dosis Normal Optimum ... 23
3. Pengaruh Pemberian Parasetamol Dosis Normal Optimum Terhadap Jumlah Sel Radang Pada Vena Porta (VP) Dan
DAFTAR GAMBAR
Halaman
1. Bagan Struktur Kimia Parasetamol ... 11
2. Bagan Struktur Aminobenzena Senyawa Parasetamol ... 11
3. Bagan Metabolisme Parasetamol ... 13
4. Perbandingan Perubahan Persentase Lesio Hepatosit Kelompok Kontrol (K) dan Perlakuan (P) ... ... 20
5. Pengaruh Pemberian Parasetamol Dosis Normal Optimum Terhadap Perubahan Hepatosit Mencit Pada Vena Porta (VP) Dan Vena Sentralis (VS) ... 23
6. Gambaran Histopatologi Jaringan Hati Kelompok Kontrol ... 25
7. Gambaran Histopatologi Jaringan Hati Kelompok Perlakuan ... 25
8. Perubahan Pada Bagian Interstitium Hati Berupa Kongesti ... 27
9. Infiltrasi Dan Akumulasi Sel Radang Perivaskuler Vena Sentralis ... 28
DAFTAR LAMPIRAN
Halaman
1. Bagan Pembuatan Sediaan Histopatologi ... 37
2. Bagan Pewarnaan Haematoksilin Eosin ... 38
TOKSIKOPATOLOGI HATI MENCIT (
Mus musculus
) PADA
PEMBERIAN PARASETAMOL
HEIRMAYANI
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
ABSTRAK
HEIRMAYANI. Toksikopatologi Hati Mencit (Mus musculus) Pada Pemberian Parasetamol. Dibimbing oleh DEWI RATIH AGUNGPRIYONO dan SRI ESTUNINGSIH.
Parasetamol adalah obat yang digunakan secara meluas di masyarakat. Digolongkan obat yang berlabel bebas terbatas, bisa dibeli secara bebas. Penggunaannya kadang menyalahi aturan pakai yang tertera pada pembungkus obat tersebut. Penelitian ini bertujuan untuk mempelajari efek parasetamol dosis normal optimum selama 6 minggu pada organ hati mencit. Hasil yang diperoleh diharapkan dapat melengkapi informasi dasar tentang toksikopatologi hati akibat obat-obatan kimiawi. Penelitian ini menggunakan 36 ekor mencit yang diberi 500 mg/ 50 kgBB parasetamol intragastric. Parameter histopatologi hati yang dipakai adalah dengan menghitung persentase sel yang mengalami degenerasi dan yang mengalami nekrosa pada kelompok yang diberi parasetamol. Data yang diperoleh dianalisa menggunakan analisis sidik ragam acak lengkap (ANOVA) dilanjutkan dengan uji Tukey (α = 0,05). Hasil penelitian menunjukkan bahwa sejalan dengan pertambahan waktu, pemberian parasetamol dosis normal optimum menyebabkan terjadinya peningkatan lesio kematian hepatosit berupa nekrosa sementara lesio degeneratifnya menurun.
Kata kunci : Parasetamol, hepatotoksikopatologi, toksikopatologi hati
ABSTRACT
HEIRMAYANI. Toxicopathology of mice liver (Mus musculus) received paracetamol. Under the direction of DEWI RATIH AGUNGPRIYONO and
SRI ESTUNINGSIH.
Paracetamol is drugs that common used widely by many people. Paracetamol classify as limited free labling drugs so that everybody can it without prescription. Many people use this drug sometimes were not follow the direction written on the label. The aim of this research was to study the effect of normal optimum dose of paracetamol for 6 weeks application within mice liver. Thirty six mice were used in this research and given 500 mg/ 50kgBW of paracetamol intragastrically. Histopathology parameters that used to evaluate the hepatocytes lesion is to count the percentage of lesion degeneration and necrosis exist. The data then were analysed statistically using Analysis of Variance (ANOVA), continued by Tukey test (α = 0,05). The result showed, as the time of paracetamol application increase, there were also increase of necrosis hepatocytes percentage while the percentage of degeneration hepatocytes were decreased.
TOKSIKOPATOLOGI HATI MENCIT (
Mus musculus
) PADA
PEMBERIAN PARASETAMOL
HEIRMAYANI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Toksikopatologi Hati Mencit (Mus musculus) Pada Pemberian Parasetamol
Nama : Heirmayani
NRP : B04103128
Disetujui
Pembimbing Skripsi I Pembimbing Skripsi II
Drh. Dewi Ratih Agungpriyono, PhD. Dr. Drh. Sri Estuningsih, MSi. NIP. 131 760 839 NIP. 131 878 929
Diketahui
Wakil Dekan FKH IPB
Dr. Drh. I Wayan Teguh Wibawan, MS. NIP. 131 129 090
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Judul yang dipilih dalam
penelitian yang dilaksanakan sejak bulan Februari sampai bulan Juli 2007 ini
adalah Toksikopatologi Hati Mencit (Mus musculus) Pada Pemberian
Parasetamol.
Terima kasih penulis ucapkan kepada Ibu Drh. Dewi Ratih Agungpriyono,
PhD dan Ibu Dr. Drh. Sri Estuningsih, MSi selaku pembimbing, Bapak Drh.
Hernomoadi Huminto, MVS selaku dosen penguji serta Bapak Dr. Drh. Eko
Sugeng Pribadi, MS yang telah banyak memberikan saran. Di samping itu, ucapan
terima kasih penulis sampaikan kepada Bapak dan Ibu Dosen beserta staf di
Bagian Patologi, Departemen Klinik, Reproduksi dan Patologi Fakultas
Kedokteran Hewan Institut Pertanian Bogor yang telah membantu dalam
pelaksanaan penelitian ini.
Terima kasih tak terhingga dan penuh hormat penulis ucapkan kepada
Bapak Enceng Suherman dan Mama Nuryani tercinta yang selalu mengasuh,
mendidik dan membimbing dengan penuh kasih sayang serta senantiasa
mendo’akan dan memberikan dorongan penuh baik moril maupun materil sampai
saat ini. Keluarga di Jakarta (Ndhe, Aa, De ira, Nenek, Engki, Om, Ante dan
semua sepupuku), terima kasih telah memberikan semangat, perhatian dan warna
dalam senyum cerianya. Achmad Isfar Shaffan Adlim dan Erly Pratita, terima
kasih atas kesabaran dan pengertian yang diberikan selama ini serta pelajaran
tentang hidup dan kedewasaan. Tak lupa penulis ucapkan terima kasih kepada
teman-teman seperjuangan Au, Ika, Reny, Bayu atas bantuannya selama ini serta
seluruh teman-teman angkatan 40, kosan Zulfa dan teman-teman yang tidak dapat
disebutkan namanya satu-persatu.
Semoga karya ilmiah ini dapat bermanfaat bagi para pembaca.
Bogor, Juli 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 21 Februari 1986 sebagai anak
pertama dari empat bersaudara, anak dari pasangan Enceng Suherman dan
Nuryani.
Tahun 2003 penulis lulus SMU Negeri 49 Jakarta dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis memilih Fakultas Kedokteran Hewan.
Selama mengikuti perkuliahan, penulis pernah aktif menjadi anggota
Ikatan Mahasiswa Kedokteran Hewan Indonesia (2004/2005), Himpunan Minat
Profesi Satwa Liar (2004/2005), Himpunan Minat Profesi Ornithologi dan Unggas
(2005/2006) serta Forum Ilmiah Mahasiswa (2005/2006). Praktik lapangan yang
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... i x PENDAHULUAN ... 1
TINJAUAN PUSTAKA Hati ... 3
Karakteristik dan data biologis mencit ... 8
Parasetamol (asetaminofen) ... 10
BAHAN DAN METODE Waktu dan tempat penelitian ... 16
Alat dan bahan ... 16
Metode penelitian ... 16
HASIL DAN PEMBAHASAN ... 19
KESIMPULAN DAN SARAN ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Halaman
1. Derajat Keparahan Lesio Hepatosit Mencit Pada Pemberian
Parasetamol Dosis Normal Optimum Dalam Waktu 6 Minggu ... 20
2. Derajat Keparahan Perubahan Hepatosit Mencit Pada Vena Porta (VP) Dan Vena Sentralis (VS)
Akibat Pemberian Parasetamol Dosis Normal Optimum ... 23
3. Pengaruh Pemberian Parasetamol Dosis Normal Optimum Terhadap Jumlah Sel Radang Pada Vena Porta (VP) Dan
DAFTAR GAMBAR
Halaman
1. Bagan Struktur Kimia Parasetamol ... 11
2. Bagan Struktur Aminobenzena Senyawa Parasetamol ... 11
3. Bagan Metabolisme Parasetamol ... 13
4. Perbandingan Perubahan Persentase Lesio Hepatosit Kelompok Kontrol (K) dan Perlakuan (P) ... ... 20
5. Pengaruh Pemberian Parasetamol Dosis Normal Optimum Terhadap Perubahan Hepatosit Mencit Pada Vena Porta (VP) Dan Vena Sentralis (VS) ... 23
6. Gambaran Histopatologi Jaringan Hati Kelompok Kontrol ... 25
7. Gambaran Histopatologi Jaringan Hati Kelompok Perlakuan ... 25
8. Perubahan Pada Bagian Interstitium Hati Berupa Kongesti ... 27
9. Infiltrasi Dan Akumulasi Sel Radang Perivaskuler Vena Sentralis ... 28
DAFTAR LAMPIRAN
Halaman
1. Bagan Pembuatan Sediaan Histopatologi ... 37
2. Bagan Pewarnaan Haematoksilin Eosin ... 38
PENDAHULUAN
Latar Belakang
Perubahan pola konsumsi masyarakat telah menyebabkan munculnya
berbagai penyakit. Studi menunjukkan bahwa masyarakat di wilayah yang terlalu
banyak mengkonsumsi protein, lemak, gula dan garam misalnya, ternyata lebih
banyak ditemukan penderita penyakit-penyakit degeneratif seperti arteriosklerosis
dan penyakit-penyakit yang berkaitan dengan organ pencernaan (hati, pankreas
dan gastrointestinal) dibandingkan masyarakat di wilayah yang banyak
mengkonsumsi karbohidrat, serat dan vitamin (Ruswandi 2005).
Salah satu fungsi hati yang penting ialah melindungi tubuh terhadap
terjadinya penumpukan zat berbahaya yang masuk dari luar, misalnya obat.
Banyak diantara obat yang bersifat larut dalam lemak dan tidak mudah
diekskresikan oleh ginjal. Untuk itu maka sistem enzim pada mikrosom hati akan
melakukan biotransformasi sedemikian rupa sehingga metabolit yang terbentuk
menjadi lebih mudah larut dalam air dan dapat dikeluarkan melalui urin atau
empedu. Dengan faal tersebut, tidak mengherankan bila hati mempunyai
kemungkinan yang cukup besar untuk dirusak oleh obat. Hepatitis karena obat
(HKO) pada umumnya tidak menimbulkan kerusakan permanen, tetapi
kadang-kadang dapat berlangsung lama dan fatal (Dalimartha 2005).
Di Indonesia, obat-obatan yang mengandung parasetamol dosis tinggi
telah bebas dijual dan beredar di masyarakat seperti Panadol® dan Mixagrip®.
Banyak masyarakat yang menggunakan parasetamol sebagai obat sakit kepala.
Konsumsi obat (parasetamol) dosis berlebih merupakan salah satu penyebab
rusaknya membran sel hati. Nekrosis hati terjadi karena interaksi radikal bebas
hasil metabolisme obat dan metabolisme tubuh dengan biomolekul penyusun
membran sel hati. Interaksi radikal bebas ini menyebabkan perubahan dan
merusak membran sel (Anonimus 2006). Menurut Clark, penggunaan obat yang
mengandung parasetamol berlebihan dalam jangka waktu tertentu akan
menyebabkan terjadinya kerusakan sel hati (Sutanto 1996).
Kerusakan sel hati yang diakibatkan parasetamol menyerupai kerusakan
2
Kerusakan sel hati menyebabkan meningkatnya lipid peroksida darah karena lipid
peroksida tubuh tidak dapat lagi didetoksifikasi dalam hati. Jumlah radikal bebas
yang melebihi ketersediaan senyawa-senyawa penetralisir dalam hati
memungkinkan terjadinya reaksi antara radikal bebas dan membran sel hati. Hal
ini mendasari dugaan mengenai kemampuan parasetamol sebagai hepatotoksikan.
Kerusakan hati yang disebabkan oleh parasetamol pada penelitian ini, diketahui
dengan cara menghitung persentase sel yang mengalami degenerasi dan nekrosa
sehingga pengaruh pemberian parasetamol dosis normal optimum terhadap
gambaran histopatologi hati mencit (Mus musculus) dapat dianalisa. Kerusakan
hati jika terjadi dalam waktu yang lama dapat menyebabkan kematian.
Tujuan
Penelitian ini bertujuan untuk mengkaji pengaruh pemberian parasetamol
dosis normal optimum terhadap gambaran histopatologi hati mencit (Mus
musculus).
Hipotesa
H0 : Parasetamol dapat menyebabkan kerusakan hati. H1 : Parasetamol tidak dapat menyebabkan kerusakan hati.
Manfaat
Hasil penelitian ini diharapkan dapat memberikan informasi dasar
mengenai kerusakan hati yang ditimbulkan pada pemakaian parasetamol dosis
TINJAUAN PUSTAKA
Hati
Anatomi dan Histologi Hati
Salah satu organ yang sering menderita karena adanya zat-zat toksik
adalah hati. Hati merupakan organ tubuh yang besar, kompleks dan terdapat di
dalam rongga perut kanan atas, tepat di bawah diafragma kanan dan dilindungi
tulang iga kanan bawah serta diselubungi oleh peritoneum. Organ ini berwarna
coklat tua dan berbobot antara 1.200-1.600 gram atau 2.5% dari bobot total orang
dewasa. Hati terbagi menjadi dua bagian dan bagian kanan besarnya enam kali
bagian kirinya (Ganong 2003).
Hati terdiri dari beberapa lobus, tergantung pada spesiesnya. Pada mencit
terdapat empat lobus (lobus medial, lobus lateral kiri, lobus lateral kanan dan
lobus kaudal (Harada et al. 1999). Di dalamnya mengalir darah yang melewati
sel-sel hati melalui sinusoid dari cabang vena porta hepatika ke dalam vena
sentralis tiap lobulus (Ganong 2003). Setiap lobulus hati terdiri dari berbagai
komponen, yaitu sel-sel parenkim hati (hepatosit), vena sentralis, sinusoid,
cabang-cabang vena porta, cabang-cabang arteri hepatika, sel Kupffer dan
kanalikuli biliaris (Handoko 2003). Vena porta, arteri hepatika dan saluran
empedu akan bergabung dalam satu daerah vena porta (segitiga Kiernaan).
Empedu akan disalurkan dari hati ke duodenum melalui saluran empedu
intrahepatik dan ekstrahepatik (Guyton 1997). Di dalam hati juga ditemukan
banyak sel-sel RES (Reticulo Endothelial System), yakni sel-sel Kupffer yang
terdapat dalam dinding-dinding kapiler dan sinusoid-sinusoid hati, berfungsi
untuk membersihkan benda-benda asing dari darah (fagositik) (Ganong 2003).
Sel hati (hepatosit) berbentuk polyhedral, berdiameter 20-25 mikron pada
hewan dewasa, sedangkan pada hewan muda sekitar 2-7 mikron. Inti bulat
ditengah-tengah dan kadang-kadang tampak lebih dari satu inti akibat pembelahan
sitoplasma yang tidak sempurna (Hartono 1992). Hepatosit tersusun radial di
sekeliling vena sentralis. Di antara sederetan hepatosit terdapat suatu saluran
sinusoid yang menuju vena sentralis. Saluran ini merupakan sistem sinusoidal,
4
empedu. Lobus hati secara histologis dibungkus oleh kapsula. Kapsula lobus hati
terdiri dari kapsula fibrosa dan kapsula serosa. Asinus hepatik dibagi lagi menjadi
tiga zona: periportal, midzonal dan sentrolobular. Hepatosit pada zona periportal
menerima darah kaya oksigen dan nutrisi karena berdekatan dengan pembuluh
afferent sedangkan sel di sekitar zona sentrolobular terletak di distal, dekat
mikrosirkulasi penerima darah yang mengandung gas dan metabolit. Hal ini yang
menyebabkan zona sentrolobular tingkat sensitifitasnya lebih tinggi. Midzonal
merupakan zona transisi dari kedua zona lain (Harada et al. 1999).
Fisiologi Hati
Fungsi hati adalah mendetoksifikasi produk buangan metabolisme,
merusak sel darah merah tua, sintesis dan sekresi lipoprotein plasma serta
mempunyai fungsi metabolisme (sintesis glikogen, glukoneogenesis, menyimpan
glikogen, beberapa vitamin dan lipid) (Burkitt et al. 1995). Fungsi detoksifikasi
sangat berhubungan erat dengan fungsi ekskresi, karena hati mempunyai
kemampuan untuk mengekskresikan berbagai macam substansia sederhana,
seperti logam berat yang tidak diubah lewat empedu (Kelly 1993). Hati juga
mempunyai fungsi dalam mengatur kadar glukosa dalam darah. Makanan berupa
glukosa akan diabsorbsi di usus, kemudian diteruskan ke hati melalui vena portal.
Sebagian dari glikogen yang disimpan akan dipecah dalam hati menjadi glukosa.
Dalam keadaan normal kadar glikogen dalam hati cukup untuk mempertahankan
kadar glukosa darah. Jika terjadi gangguan hati, dapat menyebabkan terjadinya
hiperglikemia atau hipoglikemia (Ganiswara 1995).
Aliran darah masuk ke hati melalui dua sumber. Bagian terbesar darah
masuk melalui vena porta sedangkan aliran darah yang lain melalui arteri hepatika
Darah balik seluruhnya dialirkan keluar hati melalui vena hepatika yang masuk ke
dalam vena cava caudalis. Keistimewaan hati ialah karena sirkulasinya berlainan
dari alat tubuh lain. Darah yang mengalir didalamnya terdiri dari 2/3 darah balik
dan 1/3 darah nadi (Ressang 1984). Vena porta dan arteri hepatika merupakan
pembuluh darah dari usus yang membawa nutrisi dan zat-zat lain yang diserap
oleh usus. Nutrisi yang sampai di hati melalui aliran darah portal diolah dan
5
masuk berbagai bakteri, darah merah yang sudah tua dan toksin yang harus diolah,
dihancurkan atau mungkin juga disimpan. Sebanyak 75-80% darah pada organ
hati berasal dari vena porta sedangkan dari arteri hepatika mengalir sekitar
20-25% darah yang kaya oksigen (Lu 1995).
Toksikopatologi Hati
Hati merupakan organ sekresi terbesar dan mungkin merupakan kelenjar
pertahanan yang terpenting dalam tubuh. Sel hati dapat rusak hingga lebih dari
80% tanpa menyebabkan gejala klinis yang berat dan dapat sembuh kembali
secara sempurna.
Kerusakan pada hati dapat terjadi oleh beberapa faktor yaitu onset
pemaparan yang terlalu lama atau terlalu singkat, durasi pemaparan, dosis dan sel
inang yang rentan (Jubb 1993). Kerusakan yang terjadi pada sel hati dapat
bersifat sementara dan tetap. Sel akan mengalami perubahan untuk beradaptasi
mempertahankan hidup pada kerusakan yang bersifat sementara. Perubahan ini
biasa disebut degenerasi. Degenerasi terjadi karena adanya gangguan biokimiawi
yang disebabkan oleh iskemia, anemia, metabolisme abnormal dan zat kimia yang
bersifat toksik. Hal ini menyebabkan membran sel normal akan mengalami
kerusakan sehingga keseimbangan pengeluaran K+ dan pemasukan ion Na+, Ca+
dan air akan terganggu. Kerusakan membran sel menyebabkan terjadinya
peningkatan jumlah air ke dalam sel, sehingga menyebabkan sitoplasma menjadi
bengkak dan dipenuhi butiran-butiran air. Apabila kerusakan membran sel terus
berlangsung, maka sitoplasma sel akan berisi cairan yang membentuk
vakuola-vakuola, sehingga sitoplasma terlihat lebih pucat, keadaan ini dinamakan
degenerasi hidropis (Cheville 1999).
Pada degenerasi lemak terjadi penumpukan lemak di lobuli hati yang
sering terlihat pada akhir masa kebuntingan karena kekurangan oksigen dan
adanya bahan toksik dan lain-lain. Hal ini terjadi karena adanya gangguan
keseimbangan antara trigliserida misel dan lemak globular. Ketidakseimbangan
lemak terjadi karena pengangkutan lemak ke hati meningkat, sintesis lemak di hati
meningkat dan penggunaan lemak dalam sel hati yang berkurang sehingga jumlah
6
diangkut melalui plasma ke dalam hati dalam bentuk chylomicron (butir lemak
yang sangat halus) yang sebagian besar terdiri dari trigliserida, tetapi mengandung
juga sedikit protein dan fosfolipid. Di dalam hati, trigliserida di hidrolisa menjadi
asam lemak dan gliserol. Protein yang dibentuk oleh retikulum endoplasma
mengadakan ikatan dengan trigliserida untuk membentuk lipoprotein yang
dikeluarkan ke dalam plasma. Adanya zat toksik dapat mengganggu produksi
protein sehingga lipoprotein tidak terbentuk. Hal inilah yang menyebabkan lemak
tidak bisa disekresikan sehingga menjadi terakumulasi dalam sel hati. Pada hati
secara histopatologis degenerasi lemak tampak seperti bulatan di dalam
sitoplasma yang mirip vakuol, berbentuk bundar dan kosong. Selain degenerasi
lemak, sel juga sering mengalami akumulasi terutama akumulasi protein di dalam
sitoplasmanya (Carlton dan McGavin 1995).
Kerusakan sel secara terus-menerus akan mencapai suatu titik sehingga
terjadi kematian sel. Mekanisme kematian sel terjadi melalui dua proses: yaitu
apoptosis dan nekrosa. Pada apoptosis terjadi kematian sel yang terprogram yang
dipicu oleh fragmentasi DNA dan biasanya terjadi pada satu atau sekelompok sel
saja. Lain halnya dengan nekrosa, kematian sel bersifat menyeluruh. Pada nekrosa
biasanya ditemukan sel radang dan sitoplasma sel akan terlihat asidofilik. Nekrosa
ini ada yang bersifat lokal dan ada yang bersifat difus (Lu 1995).
Hati dapat mengalami nekrosa yang disebabkan oleh dua hal yaitu 1).
Toksopatik, disebabkan oleh pengaruh langsung agen yang bersifat toksik, 2).
Trofopatik, akibat kekurangan oksigen, zat-zat makanan dan sebagainya (Ressang
1984). Degenerasi hidropis, degenerasi lemak dan nekrosa merupakan stadium
permulaan dari proses kelainan dalam hati yang kemudian menjurus kearah suatu
proses peradangan (Harold 1971). Peradangan di dalam hati dapat terjadi secara
infeksius maupun non infeksius. Peradangan secara non infeksius secara umum
disebabkan oleh toksin. Hepatitis non infeksius atau toksik dapat terjadi secara
akut maupun kronis. Secara mikroskopis sifat nekrosis disini adalah koagulatif
yang ditandai dengan piknosis dan sitoplasma yang asidofilik yang dilanjutkan
dengan penguraian dan menghilangnya komponen-komponen sel. Menurut lokasi
7
1. Nekrosa yang difus, dimana perubahan-perubahan meliputi bagian yang luas
tanpa batas-batas lobuler yang jelas.
2. Sarang-sarang nekrosis (fokal), dimana terdapat sarang-sarang nekrosis kecil
dalam ukuran sublobular di sana-sini dalam lobuli. Hal ini khas pada infeksi
yang tersebar dan sering terlihat pada hewan-hewan percobaan.
3. Nekrosa perifer, dalam hal ini terdapat nekrosis pada daerah tepi dari lobuli.
Hal ini tidak begitu sering terjadi, hanya bila toksin-toksin keras tiba dalam
lobuli melalui aliran darah tanpa menimbulkan gangguan sirkulasi dan
pemberian oksigen pada sel-sel. Sel-sel dibagian perifer inilah yang terkena
pengaruh racun dan menderita kerusakan terlebih dahulu.
4. Nekrosis bagian pertengahan lobuli (midzone), nekrosis terjadi di daerah
pertengahan antara bagian perifer lobuli dengan vena sentralis. Bentuk ini
jarang terjadi pada hewan.
5. Nekrosa sentrolobular, dalam hal ini kerusakan terutama terjadi di sekitar vena
sentralis karena pengaruh toksin dalam aliran darah dan stagnasi dari aliran
darah dengan gejala-gejala anoxianya. Bentuk ini yang biasanya terlihat pada
hepatitis toksik akut.
Gambaran mikroskopis umum dari hepatitis toksik akut ialah suatu
nekrosa sentrolobular dengan lenyapnya sebagian besar sel-sel yang terletak di
sekitar vena sentralis dan tempatnya diambil alih oleh darah. Sel-sel yang terletak
lebih perifer mengalami degenerasi lemak dan lebih perifer lagi degenerasi
hidropis. Bila keadaan berjalan beberapa hari, terdapat infiltrasi sel-sel limfosit ke
dalam tenunan ikat periportal (Harold 1971).
Makroskopis hati yang menderita hepatitis toksik akut memperlihatkan
gambaran seperti umumnya pada perubahan degenerasi hidropis, degenerasi
lemak dan nekrosis. Umumnya hati bengkak, pucat, belang sedangkan gambaran
lobular terlihat jelas. Ukuran besar dari hati cenderung untuk mengecil karena
sejumlah sel-sel parenkhimnya menghilang akibat nekrosis, tetapi pembendungan
oleh darah dan penimbunan lemak cenderung memperbesar volumenya, sehingga
secara positif tidak bisa memberikan gambaran mengenai besarnya hati yang
menderita hepatitis toksik akut, meskipun pada kasus-kasus yang parah, hati
8
Penyebab hepatitis toksik akut adalah berbagai macam toksin, sebagian
besar diantaranya masih belum diketahui. Bahan toksik tersebut dapat dibagi
menjadi 3 golongan (Nabib 1987) :
1. Racun-racun kimia, termasuk didalamnya antara lain tetrachloroethylene dan
carbontetrachloride yang keduanya digunakan sebagai obat antihelmintik.
Efek toksik dari kedua racun tersebut diantaranya menyebabkan sel-sel
parenkim hati mengalami nekrosa sentrolobular yang dapat berakibat pada
terbentuknya tumor dan kanker hati. Oleh karena efek toksiknya yang
berbahaya maka sekarang kedua racun tersebut jarang digunakan.
2. Racun tanaman, diantaranya yang terdapat pada leguminosa pohon yang
diduga memiliki efek imunomodulator.
3. Racun metabolik, termasuk didalamnya bentuk-bentuk gastroenteritis tertentu
diduga dapat menimbulkan efek hepatotoksik.
Tingginya kadar lipid peroksida dapat menjadi indikasi awal rusaknya sel
hati. Peningkatan kadar lipid peroksida lebih jauh akan menyebabkan akumulasi
trigliserida pada sel hati dan kemudian menyebabkan terjadinya nekrosis hati.
Oleh karena itu, kadar lipid peroksida dapat digunakan sebagai parameter
kerusakan awal hati (Ruswandi 2005).
Kerusakan sel hati membuat proses pencernaan dan metabolisme
terganggu. Lancarnya proses pencernaan sangat membantu proses penyembuhan
penyakit, sebab tubuh mendapat asupan protein yang mampu meningkatkan daya
tahan tubuh. Bahkan dengan membaiknya metabolisme sangat membantu hati
meregenerasi sel-sel hati yang rusak akibat hepatitis (Budi dan Paimin 2005).
Karakteristik dan Data Biologis Mencit
Mencit (Mus musculus) sebagai hewan percobaan
Hewan percobaan atau yang sering disebut sebagai hewan laboratorium
adalah semua jenis hewan dengan persyaratan tertentu untuk dipergunakan
sebagai salah satu sarana dalam berbagai kegiatan penelitian biologi dan
kedokteran (Sulaksono et al. 1986). Hewan sebagai model atau sarana percobaan
haruslah memenuhi persyaratan tertentu, antara lain persyaratan genetik atau
9
ekonomi, mudah tidaknya diperoleh dan mampu memberikan reaksi biologis.
Hewan percobaan adalah hewan yang sengaja dipelihara dan diternakkan untuk
dipakai sebagai hewan model guna mempelajari dan mengembangkan berbagai
macam bidang ilmu dalam skala penelitian dan pengamatan laboratorik.
Mencit merupakan salah satu hewan laboratorium atau hewan percobaan.
Hewan ini merupakan hewan percobaan kecil yang tersebar di seluruh dunia dan
dapat ditemukan pada tempat tinggal manusia seperti di rumah dan gedung
(Mangkoewidjojo dan Smith 1998). Mencit adalah hewan pengerat (rodentia)
yang cepat berbiak, mudah dipelihara dalam jumlah banyak dan variasi
genetiknya cukup besar serta sifat anatomis dan fisiologisnya terkarakterisasi
dengan baik.
Sistem taksonomi mencit (Ballenger 1999): Kingdom : Animalia
Filum : Chordata
Subfilum : Vertebrata
Kelas : Mamalia
Ordo : Rodensia
Genus : Mus
Spesies : Mus musculus
Data biologis mencit
Lama hidup : 1-2 tahun, bisa sampai 3 tahun
Lama produksi ekonomis : 9 bulan
Lama kebuntingan : 19-21 hari
Kawin sesudah beranak : 1-24 jam
Umur disapih : 21 hari
Umur dewasa : 35 hari
Umur dikawinkan : 8 minggu (jantan dan betina)
Siklus estrus : 4-5 hari
Siklus kelamin : poli estrus
10
Perkawinan : pada waktu estrus
Ovulasi : dekat akhir periode estrus
Fertilisasi : 2 jam sesudah kawin
Berat dewasa : jantan 20-40 gram, betina 18-35 gram
Berat lahir : 0,5-1,0 gram
Jumlah anak : rata-rata 6, bisa sampai 15
Implantasi : 4-5 hari sesudah fertilisasi
Uterus : bikornua bermuara di cerviks
Suhu : 35-39oC
Pernafasan : 140-180/menit, turun menjadi 80/menit dengan
anastesi, naik sampai 230/menit jika stress
Denyut Jantung : 600-650/menit, turun hingga 350/menit dengan
anastesi dan naik 750/menit jika stress
Tekanan darah : 130-160 sistol
(Mangkoewidjojo dan Smith 1998)
Parasetamol (Asetaminofen) Rumus Kimia
Salah satu obat yang bersifat hepatotoksik adalah parasetamol. Senyawa
ini merupakan turunan fenasetin. Parasetamol mempunyai beberapa nama generik
antara lain N-hidroksi asetanilida, N-asetil-p-aminofenol dan asetaminofen.
Parasetamol digunakan sebagai obat analgesik dan antipiretik di seluruh dunia
(Sumioka et al. 2004). Parasetamol berbentuk serbuk kristal berwarna putih, tidak
berbau, rasanya sedikit pahit, peka terhadap udara dan cahaya serta mempunyai
pH 5,3-6,5, karena toksisitas dan daya antiinflamasinya yang lemah menjadikan
parasetamol sebagai alternatif aspirin. Parasetamol relatif aman pada dosis terapi,
walaupun demikian overdosis akut parasetamol dapat menyebabkan hepatotoksik,
kerusakan (nekrosis) sentrilobular hati yang fatal (Anonimus 2006).
Penggunaan parasetamol didasarkan pada dugaan bahwa fenasetin dalam
tubuh akan dioksidasi menjadi senyawa paraaminofenol. Kemampuan
parasetamol sebagai antipiretik terdapat pada struktur aminobenzena senyawa ini.
11
analgesik dan antipiretik melalui mekanisme penghambatan prostaglandin dalam
tubuh (Susana 1987). Struktur kimia parasetamol dan struktur aminobenzena
[image:31.595.184.439.177.402.2]senyawa parasetamol dapat dilihat pada Gambar di bawah ini :
Gambar 1. Bagan Struktur Kimia Parasetamol (Anonimus 2006)
[image:31.595.214.409.467.605.2]Acetanilide Paracetamol Aniline
Gambar 2. Bagan Struktur Aminobenzena Senyawa Parasetamol (Anonimus
12
Farmakodinamik
Parasetamol telah lama diketahui mempunyai mekanisme yang sama
dengan aspirin oleh karena persamaan struktur kedua zat tersebut. Parasetamol
bekerja menghambat enzim cyclooxygenase (COX) sehingga dapat mengurangi
produksi prostaglandin, yang terlibat di dalam proses demam dan sakit.
Bagaimanapun, ada perbedaan penting antara efek aspirin dan parasetamol.
Aspirin mengandung prostaglandin yang berperan di dalam proses peradangan,
tetapi parasetamol tidak dapat berfungsi sebagai antiinflamasi. Selain itu, aspirin
bekerja menghambat enzim COX yang tidak dapat diubah, secara langsung
menghalangi lokasi aktif enzim dan mempunyai efek merugikan pada lapisan
perut. Parasetamol secara tidak langsung menghalangi enzim COX sehingga
menjadi tidak efektif terhadap peroksida. Hal ini menyebabkan parasetamol
menjadi efektif bekerja pada susunan saraf pusat dan sel endotel, tetapi bukan
pada platelet dan sel imun yang mempunyai tingkat peroksida tinggi.
Pada tahun 2002 telah dilaporkan bahwa parasetamol selektif dalam
menghalangi varian dari enzim COX yang berbeda, dikenal varian COX-1 dan
COX-2. Enzim ini hanya bereaksi di otak dan sumsum tulang, sekarang dikenal
sebagai COX-3. Sebuah penelitian menunjukkan bahwa administrasi parasetamol
meningkatkan bioavibilitas dari serotonin (5-HT) di tikus, tetapi mekanismenya
belum diketahui (Anonimus 2006).
Farmakokinetik
Parasetamol dimetabolisme terutama oleh enzim-enzim mikrosomal sel
hati. Di dalam saluran pencernaan, asetaminofen dengan cepat diserap dan dalam
waktu 30 menit akan mencapai konsentrasi puncak dalam plasma. Pada dosis
yang menyebabkan toksisitas akut, ikatan parasetamol terhadap protein plasma
bervariasi dari 20-50%. Pada dosis normal, 90-100% dari senyawa obat ini
mungkin akan dikeluarkan melalui urin. Pengeluaran senyawa obat ini terjadi
setelah melewati fase konjugasi dengan asam glukoronat (sekitar 60%), asam
sulfat (35%) dan sistein (3%) serta sejumlah kecil metabolit dalam bentuk
terhidroksilasi dan terdeasetilasi (Anonimus 2006). Berdasarkan hasil penelitian
13
parasetamol akan mengalami biotransformasi melalui reaksi konjugasi dengan
asam glukoronat atau glutation dan hasilnya diekskresi melalui urin. Sisa
parasetamol mengalami biotransformasi dengan sistem sitokrom P-450. Sitokrom
P-450, suatu sistem enzim di retikulum endoplasma segera melakukan
biotransformasi oksidatif pada 5-10% parasetamol yang masuk ke dalam tubuh.
Parasetamol yang teroksidasi berubah menjadi N-asetil p-benzokuinon imin
(NAPQI), suatu senyawa yang toksik dan reaktif (Susana 1987). Senyawa radikal
ini dapat bereaksi dengan molekul penyusun membran sel hati contohnya
fosfolipid. Oksidasi senyawa ini akan menghasilkan suatu radikal bebas yang
dapat mengoksidasi molekul fosfolipid lainnya sehingga terjadi reaksi oksidasi
berantai. Reaksi ini dapat menyebabkan berubahnya komposisi membran sel hati.
Menurut Manson, perubahan membran sel menyebabkan kerusakan sel hati dan
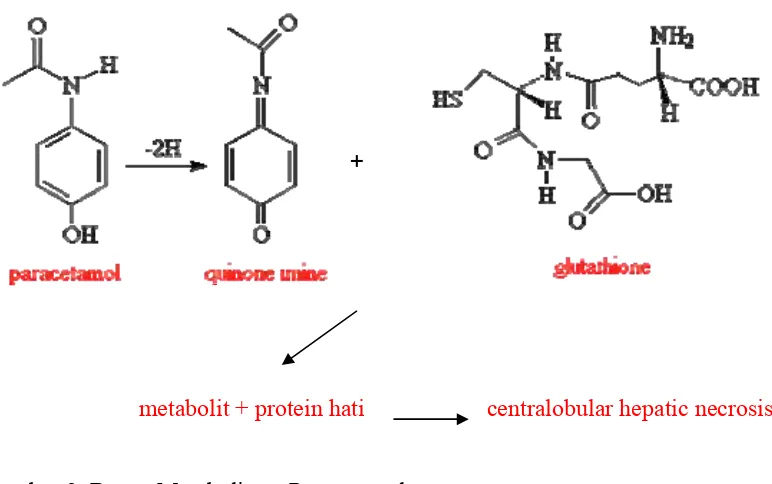
kemudian dapat menimbulkan nekrosis hati (Susana 1987). Metabolisme
parasetamol dapat dilihat pada Gambar 3.
+
[image:33.595.122.508.426.668.2]metabolit + protein hati centralobular hepatic necrosis
14
Toksikologi
Hasil penelitian Katzung menunjukkan bahwa penggunaan parasetamol
dalam dosis yang besar dapat menyebabkan gangguan fungsi hati yang disebut
nekrosis hati (Susana 1987). Dosis parasetamol sebanyak 7 g/hari atau lebih dapat
menimbulkan nekrosis hati sedangkan dosis 15 g/hari dapat menimbulkan
kerusakan hati yang lebih luas (Lelo dan Arbie 1982). Hasil penelitian oleh
Silvana menunjukkan mencit yang diberi parasetamol dengan dosis 500 mg/kg
BB menunjukkan kerusakan hati mencit tersebut (Susana 1987).
Kerusakan hati menyebabkan meningkatnya lipid peroksida darah karena
lipid peroksida tubuh tidak dapat lagi didetoksifikasi dalam hati. Menurut Thomas
dalam Susana 1987, hati memiliki mekanisme antioksidasi radikal bebas
(asetilimin benzokuinon) melalui reaksi konjugasi dengan beberapa senyawa
dalam hati seperti glutation, asam glukoronat, glisin dan asetat. Jumlah radikal
bebas yang melebihi ketersediaan senyawa-senyawa penetralisir dalam hati
memungkinkan terjadinya reaksi antara radikal bebas dan membran sel hati
(Susana 1987).
Parasetamol akan dikonversikan menjadi inaktif melalui metabolisme fase
II yang dikonjugasikan dengan sulfat dan glukuronida, yang akan beroksidasi
dalam jumlah kecil melalui sistem enzim sitokrom P450. Sitokrom P450 2E1
(CYP2E1) akan mengkonversikan parasetamol menjadi metabolit reaktif yang
tinggi, N-acetyl-p-benzo-quinone imine (NAPQI). Dalam kondisi dibawah normal,
NAPQI akan detoksifikasi oleh konjugasi dengan glutation. Pada kasus toksikasi
parasetamol, jalur sulfat dan glukuronida menjadi terurai sehingga parasetamol
merangsang sistem sitokrom P450 memproduksi NAPQI yang banyak.
Konsekuensinya NAPQI yang dikonjugasi oleh glutation (GSH) bertambah
banyak sedangkan hepatoseluler kekurangan glutation sehingga ketika melewati
kapasitas konjugasi GSH, NAPQI akan berikatan kovalen dengan makromolekul
vital sel hati (seperti lipid dan protein membran sel) dan menyebabkan nekrosis
hati (Sumioka et al. 2004). Pada kasus-kasus hewan, 70% kekurangan glutation
pada sel hati dapat menyebabkan hepatotoksisitas.
Adanya kerusakan sel-sel parenkim hati atau permebialitas membran akan
-15
glutamiltransferase bebas keluar sel, sehingga enzim yang masuk ke pembuluh
darah melebihi keadaan normal dan kadarnya dalam darah meningkat. Selain itu
parasetamol juga dapat mengalami hidroksilasi dan hasilnya dapat menimbulkan
methemoglobinemia (Hb diubah menjadi met-Hb) dan Hemolisis eritrosit
BAHAN DAN METODE
Tempat dan Waktu
Penelitian ini dilaksanakan di Bagian Patologi, Departemen Klinik,
Reproduksi dan Patologi, Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
Penelitian dimulai pada bulan Februari sampai bulan Juli 2007.
Alat dan Bahan
A. Mencit (Mus musculus) yang digunakan dalam penelitian sebanyak 36 ekor,
berumur 2 bulan dan berkelamin jantan.
B. Pengambilan sampel dan pengawetan jaringan. Alat dan bahan yang
digunakan pada proses ini adalah mencit (Mus musculus), pisau, silet, skalpel,
pinset anatomis, pinset sirurgis, gunting besar, gunting kecil, tali, label, botol
wadah spesimen, alkohol 70% atau larutan fiksatif Buffered Neutral Formalin
(BNF 10%).
C. Proses pembuatan sediaan histopatologi. Bahan dan alat yang digunakan
adalah alkohol 70%, 80%, 90%, 95%, alkohol absolut, xylol, paraffin, bunsen,
inkubator, cetakan paraffin dan mikrotom.
D. Proses pewarnaan. Alat dan bahan yang digunakan adalah wadah dari gelas
untuk tempat pewarnaan (staining jar), Mayer hematoksilin eosin, air dingin,
alkohol absolut, alkohol 70%, 80%, 90%, 95%, 100%, aquadest serta xylol.
E. Mounting menggunakan Permount® dan cover glass.
Metode
A. Parasetamol
Dosis normal optimum parasetamol yang digunakan adalah 500 mg/
50kgBB berdasarkan dosis yang umum digunakan oleh manusia dewasa.
B. Perlakuan
Penelitian ini menggunakan 36 ekor mencit (Mus musculus) yang dibagi
dalam 2 kelompok besar. Satu kelompok mencit menerima pemberian
17
berdasarkan konversi bobot badan masing-masing mencit dan satu kelompok
kontrol negatif yang diberi aquadestilata. Berdasarkan waktu pengambilan
sampel, kedua kelompok besar tersebut kemudian masing-masing dibagi menjadi
6 kelompok kecil dan masing-masing kelompok kecil terdiri dari 3 ekor mencit.
Pada awal penelitian, mencit (Mus musculus) diadaptasikan selama 2 minggu
untuk menghindari stress dan untuk menyeragamkan pola hidup masing-masing
kelompok perlakuan. Pada masa adaptasi ini, mencit (Mus musculus) hanya diberi
pakan standar, air minum adlibitum, obat cacing yang mengandung pirantel
palmoate dosis 0,5 ml/kg BB peroral dan antibiotik (ampicillin) dosis 8 mg/kg
BB peroral. Pemberian parasetamol dilakukan peroral setiap hari selama 6
minggu. Mulai minggu pertama hingga minggu ke-6, 3 ekor mencit dari
masing-masing kelompok perlakuan di euthanasia menggunakan inhalasi eter over dosis,
kemudian hatinya diambil sebagai sampel dan difiksasi dalam larutan BNF 10%.
C. Pembuatan Preparat Histopatologis
Sampel hati mencit (Mus musculus) yang telah difiksasi dalam larutan
fiksatif BNF 10%, diproses melalui serangkaian tahapan antara lain proses
dehidrasi, clearing atau penjernihan, embedding atau penanaman jaringan dalam
paraffin, pemotongan dengan menggunakan mikrotom setebal 5 µm. Proses ini
dilanjutkan dengan proses pewarnaan HE (Hematoksilin Eosin) dan yang terakhir
adalah mounting atau penutupan dengan gelas penutupnya (Humason 1985).
Pembuatan, identifikasi dan pengamatan preparat dilakukan di Bagian Patologi,
Departemen Klinik, Reproduksi dan Patologi, Fakultas Kedokteran Hewan,
Institut Pertanian Bogor.
D. Parameter Pengamatan Histopatologi
Pada hati yang menjadi perhatian pada pengamatan histopatologi adalah
perubahan-perubahan yang terjadi pada sitoplasma dan inti dari hepatosit,
sinusoid dan pembuluh darah. Parameter pengamatan histopatologi dilakukan
pada sediaan hati dengan menghitung persentase hepatosit normal, degenerasi
hidropis dan kematian sel serta jumlah sel radang dalam satu lapang pandang
18
buah di sekitar vena sentralis dan 5 buah di sekitar vena porta, total 10 lokasi
lapang pandang.
E. Evaluasi Data
Evaluasi data dilakukan dengan membandingkan kondisi hati dari
kelompok perlakuan dan kontrol serta membandingkan kondisi hati pada daerah
di sekitar vena porta dan vena sentralis. Data yang diperoleh dianalisa
menggunakan analisis sidik ragam acak lengkap (ANOVA) dilanjutkan dengan uji
HASIL DAN PEMBAHASAN
Penelitian ini memberikan informasi dasar mengenai kerusakan hati yang
ditimbulkan akibat pemberian parasetamol dosis normal optimum. Berdasarkan
hasil pengamatan histopatologi hati mencit pada kelompok kontrol maupun
perlakuan ditemukan adanya perubahan pada interstitium dan parenkim. Pada
interstitium perubahan yang terlihat yaitu kongesti dan perluasan sinusoid
sedangkan pada parenkim ditemukan adanya degenerasi hidropis dan nekrosa.
Persentase berbagai perubahan pada parenkhim hepatosit selama perlakuan (6
[image:39.595.116.514.343.512.2]minggu) disajikan pada Tabel 1 dan Gambar 4.
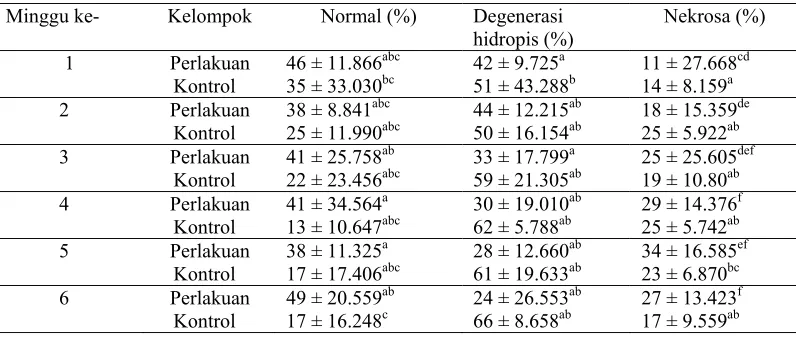
Tabel 1. Derajat keparahan lesio hepatosit mencit pada pemberian parasetamol dosis normal optimum dalam waktu 6 minggu.
Minggu ke- Kelompok Normal (%) Degenerasi hidropis (%)
Nekrosa (%)
1 Perlakuan 46 ± 11.866abc 42 ± 9.725a 11 ± 27.668cd Kontrol 35 ± 33.030bc 51 ± 43.288b 14 ± 8.159a 2 Perlakuan 38 ± 8.841abc 44 ± 12.215ab 18 ± 15.359de
Kontrol 25 ± 11.990abc 50 ± 16.154ab 25 ± 5.922ab 3 Perlakuan 41 ± 25.758ab 33 ± 17.799a 25 ± 25.605def
Kontrol 22 ± 23.456abc 59 ± 21.305ab 19 ± 10.80ab 4 Perlakuan 41 ± 34.564a 30 ± 19.010ab 29 ± 14.376f Kontrol 13 ± 10.647abc 62 ± 5.788ab 25 ± 5.742ab 5 Perlakuan 38 ± 11.325a 28 ± 12.660ab 34 ± 16.585ef
Kontrol 17 ± 17.406abc 61 ± 19.633ab 23 ± 6.870bc 6 Perlakuan 49 ± 20.559ab 24 ± 26.553ab 27 ± 13.423f Kontrol 17 ± 16.248c 66 ± 8.658ab 17 ± 9.559ab
20 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100%
%
ker
usakan hep
a
to
si
t
P K P K P K P K P K P K
I 2 3 4 5 6
Minggu
Gambar 4. Perbandingan perubahan persentase lesio hepatosit kelompok kontrol (K) dan perlakuan (P). Warna kuning menunjukkan nekrosa, warna merah menunjukkan degenerasi hidropis dan warna biru menunjukkan hepatosit normal.
Hasil analisis statistik persentase hepatosit normal minggu ke-1 sampai
minggu ke-5 pada kelompok perlakuan tidak berbeda nyata dibandingkan
kelompok kontrol (p>0,05). Pada pengamatan minggu ke-6, terlihat bahwa
persentase hepatosit normal kelompok perlakuan nyata lebih tinggi dibandingkan
kelompok kontrol (p<0,05). Hal ini membuktikan bahwa parasetamol dosis
normal optimum aman dikonsumsi dalam jangka waktu hingga 6 minggu.
Hasil analisis statistik persentase hepatosit minggu ke-1 yang mengalami
degenerasi hidropis pada kelompok perlakuan lebih rendah secara signifikan
(p<0,05) dibandingkan kelompok kontrol (Tabel 1, Gambar 4). Pada
minggu-minggu berikutnya, persentase hepatosit kelompok kontrol dan perlakuan yang
21
Peningkatan waktu pemberian parasetamol dosis normal optimum tidak diiringi
dengan peningkatan persentase hepatosit yang mengalami degenerasi hidropis.
Hal ini disebabkan sebagian hepatosit yang mengalami degenerasi hidropis
berubah kembali menjadi normal dan sebagian lagi menjadi nekrosa. Hepatosit
ini dapat kembali menjadi normal karena terkait dengan cara kerja parasetamol
sebagai analgesik dan antipiretik melalui mekanisme penghambatan enzim
cyclooxygenase (COX). Penghambatan terhadap enzim ini menyebabkan
berkurangnya produksi prostaglandin yang mengatur regulasi rasa nyeri dan
penurun panas (Goodman et al. 1980). Sedangkan peningkatan lesio hepatosit
menjadi nekrosa disebabkan adanya gangguan metabolisme sel dan akumulasi zat
toksik yang terus-menerus sehingga menyebabkan terbentuknya radikal bebas
N-asetil p-benzokuinon imin (NAPQI), suatu senyawa yang bersifat racun dan
reaktif. Senyawa radikal bebas ini akan mengoksidasi fosfolipid pada membran
sel hati dan menyebabkan terjadinya reaksi oksidasi berantai yang akhirnya dapat
merusak hepatosit (Goodman et al. 1980). Persentase hepatosit kelompok kontrol
yang mengalami degenerasi hidropis kemungkinan disebabkan adanya gangguan
metabolisme baik pada organ hati maupun pada organ lain yang tidak spesifik.
Hal ini mungkin saja terjadi karena mencit yang digunakan bukan mencit Specific
Pathogen Free (SPF).
Kondisi hepatosit minggu ke-1 dan minggu ke-2 pada kelompok perlakuan
cenderung lebih baik dibandingkan kelompok kontrol. Hal ini dikarenakan jumlah
sel hepatosit yang mengalami nekrosa pada kelompok perlakuan lebih rendah
secara signifikan (p<0,05) dibandingkan kelompok kontrol. Pada pengamatan
minggu ke-3, terlihat bahwa nekrosa nyata lebih tinggi (p<0,05) terjadi pada
kelompok perlakuan dibandingkan kelompok kontrol. Fenomena yang terjadi pada
minggu ke-3 terus berlangsung sampai minggu-minggu berikutnya. Semakin lama
waktu pemberian parasetamol dosis normal optimum maka semakin tinggi
persentase hepatosit yang mengalami kematian. Hal ini terjadi karena parasetamol
di dalam hati akan mengalami biotransformasi melalui reaksi konjugasi dengan
asam glukoronat atau glutation dan hasilnya diekskresi melalui urin. Sisa
parasetamol mengalami biotransformasi dengan sistem sitokrom P-450. Sitokrom
22
biotransformasi oksidatif pada 5-10% parasetamol yang masuk ke dalam tubuh.
Parasetamol yang teroksidasi berubah menjadi N-asetil p-benzokuinon imin
(NAPQI), suatu senyawa yang toksik dan reaktif (Susana 1987). Senyawa radikal
ini dapat bereaksi dengan molekul penyusun membran sel hati contohnya
fosfolipid. Oksidasi senyawa ini akan menghasilkan suatu radikal bebas yang
dapat mengoksidasi molekul fosfolipid lainnya sehingga terjadi reaksi oksidasi
berantai. Reaksi ini dapat menyebabkan berubahnya komposisi membran sel hati.
Menurut Manson, perubahan membran sel menyebabkan kerusakan sel hati dan
kemudian dapat menimbulkan nekrosis hati (Susana 1987).
Perubahan histopatologi tersebut dapat diamati pada seluruh bagian hati
baik di sekitar vena porta maupun vena sentralis. Persentase berbagai perubahan
hepatosit di sekitar vena porta dan vena sentralis disajikan pada Tabel 2 dan
[image:42.595.113.511.413.567.2]Gambar 5.
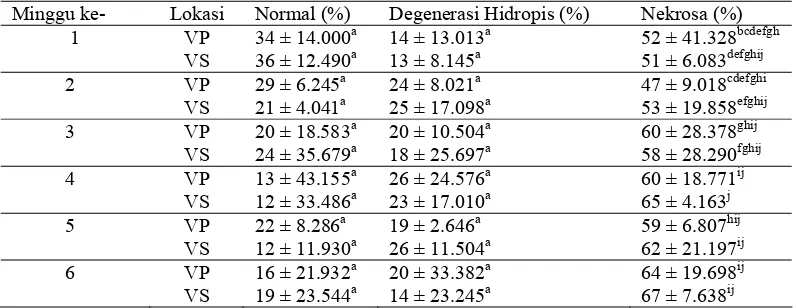
Tabel 2. Derajat keparahan perubahan hepatosit mencit pada vena porta (VP) dan vena sentralis (VS) akibat pemberian parasetamol dosis normal optimum.
Minggu ke- Lokasi Normal (%) Degenerasi Hidropis (%) Nekrosa (%) 1 VP 34 ± 14.000a 14 ± 13.013a 52 ± 41.328bcdefgh
VS 36 ± 12.490a 13 ± 8.145a 51 ± 6.083defghij
2 VP 29 ± 6.245a 24 ± 8.021a 47 ± 9.018cdefghi
VS 21 ± 4.041a 25 ± 17.098a 53 ± 19.858efghij
3 VP 20 ± 18.583a 20 ± 10.504a 60 ± 28.378ghij
VS 24 ± 35.679a 18 ± 25.697a 58 ± 28.290fghij
4 VP 13 ± 43.155a 26 ± 24.576a 60 ± 18.771ij
VS 12 ± 33.486a 23 ± 17.010a 65 ± 4.163j
5 VP 22 ± 8.286a 19 ± 2.646a 59 ± 6.807hij
VS 12 ± 11.930a 26 ± 11.504a 62 ± 21.197ij
6 VP 16 ± 21.932a 20 ± 33.382a 64 ± 19.698ij
VS 19 ± 23.544a 14 ± 23.245a 67 ± 7.638ij
23 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100% % ker usa kan hepa tosi t
VP VS VP VS VP VS VP VS VP VS VP VS
1 2 3 4 5 6
[image:43.595.141.492.89.343.2]Minggu
Gambar 5. Pengaruh pemberian parasetamol dosis normal optimum terhadap perubahan hepatosit mencit pada vena porta (VP) dan vena sentralis (VS). Warna kuning menunjukkan nekrosa, warna merah menunjukkan degenerasi hidropis dan warna biru menunjukkan hepatosit normal.
Hasil analisis statistik persentase hepatosit normal, hepatosit yang
mengalami degenerasi hidropis dan nekrosa pada seluruh kelompok perlakuan di
vena porta tidak berbeda nyata (p>0,05) dibandingkan di vena sentralis. Hal ini
membuktikan secara histopatologis bahwa kadar toksik parasetamol sebelum
dimetabolisme dan setelah dimetabolisme di dalam hati mempunyai tingkat
toksisitas yang sama terhadap sel.
Pada kasus masuknya zat toksik melalui saluran pencernaan, degenerasi
hidropis umumnya dimulai dari daerah pinggir/daerah portal yang meluas menuju
vena sentralis. Hal ini disebabkan karena suplai darah hati diperoleh dari saluran
pencernaan. Darah yang mengandung toksin dibawa dari usus, masuk ke hati
melalui vena porta kemudian melewati sinusoid menuju vena sentralis
(MacFarlane et al. 2000). Hepatosit perilobuler merupakan hepatosit paling awal
24
hepatosit ini yang pertama kali kontak dengan zat-zat toksin dari usus (Harada et
al. 1999).
Degenerasi hidropis merupakan perubahan yang bersifat sementara
(reversible), ditandai dengan kehadiran vakuol-vakuol di sitoplasma, sehingga
apabila paparan bahan toksik dihentikan sel yang mengalami kerusakan akan
kembali normal. Sel membutuhkan ATP-ase untuk mengaktifkan pompa
sodium-potasium dalam pengaturan keluar dan masuknya ion. Infeksi akut sel akan
menyebabkan air dan protein tetap berada dalam sitoplasma. Pompa lapisan
membran akan memindahkan ion dan air dengan cepat keluar dari sitosol dan
masuk ke dalam retikulum endoplasma. Hal ini akan menyebabkan kebengkakan
sel yang disebut degenerasi hidropis (Cheville 1999). Perubahan sel pada tahap ini
merupakan respon adaptasi agar sel tetap bertahan hidup.
Kerusakan sel hati akan menginduksi kenaikan konsentrasi lipid peroksida
darah mencit. Pada level tertentu jika jumlah sel hati yang rusak terlalu tinggi
maka kerusakan sel akan bersifat permanen dan akhirnya terjadi kematian sel
(apoptosis dan nekrosa). Artinya, apabila hepatosit sudah mengalami kerusakan
maka tidak akan diganti oleh hepatosit yang baru, tetapi sebagai gantinya akan
terbentuk jaringan ikat. Apoptosis dapat terjadi pada proses normal (fisiologis)
atau abnormal (patologis). Nekrosa dapat terjadi akibat bahan beracun, aktivitas
mikroorganisme, defisiensi pakan dan kadang-kadang gangguan metabolisme
termasuk hipoksia. Kematian sel secara apoptosis mencakup proses destruksi
seluler aktif yang ditandai dengan penyusutan jumlah sel, kerusakan membran dan
fragmentasi DNA inti. Nekrosis merupakan kematian sel atau kelompok sel yang
masih merupakan bagian dari organisme hidup dengan penyebab yang bervariasi.
Umumnya, hepatosit yang mengalami nekrosis menunjukkan perubahan pada inti
dan sitoplasma. Inti akan mengecil dan berwarna biru (lebih gelap), mirip sel
limfosit, akibat penggumpalan kromatin inti. Proses ini disebut piknosis. Inti juga
mungkin pecah (karyorhexis) dan bahkan menghilang (karyolisis), sedangkan
pada sitoplasma akan terlihat lebih asidofilik (Jubb et al. 1993). Gambaran
25
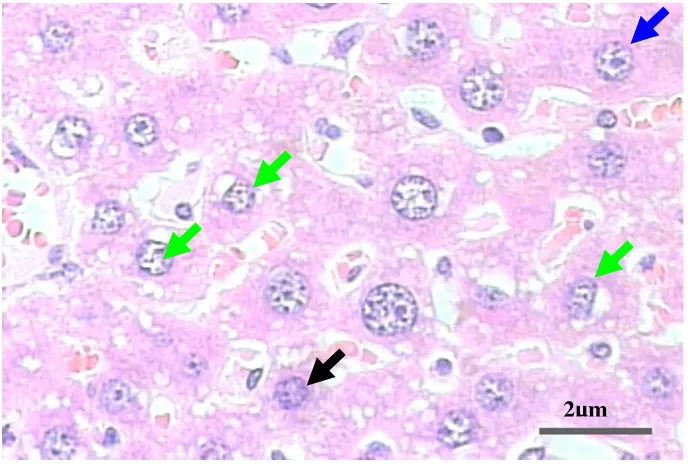
[image:45.595.144.482.85.304.2]2µm
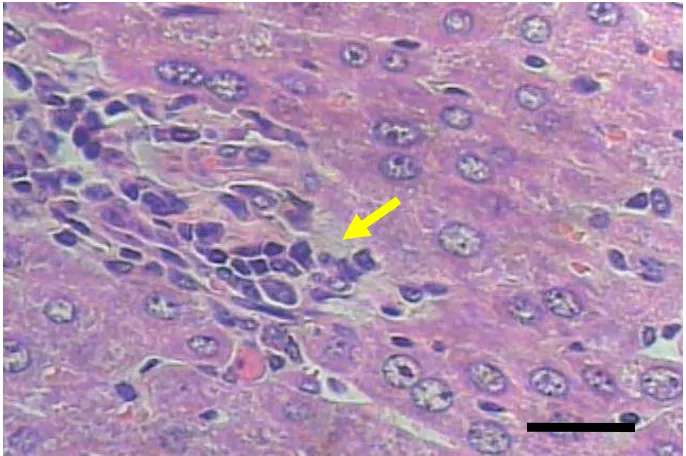
Gambar 6a. Gambaran histopatologi jaringan hati kelompok kontrol. Lesio hepatosit berupa degenerasi hidropis (panah hijau), nekrosa (panah hitam) dan hepatosit normal (panah biru). Pewarnaan HE. Perbesaran 40X.
2µm
Gambar 6b. Gambaran histopatologi jaringan hati kelompok perlakuan. Lesio hepatosit berupa degenerasi hidropis (panah hijau), nekrosa (panah hitam) dan hepatosit normal (panah biru). Pewarnaan HE. Perbesaran 40X.
Pada kelompok perlakuan, sel-sel hati tidak mampu mencegah reaksi
oksidasi yang dilakukan oleh radikal bebas asetilimin benzokuinon. Proses
[image:45.595.140.484.386.620.2]26
tubuh yang jumlahnya lebih sedikit daripada jumlah radikal bebas yang terbentuk.
Hal ini menyebabkan kelompok mencit yang diberi parasetamol mengalami
gangguan fungsi hati oleh radikal bebas parasetamol. Enzim dalam hati yang
digunakan sebagai petunjuk adanya kerusakan hati setelah pemberian parasetamol
adalah kadar enzim alanin aminotransferase (ALT) dan aspartat aminotransferase
(AST) yang meningkat (Anonimus 2006). Pada penelitian ini hewan coba yang
digunakan adalah mencit yang memiliki jumlah volume darah sedikit sehingga
tidak dilakukan penghitungan terhadap kadar enzim ALT dan AST dalam darah.
Selain perubahan pada jaringan parenkim hati, perubahan juga terjadi pada
bagian interstitiumnya yaitu ditemukannya kongesti dan perluasan sinusoid
(Gambar 7) dengan derajat yang sama disetiap kelompok perlakuan. Menurut
Abrams (1992), kongesti adalah keadaan dimana terdapat darah secara berlebihan
di dalam pembuluh darah pada daerah tertentu. Akibat dari kongesti maka
sirkulasi darah menjadi lambat sehingga oksigenasi ke jaringan menurun. Sel hati
sangat peka terhadap kekurangan oksigen atau anoksia. Adanya kongesti
menyebabkan terganggunya fungsi hati sebagai tempat metabolisme protein dan
lemak. Pada kongesti akut, hati membengkak dan terisi darah sedangkan pada
kongesti yang berjalan kronik menimbulkan penggenangan eritrosit di vena
sentralis dan di sinusoid-sinusoid sekitarnya. Apabila terjadi kongesti kronik maka
sinusoid yang melebar akan menggencet deretan sel hati (hepatosit) sekitar vena
sentralis sehingga hepatosit mengalami atrofi (mengecil). Adanya kongesti dan
perluasan sinusoid, mungkin terjadi akibat pembiusan dengan eter sebelum mencit
dimatikan. Perubahan ini terjadi pada semua kelompok kontrol dan perlakuan,
sehingga tidak dijadikan parameter dalam perubahan mikroskopis akibat
pemberian parasetamol. Menurut Ganiswara (1995), eter merupakan anastetik
yang sangat kuat, dapat menekan kontraktilitas otot jantung, menyebabkan dilatasi
27
Gambar 7. Perubahan pada bagian interstitium hati berupa kongesti (panah kuning). Pewarnaan HE.
Perubahan lain yang ditemukan adalah adanya infiltrasi sel radang limfosit
dan makrofag sehingga membentuk fokus-fokus peradangan di sekitar vena
sentralis maupun vena porta di seluruh jaringan hati (Gambar 8).
[image:47.595.139.482.457.685.2]28
Fokus-fokus peradangan tersebut terdiri dari berbagai ukuran dengan
jumlah sel limfosit dan makrofag yang bervariasi. Hasil rataan jumlah sel radang
yang diberi parasetamol dosis normal optimum dan kontrol dapat dilihat pada
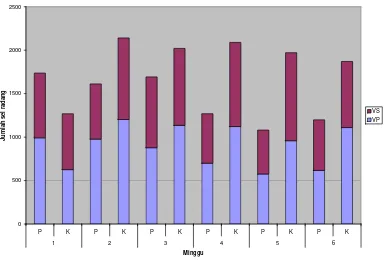
Tabel 3 dan Gambar 9.
0 500 1000 1500 2000 2500
P K P K P K P K P K P K
1 2 3 4 5 6
Minggu
J
u
ml
ah se
l r
a
da
ng
[image:48.595.123.509.214.474.2]VS VP
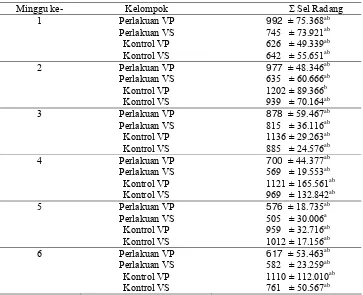
29
Tabel 3. Pengaruh pemberian parasetamol dosis normal optimum terhadap jumlah sel radang pada vena porta (VP) dan vena sentralis (VS).
Minggu ke- Kelompok Σ Sel Radang
1 Perlakuan VP 992 ± 75.368ab
Perlakuan VS 745 ± 73.921ab
Kontrol VP 626 ± 49.339ab
Kontrol VS 642 ± 55.651ab
2 Perlakuan VP 977 ± 48.346ab
Perlakuan VS 635 ± 60.666ab
Kontrol VP 1202 ± 89.366b
Kontrol VS 939 ± 70.164ab
3 Perlakuan VP 878 ± 59.467ab
Perlakuan VS 815 ± 36.116ab
Kontrol VP 1136 ± 29.263ab
Kontrol VS 885 ± 24.576ab
4 Perlakuan VP 700 ± 44.377ab
Perlakuan VS 569 ± 19.553ab
Kontrol VP 1121 ± 165.561ab
Kontrol VS 969 ± 132.842ab
5 Perlakuan VP 576 ± 18.735ab
Perlakuan VS 505 ± 30.006a
Kontrol VP 959 ± 32.716ab
Kontrol VS 1012 ± 17.156ab
6 Perlakuan VP 617 ± 53.463ab
Perlakuan VS 582 ± 23.259ab
Kontrol VP 1110 ± 112.010ab
Kontrol VS 761 ± 50.567ab
Keterangan: Superskrip yang berbeda pada kolom yang sama menunjukkan berbeda nyata (P<0,05)
Hasil analisis statistik jumlah sel radang seluruh kelompok perlakuan tidak
berbeda nyata (p>0,05) dibandingkan kelompok kontrol pada tiap minggunya.
Keadaan ini mengindikasikan bahwa fungsi parasetamol sebagai antiinflamasi
kurang signifikan. Hal tersebut sesuai dengan Goodman et al. (1980), aktivitas
antiinflamasi parasetamol sangat rendah sehingga jarang digunakan untuk terapi
klinik.
Infiltrasi sel radang limfosit dan makrofag hampir terjadi di seluruh
perlakuan, termasuk kontrol. Hal ini dikarenakan migrasi sel radang merupakan
reaksi tanggap kebal umum terhadap zat toksik yang masuk ke dalam tubuh dan
merupakan reaksi patofisiologis untuk melawan segala bentuk agen yang
merugikan. Limfosit sering menyebar dalam jaringan dan berfungsi untuk
memelihara ketahanan tubuh. Limfosit terlihat sebagai sel-sel kecil dengan inti
bulat, menyerap warna haematoksilin dan memiliki sitoplasma tipis bersifat
basofil lemah. Sel limfosit sering ditemukan pada peradangan kronis yang
30
dengan sitoplasma yang jelas dan ditengahnya terlihat nukleus yang
kebulat-bulatan, berbentuk kacang atau melekuk. Makrofag berperan dalam fagositosis
dan penghancuran partikel asing serta mengolah bahan asing sehingga dapat
membangkitkan tanggap kebal. Sel lain yang juga ditemukan adalah sel kupffer
yang berperan dalam membentuk pertahanan makrofag-monosit yang berfungsi
mengeluarkan eritrosit dan runtuhan jaringan (debris) lainnya dalam peredaran
darah, serta bersifat fagositik terhadap benda asing (Harold 1971).
Hati berperan dalam proses detoksifikasi dan ekskresi bahan xenobiotic
(zat-zat toksik) namun dalam jumlah yang terbatas. Bila dosis zat toksik melebihi
batas kemampuan detoksifikasi, maka akan timbul berbagai gangguan misalnya
lipidosis, nekrosa dan fibrosis.
Pemberian parasetamol dosis 500 mg/ 50kgBB selama 6 minggu, dapat
menurunkan persentase degenerasi hepatosit pada mencit karena sebagian
hepatosit yang mengalami degenerasi hidropis berubah kembali menjadi normal,
hal ini terkait cara kerja parasetamol sebagai analgesik dan antipiretik. Sedangkan
sebagian lagi menjadi nekrosa akibat adanya gangguan metabolisme sel dan
akumulasi zat toksik yang terus-menerus sehingga menyebabkan terbentuknya
radikal bebas N-asetil p-benzokuinon imin (NAPQI) yang akan mengoksidasi
fosfolipid pada membran sel hati dan menyebabkan terjadinya reaksi oksidasi
berantai yang akhirnya dapat merusak hepatosit. Berdasarkan hasil analisis
statistik persentase hepatosit normal, hepatosit yang mengalami degenerasi
hidropis dan nekrosa serta jumlah sel radang pada seluruh kelompok perlakuan di
vena porta tidak berbeda nyata (p>0,05) dibandingkan di vena sentralis pada tiap
minggunya. Hal ini membuktikan bahwa toksisitas parasetamol sebelum
dimetabolisme dan setelah dimetabolisme di dalam hati mempunyai tingkat
toksisitas yang sama terhadap sel hati. Jumlah sel radang di sekitar vena porta dan
vena sentralis tidak berbeda nyata, merupakan bukti bahwa indikasi parasetamol
sebagai antiinflamasi kurang signifikan, tidak cukup digunakan untuk
KESIMPULAN DAN SARAN
Kesimpulan
Sejalan dengan pertambahan waktu hingga 6 minggu, parasetamol dosis
normal optimum adalah (500 mg/ 50kgBB) menyebabkan terjadinya peningkatan
lesio kematian hepatosit berupa nekrosa sementara lesio degeneratif menurun.
Saran
1. Perlu dilakukan penelitian lebih lanjut dengan dosis bertingkat dan dengan
waktu pemberian yang lebih lama untuk mengetahui batas optimum
penggunaan parasetamol yang menyebabkan kerusakan hati.
2. Perlu digunakan hewan coba jenis lain agar dapat diperiksa enzim-enzim yang
DAFTAR PUSTAKA
Abrams GD. 1992. Gangguan Sirkulasi, dalam Price, SA dan LM. Wilson.
Patofisiologi Konsep Klinis Proses-proses Penyakit. Terjemahan. Anugerah, P. Penerbit Buku Kedokteran EGC. Jakarta. pp: 92-93.
Anonimus. 2006. Parasetamol. http://en.wikipedi.org/wiki/Paracetamol. [6
Agustus 2006].
Ballenger L. 1999. Mus musculus (house mouse). http://www.animaldiversity
umm2.umich.edu/sitc/account/information/Mus musculus.htm. [18 Maret
2006].
Budi IM, Paimin FR. 2005. Buah Merah. Jakarta: Penebar Swadaya. Hlm 7-8, 22, 41-50.
Burkitt HG, Osweiler GD. 1995. Clinical and Diagnostic Veterinary Toxicology. Edisi ke-2. Kendal/Hunt Publishing Company. Pp. 333-334.
Carlton WW, McGavin MD. 1995. Thomson’s Special Veterinary Pathology. Edisi ke-2. Mosby: St. louis. Pp. 209-245.
Cheville NF. 1999. Introduction to Veterinary Pathology. Ed ke-2. Iowa: Iowa State University Press. Hlm 5-25.
Dalimartha S. 2005. Ramuan Tradisional untuk Pengobatan Hepatitis. Jakarta: Penebar Swadaya. Hlm 33.
Donatus IA. 2001. Toksikologi Dasar. Yokyakarta: Universitas Gadjah Mada. Hlm 89.
Ganiswara SG. 1995. Farmakologi dan Terapi. Ed ke-4. Jakarta: Farmakologi Fakultas Kedokteran, Universitas Indonesia. Jakarta. pp: 116.
Ganong WF. 2003. Buku Ajar Fisiologi Kedokteran. Terjemahan dari: Review of Medical Physiology. Penerjemah: Widjajakusumah D; Editor Widjajakusumah D. San Fransisco: University of California. Hlm 486.
Goodman LS, Gilman A, Gilman AG. 1980. The Pharmacological Basic of Therapeutic Sixth Ed. New York: Macmillan co. inc. Pp. 682-723.
Guyton CA, John EH. 1997. Fisiologi Kedokteran. Penerjemah: Suryawan, Irawati. Ed-9. Jakarta: Penerbit Buku Kedokteran EGC. Hlm 1028,1030,1105-1108.
33
Harada T, Enotomo A, Boorman G and Maronpot RR. Liver and Gallbladder. In: Maronpot RR. 1999. Pathology of The Mouse. Reference and Atlas. 1st ed. Cache River Press. Hlm 120-171.
Harold AB. 1971. Pathology and Introduction. San Fransisco. Hlm 49.
Hartono. 1992. Histologi Veteriner. Organologi. Bogor: Laboratorium Histologi Jurusan Anatomi Fakultas Kedokteran Hewan Institut Pertanian Bogor. Hlm 90.
Humason GL. 1985. Animal Tissue Techniques. 4rd ed. San Francisco: W.N. Freeman and Company, USA. Pp. 1-169.
Jubb KVF, Kennedy PC and Peter C. 1993. Pathology of Domestic Animal. London: Academic Press. Hlm 325-346.
Lelo A, Arbie R. 1982. Hepatotoksisitas parasetamol. Majalah Dokter Keluarga
2(1) : 24-27.
Lu FC. 1995. Toksikologi Dasar. Edisi ke-2. Jakarta: Universitas Indonesia Press. Pp. 206-223.
Macfarlane PS, Reid R and Callander. 2000. Pathology Illustrated. Toronto: Huerchill Livingstone.
Mangkoewidjojo S, Smith JB. 1998. Pemeliharaan, Pembiakan dan Penggunaan Hewan Percobaan di Daerah Tropis. UI Press. Jakarta. Hlm 10-12.
Nabib R. 1987. Patologi Khusus Veteriner. Edisi ke-2. Bogor: Laboratorium Patologi Jurusan Parasitologi dan Patologi Fakultas Kedokteran Veteriner Institut Pertanian Bogor. Hlm 115-117.
Ressang AA. 1984. Patologi Khusus Veteriner. Edisi ke-2. Denpasar: Percetakan Bali. Hlm 45-81.
Ruswandi D. 2005. Penghambatan peroksida lipid oleh ekstrak buah mahkota dewa (Phaleria macrocarpa) pada gangguan fungsi hati tikus akibat parasetamol [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Al