LAMPIRAN
Lampiran 1 Bagan alir pembuatan ekstrak cacing tanah (Peryonix sp.)
- Dicuci bersih
- Ditimbang (Sebagai berat basah)
- Dikeringkan pada suhu ± 50oC
- Dihaluskan dengan menggunakan blender
- Ditimbang
- Dimaserasi dengan 5 L etanol - Disaring
- Dipekatkan dengan rotary evaporator pada suhu ± 55oC Cacing Tanah (Peryonix
Cacing Tanah (Peryonix sp)
Simplisia Kering 600 gram
Maserat 5 L
Lampiran 2 Bagan alir pembuatan sediaan salep ekstrak etanol cacing tanah (Peryonix sp.)
Dibuat ke dalam salep 3 konsentrasi ekstrak masing-masing 50 gram
Ekstrak Kental 350 gram
F I ( Konsentrasi ekstrak 30 % )
F III ( Konsentrasi ekstrak 50 % )
F II ( Konsentrasi ekstrak 40 % )
25 gram ekstrak 25 gram dasar salep 20 gram ekstrak
30 gram dasar salep 15 gram ekstrak
35 gram dasar salep
Evaluasi Sediaan : ‐ Uji homogenitas ‐ Uji kestabilan fisik ‐ Uji antibakteri terhadap
Staphylococcus aureus Sediaan Salep Ekstrak
Lampiran 3 Bagan uji aktivitas antibakteri ekstrak etanol cacing tanah (Peryonix sp.)
Biakan murni bakteri
Bakteri S.aureus hasil peremajaan
Inokulum bakteri S.aureus
Media NA mengandung bakteri
Media yang telah diletakkan pencadang kertas
Diambil 1 ose, kemudian diremajakan dalam media NA miring diinkubasi selam 24 jam
Hasil Inkubasi
Hasil dan Diameter Hambat
Diambil 1-2 ose dimasukkan kedalam 10 media NB, diukur dengan spektrofotometer visilel pada
panjang gelombang 580 nm hingga diperoleh % Transmitannya sebesar 25-30%
Peremajaan dilakukan minimal 3 kali
Diambil 0,1 ml dimasukkan ke dalam petri steril lalu ditambahkan media NA cair
Diratakan dengan cara memutar petri membentuk angka 8 hingga media menjadi padat Diletakkan pencadang kertas yang sudah mengandung larutan uji ke atas permukaan media
Diinkubasi pada suhu 370C selam 18-24 jam
Lampiran 5 Gambar cacing tanah (Peryonix sp.) dan simplisia cacing tanah (Peryonix sp.)
a
b
Keterangan: a. Gambar cacing tanah (Peryonix sp.)
Lampiran 6 Gambar alat rotary evaporator c.
Lampiran 7 Gambar hasil uji homogenitas
30% 40%
Lampiran 8 Gambar sediaan salep ekstrak etanol cacing tanah (Peryonix sp.)
a.
b.
Keterangan: a. Gambar sediaan salep ekstrak cacing tanah (Peryonix sp.) pada hari ke-0
b. Gambar sediaan salep ekstrak cacing tanah (Peryonix sp.) pada hari ke-60
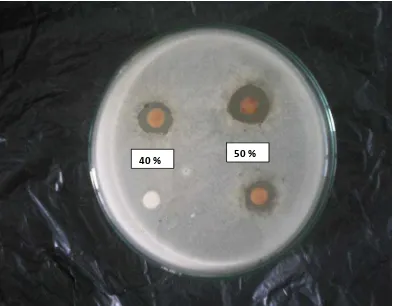
Lampiran 9 Gambar hasil uji aktivitas antibakteri ekstrak etanol cacing tanah (Peryonix sp.) terhadap bakteri Staphylococcus aureus menggunakan pencadang logam.
40 % 50 %
Lampiran 10 Gambar hasil uji aktivitas antibakteri ekstrak etanol cacing tanah (Peryonix sp.) terhadap bakteri Staphylococcus aureus menggunakan pencadang kertas
40 % 50 %
Blanko
Lampiran 11 Gambar hasil uji aktivitas antibakteri sediaan salep ekstrak etanol cacing tanah (Peryonix sp.) terhadap bakteri Staphylococcus aureus menggunakan pencadang kertas.
DAFTAR PUSTAKA
Anief, M. (1986). Ilmu Farmasi. Cetakan Kedua. Jakarta: Ghalia Indonesia. Halaman 61.
Anief, M. (1999). Ilmu Meracik Obat Teori dan Praktik. Cetakan VII. Yogyakarta: Gadjah Mada University Press. Halaman 168-169.
Anief. (2007). Farmasetika. Jakarta: UGM Press. Halaman 59.
Ansel, H.J. (1989). Pengantar Bentuk Sediaan Farmasi. Edisi 4. Terjemahan Farida Ibrahim. Jakarta: UI Press. Halaman 390.
Arlen, H.J. (1994). Cacing Tanah pada Timbunan Sampah Rumah Tangga di Beberapa Kecamatan Kotamadya Medan. Tesis. Program Studi Biologi FMIPA USU Medan.
Arlen, H.J. (1997). Cacing Tanah Sebagai Sumber Daya Alam Hayati yang Bernilai Ekonomis. Medan: Program Studi Biologi FMIPA USU.
Arlen, H.J., dan Erni. (2000). Aktivitas Amilase, Lipase, dan Protease dari Cacing Peryonix excavates. Jurnal Molekul. 4(2): 115.
Ciptanto dan Ulfah. (2011). Mendulang Emas Hitam Melalui Budidaya Cacing Tanah. Yogyakarta: Penerbit Lily Publisher. Halaman 12-18.
DIFCO. (1977). Manual of Dehydrated Culture Media and Reagents for Microbiology and Clinical Laboratory Procedures. Ninth Edition. Detroit Michigan: Difco Laboratories Incorporated. Halaman 32-33.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Depkes RI. Halaman 9.
Ditjen POM. (1985). Formularium Kosmetika Indonesia. Jakarta: Departemen Kesehatan RI. Halaman 32-36.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Depkes RI. Halaman 855, 891-898, 1033.
Ditjen POM. (1978). Formularium Nasional. Edisi Kedua. Jakarta: Depkes RI. Halaman 66.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Depkes. Halaman 10-11.
Djide dan Sartini. (2008). Dasar-Dasar Mikrobiologi Farmasi. Makasar: Lephas, Halaman 81.
Dwidjoseputro, D. (1994). Dasar-Dasar Mikrobiologi. Jakarta: Djambatan. Halaman 102-105.
Fardiaz, S. (1992). Mikrobiologi Pangan 1. Jakarta: PT. Gramedia Pustaka Utama. Halaman 15, 143-146, 163.
Harris, L.G., Foster, S.J., dan Richard, R.G. (2002). An Introduction to Staphylococcus aureus, and Techniques for Identifying and Quantifying S. aureus Adhesins in Relation Adhesion To Biomaterials: Review journal. European Cells and Materials. 4: 39-60.
Huteri. (2010). Hewan Menjijikkan Itu Bermanfaat, http://www.huteri. com/598/ hewan-menjijikkan-itu-bermanfaat.html. Diakses tanggal 14 April 2014.
Irianto, K. (2006). Mikrobiologi Menguak Dunia Mikroorganisme. Jilid I. Bandung: CV. Yrama Widya. Halaman 75, 85-87.
Jawetz, E., Menick, J.L., dan Adelberg, E.A. (2001). Mikrobiologi Kedokteran. Alih Bahasa: Eddy Mudihardi, Kuntaman, Eddy Bagus Wasito, Ni Made Mertaniasih, Setio Harsono, dan Lindawati Alimsardjono. Jakarta: Penerbit Salemba Medika. Halaman 317-318, 352, 360.
Khairuman dan Khairul A. (2010). Mengeruk Untung Dari Beternak Cacing. Jakarta: Agromedia Pustaka. Halaman 9-10.
Lay, B.W. (1996). Analisis Mikroba di Laboratorium. Jakarta: Penerbit Raja Grafindo Persada. Halaman 34, 42, 44, 70-72.
Pelczar, M.J., dan Chan, E.C.S. (1988). Elements of Microbiology. New York: McGraw-Hill Companies Inc. Terjemahan: Ratna Siri Hadioetomo, Teja Imas, Sutarmi Tjitrosomo dan Sri Lestari Angka. (1988). Dasar-Dasar Mikrobiologi. Jakarta: Penerbit UI-Press. Halaman 145.
Pratiwi, S.T. (2008). Mikrobiologi Farmasi. Jakarta: Penerbit Erlangga. Halaman 18, 111, 106, 188, 135.
Radji, M. (2011). Mikrobiologi. Jakarta: Buku Kedokteran ECG. Halaman 62-63. Sajuthi, D. (2003). Efek Antipiretik Ekstrak Cacing Tanah.
http://ulie-prasetyo.blogspot.com. Diakses tanggal 21 Juli 2014.
Suin, N.M. (1982). Cacing Tanah dari Biotop Hutan, Belukar, dan Kebun di Kawasan Gambung Jawa Barat. Bandung: ITB press. Halaman 34-35. Sumardi. (1998). Deteksi dan Karakterisasi Senyawa Antibiotik dari Ekstrak dan
Isolat Mikroba Dalam Tubuh Cacing Tanah Allolobophora rosea. Tesis. Bogor: Jurusan BiologiInstitut Pertanian Bogor.
Stanier, R.Y., Adelberg, E.A. dan Ingraham, J.L. (1982). Dunia Mikrobe I. Penerjemah: Agustin Wydia. Jakarta: Penerbit Bhratara Karya Aksara. Halaman 23-25.
Waluyo, L. (2010). Teknik Dasar Metode Mikrobiologi. Malang: UMM Press. Halaman 105, 130-133.
BAB III
METODE PENELITIAN
3.1 Metode Penelitian
Penelitian yang dilakukan bersifat eksperimental laboratorium secara in
vitro, dilakukan terhadap cacing tanah (Peryonix sp.) yang terdiri dari tahapan penyiapan bahan penelitian, determinasi bahan penelitian, pembuatan ekstrak
etanol cacing tanah, formulasi sediaan salep ekstrak etanol cacing tanah,
selanjutnya pengujian aktivitas antibakteri dengan metode difusi agar
menggunakan pencadang kertas.
3.2 Tempat dan Waktu
Penelitian dilakukan di Laboratorium Sistematika Hewan (Departemen
Biologi) FMIPA USU, Laboratorium Fitokimia USU, Laboratorium Teknologi
Sediaan Farmasi I USU, Laboratorium Mikrobiologi USU, dimulai bulan Januari
2014 sampai bulan April 2014.
3.3 Alat dan Bahan 3.3.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah neraca analitik,
spatula, batang pengaduk, blender, kertas perkamen, lumpang dan alu, rotary
evaporator, water bath, lemari pengering, autoklaf, inkubator, jangka sorong, jarum ose, kamera digital, laminar air flow cabinet, tabung reaksi, lemari
pendingin, pinset, pipet mikro, spektrofotometer visibel (Dynamica), dan alat-alat
3.3.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah cacing tanah,
etanol (Brataco), vaselin (Brataco), adeps lanae (Brataco), propilen glikol
(Brataco), nutrient agar (NA) (Oxoid), nutrient broth (NB) (Oxoid),
dimetilsulfoksida (DMSO), air suling.
3.4 Prosedur Kerja
3.4.1 Pengumpulan sampel
Pengumpulan sampel dilakukan secara purposif, yaitu tanpa
membandingkan dengan daerah lain. Sampel yang digunakan adalah cacing tanah
spesies Peryonix sp yang diperoleh dari Tempat Pembuangan Akhir (TPA) Jalan
Puluh Nibung Kelurahan Paya Pasir Kecamatan Medan Marelan.
3.4.2 Identifikasi sampel
Identifikasi cacing tanah dilakukan di Laboratorium Sistematika Hewan
Departemen Biologi FMIPA USU Medan.
3.4.3 Pengolahan sampel
Cacing tanah (Peryonix sp.) dibersihkan dari bahan organik asing dan
pengotor lain dengan cara mencucinya dengan air yang bersih, lalu ditiriskan dan
ditimbang, kemudian dikeringkan dalam lemari pengering menggunakan lampu
pijar 75 watt yang memiliki suhu sekitar 50oC, diambil suhu yang tidak terlalu
panas karena sebagian besar komponen cacing tanah merupakan protein yang
akan rusak bila dalam suhu yang tinggi. Setelah kering lalu dihaluskan dengan
menggunakan blender sehingga diperoleh simplisia cacing tanah dan siap untuk
3.4.4 Pembuatan ekstrak cacing tanah (Peryonix sp.)
Pembuatan ekstrak cacing tanah (Peryonix sp.) dilakukan secara maserasi
dengan menggunakan pelarut etanol.
Cara kerja:
Sebanyak 600 g serbuk simplisia cacing tanah (Peryonix sp.) dimaserasi
dengan pelarut etanol 96% dalam wadah tertutup rapat selama 5 hari terlindung
dari cahaya matahari sambil sering diaduk, kemudian disaring, sehingga
diperoleh maserat, pekerjaan maserasi diulangi seperti semula (Ditjen POM,
1979). Maserat diuapkan atau disuling menggunakan rotary evaporator dengan
tekanan rendah pada suhu tidak lebih dari 50oC hingga diperoleh ekstrak kental,
lalu ditimbang.
3.5 Pembuatan Formula Sediaan 3.5.1 Pembuatan salep
Formula salep diambil dari formula kloramfenikol salep dalam
Formularium Nasional halaman 66.
Formula salep:
Kloramfenikol 200 mg
Propilen glikol 1 g
Adeps lanae 1 g
Vaselin album ad 10 g
Propilen glikol pada dasar salep ini selain dapat mempermudah kelarutan
juga digunakan sebagai pembasah atau penurun sudut kontak sehingga seluruh
Cara pembuatan dasar salep menggunakan metode pencampuran dimana
komponen salep dicampur bersama sama sampai didapat massa sediaan yang
homogen
3.5.2 Komposisi sediaan
Sediaan dibuat ke dalam tiga konsentrasi dan satu blanko dimana masing
masing sediaan memiliki bobot 50 gram.
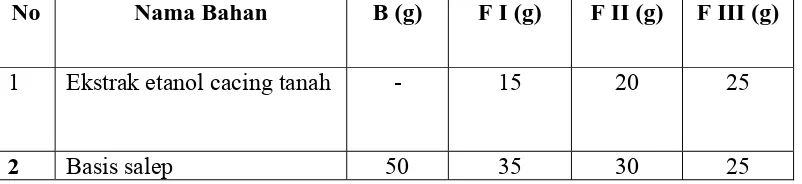
Tabel 3.1 Komposisi sediaan masing-masing formula
No Nama Bahan B (g) F I (g) F II (g) F III (g)
1 Ekstrak etanol cacing tanah - 15 20 25
2 Basis salep 50 35 30 25
Keterangan :
B : Formula tanpa mengandung ekstrak etanol cacing tanah
F I : Formula mengandung 30% ekstrak etanol cacing tanah
F II : Formula mengandung 40% ekstrak etanol cacing tanah
F III : Formula mengandung 50% ekstrak etanol cacing tanah
3.5.3 Cara pembuatan sediaan
a. Formula I
Cara pembuatan: ke dalam lumpang dimasukkan 15 g ekstrak etanol
cacing tanah lalu ditambahkan 35 g basis salep sedikit demi sedikit sambil digerus
sampai homogen.
b. Formula II
Cara pembuatan: ke dalam lumpang dimasukkan 20 g ekstrak etanol
cacing tanah lalu ditambahkan 30 g basis salep sedikit demi sedikit sambil digerus
c. Formula III
Cara pembuatan: ke dalam lumpang dimasukkan 25 g ekstrak etanol
cacing tanah lalu ditambahkan 25 g basis salep sedikit demi sedikit sambil
digerus sampai homogen.
3.6 Evaluasi Sediaan
Evaluasi formula meliputi evaluasi fisik dan biologi. Evaluasi fisik
meliputi pemeriksaan stabilitas sediaan, pemeriksaan homogenitas. Evaluasi
biologi meliputi penentuan aktivitas antibakteri sediaan salep ekstrak etanol
cacing tanah terhadap Staphylococcus aureus dengan metode difusi agar
menggunakan pencadang kertas.
3.6.1 Pemeriksaan stabilitas fisik sediaan
Sediaan dinyatakan stabil apabila warna, bau dan penampilan tidak
berubah secara visual selama penyimpanan dan juga secara visual tidak ditumbuhi
jamur. Pengamatan dilakukan pada suhu kamar pada hari ke 0, 30, dan hari ke-60.
3.6.2 Pemeriksaan homogenitas sediaan
Cara: sejumlah tertentu sediaan dioleskan pada sekeping kaca atau bahan
transparan lain yang cocok, sediaan harus menunjukkan susunan yang homogen
dan tidak terlihat adanya butiran kasar (Ditjen POM, 1979).
Pengamatan dilakukan pada suhu kamar pada hari ke 0, 30, dan hari ke-60.
3.7 Sterilisasi Alat
Alat-alat yang digunakan dalam uji aktivitas antibakteri ini disterilkan
lebih dahulu sebelum dipakai. Media disterilkan di autoklaf pada suhu 121oC
selama 15 menit dan alat-alat gelas lainnya disterilkan di oven pada suhu
3.8Pembuatan Media
3.8.1 Nutrient Agar (NA)
Komposisi : Bacto beef extract 3,0 g
Bacto peptone 5,0 g
Bacto agar 15,0 g
Air suling ad 1000 ml
Cara pembuatan:
Sebanyak 23 gram serbuk Nutrient Agar (NA) dilarutkan dalam air
suling steril sedikit demi sedikit kemudian volumenya dicukupkan hingga 1 liter
dengan bantuan pemanasan sampai semua bahan larut sempurna, kemudian
disterilkan di autoklaf pada suhu 121oC selama 15 menit (Difco Laboratories,
1977).
3.8.2 Nutrient Broth (NB)
Komposisi : Bacto beef extract 3,0 g
Bacto peptone 5,0 g
Air suling ad 1000 ml
Cara pembuatan:
Sebanyak 8 gram serbuk Nutrient Broth (NB) dilarutkan dalam air suling
steril sedikit demi sedikit kemudian volumenya dicukupkan hingga 1 liter dengan
bantuan pemanasan sampai semua bahan larut sempurna, kemudian disterilkan di
autoklaf pada suhu 121oC selama 15 menit (Difco Laboratories, 1977).
3.9 Pembuatan agar miring
Ke dalam tabung reaksi yang steril dimasukkan 3 ml media nutrient agar
miring membentuk sudut 45o, kemudian disimpan dalam lemari pendingin pada
suhu 5oC (Lay, 1996).
3.10Pembuatan Stok Kultur Bakteri
Satu koloni bakteri diambil dari biakan murni dengan menggunakan
jarum ose steril, lalu ditanam pada agar miring nutrient agar. Kemudian
diinkubasi dalam inkubator pada suhu 35 ± 2oC selama 18-24 jam (Lay, 1996).
3.11 Pembuatan Inokulum Bakteri Cara kerja:
Pengukuran jumlah inokulum bakteri dilakukan secara spektrofotometri,
diambil 1-2 ose stok kultur bakteri Staphylococcus aureus lalu dimasukkan ke
dalam tabung reaksi yang berisi 10 ml nutrient broth, diukur pada panjang
gelombang 580 nm diatur perbandingan hingga inokulum mempunyai transmittan
25% yang menyatakan bahwa telah diperoleh suspensi bakteri dengan konsentrasi
106 CFU/ml, sebagai blanko digunakan nutrient broth (Ditjen POM, 1995).
3.12 Pembuatan Larutan Uji Ekstrak Etanol Cacing Tanah dengan Berbagai Konsentrasi
Dibuat ke dalam 3 konsentrasi yaitu konsentrasi ekstrak 30%, 40%, dan
50%. Dipilih konsentrasi ini karena pada penelitian sebelumnya tiga konsentrasi
ini menghasilkan diameter daya hambat yang paling besar.
Pada penelitian sebelumnya pengujian dilakukan dengan menggunakan
pencadang logam yang menghasilkan daya hambat yang tidak terlalu besar, pada
penelitian ini dilihat perbedaan hasil antara pencadang kertas dan pencadang
logam.
Konsentrasi I (30 %): 0,3 gram ekstrak etanol cacing tanah dilarutkan ke dalam 1
Konsentrasi II (40%) : 0,4 gram ekstrak etanol cacing tanah dilarutkan ke dalam 1
ml pelarut DMSO etanol 1 : 1
Konsentrasi III (50%) : 0,5 gram ekstrak etanol cacing tanah dilarutkan ke dalam
1 ml pelarut DMSO etanol 1 : 1
3.13 Pengujian Aktivitas Antibakteri Ekstrak Etanol Cacing Tanah Terhadap Bakteri Staphylococcus aureus
Pengujian aktivitas antibakteri dilakukan terhadap ekstrak etanol cacing
tanah dengan berbagai konsentrasi. Pengujian ini dilakukan dengan metode difusi
agar menggunakan pencadang kertas.
Sebanyak 0,1 ml inokulum dimasukkan ke dalam cawan petri steril,
setelah itu dituang media nutrient agar sebanyak 20 ml dengan suhu 45-50oC,
selanjutnya cawan digoyang di atas permukaan meja agar media dan suspensi
bakteri tercampur rata. Pada media yang telah padat diletakkan beberapa
pencadang kertas, dipipet 0,1 ml larutan uji ekstrak etanol cacing tanah dengan
berbagai konsentrasi, kemudian diinkubasi dalam inkubator pada suhu 35 ± 2oC
selama 18-24 jam, lalu diukur diameter daerah hambatan (zona jernih)
pertumbuhan di sekitar pencadang dengan menggunakan jangka sorong.
3.14Pembuatan Larutan Uji Sediaan
Formula I : ditimbang salep ekstrak etanol cacing tanah 30% sebanyak 1 g lalu
dilarutkan dalam 1 ml pelarut DMSO etanol 1 : 1.
Formula II : ditimbang salep ekstrak etanol cacing tanah 40% sebanyak 1 g lalu
dilarutkan dalam 1 ml pelarut DMSO etanol 1 : 1.
Formula III : ditimbang salep ekstrak etanol cacing tanah 50% sebanyak 1 g lalu
3.15 Uji Aktivitas Antibakteri Salep Ekstrak Etanol Cacing Tanah (Peryonix sp.) Terhadap Bakteri Staphylococcus aureus
Uji mikrobiologi untuk mengetahui aktivitas antibakteri sediaan salep
ekstrak etanol cacing tanah yang dilakukan dengan metode difusi agar
menggunakan pencadang kertas dengan cara mengukur diameter hambatan
pertumbuhan bakteri terhadap bakteri Staphylococcus aureus.
Uji ini dilakukan menggunakan metode difusi agar menggunakan
pencadang kertas dengan media padat, penentuan efektivitas antibakteri dilakukan
dengan cara mengukur diameter daerah jernih di sekitar pencadang kertas
menggunakan jangka sorong.
Sebanyak 0,1 ml inokulum dimasukkan ke dalam cawan petri steril,
setelah itu dituang media nutrient agar sebanyak 20 ml dengan suhu 45 - 50oC,
selanjutnya cawan digoyang di atas permukaan meja agar media dan suspensi
bakteri tercampur rata. Pada media yang telah padat diletakkan beberapa
pencadang kertas, dipipet 0,1 ml salep ekstrak cacing tanah dimasukkan ke dalam
pencadang kertas, kemudian diinkubasi dalam inkubator pada suhu 35 ± 2oC
selama 18 - 24 jam, setelah itu diukur diameter daerah hambatan (zona jernih)
pertumbuhan di sekitar pencadang dengan menggunakan jangka sorong.
Sebagai kontrol pencadang kertas berisi basis salep yang dilarutkan dalam
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Sampel
Identifikasi cacing tanah di lakukan di Laboratorium Sistematika Hewan
Departemen Biologi FMIPA USU menyatakan bahwa cacing tanah yang
digunakan dalam penelitian ini adalah cacing tanah (Peryonix sp.). Hasil
identifikasi dapat dilihat di Lampiran 1.
4.2 Hasil Ekstraksi Cacing Tanah (Peryonix sp.)
Hasil penimbangan cacing tanah (Peryonix sp.) diperoleh sebanyak 8 kg,
setelah dikeringkan dihasilkan simplisia cacing tanah sebanyak 600 gram. Hasil
maserasi 600 gram simplisia cacing tanah dengan menggunakan pelarut etanol
96% sebanyak 5 liter dipekatkan dengan rotary evaporator dan ekstrak kental
yang didapat ditimbang, diperoleh ekstrak etanol kental 350 gram. Ekstrak kental
yang didapat lalu diformulasi menjadi sediaan salep dengan berbagai konsentrasi
dan kemudian diuji aktivitas antibakterinya terhadap bakteri Staphylococcus
aureus.
4.3Hasil Evaluasi Salep
4.3.1 Hasil uji homogenitas
Pengamatan homogenitas sediaan salep ekstrak etanol cacing tanah
dilakukan terhadap tiga formula: FI (Formula mengandung 30% ekstrak), FII
(Formula mengandung 40% ekstrak) dan FIII (Formula mengandung 50%
ekstrak) dilakukan dengan cara mengoleskan sejumlah tertentu sediaan pada
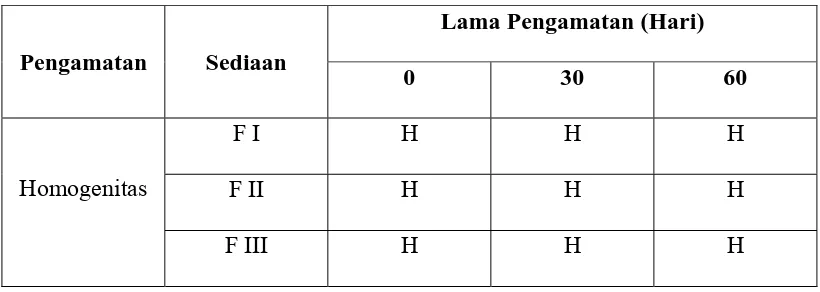
Tabel 4.1 Data pengamatan homogenitas sediaan
Hasil pemeriksaan homogenitas pada awal menunjukkan bahwa seluruh
sediaan salep tidak memperlihatkan adanya butir-butir kasar pada saat sediaan
dioleskan pada kaca transparan. Kemudian pada hari ke 30 sediaan msih
menunjukkan homogenitas yang baik terlihat tidak adanya butir-butir kasar pada
saat sediaan dioleskan pada kaca transparan. Begitupun pada hari ke 60 sediaan
masih menunjukkan homogenitas yang baik terlihat tidak adanya butir-butir kasar
pada saat sediaan dioleskan pada kaca transparan. Hal ini menunjukkan bahwa
sediaan yang dibuat mempunyai susunan yang homogen (Ditjen POM, 1979).
4.3.2 Hasil pemeriksaan stabilitas fisik sediaan
Hasil pemeriksaan stabilitas dilakukan terhadap sediaan salep ekstrak
etanol cacing tanah dilakukan pada tiga formula: FI (Formula mengandung 30%
ekstrak), FII (Formula mengandung 40% ekstrak) dan FIII (Formula mengandung
50% ekstrak) dengan melihat perubahan bentuk, warna dan bau sediaan.
Pemeriksaan dilakukan secara visual pada suhu kamar selama 60 hari dengan
rentang waktu pemeriksaan 30 hari. Sediaan salep yang terlihat baik terlihat dari
konsistensi salep yang baik, sediaan salep bewarna coklat kehitaman tanpa
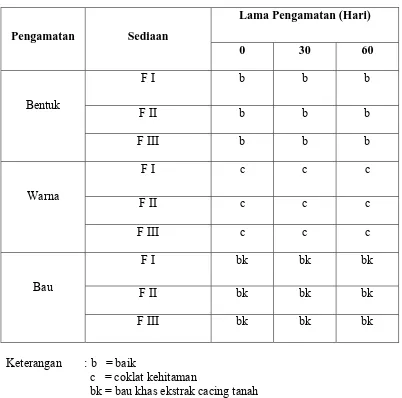
Tabel 4.2 Data pemeriksaan uji stabilitas fisik sediaan
Dari hasil uji stabilitas salep ekstrak etanol cacing tanah mempunyai
bentuk, warna dan bau sediaan yang stabil.
Suatu sediaan memiliki bentuk yang baik jika Selma proses penyimpanan
tidak terjadi bleeding yaitu terjadinya pemisahan antara basis salep dengan ekstrak
yang dapat terjadi karena basis salep dan ekstrak tidak tercampur sempurna.
Selain itu salep msih dapat dikatakan baik jika Selma penyimpanan bentuk,
warna, dan bau sediaan masih sama jika dibandingkan dengan awal salep dibuat.
Sediaan salep yang homogen mengindikasikan bahwa ketercampuran dari
didapati gumpalan ataupun butiran kasar pada sediaan. Suatu sediaan salep yang
dibuat harus homogen agar terdistribusi merata ketika digunakan.
4.4 Hasil Uji Mikrobiologi Ekstrak Etanol Cacing Tanah Terhadap Bakteri Staphylococcus aureus.
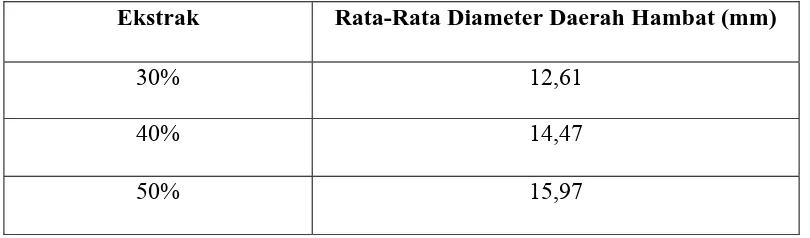
Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak etanol cacing
tanah dapat menghambat pertumbuhan bakteri Staphylococcus aureus. Semakin
tinggi konsentrasi ekstrak akan menghasilkan diameter daerah hambat yang
semakin besar. Pada konsentrasi 500 mg/ml memiliki daya hambat sebesar 15,97
mm, pada konsentrasi 400 mg/ml memiliki daya hambat sebesar 14,47 mm, pada
konsentrasi 300 mg/ml memiliki daya hambat sebesar 12,61 mm.
Hasil uji aktivitas antibakteri ekstrak etanol cacing tanah (Peyonix sp) terhadap
bakteri Staphylococcus aureus dapat dilihat dalam tabel 4.3 berikut
Tabel 4.3 Hasil uji aktivitas antibakteri ekstrak etanol cacing tanah terhadap bakteri Staphylococcus aureus menggunakan pencadang kertas.
Ekstrak Rata-Rata Diameter Daerah Hambat (mm)
30% 12,61
40% 14,47
50% 15,97
Metode yang digunakan pada pengujian ini adalah metode difusi agar
menggunakan pencadang kertas dengan mengukur diameter zona hambat
pertumbuhan bakteri, dimana diameter zona hambat akan meningkat dengan
adanya peningkatan konsentrasi ekstrak, sehingga antara peningkatan konsentrasi
ekstrak dengan peningkatan diameter zona hambat pertumbuhan bakteri
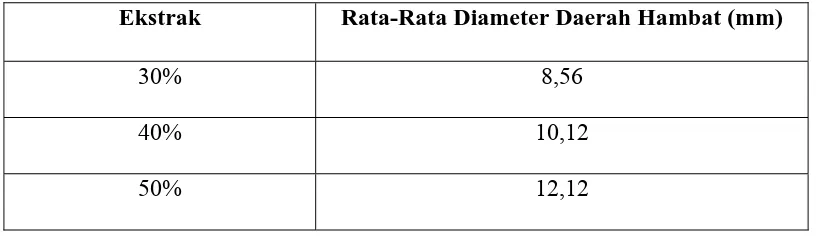
didapat ternyata pengaruh penggunaan jenis pencadang juga berpengaruh terhadap
hasil uji. Pencadang logam yang digunakan pada penelitian sebelumnya
menghasilkan daya hambat yang lebih kecil (konsentrasi 50% 13,87 mm)
daripada pencadang kertas karena pencadang logam mempengaruhi kecepatan
difusi ekstrak ke media agar.
Sebelum menngunakan pencadang kertas, peneliti juga mencoba
menggunakan pencadang logam untuk mengetahui pencadang mana yang
menghasilkan hasil yang labih baik.
Tabel 4.4 Hasil uji aktivitas antibakteri ekstrak etanol cacing tanah terhadap bakteri Staphylococcus aureus menggunakan pencadang logam.
Ekstrak Rata-Rata Diameter Daerah Hambat (mm)
30% 8,56
40% 10,12
50% 12,12
Menurut Ditjen POM (1995), suatu zat dikatakan memiliki daya hambat
yang memuaskan dengan diameter daerah hambatan lebih kurang 14 sampai 16
mm.
4.5 Hasil Uji Mikrobiologi Salep Ekstrak Etanol Cacing Tanah Terhadap Bakteri Staphylococcus aureus
Uji mikrobiologi sediaan salep ekstrak etanol cacing tanah dilakukan
terhadap tiga formula: F I (Formula mengandung 30% ekstrak), F II (Formula
mengandung 40% ekstrak) dan F III (Formula mengandung 50% ekstrak) dengan
metode difusi agar terhadap bakteri Staphylococcus aureus. Hasil dapat dilihat
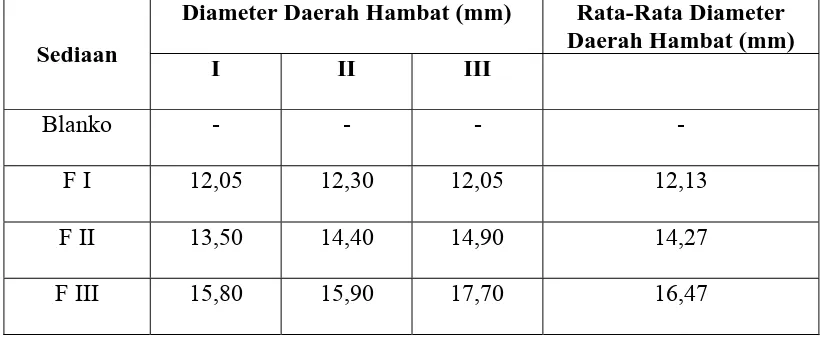
Tabel 4.5 Hasil uji aktivitas antibakteri salep ekstrak etanol cacing tanah terhadap bakteri Staphylococcus aureus.
Sediaan
Diameter Daerah Hambat (mm) Rata-Rata Diameter Daerah Hambat (mm)
B : Formula tanpa mengandung ekstrak etanol cacing tanah
F I : Formula mengandung 30% ekstrak etanol cacing tanah
F II : Formula mengandung 40% ekstrak etanol cacing tanah
F III : Formula mengandung 50% ekstrak etanol cacing tanah
Hasil uji aktivitas antimikroba dari salep ekstrak etanol cacing tanah
memiliki sedikit perbedaan dengan hasil uji ekstrak cacing tanah. Hal ini
disebabkan karena beberapa faktor yang mungkin terjadi seperti keaktivan bakteri,
banyaknya larutan uji yang terserap ke dalam pencadang kertas atau karena
perbedaan kecil dari transmitan inokulum bakteri yang mempengaruhi banyaknya
bakteri di dalam media uji.
Pada uji mikrobiologi yang ketiga konsentrasi 50% terdapat hasil yang
jauh menyimpang dari hasil-hasil sebelumnya yaitu mengalami peningkatan
diameter hambat yang cukup besar. Hal ini disebabkan karena uji mikrobiologi
dilakukan pada hari terakhir sehingga dikhawatirkan konsentrasi bakteri yang
digunakan sudah semakin melemah sehingga berpengaruh pada diameter hambat
bakteri selain itu dikarenakan kondisi listrik yang kurang stabil selama pengujian
pertumbuhan bakteri. Menurut Wattimena (1981) beberapa faktor yang
mempengaruhi metode difusi agar yaitu suhu inkubasi yang kebanyakan bakteri
tumbuh baik pada suhu 370C dan waktu inkubasi yang disesuaikan dengan
pertumbuhan bakteri, karena luas daerah hambat ditentukan beberapa jam pertama,
setelah diinokulasikan pada media agar, maka daerah hambat dapat diamati segera
setelah adanya pertumbuhan bakteri.
Menurut Ditjen POM (1995), suatu zat dikatakan memiliki daya hambat
yang memenuhi persyaratan dengan diameter daerah hambatan lebih kurang 14
sampai 16 mm. Sediaan yang memenuhi persyaratan tersebut adalah sediaan F II
(mengandung 40% ekstrak etanol cacing tanah) dan F III (mengandung 50%
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Ekstrak etanol cacing tanah dapat dibuat ke dalam bentuk sediaan salep
dan selama penyimpanan dua bulan memiliki kestabilan yang baik terlihat dari
bentuk fisik berupa parameter warna, bentuk, dan bau sediaan yang tidak berubah,
jadi salep ini dapat digunakan untuk penggunaan topikal.
Sediaan salep ekstrak etanol cacing tanah dengan konsentrasi ekstrak 40%
sudah efektif untuk menghambat pertumbuhan bakteri Staphylococcus aureus
dengan diameter zona hambat sebesar 14,27 mm dan untuk konsentrasi 50%
memiliki zona hambat sebesar 16,47 mm. Sedangkan salep dengan konsentrasi
30% tidak memenuhi persyaratan zona hambat minimum yang baik karena hanya
sebesar 12,13 mm. Sehingga hanya F II (konsentrasi ekstrak 40%) dan F III
(Konsentrasi ekstrak 50%) yang memenuhi persyaratan.
Salep ekstrak etanol cacing tanah masih memiliki zona hambat yang masih
memenuhi persyaratan sehingga tidak memiliki perbedaan dengan zona hambat
ekstrak etanol cacing tanah.
5.2 Saran
Karena konsentrasi ekstrak yang digunakan dalam salep terlalu tinggi,
maka akan kurang efektif untuk dibuat dalam sediaan salep. Untuk itu pada
penelitian selanjutnya sebaiknya dilakukan pengujian dengan menggunakan jenis
bakteri yang lebih beragam untuk mengetahui pada bakteri apa saja sediaan salep
BAB II
TINJAUAN PUSTAKA
2.1 Cacing Tanah
Disebut cacing tanah (earthworm) karena hewan ini menghabiskan sebagian
besar hidupnya di tanah. Cacing tanah merupakan hewan tingkat rendah yang
tidak memiliki tulang belakang (avertebrata) dan bertubuh lunak. Cacing tanah
digolongkan ke dalam filum Annelida karena seluruh tubuhnya tersusun atas
beberapa segmen (ruas) yang berbentuk seperti cincin (Khairuman dan Khairul,
2010). Penggolongan ini didasarkan pada bentuk morfologi, karena tubuhnya
tersusun atas segmen-segmen yang berbentuk cincin (annulus), setiap segmen
memiliki beberapa pasang seta, yaitu struktur berbentuk rambut yang berguna
untuk memegang substrat dan bergerak. Tubuh dibedakan atas bagian anterior dan
posterior, pada bagian anteriornya terdapat mulut, prostomium dan beberapa
segmen yang agak menebal membentuk klitelium (Arlen dan Erni, 2000).
Suin (1982), menyatakan bahwa keanekaragaman jenis cacing tanah yang
terdapat di Indonesia cukup tinggi, yaitu tercatat dan telah diketahui sebanyak 55
jenis cacing tanah. Jenis cacing tanah yang telah ditemukan di Pulau Sumatera
adalah Friedericia bulbosa Rosa, Pontoscolex corethrurus Fr. Mull., Pheretima darliensis Sims dan Easton, Planapheretima moultoni Michaelsen, Megascolex
sp.. Sedangkan dari hasil penelitian Arlen (1994), di tempat pembuangan akhir
(TPA) sampah dan timbunan sampah rumah tangga pada beberapa Kecamatan
Kotamadya Medan-Sumatra Utara didapatkan 6 jenis cacing yaitu Megascolex
Cacing tanah telah diakui oleh ahli biologi maupun pertanian sebagai
indikator tingkat kesuburan tanah. Sebagai makroorganisme, cacing tanah
berperan sangat besar dalam proses pelapukan bahan organik di dalam tanah dan
sangat menentukan kesuburan tanah (Ciptanto dan Ulfah, 2011).
2.1.1 Taksonomi cacing tanah
Dunia hewan berdasarkan tingkatnya terbagi dalam 15 phyla. Cacing tanah
termasuk dalam Phylum Annelida yang berarti seluruh tubuhnya terdiri dari beberapa segmen atau ruas (Ciptanto dan Ulfah, 2011).
Ciri-ciri phylum Annelida adalah tubuhnya simetri bilateral, silindris, dan bersegmen-segmen. Pada permukaan tubuh terdapat sederetan dinding tipis atau
sekat-sekat, bernapas dengan kulit atau insang, mempunyai peredaran darah
tertutup dan darahnya mengandung hemoglobin (Ciptanto dan Ulfah, 2011 ).
Phylum Annelida terbagi dalam tiga kelas yaitu Polychaeta, Oligochaeta, dan Hirudinea. Cacing tanah memiliki banyak famili atau suku. Famili cacing tanah yang banyak dibudidayakan sebagai komoditas adalah famili
Acanthrodrilidae, Lumbricidae, Megascolicidae,dan Octochatidae (Ciptanto dan Ulfah, 2011).
2.1.2 Taksonomi cacing tanah (Peryonix sp.)
Dalam taksonomi cacing tanah Peryonix sp. memiliki klasifikasi sebagai berikut:
Kingdom : Animalia
Filum : Annelida
Kelas : Chaetopoda
Famili : Megascolecidae
Genus : Peryonix
Spesies : Peryonix sp.
2.1.3 Morfologi dan anatomi cacing tanah (Peryonix sp.)
Ciri-ciri eksternal: Panjang tubuh cacing tanah dewasa adalah 14-20 cm,
ukuran tubuh lebih besar dibandingkan cacing tanah lainnya, bentuk tubuh bulat,
berwarna coklat keunguan atau sedikit kelabu, jumlah segmen 75-165, klitelium
terletak pada segmen 13 dan 17 (Ciptanto dan Ulfah, 2011).
Cacing tanah ini termasuk jenis cacing lokal. Cacing ini sangat aktif, jika
disentuh tubuhnya akan menggeliat dan segera melarikan diri. Tubuh cacing tanah
selalu ditutupi lapisan lendir yang menyebabkan tubuhnya menjadi licin. Selama
hidupnya cacing tanah hidup di dalam tanah, tubuhnya selalu tertutup lapisan
lendir pelindung yang agar selalu basah karena cacing tanah bernapas melalui
kulit yang basah. Fungsi lendir adalah untuk membantu pernapasan,
mempermudah dalam menerobos tanah dan melindungi agar zat-zat kimia penting
tetap berada di dalam tubuhnya (Ciptanto dan Ulfah, 2011).
Cacing tanah mempunyai saluran pencernaan makanan yang lengkap dan
sistem peredaran darah yang sudah menggunakan pembuluh-pembuluh darah dan
disebut sebagai sistem peredaran darah tertutup. Darah cacing terdiri dari plasma
yang berisi sel darah putih (leukosit) dan darah merah. Sistem pencernaan makanan terdiri dari mulut pada segmen pertama, pharynx, kerongkongan, crop
yang merupakan pelebaran dari kerongkongan, perut otot, usus dan anus pada
Sistem saraf yang mengatur gerakan cacing tanah terdiri dari simpul saraf
bagian depan, simpul saraf bagian perut, serta saraf-saraf serabut. Simpul saraf di
bagian depan dapat disamakan dengan otak pada hewan umumnya yang diketahui.
Cacing bertindak tidak normal bila ada cahaya dan tidak dapat bertahan apabila
terkena cahaya ultraviolet, apabila cacing terkena cahaya ultra violet lebih dari 1
menit, cacing akan mati (Ciptanto dan Ulfah, 2011).
Pada cacing tanah yang telah dewasa memiliki klittelium yang merupakan
alat untuk perkembangbiakan dalam memproduksi kokon. Cacing tanah memiliki
dua kelamin dalam satu tubuh, jantan dan betina atau disebut juga hermaphrodite biparenteral. Akan tetapi tidak dapat membuahi sendiri melainkan dengan bantuan cacing lain (Ciptanto dan Ulfah, 2011).
Siklus hidup cacing tanah dimulai dari kokon hingga menetas menjadi
cacing muda, cacing produktif dan menjadi cacing tua. Setelah kokon menetas
cacing tanah muda akan hidup dan mencapai dewasa dalam waktu 2,5 - 3 bulan.
Masa produktif cacing tanah akan berlangsung selama 4 - 10 bulan dan akan
menurun hingga cacing mengalami kematian. Cacing yang sudah tidak produktif
lagi biasanya bagian ekornya agak pipih dan warna kuning pada ekornya sudah
mencapai punggung, sedangkan masa produktif warna kuning tersebut masih
berada di ujung ekor. Lama siklus hidup cacing tanah tergantung pada kesesuaian
kondisi lingkungan, cadangan makanan dan jenis cacing itu sendiri (Ciptanto dan
2.1.4 Habitat cacing tanah (Peryonix sp.)
Cacing tanah Peryonix sp. biasanya dapat ditemukan hidup di tempat pembuangan akhir (TPA) sampah dan timbunan sampah, tempat yang disukai
cacing tanah untuk tumbuh dan berkembang biak adalah tempat yang lembab dan
tidak terkena sinar matahari langsung, umumnya memakan serasah daun dan juga
materi tumbuhan lainnya yang telah mati, kemudian dicerna dan dikeluarkan
berupa kotoran (Arlen dan Erni, 2000).
2.1.5 Kandungan kimia cacing tanah
Kandungan kimia cacing tanah dalam bentuk bahan kering untuk jenis
cacing tanah Lumbricus rubellus adalah protein (58-78%), lemak (3-10%), kalsium (0,55%), fosfor (1%), serat (1,08%), dan abu (8-10%). Kandungan
asam-asam amino esensial dan non esensial cacing tanah adalah arginine (4,13%),
fenilalanin (2,25%), histidin (1,56%), isoleusin (2,58%), leusin (4,84%), lisin
(4,33%), metionin (2,18%), treonin (2,95%), valin (3,01%), glisin (2,92%), sistin
(2,29%), serin (2,88%), dan tirosin (1,36%) (Khairuman dan Khairul, 2010).
2.1.6 Manfaat cacing tanah
Pemanfaatan cacing tanah mulai dilakukan dalam berbagai aspek
kehidupan (Ciptanto dan Ulfah, 2011):
1. Sebagai bahan sediaan farmasi
Secara tradisional, cacing tanah sering digunakan dalam pengobatan penyakit
antara lain:
a. Menurunkan demam
Berdasarkan hasil penelitian FMIPA IPB menyebutkan cacing tanah dapat
b. Menurunkan tekanan darah tinggi
Ba Hoang, seorang dokter di Vietnam, yang berpraktik pengobatan
tradisional China, telah membuktikan efektivitas cacing tanah untuk mengobati
pasien-pasiennya yang mengidap stroke, hipertensi, penyumbatan pembuluh
darah, epilepsi, dan berbagai penyakit infeksi. Resep-resepnya telah banyak
dijadikan obat paten untuk pengobatan alergi, radang usus, dan stroke. Di
Jepang, seorang peneliti bernama Mihara Hisasi berhasil mengisolasi enzim
pelarut fibrin dalam cacing tanah yang bekerja sebagai enzim proteolitik.
Karena berasal dari cacing tanah Lumbricus, maka enzim tersebut dinamakan lumbrokinase. Penelitian tersebut kemudian dikembangkan di Kanada oleh
Canada RNA Biochemical dan berhasil menstandarkan enzim lumbrokinase
menjadi obat stroke. Obat yang berasal dari cacing tanah ini populer dengan
nama dagang “Boluoke”. Lazim diresepkan untuk mencegah dan mengobati
penyumbatan pembuluh darah jantung yang beresiko mengundang penyakit
jantung koroner, tekanan darah tinggi dan stroke. Penelitian terhadap khasiat
cacing tanah sudah pernah dilakukan juga secara besar-besaran di China sejak
tahun 1990, melibatkan tiga lembaga besar, yakni Xuanwu Hospital of Capital
Medical College, Xiangzi Provincial People’s Hospital, dan Xiangxi Medical
College. Uji coba klinis serbuk enzim cacing tanah ini dilakukan terhadap 453
pasien penderita gangguan pembuluh darah dengan 73% kesembuhan total
(Ciptanto dan Ulfah, 2011).
c. Mengobati infeksi saluran pencernaan seperti tipus, disentri, diare, serta
Cacing tanah mengandung antibiotik yang mampu melumpuhkan
bermacam bakteri pathogen, khususnya Escherichia coli penyebab diare. Antibiotik membunuh mikroorganisme biasanya dengan dua mekanisme:
1. Menghentikan jalur metabolik yang dapat menghasilkan nutrient yang
dibutuhkan oleh mikroorganisme atau menghambat enzim spesifik
yang dibutuhkan untuk membantu menyusun dinding sel bakteri.
2. Mekanisme yang dilakukan oleh protein yang dimiliki oleh cacing
tanah dengan membuat pori di dinding sel bakteri. Hal ini
menyebabkan sitoplasma sel bakteri menjadi terpapar dengan
lingkungan luar yang dapat mengganggu aktivitas dalam sel bakteri
dan menyebabkan kematian.
2. Bahan campuran kosmetik
Cacing tanah dapat menghasilkan minyak yang mengandung berbagai
macam enzim dengan cara ekstraksi. Di Negara-negara maju, enzim cacing
tanah digunakan sebagai bahan industri kosmetik untuk menghaluskan dan
mengencangkan kulit, pelembut kulit, pelembab wajah, antiinfeksi dan bahan
baku pembuatan lipstik.
Enzim yang terkandung dalam tubuh cacing tanah:
a. Enzim peroksidase katalase yang berfungsi untuk memperlambat
penuaan sel.
b. Selulase lignase, berfungsi mengembalikan dan menstabilkan fungsi
pencernaan.
c. Asam arakidonat, berfungsi untuk mempercepat pembentukan sel-sel
d. Alfa-tokoferol, berfungsi mempertahankan elastisitas dan peremajaan
kulit.
e. Taurin, berfungsi mempercepat metabolisme lemak untuk menambah
energi.
3. Sebagai agen penyubur lahan pertanian
4. Sebagai pengolah sampah dan penghasil pupuk kascing
5. Sebagai bahan pakan ternak.
2.2Ekstraksi
2.2.1 Pengertian ekstraksi
Ekstraksi adalah suatu proses untuk memperoleh sediaan pekat dengan
mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan
pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan
massa atau serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku
yang telah ditetapkan (Ditjen POM, 1995).
2.2.2 Tujuan ekstraksi
Tujuan ekstraksi dimaksudkan agar zat berkhasiat yang terdapat dalam
simplisia masih berada dalam kadar yang tinggi sehingga memudahkan untuk
mengatur dosis zat berkhasiat karena dalam sediaan ekstrak dapat
distandardisasikan kadar zat berkhasiat sedangkan kadar zat berkhasiat dalam
2.2.3 Jenis ekstraksi
Menurut Ditjen POM (2000) jenis-jenis ekstraksi terdiri dari:
1. Ekstraksi secara dingin
A. Metode maserasi
Maserasi meupakan cara penyarian sederhana yang dilakukan dengan cara
merendam serbuk simplisia dalam cairan penyari selama beberapa hari pada
temperatur kamar dan terlindung dari cahaya. Metode maserasi digunakan untuk
menyari simplisia yang mengandung komponen kimia yang mudah larut dalam
cairan penyari, tidak mengandung benzoin, tiraks, dan lilin. Keuntungan dari
metode ini adalah peralatannya sederhana. Sedang kerugiannya antara lain waktu
yang diperlukan untuk mengekstraksi sampel cukup lama, cairan penyari yang
digunakan lebih banyak, tidak dapat digunakan untuk bahan-bahan yang
mempunyai tekstur keras.
B. Metode perkolasi
Perkolasi adalah cara penyarian dengan mengalirkan penyari melalui
serbuk simplisia yang telah dibasahi. Keuntungan metode ini adalah tidak
memerlukan langkah tambahan yaitu sampel padat telah terpisah dari ekstrak.
Kerugiannya adalah kontak antara sampel padat tidak merata atau terbatas
dibandingkan dengan metode refluks dan pelarut menjadi dingin selama proses
perkolasi sehingga tidak melarutkan komponen secara efisien.
2. Ekstraksi secara panas
A. Metode refluks
Keuntungan dari metode ini adalah digunakan untuk mengekstraksi
Kerugiannya adalah membutuhkan volume pelarut yang besar dan sejumlah
manipulasi dari operator.
B. Metode destilasi uap
Destilasi uap adalah metode yang popular untuk ekstraksi minyak-minyak
menguap (esensial) dari sampel tanaman. Metode destilasi uap air
diperuntukkan menyari simplisia yang mengandung minyak menguap atau
mengandung komponen kimia yang mempunyai titik didih tinggi pada tekanan
udara normal.
C. Metode soxhletasi
Soxhletasi merupakan penyarian simplisia secara berkesinambungan,
cairan penyari dipanaskan sehingga menguap, uap cairan penyari terkondensasi
menjadi molekul-molekul air oleh pendingin balik dan turun menyari simplisia
dalam klongsong dan selanjutnya masuk kembali ke dalam labu alas bulat
setelah melewati pipa sifon
2.3 Salep
Salep adalah sediaan setengah padat yang mudah dioleskan dan digunakan
sebagai obat luar. Bahan obatnya larut atau terdispersi homogen dalam dasar salep
yang cocok (Ditjen POM, 1979).
Fungsi salep adalah:
a. Pembawa (vehicle) substansi obat untuk pengobatan kulit.
b. Pelumas (emollient) pada kulit dan
c. Pelindung (protective) untuk mencegah kontak permukaan kulit dengan larutan
Salep dapat mengandung obat atau tidak mengandung obat, yang
disebutkan terakhir biasanya dikatakan sebagai “dasar salep” dan digunakan
sebagai pembawa dalam penyiapan salep yang mengandung obat (Ansel, 1989).
Dasar salep digolongkan ke dalam 4 kelompok besar: dasar salep
hidrokarbon, dasar salep absorpsi, dasar salep yang dapat dicuci dengan air, dan
dasar salep yang larut dalam air (Ansel, 1989).
1. Dasar salep hidrokarbon: bersifat lemak dan sukar dicuci dengan air. Misalnya
adalah parafin, vaselin, minyak nabati.
2. Dasar salep serap (absorpsi)
Dasar salep dapat menyerap air dalam jumlah terbatas.
Misalnya adalah: Adeps lanae, lanolin, lilin (cera). 3. Dasar salep yang dapat dicuci dengan air
Dasar salep yang merupakan emulsi minyak dalam air, misalnya salep
hidrofilik, vanishing cream.
4. Dasar salep yang dapat larut dalam air, yaitu dasar salep yang mengandung
komponen larut dalam air. Misalnya adalah: polietilenglikol (Ditjen POM,
1979).
Kualitas dasar salep adalah:
a. stabil, selama dalam proses pengobatan. Maka salep harus bebas dari inkompatibilitas, stabil pada suhu dan kelembaban pada suhu kamar.
b. Lunak, yaitu semua zat dalam keadaan halus dan seluruh produk menjadi lunak dan homogen, sebab salep digunakan untuk kulit yang teriritasi dan inflamasi.
d. Dasar salep yang cocok, yaitu dasar salep yang kompatibel secara fisika dan kimia dengan obat yang dikandungnya. Dasar salep tidak boleh merusak atau
menghambat aksi terapi dari obat yang mampu melepas obatnya pada daerah yang
diobati.
e. Terdistribusi merata, obat harus terdistribusi merata melalui dasar salep padat atau cair pada pengobatan (Anief, 2007).
Menurut Anief (1986), faktor-faktor yang mempengaruhi efek absorpsi obat
dalam salep oleh kulit adalah:
1. Segi fisiologi: keadaan kulit, luas daerah pemakaian, banyaknya pemakaian,
letak pemakaian dan lama pemakaian.
2. Keadaan hidrasi pada stratum corneum.
3. Temperatur kulit.
4. Adanya pelarut yang dapat campur atau melarut dalam stratum corneum.
5. Konsentrasi obat.
2.4 Sterilisasi
Sterilisasi dalam mikrobiologi merupakan proses penghilangan semua
jenis organisme hidup, dalam hal ini adalah mikroorganisme (protozoa, fungi,
bakteri, mycoplasma, virus) yang terdapat pada suatu benda atau bahan (Pratiwi,
2008).
2.4.1 Sterilisasi uap
Proses sterilisasi termal menggunakan uap jenuh di bawah tekanan
berlangsung di suatu bejana yang disebut autoklaf, dan mungkin merupakan
proses sterilisasi yang paling banyak digunakan (suatu siklus autoklaf yang
pada suhu 121ºC kecuali dinyatakan lain). Prinsip dasar kerja alat adalah udara di
dalam bejana sterilisasi diganti dengan uap jenuh, dan hal ini dicapai dengan
menggunakan alat pembuka atau penutup khusus (Ditjen POM, 1995).
2.4.2 Sterilisasi panas kering
Proses sterilisasi termal untuk bahan yang tertera di Farmakope dengan
menggunakan panas kering biasanya dilakukan dengan suatu proses bets di dalam
suatu oven yang didesain khusus untuk tujuan itu. Oven modern dilengkapi
dengan udara yang dipanaskan dan disaring, didistribusikan secara merata ke
seluruh bejana dengan cara sirkulasi atau radiasi menggunakan sistem semprotan
dengan peralatan sensor, pemantau, dan pengendali parameter kritis. Validasi
fasilitas sterilisasi panas kering dilakukan dengan cara yang sama seperti pada
sterilisasi panas uap. Unit yang digunakan untuk sterilisasi komponen seperti
wadah untuk larutan intravena, harus dijaga agar dapat dihindari akumulasi
partikel di dalam bejana sterilisasi. Rentang suhu khas yang dapat diterima di
dalam bejana sterilisasi kosong adalah lebih kurang 15 menit, jika alat sterilisasi
beroperasi pada suhu tidak kurang dari 250ºC (Ditjen POM, 1995).
Sebagai penambahan pada proses bets tersebut di atas, suatu proses
berkesinambungan digunakan untuk sterilisasi dan depirogenisasi alat kaca
sebagai suatu bagian sistem pengisian dan penutupan kedap secara aseptik yang
berkesinambungan terpadu (Ditjen POM, 1995).
2.4.3 Sterilisasi gas
Pilihan untuk menggunakan sterilisasi gas sebagai alternatif dari sterilisasi
termal sering dilakukan jika bahan yang akan disterilkan tidak tahan terhadap
umumnya digunakan pada sterilisasi gas adalah etilen oksida dengan kualitas
mensterilkan yang dapat diterima. Keburukan dari bahan aktif ini antara lain
sifatnya yang sangat mudah terbakar, walaupun sudah dicampur dengan gas inert
yang sesuai, bersifat mutagenik, dan kemungkinan adanya residu toksik di dalam
bahan yang disterilkan, terutama yang mengandung ion klorida. Proses sterilisasi
pada umunya berlangsung di dalam bejana bertekanan yang didesain sama seperti
pada autoklaf, tetapi dengan tambahan bagian khusus yang hanya terdapat pada
alat sterilisasi yang menggunakan gas. Fasilitas yang menggunakan bahan
sterilisasi seperti ini harus didesain sedemikian rupa hingga mampu mengeluarkan
gas sesudah proses sterilisasi, mampu untuk memantau mikroba yang masih
hidup, dan mengurangi paparan gas yang sangat berbahaya terhadap petugas yang
menangani alat tersebut (Ditjen POM, 1995).
2.4.4 Sterilisasi dengan radiasi ion
Perkembangan yang cepat alat kesehatan yang tidak tahan terhadap
sterilisasi panas dan kekhawatiran tentang keamanan etilen oksida mengakibatkan
peningkatan penggunaan sterilisasi radiasi. Tetapi cara ini juga dapat digunakan
pada bahan obat dan bentuk sediaan akhir. Keunggulan sterilisasi iradiasi meliputi
reaktivitas kimia rendah, residu rendah yang dapat diukur, dan kenyataan yang
membuktikan bahwa variabel yang dikendalikan lebih sedikit. Kenyataannya
sterilisasi radiasi adalah sesuatu kekhususan dalam dasar pengendalian yang
penting adalah dosis radiasi yang diserap, dan dapat diukur secara tepat. Oleh
karena sifat khas tersebut, banyak prosedur baru yang telah dikembangkan untuk
menetapkan dosis sterilisasi. Walaupun begitu, hal ini masih dalam peninjauan
pengendalian tambahan dan tindakan keamanan. Iradiasi hanya menimbulkan
sedikit kenaikan suhu, tetapi dapat mempengaruhi kualitas dan jenis plastik atau
kaca tertentu (Ditjen POM, 1995).
Ada dua jenis radiasi ion yang digunakan, yaitu disintegrasi radioaktif dari
radioisotop (radiasi gamma) dan radiasi berkas elektron. Pada kedua jenis
tersebut, dosis radiasi yang dapat menghasilkan derajat jaminan sterilitas yang
diperlukan harus ditetapkan sedemikian rupa hingga dalam rentang satuan dosis
minimum dan maksimum, sifat bahan yang disterilkan dpat diterima (Ditjen
POM, 1995).
2.4.5 Sterilisasi dengan penyaringan
Sterilisasi larutan yang labil terhadap panas sering dilakukan dengan
penyaringan menggunakan bahan yang dapat menahan mikroba, hingga mikroba
yang dikandung dapat dipisahkan secara fisika. Perangkat penyaring umumnya
terdiri dari suatu matriks berpori bertutup kedap atau dirangkaikan pada wadah
yang tidak permeabel. Efektivitas suatu penyaring media atau penyaring substrat
tergantung pada ukuran pori bahan dan dapat tergantung pada daya adsorpsi
bakteri pada atau di dalam matriks penyaring atau tergantung pada mekanisme
pengayakan. Ada beberapa bukti yang menyatakan bahwa pengayakan merupakan
komponen yang lebih penting dari mekanisme. Penyaring yang melepas serat,
terutama yang mengandung asbes, harus dihindarkan penggunaanya kecuali tidak
ada cara penyaringan alternatif lain yang mungkin digunakan. Jika penyaring
yang melepas serat memang diperlukan, merupakan keharusan, bahwa proses
penyaringan meliputi adanya penyaring yang tidak melepas serat diletakkan pada
2.5 Uraian Bakteri
Nama bakteri berasal dari kata “bacterion” (bahasa Yunani) yang berarti tongkat atau batang. Sekarang nama itu dipakai untuk menyebut sekelompok
mikroorganisme yang bersel satu, berbiak dengan pembelahan diri, serta demikian
kecilnya sehingga hanya tampak dengan mikroskop (Dwidjoseputro, 1994).
Berdasarkan proses pewarnaan gram, bakteri dibagi menjadi dua golongan yaitu
bakteri gram positif dan bakteri gram negatif. Bakteri gram positif menyerap zat
warna pertama yaitu kristal violet yang menyebabkan warna ungu, sedangkan
bakteri gram negatif menyerap zat warna kedua yaitu safranin dan
menyebabkannya berwarna merah. Perbedaan hasil dalam pewarnaan gram
disebabkan perbedaan struktur, terutama dinding sel kedua bakteri tersebut
(Waluyo, 2010).
2.5.1 Morfologi sel bakteri
Ada beberapa bentuk dasar sel bakteri menurut Fardiaz (1992), yaitu bulat
(tunggal: coccus, jamak: cocci), batang atau silinder (tunggal: bacillus, jamak:
bacilli), dan bentuk spiral.
a. Bentuk bulat (cocci)
Berdasarkan pengelompokkan selnya, bakteri berbentuk bulat dapat dibedakan
atas beberapa jenis, antara lain diplococci (sel yang berpasangan atau dua sel),
streptococci (rangkaian sel yang membentuk rantai panjang atau pendek), tetrad
(empat sel bulat yang membentuk persegi empat), staphylococci (kumpulan sel
yang tidak beraturan seperti buah anggur), dan sarcina (kumpulan sel berbentuk
b. Bentuk bacilli
Sebagian besar bacilli tampak sebagai batang tunggal. Terbagi dalam dua
bentuk yaitu diplobacilli (bentuk berpasangan) dan streptobacilli (membentuk
rantai).
c. Bentuk spiral
Bakteri berbentuk spiral (tunggal, spirilium; jamak, spirila) terdapat secara
terpisah-pisah (tunggal), tetapi masing-masing spesies berbeda dalam panjang,
jumlah, dan lekukan spiralnya. Bakteri yang ukurannya pendek dengan spiral
yang tidak lengkap disebut bakteri koma atau vibrio.
2.5.2 Pengaruh faktor lingkungan pada pertumbuhan
Faktor yang mempengaruhi pertumbuhan mikroorganisme dapat
dibedakan menjadi faktor fisik dan faktor kimia. Faktor fisik meliputi temperatur,
pH, dan tekanan osmosis. Faktor kimia meliputi karbon, oksigen, trace element
dan faktor-faktor pertumbuhan organik termasuk nutrisi yang terdapat dalam
media pertumbuhan (Pratiwi, 2008).
A. Pengaruh faktor fisik pada pertumbuhan
I. Temperatur
Temperatur menentukan aktivitas enzim yang terlibat dalam aktivitas
kimia. Peningkatan temperatur sebesar 10ºC dapat meningkatkan aktivitas enzim
sebesar dua kali lipat. Pada temperatur yang sangat tinggi dapat menyebabkan
denaturasi protein yang tidak dapat balik (irreversible) sedangkan pada temperatur yang sangat rendah aktivitas enzim akan berhenti. Pada temperatur
jumlah sel yang maksimal. Berdasarkan kisaran temperatur tumbuh,
mikroorganisme dibagi atas empat golongan:
a. Psikrofil, tumbuh pada temperatur maksimal 20oC dengan suhu optimal 0
sampai 15oC.
b. Psikrofil fakultatif/psikotrof, tumbuh pada temperatur maksimal 30ºC dengan
suhu optimal 20 sampai 30ºC, dapat tumbuh pada 0ºC.
c. Mesofil, tumbuh pada temperatur 15 sampai 45oC dengan suhu optimal 20
sampai 40oC.
d. Termofil, tumbuh pada temperatur 45 sampai 100oC dengan suhu optimal 55
sampai 65oC.
II. pH
pH merupakan indikasi konsentrasi ion hidrogen. Peningkatan dan
penurunan konsentrasi ion hidrogen dapat menyebabkan ionisasi gugus-gugus
dalam protein, amino dan karboksilat. Hal ini dapat menyebabkan denaturasi
protein yang mengganggu pertumbuhan sel. Kebanyakan bakteri memiliki pH
optimum terletak antara 6,5 dan 7,5.
III. Tekanan osmosis
Tekanan osmosis merupakan tekanan yang dihasilkan akibat adanya
proses osmosis. Osmosis merupakan perpindahan air melewati membran
semipermeabel karena ketidakseimbangan material terlarut dalam media. Dalam
larutan hipotonik air akan masuk ke dalam sel mikroorganisme, sedangkan dalam
larutan hipertonik air akan ke luar dari dalam sel mikroorganisme sehingga
membran plasma mengerut dan lepas dari dinding sel (plasmolisis), serta
B. Pengaruh faktor kimia pada pertumbuhan
I. Nutrisi
Nutrisi merupakan substansi yang diperlukan untuk biosintesis dan
pembentukan energi. Berdasarkan kebutuhannya, nutrisi dibedakan menjadi dua
yaitu makroelemen, yaitu elemen yang diperlukan dalam jumlah banyak dan
mikroelemen yaitu elemen nutrisi yang diperlukan dalam jumlah sedikit (Pratiwi,
2008).
II. Media kultur
Bahan nutrisi yang digunakan untuk pertumbuhan mikroorganisme di
laboratorium disebut media kultur.
III. Oksigen
Klasifikasi mikroorganisme berdasarkan kebutuhan oksigen dibagi
menjadi 4 golongan, yaitu:
a. Aerob mutlak, oksigen sebagai syarat utama metabolisme.
b. Anaerob mutlak, tidak mentoleransi adanya oksigen atau akan mati bila ada
oksigen.
c. Anaerob fakultatif, mampu tumbuh baik dalam suasana dengan atau tanpa
oksigen.
d. Mikroaerofilik, hanya tumbuh baik pada konsentrasi oksigen yang rendah yaitu
kurang dari 20%, pada konsentrasi oksigen yang tinggi menyebabkan toksik
(Pratiwi, 2008).
2.5.3 Staphylococcus aureus
Divisi : Protophyta
Kelas : Schizomycetes
Bangsa : Eubacteriales
Suku : Micrococaceae
Marga : Staphylococcus
Jenis : Staphylococcus aureus
Staphylococcus aureus adalah bakteri berbentuk bulat (kokus) dengan diameter 0,7-0,9 μm yang terdapat dalam bentuk tunggal, berpasangan, tetrad,
atau berkelompok seperti buah anggur. Nama bakteri ini berasal dari bahasa latin
“staphele” yang berarti anggur. Staphylococcus aureus merupakan bakteri gram positif, tumbuh secara anaerobik fakultatif, tumbuh dengan cepat pada temperatur
37ºC namun pembentukan pigmen yang terbaik yaitu pada temperatur kamar
(25-30ºC), patogen utama pada manusia, biasanya membentuk koloni abu-abu hingga
kuning emas (Fardiaz, 1992; Jawetz, et al., 2001).
2.5.4 Media pertumbuhan bakteri
Pembiakan bakteri di laboratorium memerlukan media yang berisi zat hara
serta lingkungan pertumbuhan yang sesuai bagi bakteri. Zat hara diperlukan untuk
pertumbuhan, sintesis sel, keperluan energi dalam metabolisme dan pergerakan.
Lazimnya, media biakan mengandung air, sumber energi, zat hara sebagai sumber
karbon, nitrogen, sulfur, fosfat, oksigen dan hidrogen, ke dalam bahan dasar
media dapat pula ditambahkan faktor pertumbuhan berupa asam amino dan
I. Berdasarkan asalnya, media dibagi atas:
a. Media sintetik yaitu media yang kandungan dan isi bahan yang ditambahkan
diketahui secara terperinci. Contoh: glukosa, kalium fosfat, magnesium fosfat.
b. Media non-sintetik yaitu media yang kandungan dan isinya tidak diketahui
secara terperinci dan menggunakan bahan yang terdapat di alam. Contohnya:
ekstrak daging, pepton (Lay, 1996).
II. Berdasarkan kegunaannya, dapat dibedakan menjadi:
a. Media umum
Media yang paling sering digunakan dalam penelitian mikrobiologi,
contohnya : Nutrient Agar merupakan media yang kaya dan subur.
b. Media selektif
Media selektif adalah media biakan yang mengandung paling sedikit satu
bahan yang dapat menghambat perkembang biakan mikroorganisme yang tidak
diinginkan dan membolehkan perkembang biakan mikroorganisme tertentu yang
ingin diisolasi, contohnya: MCA, PDA, Saboaraut Agar (SA).
c. Media diferensial
Media ini digunakan untuk menyeleksi suatu mikroorganisme dari
berbagai jenis dalam suatu lempengan agar, contohnya: EMB, SSA.
d. Media diperkaya
Media ini digunakan untuk menumbuhkan mikroorganisme yang diperoleh
dari lingkungan alami karena jumlah mikroorganisme yang ada terdapat dalam
jumlah sedikit, beberapa zat organik yang mengandung zat karbon dan nitrogen
III. Berdasarkan konsistensinya, dibagi atas (Irianto, 2006):
a. Media padat/ solid
b. Media semi solid
c. Media cair
2.5.5 Metode isolasi biakan bakteri
a) Cara gores
Ose yang telah steril dicelupkan ke dalam suspensi mikroorganisme yang
diencerkan, lalu dibuat serangkaian goresan sejajar yang tidak saling menutupi di
atas permukaan agar yang telah padat.
b) Cara sebar
Suspensi mikroorganisme yang telah diencerkan diinokulasikan secara
merata dengan menggunakan hockey stick pada permukaan media padat. c) Cara tuang
Pengenceran inokulum yang berturut-turut diletakkan pada cawan petri
steril dan dicampurkan dengan medium agar cair, lalu dibiarkan memadat. Koloni
yang berkembang akan tertanam di dalam media tersebut (Stanier, et al., 1982).
2.5.6 Pengukuran aktivitas antibakteri
Penentuan kepekaan bakteri patogen terhadap antibakteri tertentu dapat
dilakukan dengan salah satu dari dua metode pokok yaitu dilusi atau difusi.
Penting sekali menggunakan metode standar untuk mengendalikan semua faktor
yang mempengaruhi aktivitas antimikroba.
a. Metode dilusi
Metode ini menggunakan antimikroba dengan kadar yang menurun secara
uji dan dieramkan. Tahap akhir dimasukkan antimikroba dengan kadar yang
menghambat atau mematikan. Uji kepekaan cara dilusi agar memakan waktu dan
penggunaannya dibatasi pada keadaan tertentu saja (Jawetz, et al., 2001).
b. Metode difusi
Metode yang paling sering digunakan adalah metode difusi agar. Cakram
kertas saring berisi sejumlah tertentu obat ditempatkan pada permukaan medium
padat yang sebelumnya telah diinokulasi bakteri uji pada permukaannya. Setelah
inkubasi, diameter zona hambatan sekitar cakram dipergunakan mengukur
kekuatan hambatan obat terhadap organisme uji. Metode ini dipengaruhi oleh
beberapa faktor fisik dan kimia, selain faktor antara obat dan organisme (misalnya
sifat medium dan kemampuan difusi, ukuran molekular dan stabilitas obat).
Meskipun demikian, standarisasi faktor-faktor tersebut memungkinkan melakukan
uji kepekaan dengan baik (Jawetz, et al., 2001).
c. Metode turbidimetri
Bakteri yang bertambah banyak pada media cair akan menyebabkan media
menjadi keruh. Alat yang digunakan untuk pengukuran adalah spektrofotometer
dengan cara membandingkan densitas optik antara media tanpa pertumbuhan
BAB I PENDAHULUAN
1.1 Latar Belakang
Obat alami yang digunakan oleh masyarakat semuanya bersumber dari alam.
Bahan-bahan dari alam tersebut dapat berupa komponen-komponen biotik seperti
tumbuhan maupun hewan serta komponen abiotik lainnya. Pengetahuan
pemanfaatan obat alami, terutama yang bersumber dari hewan merupakan
kekayaan bangsa yang telah diwariskan secara turun temurun (Sumardi, 1998).
Hewan-hewan yang telah dijadikan sebagai obat antara lain seperti cacing tanah,
lintah, teripang, kelelawar, undur-undur, tokek dan bekicot (Huteri, 2010).
Cacing tanah merupakan hewan penghuni tanah yang kelihatan lemah dan
menjijikkan seolah-olah tidak ada manfaatnya. Tetapi bila diperhatikan dan diteliti
ternyata hewan tingkat rendah ini adalah salah satu sumber daya alam yang
mempunyai potensi yang menakjubkan bagi kehidupan dan kesejahteraan manusia
(Arlen, 1997).
Dunia pengobatan tradisional Tiongkok telah menggunakan cacing tanah
dalam ramuan untuk menyembuhkan berbagai penyakit, seperti untuk
menyembuhkan mata bengkak merah, sakit gigi, gusi berdarah, lidah
membengkak, kerongkongan bengkak, telinga bernanah dan bisul. Kemudian di
Bogor dan Sukabumi banyak warga setempat yang telah menggunakan cacing
tanah sebagai ramuan yang sangat mujarab dalam menyembuhkan tifus kronis
Aktivitas antibakteri dari cacing tanah telah banyak diteliti dan dievaluasi
oleh sejumlah peneliti (Sumardi, 1998). Menurut Sumardi (1998) senyawa
antibakteri yang terdapat pada cacing tanah memiliki mekanisme kerja dengan
cara menghambat sintesis peptidoglikan dalam menghambat pertumbuhan bakteri.
Bakteri yang memiliki kandungan peptidoglikan pada dinding selnya relatif besar
akan mudah rusak apabila biosintesis peptidoglikannya dihambat sehingga bakteri
akan mati.
Penyakit infeksi masih merupakan jenis penyakit yang paling banyak diderita
oleh penduduk di negara berkembang, termasuk Indonesia. Salah satu penyebab
penyakit infeksi adalah bakteri. Bakteri merupakan mikroorganisme yang tidak
dapat dilihat dengan mata telanjang, tetapi hanya dapat dilihat dengan bantuan
mikroskop (Radji, 2011). Bakteri patogen lebih berbahaya dan menyebabkan
infeksi baik secara sporadik maupun endemik, antara lain Staphylococcus aureus, Escherichia coli dan Pseudomonas aeruginosa (Djide dan Sartini, 2008).
Antibakteri adalah senyawa yang mengganggu pertumbuhan dan metabolisme
bakteri, sehingga senyawa tersebut dapat menghambat pertumbuhan atau bahkan
membunuh bakteri (Pelczar dan Chan, 1988). Staphylococcus aureus merupakan
bakteri gram positif yang berbentuk bulat dan merupakan patogen utama pada
manusia (Jawetz, et al., 2001). Kulit dan membran mukosa merupakan barrier
yang sangat baik terhadap invasi lokal Staphylococcus aureus. Dapat
menyebabkan infeksi lokal pada kulit, hidung, uretra, saluran pernafasan dan
saluran pencernaan (Harris, et al., 2002).
Pada penelitian sebelumnya sudah diuji bahwa ekstrak etanol cacing tanah
yang pada konsentrasi 500 mg/ml memiliki daya hambat 13,87 mm (Siregar,
2012). Ini membuktikan bahwa benar cacing tanah memiliki daya hambat
terhadap bakteri.
Penelitian yang telah dilakukan oleh Sajuthi (2003), menemukan bahwa
dalam ekstrak cacing tanah terdapat sejumlah enzim seperti lumbrokinase,
peroksidase, katalase, dan selulase. Komponen lain adalah zat antipiretik (penurun
panas) yaitu asam arakhidonat, antipurin, antiracun, dan vitamin. Ekstrak cacing
tanah juga mengandung enzim lisosim yang mempunyai kemampuan sebagai
antimikroba yang sangat efektif untuk merusak dinding sel bakteri gram positif.
Salep merupakan sediaan farmasi berbentuk setengah padat atau semi solid
dan digunakan pada permukaan tubuh atau kulit (Ditjen POM, 1995). Komposisi
salep terdiri dari bahan obat atau zat aktif dan basis salep atau biasa dikenal
dengan sebutan zat pembawa bahan aktif (Ansel, 1989). Salep memiliki fungsi
sebagai bahan pembawa zat aktif untuk mengobati penyakit pada kulit, sebagai
pelumas pada kulit dan berfungsi sebagai pelindung kulit (Anief, 2007). Karena
ekstrak etanol cacing tanah pada penelitian ini ditujukan untuk pengobatan secara
topikal maka bahan dasar salep yang digunakan yaitu dasar salep yang sukar
tercuci dengan air dimana hanya sejumlah komponen air atau senyawa polar yang
dapat dicampur kedalamnya sehingga memungkinkan untuk memperpanjang
kontak antara ekstrak dengan kulit, sukar tercuci dan tidak mengering. Digunakan
pelarut etanol dalam proses ekstraksi ini juga berguna untuk mempermudah
pengujian antibakteri karena ekstrak yang dihasilkan nantinya dapat
mempermudah ekstrak untuk berdifusi dalam media agar yang bersifat polar.
kandungan zat aktif yang terkandung dalam cacing tanah untuk digunakan dalam
sediaan topikal terutama untuk mencegah terjadinya infeksi oleh bakteri
Staphylococcus aureus.
Berdasarkan uraian di atas maka penulis melakukan penelitian untuk melihat
bagaimana aktivitas antibakteri ekstrak cacing tanah yang telah diformulasi dalam
sediaan salep.
1.2 Perumusan Masalah
1. Apakah ekstrak etanol cacing tanah Peryonix sp. dapat diformulasi dalam sediaan salep?
2. Apakah sediaan salep ekstrak etanol cacing tanah masih memiliki
aktivitas antibakteri terhadap bakteri Staphylococcus aureus? 1.3 Hipotesis
1. Ekstrak etanol cacing tanah dapat diformulasi dalam sediaan salep
2. Sediaan salep ekstrak etanol cacing tanah masih memiliki aktivitas
antibakteri sebagai antibakteri.
1.4 Tujuan Penelitian
1. Untuk membuat formulasi sediaan salep topikal yang mengandung
ekstrak etanol cacing tanah.
2. Untuk melihat apakah sediaan salep ekstrak etanol masih memiliki
1.5 Manfaat Penelitian
Dengan dilakukannya penelitian ini diharapkan akan memberikan
pandangan atau gambaran untuk nantinya dapat dilakukan pengembangan