40
ANALISIS CEMARAN TIMBAL, KADMIUM DAN TEMBAGA
PADA KUBIS HIJAU (Brassica oleracea L.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
DAVID STEFAN
NIM 111501096
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
41
ANALISIS CEMARAN TIMBAL, KADMIUM DAN TEMBAGA
PADA KUBIS HIJAU (Brassica oleracea L.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
DAVID STEFAN
NIM 111501096
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
42
PENGESAHAN SKRIPSI
ANALISIS CEMARAN TIMBAL, KADMIUM DAN TEMBAGA
PADA KUBIS HIJAU (Brassica oleracea L.) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
DAVID STEFAN
NIM 111501096
Dipertahankan Di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 9 Mei 2015
Medan, Mei 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt. NIP 195807101986012001
Disetujui Oleh: Pembimbing I,
Dr. Masfria, M.S., Apt. NIP 195707231986012001
Pembimbing II,
Sri Yuliasmi, S.Farm., M.Si., Apt. NIP 198207032008122002
Panitia Penguji,
Prof. Dr. rer. nat. E. De Lux Putra, S.U., Apt. NIP 195306191983031001
Dr. Masfria, M.S., Apt. NIP 195707231986012001
Dra. Sudarmi, M.Si., Apt. NIP 1954069101983032001
43
KATA PENGANTAR
Puji syukur ke hadirat Tuhan Yang Maha Kuasa yang telah memberikan berkah karunia yang berlimpah sehingga penulis dapat meyelesaikan penyusunan skripsi yang berjudul Analisis Cemaran Timbal, Kadmium dan Tembaga pada Kubis Hijau (Brassica oleracea L) secara Spektrofotometri Serapan Atom. Skripsi ini diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
44
Penulis mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada Ayahanda Hotman Hasibuan dan Ibunda Toman Simangunsong yang telah memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi maupun motivasi beserta doa yang tulus yang tidak pernah berhenti dan adikku tercinta Marta Dea Hasibuan dan Beatrick Rosita Hasibuan serta seluruh keluarga yang selalu mendoakan dan memberikan semangat. Penulis dengan tulus mengucapkan terima kasih kepada sahabat tercinta Dodi, Daniel, Wilmar, Xandra, Amos, Putri, Winda, Fany, Benny, Iksen, Jessica, Novriany, Muliaty, dan sahabat lainnya yang tidak dapat disebutkan satu persatu terutama kawan-kawan farmasi angkatan 2011.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, Oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Mei 2015
Penulis,
45
ANALISIS CEMARAN TIMBAL, KADMIUM DAN TEMBAGA PADA
KUBIS HIJAU (Brassica oleracea L.) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
ABSTRAK
Kadar logam berat yang cukup tinggi pada sayuran sudah semestinya mendapat perhatian serius dari semua pihak, terutama pada sayur-sayuran yang ditanam di pinggir jalan raya. Banyak jenis sayuran yang beredar di masyarakat tidak terjamin keamanannya karena diduga telah terkontaminasi logam-logam berat seperti timbal (Pb), kadmium (Cd), dan tembaga (Cu). Salah satu contohnya adalah kubis hijau. Dikarenakan waktu pemanenan kubis sekitar 3 bulan sehingga sangat berpotensi tercemar oleh logam berat dan terakumulasi dalam waktu yang lama bila ditanam pinggir jalan raya. Kubis hijau dapat dikonsumsi dengan cara direbus dahulu atau tanpa direbus (segar) misalnya dibuat gado-gado, salad, dan lalapan.
Tujuan penelitian ini untuk mengetahui kadar cemaran timbal (Pb), kadmium (Cd), dan tembaga (Cu) pada kubis hijau dan membandingkan kadar cemaran tersebut antara kubis hijau segar dan rebus.
Sampel yang digunakan dalam penelitian ini adalah kubis hijau yang ditanam di lahan pertanian pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara. Preparasi sampel dilakukan dengan cara destruksi kering. Analisis dilakukan dengan alat spektrofotometer serapan atom (SSA) pada panjang gelombang 283,3 nm untuk timbal, 228,8 nm untuk kadmium, dan 324,8 nm untuk tembaga.
Hasil penelitian menunjukkan kubis hijau yang ditanam di lahan pertanian pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara tercemar logam berat timbal, kadmium dan tembaga. Dari keenam sampel yang dianalisis yaitu kadar cemaran logam timbal pada kubis hijau segar yaitu 0,25455 ± 0,01371 mg/kg dan kubis hijau rebus yaitu 0,19635 ± 0,010739 mg/kg. Kadar cemaran logam kadmium pada kubis hijau segar yaitu 0,029915 ± 0,002901 mg/kg dan kubis hijau rebus yaitu 0,024842 ± 0,001584 mg/kg. Kadar cemaran logam tembaga pada kubis hijau segar yaitu 0,91473 ± 0,004081 mg/kg dan kubis hijau rebus yaitu 0,70805 ± 0,01298 mg/kg. Terdapat perbedaan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau yang signifikan antara kubis segar dan rebus menggunakan analisis statistik uji t dengan taraf kepercayaan α = 99%.
46
ANALYSIS OF CONTAMINATION FOR LEAD, CADMIUM AND
COPPER IN GREEN CABBAGE (Brassica oleracea L.) IN ATOMIC
ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Highly metals level in vegetables were supposed to get seriously people attention, especially the vegetables which planted near the roadside. Many types of vegetables are dispersed around people which not secured as assumed have metals contamination such as lead (Pb), cadmium (Cd), and copper (Cu). One of vegetables was green cabbage. Harvesting time for cabbage was about 3 months so it was potentially contaminated by heavy metals and accumulated in a long time when planted along the main road. Cabbage could be consumed by earlier boiling or without boiling (fresh) such as gado-gado, salads, sandwiches, burgers and vegetables.
The purpose of this study was to determine the levels of contamination of lead (Pb), cadmium (Cd), and copper (Cu) on cabbage and comparing the levels of contamination between fresh and boiled green cabbage.
The sample used in this study was green cabbage grown on agricultural land edge of Jalan Raya Jamin Ginting, Berastagi, North Sumatra taken purposively. Sample preparation was done by dry destruction. Analyses were performed by atomic absorption spectrophotometer (AAS) at a wavelength of 283.3 nm for plumbum, cadmium and 228.8 nm to 324.7 nm for copper.
The results showed green cabbage grown on agricultural land edge of Jalan Raya Jamin Ginting, Berastagi, North Sumatra contaminated plumbum, cadmium, and copper. For six samples analyzed are the levels of lead metal contamination on fresh green green cabbage is 0.25455 ± 0.01371 mg/kg and boiled green cabbage is 0.19635 ± 0.010739 mg/kg. Levels of cadmium metal contamination on fresh green cabbage is 0.029915 ± 0.002901 mg/kg and boiled green cabbage is 0.024842 ± 0.001584 mg/kg. Levels of copper metal contamination on fresh cabbage is 0.91473 ± 0.004081 mg/kg and boiled green cabbage is 0.70805 ± 0.01298 mg/kg. There is a difference level of metals contamination of plumbum, cadmium, and copper on green cabbage significant between fresh and boiled cabbage using t test with a confidence level (α ) = 99%.
47
DAFTAR ISI
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Kubis ... 5
2.1.1 Manfaat Kubis ... 6
2.1.2 Taksonomi Kubis ... 6
2.2 Pangan Tercemar ... 7
48
2.4 Timbal (Pb) ... 8
2.4.1 Toksisitas Timbal (Pb) ... 8
2.5 Kadmium (Cd) ... 9
2.5.1 Toksisitas Kadmium (Cd) ... 10
2.6 Tembaga (Cu) ... 10
2.6.1 Toksisitas Tembaga (Cu) ... 11
2.7 Spektrofotometri Serapan Atom ... 11
2.7.1 Instrumen Spektrofotometer Serapan Atom ... 13
2.7.2 Bahan Bakar dan Bahan Pengoksidasi ... 16
2.7.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom ... 16
2.8 Validasi Metode ... 17
2.8.1 Kecermatan (akurasi) ... 17
2.8.2 Ketepatan (presisi) ... 18
2.8.3 Batas Deteksi (Limit of Detection, LOD) dan Batas Kuantitasi (Limit of Quantitation, LOQ) ... 18
BAB III METODE PENELITIAN ... 19
3.1 Tempat dan Waktu Penelitian ... 19
3.2 Metode Pengambilan Sampel ... 19
3.3 Bahan ... 19
3.3.1 Sampel ... 19
3.3.2 Pereaksi ... 20
3.4 Alat ... 20
3.5 Pembuatan Pereaksi ... 20
49
3.6 Destruksi Sampel ... 20
3.7 Pembuatan Larutan Sampel ... 21
3.8 Pembuatan Larutan Standar ... 21
3.8.1 Larutan Standar Timbal (Pb) ... 21
3.8.2 Penentuan Linearitas Kurva Kalibrasi Timbal (Pb) .. 21
3.8.3 Larutan Standar Kadmium (Cd) ... 22
3.8.4 Penentuan Linearitas Kurva Kalibrasi Kadmium (Cd) ... 22
3.8.5 Larutan Standar Tembaga (Cu) ... 23
3.8.6 Penentuan Linearitas Kurva Kalibrasi Tembaga (Cu) ... 23
3.9 Pengukuran Larutan Sampel dengan Spektrofotometer Serapan Atom ... 23
3.9.1 Penghitungan Kadar Timbal, Kadmium, dan Tembaga ... 23
3.9.2 Penolakan Hasil Pengamatan ... 24
3.10 Validasi Metode ... 25
3.10.1 Uji Perolehan Kembali (Recovery) ... 25
3.10.2 Penentuan Batas Deteksi dan Batas Kuantitasi ... 26
3.10.3 Simpangan Baku Relatif ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Identifikasi Tumbuhan ... 27
4.2 Kurva Kalibrasi Timbal (Pb), Kadmium (Cd), dan Tembaga (Cu) ... 27
4.2.1 Kurva Kalibrasi Timbal (Pb) ... 27
50
4.2.3 Kurva Kalibrasi Tembaga (Cu) ... 29
4.3 Penetapan Kadar Timbal (Pb), Kadmium (Cd), dan Tembaga (Cu) ... 30
4.4 Analisis Data Secara Statistik ... 32
4.4.1 Analisis Data dengan Uji t ... 32
4.4.2 Analisis Data dengan Uji Beda Rata-Rata ... 33
4.5 Analisis Persentase Penurunan Kadar Cemaran Logam Kubis Hijau Rebus Terhadap Kubis Hijau Segar... 33
4.6 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) ... 35
4.7 Uji Perolehan Kembali (Recovery) ... 35
4.8 Simpangan Baku Relatif ... 36
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
51
DAFTAR TABEL
Tabel 2.1 Temperatur Nyala dengan Berbagai Kombinasi Bahan Bakar
dan Bahan Pengoksidasi ... 16 Tabel 4.1 Data Absorbansi dan Konsentrasi Pengukuran pada Kubis
Hijau ... 30 Tabel 4.2 Kadar Logam Timbal, Kadmium, dan Tembaga pada Kubis
Hijau ... 31 Tabel 4.3 Data Hasil Uji Beda Nilai Rata-Rata antara Kubis Hijau Segar
dan Kubis Hijau Rebus ... 33 Tabel 4.4 Data Persentase Penurunan Kadar Timbal, Kadmium, dan
Tembaga pada Kubis Hijau Rebus terhadap Kubis Hijau Segar 34 Tabel 4.5 Batas Deteksi (LOD) dan Batas Kuantifikasi (LOQ) ... 35 Tabel 4.6 Persen Uji Perolehan Kembali (Recovery) Kadar Timbal,
Kadmium, dan Tembaga ... 36 Tabel 4.7 Nilai Simpangan Baku dan Simpangan Baku Relatif Timbal,
52
DAFTAR GAMBAR
Gambar 2.1 Instrumen Spektrofotometer Serapan Atom ... 13
Gambar 4.1 Kurva Kalibrasi Timbal (Pb) ... 27
Gambar 4.2 Kurva Kalibrasi Kadmium (Cd) ... 28
Gambar 4.3 Kurva Kalibrasi Tembaga (Cu) ... 29
53
DAFTAR LAMPIRAN
Lampiran 1. Gambar Sampel Kubis Hijau ... 40 Lampiran 2. Identifikasi Tumbuhan ... 41 Lampiran 3. Bagan Alir Proses Pembuatan Larutan Sampel ... 42 Lampiran 4. Data Kalibrasi Timbal (Pb) dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi dan
Koefisien Korelasi (r) ... 44 Lampiran 5. Data Kalibrasi Kadmium (Cd) dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi dan
Koefisien Korelasi (r) ... 46 Lampiran 6. Data Kalibrasi Tembaga (Cu) dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi dan
Koefisien Korelasi (r) ... 48 Lampiran 7. Contoh Perhitungan Kadar Timbal, Kadmium dan
Tembaga pada Kubis Hijau ... 50 Lampiran 8. Data Berat Sampel, Absorbansi dan Kadar Timbal,
Kadmium, dan Tembaga dari Kubis Hijau Segar dan
Rebus ... 52 Lampiran 9. Perhitungan Statistik Kadar Timbal dalam Kubis Hijau ... 54 Lampiran 10. Pengujian Beda Nilai Rata- Rata Kadar Timbal pada
Kubis Hijau Segar dan Kubis Hijau Rebus ... 58 Lampiran 11. Perhitungan Statistik Kadar Kadmium dalam Kubis Hijau 60 Lampiran 12. Pengujian Beda Nilai Rata-Rata Kadar Kadmium pada
Kubis Hijau Segar dan Kubis Hijau Rebus ... 64 Lampiran 13. Perhitungan Statistik Kadar Tembaga dalam Kubis Hijau 66 Lampiran 14. Pengujian Beda Nilai Rata-Rata Kadar Tembaga pada
Kubis Hijau Segar dan Kubis Hijau Rebus ... 70 Lampiran 15. Perhitungan Persentase Penurunan Kadar Timbal,
Kadmium, dan Tembaga pada Kubis Hijau Rebus
54
Lampiran 16. Perhitungan Batas Deteksi dan Batas Kuantitasi
Timbal (Pb) ... 73
Lampiran 17. Perhitungan Batas Deteksi dan Batas Kuantitasi Kadmium (Cd) ... 74
Lampiran 18. Perhitungan Batas Deteksi dan Batas Kuantitasi Tembaga (Cu) ... 75
Lampiran 19. Contoh Perhitungan Uji Perolehan Kembali Kadar Timbal, Kadmium, dan Tembaga pada Kubis Hijau ... 76
Lampiran 20. Perhitungan Simpangan Baku Relatif (RSD) Kadar Timbal, Kadmium, dan Tembaga pada Kubis Hijau ... 79
Lampiran 21. Gambar Alat Spektrofotometer Serapan Atom ... 82
Lampiran 22. Gambar Tanur ... 82
Lampiran 23. Tabel Distribusi t ... 83
Lampiran 24. Tabel Distribusi F ... 84
Lampiran 25. Batas Maksimum Cemaran Logam Berat dalam Pangan Berdasarkan Badan Standardisasi Nasional ... 85
45
ANALISIS CEMARAN TIMBAL, KADMIUM DAN TEMBAGA PADA
KUBIS HIJAU (Brassica oleracea L.) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
ABSTRAK
Kadar logam berat yang cukup tinggi pada sayuran sudah semestinya mendapat perhatian serius dari semua pihak, terutama pada sayur-sayuran yang ditanam di pinggir jalan raya. Banyak jenis sayuran yang beredar di masyarakat tidak terjamin keamanannya karena diduga telah terkontaminasi logam-logam berat seperti timbal (Pb), kadmium (Cd), dan tembaga (Cu). Salah satu contohnya adalah kubis hijau. Dikarenakan waktu pemanenan kubis sekitar 3 bulan sehingga sangat berpotensi tercemar oleh logam berat dan terakumulasi dalam waktu yang lama bila ditanam pinggir jalan raya. Kubis hijau dapat dikonsumsi dengan cara direbus dahulu atau tanpa direbus (segar) misalnya dibuat gado-gado, salad, dan lalapan.
Tujuan penelitian ini untuk mengetahui kadar cemaran timbal (Pb), kadmium (Cd), dan tembaga (Cu) pada kubis hijau dan membandingkan kadar cemaran tersebut antara kubis hijau segar dan rebus.
Sampel yang digunakan dalam penelitian ini adalah kubis hijau yang ditanam di lahan pertanian pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara. Preparasi sampel dilakukan dengan cara destruksi kering. Analisis dilakukan dengan alat spektrofotometer serapan atom (SSA) pada panjang gelombang 283,3 nm untuk timbal, 228,8 nm untuk kadmium, dan 324,8 nm untuk tembaga.
Hasil penelitian menunjukkan kubis hijau yang ditanam di lahan pertanian pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara tercemar logam berat timbal, kadmium dan tembaga. Dari keenam sampel yang dianalisis yaitu kadar cemaran logam timbal pada kubis hijau segar yaitu 0,25455 ± 0,01371 mg/kg dan kubis hijau rebus yaitu 0,19635 ± 0,010739 mg/kg. Kadar cemaran logam kadmium pada kubis hijau segar yaitu 0,029915 ± 0,002901 mg/kg dan kubis hijau rebus yaitu 0,024842 ± 0,001584 mg/kg. Kadar cemaran logam tembaga pada kubis hijau segar yaitu 0,91473 ± 0,004081 mg/kg dan kubis hijau rebus yaitu 0,70805 ± 0,01298 mg/kg. Terdapat perbedaan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau yang signifikan antara kubis segar dan rebus menggunakan analisis statistik uji t dengan taraf kepercayaan α = 99%.
46
ANALYSIS OF CONTAMINATION FOR LEAD, CADMIUM AND
COPPER IN GREEN CABBAGE (Brassica oleracea L.) IN ATOMIC
ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Highly metals level in vegetables were supposed to get seriously people attention, especially the vegetables which planted near the roadside. Many types of vegetables are dispersed around people which not secured as assumed have metals contamination such as lead (Pb), cadmium (Cd), and copper (Cu). One of vegetables was green cabbage. Harvesting time for cabbage was about 3 months so it was potentially contaminated by heavy metals and accumulated in a long time when planted along the main road. Cabbage could be consumed by earlier boiling or without boiling (fresh) such as gado-gado, salads, sandwiches, burgers and vegetables.
The purpose of this study was to determine the levels of contamination of lead (Pb), cadmium (Cd), and copper (Cu) on cabbage and comparing the levels of contamination between fresh and boiled green cabbage.
The sample used in this study was green cabbage grown on agricultural land edge of Jalan Raya Jamin Ginting, Berastagi, North Sumatra taken purposively. Sample preparation was done by dry destruction. Analyses were performed by atomic absorption spectrophotometer (AAS) at a wavelength of 283.3 nm for plumbum, cadmium and 228.8 nm to 324.7 nm for copper.
The results showed green cabbage grown on agricultural land edge of Jalan Raya Jamin Ginting, Berastagi, North Sumatra contaminated plumbum, cadmium, and copper. For six samples analyzed are the levels of lead metal contamination on fresh green green cabbage is 0.25455 ± 0.01371 mg/kg and boiled green cabbage is 0.19635 ± 0.010739 mg/kg. Levels of cadmium metal contamination on fresh green cabbage is 0.029915 ± 0.002901 mg/kg and boiled green cabbage is 0.024842 ± 0.001584 mg/kg. Levels of copper metal contamination on fresh cabbage is 0.91473 ± 0.004081 mg/kg and boiled green cabbage is 0.70805 ± 0.01298 mg/kg. There is a difference level of metals contamination of plumbum, cadmium, and copper on green cabbage significant between fresh and boiled cabbage using t test with a confidence level (α ) = 99%.
55
BAB I
PENDAHULUAN
1.1 Latar Belakang
Di Indonesia, kadar logam berat yang cukup tinggi pada sayuran sudah semestinya mendapat perhatian serius dari semua pihak, terutama pada sayur-sayuran yang ditanam di pinggir jalan raya (Widaningrum, dkk., 2007). Banyak sayuran ditanam di pinggir jalan raya agar lebih mudah diangkut ke pasar sehingga polusi dari kendaraan bermotor dapat mencemari sayur-sayuran tersebut.
Banyak jenis sayuran yang beredar di masyarakat tidak terjamin keamanannya karena diduga telah terkontaminasi logam berat seperti timbal (Pb) dan kadmium (Cd). Timbal dapat berasal dari pencemaran udara terutama dari asap buangan kendaraan bermotor. Cemaran kadmium dapat berasal dari asap kendaraan bermotor dan penggunaan pupuk berlebihan yang terakumulasi di tanah. Sayuran mengakumulasi kadmium lebih banyak dibandingkan tanaman pangan yang lain (Widaningrum, dkk., 2007).
Selain timbal (Pb) dan kadmium (Cd), sayuran juga rentan terhadap kontaminasi logam berat tembaga (Cu). Cemaran tembaga terdapat pada sayuran dan buah-buahan yang disemprot dengan pestisida secara berlebihan (Widaningrum, dkk., 2007).
56
Misalnya letusan Gunung Sinabung yang tentunya membawa abu yang mengandung cemaran logam berat. Sayur-sayuran yang diambil berlokasi di Berastagi telah terkena dampak letusan Gunung Sinabung. Salah satu contohnya adalah kubis hijau. Waktu pemanenan kubis sekitar 3 bulan sehingga sangat berpotensi tercemar oleh logam-logam berat dan terakumulasi dalam waktu yang lama. Kubis dapat dikonsumsi dengan cara direbus dahulu atau tanpa direbus (segar) misalnya dibuat gado-gado, salad, dan lalapan.
Sayur-sayuran dapat menjadi mediator penyebaran logam berat pada mahluk hidup karena masuknya logam tersebut pada tumbuhan melalui akar dan mulut daun (stoma). Logam berat ini bila terakumulasi dalam sayuran dalam jumlah yang banyak akan sangat membahayakan bagi tubuh. Timbal bisa merusak sel-sel saraf dan menghambat aktivitas enzim yang terlibat dalam pembentukan hemoglobin (Darmono, 1995).
Dalam konsentrasi tinggi tembaga dapat menyebabkan kerusakan sel darah merah, kerusakan organ paru-paru, dan pankreas. Tembaga juga bisa bersifat racun apabila berlebihan yaitu dapat menyebabkan nekrosis, serosis hati, dan kematian (Almatsier, 2002).
Efek keracunan kadmium yang umum adalah iritasi pada saluran pencernaan, paru-paru, tenggorokan terasa kering, mual, muntah, salivasi, diare, kejang perut, dan sakit pada otot. Bahkan efek kronisnya ditandai kehilangan indera perasa, penciuman, batuk, berkurangnya berat badan, gigi menjadi kuning, kerusakan hati dan ginjal, gangguan kardiovaskular, dan terjadinya hipertensi.
57
yang ditanam di pinggir jalan dan membandingkan kadar cemaran baik sampel segar maupun rebus.
Untuk menganalisis timbal (Pb) dan kadmium (Cd) dapat dilakukan dengan metode kompleksometri dan spektrofotometri serapan atom (SSA). Sedangkan menganalisis tembaga (Cu) dapat menggunakan metode gravimetri, kompleksometri dan spektrofotometri serapan atom (Khopkar, 1985).
Pada penelitian ini, penulis menganalisis timbal (Pb), kadmium (Cd), dan tembaga (Cu) pada kubis menggunakan metode spektrofotometri serapan atom karena metode ini sangat tepat untuk analisis zat dalam konsentrasi rendah, tidak sulit dalam pengerjaannya, cepat, spesifik, logam-logam yang membentuk campuran kompleks dapat dianalisis, dan interferensinya sedikit (Khopkar, 1985).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur- unsur logam dalam jumlah sedikit (trace) dan sangat sedikit (ultratrace) karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul dari logam sampel. Menurut Darmono (1995), analisis timbal (Pb), kadmium (Cd), dan tembaga (Cu) hanya dapat dilakukan dengan alat SSA karena jumlahnya yang sangat sedikit dalam jaringan dan tanaman.
1.2 Perumusan Masalah
a. Apakah kubis hijau mengandung cemaran logam timbal, kadmium, dan tembaga?
58
c. Apakah terdapat perbedaan yang signifikan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau segar dan rebus?
1.3 Hipotesis
a. Kubis hijau telah tercemar logam timbal, kadmium, dan tembaga.
b. Kadar logam timbal, kadmium, dan tembaga pada kubis hijau dalam jumlah tertentu.
c. Terdapat perbedaan yang signifikan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau segar dan rebus.
1.4 Tujuan Penelitian
a. Mengetahui cemaran logam timbal, kadmium, dan tembaga pada kubis hijau.
b. Melakukan penetapan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau.
c. Membuktikan bahwa terdapat perbedaan yang signifikan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau segar dan rebus.
1.5 Manfaat Penelitian
Memberikan informasi kepada masyarakat mengenai jumlah kandungan logam timbal, kadmium, dan tembaga pada kubis hijau (Brassica oleracea L.) serta membandingkan kadar logam-logam tersebut antara kubis hijau segar dan kubis hijau rebus.
59
TINJAUAN PUSTAKA
2.1 Uraian Kubis
Menurut sejarahnya, kubis dari tipe Brassica oleracea var. Sylvestris,
pertama kali dijumpai tumbuh di sepanjang pantai Laut Mediterania dan di sepanjang pantai Atlantik, Benua Eropa. Kubis diperkenalkan ke Indonesia oleh orang-orang Eropa di masa kolonial Belanda dan menjadi sayuran sehari-hari bagi masyarakat Indonesia hingga saat ini. Banyak orang menyebutnya kol, kata serapan dari bahasa Belanda (Akbar, 2015).
Tanaman kubis memiliki akar tunggang. Daunnya berbentuk bulat, tipis, dan lentur. Kubis memiliki daun mengelopak bersusun-susun rapat, berbentuk bulat menyerupai bola disebut krop. Kita mengenal dua jenis kubis karena perbedaan krop, yaitu kubis bulat dan kubis gepeng/bulat pipih (Kaleka, 2013).
Ada kubis yang kropnya berwarna hijau sangat pucat disebut kubis putih, ada yang kropnya hijau disebut kubis hijau dan ada yang berwarna ungu kemerahan atau kubis ungu. Tanaman kubis biasa dibudidayakan di daerah sejuk atau dingin seperti di daerah pegunungan atau dataran tinggi (Prasetio, 2013).
Kubis (Brassica oleracea L.) memiliki daun yang lebar dan lunak. Daun yang lebih dahulu menutup daun yang muncul kemudian sehingga membentuk krop seperti telor dan berwarna hijau. Suhu optimum untuk budidaya kubis adalah 15-200C (Zulkarnain, 2013).
60
menggunakan tangan atau pisau. Saat memanen kubis biasanya disertakan dengan beberapa lembar daun yang hijau untuk melindungi krop (Setyaningrum dan Saparinto, 2014).
2.1.1 Manfaat Kubis
Kubis mengandung zat-zat gizi yang berguna bagi tubuh seperti vitamin A, B1 (thiamin), B2 (riboflavin), B3 (niasin), betakaroten, C, dan E. Mineral yang dikandung kubis adalah kalsium, kalium, natrium, besi, dan fosfor. Kubis juga mengandung zat yang bersifat melawan kanker, seperti lupeol, sinigrin, diindolylmethane (DIM), indole-3-carbinol (I3C), dan sulforaphane yang merangsang pembentukan glution, yaitu enzim yang bekerja menguraikan, membuang zat-zat beracun dalam tubuh dan melakukan detoksifikasi senyawa kimia berbahaya seperti timbal, merkuri, kadmium, nikel, kobalt, tembaga, dan logam berbahaya lainnya yang berlebihan dalam tubuh (Akbar, 2015).
2.1.2 Taksonomi Kubis
Menurut Zulkarnain (2013), klasifikasi tumbuhan kubis adalah sebagai berikut.
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae Ordo : Cruciferales Famili : Cruciferae Genus : Brassica
Spesies : Brassica oleracea
2.2 Pangan Tercemar
61
pangan yang mengandung cemaran yang melampaui ambang batas maksimal yang ditetapkan (Badan Standardisasi Nasional, 2009).
Cemaran yang keberadaannya dalam pangan tidak dikehendaki dan mungkin ada sebagai akibat dari berbagai tahapan sejak dari bahan baku, proses produksi, pengemasan, transportasi atau dari kontaminasi lingkungan. Batas maksimum merupakan konsentrasi maksimum cemaran logam berat yang diijinkan atau direkomendasikan dapat diterima dalam pangan (Badan Standardisasi Nasional, 2009).
2.3 Logam Berat
Logam berat adalah unsur-unsur metal yang memiliki bobot atom dan bobot jenis yang tinggi, yang dapat bersifat racun bagi makhluk hidup. Jenis cemaran logam berat dalam pangan adalah arsen (As), kadmium (Cd), merkuri (Hg), timah (Sn), dan timbal (Pb) (Badan Standardisasi Nasional, 2009).
Logam berat masih termasuk golongan logam dengan kriteria-kriteria yang sama dengan logam-logam lain. Perbedaannya terletak dari pengaruh yang dihasilkan bila logam berat ini masuk ke dalam tubuh organisme hidup. Logam berat tidak esensial, yakni logam yang keberadaannya dalam tubuh masih belum diketahui manfaatnya, bahkan bersifat toksik, seperti Hg, Cd, Pb, dan sebagainya (Darmono, 1995).
2.4 Timbal (Pb)
62
logam yang lunak berwarna abu-abu kebiruan mengkilat. Logam ini mempunyai nomor atom 82 dengan berat atom 207,20. Titik didih timbal adalah 17400 C dan meleleh pada suhu 3280 C (Widowati, dkk., 2008).
Kandungan timbal (Pb) pada tanaman pertanian maupun perkebunan yang lokasinya dengan jalan raya lebih tinggi dibandingkan dengan hasil pertanian maupun perkebunan yang lokasinya jauh dari jalan raya. Hal ini menunjukkan bahwa pencemaran timbal (Pb) yang potensial berasal dari kendaraan bermotor (Widowati, dkk., 2008).
2.4.1 Toksisitas Timbal (Pb)
Meskipun jumlah Pb yang diserap oleh tubuh hanya sedikit, logam ini ternyata menjadi sangat berbahaya. Hal ini disebabkan karena Pb adalah logam toksik yang bersifat kumulatif dan bentuk senyawanya dapat memberikan efek racun terhadap fungsi organ yang terdapat dalam tubuh (Darmono, 1995).
Dampak keterpaparan timbal (Pb) terhadap kesehatan, yaitu A. Terpapar Secara Akut
Keterpaparan timbal secara akut/ dini akan menimbulkan gejala rasa lemah, lelah, gangguan tidur, sakit kepala, nyeri otot dan tulang, sembelit, kehilangan nafsu makan dan juga dapat menyebabkan anemia. Pada beberapa kasus akut akibat terpapar timbal (Pb) terjadi oliguria (urin sedikit) dan gagal ginjal yang akut dapat berkembang secara cepat (Darmono, 1995).
B. Terpapar Secara Kronis
63
bingung atau pikiran kacau, konsentrasi berkurang, dan gangguan ingatan. Beberapa gejala lain yang diakibatkan keterpaparan timbal (Pb) secara kronis di antaranya adalah kehilangan libido, infertilitas pada laki-laki, gangguan menstruasi serta aborsi spontan pada wanita (Darmono, 1995).
Anak-anak adalah yang paling rentan terhadap timbal (Pb). Efek yang merugikan adalah penurunan intelegensia, kerusakan pada jaringan otak, dan kematian. Dampak keracunan timbal (Pb) yang terjadi pada anak bersifat jangka panjang dan tidak dapat pulih (Darmono, 1995).
2.5 Kadmium (Cd)
Kadmium adalah logam berwarna putih perak, lunak, mengkilap, tidak larut dalam basa, mudah bereaksi, serta menghasilkan kadmium oksida bila dipanaskan. Kadmium memiliki nomor atom 48, berat atom 112,4 g/mol, titik leleh 3210C dan titik didih 7670C (Widowati, dkk., 2008).
Sumber Cd berasal dari hasil penambangan, hasil sampingan peleburan Zn dan Pb, pabrik baterai, electroplating, pupuk, pestisida, limbah industri dan rumah tangga. Kadmium banyak digunakan sebagai pigmen warna cat, keramik, plastik, industri baterai, bahan fotografi, pembuatan tabung TV, dan percetakan tekstil (Darmono, 1995).
2.5.1 Toksisitas Kadmium (Cd)
64
keracunan kadmium kronis juga menyebabkan gangguan kardiovaskuler dan hipertensi (Palar, 1994).
2.6 Tembaga (Cu)
Tembaga ada dalam tubuh sebanyak 50-120 mg. Sekitar 40% ada di dalam otot, 15% di dalam hati, 10% di dalam otak, 6% di dalam darah dan selebihnya di tulang, ginjal, dan jaringan tubuh lain. Tembaga terdapat di dalam makanan. Sumber utama tembaga adalah tiram, kerang, hati, ginjal, kacang-kacangan, unggas, biji-bijian, serealia, dan cokelat. Sebanyak 35-70% diabsorbsi di bagian atas usus halus secara aktif dan pasif (Almatsier, 2002).
Tembaga merupakan bagian dari enzim metaloprotein yang terlibat dalam fungsi sitokrom dalam oksidasi di dalam mitokondria, sintesis protein-protein kompleks jaringan kolagen di dalam kerangka tubuh dan pembuluh darah serta dalam sintesis pembawa ransangan saraf (neuritransmittter) seperti noradrenalin dan neuropeptida seperti ensefalin. Tembaga memegang peranan penting dalam mencegah anemia dengan cara, yaitu membantu absorbsi besi, merangsang sintesis hemoglobin, dan melepas simpanan besi dalam hati (Almatsier, 2002).
2.6.1 Toksisitas Tembaga (Cu)
Kelebihan tembaga secara kronis menyebabkan penumpukan tembaga di dalam hati yang dapat menyebabkan nekrosis hati atau serosis hati. Konsumsi sebanyak 10-15 mg tembaga sehari dapat menimbulkan muntah-muntah dan diare, berbagai tahap pendarahan intravaskular dapat terjadi begitupun nekrosis sel-sel hati dan gagal ginjal. Konsumsi dosis tinggi dapat menyebabkan kematian (Almatsier, 2002).
65
Spektrofotometri serapan atom adalah suatu metode analisis yang digunakan untuk penentuan unsur-unsur logam dan metaloid yang berdasarkan pada proses penyerapan energi radiasi atom-atom yang berada pada tingkat energi dasar (ground state) pada panjang gelombang tertentu tergantung jenis unsur yang dianalisis (Arifin, 2008).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul logam dalam sampel tersebut. Cara ini cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm) dan pelaksanaannya relatif sederhana (Gandjar dan Rohman, 2008).
Prinsip dasar spektrofotometri serapan atom adalah interaksi antara radiasi elektromagnetik dengan sampel. Interaksi ini didasarkan pada emisi dan absorbansi dari uap atom larutan sampel. Interaksi ini diperoleh dari proses penguapan sampel yang diubah menjadi atom bebas (Gandjar dan Rohman, 2008). Atom ini akan mengabsorbsi radiasi dari sumber cahaya yang dipancarkan dari lampu katoda (Hallow cathode lamp) yang mengandung unsur dari logam yang akan ditentukan. Banyaknya penyerapan radiasi kemudian diukur pada panjang gelombang tertentu menurut jenis logamnya (Gandjar dan Rohman, 2008).
66
menyerap suatu energi maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan energinya ke tingkat eksitasi. Natrium mempunyai konfigurasi elektron 1s2, 2s2, 2p6, dan 3s1. Tingkat dasar untuk elektron valensi 3s1 ini dapat mengalami eksitasi ke tingkat 3p atau ke tingkat 4p (Gandjar dan Rohman, 2008).
Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral dan sinar yang diserap biasanya sinar tampak atau ultraviolet. Dalam garis besarnya prinsip spektrofotometri serapan atom sama dengan spektrofotometri sinar tampak dan ultraviolet. Perbedaannya terletak pada bentuk spektrum, cara pengerjaan sampel dan peralatannya (Gandjar dan Rohman, 2008).
Kelemahan spektrofotometri serapan atom adalah sampel harus dalam bentuk larutan, tidak mudah menguap, dan satu lampu katoda hanya digunakan untuk satu unsur saja (Arifin, 2008).
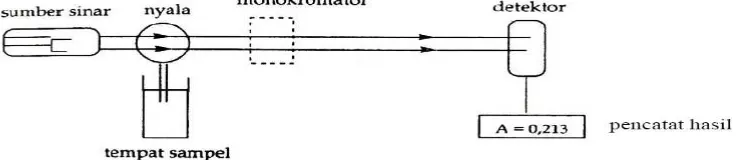
2.7.1 Instrumen Spektrofotometer Serapan Atom
Menurut Gandjar dan Rohman (2008), instrumen spektrofotometer serapan atom diperlihatkan pada Gambar 2.1 berikut ini.
Gambar 2.1 Instrumen Spektrofotometer Serapan Atom (Sumber: Gandjar dan Rohman, 2008)
67
Sumber sinar yang lazim dipakai adalah lampu katoda (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari logam dan dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon) (Gandjar dan Rohman, 2008).
Bila antara anoda dan katoda diberi selisih tegangan yang tinggi (600 volt), maka katoda akan memancarkan berkas-berkas elektron yang bergerak menuju anoda yang mana kecepatan dan energinya sangat tinggi. Elektron-elektron dengan energi tinggi ini dalam perjalanannya menuju anoda akan bertabrakan dengan gas-gas mulia yang diisikan tadi. Akibat dari tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan menjadi bermuatan positif. Ion-ion gas mulia yang bermuatan positif ini selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi pula (Gandjar dan Rohman, 2008).
Pada katoda terdapat unsur-unsur yang sesuai dengan unsur yang dianalisis. Unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar dari permukaan katoda. Atom-atom unsur dari katoda ini mungkin akan mengalami eksitasi ke tingkat energi-energi elektron yang lebih tinggi dan akan memancarkan spektrum pencaran dari unsur yang sama dengan unsur yang akan dianalisis (Gandjar dan Rohman, 2008). b. Tempat Sampel
68
dasar. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu:
i. Dengan nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara suhunya sebesar 22000C (Gandjar dan Rohman, 2008).
ii. Tanpa nyala (flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil
sedikit (hanya beberapa μL), lalu diletakkan dalam tabung grafit kemudian tabung
tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi sinar yang memenuhi kaidah analisis kuantitatif (Gandjar dan Rohman, 2008).
c. Monokromator
Monokromator dimaksudkan untuk memisahkan dan memilih panjang gelombang yang digunakan dalam analisis. Dalam monokromator terdapat
chopper (pemecah sinar), suatu alat yang berputar dengan frekuensi atau kecepatan perputaran tertentu (Gandjar dan Rohman, 2008).
d. Detektor
69
yaitu (a) yang memberikan respon terhadap radiasi resonansi dan radiasi kontinu; dan (b) yang hanya memberikan respon terhadap radiasi resonansi (Gandjar dan Rohman, 2008).
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat sinyal yang diterima dari detektor sehingga dapat dibaca alat pencatat hasil (Readout) (Gandjar dan Rohman, 2008).
f. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2008).
2.7.2 Bahan Bakar dan Bahan Pengoksidasi
[image:32.595.109.512.527.651.2]Umumnya bahan bakar yang digunakan adalah hidrogen, asetilen dan propan sedangkan oksidatornya adalah udara, oksigen dan NO2. Temperatur dari berbagai nyala dapat dilihat pada Tabel 2.1 berikut ini:
Tabel 2.1 Temperatur Nyala dengan Berbagai Kombinasi Bahan Bakar dan
Bahan Pengoksidasi
Bahan Bakar Oksidasi Temperatur Maksimum
(0K)
Asetilen Udara 2400-2700
Asetilen Nitrogen Oksida 2900-3100
Asetilen Oksigen 3300-3400
Hidrogen Udara 2300-2400
Hidrogen Oksigen 2800-3000
Sianogen Oksigen 4800
(Sumber: Khopkar, 1985)
2.7.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom
70
menjadi lebih kecil atau lebih besar dari yang nilai yang sesuai dengan konsentrasinya dalam sampel (Gandjar dan Rohman, 2008).
Menurut Gandjar dan Rohman (2008), gangguan-gangguan yang dapat terjadi dalam AAS adalah sebagai berikut:
1. Gangguan yang berasal dari matriks sampel yang dapat mempengaruhi banyaknya sampel yang mencapai nyala.
Sifat-sifat tertentu matriks sampel dapat mengganggu analisis yakni matriks tersebut dapat berpengaruh terhadap laju aliran bahan bakar/ gas pengoksidasi. Sifat-sifat tersebut adalah viskositas, tegangan permukaan, berat jenis dan tekanan unsur. Gangguan matriks yang lain adalah pengendapan unsur yang dianalisis sehingga jumlah atom yang mencapai nyala menjadi lebih sedikit dari konsentrasi yang seharusnya yang terdapat dalam sampel.
2. Gangguan kimia yang dapat mempengaruhi jumlah/banyaknya atom yang terjadi di dalam nyala
Terbentuknya atom-atom netral yang masih dalam keadaan azas di dalam nyala sering terganggu oleh dua peristiwa kimia, yaitu:
a. Disosiasi senyawa-senyawa yang tidak sempurna b. Ionisasi atom-atom di dalam nyala
2.8 Validasi Metode
71
bahwa metode analisis akurat, spesifik, reprodusibel, dan tahan pada kisaran alat yang dianalisis (Gandjar dan Rohman, 2008).
2.8.1 Kecermatan (akurasi)
Kecermatan adalah metode dapat menghasilkan nilai rata-rata (mean) yang sangat dekat dengan nilai sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
Perolehan kembali dapat ditemukan dengan membuat sampel plasebo (eksipien obat, cairan biologis), ditambahkan analit dengan konsentrasi tertentu (biasanya 80% sampai 120% dari kadar analit yang diperkirakan) kemudian dianalisis dengan metode konsentrasi yang akan divalidasi (Harmita, 2004).
Tetapi bila tidak memungkinkan membuat sampel plasebo maka dapat dipakai metode adisi. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut (Harmita, 2004).
2.8.2 Ketepatan (presisi)
Presisi merupakan ukuran keterulangan metode analisis dan biasanya diperlihatkan sebagai simpangan baku relatif (Relative Standard Deviation, RSD) dari sejumlah sampel yang berbeda secara statistik (Gandjar dan Rohman, 2008).
Dalam analisis, nilai RSD antara 1-2% biasanya dipersyaratkan untuk senyawa-senyawa aktif dalam jumlah banyak sedangkan untuk senyawa-senyawa dengan kadar kecil RSD-nya berkisar antara 5-15% (Gandjar dan Rohman, 2008).
72
Batas deteksi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang masih dapat dideteksi tetapi tidak dikuantitasi pada kondisi percobaan yang dilakukan. Batas deteksi dinyatakan dalam konsentrasi analit (persen, bagian per juta) dalam sampel (Harmita, 2004).
Batas kuantitasi didefinisikan sebagai konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi. Batas ini dinyatakan dalam konsentrasi analit (persen, bagian per juta) dalam sampel (Harmita, 2004).
BAB III
METODE PENELITIAN
Penelitian ini merupakan penelitian deskriptif yang bertujuan untuk mengetahui dan membandingkan kadar timbal, kadmium, dan tembaga pada kubis hijau segar dan rebus.
3.1 Tempat dan Waktu Penelitian
Lokasi penelitian dilakukan di Laboratorium Kimia Farmasi Kualitatif dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara. Penelitian ini dilakukan pada bulan September hingga bulan Desember 2014.
3.2 Metode Pengambilan Sampel
73
diperlukan. Jadi, sampel yang diambil pada suatu populasi telah memenuhi persyaratan dan keinginan dari peneliti.
3.3 Bahan
3.3.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah kubis hijau (Brassica oleracea L.) yang ditanam di pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara. Kubis hijau diberi dua perlakuan yaitu dengan perebusan dan tanpa perebusan (segar).
3.3.2 Pereaksi
Bahan kimia yang digunakan dalam penelitian ini adalah akuades bebas mineral, larutan standar timbal nitrat Pb(NO3)2 1000 ppm, larutan standar kadmium nitrat Cd(NO3)2 1000 ppm, larutan standar tembaga nitrat Cu(NO3)2 1000 ppm, dan asam nitrat 65% b/v.
3.4 Alat
Alat-alat yang digunakan adalah alat-alat gelas, spektrofotometer serapan atom (Hitachi Zeeman-2000) dengan nyala campuran udara-asetilen lengkap dengan lampu katoda timbal (Pb), lampu katoda kadmium (Cd) dan lampu katoda tembaga (Cu), neraca analitik (AND GF-200), tanur, penjepit tabung, bola karet,
hotplate, krus porselen, spatula, botol kaca, dan kertas saring Whatmann no. 42.
3.5 Pembuatan Pereaksi
3.5.1 Larutan HNO3 7 N
Larutan HNO3 65% b/v sebanyak 100 ml diencerkan dengan akuades hingga 200 ml.
74
Sampel dicuci dengan air mengalir hingga bersih lalu dicuci dengan akuades bebas mineral dan ditiriskan selama 15 menit. Dipotong kecil-kecil sekitar 1-2 cm sebanyak 1 kg lalu kubis hijau diberikan dua perlakuan yaitu sebanyak 500 g direbus dengan akuades bebas mineral selama 5 menit dengan air mendidih dan sisanya sebanyak 500 g tidak direbus (segar).
Sampel kubis hijau baik segar maupun rebus ditimbang sebanyak 50 g dan dimasukkan ke dalam krus porselen lalu dilakukan pengulangan 6 kali. Krus porselen yang berisi sampel dipanaskan di atas hotplate pada temperatur 1000C sampai sampel menjadi arang dan kering (± selama 8 jam) lalu diabukan dalam tanur pada suhu 5000 C selama 48 jam (Arifin, 2008).
3.7 Pembuatan Larutan Sampel
Sampel hasil destruksi yang telah menjadi abu putih dilarutkan dalam 10 ml HNO3 7 N, dituang dalam labu tentukur 100 ml dan diencerkan akuades bebas mineral hingga garis tanda (Arifin, 2008). Larutan sampel disaring dengan kertas saring Whatmann no. 42. Filtrat pertama sebanyak 2 ml dibuang untuk menjenuhkan kertas saring, filtrat berikutnya ditampung ke dalam botol.
3.8 Pembuatan Larutan Standar
3.8.1 Larutan Standar Timbal (Pb)
Larutan standar timbal nitrat (1000 ppm) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml, diencerkan hingga garis tanda dengan akuades bebas mineral disebut Larutan Induk Baku I (LIB I) konsentrasi 100 ppm.
75
3.8.2 Penentuan Linearitas Kurva Kalibrasi Timbal (Pb)
Dari LIB II (2,5 ppm) dipipet masing-masing sebanyak 1 ml; 2 ml; 3 ml; 4 ml; 5 ml. Masing-masing larutan dimasukkan ke dalam lima buah labu ukur 50 ml yang berbeda kemudian diencerkan dengan akuades bebas mineral hingga garis tanda dan dikocok hingga homogen sehingga diperoleh konsentrasi 50 ppb; 100 ppb; 150 ppb; 200 ppb; 250 ppb dan diukur absorbansi pada panjang gelombang 283,3 nm, atomisasi dilakukan dengan nyala udara-asetilen dengan laju alir 2,0 L/menit, tinggi burner 7,5 cm, dan lebar celah 0,7 nm.
3.8.3 Larutan Standar Kadmium (Cd)
Larutan standar kadmium nitrat (1000 ppm) sebanyak 5 ml, dimasukkan ke dalam labu tentukur 50 ml kemudian diencerkan hingga garis tanda dengan akuades bebas mineral disebut Larutan Induk Baku I (LIB I) konsentrasi 100 ppm.
Dari LIB I (100 ppm) dipipet sebanyak 5 ml, dimasukkan ke dalam labu tentukur 25 ml kemudian diencerkan hingga garis tanda dengan akuades bebas mineral disebut Larutan Induk Baku II (LIB II) konsentrasi 20 ppm.
Dari LIB II (20 ppm) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuades bebas mineral disebut Larutan Induk Baku III (LIB III) konsentrasi 200 ppb.
3.8.4 Penentuan Linearitas Kurva Kalibrasi Kadmium (Cd)
76
dilakukan dengan nyala udara-asetilen dengan laju alir 2,0 L/menit, tinggi burner 5 cm, dan lebar celah 0,7 nm.
3.8.5 Larutan Standar Tembaga (Cu)
Larutan standar tembaga nitrat (1000 ppm) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml kemudian diencerkan hingga garis tanda dengan akuades bebas mineral disebut Larutan Induk Baku (LIB) konsentrasi 10 ppm.
3.8.6 Penentuan Linearitas Kurva Kalibrasi Tembaga (Cu)
Dari LIB (10 ppm) dipipet masing-masing sebanyak 1 ml; 2 ml; 3 ml; 4 ml; 5 ml. Masing-masing larutan dimasukkan ke dalam lima buah labu ukur 50 ml yang berbeda kemudian diencerkan dengan akuades bebas mineral hingga garis tanda dan dikocok hingga homogen sehingga diperoleh konsentrasi 0,2 ppm; 0,4 ppm; 0,6 ppm; 0,8 ppm; 1 ppm dan diukur absorbansi pada panjang gelombang 324,8 nm, atomisasi dilakukan dengan nyala udara-asetilen dengan laju alir 2,0 L/menit, tinggi burner 7,5 cm, dan lebar celah 0,7 nm.
3.9 Pengukuran Larutan Sampel dengan Spektrofotometer Serapan
Atom
Persiapkan spektrofotometer serapan atom dengan baik. Pasang lampu katoda timbal untuk penentuan kadar timbal, lampu katoda kadmium untuk penentuan kadar kadmium, dan lampu katoda tembaga untuk penentuan kadar tembaga. Kemudian ukur absorbansi sampel dengan masing-masing kurva kalibrasi ketiga logam.
77
Data yang diperoleh dari pengukuran serapan larutan standar dibuat kurva kalibrasinya. Konsentrasi larutan sampel dihitung berdasarkan kurva kalibrasi larutan standar. Menurut Gandjar dan Rohman (2008), kadar logam dalam sampel dapat dihitung dengan persamaan
y = a x + b dimana: y = absorbansi x = konsentrasi
a = koefisien regresi (slope = kemiringan) b = tetapan regresi (intersep)
Kadar timbal, kadmium, dan tembaga dapat dihitung dengan persamaan sebagai berikut:
Kadar (mg/kg) =
Bs Fp x V x X
Keterangan:
X = konsentrasi analit dalam sampel (ppm atau ppb) V = volume total larutan sampel yang diperiksa (mL) FP = faktor pengenceran dari larutan sampel
Bs = berat sampel yang diambil dari larutan sampel (kg)
3.9.2 Penolakan Hasil Pengamatan
Kadar timbal, kadmium, dan tembaga yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis dengan metode standar deviasi. Menurut Sudjana (2005), perhitungan standar deviasi dapat dihitung dengan rumus sebagai berikut:
SD =
(
)
1 -nX
-Xi 2
∑
Keterangan :
Xi = Kadar sampel
78 Untuk mencari t hitung digunakan rumus: t hitung =
n / SD
X -Xi
dan untuk menentukan kadar logam di dalam sampel dengan interval kepercayaan
99%, α = 0,01, dk = n-1, dapat digunakan rumus:
Kadar Logam: µ = X ± (t(α/2, dk) x SD /√n ) Keterangan:
X = Kadar rata-rata sampel SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1)
α = Interval kepercayaan n = Jumlah perlakuan
3.10 Validasi Metode
3.10.1 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali dilakukan dengan metode penambahan larutan standar (standard addition method). Pertama-tama dilakukan penentuan kadar logam dalam sampel, selanjutnya dilakukan penentuan kadar logam dalam sampel setelah penambahan larutan standar dengan konsentrasi tertentu (Harmita, 2004).
79 % Recovery =
sampel dalam n ditambahka yang standar kadar sampel zat kadar -standar n ditambahka setelah zat kadar x 100%
3.10.2 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (SYX) =
(
)
2 n Yi Y 2 − −∑
Batas deteksi (LOD) =
slope X SY x 3
Batas kuantitasi (LOQ) =
slope X SY x 10
3.10.3 Simpangan Baku Relatif
Menurut Harmita (2004), keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Rumus untuk menghitung simpangan baku relatif sebagai berikut:
RSD = 100%
X SD
×
80 X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Tumbuhan yang diidentifikasi/ dideterminasi oleh Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi-LIPI Bogor adalah kubis hijau dengan nama spesies Brassica oleracea L yang dapat dilihat pada Lampiran 2 halaman 41.
4.2 Kurva Kalibrasi Timbal, Kadmium, dan Tembaga
4.2.1 Kurva Kalibrasi Timbal (Pb)
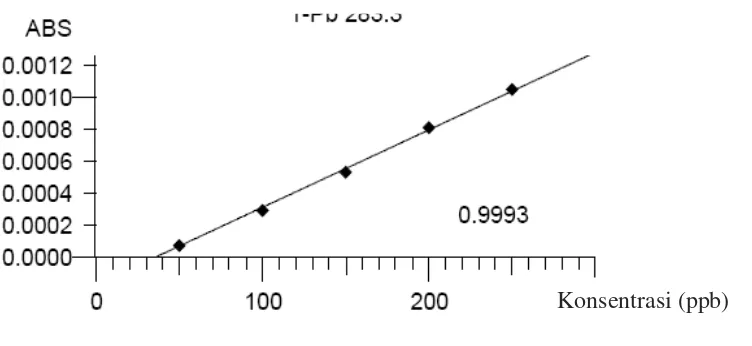
Kurva kalibrasi logam timbal diperoleh dengan cara mengukur absorbansi dari larutan standar timbal pada panjang gelombang 283,3 nm. Dari pengukuran kurva kalibrasi untuk timbal diperoleh persamaan regresi yaitu Y= 0,000004862857X – 0,0001761905 untuk timbal.
Data kalibrasi timbal, perhitungan persamaan regresi dan koefisien korelasi dapat dilihat pada Lampiran 4 halaman 44. Hasil pengukuran kurva kalibrasi timbal diperlihatkan pada Gambar 4.1 berikut.
81
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi dengan koefisien korelasi (r) timbal sebesar 0,9993. Hubungan linier dikatakan paling baik bila koefisien korelasi yang diperoleh mendekati 1 dan batas persyaratan dari koefisien korelasi masih dapat diterima adalah r = 0,9950 (Clarke, 2005). Kurva ini menunjukkan korelasi positif antara konsentrasi (X) dan absorbansi (Y) yang artinya peningkatan konsentrasi sebanding dengan naiknya absorbansi (Sudjana, 2005).
4.2.2 Kurva Kalibrasi Kadmium (Cd)
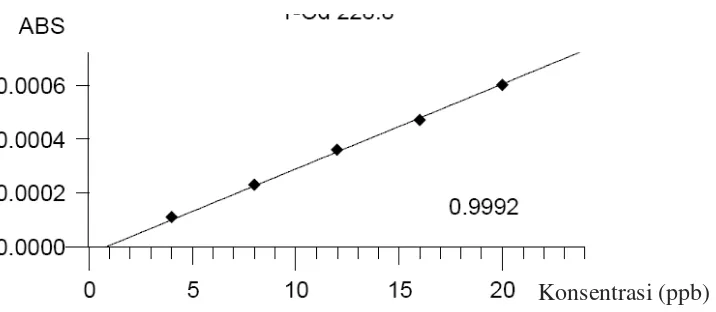
Kurva kalibrasi logam kadmium diperoleh dengan cara mengukur absorbansi dari larutan standar kadmium pada panjang gelombang 228,8 nm. Dari pengukuran kurva kalibrasi untuk kadmium diperoleh persamaan regresi yaitu Y = 0,0000315X – 0,00002666667 untuk kadmium.
Hasil pengukuran kurva kalibrasi kadmium diperlihatkan pada Gambar 4.2 berikut. Data kalibrasi kadmium, perhitungan persamaan regresi dan koefisien korelasi dapat dilihat pada Lampiran 5 halaman 46.
[image:44.595.116.492.78.251.2]Konsentrasi (ppb)
Gambar 4.1 Kurva Kalibrasi Timbal (Pb)
82
Gambar 4.2 Kurva Kalibrasi Kadmium (Cd)
Berdasarkan kurva kalibrasi kadmium diperoleh hubungan yang linear antara konsentrasi dengan absorbansi dengan koefisien korelasi (r) kadmium sebesar 0,9992. Hubungan linier dikatakan paling baik bila koefisien korelasi yang diperoleh mendekati 1 dan batas persyaratan dari koefisien korelasi masih dapat diterima adalah r = 0,9950 (Clarke, 2005). Kurva ini menunjukkan korelasi posisif antara konsentrasi (X) dan absorbansi (Y) yang artinya peningkatan konsentrasi sebanding dengan naiknya absorbansi (Sudjana, 2005).
4.2.3 Kurva Kalibrasi Tembaga (Cu)
Kurva kalibrasi logam tembaga diperoleh dengan cara mengukur absorbansi dari larutan standar tembaga pada panjang gelombang 324,8 nm. Dari pengukuran kurva kalibrasi untuk tembaga diperoleh persamaan regresi yaitu Y = 0,01181143X - 0,0001090476 untuk tembaga.
Data kalibrasi tembaga, perhitungan persamaan regresi dan koefisien korelasi dapat dilihat pada Lampiran 6 halaman 48. Hasil pengukuran kurva kalibrasi tembaga diperlihatkan pada Gambar 4.3 berikut.
Konsentrasi (ppb)
83
Gambar 4.4 Kurva Kalibrasi Tembaga (Cu)
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi dengan koefisien korelasi (r) tembaga sebesar 0,9997. Hubungan linier dikatakan paling baik bila koefisien korelasi yang diperoleh mendekati 1 dan batas persyaratan dari koefisien korelasi masih dapat diterima adalah r = 0,9950 (Clarke, 2005). Kurva ini menunjukkan korelasi posisif antara konsentrasi (X) dan absorbansi (Y) yang artinya peningkatan konsentrasi sebanding dengan naiknya absorbansi (Sudjana, 2005).
4.3 Penetapan Kadar Timbal, Kadmium, dan Tembaga
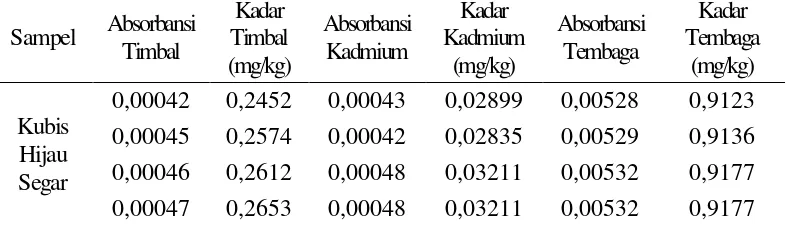
Pengukuran dilakukan pada masing-masing kurva kalibrasi ketiga logam di atas sehingga menghasilkan absorbansi dan diperoleh konsentrasi larutan sampel berdasarkan persamaan regresi masing-masing kurva kalibrasi ketiga logam di atas. Hasil perhitungan kadar dapat dilihat pada Lampiran 8 halaman 52.
Tabel 4.1 Data Absorbansi dan Konsentrasi Pengukuran pada Kubis Hijau Sampel Absorbansi
Timbal
Kadar Timbal (mg/kg)
Absorbansi Kadmium
Kadar Kadmium
(mg/kg)
Absorbansi Tembaga
Kadar Tembaga
(mg/kg) Kubis
Hijau Segar
0,00042 0,2452 0,00043 0,02899 0,00528 0,9123 0,00045 0,2574 0,00042 0,02835 0,00529 0,9136 0,00046 0,2612 0,00048 0,03211 0,00532 0,9177 0,00047 0,2653 0,00048 0,03211 0,00532 0,9177
Konsentrasi (ppm)
[image:46.595.117.510.614.728.2]84
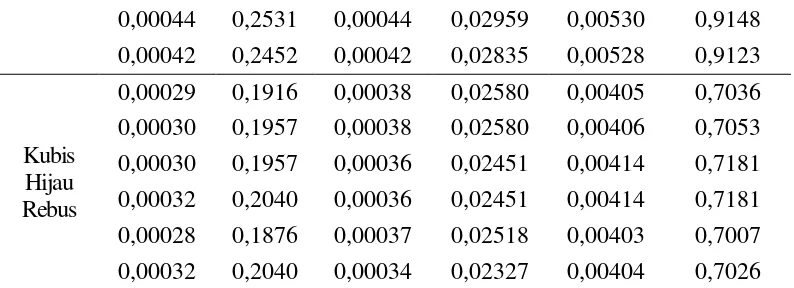
0,00044 0,2531 0,00044 0,02959 0,00530 0,9148 0,00042 0,2452 0,00042 0,02835 0,00528 0,9123
Kubis Hijau Rebus
0,00029 0,1916 0,00038 0,02580 0,00405 0,7036 0,00030 0,1957 0,00038 0,02580 0,00406 0,7053 0,00030 0,1957 0,00036 0,02451 0,00414 0,7181 0,00032 0,2040 0,00036 0,02451 0,00414 0,7181 0,00028 0,1876 0,00037 0,02518 0,00403 0,7007 0,00032 0,2040 0,00034 0,02327 0,00404 0,7026 Secara langsung dapat dilihat Tabel 4.1 bahwa ada pengaruh perebusan terhadap kadar timbal, kadmium, dan tembaga pada kubis hijau yang ditanam di pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara.
[image:47.595.114.511.84.228.2]Dari hasil perhitungan terhadap data kadar rata-rata timbal, kadmium, dan tembaga pada kubis hijau baik segar maupun rebus maka diperoleh kadar masing-masing logam pada sampel. Kadar logam timbal, kadmium, dan tembaga pada sampel dapat dilihat pada Tabel 4.2
Tabel 4.2 Kadar Logam Timbal, Kadmium, dan Tembaga pada Kubis Hijau
Kadar (mg/kg)
Timbal Kadmium Tembaga
Kubis segar 0,25455±0,01371 0,029915±0,002901 0,91473±0,004081 Kubis rebus 0,19635±0,010739 0,024842±0,001584 0,70805±0,01298
Badan Standarisasi Nasional memberikan informasi mengenai batasan cemaran logam sebagai Standar Nasional Indonesia (SNI) untuk buah dan sayur (termasuk jamur, umbi, kacang kedelai, dan lidah buaya), rumput laut, biji-bijian yaitu 0,5 mg/kg untuk timbal.
85
layak dan aman dikonsumsi (Badan Standarisasi Nasional, 2009). Akan tetapi, jika kita mengonsumsi kubis hijau yang tercemar secara terus-menerus akan mengakibatkan penumpukkan timbal dalam tubuh yang memiliki dampak sangat berbahaya yaitu gangguan gastrointestinal, kerusakan pada jaringan otak bahkan kematian (Darmono, 1995).
Badan Standarisasi Nasional memberikan informasi mengenai batasan cemaran logam sebagai Standar Nasional Indonesia (SNI) untuk buah dan sayur (termasuk jamur, umbi, kacang kedelai dan lidah buaya), rumput laut, biji-bijian yaitu 0,2 mg/kg untuk kadmium.
Berdasarkan hasil perhitungan yang dilakukan kadar kadmium yang terdapat dalam kubis hijau, yaitu 0,029915 ± 0,002901 mg/kg untuk kubis segar dan 0,024842 ± 0,001584 mg/kg untuk kubis rebus. Jadi, kadar kadmium yang mencemari kubis hijau tidak melebihi batas yang ditetapkan oleh SNI sehingga kubis hijau masih layak dan aman dikonsumsi (Badan Standarisasi Nasional, 2009). Akan tetapi, jika kita mengonsumsi kubis hijau yang tercemar secara terus-menerus akan mengakibatkan penumpukkan kadmium dalam tubuh yang memiliki dampak sangat berbahaya yaitu kerusakan organ reproduksi, kerusakan ginjal bahkan kematian (Palar, 2004).
86
kubis hijau tidak mencapai jumlah tembaga yang menyebabkan muntah-muntah dan diare, pendarahan intravaskular dapat terjadi, dan nekrosis sel-sel hati.
4.4 Analisis Data Secara Statistik
4.4.1 Analisis Data dengan Uji t
Hasil analisis data dengan uji t pada kubis hijau rebus dan segar dapat dilihat pada Lampiran 9 halaman 54 untuk timbal, Lampiran 11 halaman 60 untuk kadmium, dan Lampiran 13 halaman 66 untuk tembaga. Jadi, dapat disimpulkan bahwa semua data dengan Ho diterima atau semua data diterima dengan interval kepercayaan 99% dan nilai �= 0,01.
[image:49.595.114.506.388.445.2]4.4.2 Analisis Data dengan Uji Beda Nilai Rata-Rata
Tabel 4.3 Data Hasil Uji Beda Nilai Rata-Rata antara Kubis Hijau Segar dan Kubis Hijau Rebus
Sampel Jenis Logam Harga t0
Kubis Hijau
Timbal -13,472
Kadmium -6,189
Tembaga -61,21
Daerah kritis penolakan to< -4,0321 dan to> 4,0321. Harga to yang didapat dari masing-masing logam < -4,0321 sehingga hipotesa Ho ditolak. Harga Ho ditolak berarti terdapat perbedaan signifikan rata-rata kadar timbal, kadmium, dan tembaga antara kubis hijau segar dengan kubis hijau rebus. Analisis data secara statistik dengan uji beda nilai rata-rata dilakukan terhadap kubis hijau segar dan rebus dapat dilihat pada Lampiran 10 halaman 58 untuk timbal, Lampiran 12 halaman 64 untuk kadmium, dan Lampiran 14 halaman 70 untuk tembaga.
4.5 Analisis Persentase Penurunan Kadar Cemaran Logam Kubis Hijau
Rebus terhadap Kubis Hijau Segar
87
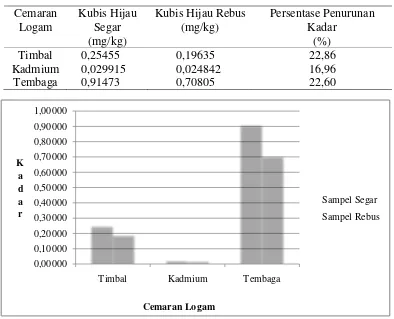
[image:50.595.114.508.251.570.2]perhitungan persentase penurunan kadar cemaran logam kubis hijau rebus terhadap kubis hijau segar dapat dilihat pada Tabel 4.4 dan Gambar 4.4.
Tabel 4.4 Data Persentase Penurunan Kadar Timbal, Kadmium, dan Tembaga
pada Kubis Hijau Rebus terhadap Kubis Hijau Segar
Gambar 4.4 Diagram Penurunan Kadar Cemaran Logam
Menurut Sari, dkk., (2014), logam-logam berat mudah mengadakan ikatan kompleks dengan nutrien dalam tanaman dan asam organik sebagai respon toleransi terhadap logam beracun sehingga dapat mendetoksifikasi logam.
Logam-0,00000 0,10000 0,20000 0,30000 0,40000 0,50000 0,60000 0,70000 0,80000 0,90000 1,00000
Timbal Kadmium Tembaga
K a d a r
Cemaran Logam
Sampel Segar
Sampel Rebus
Cemaran Logam
Kubis Hijau Segar (mg/kg)
Kubis Hijau Rebus (mg/kg)
Persentase Penurunan Kadar
(%)
Timbal 0,25455 0,19635 22,86
Kadmium 0,029915 0,024842 16,96
88
logam beracun diserap akar melewati jaringan xilem akar lalu disimpan di vakuola subseluler dan sel epidermal.
Asam organik berupa asam sitrat terdapat pada buah dan sayuran berperan sebagai chelator (pengikat logam). Gugus –OH dan –COOH pada asam sitrat menyebabkan ion sitrat bereaksi dengan ion logam membentuk garam sitrat. Adanya perebusan meningkatkan kelarutan garam dalam air sehingga mereduksi kadar logam timbal, kadmium, dan tembaga dalam sampel (Sari, dkk., 2014).
4.6 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
[image:51.595.114.506.449.518.2]Berdasarkan data kurva kalibrasi timbal, kadmium, dan tembaga dilakukan perhitungan batas deteksi dan batas kuantitasi yang dapat dilihat pada Lampiran 16 halaman 73 untuk timbal, Lampiran 17 halaman 74 untuk kadmium, dan Lampiran 18 halaman 75 untuk tembaga. Batas deteksi dan batas kuantitasi timbal, kadmium, dan tembaga dapat dilihat pada Tabel 4.5.
Tabel 4.5 Batas deteksi dan batas kuantitasi timbal, kadmium, dan tembaga Mineral Batas Deteksi Batas Kuantitasi
Timbal 11,99 ppb 39,96 ppb
Kadmium 1,01 ppb 3,38 ppb
Tembaga 0,032 ppm 0,106 ppm
Dengan melihat batas deteksi (LOD) dan batas kuantitasi (LOQ) dari masing-masing logam dan membandingkannya dengan data hasil pengukuran konsentrasi sampel dapat disimpulkan bahwa data tersebut masih berada di atas batas deteksi dan batas kuantitasi.
4.7 Uji Perolehan Kembali (Recovery)
89
[image:52.595.116.511.195.311.2]Lampiran 19 halaman 76. Contoh hasil uji perolehan kembali dari ketiga logam tersebut setelah penambahan larutan baku ketiga logam dapat dilihat pada Tabel 4.6.
Tabel 4.6 Persen Uji Perolehan Kembali (recovery) Kadar Timbal, Kadmium, dan Tembaga Logam yang dianalisis Konsentrasi dalam sampel sebelum penambahan baku (CA)
Konsentrasi bahan baku yang
ditambahkan (C*)
Konsentrasi setelah penambahan baku
(CF)
% Recovery x100% C A C F C ∗ −
Timbal 254,55 ppb 52,07 ppb 306,618 ppb 99,99% Kadmium 30,23 ppb 4,767 ppb 34,70 ppb 93,77% Tembaga 0,9147 ppm 0,7995 ppm 1,7057 ppm 98,93%
Persen recovery tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar timbal, kadmium, dan tembaga dalam sampel. Hasil uji perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80 – 120% (Ermer dan Miller, 2005).
4.8 Simpangan Baku Relatif
Nilai simpangan baku dan simpangan baku relatif untuk timbal, kadmium, dan tembaga pada sampel kubis hijau dapat dilihat pada Tabel 4.7 sedangkan perhitungannya dapat dilihat pada Lampiran 20 halaman 79.
Tabel 4.7 Nilai Simpangan Baku dan Simpangan Baku Relatif Timbal, Kadmium, dan Tembaga dalam Kubis Hijau
Logam Simpangan Baku Simpangan Baku Relatif
Timbal 7,74 7,91 %
Kadmium 7,31 7,28 %
Tembaga 2,03 2,06 %
[image:52.595.118.480.597.657.2]90
hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Kubis hijau yang ditanam di pinggir Jalan Raya Jamin Ginting, Berastagi, Sumatera Utara tercemar logam berat timbal, kadmium, dan tembaga.
b. Kadar cemaran logam timbal pada kubis hijau segar yaitu 0,25455 ± 0,01371 mg/kg dan kubis hijau rebus yaitu 0,19635 ± 0,010739 mg/kg. Kadar cemaran logam kadmium pada kubis hijau segar yaitu 0,029915 ± 0,002901 mg/kg dan kubis hijau rebus yaitu 0,024842 ± 0,001584 mg/kg. Kadar cemaran logam tembaga pada kubis hijau segar yaitu 0,91473 ± 0,004081 mg/kg dan kubis hijau rebus yaitu 0,70805 ± 0,01298 mg/kg.
c. Terdapat perbedaan yang signifikan kadar cemaran logam timbal, kadmium, dan tembaga pada kubis hijau antara kubis hijau segar dan rebus menggunakan analisis statistik uji t dengan taraf kepercayaan α= 99%.
5.2 Saran
91
2. Sebaiknya masyarakat mengkonsumsi kubis hijau yang telah direbus dari pada secara mentah karena dengan merebus dapat mengurangi logam cemaran berbahaya dalam kubis hijau.
DAFTAR PUSTAKA
Akbar, R. (2015). Aneka Tanaman Apotek Hidup Di Sekitar Kita. Cetakan I. Jakarta: One Books. Hal. 114.
Arifin, Z. (2008). Beberapa Unsur Mineral Esensial Mikro Dalam Sistem Biologi Dan Metode Analisisnya. Jurnal Litbang Pertanian, 27(3), 2008. Hal. 101. Almatsier, S. (2002). Prinsip Dasar Ilmu Gizi. Cetakan IX. Jakarta: PT Gedia
Pustaka Utama. Hal. 250-254, 268-270.
Badan Standardisasi Nasional. (2009). Batas Maksimum Cemaran Logam Berat dalam Pangan.SNI 04-7387-2009. Penerbit: Badan Standardisasi Nasional (BSN). Hal. 1-2, 4, 6-7, 13 dan 19-20.
Clarke, E.G.C. (2004). Clark’s Analysis of Drugs and Poisons in Pharmaceuticals Body Fluids, and Postmortem Material. Disunting oleh: A. C. Moffat, M. D. Osselton, dan B. Widdop. Edisi III. London: Pharmaceutical Press. Hal. 325.
Darmono. (1995). Logam dalam Sistem Biologi Mahluk Hidup. Jakarta: Penerbit Universitas Indonesia (UI-Press). Hal. 7.
Ermer, J., dan ΜB. Miller, J.H..(2005). Method Validation in Pharmaceutical Analysis.Weinheim: Wiley-Vch Verlag GmbH & Co. KgaA. Hal. 171. Gandjar, I.B., dan Rohman, A. (2008). Kimia Farmasi Analisis. Cetakan III.
Yogyakarta: Pustaka Pelajar. Hal. 298-312, 319-321.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metoda dan Cara Perhitungannya. Majalah Ilmu Kefarmasian 1(3): 117-135.
Kaleka, N. (2013). Sayuran Hijau Apotek dalam Tubuh Kita. Cetakan I. Solo: Arcita. Hal.49-50.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Terjemahan: A. Saptorahardjo. (1990). Konsep Dasar Kimia Analitik. Jakarta: UI Press. Hal. 283
92
Prasetio, B. (2013). Budi Daya Sayuran Organik di Pot. Yogyakarta: Penerbit Andi. Hal. 137-138.
Sari, K.A., Riyadi, P.H., dan Anggo, A.D. (2014). Pengaruh Lama Perebusan dan Konsentrasi Larutan Jeruk Nipis (Citrus aurantifolia) Terhadap Kadar Timbal (Pb) dan Kadmium (Cd) pada Kerang Darah (Anadara granosa).
Jurnal Pengolahan dan Bioteknologi Hasil Perikanan 3(2): 2-9.
Setyaningrum, H., dan Saparinto, C. (2014). Panen Sayur Secara Rutin di Lahan Sempit. Cetakan III. Jakarta: Penebar Swadaya. Hal. 122-123 dan 130-131. Sudjana. (2005). Metode Statistika. Edisi VI. Bandung: Tarsito. Hal.93, 168, 239. Widaningrum, R., Miskiyah, M., dan Suismono, S. (2007). Bahaya Kontaminasi
Logam Berat dalam Sayuran dan Alternatif Pencegahan Cemarannya. Buletin Tekonologi Pascapanen Pertanian 3: 19-23.
Widowati, W., Sastiono, A., dan Jusuf, R. (2008). Efek Toksik Logam. Edisi I. Yogyakarta: Andi Offset. Hal. 63-71, 109-120, 183-190.
93
94
95
Lampiran 3. Bagan Alir Proses Pembuatan Larutan Sampel
dicuci dengan air hingga bersih ditiriskan selama 15 menit ditimbang ± 1 kg lalu dibagi 2
direbus di dalam ditimbang 50 g
air mendidih selama 5 menit
disaring dan ditiriskan
ditimbang 50 g
Sampel Kubis Hijau (Brassica oleracea L.) sebanyak 2 kg
Bagian I 500 g Bagian II 500 g
96
a. Pembuatan larutan sampel dari kubis segar
diarangkan di atas hotplate selama 8 jam diabukan di tanur (T= 5000C) selama 48 jam disimpan dalam desikator
dilarutkan dengan 10 ml HNO3 7N diencerkan dalam labu tentukur 100 ml dengan akuades bebas mineral
hingga garis tanda
disaring dengan kertas saring Whatmann no. 42 dengan membuang 2 ml larutan pertama hasil penyaringan
b. Pembuatan larutan sampel dari kubis rebus
diarangkan di atas hotplate selama 8 jam diabukan di tanur (T= 5000C) selama 48 jam disimpan dalam desikator
dilarutkan dengan 10 ml HNO3 5N diencerkan dalam labu tentukur 100 ml dengan akuades bebas mineral
hingga garis tanda
disaring dengan kertas saring Whatmann no. 42 dengan membuang 2 ml larutan pertama hasil penyaringan
Kubis segar
Abu putih
Larutan Sampel
Abu putih