KAPROLAKTON) SECARA IN VITRO
MARDIANA HARDIANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Asam Glikolat) dan Poli(ε-kaprolakton) secara In Vitro. Dibimbing oleh HENDRA ADIJUWANA dan AHMAD SJAHRIZA.
Polimer telah banyak diaplikasikan dalam kehidupan manusia, salah satunya adalah untuk penyalut obat. Polimer sintetik seperti poli(asamlaktat) (PLA), poli(asamglikolat) (PGA), poli(ε-kaprolakton) (PCL), poli(asam laktat-co-asam glikolat) (PLGA) merupakan jenis-jenis poliester yang banyak digunakan untuk penyalut obat. Para peneliti telah banyak yang melakukan penelitian tentang degradasi PLA, PGA, PCL, dan PLGA, tetapi belum ada yang melakukan penelitian tentang degradasi poliblend polimer ini, salah satunya adalah poliblend PLGA dan PCL.
Poliblend dibuat empat komposisi, yaitu PLGA (90:10):PCL 3:1, PLGA(75:25):PCL 3:1, PLGA (90:10):PCL 5:1, dan PLGA (75:25):PCL 5:1. Degradasi dilakukan selama delapan minggu dengan menggunakan bufer fosfat pH 7.4 dan suhu inkubasi 37°C. Degradasi polimer diamati dengan adanya perubahan massa, viskositas intrinsik, dan bentuk permukaannya. Hasil penelitian menunjukkan bahwa komposisi PLGA (75:25):PCL 5:1 merupakan komposisi yang paling cepat terdegradasi dibandingkan dengan komposisi lainnya. Ini terlihat dari perubahan massa hingga 89.06% dan viskositas intrinsik hingga 20.13%.
ABSTRACT
Mardiana Hardianti. In Vitro Polyblend Degradation of Copolymer Poly(lactic-co-glycolic acid) and Poly(ε-caprolactone). Supervised by HENDRA ADIJUWANA and AHMAD SJAHRIZA.
Polymer has many applications in human life, one of them is in the field of health. Polymer synthetics like polylactic acid (PLA), polyglycolic acid (PGA), poly(ε -caprolactone) (PCL), and poly(lactic acid-co-glycolic acid) were kind of polyesters that is many used in field of health. Many researchers have already made research about degradation of PLA, PGA, PCL, and PLGA. However, there is no one doing research about degradation of combination between this two polymers, one of them is polyblend of PLGA and PCL.
KAPROLAKTON) SECARA IN VITRO
MARDIANA HARDIANTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM
: G44203028
Menyetujui,
Pembimbing I,
Pembimbing II,
Ir. Hendra Adijuwana, MST
Drs. Ahmad Sjahriza
NIP 130 321 037
NIP 131 842 413
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
Maria atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan dengan baik. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2007 ini ialah polimer, dengan judul Degradasi Poliblend Kopolimer Poli(asam laktat-co-asam glikolat) dan Poli(ε-kaprolakton) secara In Vitro.
Penulis mengucapkan terima kasih kepada Bapak Ir. Hendra Adijuwana, MST dan Bapak Drs. Ahmad Sjahriza selaku pembimbing, serta Ibu Tetty Kemala, MSi yang telah banyak memberi saran dalam penelitian ini. Di samping itu, penulis juga menyampaikan penghargaan kepada staf Bagian Kimia Anorganik (Bapak Sawal, Bapak Caca, Ibu Nur, dan Ibu Siti Maemunah), staf Bagian Kimia Analitik (Bapak Eman), staf Bagian Biologi (Ibu Retno dan Ibu Yuli), dan staf Bagian Departemen (Mas Heri dan Bapak Didi) yang telah banyak membantu dalam penyusunan karya ilmiah ini.
Terima kasih yang begitu besar penulis ucapkan untuk papa (Alm.), mama, Dicky, Yulius, Yane, Eva Yunita, Santika, Hendra, dan Adi atas segala bantuan baik berupa materi, dukungan, doa, nasihat, dan kasih sayangnya. Penulis juga mengucapkan terima kasih atas dukungannya kepada Elyzabet, Nurhayani, Rio, Bekti, Eko, Nuryono, kak
Budi, dan teman-teman kimia angkatan 2003.
Akhir kata, semoga karya ilmiah ini bermanfaat.
Bogor, Agustus 2007
Howarman Indrajaya (†) dan Nurgiantie. Penulis merupakan anak keenam dari delapan bersaudara.
Tahun 2003 penulis lulus dari SMU Sint Carolus Bengkulu dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB (USMI). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Kopolimer Poli(asam laktat-co-asam glikolat) ... 1
Poli(ε-kaprolakton) ... 2
Poliblend PLGA dan PCL ... 2
Degradasi Polimer ... 2
Viskometri ... 3
BAHAN DAN METODE Bahan dan Alat ... 3
Pembuatan Poliblend PLGA dan PCL (Sujatmiko 2007) ... 3
Pembuatan Buffer Fosfat pH 7.4 (Mulyono 2005) ... 4
Degradasi Poliblend secara In Vitro (Kiremitci-Gumusderelioglu& Gunday 1999) ... 4
Uji Degradasi Poliblend ... 4
HASIL DAN PEMBAHASAN Pembuatan Poliblend PLGA dan PCL ... 4
Degradasi Poliblend secara In Vitro ... 4
Perubahan Massa Sampel ... 5
Perubahan Viskositas Intrinsik ... 6
Perubahan Bentuk Permukaan Poliblend ... 6
SIMPULAN DAN SARAN Simpulan ... 7
Saran ... 8
DAFTAR PUSTAKA ... 8
1 Waktu dan produk degradasi dari beberapa polimer poliester ... 3
2 Komposisi PLGA dan PCL ... 4
DAFTAR GAMBAR
Halaman 1 Reaksi pembuatan PLGA (Kurniawan 2007) ... 12 Difraktogram XRD PLGA pada komposisi a) 75:25 dan b) 90:10 (Kurniawan 2007) ... 2
3 Struktur kimia PCL (Huang & Edelman 1995) ... 2
4 Difraktogram XRD PCL (Sujatmiko 2007) ... 2
5 Viskometer-Ostwald Cannon Fenske Routine ... 3
6 Bentuk permukaan visual poliblend dari komposisi (a) A, (b) B, (c) C, dan (d) D ... 5
7 Perubahan massa sampel ... 5
8 Laju perubahan massa sampel ... 6
9 Perubahan viskositas intrinsik ... 7
10 Bentuk permukaan awal polimer dengan perbesaran 2x10x5 pada komposisi a) A, b) B, c) C, dan d) D ... 7
11 Bentuk permukaan polimer setelah terdegradasi dengan perbesaran 2x10x5 pada komposisi a) A, b) B, c) C, dan d) D ... 7
DAFTAR LAMPIRAN
Halaman 1 Diagram alir kerja penelitian ... 112 Data perubahan dan laju perubahan massa poliblend PLGA dan PCL ... 12
3 Data viskositas intrinsik PLGA(90:10):PCL 3:1 selama waktu degradasi. 13
4 Data viskositas intrinsik PLGA(75:25):PCL 3:1 selama waktu degradasi. 17
5 Data viskositas intrinsik PLGA(90:10):PCL 5:1 selama waktu degradasi. 21
6 Data viskositas intrinsik PLGA(75:25):PCL 5:1 selama waktu degradasi. 25
kehidupan manusia. Salah satu bidang aplikasi polimer adalah di bidang kesehatan (medical applications). Aplikasi polimer ini meliputi pembuatan pin, benang jahit operasi, rekayasa jaringan, sistem pengungkungan obat, dan aplikasi dalam bidang kesehatan gigi.
Polimer yang dapat diaplikasikan dalam bidang kesehatan harus dapat terdegradasi dengan baik di dalam tubuh. Fibrin, kolagen, kitosan, dan gelatin merupakan jenis polimer alam yang telah banyak diaplikasikan dalam bidang kesehatan. Polimer biodegradabel sintetik yang telah banyak diaplikasikan dalam bidang kesehatan adalah poli(asamlaktat) (PLA), poli(asamglikolat) (PGA), poli(asam laktat-co-asam glikolat) (PLGA), dan poli(ε-kaprolakton) (PCL).
Para peneliti banyak yang memilih menggunakan polimer biodegradabel sintetik karena bentuk molekulnya yang dapat direkayasa, bebas dari sifat imunogenitas, dan bahan asalnya berasal dari sumber yang dapat diperbaharui. Polimer sintetik yang banyak digunakan adalah PCL dan PLGA. PCL hanya sesuai untuk sistem penyalut obat jangka panjang, karena sifat kristalinitas yang tinggi dan waktu degradasi yang lambat. Sementara itu, PLGA bersifat biokompatibel dengan sifat degradasi yang dapat disesuaikan, bergantung pada nisbah molar komponen monomer individu. Namun, kelemahan PLGA adalah memiliki elongasi saat putus yang rendah karena mudah putus saat regangan akibat tekanan (Porjazoska et al. 2004). Oleh karena itu, penelitian untuk menggabungkan sifat antara dua polimer ini pernah dilakukan oleh Sujatmiko (2007).
Penelitian untuk mencampur PLGA dan PCL telah dilakukan guna mendapatkan sifat terbaru dari kelebihan dan kelemahan masing-masing polimer tetapi belum ada pihak yang pernah melakukan degradasi terhadap polimer hasil penggabungan (polyblend) ini. Penelitian dari Porjazoska et al. (2004a) dan Kiremitci-Gumusderelioglu & Deniz (1999) hanya membahas tentang degradasi PLGA, yaitu dengan semakin tingginya nisbah asam glikolat, PLGA akan semakin cepat terdegradasi. Dalam penelitian lain,Edlund & Albertson (2002) juga hanya membahas tentang degradasi kopolimer asam 6-hidroksikaproat dan L-asam laktat secara in vitro pada kopolimer ini bergantung pada komposisi L-asam laktat dan kristalinitas asam 6-hidroksikaproat. Oleh karena itu,
perubahan yang terjadi selama poliblend ini terdegradasi. Penelitian ini bertujuan mengetahui komposisi dari poliblend PLGA dan PCL yang memiliki waktu degadasi relatif singkat dengan mengamati perubahan dari viskositas intrinsik, massa, dan bentuk permukaan selama masa degradasi.
TINJAUAN PUSTAKA
Kopolimer Poli(asam laktat-co-asam glikolat)
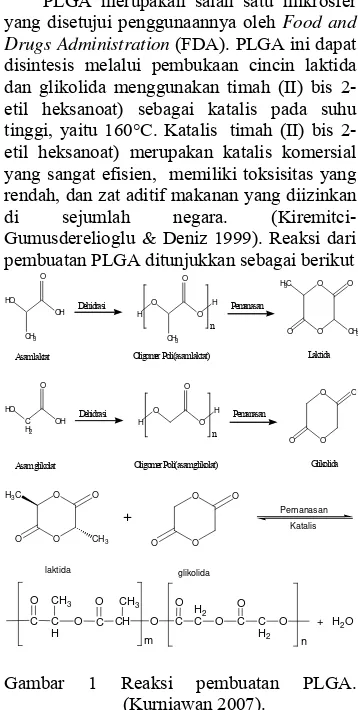
PLGA merupakan salah satu mikrosfer yang disetujui penggunaannya oleh Food and Drugs Administration (FDA). PLGA ini dapat disintesis melalui pembukaan cincin laktida dan glikolida menggunakan timah (II) bis 2-etil heksanoat) sebagai katalis pada suhu tinggi, yaitu 160°C. Katalis timah (II) bis 2-etil heksanoat) merupakan katalis komersial yang sangat efisien, memiliki toksisitas yang rendah, dan zat aditif makanan yang diizinkan di sejumlah negara. (Kiremitci-Gumusderelioglu & Deniz 1999). Reaksi dari pembuatan PLGA ditunjukkan sebagai berikut
OH CH3 O HO Dehidrasi H O O CH3 O H n O O O O H3C
CH3
Asam laktat Oligomer Poli(asam laktat) Laktida Pemanasan C H2 OH O HO Dehidrasi H O O O H n O O O O
Asam glikolat Oligomer Poli(asam glikolat) Glikolida Pemanasan
O
O O
O H3C
CH3 O
O O O + Pemanasan Katalis laktida glikolida C C H
O CH3
O C O CH O CH3 C H2 C O O C O C H2
O + H2O
m n
Gambar 1 Reaksi pembuatan PLGA. (Kurniawan 2007).
0 50 100 150 200 250 300 350
20 30 40 50 60 70 80 90
2 tetha in te n s it a s
(a) (b)
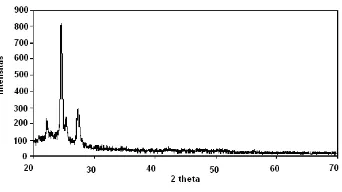
Gambar 2 Difraktogram XRD PLGA pada komposisi a) 75:25 dan b) 90:10. (Kurniawan 2007).
Poli(ε-kaprolakton)
PCL dapat disintesis dengan polimerisasi pembukaan cincin dari monomer ε -kaprolakton. PCL adalah plastik biodegradabel bersifat termoplastik. PCL memiliki sifat tahan terhadap air, minyak, pelarut, dan klorin. PCL juga memiliki transisi kaca -65 sampai 60°C dan titik leleh (58-63)°C (Matsumura 2005). Perkiraan waktu degradasi dari PCL adalah lebih dari 24 bulan.(Gunatillake & Raju 2003). PCL yang digunakan memiliki Mn = 42500 dan Mw =
65000. Gambar 3 menunjukkan struktur kimia PCL.
O (CH2)5C O
n
Gambar 3 Struktur Kimia PCL. (Huang & Edelman 1995).
Menurut Sujatmiko (2007), PCL yang digunakan pada penelitian ini termasuk jenis polimer semikristalin. Hal ini ditunjukkan pada Gambar 4 yang ditandai dengan adanya puncak-puncak yang tajam. Bentuk kristal dapat terjadi karena struktur rantai PCL yang linear, sehingga kerapatan ruang tinggi dan menjadi lebih teratur.
Gambar 4 Difraktogram XRD PCL. (Sujatmiko 2007).
Poliblend PLGA dan PCL
Proses blending dalam polimer dikelompokkan menjadi dua jenis, yaitu blending fisika dan blending kimia. Blending fisika yaitu pencampuran secara fisika antara dua jenis polimer atau lebih yang memiliki struktur berbeda dan tidak membentuk ikatan kovalen antara komponen-komponennya. Hasil pencampuran ini disebut poliblend. Interaksi yang terjadi dalam poliblend adalah ikatan Van der Waals dan ikatan hidrogen (Rabek 1980).
Poliblend dapat dibedakan menjadi dua jenis, yaitu poliblend homogen dan heterogen. Poliblend homogen akan terlihat transparan, mempunyai titik leleh tunggal, dan sifat fisiknya sebanding dengan komposisi komponen-komponen penyusunnya, sedangkan poliblend heterogen terlihat tidak
jelas dan mempunyai beberapa titik leleh (Brown 1988). Menurut penelitian Sujatmiko (2007), semakin banyak komposisi PCL maka semakin tinggi derajat kristalinitas pada poliblend.
Degradasi Polimer
Degradasi adalah reaksi yang mencakup pemutusan ikatan kimia dalam makromolekul. Mekanisme degradasi dapat melalui dua cara yaitu secara enzimatik dan hidrolisis. Degradasi dapat terjadi melalui empat tahap yaitu penyerapan air, pengurangan kekuatan mekaniknya (modulus dan kekuatan), pengurangan massa molar, dan kehilangan massa.
terdegradasi sekitar 2 sampai 6 bulan tergantung dari perbandingan komposisi monomer-monomernya. Menurut penelitian Kiremitci-Gumusderelioglu & Deniz (1999) komposisi PLGA akan lebih cepat terdegradasi jika nisbah asam glikolatnya meningkat. Hal ini karena asam glikolat memiliki sifat hidrofilik yang dapat mengakibatkan kapasitas menyerap air tinggi sehingga degradasi hidrolitik cepat terjadi. Produk degradasi dari PLGA adalah asam laktat dan asam glikolat yang akan masuk ke siklus Krebs dan akan dilepaskan sebagai karbon dioksida dan air (Bhattacharya et al. 2005)
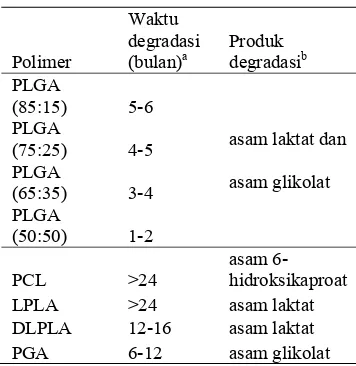
Tabel 1 Waktu dan produk degradasi dari beberapa polimer poliester
Polimer Waktu degradasi (bulan)a Produk degradasib PLGA (85:15) 5-6 PLGA
(75:25) 4-5 asam laktat dan PLGA
(65:35) 3-4 asam glikolat PLGA
(50:50) 1-2
PCL >24 asam 6-hidroksikaproat LPLA >24 asam laktat DLPLA 12-16 asam laktat PGA 6-12 asam glikolat a
Demsey et al. 2003, diacu dalam Robani 2004
b
Edlund & Albertson 2002.
Viskometri
Viskometri merupakan metode yang digunakan untuk menentukan ketahanan suatu cairan terhadap aliran (deformasi). Pengukuran-pengukuran viskositas larutan encer memberikan teknik yang paling sederhana dan paling banyak dipakai untuk menetapkan bobot molekul secara rutin. Viskositas diukur dengan cara menetapkan lamanya aliran sejumlah volume larutan melalui kapiler yang panjangnya tetap. Waktu alir dalam detik dicatat sebagai waktu untuk miniskus lewat antara dua tanda batas pada viskometer (Steven 2001).
Metode ini mengukur viskositas dengan cara membandingkan waktu alir pelarut dan larutan polimer pada berbagai kepekatan atau konsentrasi. Viskometer memiliki keunggulan, yaitu untuk mencapai berbagai
konsentrasi, larutan polimer dapat diencerkan dalam viskometer dengan menambahkan sejumlah terukur pelarut. (Steven 2001). Gambar viskometer Ostwald yang digunakan ditunjukkan pada Gambar 5.
Gambar 5 Viskometer Ostwald-Cannon Fenske Routine.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah PLGA 90:10 dan PLGA 75:25 dari penelitian Kurniawan 2007, PCL (Aldrich), kristal K2HPO4·3H2O, kristal KH2PO4,
diklorometana, dan akuades.
Alat-alat yang digunakan adalah gelas piala, labu takar, pipet Mohr, magnet, pengaduk magnet, teflon, penangas air, vial, neraca analitik, kaca preparat, viskometer Ostwald-Cannon Fenske Routine, aspirator, dan mikroskop stereo Nikon JBIC.
Pembuatan Poliblend PLGA dan PCL (Sujatmiko 2007)
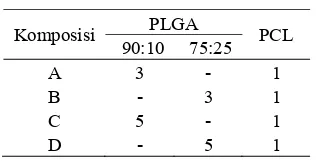
Tabel 2 Komposisi PLGA dan PCL
Komposisi PLGA PCL 90:10 75:25
A 3 - 1
B - 3 1
C 5 - 1
D - 5 1
Pembuatan Bufer Fosfat pH 7.4 (Mulyono 2005)
Kristal K2HPO4·3H2O ditimbang
sebanyak 45.6807 g lalu dilarutkan dengan akuades dan ditepatkan hingga menjadi larutan 1 liter. Kristal KH2PO4 ditimbang
sebanyak 27.2501 g lalu dilarutkan dengan akuades dan ditepatkan hingga menjadi larutan 1 liter.
Larutan K2HPO4·3H2O sebanyak 81 ml
ditambahkan dengan 19 ml larutan KH2PO4.
Campuran larutan ini diencerkan hingga 1 liter. Larutan diukur pH-nya, bila pH > 7.4 maka ditambah KH2PO4, namun bila pH < 7.4
maka ditambah K2HPO4·3H2O hingga pH
mencapai 7.4.
Degradasi Poliblend secara In Vitro
(Kiretmici-Gumusderelioglu & Deniz 1999)
Masing-masing komposisi film dipotong kecil-kecil berukuran 1x1 cm lalu ditaruh di dalam botol vial yang telah diberi label 1, 2, 3, 4, 5, 6, 7, dan 8. Sampel ini direndam dengan bufer fosfat pH 7.4 dan diinkubasi pada suhu 37°C selama 8 minggu. Setiap minggu, semua komposisi diukur nilai viskositas intrinsiknya dan perubahan massa sampel.
Uji Degradasi Poliblend
Degradasi sampel dilakukan dengan mengamati perubahan sampel setiap minggu yaitu perubahan massa sampel, viskositas intrinsik serta perubahan bentuk permukaan sampel saat minggu ke-0 dan minggu ke-8.
Setiap film dari masing-masing komposisi diambil setiap minggu dan dikeringkan pada suhu ruang lalu ditimbang perubahan massanya menggunakan neraca analitik. Setelah itu, sampel dilarutkan menggunakan pelarut diklorometana sampai homogen lalu larutan ditera menggunakan labu takar 25 ml. Larutan dipipet sebanyak 10 ml ke dalam viskometer Ostwald untuk
menentukan waktu alir tanpa sampel dan waktu alir sampel berbagai konsentrasi. Pengukuran dilakukan pada temperatur ruang (temperatur konstan). Setelah itu, viskositas relatif (ηr) ditentukan dengan cara
membandingkan waktu alir pelarut dengan waktu alir larutan polimer (t0/t). Viskositas
intrinsik [η] dicari dengan cara memplotkan η reduktif sebagai sumbu y dan konsentrasi sebagai sumbu x.
)
100
/
(
1
ml
g
i
konsentras
t
t
spesifik reduktif relatif spesifik pelarut sampel relatifη
η
η
η
η
=
−
=
=
Pengamatan perubahan bentuk permukaan sampel pada minggu ke-0 dan minggu ke-8 dilakukan dengan menggunakan mikroskop stereo. Sampel diambil beberapa milimeter lalu ditaruh di kaca preparat dan diamati bentuk permukaannnya dengan mengatur perbesaran pada mikroskop sehingga bentuk permukaan sampel dapat teramati dengan baik.
HASIL DAN PEMBAHASAN
Pembuatan Poliblend PLGA-PCL
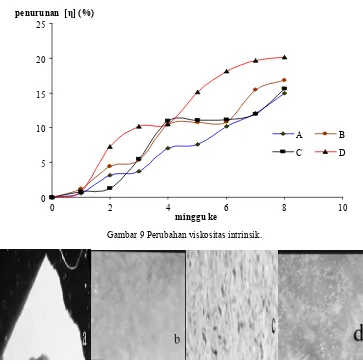
Poliblend dibuat dengan komposisi seperti yang ditunjukkan pada Tabel 2. Gambar 6 menunjukkan bentuk permukaan visual dari poliblend. Komposisi A dan B memiliki homogenitas yang lebih baik dan tingkat kerapuhan yang lebih rendah daripada komposisi C dan D.
Degradasi Poliblend secara In Vitro
Gambar 6 Bentuk permukaan visual poliblend dari komposisi (a) A, (b) B, (c) C, dan (d) D.
Perubahan Massa sampel
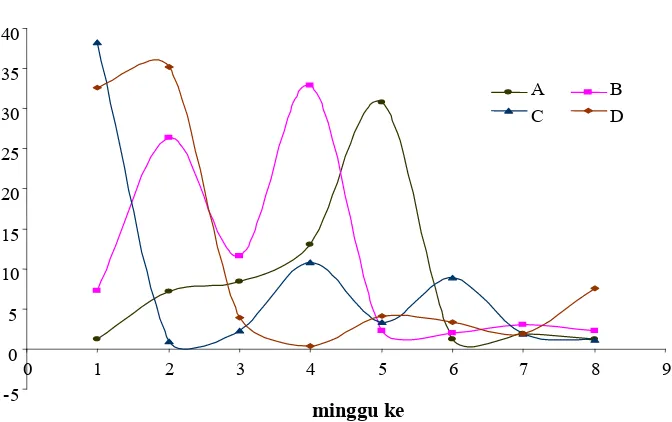
Sampel yang telah terjadi degradasi dapat diamati dari perubahan massa sampelnya. Gambar 7 menunjukkan bahwa sampel yang mengalami degradasi akan mengalami penurunan massa dari minggu ke-0 hingga minggu ke-8. Komposisi D yang terdiri dari PLGA dan PCL dengan nisbah 5:1 merupakan poliblend yang memiliki penurunan massa yang paling cepat daripada komposisi lainnya. Hal ini dikarenakan komposisi PLGAnya yang terdiri dari 75% asam laktat dan 25% asam glikolat lebih banyak daripada PCLnya sehingga sifat dari PLGA cenderung lebih mempengaruhi dari PCLnya. Penurunan massa yang terjadi pada komposisi D mencapai 89.06%. Komposisi lainnya yang telah mengalami degradasi berturut-turut adalah komposisi B, C, dan A dengan persen penurunan massanya adalah 87.69%, 67.77%, dan 64.91%. Komposisi A mengalami degradasi paling lama diantara lainnya karena pengaruh dari komposisi PLGAnya yaitu 90% asam laktat dan 10%
asam glikolat sehingga komposisi ini kurang hidrofilik. Selain itu, nisbah PLGA:PCL 3:1 membuat sifat PLGA kurang mempengaruhi jika dibandingkan dengan komposisi PLGA:PCL 5:1. Data penurunan massa ditunjukkan pada Lampiran 2.
Gambar 8 menunjukkan laju perubahan massa sampel yang fluktuatif. Pada gambar ini terlihat bahwa komposisi A memiliki perubahan laju yang signifikan pada minggu kelima sedangkan komposisi B memiliki 2 perubahan laju yaitu pada minggu kedua dan keempat. Komposisi C dan D memiliki perubahan laju signifikan di minggu pertama lalu laju ini relatif stabil hingga minggu kedelapan. Hal ini dikarenakan komposisi C dan D telah mengalami degradasi pada awal minggu perendaman dengan menggunakan bufer sedangkan komposisi A dan B masih akan mengalami degradasi pada minggu berikutnya. Data ini menunjukkan bahwa dengan semakin tinggi nisbah komposisi PLGA dari PCL akan membuat poliblend yang dihasilkan lebih cepat terdegradasi. .
Gambar 7 Perubahan massa sampel. 0
10 20 30 40 50 60 70 80 90 100
0 1 2 3 4 5 6 7 8 9
minggu ke
A B
C D
Gambar 8 Laju perubahan massa sampel.
Perubahan Viskositas Intrinsik
Proses degradasi ini juga dapat ditunjukkan dari penurunan viskositas intrinsik yang diperlihatkan pada Gambar 9. Viskositas intrinsik merupakan besaran yang sebanding dengan bobot molekul menurut persamaan Mark-Houwink. Viskositas intrinsik akan semakin menurun seiring dengan lamanya degradasi yang terjadi. Penurunan viskositas ini menandakan telah putusnya rantai polimer sehingga menyebabkan berkurangnya bobot polimer. Pada poliblend ini proses degradasi diawali dengan pemutusan ikatan Van Der Waals diikuti dengan pemutusan rantai polimer menjadi bentuk monomer-monomernya. Gambar 9 menujukkan bahwa viskositas intrinsik semakin menurun pada komposisi D. Viskositas intrinsik menurun hingga mencapai 20.13%. Komposisi A mengalami perubahan viskositas intrinsik hanya 14.97% dari nilai viskositas intrinsik awalnya. Data penurunan viskositas intrinsik ditunjukkan pada Lampiran 7.
Perubahan Bentuk Permukaan Poliblend
Degradasi poliblend ini juga didukung dengan foto dari bentuk permukaan setiap komposisi polimer pada saat sebelum dan sesudah degradasi. Gambar 10 memperlihatkan bentuk permukaan polimer awal sebelum didegradasi. Gambar 11 menunjukkan bentuk permukaan polimer setelah terdegradasi. Permukaan polimer yang telah terdegradasi ditandai dengan adanya lubang-lubang kecil. Lubang-lubang kecil ini terjadi akibat adanya interaksi air yang menyebabkan hidrolisis pada rantai polimer.
Gambar 11 ini menggunakan perbesaran 2x10x5. Degradasi tercepat ditandai dengan banyaknya lubang beserta ukurannya yang terdapat di permukaan polimer. Ini dapat dilihat di komposisi D yang memiliki ukuran dan banyaknya lubang yang lebih besar daripada komposisi B. Pada komposisi A, degradasi belum terlihat karena belum adanya lubang-lubang yang ada. Komposisi C juga telah terdegradasi yang ditandai dengan adanya lubang-lubang yang muncul. Lubang-lubang ini lebih sedikit jika dibandingkan dengan komposisi B.
-5 0 5 15 20 25 30 35 40
0 1 2 3 4 5 6 7 8 9
A B
C D
10
laju perubahan massa
Gambar 9 Perubahan viskositas intrinsik.
Gambar 10 Bentuk permukaan awal polimer dengan perbesaran 2x10x5 pada komposisi a) A, b) B, c) C, dan d) D.
Gambar 11 Bentuk permukaan polimer setelah terdegradasi dengan perbesaran 2x10x5 pada komposisi a) A, b) B, c) C, dan d) D.
SIMPULAN DAN SARAN
Simpulan
Degradasi telah terjadi pada komposisi D yaitu PLGA (75:25):PCL 5:1. Hal ini terlihat dari persen pengurangan massa polimer
hingga 89.06%, persen penurunan viskositas intrinsik hingga menjadi 20.13%, dan foto mikroskop bentuk permukaan polimer. Degradasi paling cepat terjadi pada PLGA yang memiliki komposisi asam glikolat tinggi dengan pengaruh dari sifat PCL yang semakin rendah.
0 5 10 15 20 25
0 2 4 6 8 10
A B
C D
penurunan [η] (%)
Saran
Penurunan bobot molekul perlu dilakukan menggunakan gel permeation chromatograph (GPC). Untuk foto bentuk permukaan lebih baik menggunakan scanning microscope electron (SEM). Selain itu, analisis terhadap produk akhir yang dihasilkan juga perlu dilakukan dengan menggunakan high performance liquid chromatograph (HPLC). Perlu juga diadakan penelitian lanjutan tentang penyebab poliblend ini memiliki laju perubahan massa yang fluktuatif.
DAFTAR PUSTAKA
Bhattacharya M, Reis RL, Correlo V, Boesel L. 2005. Material properties of biodegradable polymers. Di dalam: Smith R, editor. Biodegradable Polymers for Industrial Applications. England: Woodhead Publishing. hlm. 343-345.
Billings DM. 2005. Lippincott’s Review for NCLEX-RN. Philladelphia: Lippincott Williams & Wilkins.
Brown ME. 1988. Introduction to Thermal Analysis Techniques and Applications. London: Chapman and Hall.
Edlund U, Albertson AC. 2002. Degradable Polymer Microsphere for Controlled Drug Delivery. Di dalam: Albertson AC, editor. Degradable Aliphatic Polyesters. New York: Springer. hlm. 70-85.
Farahani TD, Entezami AA, Mobedi H, Abtahi M. 2005. Degradation of poly(d,l-lactide-co-glycolide) 50:50 implant in aqueous Medium. Iranian Polym J 14:753-763.
Gunatillake PA, Raju A. 2003. Biodegradable synthetic polymers for tissue enginerring. Eur Cells and Materials.5:1-16.
HAM Mulyono. 2005. Membuat Reagen Kimia di Laboratorium. Jakarta: Bumi Aksara.
Huang SJ, Edelman PG. 1995. An overview of biodegradable of polymer. Di dalam: Scott G, Dan G, editor. Degradable Polymers: Principles & Applications. London: Chapman & Hall. hlm 18-19.
Karlsson S, Albertson AC. 1995. Technique and mechanism of polymer degradation. Di dalam: Scott G, Dan G, editor. Degradable Polymers: Principles & Applications. London: Chapman & Hall. hlm 29-30.
Kiretmici-Gumusdereliouglu, Deniz G. 1999. Synthesis, characterization and in vitro degradation of poly(d,l-lactide)/poly(d,l-lactide-co-glycolide) films. Turk J Chem 23:153-161.
Kurniawan F. 2007. Pembuatan dan pencirian kopolimer poli(asam laktat)-poli(asam glikolat) menggunakan katalis timah oktoat. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Li S, Vert M. 1995. Biodegadation of aliphatic polyesters. Di dalam: Scott G, Dan G, editor. Degradable Polymers: Principles & Applications. London: Chapman & Hall. hlm 43-46, 54-58.
Madras G. 2005. Enzymatic degradation of polymers. Di dalam: Smith R, editor. Biodegradable Polymers for Industrial Applications. England: Woodhead Publishing. hlm. 419-422.
Matsumura S. 2005. Mechanism of biodegradation. Di dalam: Smith R, editor. Biodegradable Polymers for Industrial Applications. England: Woodhead Publishing. hlm. 357-361, 365-369.
Pethrick RA. 1999. Polymer Yearbook 16. Glasgow: University of Strathclyde.
Porjazoska A, et al. 2004. Synthesis and characterization of biocompatible multicomponent polymer systems as supports for cell cultures. Buletin of the chemists & tecnologiest of macedonia 23:147-156.
Porjazoska A et al. 2004a. Poly(lactide-co-glycolide) microparticles as system for controlled release of protein-preparation and characterization. Acta Pharm 54:215-229.
Robani MN. 2004. Biodegradasi struktur dan morfologi mikrosfer polilaktat. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Saladin. 2005. Human Anatomy. New York: McGraw.
Shi D. 2005. Introduction To Biomaterials. Tsinghua University Press.
Steven MP. 2001. Kimia Polimer. Sopyan I, penerjemah. Jakarta: Erlangga. Terjemahan dari Polymer Chemistry: An Introduction.
Sujatmiko R. 2007. Pencirian poliblend kopolimer poli(asamlaktat)-
poli(asamglikolat) dengan poli(ε -kaprolakton). [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lampiran 1 Diagram alir kerja penelitian
Pembuatan poliblend PLGA dan PCL
Pembuatan film
massa awal
Pengukuran awal viskositas awal
Foto bentuk permukaan awal
massa
Degradasi film
viskositas
massa akhir
Pengukuran akhir viskositas
Foto bentuk permukaan akhir
Data
Lampiran 2 Data perubahan dan laju perubahan massa poliblend PLGA dan PCL
Komposisi Minggu ke perubahan massa (%) Selisih perubahan massa
A
0 0
-1 -1,24 1,24
2 8,39 7,15
3 16,77 8,38
4 29,81 13,04
5 60,56 30,75
6 61,80 1,24
7 63,66 1,86
8 64,91 1,25
B
0 0 -
1 7,29 7,29
2 33,67 26,38
3 45,23 11,56
4 78,14 32,91
5 80,40 2,26
6 82,41 2,01
7 85,43 3,02
8 87,69 2,26
C
0 0 -
1 38,25 38,25
2 39,22 0,97
3 41,55 2,33
4 52,43 10,88
5 55,73 3,30
6 64,66 8,93
7 66,60 1,94
8 67,77 1,17
D
0 0 -
1 32,62 32,62
2 67,77 35,15
3 71,68 3,91
4 72,07 0,39
5 76,17 4,10
6 79,49 3,32
7 81,45 1,96
Lampiran 3 Data viskositas intrinsik PLGA(90:10):PCL 3:1 selama waktu degradasi
PLGA (90:10) :PCL 3:1 awal
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.1288 28.87 27.84 1.0370 0.0370 0.2872
0.0773 28.51 27.84 1.0241 0.0241 0.3113 0.0464 28.29 27.84 1.0162 0.0162 0.3484 0.0278 28.14 27.84 1.0108 0.0108 0.3876 0.0167 28.02 27.84 1.0065 0.0065 0.3892
PLGA (90:10) :PCL 3:1 minggu 1
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.1272 28.82 27.84 1.0352 0.0352 0.2767 0.0763 28.49 27.84 1.0233 0.0233 0.3059 0.0458 28.29 27.84 1.0162 0.0162 0.3530 0.0275 28.14 27.84 1.0108 0.0108 0.3927 0.0165 28.01 27.84 1.0061 0.0061 0.3704
PLGA (90:10) :PCL 3:1 minggu 2
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.1180 28.65 27.84 1.0291 0.0291 0.2466 0.0708 28.42 27.84 1.0208 0.0208 0.2943
0.0425 28.24 27.84 1.0144 0.0144 0.3382 0.0255 28.09 27.84 1.0090 0.0090 0.3523
0.0153 28.00 27.84 1.0057 0.0057 0.3758 y = -1,0112x + 0,3990
R2 = 0,9025
0,00 0,10 0,20 0,30 0,40 0,50
0,00 0,02 0,04 0,06 0,08 0,10 0,12 0,14 Konsentrasi (g/dl)
η reduktif
y = -0,9598x + 0,4014 R2 = 0,9290
0,00 0,10 0,20 0,30 0,40 0,50
0,00 0,05 0,10 0,15 konsentrasi (g/dl)
Lanjutan Lampiran 3
PLGA (90:10) :PCL 3:1 minggu 3
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c
0.1072 28.58 27.84 1.0266 0.0266 0.2480 0.0643 28.38 27.84 1.0194 0.0194 0.3016 0.0386 28.19 27.84 1.0126 0.0126 0.3258 0.0232 28.08 27.84 1.0086 0.0086 0.3723 0.0139 27.98 27.84 1.0050 0.0050 0.3620
PLGA (90:10) :PCL 3:1 minggu 4
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0904 28.67 27.84 1.0298 0.0298 0.3298 0.0542 28.35 27.84 1.0183 0.0183 0.3377 0.0325 28.16 27.84 1.0115 0.0115 0.3532
0.0195 28.04 27.84 1.0072 0.0072 0.3692 0.0117 27.96 27.84 1.0043 0.0043 0.3679
y = -1,2354x + 0,3887 R2 = 0,988
0,00 0,10 0,20 0,30 0,40
0,00 0,05 0,10 0,15 Konsentrasi (g/dl)
η reduktif
y = -1,3081x + 0,3866 R2 = 0,9594
0,00 0,10 0,20 0,30 0,40
0,00 0,02 0,04 0,06 0,08 0,10 0,12 Konsentrasi (g/dl)
η reduktif
y = -0,5248x + 0,3732
R 2 = 0,9175
0,00 0,10 0,20 0,30 0,40
0,00 0,02 0,04 0,06 0,08 0,10 Konsentrasi (g/dl)
Lanjutan Lampiran 3
PLGA (90:10) :PCL 3:1 minggu 5
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.0508 28.58 27.84 1.0266 0.0266 0.5232
0.0305 28.25 27.84 1.0147 0.0147 0.4832 0.0183 28.07 27.84 1.0083 0.0083 0.4517 0.0110 27.96 27.84 1.0043 0.0043 0.3928 0.0066 27.91 27.84 1.0025 0.0025 0.3819
PLGA (90:10) :PCL 3:1 minggu 6
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.0492 28.52 27.84 1.0244 0.0244 0.4964
0.0295 28.21 27.84 1.0133 0.0133 0.4502 0.0177 28.04 27.84 1.0072 0.0072 0.4056
0.0106 27.95 27.84 1.0040 0.0040 0.3718 0.0064 27.91 27.84 1.0025 0.0025 0.3943
PLGA (90:10) :PCL 3:1 minggu 7
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c
0.0468 28.52 27.84 1.0244 0.0244 0.5219 0.0281 28.19 27.84 1.0126 0.0126 0.4477 0.0168 28.05 27.84 1.0075 0.0075 0.4477 0.0101 27.95 27.84 1.0040 0.0040 0.3909 0.0061 27.90 27.84 1.0022 0.0022 0.3553
y = 3,2341x + 0,3708 R2 = 0,9238
0,00 0,10 0,20 0,30 0,40 0,50 0,60
0,00 0,02 0,04 0,06
Konsentrasi (g/dl)
η reduktif
y = 2,787x + 0,3604 R2 = 0,9323
0,00 0,10 0,20 0,30 0,40 0,50 0,60
0,00 0,01 0,02 0,03 0,04 0,05 0,06 Konsentrasi (g/dl)
Lanjutan Lampiran 3
PLGA (90:10) :PCL 3:1 minggu 8
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0452 28.49 27.84 1.0233 0.0233 0.5165 0.0271 28.16 27.84 1.0115 0.0115 0.4238 0.0163 28.03 27.84 1.0068 0.0068 0.4194 0.0098 27.94 27.84 1.0036 0.0036 0.3673 0.0059 27.90 27.84 1.0022 0.0022 0.3729
Contoh perhitungan:
Minggu ke 8, konsentrasi 0.0452 g/100ml:
pelarut sampel relatif
t
t
=
η
84
.
27
49
.
28
=
= 1.02331
−
=
relatif spesifikη
η
= 1.0233 – 1 = 0.0233
)
100
/
(
g
ml
i
konsentras
spesifik reduktifη
η
=
0452
.
0
0233
.
0
=
= 0.5165
Persamaan garis yang terbentuk y = a + bx Dengan y = η reduktif
a = [η]
x = konsentrasi (g/100ml) Persamaan garis yang terbentuk
y = 3.7327x + 0.3413 sehingga a = [η] = 0.3413. R2 = 0,9037
0,00 0,10 0,20 0,30 0,40 0,50 0,60
0,00 0,01 0,02 0,03 0,04 0,05 Konsentrasi (g/dl)
η reduktif
y = 3,6875x + 0,3531
R2 = 0,9449
0,00 0,10 0,20 0,30 0,40 0,50 0,60
0,00 0,01 0,02 0,03 0,04 0,05 Konsentrasi (g/dl)
η reduktif
Lampiran 4 Data viskositas intrinsik PLGA(75:25):PCL 3:1 selama waktu degradasi
PLGA (75:25) : PCL 3:1 awal
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.1592 28.89 27.84 1.0377 0.0377 0.2369
0.0955 28.62 27.84 1.0280 0.0280 0.2933 0.0573 28.37 27.84 1.0190 0.0190 0.3322 0.0344 28.18 27.84 1.0122 0.0122 0.3552 0.0206 28.07 27.84 1.0083 0.0083 0.4004
PLGA (75:25) : PCL 3:1 minggu 1
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.1476 28.86 27.84 1.0366 0.0366 0.2482 0.0886 28.55 27.84 1.0255 0.0255 0.2880 0.0531 28.33 27.84 1.0176 0.0176 0.3312 0.0319 28.18 27.84 1.0122 0.0122 0.3831 0.0191 28.04 27.84 1.0072 0.0072 0.3756
PLGA (75:25) : PCL 3:1 minggu 2
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.1056 28.71 27.84 1.0313 0.0313 0.2959 0.0634 28.41 27.84 1.0205 0.0205 0.3231 0.0380 28.21 27.84 1.0133 0.0133 0.3496 0.0228 28.08 27.84 1.0086 0.0086 0.3779 0.0137 27.98 27.84 1.0050 0.0050 0.3674
y = -1,0897x + 0,4036 R 2 = 0,9573
0,00 0,10 0,20 0,30 0,40 0,50
0,00 0,05 0,10 0,15 0,20 Konsentrasi (g/dl)
η reduktif
y = -1,0806x + 0,3988 R2 = 0,9419
0,00 0,10 0,20 0,30 0,40 0,50
0,00 0,05 0,10 0,15 0,20 Konsentrasi (g/dl)
Lanjutan Lampiran 4
PLGA (75:25) : PCL 3:1 minggu 3
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0872 28.61 27.84 1.0277 0.0277 0.3172 0.0523 28.33 27.84 1.0176 0.0176 0.3364 0.0314 28.15 27.84 1.0111 0.0111 0.3547 0.0188 28.03 27.84 1.0068 0.0068 0.3623 0.0113 27.96 27.84 1.0043 0.0043 0.3814
PLGA (75:25) : PCL 3:1 minggu 4
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0348 28.63 27.84 1.0284 0.0284 0.8154 0.0209 28.22 27.84 1.0136 0.0136 0.6537 0.0125 28.05 27.84 1.0075 0.0075 0.6021 0.0075 27.93 27.84 1.0032 0.0032 0.4301 0.0045 27.89 27.84 1.0018 0.0018 0.3982
y = -0,8787x + 0,3856 R2 = 0,9433
0,00 0,10 0,20 0,30 0,40
0,00 0,02 0,04 0,06 0,08 0,10 0,12 Konsentrasi (g/dl)
η reduktif
y = 13,601x + 0,3616
R2 = 0,9391
0,00 0,10 0,20 0,30 0,40 0,50 0,60 0,70 0,80 0,90
0,00 0,01 0,02 0,03 0,04 Konsentrasi (g/dl)
η reduktif
y = -0,7839x + 0,3819
R2 = 0,9451
0,00 0,10 0,20 0,30 0,40 0,50
0,00 0,02 0,04 0,06 0,08 0,10
Konsentrasi (g/dl)
Lanjutan Lampiran 4
PLGA (75:25) : PCL 3:1 minggu 5
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.0312 28.58 27.84 1.0266 0.0266 0.8519
0.0187 28.22 27.84 1.0136 0.0136 0.7291 0.0112 28.01 27.84 1.0061 0.0061 0.5437 0.0067 27.92 27.84 1.0029 0.0029 0.4264 0.0040 27.89 27.84 1.0018 0.0018 0.4442
PLGA (75:25) : PCL 3:1 minggu 6
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0280 28.63 27.84 1.0284 0.0284 1.0134 0.0168 28.24 27.84 1.0144 0.0144 0.8552 0.0101 28.01 27.84 1.0061 0.0061 0.6058 0.0060 27.93 27.84 1.0032 0.0032 0.5345 0.0036 27.88 27.84 1.0014 0.0014 0.3959
PLGA (75:25) : PCL 3:1 minggu 7
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0232 28.65 27.84 1.0291 0.0291 1.2541 0.0139 28.23 27.84 1.0140 0.0140 1.0064
0.0084 27.97 27.84 1.0047 0.0047 0.5591 0.0050 27.92 27.84 1.0029 0.0029 0.5734 0.0030 27.88 27.84 1.0014 0.0014 0.4779
y = 16,593x + 0,3603 R2 = 0,9532
0,00 0,10 0,20 0,30 0,40 0,50 0,60 0,70 0,80 0,90
0,000 0,005 0,010 0,015 0,020 0,025 0,030 0,035
Konsentrasi (g/dl)
η reduktif
y = 24.886x + 0.3597 R2 = 0.9543
0,00 0,20 0,40 0,60 0,80 1,00 1,20
0,000 0,005 0,010 0,015 0,020 0,025 0,030
Konsentrasi (g/dl)
Lanjutan Lampiran 4
PLGA (75:25) : PCL 3:1 minggu 8
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0196 28.63 27.84 1.0284 0.0284 1.4478 0.0118 28.17 27.84 1.0119 0.0119 1.0079 0.0071 27.95 27.84 1.0040 0.0040 0.5600 0.0042 27.91 27.84 1.0025 0.0025 0.5939 0.0025 27.88 27.84 1.0014 0.0014 0.5656
Contoh perhitungan:
Minggu ke 8, konsentrasi 0.0196 g/100ml:
pelarut sampel relatif
t
t
=
η
84
.
27
63
.
28
=
= 1.02841
−
=
relatif spesifikη
η
= 1.0284 – 1 = 0.0284
)
100
/
(
g
ml
i
konsentras
spesifik reduktifη
η
=
0196
.
0
0284
.
0
=
= 1.4478
Persamaan garis yang terbentuk y = a + bx Dengan y = η reduktif
a = [η]
x = konsentrasi (g/100ml) Persamaan garis yang terbentuk
y = 55,243x + 0.3358 sehingga a = [η] = 0.3358. y = 40,478x + 0,3411
R 2 = 0,9421
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40
0,00 0,01 0,01 0,02 0,02 0,03
Konsentrasi (g/dl)
η reduktif
y = 55,243x + 0,3358
R 2 = 0,9389
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40
0,000 0,005 0,010 0,015 0,020 0,025
Konsentrasi (g/dl)
Lampiran 5 Data viskositas intrinsik PLGA(90:10):PCL 5:1 selama waktu degradasi
PLGA (90:10):PCL 5:1 awal
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.2060 28.97 27.84 1.0406 0.0406 0.1970 0.1236 28.89 27.84 1.0377 0.0377 0.3051 0.0742 28.74 27.84 1.0323 0.0323 0.4359 0.0445 28.49 27.84 1.0233 0.0233 0.5247 0.0267 28.25 27.84 1.0147 0.0147 0.5516
PLGA (90:10):PCL 5:1 minggu 1
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.1272 29.10 27.84 1.0453 0.0453 0.3558 0.0763 28.75 27.84 1.0327 0.0327 0.4283 0.0458 28.47 27.84 1.0226 0.0226 0.4942 0.0275 28.26 27.84 1.0151 0.0151 0.5491 0.0165 28.10 27.84 1.0093 0.0093 0.5665
PLGA (90:10):PCL 5:1 minggu 2
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.1252 28.95 27.84 1.0399 0.0399 0.3185 0.0751 28.78 27.84 1.0338 0.0338 0.4495 0.0451 28.43 27.84 1.0212 0.0212 0.4702 0.0270 28.25 27.84 1.0147 0.0147 0.5446 0.0162 28.09 27.84 1.0090 0.0090 0.5534
y = -2.0513x + 0.5977 R2= 0.9722
0.00 0.20 0.40 0.60
0.00 0.05 0.10 0.15 0.20 0.25
Konsentrasi (g/dl)
η reduktif
y = -1.9443x + 0.5928 R2= 0.9808
0.00 0.10 0.20 0.30 0.40 0.50 0.60
0.00 0.02 0.04 0.06 0.08 0.10 0.12 0.14
Konsentrasi (g/dl)
Lanjutan Lampiran 5
PLGA (90:10):PCL 5:1 minggu 3
Konsentrasi T sampel (s) t pelarut (s) η rel η sp η sp/c
0.1204 28.69 27.84 1.0305 0.0305 0.2536 0.0722 28.53 27.84 1.0248 0.0248 0.3431 0.0433 28.41 27.84 1.0205 0.0205 0.4724 0.0260 28.19 27.84 1.0126 0.0126 0.4834 0.0156 28.07 27.84 1.0083 0.0083 0.5295
PLGA (90:10):PCL 5:1 minggu 4
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0980 29.49 27.84 1.0593 0.0593 0.6048 0.0588 28.79 27.84 1.0341 0.0341 0.5803 0.0353 28.40 27.84 1.0201 0.0201 0.5702 0.0212 28.16 27.84 1.0115 0.0115 0.5430 0.0127 28.03 27.84 1.0068 0.0068 0.5373
y = -2.1272x + 0.59 R2= 0.9687
0.00 0.10 0.20 0.30 0.40 0.50 0.60
0.00 0.05 0.10 0.15
Konsentrasi (g/dl)
η reduktif
y = -2.67x + 0.5646 R2= 0.9682
0.00 0.10 0.20 0.30 0.40 0.50 0.60
0.00 0.05 0.10 0.15
Konsentrasi (g/dl)
η reduktif
y = 0.7832x + 0.5317 R2= 0.9402
0.52 0.54 0.56 0.58 0.60 0.62
0.00 0.02 0.04 0.06 0.08 0.10 0.12
Konsentrasi (g/dl)
Lanjutan Lampiran 5
PLGA (90:10):PCL 5:1 minggu 5
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.0912 29.46 27.84 1.0582 0.0582 0.6380
0.0547 28.73 27.84 1.0320 0.0320 0.5842 0.0328 28.37 27.84 1.0190 0.0190 0.5798 0.0197 28.14 27.84 1.0108 0.0108 0.5470 0.0118 28.02 27.84 1.0065 0.0065 0.5479
PLGA (90:10):PCL 5:1 minggu 6
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0728 28.64 27.84 1.0287 0.0287 0.3947 0.0437 28.38 27.84 1.0194 0.0194 0.4441
0.0262 28.19 27.84 1.0126 0.0126 0.4797 0.0157 28.07 27.84 1.0083 0.0083 0.5254
0.0094 27.97 27.84 1.0047 0.0047 0.4949
PLGA (90:10):PCL 5:1 minggu 7
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0688 28.74 27.84 1.0323 0.0323 0.4699 0.0413 28.40 27.84 1.0201 0.0201 0.4873 0.0248 28.19 27.84 1.0126 0.0126 0.5076 0.0149 28.05 27.84 1.0075 0.0075 0.5076 0.0089 27.97 27.84 1.0047 0.0047 0.5237
y = -1.8783x + 0.5308 R2= 0.9072
0.00 0.10 0.20 0.30 0.40 0.50 0.60
0.00 0.02 0.04 0.06 0.08
Konsentrasi (g/dl)
ηreduktif
y = 1.1392x + 0.5313
R 2 = 0.9512
0.54 0.56 0.58 0.60 0.62 0.64 0.66
0.00 0.02 0.04 0.06 0.08 0.10
Konsentrasi (g/dl)
Lanjutan Lampiran 5
PLGA (90:10):PCL 5:1 minggu 8
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c
0.0664 28.73 27.84 1.0320 0.0320 0.4815 0.0398 28.38 27.84 1.0194 0.0194 0.4869 0.0239 28.17 27.84 1.0119 0.0119 0.4959 0.0143 28.04 27.84 1.0072 0.0072 0.5024 0.0086 27.96 27.84 1.0043 0.0043 0.5012
Contoh perhitungan:
Minggu ke 8, konsentrasi 0.0664 g/100ml:
pelarut sampel relatif
t
t
=
η
84
.
27
73
.
28
=
= 1.03201
−
=
relatif spesifikη
η
= 1.0320 – 1
= 0.0320
)
100
/
(
g
ml
i
konsentras
spesifik reduktifη
η
=
0664
.
0
0320
.
0
=
= 0.4815
Persamaan garis yang terbentuk y = a + bx Dengan y = η reduktif
a = [η]
x = konsentrasi (g/100ml) Persamaan garis yang terbentuk
y = -0,3663x + 0.5044 sehingga a = [η] = 0.5044. y = -0.3663x + 0.5044
R2= 0.9546
0.48 0.48 0.49 0.49 0.50 0.50 0.51
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07
Konsentrasi (g/dl)
η reduktif
y = -0.845x + 0.526 R2= 0.9502
0.46 0.47 0.48 0.49 0.50 0.51 0.52 0.53
0.00 0.02 0.04 0.06 0.08
Konsentrasi (g/dl)
Lampiran 6 Data viskositas intrinsik PLGA(75:25):PCL 5:1 selama waktu degradasi
PLGA (75:25) :PCL 5:1 awal
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.2048 28.96 27.84 1.0402 0.0402 0.1964
0.1229 28.89 27.84 1.0377 0.0377 0.3069 0.0737 28.56 27.84 1.0259 0.0259 0.3508 0.0442 28.39 27.84 1.0198 0.0198 0.4466 0.0265 28.19 27.84 1.0126 0.0126 0.4737
PLGA (75:25) :PCL 5:1 minggu 1
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.1380 28.88 27.84 1.0374 0.0374 0.2707 0.0828 28.67 27.84 1.0298 0.0298 0.3601
0.0497 28.40 27.84 1.0201 0.0201 0.4049 0.0298 28.22 27.84 1.0136 0.0136 0.4579
0.0179 28.07 27.84 1.0083 0.0083 0.4619
PLGA (75:25) :PCL 5:1 minggu 2
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.0660 28.81 27.84 1.0348 0.0348 0.5279 0.0396 28.40 27.84 1.0201 0.0201 0.5080 0.0238 28.17 27.84 1.0119 0.0119 0.4989 0.0143 28.03 27.84 1.0068 0.0068 0.4787 0.0086 27.95 27.84 1.0040 0.0040 0.4619
y = -1.5298x + 0.4993
R2= 0.9629
0.00 0.10 0.20 0.30 0.40 0.50
0.00 0.05 0.10 0.15 0.20 0.25
Konsentrasi (g/dl)
η reduktif
y = -1.6337x + 0.4951
R2= 0.9908
0.00 0.10 0.20 0.30 0.40 0.50
0.00 0.05 0.10 0.15
Konsentrasi (g/dl)
Lanjutan Lampiran 6
PLGA (75:25) :PCL 5:1 minggu 3
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.0580 28.78 27.84 1.0338 0.0338 0.5821 0.0348 28.37 27.84 1.0190 0.0190 0.5471 0.0209 28.13 27.84 1.0104 0.0104 0.4989
0.0125 28.00 27.84 1.0057 0.0057 0.4587 0.0075 27.94 27.84 1.0036 0.0036 0.4779
PLGA (75:25) :PCL 5:1 minggu 4
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.0572 29.36 27.84 1.0546 0.0546 0.9545 0.0343 28.52 27.84 1.0244 0.0244 0.7117 0.0206 28.19 27.84 1.0126 0.0126 0.6105 0.0124 28.01 27.84 1.0061 0.0061 0.4942 0.0074 27.96 27.84 1.0043 0.0043 0.5814
y = 1.0544x + 0.463 R2 = 0.9041
0.44 0.46 0.48 0.50 0.52 0.54
0.00 0.02 0.04 0.06 0.08
Konsentrasi (g/dl)
η reduktif
y = 2.4061x + 0.4486
R
2
= 0.9246 0.00
0.20 0.40 0.60 0.80
0.00 0.02 0.04 0.06 0.08
Konsentrasi (g/dl)
η reduktif
y = 8.4777x + 0.4469 R2 = 0.9219
0.00 0.20 0.40 0.60 0.80 1.00 1.20
0.00 0.02 0.04 0.06 0.08
Konsentrasi (g/dl)
Lanjutan Lampiran 6
PLGA (75:25) :PCL 5:1 minggu 5
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.0488 28.64 27.84 1.0287 0.0287 0.5888
0.0293 28.27 27.84 1.0154 0.0154 0.5275 0.0176 28.08 27.84 1.0086 0.0086 0.4907 0.0105 27.97 27.84 1.0047 0.0047 0.4430 0.0063 27.92 27.84 1.0029 0.0029 0.4544
PLGA (75:25) :PCL 5:1 minggu 6
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.0420 28.64 27.84 1.0287 0.0287 0.6842 0.0252 28.25 27.84 1.0147 0.0147 0.5844
0.0151 28.06 27.84 1.0079 0.0079 0.5226 0.0091 27.95 27.84 1.0040 0.0040 0.4355
0.0054 27.91 27.84 1.0025 0.0025 0.4619
PLGA (75:25) :PCL 5:1 minggu 7
Konsentrasi t sampel (s) t pelarut (s) η rel η sp η sp/c 0.0380 28.56 27.84 1.0259 0.0259 0.6806 0.0228 28.20 27.84 1.0129 0.0129 0.5672 0.0137 28.02 27.84 1.0065 0.0065 0.4726 0.0082 27.95 27.84 1.0040 0.0040 0.4814 0.0049 27.90 27.84 1.0022 0.0022 0.4376
y = 3.4192x + 0.4239 R2 = 0.9697
0.00 0.10 0.20 0.30 0.40 0.50 0.60 0.70
0.00 0.01 0.02 0.03 0.04 0.05 0.06
Konsentrasi (g/dl)
η reduktif
y = 6.6637x + 0.4087 R2 = 0.9583
0.00 0.20 0.40 0.60 0.80
0.00 0.01 0.02 0.03 0.04 0.05
Konsentrasi (g/dl)
Lanjutan Lampiran 6
PLGA (75:25) :PCL 5:1 minggu 8
Konsentrasi t sampel (s) t pelarut (s) ηrel ηsp ηsp/c 0.0224 28.82 27.84 1.0352 0.0352 1.5715
0.0134 28.20 27.84 1.0129 0.0129 0.9621 0.0081 28.00 27.84 1.0057 0.0057 0.7127 0.0048 27.93 27.84 1.0032 0.0032 0.6681 0.0029 27.89 27.84 1.0018 0.0018 0.6187
Contoh perhitungan:
Minggu ke 8, konsentrasi 0.0224 g/100ml:
pelarut sampel relatif
t
t
=
η
84
.
27
82
.
28
=
= 1.03521
−
=
relatif spesifikη
η
= 1.0352 – 1
= 0.0352
)
100
/
(
g
ml
i
konsentras
spesifik reduktifη
η
=
0224
.
0
0352
.
0
=
= 1.5715
Persamaan garis yang terbentuk y = a + bx Dengan y = η reduktif
a = [η]
x = konsentrasi (g/100ml) Persamaan garis yang terbentuk
y = 49.165x + 0.3988 sehingga a = [η] = 0.3988. y = 7.2331x + 0.4011
R2 = 0.9683
0.00 0.20 0.40 0.60 0.80
0.00 0.01 0.02 0.03 0.04
Konsentrasi (g/dl)
η reduktif
y = 49.165x + 0.3988
R 2 = 0.9545
0.00 0.50 1.00 1.50 2.00
0.00 0.01 0.01 0.02 0.02 0.03
Konsentrasi (g/dl)
Lampiran 7 Data perubahan viskositas intrinsik poliblend PLGA dan PCL
Komposisi Minggu ke η intrinsik Perubahan [η] (%)
A
0 0,4014 0
1 0.3990 0.60
2 0.3887 3.16
3 0.3866 3.69
4 0.3732 7.03
5 0.3708 7.62
6 0.3604 10.21
7 0.3531 12.03
8 0.3413 14.97
B
0 0,4036 0
1 0.3988 1.19
2 0.3856 4.46
3 0.3819 5.38
4 0.3616 10.41
5 0.3603 10.73
6 0.3597 10.88
7 0.3411 15.49
8 0.3358 16.80
C
0 0,5977 0
1 0.5928 0.82
2 0.5900 1.29
3 0.5646 5.54
4 0.5317 11.04
5 0.5313 11.11
6 0.5308 11.19
7 0.5260 12.00
8 0.5044 15.61
D
0 0,4993 0
1 0.4951 0.84
2 0.4630 7.27
3 0.4486 10.15
4 0.4469 10.49
5 0.4239 15.10
6 0.4087 18.15
7 0.4011 19.67
KAPROLAKTON) SECARA IN VITRO
MARDIANA HARDIANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Asam Glikolat) dan Poli(ε-kaprolakton) secara In Vitro. Dibimbing oleh HENDRA ADIJUWANA dan AHMAD SJAHRIZA.
Polimer telah banyak diaplikasikan dalam kehidupan manusia, salah satunya adalah untuk penyalut obat. Polimer sintetik seperti poli(asamlaktat) (PLA), poli(asamglikolat) (PGA), poli(ε-kaprolakton) (PCL), poli(asam laktat-co-asam glikolat) (PLGA) merupakan jenis-jenis poliester yang banyak digunakan untuk penyalut obat. Para peneliti telah banyak yang melakukan penelitian tentang degradasi PLA, PGA, PCL, dan PLGA, tetapi belum ada yang melakukan penelitian tentang degradasi poliblend polimer ini, salah satunya adalah poliblend PLGA dan PCL.
Poliblend dibuat empat komposisi, yaitu PLGA (90:10):PCL 3:1, PLGA(75:25):PCL 3:1, PLGA (90:10):PCL 5:1, dan PLGA (75:25):PCL 5:1. Degradasi dilakukan selama delapan minggu dengan menggunakan bufer fosfat pH 7.4 dan suhu inkubasi 37°C. Degradasi polimer diamati dengan adanya perubahan massa, viskositas intrinsik, dan bentuk permukaannya. Hasil penelitian menunjukkan bahwa komposisi PLGA (75:25):PCL 5:1 merupakan komposisi yang paling cepat terdegradasi dibandingkan dengan komposisi lainnya. Ini terlihat dari perubahan massa hingga 89.06% dan viskositas intrinsik hingga 20.13%.
ABSTRACT
Mardiana Hardianti. In Vitro Polyblend Degradation of Copolymer Poly(lactic-co-glycolic acid) and Poly(ε-caprolactone). Supervised by HENDRA ADIJUWANA and AHMAD SJAHRIZA.
Polymer has many applications in human life, one of them is in the field of health. Polymer synthetics like polylactic acid (PLA), polyglycolic acid (PGA), poly(ε -caprolactone) (PCL), and poly(lactic acid-co-glycolic acid) were kind of polyesters that is many used in field of health. Many researchers have already made research about degradation of PLA, PGA, PCL, and PLGA. However, there is no one doing research about degradation of combination between this two polymers, one of them is polyblend of PLGA and PCL.
KAPROLAKTON) SECARA IN VITRO
MARDIANA HARDIANTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
NIM
: G44203028
Menyetujui,
Pembimbing I,
Pembimbing II,
Ir. Hendra Adijuwana, MST
Drs. Ahmad Sjahriza
NIP 130 321 037
NIP 131 842 413
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
Maria atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan dengan baik. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2007 ini ialah polimer, dengan judul Degradasi Poliblend Kopolimer Poli(asam laktat-co-asam glikolat) dan Poli(ε-kaprolakton) secara In Vitro.
Penulis mengucapkan terima kasih kepada Bapak Ir. Hendra Adijuwana, MST dan Bapak Drs. Ahmad Sjahriza selaku pembimbing, serta Ibu Tetty Kemala, MSi yang telah banyak memberi saran dalam penelitian ini. Di samping itu, penulis juga menyampaikan penghargaan kepada staf Bagian Kimia Anorganik (Bapak Sawal, Bapak Caca, Ibu Nur, dan Ibu Siti Maemunah), staf Bagian Kimia Analitik (Bapak Eman), staf Bagian Biologi (Ibu Retno dan Ibu Yuli), dan staf Bagian Departemen (Mas Heri dan Bapak Didi) yang telah banyak membantu dalam penyusunan karya ilmiah ini.
Terima kasih yang begitu besar penulis ucapkan untuk papa (Alm.), mama, Dicky, Yulius, Yane, Eva Yunita, Santika, Hendra, dan Adi atas segala bantuan baik berupa materi, dukungan, doa, nasihat, dan kasih sayangnya. Penulis juga mengucapkan terima kasih atas dukungannya kepada Elyzabet, Nurhayani, Rio, Bekti, Eko, Nuryono, kak
Budi, dan teman-teman kimia angkatan 2003.
Akhir kata, semoga karya ilmiah ini bermanfaat.
Bogor, Agustus 2007
Howarman Indrajaya (†) dan Nurgiantie. Penulis merupakan anak keenam dari delapan bersaudara.
Tahun 2003 penulis lulus dari SMU Sint Carolus Bengkulu dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB (USMI). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Kopolimer Poli(asam laktat-co-asam glikolat) ... 1
Poli(ε-kaprolakton) ... 2
Poliblend PLGA dan PCL ... 2
Degradasi Polimer ... 2
Viskometri ... 3
BAHAN DAN METODE Bahan dan Alat ... 3
Pembuatan Poliblend PLGA dan PCL (Sujatmiko 2007) ... 3
Pembuatan Buffer Fosfat pH 7.4 (Mulyono 2005) ... 4
Degradasi Poliblend secara In Vitro (Kiremitci-Gumusderelioglu& Gunday 1999) ... 4
Uji Degradasi Poliblend ... 4
HASIL DAN PEMBAHASAN Pembuatan Poliblend PLGA dan PCL ... 4
Degradasi Poliblend secara In Vitro ... 4
Perubahan Massa Sampel ... 5
Perubahan Viskositas Intrinsik ... 6
Perubahan Bentuk Permukaan Poliblend ... 6
SIMPULAN DAN SARAN Simpulan ... 7
Saran ... 8
DAFTAR PUSTAKA ... 8
1 Waktu dan produk degradasi dari beberapa polimer poliester ... 3
2 Komposisi PLGA dan PCL ... 4
DAFTAR GAMBAR
Halaman 1 Reaksi pembuatan PLGA (Kurniawan 2007) ... 12 Difraktogram XRD PLGA pada komposisi a) 75:25 dan b) 90:10 (Kurniawan 2007) ... 2
3 Struktur kimia PCL (Huang & Edelman 1995) ... 2
4 Difraktogram XRD PCL (Sujatmiko 2007) ... 2
5 Viskometer-Ostwald Cannon Fenske Routine ... 3
6 Bentuk permukaan visual poliblend dari komposisi (a) A, (b) B, (c) C, dan (d) D ... 5
7 Perubahan massa sampel ... 5
8 Laju perubahan massa sampel ... 6
9 Perubahan viskositas intrinsik ... 7
10 Bentuk permukaan awal polimer dengan perbesaran 2x10x5 pada komposisi a) A, b) B, c) C, dan d) D ... 7
11 Bentuk permukaan polimer setelah terdegradasi dengan perbesaran 2x10x5 pada komposisi a) A, b) B, c) C, dan d) D ... 7
DAFTAR LAMPIRAN
Halaman 1 Diagram alir kerja penelitian ... 112 Data perubahan dan laju perubahan massa poliblend PLGA dan PCL ... 12
3 Data viskositas intrinsik PLGA(90:10):PCL 3:1 selama waktu degradasi. 13
4 Data viskositas intrinsik PLGA(75:25):PCL 3:1 selama waktu degradasi. 17
5 Data viskositas intrinsik PLGA(90:10):PCL 5:1 selama waktu degradasi. 21
6 Data viskositas intrinsik PLGA(75:25):PCL 5:1 selama waktu degradasi. 25
kehidupan manusia. Salah satu bidang aplikasi polimer adalah di bidang kesehatan (medical applications). Aplikasi polimer ini meliputi pembuatan pin, benang jahit operasi, rekayasa jaringan, sistem pengungkungan obat, dan aplikasi dalam bidang kesehatan gigi.
Polimer yang dapat diaplikasikan dalam bidang kesehatan harus dapat terdegradasi dengan baik di dalam tubuh. Fibrin, kolagen, kitosan, dan gelatin merupakan jenis polimer alam yang telah banyak diaplikasikan dalam bidang kesehatan. Polimer biodegradabel sintetik yang telah banyak diaplikasikan dalam bidang kesehatan adalah poli(asamlaktat) (PLA), poli(asamglikolat) (PGA), poli(asam laktat-co-asam glikolat) (PLGA), dan poli(ε-kaprolakton) (PCL).
Para peneliti banyak yang memilih menggunakan polimer biodegradabel sintetik karena bentuk molekulnya yang dapat direkayasa, bebas dari sifat imunogenitas, dan bahan asalnya berasal dari sumber yang dapat diperbaharui. Polimer sintetik yang banyak digunakan adalah PCL dan PLGA. PCL hanya sesuai untuk sistem penyalut obat jangka panjang, karena sifat kristalinitas yang tinggi dan waktu degradasi yang lambat. Sementara itu, PLGA bersifat biokompatibel dengan sifat degradasi yang dapat disesuaikan, bergantung pada nisbah molar komponen monomer individu. Namun, kelemahan PLGA adalah memiliki elongasi saat putus yang rendah karena mudah putus saat regangan akibat tekanan (Porjazoska et al. 2004). Oleh karena itu, penelitian untuk menggabungkan sifat antara dua polimer ini pernah dilakukan oleh Sujatmiko (2007).
Penelitian untuk mencampur PLGA dan PCL telah dilakukan guna mendapatkan sifat terbaru dari kelebihan dan kelemahan masing-masing polimer tetapi belum ada pihak yang pernah melakukan degradasi terhadap polimer hasil penggabungan (polyblend) ini. Penelitian dari Porjazoska et al. (2004a) dan Kiremitci-Gumusderelioglu & Deniz (1999) hanya membahas tentang degradasi PLGA, yaitu dengan semakin tingginya nisbah asam glikolat, PLGA akan semakin cepat terdegradasi. Dalam penelitian lain,Edlund & Albertson (2002) juga hanya membahas tentang degradasi kopolimer asam 6-hidroksikaproat dan L-asam laktat secara in vitro pada kopolimer ini bergantung pada komposisi L-asam laktat dan kristalinitas asam 6-hidroksikaproat. Oleh karena itu,
perubahan yang terjadi selama poliblend ini terdegradasi. Penelitian ini bertujuan mengetahui komposisi dari poliblend PLGA dan PCL yang memiliki waktu degadasi relatif singkat dengan mengamati perubahan dari viskositas intrinsik, massa, dan bentuk permukaan selama masa degradasi.
TINJAUAN PUSTAKA
Kopolimer Poli(asam laktat-co-asam glikolat)
PLGA merupakan salah satu mikrosfer yang disetujui penggunaannya oleh Food and Drugs Administration (FDA). PLGA ini dapat disintesis melalui pembukaan cincin laktida dan glikolida menggunakan timah (II) bis 2-etil heksanoat) sebagai katalis pada suhu tinggi, yaitu 160°C. Katalis timah (II) bis 2-etil heksanoat) merupakan katalis komersial yang sangat efisien, memiliki toksisitas yang rendah, dan zat aditif makanan yang diizinkan di sejumlah negara. (Kiremitci-Gumusderelioglu & Deniz 1999). Reaksi dari pembuatan PLGA ditunjukkan sebagai berikut
OH CH3 O HO Dehidrasi H O O CH3 O H n O O O O H3C
CH3
Asam laktat Oligomer Poli(asam laktat) Laktida Pemanasan C H2 OH O HO Dehidrasi H O O O H n O O O O
Asam glikolat Oligomer Poli(asam glikolat) Glikolida Pemanasan
O
O O
O H3C
CH3 O
O O O + Pemanasan Katalis laktida glikolida C C H
O CH3
O C O CH O CH3 C H2 C O O C O C H2
O + H2O
m n
Gambar 1 Reaksi pembuatan PLGA. (Kurniawan 2007).
[image:48.612.328.507.265.620.2]