STUDY OF EFFECT POTENTIAL, CONTACT TIME, AND
pH
ON METHOD OF THE ELECTROCOAGULATION RESTAURANTWASTEWATER USING Fe ELECTRODE WITH MONOPOLAR AND DIPOLAR ARRANGEMENT
By
KURRATUL UYUN
Electrocoagulation process is a method that is considered quite effective in removing organic compounds in wastewater compared to conventional
coagulation methods. In this research, studied the process of electrocoagulation for restaurant wastewater use Fe metal as an electrode with a continuous system. The results of electrocoagulation restaurant wastewater samples were analyzed using a spectrophotometer UV -Vis at a wavelength of 200-700 nm. Monitoring carried out at a wavelength of 254, 272, 365, 436 and 565 nm as a cue reduced concentration of organic particles in the restaurant wastewater. In addition, monitoring is also done using the ratio absorbance at a wavelength of 254 nm to a wavelength of 365 nm (E2/E3) and the ratio of absorbance at a wavelength of 436
nm to the absorbance at a wavelength of 565 nm (E4/E6) due to the higher value of
E2/E3and E4/E6values indicate that the molecular weight organic compounds in
wastes a low.
Electrocoagulation process carried out to study the influence of several
TERHADAP METODE ELEKTROKOAGULASI LIMBAH CAIR RESTORAN MENGGUNAKAN ELEKTRODA Fe
DENGAN SUSUNAN MONOPOLAR DAN DIPOLAR
Oleh
KURRATUL UYUN
Proses elektrokoagulasi merupakan suatu metode yang dianggap cukup efektif untuk menghilangkan senyawa organik dalam limbah cair dibandingkan dengan metode koagulasi konvensional. Dalam penelitian ini dipelajari proses elektrokoagulasi untuk limbah cair restoran menggunakan logm Fe sebagai elektroda dengan sistem kontinu. Hasil elektrokoagulasi pada sampel limbah cair restoran dianalisis
menggunakan spektrofotometer UV-Vis pada panjang gelombang 200-700 nm. Pemantauan dilakukan pada panjang gelombang 254, 272, 365, 436 dan 565 nm sebagai petunjuk berkurangnya kosentrasi partikel organik dalam limbah cair
restoran. Selain itu, pemantauan juga dilakukan dengan menggunakan perbandingan absorbansi pada panjang gelombang 254 nm terhadap panjang gelombang 365 nm (E2/E3) dan perbandingan absorbansi pada panjang gelombang 436 nm terhadap
absorbansi pada panjang gelombang 565 nm (E4/E6) karena semakin tinggi nilai E2/E3
dan nilai E4/E6menunjukkan bahwa bobot molekul senyawa organik dalam limbah
rendah.
I. PENDAHULUAN
A. Latar Belakang
Restoran setiap saat bertambah banyak diberbagai wilayah dan umumnya berada
di daerah pemukiman atau tempat-tempat strategis yang pada umumnya belum
memiliki Unit Pengolahan Limbah (UPL). Limbah restoran terutama limbah cair
hanya ditampung dalam suatu waduk penampungan sederhana. Untuk daerah
Provinsi Lampung sendiri, pertambahan jumlah restoran sangat signifikan setiap
waktu sehingga peluang pencemaran lingkungan oleh limbah restoran ini sangat
besar. Untuk mengatasi permasalahan yang diakibatkan limbah restoran ini, maka
ide ini digagas untuk mengolah limbah cair restoran dengan metode
elektrokoagulasi.
Metode elektrokoagulasi umumnya diterapkan pada limbah cair industri,
sedangkan untuk limbah cair restoran belum banyak dikembangkan. Dalam
bidang lingkungan, penerapan metode elektrokoagulasi sedang giat dikembangkan
untuk pengolahan limbah cair, khususnya limbah cair yang mengandung polutan
Pada prinsipnya, elektrokoagulasi merupakan pengembangan metode koagulasi
konvensional yang menggunakan koagulan berupa garam, terutama FeCl3, ZnCl2,
dan Al2(SO4)3(Holtet al.,2002; Bergmannet al., 2003). Perbedaan paling
penting antara kedua metode adalah pembentukan kation secara langsung dari
logam yang digunakan sebagai anoda dalam metode elektrokoagulasi, sehingga
tidak menghasilkan limbah sekunder berupa anion yang merupakan kelemahan
utama metode konvensional. Penerapan metode elektrokoagulasi juga tidak
membutuhkan penentuan dosis koagulan yang seringkali menjadi kendala praktis
dalam koagulasi konvensional. Selain itu, pemilihan metode elektrokoagulasi
untuk pengolahan limbah cair restoran didasarkan pada beberapa pertimbangan
antara lain; prosesnya berlangsung cepat, teknologinya murah, dapat menurunkan
total mikroorganisme dalam air seperti bakteriE. coli, peralatan yang digunakan
sederhana dan dapat dibuat dalam unit kecil sehingga sesuai untuk industri rumah
tangga seperti rumah makan (restoran).
Metode elektrokoagulasi merupakan suatu proses elektrokimia sehingga sangat
dipengaruhi oleh berbagai variabel elektrokimia. Proses elektrokoagulasi sangat
dipengaruhi oleh potensial, jenis elektroda (Tsaiet al., 1997), derajad keasaman
(pH), waktu kontak (Chenet al., 2000), jarak antar elektroda (Mameriet al.,
1998), suhu, kuat arus (Bejankiwaret al., 2002), serta jenis dan konsentrasi
polutan dalam air (Xionget al., 2001). Dari berbagai variabel tersebut, elektroda,
potensial, dan pH merupakan variabel dasar elektrokimia, sedangkan variabel
lainnya merupakan variabel pendukung yang bertujuan untuk optimasi metode
Proses elektrokoagulasi pada penelitian ini dilakukan untuk mempelajari pengaruh
beberapa parameter elektrokimia meliputi potensial, waktu kontak, dan pH,
terhadap nilai COD, BOD, dan kekeruhan limbah olahan karena ketiganya
merupakan parameter kualitas suatu limbah cair. Proses elektrokoagulasi
dilakukan menggunakan logam besi (Fe) sebagai elektroda. Penggunaan logam
ini didasarkan pada hasil penelitian sebelumnya (Wasinton dan Kamisah, 2004)
yang menunjukkan bahwa elektroda yang paling baik dalam menangani warna
adalah Fe. Untuk mempelajari pengaruh susunan elektroda dalam penelitian ini,
percobaan dilakukan dengan susunan elektroda secara monopolar dan dipolar.
Proses koagulasi pada penelitian ini dipantau dengan menggunakan
spektrofotometer UV-Vis dengan mengikuti perubahan absorbansi pada panjang
gelombang (λ) 200-700 nm. Pengukuran dilakukan untuk absorbansi pada
panjang gelombang (λ) 254, 272,365, 436 dan 565 nm, karena absorbansi pada
panjang gelombang tersebut mempunyai korelasi yang baik dengan konsentrasi
partikulat dalam limbah. Selain itu, dilakukan pula pemantauan terhadap
perubahan bobot molekul polutan dalam limbah, yaitu perubahan perbandingan
absorbansi pada λ=250/365untuk menghitung E2/E3sertaλ=436/565 untuk
menghitung E4/E5.
Dari literatur diketahui bahwa kedua perbandingan absorbansi di atas berbanding
terbalik dengan bobot molekul polutan organik sehingga perubahan nilai
keduanya akan menunjukkan selektifitas proses elektrokoagulasi terhadap bobot
B. Tujuan
Tujuan dari penelitian ini adalah sebagai berikut:
1. Mempelajari karakteristik limbah cair dari restoran.
2. Mempelajari beberapa pengaruh variabel elektrokimia yaitu potensial, waktu
kontak, dan pH terhadap efektifitas proses elektrokoagulasi limbah cair
restoran.
3. Mempelajari efektifitas proses elektrokoagulasi untuk menurunkan nilai COD
dan BOD limbah cair hasil olahan.
C. Manfaat
Penelitian ini diharapkan dapat memberikan informasi ilmiah untuk menerapkan
dan mengembangkan metode proses elektrokoagulasi untuk pengolahan limbah
II. TINJAUAN PUSTAKA
A. Limbah Cair
Secara sederhana limbah cair dapat didefinisikan sebagai air buangan yang berasal
dari aktivitas manusia dan mengandung berbagai polutan yang berbahaya baik
secara langsung maupun dalam jangka panjang. Berdasarkan sumbernya, limbah
cair dapat dibedakan atas limbah rumah tangga dan limbah industri, sedangkan
polutan yang terdapat dalam limbah dapat dibedakan atas polutan organik dan
polutan anorganik dan umumnya terdapat dalam bentuk terlarut atau tersuspensi.
Polutan yang terdapat dalam limbah cair merupakan ancaman yang cukup serius
terhadap kelestarian lingkungan, karena di samping adanya polutan yang beracun
terhadap biota perairan, polutan juga mempunyai dampak terhadap sifat fisika,
kimia, dan biologis lingkungan perairan. Dengan kata lain, perubahan sifat-sifat
air akibat adanya polutan dapat mengakibatkan menurunnya kualitas air sehingga
B. Karakteristik Limbah Cair
Limbah cair dapat didefinisikan sebagai sampah berwujud cair yang dihasilkan
dari proses industri atau kegiatan lain yang dilakukan oleh manusia. Limbah cair
dapat dibedakan menjadi beberapa golongan berdasarkan asal limbahnya yaitu,
limbah rumah tangga, limbah pertanian, dan limbah industri (Daryanto, 1995).
Apabila limbah cair dibuang langsung ke perairan tanpa diolah terlebih dahulu,
maka akan menimbulkan berbagai dampak pada biota perairan, sifat kimia dan
sifat fisika air.
Sifat fisika yang bekaitan dengan pencemaran air adalah suhu, warna, bau, rasa
dan kekeruhan. Suhu air limbah umumnya lebih tinggi dibandingkan suhu air
normal, karena kadar oksigen terlarut dalam limbah lebih rendah dari pada kadar
oksigen terlarut pada air normal. Timbulnya warna pada air disebabkan oleh
adanya bahan organik terlarut dan tersuspensi termasuk diantaranya yang bersifat
koloid. Dengan demikian, diketahui bahwa intensitas warna berbanding lurus
dengan konsentrasi polutan dalam limbah, yang artinya intensitas warna dapat
memperlihatkan kualitas suatu limbah. Bau dan rasa pada air limbah timbul
karena adanya penguraian bahan-bahan organik terlarut secara mikrobiologis.
Kekeruhan adalah ciri lain dari limbah cair yang disebabkan oleh partikel
tersuspensi dalam limbah yang menimbulkan dampak negatif paling nyata yaitu
turunnya daya serap air akan cahaya matahari, sehingga proses kehidupan biota
Selain sifat fisika, polutan dalam limbah juga akan mempengaruhi sifat kimia air
yaitu adanya perubahan derajad keasaman (pH) serta tingginya nilaiBiological
Oxygen Demand(BOD) dan nilaiChemical Oxygen Demand(COD) limbah.
Derajad keasaman air merupakan salah satu faktor yang sangat mempengaruhi
aktivitas kehidupan dalam perairan (Sutrisno, 2001). Terjadinya perubahan pH
pada air tercemar adalah akibat dari penguraian berbagai polutan organik yang
terdapat dalam limbah, sehingga akan mempengaruhi nilai COD dan BOD. pH,
COD dan BOD ketiganya merupakan parameter kualitas limbah karena dapat
menyatakan kadar oksigen yang dibutuhkan dalam menguraikan polutan organik
dalam limbah.
Di dalam air terdapat berbagai jenis mikroorganisme seperti candawan, alga,
bakteri, protozoa, dan virus (Fardiaz, 1992), yang memanfaatkan bahan organik
yang ada dalam limbah sebagai media untuk pertumbuhannya. Hal tersebut
mengakibatkan air limbah tidak layak digunakan dan dikonsumsi.
C. Parameter Kualitas Limbah Cair
Perubahan sifat-sifat pada limbah cair (sifat biologis, fisika dan kimia), sangat
berpengaruh terhadap kualitas dari suatu limbah. Dalam prakteknya, kualitas
limbah cair diukur berdasarkan parameter-parameter yang telah ditentukan di
berbagai negara termasuk negara Indonesia. Parameter-parameter yang akan
dipelajari pada penelitian ini adalah pH (derajad keasaman), kekeruhan, COD dan
BOD yang mengacu pada standar baku mutu limbah cair dalam Surat Keputusan
limbah cair industri termasuk industri rumah makan (restoran) yang tertera pada
Tabel 2.1.
Tabel 2.1 Standar Baku Mutu Limbah Cair Industri Rumah Makan (Restoran) di Provinsi Lampung Berdasarkan Surat Keputusan Gubernur Provinsi Lampung Nomor G/624/B.VII/Hk.1999
No Parameter Uji Nilai baku mutu limbah
1. Kekeruhan (NTU) 100
NTU = Nepnelometrik Turbidity Unit
1. Chemical oxygen demand(COD)
Chemical oxygen demand(COD) merupakan jumlah oksigen (mg/L) yang
dibutuhkan untuk mengoksidasi zat-zat organik yang ada dalam sejumlah sampel.
Oksidator yang paling umum digunakan adalah K2Cr2O7(Alaerts, 1984). Nilai
COD merupakan ukuran bagi pencemaran air oleh zat-zat organik yang secara
alamiah dapat dioksidasi melalui proses kimiawi. Maka, semakin tinggi COD
maka semakin tinggi kadar oksigen terlarut untuk oksidasi dan oksigen yang
tersedia untuk biota perairan semakin rendah.
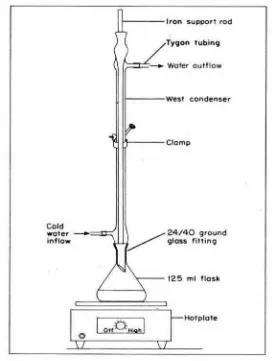
Metode pengukuran COD dilakukan dengan menggunakan peralatan khusus
reflux(seperti pada Gambar 2.1) diperlukan untuk menghindari berkurangnya air
sampel karena pemanasan.
Gambar 2.1 Peralatan khususrefluksuntuk pengukuran COD
Pada prinsipnya pengukuran COD adalah penambahan sejumlah tertentu kalium
bikromat (K2Cr2O7) sebagai oksidator pada sampel (dengan volume diketahui)
yang telah ditambahkan asam pekat dan katalis perak sulfat (Ag2SO4), kemudian
dipanaskan selama beberapa waktu. Selanjutnya, kelebihan kalium bikromat
diatasi dengan cara titrasi. Dengan demikian kalium bikromat yang terpakai
untuk oksidasi bahan organik dalam sampel dapat dihitung dan nilai COD dapat
Δ E
CaHbOc+ Cr2O72-+ H+ nCO2 + OH + 2Cr3+……….(1)
Ag2SO4
(kuning) (hijau)
Reaksi oksidasi dinyatakan berakhir, ditandai dengan adanya perubahan warna
campuran dari kuning menjadi hijau, yang menunjukkan reduksi Cr2O72-menjadi
2Cr3+(Alaerts, 1984).
2. Biological oxygen demand(BOD)
Biological Oxygen Demand(BOD) adalah suatu karakteristik yang
menunjukkan jumlah oksigen terlarut yang diperlukan oleh mikroorganisme
(biasanya bakteri) untuk mengurai atau mendekomposisi bahan organik dalam
kondisi aerobik (Metcalf, 1991). Ditegaskan lagi oleh Boyd (1990), bahwa bahan
organik yang terdekomposisi dalam BOD adalah bahan organik yang siap
terdekomposisi (readily decomposable organic matter). Mays (1996)
mengartikan BOD sebagai suatu ukuran jumlah oksigen yang digunakan oleh
populasi mikroba yang terkandung dalam perairan sebagai respon terhadap
masuknya bahan organik yang dapat diurai. Dari pengertian ini dapat dikatakan
bahwa walaupun nilai BOD menyatakan jumlah oksigen, tetapi untuk mudahnya
dapat juga diartikan sebagai gambaran jumlah bahan organik mudah terurai
Prinsip pengukuran BOD pada dasarnya cukup sederhana, yaitu mengukur
kandungan oksigen terlarut awal (DOi) dari sampel segera setelah pengambilan
contoh, kemudian mengukur kandungan oksigen terlarut pada sampel yang telah
diinkubasi selama 5 hari pada kondisi gelap dan suhu tetap (20oC) yang sering disebut dengan DO5. Selisih DOidan DO5(DOi- DO5) merupakan nilai BOD
yang dinyatakan dalam miligram oksigen per liter (mg/L). Pengukuran oksigen
dapat dilakukan secara analitik dengan cara titrasi (metode Winkler, iodometri)
atau dengan menggunakan alat yang disebut DO meter yang dilengkapi dengan
probekhusus. Jadi pada prinsipnya dalam kondisi gelap, agar tidak terjadi proses
fotosintesis yang menghasilkan oksigen, dan dalam suhu yang tetap selama lima
hari, diharapkan hanya terjadi proses dekomposisi oleh mikroorganime, sehingga
yang terjadi hanyalah penggunaan oksigen, dan oksigen tersisa adalah sebagai
DO5. Hal terpenting yang harus diperhatikan adalah mengupayakan agar masih
ada oksigen tersisa pada pengamatan hari kelima sehingga DO5tidak nol. Bila
DO5nol maka nilai BOD tidak dapat ditentukan.
3.Total suspended solid(TSS)
Total suspended solid(TSS) merupakan penyebab utama kekeruhan air yang
disebabkan oleh partikel-partikel tersuspensi di dalam air yang dapat mengganggu
penyerapan cahaya matahari ke dalam air. Partikel-partikel ini dapat berupa
senyawa organik atau anorganik (Sari, 1998). Kekeruhan akan menghambat
penembusan sinar matahari yang dibutuhkan oleh mikroorganisme dan
fitoplankton untuk melakukan fotosintesis (Arnelli dkk., 1999). Oleh karena itu,
padatan yang terdapat dalam air, baik senyawa organik maupun anorganik.
Penentuan TSS dapat dilakukan menggunnakan parameter kekeruhan.
D. Pengolahan Limbah Cair
Berbagai proses pengolahan limbah telah banyak dikembangkan untuk
memisahkan suatu kontaminan dari air limbah sampai batas yang dikehendaki.
Karena limbah yang akan dibuang ke suatu lingkungan hendaknya harus
memenuhi standar baku mutu air limbah.
Menyadari banyaknya dampak negatif yang dapat ditimbulkan oleh limbah cair,
berbagai metode pengolahan limbah cair telah dikembangkan dan secara garis
besar dapat dikelompokkan menjadi metode biologis, metode fisika dan metode
kimia. Setiap metode mempunyai keunggulan dan kelemahan, karena unjuk kerja
dari setiap metode sangat dipengaruhi oleh karakteristik limbah cair yang akan
diolah.
1. Pengolahan Limbah Cair secara Biologis
Pengolahan limbah secara biologis, biasanya dilakukan dengan menggunakan
mikroorganisme yang dapat menguraikan senyawa organik yang ada dalam
limbah cair. Menurut Mahida (1989), proses biologis mampu membusukkan
zat-zat organik dan secara efektif menstabilkannya sehingga setelah proses tersebut,
zat-zat organik tidak mampu menyerap oksigen di dalam limbah secara cepat dan
kandungan oksigennya semakin menipis. Tetapi metode pengolahan limbah
lambat karena sangat bergantung pada populasi dari mikroorganisme yang ada
dalam limbah yang berperan dalam penguraian senyawa-senyawa organik. Selain
itu, metode ini hanya efektif untuk limbah yang mempunyai COD antara
500-2000mg/L, sedangkan untuk limbah dengan COD lebih kecil, metode pengolahan
yang paling efektif adalah secara koagulasi (Oliveria,et al., 2001).
2. Pengolahan Limbah Cair secara Fisika
Pengolahan limbah secara fisika dapat dilakukan dengan dua cara yaitu secara
filtrasi dan sedimentasi (pengendapan). Kedua metode ini adalah proses yang
paling umum dilakukan untuk memisahkan padatan terendapkan dari limbah
industri atau limbah rumah tangga. Menurut Kagayaet al.(1999), pengolahan
limbah secara sedimentasi merupakan proses pengendapan senyawa organik
dalam limbah tanpa adanya perlakuan bantuan. Namun pengolahan sedimentasi
tidak efisien untuk digunakan, sebab prosesnya berlangsung lambat, apalagi jika
limbah berada dalam jumlah yang cukup besar meskipun biayanya relatif murah.
Pengolahan secara filtrasi merupakan pengolahan limbah dengan menggunakan
membran untuk menghilangkan warna yang ditimbulkan oleh kandungan
senyawa-senyawa organik (Groseet al.,1998) serta menghilangkan sebagian
mikroorganisme yang bersifat patogen (Carrolet al.,2000). Jika dibandingkan
dengan pengolahan sedimentasi, filtrasi memerlukan biaya yang relatif mahal.
Selain itu juga efektivitas dari membran cepat menurun karena pori-porinya
3. Pengolahan Limbah Cair secara Kimia
Pengolahan limbah secara kimia merupakan metode yang paling banyak
dimanfaatkan terutama karena prosesnya yang cepat dan efektifitasnya dapat
dipertahankan. Pada umumnya metode pengolahan limbah cair secara kimia yang
digunakan dalam pengolahan limbah cair adalah netralisasi, koagulasi, oksidasi,
reduksi, adsorpsi, serta pertukaran ion. Dua metode utama yang sering diterapkan
dalam pengolahan limbah secara kimia adalah metode adsorpsi (Heijmanet al.,
1999) dan juga metode koagulasi (Chowet al.,1999). Selain itu, pengolahan
limbah cair secara oksidasi juga merupakan metode yang umum diterapkan.
Dibandingkan dengan metode pengolahan limbah secara fisika dan biologis,
metode secara kimia sering digunakan karena prosesnya berlangsung cepat serta
bahan-bahan yang digunakan itu mudah didapatkan.
4. Koagulasi
Koagulasi merupakan proses pengendapan partikel yang tersuspensi dalam air
limbah dengan menetralkan muatan partikel oleh koagulan yang muatannya
berlawanan (Viesmann dan Hammer, 1998). Koagulan yang digunakan untuk
proses koagulasi biasanya bermuatan positif, karena ion-ion yang terdapat dalam
air limbah umumnya bermuatan negatif. Penetralan muatan tersebut
mengakibatkan gaya tolak menolak antar partikel polutan hilang. Dengan
hilangnya gaya tolak menolak antar partikel polutan, gaya kohesi akan bekerja
menghasilkan partikel-partikel berukuran lebih besar dan dikenal sebagaiflok.
yakni koagulasi konvensional dan koagulasi secara elektrokimia yang disebut
elektrokoagulasi.
a. Koagulasi Konvensional
Metode koagulasi konvensional sudah umum digunakan dan sudah cukup dikenal
luas. Dalam metode konvensional, koagulasi dilakukan menggunakan garam
sebagai koagulan. Koagulan yang umum digunakan adalah alumunium sulfat .dan
ferri klorida (FeCl3) (Ritteret al.,1999). Namun, dari ketiga koagulan tersebut
yang paling sering digunakan dan dikenal luas adalah Al2(SO4)3, karena harganya
murah, tidak berbahaya, dan penggunaannya mudah yakni dengan hanya
menebarkannya dalam limbah.
Pada dasarnya, reaksi yang terjadi pada koagulasi konvensional adalah
destabilisasi partikel pada limbah untuk membentukflok. Metode koagulasi
konvensional dapat berlangsung melalui empat mekanisme yaitu, netralisasi
muatan, penjebakan, adsorpsi, dan interaksi kimia (Holtet al.,2002). Netralisasi
muatan berlangsung jika kation dari koagulan berinteraksi dengan partikulat yang
bermuatan negatif menghasilkan produk yang bermuatan netral dan tak larut.
Pada saat alumunium hidroksida yang tidak larut terbentuk, senyawa-senyawa
organik yang ada dalam limbah dapat dihilangkan melalui mekanisme penjebakan
dan adsorpsi.
Mekanisme kedua yaitu penjebakan (penjeratan). Mekanisme ini terjadi karena
dengan adanya dosis koagulan yang rendah menyebabkan terjadinya destabilisasi.
Dalam mekanisme penjebakan ini, partikel koloid akan berfungsi sebagai inti
untuk pembentukan endapan selama proses agregasiflok.
Mekanisme ketiga yaitu adsorpsi. Metode ini dapat menghilangkan
partikel-partikel dengan kerapatan muatan yang lebih besar. Proses adsorpsi ini dapat
berlangsung dengan menggunakan koagulan yang dosisnya lebih besar sehingga
dapat memacu pengendapan Al(OH)3dengan cepat.
Mekanisme keempat yaitu interaksi kimia antara limbah dengan ion logam
alumunium terlarut. Pada mekanisme ini terjadi pembentukan kompleks, sehingga
pengendapan limbah dapat terjadi tanpa netralisasi muatan. Pada proses ini, akan
menghasilkan endapan apabila kelarutan kompleks dan partikel terlampaui.
Keempat mekanisme yang telah dipaparkan di atas merupakan gambaran
keseluruhan proses yang terjadi pada koagulasi konvensional yang
menggambarkan bahwa proses tersebut tidak sederhana, tetapi melibatkan
berbagai reaksi. Menurut Van Loon dan Duffy (2000), reaksi-reaksi yang terjadi
pada koagulasi konvensional dengan Al2(SO4)3sebagai koagulan adalah sebagai
Faktor-faktor yang mempengaruhi koagulasi konvensional antara lain adalah pH,
temperatur, waktu, jenis serta dosis koagulan yang digunakan. Dari berbagai
faktor tersebut, yang paling berperan dalam menentukan kondisi optimum proses
koagulasi adalah pH dan waktu (Chowet al.,1999) serta dosis dari koagulan
(Gregoret al.,1997). Dosis koagulan sangat bergantung pada jenis limbah dan
konsentrasi polutan dalam limbah. Semakin tinggi kosentrasi senyawa organik
dalam limbah, maka dosis koagulan yang digunakan dalam proses koagulasi juga
semakin besar (Vickerset al.,1995).
Faktor penting lainnya yang berpengaruh pada proses koagulasi adalah derajad
keasaman (pH). Menurut Vicker (1995), pH optimal untuk menurunkan
kekeruhan secara efektif adalah antara 5,5-7. Penelitian oleh Vann Loon dan Duff
(2000) serta Holt (2002), tentang pengaruh pH terhadap kelarutan berbagai jenis
alumunium telah dilakukan.
Dalam prakteknya, metode koagulasi konvensional memiliki beberapa kelemahan
antara lain yaitu prosesnya yang relatif lambat karena memerlukan pengadukan
dan penentuan dosis koagulan yang kurang tepat karena dipengaruhi oleh
beberapa faktor antara lain jenis dan konsentrasi polutan yang ada dalam limbah.
Hal tersebut dapat menyebabkan kekurangan dosis koagulan sehingga pada
prosesnya, koagulasi tidak berlangsung secara optimal dan kelebihan dosis
b. Metode Elektrokoagulasi
Elektrokoagulasi (koagulasi elektrokimia) merupakan teknologi yang sudah ada
sejak lama (bukan teknologi terbaru). Pengolahan limbah cair dengan
menggunakan elektrokoagulasi telah dilakukan sejak abad ke-20 dengan
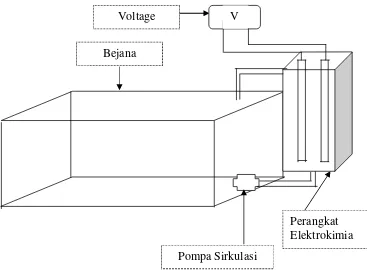
keberhasilan proses yang terbatas. Perangkat elektrokoagulator yang digunakan
terbuat dari kaca transparan sehingga berlangsungnya proses elektrokoagulasi
dapat diamati secara visual. Sebuah elektrokoagulator dilengkapi dengan 6 buah
elektroda (Fe) dan sebuah bejana (bak) untuk wadah sampel yang dihubungkan
dengan pompa sirkulasi air dan dilengkapi pula denganpower supplyyang
berfungsi sebagai potensial seperti disajikan pada Gambar 2.2.
Gambar 2.2 Perangkat Elektrokoagulasi
Prinsip dasar dari metode elektrokoagulasi adalah berdasarkan atas proses
elektrolisis dengan menggunakan elektroda sebagai koagulan, dimana merupakan Voltage
Bejana
Perangkat Elektrokimia Pompa Sirkulasi
reaksi yang kompleks dengan melibatkan berbagai mekanisme untuk
menghilangkan polutan dalam air (Songet al., 2000). Dalam proses elektrolisis,
logam pada anoda akan mengalami reaksi oksidasi menghasilkan partikel
bermuatan positif (kation), kemudian partikel tersebut akan mengalami interaksi
dengan partikel yang tidak bermuatan dan membentuk endapan.
Elektroda yang umum digunakan dalam proses elektrokoagulasi adalah logam Al
(Holtet al., 2002), Fe (Jianget al., 2002), dan Pt/I (Busoet al., 1997). Diantara
logam-logam tersebut, yang paling sering digunakan adalah logam Al, karena
logam Al lebih efektif dalam proses elektrokoagulasi dan mudah didapat.
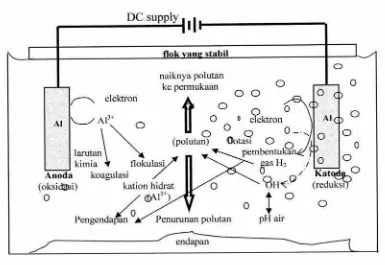
Menurut penelitian yang dilakukan Holtet al. (2002), mekanisme yang terjadi
dalam proses elektrokoagulasi disajikan dalam Gambar 2.3.
Gambar 2.3 menunjukkan berbagai macam rekasi yang terjadi di dalam reaktor
elektrokoagulasi yang melibatkan proses elektrolisis, koagulasi, dan hidrodinamis.
Pada proses elektrolisis, terjadi reaksi oksidasi pada anoda menghasilkan Al3+ dan gas oksigen, sedangkan pada katoda terjadi reaksi reduksi menghasilkan gas
hidrogen. Proses selanjutnya yaitu proses koagulasi yang terjadi karena kation
Al3+berinteraksi dengan partikel organik dalam limbah yang bermuatan negatif yang akan menghasilkan endapan. Proses selanjutnya yaitu hidrodinamis. Pada
proses hidrodinamis, endapan yang terbentuk akan bergerak karena adanya gas
hidrogen dan oksigen yang dihasilkan dari elektrolisis air. Reaksi yang terjadi
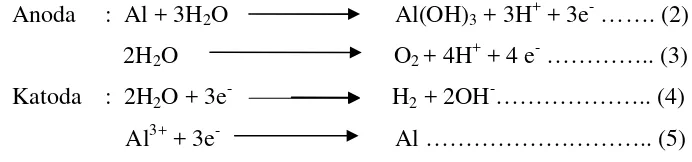
dalam proses elektrolisis dengan menggunakan elektroda Al dituliskan dalam
persamaan reaksi berikut ini:
Anoda : Al + 3H2O Al(OH)3+ 3H++ 3e-……. (2)
2H2O O2+ 4H++ 4 e-………….. (3)
Katoda : 2H2O + 3e- H2+ 2OH-……….. (4)
Al3++ 3e- Al ……….. (5)
Proses elektrokoagulassi dipengaruhi oleh beberapa faktor antara lain pH, waktu,
kuat arus (Chenet al., 2000), potensial dan jenis elektroda (Tsaiet al., 1997) serta
jarak antar elektroda (Mameriet al., 1998).
Jenis elektroda merupakan faktor penting dalam pengolahan limbah cair secara
elektrokimia. Elektroda memiliki kemampuan mengoksidasi senyawa organik
(Bejankiwaret al., 2002). Berdasarkan penelitian Shenget al., (1998) serta Sheng
organik pada pengolahan limbah industri tekstil dan industri penggaraman yang
diikuti dengan menurunnya nilai BOD dan CO
Aplikasi metode elektrokoagulasi sudah banyak diterapkan, meskipun belum
sebanyak metode koagulasi secara konvensional. Dalam penelitian yang telah
dilakukan, diketahui bahwa metode elektrokoagulasi lebih efektif dan lebih cepat
dibandingkan dengan koagulasi konvensional. Hasil penelitian Holtet al. (2002)
menunjukkan bahwa metode elektrokoagulasi mampu menurunkan kadar
kekeruhan sebesar 90%. Selain itu, Jianget al. (2002), dengan menggunakan
elektroda Al dalam penelitiannya diketahui dapat menurunkan intensitas warna
hingga 76% dan penurunan COD sebesar 51%.
Dibandingkan dengan metode koagulasi secara konvensional, metode
elektrokoagulasi mempunyai beberapa keunggulan yaitu prosesnya berlangsung
lebih cepat, peralatan yang digunakan sederhana dan dapat dibuat dalam unit kecil
sehingga sesuai untuk industri rumah tangga seperti rumah makan (restoran).
Selain itu, dalam metode elektrokoagulasi tidak memerlukan pengadukan serta
tidak meenghasilkan limbah sekunder yang biasanya dihasilkan dalam metode
koagulasi konvensional. Proses koagulasi lebih efektif untuk partikel yang
berukuran kecil (partikel mikro) karena partikel tersebut mempunyai rapatan
5. Pemantauan Proses Pengolahan Limbah Cair
Pada prinsipnya, pengolahan limbah bertujuan untuk menurunkan konsentrasi
senyawa organik dalam limbah. Tetapi karena konsentrasi polutan dalam limbah
tidak dapat diketahui, dalam prakteknya pegolahan limbah dipantau dengan
perubahan sifat-sifat limbah yang mempunyai hubungan dengan jumlah polutan
dalam limbah. Sifat-sifat limbah yang umum digunakan adalah kekeruhan, DOC
(dissolved organic carbon) dan TOC (total organic carbon). Dalam prakteknya
penentuan ketiga parameter tersebut seringkali tidak praktis karena membutuhkan
waktu yang relatif lama dan biaya yang cukup mahal. Oleh karena hal tersebut,
pemantauan dapat dilakukan dengan mengamati perubahan nilai kekeruhan,
warna, BOD, COD, dan absorbansi karakteristik pada UV-Vis (Jianget al., 2002).
Parameter-parameter tersebut dianggap berkorelasi baik dengan konsentrasi
polutan dalam limbah. Namun, parameter-parameter tersebut sering menjadi
kendala, seperti pada pengukuran COD dan BOD membutuhkan waktu yang
relatif lama antara 2-4 jam untuk COD dan 4-5 hari untuk BOD, juga memerlukan
biaya yang relatif mahal. Parameter kekeruhan meskipun sederhana dan murah,
namun pengukuran kekeruhan meliputi komponen organik dan anorganik,
sedangkan yang menjadi target hanya komponen organik saja.
Berdasarkan permasalahan yang telah dipaparkan di atas, maka pemantauan yang
dilakukan penelitian ini adalah dengan melihat perubahan nilai absorbansi pada
daerah UV-Vis menggunakan spektrofotometer UV-Vis. Pemantauan UV-Vis
dilakukan terhadap sampel sebelum dan sesudah mengalami perlakuan
absorbansi pada panjang gelombang 254, 272, dan 285 nm, karena absorbansi
pada ketiga panjang gelombang tersebut telah diketahui mempunyai korelasi yang
baik dengan konsentrasi senyawa organik dalam limbah (Kittiset al., 2002).
Perubahan perbandingan nilai absorbansi pada panjang gelombang 250 nm
terhadap absorbansi pada panjang gelombang 365 nm (E2/E3) dan perbandingan
absorbansi pada panjang gelombang 436 nm terhadap absorbansi pada panjang
gelombang 665 nm (E4/E6) juga digunakan, karena kedua perbandingan tersebut
mempunyai hubungan dengan bobot molekul senyawa organik dalam limbah
(Thomsenet al., 2002).
Prinsip dasar sperktrofotometri UV-Vis adalah interaksi antara radiasi
elektromagnetik yang dipancarkan oleh sumber energi dengan materi, dimana
hasil interaksi radiasi UV-Vis terhadap materi mengakibatkan materi tersebut
akan mengalami transisi elektronik (Fessenden dan Fessenden, 1999). Transisi
elektronik yang terjadi ada yang diserap oleh materi dan ada pula yang diteruskan.
Spektrofotometer UV-Vis didasarkan pada hukum Lambert-Beer. Lambert-Beer
menyelidiki mengenai hubungan antara adsorpsi radiasi dan panjang gelombang
melalui medium yang menyerap cahaya. Jika suatu sinar radiasi monokromatik
melewati suatu medium dengan ketebalan tertentu, diketahui bahwa tiap lapisan
menyerap bagian yang sama dari radiasi yang dipancarkan. Dari hukum Lambert
dan hukum Beer, dapat dilihat adanya hubungan antara absorbansi dengan
konsentrasi, atau disebut sebagai hukum Lambert-Beer dimana secara matematis
A = ε. b. c ………. (2)
Dengan : A= Absorbansi
ε = Serapan molar/ekstingsi
b = Panjang jalan lewat medium penyerap
c = Konsentrasi senyawa (solute yang menyerap)
Berdasarkan hal yang telah dipaparkan di atas, maka spektrofotometer UV-Vis
digunakan untuk memantau perubahan kosentrasi senyawa-senyawa organik
dalam limbah cair sebab menunjukkan adanya hubungan absorbansi dengan
III. METODOLOGI PENELITIAN
A. Tempat dan Waktu Kerja Penelitian
Penelitian ini dilakukan di Rumah Makan Sederhana Natar-Lampung Selatan.
Analisis sampel dilakukan di Laboratorium Biomassa dari bulan Juli hingga
September 2011.
B. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah perangkat
elektrokoagulator, elektroda besi, spektrofotometer UV-Vis dan perangkat gelas
yang umum.
Perangkat elektrokoagulator yang digunakan terbuat dari kaca transparan sehingga
berlangsungnya proses elektrokoagulasi dapat diamati secara visual, dengan tinggi
60 cm, panjang 30 cm dan lebar 30 cm. Elektrokoagulator ini dilengkapi dengan
pompa sirkulasi untuk mengukur waktu kontak sampel dengan elektroda sehingga
percobaan dapat dilakukan dengan sistem mengalir. Alat juga dihubungkan
denganpower supplyuntuk mengatur besarnya potensial yang digunakan dalam
Bahan-bahan yang digunakan adalah sampel limbah cair dari restoran yang
diambil di daerah Natar Lampung Selatan.
C. Persiapan
1. Penyiapan elektroda
Elektroda yang digunakan pada proses elektrokoagulasi adalah plat besi (Fe)
dengan panjang 60 cm. Elektroda tersebut dipasang secara paralel pada
elektrokoagulator dan dihubungkan denganpower supplydengan susunan
elektroda monopolar dan dipolar.
2. Pengambilan Sampel
Sampel limbah cair restoran diambil langsung dari rumah makan sederhana
Lampung Selatan. Limbah yang diambil merupakan limbah segar yang ditampung
sebelumnya menggunakan bak penampung. Ada dua jenis limbah yang
ditampung, yaitu limbah yang berasal dari aliran pembuangan pencucian piring
dan limbah yang diambil dari aliran pembuangan sisa-sisa masakan, seperti air
santan dan sebagainya.
Sebelum dilakukan elektrokoagulasi, limbah tersebut disaring terlebih dahulu,
agar limbah padat terpisah dari limbah cairnya, sehingga diperoleh sampel limbah
cair yang terbebas dari kotoran-kotoran yang terdapat dalam limbah. Limbah cair
aliran pembuangan sisa-sisa masakan, kemudian digabungkan di satu tempat lalu
diaduk agar sampel tersebut homogen.
D. Percobaan
Secara garis besar penelitian ini mencakup lima percobaan yaitu; karakterisasi
UV-Vis, variasi potensial, waktu kontak, pH, dan percobaan konfirmasi yang
bertujuan untuk melihat efekifitas proses elektrokoagulasi terhadap pengolahan
limbah cair restoran. Proses elektrokoagulasi dilakukan dengan menggunakan
elektroda besi (Fe) yang diketahui paling baik digunakan dalam penanganan
warna (Simanjuntak dan Kamisah, 2004).
1. Karakterisasi UV-Vis
Percobaan ini dilakukan untuk mendapatkan kondisi optimum yaitu kondisi
dimana nilai absorbansi terendah (paling kecil) yang diperoleh dari hasil
pengukuran. Pengukuran absorbansi sampel dilakukan pada panjang gelombang
)
(λ = 254, 272 nm untuk UV dan pada 365, 436, 565 untuk sinar tampak. Selain
itu, absorbansi sampel pada panjang gelombang 254/365 untuk menentukan nilai
E2/E3dan absorbansi pada panjang gelombang 436/565 untuk menentukan nilai
E4/E6sampel.
2. Percobaan dengan variasi potensial
Percobaan ini dilakukan untuk memepelajari pengaruh potensial terhadap
optimumnya. Oleh karena itu, pada percobaan ini digunakan variasi potensial 4,
6, 8, dan 10 volt dengan waktu kontak tetap yakni 30 menit dan pH tetap 7,0.
Untuk menentukan potensial optimumnya, dilakukan analisis menggunakan
spektrofotometer UV-Vis seperti pada percobaan (1).
3. Percobaan dengan variasi waktu kontak
Percobaan ini dilakukan untuk mempelajari pengaruh waktu kontak terhadap
efektifitas proses elektrokoagulasi yang berlangsung, serta menentukan waktu
kontak optimumnya. Oleh karena itu, pada percobaan ini digunakan variasi waktu
kontak 30, 60, 90, dan 120 menit dengan potensial potensial optimum yang telah
diperoleh pada percobaan (2) dan pH tetap 7,0. Untuk menentukan waktu kontak optimumnya, dilakukan analisis menggunakan spektrofotometer UV-Vis seperti
pada percobaan (1).
4. Percobaan dengan variasi pH
Percobaan ini dilakukan untuk mempelajari pengaruh pH terhadap efektifitas
proses elektrokoagulasi yang berlangsung, serta menentukan pH optimumnya.
Oleh karena itu, pada percobaan ini digunakan variasi pH 5, 7, dan 8, dimana
telah diketahui pada penelitian sebelumnya bahwa pH tersebut merupakanrange
pH yang efektif dalam menurunkan kosentrasi polutan organik dalam limbah.
Percobaan ini dilakukan menggunakan potensial optimum dan waktu kontak
menentukan pH optimumnya, dilakukan analisis menggunakan spektrofotometer
UV-Vis seperti pada percobaan (1).
E. Percobaan Konfirmasi
Pada percobaan ini, proses elektrokoagulasi dilakukan menggunakan potensial,
waktu kontak, dan pH optimum yang telah diperoleh dari percobaan sebelumnya
yang kemudian dilakukan proses elektrokoagualsi pada limbah cair restoran untuk
menentukan nilai COD, BOD dan kekeruhannya.
F. Analisis Sampel
Selain analisis dengan spektrofotometer UV-Vis, sampel yang digunakan pada
kondisi optimum tersebut dianalisis lebih lanjut untuk mengetahui apakah proses
elektrokoagulasi yang digunakan efektif dan mampu meningkatkan kualitas
limbah yang diolah. Parameter-parameter yang digunakan sebagai tolak ukur
adalah COD, BOD, dan kekeruhan. Untuk tujuan tersebut, nilai ketiga parameter
kualitas limbah ditentukan untuk sampel sebelum dan sesudah perlakuan dengan
variabel optimum.
1. Penentuanchemical oxygen demand (COD)
Pada penentuan COD, 10 mL sampel dimasukkan ke dalam labu refluks yang
berisi batu didih, ditambahkan 0,2 gram HgSO4dan 5 mL H2SO4- AgSO4,
dikocok secara perlahan dan didinginkan hingga suhu kamar. Kemudian
pada suhu 150 C selama 2 jam. Setelah itu didinginkan hingga suhu kamar
kemudian dititrasi dengan larutan FAS menggunakan indikator ferroin. Titik
akhir ditandai dengan adanya perubahan warna sampel limbah. Untuk blanko
sampel yang digunakan adalah air suling dengan perlakuan yang sama seperti
sampel limbah. Konsentrasi COD dapat ditentukan menggunakan persamaan
berikut:
COD (mg/L) = ( ) 8 ) 1000
Keterangan:
A = Volume titran untuk blanko (mL) B = Volume titran untuk sampel (mL) C = Volume sampel (mL)
N = Normalitas FAS (ferro ammonium sulfat) Fp = faktor pengenceran
8 = berat ekuivalen oksigen
2. Penentuanbiologycal oxygen demand (BOD)
Untuk penentuan BOD, sampel diencerkan terlebih dahulu kemudian diukur DO
(Dissolved Oxygen) menggunakan DO meter yang dianggap sebagai DO0.
Kemudian sampel dimasukkan ke dalam botol berwarna gelap dan diinkubasi di
tempat gelap selama 5 hari pada suhu 20oC. Setelah 5 hari diukur kembali DO5
menggunakan DO meter. Kosentrasi BOD dapat ditentukan menggunakan
persamaan berikut :
BOD (mg/L) = (D -D ) x P
Keterangan:
D5= Nilai oksigen terlarut sampel setelah diinkubasi selama 5 hari (mg/L)
P = Faktor pengenceran
3. Penentuan kekeruhan
Penentuan kekeruhan dilakukan menggunakan spektrofotometer UV-Vis pada
panjang gelombang 420 nm. Absorbansi pada panjang gelombang tersebut
diketahui memiliki hubungan linier dengan kekeruhan. Adapun percobaan secara
keseluruhan dirangkum dalam diagram alir percobaan yang dapat dilihat pada
V. KESIMPULAN DAN SARAN
A. Kesimpulan
Dari percobaan yang telah dilakukan, maka dapat diambil beberapa kesimpulan,
sebagai berikut:
1. Spektrum karakteristik UV-Vis sampel menunjukkan adanya penurunan
absorbansi dengan adanya pertambahan panjang gelombang. Namun, tidak
ada nilai maksimum maupun minimum yang teramati.
2. Kondisi optimum yang diperoleh dari percobaan dengan susunan elektroda
monopolar yakni diperoleh potensial 6 volt, waktu kontak 30 menit dan pH 7.
Sedangkan untuk susunan elektroda dipolar seharusnya kation yang terbentuk
lebih banyak dan seharusnya proses elektrokoagulasi bisa lebih optimal.
3. Diperoleh persen penurunan nilai kekeruhan, COD dan BOD sebesar
-21,17%; 10,05% dan 20,75%. Persen penurunan nilai kekeruhan yang
diperoleh meningkat karena sifat logam Fe yang korosif sehingga
kemungkinan Fe ikut bereaksi membentuk Fe(OH)4-pada katoda yang
menyebabkan kekeruhan dalam proses elektrokoagulasi.
5. Hasil penelitian menunjukkan bahwa proses elektrokoagulasi menggunakan
logam Fe tidak cukup efektif untuk mengurangi polutan organik dalam
limbah cair.
B. Saran
Perlu dilakukan penelitian menggunakan elektroda yang lain untuk
mengoptimalkan proses elektrokoagulasi dalam menurunkan nilai COD, BOD dan
(Skripsi)
Oleh
KURRATUL UYUN
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
(Skripsi)
Oleh
KURRATUL UYUN
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA SAINS
Pada
Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
ELEKTRODA Fe DENGAN SUSUNAN MONOPOLAR DAN DIPOLAR
Nama Mahasiswa : Kurratul Uyun
Nomor Pokok Mahasiswa : 0617011039
Jurusan : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam
MENYETUJUI
1. Komisi Pembimbing
Dra. Ilim, M.S. Wasinton Simanjuntak, Ph.D.
NIP 196505251990032002 NIP 195907061988111001
2. Ketua Jurusan
Dr. Andi Setiawan, Ph.D.
1. Tim Penguji
Ketua :Dra. Ilim, M.S. ...
Sekretaris :Wasinton Simanjuntak, Ph.D. ..………….
Penguji Utama :Diky Hidayat, M.Si. ..………...
2. Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Prof. Suharso, Ph.D.
NIP 196905301995121001
Jadikanlah sabar dan shalat sebagai penolongmu, dan
sesungguhnya yang demikian itu sungguh berat, kecuali bagi
orang-orang yang khusyu (QS. Al-Baqarah, 2:45)
Berfikirlah diluar kebiasaan, karena tantangan yang
kita hadapi sungguh luar biasa
Sesungguhnya ilmu itu diperoleh dengan belajar, kesantunan itu
diperoleh dengan kerendahan hati, sedangkan kesabaran itu
diperoleh dengan keteguhan hati
(HR. Ibnu Fajar)
Musuh yang paling berbahaya di atas dunia ini
adalah penakut dan bimbang. Teman yang paling
setia, hanyalah keberanian dan keyakinan yang teguh
teruntuk :
Mama dan Papa Tercinta , atas segala do a, kasih sayang serta
kesabarannya dalam mendidik putra-putrinya. Tak terlukiskan cinta,
pengorbanan, kasih dan sayang yang kalian berikan, dan takkan pernah
terbalaskan
Kakak-kakakku Terhebat , atas saran, motivasi, kasih sayang dan
tauladan yang telah diberikan kepadaku
Ponakan-ponakan Tersayang atas keceriaan, canda, tawa dan senyuman
kalian yang tulus
Keluarga besarku Tercinta , keluarga besar Drs. H. Ismail dan Siti
Aisyah
Almamaterku Tercinta Universitas Lampung
Penulis dilahirkan di Serang, Provinsi Banten pada tanggal 17 April
1988, sebagai anak keenam dari enam bersaudara, pasangan Bapak Drs.
H. Ismail dan Ibu Hj. Siti Aisyah.
Pendidikan formal dimulai dengan memasuki jenjang pendidikan Sekolah Dasar (SD) di
SDN 1 Tegal Jetak Kecamatan Ciruas, yang diselesaikan pada tahun 2000. Madrasah
Tsanawiyah Negeri (MTsN) di MTsN 1 Ciruas Serang-Banten, yang diselesaikan pada
tahun 2003 dan Sekolah Menengah Atas (SMA) di SMAN 1 Ciruas Serang-Banten,
yang diselesaikan pada tahun 2006.
Tahun 2006, penulis terdaftar sebagai mahasiswa Jurusan Kimia, Fakultas Matematika
dan Ilmu Pengetahuan Alam (FMIPA) Universitas Lampung, melalui jalur Seleksi
Penerimaan Mahasiswa Baru (SPMB). Selama menjadi mahasiswa, penulis aktif
diberbagai organisasi diantaranya sebagai anggota muda BEM Universitas Lampung,
anggota muda Bidang Sosial dan Kemasyarakatan (SosMas) Himpunan Mahasiswa
Kimia (HIMAKI) dan Rohani Islam (ROIS) FMIPA Universitas Lampung periode
2006/2007. Anggota Bidang Sosial dan Kemasyarakatan HIMAKI dan ROIS FMIPA
Universitas Lampung periode 2007/2008. Sekretaris Bidang (SekBid) ROIS FMIPA
FMIPA Universitas Lampung pada periode 2008/2009 dan Sekretaris Biro (SekBir)
2009/2010 untuk mahasiswa Jurusan Teknik Pertanian Fakultas Pertanian. Asisten
praktikum Kimia Fisik Dasar periode 2008/2009 dan 2009/2010 untuk mahasiswa
Jurusan Teknik Kimia Fakultas Teknik, serta asisten praktikum Kimia Fisik I periode
Segala puji bagi Allah SWT yang telah menjadikan ilmu sebagai sifat kesempurnaan
yang paling tinggi. Sholawat dan salam semoga selalu tercurah kepada suri tauladan
umat yaitu Nabi Muhammad saw. Alhamdullillah atas rahmat, lipahan berkah dan
hidayah- Nya lah penulis dapat menyelesaikan skripsi yang berjudul :
STUDI PENGARUH POTENSIAL, WAKTU KONTAK, DAN pH TERHADAP METODE ELEKTROKOAGULASI LIMBAH CAIR RESTORAN
MENGGUNAKAN ELEKTRODA Fe
DENGAN SUSUNAN MONOPOLAR DAN DIPOLAR
Dalam menyelesaikan skripsi ini penulis tidak luput dari bantuan dan bimbingan dari
berbagai pihak. Dalam kesempatan ini, penulis ingin mengucapkan terima kasih kepada :
1. Ibu Dra.Ilim, M.S, sebagai pembimbing I atas kesediaannya meluangkan waktu,
memberikan bimbingan, motivasi, nasehat, saran dan kritik dalam proses
penyelesaian skripsi.
2. Bapak Wasinton Simanjuntak, Ph.D., sebagai pembimbing II yang telah
meluangkan waktu, memberikan bimbingan, motivasi, arahan dan saran selama
penelitian dan penyelesaian skripsi.
3. Bapak Diky Hidayat, M.Si., sebagai pembahas atas bimbingan, saran dan kritik
5. Bapak Prof. Suharso Ph.D. selaku Dekan Fakultas FMIPA Unversitas Lampung.
6. Bapak dan Ibu dosen, staf pengajar dan karyawan di lingkungan FMIPA
Universitas Lampung.
7. Ibu dan Bapak “Tercinta” atas segala do’a, kasih sayang, nasehat, kesabaran serta
cinta kasih yang tiada henti yang diberikan untuk kesuksesanku.
8. Kakak kakakku tersayang yang selalu memberikan dukungan, motivasi dan do’a
untuk kesuksesanku.
9. Teman-teman seperjuangan di Rois FMIPA, Himaki, BEM FMIPA Unila, BEM
Unila atas kerjasama dan semangatnya.
10. Sahabat-sahabat terbaikku Sumartini Dwi Astuti, Feraliana, S.Si., Tutik, S.Si.,
Kartika Fandika, S.Si., Triana Widya Sari, S.Si., Rikayana, S.Si., , Vera Septaria,
S.Si. dan Ekawati S.Si. Terima kasih atas waktu, dukungan, motivasi, keceriaan
dan kebersamaan yang telah kalian berikan untuk menyemangatiku dalam
menyelesaikan skripsi.
11. Teman-teman seperjuangan dalam penelitian Mbak Yesi S.Si dan Mbak Karlin
terima kasih atas bantuan, dukungan dan kebersamaannya selama penelitian.
12. Teman-teman 2006 Sinta Ardiarti, S.Si., Idra Herlina, S.Si., Nurma Hayati S.Si.,
Rusyda Ulfa S.Si., Mustika Soraya S.Si., Nina Anggraeni, S.Si., Oktaviani A. M,
S.Si., Eka Eva Krisna, S.Si., Ni Putu Inda S.Si., RR. Ari, S.Si., Septiyana S.Si.,
Yulistia Anggraeni, S.Si., Yuniarti, S.Si., Lince Dameria, S.Si., Nova Fransisca,
Fretti, Wuri Putri, Prio Santoso,S.Si., Roni Setyo Nugroho, S.Si., Edwin Riski
Safitra S.Si., Tomi Sutrisno, S.Si., Purwanto, Slamet Kosasi, Alex Sufyantoro,
Awan Nurfatwa Sandi., Hadi Prayoga, Agung, Deri, Riski (kiki), dan Anju terima
kasih untuk kebersamaannya.
13. Teman-teman angkatan 2004, 2005, 2006, 2007, 2008 dan 2009 yang tidak bisa ku
sebutkan satu persatu.
14. Teman-teman HIMSAC Kak Lukman, S.Si., Kak Iman L. H, S.Si., Kak Cepi Arif,
S.P., dr. Rifki Fathurrosyidin, Kang Rohmat, S.T., Kang Gigin, S.T., Teh Isna.,
S.Pd., Teh Farhat, S.Pd., Teh Leli, S.Pd., Teh Hani, S.Si., Teh Ratna., S.E., Wawan
Sofwan, S.Si., Dika Ferdiansyah., Tb. Ahmad Hizbullah, Hidayat, Rizki, S.I.P.,
Afiyah, S.Pd., Sinta., S.P., Rara., S.E.,Ade Faturrohman, Widi, Ujang, Syu’eb,
Muhajir, Ina, Ummi, Tiara, Teh Iyul, Ibu HIMSAC dan seluruh anggota HIMSAC
yang tidak bisa disebutkan satu persatu. Terima kasih atas kebersamaan dan
kekeluargaan yang telah diberikan.
15. Teman-teman kosan Aisyah Mbak Iyo, Mbak Ninda, Mbak Ayi, Mbak Lia, Mbak
Hastin, Mbak Riri, Mbak Elva, Mbak Evi, Mbak Indar, Anisa Narullita, Rusyda
Fitriani, Anggi Handari, Nanik Agustina, Risma, Ayu, Ila dan keluarga besar Ayuk
Vera. Terima kasih atas bantuan dan kebersamaan yang telah diberikan, semoga
persaudaraan kita tidak terputus sampai di sini.
16. Ryandi, Novan Giri Prasetyo, karyawan dan karyawati Restoran Sederhana. Terima
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, akan
tetapi sedikit harapan semoga skripsi yang sederhana ini dapat berguna dan bermanfaat
untuk orang lain. Amin.
Bandar Lampung, Agustus 2012
Penulis