ANALISIS GENETIK DAN STUDI PEWARISAN SIFAT
KETAHANAN CABAI (Capsicum annuum L.)
TERHADAP ANTRAKNOSA
YANG DISEBABKAN OLEH Colletotrichum acutatum
MUHAMAD SYUKUR
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi “Analisis Genetik dan Pewarisan Sifat Ketahanan Cabai (Capsicum annuum L.) terhadap Antraknosa yang Disebabkan oleh Colletotrichum acutatum” adalah karya saya sendiri dengan arahan Komisi Pembimbing dan belum diajukan dalam bentuk apapun kepada Perguruan Tinggi manapun. Sumber informasi yang berasal atau kutipan dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Bogor, Agustus 2007
Muhamad Syukur
ABSTRACT
MUHAMAD SYUKUR. Genetics Analysis and Inheritance Studies of Resistance to Anthracnose caused by Colletotrichum acutatum in Pepper (Capsicum annuum L.). Under direction of SRIANI SUJIPRIHATI, JAJAH KOSWARA and WIDODO.
Pepper anthracnose is one of the most destructive diseases in Indonesia. Anthracnose in pepper caused by Colletotrichum acutatum have been reported to be predominant disease in pepper fields of Indonesia. Inheritance of resistance to anthracnose caused by C. acutatum in Capsicum annuum was studied.
Study on genetics analysis and inheritance of resistance to anthracnose were conducted in four steps: (1) resistance identification to anthracnose and caracterization of pepper germ plasm, (2) inheritance study of resistance to anthracnose in peppers, (3) diallel analysis to estimate genetics parameter of resistance to anthracnose in peppers, (4) genetic x environment interaction for resistance to anthracnose in peppers.
The experiment on step (1) used the collection of pepper genotypes from the Department of Agronomy and Horticulture, IPB. Monoconidial isolate of C. acutatum were obtained by Dr. Widodo, Plant Protection Department, IPB. Inoculation methods were performed according to the procedure by AVRDC and resistance score were performed according to the modified procedure by Yoon method. This inoculation method was used in the experiment step (2), (3) and (4). Morfological character were observed according to the procedure by IPGR. The experiment on step (2) used the two populations set derived from a cross between a resistant line ‘C-15’ and susceptible lines ‘C-2’ and ‘C-19’, that is population of (P1), (P2), F1, F1R, BCP1, BCP2 and F2, respectively. The experiment on step (3)
used the five parent lines for full diallel crosses. The experiment on step (4) used the seven pure lines in Tajur and Situ Gede, and 16 hybrids in Tajur, Leuwikopo and Ciherang.
The experiments showed that C-15 genotype was more resistant to anthracnose than another 14 genotypes. C-8 and C-49 genotypes were recorded as susceptible to anthracnose. In contrast, all other genotypes were recorded as highly susceptible to anthracnose.
There were no maternal effect based on t-test of F1 and F1R. Anthracnose
resistance were controlled by polygenic genes. The degree of dominance were partially recessive. Gene effects for resistance to anthracnose were additive and dominance. Additive effects were larger than dominance effects. Broad-sense heritability values were medium until high and narrow-sense heritability values were medium.
C-15 genotype contained a high proportion of recessive alleles. In contrast, C-2 genotype contain a high proportion of dominant alleles. Dominant genes were outnumbered than recessive genes in the parent populations. The selection for resistance to C. acutatum on pepper breeding programmes shoud be conducted on later generations and multipe crosses method with transgressive recombination are recomended. There were genetic x environment interactions in controlling of resistance to anthracnose caused by C. acutatum.
RINGKASAN
MUHAMAD SYUKUR. Analisis Genetik dan Pewarisan Sifat Ketahanan Cabai (Capsicum annuum L.) terhadap Antraknosa yang Disebabkan oleh Colletotrichum acutatum. Dibimbing oleh SRIANI SUJIPRIHATI, JAJAH KOSWARA DAN WIDODO.
Salah satu faktor dominan yang menyebabkan rendahnya produktivitas cabai Indonesia adalah serangan penyakit antraknosa. Antraknosa pada cabai disebabkan oleh genus Colletotrichum. Spesies yang paling banyak menyerang cabai di Indonesia saat ini adalah C. acutatum. Studi tentang pewarisan ketahanan cabai terhadap penyakit antraknosa perlu dilakukan guna menentukan strategi program pemuliaan yang efektif dan efisien untuk memperoleh genotipe cabai berdaya hasil tinggi dan tahan penyakit antraknosa.
Penelitian dilakukan dalam empat bagian, yaitu (1) identifikasi ketahanan cabai terhadap antraknosa dan karakterisasi plasma nutfah cabai, (2) studi pewarisan ketahanan cabai terhadap penyakit antraknosa, (3) analisis silang dialel untuk menentukan parameter genetik ketahanan cabai terhadap antraknosa, (4) interaksi genetik x lingkungan untuk ketahanan cabai terhadap antraknosa.
Penelitian bagian (1) menggunakan genotipe cabai koleksi Departemen Agronomi dan Hortikultura. Isolat yang digunakan adalah biakan murni C. acutatum koleksi Departemen Proteksi Tanaman IPB. Inokulasi menggunakan metode AVRDC dan skor ketahanan menggunakan metode Yoon yang dimodifikasi. Metode inokulasi ini seterusnya digunakan pada penelitian bagian (2), (3), dan (4). Sementara itu pengamatan terhadap karakter morfologi mengikuti descriptor for capsicum dari IPGR. Penelitian bagian (2) menggunakan dua set populasi, masing-masing terdiri atas populasi tetua tahan (P1), tetua rentan (P2), F1, F1R, BCP1, BCP2 dan F2. Sebagai tetua tahan adalah C-15, sedangkan tetua
rentan adalah C-2, dan C-19. Penelitian bagian (3) menggunakan lima tetua yang kemudian dilakukan persilangan dialel penuh. Penelitian bagian (4) menggunakan tujuh galur murni dan 16 hibrida. Penelitian yang menggunakan genotipe galur murni dilakukan pada dua lokasi yaitu Tajur dan Situgede, sedangkan yang menggunakan genotipe hibrida dilakukan pada tiga lokasi yaitu Tajur, Leuwikopo dan Ciherang.
Hasil penelitian menunjukkan bahwa genotipe C-15 secara konsisten lebih tahan terhadap antraknosa dibandingkan dengan 14 genotipe lainnya. Genotipe C-8 dan C-49 dikatagorikan sebagai rentan, sedangkan genotipe lainnya dikatagorikan sangat rentan terhadap antraknosa.
Ketahanan terhadap penyakit antraknosa yang disebabkan oleh C. acutatum dikendalikan oleh banyak gen dan tidak ada efek maternal. Gen pengendali ketahanan adalah resesif. Derajat dominansi dikategorikan sebagai resesif tak sempurna. Aksi gen pengendali ketahanan terhadap antraknosa adalah aditif dan dominan. Aksi gen aditif lebih besar dibandingkan aksi gen dominan. Nilai heritabilitas arti luas tergolong sedang hingga tinggi sedangkan heritabilitas arti sempit tergolong sedang.
tahan C. acutatum sebaiknya dilakukan pada generasi lanjut menggunakan metode persilangan ganda dengan rekombinasi transgresif. Ada interaksi genetik x lingkungan dalam mengendalikan ketahanan terhadap antraknosa yang disebabkan oleh C. acutatum, sehingga seleksi ketahanan terhadap antraknosa perlu memperhatikan lingkungan spesifik.
© Hak cipta milik Institut Pertanian Bogor, tahun 2007 Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
ANALISIS GENETIK DAN STUDI PEWARISAN SIFAT
KETAHANAN CABAI (
Capsicum annuum
L.)
TERHADAP ANTRAKNOSA
YANG DISEBABKAN OLEH
Colletotrichum acutatum
MUHAMAD SYUKUR
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Departemen Agronomi dan Hortikultura
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji pada ujian tertutup : Dr. Ir. Yudiwanti, MS
Judul Disertasi : Analisis Genetik dan Studi Pewarisan Sifat Ketahanan Cabai (Capsicum annuum L.) terhadap Antraknosa yang Disebabkan oleh Colletotrichum acutatum
Nama Mahasiswa : Muhamad Syukur Nomor Pokok : A361030011
Disetujui Komisi Pembimbing,
Dr. Ir. Sriani Sujiprihati, MS. Prof. Dr. Ir. Jajah Koswara Ketua Anggota
Dr. Ir. Widodo, MS. Anggota
Diketahui,
Ketua Program Studi Agronomi Dekan Sekolah Pascasarjana
Dr. Ir. Satriyas Ilyas, MS. Prof. Dr. Ir. Khairil A. Notodiputro, MS.
RIWAYAT HIDUP
Penulis lahir di Srikembang, Sumatera Selatan pada 2 Januari 1972, merupakan putra kedua dari lima bersaudara dari ayah Zarmawi dan ibu Nunsiha. Penulis menikah dengan Rahmi Yunianti dan dikaruniai satu orang anak Muhammad Caesar Rahmansyah.
Pada Juni 1990, penulis diterima di Program Studi Agronomi, Jurusan Budidaya Pertanian, Institut Pertanian Bogor (IPB) melalui jalur USMI dan selesai pada tahun 1997. Jenjang strata dua (S2) diikuti pada Program Studi Agronomi bidang Pemuliaan Tanaman Program Pascasarjana IPB sejak tahun 1998 dan selesai pada tahun 2002. Selanjutnya, sejak tahun 2003 mengikuti pendidikan jenjang strata tiga (S3) pada Program Studi Agronomi Sekolah Pascasarjana IPB.
Pada tahun 2000 penulis diterima sebagai staf pengajar pada Departemen Agronomi dan Hortikultura, Fakultas Pertanian IPB. Penulis bergabung pada Bagian Genetika dan Pemuliaan Tanaman.
PRAKATA
Puji syukur ke hadirat Illahi Rabbi, dengan rahmat dan hidayah-Nya, penulis dapat menyelesaikan penelitian dan penulisan disertasi yang berjudul “Analisis Genetik dan Studi Pewarisan Sifat Ketahanan Cabai (Capsicum annuum L.) terhadap Antraknosa yang Disebabkan oleh Colletotrichum acutatum”.
Penelitian dan penulisan disertasi ini berlangsung di bawah bimbingan Dr. Ir. Sriani Sujiprihati, MS. selaku Ketua Komisi Pembimbing, Prof. Dr. Jajah Koswara dan Dr. Ir. Widodo, MS. selaku Anggota Komisi Pembimbing. Pada kesempatan ini penulis menyampaikan terima kasih dan penghargaan yang tulus atas waktu dan kesempatan yang telah diluangkan dalam mengarahkan dan membimbing penulis.
Penelitian dan penyelesaian disertasi ini didanai oleh Hibah Fundamental tahun 2006-2007 dan sebagian oleh Program Penelitian Kerjasama Faperta-AVRDC 2006. Ucapan terima kasih penulis sampaikan kepada Dirjen DIKTI selaku pemberi dana bagi Hibah Fundamental, Dr. Ir. Sriani Sujiprihati, MS. selaku Ketua Peneliti serta Rahmi Yunianti, SP, MSi dan Efi Toding Tondok, SP, MSc masing-masing sebagai anggota Hibah Fundamental. Ucapan terima kasih penulis sampaikan juga kepada Tim Program Penelitian Kerjasama Faperta-AVRDC 2006 yang diketuai oleh Dr. Ir. Sri Hendrastuti Hidayat serta Dr. Ir. Widodo, MS. (anggota bidang mikologi) dan Dr. Ir. Sriani Sujiprihati, MS. (anggota bidang pemuliaan tanaman).
Penghargaan yang setinggi-tingginya serta rasa terima kasih yang tulus, penulis sampaikan kepada :
1. Rektor Institut Pertanian Bogor, Dekan Fakultas Pertanian, Ketua Departemen Agronomi dan Hortikultura yang telah memberikan izin belajar. 2. Dirjen DIKTI yang telah memberikan beasiswa BPPS
4. Dr. Ir. Hajrial Aswidinnoor selaku penguji luar komisi saat ujian prelim dan Dr. Ir. Yudiwanti, MS selaku penguji luar komisi saat ujian tertutup serta Dr. Ir. Trikoesoemaningtyas, MSc (Staf Pengajar Departemen Agronomi dan Hortikultura) dan Dr. Ir. Ani Andayani, M.Agr (Kasubdit Benih Sayuran, Ditjen Hortikultura), selaku penguji luar komisi saat ujian terbuka yang telah memberikan saran-saran dan koreksi konstruktif untuk menyempurnakan tulisan ini.
5. Staf dan Pegawai Departemen Agronomi dan Hortikultura, Fakultas Pertanian IPB atas kerjasama dan bantuannya.
6. Kepala Bagian dan Staf Bagian Genetika dan Pemuliaan Tanaman atas kebersamaan, bantuan dan do’anya.
7. Asisten Lapang: Siti Marwiyah, SP. dan Undang SP, atas bantuan dalam penelitian.
8. Para mahasiswa bimbingan S1 Departemen Agronomi dan Hortikultura:
1) Swisci Margaret (A34402034 ), 2) Neni Hariati (A34402042), 3) Endah Nur Rohmi (A34402022), 4) Habib Ilmi Dirgantara (A34403036), 5) Trias Sita Resmi (A34403035), 6) Dian Iqro (A34403068), 7) Ismayatul Maula (A34303051), 8) Madhumita ( A34303020), 9) M. Zikri Ali (A34403052), 10) Tedi Kurniawan (A34403052), 11) Tri Budianto (A34403057). Mahasiswa bimbingan S1 dari Universitas Nasional (UNAS): 1) Regi
Dwijaya (023112500150032), 2) Layla Indah WS. (023112500150021), 3) Richi Safitri (023112500150038). Mahasiswa S1 Departemen Agronomi
dan Hortikultura: 1) Ahmad Meka Rusyadi (A34401012), 2) Andry Gultom (A34401040).
9. Ayahanda Zarmawi dan Ibunda Nunsiha yang telah membesarkan, mendidik, serta selalu menyertai penulis hingga saat ini dengan kasih sayang dan do’anya.
10. Ayah Mertua Djamalan dan Ibu Mertua Farida yang selalu memberikan dorongan dan kasih sayangnya.
12. Kakak Rodiah sekeluarga; adik-adik: Nurdianah sekeluarga, Saidin dan Subhi atas iringan do’a dan motivasinya.
Semoga karya ini bermanfaat bagi pengembangan ilmu pengetahuan, khususnya di bidang pertanian. Amin.
Bogor, Agustus 2007
xii
DAFTAR ISI
Halaman
PRAKATA... x
DAFTAR ISI... xii
DAFTAR TABEL... xvi
DAFTAR GAMBAR ... xx
DAFTAR LAMPIRAN... xxiii
I. PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 2
Hipotesis... 3
Diagram Alir Penelitian ... 3
II. TINJAUAN PUSTAKA... 6
Klasifikasi, Botani dan Syarat Tumbuh Tanaman Cabai ... 6
Penyakit Antraknosa pada Cabai ... 11
Ketahanan Tanaman Cabai Terhadap Penyakit Antraknosa ... 16
Studi Pewarisan Sifat Ketahanan terhadap Penyakit Antraknosa ... 18
Analisis Silang Dialel ... 21
Interaksi Genetik x Lingkungan... 25
III. IDENTIFIKASI KETAHANAN TERHADAP ANTRAKNOSA YANG DISEBABKAN OLEH Colletotrichum acutatum DAN KARAKTERISASI PLASMA NUTFAH CABAI (Caspcisum annuum L.) ... 29
ABSTRAK ... 29
PENDAHULUAN ... 29
Latar Belakang ... 29
Tujuan Penelitian ... 31
BAHAN DAN METODE ... 31
Waktu dan Tempat Penelitian ... 31
Metode Penelitian ... 31
Penggaluran dan Pemilihan Bahan Kegenetikaan ... 31
Screening Genotipe Cabai untuk Ketahanan terhadap Antraknosa ... 32
Karakterisasi Plasma Nutfah Cabai... 34
HASIL DAN PEMBAHASAN... 34
xiii
Identifikasi Ketahanan terhadap Antraknosa ... 36
Karakterisasi Beberapa Genotipe Cabai... 39
SIMPULAN ... 48
DAFTAR PUSTAKA ... 49
IV. PEWARISAN KETAHANAN CABAI (Capsicum annuum L.) TERHADAP PENYAKIT ANTRAKNOSA YANG DISEBABKAN OLEH Colletotrichum acutatum ... 51
ABSTRAK ... 51
PENDAHULUAN ... 51
Latar Belakang ... 51
Tujuan Penelitian ... 53
BAHAN DAN METODE ... 53
Waktu dan Tempat Penelitian ... 53
Metode Penelitian ... 53
Bahan ... 53
Metode ... 53
Analisis Data ... 54
HASIL DAN PEMBAHASAN... 61
Populasi C-15 x C-2 ... 61
Sebaran Frekuensi Populasi ... 61
Efek Maternal... 63
Derajat Dominansi ... 64
Jumlah Faktor Efektif... 65
Pendugaan Komponen Genetik... 66
Heritabilitas ... 66
Kemajuan Genetik (∆G)... 67
Populasi C-19 x C-15 ... 68
Sebaran Frekuensi Populasi ... 68
Efek Maternal... 69
Derajat Dominansi ... 69
Jumlah Faktor Efektif... 70
Pendugaan Komponen Genetik... 71
Heritabilitas ... 71
SIMPULAN ... 72
DAFTAR PUSTAKA ... 72
V. ANALISIS SILANG DIALEL UNTUK PENDUGAAN PARAMETER GENETIK KETAHANAN CABAI (Capsicum annuum L.) TERHADAP ANTRAKNOSA YANG DISEBABKAN OLEH Colletotrichum acutatum ... 75
ABSTRAK ... 75
PENDAHULUAN ... 75
Latar Belakang ... 75
xiv
BAHAN DAN METODE ... 77
Waktu dan Tempat Penelitian ... 77
Metode Penelitian ... 77
Pembentukan Populasi Dialel ... 77
Pengujian Ketahanan Populasi Dialel Penuh ... 78
Analisis Data ... 78
HASIL DAN PEMBAHASAN... 84
Pendugaan Parameter Genetik ... 84
Interaksi Gen ... 85
Pengaruh Aditif (D) dan Dominansi (H1) ... 85
Distribusi Gen di dalam Tetua ... 86
Tingkat Dominansi... 86
Simpangan Rata-rata F1 dari Tetua Rata-rata... 86
Proporsi Gen Dominan terhadap Gen Resesif ... 87
Arah dan Urutan Dominansi ... 87
Jumlah Gen Pengendali Karakter... 90
Heritabilitas ... 90
Batas Tertinggi Fenotipe Hasil Seleksi ... 91
Daya Gabung... 91
Daya Gabung Umum (DGU) ... 91
Daya Gabung Khusus (DGK) ... 92
SIMPULAN ... 93
DAFTAR PUSTAKA ... 94
VI. INTERAKSI GENETIK X LINGKUNGAN UNTUK KETAHANAN CABAI (Capsicum annuum L.) TERHADAP ANTRAKNOSA YANG DISEBABKAN OLEH Colletotrichum acutatum ... 96
ABSTRAK ... 96
PENDAHULUAN ... 96
Latar Belakang ... 96
Tujuan Penelitian ... 97
BAHAN DAN METODE ... 97
Waktu dan Tempat Penelitian ... 97
Metode Penelitian ... 98
HASIL DAN PEMBAHASAN... 100
Populasi Galur Murni... 100
Populasi Hibrida... 102
Ragam Genetik dan Heritabilitas ... 108
SIMPULAN ... 109
DAFTAR PUSTAKA ... 110
VII. PEMBAHASAN UMUM... 112
VIII. SIMPULAN DAN SARAN ... 120
Simpulan ... 120
xv
IX. DAFTAR PUSTAKA ... 122
xvi
DAFTAR TABEL
No. Halaman
1. Klasifikasi Cabai yang Telah Dibudidayakan dan Tipe Liarnya serta Daerah Penyebaran ... 7
2. Keserasian Persilangan antar Spesies Capsicum dan Fertilitas Hibrid ... 8
3. Hasil Analisis Berdasarkan Marka RAPD Menggunakan dua
Primer pada 13 Isolat Colletotrichum ... 12
4. Skor dan Kriteria Ketahanan Cabai terhadap Penyakit Antraknosa Berdasarkan Kejadian Penyakit ... 31
5. Empat Belas Genotipe Cabai Terpilih ... 35
6. Ketahanan Beberapa Genotipe Cabai terhadap Penyakit Antraknosa yang Disebabkan oleh Colletotrichum acutatum Isolat BGR 027, MJK 01, PSG 07 dan PYK 04 ... 36
7. Ketahanan Beberapa Genotipe Cabai terhadap Penyakit Antraknosa yang Disebabkan oleh Colletotrichum acutatum Isolat PYK 04 Menggunakan Metode Inokulasi Tusuk dan Celup ... 38
8. Kuadrat Tengah Beberapa Sifat Kuantitatif pada Beberapa
Genotipe Cabai ... 39
9. Nilai Tengah Beberapa Sifat Kuantitatif pada Beberapa Genotipe Cabai ... 40
10.Kadar Capcaisin dan Aktivitas Peroksidase Beberapa Genotipe Cabai ... 43
11.Korelasi antara Kadar Capsaicin dan Aktivitas Peroksidase dengan Ketahanan Cabai terhadap Antraknosa ... 44
12.Nilai Akar Ciri Komponen Utama Berdasarkan Analisis
Komponen Utama ... 44
13.Nisbah Fenotipik Pewarisan Karakter Resistensi Tanaman yang Dikendalikan oleh Gen Mayor dalam Populasi Bersegregasi F2... 57
xvii
15.Jumlah Tanaman Cabai pada Setiap Populasi Berdasarkan Skor
Ketahanan terhadap Antraknosa Isolat PYK 04 ... 61
16.Jumlah Tanaman Cabai pada Setiap Populasi Berdasarkan Skor Ketahanan terhadap Antraknosa Isolat BGR 027 ... 62
17.Nilai Rata-rata dan Galat Baku Skor Ketahanan Penyakit F1 dan F1R Isolat PYK 04 dan BGR 027, Hasil Uji Beda Nilai Tengah dan Kehomogenan Ragam pada Cabai Populasi Persilangan C-15 x C-2.. 63
18.Pendugaan Parameter Genetik Ketahanan Cabai Populasi Persilangan C-15 x C-2 terhadap Antraknosa yang Disebabkan oleh C. acutatum Isolat PYK 04 dan Isolat BGR 027 Berdasarkan Skor Ketahanan ... 67
19.Jumlah Tanaman Cabai pada Setiap Populasi Persilangan C-19 x C-15 Berdasarkan Skor Ketahanan terhadap Antraknosa Isolat PYK 04 ... 68
20.Nilai Rata-rata dan Galat Baku Skor Ketahanan Penyakit F1 dan F1R, Hasil Uji Beda Nilai Tengah dan Kehomogenan Ragam pada Cabai Populasi Persilangan C-19 x C-15 ... 69
21.Pendugaan Parameter Genetik Ketahanan Cabai Populasi Persilangan C-19 x C-15 terhadap Antraknosa yang Disebabkan oleh C. acutatum Isolat PYK 04 Berdasarkan Skor Ketahanan ... 71
22.Persilangan Full Dialel dan Selfing Menggunakan LimaTetua ... 78
23.Komponen Analisis Ragam Analisis Silang Dialel ... 79
24.Setengah Dialel Ketahanan Cabai terhadap C. acutatum ... 79
25.Komponen Analisis Ragam untuk Daya Gabung Menggunakan Metode I Griffing ... 83
26.Kuadrat Tengah Genotipe Ketahanan Cabai Terhadap Antraknosa Isolat PYK 04, BGR 027, MJK 01 dan PSG 07 ... 84
27.Pendugaan Parameter Genetik Ketahanan Cabai Terhadap Antraknosa Isolat PYK 04, BGR 027, MJK 01 dan PSG 07 pada Cabai Menggunakan Analisis Silang Dialel Metode Hayman ... 85
xviii
29.Sebaran Vr + Wr ... 88
30.Analisis Ragam Daya Gabung Umum (DGU) dan Daya Gabung
Khusus (DGK) Sifat Ketahanan Cabai Terhadap Antraknosa Isolat PYK 04, BGR 027, MJK 01 dan PSG 07 ... 92
31.Nilai Daya Gabung Umum (DGU) dan Daya Gabung Khusus
(DGK) Sifat Ketahanan Terhadap Cabai Antraknosa Isolat PYK 04, BGR 027, MJK 01 dan PSG 07 ... 93
32.Kode Genotipe Populasi Cabai Hibrida ... 98
33.Analisis Ragam Gabungan di Beberapa Lokasi Pengujian
Menggunakan Model Random ... 99
34.Analisis Ragam Ketahanan Tujuh Cabai Galur terhadap Penyakit Antraknosa Isolat PYK 04, BGR 027, MJK 01 dan PSG 07 Murni di Dua Lokasi ... 101
35.Ketahanan Tujuh Cabai Galur Murni terhadap Penyakit Antraknosa Isolat BGR 027 di Dua Lokasi ... 102
36.Analisis Ragam Ketahanan 16 Cabai Hibrida terhadap Penyakit Antraknosa Isolat PYK 04, BGR 027, MJK 01 dan PSG 07 di Tiga Lokasi ... 102
37.Ketahanan 16 Cabai Hibrida terhadap Penyakit Antraknosa Isolat PYK 04 di Tiga Lokasi ... 103
38.Ketahanan 16 Cabai Hibrida terhadap Penyakit Antraknosa Isolat PSG 07 di Tiga Lokasi ... 104
39.Analisis Ragam AMMI2 16 Genotipe Cabai Hibrida Karakter
Ketahanan terhadap Antraknosa Isolat PYK 04 pada Tiga Lokasi ... 105
40.Analisis Ragam AMMI2 16 Genotipe Cabai Hibrida Karakter
Ketahanan terhadap Antraknosa Isolat PSG 07 pada Tiga Lokasi ... 107
xix
xx
DAFTAR GAMBAR
No. Halaman
1. Diagram Alir Penelitian ... 4
2. Pita Penanda Berdasarkan Analisis RAPD pada 13 Isolat
Colletotrichum ... 12
3. Gejala Serangan Antraknosa ... 14
4. Siklus Penyakit Antraknosa yang Disebabkan oleh Colletotrichum
sp. ... 15
5. Konidia Beberapa Spesies Colletotrichum ... 16
6. Isolat PYK 04, MJK 01, PSG 07 dan BGR 027 yang Siap
Digunakan ... 33
7. Konidia Isolat PYK 04 ... 33
8. Selfing Perbanyakan Tetua dengan Sungkup Individu ... 35
9. Penampilan Buah Cabai Lima Hari Setelah Inokulasi C. acutatum ... 37
10.Pengelompokan Beberapa Genotipe Cabai Berdasarkan KU I dan KU II ... 45
11.Pengelompokan Beberapa Genotipe Cabai Berdasarkan KU I dan KU III ... 46
12.Pengelompokan Beberapa Genotipe Cabai Berdasarkan KU II dan KU III ... 46
13.Dendogram Hasil Analisis Gerombol Beberapa Genotipe Cabai ... 47
14.Skema Persilangan antara Genotipe Rentan (P1) dan Genotipe Tahan (P2) Penyakit Antraknosa dalam Pembuatan Mapping
Population... 54
15.Buah Cabai P1, P2, F1, F1R dan F2 Lima Hari Setelah Inokulasi
xxi
16.Skema Posisi Relatif Nilai Tengah F1 terhadap Kedua Tetuanya Berdasarkan Skor Ketahanan Cabai Populasi Persilangan 15 x C-2 terhadap Antraknosa Isolat PYK 04 ... 64
17.Skema Posisi Relatif Nilai Tengah F1 terhadap Kedua Tetuanya Berdasarkan Skor Ketahanan Cabai Populasi Persilangan 15 x C-2 terhadap Antraknosa Isolat BGR 0C-27 pada... 64
18.Sebaran Frekuensi pada Populasi F2 Berdasarkan Skor Ketahanan Cabai Populasi Persilangan C-15 x C-2 terhadap Antraknosa Isolat PYK 04... 65
19.Sebaran Frekuensi pada Populasi F2 Berdasarkan Skor Ketahanan Cabai Populasi Persilangan C-15 x C-2 terhadap Antraknosa Isolat BGR 027 ... 65
20.Skema Posisi Relatif Nilai Tengah F1 terhadap Kedua Tetuanya Berdasarkan Skor Ketahanan Cabai Populasi Persilangan 19 x C-15 terhadap Antraknosa Isolat PYK 04 ... 70
21.Sebaran Frekuensi pada Populasi F2 Berdasarkan Skor Ketahanan Cabai Populasi Persilangan C-19 x C-15 terhadap Antraknosa Isolat PYK 04... 70
22.Hubungan Peragam (Wr) dan Ragam (Vr) Sifat Ketahanan Cabai terhadap Antraknosa yang Disebabkan oleh C. acutatum Isolat PYK 04 ... 88
23.Hubungan Peragam (Wr) dan Ragam (Vr) Sifat Ketahanan Cabai terhadap Antraknosa yang Disebabkan oleh C. acutatum Isolat BGR 027 ... 89
24.Hubungan Peragam (Wr) dan Ragam (Vr) Sifat Ketahanan Cabai terhadap Antraknosa yang Disebabkan oleh C. acutatum Isolat MJK 01 pada Cabai... 89
25.Hubungan Peragam (Wr) dan Ragam (Vr) Sifat Ketahanan Cabai terhadap Antraknosa yang Disebabkan oleh C. acutatum Isolat PSG 07 ... 90
26.Biplot Pengaruh Interaksi Model AMMI2 untuk Ketahanan Cabai terhadap Antraknosa Isolat PYK 04... 106
xxii
28.Perilaku Kromosom Meiosis pada Persilangan Interspesifik
xxiii
DAFTAR LAMPIRAN
No. Halaman
1. Descriptors for Capsicum... 129
2. Prosedur Analisis Kadar Capsaicin ... 135
3. Prosedur Analisis Peroksidase ... 137
4. Daftar Genotipe Cabai Koleksi ... 138
5. Beberapa Sifat Kualitatif pada Fase Vegetatif Beberapa Genotipe Cabai ... 141
6. Beberapa Sifat Kualitatif pada Bagian Bunga Beberapa Genotipe Cabai ... 142
7. Beberapa Sifat Kualitatif pada Bagian Buah Beberapa Genotipe Cabai ... 143
8. Kurva Sebaran Normal Hasil Uji Normalitas pada Populasi F2 Persilangan C-15 x C-2 yang Diinokulasi dengan C. acutatum
Isolat PYK 04... 144
9. Kurva Sebaran Normal Hasil Uji Normalitas pada Populasi F2 Persilangan C-15 x C-2 yang Diinokulasi dengan C. acutatum
Isolat BGR 027... 144
10.Kurva Sebaran Normal Hasil Uji Normalitas pada Populasi F2 Persilangan C-19 x C-15 yang Diinokulasi dengan C. acutatum
Isolat PYK 04... 145
11.Tabel Ketahanan Tujuh Cabai Galur Murni terhadap Penyakit Antraknosa Isolat PYK 04 di Dua Lokasi... 145
12.Tabel Ketahanan Tujuh Cabai Galur Murni terhadap Penyakit Antraknosa Isolat MJK 01 di Dua Lokasi ... 146
xxiv
14.Tabel Ketahanan16 Cabai Hibrida terhadap Penyakit Antraknosa Isolat BGR 027 di Tiga Lokasi ... 147
15.Tabel Ketahanan16 Cabai Hibrida terhadap Penyakit Antraknosa Isolat MJK 01 di Tiga Lokasi... 148
I. PENDAHULUAN
Latar Belakang
Ditinjau dari aspek luas areal pertanaman dan nilai komoditi, cabai (Capsicum annuum L.) merupakan salah satu komoditas unggulan hortikultura Indonesia. Pada tahun 2004, luas areal pertanaman cabai mencapai 194.588 ha. Namun demikian, luasnya areal pertanaman tersebut tidak diikuti oleh tingginya produktivitas. Pada tahun 2004 dan 2005, produktivitas cabai berturut-turut hanya 5.67 ton/ha dan 5.84 ton/ha (Direktorat Jenderal Bina Produksi Hortikultura 2007), padahal potensi produksi cabai dapat mencapai 12-20 ton/ha (Duriat 1996).
Salah satu faktor utama yang menyebabkan rendahnya produktivitas cabai Indonesia adalah gangguan hama dan penyakit (Semangun 2000). Beberapa penyakit yang dominan menyerang cabai adalah antraknosa, hawar Phytophthora, layu bakteri dan virus (Yoon 2003). Dari berbagai penyakit tersebut, antraknosa merupakan penyakit yang paling utama dalam menyebabkan rendahnya produktivitas cabai di Indonesia (Suryaningsih et al. 1996).
Antraknosa pada cabai disebabkan oleh genus Colletotrichum, yang digolongkan menjadi enam spesies utama yaitu Colletotrichum gloeosporioides, C. acutatum, C. dematium, C. capsici dan C. coccodes (Kim et al. 1999). Dari
enam spesies tersebut, C. gloeosporioides dan C. acutatum menyebabkan kerusakan pada buah dan kehilangan hasil paling besar (Yoon 2003). Lebih dari 90% antraknosa yang menginfeksi cabai disebabkan oleh C. gloeosporioides. Spesies ini juga dilaporkan paling virulen dibandingkan lima
spesies lainnya. Akan tetapi, akhir-akhir ini spesies paling utama yang menyerang cabai mengalami perubahan menjadi spesies Colletotrichum lain, yaitu C. acutatum (Park 2005). Di Indonesia, dari 13 isolat Colletotrichum yang dikoleksi
dari Bogor, Berebes, Bandung, Pasir Sarongge, Payakumbuh dan Mojokerto, tujuh isolat yang berasal dari enam daerah tersebut merupakan C. acutatum (Widodo (2006), pakar penyakit tanaman, komunikasi pribadi).
75% (Kusandriani dan Permadi 1996). Meskipun telah dilakukan pengendalian sangat intensif menggunakan fungisida, di daerah Brebes, Jawa Tengah, dilaporkan masih menyebabkan kerugian hingga 45%, di Demak hingga 65%, sedangkan di Sumatera Barat mencapai 35% (Sastrosumarjo 2003).
Pada kondisi kering, gejala penyakit ini hanya berupa bercak kecil pada buah cabai. Namun bercak tersebut dapat berkembang cepat selama musim hujan, dimana kelembaban udara dan suhu tinggi. Bahkan dalam kondisi lingkungan yang optimal bagi pertumbuhan patogen, penyakit ini dapat menghancurkan seluruh areal pertanaman cabai (Yoon 2003).
Petani umumnya mengendalikan penyakit antraknosa menggunakan fungisida kontak dan fungisida sistemik secara intensif. Namun penggunaan pestisida secara berlebihan tidak hanya menyebabkan peningkatan biaya produksi, tetapi juga mengakibatkan resiko kesehatan petani dan konsumen, serta kerusakan lingkungan. Oleh karena itu penggunaan varietas yang resisten merupakan cara yang paling tepat untuk mengatasi masalah penyakit antraknosa. Dalam
perakitan varietas tahan penyakit antraknosa, diperlukan tetua donor yang memiliki ketahanan terhadap penyakit antraknosa serta informasi tentang kendali genetik untuk menentukan metode introgresi serta metode seleksi yang efektif. Berdasarkan hal tersebut, maka studi tentang pewarisan ketahanan cabai terhadap penyakit antraknosa perlu dilakukan guna menentukan strategi program pemuliaan yang efektif dan efisien untuk memperoleh varietas cabai berdaya hasil tinggi dan tahan penyakit antraknosa.
Tujuan Penelitian Penelitian ini bertujuan untuk
1. Mengidentifikasi ketahanan cabai terhadap antraknosa dan mengkarakterisasi plasma nutfah cabai.
2. Mempelajari kendali genetik pewarisan sifat ketahanan cabai terhadap antraknosa yang disebabkan oleh C. acutatum.
3
4. Mempelajari interaksi genetik x lingkungan untuk ketahanan cabai terhadap antraknosa.
Hipotesis Hipotesis yang diajukan adalah :
1. Dari sejumlah genotipe cabai terpilih, terdapat setidaknya satu genotipe cabai yang tahan dan satu genotipe cabai yang rentan terhadap penyakit antraknosa disebabkan oleh C. acutatum yang dapat dijadikan tetua untuk pembuatan mapping population.
2. Terdapat lebih dari satu gen yang terkait dengan sifat ketahanan terhadap penyakit antraknosa disebabkan oleh C. acutatum dengan pola pewarisan aditif, dominan, atau resesif, tidak ada efek maternal serta masing-masing gen memiliki pengaruh yang berbeda.
3. Terdapat satu genotipe yang mempunyai daya gabung umum baik dan sepasang genotipe yang mempunyai daya gabung khusus baik untuk ketahanan terhadap penyakit antraknosa disebabkan oleh C. acutatum.
4. Terdapat interaksi genetik x lingkungan untuk ketahanan terhadap penyakit antraknosa disebabkan oleh C. acutatum.
Diagram Alir Penelitian
Kegiatan secara keseluruhan meliputi beberapa percobaan yaitu:
a. Identifikasi ketahanan cabai terhadap antraknosa dan karakterisasi plasma nutfah cabai.
b. Studi pewarisan ketahanan cabai terhadap penyakit antraknosa.
c. Analisis silang dialel untuk menentukan parameter genetik ketahanan cabai terhadap antraknosa.
d. Interaksi genetik x lingkungan untuk ketahanan cabai terhadap antraknosa.
Kendali genetik pewarisan ketahanan terhadap penyakit
antraknosa
Metode seleksi yang efektif dan efisien untuk perakitan cabai unggul tahan penyakit
antraknosa Plasma nutfah cabai koleksi
(lokal, introduksi)
Screening ketahanan cabai terhadapC. acutatum
• Genotipe tahan • Genotipe rentan
Karakterisasi plasma nutfah cabai
• Karakter morfologi dan biokmia
Hibridisasi genotipe cabai terpilih untuk studi
Interaksi genetik x lingkungan
• Ragam genetik • Ragam lingkungan • Ragam interaksi G x E • Heritabilitas arti luas • Stabilitas
• Lingkungan spesifik Studi pewarisan 6 generasi
• Heritabilitas arti luas • Heritabilitas arti sempit • Efek maternal
• Derajat dominansi • Aksi gen
• Jumlah faktor efektif
Silang full diallel
• Heritabilitas arti luas • Heritabilitas arti sempit • Aksi gen
• Sebaran gen pada tetua • DGU dan DGK • Jumlah gen pengendali
Kendali genetik pewarisan ketahanan terhadap penyakit
antraknosa
Metode seleksi yang efektif dan efisien untuk perakitan cabai unggul tahan penyakit
antraknosa Plasma nutfah cabai koleksi
(lokal, introduksi)
Screening ketahanan cabai terhadapC. acutatum
• Genotipe tahan • Genotipe rentan
Screening ketahanan cabai terhadapC. acutatum
• Genotipe tahan • Genotipe rentan
Karakterisasi plasma nutfah cabai
• Karakter morfologi dan biokmia
Karakterisasi plasma nutfah cabai
• Karakter morfologi dan biokmia
Hibridisasi genotipe cabai terpilih untuk studi
Interaksi genetik x lingkungan
• Ragam genetik • Ragam lingkungan • Ragam interaksi G x E • Heritabilitas arti luas • Stabilitas
• Lingkungan spesifik Interaksi genetik x lingkungan
• Ragam genetik • Ragam lingkungan • Ragam interaksi G x E • Heritabilitas arti luas • Stabilitas
• Lingkungan spesifik Studi pewarisan 6 generasi
• Heritabilitas arti luas • Heritabilitas arti sempit • Efek maternal
• Derajat dominansi • Aksi gen
• Jumlah faktor efektif Studi pewarisan 6 generasi
• Heritabilitas arti luas • Heritabilitas arti sempit • Efek maternal
• Derajat dominansi • Aksi gen
• Jumlah faktor efektif
Silang full diallel
• Heritabilitas arti luas • Heritabilitas arti sempit • Aksi gen
• Sebaran gen pada tetua • DGU dan DGK • Jumlah gen pengendali
Silang full diallel
• Heritabilitas arti luas • Heritabilitas arti sempit • Aksi gen
[image:30.612.112.506.88.488.2]• Sebaran gen pada tetua • DGU dan DGK • Jumlah gen pengendali
Gambar 1. Diagram Alir Penelitian
Pada percobaan a, diperoleh: (1) genotipe yang paling tahan dan genotipe yang paling rentan terhadap antraknosa dan (2) genotipe-genotipe cabai yang mempunyai potensi hasil tinggi. Dalam perakitan suatu varietas biasanya genotipe tahan dijadikan sebagai donor ketahanan untuk memperbaiki genotipe cabai yang berdaya hasil tinggi, namun tidak tahan penyakit. Genotipe cabai paling tahan dan paling rentan digunakan sebagai tetua dalam studi pewarisan ketahanan terhadap antraknosa. Hasil percobaan a digunakan pada percobaan b dan c.
5
Informasi yang diperoleh pada percobaan ini adalah pola pewarisan ketahanan cabai terhadap antraknosa sehingga dapat digunakan untuk menentukan strategi pemuliaan yang efektif.
Pada percobaan c disilangkan beberapa genotipe cabai yang diperoleh dari percobaan a. Lima genotipe cabai dilakukan persilangan dialel penuh (full diallel). Hasil silang dialel ini diuji ketahanannya terhadap antraknosa. Dari percobaan ini diperoleh informasi tentang pendugaan parameter genetik, sebaran gen pada tetua, daya gabung umum dan daya gabung khusus. Informasi ini diperlukan untuk melengkapi informasi yang diperoleh pada percobaan b.
Percobaan d bertujuan mempelajari interaksi genetik x lingkungan untuk ketahanan cabai terhadap antraknosa. Informasi ini dapat digunakan untuk memperoleh lingkungan yang cocok dalam melakukan seleksi cabai tahan antraknosa.
Klasifikasi, Botani dan Syarat Tumbuh Tanaman Cabai
Tanaman cabai tergolong divisi Magnoliophyta, kelas Magnolipsida, ordo
Solanales, famili Solanaceae, genus Capsicum. Capsicum annuum L. merupakan
salah satu spesies dari sekitar 20-30 spesies dalam genus Capsicum yang telah
dibudidayakan. Selain C. annuum spesies lain yang telah dibudidayakan adalah
C. frutescens, C. baccatum, C. pubescens, dan C. chinense (Berke 2000).
C. baccatum dan C. pubescens mudah diidentifikasi dan dibedakan satu dengan
yang lainnya, karena terdapat perbedaan yang jelas pada kedua spesies tersebut.
C. annuum, C. chinensis dan C. frustescens mempunyai banyak sifat yang sama,
untuk membedakannya dapat dengan mengamati bunga dan buah dari
masing-masing spesies (Kusandriani 1996a).
Capsicum annuum L. adalah spesies yang paling luas dibudidayakan dan
penting secara ekonomis. Spesies ini mempunyai berbagai bentuk dan ukuran dan
meliputi buah manis dan pedas. C. annuum L. dikelompokkan dalam var.
longum, var. abbreviata, var. grossum, dan var. minimum. Spesies ini
diperkirakan mempunyai pusat asal (penyebaran primer) di Meksiko, kemudian
menyebar ke daerah Amerika Selatan dan Tengah, ke Eropa dan sekarang telah
tersebar luas di daerah tropik dan subtropik (Tindall 1983). Pusat penyebaran
sekunder C. annuum adalah Guatemala (Greenleaf 1986).
Capsicum frutescens atau dikenal dengan nama cabai rawit adalah spesies
semidomestikasi yang ditemukan di dataran rendah tropika Amerika. Selain itu,
Asia Tenggara dikenal sebagai daerah pusat keragaman sekunder. Beberapa
varietas ditanam luas di wilayah panas iklim sedang maupun wilayah tropika
(Greenleaf 1986).
Domestikasi Capsicum chinense tersebar luas di wilayah tropika Amerika,
dan spesies ini sering ditanam di sekitar wilayah Amazon. Evolusi Capsicum
baccatum sebagian besar terbatas di wilayah tengah Amerika Selatan (Bolivia).
7
bentuk liarnya sebagai C. baccatum var. baccatum dan var. microcarpum
(Greenleaf 1986).
Capsicum pubescens ditanam di Amerika Tengah dan dataran tinggi
pegunungan Andes. Bunga memiliki lembar mahkota ungu, dengan kepala sari
ungu; biji keriput dan berwarna hitam. Daun berbulu dan keriting (rugulose);
jaringan dinding buah tebal. Tanaman ini beradaptasi pada suhu rendah pada
ketinggian 2.000-3.000 m di daerah tropika. Tipe moyang liarnya tidak diketahui,
tetapi spesies ini berkerabat dengan spesies liar lain dari Amerika Selatan, seperti
[image:33.612.100.506.317.691.2]C. eximium dan C. cardenasii (Greenleaf 1986).
Tabel 1. Klasifikasi Cabai yang Telah Dibudidayakan dan Tipe Liarnya serta Daerah Penyebaran (Greenleaf 1986)
Spesies Status Daerah Sebaran
A. Kelompok Berbunga Putih
1. C. annuum L. Dibudidayakan Amerika Selatan hingga Colombia tropik, subtropik dan daerah beriklim sedang
2. C. chinense Jacq. Dibudidayakan Dataran rendah Amerika Selatan bagian timur
3. C. frutescens L. Dibudidayakan Amerika tropik
4. C. baccatum L. Dibudidayakan Peru, Bolivia, Paraguay, Brazil, Argentina
5. C. praetermisum
Heiser & Smith
Liar Brazil Selatan
6. C. chacoense A.T. Hunz
Liar Argentina Utara, Bolivia, Paraguay
7. C. galapagoense A.T. Hunz
Liar Pulau Galapagos
B. Kelompok Berbunga Ungu
1. C. pubescens R&P Dibudidayakan Daerah Andes, dataran tinggi Amerika Tengah bagian utara hingga Meksiko
2. C. cardenasii Heiser & Smith
Liar Bolivia
3. C. eximium A.T. Hunz
Liar Bolivia, Argentina Utara
4. C. tovarii Eshbaugh, Smith, Nickrent
Spesies liar lain yang biasa digunakan meliputi C. galapogense,
C. chacoense, C. tovarii, C. praetermissum, C. eximium, dan C. cardenasii. Di
Bolivia C. cardenasii adalah spesies yang sangat sering dipanen dari tanaman liar
(Greenleaf 1986). Satu spesies liar yaitu C. lanceolatum mempunyai pusat
penyebaran di Guetamala (Tong dan Bosland 1997). Klasifikasi cabai dan pusat
[image:34.612.120.507.265.571.2]penyebarannya disajikan pada Tabel 1.
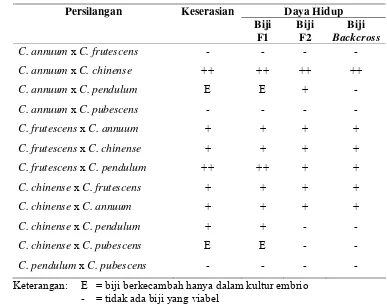
Tabel 2. Keserasian Persilangan antar Spesies Capsicum dan Fertilitas Hibrid (Greenleaf 1986)
Persilangan Keserasian Daya Hidup
Biji
F1
Biji F2
Biji Backcross
C. annuum x C. frutescens - - - -
C. annuum x C. chinense ++ ++ ++ ++
C. annuum x C. pendulum E E + -
C. annuum x C. pubescens - - - -
C. frutescens x C. annuum + + + +
C. frutescens x C. chinense + + + +
C. frutescens x C. pendulum ++ ++ + +
C. chinense x C. frutescens + + + +
C. chinense x C. annuum + + + +
C. chinense x C. pendulum + + - -
C. chinense x C. pubescens E E - -
C. pendulum x C. pubescens - - - -
Keterangan: E = biji berkecambah hanya dalam kultur embrio - = tidak ada biji yang viabel
+ = biji viabel hanya sedikit ++ = biji viabel banyak
Sebagian besar spesies Capsicum bersifat menyerbuk sendiri (self
pollination) tetapi penyerbukan silang (cross pollination) secara alami dapat
terjadi dengan bantuan lebah dengan persentase persilangan berkisar 7.6-36.8%.
Persilangan antar spesies dapat terjadi dengan relatif mudah pada beberapa
9
C. pendulum; akan tetapi sangat sulit untuk kombinasi yang lain, misalkan antara
C. annuum x C. frutescens, C. annuum x pubescens dan C. pendulum x pubescens
(Greenleaf 1986). Keserasian persilangan antar spesies Capsicum dan fertilitas
hibrid disajikan pada Tabel 2.
Tanaman cabai mempunyai jumlah kromosom somatik diploid dengan
kromosom dasar x = 12. Jumlah kromosom normal cabai adalah 2n = 2x = 24
(Berke 2000). Penyimpangan jumlah kromosom x = 13 ditemukan pada spesies
C. ciliatum asal Amerika Selatan bagian barat dan spesies liar dari Brazil, serta
C. lanceolatum asal Guatemala (Tong dan Bosland 1997).
Tanaman cabai memiliki sistem perakaran yang dangkal, diawali dengan
akar tunggang (akar primer) kemudian tumbuh akar rambut ke samping (akar
lateral/akar sekunder). Panjang akar primer berkisar 35-50 cm dan akar lateral
sekitar 35-45 cm (Rubatzky dan Yamaguchi 1997). Akar lateral cepat
berkembang di dalam tanah dan menyebar pada kedalaman 10-15 cm (Messiaen
1992).
Batang utama tegak, berkayu dan bercabang banyak dengan tinggi sekitar
45-150 cm. Pembentukan kayu pada batang utama mulai terjadi pada umur 30
hari setelah tanam (HST). Pada setiap ketiak daun akan tumbuh tunas baru yang
dimulai pada umur 10 HST. Tipe percabangan tegak atau menyebar tergantung
spesiesnya (Rubatzky dan Yamaguchi 1997). Daun-daun tumbuh pada tunas
samping secara berurutan, sedangkan pada batang utama tersebut tersusun secara
spiral. Cabai mempunyai tangkai daun panjang dan daun tunggal dengan helai
daun berbentuk ovate atau lanceolate, agak kaku, berwarna hijau muda sampai
hijau gelap dengan tepi rata (Kusandriani 1996a).
Bunga cabai tergolong bunga lengkap karena terdiri dari kelopak bunga,
mahkota bunga, benang sari dan putik. Kelopak bunga berjumlah enam helai
berwarna kehijauan. Mahkota bunga terdiri atas 5-7, petal berwarna putih susu
atau kadang-kadang ungu. Posisi bunga menggantung atau tegak, panjang bunga
biasanya 0.8-1.5 cm, lebar 0.5 cm dan panjang tangkai bunga antara 3-8 cm.
Tangkai putik berwarna putih, panjangnya sekitar 0.5 cm. Kepala putik berwarna
Kepala sari yang belum matang berwarna biru atau ungu (Berke 2000). Dalam
satu bunga terdapat satu putik dan 5-7 benang sari. Bunga cabai umumnya
merupakan bunga tunggal (kecuali pada spesies tertentu berbunga ganda), terletak
pada hampir setiap ruas (nodus). Bunga cabai cenderung bersifat protogyny dan
tepung sari keluar dari kotak sari pada saat bunga mekar (Kusandriani 1996a).
Bunga pertama terbentuk pada umur 23-31 hari sesudah tanam (HST) dan
buah pertama mulai terbentuk pada umur 29-40 HST. Buah matang dalam waktu
sekitar 45 hari setelah pembuahan. Struktur buah terdiri atas kulit, daging buah
dan sebuah plasenta tempat melekatnya biji. Daging buah umumnya renyah atau
kadang-kadang lunak pada kultivar tertentu. Biji cabai berwarna kuning jerami
(Greenleaf 1986).
Tanaman cabai dapat tumbuh pada berbagai jenis tanah, asalkan
mempunyai drainase dan aerasi yang baik. Tanah yang paling ideal untuk tanaman
cabai adalah yang mengandung bahan organik sekurang-kurangnnya 1.5% dan
mempunyai pH antara 6.0 – 6.5. Keadaan pH tanah sangat penting karena erat
kaitannya dengan ketersediaan unsur hara. Apabila ditanam pada tanah yang
mempunyai pH lebih dari tujuh, tanaman cabai akan menunjukkan gejala klorosis,
yakni tanaman kerdil dan daun menguning yang disebabkan kekurangan unsur
hara besi (Fe). Sebaliknya, pada tanah yang mempunyai pH kurang dari lima,
tanaman cabai juga akan kerdil, karena kekurangan unsur hara kalsium (Ca) dan
magnesium (Mg) atau keracunan aluminium (Al) dan mangan (Mn) (Sumarni
1996).
Suhu udara optimal untuk pertumbuhan cabai pada siang hari adalah 18o–
27oC. Suhu udara yang paling cocok untuk pertumbuhan cabai rata-rata adalah
16oC pada malam hari dan 23oC pada siang hari. Bila suhu udara malam hari di
bawah 16oC dan siang hari di atas 32oC, proses pembungaan dan pembuahan
tanaman cabai akan gagal. Cabai tidak menghendaki curah hujan yang tinggi atau
iklim yang basah, karena pada keadaan tersebut tanaman akan mudah terserang
penyakit, terutama yang disebabkan cendawan. Curah hujan yang sesuai untuk
11
Penyakit Antraknosa pada Cabai
Penyakit antraknosa merupakan kendala biologis terbesar dalam usahatani
cabai, karena disamping dapat menyerang tanaman, juga dapat menyerang buah
yang terbentuk, maupun setelah buah dipanen. Patogen yang menyerang buah
merupakan kendala terbesar dalam peningkatan produksi cabai, karena buah dapat
gugur sebelum panen atau buah menjadi busuk sebelum dan setelah panen,
sehingga mengurangi produksi buah yang dapat dipasarkan. Penyakit antraknosa
dapat berlanjut menyerang buah dalam penyimpanan di tingkat konsumen. Oleh
karena itu penyakit ini dianggap sebagai penyakit yang paling merugikan
dibanding penyakit cabai lainnya.
Antraknosa pada cabai disebabkan oleh genus Colletotrichum, yang
digolongkan menjadi enam spesies utama yaitu Colletotrichum gloeosporioides,
C. acutatum, C. dematium, C. capsici dan C. coccodes (Kim et al. 1999). Dari
enam spesies tersebut, C. gloeosporioides dan C. acutatum menyebabkan
kerusakan pada buah dan kehilangan hasil paling besar (Yoon 2003).
C. gloeosporioides merupakan spesies paling dominan yang menyerang cabai di
Korea (Yoon dan Park 2001). Lebih dari 90% antraknosa yang menginfeksi cabai
disebabkan oleh C. gloeosporioides. Spesies ini juga dilaporkan paling virulen
dibandingkan lima spesies lainnya. Akan tetapi, akhir-akhir ini spesies paling
dominan yang menyerang cabai mengalami perubahan menjadi spesies
Colletotrichum lain, yaitu C. acutatum (Park 2005).
Di Indonesia, patogen antraknosa yang paling banyak dijumpai
menyerang tanaman cabai adalah C. capsici (Syd and Bisb), C. gloeosporioides
(Penz) Sacc. Populasi C. gloeosporioides di lapangan 5-6 kali lebih banyak
daripada populasi C. capsici dan menyebabkan kerusakan lebih parah
(Suryaningsih et al. 1996). Akan tetapi akhir-akhir ini spesies yang paling banyak
dijumpai menyerang cabai di Indonesia adalah C. acutatum. Berdasarkan
penelitian Widodo (2006, pakar penyakit tanaman, komunikasi pribadi), dari 13
isolat Colletotrichum yang dikoleksi dari Bogor, Brebes, Bandung, Pasir
Sarongge, Payakumbuh dan Mojokerto, tujuh isolat yang berasal dari enam
Tabel 3. Hasil Analisis Berdasarkan Marka RAPD Menggunakan Dua Primer Pada 13 Isolat Colletotrichum (Sumber: Widodo (2006), komunikasi pribadi)
Hasil No. Kode sampel
C. acutatum C. gloeosporioides
1 BGR 22A - -
2 BGR 027 + -
3 BDG 01 + -
4 BRB 07A + -
5 BRB 11C - -
6 BRB 16 - -
7 BRB 17 - -
8 PYK 03A1 + -
9 PYK 03A - -
10 PYK 04 + -
11 BKT 04 - -
12 PSG 07 + -
13 MJK 01 + -
Gambar 2. Pita Penanda Berdasarkan Analisis RAPD pada 13 Isolat
Colletotrichum. Keterangan: Lane 1. 100 bp DNA ladder, penanda untuk Colletotrichum acutatum; 2. BGR 22A ; 3. BGR 027; 4.BDG 01; 5.BRB 07A; 6. BRB 11C; 7. BRB 16; 8.BRB 17; 9. PYK 03A1; 10. PYK 03A; 11. PYK 04; 12. BKT 04; 13. -; 14. PSG 07; 15. MJK 01; 16. 100 bp DNA ladder (Sumber: Widodo (2006), komunikasi pribadi).
±490bp 500 bp
13
Penyakit antraknosa menimbulkan gejala busuk buah yang dicirikan oleh
adanya bercak coklat kehitaman pada permukaan buah, yang selanjutnya meluas
menjadi busuk lunak. Pada bagian tengah bercak terdapat kumpulan titik-titik
hitam yang terdiri dari sekelompok seta dan konidium jamur. Serangan yang berat
dapat menyebabkan buah mengering dan keriput sehingga buah yang seharusnya
berwarna merah menjadi seperti jerami (Semangun 2000). Serangan yang terjadi
pada biji akan menyebabkan kegagalan biji untuk berkecambah, pada kecambah
dapat menimbulkan rebah kecambah (damping off) serta pada tanaman dewasa
dapat menimbulkan mati pucuk dan infeksi lebih lanjut dapat menyebabkan busuk
kering pada batang (Suryaningsih et al. 1996). Gejala serangan pada buah, daun
dan batang dapat dilihat pada Gambar 3.
Colletotrichum dapat bertahan baik pada biji, sebagai penyakit tular biji,
pada sisa-sisa tanaman yang terinfeksi maupun pada inang yang lain, diantaranya
tomat. Meskipun cendawan ini mempunyai inang yang sangat banyak, ia juga
dapat bertahan di dalam tanah. Infeksi cendawan ini bersifat laten mampu
bertahan dalam jaringan tanaman dalam bentuk aservulus. Aservulus dapat
tumbuh dan bertahan di dalam biji dalam kurun waktu yang lama, kemudian
miselium tumbuh di luar kulit biji. Miselium dan aservulus tersebut dapat tumbuh
dan bertahan di dalam biji selama ± 9 bulan. Meskipun demikian, bibit yang bebas
dari patogen tersebut di atas apabila ditanam pada lahan yang sudah terinfeksi,
patogen masih dapat menimbulkan penyakit pada buah (Suryaningsih et al.
1996).
Bagian luar dari spora cendawan mengandung perekat yang dapat dengan
mudah menempel pada sasaran infeksi lewat percikan air siraman atau air hujan.
Selain itu, spora dalam keadaan tunggal dapat pula menempel pada pakaian
pekerja, alat-alat pertanian atau terbawa oleh angin. Spora akan cepat
berkecambah apabila menemukan inang. Gejala serangan akan tampak lima hari
setelah terjadi infeksi. Kelembaban relatif udara 95% yaitu pada saat cuaca
berkabut dan berembun dengan suhu udara rata-rata 32oC akan sangat membantu
inisiasi infeksi dan perkembangan penyakit selanjutnya (Suryaningsih et al.
Gambar 3. Gejala Serangan Antraknosa. A. Gejala serangan pada daun, B. Gejala serangan pada buah matang, C. Gejala serangan pada batang, D. Gejala serangan pada buah hijau.
Colletotrichum dapat menyerang buah yang masih hijau dan dapat
menyebabkan mati pucuk. Gejala yang disebabkan oleh Colletotrichum
mula-mula berbentuk bintik-bintik kecil berwarna kehitaman dan berlekuk, pada buah
yang masih hijau atau yang sudah masak. Bintik-bintik ini tepinya berwarna
kuning, membesar dan memanjang. Bagian tengahnya menjadi semakin gelap.
Dalam keadaan lembab, cendawan membentuk badan buah (aservulus) dalam
lingkaran-lingkaran sepusat, yang membentuk massa spora (konidium) berwarna
merah jambu. Penyakit masih berkembang terus pada waktu buah cabai disimpan
atau diangkut. Colletotrichum dapat menyerang daun dan batang tanpa
A B
15
menimbulkan kerugian berarti (Semangun 2000). Cendawan tersebut
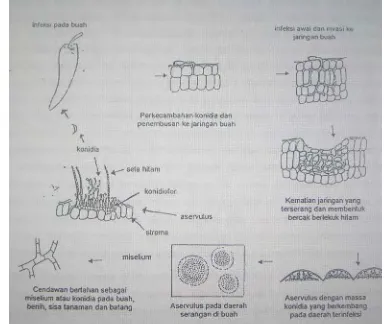
[image:41.612.124.508.145.469.2]bereproduksi dengan membentuk massa konidia dalam aservulus (Gambar 4).
Gambar 4. Siklus Penyakit Antraknosa yang Disebabkan oleh Colletotrichum sp. (Sumber: Agrios 1997 yang dimodifikasi)
C. acutatum mempunyai miselium berwarna putih hingga abu-abu. Koloni
jika dibalik berwarna oranye hingga merah muda. Konidia berbentuk silindris dengan ujung runcing, berukuran 15.1 (12.8-16.9) x 4.8 (4.0 – 5.7) μm. Temperatur optimal adalah 28oC dengan rata-rata pertumbuhan 10.3 mm/hari
Gambar 5. Konidia Beberapa Spesies Colletotricum. A. Konidia
C. gloeosporioides; B & C. Konidia C. acutatum; D. Konidia
C. capsici (Sumber: AVRDC 2003).
Ketahanan Tanaman Cabai Terhadap Penyakit Antraknosa
Tanaman yang tahan terhadap penyakit adalah tanaman yang mampu
menghambat perkembangan patogen sehingga patogen tersebut tidak dapat
berkembang dan menyebar. Sebaliknya tanaman rentan adalah tanaman yang
tidak mampu menghambat perkembangan patogen penyebab penyakit.
Ketahanan terhadap penyakit ini dapat dikelompokkan ke dalam ketahanan
struktural dan ketahanan fungsional. Ketahanan struktural adalah ketahanan
terhadap penyakit yang disebabkan struktur tanaman itu sendiri sehingga patogen
tidak menyukai atau tidak dapat menyerang tanaman tersebut. Ketahanan
struktural ini disebut juga ketahanan pasif atau ketahanan prainfeksi karena
tanaman tidak melakukan reaksi terhadap patogen. Sementara itu, ketahanan
fungsional atau ketahanan aktif adalah ketahanan yang disebabkan oleh adanya
reaksi biokimia tanaman sehingga perkembangan patogen dapat terhambat.
Ketahanan ini disebut juga ketahanan pascainfeksi. Kombinasi antara sifat
struktural dan reaksi biokimia yang digunakan untuk pertahanan bagi tanaman
berbeda antara setiap sistem kombinasi inang-patogen. Bahkan pada inang dan
patogen yang sama, kombinasi tersebut dapat berbeda berdasarkan umur tanaman,
jenis organ dan jaringan tanaman yang diserang, keadaan hara tanaman dan
kondisi cuaca (Agrios 1997). Oleh karena itu tampilan struktural (morfologi)
tanaman ataupun aktifitas biokimia kemungkinan dapat dijadikan penanda ada
17
Ketahanan tanaman cabai menghentikan serangan C. acutatum tergantung
pada pertahanan pasif dan tanggapan aktif yang diinduksi oleh patogen. Dinding
sel tanaman umumnya mengandung polisakarida selulosa dan non-selulosa,
termasuk protein dan berperan sebagai bio-polimer protektif. Salah satu senyawa
protein yang efektif sebagai barier pertahanan adalah glico-protein yang kaya
hidroxiprolin. Pada beberapa tanaman ditemukan teonin yang memiliki aktivitas
anti fungal dan menjadi barier pertahanan melawan cendawan patogen. Senyawa
protein tersebut diproduksi atas perintah gen yang diinduksi oleh serangan
cendawan patogen. Bio-polimer yang lain adalah lignin yang terbentuk melalui
kondensasi fenilpropanoid alkohol dan merupakan komponen dinding sel
sekunder. Lignifikasi dinding sel yang diinduksi oleh patogen umumnya
merupakan produk kerja banyak gen yang terkait dengan biosintetik enzim
biosíntesis lignin, misalnya cynamil alkohol dan dehidrogenase, peroxidase, dan
polifenol oxidase. Calose dan β1-3 glucon diketahui terakumulasi di dinding sel
tanaman setelah terjadi infeksi dan kerusakan mekanik (Huang 2001).
Salah satu senyawa kimia yang terlibat dalam pertahanan tanaman
terhadap serangan patogen adalah senyawa fenolik. Senyawa fenolik yang terlibat
dalam ketahanan penyakit banyak terdapat pada tanaman baik pada tanaman sehat
dan juga pada tanaman sakit, tetapi sintesis atau akumulasinya dipercepat setelah
infeksi adalah senyawa fenolik umum. Senyawa fenolik yang tidak terdapat pada
tanaman sehat, tetapi dihasilkan setelah dirangsang oleh patogen dikenal dengan
istilah fitoaleksin (Agrios 1997).
Salah satu enzim yang dapat mengoksidasi fenolik adalah peroksidase.
Enzim ini dapat mengoksidase fenol menjadi kinon, yang sering lebih beracun
bagi mikroorganisme dibandingkan dengan fenolnya sendiri. Peroksidase juga
meningkatkan laju polimerisasi senyawa fenolik menjadi
senyawa-senyawa seperti lignin, yang terdeposit dalam dinding sel dan papilla tanaman dan
selanjutnya mengganggu pertumbuhan dan perkembangan patogen (Agrios 1997;
Huang 2001). Peningkatan aktivitas enzim peroksidase akan meningkatkan
produk toksin bagi patogen, oleh karena itu menghasilkan tingkat ketahanan lebih
Suatu enzim pada tanaman gandum yang meningkat setelah diinfeksi oleh
Erysiphe graminis adalah peroksidase. Gen yang mengkode enzim peroksidase ini
telah diisolasi. Pada padi, infiltrasi Pseudomonas syringae pv. syringae pada fase
bibit untuk menginduksi ketahanan sistemik terhadap Pyricularia oryzae,
meningkatkan aktivitas enzim peroksidase (Huang 2001). Peningkatan aktivitas
enzim peroksidase berhubungan secara nyata dengan ketahanan terhadap penyakit
greening pada tanaman jeruk (Lelyveld dan Vuuren 1988). Daun tembakau yang
mempunyai aktivitas peroksidase tinggi lebih tahan terhadap infeksi
Pseudomonas tabaci (Lovrekovich et al. 1986).
Dalam rangka mendapatkan informasi tentang karakteristik cabai yang
tahan terhadap antraknosa, Tenaya et al. (2001) melaporkan adanya korelasi yang
kuat antara kadar capsaicin dan fruktosa pada buah, serta aktivitas enzim
peroksidase pada daun dengan ketahanan terhadap antraknosa. Kadar capsaicin
dan aktivitas enzim peroksidase yang tinggi dengan kadar fruktosa rendah
mengindikasikan tanaman tersebut tahan terhadap penyakit antraknosa.
Hasil penelitian Zen et al. (2002) menyebutkan bahwa tidak terdapat
korelasi antara intensitas penyakit antraknosa pada buah cabai dengan aktivitas
enzim peroksidase pada daun fase bibit. Aktivitas enzim peroksidase yang tinggi
tidak berkaitan dengan intensitas serangan penyakit yang rendah. Aktivitas
peroksidase tidak dapat dipakai sebagai kriteria seleksi untuk katahanan terhadap
tanaman cabai terhadap antraknosa.
Studi Pewarisan Sifat
Ketahanan terhadap Penyakit Antraknosa
Pada penelitian pewarisan suatu karakter, sering diperlukan analisis
segregasi dari populasi yang bersegregasi (populasi F2) dengan melibatkan enam
populasi yaitu dua populasi tetua, dua populasi F1 dan dua populasi silang balik
(Back Cross). Asumsi yang digunakan untuk melakukan analisis statistik dan
analisis genetik guna melacak gen-gen pengendali karakter tersebut adalah (1)
tidak ada efek lingkungan, (2) tidak ada efek dominansi antar alel, (3) tidak ada
efek epistasis, (4) gen memberikan efek yang sama dan bersifat aditif untuk
19
lengkap dan tanaman F1 dalam keadaan heterozigositas lengkap (Burns 1976;
Poehlman 1979).
Ketahanan tanaman terhadap penyakit dapat merupakan sifat kualitatif
yang dikendalikan gen mayor atau sifat kuantitatif yang dikendalikan oleh banyak
gen minor. Bila ketahanan dikendalikan oleh satu atau dua gen mayor, ragam
ketahanan akan menunjukkan sebaran diskontinu sehingga umumnya individu
tanaman yang tahan mudah diidentifikasi. Klasifikasi tanaman dalam populasi
yang bersegregasi dapat dibedakan dalam dua kategori, yaitu tahan (infeksi
rendah) dan rentan (infeksi tinggi) (Allard 1960; Russel 1981).
Pada gen-gen yang mengikuti prinsip Mendel (disebut gen mayor) peranan
ragam lingkungan relatif kecil dibandingkan peranan ragam lingkungan gen-gen
minor. Karena jumlah gen mayor umumnya tidak banyak dan peranan faktor
lingkungan relatif kecil, maka ragam fenotipe yang ditampilkan dalam populasi
bersegregasi sebagian besar merupakan ragam genetik, bersifat diskontinu dan
merupakan akibat adanya efek dominan.
Ketahanan sering dikendalikan secara poligenik dan perbedaan antara
tanaman tahan dengan tanaman rentan dalam populasi bersegregasi tidak jelas.
Dalam hal ini, wujud penampilan ketahanan merupakan ragam kontinu dengan
perubahan perbedaan ketahanan yang kecil.
Bila dalam suatu karakter kuantitatif ikut serta efek gen mayor, maka pada
generasi bersegregasi akan terlihat bentuk sebaran frekuensi dengan puncak lebih
dari satu (bimodal atau trimodal) (Chandraratna 1964). Bila alel-alel mempunyai
arah dominasi yang sama akan terlihat adanya kemenjuluran puncak (skewness)
sebaran frekuensi. Heritabilitas yang tinggi adalah manifestasi bentuk sebaran
dengan puncak jamak dan kemenjuluran puncak (Sastrosumarjo 1987).
Untuk menentukan apakah ragam pada karakter tersebut disebabkan oleh
faktor genetik atau oleh faktor lingkungan dilakukan pendugaan nilai
heritabilitas. Heritabilitas sering juga dipakai sebagai tolok ukur kemajuan genetik
yang dapat diharapkan dalam suatu program seleksi (Allard 1960). Sesuai dengan
komponen ragam genetiknya, heritabilitas dibedakan menjadi heritabilitas dalam
arti luas (broad sense heritability) (h2bs) dan heritablitas dalam arti sempit
perbandingan antara ragam genetik total dan ragam fenotipe (h2bs = σ2G / σ2P).
Seperti yang telah diuraikan sebelumnya, bahwa ragam genetik terdiri dari ragam genetik aditif (σ2
A), ragam genetik dominan (σ2D) dan ragam genetik epistasis (σ2I). Heritabilitas dalam arti sempit merupakan perbandingan antara ragam aditif
dan ragam fenotipe (h2ns = σ2A / σ2P) (Baihaki 2000).
Umumnya heritabilitas dalam arti sempit banyak mendapatkan perhatian
karena pengaruh aditif dari tiap alelnya diwariskan dari tetua kepada
keturunannya. Kontribusi penampilan tidak tergantung pada adanya interaksi
antar alel. Dalam pemuliaan tanaman, seleksi sifat-sifat yang dikendalikan oleh
gen aditif diharapkan mendapatkan kemajuan seleksi yang besar dan cepat
(Baihaki 2000).
Pada tanaman, ada banyak metode untuk menduga nilai hiritabilitas dan
komponen ragam. Heritabilitas dapat diduga dengan cara tidak langsung dari
pendugaan komponen ragam, diantaranya adalah perhitungan ragam turunan dan
perhitungan komponen ragam dari analisis ragam; atau dengan cara langsung dari
pendugaan koefisien regresi (b) dan korelasi antar klas (t). Metode yang
digunakan untuk menduga nilai tersebut tergantung dari populasi yang dimiliki
oleh pemulia dan tujuan yang ingin dicapai (Baihaki 2000). Salah satu cara
pendugaan nilai heritabilitas arti sempit adalah dengan pendugaan nilai ragam
lingkungan yang mengikutsertakan satu set tanaman induk kedua tetua (P1 dan
P2), F1 (P1 x P2), silang balik BCP1 (F1 x P1), silang balik BCP2 (F1 x P2) dan F2 (F1 x
F1) (Warner 1952).
Pada analisis genetik biometrik penelusuran dan pelacakan sifat, perilaku,
struktur dan kuantitas gen pengendali karakter kuantitatif dilakukan melalui
pendugaan sumbangan masing-masing komponen sumber ragam mewaris. Akan
tetapi analisis tersebut hanya akan memberikan hasil yang baik bila tidak ada
interaksi antara gen bukan sealel dan interaksi antara genotipe dan lingkungan
(Jinks 1979).
Dua macam pengujian yang dapat digunakan untuk mengetahui apakah
kedua sumber ragam dari interaksi tersebut ada atau tidak adalah dengan : (a) uji
keskalaan (scaling test) individu (A, B, C) menurut cara Mather dan Jinks (1977)
21
keskalaan gabungan (joint scaling test). Bila salah satu dari kedua pengujian
tersebut dan atau keduanya menunjukkan adanya simpangan nyata dari 0, maka
hal tersebut memberi petunjuk adanya efek epistasis atau interaksi genotipe x
lingkungan.
Laporan tentang kendali genetik ketahanan cabai terhadap penyakit
antraknosa masih bervariasi. Cheema et al. (1984) menyatakan bahwa ketahanan
terhadap antraknosa adalah bersifat aditif dan resesif. Amilin et al. (1995)
menyatakan bahwa sifat ketahanan terhadap penyakit antraknosa yang disebabkan
oleh C. gloesporioides pada persilangan interspesifik antara C. annuum dengan
C. frustescens adalah dikendalikan oleh satu gen dengan aksi gen resesif. Hal
yang sama dilaporkan oleh Pakdeevaraporn et al. (2005), bahwa persilangan
interspesifik antara C. annuum dengan C. chinense (PBC 932) mengindikasikan
ketahanan terhadap antraknosa dikendalikan oleh satu gen resesif. Sementara
menurut Park et al. (1990) gen ketahanan terhadap antraknosa bersifat dominan
parsial dan poligenik; Sanjaya, Herison dan Suryotomo (2001) menyatakan bahwa
pewarisan ketahanan terhadap antraknosa (C. gloesporioides) pada persilangan C.
annuum dan C. chinense bersifat aditif dan poligenik dengan tujuh gen yang
terlibat dalam pengendalian karakter ketahanan tersebut; Wusani (2004),
ketahanan terhadap antraknosa dikendalikan oleh gen dominan.
Analisis Silang Dialel
Analisis persilangan dialel merupakan salah satu rancangan persilangan
yang banyak sekali dipakai dalam pemuliaan tanaman. Terutama dalam hal
pendugaan daya gabung umum dan daya gabung khusus dari suatu program
persilangan. Persilangan dialel adalah seluruh kombinasi persilangan yang
mungkin diantara sekelompok genotipe atau tetua, termasuk tetua itu sendiri
lengkap dengan F1 turunannya. Tujuan dari persilangan dialel adalah untuk
mengevaluasi dan menyeleksi tetua yang menghasilkan turunan terbaik.
Genotipe-genotipe tersebut bisa berupa individu, klon atau galur homozigot. Untuk jumlah
genotipe yang besar (populasi dasar dari banyak tetua) maka jumlah persilangan
tenaga yang lebih besar. Untuk itu maka persilangan tersebut dapat
disederhanakan, dengan maksud meniru populasi kawin acak (Griffing 1956).
Rancangan persilangan dialel meliputi semua atau sebagian persilangan
single cross yang mungkin, termasuk resiprok dan selfingnya. Ada empat
kemungkinan silang dialel berdasarkan pendekatan Griffing, yaitu 1) single cross
dengan resiprokal dan selfing (Metode I); 2) single cross dengan selfing tanpa
resiprokal (Metode II); 3) single cross dengan resiprokal (Metode III); 4) single
cross tanpa resiprokal dan tanpa selfing (Metode IV). Tetua single cross
merupakan individu yang diambil secara acak dari suatu populasi. Ragam yang
ada diantara persilangan tersebut adalah ragam half sib dan ragam full sib (Grifing
1956).
Penampilan famili half sib ditentukan oleh nilai tengah semua penampilan
persilangan dari seluruh persilangan dengan tetua yang sama. Ragam diantara
famili-famili half sib merupakan penduga GCA (general combining ability atau
kemampuan daya gabung umum). Famili full sib adalah persilangan dua tetua,
karenanya jumlah full sib dalam dialel sama dengan jumlah single cross yang
dievaluasi. Penampilan famili full sib adalah pendugaan SCA (specific combining
ability atau kemampuan daya gabung khusus) (Baihaki 2000).
Komponen ragam genetik yang menyangkut kovarian half sib (Cov HS)
dan kovarian full sib (Cov FS) tergantung dari nilai inbreeding (F) dan genotipe
tetua yang digunakan dalam dialel. Bila tetuanya adalah tanaman F2 atau tanaman
S0 atau galur yang diturunkan dari populasi tersebut, dimana nilai F = 0, maka komponen ragam genetiknya adalah: Cov HS = 1/4 σ2
A + 1/16 σ2AA + epistasis aditif tingkat tinggi; Cov FS = 1/2 σ2A + 1/4 σ2D + 1/4 σ2AA + aditif dan dominan
epistasis. Bila diasumsikan tidak ada epistasis, maka dapat diduga nilai ragam
aditif sebagai berikut: σ2A = 4 Cov HS dan dominan: σ2D = 4 (Cov FS-2Cov HS)
(Baihaki 2000).
Bila tetuanya merupakan galur murni dari suatu populasi, dengan nilai F =
1, maka: Cov HS = 1/2 σ2A + 1/4 σ2AA + epistasis aditif tingkat tinggi; Cov FS = σ2
A + σ2D + σ2AA + aditif dan dominan epistasis. Bila diasumsikan tidak ada epistasis, maka dapat diduga nilai ragam aditif sebagai berikut: σ2A = 2 Cov HS dan dominan: σ2
23
Penggunaan analisis silang dialel memiliki beberapa keuntungan
dibandingkan dengan metode analisis lainnya. Diantaranya adalah: (1) secara
eksprimental merupakan pendekatan sistematik; (2) secara analitik merupakan
evaluasi genetik menyeluruh yang berguna dalam mengi