REVALIDASI PENGARUH VARIASI KOMPOSISI MEDIUM KULTUR TERHADAP PRODUKSI ENZIM
AMILASE DARI Bacillus sp. STRAIN LTE-6 (Skripsi)
Oleh:
Okta Riyani
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
MENYETUJUI,
1. Komisi Pembimbing
Mulyono, Ph.D
NIP.197406112000031002
Dian Septiani Pratama, M.Si NIP.198009082009122003
2. Ketua Jurusan Kimia
Andi Setiawan, Ph.D NIP.195809221988111001
Judul Skripsi : REVALIDASI PENGARUH VARIASI
KOMPOSISI MEDIUM KULTUR TERHADAP PRODUKSI ENZIM AMILASE DARI Bacillus sp STRAIN LTE-6
Nama Mahasiswa : Okta Riyani
No. Pokok Mahasiswa : 0517011047
Jurusan : Kimia
ABSTRAK
REVALIDASI EFFECT OF MEDIUM COMPOSITION
VARIATIONS OF CULTURE OF PRODUCTION enzyme
amylase Bacillus sp. STRAIN LTE-6
Oleh
Okta Riyani
ABSTRAK
REVALIDASI PENGARUH VARIASI KOMPOSISI
MEDIUM KULTUR TERHADAP PRODUKSI ENZIM
AMILASE DARI
Bacillus
sp.
STRAIN
LTE-6
Oleh
Okta Riyani
REVALIDASI PENGARUH VARIASI KOMPOSISI MEDIUM KULTUR TERHADAP PRODUKSI ENZIM
AMILASE DARI Bacillus sp. STRAIN LTE-6
Oleh
Okta Riyani
Skripsi
Sebagai Salah Satu Syarat Untuk Mencapai Gelar SARJANA SAINS
Pada
Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
MENGESAHKAN
1. Tim Penguji
Ketua : Mulyono, Ph.D. …………....
Sekretaris : Dian Septiani Pratama, M.Si …………....
Penguji
Bukan Pembimbing : Andi Setiawan, Ph.D. …………....
2. Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Prof. Suharso, Ph.D. NIP 196905301995121001
RIWAYAT HIDUP
Penulis dilahirkan di Teluk Betung, Bandar Lampung pada tanggal 30 Oktober
1987, sebagai anak bungsu dari lima bersaudara, putri dari Azhar Dairi dan
Samiyati.
Jenjang pendidikan diawali dari Sekolah Dasar (SD) di SD Negeri 2 Teluk Betung
diselesaikan pada tahun 1999. Sekolah Menengah Pertama (SMP) di SMP Negeri
3 Bandar Lampung diselesaikan pada tahun 2002, dan Sekolah Menengah Atas
(SMA) di SMA Negeri 8 Bandar Lampung diselesaikan pada tahun 2005. Tahun
2005, penulis terdaftar sebagai Mahasiswa Jurusan Kimia FMIPA Unila melalui
jalur SPMB ( Seleksi Penerimaan Mahasiswa Baru)
Pada tahun 2011 Penulis melakukan Praktek Kerja Lapangan di Laboratorium
Analitik Jurusan Kimia FMIPA Univers Lampung di Bandar Lampung. Selama
menjadi mahasiswa penulis pernah menjadi asisten praktikum Kimia Dasar I dan
Biokimia I
Penulis mulai aktif mengikuti organisasi sejak SMA yaitu pada organisasi Rohis
(Rohani Islam) sebagai Wakil Ketua Umum kepengurusan 2003/2004. Penulis
juga aktif di Rois serta Himpunan Mahasiswa Kimia (HIMAKI) FMIPA Unila
sebagai anggota Kader Muda kepengurusan 2005/2006, selain itu penulis aktif dan
menjadi sekretaris Umum Tim Kerja Dakwah Sekolah (TKS) kepengurusan
2008-2010 serta Bendahara umum Tim Kerja Dakwah Sekolah pada periode 2008-
اًرسي رسعلا عم نإف
“Karena sesungguhnya sesudah kesulitan itu ada kemudahan.” (QS. Alam Nasyroh: 5)
Jangan pernah lari dari masalah, mereka akan selalu mengikuti kita. Hadapilah itu karena
masalah akan membuat kita menjadi pribadi yang lebih kuat.
Jangan pernah menyerah atas impianmu. Rintangan memang kadang menjatuhkan, namun
anda harus bangkit dan terus melangkah.
Berlarilah mengejar impian dan cita-cita tanpa kenal lelah hingga lelah itu berhenti
mengikutimu
Kesuksesan bermula pada saat kita menjaga pikiran agar tetap FOKUS pada hasil yang kita
inginkan, bukan pada keterbatasan-keterbatasan kita.
Seberapapun kecilnya nilai kesuksesan tersebut, kalau kita menikmati dan merasakannya,
tentu akan membuahkan kebahagiaan dan kepuasan, itulah inti sebenarnya dari
Dengan segala kerendahan hati serta rasa syukurku kepada Allah SWT pemilik
jiwaku, dan Muhammad SAW sebagai suri teladanku
Kupersembahkan karya kecilku ini untuk orang-orang yang kucintai dan
kusayangi.
Ayahku tercinta A. Dairi dan ibuku tercinta Samiyati yang tak henti-hentinya
selalu memberikan kasih sayang,serta doa dalam perjalanan hidupku
Ayuk mila, Ayuk Fitri, Kak Fredi, dan mbak desti serta seluruh keluarga besarku
tersayang yang selalu menemaniku serta mendoakan keberhasilan untukku
Seseorang yang kelak mendampingi hidupku
SANWACANA
Assalamu’alaykum Wr. Wb.
Alhamdulilah Puji dan syukur Penulis ucapkan atas kehadirat Allah SWT, karena atas segala
rahmat dan hidayah-Nya skripsi ini dapat diselesaikan.
Skripsi dengan judul “ Revalidasi Pengaruh Variasi Komposisi Medium Kultur Terhadap Produksi Enzim Amilase dari Bacillus sp. Strain LTE-6” adalah salah satu syarat untuk memperoleh gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam, Universitas Lampung.
Dalam pelaksanaan dan penulisan skripsi ini tidak lepas dari kesulitan dan rintangan, namun itu
semua dapat penulis lalui berkat rahmat dan ridha Allah SWT serta bantuan dan dorongan
semangat dari orang-orang di sekitar penulis. Dalam kesempatan ini, penulis menyampaikan
terima kasih setulus-tulusnya kepada:
1. Bapak Mulyono, Ph.D., selaku pembimbing utama yang telah banyak memberikan ilmu
pengetahuan, gagasan, bimbingan, bantuan, dukungan, saran dan kritik kepada penulis
dalam proses perencanaan dan pelaksanaan penelitian, serta dalam penulisan skripsi ini.
2. Ibu Dian Septiani Pratama, M.Si., selaku pembimbing kedua atas kesediaan memberikan
3. Bapak Andi Setiawan, Ph.D., selaku pembahas dan Ketua Jurusan yang telah meluangkan
waktu, memberikan kritik, saran, dan arahan yang diberikan kepada penulis sehingga
skripsi ini terselesaikan dengan baik.
4. Ibu Dra Aspita Laila, M.S., selaku Pembimbing Akademik atas kesediaannya untuk
memberikan bimbingan, bantuan, nasehat, dan informasi yang bermanfaat kepada
penulis.
5. Segenap dosen yang telah mendidik dan memberikan ilmu pengetahuan kepada penulis
selama kuliah.
6. Bapak Suharso, Ph.D., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Lampung.
7. Kedua orang tuaku yang teramat aku cintai. Ibunda Samiyati dan Azhar Dairi yang telah
memberikan kasih sayang dan cintanya untukku, selalu mendoakan demi keberhasilanku,
memberikan perhatian dan tauladan terbaik untukku. Semua jasa yang telah diberikan
kepadaku takkan bisa ku ganti dengan apapun.
8. Saudara-saudara ku tersayang Mila Andriyani (Ayunda), Fitri Astuti (Ayunda) Desti
Yanti (Mbak), Fredi Antoni (Kakak). Kalian yang tak henti-hentinya memberikan
motivasi, dukungan dan semangat kepadaku bahwa aku bisa menyelesaikan studi ini.
9. Sahabat-sahabat terbaikku : Riya Adlaila, S.Si., Nelda Susanti S.Pd., Vonny Apriati,S.Si.,
Mira Mustika,S.Si., Hafizah Helma,S.Si., Nuraida terimakasih atas segala dukungan,
kasih sayang, rasa kebersamaan, dan keceriaan yang selalu kalian hadirkan disetiap
hari-hariku, aku bangga mengenal kalian.
11. Teman- teman Biochemistry. Adek Purnawati S.Si, M Ramdhan S.Si.,Tyas R., Miftah,
Fatma, Fitri, Vivi, M Amin,
12. Tutik, S.Si., Nurjannah Harun, Mustika, S.Si., Reni Astari,S.Pd., yang bersedia
menemani ataupun menjemputku di Laboratorium Biokimia tanpa mengenal
waktu.Terima Kasih
13. Teman-teman Kimia’04,’05’06,’07, ’08, ’09, ’10,11 FMIPA UNILA terimakasih atas
segala dukungannya.
14. terimakasih atas segala semangat, motivasi, perhatian, keceriaan, kesabaran dan cinta
kasih yang telah diberikan selama ini.
15. Semua pihak yang telah membantu dan mendukung penulis dalam penyusunan skripsi
ini.
Akhir kata, Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan. Akan tetapi
dengan segala kerendahan dan keikhlasan yang ada dalam hati, penulis berharap semoga skripsi
yang sederhana ini dapat berguna dan bermanfaat bagi kita semua. Amin.
Bandar Lampung, 28 Desember 2012
Penulis
DAFTAR ISI
Mekanisme Kerja Enzim……… 6
Faktor-Faktor Yang Mempengaruhi Reaksi Enzim... ... 8
Kinetika Reaksi Enzim……….. 9
Enzim Amilase………. .. 10
Amilum………. 13
Nutrien Mikroba ... 14
Fase Pertumbuhan Bakteri ... 15
Karakterisasi bakteri isolat LTE-6 ... 17
Spektrofotometer ... 18
ii
Penentuan Kadar Protein Metode Lowry ... 26
Penentuan Aktivitas Enzim Metode Fuwa ... 26
Variasi Komposisi Produksi Enzim Amilase ... 27
Variasi Komposisi Sumber C ... 27
Variasi Komposisi Sumber N ... 27
Variasi Komposisi Ion Logam ... 27
Variasi pH terhadap Pertumbuhan dan Produksi Enzim ... 28
IV. HASIL DAN PEMBAHASAN Peremajaan Isolat LTE-6………. 29
Monitoring Pertumbuhan dan Produksi Enzim Amilase……….. 29
Pengaruh Variasi komposisi Medium Kultur……... 31
SIMPULAN DAN SARAN………. .. 43
Simpulan………... 44
Saran……… . 45
DAFTAR PUSTAKA……….. 46
iii
DAFTAR GAMBAR
Gambar Halaman
1 Model kunci dan anak kunci ... 6
2 Model induced fit ... 8
Kurva Lineweaver-Burk ... 10
4 Struktur Kimia dari Amilosa dan Amilopektin ... 14
5. Bakteri Isolat LTE-6……… 16
6. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber karbon glukosa……….. 28
7. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber karbon fruktosa……… 28
8. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber karbon Arabinosa………. 28
9. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber karbon gula………... 28
10 Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber nitrogen pepton………. 30
11. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber nitrogen NaNO3……… 30
12. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber nitrogen NH4Cl………. 30
13. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber nitrogen Ekstrak Ragi……… 30
iv
15. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber ion logam MgSO4……… 33
16. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber ion logam MnSO4……….. 34
17. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan sumber ion logam ZnSO4………. 34
18. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan pH 5……… 34
19. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan pH 6……… 36
20. Profil pertumbuhan sel dan Aktivitas Unit pada medium pati singkong dengan pH 7………. 36
v
DAFTAR TABEL
Tabel Halaman
1 Pertumbuhan sel dan produksi enzim isolat LTE-6 pada berbagai medium dengan variasi sumber Karbon ……… 33
2. Pertumbuhan sel dan produksi enzim isolat LTE-6 pada berbagai medium dengan variasi sumber Nitrogen………... 33
3. Pertumbuhan sel dan produksi enzim isolat LTE-6 pada berbagai medium dengan variasi sumber Ion Logam ……….. 36
4. Pertumbuhan sel dan produksi enzim isolat LTE-6 pada berbagai medium dengan variasi sumber pH ………... 36
5. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat LTE-6 pada variasi
komposisi sumber karbon………. . 41
6. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat CP-2 pada variasi
komposisi sumber karbon……… .. 42
7. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat LTE-6 ada variasi
komposisi sumber Nitrogen ………. . 43
8. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat CP-2 pada variasi
komposisi sumber Nitrogen……… ... 44
9. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat LTE-6 pada variasi
komposisi sumber Ion Logam……… 45
10. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat CP-2 pada variasi
vi
11. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat LTE-6 pada variasi
komposisi sumber pH……….. .. 47
12. Absorbansi Sel (OD600), Aktivitas Unit, Kadar Protein dan Aktivitas Spesifik enzim amilase dari isolat LTE-6 pada variasi
komposisi sumber pH……… 48
I. PENDAHULUAN
I.1 Latar Belakang
Enzim adalah katalis yang memiliki keunggulan sifat dapat membantu
proses-proses kimia kompleks pada kondisi percobaan yang lunak dan lebih ramah
lingkungan (Mateo et al., 2007).
Kelebihan enzim sebagai katalisator antara lain enzim memiliki spesifitas tinggi,
mempercepat reaksi kimiawi spesifik tanpa pembentukan senyawa samping,
produktivitas tinggi, dan umumnya produk akhir yang terbentuk tidak
terkontaminasi sehingga mengurangi biaya purifikasi (Chaplin dan Bucke, 1990).
Produksi dan perdagangan enzim didominasi oleh kelompok enzim hidrolitik
seperti amilase, protease, katalase dan lipase. Kebutuhan amilase di dunia sangat
tinggi yaitu mencapai 300 ton enzim murni pertahun yang diproduksi oleh
Bacillus lichineformis dan Aspergillus sp (Sivaramkrisnan et al., 2006).
Amilase merupakan enzim yang bekerja menghidrolisis pati yang dapat
dihasilkan oleh bakteri, fungi, tumbuhan dan hewan. Amilase yang
dihasilkan oleh bakteri banyak dimanfaatkan dalam industri, terutama industri
makanan, minuman, tekstil, farmasi, dan detergen. Hal ini karena umumnya
2
dibandingkan yang berasal dari tumbuhan dan hewan. Sebagian besar industri,
seperti industri makanan dan minuman menggunakan amilase tahan asam
(Whittaker, 1994).
Pada penelitian sebelumnya (Mulatasih, 2010) diperoleh kondisi optimum pada
isolat LTE-6 dengan nilai aktivitas unit 5,47 U/mL dan aktivitas spesifik 349,29
U/mg. Kemudian dilakukan variasi komposisi medium kultur terhadap produksi
enzim amilase dari isolat LTE-6 (Fandika, 2011) dengan variasi komposisi berupa
variasi sumber N, variasi sumber C, variasi Ion Logam, serta variasi pH sehingga
diperoleh hasil dengan nilai aktivitas unit berturut-turut 9,8 U/mL; 10,83 U/mL;
9,5 U/mL; 8,7 U/mL serta dengan aktifitas spesifik berturut-turut 130,70 U/mg;
55,00 U/mg; 15,04 U/mg; 20,90 U/mg. Setelah dilakukan variasi komposisi
tersebut, pada ion logam dan pH 6 terjadi penurunan nilai aktivitas unit
berturut-turut menjadi 9,5 U/mL; 8,7 U/mL. Hal itu dapat terlihat bahwa terjadinya
penurunan produksi enzim amilase dari bacillus sp strain LTE-6. Untuk
meyakinkan data hasil penelitian tersebut maka perlu dilakukan penelitian
kembali.
Pada penelitian ini telah dilakukan variasi komposisi pada medium kultur
menggunakan bakteri isolat LTE-6. Sumber karbon yang digunakan adalah pati
singkong kering 1% (w/v). Pengukuran dilakukan dengan spektrofotometer untuk
mengetahui pertumbuhan sel dan uji aktivitas enzim menggunakan metode fuwa
3
I.2 Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah untuk uji ulang data hasil penelitian
sebelumnya (Fandika, 2012) tentang bagaimana pengaruh variasi komposisi
medium kultur terhadap produksi enzim amilase dari Bacillus sp strain LTE-6.
I.3 Manfaat penelitian
Manfaat dari penelitian ini adalah untuk mendapatkan kondisi optimum medium
kultur terhadap produksi enzim amilase Bacillus sp strain LTE-6 sehingga dapat
II. TINJAUAN PUSTAKA
A. Enzim
Enzim merupakan biokatalisator yang diproduksi oleh jaringan makhluk hidup
digunakan untuk mengkatalisis reaksi yang terdapat pada makhluk hidup dan
dapat meningkatkan laju reaksi yang terdapat pada jaringan. Enzim juga dapat
dikaitkan sebagai unit fungsional dari metabolisme sel, bekerja dengan urutan
tertentu, mengkatalisis reaksi bertahap yang berjumlah hingga ratusan yang
menyimpan dan mentransformasikan energi kimiawi dan membuat makromolekul
dari prekursor yang sederhana (Lehninger, 1990).
1. Klasifikasi Enzim
Enzim digolongkan menurut reaksi yang diikutinya, sedangkan masing-masing
enzim diberi nama menurut nama substratnya, misalnya urease, arginase dan
lain-lain. Di samping itu ada pula beberapa enzim yang dikenal dengan nama lama
misalnya pepsin, tripsin dan lain-lain.
International Union of Biochemistry and Molecular Biology (IUBMB)
mengklasifikasi enzim berdasarkan tipe reaksi yang dikatalisisnya. Berdasarkan
tipe reaksi yang dikatalisis itu, enzim dibagi menjadi 6 kelas dan masing-masing
kelas terbagi lagi menjadi subkelas (4-13 subkelas) dan dari subkelas dibagi lagi
5
1. Oksidoreduktase, mengkatalisis oksidasi dan reduksi. Contoh : alkohol
dehidrogenase (EC1.1.1.1)
2. Transferase, mengkatalisis pemindahan gugus seperti : Glikosil, Metil,
fosforil, aldehid dan keton. Contoh: ATP
(D-heksosa-6-fosfotransferase/heksokinase) (EC2.7.1.1)
3. Hidrolase, mengkatalisis pemutusan hidrolitik dalam ikatan C-C, C-O, C-N
dan ikatan lain. Contoh: Beta-Galaktosidase (EC3.2.1.23).
4. Liase, mengkatalisis pemutusan ikatan C-C, C-O, C-N, dan ikatan lain
dengan eliminasi atom yang menghasilkan ikatan rangkap. Contoh : Fumarat
hidratase (Fumarase) (EC4.2.1.2).
5. Isomerase, mengkatalisis perubahan geometrik atau struktural di dalam satu
molekul. Contoh: triosafosfat isomerase (EC5.3.1.1).
6. Ligase, mengkatalisis penyatuan dua molekul yang dikaitkan dengan
hidrolisis ATP.Contoh: Asetil-KoA-karboksilase (EC6.4.1.2).
Dalam mempelajari mengenai enzim, dikenal beberapa istilah diantaranya
holoenzim, apoenzim, kofaktor, gugus prostetik, koenzim, dan substrat. Apoenzim
adalah suatu enzim yang seluruhnya terdiri dari protein, sedangkan holoenzim
adalah enzim yang mengandung gugus protein dan gugus non protein. Gugus
yang bukan protein tadi dikenal dengan istilah kofaktor. Pada kofaktor ada yang
terikat kuat pada protein dan sukar terurai dalam larutan yang disebut gugus
prostetik dan adapula yang tidak terikat kuat pada protein sehingga mudah terurai
yang disebut koenzim. Baik gugus prostetik maupun koenzim, keduanya
merupakan bagian yang memungkinkan enzim bekerja pada substrat. Substrat
6
Secara disingkat, sifat-sifat enzim tersebut antara lain (Dwidjoseputro, 1992)
berfungsi sebagi biokatalisator, merupakan suatu protein, bersifat khusus atau
spesifik, merupakan suatu koloid, jumlah yang dibutuhkan tidak terlalu banyak,
serta tidak tahan panas.
Fungsi enzim sebagai katalis untuk reaksi kimia dapat terjadi baik didalam
maupun di luar sel. Suatu enzim bekerja secara khas terhadap suatu substrat
tertentu. Suatu enzim dapat bekerja 108 sampai 1011 kali lebih cepat
dibandingkan laju reaksi tanpa katalis. Enzim bekerja sebagai katalis dengan cara
menurunkan energi aktivasi, sehingga laju reaksi meningkat (Poedjadi, 2006).
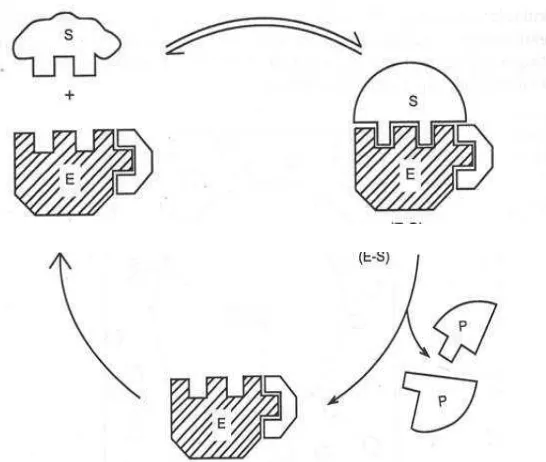
2. Mekanisme Kerja Enzim
Prinsip kerja enzim berlangsung dalam dua tahap. Pada tahap pertama, enzim (E)
bergabung dengan substrat (S) membentuk kompleks enzim substrat (E-S). Tahap
kedua, kompleks enzim-substrat terurai menjadi produk dan enzim bebas.
Terdapat dua model yang diusulkan pada kegiatan enzim dalam mempengaruhi
substrat sehingga diperoleh zat hasil, yaitu model kunci dan anak kunci, dan
7
Gambar 1. Model Kunci dan Anak Kunci (Santoso, 2010)
Pada model kunci dan anak kunci (Gambar 1), substrat atau bagian substrat harus
mempunyai bentuk yang sangat tepat dengan sisi katalitik enzim. Substrat ditarik
oleh sisi katalitik enzim yang cocok untuk substrat tersebut sehingga terbentuk
kompleks enzim substrat.
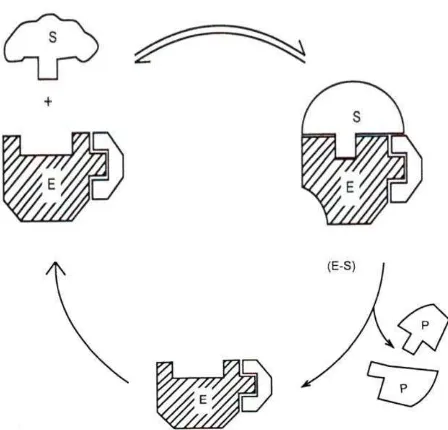
Pada model induced fit (Gambar 2), lokasi aktif beberapa enzim mempunyai
konfigurasi yang tidak kaku. Enzim berubah bentuk menyesuaikan diri dengan
bentuk substrat setelah terjadi pengikatan. Jadi, tautan yang cocok pada keduanya
8
Gambar 2. Model Induced Fit (Santoso, 2010).
3. Faktor faktor yang dapat mempengaruhi enzim
Faktor-faktor yang dapat mempengaruhi fungsi enzim diantaranya adalah
(Dwidjoseputro, 1992) :
a. Suhu
Oleh karena reaksi kimia itu dapat dipengaruhi suhu maka reaksi menggunakan
katalis enzim dapat dipengaruhi oleh suhu. Di samping itu, karena enzim adalah
suatu protein maka kenaikan suhu dapat menyebabkan denaturasi dan bagian aktif
enzim akan terganggu sehingga konsentrasi dan kecepatan enzim berkurang.
b. pH
Umumnya enzim efektifitas maksimum pada pH optimum, yang lazimnya
berkisar antara pH 4,5-8,0. Pada pH yang terlalu tinggi atau terlalu rendah
umumnya enzim menjadi non aktif secara irreversibel karena menjadi denaturasi
9
c. Konsentrasi enzim
Seperti pada katalis lain, kecepatan suatu reaksi yang menggunakan enzim
tergantung pada konsentrasi enzim tersebut. Pada suatu konsentrasi substrat
tertentu, kecepatan reaksi bertambah dengan bertambahnya konsentrasi enzim.
d. Konsentrasi substrat
Hasil eksperimen menunjukkan bahwa dengan konsentrasi substrat akan
menaikkan kecepat reaksi. Akan tetapi, pada batas tertentu tidak terjadi kecepatan
reaksi, walaupn konsenrasi substrat diperbesar.
e. Zat-zat penghambat
Hambatan atau inhibisi suatu reaksi akan berpengaruh terhadap penggabungan
substrat pada bagian aktif yang mengalami hambatan.
4. Kinetika Reaksi Enzim
Kinetika enzim adalah salah satu cabang enzimologi yang membahas faktor-faktor
yang mempengaruhi kecepatan reaksi enzimatis. Salah satu faktor yang
mempengaruhi aktivitas enzim adalah konsentrasi substrat. Konsentrasi substrat
dapat divariasikan untuk mempelajari mekanisme suatu reaksi enzim, yakni
bagaimana tahap-tahap terjadinya pengikatan substrat oleh enzim maupun
pelepasan produknya (Suhartono, 1989).
Untuk mempermudah menghitung konsentrasi substrat yang diperlukan dalam
mencapai kecepatan maksimum, digunakan tetapan Michaelis-Menten (KM).
Berdasarkan pada grafik laju reaksi-konsentrasi substrat diperoleh suatu
10
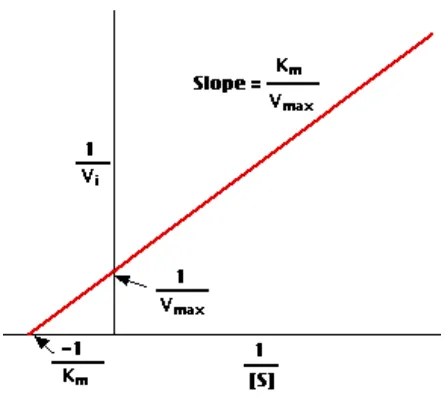
Cara lain untuk menentukan harga Vmaks dan KM adalah membuat grafik antara
1/V dengan 1/S. Persamaan Michaelis-Menten menjadi:
Persamaan tersebut dikenal dengan Lineweaver-Burk yang yang digunakan untuk
menentukan Vmaks dan KM (Poedjadi, 1994). Grafik persamaan Lineweaver-Burk
dapat dilihat pada gambar berikut (Gambar 3).
Gambar 3. Lineweaver-Burk
B. Amilase
Amilase merupakan enzim pemecah pati, glikogen dan polisakarida lain dengan
cara menghidrolisis ikatan glikosidik α-1,4 atau ikatan glikosidik α-1,6. Amilase
dibagi menjadi empat golongan, yaitu: α-amilase, -amilase, glukoamilase dan
enzim pemutus cabang. Berdasarkan produk akhir hidrolisisnya, enzim amilase
11
memberikan produk akhir gula bebas sedangkan golongan kedua adalah enzim
yang memecah pati tetapi tidak menghasilkan gula bebas, kedua golongan amilase
ini dibedakan secara eksperimen (Crueger, 1984).
Enzim α-amilase (α-1,4 glukan-glukanhidrolase), termasuk enzim pemecah dari
dalam molekul, bekerja menghidrolisis dengan cepat ikatan α-1,4 glukosida pada
pati. Berat molekul α-amilase ± 50 kDa (Suhartono, 1989). Enzim ini banyak
digunakan pada industri sirup, sari buah, dan selai. Enzim α-amilase mengandung
paling sedikit 1 atom kalsium permolekul dan melekat dengan erat pada molekul
enzim. Adanya kalsium tersebut menyebabkan enzim ini disebut “calcim metal
coenzyme” (Judoamidjojo dkk., 1989). Ion kalsium ini penting untuk stabilitas
dan aktivitas enzim. Afinitas ion kalsium pada α-amilase lebih kuat dari
kation lain. Masih belum jelas apakah ion kalsium dapat diganti oleh
kation-kation lain (Vihinen and Mantsala, 1989).
Mekanisme kerja enzim α-amilase pada amilosa dibagi dalam dua tahap, pertama
degradasi secara cepat molekul amilosa menjadi maltosa dan maltotriosa yang
terjadi secara acak. Pada tahap ini terjadi penurunan kekentalan dengan cepat.
Tahap kedua, degradasi α-amilase pada amilosa menghasilkan glukosa dan
maltosa dengan laju lebih lambat dan tidak secara acak (Winarno, 1995).
Aktivitas α-amilase dapat diukur berdasarkan penurunan kadar pati yang larut,
kadar dekstrin yang terbentuk, dan pengukuran viskositas atau jumlah gula
pereduksi yang terbentuk (Judoamidjojo dkk., 1989).
-amilase ( -1,4 glukan maltohidrolase), memutus dari luar molekul dan
12
Bila tiba pada ikatan α-1,6 glikosida seperti yang dijumpai pada amilopektin atau
glikogen, aktivitas enzim ini akan terhenti. Enzim ini bekerja pada ikatan α-1,4
dengan menginversi konfigurasi posisi atom C (1) atau atom C nomor 1 molekul
glukosa dari α menjadi . Enzim -amilase memiliki pH optimum antara 5-6
(Judoamidjojo dkk., 1989).
Gamma amilase ( –amilase), EC.3.2.1.3. disebut juga glukan 1,4-α–glukosidase,
amiloglukosidase, ekso-1,4-α–glukosidase, lisosomal α-glukosidase,
glukoamilase, 1,4-α-D-glukan glukohidrolase. Merupakan pemutus terakhir
ikatan glikosida pada bagi ujung nonreduksi dari amilosa dan amilopektin untuk
menghasilkan unit glukosa.
Pullulanase, EC.3.2.1.41. merupakan enzim pemutus cabang, menghidrolisis
hanya pada ikatan α-1,6 glikosida, seperti pullulan 6-glukanohydrolase. α
-Glukosidase, EC.γ.β.1.β0. Memutus ikatan α-1,4 glikosida dari molekul amilosa
ataupun amilopektin menjadi rantai-rantai pendek oligosakarida (Hagihara et al.,
2001).
Berdasarkan arah memutusnya ikatan glikosida dari amilum, maka enzim amilase
dapat dikategorikan menjadi 2 kelompok (Reddy et al., 2003) yaitu endoamilase
dan ektoamilase. Endoamilase melakukan hidrolisis secara acak dari bagian
depan molekul amilum sehingga menghasilkan molekul oligosakarida dalam
bentuk rantai lurus maupun bercabang dengan panjang rantai yang bervariasi
sedangkan ektoamilase melakukan hidrolisis dari ujung nonreduksi dan dengan
13
Komposisi dan konsentrasi media sangat mempengaruhi produksi dari enzim
amilase ekstraseluler pada bakteri, yeast, dan Aspergillus sp. Shinke dalam
Srivastava (2008) menyatakan bahwa komposisi medium sangat mempengaruhi
produksi amilase, seperti halnya sporulasi pada Bacillus cereus. Keberadaan pati
akan menginduksi produksi amilase. Keadaan lingkungan dan sumber nitrogen
pada media kultur juga akan mempengaruhi pertumbuhan produksi amilase.
Disamping karbon dan nitrogen, sodium dan garam potassium, ion metal, dan
detergen juga akan mempengaruhi produksi amilase dan pertumbuhan
mikroorganisme (Srivastava, 2008).
Aktivitas enzim α-amilase ditentukan dengan mengukur penurunan kadar pati
yang larut dengan menggunakan substrat jenuh. Kejenuhan pati berpengaruh
terhadap laju reaksi enzimatis. Apabila larutan pati terlalu jenuh maka enzim sulit
terdifusi ke dalam larutan sehingga kerja enzim akan terhambat (Winarno, 1995).
C. Pati atau Amilum
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Pati terdiri dari
dua fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa
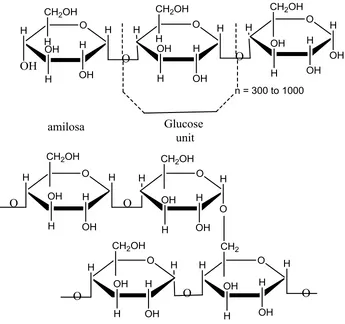
dan fraksi tidak larut disebut amilopektin (Winarno, 1984). Struktur amilosa
merupakan struktur lurus dengan ikatan α-(1,4)-D-glukosa. Amilopektin terdiri
dari struktur bercabang dengan ikatan α-(1,4)-D-glukosa dan titik percabangan
amilopektin merupakan ikatan α-(1,6). Berat molekul amilosa dari beberapa ribu
hingga 500.000, begitu pula dengan amilopektin (Lehninger, 1982).
Amilopektin, suatu polisakarida yang jauh lebih besar daripada amilosa,
14
amilosa, rantai utama dari amilopektin mengandung 1,4-α-D-glukosa. Tidak
seperti amilosa, amilopektin bercabang sehingga terdapat satu glukosa ujung
untuk kira-kira tiap 25 satuan glukosa. Ikatan pada titik percabangan adalah
1,6-α-glikosida. Bila amilopektin dihidrolisis lengkap maka akan terbentuk
D-glukosa. Hidrolisis tak lengkap menghasilkan suatu campuran disakarida atau
campuran oligosakarida. Campuran disakarida hasil hidrolisis berupa maltosa dan
isomaltosa sedangkan campuran oligosakarida berupa dekstrin (Fessenden dan
Fessenden, 1982).
Gambar 4. Struktur amilosa dan amilocpektin.
Pati termasuk karbohidrat jenis polisakarida. Polisakarida ini banyak terdapat di
15
tumbuhan, pati merupakan simpanan karbohidrat yang dihasilkan dari proses
fotosintesis. Bagi hewan dan manusia, pati merupakan sumber karbohidrat utama
yang banyak dikonsumsi sebagai sumber energi yang penting.
Pati atau amilum bersifat tidak larut dalam air pada suhu kamar, berwujud bubuk
putih, tidak berasa dan tidak berbau. Di dalam tumbuhan, pati disimpan dalam sel
sebagai granula kecil yang dapat dilihat di bawah mikroskop. Bentuk granula pati
berbeda-beda tergantung dari tumbuhan sumber patinya. Pati singkong memiliki
granula dengan ukuran 5-35 μm dengan rata-rata ukurannya diatas 17 μm
(Samsuri, 2008).
Pati bereaksi dengan iodium membentuk kompleks berwarna biru kehitaman.
Kompleks warna ini terjadi bila molekul iodium masuk ke dalam bagian kosong
pada molekul zat pati (amilosa) yang berbentuk spiral. Proses iodinisasi zat pati
menghasilkan molekul yang mengabsorbsi semua cahaya, kecuali warna biru.
Bila zat pati telah diuraikan menjadi maltose atau glukosa, warna biru tidak terjadi
lagi karena tidak adanya bentuk spiral pati (Lay, 1994)
D. Bakteri
Ada tiga bentuk dasar bakteri, yaitu bentuk bulat atau kokus, bentuk batang
silindris, bentuk lengkung atau vibri. Bentuk bulat atau kokus dapat dibedakan
dalam : mikrokokus, diplokokus, streptokokus, tetrakokus, sarsina dan stafilo
kokus. Bakteri berbentuk batang dapat dibedakan ke dalam bentuk batang
panjang dan batang pendek dengan ujung datar atau lengkung. Bakteri berbentuk
16
dari setengah lingkaran. Bentuk bakteri dipengaruhi oleh umur dan syarat
pertumbuhan tertentu (Hidayat dkk., 2006).
1. Nutrien untuk Pertumbuhan Bakteri
Kebutuhan nutrien harus meliputi unsur makro esensial dan mikro esensial yang
terlibat baik dalam proses metabolisme sel juga untuk mengaktifkan enzim,
mensintesis vitamin dan berperan dalam sporulasi. Nutrien dasar bagi
mikroorganisme harus mengandung sumber energi untuk tumbuh seperti unsur
karbon, nitrogen, dan logam. Nutrien yang tergolong sumber energi adalah
senyawa hasil oksidasi dari lemak, protein, amonium, karbohidrat, dan gula
sederhana. Kebutuhan sumber karbon dapat dipenuhi dengan adanya CO2 atau
senyawa seperti gula, pati, dan karbohidrat lain. Kebutuhan akan nitrogen dapat
dipenuhi oleh NH4+ atau senyawa nitrat organik/anorganik. Untuk pertumbuhan
normal mikroorganisme membutuhkan ion logam yang berfungsi sebagai kofaktor
(Suhartono, 1989).
Histidin, ditiotreitol dan merkaptoetanol merupakan senyawa yang berperan
sebagai kofaktor enzim ini. Selain itu beberapa logam juga dapat berperan
sebagai kofaktor antara lain Ca2+, Ba2+, Mn2+, Ag+, dan Fe2+. Sedangkan Hg2+,
Cu2+, Mg2+, Rb2+, Fe3+, Al3+, Cd2+ dan Ni2+merupakan inhibitor enzim α-amilase
(Schomburg and Salzmann, 1991).
2. Fase Pertumbuhan Bakteri
Suatu mikroorganisme mempunyai siklus pertumbuhan tertentu tergantung
produk yang akan dihasilkan. Pertumbuhan mikroorganisme dibagi dalam
17
dan fase kematian. Fase adaptasi, sel-sel bakteri mulai membesar namun belum
mengadakan pembiakan. Pada fase ini bakteri baru menyesuaikan diri dengan
lingkungan baru. Fase lag, bakteri mulai membelah diri, tetapi waktu generasinya
masih panjang. Fase statisioner, jumlah bakteri yang dihasilkan sama dengan
jumlah bakteri yang mati sehingga jumlah sel bakteri yang hidup menjadi konstan.
Fase kematian, jumlah bakteri yang mati makin banyak sedangkan kecepatan
pembelahannya jadi nol (Irianto, 2006).
3. Karakteritik Bakteri Isolat LTE-6
Hasil penelitian yang telah dilakukan (Mulatasih, 2010) pada isolat LTE-6 di
bawah mikroskop, isolat tersebut berbentuk basil dan merupakan bakteri dengan
Gram negatif. Bakteri Gram negatif mampu mengikat cat warna utama dengan
tidak kuat sehingga dapat dilunturkan oleh peluntur cat dan dapat diwarnai oleh
cat lawan. Pada pengamatan mikroskopik sel-sel bakteri ini akan berwarna
merah.
18
Metode yang digunakan Fuwa (1954), Marshall dan Lauda (1975), dan Xiao et al.
(β006) dalam mengukur aktivitas enzim α-amilase adalah dengan mengukur
warna kompleks iodin dengan pati. Semakin besar aktivitas penghambatan
phaseolamin, maka jumlah pati yang terhidrolisis semakin sedikit sehingga
komplek iodin dengan pati yang terbentuk semakin banyak dan menghasilkan
warna biru. Warna kompleks tersebut dapat dikuantifikasi dengan pengukuran
menggunakan spektrofotometer.
f. Spektrofotometer
Spektrofotometri merupakan suatu metode analisis yang didasarkan pada
pengukuran serapan sinar makromatis oleh suatu lajur larutan berwarna pada
panjang gelombang spesifik dengan menggunakan monokromator prisma atau kisi
difraksi dengan fototube atau tabung foton hampa. Alat yang digunakan adalah
spektrofotometer, yaitu suatu alat yang di gunakan untuk menentukan suatu
senyawa baik secara kuantitatif maupun kualitatif dengan mengukur transmitan
atau absorbansi dari suatu cuplikan sebagai fungsi dari konsentrasi. Pada titrasi
spektrofotometri, sinar yang digunakan merupakan satu berkas yang panjangnya
tidak berbeda banyak antara satu dengan yang lainnya, sedangkan dalam
kalorimetri perbedaan panjang gelombang dapat lebih besar. Dalam hubungan ini
dapat disebut juga spektrofotometri adsorbsi atomic (Hardjadi, 1990).
Spektrofotometer menghasilkan sinar dan spectrum dengan panjang gelombang
tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan
19
adalah panjang gelombang dari sinar putih dapat lebih terseleksi dan ini diperoleh
dengan alat pengurai seperti prisma, grating, atau celah optis. Pada fotometer
filter dari berbagai warna yang mempunyai spesifikasi melewatkan trayek panjang
gelombang tertentu. Pada fotometer filter tidak mungkin diperoleh panjang
gelombang 30-40 nm. Sedangkan pada spektrofotometer, panjang gelombang
yang benar-benar terseleksi dapat diperoleh dengan bantuan alat pengurai cahaya
seperti prisma. Suatu spektrofotometer tersusun dari sumber spektrum tampak
yang kontinyu, monokromator, sel pengabsorbsi untuk larutan sampel blanko dan
suatu alat untuk mengukur perbedaan absorbsi antara sampel dan blanko ataupun
pembanding (Khopkar, 2002).
Sinar yang melewati suatu larutan akan terserap oleh senyawa-senyawa dalam
larutan tersebut. Intensitas sinar yang diserap tergantung pada jenis senyawa yang
ada, konsentrasi dan tebal atau panjang larutan tersebut. Makin tinggi konsentrasi
suatu senyawa dalam larutan, makin banyak sinar yang diserap.
Spektrofotometri terdiri dari beberapa jenis berdasar sumber cahaya yang
digunakan. Diantaranya adalah sebagai berikut:
1. Spektrofotometri Visible
Pada spektrofotometri ini yang digunakan sebagai sumber sinar atau energi adalah
cahaya tampak (visible). Cahaya variable termasuk spektrum elektromagnetik
yang dapat ditangkap oleh mata manusia. Panjang gelombang sinar tampak
adalah 380-750 nm. Sehingga semua sinar yang didapat berwarna putih, merah,
biru, hijau, apapun itu, selama ia dapat dilihat oleh mata. Maka sinar tersebut
20
dipakai pada spektro visible adalah lampu Tungsten. Tungsten yang dikenal juga
dengan nama Wolform merupakan unsur kimia dengan simbol W dan nomor atom
74. Tungsten memiliki titik didih yang tinggi (34 22oC) dibanding logam lainnya.
Karena sifat inilah maka ia digunakan sebagai sumber lampu. Sampel yang dapat
dianalisa dengan metode ini hanya sample yang memiliki warna. Hal ini menjadi
kelemahan tersendiri dari metode spektrofotometri visible. Oleh karena itu, untuk
sampel yang tidak memiliki warna harus terlebih dahulu dibuat berwarna dengan
menggunakan reagen spesifik yang akan menghasilkan senyawa berwarna.
Reagen yang digunakan harus benar-benar spesifik hanya bereaksi dengan analat
yang akan dianalisa. Selain itu juga produk senyawa berwarna yang dihasilkan
harus benar-benar stabil.
2. Spektrofotometri UV (Ultraviolet)
Berbeda dengan spektrofotometri visible, pada spektrofotometri UV berdasarkan
interaksi sampel dengan sinar UV. Sinar UV memiliki panjang gelombang
190-380 nm. Sebagai sumber sinar dapat digunakan lampu deuterium. Deuterium
disebut juga heavy hidrogen. Dia merupakan isotop hidrogen yang stabil yang
terdapat berlimpah dilaut dan daratan. Inti atom deuterium mempunyai satu
proton dan satu neutron, sementara hidrogen hanya memiliki satu proton dan tidak
memiliki neutrron. Nama deuterium diambil dari bahasa Yunani, deuteras yang
berarti dua, mengacu pada intinya yang memiliki 2 partikel. Karena sinar UV
tidak dapat dideteksi dengan mata kita maka senyawa yang dapat menyerap sinar
ini terkadang merupakan senyawa yang tidak memiliki warna, bening dan
transparan. Oleh karena itu, sampel tidak berwarna tidak perlu dibuat berwarna
21
meskipun tanpa preparasi. Namun perlu diingat, sampel keruh tetap harus dibuat
jernih dengan filtrasi atau sentifungi. Prinsip dasar pada spektrofotometri adalah
sampel harus jernih dan larut sempurna. Tidak ada partikel koloid/ suspensi.
3. Spektrofotometri UV Vis
Merupakan alat dengan teknik spektrofotometer pada daerah ultra-violet dan sinar
tampak. Alat ini digunakan mengukur serapan sinar ultra violet atau sinar tampak
oleh suatu materi dalam bentuk larutan. Konsentrasi larutan yang dianalisis
sebanding dengan jumlah sinar yang diserap oleh zat yang terdapat dalam larutan
tersebut. Dalam hal ini, hukum Lamber beer dapat menyatakan hubungan antara
serapan cahaya dengan konsentrasi zat dalam larutan. Dibawah ini adalah
persamaan Lamber beer:
A = - log T = ε.b.c
Dimana :
A = Absorbansi
T = Transmitan
ε = absorvitas molar (Lcm-4
. mol-1)
c = panjang sel (cm)
b = konsentrasi zat (mol/jam)
Pada spektrofotometer UV-Vis, warna yang diserap oleh suatu senyawa atau
unsur adalah warna komplementer dari warna yang teramati. Hal tersebut dapat
diketahui dari larutan berwarna yang memiliki serapan maksimum pada warna
22
putih, maka radiasi tersebut pada panjang gelombang tertentu, akan secara selektif
23
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di
Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Lampung.
B. Alat dan Bahan
Alat-alat yang akan digunakan dalam penelitian ini antara lain spektrofotometer
UV-Vis, sentrifuga, mikropipet, shaker (orbit environ shaker), laminar air flow,
pH meter, pH universal, autoklaf, jarum ose, pembakar spiritus, neraca analitik
dan alat-alat gelas laboratorium lainnya.
Bahan-bahan yang akan digunakan adalah pati singkong, glukosa, fruktosa,
arabinosa, gula, pepton, Yeast Ekstrak, NH4Cl, NaCl, K2HPO4, KH2PO4,
MgSO4.7H2O, MnSO4.H2O, FeSO4, (NH4)2HPO4,ZnSO4, NaOH, pereaksi iodin,
BSA (Bovine Serum Albumin), Na2CO3, Na-K- tartarat, CuSO4.5H2O, reagen folin
24
C. Prosedur Penelitian
1. Peremajaan Isolat LTE-6
Peremajaan isolat LTE-6 dilakukan dengan cara memasukan 2,8 gram Nutrien
Agar (NA) dalam 100 ml air. Larutan dipanaskan hingga larutan jernih dan
dimasukkan ke dalam tabung reaksi sebanyak 5 mL. kemudian dilakukan
sterilisasi,dimiringkan dan didiamkan pada suhu kamar. Setelah media memadat
dilakukan inokulasi bakteri isolat LTE-6 pada media agar miring. Kemudian
diinkubasi selama 3 hari dalam inkubator.
2. Penyiapan Medium dan Pereaksi a. Penyiapan Medium Kultur
Medium yang digunakan adalah medium yangdalam setiap 100 ml mengandung
1% (w/v) pati singkong, 0,05% (w/v) K2HPO4, dan 0,05% (w/v) KH2PO4,
kemudian medium diatur pada pH 6.0
b. Pembuatan Pereaksi untuk Pengukuran Aktivitas Enzim Amilase Metode Fuwa (Fuwa, 1954)
Pembuatan pereaksi iodin yaitu dengan cara melarutkan 3 g KI dengan sedikit
akuades di dalam labu takar 100 mL, lalu ditambahkan 0,3 g I2 dan ditambahkan
dengan akuades hingga tanda batas.
Pembuatan larutan pati yaitu dengan cara memasukkan 0,5 gram pati ke dalam
labu takar 100 mL kemudian ditambahkan 0,1 M buffer asetat hingga tanda batas,
25
c. Pembuatan Pereaksi Lowry untuk Pengukuran Kadar Protein (Lowry et al., 1951).
Pereaksi Lowry terdiri atas 4 macam, yang meliputi pereaksi A,B,C, dan D.
Pereaksi A dapat dibuat dengan cara melarutkan 2 g Na2CO3 dengan 100 mL
NaOH 0,1N. Pereaksi B dapat dibuat dengan cara menambahkan 5 ml
CuSO4.5H2O 1% (w/v) ke dalam 5 mL larutan Na-K-tartarat 1%. Pereaksi C
dapat dibuat dengan cara menambahkan 2 mL pereaksi B dengan 100 mL pereaksi
A. Pereaksi D dapat dibuat dengan cara mengencerkan reagen folin-ciocelteau
dengan akuades 1:1.
3. Pembuatan Medium Nutrien Broth (NB)
Medium NB dibuat dengan komposisi 0,3% (w/v) ekstrak ragi, 0,5% (w/v) pepton
dan 0,5 % NaCl, kemudian disterilisasi. Medium NB digunakan sebagai
penyiapan inokulum (starter) dengan cara menginokulasikan 1 ose mikroba dari
isolat LTE-6 masing-masing ke dalam erlenmeyer yang telah berisi medium NB
cair steril yang telah berusia 3 hari kedalam masing-masing erlenmeyer yang
berisi 5 mL medium NB. Setelah diinokulasi, biakan diinkubasi pada shaker
dengan kecepatan 95 rpm pada suhu 37oC selama 1 malam (overnight: 16-20
jam).
4. Penentuan Pertumbuhan Sel (OD)
Penentuan Pertumbuhan sel bakteri digunakan untuk mengetahui pertumbuhan
dari sel bakteri. Sebanyak 0,3 mL kultur dimasukkan kedalam tabung reaksi
kemudian ditambahkan 2,7 mL akuades lalu diukur serapannya menggunakan
26
5. Penentuan Kadar Protein
Metode Lowry digunakan untuk mengetahui kadar protein (Lowry et al., 1951).
Sebanyak 0,1 mL enzim ditambahkan 0,9 mL akuades lalu direaksikan dengan 5
mL pereaksi C. Campuran diaduk secara merata dan dibiarkan selama 10 menit
pada suhu kamar. Kemudian ditambahkan dengan cepat 0,5 mL pereaksi D dan
diaduk dengan sempurna. Setelah itu didiamkan selama 30 menit pada suhu
kamar. Untuk kontrol sama dengan perlakuan pada sampel. Pengukuran serapan
dilakukan pada 600 nm. Konsentrasi protein enzim ditentukan dengan
menggunakan kurva standar Bovine Serum Albumin (BSA).
6. Penentuan Aktivitas Enzim
Aktivitas α-amilase ditentukan oleh metode iodin (Fuwa, 1954). Pati soluble
0,5% di dalam buffer asetat 0,1 M sebanyak 300 L ditambahkan dengan enzim
sebanyak 100 L dipanaskan pada suhu 55oC selama 10 menit lalu ditambahkan
0,2 M HCl sebanyak 4 mL, ditambahkan larutan iodin 0,5 mL, dan ditambahkan
H2O hingga volumenya 10 mL, lalu diukur dengan spektrofotometer UV-Vis pada
max 700 nm. Kontrol dibuat dengan cara memanaskan enzim pada suhu 100oC
selama 30 menit. Aktivitas unit dihitung dari jumlah enzim yang mereduksi
warna biru 10% permenit.
7. Variasi komposisi a. Sumber Karbon (C)
Sumber C yang digunakan adalah glukosa, fruktosa, arabinosa, dan gula.
Masing-masing sumber C sebesar 0,5% (w/v) ditambahkan ke dalam medium standar.
27
dan ditumbuhkan seperti yang dijelaskan pada prosedur 4. Sampling dilakukan
pada rentang waktu 12, 24, 36, 48, 60, dan 72 jam. Sampel kultur diukur nilai
OD, kadar protein, dan aktivitas enzim seperti pada prosedur 4, 5 dan 6.
b. Sumber Nitrogen (N)
Sumber N yang digunakan adalah pepton, NaNO3, NH4Cl,dan ekstrak ragi.
Masing-masing sumber N sebanyak 0,5% (w/v) ditambahkan ke dalam medium
tanpa perlakuan Medium kultur dengan komposisi tersebut kemudian diinokulasi
dengan starter dan ditumbuhkan seperti yang dijelaskan pada prosedur 4.
Sampling dilakukan pada setiap 12 jam selama 72 jam. Sampel kultur diukur nilai
OD, kadar protein, dan aktivitas enzim seperti pada prosedur 4, 5 dan 6.
c. Ion Logam
Sumber ion logam yang digunakan adalah MgSO4, ZnSO4, MnSO4, dan FeSO4.
Masing-masing sumber ion logam sebanyak 0,01 % (w/v) ditambahkan ke dalam
medium tanpa perlakuan. Medium kultur dengan komposisi tersebut kemudian
diinokulasi dengan starter dan ditumbuhkan seperti yang dijelaskan pada prosedur
4. Sampling dilakukan pada rentang waktu 12, 24, 36, 48, 60, dan 72 jam.
Sampel kultur diukur nilai OD, kadar protein, dan aktivitas enzim seperti pada
prosedur 4, 5 dan 6. Untuk sumber ion logam terbaik kemudian dilakukan uji
variasi pH.
d. Variasi pH
Medium yang digunakan untuk menginokulasi bakteri divariasikan pHnya yaitu
pH 5, pH 6, pH 7 dan pH 8. Medium kultur dengan komposisi tersebut kemudian
28
4. Sampling dilakukan pada rentang waktu 12, 24, 36, 48, 60, 72 jam. Sampel
kultur diukur nilai OD, kadar protein dan aktivitas enzim seperti pada prosedur 3,
SIMPULAN DAN SARAN
A. SIMPULAN
Berdasarkan hasil penelitian yang telah dilakukan, dapat diperoleh kesimpulan
sebagai berikut:
1. Kondisi optimum isolat LTE-6 dalam memproduksi enzim amilase berada
pada pH 7 dengan nilai aktivitas unit dan spesifik yang dihasilkan secara
berurutan yaitu 9,961 U/ml dan 36,11 U/mg
2. Pada medium pati singkong setelah dilakukan variasi komposisi sumber
Karbon, Nitrogen, Ion logam dan pH terjadi peningkatan pertumbuhan dan
aktivitas unit enzim amilase.
3. Pada sumber variasi sumber Karbon, Nitrogen, ion logam dan pH
berturut-turut terbaik terdapat pada gula, pepton, Mg dan pada pH 7.
B. SARAN
Kondisi optimum yang diperoleh pada penelitian ini diharapkan dapat digunakan
DAFTAR PUSTAKA
Crueger, W. and A. Crueger. 1984. Biotechnology A Text Book of Industrial Microbiology. Translated by Caroline Haessly. Science Tech. Madison.
De Carvalho, R.V., Correa,T and da Silva, J. 2008. Properties of An Amylase From Thermophillic Bacillus sp. Brazillian Journal of Microbiology. 39: 102-107.
Chaplin, M.F., and Bucke. 1990. Enzyme Technology. Cambridge University
Dwidjoseputro, D. 1992. Dasar-Dasar Mikrobiologi. Djambatan. Jakarta.
Fuwa, H. 1954. A New Method For Microdetermination of Amylase Activity by The Use of Amylose As The Substrate. J Biochem. Tokyo. 41. 583-603.
Fandika, K. 2011. Pengaruh Beberapa Faktor pada Medium Kultur Terhadap Produksi Enzim Amilase dari Bakteri Amilolitik Isolat Lokal. Skripsi. Universitas Lampung. Bandar Lampung
Hagihara, H., Igarashi, K and Hayashi, Y. 2001. Novel α-amylase that is highlyn Resistant to chelating reagents and chemical oxidants from the Alkaliphilic Bacillus Isolate KSM-K38. Applied and Environmental Microbiology. 67:1744–1750.
Hidayat, N., M.C Padaga dan S. Suhartini. 2006. Mikrobiologi Industri. Penerbit ANDI. Yogyakarta.
Judoamidjojo, R. M., Gumbira, Hartoto. L. 1989. Biokonversi. Depdikbud Dirjen Dikti. PAU Bioteknologi IPB. Bogor.
Khopkar, S.M. 1990. Konsep Dasar Kimia Analitik. Universitas Indonesia Press. Jakarta.
Lehninger, A.L. 1990. Dasar-Dasar Biokimia. Penerjemah: Maggy Thenawidjaya. Erlangga. Jakarta.
Lay, B.W. 1994. Analisis Mikroba di Laboratorium. Raja Grafindo Persada. Jakarta. 168.
Mateo, C,, JM. Palomo, GF, lorente, J.M. Guisan and R.F. Lafuente, 2007, “ Impovement of Enzyme Activity and Selectivity via Immobilization
Techniquez” Enzym Microb Techmol 40, 1451 – 1463.
Meryandini, A. 2009. Isolasi bakteri selulolitik dan karakterisasi enzimnya. Makara Sains 2009; 13: 33-38.
Mulatasih, E.R. 2010. Penapisan dan Optimasi Bakteri Amilolitik Isolat Lokal dari Pabrik Tapioka untuk degradasi Pati Singkong Segar.Skripsi. Universitas Lampung. Bandar Lampung.
Page, D.S. 1997. Prinsip-Prinsip Biokimia. Erlangga. Jakarta. 465.
Palmer, T. 1985. Understanding Enzyme. Ellishorwood Publisher.
Poedjadi, A. 2006. Dasar-Dasar Biokimia. UI Press. Jakarta.
Reddy, N.S., Nimmagadda, A. and Rao,K.R. 2003. An Overview of
Themicrobial α-Amylase Family. African Journal of Biotechnology. 2: 645–648.
Schomburg, D and Salzmann, M. 1991. Enzyme Handbook 4. Springer. Verlag Berlin Heidelberg.
Sivaramakrishnan, S. Gangadharan, D. Nampoothiri, K.D. Sossol, C.R. and Pandey, A. 2006. Α-amylase from microbial sources an overview on recent developments. Food. Technol. Biotechnol. 44:173-184.
Reddy, N.S., Nimmagadda, A. and Rao,K.R. 2003. An Overview of
Themicrobial α-Amylase Family. African Journal of Biotechnology. 2: 645–648
Santoso. 2010. Enzimologi. Seri Buku Kuliah Biokimia Kedokteran I. Semarang.
Suhartono, M.T. 1989. Enzim dan Bioteknologi. Depdikbud Dirjen Dikti Antar Universitas Bioteknologi IPB. Bogor.
Underwood, A. L., Day, R. A. 2002. Analisa Kimia Kuantitatif Edisi Kelima. Erlangga. Jakarta.
Vihinen, M. and P. Manstala. 1989. Site-directed Mutagenesis of a
Thermostable α-amylase from Bacillus stearothermophillus: Putative Role of Three Coserved Residues, Crit. Rev. Biochem. Mol. Biol., 24: 329-415.
Winarno, F.G. 1995. Enzim Pangan. PT Gramedia Pustaka Umum. Jakarta. 115.