Tandan Kosong Sawit
(TKS)
(Skripsi)
Oleh Mardiyah
JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
ABSTACT
DELIGNIFICATION EFFECT ON THE YIELD OF FURFURAL ON ACID HYDROLYSIS OF OIL PALM EMPTY FRUIT BUNCHES
(OPEFB)
By
Mardiyah
In this research, the process of delignification and hydrolysis of Oil Palm Empty Fruit Bunches (OPEFB) powder was done. Delignification carried out using sodium hydroxide (NaOH) (1%, 3%, and 5% (w/v)) were soaked for 24 and 48 hours. Hydrolysis process using OPEFB without delignification and OPEFB with delignification with various concentration of sulfuric acid (H2SO4) (0%; 1%; and
5% (v/v)), various temperature (80, 90, and 100oC), and various time (30, 45, 60, and 90 minute) to obtain the optimum yield of furfural. Identification furfural using color test with aniline-acetate, spectrophotometer UV-Vis and FT-IR also using GC-MS. The highest furfural produced by OPEFB without delignification and OPEFB with delignification using NaOH 3% were soaked for 48 hours at optimum hydrolysis condition with concetration of H2SO4 5%, temperature
100oC, and for 60 minutes, respectively 0,3132 dan 0,4932 (mg/mL) with
respective yield of 20,32% dan 32,42%. The color test showed positive result with the formation of red color. The maximum wavelength of UV-Vis
spectrophotometry is (λmaks) 273,5 nm and vibrational number of wavelengths
corresponding to the theory and standard furfural in FTIR spectrophotometry and also molecular ion peak at m/z 96 which is the molecular weight of furfural on GC-MS analysis.
PENGARUH DELIGNIFIKASI TERHADAP PEROLEHAN FURFURAL PADA HIDROLISIS ASAM
TANDAN KOSONG SAWIT (TKS)
Oleh
Mardiyah
Pada penelitian ini dilakukan proses delignifikasi dan hidrolisis serbuk Tandan Kosong Sawit (TKS). Delignifikasi menggunakan sodium hidroksida (NaOH) (1%; 3%; dan 5% (w/v)) yang direndam selama 24 dan 48 jam. Proses hidrolisis menggunakan TKS tanpa delignifikasi dan TKS dengan delignifikasi dengan variasi konsentrasi asam sulfat (H2SO4) (0%; 1%; dan 5% (v/v)), variasi suhu (80,
90, dan 100oC), dan variasi waktu (30, 45, 60, dan 90 menit) untuk mendapatkan perolehan furfural optimum. Identifikasi furfural menggunakan uji warna dengan anilin-asetat, spektrofotometer UV-Vis dan FT-IR serta menggunakan GC-MS. Furfural tertinggi dihasilkan oleh TKS tanpa delignifikasi dan TKS dengan delignifikasi NaOH 3% yang direndam selama 48 jam, pada kondisi hidrolisis optimum dengan konsentrasi H2SO4 5%, suhu 100oC, dan waktu 60 menit, yaitu
masing-masing 0,3132 dan 0,4932 (mg/mL) dengan masing-masing perolehan sebesar 20,32% dan 32,42%. Pada uji warna menunjukkan hasil positif dengan terbentuknya warna merah. Panjang gelombang maksimal (λmaks) 273,5 nm pada
analisis spektrofotometri UV-Vis, dan vibrasi bilangan panjang gelombang yang sesuai dengan teori dan furfural standart pada analisis spektrofotometri FT-IR serta puncak ion molekul pada m/z 96 yang merupakan berat molekul furfural pada analisis GC-MS.
Penulis dilahirkan di Suka Agung pada tanggal 04 Januari 1992, sebagai anak kedua (kembar) dari tiga bersaudara dari pasangan Bapak M. Fatoni dan Ibu Sri Supriyati. Jenjang pendidikan diawali dari Sekolah Dasar (SD) di SD Negeri 1 Suka Agung Kecamatan Bulok-Tanggamus yang diselesaikan pada tahun 2003. Sekolah Menengah Pertama (SMP) di SMP Negeri 1 Pardasuka Tanggamus dan diselesaikan di SMP Negeri 1 Pagelaran Pringsewu pada tahun 2006. Sekolah Menengah Atas (SMA) di SMA Negeri 1 Pringsewu diselesaikan pada tahun 2009. Pada tahun 2009, penulis terdaftar sebagai Mahasiswa Jurusan Kimia FMIPA Unila melalui jalur Ujian Mandiri (UM).
MOTO
“Bacalah, dan Tuhan
-mulah yang Maha Mulia. Yang
mengajar (manusia) dengan pena. Dia mengajarkan manusia
apa yang tidak diketahuinya.”
(QS. Al-Alaq, 96:3-5)
“Science without religions is lame, religion without science is
blind.”
(Albert Einstein)
“Selalu lakukan yang terbaik. Dan biarkan Tuhan yang
melakukan selanjutnya.”
(Ben Carson)
“Jadikanlah sabar dan shalat sebagai penolongmu, dan
sesungguhnya yang demikian itu sungguh berat kecuali bagi
orang-
orang yang khusyu.”
(QS. Al-Baqarah, 2:45)
Semper Fi! Carpe Diem (Semangat! Raih harimu)
Jangan terlalu bergantung pada orang lain karena
bayanganmu sendiri pun akan meninggalkanmu saat kamu
berada di kegelapan.
ini kepada
Ayahanda M. Fatoni dan Ibunda Sri Supriyati yang tercinta
atas do’a, kasih sayang, dukungan,
semangat, nasihat dan
kesabaran dalam mendidikku.
Kakakku tersayang Sofia Safitri, S. Pd. dan saudara
kembarku Maryam, Amd. atas keceriaan, motivasi, nasihat, dan
kasih sayang untukku.
Segenap keluargha besar yang selalu mendo’akan keberhasilanku.
Dengan rasa hormat kepada Dr. Eng. Suripto Dwi Yuwono,
M. T.
Sahabat dan teman-temanku yang selalu berbagi keceriaan.
SANWACANA
Bismilahir rahmanir rahim,
Assalamu’alaikum wa rahmatullahi wa barakatuh.
Alhamdulillah puji dan syukur Penulis ucapkan kehadirat Allah SWT atas segala rahmat dan karunia-Nya, sripsi ini dapat diselesaikan.
Skripsi yang berjudul “Pengaruh Delignifikasi Terhadap Perolehan Furfural pada Hidrolisis Asam Tandan Kosong Sawit (TKS)” adalah salah satu syarat untuk memperoleh gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung. Dalam pelaksanaan dan penulisan skripsi ini tidak lepas dari kesulitan dan rintangan. Namun, itu semua dapat penulis lalui berkat rahmat dan ridha Allah SWT serta bantuan dan
dorongan semangat dari orang-orang yang hadir dalam kehidupan penulis. Dalam kesempatan ini, Penulis menyampaikan terima kasih kepada :
semangat, kritik, saran, dan arahan kepada penulis sehingga skripsi ini terselesaikan dengan baik.
4. Bapak Rudy TM Situmeang, Ph. D., selaku pembimbing Akademik atas kesediaannya untuk memberikan bimbingan, bantuan, dan nasehat.
5. Bapak Prof. Suharso, Ph. D., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
6. Bapak Dr. Eng. Suripto Dwi Yuwono, M. T., selaku ketua Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. 7. Seluruh guru dari SD, SMP, dan SMA yang dengan senang hati dan kesabaran
memberikan ilmu pengetahuan yang sangat berguna kepada penulis. 8. Seluruh dosen FMIPA Unila yang dengan senang hati memberikan ilmu
pengetahuan yang sangat berguna kepada penulis selama kuliah.
9. Mbak Wiwit, mbak Nora , mbak Iin, uni Non, mbak Liza, mas Udin, pak Gani, pak Man, mas Nomo, dan seluruh staf Jurusan Kimia FMIPA Unila yang telah membantu mengurus semua administrasi penulis selama kuliah. 10.Kedua orangtuaku yang sangat aku cintai dan sayangi. Ayahku tersayang M.
Fatoni, dengan kesederhanaannya selalu menjadi inspirasiku, selalu
senantiasa mendoakan keberhasilanku. Ibundaku tersayang, Sri Supriyati, dengan kesabarannya membimbing dan mendukungku, selalu memberikan kasih sayang, motivasi dan nasehat yang menyemangatiku, serta tiada hentinya mendoakan keberhasilanku. Terima kasih dengan sangat tulus kuucapkan atas segala hal yang terbaik, kebahagiaan dan semua yang telah diberikan kepadaku yang takkan bisa aku ganti dengan apapun. Aku hanya bisa berdo’a semoga ayah dan ibunda sehat, panjang umur, dan kelak aku bisa membahagiakannya.
11.Kakakku tersayang, Sofia Safitri, S. Pd., yang selalu berbagi keceriaan, mendukung dan memberikan nasehat yang menyemangatiku. Saudara kembarku tersayang, Maryam, Amd., yang selalu mendukung dan dengan keceriannya selalu memberikan semangat disaat aku letih.
12.Keluarga besar di Sekampung Metro, mbah putri, bulek dan oomku yang
selalu mendo’akanku , serta sepupu-sepupu kecilku yang selalu memberikan kelucuan dan keceriaannya.
13.Partner terbaik, Rhamadya Teta Parasta, atas kerja sama yang sangat baik, bantuan, dukungan, semangat, dan keceriaannya selama penelitian. Semua usaha, kerja keras, dan semua yang kita perjuangkan akhirnya kita dapatkan, terima kasih teman.
14.Sahabat terbaik, Tiurma Nainggolan, yang tidak hentinya menyemangati dan menemani serta membantuku selama ini.
15.Adik-adik terbaik, Chyntia Gustianda dan Susi Susanti, yang selalu
17.Teman-teman angkatan 2009, Rhamadya Teta Parasta, Tiurma Nainggolan, Delphiana, Resca Ridhatama, Neneg Suryani, Siska Dwi Aryani, Fitriyanti, Delviana Br Sidabalok, Nurjannah, mbak Karlina, Ruth Meta Megawati, Juwita Ratna Sari, Retno Nur Rhamadani, Stephanie Oktiana, Sherly Nurimani, Luh Gede Rai Putri, Rizki Yuliandari, Tyas Rosawinda, Fatma Timur, Lia Andriani, Indah RN Pramudita, Miftahul Jannah, Rinawati, Mersiana, Yahya Ariyanta, Dani Agus Setiawan, M. Padli, Ignatius Shandy Ellen, Khoirul Umam, Dwiyanto, Purna Firdaus, Ari Bowo Slamet Efendy dan Suparno atas segala bantuan dan kebersamaannya selama ini.
18.Teman-teman Laboraturium Kimia Organik, mbak Eka, kak Heri, mbak Wiwit, Teta, Resca, Chyntia, Fajri, Awan, Purniawati, Lili, Yulia, Mirfat, Junet dan Ridho atas bantuan dan kerjasamanya di laboraturium.
19.Kakak-kakak tingkat angkatan 2007 dan 2008 serta adik-adik tingkat angkatan 2010 sampai angkatan 2013 Kimia FMIPA Unila, terima kasih atas segala dukungannya.
21.Teman-teman bermain, Susi, Asih, Yanti, Yetti, kak Endru, Candra, Septi, dan Lina. Terima kasih sudah menemani, menghibur, dan mengajakku bermain saat aku jenuh.
22.Teman-teman KKN di Desa Bengkulu Rejo Kecamatan Gunung Labuhan Waykanan, Lia, Anida, Dedeh, Meli, Tiya, Afdi, Dicky, Uska, Dewa dan Astra. Keluarga baruku di Bengkulu Rejo, ayah, ibu, kak Rini, Tri, Lili, uwak, tante, dan om. Terima kasih atas kebersamaan dan keceriannya selama KKN. 23.Semua pihak yang tidak dapat dituliskan satu persatu yang telah membantu
penulis selama kuliah, penelitian, hingga penulisan skripsi ini.
Semoga Allah SWT membalas segala kebaikan yang telah diberikan kepada penulis. Penulis sangat menyadari bahwa skripsi ini masih jauh dari
kesempurnaan. Akan tetapi, sedikit harapan semoga skripsi yang sederhana ini dapat berguna dan bermanfaat bagi diri penulis secara pribadi maupun bagi pembaca. Amin.
Wassalamu’alaikum warahmatullahi wabarakatuh.
Bandar Lampung, Agustus 2014 Penulis
DAFTAR ISI
1. Konsentrasi Katalisator ... 14
2. Suhu Reaksi ... 15
1. Spektrofotometri UV-Vis ... 20
2. Spektrofotometri IR ... 21
J. Kromatografi Gas dan Spektroskopi Massa (GC-MS) ... 23
K. Penelitian Terdahulu ... 24
iv
3. Uji Kualitatif pada Lindi ... 29
4. Uji Kuantitatif pada TKS Terdelignifikasi ... 30
5. Hidrolisis Asam Menggunakan H2SO4 ... 31
6. Pemurnian Crude Furfural ... 32
7. Pemisahan Kloroform-Furfural ... 33
8. Analisis Furfural ... 33
IV. HASIL DAN PEMBAHASAN A. Proses Preparasi Sampel ... 35
B. Proses Delignifikasi ... 36
C. Uji Kuantitatif pada Lindi Hasil Delignifikasi ... 40
D. Uji Kuantitatif pada TKS Terdelignifikasi ... 41
E. Hidrolisis TKS dengan Asam Sulfat dan Uji Kuantitatif Furfural ... 43
1. Penggunaan TKS Terdelignifikasi ... 44
2. Optimalisasi Suhu Hidrolisis ... 45
3. Optimalisasi Waktu Hidrolisis ... 45
4. Optimalisasi Konsentrasi Asam Sulfat ... 46
F. Uji Kualitatif Furfural ... 47
V. SIMPULAN DAN SARAN A. Simpulan ... 55
B. Saran ... 56
DAFTAR GAMBAR
6. Proses Pembentukan Furfural ... 14
7. Reaksi Lignin Dengan Gugus Hidroksil pada Proses Delignifikasi ... 17
8. Spektrum IR Standart Furfural ... 22
9. Preparasi Sampel (a) Serat Tandan Kosong Sawit (TKS). (b) Serbuk Tandan Kosong Sawit (TKS) ... 36
10. Warna Lindi Hasil Perendaman Selama 24 Jam ... 37
11. Warna Lindi Hasil Perendaman Selama 48 Jam ... 37
12. Berat Akhir dari TKS Terdelignifikasi ... 39
13. Nilai Permanganat pada Lindi Hasil Perendaman TKS ... 40
14. Reaksi Antara Permanganat dan Unit Lignin... 41
15. Bilangan Kappa dari Residu Serbuk TKS Terdelignifikasi ... 42
16. Jumlah Lignin Yang Tersisa pada Serbuk TKS Terdelignifikasi... 43
17. Pengaruh Suhu Hidrolisis Terhadap Perolehan Furfural ... 45
18. Pengaruh Waktu Hidrolisis Terhadap Perolehan Furfural ... 46
19. Pengaruh Konsentrasi Asam Sulfat Terhadap Perolehan Furfural ... 47
20. Uji Warna Anilin-Asetat (a) Sebelum Ditetesi Anilin-Asetat dan (b) Setelah Ditetesi Anilin-Asetat ... 48
21. Reaksi Anilin-Asetat Terhadap Furfural ... 48
22. Spektrum UV-Vis (a) Furfural Standart; (b) Furfural TKS Tanpa Delignifikasi, dan (c) FurfuralTKS Terdelignifikasi ... 49
23. Spektra FT-IR (a) Furfural TKS Terdelignifikasi; (b) Furfural TKS Tanpa Delignifikasi; dan (c) Furfural Standart ... 51
24. Hasil GC Furfural Standart dengan Waktu Retensi 5,263 ... 52
25. Hasil GC Furfural TKS Tanpa Delignifikasi dengan Waktu Retensi 5,039 ... 53
vi
27. Hasil MS (a) Furfural Standart, (b) Furfural TKS Tanpa
DAFTAR TABEL
Tabel Halaman
1. Data Perkebunan Kelapa Sawit Provinsi Lampung ... 7 2. Komposisi Tandan Kosong Sawit (TKS) ... 8 3. Bilangan Gugus Fungsi Per-Variabel Bebas dari Furfural
Secara Teoritis ... 22 4. Faktor Kolerasi Terhadap Pemakaian Permanganat ... 31 5. Penggunaan TKS Terdelignifikasi ... 44 6. Bilangan Gelombang Gugus Fungsi Per Variable Bebas
1
I. PENDAHULUAN
A. Latar Belakang
Furfural merupakan salah satu senyawa kimia yang memiliki banyak manfaat, yaitu sebagai pelarut dalam memisahkan senyawa jenuh dan tidak jenuh pada industri minyak bumi serta sebagai senyawa intermediet pada pembuatan bahan kimia industri lainnya. Banyaknya manfaat dari furfural mendorong minat para peneliti untuk mengembangkan dan memproduksi furfural dari biomassa yang terbaharukan. Biomassa lignoselulosa merupakan salah satu bahan alam terbaharukan yang banyak ditemukan pada limbah hasil pertanian dan
perkebunan. Selain ekonomis, tersediaannya yang berlimpah sepanjang tahun, mudah dalam pengumpulan dan mudah ditemukan menjadi alasan lain untuk memanfaatkan biomassa lignoselulosa menjadi bahan baku pembuatan furfural. Salah satunya adalah tandan kosong sawit (TKS).
Yuwono dan Susanto (2000) melakukan penelitian tentang model Waste
Utilization Value pada limbah pertanian sebagai bahan baku furfural. Yuwono dan
dan tekanan 1 atm.
TKS merupakan limbah pertanian yang berasal dari pengolahan kelapa sawit (Elaeis guineensis Jacq.). Di Indonesia, jumlah TKS makin berlimpah. Hal ini dapat dilihat dengan adanya peningkatan luas perkebunan rakyat, yaitu sekitar 1,1 juta hektar tahun 2000 menjadi 3,6 juta hektar tahun 2011 (angka sementara). Perkebunan negara juga meningkat, dari 588 ribu hektar tahun 2000 menjadi 636 ribu hektar tahun 2011. Demikian pula perkebunan swasta, meningkat dari 2,4 juta hektar tahun 2000 menjadi 3,6 juta hektar tahun 2011. Jadi, perkebunan kelapa sawit Indonesia meningkat dari 4,1 juta hektar tahun 2000 menjadi 8,9 juta hektar tahun 2011 (angka sementara) atau dua kali lipat dalam 10 tahun
(Direktorat Jenderal Perkebunan Indonesia, 2011).
Seiring dengan peningkatan luas areal perkebunan kelapa sawit, jumlah limbah hasil pengolahan di pabrik kelapa sawit (PKS) pun meningkat. Setiap pengolahan tandan segar sawit (TBS) dihasilkan TKS sebanyak 25%. TKS ini belum banyak dimanfaatkan dengan baik oleh PKS. Pada umumnya, TKS hanya dimanfaatkan sebagai bahan pembuatan pupuk kompos organik (Darnoko et al., 1993 dalam Ganjar, 2011) atau dibakar dengan increrator sehingga abunya dapat
3
Jika ditinjau lebih lanjut, TKS mengandung tiga komponen utama, yaitu selulosa, hemiselulosa, dan lignin. Sekitar 44,2% selulosa; 33,5% hemiselulosa; dan 20,4% lignin terdapat di dalam TKS (Hamzah et al., 2011). Hasil penelitian Darnoko et al. (1992) dalam Yuwono (2000), menunjukan hal berbeda, TKS mengandung
45,95% selulosa; 22,84% hemiselulosa; dan 16,49% lignin. Selulosa adalah rantai lurus homopolisakarida yang tersusun atas unit-unit D-glukosa. Hemiselulosa merupakan polisakarida yang berikatan dengan selulosa dan tersusun dari pentosan dan heksosan. Lignin merupakan polimer fenolik yang dapat
menghalangi pemanfaatan selulosa dan hemiselulosa secara optimal. Kandungan hemiselulosa yang cukup tinggi dapat dimanfaatkan dalam pembuatan furfural melalui proses hidrolisis asam, dimana hemiselulosa tersusun dari pentosan yang merupakan prekursor utama furfural. Menurut Yuwono (2000), kandungan pentosan pada TKS adalah 23,08% dapat menghasilkan furfural sebanyak 9,08% dengan suhu pemasakan 150oC.
Furfural pertama kali diisolasi pada tahun 1821 oleh Dobereiner, menggunakan gula, asam sulfat, dan mangan dioksida untuk membuat asam formiat sebagai bahan awal pembuatan furfural. Selanjutnya, Emmeti mengganti produksi furfural yang sebelumnya menggunakan asam formiat dengan bahan baku tumbuhan yang mengandung pentosan. Proses pembentukan furfural dari bahan baku yang
mengandung hemiselulosa adalah hidrolisis pentosan yang terdapat pada
hidrolisis selulosa yang dapat memperlambat reaksi (Sasaki et al., 2012). Karbon-karbon lignin berikatan dengan gugus eter membentuk jaringan tri-dimensi yang terhubung pada polisakarida hemiselulosa di dalam dinding. Dengan kata lain, lignin dapat menghalangi proses hidrolisis hemiselulosa dalam pembentukan furfural. Untuk itu dilakukan perlakuan awal untuk menghilangkan lignin atau yang disebut dengan delignifikasi. Pada penelitian ini, dilakukan proses
delignifikasi sampel TKS menggunakan basa (NaOH) untuk melihat pengaruh delignifikasi terhadap perolehan furfural.
B. Tujuan
Tujuan dari penelitian ini adalah:
1. Mengetahui pengaruh konsentrasi NaOH danwaktu perendaman terhadap lignin yang hilang atau terdelignifikasi.
2. Mengetahui pengaruh delignifikasi terhadap perolehan furfural pada hidrolisis asam tandan kosong sawit (TKS).
5
C. Manfaat
II. TINJAUAN PUSTAKA
A. Data Perkebunan Sawit
Tanaman kelapa sawit (Elaeis quineensis Jacq) adalah tanaman penghasil minyak, baik minyak nabati maupun minyak industry (biodesel). Di Indonesia, potensi areal kelapa sawit masih luas. Hal ini dikarenakan kecenderungan peningkatan luas areal perkebunan kelapa sawit, khususnya perkebunan rakyat. Peningkatan perkebunan rakyat pada priode tiga puluh tahun terakhir mencapai 45,1% per tahun sementara areal perkebunan negara meningkat 6,8% per tahun, dan areal perkebunan swasta meningkat 12,8% pertahun. Industri pengolahan kelapa sawit di Indonesia juga terus mengalami peningkatan (Fauzi, 2004). Penyebarannya pun sudah semakin pesat, telah menyebar di 22 propinsi, yang pada tahun 2010
luasnya mencapai 8,3 juta Ha, yang sekitar 41% merupakan perkebunan rakyat (Direktorat Jenderal Perkebunan, 2011).
Lampung merupakan salah satu provinsi di Indonesia yang memiliki areal perkebunan kelapa sawit yang cukup luas. Data kebun sawit rakyat terluas
7
dari kebun sawit rakyat tersebut adalah binaan dari perusahaan Perkebunan Swasta. Luas perkebunan sawit swadaya masyarakat di Kabupaten Waykanan adalah seluas 11.089 ha dan tersebar di 14 kecamatan. Luasan perkebunan kelapa sawit di Lampung disajikan pada Tabel 1.
Tabel 1. Data Perkebunan Kelapa Sawit Provinsi Lampung.
No. Kabupaten TBM (ha) TM (ha) TR (ha) Total Luas (ha)
TBM= Tanaman Belum menghasilkan, TM= Tanaman Menghasilkan, TR= Tanaman Rusak,
*data tahun 2010
B. Tandan Kosong Sawit (TKS)
Gambar 1. Perkiraan Jumlah TKS Tahun 2000-2009.
Pemanfaatan TKS yang masih kurang baik, menyebabkan potensi TKS hanya menjadi limbah menjadi cukup besar. Padahal bila ditinjau dari komposisi yang terkandung di dalamnya, TKS masih dapat dimanfaatkan dalam industri berbasis lignoselulosa, seperti pembuatan kertas, gula, furfural dan lignin (Susanto et al. 1999 dalam Simatupang, 2012). Menurut Syafwina et al. (2002) kandungan selulosa, hemiselulosa dan lignin pada tandan kosong kelapa sawit berturut-turut adalah 41,30 – 46,50 % selulosa, 25,30 – 33,80 % hemiselulosa dan 27,60 – 32,50 % lignin.
Tabel 2. Komposisi Tandan Kosong Sawit (TKS) (Darnoko et al., 1992 dalam Yuwono, 2000).
Komposisi TKS Bobot Kering (%)
Selulosa 45,95
Hemiselulosa (pentosa) 22,84
Lignin 16,49
Selulosa adalah polimer tak bercabang dari monomer D-glukosa yang
dihubungkan melalui ikatan beta-1,4 atau 1,4-β-glukosida (Goyal et al., 2006
9
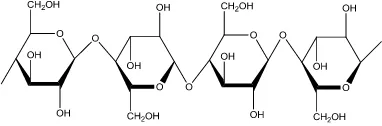
dalam Riansa-ngawong, 2011). Sebanyak 5000 unit glukosa membentuk polimer berantai lurus yang terikat melalui ikatan hidrogen di antara gugus hidroksil pada rantai di sebelahnya. Struktur dari selulosa disajikan dalam Gambar 2.
Gambar 2. Struktur Selulosa (Pushpamalar, 2006)
Selulosa merupakan bahan dasar dalam industri pembuatan kertas, dan serat. Di alam, selulosa hampir ditemukan pada semua jenis tanaman dengan kadar yang berlimpah. Kandungan selulosa kayu berkisar 48 – 50%, pada bagas berkisar antara 50 – 55% dan pada tandan kosong kelapa sawit sekitar 45%. Selulosa dapat dihidrolisis dengan asam kuat maupun dengan enzim selulase serta mikroba seperti bakteri dan kapang. Hidrolisis sempurna akan menghasilkan glukosa dan hidrolisis tidak sempurna menghasilkan disakarida berupa selobiosa. Hasil hidrolisis ini dapat dikonversi menghasilkan etanol dan asam asetat.
2. Hemiselulosa
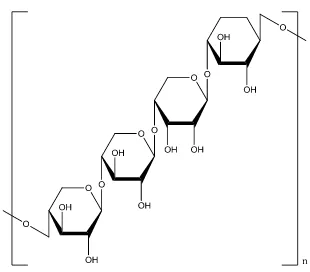
menyebabkan terjadinya sifat polar pada adsorben tersebut. Dengan demikian, selulosa dan hemiselulosa lebih kuat menjerap zat yang bersifat polar dari pada zat yang kurang polar (Steven, 2001). Struktur dari hemiselulosa disajikan pada Gambar 3.
Gambar 3. Struktur Hemiselulosa (Carpita, 2000).
11
akan melunak dan pada saat hemiselulosa melunak, serat yang sudah terpisah akan lebih mudah menjadi berserabut (Oktarina, 2009).
3. Lignin
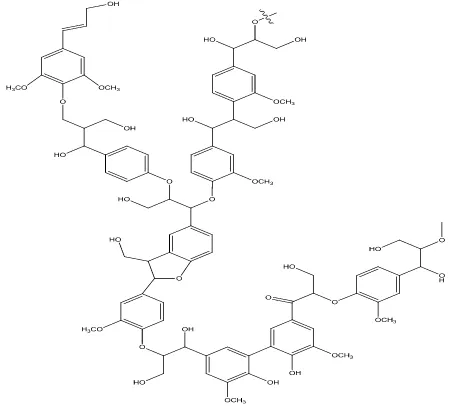
Jumlah lignin pada TKS cukup banyak, terdapat sekitar 16,49% (Darnoko, 1992 dalam Yuwono,2000). Lignin merupakan senyawa kompleks yang berbentuk aromatik dan memiliki gugus metoksil (Fengel, 1995 dalam Lubis, 2007). Struktur dasar lignin adalah fenil propana yang terhubung satu sama lainnya dengan ikatan karbon-karbon (C – C), ikatan karbon-oksigen (C–O), dan ikatan eter (-O-). Menurut Achmadi (1990) dalam Heradewi (2007), lebih dari dua per tiga unit fenil propana dalam lignin dihubungkan dengan ikatan eter, sedangkan sisanya (satu per tiga) dihubungkan melalui ikatan karbon-karbon. Struktur lignin yang kompleks memungkinkan lignin berfungsi sebagai semen atau lem yang dapat mengikat serat-serat dan memberikan sifat keras pada tanaman. Struktur lignin disajikan dalam Gambar 4.
menjadi kurang maksimal sehingga perlu dilakukannya perlakuan awal untuk menghilangkan lignin. Sifat lignin adalah tidak larut dalam air (hidrofobik) dan pelarut sederhana, namun dapat larut dalam larutan alkali. Pada saat pembuatan pulp, perlakuan kayu dengan ion -OH akan menyebabkan degradasi parsial pada ikatan eternya, menghasilkan lignin alkali yang bersifat larut dalam air
(hidrofilik).
C. Pemanfaatan TKS
TKS banyak dijumpai di sekitar pabrik kelapa sawit (PKS), merupakan limbah berlignoselulosa yang belum dimanfaatkan secara maksimal.TKS hanya
dimanfaatkan sebagai bahan bakar boiler di jalan-jalan sekitar perkebunan kelapa sawit untuk mengeraskan jalan atau dibuang diperkebunan kelapa sawit sebagai pupuk alami (Darwis et al. 1988 dalam Heradewi, 2009). Sebagai limbah
berlignoselulosa, TKS dapat dimanfaatkan sebagai penetral pH limbah cair Pabrik Kelapa Sawit (PKS) dan pupuk kalium dengan menggunakan abu dari hasil pembakaran TKS, pembuatan karbon aktif dengan cara karbonisasi pada
13
D. Furfural
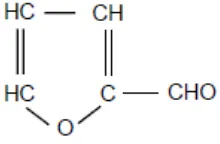
Furfural (C5H4O2) atau disebut furankarboksaldehid, furanaldehid,
2-furfuraldehid, furaldehid merupakan senyawa organik turunan furan yang
berbentuk cair dan berwarna kuning-kecoklatan. Senyawa furfural memiliki titik didih 161,5oC dengan berat molekul sebesar 96,086 g/gmol, dan densitas pada suhu 20oC sebesar 1,16 g/cm3. Furfural juga memiliki sifat yang kurang larut dalam air, namun dapat larut dalam pelarut-pelarut organik, seperti alkohol, eter, dan benzen (Kirk and Othmer, 1955 dalam Ganjar, 2011).
Gambar 5. Rumus Struktur Furfural (Ganjar, 2011)
Furfural memiliki aplikasi yang cukup luas terutama untuk mensintesis senyawa-senyawa turunannya. Di dunia hanya 13% saja yang langsung menggunakan furfural sebagai aplikasi, selebihnya disintesis menjadi produk turunannya
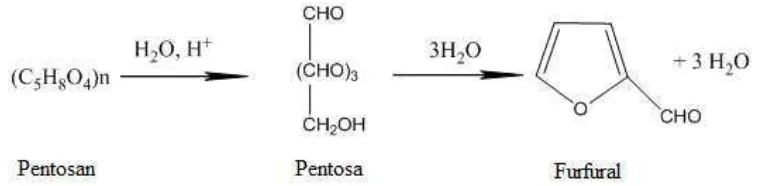
awal untuk memproduksi furfural. Namun saat ini secara sintesis, furfural merupakan senyawa kimia yang dihasilkan dari reaksi hidrolisis dan dehidrasi pentosan dengan bantuan katalis asam. Pembentukan furfural dari pentosan melalui dua tahap, tahap pertama melibatkan reaksi hidrolisis katalis-asam, dimana rantai pentosan dihidrolisis pada suhu tinggi membentuk monomer pentosa dalam media berair. Sedangkan pada tahap kedua, pentosa dikonversi menjadi furfural melalui penghilangan air atau disebut proses siklodehidrasi seperti yang disajikan dalam Gambar 6.
Gambar 6. Proses Pembentukan Furfural (Othmer et al. 1980 dalam Ardiana, 2012)
Beberapa faktor penting yang berpengaruh terhadap pembuatan furfural dari lignoselulosa (limbah pabrik) adalah:
1. Konsentrasi Katalisator
15
reaksi bertambah cepat pula. Namun, setelah mencapai kosentrasi asam yang optimum maka hasil furfural akan menurun karena peruraian furfural menjadi asam furoat sebagai hasil dari pemecahan gugus aldehid dan terbentuk sejenis damar yang berwarna hitam.
2. Suhu Reaksi
Reaksi akan berjalan cepat apabila suhu dinaikkan karena gerakan-gerakan molekul menjadi lebih cepat dengan bertambahnya suhu reaksi. Kecepatan reaksi hidrolisis akan meningkat hampir 2 kali untuk setiap kenaikan suhu 10oC
(Groggins, 1958 dalam Ganjar, 2011). Dengan menggunakan suhu tinggi, kosentrasi asam yang rendah dan waktu yang diperlukan menjadi lebih singkat. Sedangkan suhu yang rendah akan menyebabkan konsentrasi asam yang
digunakan lebih tinggi.
3. Waktu Reaksi
Semakin lama waktu reaksi maka hasil yang diperoleh akan bertambah besar karena pentosan yang bereaksi dengan asam lebih lama. Tetapi pertambahan hasil furfural tidak berbanding lurus dengan penambahan waktu proses karena terlalu lama waktu reaksi dapat menimbulkan terbentuknya sejenis damar.
4. Kecepatan Pengadukan
Semakin kecil ukuran butir maka semakin luas bidang persentuhan antar zat pereaksi, sehingga kontak antar molekul juga semakin besar. Hal ini sesuai dengan persamaan Arhenius yaitu semakin kecil ukuran butir maka nilai A (faktor frekuensi tumbukan) semakin besar sehingga nilai konstanta kecepatan reaksi akan semakin besar pula.
E. Delignifikasi
Delignifikasi merupakan proses pelarutan lignin dalam proses pembuatan bubur dalam industri kertas (pulping). Gullichsen (2000) mengatakan bahwa prinsip proses delignifikasi tergantung pada struktur kayu, metode pulping dan komponen bahan kimia yang akan digunakan. Proses delignifikasi yang umum digunakan adalah mekanis, semi kimia, kimia (alkali, sulfat/kraft, sulfit), dan proses non konvensional yang lebih berwawasan lingkungan. Salah satu proses delignifikasi yang sering digunakan adalah proses kimia menggunakan larutan alkali atau yang dikenal dengan proses pulping alkali. Delignifikasi dengan alkali dapat
17
derajat polimerisasi rendah yang dapat larut dalam alkali (Achmadi, 1990 dalam Heradewi, 2007).
Selain itu, suhu, tekanan dan konsentrasi larutan pemasak yang digunakan selama proses pulping sangat mempengaruhi kecepatan pelarutan lignin, hemiselulosa, dan selulosa. Dimana selulosa tidak akan rusak pada proses pelarutan lignin jika konsentrasi pelarut yang digunakan rendah dan suhu yang dipakai juga sesuai. Akan tetapi, pemakaian suhu di atas 180oC akan menyebabkan degradasi selulosa lebih tinggi, dimana pada suhu tersebut lignin sudah habis terlarut dan sisa bahan pemasak akan mendegradasi selulosa.
Sodium hidroksida (NaOH) umumnya digunakan dalam delignifikasi menggunakan larutan alkali (pulping alkali). Penambahan NaOH dapat
menyebabkan tingginya konsentrasi ion hidroksil dalam larutan pemasak sehingga mempercepat pemutusan ikatan intra-molekul lignin pada saat proses delignifikasi sehingga lignin akan larut dalam larutan pemasak (Damat, 1989 dalam
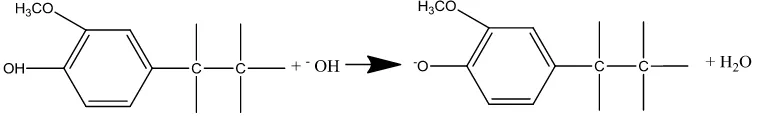
Simatupang, 2012). Larutnya lignin disebabkan oleh terjadinya transfer ion hidrogen dari gugus hidroksil pada lignin ke ion hidroksil (Gilligan, 1974 dalam Lubis, 2007) seperti yang disajikan pada Gambar 7.
asam yang akan digunakan, terutama dalam menghidrolisis hemiselulosa. Hidrolisis hemiselulosa dengan asam encer akan menghasilkan tiga jenis monosakarida, yaitu xylosa, arabinosa, dan glukosa. Dari ketiga monosakarida tersebut, kadar glukosa merupakan yang terendah sehingga tidak terjadi hidrolisis selulosa dalam filtrat. Hidrolisis hemiselulosa biasanya terjadi dalam
pembentukan furfural. Ikatan glikosida pada hemiselulosa sangat rentan terhadap pemutusan oleh efek katalis berupa ion hidronium (Achmadi, 1990 dalam
Nofriadi, 2009). Banyaknya hidrolisa asam bergantung pada bentuk ikatan glikosida, konsentrasi asam, suhu, dan lama reaksi. Degradasi hemiselulosa oleh asam lebih meningkat dibandingkan delignifikasi (penghilangan lignin), apabila suhu dinaikkan. Meskipun kebanyakan ikatan glikosida dalam hemiselulosa rentan terhadap hidrolisa asam, tetapi glikosida di antara asam glukoronat dengan rantai utama ternyata sangat kuat.
19
menggunakan asam klorida. Namun, asam klorida jarang digunakan karena bersifat korosif dan tingkat keasamannya lebih besar dari asam sulfat serta lebih mudah melepaskan ion H+. Ion H+ inilah yang diperlukan dalam proses hidrolisis.
G. Refluks
Refluks merupakan teknik laboratorium yang dilakukan dengan cara mendidihkan campuran cairan dalam wadah yang disambungkan dengan pendingin (kondensor) sehingga uap dari cairan akan mengembun pada kondensor dan jatuh kembali ke dalam wadah. Teknik ini digunakan untuk reaksi yang berlangsung dalam waktu lama, seperti sintesis senyawa organik (Anonim, 2013).
H. Distilasi
Distilasi atau penyulingan adalah suatu metode pemisahan bahan kimia
pengukuran serapan sinar monokromatis oleh suatu larutan berwarna pada panjang gelombang yang spesifik dengan menggunakan monokromator
prisma/kisi difraksi dan detektor tabung foto hampa. Spektrofotometer adalah alat yang digunakan untuk menganalisa suatu senyawa baik kuantitatif maupun kualitatif, dengan cara mengukur transmitan ataupun absorban suatu cuplikan sebagai fungsi dari konsentrasi. Untuk menganalisis furfural dapat digunakan spektofotometer UV-Vis dan spektofotometer IR.
1. Spektrofotometri UV-Vis
21
lebih banyak energi akan menyerap panjang gelombang yang lebih pendek. Sedangkan molekul-molekul yang memerlukan energi lebih sedikit akan menyerap panjang gelombang yang lebih panjang. Senyawa yang menyerap cahaya dalam daerah Visible (senyawa berwarna) mempunyai elektron yang lebih mudah dipromosikan daripada senyawa yang menyerap cahaya pada daerah UV (Fessenden dan Fessenden, 1982). Pengukuran sebaiknya pada panjang
gelombang dimana serapannya maksimum. Panjang gelombang ini disebut dengan panjang gelombang maksimal (λmaks). Secara teoritis λmaks furfural murni adalah
276 nm (Othmer, 1980 dalam Ardiana, 2012).
2. Spektrofotometri IR
Inti-inti atom yang terikat oleh ikatan kovalen mengalami getaran (vibrasi). Hanya vibrasi yang bersifat asimetrik atau merubah kepolaran saja yang aktif pada
inframerah karena mempunyai momen dipole. Bila molekul menyerap radiasi inframerah, energi yang diserap menyebabkan kenaikan dalam amplitudo getaran atom-atom yang terikat. Jadi, molekul ini berada dalam keadaan vibrasi
tereksitasi.
Table 3. Bilangan Gugus Fungsi Per-Variabel Bebas dari Furfural Secara Teoritis (Fessenden dan Fessenden, 1982)
No. Gugus Fungsi Daerah Serapan (cm-1) Vibrasi
23
J. Kromatografi Gas dan Spektroskopi Massa (GC-MS)
Selain menggunakan spektrofotometer, furfural juga dapat dikarakterisasi
menggunakan kromatografi. Kromatografi merupakan salah satu metode analitik untuk pemurnian atau pemisahan senyawa-senyawa organik dan anorganik sehingga senyawa tersebut dapat dianalisis dan dipelajari. Metode kromatografi adalah cara pemisahan dua atau lebih senyawa atau ion berdasarkan pada
perbedaan migrasi dan distribusi senyawa atau ion-ion tersebut di dalam dua fasa yang berbeda. Dua fasa tersebut dapat berwujud padat-cair, cair-cair, atau gas-cair. Zat terlarut di dalam fasa gerak mengalir pada suatu fasa diam. Zat terlarut yang memiliki afinitas terhadap fasa gerak yang lebih besar akan tertahan lebih lama pada fasa gerak, sedangkan zat terlarut yang afinitasnya terhadap fasa gerak kecil akan tertahan lebih lama pada fasa diam. Dengan demikian
senyawa-senyawa dapat dipisahkan komponen demi komponen akibat perbedaan migrasi di dalam fasa gerak dan fasa diam (Rohman, 2009).
secara teliti.
Pada spektro massa, bahan yang sedang diteliti ditembaki dengan berkas elektron dan secara kuantitatif mencatat hasilnya sebagai suatu spektrum fragmen ion positif. Terpisahnya fragmen-fragmen ion positif didasarkan pada massanya (lebih tepat massa dibagi muatan, tetapi kebanyakan ion bermuatan tunggal) (Fessenden dan Fessenden, 1982). Spektroskopi massa memungkinkan kita untuk
mengidentifikasi suatu senyawa yang tidak diketahui, dengan mengkalibrasikan terhadap senyawa yang sudah diketahui. Jadi spektrum massa dipakai untuk menentukan berat molekul atau rumus molekul atau mengidentifikasi senyawa dari pola fragmentasinya.
K. Penelitian Terdahulu
1. Handojo, L. Herri Susanto, dan Nurul Seto W, 1999
Melakukan penelitian tentang pemulihan lindi hitam pemasakan tandan kosong sawit (TKS) dalam pelarut organik. Dalam penelitian tersebut disimpulkan bahwa reaksi pembentukan furfural berlangsung secara seri dan dilakukan secara
25
2. Suripto Dwi Yuwono dan Herri Susanto, 2000
Melakukan penelitian tentang model Waste Utilization Value pada limbah pertanian sebagai bahan baku furfural, mereka mengatakan bahwa potensi pemanfaatan limbah pertanian sebagai sumber furfural dapat dinilai dengan menggunakan Waste Utilization Value (WUV). Tongkol jagung sebagai sumber furfural dengan potensi tertinggi setelah tandan kosong sawit (TKS).
3. A.Z. Habibie dan M.A. Angka Wijaya, 2002
Melakukan penelitian tentang pemisahan furfural dari hidrolisa pemasakan tandan kosong sawit. Pemisahan furfural dapat dilakukan dengan cara distilasi pada suhu 100 oC dan tekanan 1 atm.
4. Henny Suryani dan Maharini Rahmawati, 2006
Melakukan penelitian tentang pembuatan furfural dari bagasse dari limbah pabrik gula untuk mencari kondisi operasi yang optimum. Dari penelitian tersebut, disimbulkan bahwa kondisi optimum proses hidrolisa menjadi furfural adalah pada suhu 100oC dengan konsentrasi asam sulfat 7%. Perolehan furfural adalah 48,04% berat untuk hasil hidrolisa dan 49,241% berat setelah proses distilasi dilakukan.
5. Suharto dan Herri Susanto, 2006
6. Ganjar Andaka, 2011
Melakukan penelitian tentang hidrolisis ampas tebu menjadi furfural dengan katalisator asam sulfat. Hasil penelitian menunjukan perolehan furfural mencapai titik maksimum pada suhu 100oC sebesar 5,07% dan perolehan furfural optimum pada waktu reaksi selama 120 menit, yaitu 5,67%.
7. Rena Ardiana dan Mitarlis, 2012
27
III. METODELOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Oktober 2013 sampai Maret 2014, yang dilakukan di Laboratorium Organik dan analisis yang dilakukan di Laboratorium Biokimia Fakultas Matematika dan Ilmu Pengetahuan Alam, serta analisis di Laboratorium Biomassa Terpadu Universitas Lampung.
B. Alat dan Bahan Penelitian
Alat-alat yang digunakan pada penelitian ini adalah peralatan gelas yang biasa digunakan di dalam laboratorium organik, satu set alat distilasi dan satu set alat refluks, neraca analitik, corong pisah, biuret, hot plate magnetic stirrer, kertas saring, aluminium foil, plastik wrap, tissue, sarung tangan, label penanda, kaca arloji, serta alat bantu identifikasi senyawa furfural antara lain; Spektofotometer UV-Vis, spektrofotometer FT-IR dan GC-MS.
1%.
C. Prosedur Kerja
1. Preparasi Sampel
Sampel yang digunakan adalah Tandan Kosong Sawit (TKS), yang digunakan sebagai sumber pentosan untuk pembuatan furfural selama proses hidrolisis asam. TKS yang akan digunakan diperoleh dari perkebunan milik pribadi di Rawa Jitu, Tulang Bawang. TKS dicuci agar terbebas dari getah dan kotoran saat
pengambilan. Selanjutnya dikeringkan dan digiling sampai halus.
2. Proses Delignifikasi Sampel
Sampel A sebanyak 55 gram merupakan sampel TKS murni yang tidak melalui proses delignifikasi. Sampel B, C, dan D masing-masing sebanyak 55 gram diperoleh melalui proses delignifikasi menggunakan NaOH dengan variasi konsentrasi 1%; 3%; dan 5% (w/v). Perbandingan padatan-cairan adalah 1 gram per 20 mL. Campuran serat TKS dan NaOH direndam dengan variasi waktu, yaitu 24 dan 48 jam. Padatan dan cairan yang terbentuk dipisahkan dengan cara
29
3. Uji Kuantitatif pada Lindi
Sebanyak 1 mL lindi dimasukkan ke dalam gelas beaker dan ditambah 25 mL akuades. Larutan ditetesi KMnO4 sampai berwarna merah muda dan ditambah 5
mL H2SO4 8N. Kemudian distirrer dengan hot plate selama 5 menit sampai suhu
70oC. Selanjutnya ditambah 10 mL larutan H2C2O4 0,01N dan dipanaskan sambil
distirrer lagi selama 5 menit. Setelah pemanasan, langsung dititrasi dengan KMnO4 yang sudah distandarisasi sampai terbentuk warna merah muda.
Dilakukan perlakuan yang sama terhadap blanko tanpa penambahan lindi hitam.
Kadar lignin yang terdapat pada lindi dapat diindikasikan oleh nilai permanganat. Nilai permanganat dapat dihitung menggunakan persamaan berikut.
[ ]
Keterangan :
a : Volume larutan standar KMnO4 0,01N b : Normalitas KMnO4 yang sebenarnya (0,1 N) c : Normalitas asam oksalat
perhitungan kadar lignin pada TKS terdelignifikasi, kemungkinan masih ada lignin yang tersisa. Pada uji kuantitatif ini, dilakukan titrasi pada padatan berupa TKS yang terdelignifikasi atau yang dikenal dengan metode penentuan bilangan Kappa.
Sebanyak 5 gram TKS terdelignifikasi (sampel) dioven pada suhu 60oC selama 15 menit. Lalu didinginkan dalam desikator. Sebanyak 2 gram sampel kering
ditimbang dimasukkan ke dalam gelas beaker yang berisi 40 mL akuades dan distirrer 10 menit. Masing-masing 5 mL larutan H2SO4 4N dan KMnO4 0,1N
ditambahkan selama bersamaan sambil dihidupkan stopwatch untuk menghitung waktu. Campuran distirrer selama 10 menit. Pada menit ke-5 dilakukan
pengukuran suhu. Setelah 10 menit, stirrer dimatikan dan ditambahkan 1 mL larutan KI 0,1N. Segera dilakukan titrasi menggunakan larutan natrium tiosulfat 0,1 N sampai larutan menjadi kuning. Kemudian ditambahkan beberapa tetes indikator amilum 1% dan dititrasi lagi menggunakan larutan natrium tiosulfat sampai berubah warna menjadi bening (tidak berwarna). Dicacat volume natrium tiosulfat yang digunakan dalam titrasi. Dilakukan perlakuan yang sama pada blanko tanpa penambahan sampel.
31
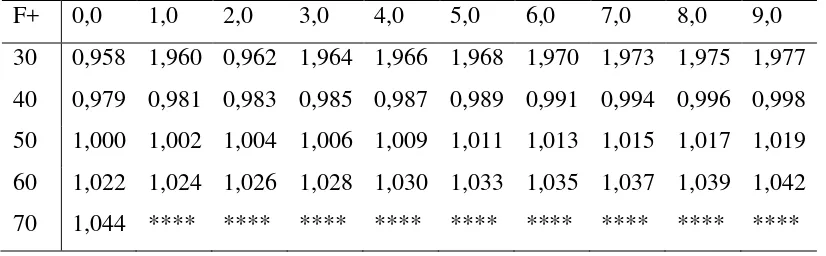
F = faktor kolerasi terhadap pemakaian permanganat (disajikan pada tabel 1) T = temperatur larutan
N = normalitas natrium tiosulfat a = volume Na2S2O4 untuk sampel
b = volume Na2S2O4 untuk blanko
W = berat sampel
Tabel 4. Faktor Kolerasi Terhadap Pemakaian Permanganat
F+ 0,0 1,0 2,0 3,0 4,0 5,0 6,0 7,0 8,0 9,0
5. Hidrolisis Asam Menggunakan H2SO4
optimum. Variasi waktu hidrolisis atau waktu pemasakan juga dilakukan (30, 45, 60, dan 90 menit) untuk mendapatkan waktu hidrolisis optimum. Setelah didapat kondisi TKS dan kondisi pemasakan optimum, maka dilakukan variasi
konsentrasi asam sulfat (0%; 1%; dan 5% (v/v)) untuk mengetahui konsentrasi asam sulfat yang optimum.
Prosedur yang dilakukan 10 gram sampel dimasukkan ke dalam labu bundar dan ditambahkan 200 mL larutan H2SO4. Labu bundar dirangkai pada alat refluks dan
dipanaskan pada suhu yang sudah ditentukan selama waktu yang sudah
ditentukan. Setelah pemanasan, filtrat dan residu dipisahkan dengan cara disaring. Filtrat yang didapat masih berupa crude furfural yang dimurnikan dengan cara ekstraksi menggunakan kloroform.
6. Pemurnian Crude Furfural
Crude furfural yang didapatkan dari proses hidrolisis dimurnikan dengan cara
ekstraksi. Crude furfural dimasukan ke corong pisah, kemudian ditambahkan 50 mL kloroform. Campuran dikocok dan klep corong pisah dibuka untuk
33
Kandungan bawah ini yang kemudian dipisahkan dan didistilasi untuk memisahkan furfural dari kloroform.
7. Pemisahan Furfural-Kloroform
Pemisahan furfural dari kloroform dengan distilasi sederhana. Distilasi dilakukan pada suhu antara 60-70oC karena kloroform memiliki titik didih yaitu 61.2oC. Distilat yang diperoleh berwarna kuning kecoklatan akan digunakan untuk menghitung rendemen furfural.
8. Analisis Furfural
Analisis yang dilakukan adalah uji warna anilin-asam asetat, volumetri (titrasi), penentuan panjang gelombang maksimum dengan spektofotometer UV-Vis, dan penetuan gugus fungsi dengan spektrofotometer FT-IR serta penentuan berat molekul menggunakan GC-MS.
a. Uji warna anilin-asam asetat
Larutan anilin-asam asetat dibuat dengan rasio 1:1. Cairan distilat diteteskan di atas kaca arloji secukupnya dan ditetesi dengan larutan anilin-asam asetat. Jika terbentuk warna kemerah-merahan maka cairan tersebut mengandung furfural.
b. Volumetri (titrasi)
Cairan distilat sebanyak 5 mL ditambah dengan akuades 5 mL dan dikocok sampai homogen. Kemudian ditambahkan 10 mL larutan KIO3 0,1N dan 5 mL
menggunakan prosedur yang sama.
Menurut Dunlop (1948), Dunlop dan Trymble (1939), untuk mengetahui besarnya yield furfural dapat dihitung dengan rumus :
∑
[ ] ∑
∑ [ ]
∑
Keterangan :
b : volume Na2S2O3 blanko
a : volume Na2S2O3 sampel
N : normalitas Natrium tiosulfat BM furfural : 96 mg/mmol
55
V. SIMPULAN DAN SARAN
A. Simpulan
Dari hasil yang diperoleh maka dapat ditarik simpulan sebagai berikut: 1. TKS dengan delignifikasi yang optimal adalah TKS yang terdelignifikasi
NaOH 5% selama 48 jam dengan jumlah lignin yang tersisa 1,03 mg per gram serbuk TKS.
2. Furfural tertinggi dihasilkan oleh TKS tanpa delignifikasi dan TKS dengan delignifikasi, pada kondisi pemasakan optimum dengan konsentrasi H2SO4
5%, suhu 100oC, dan waktu 60 menit, yaitu masing-masing 0,3132 dan 0,4932 (mg/mL) dengan masing-masing perolehan sebesar 20,32% dan 32,42%. 3. Analisis kualitatif furfural, pada uji warna dengan anilin-asetat menunjukkan
hasil positif dimana warna kuning menjadi merah, panjang gelombang
maksimal (λmaks) 273,5 nm pada analisis spektrofotometri UV-Vis, puncak ion
1. Proses pemasakan menggunakan Refluks memiliki kendala, seperti kapasitas pemasakan yang sedikit menyebabkan perolehan furfural yang dihasilkan tidak banyak. Untuk itu, diperlukan metode pemasakan lain yang dapat memproduksi furfural dalam jumlah yang besar, seperti dengan digester. 2. Konsentrasi asam sulfat yang digunakan dalam proses pemasakan TKS belum
mencapai titik optimum. Untuk itu, diperlukan variasi konsentrasi H2SO4 yang
lebih tinggi untuk mengetahui konsentrasi H2SO4 optimum untuk
menghasilkan perolehan furfural tertinggi.
3. Diperlukannya tekanan yang tinggi untuk penggunaan variasi suhu yang tinggi saat pemasakan atau hidrolisis sehingga dapat dicapai suhu optimum
pemasakan atau hidrolisis.
57
DAFTAR PUSTAKA
Alam, M. Z., Ameem, E. S., Muyibi, S. A., and Kabbashi, N. A. 2009. The factors affecting the performance of activated carbon prepared from oil palm empty fruit bunches for adsorption of phenol. Chemical engineering journal 155(1-2), 191-198.
Anonim. 2013. Http: //google.com/refluks. Diakses pada tanggal 15 Desember 2013 pukul 20:15
Ardiana, R. dan Mitarlis. 2012. Pemanfaatan Kulit Buah Siwalan (Borassus
Flabellifer L.) Sebagai Bahan Dasar Pembuatan Furfural. UNESA Journal of Chemistry Vol. 1, No. 2.
Azizin, S.M. 2010. Isolation of Hemisellulose From Surgarcane Bagasse By Alkaline Extraction. Malaysia : Universiti Teknologi Mara Selangor.
Carpita, N., and M. McCann. 2000. The Cell Wall In Biochemistry and Molecular Biology of Plants. http://www.sigmaaldrich.com/.../lysing-enzymes.html. Diakses pada tanggal 14 Mei 2013 pukul 20:32.
Dinas Perkebunan Provinsi Lampung. 2013. Statistika Kelapa Sawit Provinsi Lampung. Lampung : Dinas Perkebunan Povinsi Lampung.
Direktorat Jenderal Perkebunan. 2011. Statistika Perkelapa Sawitan Indonesia Tahun 2011, Departemen Pertanian. Jakarta : Direktorat Jenderal Perkebunan
Indonesia.
Fauzi, 2004. Kelapa Sawit. Jakarta : Penebar Swadaya.
Fessenden dan Fessenden. 1982. Kimia Organik Edisi Ketiga Jilid I. Jakarta : Penerbit Erlangga.
Gullichsen J dan H Paulapuro. 2000. Chemical Pulping. USA: TAPPI Press. Habibie, AZ, dan MA, Angkawijiya. 2002. Pemisahan Furfural dan Hidrolisa
Pemasakan Tandan Kosong Sawit. Prosiding Seminar Nasional Fundamental dan Aplikasi Teknik Kimia ITS.
Hamzah, F., Idris, A., and Shuan, T. K. 2011. Preliminary Study on Enzymatic hydrolysis of treated oil palm (Elaeis) empty fruit bunches fibre (EFB) by using
combination of cellulose and β 1-4 glucosidase. Biomass and Bioenergy 35(3),
1055-1059.
Heradewi. 2007. Isolasi Lignin dari Lindi Hitam Proses Pemasakan Organosolv Serat Tandan Kelapa Sawit (TKKS). Bogor : Fakultas Teknologi Pertanian Institut Pertanian Bogor.
Hijayanti, N. 2006. Pengolahan Tongkol Jagung sebagai Bahan Pembuatan Furfural (The Treatment of the Corn-Knob as A Raw Material for Making Furfural). Jurnal ILMU DASAR, Vol. 8 No. 1 2006 : 45-53.
Humas PTPN XIII. 2008. Limbah Kelapa Sawit Pengganti Pupuk. Http :
//www.PTPN-XIII.com.html. Diakses pada tanggal 24 April 2013 pukul 21:05 Jiang, Zhi-Hua; Audet, Andre; van Lierop, Barbara; Berry, Richard; Menegotto,
Robert. 2004. Kappa number with better repeatability and at a lower cost. 90th Annual meeting, PAPTAC. Montreal, Canada, Preprint Book C, p.111-115
Lubis, Afni A. 2007. Isolasi Lignin dari Lindi Hitam (Black Liquor) Proses Pemasakan Pulp Soda dan Pulp Sulfat (Kraft). Bogor : Fakultas Teknologi Pertanian Institut Pertanian Bogor.
Mitarlis, Ismono, Tukiran. 2011. Pengembangan Metode Sintesis Furfural Berbahan Dasar Campuran Limbah Pertanian Dalam Rangka Mewujudkan Prinsip Green Chemistry. Surabaya : Departermen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Surabaya.
59
Oktarina, Ifrilla. 2009. Pengaruh Konsentrasi Dua Jenis Bahan Pemutih terhadap Sifat Kimia dan Warna Serat Batang Pisang. Bandar Lampung : Jurusan Teknologi Hasil Pertanian Universitas Lampung.
Ong, H.K. and M. Sashikala. 2007. Identification Of Furfural Synthesized From Pentosan In Rice Husk. J. Trop. Agric. and Fd. Sc. 35(2).
Parkas, J., Brunow, B. and Knut, L. 2007. Quantitative Lignin Analysis Based On Permanganate Oxidation. BioResource 2 (2), 169-178.
Pushpamalar, V., Langford, S.J., Ahmad, M. and Lim, Y.Y. 2006. Optimization of Reaction Conditions For Preparing Carboxymethyl Cellulose From Sago Waste Carbohyd. Polym. 64: 312-318
Riansa-ngawong, W. 2011. Bioetanol and Furfural Production From Palm Press Fiber. Thesis. The Graduate School, Prince of Songkala
University.
Rohman, Abdul. 2009. Kromatografi untuk Analisis Obat. Yogyakarta : Delta Buku. Sasaki, C., Sumimoto, K., Asada, C., and Nakamura Y. 2012. Direct hydrolysis of
cellulose to glucose using ultra-high temperature and pressure steam explosion. Carbohydrate Polymers 89(1), 298-301
Simatupang, H., Nata, A. dan Netti, H. 2012. Studi Isolasi dan Rendemen Lignin Dari Tandan Kosong Kelapa Sawit (TKKS). Medan : Universitas Sumatera Utara.
Stevens, M.P. 2001. Kimia Polimer. Jakarta : Pradnya Paramita.
Suharto dan Susanto, H., 2006. Pengaruh Konsentrasi Katalis terhadap Perolehan Furfural pada Hidrolisis Tongkol Jagung. Seminar Nasional IPTEK Solusi Kemandirian Bangsa, Yogyakarta.
Syafwina, E.D. Wong, Y. Honda, T. Watanabe, and M. Kuwahara. 2002. Pretreatment of empty fruit bunch of oil palm by white-rot fungi for the utilization of its component. p. 351–356.
Witono, J. A., 2005. Produksi Furfural dan Turunannya: Alternatif Peningkatan Nilai Tambah Ampas Tebu Indonesia. Http://www.chem-is-try.org/, diakses tanggal 24 April 2013 pukul 20:19.