OPTIMALISASI PEMBENTUKAN FURFURAL DARI TANDAN KOSONG KELAPA SAWIT MENGGUNAKAN
METODE HIDROLISIS ASAM
(Skripsi)
Oleh
RHAMADYA TETA PARASTA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
ABSTRAK
OTIMALISASI PEMBENTUKAN FURFURAL DARI TANDAN KOSONG SAWIT MENGGUNAKAN METODE HIDROLISIS ASAM
Oleh
Rhamadya Teta Parasta
Pada penelitian ini telah dilakukan pembentukan dan identifikasi senyawa furfural dari Tandan Kosong Sawit (TKS) yang diperoleh dari kota Rawajitu, Lampung Tengah. Tahapan pada penelitian ini meliputi pengumpulan, preparasi sampel, hidrolisis asam, pemurnian, dan identifikasi. Hidrolisis asam dilakukan
menggunakan metode refluks, pada tahap ini dilakukan variasi suhu, konsentrasi asam, dan waktu hidrolisis. Identifikasi senyawa dilakukan menggunakan
spektrofotometri UV-Vis, IR, dan Kromatografi Gas–Spektroskopi massa (GC-MS). Hasil hidrolisis asam diperoleh kondisi optimum untuk pembentukan furfural adalah pada suhu 90oC, konsentrasi asam 15%, dan waktu hidrolisis 120 menit, diperoleh furfural dengan konsentrasi 0,368 mg/mL dan persentasi
perolehan 30,357%. Hasil analisis IR muncul spektrum pada panjang gelombang 2850 cm-1 dan 1731 cm-1 yang menunjukkan vibrasi ulur C-H dan C=O aldehid, panjang gelombang 1517 cm-1 menunjukkan vibrasi –C=C- dan 1225 cm-1 menunjukkan vibrasi –C-O-C-. Analisis GC-MS muncul puncak ion molekul di m/e 96 yang merupakan berat molekul furural. Dari data yang diperoleh ini memiliki kesamaan bila dibandingkan dengan spektrum dari furfural standar, sehingga dapat disimpulkan bahwa senyawa yang diperoleh adalah furfural.
ABSTRACT
OPTIMALIZATION OF FURFURAL FORMATION FROM OIL PALM EMPTY FRUIT BUNCHES USING ACID HYDROLYSIS METHOD
By
Rhamadya Teta Parasta
In this study, formation and identification furfural compound from oil palm empty fruit bunches, that have been obtained from Rawajitu, Lampung Tengah. The step of this study include collecting, sample preparation, acid hydrolysis, purification, and identification. Acid hydrolysis using refluks method, at this stage, the
variation of themprature, acid consentration, and hidrolisis time. Identification of compound was performed using UV-Vis spectrophotometry, IR, and Gas
Chromatography-Mass Spektroscopy (GC-MS). Acid hydrolysis result obtained conditions for the formation of furfural is at a themperature 90oC, 15% acid concentration, and hydrolysis time 120 minutes, furfural obtained with consetration of 0.368 mg/mL and the persetage yield of 30.357%. IR analysis result appear spectrum at a wavelength of 2850 cm-1 and 1731 cm-1 which shows the stretching vibration of C-H and C=O aldehide, wavelength 1517 cm-1 which show –C=C- and at wavelength 1225 cm-1 which shows –C-O-C-. GC-MS analysis of emerging molecular ion peak at m/e 96 which is the molecular weight of furfural. Data obtained from these have in common when compared with the spectrum of furfural standard, so it can be conclude that the compound obtained is furfural.
RIWAYAT HIDUP
Penulis dilahirkan di Palembang pada tanggal 24 Maret 1991, sebagai anak keempat dari Bapak Muksin dan Ibu Meilliyana Wardiaty.
Penulis menyelesaikan pendidikan Sekolah Dasar di SD Negeri 1 Langkapura Bandar Lampung pada tahun 2003, Sekolah Menengah Pertama di SMP Negeri 14 Bandar Lampung pada tahun 2006, dan Sekolah Menengah Atas di SMA Negeri 3 Bandar Lampung pada tahun 2009. Penulis diterima di Universitas Lampung, Fakultas Matematika dan Ilmu Pengetahuan Alam Jurusan Kimia pada tahun 2009 melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).
MOTO
Orang yang luar biasa tidak pernah memperhatikan
hasil, tetapi mereka hanya memikirkan dan
mengerjakan prosesnya
(Asep Hilman)
“
Orang bijak bisa lebih banyak belajar dari orang bodoh, tetapi orang
bodoh menolak belajar dari orang bijak.
(Mario Teguh)
Keberuntungan adalah sesuatu yang terjadi ketika
kesempatan bertemu dengan kesiapan.
(Thomas A. Edison)
Don’t follow your dreams
, CHASE THEM..
Dengan segala kerendahan hati
Karya kecil ini kupersembanhkan sebagai tanda
bhakti dan sayangku yang tiada tara kepada:
Ibu, Ibu, ibu, ayah, nyai dan akas
yang tak pernah putus mencurahkan cinta,
kasih sayang, motivasi, dan doa.
Kakak-kakakku
Yang selalu sabar membimbingku
Teman-Teman Seperjuangan Kimia
Seseorang yang belum kutemukan hingga kini,
yang telah khusus Tuhan ciptakan untuk
menjadi imamku
SANWACANA
Assalamualaikum Wr. Wb
Puji dan syukur penulis panjatkan kehadirat Allah SWT, karena berkat rahmat, ridho, dan karunia-Nya penulis dapat menyelesaikan skripsi ini. Shalawat dan salam tidak lupa penulis haturkan kepada Nabi Muhammad SAW sebagai suri tauladan.
Skripsi dengan judul “Optimalisasi Pembentukan Furfural dari Tandan
Kosong Sawit Menggunakan Metode Hidrolisis Asam” merupakan syarat
untuk mencapai gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Pada kesempatan ini penulis mengucapkan terima kasih dan penghargaan yang tulus kepada :
1. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T. selaku Pembimbing Utama yang telah membimbing penulis dengan sabar, memberikan banyak ilmu pengetahuan, saran, arahan, dan motivasi sehingga penulis dapat
2. Bapak Andi Setiawan, Ph.D. selaku pembimbing Kedua yang telah membimbing, memberikan petunjuk, saran, serta nasehat dalam menyelesaikan skripsi ini.
3. Ibu Prof. Dr. Tati Suhartati, M.S. selaku Pembahas yang telah banyak memberikan banyak arahan, kritik dan saran demi terselesaikannya skripsi ini.
4. Bapak Dr. Hardoko Insan Qudus, M.S. selaku Pembimbing Akademik yang telah memberi motivasi dan dukungannya.
5. Bapak Prof. Dr. Suharso, Ph.D selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
6. Bapak Dr. Eng. Surpto Dwi Yuwono, M.T. selaku Ketua Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. 7. Mba Nora, Pak Gani, Mas Nomo, Pak Man, Mba Wiwit, serta seluruh staf
pengajar dan karyawan Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
8. Ibu, ibu, ibu, ayah, nyai, dan akas atas limpahan kasih sayang yang tak pernah habis untukku, keikhlasan merawat dan menjagaku, segala nasihat dan semangat serta doa tulus yang tiada henti, dan perhatian yang takkan pernah habis demi keberhasilan penulis.
9. Ketiga Ayukku tersayang dr. Andika Okparasta, Yuanita Dwi Parasta,
seluruh keluarga besarku yang selalu memberikan motivasi, dukungan dan doa untuk keberhasilanku.
10.Patner Penelitianku, Mardiyah (09), yang selalu meberikan semangat, dukangan, selalu mengingatkan penulis ketika lalai, dan setia menjadi teman diskusi selama penulis menyelesaikan penelitian
11.Patner kerja selama di Lab. Kimia Organik, Awan (10), Purniawati (10), Bu Wid, Chintia (10), Fajri (10), atas kerja sama yang sangat baik serta bantuan, dukungan, dan motivasinya selama penelitian.
12.Sahabat-sahabat terbaikku, Delphiana, Mardiyah, Nurjannah S.Si., Resca Ridhatama, S.Si., atas segala bantuan dan motivasinya.
13.Teman-teman se-angkatan 2009, Juwita Ratna Sari, S.Si., M. Padli, Mersiana, S.Si., Rizki Yuliandari,S.Si., Sherly Nurimani, S.Si., Suparno, Ari Bowo, Dani Agus, Luh Gede, S.Si., Delphiana, Delfiana Sidabalok, Dwiyanto,S.Si., Fitriyanti, S.Si., Ignatius S. Ellen, Khoirul Umam, S.Si., Neneng Suryani, S.Si., Nurjannah, S.Si., Purna Pirdaus, Resca Ridhatama, S.Si., R. Meta Megawati, S.Si., Retno Nur Ramadhani, Rinawati, S.Si, Siska Dwi Aryani, S.Si., Tiurma N, Yahya Ariyanta, Mardiyah, Stephanie Oktiana, dan Lia Andriani, atas kebersamaannya selama ini.
14.Adik-adik tingkat 2011-2012, atas bantuan dan semangat yang diberikan kepada penulis
Akhir kata, penulis menyadari bahwa skripsi inni masih jauh dari kesempurnaan, akan tetapi sedikit harapan semoga skripsi ini dapat berguna dan bermanfaat bagi kita semua. Amin.
Bandar Lampung, Juni 2014 Penulis
DAFTAR ISI B. Tujuan Penelitian ... C. Manfaat Penelitian ...
1 3 4 II TINJAUAN PUSTAKA
A. Kelapa Sawit ... I. Spektrofotometri Inframerah (IR) ... J. Spektrofotometri UV-Vis………...….
K. Spekroskopi Masa (MS) ……….... 24 III METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian ... B. Alat dan Bahan Peneniltian ... C. Prosedur Kerja ...
1. Preparasi Bahan Baku …... 2. Hidrolisis Asam dari serbuk TKS ...
a. Variasi Suhu Pemasakan ….…..……... b. Variasi Konsentrasi Asam Sulfat …………... c. Variasi Waktu Pemasakan ..……..……... 3. Pemisahan Campuran Kloroform-Furfural ... 4. Analisis Kadar Furfural ..………..…… 5. Karakteristik Furfural ……..……….…...
25
IV HASIL dan PEMBAHASAN
A. Preparasi Sampel TKS ………....
B. Hidrolisis Asam TKS dan Uji Kuantitatif Furfural …………. 1. Penentuan Suhu Optimum ………...
2. Penentuan Konsentrasi Asam Pemasakan Optimum …...
3. Penentuan Waktu Optimum ………...
DAFTAR TABEL
Tabel Halaman
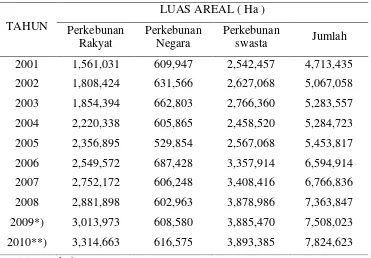
1. Luas area perkebunan kelapa sawit ... 5
2. Komposisi tandan kosong kelapa sawit …...…………... 8
3. Aplikasi furfural di dunia ... 17
4. Karakteristik frekuensi uluran beberapa gugus molekul ... 23
DAFTAR GAMBAR
Gambar Halaman
1.Peta penyebaran lahan kelapa sawit di Lampung ... 6
2.Grafik jumlah TKS tahun 2000-2009 ... 7
3.Struktur senyawa selulosa ………..………... 9
4.Struktur senyawa hemiselulosa ………...………….…... 12
5.Struktur senyawa lignin …………...………... 13
6.Struktur senyawa furfural …………..………... 16
7.Rangkaian alat distilasi uap ………... ... 19
8.Komponen instrumentasi spektrofotometer inframerah ... 22
9.Serat tandan kosong sawit (TKS) ... 30
10.Serbuk tandan kosong sawit (TKS) ... 31
11.Grafik pengaruh suhu terhadap perolehan furfural ... 32
12.Grafik pengaruh konsentrasi asam terhadap perolehan furfural... 33
13.Grafik pengaruh waktu pemasakan terhadap perolehan furfural .... 34
14.Analisis uji anilin-asetat (1:1) terhadap remdemen ... 36
15.Spektrum Uv-Vis (a) rendemen TKS asam sulfat 15%, (b) furfural standar ... 37
16.Spektrum FT-IR (a) furfural standar;dan (b) furfural TKS... 39
17.Hasil analisis kualitatif GC-MS furfural standar, dan ... 39
18.Hasil analisis kualitatif GC-MS furfural hasil hidrolisis TKS ... 40
19.Spektra fragmentasi GC-MS (a) Furfural standar, dan (b) furfural hasil hidrolisis TKS... 40
1
I. PENDAHULUAN
A. Latar Belakang
Dewasa ini pertanian dan perkebunan Indonesia semakin meluas dan
meningkat, seiring dengan besarnya devisa yang dihasilkan dari hasil pertanian dan perkebuanan. Salah satunya berasal dari perkebunan kelapa sawit. Salah satu daerah pemasok kelapa sawit adalah provinsi Lampung. Pada tahun 2006 luas areal tanaman kelapa sawit sekitar 75.150 Ha, tersebar di Kabupaten Tulang Bawang(BPS Indonesia, 2010). Tanaman kelapa sawit digunakan untuk berbagai manfaat, terutama untuk minyak makan, minyak industri, maupun bahan bakar (biodiesel) .
Semakin meluasnya perkebuanan kelapa sawit akan semakin meningkat pula limbah cair maupun limbah padat yang dihasilkan. Satu ton tandan buah segar, 42% nya merupakan limbah bentuk tandan kosong sebanyak 0,23 ton (23%), serat dan cangkang biji yang masing – masing 0,135 ton (13,5%) dan 0,055 ton (5,5%) (Darnoko, 1992).
2
dihasilkan dibakar untuk bahan bakar, sebagai pupuk, atau bahan pembuat etanol dan pulp. Upaya pemanfaatan TKS yang mulai diminati orang adalah sebagai bahan baku pembuatan furfural. Furfural digunakan pada beberapa industri seperti pada pengolahan minyak, pembuatan nilon, pembuatan resin, dan farmasi, sedangkan furfural masih diimpor dari negara lain.
Furfural pertama kali diisolasi pada tahun 1821 oleh Dobereiner, dengan mengubah asam formiat yang diperoleh dari reaksi antara gula, asam sulfat, dan mangan dioksida menjadi furfural. Selanjutnya, Emmeti mengganti asam formiat dengan bahan baku tumbuhan yang mengandung pentosa untuk membuat furfural. Pada penelitian Yuwono (2000), kadar furfural yang terdapat dalam limbah-limbah pertanian yang diperoleh melalui hidrolisis menggunakan asam sulfat, untuk 10 g sekam padi diperoleh furfural sebanyak 3,27 g/L; 20 g tongkol jagung diperoleh 5,87 g/L; dan 20 g TKS furfural yang diperoleh sebanyak 4,57 g/L.
Handojo dkk. (1999) melakukan penelitian tentang pemulihan lindi hitam pemasakan TKS dalam pelarut organic, penelitian tersebut menyimpulkan bahwa reaksi pembentukan furfural berlangsung secara seri dan dilakukan secara enzimatik atau menggunakan katalis H2SO4. Habibie dan Angkawijaya
(2002) melakukan pemisahan furfural dari hidrolisis pemasakan TKS.
3
Berdasarkan penelitian Wankasi dan Naidoo (2012), senyawa furfural ini dapat diperoleh dengan cara menghidrolisis pentosan yang terdapat dalam buah maupun limbah pertanian seperta tongkol jagung dan sekam padi
menggunakan asam yang dilanjutkan dengan pemanasan. Pentosan merupakan salah satu senyawa penyusun hemiselulosa, yang terdiri dari 5 atom karbon. Hemiselulosa adalah polimer polisakarida heterogen tersusun dari pentosan (C5H8O4) dan heksosan (C6H10O5).
Pada penelitian ini untuk memperoleh furfural dilakukan melalui reaksi hidrolisis asam menggunakan asam sulfat, hemiselulosa akan dihidrolisis menjadi pentosan dan pentosa. kemudian pentosa didehidrasi menghasilkan furfural. Furfural yang dihasilkan dimurnikan menggunakan distilasi
sederhana. Hasil yang furfural diperoleh diuji kadarnya menggunakan metode titrasi dengan larutan standar 0,1 N natrium tiosulfat (Na2S2O3) sebagai
pentiternya. Karakterisasi furfural dilakukan menggunakan Spektrofotometer IR, UV-Vis, Spektroskopi GC-MS.
B. Tujuan Penelitian
Tujuan dilakukannya penelitian ini adalah :
1. Mengisolasi furfural dari TKS dengan menghidrolisis hemiselulosa menggunakan asam sulfat melalui metode hidrolisis asam.
4
3. Karakterisasi furfural yang diperoleh.
C. Manfaat Penelitian
5
II. TINJAUAN PUSTAKA
A. Kelapa Sawit
Indonesia merupakan negara yang kaya akan hasil perkebunannya. Salah satu perkebunan yang terdapat di Indonesia adalah kelapa sawit. Indonesia memiliki perkebunan kelapa sawit terluas kedua setelah Malaysia . Berdasarkan
Direktorat Jendral Perkebunan luas area perkebunan kelapa sawit di Indonesia hingga tahun 2010 disajikan pada Tabel 1.
Tabel 1. Luas area perkebunan kelapa sawit
6
Sekitar 440.312 Ha di provinsi Lampung merupakan lahan kering yang sebagian besar dimanfaatkan untuk usaha tani perkebunan seperti lada, kopi, kakao, karet dan kelapa sawit. Pada tahun 2006 luas areal tanaman kelapa sawit sekitar 75.150 Ha, tersebar di Kabupaten Tulang Bawang, Lampung.
Penyebaran perkebunan kelapa sawit di Lampung disajikan pada Gambar 1. Pengembangan produksi kelapa sawit diarahkan pada perluasan areal
pertanaman, rehabilitasi dan intensifikasi. Usaha tani kelapa sawit di Lampung dilakukan oleh perusahaan perkebunan
Gambar 1. Peta penyebaran lahan kelapa sawit di Lampung (Dirjen Perkebunan, 2012)
7
sawit kasar sebanyak 0,21 ton (21 %) , minyak inti sawit sebanyak 0,05 ton (5%) dan sisanya merupakan limbah dalam bentuk tandan kosong sebanyak 0,23 ton (23%), serat dan cangkang biji yang masing – masing, 0,135 ton (13,5%) dan 0,055 ton (5,5%) (Darnoko, 1992).
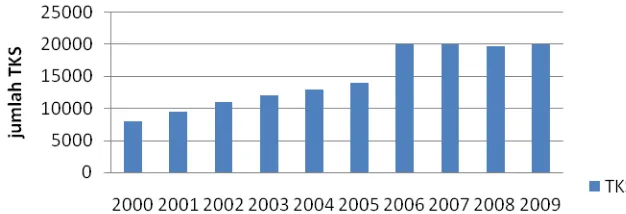
Berdasarkan data Dirjenbun, potensi limbah TKS sangat besar, seperti yang ditunjukkan pada Gambar 2.
Gambar 2. Grafik jumlah TKS tahun 2000-2009
Tandan kelapa sawit merupakan limbah utama berligniselulosa yang belum termanfaatkan secara optimal dari industri pengolahan kelapa sawit. Selama ini pengolahan TKS oleh PKS masih sangat terbatas yaitu dibakar dalam
8
Tabel 2. Komposisi tandan kosong sawit (TKS)
B. Selulosa
Selulosa adalah polimer tak bercabang dari glukosa yang dihubungkan melalui ikatan beta 1,4 atau 1,4-β-glukosida. Selulosa merupakan jenis polisakarida yang paling melimpah pada hampir setiap struktur tanaman. Kandungan selulosa kayu berkisar 48 – 50%, pada bagas berkisar antara 50 – 55% dan pada tandan kelapa sawit sekitar 45%. Selulosa dapat dihidrolisis dengan asam kuat maupun dengan enzim selulosa. Selain itu juga bisa dihidrolisis oleh mikroba seperti bakteri dan kapang. Hidrolisis sempurna akan menghasilkan glukosa dan hidrolisis tidak sempurna menghasilkan disakarida berupa
selobiosa (Winarno, 1980). Hasil hidrolisis ini dapat dikonversi menghasilkan etanol dan asam asetat. Selulosa adalah salah satu komponen utama dari
ligniselulosa yang terdiri dari unit monomer D-glukosa yang terikat pada ikatan Komposisi TKS
Dasar Kering (%)
9
1,4-glikosidik (Anindyawati,2009). Adapun struktur selulosa disajikan pada Gambar 3.
Gambar 3. Struktur senyawa selulosa
Sumber utama selulosa ialah kayu, umumnya kayu mengandung sekitar 50% selulosa, bersama dengan penyusun lainnya, seperti lignin. Pemisahan selulosa dari kayu melibatkan pencernaan kayu dengan larutan belerang dioksida dan hidrogen sulfit (bisulfit) dalam air pada proses sulfit, atau larutan natrium Hidroksida dan natrium sulfida dalam air pada proses sulfat (proses Kraft). Pada kedua proses ini lignin dilarutkan sehingga diperoleh selulosa. Sumber lain selulosa ialah kapas yang hampir seluruhnya memang selulosa. Ekstraksi dilakukan dengan mereaksikannya dengan larutan natrium hidroksida di bawah tekanan, yang kemudian dilanjutkan dengan pengelantangan dengan gas klor atau kalsium hipoklorit (Cowd, 1991).
10
dan Susilowati, 2010). Selulosa berperan besar dalam memberikan kekuatan tarik sedangkan lignin memberi kekuatan tekan dan mencegah pelipatan mikrofibril. Selulosa dan lignin diikat dengan hemiselulosa. Gugus fungsional dari gugus selulosa adalah gugus hidroksil. Gugus hidroksil selulosa
menyebabkan permukaan selulosa menjadi hidrofilik. Struktur rantai selulosa distabilkan oleh ikatan hidrogen yang kuat di sepanjang rantai. Di dalam selulosa alami dari tanaman, rantai selulosa diikat bersama-sama membentuk mikrofibril yang sangat terkristal (highly cristalline) dimana setiap rantai selulosa diikat bersama-sama oleh ikatan hidrogen (Dewi, 2011).
Ditinjau dari strukturnya, dapat saja diharapkan selulosa mempunyai kelarutan yang besar dalam air, karena banyak kandungan gugus hidroksil yang dapat membentuk ikatan hidrogen dengan air (interaksi yang tinggi antara pelarut-terlarut). Akan tetapi kenyataannya tidak demikian, dan selulosa bukan hanya tak larut dalam air tetapi juga dalam pelarut lain. Penyebabnya ialah kekakuan rantai dan tingginya gaya antar-rantai akibat ikatan hidrogen antar gugus hidroksil yang berdekatan. Faktor ini dipandang menjadi penyebab kekristalan yang tinggi dari serat selulosa (Cowd, 1991).
C. Hemiselulosa
Hemiselulosa adalah polimer polisakarida heterogen tersusun dari pentosan (C5H8O4) dan heksosan (C6H10O5). Hemiselulosa pada kayu berkisar antara
11
terikat dapat berinteraksi dengan komponen adsorbat. Adanya gugus OH, pada selulosa dan hemiselulosa menyebabkan terjadinya sifat polar pada adsorben tersebut. Dengan demikian selulosa dan hemiselulosa lebih kuat menjerap zat yang bersifat polar dari pada zat yang kurang polar (Sukarta, 2008).
Hemiselulosa bersifat non-kristalin dan tidak bersifat serat, mudah
mengembang, karena itu hemiselulosa sangat berpengaruh terhadap bentuknya jalinan antara serat pada saat pembentukan lembaran, lebih mudah larut dalam pelarut alkali dan lebih mudah dihidrolisis dengan asam. Perbedaan
12
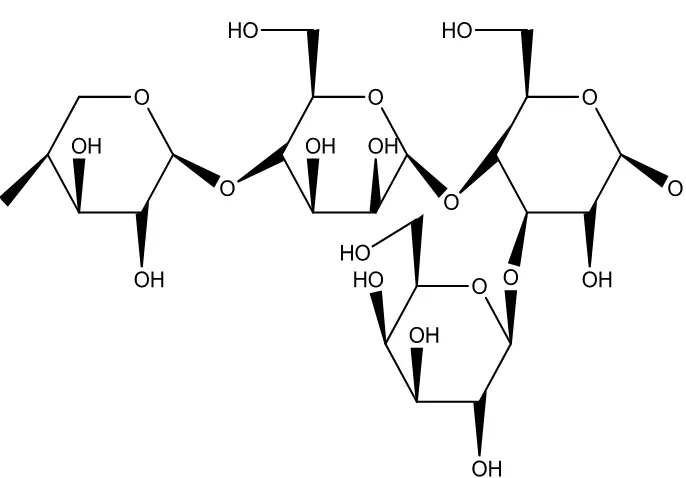
Gambar 4. Struktur senyawa hemiselulosa (-Xylosa-β
(1,4)-Mannosa-β(1,4)-Glukosa-α(1,3)-Galaktosa-)
D. Lignin
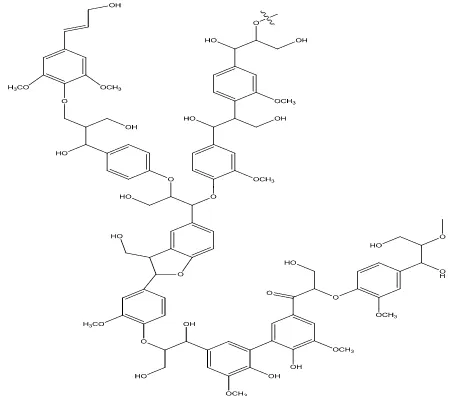
Lignin, suatu konstituen utama kayu, merupakan polimer fenol yang rumit yang mempunyai kemiripan superfisial dengan damar-damar fenol sintesis. Kayu hampir seluruhnya terdiri dari tiga bahan: polisakarida, selulosa dan hemiselulosa, dan lignin. Sebanyak 25- 30% dari kayu adalah lignin, lignin merupakan polimer yang sangat melimpah yang mesti mencapai potensinya berkaitan dengan aplikasi-aplikasi polimer. Saat ini sebagian besar lignin yang diproduksi dalam operasi-operasi pembuburan kayu dibakar sebgai bahan bakar pada tempat pembuburan. Struktur lignin bervariasi menurut sumbernya., tetapi suatu pendekatan dari segmen lignin kayu lunak mengilustasikan
13
Gambar 5. Struktur senyawa lignin (Gregory, 2007)
E. Pemanfaatan TKS
Limbah terbanyak dari produksi kelapa sawit adalah TKS , 23% dari satu ton tandan segar kelapa sawit. Limbah TKS yang ada dimanfaatkan sebagai alternatif pupuk organik yang juga akan memberikan manfaat lain dari sisi ekonomi. Beberapa alternatif pemanfaatan TKS yang dapat dilakukan sebagai berikut :
1. Pupuk Kompos
14
2. Pupuk Kalium
TKS sebagai limbah padat dapat dibakar dan akan menghasilkan abu
tandan. Abu tandan tersebut ternyata memiliki kandungan 30-40% K2O, 7%
P2O5, 9% CaO, dan 3% MgO. Selain itu juga mengandung unsur hara mikro
yaitu 1.200 ppm Fe, 100 ppm Mn, 400 ppm Zn, dan 100 ppm Cu. Sebagai gambaran umum bahwa pabrik yang mengolah kelapa sawit dengan kapasitas 1200 ton TBS per hari akan menghasilkan abu tandan sebesar 10,8% per hari. Setara dengan 5,8 ton KCL; 2,2 ton kiersit; dan 0,7ton TSP. dengan penambahan polimer tertentu pada abu tandan dapat dibuat pupuk butiran berkadar K2O 30-38% dengan pH 8 – 9.
3. Bahan Serat
TKS juga menghasilkan serat kuat yang dapat digunakan untuk berbagai hal, diantaranya serat berkaret sebagai bahan pengisi jok mobil dan matras, polipot (pot kecil), papan ukuran kecil dan bahan pengepak industri.
4. Papan partikel
Pemanfaatan TKS paling potensial adalah untuk pembuatan papan partikel. Tandan kelapa sawit memiliki kadar selulosa tinggi, yaitu 67,88%
15
kadar air 73%, minyak 9%, dan kotoran sehingga perlu dipres. Setelah rajangan dipres menggunakan mesin kempa tipe ulir, kadar air dan kadar minyak berkurang menjadi 36% dan 7%. Proses belum berakhir karena TKS perlu dijemur untuk menurunkan kadar air hingga 10%. Dalam pembuatan papan dibutuhkan perekat, seperti 8% lateks, 10% lem kanji, atau 12% polivinil akrilik.
5. Pulp
Pulp atau bubur kertas merupakan serat berwarna putih yang diperoleh melalui proses penyisihan lignin dari biomassa. (Jalaluddin, 2005). Pulp dapat diolah dengan lebih lanjut menjadi kertas, rayon, selulosa asetat dan turunan selulosa yang lain. Sebagai bahan baku pulp dipakai bahan baku jerami dan merang dan meningkat menjadi bahan baku bambu, ampas, tebu, pohon kapas,serat dan jenis rumput – rumputan.
6. Furfural
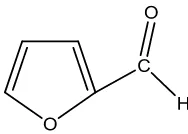
Furfural (C5H4O2) atau sering disebut dengan 2-furankarboksaldehid,
16
Gambar 6. Struktur senyawa furfural
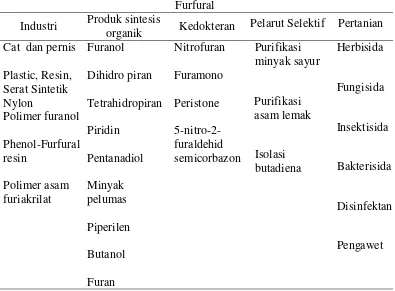
Furfural memiliki aplikasi yang cukup luas terutama untuk mensintesis senyawa-senyawa turunannya. Di dunia hanya 13% saja yang langsung menggunakan furfural sebagai aplikasi, selebihnya disintesis menjadi
produk turunannya. Tabel 3 menunjukan beberapa aplikasi furfural di dunia. Selain itu furfural juga memiliki beberapa manfaat antara lain sebagai berikut :
• Bahan baku pada pembuatan resin, terutama jenis fenol aldehid untuk pembuatan plastik.
• Pelarut selektif untuk memisahkan senyawa dalam minyak petroleum, minyak gas, bahan baker diesel, minyak nabati, dll.
• Bahan dasar pembuatan turun-turunan furan pada industri pabrik kimia (furil alkohol, tetrafuril alkohol, tetrahidro furan)
• Berguna untuk destilasi ekstraktif/ penyaringan butadiena dan 4 karbon lain pada industri karet sintetis.
17
Furfural dihasilkan dari biomassa lewat dua tahap reaksi, yaitu hidrolisis dan dehidrasi. Untuk itu digunakan bantuan katalis asam, misalnya: asam sulfat, dan lain-lain. Secara komersial, pembuatan Furfural dapat
berlangsung dalam siklus batch maupun kontinyu.
Reaksi utama pembuatan Furfural adalah sebagai berikut :
Hidrolisis pentosan menjadi pentosa :
(C5H8O4)n + n H2O asam n C5H10O5 ………..( 1 )
Dehidrasi pentosa membentuk Furfural :
n C5H10O5 asam n C5H4O2 + 3 nH2O ………..( 2 )
Tabel 3. Aplikasi furfural di dunia
Furfural Industri Produk sintesis
18
Saat memproduksi furfural juga terdapat produk samping yang dihasilkan. Jenis hasil samping tersebut dapat berupa glukosa, asam asetat, atau panas. Jenis hasil samping tersebut tergantung pada kondisi operasi yang digunakan serta cara pemisahan yang dilakukan untuk setiap produk.
F. Refluks
Refluks merupakan teknik laboratorium yang dilakukan dengan cara mendidihkan campuran cairan dalam wadah yang disambungkan dengan pendingin (kondensor) sehingga uap dari cairan akan mengembun pada kondensor dan jatuh kembali ke dalam wadah. Teknik ini digunakan untuk reaksi yang berlangsung dalam waktu lama, seperti sintesis senyawa organik (Fieser, 1957).
G. Distilasi Uap
Distilasi atau penyulingan adalah suatu metode pemisahan bahan kimia
berdasarkan perbedaan kecepatan atau kemudahan menguap (volatilitas) suatu bahan. Dalam penyulingan, campuran zat dididihkan sampai menguap dan uap ini kemudian didinginkan kembali ke dalam bentuk cairan. Zat yang memiliki titik didih lebih rendah akan menguap lebih dulu (Choi and Hong, 1999; Pudjaatmaka dan Qodratillah, 2004).
Distilasi uap adalah istilah yang secara umum digunakan untuk distilasi campuran air dengan senyawa yang tidak larut dalam air, dengan cara
19
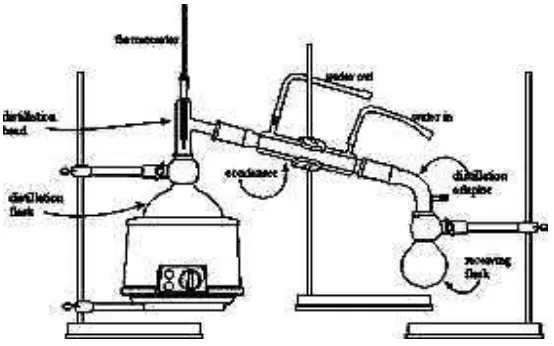
berubah menjadi uap pada temperatur yang lebih rendah dari pada dengan pemanasan langsung. Untuk distilasi uap, labu yang berisi senyawa yang akan dimurnikan dihubungkan dengan labu pembangkit uap seperti terlihat pada Gambar 7.
Gambar 7. Rangkaian alat destilasi uap
Uap air yang dialirkan ke dalam labu yang berisi senyawa yang akan dimurnikan, dimaksudkan untuk menurunkan titik didih senyawa tersebut, karena titik didih suatu campuran lebih rendah dari pada titik didih komponen-komponennya (Anonym, 2013).
H.Hidrolisis Asam
20
menjadi pentosa dan dilanjutkan degan reaksi kedua yaitu dehidrasi pentosa membentuk furfural.
(C5H8O4)n + n H2O asam nC5H10O5 (1)
nC5H10O5 asam nC5H4O2 + 3 n H2O (2)
pada proses hidrolisis, pentosa merupakan produk antara dan tidak semuanya akan menjadi furfural. Sehingga pada akhir hidrolisis, dalam hidrolisat juga dapat terkandung senyawa organik lainnya seperti metanol (Brownlee, 1948)
Pada proses hidrolisis hemiselulosa, pentosan mengalami dekomposisi menjadi pentose. Selanjutnya pentose terdehidrasi menjadi furfural. Hidrolisis
hemiselulosa dapat dilakukan sacara enzimatik atau dengan penggunaan katalis asam (Zeitsch, 1990). Namun proses yang umum dilakukan dalam produksi furfural adalah hidrolisis dengan asam.
21
Asam sulfat lebih sering digunakan sebagai katalis pada industry furfural. Karena sam sulfat merupakan asam kuat yang tidak mudah menguap, sehingga kontak dengan partikel bahan baku akan lebih lama (Krik dan Othmer, 1969). Penggunaan asam sulfat cukup efektif untuk menghilangkan hemiselulosa tanpa merusak selulosanya. Jumlah asam sulfat yang sering digunakan sekitar 2-4% dari berat bahan baku. Jumlah ini dapat menutupi 1% dari seluruh permukaan paktikel bahan baku (Medeiros, 1985).
Pembentukan furfural juga dapat dilakukan dengan menggunakan katalis asam klorida (HCl). Tetapi HCl jarang sekali digunakan karena mudah menguap dan sangat korosif. Penggunaan asam klorida sebagai katalis memberi konversi hemiselulosa lebih baik dibandingkan dengan asam sulfat (Fadjarwaty dan Susanto, 2000). Hal ini dikarenakan HCl mempunyai tingkat keasaman lebih besar dibanding H2SO4 dan lebih mudah melepas ion H+. Ion H+ inilah yang
diperlukan dalam prosses hidrolisis. Proses hidrolisis dengan katalis asam yang selama ini telah dilakukan menghasilkan hidrolisat dengan kandungan furfural sekitar 8-10g/L. pada konsentrasi ini, furfural dari hidrolisat dapat dipisahkan dengan distilasi azeotrop menjadi dua lapisan yaitu lapisan air dan lapisan furfural. Untuk mendapatkan furfural murni dilakukan dengan distilasi vakum terhadap lapisan kaya furfural
I. Spektrofotometri (IR)
22
dkk, 1994). Teknik spektroskopi dapat digunakan untuk mengidentifikasi struktur suatu senyawa dan mempelajari karakteristik ikatan dari suatu
senyawa tersebut karena senyawa akan menyerap energi cahaya pada panjang gelombang tertentu (Fessenden, 1999). Metode spektroskopi yang dipakai pada penelitian ini adalah spektroskopi inframerah (IR). Berikut adalah gambar instrumentasi inframerah yang disajikan pada Gambar 8.
Gambar 8. Komponen instrumentasi spektrofotometer inframerah
Pada spektroskopi inframerah (IR), senyawa organik akan menyerap berbagai frekuensi radiasi elektromagnetik inframerah. Radiasi yang terserap
menyebabkan molekul dari senyawa tervibrasi dan energi vibrasi yang timbul diukur aleh detektor, ssehingga energi vibrasi dari gugus fungsi tertentu akan menghasilkan frekuensi yang spesifik. (Supriyanto, 1999).
Pada pengukuran senyawa organik, lazimnya digunakan daerah 650-4000 cm-1. Daerah di bawah frekuensi 650 cm-1 dinamakan daerah inframerah jauh dan daerah di atas frekuensi 4000 cm-1 dinamakan inframerah dekat (Sudjadi, 1983). Daerah antara 1400-4000 cm-1 merupakan daerah khusus yang berguna untuk identifikasi gugus fungsional. Daerah ini menunjukkan absorpsi yang
23
disebabkan oleh vibrasi uluran. Daerah antara 1400-700 cm-1 (daerah sidik jari) seringkali sangat rumit karena menunjukkan absorpsi yang disebabkan oleh vibrasi uluran dan tekukan (Fessenden, 1999). Karakteristik frekuensi uluran beberapa gugus molekul ditunjukkan pada Tabel 4.
Tabel 4. Karakteristik frekuensi uluran beberapa gugus molekul
Gugus Serapan (cm-1) Keterangan
C=O 1760-1665 Aldehi, keton, ester C – O – C 1200-1100 Eter
Sumber : Banwell, 1994.
J. Spektroskopi UV-Vis
Spektroskopi UV-Vis umumnya digunakan untuk melihat panjang gelombang maksimum (λmaks) yang diserap oleh suatu senyawa. Spektrum absorpsi dalam daerah-daerah ultraviolet dan sinar tampak umumnya terdiri dari satu atau beberapa pita absorpsi. Semua molekul dapat menyerap radiasi dalam daerah UV-Vis karena mengandung elektron yang dipakai bersama maupun yang tidak dapat dieksitasikan ke tingkat energi yang lebih tinggi. Secara teoritis
24
K. Spektroskopi Masa (MS)
Spektrometer massa adalah suatu instrumen yang dapat menyeleksi molekul-molekul gas bermuatan berdasarkan massa atau beratnya. Spektrum massa memberikan informasi berat molekul yang berguna untuk mengidentifikasi rumus bangun molekul bersama spektrum IR dan NMR. Metode spektroskopi massa didasari pada pengubahan komponen sampel menjadi ion-ion dan misahkannya berdasarkan perbandingan massa terhadap muatan (m/e). Untuk memperoleh spektrum massa, senyawa yang terdapat didalam sampel diubah mendadi ion-ion yang bergerak cepat yang dipisahkan berdasarkan
perbandingan massa dan muatan (Hendayana, 1994).
25
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian dilakukan pada bulan September 2013 sampai bulan Maret 2014 yang dilakukan di Laboratorium Kimia Organik Fakultas MIPA Unila, dan analisis gugus fungsi dilakukan di Laboratorium Biomasa UNILA, analisis spektrofotometri UV-Vis dilakukan di laboratorium Biokimia Fakultas MIPA Unila, dan analisis Gas Kromatografi-Masa Spektrokopi di Universitas Gajah Mada.
B. Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini adalah peralatan gelas yang biasa digunakan di dalam laboratorium kimia organik, satu set alat distilasi, satu set alat refluks, neraca analitik, magnetic stirer, corong pemisah, biuret,
aluminium foil, plastik wrap, tissue, kapas, sarung tangan, label penanda, dan alat bantu identifikasi senyawa furfural antara lain spektrosfotometri
26
bromat/bromida (KBrO3/KBr) 0,05 M, kalium iodida (KI) 10% (0,05M),
natrium tiosulfat (Na2S2O3) 0,1 N, dan furfural standar
C. Prosedur Kerja
1. Preparasi Bahan Baku
Bahan baku yang digunakan adalah TKS yang digunakan sebagai sumber pentosa dalam pembentukan furfural pada tahap hidrolisis. Sampel TKS didapatkan dari perkebunan sawit pribadi yang ada di Propinsi Lampung, tepatnya di kota Rawajitu, Lampung Tengah. Sebelum digunakan, TKS dicuci, dikeringkan kemudian dihaluskan.
2. Hidrolisi asam dari serbuk tandan kosong sawit
Bahan dasar TKS yang telah berbentuk serbuk dikeringkan menggunakan oven hingga kandung air pada tandan 10%. Sebanyak 10 g sampel dimasukkan kedalam labu bundar 500 mL, bersamaan dengan 250 mL asam sulfat (H2SO4)
27
suhu pemasakan, variasi konsentrasi asam sulfat sebagai katalis, dan variasi waktu pemasakan.
a. Variasi suhu Pemasakan
Serbuk TKS sebanyak 10 g dimasukkan dalam labu bundar 500 mL, kemudian ditambah 250 mL asam sulfat 10%, lalu direfluks dengan variasi suhu 80, 90, 100, dan 105oC selama 60 menit. Setelah waktu hidrolisis tercapai proses pemasakan dihentikan, kemudian hidrolisat disaring dan dihitung kadar furfuralnya menggunakan titrasi, sehingga suhu optimum dapat diketahui untuk digunakan pada hidrolisis asam variasi konsentrasi asam sulfat.
b. Variasi konsentrasi asam sulfat
10 g serbuk TKS dimasukkan dalam labu bundar 500 mL, kemudian ditambah 250 mL asam sulfat dengan variasi 5, 8, 10, dan 15%, lalu direfluks dengan suhu optimum yang telah diketahui selama 60 menit. Setelah waktu hidrolisis tercapai proses pemasakan dihentikan, kemudian hidrolisat disaring dan dihitung kadar furfuralnya menggunakan titrasi, sehingga konsentrasi asam sulfat optimum dapat diketahui untuk digunakan pada hidrolisis asam variasi waktu.
c. Variasi waktu pemasakan
28
diketahui, lalu direfluks dengan variasi waktu 30, 60, 90, dan 120 menit pada suhu optimum yang telah diketahui. Setelah waktu hidrolisis tercapai proses pemasakan dihentikan, kemudian hidrolisat disaring dan dihitung kadar furfuralnya menggunakan titrasi, sehingga waktu optimum dapat diketahui.
3. Pemisahan Campuran kloroform-furfural
Hidrolisat yang diperoleh ditambah dengan 50 mL klorofom, sehingga akan menghasilkan dua lapisan, lapisan asam sulfat dan air di bagian atas dan lapisan kloroform-furfural di bagian bawah. Lapisan dipisahkan dengan
menggunakan corong pisah. Lapisan kloroform dan furfural dipisahkan dengan distilasi pada suhu 70oC, sehingga akan didapat furfural kasar. Furfural dapat dimurnikan dengan menggunakan evaporator pada suhu 100oC
4. Analisis Kadar furfural
Untuk mengetahui kadar furfural, 5 mL hidrolisat hasil pemasakan
dimasukkan ke dalam Erlenmeyer, kemudian ditambahkan 5 ml asam sulfat 4 N dan 5 mL larutan kalium bromat/bromida (KBrO3/KBr) 0,05 M, lalu
ditutup dan didiamkan dalam lemari gelap 30 menit. Kemudian ditambahkan 10 mL kalium iodida (KI) 5% (0,05M) dan dititrasi dengan standar 0,1 N natrium tiosulfat (Na2S2O3). Sebagai pembanding, dibuat blanko tanpa
29
Menurut Dunlop (1948), untuk mengetahui besarnya yield furfural dapat dihitung dengan rumus :
Konsentsari Furfural = jumlah furfural dalam filtrat/ volume sample Keterangan :
b : volume Na2S2O3 blanko
a : volume Na2S2O3 sampel
Fp : factor pengenceran
5. Karakterisasi furfural
Furfural yang diperoleh dikarakterisasi menggunakan Spektrofotometer IR dan UV-Vis, dan Gas Chromatografi- Masa Spektroskopi (GC-MS) . Pada
Spektrofotometer IR dapat diketahui struktur senyawa furfural dan
42
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan pembahasan hasil penelitian, maka dapat ditarik simpulan sebagai berikut :
1. Pada penelitian ini telah berhasil diisolasi dan diidentifikasi senyawa furfural dari hidrolisis TKS
2. Kondisis optimum produksi furfural dari TKS adalah pada suhu 90oC, konsentrasi katalis 15% ,dan waktu 2 jam, dengan konsentrasi furfural 0,368 mg/mL, dengan perolehan kadar 30,357%.
3. Hasil analisis dengan uji anilin-asetat adanya perubahan warna pada furfural hasil hidrolisis dari kuning menjadi merah, analisis dengan
spektrofotometri UV-Vis furfural muncul puncak pada panjang gelombang maksimal (λmaks) 273 nm, analisis mengunakan spektrofotometri FT-IR munculnya serapan pada panjang gelombang 2850,27 cm-1 dan 1731,02 cm-1 yang menunjukan vibrasi ulur C-H dan C=O aldehid, 1517,81 cm-1
43
B. Saran
Adapun saran terhadap penelitian selanjutnya adalah sebagai berikut :
1. Diperlukannya variasi lebih lanjut untuk konsentasi asam dan waktu hidrolisis TKS dengan asam.
2. Perlunya dilakukan peninjauan parameter lain yang belum dilakukan seperti pengaruh lignin terhadap perolehan furfural dan perbandingan serbuk TKS dengan cairan pemasak.
44
DAFTAR PUSTAKA
Anindyawati, Trisanti. 2009. Prospek Enzim Dan Limbah Ligniselulosa Untuk produksi Bioetanol. Bogor: LIPI.
Anwar, C., B. Purwono., H.D. Pranowo, dan T.D.Wahyuningsih. 1994. Pengantar Praktikum Kimia Organik. Penerbit UGM. Yogyakarta. 270 hlm.
Ardiana, Rena dan Mitarlis. 2012. Pemanfaatan Kulit Buah Siwalan (Borassus Flabellifer L.) Sebagai Bahan Dasar Pembuatan Furfural.UNESA Journal of Chemistry. 1 (2).
Aryafatta. Http: //Aryafatta.com/mengolah-limbah-sawit-jadi-bioetanol. Diakses pada tanggal 25 April 2013 pukul 21:43.
Banwell, Colin N., dan E.M. McCash. 1994. Fundamental of Molecular Spectroscopy. Mc Graw-Hill Book Company. London.
Brownlee, HJ. 1948. Industrial Development Of Furfural. Industry and engineering Chemistry. Februari
Choi, J. I and W.H. Hong. 1999. Recovery of lactic acid by batch distillation with chemical reactions using ion exchange resin. J. Chem. Eng. 32(184-189).
Cowd, M.A. 1991. Kimia Polimer. Bandung : Penerbit ITB
Darnoko. 1992. Pengaruh Konsentrasi Asam, Suhu, dan Waktu terhadap Hidrolisis Hemiselulose tandan Kosong Kelapa Sawit. Menara Perkebunan.
Dian Anggraini dan Han Roliadi.2011. Pembuatan Pulp Dari Tandan Kosong Kelapa Sawit Untuk Karton Pada Skala Usaha Kecil.Jurnal Penelitian
45
Direktorat Jenderal Perkebunan. 2011. Statistika Perkelapa Sawitan Indonesia Tahun 2011, Departemen Pertanian. Jakarta : Direktorat Jenderal Perkebunan Indonesia.
Direktorat Jenderal Perkebunan. 2012. Statistika Perkelapa Sawitan Indonesia Tahun 2012, Departemen Pertanian. Jakarta : Direktorat Jenderal Perkebunan Indonesia.
Dunlop, A. P., 1948. Furfural Formation and Behavior, Ind. Eng. Chem. 40, pp. 204 – 209, The Quaker Oats Company, Chicago.
Fadjarwaty, D.dan Susanto, H. 2000. Optimasi Kondisi Hidrolisis Tandan Kosong Sawit untuk produksi Gula dan Furfural. Prosiding Seminar Nasional Rekayasa Kimia dan Proses. Universitas Diponegoro. Semarang
Fessenden, R.J., dan Fessenden, J.S. 1999. Kimia Organik Jilid I. Alih Bahasa H. Pudjaatmaka. Erlangga. Jakarta.
Ganjar,Andaka. 2011. Hidrolisis Ampas Tebu Menjadi Furfural dengan Katalisator Asam Sulfat. Jurnal Teknologi. 4 (2).
Gregory, A. P. 2007. Green Chemistry. Http: // www.research.uky.edu /images /lignin.jpg. Diakses pada tanggal 14 Mei 2013 pukul 20:22
Groggins, P. H., 1958, Unit Processes in Organic Synthesis, 5th ed., pp. 775 – 777, McGraw–Hill Book Company, New York.
Habibie, A.Z, dan M.A, Angkawijaya. 2002. Pemisahan Furfural dan Hidrolisa Pemasakan Tandan Kosong Sawit. Prosiding Seminar Nasional
Fundamental dan Aplikasi Teknik Kimia ITS.
Handojo, L, H Susanto, dan NS, Wardhani. 1999. Pemulihan Furfural dari Lindi Hitam Pemasakan TKS dalam Pelarut Organik. Prosiding Seminar Nasional Fundamental dan Aplikasi Teknik Kimia ITS.
46
Hendayana, S. 1994. Kimia analitik Instrumentasi. Penerbit Institut Keguruan dan Ilmu Pendidikan Semarang Press. Semarang.
Hermiati, Euis. 2010. Pemanfaatan Biomassa Lignoselulosa Ampas Tebu Untuk Produksi Bioetanol . Jurnal Litbang Pertanian, 29(4)
Hidajati, N. 2006, Pengolahan Tongkol Jagung sebagai Bahan Pembuatan Furfural. Jurnal Ilmu Dasar . 8, p. 48, Jurusan Kimia FMIPA, Universitas Negeri Surabaya.
H.K. Ong and M. Sashikala. 2007. Identification of furfural synthesized from pentosan in rice husk.Strategic Resources Research Centre, MARDI Headquarters, Serdang. J. Trop. Agric. and Fd. Sc. 35(2)(2007): 305– 312
Jalaluddin, Samsul R. 2005. Pembuatan Pulp Dari Jerami Padi Dengan Menggunakan Natrium Hidroksida. Jurnal Sistem Teknik Industri. 6
(5): 53-56.
Kirk, R. E. and Othmer K., 1955, Encyclopedia of Chemical Technology, Vol. 10, pp. 237 – 250, The Interscience Encyclopedia Inc., New York.
Medeiros, D.J . 1985. Furfural Process, US Patent. No.4.533.743.
Oktarina, Ifrilla. 2009. Pengaruh Konsentrasi Dua Jenis Bahan Pemutih terhadap Sifat Kimia dan Warna Serat Batang Pisang. Bandar Lampung : Jurusan Teknologi Hasil Pertanian Universitas Lampung.
Othmer, K., 1980, Encyclopedia of Chemical Technology: Flourine Compounds, Organic to Gold Compound. Volume 11, John Wiley and Sons,
NewYork.
Putri,P. 2012.”Distilasi Uap” Http://theprincess9208.wordpress.com/2012/11/20/
distilasi uap/, diakses tanggal 24 April 2013 pukul 20:19.
Pudjaatmaka, A. Hadyana dan Meity Taqdir Qodratillah. 2004. Kamus Kimia. Jakarta. Balai Pustaka.
47
Sudjadi. 1983. Penentuan Struktur Senyawa Organik. Ghalia Indonesia. Jakarta. Hlm 175-232.
Sukarta, I.N., 2008, Adsorpsi Ion Cr3+ Oleh Serbuk Gergaji Kayu Albizia (Albizzia Falcata): Studi Pengembangan Bahan Alternatif Penjerap Limbah Logam Berat, Sekolah Pascasarjana, IPB, Bogor
Suharto dan Susanto, H., 2006, Pengaruh Konsentrasi Katalis terhadap
Perolehan Furfural pada Hidrolisis Tongkol Jagung, Seminar Nasional IPTEK Solusi Kemandirian Bangsa, Yogyakarta.
Supriyanto, R. 1999. Buku Ajar Kimia Analitik III. FMIPA Universitas Lampung. Bandar Lampung. Hal 2-3.
Wankasi and E.B Naidoo.2012. Furfural Production From The Epicrap Of Wild Mango Fruits by Acid Catalyzed Hydrolysis. American jurnal Food and nutrition. 2(2): 47-50
Winarno, F. G. 1980. Kimia Pangan. Jakarta: Gramedia
Witono, J. A. 2005. Produksi Furfural dan Turunannya: Alternatif Peningkatan Nilai Tambah Ampas Tebu Indonesia. Http://www.chem-is-try.org/, diakses tanggal 23 April 2013 pukul 22:19.
Yuwono, S.D. 2000. Evaluasi Pemanfaatan Limbah Pertanian Menjadi Produk Furfural. ITB