Dewi Cakrawati
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis “Rekayasa Proses Isolasi
Limonin dari Limbah Pembuatan Sari Jeruk Siam” adalah karya saya sendiri
dengan arahan komisi pembimbing dan belum pernah diajukan dalam bentuk apa
pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau
dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah
disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis
ini.
Bogor, Januari 2010
Dewi Cakrawati
Siam Citrus Juice Processing. Supervised by ERLIZA NOOR AND SETYADJIT.
Limonin is related to triterpene derivatives found in Rutaceae families. It is generally not desirable in citrus juice, because of its bitter taste. Limonin have been shown to have biological activities such as amoebicidal agent and chemo preventive agent. Limonin has a future chances to be a valuable chemical for health treatment. The aims of this study were (1) determined extraction condition for isolating limonin from Pontianak tangerine juice by product such as from flavedo, seeds, pulp, backwashed water; (2) determined the effect of ethanol washing in the seed extraction process; (3) determined the optimum precipitation process (solvent ratio, time) to obtain high yield of limonin. Limonin isolation from backwashed water conducted with two methods, firstly, maceration of pulp using acetone and dichloromethane; secondly, liquid-liquid extraction of backwashed water using dichloromethane. Limonin isolation from membran segment, seed and pulp conducted with continous soxhlet extraction using hexane and acetone. The precipitate obtained from extraction were given two treatment, there were washed and unwashed with ethanol 95% to dissolved the impurities. Optimization process was conducted on precipitation stage using response surface method. Precipitation conditions were ratio between acetone extract and hexane and precipitation time. The result shown that none of limonin was detected in
backwashed water and pulp. Limonin content from flavedo was 2,5.10-5 mg,
while limonin content from citrus seed with ethanol washing was 0,215 mg limonin/g dried citrus seeds and limonin content from citrus seed without ethanol washing was 0,676 mg limonin/g dried citrus seeds. The preliminary research shown that seeds contain higher limonin than any other part of citrus fruit so the optimization only conducted on citrus seeds without ethanol washing. Optimum precipitation conditions by experiment was agreed with optimum condition by model obtain from response surface method, those were ratio between acetone extract and hexane 1:4 and precipitation time 20 hours with yield of limonin 1,502 mg limonin/g dried citrus seed. Design process of limonin isolation in this reasearch was good enough because it could give high extraction yield approximately 93%.
RINGKASAN
DEWI CAKRAWATI.Rekayasa Proses Isolasi Limonin dari Limbah Pembuatan
Sari Jeruk Siam. Dibimbing oleh ERLIZA NOOR DAN SETYADJIT.
Limonoid merupakan senyawa khas yang terdapat pada jeruk yang keberadaannya kurang disukai karena menyebabkan rasa pahit pada sari jeruk. Meskipun demikian, limonin memiliki manfaat yang besar bagi kesehatan diantaranya menghambat pertumbuhan tumor dan membantu mengurangi resiko penyakit penyumbatan pembuluh darah. Limonin telah diproduksi oleh Biosecure Lab Inc, suatu perusahaan farmasi dari Kanada menggunakan limonin serta senyawa aktif dalam jeruk seperti bioflavonoid, asam askorbat dalam produk
bernama AntimicrobesTM, suatu produk antiviral, antibakteri, antiparasit,
antioksidan, bakteriostatis, fungisidal, antiseptik dan desinfektan, yang dapat dikonsumsi atau digunakan sebagai obat luar. Limonin terutama terdapat pada bagian jeruk yang tidak dapat dimakan, sehingga bahan baku untuk isolasi limonin dapat diperoleh dari industri pembuatan sari jeruk yang menghasilkan
limbah seperti biji, kulit ari, sisa penyaringan awal (pulp) dan sisa penyaringan
membran. Adapun tujuan dari penelitian ini adalah (1) untuk memperoleh kondisi ekstraksi untuk mengisolasi limonin dari limbah pembuatan sari jeruk seperti biji,
kulit ari dan air backwash; (2) mengetahui pengaruh pencucian dengan etanol
95% terhadap presipitat yang dihasilkan dari biji jeruk siam; (3) memperoleh kondisi optimum proses presipitasi meliputi rasio ekstrak aseton dengan heksan serta lama presipitasi pada isolasi limonin dari biji jeruk.
Isolasi limonin dari air backwash dilakukan dengan dua metode, pertama
maserasi endapan air backwash menggunakan pelarut aseton dan diklorometan
pada suhu ruang selama 4 jam, metode kedua adalah ekstraksi cair-cair dari air
backwash menggunakan pelarut diklorometan. Isolasi limonin dari kulit ari dan biji jeruk dilakukan dengan metode soxhletasi bertahap, tahap pertama menggunakan pelarut heksan selama 10 jam, tahap kedua menggunakan pelarut aseton selama 10 jam. Untuk mempermudah proses ekstraksi, biji, kulit ari, dan
pulp dikeringkan dengan oven blower pada suhu 50oC sampai berat ketiga bahan
tersebut konstan, selanjutnya dilakukan pengecilan ukuran menggunakan hammer
mill sampai berukuran 10 mesh. Presipitat yang dihasilkan kemudian diberi
perlakukan tanpa dan dengan pencucian etanol 95%. Selanjutnya dilakukan isolasi limonin pada bahan baku dengan kandungan limonin paling tinggi dengan optimasi rekayasa proses isolasi dilakukan dengan metode permukaan respon (response surface method -RSM) dengan rancangan komposit terpusat pada tahapan proses presipitasi dengan dua faktor yaitu rasio ekstrak aseton dengan pelarut heksan serta lama presipitasi.
Analisis limonin dilakukan dengan metode spektrofotometri pada panjang
gelombang 503 nm. Isolasi limonin dari air backwash metode maserasi endapan
maupun ekstraksi cair-cair menunjukkan kandungan limonin tidak terdeteksi. Isolasi limonin dari pulp juga menunjukkan kandungan limonin tidak terdeteksi sedangkan isolasi limonin dari kulit ari menunjukkan kandungan limonin sebesar
2,5.10-5 mg limonin/g bahan kering. Isolasi limonin dari biji jeruk dengan metode
menunjukkan kondisi optimum hasil eksperimen sesuai dengan hasil optimasi berdasarkan metode permukaan respon, yaitu diperoleh pada rasio ekstrak aseton dengan heksan yaitu 1:4 dengan lama presipitasi 20 jam dengan respon jumlah limonin 1,502 mg limonin/g biji kering. Rekayasa proses isolasi limonin pada penelitian ini sudah cukup baik karena dapat mengisolasi limonin sebesar 93% dari biji jeruk siam.
Biji jeruk siam merupakan bahan baku potensial untuk produksi limonin karena kandungan limonin yang tinggi serta ketersediaannya yang mencukupi dan dapat diperoleh dari limbah industri pengolahan sari jeruk. Penelitian ini menghasilkan presipitat dengan tingkat kemurnian limonin sebesar 27%, hal ini berarti limonin ini dapat diaplikasikan dalam produk pangan dan farmasi dan
digolongkan dalam phamaceutical grade.
© Hak Cipta Milik Institut Pertanian Bogor (IPB) tahun 2010
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
Dewi Cakrawati
Tesis
Sebagai salah satu syarat untuk memperoleh
gelar Magister Sains pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
LEMBAR PENGESAHAN
Judul Tesis : Rekayasa Proses Isolasi Limonin dari Limbah
Pembuatan Sari Jeruk Siam
Nama : Dewi Cakrawati
NIM : F351070151
Disetujui
Komisi Pembimbing
Dr. Ir. Erliza Noor Dr. Ir. Setyadjit, M.App.Sc
Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana
Teknologi Industri Pertanian
Prof. Dr. Ir. Irawadi Djamaran Prof. Dr. Ir. Khairil A. Notodiputro, M.Si
Segala puji hanyalah milik Allah SWT yang telah memperkenankan
penulis menyelesaikan penelitian dan menuangkan hasilnya dalam bentuk tesis
yang berjudul “Rekayasa Proses Isolasi Limonin dari Limbah Pembuatan Sari
Jeruk Siam” sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada Program Studi Teknologi Industri Pertanian Insitut Pertanian Bogor.
Penulis menyadari bahwa karya ilmiah ini tidak akan terselesaikan tanpa
bantuan dari berbagi pihak, karenanya pada kesempatan ini penulis mengucapkan
terima kasih sebesar-besarnya kepada :
1. Ibu Dr. Ir. Erliza Noor dan Bapak Dr. Ir. Setyadjit, M.App.Sc. selaku komisi
pembimbing atas segala bimbingan, arahan, bantuan, dan motivasi baik
berupa moril dan materil yang telah diberikan selama penelitian dan
penyusunan tesis.
2. Prof. Dr. Ir. Irawadi Djamaran dan Dr. Ir. Ani Suryani, DEA., selaku Ketua
dan Sekretaris Program Studi Teknologi Industri Pertanian atas bantuan dan
masukan yang diberikan untuk kelancaran studi penulis.
3. Seluruh staf pengajar Sekolah Pasca Sarjana IPB yang telah memberi ilmu
pengetahuan dan bimbingan kepada penulis selama menimba ilmu
pengetahuan serta laboran dan teknisi laboratorium Departemen Teknologi
Industri Pertanian yang telah banyak memberikan bantuan kepada penulis
selama melaksanakan penelitian.
4. Sekretariat Jendral Penelitian dan Pengembangan Departemen Pertanian yang
telah memberi dukungan finansial bagi pelaksanaan penelitian ini melalui
Program Kerjasama Kemitraan Penelitian Pertanian dengan Perguruan Tinggi
(KKP3T).
5. Kepala Balai Besar Penelitian dan Pengembangan Pasca Panen Pertanian
Departemen Pertanian yang telah bersedia memfasilitasi penelitian ini serta
staf dan teknisi Balai Besar Litbang Pasca Panen yang telah banyak
membantu demi kelancaran pelaksanaan penelitian ini.
6. Rekan-rekan seperjuangan, mahasiswa S1, S2 dan S3 TIP atas bantuan,
dukungan, dan motivasi yang diberikan kepada penulis selama penelitian dan
7. Ayah H. Wahidin, Ibu Hj. Dewi Laraswati dan adik tercinta atas bantuan,
dorongan, iringan doa yang tulus kepada penulis selama menyelesaikan
pendidikan S2.
8. Suami tercinta Yuyus Sirhanudin Permana S.Si., Apt, untuk kesabaran,
pengertian, dukungan, serta motivasi yang tidak pernah berhenti diberikan
kepada penulis selama menyelesaikan pendidikan S2 serta untuk
diskusi-diskusi panjang dan masukan yang bermanfaat yang diberikan kepada penulis
selama melaksanakan penelitian dan penyusunan tesis.
9. Semua pihak yang telah banyak membantu penulis baik secara langsung
maupun tidak langsung yang tidak dapat penulis sebutkan satu persatu.
Penulis berharap semoga karya ini bisa bermanfaat bagi pihak yang
membutuhkan. Semoga dengan mengetahui sedikit tentang limonin bisa
menambah keimanan kita kepada Sang Khalik yang Maha Mengetahui Segala
Sesuatu.
Bogor, Januari 2010
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 24 Agustus 1983 dari Ayah H.
Wahidin dan Ibu Hj. Dewi Laraswati. Penulis merupakan putri pertama dari dua
bersaudara. Penulis menyelesaikan pendidikan dari SMU Negeri 20 Bandung
pada tahun 2001 dan pada tahun yang sama memperoleh kesempatan untuk
melanjutkan pendidikan di Universitas Padjadjaran pada Jurusan Teknologi
Industri Pangan, Fakultas Teknologi Industri Pertanian melalui jalur Ujian Masuk
Perguruan Tinggi Negeri (UMPTN) dan lulus tahun 2006. Penulis melanjutkan
pendidikan S2 pada Program Studi Teknologi Industri Pertanian Insititut
xii
DAFTAR TABEL ...
DAFTAR GAMBAR ...
DAFTAR LAMPIRAN ………..
I. PENDAHULUAN
1.1Latar Belakang ………
1.2Perumusan Masalah ………
1.3Tujuan Penelitian………
1.4Ruang Lingkup Penelitian ………
II. TINJAUAN PUSTAKA
2.1Senyawa Limonoid ………….………
2.2Ekstraksi ………
2.3Teknik Separasi……….……….
2.4Penelitian Terdahulu ………..
III. METODOLOGI PENELITIAN
3.1Kerangka Pemikiran ………...
3.2Tempat dan Waktu Penelitian ………
3.3Bahan dan Alat ………...
3.4Tahapan Penelitian ………
3.5Rancangan Percobaan ………
IV. HASIL DAN PEMBAHASAN
4.1Isolasi Limonin dari Air Backwash, Kulit Ari, Biji dan
Sisa Penyaringan Awal (Pulp) ………...
4.2Optimasi Proses Isolasi Limonin dari Biji Jeruk …………
V. SIMPULAN DAN SARAN
5.1Simpulan ……….
5.2Saran ………..
DAFTAR PUSTAKA. ………
xiii DAFTAR TABEL Halaman 1 2 3 4 5 6 7 8 9 10 11
Senyawa limonoid aglikon dan limonoid glukosida ……….
Beberapa penelitian tentang limonin ………
Desain rancangan percobaan ……….
Konsentrasi limonin dalam permeat, retentat dan air backwash…
Hasil analisis isolasi limonin dari air backwash ………...
Komposisi asam lemak pada minyak biji jeruk ………
Kandungan limonin dalam kristal yang diperoleh dari biji, kulit
ari, pulp jeruk ………
Kandungan limonin pada berbagai perlakuan rasio pelarut dan lama presipitasi ……….
Koefisien parameter dengan respon jumlah limonin yang diperoleh ………...
Nilai optimum faktor rasio volume ekstrak aseton dengan heksan dan lama presipitasi ……….………..
Kandungan limonin pada beberapa sari dan biji jeruk …………..
xiv Halaman 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21
Biosintesis limonin dalam buah jeruk ………
Mekanisme pembentukan rasa pahit pada buah jeruk ………...
Struktur molekul limonin 17-β-D- glucopyranosida …………..
Distribusi limonin dalam jeruk ………...
Perangkat ekstraksi soxhletasi ………
Diagram proses persiapan bahan baku ………
Skema proses mikrofiltrasi sari jeruk ………
Skema proses backwash membran ………..
Diagram proses maserasi endapan air backwash dengan pelarut
aseton dan diklorometan ………...
Diagram proses ekstraksi air backwash dengan metode ekstraksi
cair-cair ………..
Diagram proses isolasi limonin dari biji, kulit ari dan pulp jeruk
tanpa pencucian etanol ………..
Diagram proses isolasi limonin dari biji, kulit ari dan pulp jeruk
dengan pencucian etanol ………...
Optimasi proses isolasi limonin dari biji jeruk ……….
Struktur molekul limonin dan beberapa turunannya ………
Ekstraksi maserasi hasil sentrifugasi air backwash …………...
Proses ekstraksi cair-cair ………..
Biji jeruk hasil pengeringan dan pengecilan ukuran …………....
Minyak biji jeruk siam ………..
Kristal limonin dari biji jeruk pada berbagai perlakuan rasio volume ekstrak aseton dengan heksan serta lama presipitasi...
Permukaan respon jumlah limonin yang diperoleh ……..………
Kontur permukaan respon jumlah limonin yang diperoleh …...
xv
DAFTAR LAMPIRAN
Halaman
1
2
3
4
5
6
7
Prosedur analisa ……….………
Kurva standar limonin ……….……..
Analisis Limonin dalam presipitat………
Hasil Analisis Limonin ………
Hasil optimasi jumlah limonin dengan metode permukaan respon
Pengolahan data rasio volume ekstrak aseton – pelarut heksan terhadap jumlah limonin yang dihasilkan ……….
Perhitungan persen recovery isolasi limonin ……….
54
56
57
58
60
61
1
Limonin merupakan senyawa limonoid utama yang terdapat pada hampir
semua jenis jeruk dalam jumlah signifikan. Limonin juga merupakan penyebab
utama timbulnya rasa pahit pada sari jeruk. Meskipun demikian, limonin
memiliki manfaat yang besar bagi kesehatan diantaranya dapat menghambat
pertumbuhan tumor (Ishii et al. 2003), menurunkan rasio kolesterol LDL/HDL
dan mempercepat oksidasi LDL di usus sehingga membantu mengurangi resiko
penyakit penyumbatan pembuluh darah (Dandeekar et al. 2007).
Beberapa perusahaan farmasi diantaranya Shanghai Xinma Bio-tech
Co,Ltd dari Cina; Alexis Biochemicals, perusahaan farmasi Swiss-Amerika
Serikat telah memproduksi limonin dalam skala pabrik untuk selanjutnya
dijadikan bahan tambahan makanan dan minuman, suplemen kesehatan dan
biopestisida. Saat ini, Biosecure Lab Inc, suatu perusahaan farmasi dari Kanada
menggunakan limonin serta senyawa aktif dalam jeruk seperti bioflavonoid,
asam askorbat dalam pembuatan produk bernama AntimicrobesTM, suatu
produk antiviral, antibakteri, antiparasit, antioksidan, bakteriostatis, fungisidal,
antiseptik dan desinfektan, yang berbentuk spray dan konsentrat serta dapat
dikonsumsi atau digunakan sebagai obat luar. Sedangkan di Indonesia data
mengenai produksi limonin serta perusahaan farmasi yang memproduksinya
belum tersedia.
Limonin (Limonoic Acid 3,19:16, 17-dilactone) adalah senyawa
limonoid aglycone dengan rumus molekul C26H30O8 memiliki berat molekul
470,5 Da, titik didih 280 ºC, bersifat tidak larut dalam air, tetapi larut dalam
dimetilformamida, dichloromethane, acetonitrile, asam asetat glasial, dan
alkohol. Senyawa dengan bentuk kristal berwarna putih kekuningan ini
ditemukan pada semua spesies jeruk, dengan kandungan tertinggi pada biji.
Limonin pada buah jeruk awalnya terdapat sebagai senyawa limonoic acid A
ring lactone yang memiliki satu gugus lakton dan tidak memiliki rasa pahit, pada saat proses ekstraksi sari jeruk, senyawa ini terlaktonisasi karena menjadi
limonoid dilakton yang memiliki dua gugus lakton dan memiliki rasa pahit.
2
D-ring lakton hidrolase. Adanya penambahan panas selama proses pasteurisasi
dan evaporasi akan mempercepat reaksi ini (Mozaffar et al. 2000).
Penelitian Aghitsni (2008) mengenai mikrofilrasi sari jeruk menghasilkan
produk samping berupa kulit ari, biji, sisa penyaringan awal dan lapisan cake
yang tertahan di membran yang diduga mengandung limonin. Limonin bernilai
tinggi yaitu sebesar US$ 109,5 untuk 5 mg limonin murni (SIGMA, 2009),
pada produk komersial limonin dijual dengan tingkat kemurnian 75% ± 5%
(SIGMA 2007).
Beberapa penelitian telah dilakukan untuk mengisolasi limonin,
diantaranya Ifuku et al. (1998), yang mengajukan paten produksi limonoid
glukosida dari biji dan sari jeruk menggunakan ekstraksi supercritical fluida.
Yu (2004), ekstraksi limonin aglikon dan glukosida dari biji grapefruit
menggunakan Supercritical CO2 pada kondisi optimum tekanan -48,3 MPa
selama 60 menit, kecepatan alir 5 l/menit, menghasilkan rendemen limonin 6,3
mg limonin/biji grapefruit kering, ekstraksi limonin glukosida pada kondisi
optimum tekanan -42 Mpa, 45% etanol selama 40 menit, kecepatan alir 5
l/menit menghasilkan rendemen 0,73 mg limonin glukosida/g biji grapefruit
kering. Dandeekar et al. (2007) memperkenalkan proses baru dalam ekstraksi
limonoid aglikon dari biji jeruk asam (Citrus aurantium L.) menggunakan dua
larutan hidrotrop yaitu garam natrium salisilat (Na-Sal) dan natrium cumene
sulfonat (Na-CuS) dengan hasil penelitian menunjukkan rendemen limonin
paling tinggi diperoleh pada kondisi konsentrasi larutan 2 M, suhu 45oC dan
persen bahan 10% dimana larutan Na-CuS menghasilkan limonin 0,65 mg/g
biji jeruk sedangkan larutan Na-Sal menghasilkan 0,46 mg/g biji.
Pada penelitian ini dilakukan isolasi senyawa limonin yang diperoleh dari
biji jeruk siam. Rekayasa proses isolasi dilakukan dengan metode ekstraksi
bertahap, presipitasi dan purifikasi. Optimasi rekayasa proses isolasi dilakukan
dengan metode permukaan respon atau response surface method (RSM)
dengan rancangan komposit terpusat dengan pada tahap proses presipitasi
dengan perlakuan rasio volume pelarut heksan serta lama presipitasi. Isolasi
senyawa limonin sebagai pemanfaatan produk samping mikrofiltrasi sari jeruk
Secara umum, produk limonin diharapkan dapat dimanfaatkan lebih lanjut pada
industri farmasi.
1.2 Perumusan Masalah
Limonin yang ada saat ini diperoleh dari biji lemon, grapefruit dan
jeruk asam (Citrus aurantifolium L.) sedangkan isolasi limonin dari biji jeruk
siam (Citrus nobilis var microcarpa) yang juga diduga mengandung limonin
belum pernah dilakukan. Isolasi limonin saat dilakukan dengan metode
ekstraksi menggunakan pelarut petroleum eter yang bersifat toksik. Selain itu,
tahapan proses isolasi limonin cukup panjang sehingga perlu ada optimasi
rekayasa proses ekstraksi dan presipitasi supaya tahapan proses bisa lebih
singkat dan bisa meningkatkan rendemen limonin yang dihasilkan.
1.3 Tujuan penelitian
Adapun tujuan dari penelitian ini adalah
1. Mengetahui kandungan limonin dalam limbah pengolahan sari jeruk,
seperti air backwash membran, kulit ari, sisa penyaringan awal (pulp) dan
biji jeruk
2. Memperoleh kondisi optimum proses isolasi limonin dari bahan baku
dengan kandungan limonin paling tinggi (biji jeruk) agar dihasilkan
limonin dengan rendemen paling tinggi
1.4 Ruang Lingkup Penelitian
Penelitian ini meliputi penelitian pendahuluan dan penelitian utama.
Penelitian pendahuluan meliputi isolasi limonin dari air backwash, kulit ari
dan biji jeruk siam serta penentuan metode isolasi limonin dari biji jeruk.
Penelitian utama meliputi penentuan kondisi optimum proses isolasi
limonin dari bahan baku dengan kandungan limonin paling tinggi pada tahap
presipitasi dengan perlakuan rasio volume ekstrak aseton dengan pelarut
4
II. TINJAUAN PUSTAKA
2.1 Senyawa Limonoid
Menurut Yu (2004), senyawa limonoid pada jeruk merupakan
kelompok metabolit sekunder yang belum diketahui memiliki fungsi langsung
pada pertumbuhan dan perkembangan tanaman. Menurut Ishii et al. (2003),
limonoid merupakan senyawa kimia dengan struktur triterpenoid dengan
kandungan oksigen yang tinggi. Limonoid merupakan penanda taksonomi
yang baik karena senyawa ini spesifik untuk tanaman Rutaceae. Maier et al.
dalam Nagy et al. (1977) menambahkan limonoid memiliki beberapa
karakteristik yaitu cincin furan yang terikat pada cincin D pada C-17, gugus
fungsional yang mengandung oksigen pada C-3, C-4, C-16 dan C-17, gugus
epoksida pada C-14 dan C-15. Limonoid terdapat secara alami dalam dua
bentuk yaitu limonoid aglikon dan limonoid glukosida. Limonoid aglikon
diklasifikasikan menjadi dua kelompok, pertama limonoid monolakton yang
memiliki cincin D terbuka, misalnya limonoat A-ring lakton yang banyak
terdapat pada daun dan buah jeruk; kedua limonoid dilakton yang memiliki
cincin D tertutup, misalnya limonin yang banyak terdapat pada biji jeruk.
Limonin pertama kali diisolasi dari jeruk navel, dengan komposisi kimia
C26H30O8 dengan berat molekul 470 Da.
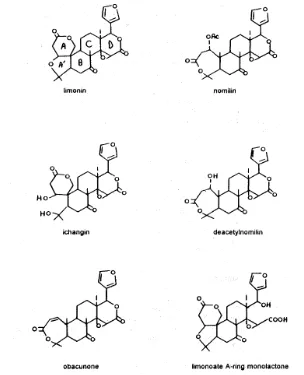
Menurut Hasegawa dan Maier dalam Rouseff (1990), dari 37 jenis
senyawa limonoid aglikon yang berhasil diisolasi, empat diantaranya
menyebabkan rasa pahit pada jeruk, yaitu limonin, nomilin, ichangin dan
nomilinat. Limonin terbentuk seiring proses pertumbuhan jeruk dan diduga
terbentuk pada jaringan albedo buah jeruk. Diduga senyawa limonoid yang
mula-mula terbentuk adalah deasetilnomilin selanjutnya nomilin, obacunone
lalu limonin. Limonoate A-ring lakton merupakan garam dari asam limonoat
A-ring lakton yang terdapat dalam jaringan buah jeruk, sedangkan dalam biji
jeruk terdapat dalam bentuk limonoat dilakton atau disebut juga limonin.
Pahit Tidak Pahit
Gambar 1. Biosintesis limonin dalam buah jeruk
Sumber : Eskin (1979); Maier et al. dalam Nagy et al. (1977)
Limonoat A-ring lakton terdapat pada bagian membran sel dari vesicle
jeruk dan tidak memiliki rasa pahit tetapi ketika diekstraksi dan terjadi kontak
dengan sari jeruk yang bersifat asam, senyawa ini terlaktonisasi menjadi
limonoat dilakton yang memiliki rasa pahit. Perubahan limonin dari
monolakton menjadi dilakton terjadi pada suasana pH 5,4-6,2 dan suhu
15-45oC. Proses ini dipengaruhi oleh aktivitas enzim limonoid D-ring lakton
hidrolase. Selama proses pasteurisasi dan evaporasi, adanya penambahan
panas akan mempercepat reaksi ini (Mozaffar et al. 2000). Mekanisme
terbentuknya rasa pahit pada buah jeruk disajikan pada Gambar 2.
6
Menurut Breksa dan Manners (2006), limonoid glukosida merupakan
turunan bentuk ester ion cincin A dan D, misalnya glikosilasi pada posisi
D-hidroksi dari ester ion limonoid D-ring. Senyawa limonoid aglikon dan
limonoid glukosida disajikan pada Tabel 1.
Tabel 1. Senyawa limonoid aglikon dan limonoid glukosida
Limonoid aglikon Limonoid glukosida
1. Limonin 2. Nomilin 3. Obacunone 4. Deacetylnomilin 5. Ichangin 6. Deoxylimonin 7. Deoxylimonol 8. Limonol
9. Limonyl acetate
10. 7α-Obacunol
11. 7α-Obacunyl acetate
12. Ichangensin 13. Citrusin
14. 1- (10-19)Abeo-obacun-
15. Calamina hydroxy-isoobacunoic acid
16. Retrocalamina
17. Cyclocalamina
18. Methyl isoobacunoate diosphenola
19. Methyl deacetylnomilinatea
20. 6-Keto-7β- deacetylnomilola
21. Methyl 6-hydroxy isoobacunoatea
22. Isocyclocalamina
23. Asam Deacetylnomilinic 24. Asam Nomilinic
25. Asam Isoobacunoic 26. Asam Epiisoobacunoic 27. Asam Isolimonic
28. Limonoic acid A-ring lactone 29. Asam Deoxylimonic
30. 17-Dehydrolimonoic acid A-ring lactone 31. Asam Trans-19- hydroxyobacunoic 32. Asam Calaminic
33. Asam Retrocalaminic 34.Asam Cyclocalaminic
35. Isoobacunoic acid diosphenola
36. Obacunoic acida 9 (11) -en-7α-yl acetate
37. 1- (10-19)Abeo-7o- acetoxy-lOβ-
1. Limonin 17-β-D-glukopiranosida
2. Nomilin 17-β-D-glukopiranosida
3. Deacetylnomilin 17-β
-D-glukopiranosida
4. Obacunone 17-β
-D-glukopiranosida
5. Asam Nomilinat 17-β
-D-glukopiranosida
6. Asam Deacetylnomilinat 17-β
-D-glukopiranosida
7. Obacunoat 17-β
-D-glukopiranosida
8. Asam Trans-obacunoat 17-β
-D-glukopiranosida
9. Asam Isoobacunoat 17-β
-D-glukopiranosida
10. Asam Epiisoobacunoat 17-β
-D-glukopiranosida
Keterangan : a diisolasi dari biji jeruk calamondin
Contoh senyawa limonoid glukosida disajikan pada Gambar 3.
Gambar 3. Struktur molekul Limonin 17-β-D- glukopiranosida
Sumber : Hasegawa et al. (1997)
Senyawa limonoid terdapat pada jaringan buah dan biji jeruk yang
telah matang dalam bentuk turunan aglikon dan glukosida. Menurut Maier et
al. (1977), biji merupakan bagian yang paling banyak mengandung senyawa
limonoid, karenanya hampir semua proses isolasi dilakukan pada biji jeruk.
Distribusi limonin dalam jeruk disajikan pada Gambar 4.
Gambar 4. Distribusi limonin dalam jeruk Sumber : Li (2000)
Menurut Mozaffar et al. (2000), limonin (Limonoate 3,19:16,
17-dilactone) adalah senyawa limonoid aglikon dengan rumus molekul C26H30O8
memiliki berat molekul 470,5 Da, titik didih 280 ºC, bersifat tidak larut dalam
air, tetapi larut dalam dimetilformamide, dichloromethane, acetonitrile, asam
asetat glasial, dan alkohol. Senyawa dengan bentuk kristal berwarna putih
kekuningan ini ditemukan pada semua spesies jeruk, dengan kandungan
tertinggi pada biji. Limonin merupakan senyawa dominan yang terdapat pada
8
Valencia, grapefruit dan jeruk siam. Menurut Maier et al. dalam Nagy et al.
(1977), limonin terdekomposisi oleh asam kuat membentuk asam limoneksik
yang tidak memiliki aktivitas antioksidan. Limonin juga bereaksi dengan basa
pada pH 10-12 membentuk garam dari asam limonoat.
Limonin memiliki kelarutan yang terbatas dalam air yaitu < 40 mg/l,
memiliki rasa pahit dan ditemukan dalam konsentrasi tinggi pada bagian
jeruk yang tidak dapat dimakan seperti biji dan kulit. Konsentrasi limonin
pada sari jeruk biasanya kurang dari 20 mg/l, tetapi pada konsentrasi 6 mg/l
telah menimbulkan rasa pahit dan menyebabkan sari jeruk tidak diterima
konsumen. Sebaliknya, limonoid glukosida larut air, tidak berasa dan
ditemukan dalam sari jeruk dengan konsentrasi sebesar 720 mg/l (Breksa dan
Dragull, 2008). Ozaki (1990) menambahkan biji jeruk mengandung sejumlah
besar senyawa limonoid serta dapat melakukan biosintesis senyawa limonoid
aglikon dan limonoid glukosida. Limonin mulai terbentuk pada awal
pembentukan biji sedangkan limonoid glukosida terbentuk hanya pada biji
yang matang.
Limonin adalah komponen kimia yang mengandung furan. Banyak
produk alami yang mengandung furan yang diperoleh dari tanaman telah
terbukti meningkatkan sistem enzim detoksifikasi, glutathione S-transferase
(GST) dan menghambat atau menghambat pembentukan kimia dari
karsinogenesis sehingga disebut suppresive agent. Aktivitas antikarsinogen
dari limonoid aglikon telah diteliti lebih lanjut. Penelitian menunjukkan
limonoid aglikon (limonin, nomilin, obacunone, isoobacunone, ichangin)
meningkatkan pembentukan enzim detoksifikasi glutathione S-transferase dan
menghambat pembentukan tumor pada kulit, berbagai jaringan pada tikus dan
pada hamster dengan cara mengkatalisis konjugasi glutathione yang
menghambat pembentukan benzo [a] pyrene, salah satu penyebab kanker.
Limonoid aglikon juga menghambat pembentukan, pertumbuhan dan
perkembangan hormon-independen sel kanker payudara manusia dalam
jaringan (Hasegawa et al. dalam Shahidi, 2008). Hasil penelitian
menunjukkan limonin 17-D-glukopiranosida berfungsi sebagai anti kanker
menunjukkan bahwa limonoid pada jeruk menurunkan rasio kolesterol
LDL/HDL dan mempercepat oksidasi LDL di usus sehingga membantu
mengurangi resiko penyakit penyumbatan pembuluh darah (Dandeekar et al.
2007).
2.2 Ekstraksi
Ekstraksi adalah suatu proses untuk memisahkan komponen dari
bahan berdasarkan kelarutan komponen tersebut dalam pelarut. Produk
natural perlu dipisahkan dari biomassa melalui proses ekstraksi mengingat
produk natural sangat beragam dan memiliki sifat fisikokimia yang berbeda
maka diperlukan metode ekstraksi yang mengekstrak bahan yang diinginkan
secara efisien. Metabolit sekunder dapat diekstraksi dari berabagai sumber
alam, seperti tanaman, mikroorganisme, binatang laut, serangga dan hewan
amfibi (Seidel, 2006).
Prosedur ekstraksi yang ideal harus dapat mengekstrak sebanyak
mungkin senyawa yang diinginkan, juga harus cepat, sederhana dan efisien.
Pemilihan metode ekstraksi didasarkan pada pengetahuan mengenai senyawa
yang ingin diekstrak. Hal ini meliputi koefisien partisi dalam air atau pelarut
organik, polaritas dari senyawa, stabilitas molekul dalam terang atau gelap,
atau pada kondisi suhu tertentu. Apabila senyawa larut air biasanya diekstrak
dengan air atau larutan buffer sedangkan senyawa yang tidak larut air
diekstrak dengan pelarut organik. Untuk mempermudah proses ektraksi
biasanya dilakukan proses preparasi pada bahan yang akan diekstraksi
misalnya dengan pengeringan serta penghancuran dinding sel atau jaringan,
hal ini dapat dilakukan dengan bantuan enzim, atau dengan pengecilan ukuran
bahan (Jones, 2006).
Menurut Cseke et al. (2000), ekstraksi herbal secara tradisional
dilakukan menggunakan air, dimana untuk jaringan lunak seperti daun,
bunga, akar atau buah dengan tekstur lembut yang memiliki kadar air tinggi
(60-95%) dilakukan menggunakan air dingin atau panas dengan perlakuan
fisik yang minimal. Sedangkan untuk jaringan dengan kandungan lignin
tinggi dengan kadar air rendah (5-50%), perlu diberi perlakuan fisik seperti
10
Apabila senyawa yang diinginkan tidak larut air karena bersifat non-polar,
maka dilakukan ekstraksi menggunakan pelarut organik (misalnya aseton,
methanol, etanol, kloroform, dietil eter, metilen klorida atau kombinasi
beberapa pelarut organik). Suhu ekstraksi tergantung titik didih pelarut yang
digunakan dan sehingga harus disesuikan dengan peralatan yang digunakan.
Seidel (2006) menambahkan metode yang dapat digunakan yaitu
maserasi, perkolasi dan soxhletasi. Maserasi dilakukan dengan cara
merendam bahan dalam pelarut organik kemudian dilakukan pengadukan
menggunakan stirrer atau shaker untuk mempercepat ekstraksi. Proses
ekstraksi dihentikan ketika kondisi equilibrium tercapai antara konsentrasi
metabolit dalam ekstrak dan dalam bahan. Ekstraksi perkolasi dilakukan
dengan melewatkan pelarut pada bahan yang disimpan dalam percolator yaitu
sebuah tabung dengan keran di bagian bawah. Metode ini memiliki beberapa
kelemahan diantaranya membutuhkan pelarut yang banyak, waktu ekstraksi
yang lama serta rendemen sedikit karena pelarut tidak merata ke seluruh
bahan. Ekstraksi soxhletasi paling banyak digunakan untuk mengekstrak
bahan dari tanaman karena prosesnya yang bersifat kontinyu. Ekstraksi ini
menggunakan perangkat ekstraksi soxhlet, yang didasarkan pada metode
refluks dimana bahan disimpan dalam hull yang terbuat dari selulosa yang
diletakkan dalam tabung soxhlet yang berada di antara kondensor dan labu
yang menampung pelarut. Pada proses ini, pelarut ditambahkan ke dalam
labu dan suhu diatur sesuai titik didih pelarut, ketika mencapai titik didihnya,
pelarut akan menguap dan terkondensasi sehingga terkumpul dalam labu
soxhlet dan merendam bahan, setelah mencapai ketinggian tertentu, pelarut
akan terefluks dan kembali ke labu pelarut di bagian bawah. Perangkat
Gambar 5. Perangkat ekstraksi soxhletasi
Sumber : Cseke et al. 2006
Ekstraksi juga dapat dilakukan menggunakan detergen (XAD-4,
styrene-divinylbenzene), alkohol (metanol, etanol dan alkohol rantai panjang)
dan dimetilsulfoksida untuk mengekstrak komponen yang diinginkan tanpa
membunuh organisme yang mengandung komponen tersebut. Metode ini
tergantung pada koefisien partisi dari pelarut yang digunakan, polaritas
molekul yang akan diekstrak dan kemudahan pelarut untuk berpenetrasi ke
dalam jaringan tanpa membunuh jaringan tersebut (Seidel, 2006).
Menurut Seidel (2006), ekstraksi ultrasonik atau disebut juga
ultrasonifikasi, merupakan modifikasi dari ekstraksi maserasi, yaitu metode
ekstraksi menggunakan suara dengan frekuensi tinggi untuk memisahkan
senyawa fitokimia dari jaringan tanaman. Pada metode ini, bubuk tanaman
disimpan dalam vial yang diletakkan dalam bak ultrasonik dan suara ultra
digunakan untuk meningkatkan tekanan mekanik pada sel karena
menyebabkan terbentuknya rongga dalam sel. Sonifikasi berlangsung lebih
cepat dibanding metode ekstraksi biasa seperti soxhletasi atau maserasi,
12
frekuensi instrumen, suhu dan lama ekstraksi. Metode ini digunakan untuk
isolasi minyak essensial, polisakarida dan zat bioaktif fitokimia. Proses
ultrasonifikasi dapat menimbulkan panas, sehingga sonifikasi komponen yang
mudah rusak karena panas memerlukan tahapan proses untuk menjaga agar
suhu komponen tetap dingin.
Ekstraksi dengan bantuan microwave dilakukan dengan cara meradiasi
sampel yang ditambah pelarut organik yang sesuai dengan kekuatan 100-150
W, biasanya dilakukan pada interval waktu yang pendek untuk mencegah
sampel mendidih. Ekstraksi dengan microwave memberikan rendemen yang
lebih tinggi dibanding ekstraksi konvensional (Cseke et al. 2000).
Ekstraksi superfluida critical, biasanya menggunakan CO2 sebagai
pelarut, ekstraksi ini digunakan pada proses dekafeinasi kopi arabika dalam
skala besar. Kondisi supercritical tercapai ketika tekanan dan suhu sama atau
melebihi titik kritis (31oC dan 73 atm untuk CO2) dimana pada kondisi ini
CO2 tidak berupa gas atau cairan tetapi merupakan antara dua fase tersebut
yang menyebabkan superfluida critical memberikan kondisi ideal untuk
ekstraksi komponen (Cseke et al. 2000).
Gaikar dan Dandeekar (2001) mengajukan paten mengenai ekstraksi
curcuminoid menggunakan larutan hidrotrop. Ekstraksi ini disebut ekstraksi
hidrotropik dimana pelarut yang digunakan adalah larutan dari garam
hidrotrop. Hidrotrop adalah komponen ampifilik berupa alkil rantai pendek
yang larut air, yang dihasilkan dari sulfonasi hidrokarbon aromatik. Hidrotrop
digunakan sebagai agen ganda untuk melarutkan zat yang tidak larut dalam
air dan zat–zat yang kurang larut pada produk pembersih rumah tangga,
perawatan tubuh. Fungsi hidrotrop adalah menstabilkan larutan, memodifikasi
viskositas dan titik awan, membatasi pemisahan fase pada suhu rendah dan
mengurangi busa. Meskipun bukan sebagai surfaktan, hidrotrop merupakan
senyawa ampifilik yang mempunyai gugus hidrofob dan hidrofil. Bagian
hidrotrop yang bersifat hidrofob adalah benzene, yaitu metal benzene (nama
umum: toluene, dimetil benzene (xilene) dan metal etil benzene (cumene)
yang non-polar. Bagian hidrofilik yang bersifat polar adalah gugus sulfonat
kalium. Hidrotrop bukan surfaktan tapi digunakan untuk melarutkan
komponen yang tidak larut air, menstabilkan larutan, memodifikasi
viskositas. Larutan hidrotop bekerja dengan cara berpenetrasi ke dalam
dinding sel, menghancurkan struktur dinding sel sehingga membuat bahan
yang diinginkan lebih mudah larut.
2.3 Teknik Separasi
Setelah dilakukan ekstraksi, suatu komponen biasanya terdapat dalam
bentuk cair berupa ekstrak untuk itu perlu diubah menjadi bentuk padat atau
bentuk lain yang lebih mudah digunakan. Hal ini dapat dilakukan dengan cara
presipitasi, biasanya dilakukan dengan cara menambahkan sejumlah pelarut
ke dalam ekstrak dimana kelarutan komponen dalam pelarut tersebut rendah
sehingga komponen kemudian mengendap. Hasil presipitasi biasanya masih
mengandung banyak pengotor karena itu perlu dilakukan metode separasi
untuk memisahkan komponen menjadi bentuk yang lebih murni. Dalam hal
ini, separasi tidak berarti menghasilkan bahan yang betul-betul murni, tetapi
kadar pengotor berada pada batas yang diperbolehkan (Florence et al. dalam
Sarker et al. 2006). Beberapa metode separasi antara lain :
1. Destilasi
Salah satu cara yang paling banyak diaplikasikan dalam purifikasi cairan
atau bahan organik dengan titik didih rendah adalah destilasi fraksional
pada tekanan atmosfer atau tekanan rendah. Efisiensi proses destilasi
tergantung pada titik didih senyawa yang ingin dimurnikan serta
pengotornya. Apabila pengotor bersifat non-volatil maka destilasi
sederhana sudah cukup tetapi apabila pengotor bersifat volatil maka
destilasi perlu dilakukan bertahap menggunakan kolom yang efisien
(Armarego & Perrin, 2000).
2. Presipitasi
Menurut Noor (2002), presipitasi adalah salah satu metode langsung
pemisahan solut, dalam proses ini dihasilan produk non-kristal yang
14
Prinsip pemisahannya adalah dengan pengaturan kondisi lingkungan
seperti suhu, pH, konstanta dielektrik, kekuatan ion atau komposisi.
Salah satu cara paling mudah dalam teknik kristalisasi adalah ketika
suatu komponen sangat larut dalam pelarut pertama dan tidak larut dalam
pelarut kedua. Penambahan secara sedikit demi sedikit pelarut kedua pada
larutan yang mengandung bahan dan pelarut pertama akan menyebabkan
terbentuknya kristal karena kelarutan bahan menjadi menurun. Ada
beberapa kelemahan dari teknik ini, pertama kedua pelarut harus
bercampur, kedua bahan yang dikristalisasi harus memiliki kelarutan
seperti disebutkan sebelumnya (Mayo, 2001).
3. Kromatografi
Ada beberapa jenis kromatografi yang dapat digunakan, yaitu :
1. Low Preasure Liquid Chromatography (LPLC)
Pada metode ini, separasi berlangsung melalui distribusi selektif pada
fase mobile berupa pelarut organik dan fase stasioner dapat berupa
silika gel, alumina, polistyrene. Separasi didasarkan pada perbedaan
afinistas adsorpsi dari molekul pada permukaan fase stasioner, yang
dipengaruhi oleh ikatan hidrogen, ikatan van der walls, interaksi dipol,
sifat asam-basa (Reld dan Sarker dalam Sarker et al. 2006).
2. Ion-exchange Chromatography
Proses ion-exchange didasarkan pada ikatan reversible molekul kation
atau anion pada resin matriks insoluble melalui pertukaran ion yang
berlawanan. Pemilihan jenis resin dan pengaturan kondisi pH dapat
dilakukan untuk memilih molekul yang akan diionisasi (Durham dalam
Sarker et al. 2006).
3. High-Speed Counter Current Chromatography
Metode ini digunakan untuk mengisolasi komponen yang tidak stabil
atau sensitif. Media yang akan kontak dengan sampel terdiri dari pelarut
dan tabung Teflon. Pelarut yang digunakan dalam sistem dua-fase yang
digunakan disesuaikan dengan sampel yang ingin diisolasi (McApline
4. High Performance Liquid Chromatography (HPLC)
HPLC terdiri dari fase stasioner, instrument dan pelarut yang
digunakan. Purifikasi komponen menggunakan HPLC biasanya
menggunakan salah satu dari empat tipe berikut : normal-phase,
reversed-phase, gel permeation gel dan ion exchange kromatografi. Tipe ini ditentukan oleh fase stasioner dan kolom preparative yang
digunakan (Latif dalam Sarker et al. 2006).
2.4 Penelitian Terdahulu
Penelitian mengenai senyawa limonoid telah banyak dilakukan untuk
beberapa tujuan yaitu menghilangkan rasa pahit pada sari jeruk, menandai
taksonomi dari tanaman jeruk karena setiap varietas tanaman jeruk memiliki
kandungan dan jenis senyawa limonoid yang khas. Dewasa ini, penelitian
mengenai senyawa limonoid terutama limonin dilakukan untuk mengisolasi
dan memproduksi limonin dari jeruk karena diketahui limonin memiliki
aktivitas biologis sebagai senyawa anti kanker dan permintaan akan senyawa
ini semakin meningkat. Beberapa hasil penelitian mengenai limonin disajikan
pada Tabel 2.
Tabel 2. Beberapa penelitian tentang limonin
No Peneliti, tahun Hasil Penelitian
1 Konno et al.
1982
Penambahan 0,5% β-siklodekstrin mampu mengurangi rasa
pahit sampai setengahnya, berdasarkan pengukuran
menggunakan NMR β-siklodekstrin membentuk kompleks
dengan senyawa limonin dan naringin.
2 Mitchell, 1985 Paten proses pengurangan kandungan limonin dan naringin
menggunakan resin anion exchange basa lemah dengan
matrik polimer stirene yang mengandung gugus fungsional
turunan mono atau poli amine. Paten ini diberi judul
“Upflow Ion Exchange Treatment Of Natural Edible Juices
Containing High Acidity And Suspended Solids”. Perlakuan
ion exchange juga mengurangi kandungan asam pada sari
jeruk tetapi tidak mempengaruhi kandungan nutrisi atau
16
Tabel 2. Lanjutan
3 Ozaki et al. 1990 Pengukuran konsentrasi limonoid glukosida pada bagian biji
beberapa varietas jeruk yaitu grapefruit (Citrus paradisi),
lemon (C limon), jeruk Valencia (C. sinensis), tangerine (C
reticulata), Fukuhara (C sinensis Osbeck Hort.),
Hyuganatsu (C tamurana Hort. ex Tanaka), Shimamikan
(C. kinokuni Hort. Ex Tanaka) dan Sanbokan (C. sideata
Hort. ex Takahashi). Semua biji jeruk tersebut mengandung
17 –D-glukopiranosida dari limonin, nomilin, obakunon,
deasetilnomilin, asam nomilinat dan asam deasetilnomilinat.
Kandungan total limonoid glukosida berkisar antara 0,31 to
0,87% dari biji jeruk kering. Kandungan nomilin glukosida
tertinggi terdapat pada biji.
4 Pifferi et al. 1993 Ekstraksi limonin dari biji lemon dengan metode soxhletasi
bertahap menggunakan pelarut petroleum eter diikuti
dengan aseton, menghasilkan limonin sebesar 0,732 mg/g
biji lemon kering.
5 Ifuku et al. 1998 Paten produksi limonoid glukosida menggunakan
supercritical fluida dimana larutan yang mengandung
limonid glukosida diletakkan di dalam tangki ekstraksi dari
peralatan supercritical karbondioksida yang dioperasikan
selama 20 menit dengan laju 4 gram per menit pada suhu
40oC dan tekanan 300 kg/cm2 untuk menghilangkan
pengotor dari limonoid glukosida.
6 Yu, J. 2004 Ekstraksi limonin aglikon dan glukosida dari biji grapefruit
menggunakan supercritical CO2 pada kondisi optimum
tekanan -48,3 MPa selama 60 menit, kecepatan alir 5
l/menit, menghasilkan rendemen limonin 6,3 mg
limonin/biji grapefruit kering, ekstraksi limonin glukosida
pada kondisi optimum tekanan -42 Mpa, 45% etanol selama
40 menit, kecepatan alir 5 l/menit menghasilkan rendemen
Tabel 2. Lanjutan
7 Manners dan
Breksa, 2006
Paten mengenai produksi dan isolasi senyawa limonoid dari
jeruk menggunakan kromatografi ion exchange anion (amin
kuartener) kuat.
8 Dandekar et al.
2007
Ekstraksi hidrotropik menggunakan dua hidrotrop yaitu
garam natrium salisilat (Na-Sal) dan natrium cumene
sulfonat (Na-CuS) dengan rancangan percobaan
menggunakan analisis respon permukaan (Response Surface
Analysis–RSA) dengan rancangan Box-Behnken. Ekstraksi
dilakukan dengan variabel konsentrasi larutan hidrotrop,
suhu ekstraksi dan persen bahan yang diekstrak. Hasil
penelitian menunjukkan rendemen limonin paling tinggi
diperoleh pada kondisi konsentrasi larutan 2 M, suhu 45oC
dan persen bahan 10% dimana larutan Na-CuS
menghasilkan limonin 0,65 mg/g biji jeruk sedangkan
larutan Na-Sal menghasilkan 0,46 mg/g biji jeruk.
9 Breksa & Dragull, 2008
Pemisahan limonin dari limonoid glukosida menggunakan
18
III. METODOLOGI PENELITIAN 3.1 Kerangka Pemikiran
Limonin memiliki manfaat bagi kesehatan, diantaranya dapat
menghambat pertumbuhan tumor, menurunkan rasio kolesterol LDL/HDL,
mengurangi resiko penyakit penyumbatan pembuluh darah karenanya limonin
memiliki nilai ekonomi yang tinggi. Limonin terdapat pada semua bagian
buah jeruk seperti biji, kulit ari dan sari jeruk dengan kandungan terbesar
terdapat pada bagian jeruk yang tidak dapat dimakan yaitu biji jeruk. Oleh
karena itu, limbah pembuatan sari jeruk berpotensi sebagai sumber bahan
baku untuk isolasi limonin dan diharapkan dapat memberikan nilai tambah
pada industri pembuatan sari jeruk.
Isolasi limonin dilakukan dari limbah pembuatan sari jeruk meliputi air
backwash, kulit ari dan biji jeruk. Kandungan limonin pada permeat dan retentat hasil mikrofiltrasi sari jeruk rendah sehingga menimbulkan dugaan
bahwa limonin tertahan pada membran karena membentuk senyawa
kompleks. Pencucian membran dengan metode backwash dilakukan untuk
membersihkan membran, mengembalikan fluksi membran serta memperoleh
limonin yang tertahan pada permukaan membran. Isolasi limonin dari air
backwash dilakukan dengan dua metode metode ekstraksi endapan dari hasil
sentrifugasi air backwash dan ekstraksi cair-cair dari air backwash. Ekstraksi
endapan menggunakan pelarut yaitu diklorometan dan aseton, sedangkan
ekstraksi cair-cair menggunakan pelarut diklorometan. Isolasi limonin dari
biji dan kulit ari dilakukan dengan ekstraksi soxhletasi bertahap
menggunakan pelarut heksan kemudian aseton. Pengukuran kandungan
limonin dalam air backwash, kulit ari dan biji jeruk dilakukan dengan metode
spektrofotometri.
Selanjutnya isolasi limonin dilakukan dari bahan dengan kandungan
limonin paling tinggi yaitu biji jeruk. Optimasi proses ekstraksi dilakukan
pada tahap presipitasi dengan metode respon permukaan atau response
19
dua faktor yaitu rasio volume ekstrak aseton dengan pelarut heksan serta lama
presipitasi.
3.2 Tempat dan Waktu Penelitian
Penelitian telah dilaksanakan pada bulan April sampai Oktober 2009
di Laboratorium di lingkungan Departemen Teknologi Industri Pertanian,
Fakultas Teknologi Pertanian IPB dan Laboratorium di lingkungan Balai
Besar Pasca Panen Departemen Pertanian.
3.3 Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah :
1. Bahan baku berupa jeruk Pontianak
2. Bahan kimia untuk esktraksi limonin yang terdiri dari heksan, aseton,
diklorometan, isopropanol.
3. Bahan kimia untuk analisis yang terdiri dari : etanol PA, 4-dimethylamino
benzaldehide, asam asetat glasial, asam perklorat, kloroform, limonin standar, dan acetonitrile.
Peralatan yang digunakan dalam penelitian ini adalah pulper,
penyaring ukuran 65 mesh, 150 mesh dan 200 mesh, membran mikrofiltrasi
polipropilen (ukuran 0,1 µm), spektrofotometer, alat sentrifugasi, rotary
evaporator vakum, termometer, oven, timbangan analitik, corong pemisah, perangkat ekstraksi soxhlet dan alat-alat gelas.
3.4 Tahapan Penelitian
Penelitian ini terdiri dari penelitian pendahuluan dan penelitian utama,
penelitian pendahuluan terdiri dari empat tahap, dengan tahapan penelitian
sebagai berikut :
1. Penelitian Pendahuluan
Tahap 1. Persiapan Bahan Baku
Bahan baku yang digunakan adalah jeruk Pontianak (Citrus nobilis L. var
20
20
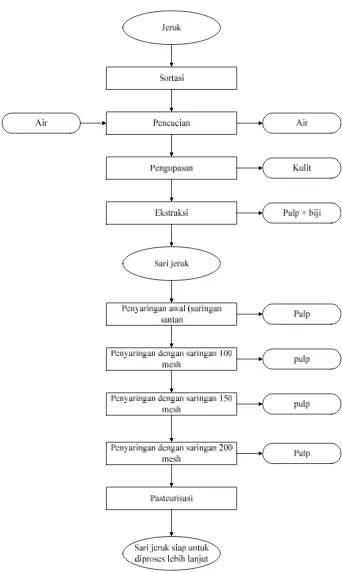
1. Sortasi
Sortasi bertujuan untuk memisahkan buah yang digunakan agar diperoleh
buah jeruk yang baik dan tidak busuk.
2. Pencucian dan Pengupasan Kulit Buah
Pencucian bertujuan untuk membersihkan kulit buah dari kotoran-kotoran
seperti tanah dan lumpur serta sisa pestisida yang melekat. Selanjutnya
dilakukan pengupasan kulit buah agar minyak yang terkandung di dalam
kulit tidak terbawa ke dalam sari buah.
3. Ekstraksi
Jeruk yang telah dicuci dan dikupas selanjutnya dimasukkan ke dalam
mesin pulper untuk memperoleh sari jeruk. Sari jeruk ditampung di dalam
wadah, sedangkan ampasnya yang berupa biji dan pulp langsung terpisah.
4. Penyaringan
Penyaringan dilakukan untuk memisahkan serat, pulp serta biji yang dapat
menghambat proses pemisahan dengan membran mikrofiltrasi. Penyaringan
dilakukan dalam beberapa tahap, yaitu :
- Penyaringan pertama dilakukan menggunakan saringan santan
- Penyaringan kedua dilakukan menggunakan saringan 100 mesh.
- Penyaringan ketiga menggunakan saringan 150 mesh.
- Penyaringan keempat menggunakan saringan 200 mesh.
5. Pasteurisasi
Pasteurisasi sari jeruk bertujuan untuk inaktivasi enzim dan membunuh
mikroorganisme yang dapat menyebabkan fermentasi dan kerusakan pada
sari jeruk. Pada penelitian ini, pasteurisasi dilakukan menggunakan suhu
70ºC selama 10 menit.Diagram proses persiapan bahan baku disajikan pada
Gambar 6.
Tahap 2. Mikrofiltrasi Sari Jeruk
Penyaringan sari jeruk dilakukan menggunakan membran mikrofiltrasi yang
dilakukan pada kondisi operasi laju alir 0,08 m/det yang didasarkan pada
hasil penelitian Agihitsni (2008). Skema proses mikrofiltrasi sari jeruk
21
22 22 E-1 E-2 V-1 P I-1 E-3 V-2 P I-2 V-3 V-4 V-5 V-6 V-7 S1 S2 S3 T1 T2 S4 Keterangan :
E-1 = tangki umpan E-2 = pompa
E-3 = membran ultrafiltrasi I-1 = pressure gauge in I-2 = pressure gauge out
V-1, V-2 = katup pengatur tekanan dan laju alir V-3, V-4, V-5 = three way valve
V-6 = katup sampling permeat V-7 = katup sampling retentat S1,S2,S3,S4 = Selenoid
T1, T2 = timer elektronik
[image:38.595.115.482.64.280.2]Selenoid merupakan valve elektronik, timer T1 mengatur S1 dan S3 yang merupakan pengatur selang periode (frekuensi) backwash, sedangkan timer T2 mengatur S1 dan S2 yang menentukan lamanya (durasi) backwash
Gambar 7.Skema proses mikrofiltrasi sari jeruk
Sumber : Noor et al. (2007)
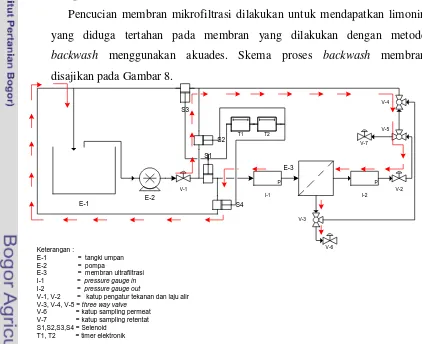
Tahap 3. Backwash Membran Mikrofiltrasi
Pencucian membran mikrofiltrasi dilakukan untuk mendapatkan limonin
yang diduga tertahan pada membran yang dilakukan dengan metode
backwash menggunakan akuades. Skema proses backwash membran disajikan pada Gambar 8.
Gambar 8.Skema proses backwash membran
Sumber : Noor et al (2007)
E-1 E-2 V-1 P I-1 E-3 V-2 P I-2 V-3 V-4 V-5 V-6 V-7 Keterangan :
E-1 = tangki umpan E-2 = pompa
E-3 = membran mikrofiltrasi I-1 = pressure gauge in I-2 = pressure gauge out
V-1, V-2 = katup pengatur tekanan dan laju alir V-3, V-4, V-5 = three way valve
[image:38.595.84.506.347.691.2]23 Tahap 4. Isolasi Limonin
Isolasi limonin dilakukan pada air backwash, kulit ari dan biji jeruk.
a. Isolasi Limonin Dari Air Backwash
Ekstraksi limonin dari air backwash dilakukan dengan dua metode :
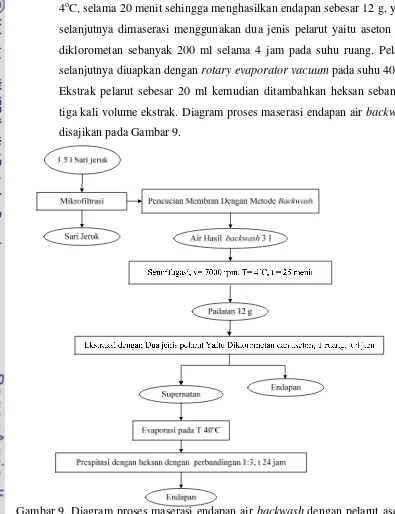
1. Metode pertama adalah maserasi endapan air backwash. Pada metode ini,
air backwash sebanyak 3 liter disentrifugasi pada 7000 rpm pada suhu
4oC, selama 20 menit sehingga menghasilkan endapan sebesar 12 g, yang
selanjutnya dimaserasi menggunakan dua jenis pelarut yaitu aseton dan
diklorometan sebanyak 200 ml selama 4 jam pada suhu ruang. Pelarut
selanjutnya diuapkan dengan rotary evaporatorvacuum pada suhu 40 oC.
Ekstrak pelarut sebesar 20 ml kemudian ditambahkan heksan sebanyak
tiga kali volume ekstrak. Diagram proses maserasi endapan air backwash
[image:39.595.97.492.208.722.2]disajikan pada Gambar 9.
Gambar 9. Diagram proses maserasi endapan air backwash dengan pelarut aseton
24
24
2. Metode ekstraksi cair-cair menggunakan pelarut diklorometan dengan
menggunakan corong pemisah. Ekstraksi 2 liter air backwash dengan 100
ml dengan diklorometan dilakukan menggunakan corong pemisah dimana
200 ml air backwash ditambahkan dengan 100 ml pelarut selanjutnya
dilakukan pengocokan supaya limonin yang terdapat pada fase air dapat
pindah ke fase diklorometan. Kemudian didiamkan selama 15 menit
sampai terbentuk dua fase dimana bagian bawah adalah diklorometan dan
bagian atas adalah air. Kedua fase tersebut lalu dipisahkan kemudian fase
diklorometan dipresipitasi dengan cara ditambahkan heksan sebanyak tiga
kali volume pelarut lalu didiamkan selama 20 jam pada suhu refrigerasi.
Ekstraksi air backwash dengan metode ekstraksi cair-cair disajikan pada
Gambar 10.
Gambar 10. Diagram proses ekstraksi air backwash dengan metode ekstraksi
cair-cair
b. Isolasi limonin dari biji, kulit ari dan pulp jeruk
Isolasi limonin juga dilakukan dari bagian jeruk yang lain yang diduga
mengandung limonin seperti biji jeruk dan kulit ari, sisa penyaringan jeruk
tahap awal (pulp) jeruk. Biji jeruk dan kulit ari dikeringkan menggunakan
oven blower suhu 50oC sampai berat kedua bahan tersebut konstan
kemudian dilakukan pengecilan ukuran menggunakan hammer mill.
Selanjutnya biji dan kulit ari jeruk diekstraksi secara bertahap, tahap
pertama menggunakan heksan yang bertujuan untuk menghilangkan
25
jeruk, tahap kedua menggunakan aseton yang bertujuan untuk
mengekstrak limonin dengan menggunakan perangkat ekstraksi soxhlet.
Proses isolasi dilakukan dengan 2 cara yaitu dengan pencucian etanol dan
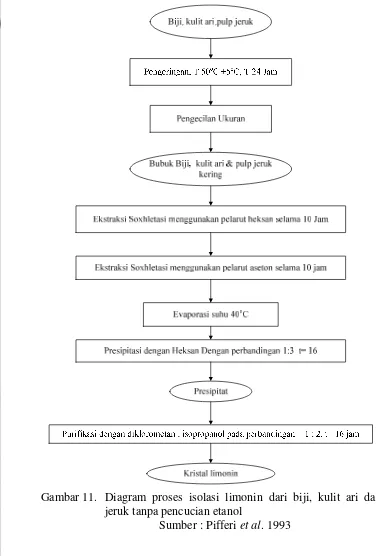
tanpa pencucian etanol. Diagram proses isolasi limonin dari biji, kulit ari
[image:41.595.101.477.189.745.2]dan pulp jeruk tanpa pencucian etanol disajikan pada Gambar 11.
Gambar 11. Diagram proses isolasi limonin dari biji, kulit ari dan pulp
jeruk tanpa pencucian etanol
26
26
Diagram proses isolasi limonin dari biji, kulit ari dan pulp jeruk dengan
[image:42.595.109.450.126.710.2]pencucian menggunakan etanol disajikan pada Gambar 12.
Gambar 12. Diagram proses isolasi limonin dari biji, kulit ari dan pulp jeruk
dengan pencucian etanol
27
2. Penelitian Utama
Pada penelitian utama dilakukan optimasi proses isolasi limonin dari
bahan baku dengan kandungan limonin paling tinggi yaitu biji jeruk dengan
metode ekstraksi tanpa pencucian dengan etanol. Optimasi dilakukan pada
tahap proses presipitasi dengan dua faktor yaitu rasio ekstrak aseton dan
pelarut heksan dengan rentang 1:3 – 1:5 (v/v) dan lama presipitasi pada
rentang waktu 16-24 jam. Presipitasi dilakukan pada kondisi suhu refrigerasi.
Diagram proses optimasi isolasi limonin dari biji jeruk siam disajikan pada
Gambar 13.
3.5 Rancangan Percobaan
Rancangan percobaan optimasi ekstraksi limonin menggunakan
metode permukaan respon (respon surface method). Faktor yang dianalisis ada
dua yaitu:
1. Rasio volume ekstrak aseton : pelarut heksan dengan rentang 1:3 – 1:5
(v/v)
2. Lama presipitasi dengan rentang 16-24 jam.
Dengan basis percobaan 81 gram biji jeruk kering.
Desain rancangan percobaan disajikan pada Tabel 2.
Tabel 3. Desain rancangan percobaan
No. Rasio volume
pelarut heksan Lama presipitasi (jam)
Kode Variabel
X1 X2
1 3 16 -1 -1
2 5 24 1 -1
3 3 16 -1 1
4 5 24 1 1
5 2,6 20 -1.41 0
6 5,4 20 1.41 0
7 4 14 jam 21 menit 0 -1.41
8 4 25 jam 40 menit 0 1.41
9 4 20 0 0
28
28
Respon utama (parameter) yang dianalisis adalah konsentrasi limonin
yang diperoleh (Y). Model rancangan percobaan faktorial untuk mengetahui
pengaruh dari kedua faktor terhadap respon yang diinginkan adalah sebagai
berikut:
2 1 5 2 2 4 2 1 3 2 2 1 1
0
a
x
a
x
a
x
a
x
a
x
x
a
Y
=
+
+
+
+
+
Keterangan :
Y = Jumlah limonin (mg)
a0, a1, a2, a3, a4, a5 = Koefisien regresi
X1 = Pengaruh linier faktor rasio volume ekstrak aseton
dan heksan
X2 = Pengaruh linier faktor lama presipitasi
X1X2 = Pengaruh linier interaksi faktor rasio volume
ekstrak aseton dan heksan serta lama presipitasi
X12 = Pengaruh kuadratik faktor rasio volume ekstrak
aseton dan heksan
29 Biji jeruk
Pengeringan, T 50oC ±5oC, T 24 Jam
Pengecilan Ukuran
Ekstraksi Dengan aseton Menggunakan Soxhlet Selama 10 Jam
Evaporasi Suhu 40OC
Optimasi Presipitasi Dengan Faktor Rasio Ekstrak Aseton : Pelarut Heksan = 1:301:5 Dan Lama Presipitasi 16024 Jam
Kristal limonin
Ekstraksi dengan heksan Menggunakan Soxhlet Selama 10 Jam
Purifikasi dengan diklorometan : isopropanol = 1 : 3, t=16 jam Presipitat
[image:45.595.88.504.83.775.2]Bubuk Biji jeruk kering
Gambar 13. Optimasi proses isolasi limonin dari biji jeruk
30
IV. HASIL DAN PEMBAHASAN
4.1 Isolasi Limonin dari Air Backwash, Kulit Ari, Biji dan Sisa Penyaringan Awal (Pulp)
Berdasarkan hasil penelitian Setyadjit (2006) terhadap beberapa
varietas jeruk yang beredar di Indonesia, konsentrasi limonin paling tinggi
terdapat pada sari jeruk nipis yaitu 16,25 µg ml-1, sari jeruk siam menempati
tempat kedua dengan kandungan limonin sebesar 13,70 µg ml-1, kemudian sari
jeruk Medan, 4,30µg ml-1, sari jeruk Argentina 3,13 µg ml-1 sedangkan sari
jeruk sunkist tidak mengandung limonin.
Mikrofiltrasi sari jeruk yang didasarkan pada penelitian Aghitsni (2008)
telah berhasil menghilangkan rasa pahit pada sari jeruk dimana kandungan
limonin pada sari jeruk hasil mikrofiltrasi yaitu permeat dan retentat berada di
bawah batasan konsentrasi yang dapat diterima konsumen yaitu 6 7g ml-1
(Mozaffar 1998). Konsentrasi limonin pada permeat dan retentat disajikan
pada Tabel 4.
Tabel 4. Konsentrasi limonin dalam permeat, retentat dan air backwash
Hasil analisis kandungan limonin pada Tabel 4 menunjukkan
kandungan limonin pada sari jeruk berbeda dengan hasil penelitian Setyadjit
(2006), hal ini bisa dikarenakan perbedaan masa panen jeruk siam dimana
jeruk siam yang dipanen pada musim kemarau memiliki kandungan limonin
lebih tinggi. Limonin merupakan metabolit sekunder dan diduga
kandungannya akan semakin tinggi apabila jeruk menerima tekanan dari
lingkungan sekitar.
Penurunan kandungan limonin pada permeat maupun retentat hasil
mikrofiltrasi menimbulkan dugaan senyawa-senyawa tersebut tertahan di
dinding membran. Tertahannya limonin dan naringin pada membran juga
Konsentrasi (ppm)
Sari jeruk 13,061
Permeat 2,347
Retentat 3,980
ditunjukkan oleh konsentrasi keluaran di retentat yang tidak jauh berbeda
dengan konsentrasi pada permeat, diduga limonin membentuk lapisan cake
pada permukaan membran akibat polarisasi konsentrasi. Untuk memperoleh
limonin yang diduga tertahan pada membran dilakukan pencucian membran
dengan metode backwash menggunakan akuades. Air backwash selanjutnya
dianalisis dengan metode spektrofotometer berdasarkan metode Abbasi et al.
(2005) yang telah dimodifikasi oleh Setyadjit (2005). Analisis limonin dari air
backwash menunjukkan bahwa air backwash mengandung limonin sebesar 5,715 ppm karenanya pada penelitian pendahuluan dilakukan isolasi limonin
dari air backwash.
Mikrofiltrasi juga menghasilkan produk samping seperti biji jeruk, kulit
ari dan sisa penyaringan awal (pulp) yang juga diduga mengandung limonin.
Oleh karena itu pada penelitian pendahuluan dilakukan isolasi limonin dari
biji jeruk, kulit ari dan pulp. Analisis limonin dilakukan menggunakan alat
spektrofotometer berdasarkan metode Abbasi et al. (2005) yang telah
dimodifikasi oleh Setyadjit (2005). Meskipun jumlah laporan yang
menggunakan metode spektrofotometri untuk analisis limonin relatif sedikit
tetapi metode ini memiliki kelebihan yaitu sederhana sehingga mudah
diaplikasikan misalnya pada proses pengawasan mutu pada industri
pembuatan sari jeruk (Abbasi et al. 2005). Metode ini menggunakan pelarut
kloroform untuk menghilangkan senyawa polar pada bahan yang dianalisis
serta menggunakan reagen burham yang terdiri dari asam asetat glasial, asam
perklorat dan 4-dimetilaminobenzaldehid, yang bereaksi dengan limonin
menghasilkan warna kuning-orange sampai merah yang kemudian diamati
nilai absorbansinya pada panjang gelombang 503 nm. Masing-masing
senyawa limonoid dibedakan dari komponen yang terikat pada cincin A dan
D, sehingga diduga reagen burham bereaksi secara spesifik dengan cincin A
dan D dari limonin yang merupakan senyawa lakton. Semakin tinggi
kandungan limonin, warna yang dihasilkan semakin mendekati warna merah
dan nilai absorbansi semakin tinggi. Menurut Harris (1999), pada panjang
gelombang 470-500, warna yang diserap adalah biru-hijau dan warna yang
32
[image:48.595.153.457.125.500.2]Struktur molekul limonin dan beberapa turunannya disajikan pada
Gambar 14.
Gambar 14. Struktur molekul limonin dan beberapa turunannya
Sumber : Maier et al. dalam Nagy et al. (1977); Li (2000)
1. Isolasi Limonin dari Air Backwash.
Isolasi limonin dari air backwash dilakukan dengan dua metode yaitu
ekstraksi maserasi sludge hasil sentrifugasi air backwash dan ekstraksi
cair-cair.
a. Ekstraksi Maserasi Endapan Hasil Sentrifugasi Air Backwash
Limonin tidak larut dalam air karenanya dilakukan sentrifugasi pada
air backwash yang bertujuan untuk mengendapkan limonin. Sentrifugasi memanfaatkan adanya perbedaan densitas antara padatan dan cairan. Bila
suspensi dibiarkan maka padatan yang mempunyai densitas lebih besar
pengendapan ini dapat dipercepat dengan adanya gaya sentrifugal dengan
proses sentrifugasi (Noor, 2002). Sentrifugasi air backwash dilakukan
dengan kecepatan 7000 rpm suhu 4oC selama 20 menit. Hasil sentrifugasi
3 liter air backwash diperoleh endapan sebesar 12 gram. Endapan
selanjutnya dimaserasi, pertama menggunakan pelarut aseton dan kedua
menggunakan diklorometan, pada kondisi suhu ruang selama 4 jam.
Perangkat ekstraksi dilengkapi dengan magnetik stirer untuk mempercepat
proses ekstraksi serta pendingin balik untuk mencegah pelarut menguap.
[image:49.595.236.439.276.548.2]Maserasi hasil sentrifugasi disajikan pada Gambar 15.
Gambar 15. Ekstraksi maserasi hasil sentrifugasi