2
1 PENDAHULUAN
1.1Latar Belakang
Tumbuhan air memiliki kemampuan reproduksi secara anakkan maupun tunas rimpang dengan kecepatan reproduksi yang tinggi sehingga tumbuhan air sering dianggap sebagai gulma. Salah satu jenis tumbuhan air adalah genjer (Limnocharis flava L. Buchenau). Genjer dianggap sebagai gulma air di sawah dan menghalangi saluran air untuk irigasi. Masyarakat setempat umumnya menggunakan genjer sebagai sumber makanan dan untuk meningkatkan ekonomi mereka (Tawan et al. 2007). Genjer merupakan tanaman yang biasa dikonsumsi masyarakat. Genjer tumbuh di rawa atau kolam berlumpur yang banyak airnya. Gejer berasal dari daerah tropis Amerika, tetapi dapat tumbuh liar di daerah panas lainnya. Selain daunnya, bunga genjer muda juga enak dijadikan masakan. Tumbuh-tumbuhan diketahui kaya dengan antioksidan misalnya vitamin C, beta karoten, vitamin E, dan flavonoid (Alfa 2003).
Sayuran berdaun telah dilaporkan memiliki peran penting dalam nutrisi manusia, terutama sebagai sumber vitamin (A, B, C, E), mineral, dan serat makanan (Almatsier 2004). Nilai gizi sayuran bervariasi sesuai dengan faktor lingkungan, perbedaan varietas, praktek budidaya, tahap pemanenan tanaman, metode penyimpanan, pengolahan, dan persiapan (Flyman dan Afolayan 2008). Salah satu sumber vitamin yang banyak terdapat pada sayuran hijau adalah vitamin C. Vitamin C merupakan vitamin yang paling mudah rusak karena mudah teroksidasi dan proses tersebut dipercepat oleh panas, sinar, alkali, enzim, oksidator serta oleh katalis tembaga dan besi. Oksidasi akan terhambat apabila vitamin C dibiarkan dalam kondisi asam atau suhu rendah (Winarno 2008).
2
Penelitian mengenai tumbuhan air khususnya genjer, baik kandungan gizi maupun pengaruhnya setelah proses pemasakan saat ini masih sedikit. Informasi ini diperlukan dalam bidang pendidikan sebagai sumber informasi ilmiah. Salah satu informasi penting yang perlu diketahui adalah jumlah vitamin dan mineral pada genjer baik sebelum maupun setelah proses pemasakan.
Genjer umumnya dikonsumsi masyarakat melalui proses pemasakan (pengukusan) dan penambahan bumbu. Pemasakan atau pengukusan bahan makanan akan mempengaruhi kelarutan nilai gizi bahan makanan tersebut, termasuk kandungan vitaminnya (Haris dan Karmas 1989). Dengan adanya informasi kandungan gizi genjer khususnya vitamin C dan kandungan mineral, baik pada genjer segar maupun setelah mengalami proses pemasakan (pengukusan), maka diharapkan pemanfaatan genjer ke depan sebagai bahan pangan akan lebih optimal.
1.2 Tujuan
3
2 TINJAUAN PUSTAKA
2.1 Deskripsi dan Klasifikasi Genjer (L. flava)
Genjer di Indonesia ditemukan di Pulau Sumatra dan Jawa. Genjer di Jawa terdapat di dataran rendah bagian barat sampai dengan ketinggian ±1300 m di atas permukaan laut. Menurut Heyne (1987) genjer digunakan sebagai makanan ternak babi di Daerah Toba. Tanaman genjer juga dapat dimanfaatkan menjadi bahan makanan yaitu salah satu jenis sayuran. Daun-daun muda dan bunga majemuk yang belum mekar merupakan sayuran yang sering dijual pada pasar-pasar tradisional di Daerah Jawa Barat. Morfologi tanaman genjer disajikan pada Gambar 1. Klasifikasi tanaman genjer menurut Plantamor (2008) adalah sebagai berikut:
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh) Super Divisi : Spermatophyta (Menghasilkan biji) Divisi : Magnoliophyta (Tumbuhan berbunga) Kelas : Liliopsida (berkeping satu atau monokotil) Sub Kelas : Alismatidae
Ordo : Alismatales Famili : Limnocharitaceae Genus : Limnocharis Spesies : L. flava (L.) Buch
Gambar 1 Tanaman genjer (L. flava)
4
bunganya sehingga terbentuk akar pada ujungnya. Tanaman tersebut berumur lebih dari 1 tahun. Jenis sayur tersebut tumbuh luas merumpun, tinggi sekitar 30-80 cm. Daun berbentuk bulat telur, tebal berisi dengan tangkai daun yang panjang, berwarna hijau muda, bersisi tiga, sisi belakang ujung daun berpori air dengan tepi berwarna keunguan, dan panjang daunnya berkisar 7,5-27 cm (Heyne 1987).
Tanaman genjer merupakan tumbuhan yang hidup bertahun-tahun, tegak tanaman akuatik hingga rawa-terestrial, memiliki ketinggian 20 cm hingga 100 cm. Batang tanaman memiliki panjang 5-7,5 cm, tebal, berbentuk segitiga dengan banyak ruang udara, terdapat pelipis pada bagian dasar. Helaian daun bulat, luasan berbentuk bulat panjang atau bulat telur berukuran 5-30 cm x 4-25 cm, berwarna kuning-hijau, bergurat, 9-13 gurat utama dengan sejumlah gurat paralel melintang yang bertindak sebagai gurat sekunder (Bergh 1994).
Bunga berjumlah 3 hingga 15, panjang ibu tangkai bunga mencapai 90 cm, tegak, ketika berbunga, melengkung ketika berbuah, bunga di dalam axil dari tanaman berselaput. Kelopak bunga berjumlah 3 dengan panjang 2 cm, mahkota berjumlah 3 dengan bentuk bulat telur hingga bulat dan panjang 1,5-3 cm, tertutup oleh kelopak. Biji berbentuk seperti sepatu kuda dengan panjang 1-1,5 mm, dilengkapi dengan mahkota yang melintang, berwarna coklat gelap. Kotiledon memiliki panjang 8-11,5 mm (Bergh 1994).
Tanaman genjer dapat bereproduksi secara vegetatif maupun dengan biji. Biji yang tekandung dalam kapsul matang atau tolikel merupakan biji yang ringan dan dapat disebarkan oleh aliran air. Reproduksi secara vegetatif yakni, kapsul yang menekuk ke arah air, menyediakan biji-bijian untuk dilepas. Kapsul yang kosong dapat berkembang menjadi tanaman vegetatif yang membentuk tanaman inang atau mengapung untuk menetap di tempat lain. Tanaman ini selalu berbunga sepanjang tahun di wilayah dengan kelembaban yang cukup. Namun tanaman ini dapat menjadi tanaman tahunan dimana kelembaban bersifat musiman (Departement of Primary Industries and Fisheries 2007).
5
epidermis terdapat korteks yang tersusun tidak beraturan. Jaringan korteks terletak di bagian dalam epidermis yang tersusun dari beberapa lapis sel berkloroplas serta jaringan pembuluh pengangkut yang tersebar. Jaringan korteks ke arah tengah daun berkembang dan membentuk ruang antar sel yang besar sebagai tempat untuk pertukaran dan penyimpanan udara.
Daun tanaman genjer tersusun atas jaringan epidermis, jaringan dasar (mesofil), jaringan pengangkut, dan jaringan penguat. Permukaan atas dan bawah daun genjer dilapisi oleh jaringan epidermis. Sel penyusun epidermis tanaman genjer memiliki bentuk tidak beraturan dan memanjang serta tersusun dengan rapat. Permukaan epidermis sering dilapisi oleh kutikula atau rambut halus (pilus), untuk melindungi daun dari serangan pemangsa, spora jamur atau tetesan air hujan (Wardana 2012).
2.2 Kandungan Gizi pada Sayuran
Sayuran merupakan salah satu jenis pangan yang mengandung berbagai zat gizi yang sangat diperlukan oleh tubuh untuk melakukan berbagai aktivitas. Zat gizi tersebut adalah karbohidrat, lemak, protein, vitamin, mineral, dan air. Vitamin dan mineral merupakan zat gizi utama yang terkandung dalam sayuran dan buah, sedangkan zat gizi lainnya umumnya terdapat dalam jumlah yang tidak terlalu banyak (Wirakusumah 2007). Zat-zat gizi menyediakan kebutuhan sel-sel tubuh yang beraneka ragam. Sel memerlukan energi, bahan-bahan pembangunan dan bahan-bahan untuk memperbaiki bagian yang rusak menggunakan zat-zat gizi (Muchtadi 2001). Kandungan gizi beberapa jenis sayuran disajikan pada Tabel 1.
6
2.2.1 Protein
Protein adalah molekul makro yang memiliki berat molekul antara lima ribu hingga beberapa juta dalton. Protein tersusun dari satuan-satuan dasar kimia yaitu asam amino yang terdiri dari unsur-unsur organik yaitu karbon, hidrogen, oksigen dan nitrogen. Beberapa asam amino mengandung unsur-unsur mineral diantaranya fosfor, besi, iodium, dan kobalt (Almatsier 2004). Protein berfungsi sebagai bahan dasar pembentuk sel-sel dan jaringan tubuh. Protein juga berperan dalam proses pertumbuhan, pemeliharaan, dan perbaikan jaringan tubuh yang mengalami kerusakan. Sayuran yang mengandung protein tinggi biasanya berasal
dari biji-bijian, seperti kacang panjang, buncis, dan kecambah (Wirakusumah 2007).
Kandungan protein pada bahan pangan dapat dianalisis menggunakan uji berdasarkan kandungan nitrogen (metode Kjeldahl). Metode ini pada prinsipnya adalah oksidasi senyawa organik oleh asam sulfat untuk membentuk karbondioksida dan air serta pelepasan nitrogen dalam bentuk amonia. Jumlah gram protein dalam bahan pangan (makanan) biasanya dihitung dalam hasil perkalian jumlah gram nitrogen dengan 6,25. Konstanta ini diperoleh dari asumsi bahwa protein mengandung 16% nitrogen dan 100/16 = 6,25 (Muchtadi 2001).
2.2.2 Lemak
Lemak merupakan persenyawaan yang terbentuk dari asam lemak dan gliserol, tersusun oleh unsur-unsur karbon (C), hidrogen (H), dan oksigen (O). Lemak mempunyai sifat dapat larut dalam pelarut organik seperti petrolium benzene, eter, dan sebagainya, tetapi tidak larut dalam air. Bentuk lemak ada dua yaitu lemak (fat) yang berupa padatan pada suhu kamar misalnya lemak hewan dan minyak (oil) yang berbentuk cairan dalam suhu kamar misalnya minyak jagung, minyak kedelai, minyak kelapa sawit dan minyak zaitun. Secara umum formulasi kimia suatu asam lemak adalah CH3(CH2)nCOOH (Muchtadi 2001). Kandungan lemak pada buah dan sayuran umumnya sedikit, lemak yang terkandung dalam pangan nabati biasanya berupa asam lemak tidak jenuh (Wirakusumah 2007).
7
lemak essensial yang penting bagi tubuh, pembawa vitamin larut lemak, pelumas diantara persendian, membantu pengeluaran sisa makanan serta pemberi kepuasan cita rasa dan agen pengemulsi (Suhardjo dan Kusharto 1988). Lemak yang terdapat pada bahan pangan nabati umumnya berupa asam lemak tidak jenuh. Fungsi dari asam lemak tak jenuh yaitu sebagai komponen dari sel-sel saraf, membran selular, dan senyawa yang menyerupai hormon. Asam lemak tidak jenuh juga berfungsi sebagai proteksi dan terapi untuk penyakit jantung serta kanker (Wirakusumah 2007).
2.2.3 Serat
Serat makanan (diatery fiber) adalah komponen dalam tanaman yang tidak tercerna secara enzimatik menjadi bagian-bagian yang dapat diserap di saluran pencernaan. Serat secara alami terdapat dalam tanaman. Serat terdiri dari berbagai substansi yang kebanyakan diantaranya adalah karbohidrat kompleks. Serat makanan dibagi menjadi dua kelompok, yaitu serat larut (soluble fiber) dan serat tidak larut (insoluble fiber). Umumnya, tanaman mengandung kedua-duanya dengan serat tidak larut pada porsi yang lebih banyak. Serat yang larut di dalam air antara lain terdiri atas pektin, getah tanaman, dan beberapa hemiselulosa. Contoh serat tidak larut adalah lignin dan selulosa (Hermaningsih 2008).
8
aromatik yang tersusun dari polimer fenil propan. Lignin bersama-sama dengan holoselulosa (gabungan selulosa dan hemiselulosa) berfungsi membentuk jaringan tanaman (Soelistijani 2005).
2.3 Vitamin
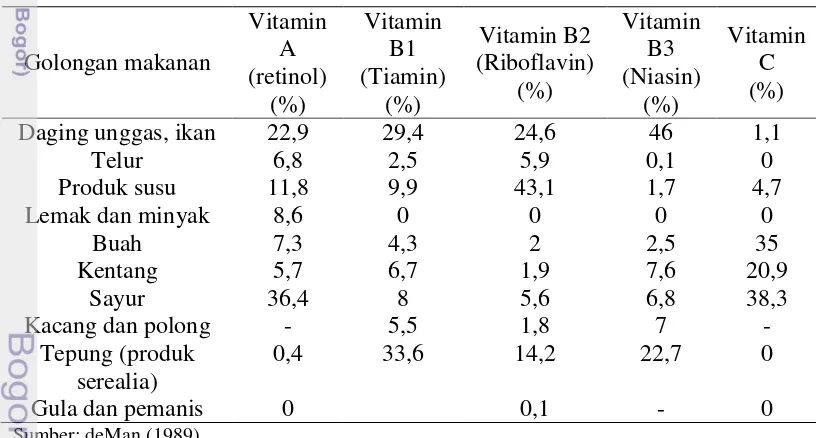
Vitamin adalah komponen tambahan makanan yang berperan sangat penting dalam gizi manusia, banyak vitamin tidak stabil pada kondisi pemrosesan tertentu dan penyimpanan, karena itu kandungan vitamin dalam makanan yang diproses dapat sangat menurun bahkan hilang. Vitamin merupakan zat-zat organik kompleks yang dibutuhkan dalam jumlah yang sangat kecil. Vitamin berperan sebagai zat pengatur yang dikelompokkan menjadi dua, yaitu vitamin larut dalam lemak ( vitamin A, D, E, dan K) dan vitamin larut dalam air (B1, B2, B3, B4, B5, B6, B12, asam folat, biotin, dan vitamin C) (Wirakusumah 2007). Kandungan vitamin pada berbagai golongan makanan dapat dilihat pada Tabel 2.
Tabel 2 Kandungan vitamin pada beberapa golongan makanan
Golongan makanan
9
vitamin. Provitamin adalah senyawa yang tidak termasuk vitamin tetapi dapat diubah menjadi vitamin. Beta karoten dapat diubah menjadi vitamin A pada dinding usus, 7-dehidrokolesterol dapat diubah menjadi vitamin D3 oleh sinar ultraviolet. Iradiasi pada tanaman dapat mengubah ergosterol menjadi vitamin D2. Asam amino triptofan bisa diubah menjadi niasin (60 mg triptofan menghasilkan 1 mg niasin) (Nasoetion 1987).
Kekurangan vitamin telah lama dikenal mengakibatkan penyakit defisiensi yang serius. Kelebihan dosis vitamin tertentu, terutama vitamin yang larut dalam lemak, dapat mengakibatkan keracunan yang serius, karena alasan ini penambahan vitamin ke dalam makanan harus dikendalikan secara hati-hati (deMan 1989). Vitamin walaupun sifatnya mikro namun memiliki peran yang penting. Untuk menguji kandungan vitamin dalam bahan pangan dapat digunakan metode kromatografi (Huyghebaert et al 2003).
2.3.1 Vitamin C
Vitamin C disebut juga asam askorbat, merupakan vitamin yang paling sederhana, mudah berubah akibat oksidasi, tetapi amat berguna bagi manusia. Struktur kimianya terdiri dari 6 rantai atom C (C6H8O6), karena mudah bereaksi dengan O2 di udara menjadi asam dehidroaskorbat. Vitamin ini merupakan fresh food vitamin karena sumber utamanya adalah buah-buahan dan sayuran segar. Sumber-sumbernya diantaranya adalah jeruk, brokoli, brussel sprout, kubis, lobak dan stroberi (Kamiensky dan Keogh 2006).
Vitamin C diproduksi oleh tumbuhan dalam jumlah yang besar. Fungsi vitamin C bagi tumbuhan adalah sebagai agen antioksidan yang dapat menetralkan singlet oksigen yang sangat reaktif, berperan dalam pertumbuhan sel,
berfungsi seperti hormon, dan ikut berperan dalam proses fotosintesis (Davey 2006). Vitamin C hanya dapat dibentuk oleh tumbuhan dan terdapat pada
sayuran serta buah-buahan dalam jumlah yang besar. Hal ini disebabkan karena tumbuhan memiliki enzim mikrosomal L-gulonolakton oksidase, sebagai komponen dalam pembentukan asam askorbat (Nasoetion & Karyadi 1987 dan Padayatty et al. 2003).
10
Vitamin C digunakan dalam metabolisme karbohidrat dan sintesis protein, lipid, dan kolagen. Vitamin C juga dibutuhkan oleh endotel kapiler dan perbaikan jaringan. Vitamin C bermanfaat dalam absorpsi zat besi dan metabolisme asam folat. Tidak seperti vitamin yang larut lemak, vitamin C tidak disimpan dalam tubuh dan diekskresikan di urin (Kamiensky dan Keogh 2006).
Kebutuhan vitamin C berdasarkan U.S. RDA antara lain untuk pria dan wanita sebanyak 60 mg/hari, bayi sebanyak 35 mg/hari, ibu hamil sebanyak 70 mg/hari, dan ibu menyusui sebanyak 95 mg/hari. Kebutuhan vitamin C meningkat 300-500% pada penyakit infeksi, TB, tukak peptik, penyakit neoplasma, pasca
bedah atau trauma, hipertiroid, kehamilan, dan laktasi (Kamiensky dan Keogh 2006).
2.3.2 Beta karoten
Beta karoten merupakan karotenoid, salah satu pigmen tanaman yang dikenal memiliki antioksidan. Zat ini cepat dikonversi menjadi vitamin A oleh tubuh. Menurut Andarwulan dan Koswara (1992), perbedaan antara satu provitamin A dengan yang lainnya terletak pada struktur cincin yang terdapat dikedua sisi rantai alifatik. Beta karoten mempunyai dua struktur cincin -ionon, α-karoten mempunyai satu struktur cincin -ionon dan sisi lainnya terdapat struktur cincin α-ionon (ikatan rangkap pada posisi 4 dan 5), -karoten pada satu sisi mempunyai struktur cincin -ionon sedangkan pada sisi lainnya tidak mempunyai struktur cincin, tetapi memiliki jumlah atom karbon yang sama dengan provitamin A lainnya.
11
2.3.3 High performance liquid chromatography (HPLC)
High performance liquid chromatography (HPLC) adalah metode kromatografi yang dikembangkan menggunakan cairan sebagai fase gerak baik cairan polar maupun non polar, dan bekerja pada tekanan tinggi (Adnan 1997). Dalam kromatografi partisi cair baik fase stasioner maupun fase mobile berupa cairan. Pelarut yang digunakan harus tidak dapat bercampur. Perlarut yang lebih polar biasanya digunakan sebagai fase stasioner, oleh karena itu sistem ini dinamakan kromatografi fase normal (normal phase chromatography). Bila fase stasioner yang dipakai senyawa non polar, sedangkan fase mobilnya polar atau terbalik dengan sistem fase normal maka sistemnya disebut kromatografi fase balik (reverse phase chromatography). Komponen utama alat yang dipakai dalam HPLC antara lain (1) reservoir zat pelarut untuk fase gerak; (2) pompa; (3) injektor; (4) kolom; (5) detektor dan (6) rekorder (Adnan 1997).
Komposisi vitamin dapat ditentukan menggunakan HPLC (Robinson 1995). Penggunaan HPLC yang digabungkan dengan detektor
flourimetrik memungkinkan berfungsi sebagai metode khusus dan sensitif yang dapat dikembangkan untuk penentuan beberapa vitamin dalam bahan makanan, diantara banyak metode yang dianjurkan, vitamin merupakan yang paling sering diuji dalam bentuk bebas, meliputi hidrolisis dari bentuk fosforilase (Ndaw et al. 2000).
2.4 Mineral
12
Penggolongan mineral terdiri dari mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg/hari yaitu natrium, klorida, kalsium, fosfor, magnesium dan belerang Mineral mikro adalah mineral yang dibutuhkan kurang dari 100 mg/hari antara lain besi, iodium, mangan, dan seng. Jumlah mineral mikro di dalam tubuh kurang dari 15 mg. Hingga saat ini dikenal sebanyak 24 mineral yang dianggap esensial (Almatsier 2004).
2.4.1 Mineral makro
Unsur mineral makro merupakan unsur mineral pada tubuh manusia yang terdapat dalam jumlah besar. Mineral makro dibutuhkan tubuh dalam jumlah lebih dari 100 mg/hari. Kelompok mineral makro terdiri dari kalium, kalsium, magnesium, natrium, sulfur, klor dan fosfor (Winarno 2008). Unsur mineral makro yang dibutuhkan oleh tubuh adalah:
a. Kalsium (Ca)
Kalsium merupakan unsur terbanyak di dalam tubuh manusia. Tubuh orang dewasa memiliki kalsium sebanyak 1,0-1,4 kg atau sekitar 2% dari berat badan. Kalsium terkonsentrasi pada tulang rawan dan gigi, sisanya terdapat dalam cairan tubuh dan jaringan lunak (Winarno 2008). Peranan kalsium adalah untuk pembentukan tulang dan pemeliharaan jaringan tulang, namun ion kalsium terdistribusi secara luas dalam jaringan lunak. Fungsi lain dari kalsium meliputi kontraksi otot, proses pembekuan darah, transmisi saraf, pemeliharaan keutuhan membran sel dan aktivasi beberapa enzim penting (Halver 1989).
13
gangguan kalsifikasi pada tulang. Apabila kadar kalsium dalam darah menurun, maka keseimbangan diperoleh dengan mengambil cadangan dari tulang-tulang dan gigi. Keadaan ini menyebabkan keropos tulang (osteoporosis) dan gigi geligi tanggal (Nasoetion et al. 1994).
b. Kalium (K)
Kalium merupakan kation utama dalam sebagian besar sel (cairan intraseluler) dan otot (Harjono et al. 1996). Kalium berperan dalam pengaturan kandungan cairan sel. Kalium bersama dengan klorida membantu menjaga tekanan osmotik dan keseimbangan asam basa. Kalium juga membantu dalam mengaktivasi reaksi enzim yaitu piruvat kinase yang dapat menghasilkan asam piruvat dalam proses metabolisme karbohidrat (Winarno 2008). Kalium juga berperan dalam pengaturan fungsi otot. Kalium yang dikonsumsi dalam jumlah besar akan menurunkan tekanan darah, sehingga dapat mencegah penyakit darah tinggi (Okuzumi dan Fujii 2000).
Angka kecukupan gizi kalium pada orang dewasa adalah sebesar 2.000 mg/hari. Kekurangan kalium pada manusia akan mengakibatkan lemah, lesu, kehilangan nafsu makan dan kelumpuhan, sedangkan kelebihan akan menyebabkan gagal jantung yang berakibat kematian serta gangguan fungsi ginjal (Almatsier 2004).
c.Natrium (Na)
14
disebabkan oleh pola konsumsi dengan kandungan natrium yang tinggi yaitu 7,6-8,2 g/hari (Winarno 2008).
2.4.2 Mineral mikro
Mineral mikro merupakan mineral yang terdapat di dalam tubuh dalam jumlah yang kecil dan secara tetap terdapat dalam sistem biologis. Kebutuhan tubuh akan mineral mikro kurang dari 100 mg sehari. Mineral mikro terdiri atas besi, iodium, seng, mangan, kobalt, fluorin dan tembaga (Winarno 2008). Mineral mikro memegang peranan penting untuk memelihara kehidupan, pertumbuhan dan reproduksi (Muchtadi et al. 2001).
a. Besi (Fe)
Besi memiliki fungsi untuk transportasi oksigen ke jaringan (hemoglobin) dan dalam mekanisme oksidasi seluler. Penipisan cadangan besi dapat mengakibatkan anemia defisiensi besi (Harjono et al. 1996). Absorpsi besi merupakan proses yang kompleks. Banyaknya besi yang diserap sangat bergantung pada kebutuhan tubuh akan besi . Zat besi dapat diabsorpsi oleh tubuh dalam kondisi normal sekitar 15% dari makanan yang dikonsumsi, sedangkan pada kondisi kekurangan zat besi tubuh dapat mengarbsorpsi sampai dengan 35% (Winarno 2008).
Angka kecukupan gizi rata-rata besi bayi 0-12 bulan adalah 0,5-7 mg/hari, anak-anak 1-9 tahun sebesar 8-10 mg/hari, laki-laki dan wanita 10-18 tahun
sebesar 13-19 mg/hari serta usia 19-65 tahun sebesar 13-26 mg/hari (Widyakarya Nasional Pangan dan Gizi 2004). Kekurangan besi dapat
menyebabkan anemia, pertumbuhan terganggu dan kehilangan nafsu makan. Kekurangan besi banyak dialami bayi di bawah usia 2 tahun serta para ibu yang sedang mengandung dan menyusui (Winarno 2008).
b. Seng (Zn)
15
bulan adalah sebesar 1,3-7,5 mg/hari, anak-anak 1-9 tahun sebesar 8,2-11,2 mg/hari, laki-laki dan wanita 10-18 tahun sebesar 12,6-17,4 mg/hari serta usia 19-65 tahun ke atas sebesar 9,3-13,4 mg/hari (Widyakarya Nasional Pangan dan Gizi 2004). Kekurangan seng dapat terjadi pada golongan rentan yaitu anak-anak, ibu hamil dan menyusui serta orang tua. Kekurangan seng dapat menyebabkan terjadinya diare, gangguan pertumbuhan, gangguan kematangan seksual, gangguan sistem saraf, sistem otak dan gangguan pada fungsi kekebalan (Almatsier 2004).
2.4.3 Atomic absorption spectrophotometer (AAS)
Atomic absorption spectrophotometer atau spektroskopi serapan atom merupakan suatu metode yang digunakan untuk penentuan unsur-unsur logam dan metaloid (Chasteen 2007). Analisis unsur dengan panjang gelombang pada daerah sinar tampak seperti Ca, K, Na, Mg, P dan sebagainya dapat dilakukan dengan cara spektroskopi serapan atom dan spektroskopi emisi nyala. Spektroskopi serapan atom mengukur radiasi yang diserap oleh atom-atom yang tidak tereksitasi sedangkan pada spektroskopi emisi nyala yang diukur adalah radiasi yang dipancarkan dengan panjang gelombang tertentu oleh atom-atom yang tereksitasi (Nur 1989).
Prinsip pemeriksaan spektrofotometer serapan atom yaitu molekul sampel diubah menjadi atom-atom bebas dengan bantuan nyala atau flame. Atom-atom akan mengabsorbsi cahaya yang sesuai dengan panjang gelombang dari atom tersebut dan intensitas cahaya yang diserap sebanding dengan panjang gelombang dari atom tersebut serta intensitas cahaya yang diserap sebanding dengan banyaknya cahaya. Waktu pengujian dengan instrumen AAS lebih cepat dibandingkan dengan metode pengujian gravimetri dan titrimetri, karena preparasi sampel lebih cepat, yakni disediakan dalam larutan kemudian dimasukkan untuk dibakar (Chasteen 2007).
2.5 Pengukusan
16
mempunyai pengaruh yang merugikan pada zat gizi, karena degradasi panas dapat terjadi pada zat gizi (Harris dan Karmas 1989).
Pengolahan yang biasa dilakukan terhadap sayuran seperti semanggi sebelum dikonsumsi adalah pengukusan. Pengukusan termasuk perlakuan pemasakan menggunakan panas basah untuk mendapatkan hasil yang diinginkan
yaitu aman, bergizi dan dapat diterima secara sensori maupun kimia (Harris dan Karmas 1989). Pengukusan secara nyata dapat menurunkan kadar zat
gizi makanan yang besarnya bergantung pada cara mengukus dan jenis makanan yang dikukus. Keragaman susut zat gizi di antara berbagai cara pengukusan terutama terjadi akibat degradasi oksidatif (Harris dan Karmas 1989).
17
3 METODOLOGI
3.1 Waktu dan Tempat
Penelitian dilaksanakan pada bulan Februari 2012 sampai Mei 2012. Preparasi bahan baku dilakukan di Laboratorium Karakteristik Bahan Baku Industri Hasil Perairan dan Laboratorium Preservasi dan Pengolahan Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan. Analisis proksimat di Laboratorium Biokimia Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Analisis mineral di Laboratorium Pengujian Nutrisi Pakan Fakultas Peternakan dan analisis kadar vitamin dilakukan di Balai Besar Industri Agro (BBIA) Bogor.
3.2 Bahan dan Alat
Bahan utama yang digunakan untuk penelitian ini adalah genjer (L. flava). Bahan-bahan yang dibutuhkan untuk analisis proksimat meliputi
akuades; kjeltab jenis selenium; larutan H2SO4 pekat, asam borat (H3BO3) 2% yang mengandung indikator bromcherosol green-methyl red (1:2) berwarna merah muda; larutan HCl 0,1 N; pelarut lemak (n-heksana); larutan HCl 10%; dan larutan AgNO3 0,10 N. Analisis serat kasar menggunakan H2SO4 1,25%; NaOH 1,25%; dan alkohol. Bahan yang digunakan untuk analisis vitamin C adalah asam metafosfat 0,3 M dan asam asetat 1,4 M. Analisis beta karoten menggunakan bahan-bahan yaitu KOH dalam metanol 5%; hekasana aseton; akuades; gas N2 dan Na2SO4; dan Fenolftalein 1%. Bahan yang digunakan untuk analisis mineral adalah HNO3; HClO4; H2SO4; dan HCl.
18
3.3 Metode Penelitian
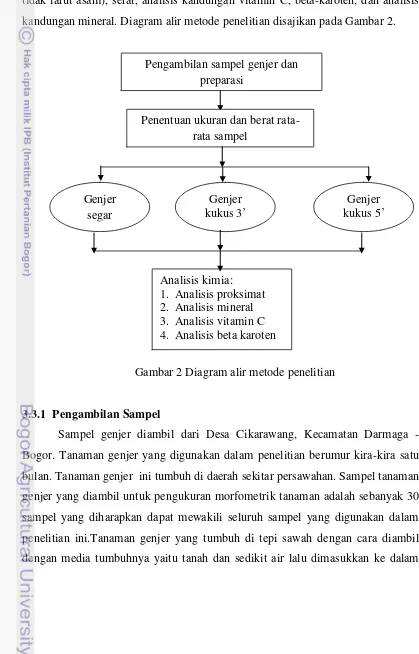
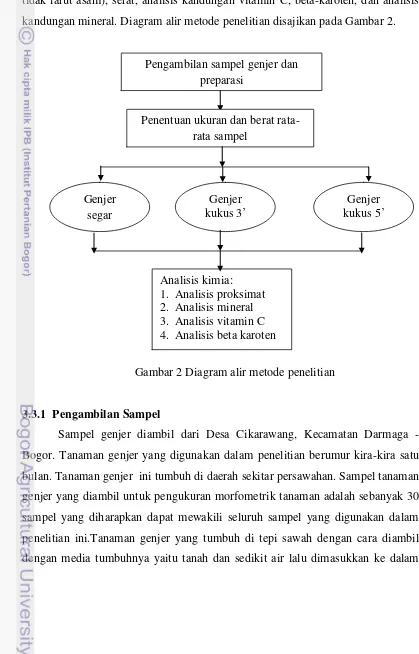
Penelitian terdiri dari beberapa tahapan, yaitu tahapan pengambilan sampel, preparasi bagian sampel yang dapat dimakan, pengukusan, analisis kimia tanaman genjer berupa analisis proksimat (kadar air, lemak, protein, abu, dan abu tidak larut asam), serat, analisis kandungan vitamin C, beta-karoten, dan analisis kandungan mineral. Diagram alir metode penelitian disajikan pada Gambar 2.
Gambar 2 Diagram alir metode penelitian
3.3.1 Pengambilan Sampel
Sampel genjer diambil dari Desa Cikarawang, Kecamatan Darmaga - Bogor. Tanaman genjer yang digunakan dalam penelitian berumur kira-kira satu bulan. Tanaman genjer ini tumbuh di daerah sekitar persawahan. Sampel tanaman genjer yang diambil untuk pengukuran morfometrik tanaman adalah sebanyak 30 sampel yang diharapkan dapat mewakili seluruh sampel yang digunakan dalam penelitian ini.Tanaman genjer yang tumbuh di tepi sawah dengan cara diambil
Pengambilan sampel genjer dan preparasi
Penentuan ukuran dan berat rata-rata sampel
Analisis kimia:
1. Analisis proksimat 2. Analisis mineral 3. Analisis vitamin C 4. Analisis beta karoten Genjer
segar
Genjer kukus 5’ Genjer
19
kantong plastik agar sampel tidak mudah layu. Sampel selanjutnya dipreparasi untuk tahap selanjunya.
3.3.2 Pengukuran tanaman genjer
Pengukuran tanaman genjer dilakukan terhadap daun dan batang tanaman. Tanaman genjer yang diukur berjumlah 30 sampel. Pengukuran daun meliputi panjang dan lebar daun serta pengukuran batang meliputi panjang dan tebal batang. Pengukuran panjang dan lebar daun, serta panjang tangkai dilakukan dengan penggaris stainless merk kenko. Pengukuran tebal tangkai menggunakan jangka sorong merk NSK. Panjang daun diukur dari ujung daun hingga pangkal dekat batang dengan menggunakan penggaris. Diameter daun diukur dari sisi kanan hingga kiri pada bagian tengah daun dengan menggunakan penggaris. Panjang batang diukur dari ujung batang dekat daun hingga pangkal batang dekat akar dengan menggunakan penggaris. Ketebalan batang diukur pada bagian tengah batang dengan menggunakan jangka sorong (Lampiran 15). Setelah pengukuran selesai, genjer kemudian diprepasi untuk diambil bagian-bagian yang biasanya dikonsumsi masyarakat. Tanaman genjer selanjutnya dibagi dalam tiga perlakuan, yaitu segar, kukus 3 menit, dan kukus 5 menit.
3.3.3 Pengukusan Tanaman Genjer
Pengukusan genjer dilakukan terhadap bagian dari tanaman genjer yang dapat dikonsumsi, yaitu daun dan batang. Proses pengukusan bertujuan untuk menentukan perubahan yang terjadi terhadap analisis proksimat, kandungan vitamin C, beta karoten, serta mineral genjer. Proses pengukusan dilakukan pada menit ke 3 dan 5 hingga daun terlihat agak layu tetapi warna genjer tetap hijau. Waktu pengukusan yang digunakan merupakan waktu yang biasa digunakan masyarakat ketika mengukus.
20
3.3.4 Analisis proksimat (AOAC 2005)
Analisis proksimat merupakan suatu analisis yang dilakukan untuk memprediksi komposisi kimia suatu bahan, termasuk didalamnya analisis kadar air, abu, lemak, protein dan abu larut asam.
1) Analisis kadar air (AOAC 2005)
Tahap pertama yang dilakukan untuk menganalisis kadar air adalah mengeringkan cawan porselen dalam oven pada suhu 105 oC selama 1 jam. Cawan tersebut diletakkan ke dalam desikator (kurang lebih 15 menit) dan dibiarkan sampai dingin kemudian ditimbang. Cawan tersebut ditimbang kembali hingga beratnya konstan, sebanyak 5 gram contoh dimasukkan ke dalam cawan, kemudian dikeringkan dengan oven pada suhu 105 oC selama 5 - 8 jam atau hingga beratnya konstan. Setelah selesai proses kemudian cawan tersebut diletakkan pada desikator ± 30 menit dan dibiarkan sampai dingin dan
B = Berat cawan yang diisi dengan sampel (gram)
C = Berat cawan dengan sampel yang sudah dikeringkan (gram)
2) Analisis kadar abu (AOAC 2005) sampai pengabuan sempurna, kemudian ditimbang hingga didapatkan berat yang konstan.
Kadar abu ditentukan dengan rumus:
21
Keterangan : A = Berat cawan porselen kosong (gram) B = Berat cawan dengan sampel (gram)
C = Berat cawan dengan sampel setelah dikeringkan (gram)
3) Analisis kadar abu tidak larut asam menurut SNI-2354.1-2010 (SNI 2010)
Abu bekas pengukuran kadar abu total dilarutkan dengan penambahan 25 ml HCl 10%, didihkan selama 5 menit, saring larutan dengan kertas saring bebas abu dan cuci dengan air suling sampai bebas klorida. Selanjutnya keringkan kertas saring dalam oven, setelah dikeringkan kertas saring dimasukkan di dalam cawan porselin yang sudah diketahui berat tetapnya kemudian abukan dalam tanur listrik pada suhu 600 ⁰C. Setelah dilakukan pengabuan sampel didinginkan di dalam desikator dan kemudian ditimbang beratnya dan diukur kadar abu tidak larut asam dengan rumus:
% Kadar serat kasar = C– A x 100% Berat sampel
Keterangan : A = Berat cawan porselen kosong (gram)
C = Berat cawan dengan sampel abu tak larut asam (gram)
4) Analisis kadar protein (AOAC 2005)
Tahap-tahap yang dilakukan dalam analisis protein terdiri dari tiga tahap yaitu destruksi, destilasi, dan titrasi. Sampel ditimbang sebanyak 0,25 gram; kemudian dimasukkan ke dalam labu Kjeldahl 100 ml; lalu ditambahkan 0,25 gram selenium dan 3 ml H2SO4 pekat. Sampel didestruksi pada suhu 410 oC sampai larutan jernih lalu didinginkan. Setelah dingin, ditambahkan 50 ml akuades dan 20 ml NaOH 40%; kemudian dilakukan proses destilasi. Hasil destilasi ditampung dalam labu Erlenmeyer 125 ml yang berisi campuran 10 ml asam borat (H3BO3) 2% dan 2 tetes indikator bromcherosol green-methyl red yang berwarna merah muda. Setelah volume destilat mencapai 200 ml maka proses destilasi dihentikan, lalu destilat dititrasi dengan HCl 0,1 N sampai terjadi perubahan warna merah muda. Volume titran dibaca dan dicatat. Larutan blanko dianalisis seperti contoh.
Kadar protein dihitung dengan rumus sebagai berikut :
22
% Kadar protein = % N x faktor konversi * *) Faktor Konversi = 6,25
5) Analisis kadar lemak (AOAC 2005)
Sampel seberat 5 gram (W1) dimasukkan ke dalam kertas saring dan selanjutnya dimasukkan ke dalam selongsong lemak, kemudian sampel yang telah dibungkus dimasukkan ke dalam labu lemak yang sudah ditimbang berat tetapnya (W2) dan disambungkan dengan tabung soxhlet. Selongsong lemak dimasukkan ke dalam ruang ekstraktor tabung soxhlet dan disiram dengan pelarut lemak. Tabung ekstraksi dipasang pada alat destilasi soxhlet, lalu dipanaskan pada suhu 40 ºC dengan menggunakan pemanas listrik selama 16 jam. Pelarut lemak yang ada dalam labu lemak didestilasi hingga semua pelarut lemak menguap. Pada saat destilasi pelarut akan tertampung di ruang ekstraktor, pelarut dikeluarkan sehingga tidak kembali ke dalam labu lemak, selanjutnya labu lemak dikeringkan dalam oven pada suhu 105 oC, setelah itu labu didinginkan dalam desikator sampai beratnya konstan (W3).
Perhitungan kadar lemak:
3.3.5 Analisis kadar serat kasar (SNI 01-2891-1992)
23
dikeringkan dalam oven 130 oC selama 2 jam. Setelah dingin residu beserta cawan porselin ditimbang (A), dan dimasukkan dalam tanur 600 oC selama 30 menit, lalu didinginkan dan ditimbang kembali (B).
Penghitungan kadar serat kasar pada genjer:
% kadar serat kasar = berat endapan pada kertas saring – berat abu x 100% berat sampel
3.3.6 Analisis vitamin C (Ismail dan Fun 2003)
Vitamin C diekstraksi menurut metode modifikasi dari Abdulnabi et al. (1997). Sebanyak 10 gram sampel dihomogenkan dengan asam
metafosfat 0,3 M dan asam asetat 1,4 M. Campuran ditempatkan dalam gelas ukur (dibungkus dengan aluminium foil) dan dihomogenkan dengan orbital shacker pada kecepatan 100 rpm selama 15 menit pada suhu ruang. Campuran tersebut kemudian disaring melalui kertas Whatman No 4 untuk mendapatkan ekstrak. Semua sampel diekstraksi dalam tiga ulangan. Dua teknik yang digunakan untuk mengidentifikasi vitamin C pada kromatogram adalah membandingkan waktu retensi dan spiking tes dengan L-asam askorbat. Standar vitamin C dibuat dengan melarutkan 100 mg asam L-askorbat dalam asam metafosfat 0,3 M dan asam asetat 1,4 M, larutan pada konsentrasi akhir 1 mg / ml.
Ekstrak yang berisi vitamin C dapat dianalisis menggunakan HPLC. Sistem yang dianjurkan adalah sebagai berikut:
Fase gerak : 0,1 M potassium acetate (pH 4,9), Acetonitrile-air (50:50) Kolom : reverse phase C18
Kecepatan aliran : 1,5 ml/menit Detektor : UV visible 254 nm Rekorder : 1 cm/menit
3.3.7 Analisis beta karoten (Ismail dan Fun2003)
24
kemudian dipindahkan ke labu ukur dan ditambahkan 50 ml n-heksan hingga tanda tera. Labu ukur kemudian dikocok kuat selama beberapa detik untuk memisahkan lapisan. Lapisan atas (ekstrak heksana) dipipet keluar dan lapisan berair kembali diekstraksi dua kali dengan 50 ml n-heksan. Lapisan atas ini dikumpulkan dan dicuci dengan air suling sampai bebas alkali. Fenolftalein (1%) digunakan untuk memeriksa apakah masih ada alkali atau tidak. Kehadiran alkali memberikan indikator warna merah muda. Ekstrak kemudian disaring dengan Na2SO4 untuk menghilangkan semua sisa air. Residu heksana dihapus dengan menggunakan rotary evaporator pada tekanan rendah (45 °C). Ekstrak yang dihasilkan diencerkan sampai 10 ml dengan n-heksana. Semua sampel dilakukan di tiga ulangan. Ekstrak yang berisi beta karoten dapat dianalisis menggunakan HPLC. Sistem yang dianjurkan adalah sebagai berikut:
Fase gerak : Acetonitrile:methanol:ethyl acetate (88:10:2) Kolom : reverse phase C18
Kecepatan aliran : 1.0 ml/min
Detektor : UV visible 250 nm Rekorder : 1 cm/menit
3.3.8 Analisis mineral (APHA 2005)
Analisis mineral dan logam berat dilakukan untuk mengetahui profil atau komposisi mineral makro, mineral mikro dan logam berat yang terdapat pada genjer.
a. Pengujian mineral (Fe, Zn, Ca, K, Mg, Cu, dan Na)
25
ditambahkan 2 ml akuades dan 0,6 ml HCl pekat. Larutan contoh kemudian diencerkan menjadi 100 ml dalam labu takar. Sejumlah larutan stok standar dari masing-masing mineral diencerkan dengan menggunakan akuades sampai konsentrasinya berada dalam kisaran kerja logam yang diinginkan.
Larutan standar, blanko dan contoh dialirkan ke dalam AAS merk Shimadzu tipe AA 680 flame emission. Kemudian diukur absorbansinya atau tinggi puncak dari standar blanko dan contoh pada panjang gelombang dan parameter yang sesuai untuk masing-masing mineral dengan spektrofotometer. Merk lampu katoda yang digunakan dalam analisis mineral adalah Hammamatsu, dengan panjang gelombang untuk mineral natrium adalah 589,0 nm; kalsium dengan panjang gelombang 422,7 nm; kalium dengan 766,5 nm; magnesium dengan 285,2 nm; besi dengan 248,3 nm; seng dengan 213,9 nm; tembaga dengan 324,7 nm; dan selenium dengan panjang gelombang 196,0 nm. Pembakaran sampel dilakukan dengan campuran udara dan asetilen.
b. Pengujian fosfor
Sampel diperlakukan dengan asam nitrat untuk mengubah semua metafosfat dan pirofosfat menjadi ortofosfat. Sampel dicampurkan dengan asam molibdat dan asam vanadat sehingga ortofosfat yang ada dalam sampel akan bereaksi dengan pereksi-pereksi tersebut dan membentuk kompleks asam vanadimolibdifosfat yang berwarna biru dan intensitas warnanya diukur dengan panjang gelombang 660 nm.
Sebanyak 20 g ammonium molibdat dilarutkan dalam 400 ml akuades hangat untuk pembuatan pereaksi molibdat. Kemudian timbang 1 gram ammonium vanadat untuk dilarutkan dalam 300 ml akuades dan didinginkan, secara perlahan-lahan ditambah 140 ml asam nitrat pekat, setelah tercampur ditambahkan pereaksi larutan vanadat molibdat dan diencerkan sampai volume 1 liter dengan akuades.
3.4 Rancangan Percobaan dan Analisis Data
26
dilakukan dengan 2 kali ulangan. Model rancangan penelitian ini adalah sebagai berikut:
yijk = µ + Ai + Bj + (ABij) + έijk Keterangan:
yij = hasil pengamatan faktor A taraf ke-I (I = 1, 2,3) dan faktor B taraf ke-j (j 1, 2, 3) pada ulangan ke-k (k = 1, 2)
µ = rataan umum
Ai = pengaruh faktor kondisi sampel (faktor A) taraf ke-i Bj = pengaruh faktor waktu pengukusan (faktor B) taraf ke-j
(ABij) = pengaruh interaksi kondisi sampel taraf ke-i dan waktu pengukusan taraf ke-j
έijk = sisaan akibat kondisi sampel taraf ke-I dan waktu pengukusan taraf ke-j pada ulangan ke-k
Hipotesa terhadap karakteristik genjer dengan waktu pengukusan yang berbeda adalah sebagai berikut:
H0 = Perbedaan waktu pengukusan tidak memberikan pengaruh terhadap karakteristik kimia, vitamin, dan mineral genjer
H1 = Perbedaan waktu pengukusan memberikan pengaruh terhadap karakteristik kimia, vitamin, dan mineral genjer
Jika uji F pada ANOVA memberikan pengaruh yang berbeda nyata terhadap karakteristik kimia dan mineral genjer maka dilanjutkan dengan uji lanjut Duncan dengan rumus sebagai berikut:
Duncan = q (p,dbs) Keterangan :
q = Nilai tabel q
27
4 HASIL DAN PEMBAHASAN
4.1 Karakteristik dan Morfologi Genjer (L. flava)
Sampel genjer terlebih dahulu dipreparasi, kemudian sampel diukur morfometriknya. Besaran yang digunakan dalam pengukuran tanaman genjer pada penelitian ini adalah panjang daun, diameter daun, panjang batang dan diameter batang. Secara umum hasil pengukuran tanaman genjer disajikan pada Tabel 3.
Tabel 3 Hasil pengukuran tanaman genjer (L. flava) Besaran Keterangan: Data diperoleh dari 30 tangkai tanaman genjer (L. flava)
Hasil pengukuran daun genjer meliputi panjang daun dan diameter daun menunjukkan nilai berkisar pada 9,63± 0,54 cm dan 7,51± 0,12 cm. Panjang daun minimal adalah 9 cm dan maksimal adalah 10,70 cm. Diameter daun minimal sebesar 7,30 cm dan diameter daun maksimal sebesar 7,70 cm. Hasil pengukuran batang genjer meliputi panjang batang dan tebal batang menunjukkan nilai berkisar pada 24,12± 0,77 cm dan 0,67± 0,11 cm. Panjang batang genjer minimal sebesar 23 cm dan maksimal sebesar 25,50 cm. Tebal batang minimal sebesar 0,43 cm dan maksimal sebesar 0,97 cm.
Selubung daun genjer sempit ke arah atas dan helai daun tipis, berwarna hijau muda, bentuk (bulat, bulat telur atau berbentuk bulat panjang yang luas) dan memiliki panjang daun berkisar antara 6 - 20 cm (hampir sama-sama lebar). Puncak daun umumnya apiculate dengan hydathode kecil di ujungnya, dasar daun cuneate, dan margin daun berombak-ombak. Terdapat sekitar 1-4 peduncles (tangkai bunga), yang aksila, tegak, berbentuk segitiga, diratakan di dasar dan memiliki panjang 120 cm (Abhilash et al. 2009).
28
4.2 Komposisi Kimia Genjer (L. flava)
Analisis komposisi kimia genjer dilakukan melalui uji proksimat dalam kondisi segar dan setelah pengukusan dengan waktu pengukusan yang berbeda. Bagian tanaman genjer yang yang diteliti yaitu bagian yang dapat dimakan, terdiri dari daun dan batang. Analisis komposisi kimia yang dilakukan terdiri dari analisis kadar air, protein, lemak, abu, abu tidak larut asam, dan serat kasar. Komposisi kimia tanaman genjer dalam basis basah disajikan pada Tabel 4.
Tabel 4 Komposisi kimia tanaman genjer dalam berat basah Analisa Proksimat Segar* (%) Segar** (%) Kukus 3
menit (%)
Kukus 5 menit (%) Kadar air 93,91±0,13 79,34±0,15 92,49±0,04 91,27±0,04
Protein 2,38±0,00 0,28±0,01 2,81±0.53 2,03±0,31
Hasil analisis komposisi kimia berdasarkan Tabel 4 menunjukkan perbedaan antara hasil penelitian dengan hasil Saupi el al. (2009). Menurut Miller (1996), komposisi akhir dari bagian tanaman yang dapat dimakan dipengaruhi dan dikontrol oleh kesuburan tanah, genetik tanaman, dan lingkungan pertumbuhan tanaman. Hal inilah yang menyebabkan hasil penelitian berbeda dengan yang dikemukakan oleh Saupi et al. (2009). Hasil analisis komposisi kimia genjer segar menunjukkan perubahan setelah dilakukan pengukusan. Kadar air, protein, dan abu mengalami penurunan, sedangkan kadar lemak, dan serat kasar mengalami peningkatan.
29
pada tumbuhan dapat mencapai 85-98%. Difusi gas ke dalam sel-sel tanaman diduga berawal dari pengangkutan sejumlah air oleh sistem pembuluh, kemudian terjadi penyerapan gas dengan tidak mengikutsertakan air melalui diafragma dari ruang antar selnya. Oleh karena itu semakin banyak gas yang dibutuhkan oleh tanaman air, maka semakin besar pula presentase air yang dikandung tanaman.
Kadar air genjer setelah dilakukan proses pengukusan mengalami penurunan. Menurut Sulistiono (2009), perubahan kadar air pada proses pengukusan semanggi air disebabkan karena transfer panas dan pergerakan aliran air maupun udara, sehingga terjadi proses penguapan dan pengeringan pada bahan makanan yang mengakibatkan perubahan proses dehidrasi seperti penurunan konsentrasi protein pada makanan. Menurunnya kadar air pada sayuran akan mengakibatkan perubahan tekstur pada sayuran tersebut. Sayuran setelah dikukus akan menjadi lunak dan lebih mudah dikonsumsi.
Kadar protein genjer segar hasil penelitian sebesar 2,38% lebih rendah dibandingkan bayam (3,50%), kangkung (3,00%), daun singkong (6,80%), daun pepaya (8,00%). Menurut Nosoetion et al. (1994) ketersediaan unsur nitrogen didalam media tumbuh tanaman tidak kalah penting dalam proses sintesis protein, baik sebagai asam amino, protein, klorofil dan tersedianya basa nitrogen terutama purin dan pirimidin. Hal inilah yang menyebabkan terjadinya perbedaan kandungan protein dari tiap-tiap jenis sayuran yang berbeda tempat hidupnya. Kadar protein genjer mengalami perubahan setelah dilakukan pengukusan yang menunjukkan adanya pengaruh proses pengukusan terhadap kadar protein genjer.
30
peningkatan kadar lemak setelah pengukusan, hal ini diduga karena proporsional terhadap penurunan kadar air, protein, dan abu.
Kadar abu genjer segar hasil penelitian sebesar 0,90% berbeda dengan hasil kadar abu genjer segar yang dilakukan oleh Saupi et al. (2009) yaitu sebesar 0,79%. Perbedaan ini disebabkan oleh kondisi habitat dan kandungan mineral di dalam tanah maupun lumpur yang berbeda. Kandungan abu dan komponennya tergantung pada macam bahan dan cara pengabuannya. Kadar abu genjer segar mengalami perubahan setelah dilakukan pengukusan.
Kandungan serat kasar genjer segar hasil penelitian sebesar 1,31%. Kandungan serat ini lebih besar apabila dibandingkan dengan kandungan serat pada bayam (0,9%) dan selada (0,8%). Serat banyak berasal dari dinding sel berbagai sayur dan buah-buahan. Secara kimia dinding sel tersebut terdiri dari selulosa, hemiselulosa, pektin, dan non-karbohidrat seperti polimer lignin, beberapa gumi, dan mucilage. Serat pada bahan pangan merupakan komponen dari jaringan tanaman yang tahan terhadap proses hidrolisis oleh enzim dalam lambung dan usus kecil (Winarno 2008).
Kadar abu tidak larut asam yang diperoleh dalam penelitian adalah sebesar 0,10%, kadar tersebut masih memenuhi standar yang ditetapkan EEC yaitu maksimum sebesar 2%, sedangkan FAO dan FCC menetapkan maksimum 1%. Menurut Basmal et al. (2003), kadar abu tak larut asam merupakan salah satu kriteria dalam menentukan tingkat kebersihan dalam proses pengolahan. Tingginya kadar abu tak larut asam pada teh daun murbei kanva mencerminkan tingginya kandungan logam yang terkandung di dalamnya. Abu tak larut asam dicerminkan oleh adanya kontaminasi mineral atau logam yang tidak larut asam
dalam tanaman genjer.
31
Tabel 5 Komposisi kimia tanaman genjer (berat kering) setelah pengukusan Analisa proksimat Segar (%) Kukus 3 menit
(%)
Kukus 5 menit (%)
Kadar air 0 0 0
Protein 39,12±0,86a 37,46±6,84a 23,23±3,46b Lemak 3,29±2,10a 3,92±0,01a 4,52±0,06a Kadar abu 14,73±2,54a 13,24±0,02a,b 8,01±1,58b Serat kasar 21,54±1,41a 17,84±0,47a 17,51±2,02a Abu tak larut asam 1,64±0,04a 1,31±0,00c 1,13±0,01b Keterangan : Angka yang diikuti oleh huruf yang sama dalam satu baris menunjukkan bahwa
perbedaan waktu pengukusan tidak memberikan pengaruh yang berbeda nyata terhadap komposisi kimia (p<0,05)
Tabel 5 menunjukkan hasil perubahan komposisi kimia genjer setelah pengukusan dalam berat kering. Menurut Rahayu (2010) pemanasan dengan pengukusan kadang-kadang tidak merata karena bahan makanan di bagian tepi biasanya mengalami pengukusan berlebihan, sementara di bagian tengah mengalami pengukusan lebih sedikit. Pengukusan secara nyata dapat menurunkan kadar zat gizi makanan yang besarnya bergantung pada cara mengukus dan jenis makanan yang dikukus (Harris dan Karmas 1989).
Kadar protein genjer segar (basis kering) sebesar 39,14% menurun menjadi 32,49% setelah pengukusan 3 menit dan 20,73% setelah pengukusan 5 menit. Hasil uji lanjut duncan (Lampiran 13d), menunjukkan bahwa perlakuan kukus 3 menit tidak memberikan pengaruh yang berbeda nyata terhadap kadar protein genjer segar, namun memberikan pengaruh yang berbeda nyata terhadap kadar protein genjer dengan perlakuan kukus 5 menit. Menurut Gaman dan Sherrington (1992), perlakuan pemanasan pada suatu bahan pangan menyebabkan protein terkoagulasi dan terhidrolisis secara sempurna. Pengaruh pengukusan menyebabkan protein terdenaturasi dan membentuk agregat-agregat (gel, endapan dan sebagainya). Dalam jaringan sel sayuran, protein tersimpan di vakuola dalam bentuk asam amino, di membran sel dalam bentuk lipoprotein dan dalam inti sel sebagai nukleoprotein (Johnson dan Uriu 1990).
32
genjer. Hal ini menunjukkan bahwa meningkatnya kadar lemak secara nominal pada pengujian sebenarnya tidak berpengaruh secara statistik.
Kadar abu pada genjer segar (basis kering) yaitu sebesar 14,80%, menurun setelah mengalami proses pengukusan menjadi 13,31% pada kukus 3 menit dan 8,02% pada kukus 5 menit. Berdasarkan hasil uji lanjut duncan (Lampiran 13e) menunjukkan bahwa perlakuan waktu pengukusan yang berbeda memberikan pengaruh yang berbeda nyata terhadap kadar abu genjer. Hal ini sejalan dengan penelitian Rusydi (2010) yang menyatakan bahwa presentase air yang hilang pada proses pengukusan genjer sedikit, sehingga kehilangan mineral yang larut dalam air juga sangat sedikit.
Kadar serat kasar genjer segar (basis kering) menurun dari 21,55% menjadi 17,84% pada kukus 3 menit dan menjadi 17,53% pada kukus 5 menit. Hasil uji lanjut duncan (Lampiran 13g) menunjukkan bahwa perlakuan waktu pengukusan tidak memberikan pengaruh yang berbeda nyata terhadap kadar serat kasar genjer. Kadar serat dalam makanan dapat mengalami perubahan akibat pengolahan yang dilakukan terhadap bahan asalnya (Muchtadi 2001). Sebagian besar serat pada tumbuhan berupa selulosa dan terhidrolisis menjadi senyawa-senyawa yang lebih sederhana seperti selodekstrin yang terdiri dari satuan glukosa atau lebih sedikit, kemudian selobiosa dan akhirnya glukosa (Robinson 1995).
Kadar abu tidak larut asam genjer segar (basis kering) sebesar 1,64%, mengalami penurunan menjadi 1,33% pada kukus 3 menit dan 1,14% pada kukus 5 menit. Hasil uji lanjut duncan (Lampiran 13f) menunjukkan bahwa perlakuan waktu pengukusan memberikan pengaruh yang berbeda nyata terhadap kadar abu tidak larut asam genjer. Menurut Basmal et al. (2003), kadar abu tak larut asam merupakan salah satu kriteria dalam menentukan tingkat kebersihan dalam proses pengolahan. Abu tak larut asam dicerminkan oleh adanya kontaminasi mineral atau logam yang tidak larut asam dalam tanaman genjer.
4.3 Kandungan Vitamin Genjer (L. flava)
33
dengan yang dikemukakan oleh Direktorat Gizi, Departemen Kesehatan (1992) yang diacu dalam Astawan dan Kasih (2008), kandungan vitamin C genjer segar (Limnocharis flava) adalah sebesar 54 mg/100 g. Perbedaan tersebut diduga karena perbedaan lokasi tumbuh dan keadaan alam dari tempat hidup genjer. Kandungan vitamin C pada genjer segar ini tergolong sedang. Menurut Somsub et al. (2007) kandungan vitamin C dalam sampel sayur dibagi dalam tiga tingkatan yaitu kategori tinggi (71,8 mg/100 g), sedang (9,6-71,6 mg/100 g), dan rendah (kurang dari 9,6 mg/100 g).
Hasil kandungan vitamin C genjer segar dan genjer kukus menunjukkan penurunan, nilai vitamin C pada genjer segar sebesar 46,63 mg/100 g menurun setelah pengukusan 3 menit menjadi 43,81 mg/100 g dan pada pengukusan 5 menit semakin menurun menjadi 37,34 mg/100 g. Pada pengukusan 3 menit, kadar vitamin C menurun sebesar 6,05% dan pada pengukusan 5 menit menurun sebesar 20,06%. Hal ini menunjukkan bahwa semakin lama waktu pengukusan menyebabkan kandungan vitamin C semakin menurun.
Berdasarkan hasil uji lanjut duncan (Lampiran 15c) menyatakan bahwa perlakuan kukus 3 menit tidak memberikan pengaruh yang berbeda nyata terhadap kandungan vitamin C genjer segar, namum memberikan pengaruh yang berbeda
nyata terhadap kadar vitamin C pada pengukusan 5 menit. Menurut Somsub et al.(2007) kandungan vitamin C secara signifikan menurun pada tiga
34
Kandungan beta karoten genjer segar dan setelah pengukusan mengalami penurunan. Nilai beta karoten genjer segar dalam berat kering sebesar 69,62 mg/100 g, berubah setelah pengukusan 3 menit menjadi 44,87 mg/100 g, dan pada pengukusan 5 menit menjadi 18,44 mg/100 g. Menurut Subekti (1998) pengukusan menurunkan kandungan beta karoten secara nyata padasawi hijau (59%), bunga kol (14%), dan bayam (17%). Sebagimana menurut Apriyantono (2002) bahwa pada zat gizi lainnya, nilai beta karoten akan menurun akibat adanya proses pemanasan.
Proses pengukusan pada penelitian ini menyebabkan kehilangan kadar beta karoten sebesar 33,55% pada pengukusan 3 menit dan pada pengukusan 5 menit sebesar 73,51%. Berdasarkan hasil uji lanjut duncan (Lampiran 15d) menyatakan bahwa perbedaan waktu pengukusan memberikan pengaruh yang berbeda nyata terhadap kadar beta karoten genjer. Hal ini menunjukkan bahwa semakin lama waktu pengukusan menyebabkan kadar beta karoten semakin menurun. Menurut Olemo et al. (2011) kehilangan beta karoten dengan presentase rendah (10%) diamati pada Solanum incanum dapat dikaitkan dengan metode pengolahan yang berbeda. Beta karoten adalah zat gizi mikro aktif sebagai komponen dari karotenoid yang dikenal sebagai pro vitamin A (Almatsier 2004). Walaupun genjer mengandung pro vitamin A tetapi hasil analisis vitamin A pada genjer segar terdeteksi dalam jumlah kecil dibawah limit deteksi alat (0,005 ppm).
4.4 Kandungan Mineral Genjer ((Limnocharis flava)
35
Kalium (K) 412,64±3,10 386,46±2,07 326,87±3,61 Natrium (Na) 34,92±1,56 12,75±0,32 8,59±0,27 Mineral mikro
Besi (Fe) 117,02±5,09 140,17±0,87 104,84±5,03 Seng (Zn) 45,51±1,11 22,70±0,80 22,90±1,08
Tabel 6 menunjukkan kandungan mineral genjer segar dan setelah pengukusan. Kandungan mineral makro tertinggi pada genjer segar adalah kalium dan mineral terendah adalah natrium. Kandungan mineral mikro tertinggi pada genjer segar adalah besi dan terendah adalah seng. Kelima jenis mineral makro yang diteliti menunjukkan bahwa empat mineral mengalami penurunan setelah pengukusan yaitu fosfor, kalsium, kalium, dan natrium. Sedangkan magnesium mengalami peningkatan setelah pengukusan. Kehilangan mineral tertinggi pada pengukusan dengan waktu 3 menit dan 5 menit terdapat pada mineral natrium, sedangkan kehilangan mineral terendah yaitu kalium. Kehilangan mineral ini diakibatkan oleh pengolahan dengan pemanasan suhu dan media uap air. Menurut Palupi et al. (2007), mineral yang terkandung dalam bahan pangan akan rusak pada sebagian besar proses pengolahan karena sensitif terhadap pH, oksigen, sinar dan panas atau kombinasi diantaranya.
36 pengukusan tidak memberikan pengaruh yang berbeda nyata terhadap komposisi kimia (p<0,05)
Tabel 7 menunjukkan hasil kandungan mineral genjer setalah proses pengukusan. Beberapa mineral makro seperti fosfor, kalsium, kalium, dan natrium mengalami penurunan setelah proses pengukusan. Begitu pula yang terjadi pada mineral mikro besi dan seng mengalami penurunan setelah pengukusan. Menurut Rahayu (2010) ketika makanan dimasak, diproses, atau disimpan, mineral dapat bergabung dengan komponen kimia makanan lain atau bahkan larut akibat pemanasan. Sama halnya dengan vitamin, variasi kandungan mineral alamiah makanan mentah dan metode memasak yang berbeda dapat menghasilkan variasi kadar mineral. Mineral pada umumnya tidak peka terhadap panas, tetapi rentan terhadap pencucian atau pengolahan yang melibatkan air seperti perebusan dan pengukusan. Penurunan mineral selama pencucian dapat diperkecil dengan mengurangi jumlah air yang digunakan untuk memasak bahan makanan.
37
pengaruh yang berbeda nyata terhadap perlakuan kukus 5 menit. Menurut Bourne (1985) sebagian fosfor yang terdapat pada tanaman larut dalam air, seperti berkurangnya fosfor pada jerami yang terendam air hujan dan berkurangnya fosfor pada saat ibu rumah tangga merebus sayuran dan membuang airnya. Hal ini menyebabkan semakin lama waktu pengukusan maka kadar fosfor pada bahan akan semakin banyak hilang.
Kandungan kalsium pada genjer segar sebesar 1.892,25 mg/100 g, berbeda jauh dengan yang dikemukakan oleh Saupi et al. (2009) yaitu kandungan kalsium pada bagian genjer segar yang dapat dimakan yaitu sebesar 770,87 mg/100 g. Hal ini dapat disebabkan oleh kondisi habitat dan kandungan mineral dalam tanah maupun lumpur yang berbeda. Pada saat kalsium terdapat melimpah di dalam tanah, kalsium juga banyak terdapat pada daun yang diambil secara pasif melalui pertumbuhan akar. Daun yang lebih tua biasanya mengandung kalsium yang lebih banyak daripada daun muda. Kalsium sebagian besar terdapat dalam xylem dan dalam konsentrasi lebih kecil terdapat pada floem (Johnson dan Uriu 1990).
Kandungan kalsium genjer menurun setelah mengalami proses pengukusan. Kehilangan mineral kalsium pada waktu pengukusan 3 menit adalah sebesar 1.080,36 mg/100g dan pada pengukusan 5 menit sebesar 1.446,49 mg/100 g. Hasil uji lanjut duncan (Lampiran 14c) menyatakan bahwa perbedaan waktu pengukusan memberikan pengaruh yang berbeda nyata terhadap kandungan mineral kalsium genjer. Menurut Rahayu (2010) mineral yang terkandung dalam bahan pangan akan rusak pada sebagian besar proses pengolahan karena sensitif terhadap pH, oksigen, sinar dan panas atau kombinasi diantaranya. Hal ini menunjukkan bahwa semakin lama waktu pengukusan akan menyebabkan kehilangan mineral kalsium semakin besar.
38
Kandungan kalium genjer setelah proses pengukusan mengalami penurunan menjadi 5.146,47 mg/100 g pada pengukusan 3 menit dan 3.744,55 mg/100 g pada pengukusan 5 menit. Hal ini menunjukkan bahwa semakin lama waktu pengukusan akan mengakibatkan penurunan kadar kalium pada genjer. Hasil uji lanjut duncan (Lampiran 14d) menyatakan bahwa perbedaan waktu pengukusan memberikan pengaruh yang berbeda nyata terhadap kandungan kalium genjer. Lewu et al. (2010) menyatakan bahwa terjadi penurunan yang signifikan pada kandungan kalium Colocasia esculenta (L.) Schott setelah
dilakukan proses perebusan. Hasil ini juga didukung oleh penelitian Bethke et al. (2008) yang menyatakan kentang putih (Solanum tuberosum L.)
merupakan sumber kalium di Amerika Selatan, namun tidak baik dikonsumsi oleh orang yang menderita gagal ginjal. Perebusan pada kentang dapat menurunkan kadar kalium, sehingga dapat dikonsumsi oleh orang yang gagal ginjal.
Kandungan natrium genjer segar sebesar 574,34 mg/100 g berbeda dengan yang dikemukakan Saupi et al.(2009) yaitu kandungan natrium pada bagian genjer segar sebesar 107,72 mg/100 g. Hal ini disebabkan karena tempat hidup yang berbeda. Kandungan natrium tanaman genjer setelah proses pengukusan mengalami penurunan menjadi 169,74 mg/100 g pada pengukusan 3 menit dan 98,35 mg/100 g pada pengukusan 5 menit. Hal ini menunjukkan bahwa semakin lama waktu pengukusan akan mengakibatkan semakin tingginya penurunan kadar natrium pada genjer. Hasil uji lanjut duncan (Lampiran 14e) menyatakan bahwa perbedaan waktu pengukusan memberikan pengaruh yang berbeda nyata terhadap kandungan natrium genjer. Menurut Lewu et al. (2010) sebagian besar mineral dan vitamin larut dalam air. Merendam sayur dalam air sebelum pemasakan atau selama pemasakan akan menyebabkan hilangnya vitamin dan beberapa mineral penting. Dalam pengukusan, air yang keluar dari sayuran hanya dalam jumlah yang sedikit sehingga jumlah penurunan mineral yang terlarut dalam air pun dalam jumlah yang sedikit pula.
39
elemen, metode penanaman, serta keadaan iklim (Bethke dan Jansky 2008). Kandungan besi genjer mengalami penurunan setelah dilakukan proses pengukusan. Berdasarkan hasil uji lanjut duncan (Lampiran 14f) menyatakan bahwa perlakuan waktu pengukusan 3 menit tidak memberikan pengaruh yang berbeda nyata terhadap kandungan besi genjer segar, namun memberikan pengaruh yang berbeda nyata terhadap pengukusan 5 menit. Hasil yang diperoleh didukung oleh penelitian Karkle dan Beleia (2009) dari enam varietas soybeans yang diuji kadar besi setelah direbus, semua tidak memberikan pengaruh yang berbeda terhadap kedelai segar.
Kandungan seng pada genjer segar sebesar 749,48 mg/100 g jauh lebih tinggi bila dibandingkan hasil penelitian Saupi et al. (2007). Berdasarkan uji kandungan seng pada hasil penelitian ini menunjukkan bahwa genjer banyak menyerap seng dan besi daripada tembaga yang dideteksi ternyata hasilnya dibawah limit deteksi alat (<0,0005). Seng yang terserap oleh tanaman genjer ini kemungkinan besar juga berasal dari lingkungan perairan sawah yang banyak mengandung logam tersebut.
40
5 KESIMPULAN DAN SARAN
5.1 Kesimpulan
Komposisi kimia genjer mengalami penurunan setelah pengukusan, dimana pengukusan dengan waktu 5 menit lebih banyak menyebabkan kehilangan komposisi kimia. Hasil komposisi kimia tanaman genjer genjer segar (bk) meliputi protein (39,12%), lemak (3,29%), abu (14,73%), serat kasar (21,54%), dan abu tidak larut asam (1,64%). Perubahan komposisi kimia (bk) pada pengukusan 3 menit yaitu, protein (37,34%), lemak (3,92%), abu (13,24%), serat kasar (17,84%), dan abu tidak larut asam (1,31%). Pada pengukusan 5 menit yaitu, protein (23,23%), lemak (4,52%), abu (8,01%), serat kasar (17,51%), dan abu tidak larut asam (1,13%).
Kandungan vitamin C dan beta karoten genjer segar dan setelah proses pengukusan mengalami penurunan, semakin menurun dengan meningkatnya waktu pemasakan. Kandungan vitamin C genjer segar sebesar 46,63 mg/100 g menurun setelah pengukusan 3 menit menjadi 43,81 mg/100 g dan pada pengukusan 5 menit mejadi 37,34 mg/100 g. Kandungan beta karoten genjer segar sebesar 69,62 mg/100 g menurun setelah pengukusan 3 menit menjadi 44,87 mg/100 g dan pada pengukusan 5 menit menjadi 18,44 mg/100 g.
41
5.2 Saran
PERUBAHAN KOMPOSISI KIMIA, VITAMIN C, DAN
MINERAL PADA PENGUKUSAN
GENJER (
Limnocharis flava
)
TRI KALBU ARDININGRUM SEJATI
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
RINGKASAN
TRI KALBU ARDININGRUM SEJATI. C34080037. Perubahan Komposisi Kimia, Vitamin C, dan Mineral pada Pengukusan Genjer (Limnocharis flava). Dibimbing oleh NURJANAH dan RONI NUGRAHA.
Genjer merupakan tanaman yang biasa dikonsumsi masyarakat, tanaman ini diambil dari sekitar persawahan di Desa Cikarawang, Kelurahan Situ Gede, Bogor. Penelitian ini bertujuan untuk menentukan kandungan zat gizi (air, lemak, protein, abu, abu tidak larut asam, dan serat kasar), vitamin C, dan mineral pada genjer (L. flava) segar dan menentukan waktu pengukusan terbaik yang selama menit. Kadar lemak genjer meningkat sebesar 0,60% setelah pengukusan 3 menit dan 15,21% setelah pengukusan 5 menit. Kadar abu genjer segar mengalami penurunan sebesar 5,30% pada pengukusan 3 menit dan 29,71% pada pengukusan 5 menit. Kadar abu tidak larut asam genjer segar menurun sebesar 10,44% pada pengukusan 3 menit dan 17,98% pada pengukusan 5 menit. Serat kasar genjer segar menurun sebesar 9,42% setelah pengukusan 3 menit dan 10,29% setelah pengukusan 5 menit. Kandungan vitamin C genjer segar mengalami kehilangan vitamin C sebesar 3,20% setelah pengukusan 3 menit dan 20,06% setelah pengukusan 5 menit. Beta karoten genjer segar menurun sebesar 35,55% pada pengukusan 3 menit dan 73,51% pada pengukusan 5 menit.
PERUBAHAN KOMPOSISI KIMIA, VITAMIN C, DAN
MINERAL PADA PENGUKUSAN
GENJER (
Limnocharis flava
)
TRI KALBU ARDININGRUM SEJATI C34080037
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
Judul :Perubahan Komposisi Kimia, Vitamin C, dan Mineral pada Pengukusan Genjer (Limnocharis Flava)
Nama : Tri Kalbu Ardiningrum Sejati NIM : C34080037
Program studi : Teknologi Hasil Perairan
Menyetujui:
Dosen Pembimbing I Dosen Pembimbing II
Dr. Ir. Nurjanah MS Roni Nugraha, S.Si., M.Sc NIP. 1959 1013 1986 01 2 002 NIP. 19830421 200912 1 003
Mengetahui:
Ketua Departemen Teknologi Hasil Perairan
Dr. Ir. Ruddy Suwandi, MS, M.Phil NIP. 19580511 198503 1 002
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi dengan judul ”Perubahan
Komposisi Kimia, Vitamin C, dan Mineral pada Pengukusan Genjer (Limnocharis flava)” adalah karya saya sendiri dan belum diajukan dalam bentuk apapun kepada Perguruan Tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang telah diterbitkan oleh penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Agustus 2012
KATA PENGANTAR
Puji dan syukur dipanjatkan kehadirat Allah SWT karena telah memberikan rahmat dan hidayah-Nya kepada penulis sehingga dapat menyelesaikan penyusunan skripsi ini dengan lancar. Skripsi ini berjudul
”Perubahan Komposisi Kimia, Vitamin C, dan Mineral pada Pengukusan Genjer (Limnocharis flava)”, merupakan salah satu syarat kelulusan pada Program Sarjana Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu penulis dalam menyelesaikan skipsi ini, terutama kepada:
1. Ibu Dr. Ir. Nurjanah MS. dan Bapak Roni Nugraha, S.Si, M.Sc selaku dosen pembimbing, atas segala bimbingan dan pengarahan yang diberikan kepada penulis.
2. Bapak Dr. Ir. Ruddy Suwandi MS, M.Phil selaku dosen penguji, atas segala saran dan masukan yang diberikan kepada penulis.
3. Segenap jajaran laboratorium di lingkungan Departemen Teknologi Hasil Perairan, IPB dan Balai Besar Industri Agro (BBIA) Bogor, atas kerjasamanya dalam membantu dan membimbing selama proses penelitian. 4. Ibu Dian selaku laboran di Laboratorium Pengujian Nutrisi Pakan Fakultas
Peternakan, IPB atas bantuan dan arahannya selama penelitian.
5. Keluarga terutama Ayah (papa Suparno) dan Ibu (mama Tri Wihartini) tercinta, serta Kakak dan Adik (Ibnu dan Fadli) yang telah memberikan semangat, dukungan, dan doa kepada penulis dalam menyelesaikan skripsi ini. 6. Marisa Permatasari dan Euis Nur Aisyah selaku teman dan rekan kerja yang
baik dalam suka dan duka selama proses penelitian berlangsung.
7. Teman-teman THP 45 terutama Hilma, Fitri, Hana, Silvia, Helmi, Rico, Andi, Iis, Tacul, okta, siska, bayu, Tim ADV 45 dan yang lainnya atas dukungan serta semangat yang telah banyak membantu penulis.
9. Keluarga Pondok Putri Rahma Lantai 2 terutama Sarah, Ririn, Rivi, Muti, Oppa, Fiqa, Mamake, ka Vitria, Diska, Ikul, Ipit, ka Ratna, dan Belen atas kekeluargaan dan kebersamaannya.
10.Keluarga geng SAMPAH priska, rosi, sarah, ginas, dan nurul atas dorongan semangat dan doanya.
11.Keluarga besar Departemen Teknologi Hasil Perairan (THP), staf Dosen, Tata Usaha (TU), dan staf laboratorium (Bu Ema, Mas Zaky, Mas Andri, Mas Ipul, Mba Dini, dan Mba Lastri yang telah membantu dan mengajarkan pengujian dalam penelitian.
12.Kakak-kakak THP 43 dan adik-adik THP 47 yang telah banyak memberikan masukan dan informasi penting pada penulis sehingga skripsi ini dapat diselesaikan dengan baik.
13.Seluruh pihak yang telah membantu dalam penulisan skripsi ini, yang tidak dapat penulis sebutkan satu persatu.
Penulis menyadari bahwa masih banyak kekurangan dalam penulisan skripsi ini. Oleh karena itu, apabila terdapat kesalahan dalam penulisan skripsi ini penulis memohon maaf yang sebesar-besarnya. Penulis juga sangat mengharapkan kritik dan saran yang dapat membangun dalam penyempurnaan penyusunan skripsi ini. Semoga tulisan ini bermanfaat bagi banyak pihak yang memerlukannya.
Bogor, Agustus 2012
RIWAYAT HIDUP
Penulis dilahirkan di Kota Purwokerto, Provinsi Jawa Tengah pada tanggal 15 Februari 1991 sebagai anak ketiga dari empat bersaudara pasangan Suparno dan Tri Wihartini.
Penulis memulai pendidikannya di TK Bhayangkara (1994-1996) dan SD Negeri II Dukuhwalu kota Purwokerto (1996-2002). Penulis melanjutkan pendidikannya di SMP Negeri 3 Purwokerto (2002-2005) dan pendidikan menengah atas ditempuh penulis di SMA Muhammadiyah 1 Purwokerto (2005-2008). Pada tahun 2008, penulis diterima di Institut Pertanian Bogor melalui jalur USMI (Undangan Seleksi Masuk IPB). Penulis diterima di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Selama masa perkuliahan, penulis aktif dalam berbagai organisasi kemahasiswaan, antara lain anggota Fisheries Processing Club (FPC) periode 2008-2009, anggota Divisi Infokom Himpunan Mahasiswa Teknologi Hasil Perairan (Himasilkan) periode 2010-2011, dan anggota OMDA Ikatan Mahasiswa Banyumas (IKAMAHAMAS). Penulis juga aktif dalam kepanitian berbagai kegiatan mahasiswa di Institut Pertanian Bogor serta aktif menjadi asisten beberapa mata kuliah di Departemen Teknologi Hasil Perairan, Institut Pertanian Bogor.