PENGARUH JENIS KEDELAI, NATRIUM METABISULFIT,
DAN ASAM ASKORBAT TERHADAP KARAKTERISTIK
FISIKOKIMIA, FUNGSIONAL, DAN ORGANOLEPTIK
TEPUNG TEMPE
MUSTIKA AMINTA
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Pengaruh Jenis Kedelai, Natrium Metabisulfit, dan Asam Askorbat Terhadap Karakteristik Fisikokimia, Fungsional, dan Organoleptik Tepung Tempe adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2014
Mustika Aminta
ABSTRAK
MUSTIKA AMINTA. Pengaruh Jenis Kedelai, Natrium Metabisulfit, dan Asam Askorbat Terhadap Karakteristik Fisikokimia, Fungsional, dan Organoleptik Tepung Tempe. Dibimbing oleh JOKO HERMANIANTO dan MADE ASTAWAN.
Pengolahan lanjut tempe menjadi tepung bertujuan memperpanjang umur simpannya. Permasalahan browning dan belum adanya standar nasional tepung
tempe menjadi perhatian dalam penelitian ini. Penelitian ini bertujuan untuk mengevaluasi metode pembuatan tepung tempe, serta memeriksa sifat fisikokimia, fungsional, dan organoleptik tepung tempe berdasarkan interaksi jenis kedelai dan zat anti pencoklatan yang digunakan. Jenis kedelai yang digunakan adalah kedelai asal Grobogan dan kedelai pangan rekayasa genetik (PRG), sedangkan zat anti pencoklatan berupa natrium metabisulfit dan asam askorbat. Hasil penelitian menunjukkan bahwa tepung tempe paling baik dibuat pada suhu pengeringan 70oC dengan blansir selama lima menit pada konsentrasi zat anti pencoklatan sebesar 0.1 %. Interaksi perlakuan berpengaruh nyata (p<0.01) terhadap redness,
pH, kadar protein, dan warna organoleptik, namun tidak berpengaruh nyata (p>0.01) terhadap derajat putih, kecerahan, yellowness, aw, kadar air, abu, lemak,
karbohidrat, indeks penyerapan dan kelarutan air, aktivitas emulsi, kapasitas gelasi, serta aroma dan rasa organoleptik tepung tempe.
Kata kunci: tepung tempe, natrium metabisulfit, asam askorbat, kedelai, fisikokimia
ABSTRACT
MUSTIKA AMINTA. The Impact of Soybean Varieties, Sodium Metabisulfite, and Ascorbic Acid to Physicochemical, Functional, and Organoleptic Characteristics of Tempe Flour. Supervised by JOKO HERMANIANTO and MADE ASTAWAN.
Further processing of tempe becomes flour aims to extend its shelf life. The browning problem and the absence of tempe flour national standard may be concern in this study. The objective of this research was to evaluate the method of tempe flour making, and also asses physicochemical, functional, and organoleptic properties according to the interaction between soybean varieties and anti browning agents used. The soybean varieties used were Grobogan soybean and genetically modified organism (GMO) soybean. The anti browning agents used were sodium metabisulfite and ascorbic acid. The result showed that the best method of tempe flour making was within 70 oC of drying temperature, five
minutes of blanching, and 0,1 % of anti browning agent in blanching solution. The interaction between treatments was significantly impacting (p<0.01) redness, pH, protein content, and organoleptic color, yet not significantly impacting (p>0.01) whiteness degree, lightness, yellowness, aw, water, ash, fat, carbohydrate content,
water absorption and solubility index, emulsion activity, gelation capacity, also organoleptic aroma and taste.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Ilmu dan Teknologi Pangan
PENGARUH JENIS KEDELAI, NATRIUM METABISULFIT,
DAN ASAM ASKORBAT TERHADAP KARAKTERISTIK
FISIKOKIMIA, FUNGSIONAL, DAN ORGANOLEPTIK
TEPUNG TEMPE
MUSTIKA AMINTA
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Bapa Surgawi atas segala kasih, berkat, dan karunia-Nya sehingga penulis dapat memperoleh kekuatan, kesabaran, dan kelancaran dalam menyelesaikan skripsi ini. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2014 ini ialah tepung tempe, dengan judul Pengaruh Jenis Kedelai, Natrium Metabisulfit, dan Asam Askorbat Terhadap Karakteristik Fisikokimia, Fungsional, dan Organoleptik Tepung Tempe.
Selama penelitian dan penulisan skripsi, penulis banyak dibantu oleh berbagai pihak; oleh karena itu, terima kasih dan penghargaan setinggi-tingginya penulis ucapkan kepada:
1. Keluargaku tercinta: Ayahanda Togar Marulitua Sibuea, Ibunda Etty Saraswati, dan Mutiara Ayu Amanda untuk semua doa, kasih sayang, dukungan, dan semangat yang diberikan.
2. Bapak Dr. Ir. Joko Hermanianto selaku dosen pembimbing I yang telah memberi banyak bimbingan, nasehat, motivasi, semangat, dan penghiburan selama penelitian hingga penyusunan skripsi.
3. Bapak Prof. Dr. Ir. Made Astawan, MS selaku dosen pembimbing II yang telah memberikan topik penelitian, serta bimbingan dan evaluasi selama penelitian hingga penyusunan skripsi.
4. Eris Astari Putra, untuk semua waktu, tenaga, semangat, dan kepercayaan yang diberikan. You’re my best supporter.
5. Ayu Pramesti, Gideon Satria PS, dan Gerardus Yosua. Tanpa kalian mungkin kuliah dan tingkat akhir tidak akan semenyenangkan ini.
6. Satu tim penelitian tempe: Tessa Winandita, Dicky Aulia Rochim, Jefriaman Sirait, Armando Saragih, dan Khalid A. untuk semua suka duka yang dilewati bersama.
7. Mas Yanto dan Mas Andri, pengrajin tempe di Rumah Tempe Indonesia, untuk semua ilmu, kebaikan, dan kesabarannya mengajari cara membuat tempe.
8. Laboran ITP dan teknisi SEAFAST: Pak Sobirin, Mbak Ulfa, Pak Yahya, Mbak Irin, serta Pak Jun dan Pak Deni untuk semua bantuan dan saran yang diberikan selama penelitian.
9. Rachel Puspa dan Kartika Rizky, sahabat penulis sedari SMA, atas doa, semangat, dan dukungannya yang diberikan kepada penulis.
10.ITP 47 dan semua pihak yang tidak dapat disebutkan satu persatu untuk semua kebaikan yang telah diberikan kepada penulis selama penelitian. Semoga karya ilmiah ini bermanfaat bagi pembaca. Terima kasih.
Bogor, September 2014
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN ix
PENDAHULUAN 1
Latar Belakang 1
Tujuan 2
Manfaat 2
METODOLOGI 2
Waktu dan Tempat Pelaksanaan 2
Bahan 3
Alat 3
Tahapan Penelitian 3
Rancangan Percobaan 6
Prosedur Pengamatan 7
Pengolahan dan Analisis Data 9
HASIL DAN PEMBAHASAN 9
Penelitian Pendahuluan 9
Penelitian Utama 14
SIMPULAN DAN SARAN 36
Simpulan 36
Saran 36
DAFTAR PUSTAKA 36
LAMPIRAN 40
DAFTAR TABEL
1 Perbandingan karakteristik tepung tempe berdasarkan suhu pengeringan 10 2 Pengaruh lama blansir terhadap derajat putih dan warna tepung tempe 11 3 Pengaruh konsentrasi larutan natrium metabisulfit terhadap derajat
putih dan warna tepung tempe 12
4 Pengaruh jenis kedelai dan larutan blansir terhadap derajat putih tepung
tempe 14
5 Pengaruh jenis kedelai dan larutan blansir terhadap warna tepung tempe 18 6 Pengaruh jenis kedelai dan larutan blansir terhadap aktivitas air tepung
tempe 20
7 Pengaruh jenis kedelai dan larutan blansir terhadap pH tepung tempe 21 8 Pengaruh jenis kedelai dan larutan blansir terhadap analisis proksimat
tepung tempe 23
9 Pengaruh jenis kedelai dan larutan blansir terhadap IPA dan IKA
tepung tempe 29
10 Pengaruh jenis kedelai dan larutan blansir terhadap aktivitas dan
stabilitas tepung tempe 31
11 Pengaruh jenis kedelai dan larutan blansir terhadap kapasitas terendah
gelasi tepung tempe 32
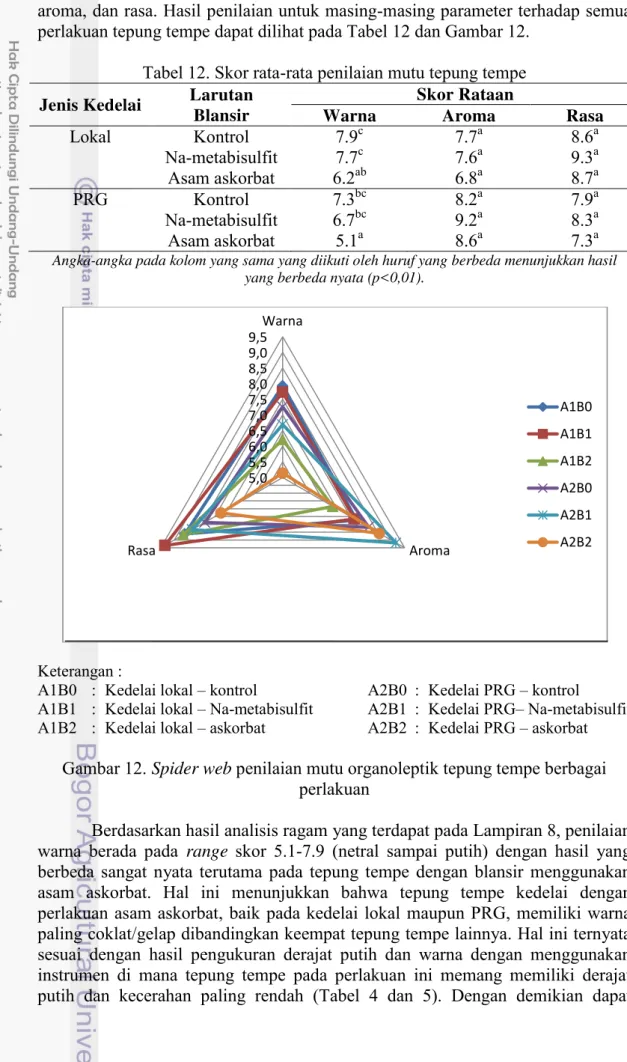
12 Skor rata-rata penilaian mutu tepung tempe 34
DAFTAR GAMBAR
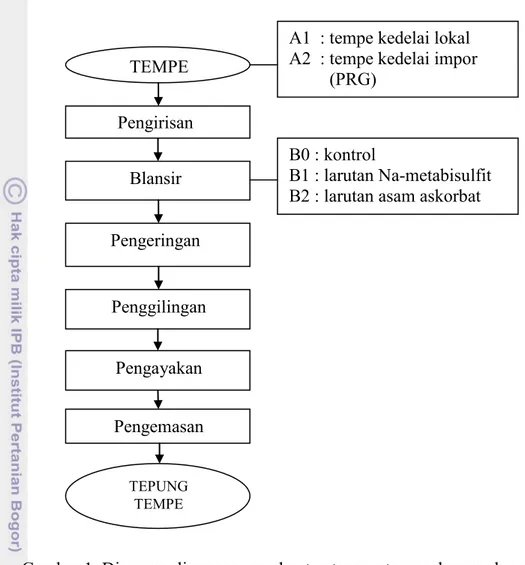
1 Diagram alir proses pembuatan tempe dengan dua perlakuan 5 2 Diagram alir metode terpilih pembuatan tepung tempe dengan dua
perlakuan 13
3 Alur reaksi Maillard 15
4 Reaksi penguraian natrium metabisulfit dalam air 15 5 Penghambatan reaksi pencoklatan non enzimatis oleh sulfit 16
6 Reaksi pencoklatan pada asam askorbat 17
7 Tepung tempe kedelai lokal 18
8 Tepung tempe kedelai PRG 18
9 Hubungan laju reaksi relatif dengan aktivitas air dalam pangan 20
10 Reaksi pembentukan lemak 25
11 Pengaruh lama penyimpanan terhadap pembentukan bilangan TBA
pada masing-masing perlakuan tepung tempe 26
12 Spider web penilaian mutu organoleptik tepung tempe berbagai
perlakuan 34
DAFTAR LAMPIRAN
1 Diagram alir proses pembuatan tempe 40
2 Diagram alir proses penetapan metode pembuatan tepung tempe 41
3 Form uji organoleptik tepung tempe 42
PENDAHULUAN
Latar Belakang
Protein dapat ditemukan pada bahan pangan hewani, seperti daging, ikan, telur, susu, serta pada bahan pangan nabati, seperti serealia dan kacang-kacangan. Protein hewani merupakan protein dengan kualitas teratas karena memiliki kandungan asam amino esensial yang lengkap, namun harganya lebih mahal dan pengadaannya membutuhkan waktu yang lebih lama. Hal inilah yang membuat protein nabati menjadi pilihan tepat untuk memenuhi kekurangan protein, terutama bagi masyarakat dengan daya beli rendah.
Pada Maret 2013, jumlah penduduk miskin di Indonesia tercatat 28,07 juta orang (BPS 2013). Ini menunjukkan bahwa sekitar 11,37 % penduduk Indonesia kesulitan untuk memenuhi kebutuhan mereka sehari-hari, termasuk membeli makanan sehat yang sesuai dengan kebutuhan gizi mereka. Menurut Bardosono (2009), Indonesia masih cukup tinggi mengalami permasalahan gizi, terutama kekurangan energi protein (KEP). Permasalahan ini membutuhkan solusi berupa sumber protein yang murah dan berkualitas tinggi.
Kedelai merupakan salah satu sumber protein nabati yang berpotensi untuk menggantikan protein hewani. Protein kedelai mengandung asam amino esensial yang lengkap dalam jumlah yang relatif lebih tinggi dibandingkan protein biji-bijian lainnya, terutama asam amino lisin, dengan metionin sebagai asam amino pembatas. Hal ini menyebabkan protein kedelai dapat digunakan untuk mensubstitusi kekurangan protein dalam makanan pokok, seperti beras dan jagung. Kandungan protein pada kedelai cukup tinggi, yaitu sekitar 40-50% dengan susunan asam amino mendekati susunan asam amino susu sapi, serta mendekati pola yang direkomendasikan oleh FAO (Palander et al. 2006).
Kedelai banyak diolah menjadi produk pangan melalui proses fermentasi oleh sejumlah kapang, seperti Rhizopus oligosporus, R. oryzae, R. stolonifer, R. arrhizus, Aspergillus oryzae, dan Mucor. Di Indonesia sendiri, produk fermentasi
kedelai yang paling banyak diproduksi adalah tempe. Sebanyak 60 % dari total kedelai nasional diolah menjadi tempe. Kedelai yang digunakan untuk pembuatan tempe sebesar 1,2 juta ton/tahun (Rosalina 2011). Menurut Astawan (2009), konsumsi tempe sebagai makanan pendamping makanan pokok di Indonesia mencapai 8,5 kg/kapita/tahun dengan 69,89 % tingkat konsumsinya terjadi di rumah tangga. Hal ini menunjukkan bahwa tempe sangat diminati oleh masyarakat Indonesia.
Permasalahan yang sering dihadapi adalah tempe merupakan produk dengan daya simpan yang rendah. Jika disimpan dalam bentuk segar hanya dapat bertahan selama dua hari pada suhu ruang, sedangkan jika disimpan dalam suhu refrigerator dengan dilapis plastik tertutup dapat memperpanjang umur simpannya menjadi satu minggu (Widowati et al. 2004). Hal ini disebabkan oleh terjadinya
fermentasi lanjut, sehingga terjadi degradasi protein lanjut membentuk amoniak yang menyebabkan timbulnya aroma busuk. Berdasarkan sifat tempe yang
perishable namun khasiatnya penting bagi gizi dan kesehatan, maka
2
Salah satu produk turunan tempe adalah tepung tempe. Tepung tempe adalah tempe generasi II, yaitu tempe yang diolah lebih lanjut sehingga tidak mempunyai bentuk dan rasa khas tempe. Selanjutnya tepung tempe dapat diaplikasikan secara luas ke produk pangan lain, seperti cake substitusi, bubur
bayi, minuman, biskuit, es krim, dan sebagainya. Akan tetapi masalah yang dihadapi adalah terjadinya browning selama pembuatan tepung sehingga
menimbulkan warna coklat yang kurang diminati masyarakat dan juga belum adanya standar nasional (SNI) untuk tepung tempe. Penggunaan zat anti pencoklatan kemudian dipertimbangkan untuk memperbaiki warna dari tepung tempe. Penelitian ini diadakan untuk mengkaji metode pembuatan serta karakterisasi sifat fisikokimia tepung tempe yang dihasilkan, baik dengan atau tanpa penggunaan zat anti pencoklatan, sehingga dapat diketahui prospek pengolahan lanjut dari tepung tempe.
Tujuan
Tujuan penelitian ini adalah mengevaluasi metode pembuatan tepung tempe, dari segi suhu pengeringan, lama waktu blansir, dan konsentrasi zat anti pencoklatan dalam larutan blansir yang digunakan (yang efisien waktu serta menghasilkan tepung dengan derajat putih dan kecerahan terbaik); mengevaluasi pengaruh natrium metabisulfit dan asam askorbat terhadap derajat putih dan kecerahan tepung tempe; mengevaluasi pengaruh jenis zat anti pencoklatan dan jenis kedelai yang digunakan terhadap sifat fisikokimia, fungsional, dan organoleptik tepung tempe; serta menentukan tepung tempe terbaik berdasarkan penilaian organoleptik.
Manfaat
Manfaat dari penelitian ini adalah menghasilkan produk turunan tempe, dalam bentuk tepung, yang memiliki umur simpan lebih lama, dapat diaplikasikan ke dalam banyak jenis makanan dan minuman olahan lainnya, serta tetap memiliki kandungan gizi yang setara dengan kandungan gizi dalam tempe asli.
METODOLOGI
Waktu dan Tempat Pelaksanaan
3 Bahan
Bahan yang digunakan dalam penelitian ini terbagi menjadi dua kelompok, yaitu bahan untuk membuat tepung tempe dan bahan untuk analisis. Bahan untuk membuat tepung tempe terdiri atas kedelai asal Grobogan dan kedelai produk rekayasa genetik (PRG), yang diperoleh dari KOPTI Bogor, air, kain saring, ragi merk Raprima, plastik pengemas polipropilen, natrium metabisulfit, dan asam askorbat. Adapun bahan-bahan yang diperlukan untuk analisis meliputi K2SO4,
HgO, H2SO4 pekat, akuades, larutan 60% NaOH - 5% Na2S2O3.5H2O, H2BO3,
alumunium foil, indikator merah metilen dan biru metilen, etanol, indikator PP 1%, HCl 0,02 N dan 4 M, larutan HCl 25%, kertas saring Whatman No. 1, kapas bebas lemak, heksana, batu didih, minyak sawit komersial, Thio Barbituric Acid
(TBA), dan asam asetat glasial 90%. Alat
Alat yang digunakan dalam penelitian ini meliputi alat-alat untuk membuat tempe, tepung tempe, dan analisis. Alat untuk membuat tempe terdiri atas ember, wadah perebus antikarat, mesin pengupas kulit kedelai antikarat, rak fermentasi antikarat, dan ruang fermentasi. Alat untuk membuat tepung tempe meliputi timbangan, baskom, pisau, slicer, dandang, tray drier, blender, termometer,
ayakan 40 mesh, dan sealer. Alat yang digunakan untuk analisis yaitu neraca
analitik, whiteness meter, chromameter, aw meter, pH meter, oven pengering,
cawan alumunium, cawan porselen, pemanas Kjeldahl, labu Kjeldahl 30 mL, buret 50 mL, labu takar, labu lemak, labu destilasi, Soxhlet, desikator berisi bahan pengering (P2O5 kering, CaCl2 kering, atau butiran silika berwarna biru), tanur,
destilator, labu Erlenmeyer, gelas piala, gelas ukur, pendingin balik, mixer,
sentrifuse, tabung sentrifus, penangas air, hot plate, magnetic stirrer, pipet tetes,
sudip, spatula, tabung reaksi bertutup, rak tabung reaksi, pipet Mohr, bulb, penggaris, vortex, dan spektrofotometer.
Tahapan Penelitian
Penelitian ini dibagi menjadi dua tahap, yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan terdiri atas proses pembuatan tempe, penentuan metode pembuatan tepung tempe yang tepat, serta penentuan konsentrasi larutan perendam natrium metabisulfit dan asam askorbat. Penelitian utama terdiri atas tahap pembuatan tepung tempe dengan blansir menggunakan larutan natrium metabisulfit dan asam askorbat, serta tahap analisis sifat fisikokimia, fungsional, dan uji organoleptik tepung tempe yang dihasilkan. Penelitian Pendahuluan
Proses Pembuatan Tempe
Pembuatan tempe dilakukan dengan menerapkan Good Hygienic Practices
4
kemudian direbus selama 30-45 menit. Kedelai lalu direndam dalam air selama 15 jam. Setelah itu kedelai dipecah, kulit dikupas dan dicuci kembali hingga bersih. Selanjutnya kedelai kupas disiram dengan air panas beberapa kali, kemudian ditiriskan dan didinginkan hingga mencapai suhu 35-40 oC. Kedelai lalu
diinokulasi dengan ragi tempe merk Raprima dengan formula 1 gram ragi per kg kedelai, diaduk hingga ragi merata, dan dibungkus dengan plastik pembungkus. Pembungkus yang digunakan berupa plastik perforasi untuk mengatur suhu dan kelembaban yang dibutuhkan untuk pertumbuhan kapang. Selanjutnya kedelai diinkubasi agar terjadi proses fermentasi selama 36-48 jam. Diagram alir proses pembuatan tempe dapat dilihat pada Lampiran 1.
Penetapan Metode Pembuatan Tepung Tempe
Pembuatan tepung tempe memiliki tahapan yang secara umum sama, yaitu pengirisan tempe, blansir, pengeringan tempe, penggilingan, dan pengayakan. Pada tahap pertama dilakukan penetapan suhu pengeringan dalam pengolahan tepung tempe. Parameter suhu yang diujikan, yaitu 60 oC (Murni 2013), 70 oC
(Bastian et al. 2013), dan 80 oC (Inayati 1991). Hasil dari masing-masing suhu
pengeringan kemudian diuji nilai derajat putih dan warnanya untuk menentukan suhu terpilih. Suhu terpilih selanjutnya diuji kembali dengan menerapkan empat lama waktu blansir, yaitu 3, 5, 10, dan 15 menit. Tepung yang dihasilkan kemudian diuji nilai derajat putih dan warnanya. Tahapan proses penetapan metode dapat secara sistematis dilihat pada Lampiran 2.
Penentuan Parameter Konsentrasi Larutan Blansir
Penentuan konsentrasi larutan blansir dilakukan dengan menggunakan natrium metabisulfit sebagai acuan. Konsentrasi natrium metabisulfit yang digunakan adalah 0, 0.1, dan 0.3%. Tepung yang dihasilkan kemudian diukur warnanya (L,a,b) dengan chromameter dan derajat putihnya dengan whiteness meter untuk menentukan konsentrasi larutan terbaik.
Penelitian Utama
Pembuatan Tepung Tempe dengan Dua Perlakuan
5
Gambar 1. Diagram alir proses pembuatan tepung tempe dengan dua perlakuan
Karakterisasi Fisik Tepung Tempe
Karakterisasi fisik tepung tempe meliputi uji derajat putih, uji warna notasi Hunter, dan uji aktivitas air.
Karakterisasi Kimia Tepung Tempe
Karakterisasi kimia tepung tempe meliputi uji nilai pH, kadar air, kadar abu, kadar protein, kadar lemak, kadar karbohidrat, dan uji bilangan TBA (thiobarbituric acid).
Karakterisasi Fungsional Tepung Tempe
Karakterisasi fungsional tepung tempe meliputi uji indeks penyerapan air dan indeks kelarutan air, uji aktivitas emulsi, serta uji kapasitas gelasi.
TEMPE
Pengirisan
Blansir
A1 : tempe kedelai lokal A2 : tempe kedelai impor (PRG)
B0 : kontrol
B1 : larutan Na-metabisulfit B2 : larutan asam askorbat Pengeringan
Penggilingan
Pengayakan
6
Uji Organoleptik Tepung Tempe
Uji organoleptik tepung tempe dilakukan dengan menggunakan 16 orang panelis semi terlatih. Uji organoleptik yang dilakukan adalah uji rating mutu menggunakan skala garis yang dapat disetarakan dengan skor 1-9. Panelis memberikan penilaian terhadap parameter uji tanpa membandingkan antarsampel. Parameter yang dinilai meliputi, warna, aroma, dan rasa tepung tempe. Skor penilaian untuk parameter warna berupa amat sangat coklat sampai dengan amat sangat putih, skor penilaian untuk parameter aroma berkisar antara amat sangat tengik sampai amat sangat khas aroma tempe, dan skor penilaian untuk parameter rasa dimulai dari amat sangat berasa hingga amat sangat tawar. Form uji organoleptik dapat dilihat pada Lampiran 3.
Rancangan Percobaan
Model rancangan percobaan yang digunakan dalam penelitian ini adalah Rancangan Acak Faktorial dengan dua perlakuan, yaitu jenis kedelai dan jenis zat anti pencoklatan, serta dua kali ulangan. Faktor yang diteliti adalah pengaruh jenis bahan baku kedelai pada pembuatan tempe (A) dan pengaruh penggunaan jenis zat anti pencoklatan sebagai larutan blansir (B).
Faktor A : jenis bahan baku kedelai A1 : kedelai lokal
A2 : kedelai impor PRG Faktor B : jenis zat anti pencoklatan
B0 : kontrol
B1 : Natrium metabisulfit B2 : Asam askorbat
Peubah yang diukur adalah sifat fisik (derajat putih, warna, dan aktivitas air), sifat kimia (pH, analisis proksimat, dan nilai TBA), sifat fungsional (indeks penyerapan dan kelarutan air, emulsi, dan gelasi), serta organoleptik tepung tempe yang dihasilkan. Adapun model matematis untuk rancangan acak faktorial adalah sebagai berikut:
Yijk = µ + Ai + Bj +ABij + ɛ(k)ij
Keterangan :
Yijk = pengaruh faktor A taraf ke-i, faktor B taraf ke-j, dan ulangan ke-k.
µ = rata-rata umum
Ai = efek perlakuan ke-i faktor A terhadap peubah respon
Bj = efek perlakuan ke-j faktor B terhadap peubah respon
ABij = efek dari interaksi taraf ke-i faktor A dan taraf ke-j faktor B terhadap
peubah respon
ɛ(k)ij = galat percobaan ulangan ke-k karena pengaruh faktor A ke-i dan faktor
B ke-j
i = jenis bahan baku kedelai (kedelai lokal, impor PRG)
7 Prosedur Pengamatan
Prosedur Analisis Sifat Fisik
Analisis Derajat Putih (Andarwulan et al. 2011)
Pengukuran derajat putih menggunakan alat KETT Digital Whiteness Meter
Model C-100. Sampel ditempatkan dalam cawan sampel dengan jumlah sedikit melebihi bibir cawan. Cawan berisi sampel ditempatkan ke dalam wadah sampel. Wadah contoh dimasukkan ke tempat pengukuran, sehingga alat menyala. LED menampilkan nilai derajat putih dan nomor urutan pengukuran. Standar menggunakan MgO dengan nilai 81.6. Nilai derajat putih sampel diukur dengan membandingkan nilai derajat putih yang terbaca pada alat dengan nilai derajat putih BaSO4 sebagai standar yaitu sebesar 110.8.
Analisis Warna Notasi Hunter (Djuanda 2003)
Pengukuran warna menggunakan alat chromameter CR 300 Minolta.
Sampel dimasukkan ke dalam cawan kaca sampai permukaannya sama rata dengan bibir cawan. Measuring head chromameter diletakkan pada sampel yang
akan diukur kemudian tombol „MEASURE‟ pada measuring head ditekan. Warna
dibaca oleh detektor digital dan hasilnya ditampilkan di layar. Pengukuran dilakukan sebanyak tiga kali untuk masing-masing sampel. Notasi L, a, b digunakan sebagai parameter warna. Notasi L menggambarkan kecerahan dengan kisaran 0-100, nilai 0 berarti hitam dan 100 berarti putih. Notasi a menggambarkan warna kromatik campuran merah-hijau dengan nilai +a dari 0-(+100) untuk warna merah dan –a dari 0-(-80) untuk warna hijau. Notasi b menggambarkan warna kromatik campuran biru-kuning dengan nilai +b dari 0-(+70) untuk warna kuning dan –b dari 0-(-70) untuk warna biru.
Analisis Aktivitas Air (Nurhayati 2010)
Penetapan aw dilakukan dengan menggunakan alat aw meter Shibaura WA
360. Sebanyak ±1 gram sampel dimasukkan ke dalam wadah aw meter.
Pembacaan skala dilakukan setelah indikator proses pada layar penunjuk proses pengukuran telah selesai (Nurhayati 2010).
Prosedur Analisis Sifat Kimia
Analisis Nilai pH dan Proksimat (AOAC 2005)
8
Analisis Bilangan TBA (Metode Tarladgis (1960), dikutip oleh Andarwulan et al. (2011))
Sebanyak 10 gram tepung tempe disuspensikan dengan 50 mL akuades menggunakan waring blender selama dua menit. Suspensi kemudian dipindahkan
secara kuantitatif ke labu destilasi sambil dicuci dengan 47,5 mL akuades. Sebanyak 2,5 mL HCl 4 M ditambahkan sampai pH turun menjadi 1,5. Batu didih dan vaselin secukupnya juga ditambahkan, kemudian labu destilasi dipasang pada alat destilasi.
Destilasi dilakukan pada suhu 90oC selama 10 menit sampai diperoleh 50
mL destilat. Sebanyak 5 mL destilat kemudian dipipet ke dalam tabung reaksi bertutup. Setelah itu, ditambahkan 5 mL pereaksi TBA, tabung reaksi ditutup,
di-vortex, dan dipanaskan di air mendidih selama 35 menit. Selanjutnya tabung
reaksi didinginkan dengan air pendingin selama 10 menit. Absorbansi (D) larutan diukur pada panjang gelombang 528 nm dengan blanko sebagai titik nol. Blanko dibuat dengan mencampurkan 5 mL akuades dengan 5 mL pereaksi. Bilangan TBA diketahui dengan perhitungan sebagai berikut.
Bilangan TBA = 7,8 X D
Prosedur Analisis Sifat Fungsional
Analisis Indeks Penyerapan Air dan Indeks Kelarutan Air (Metode Sentrifugasi Anderson, dikutip oleh Muchtadi et al. 1988)
Sebanyak satu gram tepung sampel dimasukkan dalam tabung sentrifus. Setelah itu ditambahkan 10 mL akuades dan diaduk dengan menggunakan vortex
sampai semua bahan terdispersi secara merata. Selanjutnya tabung disentrifugasi dengan kecepatan 2000 rpm pada suhu ruang selama 15 menit. Supernatan yang diperoleh dituang secara hati-hati ke dalam wadah lain, sedangkan tabung sentrifus beserta isinya dipanaskan dalam oven. Tabung diletakkan dalam oven yang diatur pada suhu 50 oC selama 25 menit. Akhirnya tabung residu ditimbang untuk menentukan berat air yang terserap. Dari supernatan yang diperoleh, diambil sampel sebanyak 2 mL dan dimasukkan ke dalam cawan alumunium yang telah diketahui beratnya. Cawan dimasukkan ke dalam oven dan dikeringkan pada suhu 105 oC selama tiga jam. Setelah itu cawan didinginkan dan ditimbang untuk mengetahui berat padatan kering yang terdapat dalam supernatan.
⁄
⁄
Analisis Aktivitas Emulsi (Andualem dan Amare 2013)
9 campuran dan kemudian diaduk selama lima menit. Sampel yang teremulsi lalu dibagi menjadi dua bagian sama banyak (50 mL), dimasukkan ke dalam tabung sentrifus, dan masing-masing digunakan untuk menentukan aktivitas emulsi dan stabilitas emulsi. Penentuan aktivitas emulsi dilakukan dengan sentrifugasi sampel pada kecepatan 4000 rpm selama 30 menit. Selanjutnya hasil sentrifugasi dituang ke dalam gelas ukur 50 mL lalu tunggu selama beberapa menit sampai lapisan emulsinya stabil. Aktivitas emulsi ditunjukan sebagai presentase dari tinggi lapisan minyak teremulsi dibandingkan dengan tinggi dari semua lapisan yang terbentuk.
Analisis Kapasitas Gelasi (modifikasi Andualem dan Amare 2013)
Suspensi sampel tepung tempe dibuat pada konsentrasi 2-25 % dalam lima mililiter akuades di tabung reaksi bertutup. Sampel kemudian dipanaskan selama satu jam di dalam penangas air mendidih. Selanjutnya sampel didinginkan secara cepat di air mengalir. Sampel lalu didinginkan pada suhu 4 oC selama dua jam.
Konsentrasi terendah gelasi ditentukan sebagai konsentrasi ketika sampel tidak tumpah saat tabung dibalik.
Pengolahan dan Analisis Data
Data hasil analisis sifat fisik, kimia, fungsional, dan organoleptik tepung tempe hasil penelitian diolah menggunakan Microsoft Excel selanjutnya dianalisis
menggunakan sidik ragam (ANOVA) dengan program SPSS 20 for Windows. Jika
hasil sidik ragam menunjukkan pengaruh yang nyata, maka dilakukan uji lanjut Duncan.
HASIL DAN PEMBAHASAN
Penelitian Pendahuluan Penentuan Metode Pembuatan Tepung Tempe
Salah satu tahapan dalam pembuatan tepung tempe adalah pengeringan. Pengeringan merupakan proses mengeluarkan atau menghilangkan sebagian air dari suatu bahan dengan cara menguapkan air tersebut menggunakan energi panas. Pengolahan bahan pangan dengan metode pengeringan dimaksudkan untuk mengendalikan laju kerusakan bahan pangan agar diperoleh bahan pangan olahan kering yang bermutu, aman, dan stabil selama masa penyimpanan (Dewi 2006). Penentuan metode pembuatan tepung tempe pada penelitian ini diawali dengan menetapkan suhu pengeringan. Hal ini penting karena suhu pengeringan dapat berdampak pada perubahan bentuk, sifat fisik, kimia, dan organoleptik, serta penurunan mutu dari sifat asal bahan yang digunakan (Lubis 2009). Faktor suhu yang diujikan adalah suhu 60, 70, dan 80 oC. Pengaruh suhu pengeringan terhadap
10
Tabel 1. Perbandingan karakteristik tepung tempe berdasarkan suhu pengeringan Suhu 60 45.63±0.81 75.31±0.88 0.45±0,13 20.46±0.46 23.06±4.84 70 45.96±2.77 75.50±1.46 0.82±0.13 19.47±1.63 23.83±4.82 80 40.00±2.64 72.14±1.48 2.27±0.31 22.78±1.22 24.47±2.38 Hasil menunjukkan bahwa suhu 80 oC menyebabkan tepung tempe
memiliki derajat putih (40.00±2.64 %) dan nilai L (72.14±1.48) yang paling rendah dibandingkan dengan tepung yang dikeringkan pada suhu 60 dan 70 oC.
Menurut Rizal et al. (2013), semakin tinggi suhu pengeringan akan menurunkan
derajat putih bahan. Penurunan derajat putih disebabkan reaksi pencoklatan non enzimatik akibat bahan yang sensitif terhadap suhu tinggi. Laju reaksi pencoklatan meningkat tajam pada suhu yang lebih tinggi, sehingga menyebabkan proses pencoklatan semakin cepat terjadi.
Pengaruh suhu pengeringan juga dilihat terhadap karakteristik warna dengan menggunakan notasi Hunter. Sistem notasi warna Hunter dicirikan dengan tiga parameter warna, yaitu kecerahan (L), warna kromatik (a), dan intensitas warna (b) (Andarwulan et al. 2011). Nilai a (redness) merupakan kisaran nilai
yang menunjukkan intensitas warna hijau (a negatif) sampai merah (a positif.). Nilai b (yellowness) merupakan kisaran nilai yang menunjukkan intensitas warna
biru (b negatif) sampai kuning (b positif) (Purwanto et al. 2013). Apabila melihat
hasil pengamatan terhadap nilai a, suhu 80 oC memberikan pengaruh terhadap
tingginya intensitas redness dibandingkan dengan suhu 60 dan 70 oC. Dengan
demikian dapat diketahui bahwa suhu 80 oC menyebabkan tepung memiliki
intensitas warna merah yang paling besar. Hasil pengukuran terhadap nilai b juga memberikan hasil serupa. Pengeringan pada suhu 80 oC ternyata juga
menyebabkan warna kuning yang paling dominan di antara tepung lainnya. Nilai a dan b yang semakin besar berpengaruh pada rendahnya nilai L dan derajat putih. Hal ini sesuai dengan hasil penelitian Dewi (2006) bahwa semakin tinggi suhu pengeringan yang digunakan maka semakin gelap pula warna tepung tempe yang dihasilkan. Alasannya karena proses pengeringan yang berlangsung cepat pada suhu tinggi menyebabkan perubahan warna yang lebih banyak daripada pengeringan pada suhu dan kecepatan yang lebih rendah (Fellows 1990 di dalam Dewi 2006). Berdasarkan hasil pengamatan ini, dapat disimpulkan suhu 80 oC
paling tidak baik untuk digunakan sebagai suhu pengeringan tepung tempe.
Berdasarkan hasil pada Tabel 1, karakteristik kecerahan (L) dan derajat putih paling tinggi dihasilkan oleh tepung dengan suhu pengeringan 70 oC. Selain itu, pertimbangan akan efisiensi waktu pengeringan dan pemakaian energi panas juga turut mendukung pemilihan suhu tersebut. Suhu 70oC menurut metode
Bastian et al. (2013) adalah suhu terpilih karena waktu pengeringannya hanya
berlangsung selama 4-4,5 jam dibandingkan suhu 60 oC yang berlangsung selama
5-5,5 jam.
11 beberapa menit pada suhu mendekati air mendidih atau tepat pada suhu air mendidih. Dalam proses pengeringan, blansir dimaksudkan untuk mencegah perubahan akibat aktivitas enzim, serta mematikan dan mengurangi mikroba yang ada di permukaan bahan (Dewi 2006). Perlakuan blansir mampu menginaktivasi enzim sehingga tidak merangsang reaksi metabolisme yang menyebabkan perubahan warna dan timbulnya bau tidak enak (Ikrawan 2004). Akan tetapi, karena perubahan warna yang terjadi pada pembuatan tepung tempe bukan disebabkan reaksi enzimatis maka perlu diketahui apa ada pengaruh lama blansir terhadap karakteristik derajat putih dan warna dari tepung tempe.
Suhu blansir yang digunakan adalah 99±1 oC dengan metode perebusan.
Suhu ini sudah memenuhi syarat untuk mematikan mikroba target pada tempe, yaitu kapang Rhizopus, yang tidak dapat hidup di atas suhu 42oC (Dewi 2006).
Lama waktu yang digunakan untuk blansir bervariasi antara 3-15 menit. Pengujian ini dimaksudkan untuk melihat perbedaan lama blansir terhadap karakteristik (derajat putih dan warna) tepung tempe yang dihasilkan pada suhu pengeringan 70oC. Hasil analisis selengkapnya dapat dilihat pada Tabel 2.
Tabel 2. Pengaruh lama blansir terhadap derajat putih dan warna tepung tempe Lama blansir Hasil penelitian menunjukkan bahwa semakin lama waktu blansir akan semakin rendah derajat putihnya, namun akan semakin tinggi kecerahannya (nilai L) sampai menit ke-10. Lama waktu blansir memberikan pengaruh yang berbeda terhadap nilai a dan b. Hasil ini sesuai dengan penelitian Isnaini dan Aniswatul (2010) bahwa lama blansir memiliki pengaruh nyata terhadap warna produk. Blansir selama tiga dan lima menit menyebabkan intensitas warna merah dan kuning yang lebih rendah sehingga berpengaruh terhadap tingginya derajat putih. Sebaliknya, blansir selama 10 dan 15 menit memperkuat intensitas warna merah dan kuning. Hal ini sesuai dengan salah satu fungsi blansir, yaitu untuk mempertajam warna alami bahan pangan (Purwanto et al. 2013). Terdapat
perbedaan hasil terbaik antara karakteristik derajat putih dan kecerahan. Nilai derajat putih tertinggi (47.06±1.08 %) dihasilkan dari blansir selama lima menit sedangkan nilai kecerahan tertinggi (76.34±0.01) dihasilkan tepung yang diblansir selama 10 menit. Meskipun demikian, blansir selama lima menit kemudian dipilih karena menghasilkan derajat putih yang paling tinggi dan nilai kecerahan yang juga tinggi.
Penentuan Parameter Konsentrasi Larutan Blansir
12
pencoklatan, baik secara enzimatis maupun non enzimatis, pada bahan pangan, seperti pada pengolahan gula pasir (Alreza 2012). Selain itu sifatnya efektif, stabil, dan harganya murah (Rahayu 1997).
USFDA pda tahun 1995 telah memasukkan sulfur dioksida dan beberapa garam sulfit lainnya sebagai GRAS (21 CFR 182), tetapi tidak boleh digunakan dalam daging atau pangan sumber thiamin, buah, dan sayuran segar. Regulasi penggunaan sulfit pada makanan berbeda-beda untuk setiap negara. FDA mengatur batas maksimum penggunaan SO2 pada makanan yang dikeringkan
sebesar 2000-3000 ppm. Batas maksimum residu SO2 dalam produk tepung
maksimum 70 mg/kg menurut Peraturan KBPOM Nomor 36 Tahun 2013 tentang Batas Maksimum Penggunaan BTP Pengawet.
Konsentrasi natrium metabisulfit yang diujikan adalah 0; 0,1; dan 0,3 %. Konsentrasi tersebut dipilih mengingat proses blansir yang hanya dilakukan dalam waktu singkat, di mana tidak 100 % senyawa sulfit akan terserap tempe, dan adanya proses pengeringan. Kelebihan sulfur dioksida dapat hilang selama proses pengeringan. Dengan demikian konsentrasi larutan blansir yang tinggi sepertinya tidak akan meninggalkan residu SO2 yang melewati batas maksimum regulasinya.
Tepung tempe yang dihasilkan selanjutnya dianalisis derajat putih dan nilai L, a, b. Hasil analisis selengkapnya dapat dilihat pada Tabel 3.
Tabel 3. Pengaruh konsentrasi larutan Na-metabisulfit terhadap derajat putih dan warna tepung tempe
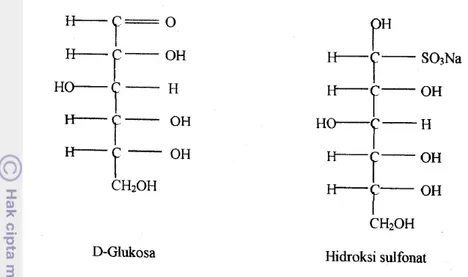
Berdasarkan Tabel 3 dapat diketahui bahwa konsentrasi larutan blansir mempengaruhi intensitas derajat putih, nilai L, a, dan b tepung tempe. Semakin tinggi konsentrasi larutan natrium metabisulfit maka semakin besar kecerahan tepung tempe. Hal ini disebabkan oleh fungsi sulfit yang dapat menghambat reaksi pencoklatan dengan cara membentuk ikatan dengan gugus aldehid gula pereduksi sehingga gugus aldehid tidak memiliki kesempatan untuk bereaksi dengan asam amino. Dengan demikian sulfit mencegah konversi D-glukosa menjadi 5-hidroksi metal furfural atau HMF. Senyawa ini merupakan senyawa antara yang berkontribusi pada pembentukan pigmen melanoidin yaitu pigmen yang berperan dalam pembentukan warna coklat pada pangan (Purwanto et al.
2013).
Perendaman dengan natrium metabisulfit berpengaruh terhadap peningkatan intensitas warna merah pada tepung tempe. Peningkatan intensitas warna merah sepertinya diakibatkan pigmen alami dalam kedelai yang diperkuat karena pengaruh blansir. Seperti yang telah disebutkan sebelumnya, salah satu fungsi blansir dapat meningkatkan warna alami bahan pangan (Purwanto et al.
13 metabisulfit dengan konsentrasi 0,1 % terpilih karena memiliki nilai derajat putih tertinggi dan nilai kecerahan yang tinggi pula.
Berdasarkan hasil uji pendahuluan untuk menentukan suhu pengeringan, lama waktu blansir, dan konsentrasi larutan blansir yang akan digunakan dalam pengolahan tepung tempe maka diperoleh metode pembuatan tepung tempe dalam penelitian ini sebagai berikut. Sebanyak 500 gram tempe diiris tipis menggunakan
slicer lalu tempe diblansir dalam larutan blansir 0.1 % selama lima menit pada
suhu 99±1 oC. Selanjutnya tempe ditiriskan. Kemudian tempe dikeringkan menggunakan tray drier pada suhu 70 oC selama 4-4.5 jam. Setelah itu tempe
kering digiling menggunakan blender dan diayak menggunakan saringan 40 mesh.
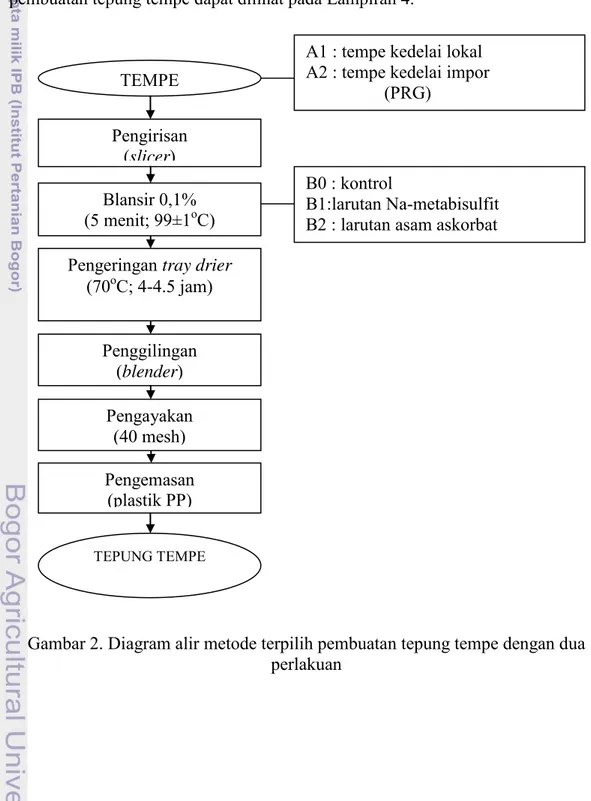
Tepung tempe dikemas dalam pastik polipropilen. Metode pembuatan tepung tempe secara sistematis dapat dilihat pada Gambar 2. Dokumentasi proses pembuatan tepung tempe dapat dilihat pada Lampiran 4.
Gambar 2. Diagram alir metode terpilih pembuatan tepung tempe dengan dua perlakuan
TEMPE
Pengirisan (slicer)
Blansir 0,1% (5 menit; 99±1oC)
A1 : tempe kedelai lokal A2 : tempe kedelai impor
(PRG)
B0 : kontrol
B1:larutan Na-metabisulfit B2 : larutan asam askorbat Pengeringan tray drier
(70oC; 4-4.5 jam)
Penggilingan (blender)
Pengayakan (40 mesh)
TEPUNG TEMPE Pengemasan
14
Penelitian Utama Karakteristik Fisik
Derajat Putih
Derajat putih adalah daya memantulkan cahaya yang mengenai permukaan bahan. Nilai yang diperoleh adalah perbandingan dengan warna putih barium sulfat (Nurhayati 2010). Derajat putih suatu produk berkisar antara 0 sampai 100. Nilai 0 menunjukkan warna hitam sedangkan nilai 100 menunjukkan warna putih (Rizal et al. 2013). Hasil pengukuran derajat putih tepung tempe pada penelitian
ini berkisar antara 40.54-48.11 %. Derajat putih tertinggi dimiliki oleh tepung tempe kedelai lokal pada perlakuan kontrol dan yang diblansir menggunakan larutan natrium metabisulfit 0.1 %, sedangkan derajat putih terendah dimiliki oleh tepung tempe kedelai PRG dengan blansir menggunakan larutan asam askorbat 0,1 %. Hasil selengkapnya dapat dilihat pada Tabel 4.
Tabel 4. Pengaruh jenis kedelai dan larutan blansir terhadap derajat putih tepung tempe
Jenis Kedelai Larutan Blansir Derajat Putih (%)
Lokal Kontrol 46.86±1.50
Angka-angka pada kolom yang sama yang diikuti oleh huruf yang berbeda menunjukkan hasil yang berbeda sangat nyata (p<0,01).
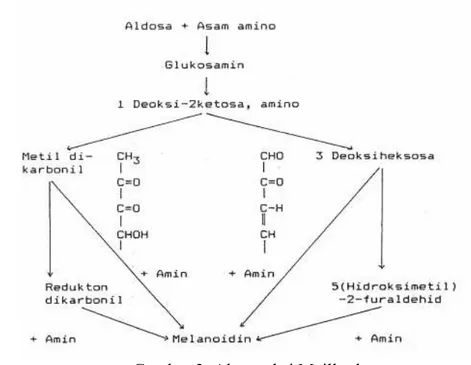
Nilai derajat putih tepung tempe berbeda sangat nyata (p<0.01) antarjenis kedelai dan larutan blansir berdasarkan hasil analisis ragam seperti yang terdapat pada Lampiran 5. Hasil analisis ragam juga menunjukkan bahwa tidak ada interaksi yang terjadi antara variabel jenis kedelai dengan jenis larutan blansir selama pengolahan tepung tempe. Dapat diketahui bahwa nilai derajat putih tepung tempe kedelai PRG memiliki kisaran yang lebih rendah jika dibandingkan dengan tepung tempe kedelai lokal. Secara umum, tepung tempe kontrol pada kedelai lokal maupun PRG memiliki derajat putih yang rendah, yaitu kurang dari 50.00%. Rendahnya derajat putih disebabkan terjadinya reaksi pencoklatan non enzimatis, yaitu reaksi Maillard. Reaksi Maillard dapat terjadi karena adanya reaksi antara senyawa yang mengandung gugus amin bebas (asam amino, protein, atau senyawa lain yang mengandung gugus amin) dengan gugus karbonil gula-gula pereduksi (gula-gula aldosa) dalam bahan pangan, dikatalis dengan adanya pemanasan, yang dalam hal ini terjadi pada saat proses pengeringan, dan pada kondisi aktivitas air sebesar 0.50-0.80. Reaksi awal gugus amin dengan gugus karbonil gula pereduksi menghasilkan senyawa glucosyl amine. Senyawa ini
kemudian melalui Amadori rearrangement membentuk amino-deoxy-ketose.
15
Gambar 3. Alur reaksi Maillard
(Whistler dan Daniel 1985, dalam Chandra et al. 2013)
Penggunaan natrium metabisulfit cenderung meningkatkan derajat putih tepung tempe jika dibandingkan dengan kontrol pada kedua jenis kedelai, meskipun tidak secara signifikan. Mekanisme pencegahan pencoklatan oleh natrium metabisulfit adalah sebagai berikut. Natrium metabisulfit di dalam air akan terurai menjadi sulfur dioksida (SO2), ion HSO3-, dan asam sulfit (Frazier
1976, dalam Chandra et al. 2013). Reaksi penguraian garam sulfit menjadi ion-ion
sebagaimana telah dipaparkan sebelumnya dapat dilihat pada Gambar 4.
Gambar 4. Reaksi Penguraian Natrium Metabisulfit dalam Air
Menurut Braverman (1963) dalam Chandra et al. (2013), mekanisme
16
Gambar 5. Penghambatan reaksi pencoklatan non enzimatis oleh sulfit Peningkatan derajat putih secara signifikan dapat dilakukan dengan meningkatkan konsentrasi larutan perendam natrium metabisulfit. Sementara itu, asam askorbat yang diharapkan mampu menjadi anti browning agent ternyata
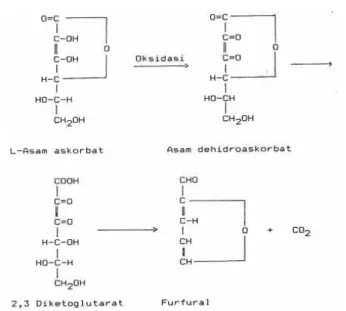
menurunkan derajat putih tepung tempe secara sangat nyata, baik pada tepung tempe kedelai lokal maupun PRG. Hal ini terjadi karena asam askorbat merupakan senyawa yang tidak stabil dalam bentuk larutan dan bila terpapar panas. Asam askorbat merupakan senyawa yang lebih efektif untuk mencegah pencoklatan enzimatis karena kapasitasnya sebagai antioksidan (Fennema 2007), sedangkan reaksi pencoklatan yang dialami tepung tempe bukanlah reaksi pencoklatan enzimatis, melainkan non enzimatis. Dengan demikian yang terjadi adalah asam askorbat teroksidasi dan terdegradasi karena pengaruh pemanasan selama blansir dan pengeringan. Menurut Andarwulan dan Sutrisno (2008), perlakuan panas pada saat pengolahan pangan selama satu jam dapat menyebabkan kerusakan asam askorbat sebanyak 50 %. Kerusakan asam askorbat akibat oksidasi sendiri merupakan salah satu penyebab dalam reaksi pencoklatan non enzimatis (Prangdimurti et al. 2007). Winarno (1986) dalam Chandra et al.
(2013) juga menyebutkan bahwa asam askorbat merupakan suatu senyawa reduktor dan dapat bertindak sebagai prekursor untuk pembentukan warna coklat non-enzimatik. Asam askorbat berada dalam keseimbangan dengan asam dehidroaskorbat. Dalam suasana asam, cincin lakton asam dehidroaskorbat terurai secara irreversible dengan membentuk senyawa diketoglutarat dan kemudian
17
Gambar 6. Reaksi pencoklatan pada asam askorbat (Theander 1980, dalam Chandra et al. 2013)
Warna
Warna merupakan salah satu atribut mutu yang sangat penting pada bahan dan produk pangan. Peranan warna sangat nyata karena umumnya konsumen akan mendapat kesan pertama, baik suka atau tidak suka terhadap suatu produk pangan. Warna memiliki arti dan peranan penting pada produk pangan sebagai penciri jenis, tanda-tanda pematangan buah, tanda-tanda kerusakan, petunjuk tingkat mutu, pedoman proses pengolahan, dan sebagainya. Analisis terhadap warna dinyatakan dalam sistem notasi. Sistem notasi warna adalah suatu cara sistematik dan objektif untuk menyatakan atau mendeskripsikan suatu jenis warna. Warna dinyatakan secara kuantitatif dalam notasi huruf dan atau angka sehingga dapat dipahami secara konsisten oleh semua pihak (Andarwulan et al. 2011).
Analisis warna pada penelitian ini dinyatakan dalam sistem notasi Hunter, yaitu L,a,b. Pengaruh interaksi jenis kedelai dengan jenis larutan blansir terhadap warna tepung tempe disajikan pada Tabel 5. Tabel 5 menunjukkan bahwa blansir menggunakan natrium metabisulfit dan asam askorbat tidak berpengaruh secara nyata terhadap nilai L (lightness) namun berpengaruh sangat nyata terhadap nilai a
(redness) dan b (yellowness).
Menurut hasil analisis ragam pada Lampiran 5, pengaruh sangat nyata yang timbul pada nilai a disebabkan karena faktor jenis kedelai dan larutan blansir itu sendiri, serta disebabkan adanya interaksi antara kedua faktor tersebut selama pengolahan. Sementara itu pada nilai b, perbedaan yang ada disebabkan perbedaan jenis kedelai saja, tidak dipengaruhi jenis larutan blansir, serta tidak ditemukan adanya interaksi antara kedua faktor uji terhadap intensitas yellowness
18
Tabel 5. Pengaruh jenis kedelai dan larutan blansir terhadap warna tepung tempe
Jenis Kedelai Larutan
Blansir
Nilai L (Kecerahan)
Nilai a (Redness)
Nilai b (Yellowness)
Lokal Kontrol 79.96±2.37
a 2.13±0.01d 18.42±0.15a
Na-metabisulfit 80.50±1.62a 2.02±0.02c 18.17±0.20a
Asam askorbat 77.48±4.07a 5.02±0.01f 19.66±0.89a
PRG Kontrol 80.44±0.86
a 0.15±0.01b 23.32±0.12b
Na-metabisulfit 80.93±0.93a 0.11±0.01a 21.99±1.82b
Asam askorbat 77.07±2.70a 3.41±0.03e 23.07±0.29b
Angka-angka pada kolom yang sama yang diikuti oleh huruf yang berbeda menunjukkan hasil yang berbeda sangat nyata (p<0,01).
Penggunaan natrium metabisulfit sebesar 0.1 % dalam larutan blansir tidak cukup mampu meningkatkan kecerahan tepung tempe, demikian pula dengan asam askorbat. Penampakan secara umum warna tepung tempe kontrol adalah kuning, tepung tempe dengan Na-metabisulfit berwarna kuning pucat, dan tepung tempe dengan asam askorbat berwarna kemerahan. Dokumentasi tepung tempe hasil penelitian ini dapat dilihat pada Gambar 7 dan 8.
Gambar 7. Tepung tempe kedelai lokal (A=kontrol, B=Na-metabisulfit, C=askorbat)
Gambar 8. Tepung tempe kedelai PRG (A=kontrol, B=Na-metabisulfit, C=askorbat)
Warna yang berbeda pada masing-masing perlakuan tidak hanya disebabkan reaksi pencoklatan non enzimatis yang terjadi pada tepung tempe, melainkan turut dipengaruhi oleh pigmen yang terdapat pada kacang kedelai itu sendiri. Reaksi yang dimunculkan oleh pigmen kedelai dipengaruhi oleh pH lingkungannya. Penggunaan asam askorbat dapat menurunkan pH tepung tempe akibat sifat asam dari senyawa itu sendiri.Kedelai memiliki kandungan flavonoid
B C
A
19 di dalam bijinya. Senyawa flavonoid yang dikandung kedelai terdiri dari isoflavon, yang berperan sebagai antioksidan, serta antosianin dan flavonol, yang berfungsi memberikan warna pada kedelai. Antosianin terakumulasi lebih banyak dan terekspresi pada kedelai hitam karena adanya peran dari gen I dan gen R yang
bersifat pleiotropik. Kedelai kuning tidak memiliki gen tersebut sehingga akumulasinya tidak sebanyak pada kedelai hitam dan juga tidak terekspresi. Senyawa flavonol, yang memberikan warna kuning, lebih terekspresi pada kedelai kuning (Wirnas et al. 2012).
Pada pH 1-4, antosianin berada pada bentuk terstabilnya yaitu kation flavilium dan memunculkan warna merah atau ungu, sedangkan pada pH di atas 4, antosianin terdapat dalam bentuk kalkon yang berwarna kuning (SEAFAST 2012). Hal ini menunjukkan kenaikan intensitas redness pada tepung tempe dengan
perlakuan asam askorbat dapat dipengaruhi dari menurunnya pH sehingga mengaktifkan warna merah dari antosianin. Selain itu diketahui bahwa senyawa asam askorbat dapat mempercepat degradasi antosianin karena asam askorbat mampu berkondensasi dengan antosianin membentuk senyawa phlobafen yang berwarna coklat (SEAFAST 2012). Ini berarti penampakan tepung tempe dengan warna kemerahan merupakan percampuran dari adanya sebagian antosianin yang membentuk kation flavilium dan phlobafen. Sementara itu tepung tempe dengan natrium metabisulfit tidak berwarna kemerahan disebabkan pemberian senyawa sulfit menyebabkan SO2 bereaksi dengan antosianin menghasilkan senyawa tidak
berwarna (SEAFAST 2012). Aktivitas Air (aw)
Aktivitas air adalah parameter yang paling umum digunakan sebagai kriteria untuk keamanan pangan dan kualitas pangan. Aktivitas air adalah parameter yang dapat digunakan untuk menjelaskan bagaimana air berpengaruh pada stabilitas dan keawetan pangan, laju reaksi kimia, aktivitas enzim dan pertumbuhan mikroba. Semakin tinggi nilai aw akan semakin tinggi pula
kemungkinan tumbuhnya mikroorganisme dalam bahan pangan tersebut.
Aktivitas air diukur secara sederhana menggunakan alat aw-meter. Nilai aw
tersebut dapat berubah bila kelembapan relatif lingkungannya berubah. Nilai aw
berkisar antara 0.0-1.0, yang diperoleh dari rasio antara tekanan uap air (P) pada kelembapan relatif tertentu dengan tekanan uap murni (Po). Bila aw = 0 maka
bahan bersifat kering mutlak, sedangkan bila aw = 1 maka bahan adalah air murni
(Kusnandar 2010).
Tabel 6 menunjukkan hasil pengukuran aktivitas air pada enam sampel tepung tempe. Pengukuran dilakukan pada suhu 30.80 oC. Hasil pengukuran menunjukkan tepung tempe memiliki nilai aw sebesar 0.583-0.601.
Faktor jenis kedelai, larutan blansir, serta interaksi antarperlakuan jenis kedelai dan larutan blansir ternyata tidak berpengaruh nyata, menurut hasil analisis ragam pada Lampiran 5, terhadap aktivitas air tepung tempe yang dihasilkan. Aktivitas air tepung tempe rata-rata senilai 0.592±0.044. Menurut Kusnandar (2010), nilai aktivitas air tepung pada umumnya sebesar 0.72. Dengan demikian hasil penelitian menunjukkan hasil yang lebih rendah dibandingkan nilai aktivitas air tepung secara umum. Nilai aw yang rendah berkorelasi dengan
20
dalam kurva hubungan laju reaksi relatif dengan aktivitas air dalam pangan pada Gambar 9.
Tabel 6. Pengaruh jenis kedelai dan larutan blansir terhadap aktivitas air tepung tempe
Jenis Kedelai Larutan Blansir Aktivitas Air
Lokal Kontrol 0.601±0.033
a
Na-metabisulfit 0.592±0.045a
Asam askorbat 0.583±0.036a
PRG Kontrol 0.585±0.050
a
Na-metabisulfit 0.596±0.060a
Asam askorbat 0.596±0.040a
Angka-angka pada kolom yang sama yang diikuti oleh huruf yang sama menunjukkan hasil yang tidak berbeda nyata (p>0,05).
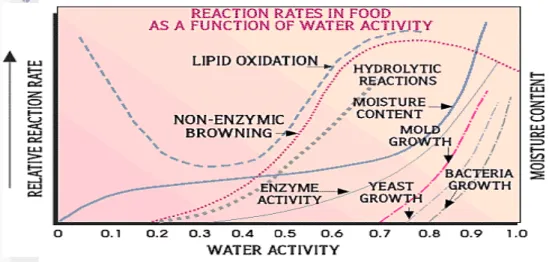
Berdasarkan Gambar 9 dapat diketahui bahwa kisaran nilai aktivitas air tepung tempe pada penelitian ini berada pada nilai di mana pertumbuhan mikroba pembusuk, seperti kapang, khamir, dan bakteri belum terjadi. Ini berarti kandungan air bebas dalam tepung tempe tidak cukup tersedia bagi pertumbuhan mikroorganisme tersebut. Dengan demikian, laju kerusakan mikrobiologis pada tepung tempe terbilang rendah sehingga umur simpannya menjadi lebih lama.
Gambar 9. Hubungan laju reaksi relatif dengan aktivitas air dalam pangan (Anonim 2012)
Gambar yang sama sekaligus menjelaskan beberapa hal yang dapat terjadi sehubungan dengan aktivitas air. Dapat dilihat bahwa reaksi pencoklatan non enzimatis, atau pada penelitian ini merupakan reaksi Maillard, dapat berlangsung pada kisaran aw sebesar 0.2 dan berangsur meningkat hingga aw 0.7. Peningkatan
keberlangsungan reaksi Maillard disebabkan mobilitas reaktan (gula pereduksi dan gugus amin) lebih mudah terjadi pada kadar air dan aw yang lebih tinggi
(maksimum 0.7). Hal ini menjelaskan mengapa pembentukan warna coklat mudah terjadi pada proses pembuatan tepung tempe. Sementara itu pada aw lebih dari 0.7,
21 peningkatan jumlah air, seperti yang terjadi pada pangan dengan aw di atas 0.7,
akan menggeser reaksi ke arah kiri atau menekan pembentukan N-Substituted Glycosylamine (Kusnandar 2010).
Oksidasi lemak adalah hal yang juga dapat terjadi pada tepung tempe sehubungan dengan aktivitas airnya. Nilai aw tepung tempe berada pada kisaran di
mana oksidasi lemak mengalami peningkatan reaksi. Hal ini disebabkan hidrasi air membuka sisi-sisi reaktif makromolekul sehingga memungkinkan terjadinya reaksi oksidasi (Kusnandar 2010). Hal ini menunjukkan ada resiko timbulnya ketengikan selama penyimpanan tepung tempe. Pengujian terhadap derajat ketengikan tepung tempe akan dibahas pada bagian berikutnya.
Karakteristik Kimia pH
Nilai pH digunakan untuk menyatakan tingkat keasaman suatu bahan. Suatu pH dikatakan normal apabila memiliki nilai 7 sementara bila nilai pH > 7 menunjukkan bahan tersebut memiliki sifat basa dan bila nilainya kurang dari tujuh menunjukkan sifat asam. pH bernilai 0 menunjukkan derajat keasaman tertinggi sedangkan nilai 14 menunjukkan derajat kebasaan tertinggi. Asam atau basa merupakan besaran yang sering digunakan dalam pengolahan pangan, baik di industri maupun dalam kehidupan sehari-hari.
Nilai pH tepung tempe berada pada kisaran nilai 5.24-6.54. Hal ini menunjukkan bahwa tepung tempe tergolong dalam makanan yang bersifat asam rendah. Asam dalam tepung tempe dihasilkan dari aktivitas proteolitik dan lipolitik kapang yang membebaskan asam-asam amino dan asam-asam lemak selama fermentasi kedelai berlangsung. Perlakuan jenis kedelai serta blansir menggunakan larutan natrium metabisulfit dan asam askorbat berpengaruh terhadap nilai pH tepung tempe yang dihasilkan. Hasil pengukuran pH tepung tempe dapat dilihat pada Tabel 7.
Tabel 7. Pengaruh jenis kedelai dan larutan blansir terhadap pH tepung tempe
Jenis Kedelai Larutan Blansir pH
Lokal Kontrol 6.54±0.04
Angka-angka pada kolom yang sama yang diikuti oleh huruf yang berbeda menunjukkan hasil yang berbeda sangat nyata (p<0,01).
22
menggunakan larutan natrium metabisulfit menurunkan pH pada tepung tempe kedelai lokal dan PRG. Penurunan pH dapat disebabkan adanya disosiasi asam sulfit selama pengolahan yang berkontribusi terhadap pengikatan ion H+ pada
sampel. Asam sulfit adalah zat antara yang terbentuk ketika garam-garam sulfit dilarutkan di dalam air. Asam sulfit lebih mudah terdisosiasi pada pH lingkungan yang mendekati netral (Wicaksono 2007). Perlakuan blansir dengan menggunakan asam askorbat jelas menurunkan nilai pH tepung tempe menjadi 5.45 dan 5.24 karena asam askorbat merupakan asam organik larut air yang mampu berdifusi ke dalam tempe ketika blansir berlangsung akibat adanya perbedaan konsentrasi antara larutan blansir dengan kandungan air di dalam tempe.
Nilai pH dapat menjadi salah satu karakteristik intrinsik yang dominan mempengaruhi potensi bahaya pada pangan, selain aktivitas air. Berdasarkan klasifikasi US-FDA dengan mengacu pada nilai pH dan aw, bahan pangan dapat
dikelompokkan ke dalam tiga golongan menurut tingkat potensi bahayanya. Kelompok pertama adalah bahan pangan dengan nilai aw > 0.85 dan pH > 4.5.
Bahan pangan ini memiliki potensi bahaya yang tinggi (high, H), sering disebut potentially hazardous foods, dengan karakteristik basah dan tidak asam.
Kelompok kedua adalah bahan pangan dengan (i) nilai aw > 0.85 tapi pH < 4.5
atau (ii) nilai aw < 0.85 tapi pH > 4.5. Kelompok ini merupakan kelompok dengan
potensi bahaya medium (M). Kelompok M pertama, bahan pangan basah tetapi asam, disebut sebagai acidified foods atau pH-controlled foods. Kelompok M
kedua, bahan pangan kering tapi asam, disebut sebagai aw-controlled foods.
Kelompok ketiga adalah kelompok pangan kering dan asam (aw < 0.85 dan pH
<4.5), umumnya relatif awet dan potensi bahayanya rendah (L) (Hariyadi 2009). Diketahui tepung tempe yang dihasilkan memiliki pH sebesar 5.24–6.54 dengan aw sebesar 0.582-0.601. Ini berarti tepung tempe masuk pada kategori
pangan dengan dengan potensi bahaya medium II (tidak asam dan kering). Produk pangan berasam rendah memiliki resiko ditumbuhinya mikroba patogen. Hal ini disebabkan mikroba patogen pada umumnya menginginkan kondisi pH pertumbuhan yang mendekati kisaran pH netral. Selain itu resiko germinasi spora
Clostridium botulinum juga terjadi. Clostridium botulinum adalah bakteri
pembentuk spora yang menyukai kondisi pangan berasam rendah, dapat hidup pada kondisi anaerobik, dan menghasilkan toksin botulin yang mematikan bila dikonsumsi oleh manusia. Akan tetapi karena tepung tempe memiliki aw yang
rendah, tidak perlu dilakukan proses sterilisasi komersial terhadap produk. Proses sterilisasi komersial dilakukan apabila produk memiliki aw tinggi karena C. botulinum dapat tumbuh dengan baik pada aw tinggi (Kusnandar 2010). Proses
termal dengan target 6 D sudah dirasa cukup jika dilakukan (Hariyadi 2009). Dengan demikian hal yang dapat dilakukan untuk menurunkan resiko kerusakan mikrobiologis pada tepung tempe, selain dengan proses termal, adalah memperhatikan kebersihan dan kerapatan kemasan, serta kondisi ruang penyimpanan tepung sehingga kontaminasi mikroba tidak banyak terjadi.
Analisis Proksimat
23 masing-masing tepung. Komposisi kimia dalam basis kering, kecuali kadar air, dari tepung tempe ini dinyatakan dalam Tabel 8.
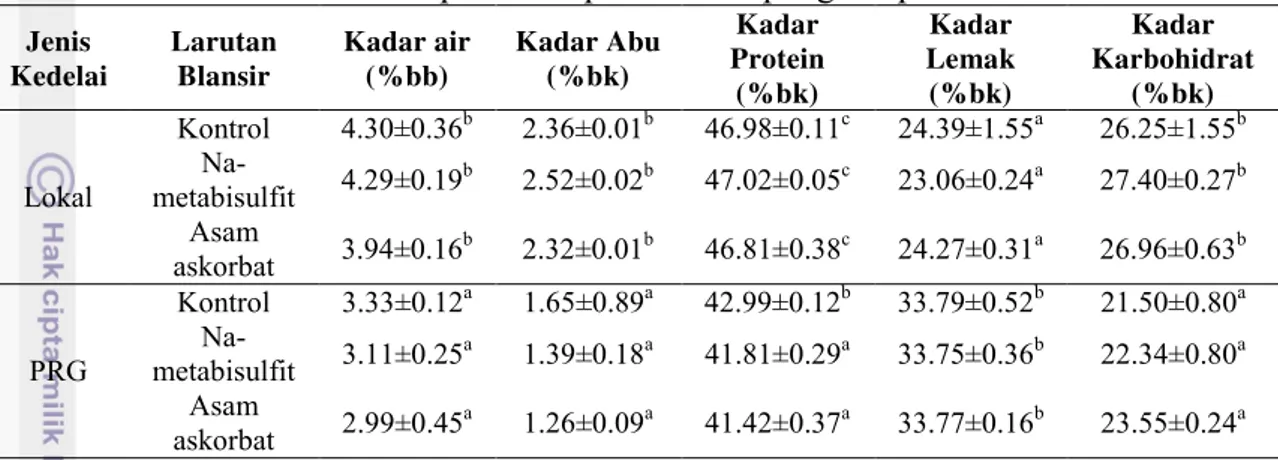
Tabel 8. Pengaruh jenis kedelai dan larutan blansir terhadap analisis proksimat tepung tempe
Kontrol 4.30±0.36b 2.36±0.01b 46.98±0.11c 24.39±1.55a 26.25±1.55b
Na-metabisulfit 4.29±0.19b 2.52±0.02b 47.02±0.05c 23.06±0.24a 27.40±0.27b Asam
askorbat 3.94±0.16b 2.32±0.01b 46.81±0.38c 24.27±0.31a 26.96±0.63b
PRG
Kontrol 3.33±0.12a 1.65±0.89a 42.99±0.12b 33.79±0.52b 21.50±0.80a
Na-metabisulfit 3.11±0.25a 1.39±0.18a 41.81±0.29a 33.75±0.36b 22.34±0.80a Asam
askorbat 2.99±0.45a 1.26±0.09a 41.42±0.37a 33.77±0.16b 23.55±0.24a Angka-angka pada kolom yang sama yang diikuti oleh huruf yang berbeda menunjukkan hasil
yang berbeda sangat nyata (p<0.01).
Kandungan air pada bahan pangan sangat bervariasi. Keberadaan air dalam bahan pangan sering dihubungkan dengan mutu bahan pangan, sebagai pengukur bagian bahan kering atau padatan, penentu indeks kestabilan selama masa penyimpanan, serta penentu mutu organoleptik terutama rasa dan keempukan. Jumlah absolut air yang terdapat dalam pangan sebagai komponen pangan dinyatakan sebagai kadar air (Andarwulan et al. 2011). Hasil analisis
menunjukkan kadar air tepung tempe berkisar antara 2.99-4.30 %. Berdasarkan hasil analisis ragam pada Lampiran 6 diketahui bahwa interaksi jenis kedelai dan larutan blansir tidak berpengaruh nyata terhadap kadar air tepung tempe. Jenis kedelai sebagai bahan baku memberikan pengaruh sangat nyata terhadap variasi kadar air pada tepung tempe yang dihasilkan. Hal ini sesuai dengan pernyataan Akubor et al. (2013) bahwa perbedaan nilai kadar air yang terjadi dipengaruhi
oleh perbedaan jenis dan varietas bahan baku, serta proses penyimpanan. Dapat diketahui bahwa kadar air tepung tempe kedelai PRG lebih rendah jika dibandingkan dengan tepung tempe kedelai lokal. Apabila nilai-nilai ini dibandingkan dengan standar kadar air beberapa tepung lainnya (mengingat tepung tempe belum memiliki Standar Nasional Indonesia), seperti tepung sagu (BSN 2008), tepung beras (BSN 2009), tepung terigu (BSN 2009), dan tepung tapioka (BSN 1994) dengan batas maksimum 13-15 %, maka kadar air tepung tempe memenuhi standar mutu. Kadar air tepung yang rendah dapat meningkatkan umur simpannya dengan mencegah pertumbuhan kapang dan menekan reaksi biokimia yang berlangsung karena ketersediaan air bebas (Omimawo dan Akubor 2012). Hal ini berhubungan dengan karakter aktivitas air tepung yang juga rendah. Hubungan antara kadar air dan aktivitas air bahan pangan dinyatakan dalam kurva isoterm sorpsi air yang berbentuk sigmoid dan bentuknya bervariasi pada berbagai jenis bahan pangan. Secara umum, semakin rendah aw maka semakin rendah pula
kadar air kesetimbangannya. Telah diketahui dari Tabel 6 bahwa aw tepung tempe
bernilai rendah dan telah dibahas sebelumnya juga bahwa aw yang rendah
24
Kadar abu menunjukkan kandungan mineral dalam suatu bahan pangan dan jumlahnya bervariasi tergantung jenis mineral dengan komposisi bagaimanakah yang tersusun dalam bahan pangan tersebut. Analisis kadar abu sangat penting dilakukan untuk mengetahui kualitas gizi suatu bahan pangan dan digunakan pula sebagai indikator mutu pangan lain (Andarwulan et al. 2011).
Kadar abu tepung tempe berkisar antara 1.26-2.61 %. Interaksi antara jenis kedelai dengan jenis larutan blansir tidak berpengaruh nyata menurut hasil analisis ragam pada Lampiran 6. Variasi kadar abu antarperlakuan dipengaruhi secara sangat nyata oleh kandungan mineral dari jenis kedelai asal. Berdasarkan hasil penelitian diketahui bahwa kadar abu tepung tempe kedelai lokal (2.40 %) lebih besar dibandingkan kedelai PRG (1.43 %). Ini sesuai dengan penelitian Yuwono
et al. (2012) bahwa kadar abu kedelai lokal, kecuali varietas Pangrango, memang
lebih tinggi jika dibandingkan dengan kedelai impor. Kandungan abu atau mineral dalam tepung tempe berasal dari besi, tembaga, dan seng yang masing-masing nilainya 9.39; 2.87; dan 8.05 mg dalam 100 gram tempe (Lestari 2011). Selain itu kapang tempe dapat menghasilkan enzim fitase yang dapat menguraikan asam fitat menjadi fosfor dan inositol. Asam fitat merupakan senyawa pada kotiledon kacang-kacangan yang dapat menghalangi proses penyerapan mineral dalam tubuh. Asam fitat itu sendiri mengandung 70 % fosfor (Sunaryanto 2014). Dengan terurainya asam fitat, mineral-mineral seperti besi, kalsium, magnesium, dan seng meningkat jumlah dan bioavalabilitasnya.
Protein merupakan makronutrien yang diunggulkan dalam produk berbasis kedelai. Kandungan total protein dalam dari suatu bahan pangan disebut kadar protein. Pengetahuan mengenai kandungan protein dalam pangan penting untuk keperluan pelabelan gizi, mengetahui sifat fungsionalnya, dan penentuan sifat biologis protein (Andarwulan et al. 2011). Kadar protein yang terdapat dalam
tepung tempe berkisar antara 41.42-47.02 %. Tingginya kandungan protein dalam tepung tempe didukung dengan kandungan asam amino, terutama asam amino esensial, yang juga tinggi pada tempe sebagai produk intermediet. Asam amino esensial tersebut ialah sistin, isoleusin, leusin, lisin, metionin, fenilalanin, treonin, triptofan, dan valin (Sunaryanto 2014). Kadar protein tepung tempe kedelai lokal (46.80 %) lebih tinggi nilainya jika dibandingkan tepung tempe kedelai PRG (42.98 %). Hal ini dapat disebabkan adanya modifikasi protein yang dilakukan pada kedelai PRG (GMO Compass 2010) sehingga menurunkan kadar protein total dari bahan baku kedelai itu sendiri. Selain itu dapat pula disebabkan masa simpan kedelai impor dari saat dipanen hingga dipasarkan di Indonesia yang lebih lama daripada kedelai lokal. Masa simpan yang lama ini menyebabkan penurunan kandungan protein dalam bahan baku (Ginting et al. 2009). Hal ini disebabkan
sebagian protein mengalami degradasi secara kimia maupun fisik sehingga protein berubah struktur dan kehilangan aktivitasnya. Faktor kimia penyebab degradasi protein berupa air, pH, dan suhu selama penyimpanan sedangkan faktor fisik berupa kegiatan mekanik seperti benturan. Interaksi antara jenis kedelai dan jenis larutan blansir memberikan pengaruh nyata terhadap penurunan kadar protein jika dibandingkan dengan kontrol pada tepung tempe kedelai PRG namun tidak pada tepung tempe kedelai lokal.
25 kebutuhan. Lemak yang berada dalam tepung tempe tergolong dalam lemak nabati karena sumbernya berupa kacang kedelai. Secara umum, lemak nabati mengandung lemak tidak jenuh yang relatif tinggi sehingga cenderung tidak stabil terhadap oksidasi (Andarwulan et al. 2011). Berdasarkan hasil analisis ragam
pada Lampiran 6 dapat diketahui bahwa interaksi jenis kedelai dan larutan blansir tidak berpengaruh nyata terhadap kadar lemak tepung tempe. Perbedaan kadar lemak pada keenam jenis tepung dipengaruhi oleh kadar lemak dalam kedelai. Hasil penelitian yang dilakukan oleh Yuwono et al. (2012) dan Ichsani (2013)
menunjukkan bahwa kedelai lokal memang memiliki kadar lemak yang lebih rendah daripada kedelai impor. Hal ini sejalan dengan hasil penelitian ini. GMO Compass (2010) menyatakan bahwa pada kedelai PRG dilakukan pemerkayaan asam lemak oleat hingga 86 % dan penambahan sejumlah asam lemak lainnya. Penambahan asam lemak inilah yang meningkatkan kadar lemak secara keseluruhan pada tepung sebagai produk akhir.
Lemak merupakan lipid sederhana dari ester gliserol yang disusun oleh asam lemak dan gliserin. Dalam struktur lemak, molekul gliseril mengikat tiga rantai asam lemak dan kemudian membentuk senyawa ester yang bersifat non polar. Semakin banyak ester gliserol yang terbentuk maka semakin banyak kandungan lemak dalam bahan pangan. Mekanisme pembentukan lemak dapat dilihat pada Gambar 10. Asam lemak yang terdapat pada tepung tempe secara umum sama dengan yang terdapat dalam tempe. Proses fermentasi kedelai menjadi tempe menyebabkan terjadinya peningkatan derajat ketidakjenuhan pada lemak. Asam lemak dominan tersebut ialah asam oleat dan asam linolenat sementara asam palmitat dan asam linoleat sedikit mengalami penurunan (Lestari 2011).
Gambar 10. Reaksi pembentukan lemak
26
Bilangan TBA
Uji bilangan TBA (thiobarbituric acid) umum digunakan untuk mengukur
tingkat ketengikan lemak/minyak atau produk pangan yang mengandung lemak/minyak. Tingkat ketengikan menunjukkan seberapa besar kerusakan lemak/minyak telah terjadi akibat oksidasi. Dalam reaksi oksidasi lemak, komponen hasil dekomposisi lemak yang dapat terbentuk adalah senyawa turunan aldehida, yaitu malonaldehid. Keberadaan malonaldehid pada produk menunjukkan bahwa lemak/minyak di dalamnya telah mengalami oksidasi lanjut. Senyawa malonaldehid yang terbentuk akan bereaksi dengan pereaksi TBA dan menghasilkan pigmen warna merah. Intensitas warna merah ini diukur secara spektroskopis pada panjang gelombang 528 nm. Hasil pengukuran yang diperoleh dinyatakan sebagai bilangan TBA yang nilainya setara dengan jumlah malonaldehida pada contoh. Semakin tinggi bilangan TBA maka semakin tinggi tingkat oksidasi lemak/minyak (Kusnandar 2010).
Tepung tempe merupakan tepung dengan kadar lemak yang cukup tinggi (23.06–33,79 %) serta memiliki nilai aw yang masuk dalam rentang di mana reaksi
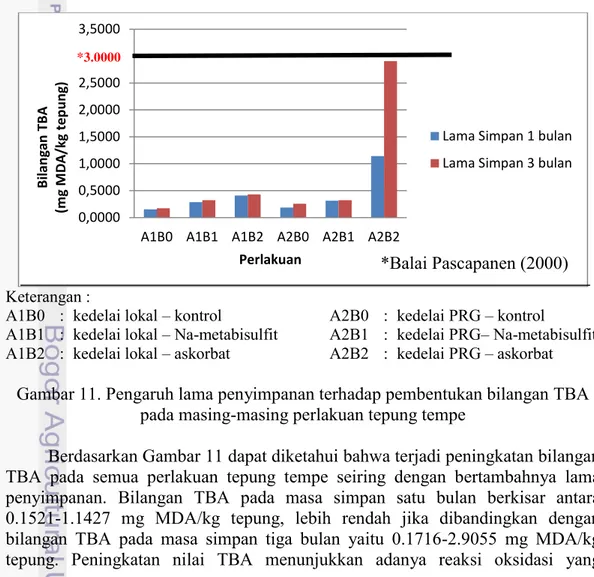
oksidasi lemak dapat berlangsung. Hal ini memungkinkan terjadinya oksidasi lemak selama penyimpanan tepung. Hasil analisis bilangan TBA tepung tempe yang telah disimpan selama satu dan tiga bulan dapat dilihat pada Gambar 11.
Keterangan :
A1B0 : kedelai lokal – kontrol A2B0 : kedelai PRG – kontrol
A1B1 : kedelai lokal – Na-metabisulfit A2B1 : kedelai PRG– Na-metabisulfit
A1B2 : kedelai lokal – askorbat A2B2 : kedelai PRG – askorbat
Gambar 11. Pengaruh lama penyimpanan terhadap pembentukan bilangan TBA pada masing-masing perlakuan tepung tempe
Berdasarkan Gambar 11 dapat diketahui bahwa terjadi peningkatan bilangan TBA pada semua perlakuan tepung tempe seiring dengan bertambahnya lama penyimpanan. Bilangan TBA pada masa simpan satu bulan berkisar antara 0.1521-1.1427 mg MDA/kg tepung, lebih rendah jika dibandingkan dengan bilangan TBA pada masa simpan tiga bulan yaitu 0.1716-2.9055 mg MDA/kg tepung. Peningkatan nilai TBA menunjukkan adanya reaksi oksidasi yang