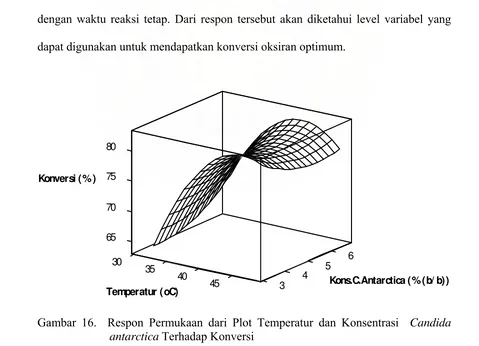
PEMBUATAN SENYAWA EPOKSI DARI METIL ESTER ASAM
LEMAK SAWIT DESTILAT SECARA ENZIMATIS
T E S I S
Oleh
AZHAR RAMADHANI TARIGAN
067022002/TK
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
PEMBUATAN SENYAWA EPOKSI DARI METIL ESTER ASAM
LEMAK SAWIT DESTILAT SECARA ENZIMATIS
TESIS
Untuk Memperoleh Gelar Magister Teknik dalam Program Studi Teknik Kimia
pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
AZHAR RAMADHANI TARIGAN
067022002/TK
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
MEDAN
Judul Tesis : PEMBUATAN SENYAWA EPOKSI DARI METIL ESTER ASAM LEMAK SAWIT DESTILAT SECARA ENZIMATIS
Nama Mahasiswa : Azhar Ramadhani Tarigan Nomor Pokok : 067022002
Program Studi : Teknik Kimia
Menyetujui
Komisi Pembimbing
(Prof.Dr.Ir. Setiaty Pandia) (Ir.Renita Manurung, MT) Ketua Anggota
Ketua Program Studi Direktur
Tanggal lulus : 21 Februari 2009 Telah diuji pada
Tanggal : 21 Februari 2009
PANITIA PENGUJI TESIS
K e t u a : Prof. Dr. Ir. Setiaty Pandia A n g g o t a : 1. Ir. Renita Manurung, MT 2. Dr.Ir. Tjahyono Herawan, MSc
ABSTRAK
Senyawa epoksi merupakan produk komersial yang dapat diaplikasikan untuk beberapa kegunaan seperti pelentur (plasticizer), stabiliser dan coating pada resin polimer, serta merupakan antioksidan pada pengolahan karet alam. Asam lemak sawit
destilat (ALSD) merupakan derivat minyak nabati yang kurang dimanfaatkan
disamping fraksi-fraksi lain seperti olein, stearat dan lain-lain dalam penggunaannya untuk aplikasi produk oleokimia. ME-ALSD diepoksidasikan secara enzimatis untuk mendapatkan senyawa epoksi menggunakan beberapa biokatalis dari enzim lipase
imobilis seperti Rhizomucor miehei, Candida antarctica, dan Carica papaya. Enzim lipase Rhizomucor miehei, dan Carica papaya tidak menghasilkan oksiran oksigen
yang maksimum hanya enzim lipase Candida antarctica yang mampu melakukan
reaksi epoksi terhadap metil ester ALSD dengan hasil oksiran oksigen maksimum sebesar 2,43% pada konsentrasi sebesar 5%, temperatur 40OC dan waktu reaksi 42 jam. Proses epoksidasi dioptimasikan berdasarkan metode RSM (Response Surface Methodology) pada konsentrasi enzim sebesar 3,3%; 4%; 5%; 6%; 6,7% (b/b), temperatur reaksi 31,6OC; 35OC; 40OC; 45OC; 48,4OC, dan pada waktu reaksi 40,3 jam; 41 jam; 42 jam; 43 jam; 43,7 jam. Konversi optimum epoksidasi sebesar 79,85 % diperoleh pada konsentrasi Candida antarctica 4% (b/b), temperatur reaksi 45oC dan waktu reaksi selama 41 jam.
ABSTRACT
Epoxy compound is commercial product available for application for a few usefulness like plasticizer, stabilizer and coating at polymer resin, and also antioxidant at processing of natural rubber. Palm fatty acid distillate (PFAD) is derivat vegetable oil which is exploited by side fractions like olein, stearat and others in its use for the application of oleochemical product. ME-PFAD epoxidized in enzymatic for getting epoxy compound apply some biocatalyst from lipase enzymes immobillis like Rhizomucor miehei, Candida antarctica, and Carica papaya. Enzyme
Rhizomucor miehei, and Carica papaya are hasn't yield oxyran oxygen of maximum only enzyme Candida antarctica capable to doing reaction of epoksi to methyl ester PFAD with result oksiran oxygen maximum 2,43% at concentration of 5%, temperature of 40OC, and reaction time of 42 hour. Epoxidation process optimization based on Response Surface Methodology (RSM) at concentrations of3,3%; 4%; 5%; 6%; 6,7% (w/w), reaction temperature at 31,6OC; 35OC; 40OC; 45OC; 48,4OC, and reaction time at 40,3 hour; 41 hour; 42 hour; 43 hour; 43,7 hour. The optimum convertion epoxidation is 79,85% obtained at concentration of Candida antarctica
4% (w/w), reaction temperature 45OC and reaction time during 41 hour.
KATA PENGANTAR
Pujian hanya berhak disampaikan kepada-Nya, karena hanya Allah SWT yang
sanggup menyangga segala macam pujian yang ditujukan kepada-Nya. Teriring pula
ucapan Alhamdulillahi rabbil’alamin atas segala karunia-Nya sehingga penyusunan
tesis ini dapat diselesaikan. Tulisan ini berjudul ”Pembuatan Senyawa Epoksi dari
Metil Ester Asam Lemak Sawit Destilat Secara Enzimatis”. Tesis ini disusun
setelah melalui tahapan penelitian yang dilaksanakan di Pusat Penelitian Kelapa
Sawit (PPKS) Medan, untuk itu penulis mengucapkan terima kasih sebesar-besarnya
atas segala bantuan dan fasilitas yang telah diterima. Penulis mengucapkan terima
kasih dan penghargaan yang tinggi kepada dosen pembimbing Prof.Dr.Ir. Setiaty
Pandia dan Ir. Renita Manurung, MT atas bantuan, bimbingan, curahan ilmu, asih
dan asuh yang telah diberikan selama penyusunan tesis dan sepanjang penyelesaian
pendidikan kesarjanaan ini. Pada kesempatan ini, disampaikan pula ucapan terima
kasih kepada yang terhormat :
1. Prof. Chairuddin P. Lubis, DTM&H, Sp.A(K) selaku Rektor Universitas
Sumatera Utara atas kesempatan yang diberikan untuk mengikuti Pendidikan
2. Prof. Dr. Ir. T.Chairun Nisa B, M.Sc selaku Direktur Sekolah Pascasarjana
Universitas Sumatera Utara atas kesempatan menjadi Mahasiswa Magister
Teknik Kimia pada Sekolah Pascasarjana.
3. Prof. Dr. Ir. Setiaty Pandia, Ketua Program Studi Magister Teknik Kimia,
Universitas Sumatera Utara sekaligus sebagai komisi pembimbing.
4. Dr.Halimatuddahliana, ST, MSc selaku Sekretaris Program Studi Magister
Teknik Kimia, Universitas Sumatera Utara.
5. Kedua orang tua, H. Jamal H Tarigan dan Hj. Zainab Ginting, kakak ku dr. Erma
Ridhani Tarigan, abang ku Irfan Sanusi Tarigan, SE, MMA dan M. Irwan
Tarigan, SP serta keluarga besar untuk dukungan dan doa yang begitu tulus.
6. Bapak Dr.Ir.Tjahyono Herawan, MSc dan seluruh staff beserta teknisi PPKS
Medan yang telah mengikhlaskan waktu dan pemikiran selama penelitian.
7. Staf pengajar Magister Teknik Kimia dan MIPA-Kimia, Universitas Sumatera
Utara atas bimbingannya.
8. Pegawai administrasi SPs Universitas Sumatera Utara Magister Teknik Kimia.
9. Sahabat ku Faisal Amri, S.ST, MT., abang T. Faisal Z Hamid, ST, MT., abang
Syawaluddin Nst, ST. serta seluruh rekan Magister Teknik Kimia, Universitas
Sumatera Utara.
Sesudahnya saya memohon nasehat dan saran, karena tulisan ini
Medan, Maret 2009
Penulis
RIWAYAT HIDUP
Nama : Azhar Ramadhani Tarigan
Tempat/Tanggal Lahir : Medan, 03 Juli 1983
Agama : Islam
Pendidikan : SD Negeri 060882 Medan (1989-1995)
Pesantren Ar-Raudhatul Hasanah Medan (1995-2001)
Program Studi Teknologi Kimia Industri (2001-2006)
Universitas Sumatera Utara
Status Keluarga : Anak ke empat dari empat bersaudara
1. Ayah : H. Jamal Hayrudin Tarigan
2. Ibu : Hj. Zainab Ginting
3. Kakak : dr. Erma Ridhani Tarigan
4. Abang : Irfan Sanusi Tarigan, SE, MMA
DAFTAR ISI
Halaman
ABSTRAK ... i
ABSTRACT... ii
KATA PENGANTAR ... iii
RIWAYAT HIDUP... v
DAFTAR ISI... vi
DAFTAR TABEL... viii
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN... xii
DAFTAR SINGKATAN ... xiii
I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 4
1.5 Lingkup Penelitian ... 4
II TINJAUAN PUSTAKA... 6
2.1 Senyawa Epoksi ... 6
2.3 Metil Ester Asam Lemak Sawit Destilat... 13
2.4 Enzim ... 16
2.4.1 Enzim Lipase ... 19
2.4.2 Lipase dalam Industri Oleokimia ... 22
2.4.3 Lipase dalam Reaksi Epoksidasi... 23
2.5 Rancangan Percobaan ... 25
III METODOLOGI PENELITIAN... 29
3.1 Lokasi dan Waktu Penelitian ... 29
3.2 Bahan ... 29
3.3 Metode Penelitian ... 30
3.3.1 Rancangan Percobaan ... 30
3.3.2 Pengolahan Data... 32
3.3.2.1 Optimasi Epoksidasi Metil Ester Asam Lemak Sawit Destilat (Me-ALSD) ... 32
3.3.2.2 Analisa Response Surface Methodology (RSM) ... 32
3.3.3 Tahapan Penelitian ... 33
3.3.3.1 Karakteristik Bahan Baku ... 33
3.3.3.2 Reaksi Epoksidasi ... 33
3.3.3.3 Analisa Senyawa Epoksi ... 35
IV HASIL DAN PEMBAHASAN ... 37
4.1 Penelitian Pendahuluan ... 37
4.1.1 Karakteristik Bahan Baku Metil Ester ALSD... 37
4.1.2 Penentuan Level Terkode Central Composite Design (CCD) .. 38
4.1.2.1 Penentuan Jumlah Biokatalis ... 38
4.1.2.2 Penentuan Nilai Temperatur ... 40
4.1.2.3 Penentuan Waktu Reaksi ... 42
4.2 Optimasi Epoksidasi Menggunakan Candida antarctica... 44
4.2.1 Analisa Pengaruh Variabel... 45
4.2.1.1 Pengaruh Temperatur dan Konsentrasi Biokatalis Terhadap Konversi ... 48
4.2.1.2 Pengaruh Waktu Reaksi dan Konsentrasi Biokatalis Terhadap Konversi ... 51
4.2.1.3 Pengaruh Temperatur dan Waktu Reaksi Terhadap Konversi ... 53
4.3 Analisa Variansi (ANAVA)... 57
4.3.1 Uji Verifikasi Model Penelitian ... 60
4.4 Analisa Bilangan Iod, Bilangan Hidroksi dan Bilangan Asam... 63
V KESIMPULAN DAN SARAN... 66
5.2 Saran... 67
DAFTAR PUSTAKA ... 68
DAFTAR TABEL
Nomor Judul Halaman 1. Hasil-hasil Reaksi Epoksidasi dengan Asam Perasetat Secara Insitu... 92. Pengaruh Rasio Molar (Asam Asetat dan Hidrogen Peroksida) terhadap Hasil Epoksidasi Tidak Jenuh ... 13
3. Kandungan Asam Lemak pada Minyak Kelapa Sawit dan ALSD ... 14
4. Perlakuan Terkode Epoksidasi... 31
5. Central Composite Design (CCD) untuk 3 Variabel ... 31
6. Hasil Analisa Bahan Baku Metil Ester ALSD ... 37
7. Kandungan Asam Lemak Bahan Baku Metil Ester ALSD... 38
8. Pengaruh Level Konsentrasi Biokatalis Terhadap Bilangan Oksiran... 39
9. Pengaruh Level Temperatur Terhadap Bilangan Oksiran ... 41
10. Pengaruh Level Waktu Terhadap Bilangan Oksiran ... 42
11. Level Terkode Epoksidasi... 44
13. Hasil Statistika Minitab 14 Untuk Response Surface Methodology
(RSM) ... 46
14. ANAVA Model Persamaan Regresi Pada Epoksisi Asam Lemak Sawit Distilat Menjadi Epoksi Menggunakan Minitab 14... 58
15. Hasil analisa Bilangan Iod, Bilangan Hidroksi dan Bilangan Asam Senyawa Epoksi ... 64
DAFTAR GAMBAR
Nomor Judul Halaman 1. Reaksi dari Epoksidasi Hidrokarbon ... 62. Reaksi Pembentukan Asam Peroksi pada Kondisi Proses Tertentu ... 7
3. Mekanisme Kerja Senyawa Epoksi sebagai Penstabil dan Pelentur pada Polivinil Khlorida ... 10
4. Reaksi Kimia Proses Epoksidasi secara in situ... 11
5. Mekanisme Pembentukan Senyawa Epoksi Melalui Reaksi Epoksidasi ... 12
6. Bagan Proses Pengolahan Kelapa Sawit Menjadi Minyak Goreng ... 15
7. Reaksi Pembentukan Senyawa Metil Ester Asam Lemak ... 16
8. Proses Penguraian Substrat Oleh Suatu Enzim... 18
9. Epoksidasi Prileshajev dengan Katalis Enzim Lipase ... 23
10. Proses Reaksi Epoksidasi Menggunakan Enzim ... 25
11. Diagram kerja Epoksidasi ... 35
ditambahkan dengan hidrogen peroksida (H2O2); (b) Peralatan
epoksidasi setelah penambahan dengan hidrogen peroksida (H2O2) .... 36
13. Pengaruh Level Konsentrasi Biokatalis Terhadap Bilangan Oksiran Oksigen ... 39
14. Pengaruh Level Temperatur Terhadap Bilangan Oksiran Oksigen ... 41
15. Pengaruh Level Waktu Terhadap Bilangan Oksiran Oksigen ... 43
16. Respon Permukaan dari Plot Temperatur dan Konsentrasi Candida antarctica Terhadap Konversi... 48
17. Kontur dari Plot Konsentrasi Candida antarctica Terhadap Temperatur ... 49
18. Respon Permukaan dari Waktu Reaksi dan Konsentrasi Candida antartica Terhadap Konversi ... 51
19. Kontur dari Plot Temperatur Terhadap Waktu Reaksi ... 52
20. Respon Permukaan dari Temperatur dan Waktu Reaksi Terhadap Konversi... 53
21. Kontur dari Plot TemperaturTerhadap Waktu Reaksi ... 55
22. Plot Residual Dengan Taksiran Model ... 60
23. Plot Residual Dengan Order Model... 60
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Prosedur Analisis ... 73
2. Response Surface Methodology... 78
3. Output Analisa Statistika ... 81
4. Tabel Statistika... 84
5. Hasil Analisa GC ... 85
6. Hasil Analisa FTIR ... 88
DAFTAR SINGKATAN
ALSD : Asam Lemak Sawit Destilat
ALTJ : Asam Lemak Tidak Jenuh
ANAVA : Analisa Variansi
AOCS : American Oil Chemistry Society
CPO : Crude Palm Olein
DOA : Dioktil Adipat
FTIR : Fourier Transform Infra Red
GC : Gas Cromatografy
KS : Kolmogorov Smirnov
ME-ALSD : Metil Ester Asam Lemak Sawit Destilat
ME-PFAD : Methyl Ester Palm Fatty Acid Distillate
CCD : Central Composite Design
IOPRI : Indonesian Oil Palm Research Institute
PPKS : Pusat Penelitian Kelapa Sawit
PVC : Poly Vinil Clorida
RSM : Response Surface Methodology
I.
PENDAHULUAN
1.1 Latar Belakang
Senyawa epoksi merupakan produk komersial yang dapat diaplikasikan untuk
beberapa kegunaan seperti pelentur (plasticizer), stabiliser dan coating pada resin
polimer, serta merupakan antioksidan pada pengolahan karet alam. Senyawa epoksi
juga dapat digunakan sebagai surfaktan dan agen anti korosif (Yamamura dkk, 1989),
aditif pada minyak pelumas dan bahan baku pestisida (Sadi dkk, 1995).
Senyawa epoksi dapat disintesa dari minyak nabati (minyak kedelai, minyak
biji bunga matahari, minyak jarak dan minyak sawit). Minyak sawit merupakan
minyak nabati yang mengandung asam lemak jenuh (saturated fatty acid) dan asam
lemak tidak jenuh (unsaturated fatty acid). Kandungan asam lemak jenuh minyak
sawit terutama asam palmitat sekitar 32-47%, sedangkan kandungan asam lemak
Tingginya kandungan asam lemak tidak jenuh ini, memungkinkan terjadinya reaksi
epoksidasi pada suhu dan waktu tertentu dengan bantuan katalis yang menghasilkan
minyak sawit epoksi. Bahan baku senyawa epoksi dari minyak nabati ini sendiri bisa
berupakan minyak nabati mentah ataupun minyak nabati yang sudah mengalami
pengolahan lebih lanjut.
Proses sintesa senyawa epoksi dengan reaksi epoksidasi terus dikembangkan
untuk memperoleh senyawa epoksi dengan kandungan oksiran oksigen yang lebih
tinggi. Optimasi proses dilakukan dengan berbagai cara seperti, diversifikasi bahan
baku, penggunaan katalis, penggunaan suhu selama reaksi dan waktu operasi.
Penggunaan minyak sawit mentah (CPO) sebagai bahan baku reaksi epoksidasi
dilaporkan oleh Haya (1991) menghasilkan senyawa epoksi dengan kandungan
oksiran oksigen sebesar 3,4% pada suhu reaksi 100 ± 5OC dan pelarut n-heksan 10%. Haryati dan S. Oerip juga melakukan epoksidasi dari minyak sawit mentah (CPO)
dan menghasilkan senyawa epoksi dengan kandungan oksiran oksigen sebesar 1,19%
pada suhu 70OC dan pelarut n-heksan pada kisaran 10-30% (Haryati dan Oerip 1991). Kandungan oksiran oksigen teoritis epoksi minyak sawit adalah 3,90% (Sadi, 1992).
Penggunaan katalis kimia memiliki kelemahan yang berhubungan dengan
penggunaan energi dan selain dihasilkan produk epoksi juga dihasilkan produk
samping sebagai hasil degradasi oksiran dan hasil reaksi samping seperti asam
dihidroksi dan estolida (gen Klaas dan Warwel, 1996). Oleh sebab itu dikembangkan
dengan menggunakan biokatalisator. Biokatalisator yang digunakan dapat berupa
enzim lipase yang telah diimobilisasi. Enzim lipase yang digunakan harus memiliki
sifat kemampuan untuk beraktifitas pada satu jenis substrat tertentu (spesificity) yang
mengandung asam palmitat.
Penggunaan reaksi enzimatis pada asam lemak dan minyak nabati memiliki
beberapa keuntungan yaitu (i) kondisi reaksi sedang, yaitu campuran reaksi pada pH
netral, (ii) ramah lingkungan (Green Chemistry), (iii) efisiensi katalis tinggi, (iv)
pembentukan hidroperoksida stabil secara langsung dari asam lemak, yaitu tidak
memelukan penambahan asam asetat.
Asam lemak sawit destilat (ALSD) merupakan derivat minyak nabati yang
kurang dimanfaatkan disamping fraksi-fraksi lain seperti olein, stearat dan lain-lain
dalam penggunaannya untuk aplikasi produk oleokimia. Oleh karena itu ALSD yang
telah di transesterifikasikan menggunakan metanol menjadi metil ester asam lemak
sawit destilat (ME-ALSD) dicoba diepoksidasikan secara enzimatis untuk
mendapatkan senyawa epoksi menggunakan beberapa enzim lipase imobilis seperti
Rhizomucor miehei, Candida antarctica, dan Carica papaya. Dimana dari ketiga
enzim tersebut merupakan enzim lipase hidrolase yang mampu mengkatalisis
hidrolisa ikatan karbon.
Perumusan masalah pada penelitian ini adalah sejauh mana pengaruh suhu,
waktu dan konsentrasi biokatalis pada reaksi epoksidasi metil ester asam lemak sawit
destilat (ME-ALSD) menjadi senyawa epoksi yang dihasilkan dari beberapa
biokatalis seperti Rhizomucor miehei, Candida antarctica, dan Carica papaya secara
batch.
1.3Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui kinerja (suhu, waktu reaksi dan
konsentrasi biokatalis) dari beberapa biokatalis seperti Rhizomucor miehei, Candida
antarctica, dan Carica papaya yang digunakan untuk reaksi epoksidasi ME-ALSD
sehingga menghasilkan senyawa epoksi dengan kandungan oksiran oksigen
maksimum.
1.4Manfaat Penelitian
Hasil penelitian ini diharapkan dapat digunakan sebagai informasi dalam
memilih enzim lipase imobilis yang tepat sebagai biokatalisator untuk menghasilkan
senyawa epoksi metil ester asam lemak destilat dengan kandungan oksiran oksigen
optimum, sehingga dapat mendukung usaha peningkatan nilai tambah derivat minyak
mikrobial, pencegah korosi, bahan tambahan pada minyak pelumas dan sebagai
bahan baku pestisida.
1.5Lingkup Penelitian
Bahan baku yang digunakan dalam penelitian ini adalah metil ester asam
lemak sawit destilat (ME-ALSD) dan hidrogen peroksida sebagai oksidan dengan
biokatalis Rhizomucor miehei, Candida antarctica, dan Carica papaya.
Pada penelitian awal yang dilakukan ternyata biokatalis Rhizomucor miehei
dan Carica papaya tidak berhasil melakukan epoksidasi terhadap ME-ALSD (data di
Lampiran 6).
Variabel percobaan berdasarkan Respon Surface Methodology (RSM) untuk
biokatalis Candida antarctica :
Jumlah biokatalis : 3,3% ; 4% ; 5% ; 6% dan 6,7% (w/w)
Temperatur reaksi : 31,6 ; 35 ; 40 ; 45 dan 48,4°C
Waktu reaksi : 40,3 ; 41 ; 42 ; 43 dan 43,7 (Jam)
Parameter uji yang digunakan untuk karakterisasi epoksi yang diperoleh
adalah perubahan oksiran oksigen (AOCS Cd 9-57, (1989)), bilangan hidroksi
(AOCS Cd- 13-60 (1989)), bilangan iod (AOCS Cd 1-25, (1989)) dan bilangan asam
II. TINJAUAN PUSTAKA
2.1 Senyawa Epoksi
Senyawa epoksi adalah senyawa yang dihasilkan dari reaksi epoksidasi
minyak nabati atau minyak bumi yang memiliki ikatan tidak jenuh. Penggunaan
minyak bumi sebagai bahan baku sudah jarang dilakukan dengan keterbatasan
sumber bahan baku minyak bumi. Minyak nabati dan derivatnya merupakan bahan
baku yang kini banyak digunakan untuk sintesa senyawa epoksi.
Reaksi epoksidasi adalah reaksi asam peroksi organik dengan ikatan rangkap
untuk membentuk senyawa oksiren (Wood dan Termini, 1958), atau reaksi dimana
senyawa hidrokarbon tidak jenuh diubah menjadi siklik eter (Kirk dan Othmer,
1965). Persamaan reaksi dari proses epoksidasi adalah sebagai berikut :
Gambar 1. Reaksi dari Epoksidasi Hidrokarbon
Dalam mempelajari pembuatan senyawa epoksi dari olefin, asam lemak tidak
jenuh dan ester tidak jenuh yang direaksikan dengan asam peroksi alifatik. Asam
peroksi asetat bebas air diperoleh dari reaksi antara asam asetat anhidrat dan hidrogen
peroksida. Asam peroksi dibentuk melalui interaksi antara asam karboksilat dengan
hidrogen peroksida.
H2O2 + RCO2H RCO3H + H2O Hidrogen Peroksida Asam Karboksilat Asam Peroksi air
Gambar 2. Reaksi Pembentukan Asam Peroksi pada Kondisi Proses Tertentu
Pembentukan asam peroksida dengan menggunakan hidrogen peroksida dapat
dilakukan dengan empat cara :
1. Asam peroksi asetat yang dibentuk terlebih dahulu.
2. Asam peroksi asetat yang dibentuk secara in situ.
3. Asam peroksi format yang dibentuk terlebih dahulu.
Dalam penyediaan asam peroksi dikenal dua cara yang biasa ditempuh.
Pertama, penyediaan asam peroksi secara terpisah (preformed) dan penyediaan secara
insitu. Penyediaan secara insitu lebih baik daripada secara terpisah karena hal-hal
sebagai berikut :
a. Penyediaan secara terpisah memerlukan tempat tersendiri, waktu proses yang
lebih lama, proses pemurnian dan penyimpanan hasil pada suhu rendah untuk
menghindari dekomposisi dan ledakan.
b. Penyediaan secara insitu selain tidak memerlukan hal-hal diatas juga hanya
membutuhkan pereaksi dengan jumlah minimum, menghasikan campuran fase
air dan minyak dengan konsentrasi hasil yang rendah sehingga lebih aman
(Yadav dan Satoskar, 1997).
Reaksi epoksidasi adalah reaksi adisi sehingga menghasilkan epoksida cis dan
trans dari cis dan trans alkena sebagai contoh asam oleat cis dan trans (elaidat) akan
menghasilkan isomer cis dan trans asam epoksi stearat yang muncul sebagai rasemat
tunggal (Gunstone,1993). Reaksi dapat dilihat pada reaksi berikut ini :
(Swern, 1982; Gunstone dan Norris, 1983)
Dalam reaksi epoksidasi, selain dihasilkan produk epoksi juga dihasilkan
produk samping sebagai hasil degradasi oksiran dan hasil reaksi samping. Untuk
moderat dan dengan menggunakan pelarut organik yang sesuai seperti heptana,
heksana atau toluena. Tabel 1 memperlihatkan hasil-hasil reaksi epoksidasi
menggunakan asam perasetat secara insitu.
Tabel 1. Hasil-hasil Reaksi Epoksidasi dengan Asam Perasetat Secara Insitu
H+ H+ H+ H+ H+ H+
No. Reaksi Keterangan
1. 2. 3a. 3b. 3c. 3d. 3e.
H2O2 + CH3CO2H CH3CO3H + H2O
R-CH=CH-R’ + CH3CO3H R-CHOCH-R’ + CH3CO2H
R-CHOCH-R’ + CHCO2H R-CH(OH)-CH(O2CCH3)-R’
R-CHOCH-R’ + H2O R-CH(OH)-CH(OH)-R’
R-CHOCH-R’ R-CO-CH2-R’
R-CHOCH-R’ + CH3CO3H R-CH(OH)CH(O3CCH3)-R
R-CHOCH-R’ + H2O2 R-CH(OH)-CH(O2H)-R’
Pembentukan Perasetat Reaksi epoksidasi Reaksi samping Reaksi samping Reaksi samping Reaksi samping Reaksi samping
Sumber : Lutz, 1978
Minyak nabati yang baik digunakan dalam pembuatan epoksi adalah yang
kedelai. Senyawa epoksi dapat dibuat dari minyak nabati (minyak terepoksidasi),
epoksi ester campuran dan epoksi ester spesifik. Senyawa epoksi sering digunakan
sebagai plasticizer dan stabilizer pada resin polivinil klorida (Carlson dan Chang,
1985).
Ester-ester tersebut telah digunakan sebagai pemlastis dan aditif untuk PVC
seperti terlihat pada Gambar 3 menghasilkan stabilititas cahaya dan panas yang baik,
yang tidak hanya disebabkan oleh kemampuannya mengikat hidrogen klorida terlepas
tetapi juga karena kemampuannya menggantikan atom klorin labil dalam rantai PVC
sehingga mencegah dehidroklorinasi lanjutan.
Gambar 3. Mekanisme Kerja Senyawa Epoksi sebagai Penstabil dan Pelentur pada Polivinil Khlorida (Swern, 1982)
Trigliserida atau ester terepoksi memiliki volatilitas rendah dan tahan terhadap
ekstraksi, sebagai contoh butil epoksi stearat adalah pemlastis yang sama baiknya
dengan pemlastis komersial dioktil adipat (DOA) dan menghasilkan kekuatan tarik
Senyawa epoksi dapat disintesis dari minyak nabati yang mengandung asam
lemak tak jenuh (ALTJ) cukup tinggi, yaitu sekitar 50%. Pada umumnya senyawa
epoksi disintesis dari minyak kedelai. Namun demikian, pada saat ini telah
dikembangkan penggunaan minyak sawit mentah sebagai bahan bakunya, karena
minyak sawit mentah mengandung asam lemak tak jenuh (ALTJ) yang cukup tinggi,
yaitu sekitar 48% (Kaufman. dkk, 1991).
Senyawa epoksida juga dapat berbentuk ester, sebagai contoh epoksi ester
minyak kedelai menguasai 70% (70 ribu ton per tahun) pasaran pemlastis ester karena
fungsinya bukan saja sebagai pemlastis namun juga sebagai penstabil. Ada tiga
kelompok dasar ester epoksida yang dibuat dari minyak/asam lemak nabati yaitu :
a. Trigliserida terepoksida
b. Campuran ester-ester epoksi (seperti : linseed, tall)
c. Ester epoksi khusus (seperti : oleat dan stearat) (Carlson dan Chang, 1985).
Reaksi kimia epoksidasi secara in situ dapat dilihat pada gambar berikut :
Mekanisme pembentukan senyawa epoksi melalui reaksi epoksidasi seperti
terlihat pada Gambar 5 pertama sekali ditemukan pada tahun 1955 oleh Bartlett
(Kwart dan Hoffman, 1966).
C C + O O O O O O O O C C C C C H H R R Senyawa tidak
jenuh Asam peroksi Produk intermediet
C
C
+ HO
R
Senyawa epoksi Asam karboksilat
Gambar 5. Mekanisme Pembentukan Senyawa Epoksi Melalui Reaksi Epoksidasi
Gall dan Greenspan (1955) mengatakan bahwa senyawa epoksi dengan
bilangan Iod yang rendah menunjukkan mutu yang baik. Reaksi epoksidasi
menggunakan teknik in situ memiliki beberapa keuntungan, antara lain mengurangi
bahaya yang dapat ditimbulkan oleh reaksi epoksidasi, mengurangi pemakaian
hidrogen peroksida serta mengurangi biaya (Swern, 1982).
Katalis yang dapat digunakan pada reaksi epoksidasi adalah asam sulfat pekat
dan resin penukar ion. Produksi optimal senyawa epoksi diperoleh dengan
ambarlite dan lama reaksi sekitar 8-14 jam. Reaksi ini dapat dipersingkat dengan
menggunakan hidrogen peroksida yang berlebih (Gall dan Greenspan, 1955).
Penggunaan rasio molar (asam asetat dan hidrogen peroksida yang tinggi)
menyebabkan terbukanya cincin epoksi sehingga rendemen epoksi ester yang
dihasilkan relatif rendah seperti yang disajikan pada Tabel 2.
Tabel 2. Pengaruh Rasio Molar (Asam Asetat dan Hidrogen Peroksida) terhadap Hasil Epoksidasi Tidak Jenuh
Epoksi Ester Rasio
Molar
Waktu Reaksi (jam)
Oksiran Oksigen (%)
Rendemen Bilangan
Bilangan Iod (%)
Reaksi (%)
15 : 11 3 0.0 0.0 4 95
1.7 : 1 8 0.2 4.4 8 89
0.5 : 1 13 3.6 80.0 5 93
Sumber : Gall dan Greenspan, (1955).
Wood dan Termini (1958) menyatakan bahwa proses epoksidasi biasanya
dilakukan pada suhu 65 – 75 OC, bila digunakan suhu yang lebih rendah akan
memperpanjang waktu epoksidasi dan menurunkan efisiensi epoksidasi. Hasil
penelitian Haya (1991) menunjukkan bahwa epoksidasi juga dapat dilakukan pada
suhu 100±5OC.
2.3 Metil Ester Asam Lemak Sawit Destilat
ALSD merupakan hasil samping pada tahap refining dalam industri minyak
(Nuryanto. dkk, 2002). Kandungan asam lemak pada minyak kelapa sawit dan ALSD
terlihat pada pada Tabel 3.
Tabel 3. Kandungan Asam Lemak Pada Minyak Kelapa Sawit dan ALSD
Komposisi Minyak Kelapa Sawit (%)* ALSD (%)**
Asam Laurat (C12) - 0,45
Asam Miristat (C14) 0,96 2,38
Asam Palmitat (C16) 41,62 60,50
Asam Stearat (C18) 4,23 2,57
Asam Oleat (C18-1) 42,12 27,08
Asam Linoleat (C18-2) 10,41 6,82
Asam Linolenat (C18-3) 0,22 0,19
Sumber : * Haryati. dkk (2002),
**Pusat Penelitian Kelapa Sawit (2008)
Perkembangan industri minyak goreng sawit pada dasawarsa terakhir
mengalami peningkatan sejalan dengan beralihnya pola konsumsi masyarakat dari
minyak goreng kelapa ke minyak goreng kelapa sawit. Konsumsi per kapita minyak
goreng Indonesia mencapai 16,5 kg per tahun dimana konsumsi per kapita khusus
untuk minyak goreng sawit sebesar 12,7 kg per tahun (Rephi’s, 2007). Kondisi ini
memberikan gambaran, bahwa dengan peningkatan industri minyak goreng maka
perolehan asam lemak sawit distilat turut meningkat. Hingga saat ini, pemanfaatan
asam lemak sawit distilat masih terbatas pada pembuatan sabun kualitas rendah.
Sehingga membutuhkan pengembangan lebih lanjut untuk meningkatkan nilai tambah
Senyawa metil ester asam lemak dapat diperoleh dengan cara esterifikasi
asam lemak bebas dengan gugus metil, yang disebut dengan metilasi. Pada proses ini
asam lemak bebas diesterifikasi dengan menggunakan metanol anhidrat berlebihan
dalam suasana asam. Pereaksi yang biasa digunakan pada proses ini adalah asam
klorida anhidrat dalam metanol (Anonim, 1977).
Berikut adalah bagan proses refining dalam industri pengolahan minyak kelapa sawit.
Crude Palm Olein (CPO)
Penghilangan Getah (Degumming)
Penjernihan Warna (Bleaching)
H3PO4
Deacidification & Deodorisation
RBD Palm Oil Asam Lemak Sawit Distilat
Olein RBD Stearin
Filtrasi Fraksinasi
Bleaching Earth
Gambar 6. Bagan Proses Pengolahan Kelapa Sawit Menjadi Minyak Goreng
Metil ester yang diperoleh dapat diekstrak dengan menggunakan pelaru inert
seperti, heksan dan petroleum eter (Anonim, 1966). Paquot dan Hutfenne (1987)
mengatakan, bahwa pembuatan metil ester dapat dilakukan secara langsung dari
trigliserida, melalui reaksi transesterifikasi menggunakan metanol berlebih, dan
katalis asam. Pereaksi lain yang dapat digunakan pada proses metilasi adalah
H2SO4/Metanol, HCl/Metanol dan diazometer/eter. Reaksi pembentukan senyawa
metil ester asam lemak sawit destilat dapat ditunjukkan pada gambar berikut :
Gambar 7. Reaksi Pembentukan Senyawa Metil Ester Asam Lemak
2.4 Enzim
Enzim adalah satu atau beberapa gugus polipeptida (protein) yang berfungsi
sebagai katalis dalam suatu reaksi kimia. Enzim bekerja dengan cara menempel pada
reaksi. Percepatan terjadi karena enzim menurunkan energi pengaktifan yang dengan
sendirinya akan mempermudah terjadinya reaksi. Sebagian besar enzim bekerja
secara khas, yang artinya setiap jenis enzim hanya dapat bekerja pada satu macam
senyawa atau reaksi kimia. Hal ini disebabkan perbedaan struktur kimia tiap enzim
yang bersifat tetap. Jadi enzim dapat berfungsi sebagai katalis yang sangat efisien,
disamping mempunyai kekhasan (spesifik) yang tinggi. Seperti juga katalis yang
lainnya, maka enzim dapat menurunkan energi aktivasi suatu reaksi kimia. Reaksi
kimia ada yang membutuhkan energi (reaksi endergonik) dan ada pula yang
menghasilkan energi atau mengeluarkan energi (eksergonik). Sifat spesifik
(kekhasan) enzim menyebabkan enzim hanya dapat bekerja pada satu reaksi saja
(Poedjiadi, 1994). Untuk dapat bekerja terhadap suatu zat atau substrat harus ada
hubungan atau kontak antara enzim dengan substrat. Suatu enzim mempunyai ukuran
yang lebih besar daripada substrat. Oleh karena itu tidak seluruh bagian enzim dapat
berhubungan langsung dengan substrat. Hubungan antara substrat dengan enzim
hanya terjadi pada bagian atau tempat tertentu saja. Tempat atau bagian enzim yang
mengadakan hubungan atau kontak dengan substrat dinamai bagian aktif (active site).
Hubungan hanya mungkin terjadi apabila bagian aktif mempunyai ruang yang tepat
untuk menampung substrat. Apabila substrat mempunyai bentuk atau konformasi
lain, maka tidak dapat ditampung pada bagian aktif suatu enzim. Dalam hal ini enzim
tidak dapat berfungsi terhadap substrat. Ini adalah penjelasan mengapa tiap enzim
kontak antara enzim dengan substrat menyebabkan terjadinya kompleks enzim
substrat. Kompleks ini merupakan kompleks yang aktif, yang bersifat sementara dan
akan terurai lagi apabila reaksi yang diinginkan telah terjadi. Secara sederhana sekali
penguraian suatu senyawa atau substrat oleh suatu enzim dapat digambarkan sebagai
berikut :
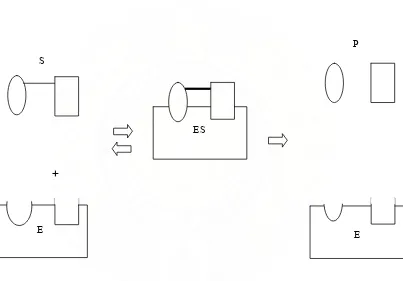
+
[image:34.612.121.524.251.532.2]
Gambar 8. Proses Penguraian Substrat Oleh Suatu Enzim
Atau :
E + S ES E +
S
ES
E P
E
yang identik, E menyatakan sisi aktif molekul enzim dan bukan molekul enzim).
Berdasarkan model ini, bila konsentrasi substrat menjadi tinggi sehingga cukup
secara keseluruhan untuk mengubah enzim ke bentuk ES, maka tahap kedua reaksi
menjadi mempunyai batas kecepatan dan seluruh tingkat reaksi menjadi tidak sensitif
(Simanjuntak dan Silalahi, 2003). Sebagai contoh, enzim -amilase hanya dapat
digunakan pada proses perombakan pati menjadi glukosa.
Enzim adalah material yang penerapannya pada kehidupan sudah dilakukan
manusia sejak peradaban dimulai. Proses fermentasi untuk membuat roti atau
minuman telah dilakukan oleh bangsa Mesir sejak 6000 tahun lalu. Dari pandangan
sains, penelitian tentang enzim sendiri telah dimulai sejak abad ke-tujuh belas.
Sampai sekarang berlalu empat abad, lebih dari 1000 jenis enzim yang berbeda telah
diketahui manusia. Akan tetapi tak sampai 200 jenis saja yang telah dikarakterisasi
secara detail dari segi struktur dan molekuler. Enzim sangat spesifik terhadap substrat
dan dapat menghasilkan produk utama hampir tanpa produk sampingan.
Keunggulan-keunggulan ini menyebabkan enzim menjadi katalis hayati yang jauh lebih unggul
daripada katalis kimiawi. Prospeknya sebagai biokatalis yang ramah lingkungan
karena proses yang efisien, spesifik, dan tak menghasilkan limbah yang merepotkan
sangat dinantikan oleh kalangan industri manufaktur dan masyarakat yang mencintai
lingkungan.
Pada tahun 1856, Claude Bernard pertama kali menemukan lipase dalam
ekstrak pankreas sebagai enzim yang dapat menghidrolisa minyak dan mengubahnya
ke produk lain yang memiliki kemampuan melarut. Dahulu enzim lipase diperoleh
melalui cara tradisional, yaitu dari pankreas hewan dan digunakan sebagai obat
saluran pencernaan. Ketertarikan terhadap lipase mikrobial diawali dengan
kekurangan pankreas dan sulitnya menemukan material dengan karakteristik yang
sama. Enzim dikenal sebagai katalis alam, saat ini sebagian besar enzim diperoleh
melalui proses fermentasi bahan-bahan alami. Pemanfaatan mikroorganisme telah
lama digunakan untuk memproduksi emulsifier dan biosurfaktan, untuk membantu
kelarutan dari lemak (Hasan. dkk, 2005). Ratusan enzim telah diketahui
spesificity-nya terhadap substrat yang berbeda, tetapi haspesificity-nya beberapa yang diisolasi dalam
bentuk murni dan dikristalkan, serta hanya sedikit yang diketahui strukturnya.
Keunggulan penggunaan protein dalam engineering, menjadikan industri enzim
menjadi penting. Misalnya protease dan lipase digunakan dalam industri deterjen,
amilase dan glukosa isomerisasi digunakan dalam industri pati atau dalam sintesa
senyawa organik lainnya. Hal ini mendorong dilakukannya klasifikasi enzim yang
rasional dan juga nomenklatur. Pada tahun 1961, International Union of Biochemistry
menetapkan klasifikasi enzim menjadi enam kelas dasar (Manitto, 1981), yaitu :
1. Oksidoreduktase
Mengkatalisis reaksi oksidasi reduksi, jadi memindahkan elektron-elektron dari
2. Transferase
Mengkatalisis pemindahan gugus atom dari suatu donor ke suatu akseptor
3. Hidrolase
Mengkatalisis hidrolisa ikatan C-O dan C-N
4. Liase
Meningkatkan terjadinya pemisahan (secara non hidrolitik) suatu gugus atom
dari substrat, sehingga terbentuk suatu ikatan rangkap atau penambahan suatu
gugus atom pada suatu ikatan rangkap
5. Isomerase
Mengubah substrat menjadi suatu isomernya
6. Ligase
Turut dikenal sebagai sintetase, yang mengkatalisis persatuan dua molekul
dengan cara memecahkan ikatan piroposfat dalam ATP atau triposfat lainnya.
Enzim lipase umumnya bekerja pada kondisi suhu 30 – 40 oC dan tekanan udara 1 atm sehingga diperoleh produk dengan mutu yang lebih baik karena kondisi
prosesnya menunjang kebutuhan tersebut. Mikroorganisme penghasil lipase juga
terdapat di Indonesia dan cukup potensial yaitu dari bakteri, kapang dan khamir.
Kerja enzim dipengaruhi oleh beberapa faktor, terutama adalah substrat, suhu,
keasaman) optimum yang berbeda-beda karena enzim adalah protein, yang dapat
mengalami perubahan bentuk jika suhu dan keasaman berubah. Di luar suhu atau pH
yang sesuai, enzim tidak dapat bekerja secara optimal atau strukturnya akan
mengalami kerusakan. Hal ini akan menyebabkan enzim kehilangan fungsinya sama
sekali. Kerja enzim juga dipengaruhi oleh kofaktor dan inhibitor.
Lipase adalah kelas enzim yang dapat mengkatalisis reaksi hidrolisa dari
trigliserida rantai panjang. Sejak berkembangnya bioteknologi, lipase mendapatkan
perhatian yang besar. Lipase merupakan kelas biokatalis yang penting dalam aplikasi
bioteknologi.
2.4.2 Lipase dalam Industri Oleokimia
Lipase merupakan bagian dari enzim hidrolisa yang dapat menyerang ikatan
karboksilat. Psikologis lipase adalah menghidrolisa trigliserida menjadi digliserida,
monogliserida, asam lemak dan gliserol (Hasan. dkk, 2005). Sebagai tambahan dari
fungsi alami hidrolisa ikatan ester karboksilat, lipase dapat menjadi katalis reaksi
esterifikasi, interesterifikasi dan transesterifikasi dalam media nonaquoeus.
Kemampuannya ini menjadikan lipase sebagai pilihan dalam aplikasinya pada
industri makanan, deterjen, farmasi, penyamakan kulit, tekstil, kosmetik dan kertas.
Beberapa jenis lemak memiliki nilai yang lebih tinggi dibandingkan yang lainnya,
karena bentuk dan strukturnya. Lemak dapat diubah menjadi jenis yang lain dengan
halnya dengan lipase, yang dapat mengkatalisis reaksi transesterfikasi minyak dan
lemak yang lebih murah, seperti produksi cocoa butter dari palmitat yang berasal dari
setengah fraksinasi. Dalam perkembangannya, lipase dapat menjadi katalis reaksi
transesterifikasi dalam pelarut organik. Sebagai contoh lipase dari pepaya (Carica
papaya) getah (CPL), Lipase Candida antarctica B (Novozyme 435, NOV) dan
Lipase Rhizomucor miehei (Lipozyme IM 20, LIP) digunakan sebagai biokatalisator
untuk esterifikasi (Gandhi, dkk, 2000).
2.4.3 Lipase dalam Reaksi Epoksidasi
Aktivitas katalitik enzim lipase untuk reaksi esterifikasi dan hidrolisis ester
telah banyak diaplikasikan dalam beberapa bidang oleokimia. Reaksi katalitik enzim
lipase pada asam lemak pertama dijelaskan oleh sebuah grup peneliti dari Novo
Nordisk A/S (Copenhagen, Denmark)(Godtfredsen. dkk, 1991).
Beberapa enzim lipase imobilis mengkatalisa bentuk asam lemak peroksi dari
asam lemak dan hidrogen peroksida yang terlihat pada Gambar 8. Normalnya reaksi
ini hanya dapat dicapai menggunakan asam mineral yang kuat seperti asam sulfat
konsentrasi tinggi sebagai katalis dan dalam kasus asam lemak rantai yang lebih
[image:39.612.115.449.282.367.2]panjang, asam bertindak sebagai pelarut (Weigert, 1978).
Reaksi katalisa dengan lipase imobilis, reaksi berlangsung pada kondisi yang
moderat ringan; oleh karena itu sangat sensitif terhadap asam sehingga asam
dikonversikan menjadi asam peroksi (perasam). Bjorkling, dkk (1990 dan 1992),
telah melakukan epoksidasi-Prileshajev in situ pada olefin sederhana dengan asam
peroksi, yang disiapkan dengan cara ini. Reaksi katalitik menyertakan ikatan C=C
dalam asam lemak tidak jenuh dan ester-esternya telah menjadi bidang penelitian
selama beberapa tahun (Warwel, 1996). Hal ini juga termasuk oksidasi C=C dengan
asam parasetik, hidrogen peroksida dan donor oksigen tunggal lainnya (Warwel,
1991). Titik awal dari penelitian ini adalah oksidasi katalitik lipase yaitu epoksidasi
“sendiri” secara kemoenzimatik asam lemak tak jenuh.
Jika katalis lipase yang disiapkan dengan asam peroksi diaplikasikan pada asam
lemak tak jenuh, pada Gambar 9 terlihat ada dua langkah reaksi yang akan terjadi.
Dalam langkah pertama, asam lemak tak jenuh (asam oleat yang ditunjukkan disini
adalah sebagai contoh) dikonversikan menjadi asam lemak peroksi tak jenuh.
Perasam tak jenuh ini hanya sebagai produk antara; senyawa ini mengepoksidasi
dirinya sendiri (epoksidasi-Prileshajev) dalam langkah kedua; dan produk akhir reaksi
adalah asam epoksi; asam lemak tak jenuh mengandung ikatan C=C dan group
perkarboksil untuk epoksidasi “sendiri”. Melalui cara ini, beberapa bahan alami,
asam lemak tak jenuh internal diepoksidasi. Kebanyakan minyak nabati tak jenuh
COOH
Enzim/H2O2
COOOH
Asam oleat peroksi
COOH
O
Gambar 10. Proses Reaksi Epoksidasi Menggunakan Enzim (Warwel, 1995)
2.5 Rancangan Percobaan
Penelitian ini menggunakan Response Surface Methodology (RSM) untuk
optimasi proses. RSM merupakan teknik matematika dan statistika yang berguna
untuk pemodelan dan analisa masalah dimana responnya dipengaruhi oleh beberapa
variabel. Tujuannya adalah untuk mengoptimalkan respon tersebut. Adapun metode
RSM meliputi perancangan percobaan, pengembangan model matematis dan
penentuan kondisi optimum untuk variabel bebas sehingga diperoleh hasil maksimum
dan minimum dari percobaan ini. Langkah awal dalam desain RSM adalah dengan
menentukan perkiraan yang sesuai untuk relasi fungsi yang tepat antara respon dan
variabel bebas. Dengan metode RSM diperoleh persamaan kuadratik yang dapat
digunakan untuk memperkirakan hasil dari fungsi variabel bebas seperti interaksinya.
Untuk menentukan level optimum pada variabel penelitian digunakan
faktorial CCD dimana desain eksperimen dalam perhitungan statistika dikodekan
dengan X1 dan aktual (Xi) seperti ditunjukkan dalam Persamaan 2.1 berikut ini.
1) 2. Pers ( 3...) 2, 1, (i X X X j i i 1 = ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ − = − X Dimana :
−
1
x : rata-rata nilai nyata variabel bebas pada rendah (low) dan tinggi (high) xj : selisih antar rentang
Secara umum hasil yang diperoleh dapat dianalisa dengan menggunakan
multiple regression yang memenuhi persamaan berikut (Montgomery, 1997)
2) . 2 (Pers X X X X X X X X X X X Y 2 3 10 2 2 9 8 3 1 7 3 2 6 2 1 5 3 4 2 3 1 2 1 + + + + + + + + + + = Dimana :
Y : Variabel respon yang diukur yaitu % konversi dietanolamida
1- 10 : Konstanta linier, kuadratik dan hasil regresi koefisien diagonal
: error term
Penyelesaian multi regresi dilakukan dengan metode sum of square of error
(SSE) untuk mendapatkan regresi dan plot-plot dimensi hasil perhitungan. Faktorial
CCD digunakan untuk optimasi amidasi asam lemak sawit distilat menjadi
dietanolamida menggunakan lipase dalam menganalisa variabel yang paling
berpengaruh yaitu temperatur, konsentrasi biokatalis dan rasio mol dietanolamina
terhadap ALSD. Matriks eksperimental (Tabel 5) untuk rancangan tiga faktor dengan
dua level (23) yang terdiri dari 8 run pertama (1-8) dengan variabel terkode (± 1) untuk masing-masing faktor (factorial point). Selanjutnya 6 run yang disebut star
point dengan level terkode (± ) sebagai significant curvature effect (9-14),
perkiraan daerah lekukan kurva dengan kode 0 untuk masing-masing faktor. Jarak
star point dengan center point adalah = 2n/4 (untuk 3 faktor, = 1,682). Hasil statistik 20 set run desain optimasi response surface methodology (RSM), analisa
regresi dan signifikansi statistikal dianalisa dengan dengan menggunakan simulasi
statsoft Minitab Release 14 untuk memberikan perkiraan pengaruh level optimum
dari ketiga faktor operasi dan interaksinya masing-masing yang diperoleh dari
penyelesaian persamaan regresi, analisa kontur dan plot respon permukaan (contour
and surface response). Cara dalam menentukan besarnya harga perlakuan setiap
komposit sebelah kiri dan kanan dari komposit pusat (kode 0) dihitung dengan cara :
1. Menetapkan terlebih dahulu perkiraan besarnya harga perlakuan tiap variabel
yang dianggap optimal (informasi tentang kondisi optimal dapat diperoleh dari
literatur atau melalui penelitian awal atau orientasi). Misal : 10% untuk
konsentrasi katalis pada pusat (kode 0)
2. Harga komposit berikutnya (kode 1) ditetapkan sembarang (dengan harga yang
wajar). Misal ditetapkan 12, berarti sebelah kiri (kode -1) ditetapkan 8 supaya
selisih sama berharga 2.
3. Untuk komposit (kode ) dihitung dengan menggunakan rumusan (Pers 2.1).
Misal : Center point : 10
Kode (1) : 12 dan kode (-1) : 8
Untuk : 1, 682
1,682 :
Dilanjutkan untuk setiap variabel, hasil perhitungan diterakan pada Tabel 4
Untuk menentukan keakuratan model matematis terhadap data hasil percobaan
diperiksa dengan analisis variansi (ANAVA). Ketepatan parameter persamaan untuk
[image:45.612.113.460.315.465.2]masing-masing variabel dilihat dari nilai p. Respon permukaan tiga dimensi dan
grafik kontur digunakan untuk mengetahui pengaruh variabel percobaan terhadap
hasil yang diperoleh.
III. METODOLOGI PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Oleokimia, Pusat Penelitian Kelapa
Sawit (PPKS) / Indonesian Oil Palm Research Institute (IOPRI), Jl. Brigjend.
Katamso No.51, Kampung Baru, Medan - Sumatera Utara. Penelitian dilakukan
selama 9 (Sembilan) bulan, mulai Maret 2008 sampai November 2008
3.2 Bahan
Bahan baku yang digunakan adalah metil ester asam lemak sawit destilat
(p.a) dan biokatalis Rhizomucor meihei diperoleh dari Sigma Chemical Co. (St.
Louis, MO). Candida antarctica diperoleh dari Novo Nordisk AS, dan Carica
papaya diperoleh dari Pusat Penelitian Kimia Lembaga Ilmu Pengetahuan Indonesia
(LIPI). Peralatan yang digunakan dalam percobaan ini adalah :
1. Labu leher satu 250 ml sebagai tempat berlangsungnya reaksi, yang
dilengkapi dengan termometer.
2. Hot plate merek Cimarex yang dilengkapi pengaduk magnetis dengan
kecepatan pengadukan 400 rpm digunakan sebagai media pemanas.
3. Filter vakum dan kertas saring digunakan pada tahap prurifikasi untuk
memisahkan campuran produk dengan Biokatalis.
4. Rotary evaporator pada tekanan 1 atm digunakan untuk menguapkan sisa
pelarut.
5. Kromatografi gas digunakan untuk analisa konversi oksiran dan kandungan
asam lemak.
6. Alat untuk analisa bilangan oksiran oksigen, bilangan iodium, bilangan
hidroksi dan bilangan asam karakteristik produk antara lain : buret, pipet tetes,
erlenmeyer, beaker glass, labu takar, pipa kapiler.
3.3 Metode Penelitian
Metode Response Surface Methodology (RSM) digunakan untuk merancang
percobaan dalam menentukan kondisi optimum epoksidasi metil ester dari asam
lemak destilat menggunakan biokatalis dengan tiga faktor sebagai variabel bebas,
yaitu :
1. Konsentrasi katalis
2. Temperatur reaksi
3. Waktu reaksi
Percobaan dirancang mengikuti bentuk Central Composite Design (CCD)
[image:47.612.116.525.356.518.2](Cochran & cox, 1962). Level terkode untuk penelitian disajikan pada Tabel 4 dan
Tabel 5 dibawah ini.
Tabel 4. Perlakuan Terkode Epoksidasi
Perlakuan Terkode Perlakuan
-1,682 -1 0 1 1,682
Katalis (% b/b) 3,3 4 5 6 6,7
Temperatur (°C) 31,6 35 40 45 48,4
[image:47.612.115.527.569.695.2]Waktu reaksi (Jam) 40,3 41 42 43 43,7
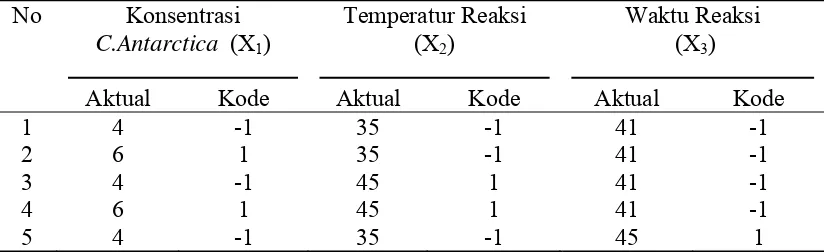
Tabel 5. Central Composite Design (CCD)untuk 3 variabel
Konsentrasi
C.Antarctica (X1)
Temperatur Reaksi (X2)
Waktu Reaksi (X3)
No
Aktual Kode Aktual Kode Aktual Kode
1 4 -1 35 -1 41 -1
2 6 1 35 -1 41 -1
3 4 -1 45 1 41 -1
4 6 1 45 1 41 -1
6 6 1 35 -1 45 1
7 4 -1 45 1 45 1
8 6 1 45 1 45 1
9 3,3 -1,682 40 0 42 0
10 6,7 1,682 40 0 42 0
11 5 0 31,6 -1,682 42 0
12 5 0 48,4 1,682 42 0
13 5 0 40 0 40,3 -1,682
14 5 0 40 0 43,7 1,682
15 5 0 40 0 42 0
16 5 0 40 0 42 0
17 5 0 40 0 42 0
18 5 0 40 0 42 0
19 5 0 40 0 42 0
20 5 0 40 0 42 0
Respons Surface Methodology (RSM) adalah suatu metode rancangan
percobaan yang digunakan secara luas dalam penelitian-penelitian untuk memperoleh
kondisi optimum dari variabel operasi. (Cochran and Cox, 1962). Nilai optimum yang
diperoleh dapat berupa titik maupun daerah/zona tertentu. Hal ini memberi bantuan
dalam menentukan kondisi operasi yang digunakan berkaitan dengan keterbatasan
alat dan ketersediaan bahan yang digunakan. Diharapkan dengan jumlah
perlakuan/run percobaan yang lebih sedikit dapat memberikan hasil yang sama
dengan metode lain yang jumlah run/perlakuannya jauh lebih banyak.
3.3.2 Pengolahan Data
3.3.2.1Optimasi Epoksidasi Metil Ester Asam Lemak Sawit Destilat (Me-ALSD)
untuk mengetahui kondisi optimum epoksidasi. Untuk melihat pengaruh-pengaruh
diatas, digunakan regresi multiple untuk memenuhi persamaan berikut ini :
Y = β1+β2x1+β3x2 + β4x3 +β5x1x2+β6x2x3+β7x1x3+β8x12+β9x22+β10x32+ε
Keterangan :
Y : Variabel response yang diukur yaitu % yield epoksidasi
1- 10 : Konstanta linier, kuadratik dan hasil regresi koefisien diagonal
: error term
3.3.2.2Analisa Response Surface Methodology (RSM)
Data percobaan diolah dengan menggunakan software Minitab 14 untuk
mendapatkan koefisien, model dan persamaan statistiknya. Untuk menentukan faktor
yang paling berpengaruh secara signifikan nilai p (probabilitas) dibatasi pada p ≤ 5%
(Cochran & Cox, 1962).
3.3.3 Tahapan Penelitian
Tahapan penelitian dilakukan secara bertahap sebagai berikut :
1. Karakterisasi Bahan Baku
2. Reaksi Epoksidasi
3. Analisa Senyawa Epoksi
3.3.3.1Karakterisasi Bahan Baku
Analisa komposisi asam lemak jenuh dan tidak jenuh pada metil ester ALSD
sebagai bahan baku epoksi dilakukan dengan menggunakan gas kromatografi
tebal film 0,1 µm, carrier gas: Helium, flushing gas: Nitrogen, suhu oven 50OC, suhu injektor 400OC dan suhu detektor 400OC).
3.3.3.2Reaksi Epoksidasi
Prosedur penelitian pembuatan epoksi meliputi :
1. Metil ester asam lemak sawit destilat (ME-ALSD) yang telah ditimbang
sebanyak 50 gr dimasukkan ke dalam reaktor (labu leher satu) dilengkapi
thermocouple dan pemanas berpengaduk (hot plate stirrer).
2. Kemudian dimasukkan pelarut n-Heksan dan penambahan biokatalis (enzim)
yang digunakan divariasikan jumlahnya.
3. Campuran dipanaskan pada media pemanas pada suhu yang divariasikan
sambil diaduk, kemudian ditambahkan hidrogen peroksida (H2O2) 30% secara
perlahan-lahan.
4. Setelah selesai penambahan hidrogen peroksida, campuran tetap dipanaskan
pada suhu dan waktu yang telah ditentukan berdasarkan perlakuan percobaan.
5. Setelah reaksi epoksidasi berlangsung selama waktu yang telah dilakukan,
reaksi dihentikan kemudian biokatalis dipisahkan dengan menggunakan filter
vacuum.
6. Campuran dicuci dengan air untuk memisahkan hidrogen peroksida (H2O2)
sisa.
7. Hasil cucian dikeringkan dengan natrium sulfat anhidrous (Na2SO4), lalu
8. Produk epoksi (filtrat) yang bercampur dengan n-Heksana dipisahkan dengan
menggunakan rotary evaporator pada temperatur 80OC.
9. Setelah proses pemisahan, epoksi kemudian dianalisa dan dilakukan
karakterisasi.
Untuk diagram kerja epoksidasi secara enzimatis terhadap metil ester ALSD
dapat dilihat pada Gambar 10 dibawah ini. Dan rangkaian peralatan epoksidasi metil
ester ALSD dapat dilihat pada Gambar 11.
Azhar Ramadhani Tarigan 067022002 Metil ester ALSD
Epoksidasi
Pencucian
Biokatalis (Candida antarctica;
Rhizomucor miehei;
Carica papaya) Hidrogen peroksida (H2O2)
H2O2 sisa
Filtrasi
Biokatalis n-Heksane
Dikeringkan
Filtrasi
Na2SO4
Gambar 11. Diagram kerja Epoksidasi
3.3.3.3Analisa Senyawa Epoksi
Analisa senyawa epoksi dilakukan dengan pengujian seperti : analisa
kandungan oksiran oksigen (AOCS Cd 9-57, (1989)), bilangan hidroksi (AOCS Cd-
13-60 (1989)), analisa bilangan iod (AOCS Cd 1-25, (1989)), dan bilangan asam
(Porim Test Methods, 1995) (Lampiran 1). Karakterisasi dilakukan dengan
berdasarkan gas kromatogram dan gugus fungsionalnya berdasarkan spektrofotometer
(FTIR).
(a) (b)
Gambar 12. Rangkaian Peralatan Epoksidasi; (a) Peralatan epoksidasi pada saat
ditambahkan dengan hidrogen peroksida (H2O2); (b) Peralatan
epoksidasi setelah penambahan dengan hidrogen peroksida (H2O2)
IV. HASIL DAN PEMBAHASAN
4.1 Penelitian Pendahuluan
Metil ester ALSD terdiri dari senyawa ester jenuh dan tidak jenuh.
Karakteristik bahan baku metil ester ALSD meliputi bilangan iod, bilangan oksiran
oksigen, bilangan hidroksi dan bilangan asam seperti disajikan pada Tabel 6.
Tabel 6. Hasil Analisa Bahan Baku Metil Ester ALSD
Parameter Hasil
Bilangan Oksiran Oksigen (%) 0,0114
Bilangan Hidroksi (mg KOH/g) 0,6592
Bilangan Iodin (mg/g) 50,651
Bilangan Asam (mg KOH/g) 5,8899
Untuk mengetahui komposisi asam lemak jenuh dan asam lemak tidak jenuh,
maka bahan baku metil ester ALSD dianalisis secara kromatografi gas. Hasil analisa
tertera dalam Tabel 7 dan data spektrum GC dapat dilihat pada Lampiran 5.
Tabel 7 memperlihatkan bahwa bahan baku metil ester ALSD mengandung
asam lemak jenuh dan asam lemak tidak jenuh. Kadar asam lemak jenuh yaitu asam
palmitat lebih besar dibanding dengan kadar asam lemak tidak jenuh yaitu asam oleat
dan asam linoleat. Kedua asam lemak tidak jenuh inilah yang memberikan bilangan
iodine yang tinggi (tertera dalam Tabel 6).
Tabel 7. Kandungan Asam Lemak Bahan Baku Metil Ester ALSD
Nama Jumlah C Komposisi
Asam Laurat C12-0
Asam Miristat C14-0 1,1479 %
Asam Stearat C18-0 3,8133 %
Asam Oleat C18-1 36,0950 %
Asam Linoleat C18-2 6,9769 %
Asam Linolenat C18-3 0,2114 %
4.1.2 Penentuan Level Terkode Central Composite Design (CCD)
4.1.2.1 Penentuan Jumlah Biokatalis
Biokatalis yang digunakan adalah enzim lipase yang mampu bekerja pada substrat
asam lemak dan minyak. Rhizomucor miehei, Candida antartica, dan Carica papaya
merupakan jenis lipase yang dijustifikasi mampu bekerja pada substrat asam lemak
sawit distilat yang banyak mengandung asam palmitat. Konsentrasi ketiga biokatalis
dilakukan pada 5 level dalam persen berat (b/b) yaitu 3%, 5%, 7%, 9% dan 0% (non
enzim) sebagai kontrol reaksi. Ini mengacu dari hasil-hasil penelitian yang dilakukan
oleh Rusch gen Klass dkk (1996) konsentrasi biokatalis yang digunakan dalam
jumlah 5% - 6% dan penelitian T. Vlcek dan Z. S. Petrovic (2006) digunakan
biokatalis dalam jumlah antara 2% - 10% (b/b) untuk menghasilkan produk epoksi.
Reaksi epoksidasi dilakukan selama 24 jam dan pada temperatur ruang (30OC).
Setelah waktu reaksi mencapai 24 jam dilakukan pengambilan sampel guna dianalisa
bilangan oksirannya. Hasil percobaan dapat dilihat pada Tabel 8 dan Gambar 13
berikut dibawah ini.
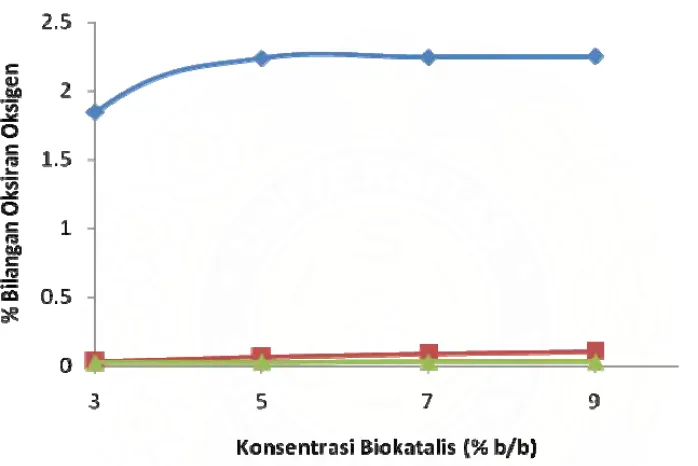
Tabel 8. Pengaruh Level Konsentrasi Biokatalis Terhadap Bilangan Oksiran
Biokatalis (b/b) CA RM CP
3% 1,8462 0,0342 0,0224
5% 2,2376 0,0673 0,0273
7% 2,2435 0,0922 0,0312
9% 2,2481 0,1051 0,0291
Suhu (T) : 30OC dan Waktu (S) : 24 Jam
[image:56.612.117.466.237.470.2]Keterangan : CA : Candida Antartica ; RM : Rhizomucor meihei CP : Carica papaya
Gambar 13. Pengaruh Level Konsentrasi Biokatalis Terhadap Bilangan Oksiran Oksigen
Terlihat pada Gambar 13 biokatalis Candida antarctica mampu melakukan
epoksidasi dengan hasil analisa bilangan oksiran oksigen rata-rata sebesar 2,2%
sedangkan biokatalis Rhizomucor miehei dan Carica papaya tidak menghasilkan
bilangan oksiran oksigen yang maksimum. Ini dikarenakan enansiomer metil ester
lebih sesuai dengan bagian aktif (active site) lipase Candida antarctica (Haoude, dkk,
biokatalis pada reaksi epoksidasi dengan ditetapkan jumlah biokatalis pada level
terkode sebagai center point sebesar 5% dalam desain response surface methodology
(RSM) yang akan digunakan.
4.1.2.2Penentuan Nilai Temperatur
Reaksi epoksidasi dengan biokatalis pada umumnya dapat bereaksi pada
temperatur antara 25 – 50°C. Untuk menentukan nilai atau harga temperatur pada
level terkode mengacu pada penelitian Rusch gen Klass (1996) yang melakukan
penelitian epoksidasi asam lemak tidak jenuh pada minyak kedelai untuk merubah
ikatan rangkap karbon (C=C) pada temperatur 40°C, dan T. Vlcek dan Z. S. Petrovic
(2006) yang melakukan penelitian optimasi epoksidasi minyak kedelai secara
enzimatik pada suhu 25°C dan 50°C. Maka dilakukan percobaan epoksidasi dari
ketiga biokatalis yaitu Candida antarctica, Rhizomucor miehei dan Carica papaya
dengan variasi temperatur reaksi sebesar 30°C, 40°C, 50°C dan 60°C. Reaksi
dilakukan dengan besar konsentrasi ketiga biokatalis sebesar 5% (b/b) dan waktu
reaksi selama 24 jam. Setelah waktu reaksi mencapai 24 jam dilakukan pengambilan
sampel guna dianalisa bilangan oksirannya. Hasil percobaan dapat dilihat pada Tabel
9 dan Gambar 14 berikut dibawah ini.
Tabel 9. Pengaruh Level Temperatur Terhadap Bilangan Oksiran
Bilangan Oksiran Oksigen Level Temperatur
(OC) CA RM CP
30 1,6742 0,0231 0,0218
40 2,2142 0,0346 0,0187
60 0,9723 0,0246 0,0141
Konsentrasi Biokatalis : 5% (b/b) dan Waktu (S) : 24 Jam Keterangan : CA : Candida Antartica ; RM : Rhizomucor meihei
[image:58.612.115.504.129.412.2]CP : Carica papaya
Gambar 14. Pengaruh Level Temperatur Terhadap Bilangan Oksiran Oksigen
Dari Gambar 14 dapat diketahui bahwa untuk reaksi yang melibatkan
Candida antarctica, Rhizomucor meihei, dan Candida antarctica.Perolehan bilangan
oksiran oksigen terbaik terdapat pada enzim Candida antarctica. Perolehan produk
epoksi meningkat hingga temperatur 40OC, tetapi pada saat temperatur yang lebih
tinggi digunakan (50OC dan 60OC), aktifitas lipase menurun sehingga perolehan
epoksi juga mengalami penurunan. Berdasarkan hasil di atas, ditetapkan temperatur
40OC sebagai nilai center point dalam desain response surface methodology (RSM)
yang akan digunakan.
Pada umumnya, reaksi yang melibatkan katalis hayati (biokatalis) berlangsung
dalam waktu reaksi yang cukup lama, hal ini berkaitan dengan kemampuan lipase
untuk merombak atau mensintesa suatu substrat pada kondisi tertentu. Guna
penentuan waktu reaksi adalah untuk mengetahui waktu terbaik yang dibutuhkan
dalam reaksi epoksidasi. Reaksi dilakukan pada suhu 40°C dan konsentrasi ketiga
biokatalis 5% (b/b). Reaksi berlangsung selama 18, 24, 42, 48 dan 66 jam. Waktu
yang ditentukan ini berdasarkan penelitian Rusch gen Klass (1996) yang melakukan
penelitian epoksidasi asam lemak tidak jenuh pada minyak kedelai selama 10 – 66
jam. Selama waktu reaksi yang telah ditentukan dilakukan analisa bilangan oksiran
oksigen. Hasil percobaan dapat dilihat pada Tabel 10 dan Gambar 15.
Tabel 10. Pengaruh Level Waktu Terhadap Bilangan Oksiran
Bilangan Oksiran Oksigen Waktu Reaksi
(jam) CA RM CP
0 0.0114 0.0114 0.0114
18 2.2033 0.0905 0.0556
24 2.2865 0.1058 0.0278
42 2.4321 0.0375 0.0295
48 2.4275 0.0803 0.0360
66 2.2950 0.0648 0.0343
Suhu (T) : 40OC dan Konsentrasi Biokatalis : 5% (b/b)
Gambar 15. Pengaruh Level Waktu Terhadap Bilangan Oksiran Oksigen
Gambar 15 memperlihatkan bilangan oksiran (%) terhadap waktu pada reaksi
epoksidasi pada berbagai variasi waktu reaksi pada masing-masing jumlah biokatalis
5% (b/b) dengan temperatur reaksi 40°C menunjukkan persen bilangan oksiran
cenderung meningkat sangat signifikan pada biokatalis Candida antarctica dengan
waktu reaksi selama 42 jam, sedangkan pada biokatalis Rhizomucor miehei dan
enzim Carica papaya menunjukkan nilai bilangan oksiran yang sangat rendah.
Mengarah pada konsep dan kondisi tersebut maka center point ditetapkan waktu
reaksi selama 42 jam dalam desain response surface methodology (RSM) yang akan
digunakan dan biokatalis yang dipilih untuk optimasi reaksi epoksidasi adalah
Candida antarctica.
4.2 Optimasi Epoksidasi Menggunakan Candida antarctica
Reaksi epoksidasi metil ester ALSD direaksikan menggunakan enzim lipase
Surface Methodology (RSM) meliputi variabel konsentrasi biokatalis (b/b),
temperatur reaksi dan waktu reaksi dengan desain percobaan berbentuk Central
Composite Design (CCD).
Tabel 11. Level Terkode Epoksidasi
Perlakuan Terkode Perlakuan
-1,682 -1 0 1 1,682
Biokatalis (% b/b) 3,3 4 5 6 6,7
Temperatur (°C) 31,6 35 40 45 48,4
Waktu reaksi (Jam) 40,3 41 42 43 43,7
Level-level pada variabel di atas diperoleh dengan mempertimbangkan
batas-batas pengoperasian alat-alat dan bahan-bahan penelitian serta sifat-sifat reaktan.
Respon yang diamati untuk diukur adalah konversi oksiran oksigen yang terbentuk
setelah reaksi berlangsung. Konversi oksiran oksigen yang diperoleh pada setiap run
dianalisa menggunakan Gas Cromatografy (GC). Percobaan terdiri atas 20 kombinasi
pada berbagai variasi jumlah biokatalis, temperatur reaksi dan waktu reaksi.
Penelitian ini memilih CCD sebagai bentuk desain eksperimen disebabkan oleh CCD
memberikan rancangan yang sistematik untuk memperoleh interaksi antar variabel.
Dari rancangan CCD ini akan diperoleh interaksi dari ketiga variabel yaitu
konsentrasi biokatalis (X1), temperatur reaksi (X2) dan waktu reaksi (X3). Berikut
adalah hasil percobaan yang telah dilakukan.
Tabel 12. Hasil Percobaan
No Konsentrasi
Candida antarctica
Temperatur Reaksi
(X2)
Waktu Reaksi
(X3)
Bil. Oksiran Oksigen
(X1) (%)
Aktual Kode Aktual Kode Aktual Kode
(%)
1 4 -1 35 -1 41 -1 2,132 68,539
2 6 1 35 -1 41 -1 2,453 78,914
3 4 -1 45 1 41 -1 2,482 79,851
4 6 1 45 1 41 -1 2,445 78,655
5 4 -1 35 -1 45 1 2,393 76,975
6 6 1 35 -1 45 1 2,262 72,741
7 4 -1 45 1 45 1 2,428 78,106
8 6 1 45 1 45 1 2,456 79,011
9 3,3 -1,682 40 0 42 0 2,412 77,589
10 6,7 1,682 40 0 42 0 2,432 78,235
11 5 0 31,6 -1,682 42 0 1,853 59,522
12 5 0 48,4 1,682 42 0 2,462 79,205
13 5 0 40 0 40,3 -1,682 1,932 62,075
14 5 0 40 0 43,7 1,682 2,453 78,914
15 5 0 40 0 42 0 2,446 78,688
16 5 0 40 0 42 0 2,458 79,076
17 5 0 40 0 42 0 2,453 78,914
18 5 0 40 0 42 0 2,454 78,946
19 5 0 40 0 42 0 2,456 79,011
20 5 0 40 0 42 0 2,432 78,235
*Konversi Oksiran
Oksiran Oksigen Teoritis = 3,094%
4.2.1 Analisa Pengaruh Variabel
Matrik eksperimental (Tabel 12) untuk rancangan tiga faktor dengan dua level
(23) yang terdiri dari 8 run pertama (run 1-8) dengan level terkode (±1) untuk masing faktor. Selanjutnya 6 run yang disebut star point dengan level terkode (± ) sebagai
significant curvature effect (run 9-14), sedangkan 6 run tambahan (run 15-20)
Pengaruh signifikansi variabel-variabel yang digunakan dapat diobservasi dari
hasil pengolahan data percobaan. Analisa statistika untuk signifikansi pengaruh dari
ketiga variabel yaitu konsentrasi biokatalis (X1), temperatur reaksi (X2) dan Waktu
reaksi (X3) dari masing-masing biokatalis serta interaksinya masing-masing
[image:63.612.115.528.278.495.2]tercantum pada Tabel 13 berikut ini.
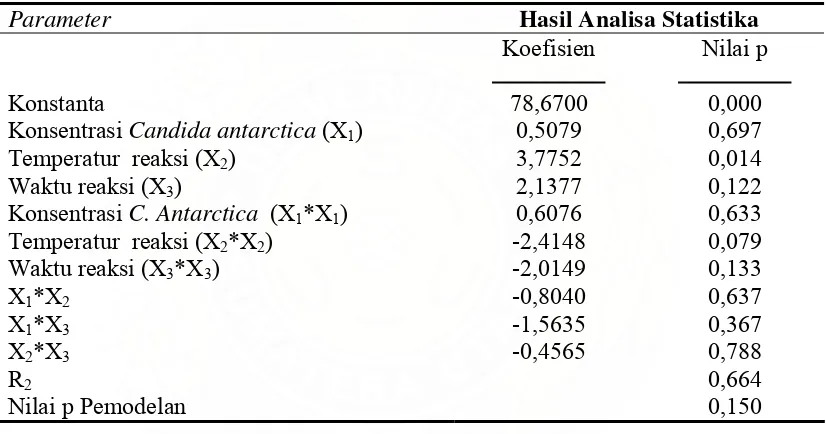
Tabel 13. Hasil Statistika Minitab 14 Untuk Response Surface Methodology (RSM)
Parameter Hasil Analisa Statistika
Koefisien Nilai p
Konstanta 78,6700 0,000
Konsentrasi Candida antarctica (X1) 0,5079 0,697
Temperatur reaksi (X2) 3,7752 0,014
Waktu reaksi (X3) 2,1377 0,122
Konsentrasi C. Antarctica (X1*X1) 0,6076 0,633
Temperatur reaksi (X2*X2) -2,4148 0,079
Waktu reaksi (X3*X3) -2,0149 0,133
X1*X2 -0,8040 0,637
X1*X3 -1,5635 0,367
X2*X3 -0,4565 0,788
R2 0,664
Nilai p Pemodelan 0,150
Keterangan : * Faktor signifikansi (p<0,05)
Berdasarkan hasil analisa statistika diatas, dapat diketahui bahwa konsentrasi
biokatalis (Candida antarctica) memberikan pengaruh yang positif sebesar 0,5079
dan signifikan terhadap pembentukan produk. Tetapi kuadrat variabel konsentrasi
biokatalis Candida antarctica memberikan pengaruh positif sebesar 0,6076 dan
interaksinya dengan temperatur memberikan efek negatif sebesar -0,8040 meskipun
reaksi yang memberikan efek negatif -1,5635 dengan nilai p 0,367. Hal ini
menunjukkan adanya batasan dalam penggunaan Candida antarctica, temperatur dan
waktu reaksi yang dilibatkan pada reaksi. Temperatur reaksi turut memberikan
pengaruh yang signifikan dan positif yang cukup besar dibandingkan variabel lainnya
sebesar 3,7752. Tetapi interaksinya dengan waktu reaksi (X2.X3) memberikan efek
negatif yang tidak signifikan.
Variabel waktu reaksi, turut memberikan efek yang singifikan dn positif
sebesar 2,1377. Interaksi temperatur dengan variabel reaksi lainnya juga tidak
signifikan. Ini menunjukkan bahwa laju reaksi enzimatis antara metil ester asam
lemak sawit distilat dengan hidrogen peroksida banyak dipengaruhi oleh besarnya
temperatur reaksi dan waktu reaksi terhadap metil ester asam lemak sawit distilat,
sedangkan peningkatan konsentrasi Candida antarctica memberikan pengaruh yang
tidak signifikan terhadap laju pembentukan produk epoksi. Namun penggunaan
variabel temperatur reaksi dan waktu reaksi ju