PENGARUH KONSENTRASI RAGI DAN LAMA FERMENTASI
TERHADAP MUTU MINUMAN BERALKOHOL DARI NENAS
(Ananas sativus)
SKRIPSI
OLEH:
ANDRI S SIAHAAN 040305007 / THP
DEPARTEMEN TEKNOLOGI PERTANIAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGARUH KONSENTRASI RAGI DAN LAMA FERMENTASI
TERHADAP MUTU MINUMAN BERALKOHOL DARI NENAS
(Ananas sativus)
SKRIPSI
OLEH:
ANDRI S SIAHAAN 040305007 / THP
Skripsi Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Teknologi Pertanian di Fakultas Pertanian
Universitas Sumatera Utara
DEPARTEMEN TEKNOLOGI PERTANIAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
2010
Judul Skripsi : Pengaruh Konsentrasi Ragi Dan Lama Fermentasi Terhadap Mutu Minuman Beralkohol Dari Nenas (ananas sativus)
Mama : Andri S Siahaan NIM : 040305007
Program Studi : Teknologi Hasil Pertanian
Disetujui Oleh Komisi Pembimbing,
Ir. Sentosa Ginting, MP DR. Ir. Elisa Julianti, MS Ketua Anggota
Mengetahui
Ir. Saipul Bahri Daulay, M.Si Ketua Departemen
ABSTRACT
THE EFFECT OF YEAST CONCENTRATION AND FERMENTATION TIME ON THE QUALITY OF ALCOHOLIC DRINK FROM PINEAPLE
The research was performed to find the effect of yeast percentage and fermentation time on the quality of alcoholic drink from pineaple. The research have been performed using factorial completely randomized design with two factors i.e percentage of yeast (K) : (1, 2, 3, 4, and 5%) and fermentation time (L) : (4 , 8 , and 12 days). Parameters analysed were total soluble solid, total acid, pH, total alcohol, organoleptic values of wine from pineaple. The results showed that both yeast percentage and fermentation time had highly significant effect all parameters.. The interaction of yeast percentage and fermentation time had highly significant effect on pH and total alcohol. Yeast percentage 1% and fermentation time 12 days produced the best quality of alcoholic drink from pineaple.
Keywords : Yeast percentage, Fermentation timealcoholic drink, pineaple.
ABSTRAK
PENGARUH KONSENTRASI RAGI DAN LAMA FERMENTASI TERHADAP MUTU MINUMAN BERALKOHOL DARI NENAS
Penelitian ini dilakukan untuk mengetahui pengaruh persentase ragi dan lama fermentasi terhadap mutu minuman beralkohol dari nenas. Penelitian ini menggunakan metode rancangan acak lengkap dengan dua faktor, yakni dengan persentase ragi (K) : ( 1, 2, 3, 4, dan 5%) dan lama fermentasi (L) : (4 , 8 dan 12 hari). Parameter analisa adalah total padatan terlarut, kadar asam mudah menguap, pH, kadar alkohol dan uji organoleptik dari anggur sari buah nenas. Hasil penelitian menunjukkan bahwa baik persentase ragi maupun lama fermentasi memberikan pengaruh yang berbeda sangat nyata terhadap semua parameter. Interaksi antara persentae ragi dan lama fermentasi memberikan pengaruh nyata terhadap pH dan Kadar alkohol. Persentase ragi 1 % dan lama fermentasi 12 hari menghasilkan mutu minuman beralkohol dari nenas yang terbaik.
ABSTRACT
THE EFFECT OF YEAST CONCENTRATION AND FERMENTATION TIME ON THE QUALITY OF ALCOHOLIC DRINK FROM PINEAPLE
The research was performed to find the effect of yeast percentage and fermentation time on the quality of alcoholic drink from pineaple. The research have been performed using factorial completely randomized design with two factors i.e percentage of yeast (K) : (1, 2, 3, 4, and 5%) and fermentation time (L) : (4 , 8 , and 12 days). Parameters analysed were total soluble solid, total acid, pH, total alcohol, organoleptic values of wine from pineaple. The results showed that both yeast percentage and fermentation time had highly significant effect all parameters.. The interaction of yeast percentage and fermentation time had highly significant effect on pH and total alcohol. Yeast percentage 1% and fermentation time 12 days produced the best quality of alcoholic drink from pineaple.
Keywords : Yeast percentage, Fermentation timealcoholic drink, pineaple.
ABSTRAK
PENGARUH KONSENTRASI RAGI DAN LAMA FERMENTASI TERHADAP MUTU MINUMAN BERALKOHOL DARI NENAS
Penelitian ini dilakukan untuk mengetahui pengaruh persentase ragi dan lama fermentasi terhadap mutu minuman beralkohol dari nenas. Penelitian ini menggunakan metode rancangan acak lengkap dengan dua faktor, yakni dengan persentase ragi (K) : ( 1, 2, 3, 4, dan 5%) dan lama fermentasi (L) : (4 , 8 dan 12 hari). Parameter analisa adalah total padatan terlarut, kadar asam mudah menguap, pH, kadar alkohol dan uji organoleptik dari anggur sari buah nenas. Hasil penelitian menunjukkan bahwa baik persentase ragi maupun lama fermentasi memberikan pengaruh yang berbeda sangat nyata terhadap semua parameter. Interaksi antara persentae ragi dan lama fermentasi memberikan pengaruh nyata terhadap pH dan Kadar alkohol. Persentase ragi 1 % dan lama fermentasi 12 hari menghasilkan mutu minuman beralkohol dari nenas yang terbaik.
PENDAHULUAN
Latar Belakang
Indonesia merupakan suatu negara agraris yang menghasilkan beraneka ragam sayuran dan buah-buahan. Salah satu jenis buah-buahan yang banyak ditanam di Indonesia adalah nenas. Secara umum diketahui bahwa buah nenas termasuk salah satu buah yang tidak dapat disimpan lama dan pada musim panen jumlahnya berlimpah dan tidak seluruhnya habis terjual atau dikonsumsi dalam bentuk segar.
Bagian utama yang bernilai ekonomi dari tanaman nenas adalah buahnya. Buah nenas selain dikonsumsi segar dapat juga diolah menjadi berbagai macam makanan atau minuman, seperti selai (jam), anggur, sirup, dan lain-lain.
Buah Nenas merupakan buah yang kaya akan karbohidrat, terdiri atas beberapa gula sederhana misalnya sukrosa, fruktosa, dan glukosa, serta enzim bromelin yang dapat merombak protein menjadi asam amino agar mudah diserap tubuh.
Dalam beberapa tahun terakhir ini, peminat minuman anggur di Indonesia berkembang pesat. Harga minuman anggur pun meningkat. Dahulu hampir semua minuman anggur di Indonesia berasal dari Prancis, sekarang minuman anggur di Indonesia datang dari berbagai negara, di antaranya Australia, Amerika, Afrika Selatan, Chili dan negara-negara penghasil minuman anggur lainnya.
Melihat semakin besarnya peminat minuman anggur saat ini, diperlukan pengembangan yang lebih serius sehingga pasar minuman anggur Indonesia tidak lagi bergantung kepada produk dari negara-negara lain terutama Eropa. Indonesia sendiri sebagai negara tropis memiliki banyak jenis-jenis buah yang dapat dijadikan sebagai anggur. Salah satu buah yang cukup berpotensi untuk digunakan dalam pembuatan anggur dari sari buah adalah nenas. Cita rasa buah nenas yang sangat khas dan menyegarkan dapat memberikan rasa anggur yang cukup bemutu. Nenas juga cukup memenuhi syarat untuk dapat digunakan dalam memproduksi anggur karena memiliki kandungan gula yang cukup tinggi.
Pada fermentasi sari buah, Winton dan Wintoan (1958) menyebutkan pembentukan alkohol terjadi akibat perombakan gula seperti glukosa dan fruktosa oleh enzim zymase (dari kelompok enzim invertase) yang berasal dari khamir
Saccharomyces ellipsoideus, S. apiculatus atau Saccharomyces lainnya; yang secara
alami terjadi pada buah dan proses tersebut akan berlangsung lebih cepat pada sari buah.
Stater yang ditambahkan pada perasan buah yang akan difermentasikan banyaknya antara 2-5 %. Semakin banyak stater yang ditambahkan maka akan semakin baik karena dapat memperpendek fase adaptasi . Lamanya waktu fermentasi juga akan mempengaruhi kualitas anggur sari buah yang dihasilkan.
Khamir yang digunakan untuk pembuatan anggur harus tahan terhadap alkohol yang tinggi dan dapat beradaptasi terhadap SO2. Disisi lain mikroorganisme tersebut
Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui pengaruh konsentrasi ragi, lama fermentasi dan interaksi antara konsentrasi ragi dan lama fermentasi terhadap mutu minuman beralkohol dari nenas.
Kegunaan Penelitian
- Sebagai sumber informasi dalam pembuatan anggur dari sari buah nenas. - Sebagai sumber data dalam penyusunan skripsi di Departemen Teknologi
Pertanian Fakultas Pertanian Universitas Sumatera Utara, Medan. Hipotesa Penelitian
- Penambahan konsentrasi ragi dan lama fermentasi berpengaruh terhadap total padatan terlarut, kadar asam mudah menguap, pH, kadar alkohol , uji kesukaan dari anggur sari buah nenas.
TINJAUAN PUSTAKA
Tanaman Nenas (Ananas sativus)
Nenas (Ananas sativus) termasuk famili Bromeliceae dari kelas Monokotyledoneae. Tanaman ini merupakan hortikultura yang mulai berproduksi pada umur 12 bulan. Nenas yang terkenal di Indonesia adalah nenas dari Sumatera (nenas Siantar dan Palembang), dan di Jawa adalah nenas Bogor, nenas klayatan. Sedangkan di luar negeri yang terkenal adalah dari Pilipina, Hawai dan Brazilia (Djatmiko, 1985).
Tanaman nenas tumbuh secara liar di dataran tinggi yang kering di Brazil dan Paraguai dan kemungkinan sekali tanaman nenas ini berasal dari negara tersebut. Kemudian tersebar ke Amerika, Spanyol, Portugis hingga akhirnya sampai ke daerah tropis seperti Pilipina dan Asia Tenggara. Nenas dapat tumbuh pada ketinggian 90 – 800 meter di atas permukaan laut. Temperatur optimum untuk pertumbuhan adalah berkisar 21-27 oC (Logman Group, !975).
Buah Nenas merupakan buah yang kaya akan karbohidrat, terdiri atas beberapa gula sederhana misalnya sukrosa, fruktosa, dan glukosa, serta enzim gromelin yang dapat merombak protein menjadi asam amino agar mudah diserap tubuh (Rismunandar, 1989).
Komposisi Buah Nenas
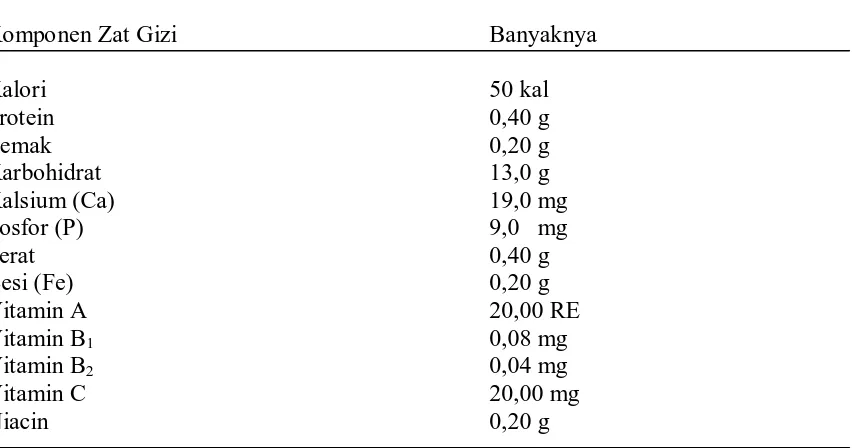
Buah nenas yang masak pohon mengandung zat gizi yang cukup tinggi. Tabel 1 menunjukkan kandungan zat gizi dalam 100 g buah nenas masak.
Tabel 1. Kandungan zat gizi dalam 100g buah nenas masak
Komponen Zat Gizi Banyaknya
Kalori 50 kal
Protein 0,40 g
Lemak 0,20 g
Karbohidrat 13,0 g
Kalsium (Ca) 19,0 mg
Sumber: Buah Dan Sayuran Untuk Terapi, 2000
Sedangkan Komposisi sari nenas dapat dilihat pada Tabel 2 berikut: Tabel 2. Komposisi sari nenas dalam 100 g bahan
Komponen Banyaknya
Air 85,00 %
Sumber : Departemen Perindustrian, 1977
Anggur Sari Nenas
Minuman beralkohol adalah minuman yang mengandung etil alkohol dan dapat mengandung zat lain dalam kadar tertentu yang tidak membahayakan kesehatan. Jenis minuman beralkohol antara lain : Anggut (wine), bir dan minuman keras. Anggur (wine) merupakan minuman hasil fermenasi perasan buah anggur yang dilakukan oleh sel khamir pada proses fermentasi gula yang terdapat di dalam perasan buah anggur akan dirombak oleh sel khamir menjadi alkohol dan CO2 (Sa’id 1987).
Anggur sari buah nenas adalah minuman yang merupakan hasil fermentasi larutan sari nenas bergula yang mempunyai rasa manis keasam-asaman yang menyegarkan dan mengandung alkohol. Komposisi anggur sangat bervariasi terutama kadar gula, kadar alkohol yang dihasilkan biasanya 3.5 – 7.3 %. Sedangkan kadar
alkohol yang telah mencapai 11-13 % biasanya disebut anggur keras (hard wine) (Amerine et al, 1982).
Proses Fermentasi
Fermentasi adalah suatu reaksi oksidasi-reduksi di dalam sistem biologi yang menghasilkan energi, dimana sebagai donor dan akseptor elektron menggunakan senyawa organik. Senyawa organik yang biasa digunakan sebagai substrat adalah karbohidrat dalam bentuk glukosa. Senyawa tersebut akan diubah oleh reaksi-reaksi dengan katalis enzim menjadi suatu bentuk lain misalnya aldehid dan dapat dioksidasi menjadi asam (Winarno dan Fardiaz, 1990).
fungsi substrat yang terpenting adalah sebagai sumber energi disamping sebagai bahan pembentuk sel dan produk metabolisme (Rahman, 1989).
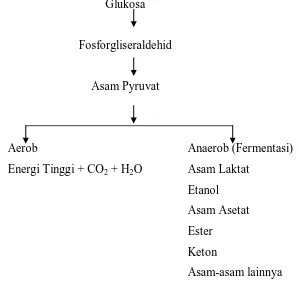
Proses dasar biokimia dari fermentasi dapat ditunjukkan pada Gambar 1. Glukosa
Fosforgliseraldehid
Asam Pyruvat
Aerob Anaerob (Fermentasi)
Energi Tinggi + CO2 + H2O Asam Laktat
Etanol Asam Asetat Ester
Keton
Asam-asam lainnya
Gambar 1. Jalur EMP atau proses glikolisis
Pembentukan alkohol dari gula dilaksanakan oleh khamir penghasil alkohol, seperti Saccharomyces ellipsoideus (Desrosier, 1988).
Selama fermentasi berlangsung, gula dalam bentuk glukosa dirombak menjadi etanol dan berbagai substansi lainnya seperti gliserol dan asam laktat yang disebut sebagai produk fermentasi. Perombakan tersebut berlangsung bersamaan dengan pembentukkan asam-asam, khususnya asam asetat yang semakin meningkat jumlahnya dari asam-asam volatile lainnya (Winton dan Winton, 1958).
Saccharomyces ellipsoideus, S. apiculatus atau Saccharomyces lainnya; yang secara
alami terjadi pada buah dan proses tersebut akan berlangsung lebih cepat pada sari buah.
zymase
Reaksinya adalah : C6H12O6 2 C2H5OH + 2CO2
Secara umum proses fermentasi alkohol terjadi dari pemecahan karbohidrat melalui suatu degradasi dari monosakarida yaitu glukosa menjadi asam piruvat. Asam piruvat ini selanjutnya akan dirombak menjadi etanol dan juga CO2 yang biasanya
berlangsung melalui proses oksidasi reduksi dengan menggunakan DNPH + H+ sebagai donor elektron (Winarno dan Fardiaz, 1990).
S. cerevisiae merupakan khamir sejati tergolong eukariot yang secara morfologi hanya membentuk blastospora berbentuk bulat lonjong silindris, oval atau bulat telur yang dipengaruhi oleh strainnya. Dapat berkembang biak dengan membelah diri melalui pertunasan. Reproduksinya dapat dipengaruhi oleh keadaan lingkungan serta jumlah nutrisi yang tersedia bagi pertumbuhan sel. Penampilan makroskopik mempunyai koloni berbentuk bulat, warna kuning muda, permukaan berkilau, licin, tekstur lunak dan memiliki sel bulat dengan askospora 1-8 buah (Nikon, 2004).
Taksonomi Saccharomyces sp adalah sebagai berikut (Sanger, 2009) : Super Kingdom : Eukaryotik
Phylum: Fungi
Species: Saccharomyces cerevisiae
Khamir dapat berkembang biak dalam gula sederhana seperti glukosa, maupun gula kompleks disakarida yaitu sukrosa . Selain itu untuk menunjang kebutuhan hidup diperlukan oksigen, karbohidrat, dan nitrogen . Pada uji fermentasi gula-gula mempunyai reaksi positif pada gula dekstrosa, galaktosa, sukrosa, maltosa, raffinosa, trehalosa, dan negatif pada gula laktosa (Lodder, 1970) .
Tabel 3 . Komposisi sel khamir S. cerevisiae
Senyawa Jumlah (%)
Abu 5,0-9,5
Asam nukleat 6,0-12,0
Lemak 2,0-6,0
Nitrogen 7,5-8,5
Sumber: Suriawiria (1990)
Mekanisme Fermentasi
Menurut Reed (1982), bahwa sukrosa mula-mula dihidrolisis menjadi glukosa dan fruktosa oleh enzim invertase kemudian glukosa dan fruktosa juga menjadi asam pyruvat melalui tahap-tahap reaksi pada jalur Embden-Meyerhof-Parnas. Selanjutnya asam pyruvat didekarbosilasi menjadi asetaldehida menjadi etanol (Gambar 2).
Faktor-Faktor yang Mempengaruhi Fermentasi
Faktor-faktor yang mempengaruhi fermentasi alkohol adalah : - Konsentrasi gula yang ada/ditambahkan
- Derajat keasaman bahan/pH - Temperatur
- Jenis khamir yang digunakan
ATP
Dehidroksi triofosfofoisomerase Aldolase Fruktosa 1,6 difosfat
Asetonfosfa
DPN difosfogliseraldehid
dehidrogenase dehidrogenase
DPNH2
Mg++ transfosforilase
ATP fosfopyruvat
Konsentrasi gula yang ada/ditambahkan
Pada proses fermentasi biasanya perlu ditambahkan sejumlah gula. Sebenarnya tanpa penambahan gula, fermentasi juga dapat berlangsung. Tujuan penambahan gula sebenarnya adalah untuk mendapatknan konsentrasi alkohol yang diinginkan (Departemen Perindustrian, 1975).
Menurut Sa’id (1987), gula yang ditambahkan pada sari buah bertujuan untuk memperoleh kadar alkohol yang lebih tinggi, tetapi bila kadar gula terlalu tinggi aktivitas khamir akan terhambat. Konsentrasi gula yang optimum adalah 28%. Konsentrasi gula yang baik untuk permulaan fermentasi yang baik adalah 16%, hal ini bertujuan untuk mempercepat pertumbuhan khamir pada awal fermentasi. Penambahan gula akan mengarahkan fermentasi lebih sempurna,menjamin kestabilan anggur yang dihasilkan serta menghasilkan alkohol yang tinggi. Kadar gula yang minimum untuk pertumbuhan khamir adalah 10%.
Menurut Prescott dan Dunn (1959), kadar gula yang sering digunakan pada fermentasi adalah 12%. Konsentrasi gula yang terlalu tinggi selama fermentasi alkohol berlangsung akan menghambat aktivitas khamir untuk memproduksikan alkohol.
Derajat keasaman bahan/pH
Menurut Prescott dan Dunn (1959), untuk mendapatkan pH yang optimum (4,0-4,5) dapat dilakukan dengan menambahkan asam, misalnya asam sitrat, tartarat atau malat dan bisa juga dengan menambah basa, misalnya KOH. Selama fermentasi berlangsung pH akan menurun dari pH semula. Penurunan pH selama fermentasi adalah disebabkan sebahagian alkohol diubah menjadi asam-asam organik, seperti reaksi berikut:
Suhu
Suhu merupakan faktor penting dalam proses fermentasi. Suhu ini sangat berpengaruh terhadap pertumbuhan Khamir. Temperatur minimum untuk pertumbuhan khamir adalah sekitar 1-3oC. Selama proses fermentasi berlangsung, suhu ini biasanya naik. Untuk mengatasi ini, tangki-tangki fermentasi selalu dilengkapi denagn alat pendingin. Pengadukan media dilakukan setelah starter dimasukkan dan dilakukan sekurang-kurangnya 2 kali sehari yaitu dengan cara memompa medium yang ada didasar tangki ke atas permukaan (Anonimous, 1078). Jenis khamir yang digunakan
Pada industri fermentasi alkohol jenis khamir yang umum digunakan adalah dari golongan Saccharomyces cereviceae, di mana khamir ini mempunyai kesanggupan yang tinggi untuk menghasilkan alkohol. Untuk memperoleh hasil fermentasi yang optimum, persyaratan yang dibutuhkan khamir (Winarno dan Fardiaz, 1990) adalah :
- pH dan kadar karbohidrat substrat - Temperatur selama fermentasi - Kemurnian dari khamir itu sendiri .
Starter khamir yang ditambahkan ke dalam sari buah banyaknya sekitar 2-5% dari volume sari buah (Frazier dan Westhoff, 1978).
Komposisi zat nutrisi di dalam bahan
Meskipun dalam bahan yang akan difermentasi telah mengandung zat makanan yang cukup untuk keperluan pertumbuhan mikrobia, sering ditambahkan sejumlah unsur-unsur tertentu dalam substrat, antara lain :
- garam amonium (NH4) SO4 sebagai sumber Nitrogen
- unsur makanan lainnya yang dibutuhkan untuk pembentukan energi (Prescott dan Dunn, 1959).
Biotin merupakan vitamin yang mutlak dibutuhkan oleh khamir,
Saccharomyces cereviceae membutuhkan biotin, thiamin, asam pantotenat, piridoksin
dan misionositol. Sedangkan vitamin lainnya dapat disintesa oleh khamir ini (Read dan Peppler, 1937).
Keadaan Oksigen Selama Fermentasi
Keadaan oksigen selama fermentasi harus diatur sebaik mungkin untuk memperbanyak atau menghambat pertumbuhan mikrobia tertentu. Setiap mikrobia membutuhkan oksigen yang berbeda-beda jumlahnya untuk pertumbuhan mikrobia tertentu dan juga untuk pembentukan sel-sel baru dalam fermentasi. Misalnya ragi roti atau khamir dan ragi anggur (Saccharomyces ellipsoideus), keduanya akan baik pada keadaan aerob, tetapi keduanya akan melakukan fermentasi terhadap gula jauh lebih bagus atau cepat pada keadaan anaerob (Winarno dan Fardiaz, 1980).
Asam-Asam yang Mudah Menguap
Asam-asam yang mudah menguap terdiri dari asam-asam yang biasanya terdapat dalam anggur sebagai hasil sampingan dari proses fermentasi. Di samping asam asetat dan asam laktat terdapat juga asam format, asam butirat dan asam propionat.
terjadinya oksidasi alkohol dan perombakan bakteri terhadap gula, asam sitrat, gliserol dan lainnya.
Asam-asam yang mudah menguap yang terdapat pada anggur sangat berpengaruh terhadap flavor anggur. Determinasi dari asam-asam yang mudah menguap pada anggur adalah sebagai salah satu kerusakan, yang merupakan prosedur penting untuk standarisasi mutu anggur. Pada pembuatan anggur yang baik asam-asam yang mudah menguap (dihitung sebagai asam-asam asetat) adalah kurang dari 0,030 g/100ml (Amerine el al, 1982).
Menurut Departemen Perindustrian 1973, syarat mutu anggur buah di Indonesia dapat dilihat pada Tabel-4.
Tabel-4 Syarat mutu anggur buah-buahan di Indonesia
No Komponen Jumlah
1 Etil Alkohol 9-18 % (V/V)
2 Metil Alkohol Maks 0,1%
3 Zat warna Tidak membahayakan
4 Logam berbahaya (Pb, Cu, Hg, As) Negatif 5 Bahan Pengawet
- Sulfit (SO2 maks) 200 mg/lt (ppm)
(SO2 bebasmaks) 50 mg/lt (ppm)
- Campuran
SO2 Bebas maks 50 mg/lt (ppm)
Benzoat (Asam Benzoat) 300 mg/lt (ppm)
Asam salisilat Negatif
Asam mudah menguap 0,2 %
6 Bau dan rasa Normal
BAHAN DAN METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian dilaksanakan pada bulan Januari 2010 di Laboratorium Mikrobiologi Umum Departemen Teknologi pertanian Fakultas Pertanian Universitas Sumatera Utara Medan.
Bahan Dan Alat Penelitian Bahan
Buah Nenas matang morfologi yang diperoleh dari pajak sore Padang Bulan dan Ragi Roti merek Saf-instant
Reagensia
NaOH 40 %, NaOH 0,1 N, KOH 30 %, Phenolftalen, dan Aquadest Alat Penelitian
Beaker glass, Pipet Skala, Hand Refractrometer, Labu Suling, Biuret,
Metode Penelitian
Penelitian ini menggunakan metode Rancangan Acak Lengkap (RAL) faktorial yang terdiri dari 2 faktor, yaitu :
Faktor I : Konsentrasi Ragi (K) : K1 = 1 %, K2 = 2 %, K3 = 3 %, K4 = 4 %,
K5 = 5 %
Faktor II : Lama Fermentasi (L) : L1 = 4 Hari, L2 = 8 Hari, L3 = 12 Hari
Banyaknya kombinasi perlakuan (treatment Combination) adalah 3 x 5 = 15, maka jumlah ulangan (n) minimum adalah sebagai berikut :
Tc ( n – 1 ) ≥ 15
15 ( n – 1 ) ≥ 15
15n – 15 ≥ 15
15n ≥ 30
n ≥ 2
Untuk memperoleh ketelitian dilakukan 2 kali ulangan. Model Rancangan (Bangun, 1991)
Rancangan yang digunakan adalah Rancangan acak lengkap (RAL) dua faktorial dengan model sebagai berikut :
Yijk = µ + αi + βj + (αβ)ij + εijk
dimana :
Yijk = Hasil Pengamatan
µ = Efek nilai tengah
αi = Efek dari faktor lama fermentasi pada taraf ke-i
βj = Efek dari faktor konsentrasi ragi pada taraf ke-l
(αβ)ij = Efek interaksi dari faktor lama fermentasi (L) pada taraf ke-i dan faktor
εijk = Efek galat dari faktor fermentasi (L) pada taraf ke-i dan faktor Konsentrasi
ragi (K) pada taraf ke-j dalam ulangan ke-k
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji dilanjutkan dengan uji beda rataan dengan menggunakan uji LSR (Least Significant
Range).
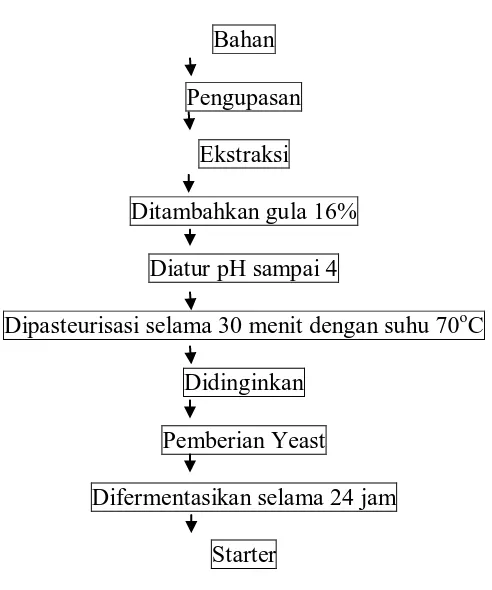
Pelaksanaan Penelitian Pembuatan starter
- Buah nenas segar dikupas, dan dihancurkan dengan blender - Ditambah air dengan perbandingan air : nenas 2 : 1
- Disaring dengan kain saring untuk mendaptkan sari nenas - Ditambahkan gula sebayak 16 % dari sari nenas
- Diatur pH sampai pH 4
- Dipasteurisasi dengan suhu 70oC selama 30 menit - Didinginkan
- Ditambahkan Yeast (Khamir Roti) sebanyak 3 gram tiap 100 ml - Dipermentasi selama 24 jam.
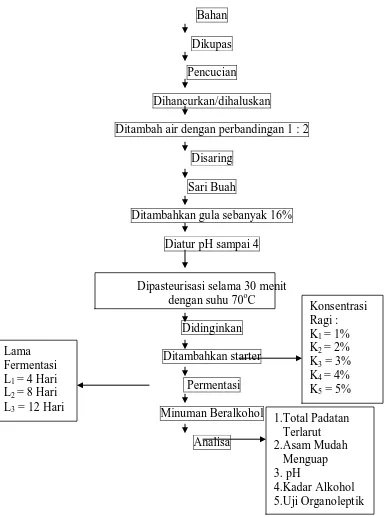
Pembuatan sari buah
- Buah Nenas segar dikupas, dihancurkan dengan belender - Ditambah air dengan perbandingan air : nenas 2 : 1 - Disaring dengan kain saring untuk mendaptkan sari nenas - Ditambahkan gula sebanyak 16 % dari sari buah nenas
Pembuatan minuman beralkohol
- Ditambahkan starter pada sari buah nenas dengan konsentrasi 1%, 2%, 3%, 4%, dan 5%
- Dipermentasikan selama 4, 8, dan 12 hari
- Dilakukan analisa terhadap parameter yang diamati Parameter Penelitian
Total padatan terlarut
Bahan dari tiap perlakuan dipipet ke dalam handrefraktometer ( 1 tetes ) kemudian dilakukan pengamatan dengan mengarahkan handrefraktometer kearah cahaya. Untuk setiap pergantian pengamatan, Handrefraktometer dibersihkan dengan aquadest dan dilap dengan tisu. Pada setiap pengamatan handrefraktometer akan menunjukkan angka pada skala hasil/nilai Total soluble Solid (TSS).
Penentuan kadar asam mudah menguap
Kadar asam mudah menguap dihitung sebagai asam asetat. Kadar asam asetat dapat dihitung dengan metode Jacobs (Sudarmadji et al, 1989) sebagai berikut :
Hasil sulingan diambil sebanyak 10 ml, ditetesi phenolftalein sebanyak 2 – 3 tetes sebagai indikator. Kemudian dititrasi dengan NaOH 0,1 N sampai terjadi perubahan warna merah muda, dan dicatat jumlah ml NaOH yang digunakan. Persentase kadar asam asetat ditentukan dengan rumus :
)
diukur elektroda dibilas kembali dengan aquadest kemudian dikeringkan kembali dengan tisu.
Penentuan kadar alkohol
Sari buah nenas yang sudah selesai difermentasikan diambil sebanyak 50 ml dan dimasukkan ke dalam labu ukur kemudian diukur kadar alkohol dengan menggunakan alkoholmeter. Setiap pergantian sampel alkohol meter dibilas dengan
aquadest lalu dikeringkan dengan tisu .
Uji organoleptik
Uji organoleptik dilakukan dengan uji kesukaan atau uji hedonik. Terhadap warna dan aroma dengan 10 orang panelis. Skala yang digunakan adalah 1-4 seperti pada tabel 5. Nilai organoleptik produk diperoleh dengan mengambil nilai warna dan aroma dengan perbandingan 50:50
Tabel 5. Skala uji hedonik
Skala Hedonik Skala Numerik
Sangat disukai 4
Disukai 3
Kurang disukai 2
SKEMA PENELITIAN
Bahan
Pengupasan
Ekstraksi
Ditambahkan gula 16%
Diatur pH sampai 4
Dipasteurisasi selama 30 menit dengan suhu 70oC
Didinginkan
Pemberian Yeast
Difermentasikan selama 24 jam
Starter
Konsentrasi
Ditambah air dengan perbandingan 1 : 2
Disaring
Sari Buah
Ditambahkan gula sebanyak 16%
Diatur pH sampai 4
Dipasteurisasi selama 30 menit dengan suhu 70oC
HASIL DAN PEMBAHASAN
Pengaruh Konsentrasi Ragi Terhadap Parameter Yang Diamati
Dari hasil penelitian dan analisis statistik yang telah dilakukan diperoleh bahwa konsentrasi ragi memberikan pengaruh terhadap total padatan terlarut, asam mudah menguap, pH, kadar alkohol dan uji organoleptik . Pengaruh konsentrasi ragi terhadap parameter yang diamati dapat dilihat pada Tabel 6.
Tabel 6. Hasil analisis pengaruh konsentrasi ragi terhadap parameter yang diamati Konsentrasi
Semakin besar persentase konsentrasi ragi yang diberikan maka kadar alkohol ,asam mudah menguap dan Uji Organoleptik semakin meningkat sedangkan total padatan terlarut, dan pH semakin turun.
Dari Tabel 6 dapat dilihat bahwa total padatan terlarut tertinggi terdapat pada perlakuan K1 dan terendah pada perlakuan K5, Jumlah asam mudah menguap yang tertinggi terdapat pada
perlakuan k5 dan terendah terdapat pada perlakuan K1, Kadar pH tertinggi terdapat pada
perlakuan K1 dan pH terendah terdapat pada perlakuan K5, Kadar alcohol tertinggi terdapat pada
organoleptik nilai terendah terdapat pada perlakuan K1 dan nilai tertinggi terdapat pada
perlakuan K5.
Pengaruh Lama Fermentasi Terhadap Parameter yang Diamati
Hasil penelitian secara umum tentang pengaruh lama fermentasi terhadap Total padatan terlarut, Asam mudah menguap, pH, kadar alkohol dan uji organoleptik dapat dilihat pada Tabel 7.
Tabel 7. Pengaruh lama fermentasi terhadap parameter yang diamati
Semakin lama waktu fermentasi maka Semakin tinggilah kandungan asam mudah menguap, kadar alkohol dan nilai organoleptik, sedangkan total padatan terlarut dan pH semakin menurun.
Dari Tabel 7 dapat dilihat bahwa total padatan terlarut terbesar terdapat pada L1
sedangkan yang terendah terdapat pada perlakuan L3, Jumlah asam mudah menguap tertinggi
terdapat pada L3 sedangkan yang terendah terdapat pada L1, pH yang tertinggi terdapat pada L1
sedangkan yang terendah terdapat pada L3, Kadar alkohol yang tertinggi terdapat pada perlakuan
L3 sedangkan yang terendah terdapat pada L1, Kemudian uji organoleptik yang tertinggi terdapat
pada L2 sedangkan yang terendah terdapat pada L1.
Total Padatan Terlarut
Dari daftar analisa sisik ragam (Lampiran 1) dapat diketahui bahwa penambahan ragi memberi pengaruh yang berbeda sangat nyata(P<0.01) terhadap total padatan terlarut yang dihasilkan. Untuk mengetahui perbedaan total padatan terlarut akibat penambahan ragi yang dilakukan pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR (least
significant ranges), seperti tertera pada Tabel 8.
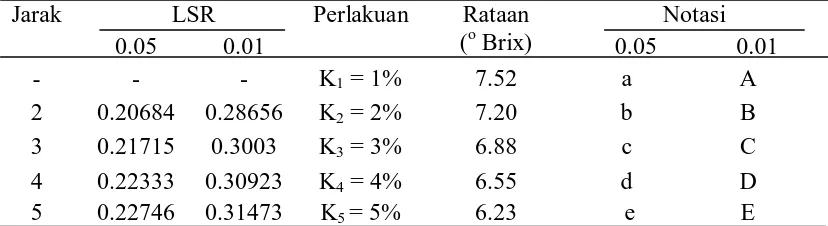
Tabel 8.Uji LSR pengaruh konsentrasi ragi terhadap total padatan terlarut (o Brix)
Jarak LSR Perlakuan Rataan
(o Brix)
Notasi
0.05 0.01 0.05 0.01
- - - K1 = 1% 7.52 a A
2 0.20684 0.28656 K2 = 2% 7.20 b B
3 0.21715 0.3003 K3 = 3% 6.88 c C
4 0.22333 0.30923 K4 = 4% 6.55 d D
5 0.22746 0.31473 K5 = 5% 6.23 e E
Keterangan : Notasi huruf yang berbeda menunjukkan berbeda nyata pada 0.05 (huruf kecil) dan berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 8 dapat dilihat bahwa perlakuan K1 memberikan pengaruh yang berbeda
sangat nyata terhadap perlakuan K2 , K3, K4, dan K5. Perlakuan K2 memberi pengaruh yang
sangat nyata terhadap perlakuan K3, K4, dan K5. . Perlakuan K3 memberi pengaruh yang sangat
nyata terhadap perlakuan K4 dan K5. Perlakukan K4 memberi pengaruh yang sangat nyata
terhadap perlakuan K5 .
Total padatan terlarut tertinggi diperoleh pada perlakuan K1 (pemberian ragi 1%) sebesar
7.52o Brix dan terendah diperoleh pada perlakuan K5 (pemberian ragi 5%) sebesar 6.23oBrix.
Gambar 5. Grafik Hubungan Penambahan ragi dengan total padatan terlarut.
Dari Gambar 5 dapat dilihat bahwa total padatan terlarut dengan perlakuan K1(1%) lebih
besar dibandingkan perlakuan K2(2%) dan mengalami penurunan sampai perlakuan K3(3%),
K4(4%), dan K5(5%). Hal ini dapat dijelaskan karena semakin besar penambahan ragi maka
jumlah khamir perombak yang terdapat pada sari buah nenas semakin besar sehingga semakin besar pula jumlah gula yang dirombak menjadi alkohol dan menurunkan total padatan terlarut dari minuman fermentasi. Semakin tinggi persentase ragi maka semakin besar kandungan khamir dan mikroba perombak yang terdapat sehingga semakin banyak karbohidrat yang dirombak menjadi alkohol, asam asetat dan senyawa lainnya (Tim Penulis UNAIR, 2007).
Pengaruh lama fermentasi terhadap total padatan terlarut
Dari analisa sisik ragam (Lampiran 1) dapat diketahui lama fermentasi memberi pengaruh yang berbeda sangat nyata (P<0.01) terhada total padatan terlarut.
Untuk mengetahui perbedaan total padatan terlarut akibat lama fermentasi yang dilakukan pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR (least
significant ranges), seperti tertera pada Tabel 9.
Tabel 9. Uji LSR pengaruh lama fermentasi terhadap total padatan terlarut (o Brix)
0.05 0.01 (o Brix) 0.05 0.01
- - - L1 = 4 hari 7.88 a A
2 0.16022 0.22197 L2 = 8 hari 7.70 b B
3 0.1682 0.23261 L3 =12 hari 5.05 c C
Keterangan : Notasi huruf yang berbeda menunjukkan berbeda nyata pada 0.05 (huruf kecil) dan berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 9 dapat diketahui bahwa L1 memberi pengaruh yang berbeda nyata terhadap
L2 tetapi memberi pengaruh yang berbeda sangat nyata terhadap L3. Perlakuan L2 memberi
pengaruh berbeda sangat nyata terhadap L3.
Total padatan terlarut paling tinggi terdapat pada lama fermentasi 4 hari (L1) sebesar
7.88oBrix sedangkan total padatan terlarut paling rendah terdapat pada lama fermentasi 12 hari (L3) sebesar 5.05oBrix.
Hubungan lama fermentasi terhadap kandungan padatan terlarut dapat dilihat pada Gambar 6.
Gambar 6 . Hubungan antara lama fermentasi dengan total padatan terlarut.
Dari Tabel 9 dan Gambar 6 diatas dapat dilihat bahwa total padatan terlarut dengan perlakuan L1 (4 hari) lebih besar dibandingkan L2 (8 hari) dan mengalami penurunan hingga pada
perlakuan L3 (12 hari). Semakin lama waktu fermentasi yang dilakukan maka semakin rendah
kandungan total padatan terlarut. Penurunan total padatan terlarut disebabkan selama proses fermentasi karbohidrat dirombak menjadi senyawa-senyawa yang lebih sederhana. Menurut Hidayat, et al. (2006) fermentasi dapat diartikan sebagai perubahan gradual oleh enzim beberapa bakteri, khamir dan jamur. Dalam hal ini, semakin lama proses fermentasi berlangsung, maka jumlah karbohidrat yang dirombak menjadi senyawa yang lebih sederhana semakin banyak sehingga semakin lama proses fermentasi maka semakin rendah lah nilai total padatan terlarut.
Pengaruh interaksi penambahan ragi dan lama fermentasi dengan total padatan terlarut Dari analisa sidik ragam (Lampiran 1) pengaruh interaksi penambahan ragi dan lama fermentasi memberi pengaruh yang tidak nyata (p>0.05) terhadap total padatan terlarut sehingga uji LSR tidak dilanjutkan.
Asam Mudah Menguap
Pengaruh penambahan ragi terhadap asam mudah menguap (dihitung sebagai asam asetat)
Dari analisa Sidik ragam pada Lampiran 2 dapat diketahui bahwa penambahan ragi memberi pengaruh yang berbeda sangat nyata (P<0.01) terhadap kadar asam mudah menguap yang dihasilkan.
Untuk mengetahui perbedaan kadar asam mudah menguap akibat penambahan konsentrasi ragi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR (least significant Ranges), seperti tertera pada Tabel 10.
Tabel 10. Pengaruh konsentrasi ragi terhadap kandungan asam mudah menguap (x10-2 %)
Jarak LSR Perlakuan Rataan (x10-2 %)
Notasi
- - - K1 = 1% 2.63 e E berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 10 dapat kita lihat bahwa K1 memberi pengaruh berbeda sangat nyata
terhadap K2, K3, K4 dan K5. Perlakuan K2 memberi pengaruh berbeda sangat nyata terhadap K3,
K4,dan K5. Perlakuan K3 memberi pengaruh berbeda sangat nyata terhadap K4 dan K5.
Perlakuan K4 Memberi pengaruh berbeda sangat nyata terhadap perlakuan K5
Total kandungan asam mudah menguap tertinggi terdapat pada perlakuan K5 (pemberian
ragi 5%) yaitu sebesar 4.04 x 10-2 %, sedangkan total kandungan asam mudah menguap terendah terdapat pada perlakuan K1(pemberian ragi 1%) yaitu sebesar 2.63 x 10-2 %.
Hubungan penambahan ragi terhadap total kandungan asam mudah menguap mengikuti garis regresi linier dapat dilihat pada Gambar 7.
Gambar 7. Grafik hubungan penambahan ragi dengan kandungan asam mudah menguap
Dari Gambar 7 dapat kita lihat ada peningkatan kandungan asam mudah menguap dari perlakuan K1(1%) menuju perlakuan K2(2%). Dan terus mengalami peningkatan hingga
perlakuan K3(3%), K4(4%), dan K5(5%). Semakin besar konsentrasi ragi yang diberikan jumlah
mikroba perombak pun semakin besar, maka keasaman bahan semakin tinggi, dimana asam dihasilkan dari perombakan alkohol menjadi asam asetat dan asam-asam lainnya. Menurut Amerine, et al, (1972) pada proses fermentasi dihasilkan asam-asam mudah menguap, di antaranya asam laktat, asam asetat, asam formiat, asam butirat dan asam propionat. Sehingga Semakin besar persentase ragi maka jumlah asam semakin tinggi.
Semakin tinggi persentase ragi, semakin banyak khamir dan bakteri yang terdapat di dalam minuman anggur, sehingga semakin banyak karbohidrat yang dirombak menjadi glukosa, alkohol , asam asetat dan senyawa lainnya. Sehingga semakin besar jumlah persentase ragi maka akan semakin besar asam mudah menguap yang dihasilkan (Tim Penulis UNAIR, 2007).
Pengaruh lama fermentasi terhadap kandungan asam mudah menguap
Dari analisa sidik ragam pada Lampiran 2 dapat diketahui bahwa Lama fermentasi akan memberikan pengaruh yang berbeda sangat nyata (P<0.01) terhadap kandungan asam mudah menguap.
Untuk mengetahui perbedaan kadar asam mudah menguap akibat lama waktu fermentasi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR, seperti tertera pada Tabel 11.
Dari Tabel 11 dapat diketahui bahwa taraf lama fermentasi perlakuan L1 memberi
pengaruh yang sangat nyata terhadap perlakuan L2 dan L3. Perlakuan L2 memberi pengaruh
yang sangat nyata pada perlakuan L3.
2 0.12025 0.16659 L2 = 8 hari 3.37 b B
3 0.12624 0.17458 L3 = 12 hari 3.78 a A
Keterangan : Notasi huruf yang berbeda menunjukkan berbeda nyata pada 0.05 (huruf kecil) dan berbeda sangat nyata pada 0.01 (huruf besar)
Total asam mudah menguap tertinggi terdapat pada L3 (lama fermentasi 12 hari) yaitu
sebesar 3.78 x 10-2 % dan kandungan asam mudah menguap terendah terdapat pada L1 (lama
fermentasi 4 hari) yaitu sebesar 2.89 x 10-2 %.
Hubungan lama fermentasi dengan kandungan asam mudah menguap dapat dilihat pada Gambar 8 yang mengikuti garis regresi linier.
Gambar 8. Grafik hubungan lama fermentasi dengan kandungan asam mudah menguap
Dari Gambar 8 dapat dilihat bahwa ada peningkatan kandungan asam mudah menguap dari perlakuan L1 (4 hari) menuju L2 (8 hari) dan terus mengalami peningkatan hingga L3 (12
hari). Semakin lama proses fermentasi berlangsung maka semakin besar asam-asam organik yang dihasilkan, hal ini sesuai dengan literatur Amerine, et al. (1972) yang menyatakan semakin lama fermentasi , maka asam-asam mudah menguap yang dihasilkan semakin banyak.
Semakin lama fermentasi maka kadar keasamannya semakin tinggi , Desroiser (1988), menyatakan bahwa pada proses fermentasi akan dihasilkan asam-asam mudah menguap,
diantaranya asam laktat, asam asetat, asam formiat, asam butirat, dan asam propionat. Asam dihasilkan dari perombakan glukosa dan alkohol.
Pengaruh interaksi penambahan konsentrasi ragi dan lama fermentasi dengan kandungan asam mudah menguap
Dari analisa sidik ragam pada Lampiran 2 pengaruh interaksi penambahan konsentrasi ragi dan lama fermentasi memberi pengaruh yang tidak nyata (p<0.05) terhadap kandungan asam mudah menguap yang dihasilkan sehingga uji LSR tidak dilanjutkan.
pH
Pengaruh penambahan ragi terhadap pH
Dari analisa sidik ragam pada Lampiran 3 dapat diketahui bahwa penambahan konsentarsi ragi memberi pengaruh sangat nyata(P<0,01) terhadap nilai pH. Untuk mengetahui perbedaan pH akibat penambahan konsentrasi ragi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR , seperti tertera pada Tabel 12.
Tabel 12. Uji LSR pengaruh konsentrasi ragi terhadap nilai pH
Jarak LSR Perlakuan Rataan Notasi berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 12 dapat diketahui bahawa K1 memberi pengaruh berbeda sangat nyata
terhadap perlakuan K2 , K3 , K4 dan K5. Perlakuan K2 memberi pengaruh berbeda sangat nyata
terhadap perlakuan K3 , K4 dan K5. Perlakuan K3 Memberi pengaruh berbeda sangat nyata
pH tertinggi diperoleh pada perlakuan K1 (pemberian ragi 1 %) yaitu sebesar 3.90
sedangkan kadar pH Terendah terdapat pada perlakuan K5 (pemberian ragi 5 %) yaitu sebesar
3,68 .
Hubungan besar konsentrasi ragi terhadap kandungan pH dapat dilihat pada Gambar 9.
Gambar 9 .Grafik hubungan konsentrasi ragi dengan pH
Dari Gambar 9 dapat dilihat bahwa pH dari perlakuan K1 lebih besar dibandingkan
perlakuan K2 (2%) dan terus mengalami penurunan sampai perlakuan K3(3%), K4(4%), dan
K5(5%). Hal ini disebabkan semakin besar konsentrasi ragi yang diberikan maka semakin besar
jumlah mikroba perombak yang terdapat pada sari buah nenas, Maka keasaman bahan semakin meningkat , dimana asam dihasilkan dari perombakan alkohol menjadi asam asetat dan asam-asam lainnya, sehingga pH minuman fermentasi yang dihasilkan semakin menurun. Menurut Amerine, et al, (1972) pada proses fermentasi dihasilkan asam-asam mudah menguap, diantaranya asam laktat, asam asetat, asam formiat, asam butirat dan asam propionat. Sehingga Semakin besar persentase ragi maka jumlah asam semakin tinggi. Semakin tinggi kadar keasaman bahan maka pH semakin menurun.
Menurut Buckle, et al. (1987) karbon dan energi dapat diperoleh dari gula karbohidrat sederhana seperti glukosa. Karbohidrat merupakan sumber karbon yang paling banyak digunakan dalam fermentasi oleh sel khamir.Bakteri asam asetat melakukan metabolisme yang bersifat aerobik. Peranan utamanya dalam fermentasi yaitu mengoksidasi alkohol dan karbohidrat lainnya menjadi alkohol dan asam asetat. Asam yang dihasilkan pada proses tersebut akan menurunkan pH lingkungan dan menimbulkan rasa asam. Jika tumbuh dalam anaerobik, kebanyakan khamir cenderung memfermentasikan substrat karbohidrat untuk menghasilkan etanol bersama sedikit produk lainnya. Jika persentase ragi semakin tinggi, kadar alkohol dan keasaman akan semakin meningkat dan kadar gula pun akan menurun.
Pengaruh lama fermentasi terhadap nilai pH
Dari analisa sidik ragam pada Lampiran 3 dapat diketahui bahwa lama waktu fermentasi memberi pengaruh berbeda sangat nyata (P<0.01) terhadap pH. Untuk mengetahui perbedaan pH akibat lama waktu fermentasi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR, seperti tertera pada Tabel 13.
Tabel 13. Uji LSR pengaruh lama fermentasi terhadap nilai pH
Jarak LSR Perlakuan Rataan Notasi
0.05 0.01 0.05 0.01
- - - L1 = 4 hari 3.94 a A
2 0.03445 0.04773 L2 = 8 hari 3.67 c C
3 0.03617 0.05002 L3 =12 hari 3.72 b B
Keterangan : Notasi huruf yang berbeda menunjukkan berbeda nyata pada 0.05 (huruf kecil) dan berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 13 dapat diketahui bahwa taraf lama fermentasi perlakuan L1 memberi
pengaruh berbeda sangat nyata terhadap perlakuan L2 dan L3 . Perlakuan L2 memberi pengaruh
Kadar pH tertinggi terdapat pada perlakuan L1 (lama fermentasi 4 hari) yaitu 3.94
sedangkan kadar pH terendah pada perlakuan L2 (lama fermentasi 8 hari) yaitu 3.67.
Hubungan lama fermentasi terhadap kandungan pH dapat dilihat pada Gambar 10.
-Gambar 10. Grafik hubungan lama fermentasi dengan nilai pH
Dari Gambar 10 dapat dilihat bahwa pH dari perlakuan L1 (lama fermentasi 4 hari) lebih
besar dari pada perlakuan L2 (lama fermentasi 8 hari) dan L3 (lama fermentasi 12 hari). Hal ini
disebabkan oleh karena semakin lama fermentasi maka semakin besar asam-asam organik yang dihasilkan , Menurut Desroiser (1988), pada proses fermentasi akan dihasilkan asam-asam mudah menguap, diantaranya asam laktat, asam asetat, asam formiat, asam butirat, dan asam propionat. Sehingga apabila semakin besar kandungan asam yang terdapat pada bahan maka nilai pH pun menurun.
Pada Tabel 13 dan Gambar 10 dapat dilihat ada peningkatan nilai pH dari taraf 8 hari menuju 12 hari yaitu dari 3,67 menuju 3,72. Hal ini dapat disebabkan oleh karena pada proses fermentasi dihasilkan asam-asam mudah menguap. Diantara asam-asam mudah menguap yang dihasilkan terdapat asam laktat yang termasuk dalam asam karboksilat. Asam laktat yang semula diproduksi selama proses fermentasi bereaksi dengal alkohol menghasilkan ester dan air
sehingga pada taraf 12 hari terjadi peningkatan nilai pH. Menurut Gaman dan Sherington (1992) asam karboksilat yang bereaksi dengan alkohol akan menghasilkan ester dan air, karena ion H+ -dari asam laktat bergabung dengan ion-ion hidroksil -dari alkohol dan menghasilkan air.
Semakin lama proses fermentasi berlangsung maka semakin banyak alkohol dan asam-asam organik yang dihasilkan, hal ini sesuai dengan literatur Amerine, et al. (1972) yang menyatakan semakin lama fermentasi, maka asam-asam mudah menguap yang dihasilkan semakin banyak. Dengan semakin banyaknya asam-asam mudah menguap yang dihasilkan maka nilai pH akan semakin menurun.
Pengaruh interaksi penambahan ragi dan lama fermentasi terhadap nilai pH
Dari analisa sidik ragam pada Lampiran 3 pengaruh interaksi penambahan ragi dan lama fermentasi memberi pengaruh berbeda nyata (p<0.05) terhadap nilai pH . Untuk mengetahui perbedaan pada masing-masing taraf perlakuan dilanjutkan dengan uji LSR seperti terlihat pada Tabel 14.
Dari Tabel 14 diperoleh nilai pH tertinggi diperoleh pada kombinasi perlakuan K1L1
dengan nilai pH sebesar 4.07 sedangkan nilai pH terendah diperoleh pada kombinasi K5L3
dengan nilai pH sebesar 3.50.
Hubungan interaksi perlakuan penambahan gula dengan lama fermentasi terhadap nilai pH dapat dilihat pada Gambar 11.
bahan semakin tinggi, dimana asam dihasilkan dari perombakan alkohol menjadi asam asetat dan asam-asam lainnya , sehingga pH yang dihasilkan semakin menurun.
Tabel 14. Efek pengaruh interaksi konsentrasi ragi dan lama fermentasi terhadap nilai pH
Jarak LSR Perlakuan Rataan Notasi
0.05 0.01 0.05 0.01
- - - K1L1 4.07 a A
2 0.07703 0.10672 K1L2 3.76 d D
3 0.08087 0.11184 K1L3 3.88 bc B
4 0.08318 0.11517 K2L1 4.02 ab A
5 0.08471 0.11722 K2L2 3.70 e D
6 0.08599 0.11875 K2L3 3.84 c C
7 0.0865 0.1208 K3L1 3.96 b AB
8 0.08702 0.12208 K3L2 3.68 e DE
9 0.08753 0.1231 K3L3 3.73 de D
10 0.08778 0.12387 K4L1 3.87 c BC
11 0.08778 0.12464 K4L2 3.64 ef E
12 0.08804 0.12541 K4L3 3.67 e E
13 0.08804 0.12592 K5L1 3.79 cd CD
14 0.0883 0.12643 K5L2 3.57 f EF
15 0.0883 0.12669 K5L3 3.50 g F
Keterangan : Notasi huruf yang berbeda menunjukkan berbeda nyata pada 0.05 (huruf kecil) dan berbeda sangat nyata pada 0.01 (huruf besar)
Gambar 11. Grafik hubungan interaksi konsentrasi ragi dan lama fermentasi dengan nilai pH
Semakin tinggi persentase ragi maka semakin besar kandungan khamir dan bakteri yang terdapat sehingga semakin banyak karbohidrat yang dirombak menjadi alkohol, asam asetat dan senyawa lainnya (Tim Penulis UNAIR, 2007).
Menurut Amerine, et al, (1972) pada proses fermentasi dihasilkan asam-asam mudah menguap, di antaranya asam laktat, asam asetat, asam formiat, asam butirat dan asam propionat. Sehingga apabila semakin lama proses fermentasi maka asam-asam mudah menguap yang dihasilkan akan semakin besar, Semakin besar jumlah asam-asam mudah menguap maka semakin turunlah nilai pH.
Kadar Alkohol
Pengaruh penambahan ragi terhadap kadar alkohol
Dari analisa sidik ragam pada Lampiran 4 dapat diketahui bahwa penambahan ragi memberi pengaruh yang berbeda sangat nyata (p<0.01) terhadap kadar alkohol yang dihasilkan.
Untuk mengetahui perbedaan kadar alkohol akibat penambahan Konsentrasi ragi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR seperti tertera pada Tabel 15.
Dari Tabel 15 dapat diketahui bahwa K1 memberi pengaruh berbeda sangat nyata
terhadap perlakuan K2 , K3 , K4 dan K5. Perlakuan K2 memberi pengaruh berbeda sangat nyata
terhadap perlakuan K3 , K4 dan K5. Perlakuan K3 Memberi pengaruh berbeda sangat nyata
terhadap Perlakuan K4 dan K5. Perlakuan K4 memberi pengaruh sangat nyata pada perlakuan K5.
Tabel 15. Uji LSR pengaruh konsentrasi ragi terhadap kadar alkohol
Jarak LSR Perlakuan Rataan berbeda sangat nyata pada 0.01 (huruf besar)
Kadar alkohol tertinggi terdapat pada perlakuan K5(konsentrasi ragi 5 %) yaitu 5.53 %
dan kadar alkohol terndah terdapat pada perlakuan K1 (konsentrasi ragi 1 %) yaitu 3.35 %.
Hubungan besar konsentrasi ragi terhadap kadar alkohol dapat dilihat pada Gambar 12 yang mengikuti garis regresi linier.
Dari Gambar 12 dapat kita lihat bahwa ada peningkatan kadar alkohol pada perlakuan K2
(2%) lebih besar dari perlakuan K1 (1%) dan terus mengalami peningkatan hingga K3(3%),
K4(4%) dan K5(5%). Semakin besar konsentrasi ragi yang diberikan maka semakin besar jumlah
khamir yang terdapat pada sari buah nenas terutama Sacharomyces cerevisiae. Khamir inilah yang merombak gula-gula sederhana yang terdapat pada sari buah menjadi alkohol melalui proses fermentasi. Hal ini sesuai dengan Judoamidjojo, et al (1992) yang menyatakan, salah satu jenis mikroorganisme yang memiliki daya konversi gula yang sangat tinggi adalah
Sacharomyces cerevisiae. Mikroorganisme ini menghasilkan enzim zimase dan invertase. Enzim
zimase berfungsi sebagai pemecah sukrosa menjadi monosakarida (glukosa dan fruktosa). Enzim invertase selanjutnya mengubah glukosa menjadi alkohol.
Pengaruh lama fermentasi terhadap kadar alkohol
Dari analisa sidik ragam pada Lampiran 4 dapat diketahui bahwa lama fermentasi memberi pengaruh berbeda sangat nyata (p<0.01) terhadap kadar alkohol yang dihasilkan. Untuk mengetahui perbedaan kadar alkohol akibat lama fermentasi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR seperti tertera pada Tabel 16.
Tabel 16. Uji LSR pengaruh lama fermentasi terhadap kadar alkohol (%)
Jarak LSR Perlakuan Rataan berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 16 dapat diketahui bahwa taraf lama fermentasi perlakuan L1 memberi
pengaruh berbeda sangat nyata terhadap perlakuan L2 dan L3 . Perlakuan L2 memberi pengaruh
Kadar alkohol terendah terdapat pada perlakuan L1 (lama fermentasi 4 hari) yaitu 2.03%
sedangkan kadar alkohol tertinggi pada perlakuan L3 (lama fermentasi 8 hari) yaitu 6.44%.
Hubungan lama fermentasi terhadap kandungan pH dapat dilihat pada Gambar 13 yang mengikuti garis regresi linier.
Gambar13 .Grafik hubungan lama fermentasi dengan kadar alkohol (%)
Dari Gambar 13 dapat dilihat bahwa ada peningkatan kadar alkohol dari dari perlakuan L1 (lama fermentasi 4 hari) kepada perlakuan L2 (lama fermentasi 8 hari) dan terus terjadi
peningkatan kadar alkohol hingga perlakuan L3 (lama fermentasi 12 hari).
Dari Tabel 16 dan Gambar 13 dapat dilihat bahwa dengan semakin lama dilakukan fermentasi maka kadar alkohol yang dihasilkan semakin meningkat, karena dengan semakin lamanya fermentasi yang dilakukan maka akan semakin banyak waktu yang dipergunakan oleh khamir dan enzim dalam merombak gula menjadi alkohol. Hal inilah yang menyebabkan kadar alkohol yang dihasilkan semakin meningkat hal ini sesuai dengan Said (1987) yang meyatakan bahwa dengan semakin lamanya fermentasi maka kadar alkohol akan semakin meningkat yang berhubungan erat dengan terjadinya peningkatan jumlah sel khamir dan enzim.
Pengaruh interaksi penambahan ragi dan lama fermentasi dengan kadar alkohol
Dari analisis sidik ragam (Lampiran 4) pengaruh interaksi penambahan konsentrasi ragi dan lama fermentasi memberi pengaruh berbeda nyata (P<0.05) terhadap alkohol yang dihasilkan.
Untuk melihat perbedaan kadar alkohol pada masing-masing taraf perlakuan dilanjutkan dengan uji LSR seperti terlihat pada Tabel 17.
Dari Tabel 17 diperoleh bahwa kadar alkohol tertinggi diperoleh pada kombinasi perlakuan K5L3 (konsentrasi ragi 5% dan lama fermentasi 12 hari) sebesar 8.05%, dan kadar
alkohol terendah diperoleh pada kombinasi perlakuan K1L1 (Konsentrasi ragi 1% dan lama
fermentasi 4 hari) sebesar 1.25%.
12 0.70078 0.99821 K4L3 7.05 ab AB
13 0.70078 1.00228 K5L1 2.90 f F
14 0.70282 1.00635 K5L2 5.60 cd CD
15 0.70282 1.00839 K5L3 8.05 a A
Keterangan : Notasi huruf yang berbeda menunjukkan berbeda nyata pada 0.05 (huruf kecil) dan berbeda sangat nyata pada 0.01 (huruf besar)
Hubungan interaksi perlakuan penambahan gula dengan lama fermentasi terhadap kadar alkohol dapat dilihat pada Gambar 14.
Gambar 14. Grafik interaksi konsentrasi ragi dan lama fermentasi dengan kadar alkohol
Dari Gambar 14 dapat dilihat bahwa semakin besar konsentrasi ragi yang diberikan serta semakin lama waktu fermentasi maka kadar alkohol yang dihasilkan semakin meningkat. Semakin besar konsentrasi ragi yang diberikan maka akan semakin besar jumlah mikroba perombak yang terdapat didalam sari buah nenas, hal ini sesuai dengan Tim Penulis UNAIR (2007) yang menyatakan semakin tinggi persentase ragi maka semakin besar kandungan khamir dan bakteri yang terdapat sehingga semakin banyak karbohidrat yang dirombak menjadi alkohol, asam asetat dan senyawa lainnya.
Semakin lama waktu fermentasi maka semakin meningkatlah jumlah mikroba perombak yang terdapat pada anggur dari buah nenas. Hal ini sesuai dengan Said (1987) yang meyatakan bahwa dengan semakin lamanya fermentasi maka kadar alkohol akan semakin meningkat yang berhubungan erat dengan terjadinya peningkatan jumlah sel khamir dan enzim.
Sehingga apa bila konsentrasi ragi diperbesar dan waktu fermentasi diperpanjang maka jumlah mikroorganisme pengurai akan semakin besar dan akan dapat lebih berkembang lagi seiring bertambhanya waktu sehingga jumlah gula-gula sederhana yang dirombak menjadi alkohol akan semakin besar atau meningkat.
Uji Organoleptik
Pengaruh penambahan ragi terhadap uji organoleptik warna dan aroma
Dari analisa sidik ragam pada Lampiran 5 dapat diketahui bahwa penambahan konsentarsi ragi memberi pengaruh berbeda sangat nyata (p<0.01) terhadap Uji Organoleptik. Untuk mengetahui perbedaan uji organoleptik akibat penambahan Konsentrasi Ragi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR seperti tertera pada Tabel 18. Tabel 18. Uji LSR pengaruh konsentrasi ragi terhadap uji organoleptik warna dan aroma (numerik) berbeda sangat nyata pada 0.01 (huruf besar)
Dari Tabel 18 dapat dilihat bahwa perlakuan K1 memberi pengaruh berbeda sangat nyata
pengaruh berbeda nyata terhadap K3, berbeda sangat nyata terhadap K4 dan K5. Perlakuan K3
memberi pengaruh berbeda nyata dengan perlakuan K4 dan berbeda sangat nyata terhadap
perlakuan K5. Perlakuan K4 memberi pengaruh berbeda sangat nyata terhadap perlakuan K5.
Nilai organoleptik tertinggi terdapat pada perlakuan K5 (Konsentrasi ragi 5 %) sebesar
3.55 dan terendah terdapat pada perlakuan K1 (konsentrasi ragi 1 %) yaitu sebesar 2.86.
Hubungan antara konsentrasi ragi dengan nilai organoleptik dapat dilihat pada Gambar 15 yang mengikuti garis regresi linier
Gambar 15.Grafik hubungan konsentrasi ragi dengan nilai organoleptik
Dari Gambar 15 dapat kita lihat bahwa ada pertambahan nilai organoleptik dari perlakuan K1 (1%) menuju K2(2%) dan terus mengalami peningkatan hingga K3(3%), K4(4%)
dan K5(5%). Hal ini dapat disebabkan oleh karena semakin besar konsentrasi ragi maka semakin
besar pula kandungan mikroba perombak yang terdapat pada anggur dari buah nenas. Menurut Setyohadi (2006), semakin tinggi jumlah ragi tape, maka semakin banyak khamir
(Saccharomices cereviceae) dan bakteri (Acetobacter aceti) di dalam bahan yang dibuat,
enzim-enzim amilase yang dihasilkan oleh khamir pun akan semakin banyak. Enzim-enzim-enzim amilase ini dapat merombak pati menjadi glukosa. Glukosa tersebut akan dirubah menjadi alkohol dan
menurut Buckle, et al., (1987) bakteri asam asetat seperti Acetobacter aceti dalam proses fermentasi bahan pangan akan mengoksidasi alkohol dan karbohidrat lainnya menjadi asam aestat. Dengan semakin besar persentasi ragi maka semakin banyak jumlah mikroorganisme perombak glukosa menjadi alkohol dan asam. Semakin tinggi jumlah gula, alkohol, asam asetat dan senyawa lainnya menbuat aroma minuman anggur semakin disukai.
Pengaruh lama fermentasi terhadap nilai uji organoleptik
Dari analisa sidik ragam pada lampiran 5 dapat diketahui bahwa penambahan lama fermentasi memberi pengaruh berbeda sangat nyata (p<0.01) terhadap Uji Organoleptik. Untuk mengetahui perbedaan Uji Organoleptik akibat lama fermentasi pada masing-masing taraf perlakuan maka dilanjutkan dengan uji LSR, Seperti tertera pada Tabel 19 .
Dari Tabel 19 dapat diketahui bahwa taraf lama fermentasi perlakuan L1 memberi
pengaruh berbeda sangat nyata terhadap perlakuan L2 dan L3 . Perlakuan L2 memberi pengaruh
berbeda sangat nyata pada perlakuan L3.
Tabel 19.Uji LSR pengaruh lama fermentasi terhadap nilai organoleptik warna dan aroma (numerik) berbeda sangat nyata pada 0.01 (huruf besar)
Nilai organoleptik tertinggi terdapat pada perlakuan L3 (lama fermentasi 12 hari) yaitu
sebesar 3.65. Sedangkan nilai Organoleptik terendah terdapat pada perlakuan L1(lama fermentasi
4 hari) yaitu sebesar 2.72.
Gambar 16.Grafik hubungan konsentrasi ragi dengan nilai organoleptik
Dari Gambar 16 dapat kita lihat bahwa ada penurunan nilai organoleptik dari perlakuan K1 (1%) menuju K2(2%). Kemudian ada peningkatan nilai organoleptik dari perlakuan L2 (lama
fermentasi 8 hari) menuju L3 (lama fermentasi 12 hari). Semakin lama waktu fermentasi maka
kadar alkohol akan semakin meningkat. Peningkatan kadar alkohol akan menyebabkan anggur memiliki berat jenis yang lebih kecil sehingga sel khamir dan komponen lain yang menyebabkan kekeruhan akan mengendap sehingga anggur terlihat jernih. Hal ini sesuai dengan Suryadarma (1986) peningkatan konsentrasi gula mengakibatkan peningkatan jumlah alkohol, anggur buah dengan kadar alkohol lebih tinggi akan mempunyai berat jenis yang lebih kecil sehingga sel khamir dan komponen lain penyebab kekeruhan akan mengendap.
Semakin lama proses fermentasi berlangsung maka semakin banyak alkohol dan asam-asam organik yang dihasilkan, hal ini sesuai dengan literatur Amerine, et al. (1972) yang menyatakan semakin lama fermentasi, maka asam-asam mudah menguap yang dihasilkan semakin banyak. Dengan semakin banyaknya asam-asam mudah menguap, alkohol, dan senyawa lainnya akan membuat aroma lebih disukai.
Pengaruh Interaksi Penambahan Konsentrasi Ragi Dan Lama Fermentasi Terhadap Nilai Organoleptik
KESIMPULAN DAN SARAN
Kesimpulan
Dari hasil penelitian pengaruh penambahan konsentrasi ragi dan lama fermentasi dari sari buah nenas terhadap mutu anggur sari buah nenas dapat diambil beberapa kesimpulan yaitu sebagai berikut:
1. Penambahan konsentrasi ragi memberi pengaruh berbeda sangat nyata tehadap total padatan
terlarut, kadar asam mudah menguap, pH, kadar alkohol , dan uji organoleptik. Semakin tinggi
konsentrasi ragi maka akan semakin besar jumlah mikroba perombak yang merombak gula-gula
sederhana menjadi alkohol dan alkohol menjadi asam asetat, sehingga semakin besar konsentrasi
ragi maka nilai total padatan terlarut, kadar asam mudah menguap, kadar alkohol dan uji
organoleptik meningkat sedangkan nilai pH menurun.
2. Lama fermentasi memberi pengaruh berbeda sangat nyata tehadap total padatan terlarut, kadar
asam mudah menguap, pH, kadar alkohol, dan uji organoleptik dari anggur sari buah nenas. Semakin
lama waktu fermentasi maka semakin besar jumlah alkohol dan asam mudah menguap yang
dihasilkan, sehingga nilai total padatan terlarut dan pH semakin menurun sedangkan nilai kadar
asam mudah menguap, kadar alkohol, dan uji organoleptik meningkat.
3. Interaksi perlakuan penambahan konsentrasi ragi dan lama fermentasi memberi pengaruh berbeda
nyata terhadap kadar alkohol dan nilai pH tetapi memberi pengaruh tidak nyata terhadap total
padatan terlarut, kadar asam mudah menguap dan uji organoleptik.
1. Untuk memperoleh mutu minuman anggur yang bermutu baik dari sari buah nenas disarankan
dilakukan penambahan ragi sebesar 1 % dan lama fermentasi 12 hari karena pada kombinasi
perlakuan ini akan diperoleh minuman anggur sari buah nenas dengan kadar alkohol dan asam
asetat yang tidak terlalu tinggi dan ph yang tidak terlalu rendah. Kadar alkohol yang diperoleh
sebesar 4.75%, asam mudah menguap 2.63 x 10-2% dan pH sebesar 3.88.
2. Perlu dilakukan penelitian yang lebih lanjut dengan faktor penambahan gula untuk mengetahui
mutu yang lebih baik dari minuman beralkohol sari buah nenas.
Amerine, M. A., dan C.S. Ough., 1980. Methods for Analysis of Musts and Wines. John Wiley & Sons, Inc., New York.
Amerine, M.A., H.W. Berg, R.E. Kunkee, C.S. Ough, V.I. Singleton, and A.D. Webb, 1982, Technology of Wine Making, The AVI Publ. Co., Inc., Westport, Connecticut.
Anonymous, 1978, Laporan Penataran Pengusaha Minuman Beralkohol, Departemen Perindustrian BPK Ujung Pandang, No. 40/XIV/3/78.
Atres, J.C., J.O. Mundt, and W.E. Sandine, 1980, Microbiologgy of Foods, W.H. Freeman and Co., San Fransisco.
Bangun, M.K., 1991, Rancangan Percobaan, Fakultas Pertanian Universitas Sumatera Utara, Medan.
Buckle, K.A., R.A. Edwards, G.H. Fleet, M. Wootton, 1987, Ilmu Pangan, Terjemahan Hari Purnomo dan Adiono, UI-Press, Jakarta.
Budiyanto, M.A.K, 2004. Mikrobiologi Terapan, Universitas Muhammadiyah Malang, Malang. Collins, J.L., 1960, The Pine Apple, Interscience Publisher Inc., Leonard Hill, London.
Departemen Perindustrian, 1973, Mutu dan Cara Uji Minuman Beralkohol, Jakarta.
Departemen Perindustrian, 1975, Penelitian Pembuatan Alkohol dari Nira Aren dan Lontar, BPK Ujung Pandang, Proyek Nomor 28/XIX/5/75.
Departemen Perindustrian, 1977, Proses Pembuatan Minuman Asal Buah-buahan, Proyek Bimbingan dan Penegmbangan Industri Kecil.
Departemen Kesehatan, 1989, Daftar Komposisi Zat Makanan, Direktorat Gizi, Jakarta.
Desrosier, N.W., 1988, Teknologi Pengawetan Pangaan, Terjemahan Muchji Mulohardjo, UI-Press, Jakarta.
Djatmiko, H, 1985. Nenas, Budidaya, Guna, Hasil Olahan, C.V. Yasaguna, Jakarta.
Gaman, PM, dan Sherrington KB. 1992, Ilmu Pangan, Pengantar Ilmu Pangan, Nutrisi dan Mikrobiologi, Gajah Mada University Press, Yogyakarta
Judoamidjojo, M., A. A. Darwis dan E. G. Sa’id, 1992. Teknologi Fermentasi. Rajawali Press, Jakarta.
Lodder, J. 1970. The Yeast, A Taxonomic Study Second Revised and Enlarged Edition, The Netherland, Northolland Publishing Co, Amsterdam.
Masuda, M., M. Yamamoto dan Y. ASAPURA, 1985., Direct gas chromatographic analysis of fusel alcohols, fatty acid and esters of distilled alcoholic beverages, j. food. sci.
Nikon. 2009. Saccharomyeces yeast cells : nikon microscopy . phase contrast lmageGaIlery .http//www.microscopyu.com/galleries/pliasecontrast/
saccharomvcessmall .html ( November 2009) .
Prescot, S.C., and G.C. Dunn, 1959, Industrial Mikrobiologi, Mc. Graw Hill Book Company, Inc., New York.
Rismunandar, 1989, Membudidayakan tanaman Buah-buahan, Penerbit Sinar Bru Bandung. Rahman, 1989. Penuntun Praktikum Teknologi Fermentasi. Jurusan Teknologi Pangan dan
Gizi-IPB Bogor.
Reed, G. 1982. Industryal Microbiology. Avi publ. Company., Inc., Westport, Connecticut. Reed, G. dan H.J. Peppler, 1973. Yeast Teknologi Fermentasi. P.T Medyatama Sarana Perkasa,
Jakarta.
Sa’id, E.G., 1987, Bio Industri Penerapan teknologi Fermentasi. P.T Medyatama Sarana Perkasa, Jakarta.
Sanger. 2004. Peptidase of saccharomyces cerevisea. http//merops. sanger.ac.uk/ speccards/peptidase/spoo0895 . htm. (20 juli 2009)
Setyohadi, 2006. Proses Mikrobiologi Pangan (Proses Kerusakan dan Pengolahan). USU-Press, Medan
Siddharta, F.M. 1989, Pemanfaatan Limbah Pengolahan Nenas sebagai Bahan Baku Pembuatan Silase secara Biologis. Skripsi Fateta, IPB Bogor.
Suryadarma, L., 1986, Mempelajari pengaruh jenis starter, konsentrasi gula dan lama pemeraman terhadap buah rambutan (Nephelium lappaceum L.), Skripsi Fateta, IPB Bogor.
Suriawiria, U. 1990. Pengantar Biologi Umum. Penerbit angkasa. Bandung
Tim Penulis UNAIR, 2007. Ragi.
Winarno, F.G., S. Fardiaz, dan D. Fardiaz, 1980, Pengantar Teknologi Pangan, PT. Gramedia, Jakarta.
Winton, A.L., and K.B. Winton, 1958, The Analysis of Food, New York-John Wiley and Sons, Inc., Chapman and Hall, Ltd. London.
Wirakusumah, E.S. 2000. Buah Dan Sayur Untuk Terapi. Penebar Swadaya. Jakarta.
Lampiran-1. Data Hasil Analisa Total Padatan Terlarut (oBrix)
K1T1 8.70 8.50 17.20 8.60
Daftar analisa Sidik Ragam Total Padatan Terlarut
Lampiran-2. Data Hasil Analisa Asam Mudah Menguap (x10-2%)
Perlakuan Ulangan Total Rataan I II
Daftar analisa Sidik Ragam Asam Mudah Menguap
** sangat nyata * nyata
tn tidak nyata
Lampiran 3. Data Hasil Analisa pH
Perlakuan Ulangan Total Rataan I II
Daftar analisa Sidik Ragam pH
Lampiran 4. DataHasil Analisa Kadar Alkohol (%)
Perlakuan Ulangan Total Rataan I II
Daftar Analisa Sidik ragam Kadar Alkohol (%)
KxT 8 2.0913 0.2614 3.1495984 * 2.64 4.00
Lampiran-5 Data Hasil Analisa uji Organoleptik (Numerik)
Perlakuan Ulangan Total Rataan I II
Daftar Analisa Sidik ragam Nilai Organoleptik
T Lin 1 1.0170 1.0170 60.261011 ** 4.54 8.68
T Kuad 1 3.3088 3.3088 196.05777 ** 4.54 8.68
KxT 8 0.1253 0.0157 0.9280071 tn 2.64 4.00
Error 15 0.2532 0.0169
Total 29 6.4623
Keterangan:
FK 304.45416
KK 0.0407796 4.07796 %
** sangat nyata * nyata