i
ABSTRAK
PENGARUH VARIASI VOLTASE PROSES ANODISASI PADA
ALUMINIUM TERHADAP KEKASARAN DAN KANDUNGAN
FASA
Oleh
M.ZANUARDI.W
Pengembangan ilmu tentang kekuatan material selalu mengalami kemajuan
seiring dilakukannya pembangunan yang terus berlanjut dan terus berkembang, di
segala aspek pembangunan.Proses Anodisasi adalah termasuk pengembangan
tentang ilmu material, dimana proses dari anodisasi itu sendiri yang bertujuan
untuk menguatkan bahan material dan menambah umur pakai dari material.
Selain untuk menambah umur pakai material yang digunakan, anodisasi juga
dapat berguna untuk menambahkan performa dari suatu material dan dapat
merubah unsur dari material sesuai dengan apa yang diinginkan menyesuaikan
dengan proses anodisasi yang dilakukan.
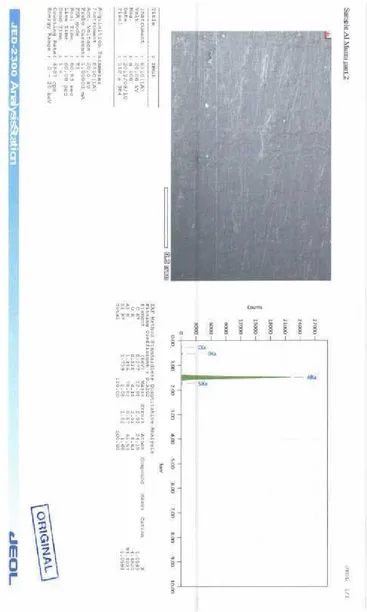
7,643%, untuk 12 V nilai Al =84,529% dan nilai AlP =15,471%, dan 15 V nilai
Al =76,973%, dan nilai AlP = 23,027%.
ABSTRA
CT
THE INFLUENCE OF VARYING VOLTAGES IN
ALUMINUM ANODIZING PROCESS TO SURFACE ROUGHNESS
AND PHASE CONTENT
By
M. ZANUARDI. W
✁✂✄
n
✁✄☎ ✄v
✄lopm
✄nt on m
✆t
✄r
✂✆l str
✄n
✝t
✞✞✆s
✟ ✄✄n
☎✄v
✄lop
✂n
✝✁ont
✂nuously
✂n
✆ll
☎ ✄v
✄lopm
✄nt
✆sp
✄✁ts.
✠no
☎✂zing process is one of developments in material
science, where anodizing process objective is to strengthen material and to
increase material durability.
Besides increasing durability, anodizing process is also useful to improve material
performance and can change desired material elements according to anodizing
process.
Anodizing process in this research used aluminum specimen with aluminum
content of 93.4037%. Three different voltages variations were conducted in the
process by using 0.2 Ampere power supply and phosphate acid electrolyte. After
anodized, the specimen was tested with phase content test and surface roughness
test. The surface roughness test result showed increasing result along with
increasing voltage. The results in orders for 9V, 12V, and 15V were respectively
0.4878, 0.5482, and 1.3868. The phase content test results obtained A1 value =
92.357% and A1P value = 7.643% for 9V; A1 value = 84.529% and A1P value =
15.471% for 12 V; and A1 value = 76.973% and A1P value = 23.027% for 15 V.
PENGARUH VARIASI VOLTASE PROSES ANODISASI PADA
ALUMINIUM TERHADAP KEKASARAN DAN KANDUNGAN
FASA
Oleh
M. Zanuardi. W
Skripsi
Sebagai Salah SatuSyaratUntukMencapaiGelar
SARJANA TEKNIK
Pada
JurusanTeknikMesin
FakultasTeknikUniversitas Lampung
FAKULTAS TEKNIK
UNIVERSITAS LAMPUNG
✡☛ ☞✌✍ ✌✎✏☛✑✒✓
✔✕✖✗ ✘✙
s
✚ ✙✘✛✜ ✙✢ ✛r
n
✚ ✙ ✣ ✛✖ ✚✛r
✤ ✛✥ ✦✗✖✧ ✦✛✚ ✛t
✛✖✧ ✧ ✛✘ ★✩ ✪ ✛✖✗ ✛r
✙ ★✫89
✬s
✕✭✛✧✛✙ ✛✖ ✛✢ ✢✕t
✙✧ ✛ ✚✛r
✙t
✙✧ ✛ ✭✕✛✗✚✛rs
✛✬r
✚✛r
✙ ✦✛s
✛✖✧ ✛✖ ✮✯ ✚✚✰✱y
✚✛✖✮✲ ✙✳✗✜✛✖t
✙✔✕✖ ✚✙✚ ✙✢ ✛✖ ✚ ✙ ✱ ✕✢ ✯✘✛✜ ✮✛
s
✛r
✴✘ ✵ ✶✛u
ts
✛r
✷✛✸✛✭✛s
✛ ✬ ✣ ✛✖✚ ✛r
✤ ✛✥✦✗✖✧ ✚✙s
✕✘✕s
✛✙✢✛✖ ✦✛✚ ✛t
✛✜✗✖ ✹✺✺★✬ ✱ ✕✢ ✯ ✘✛✜ ✻ ✕✖✕✖✧ ✛✜ ✔✕✛✥✛rt
✴✘ ✶✛u
ts
✛r
✷✛✸✛✭✛s
✛ ✣ ✛✖ ✚✛r
✤ ✛✥p
u
✖✧ ✚✙✕✘✕s
s
✛✙✢ ✛✖ ✦✛✚ ✛t
✛✜✗ ✖ ✹✺✺✼ ✬ ✱ ✕✢✯✘✛✜ ✻✕✖ ✕✖✧ ✛✜ ✴✘ ✵ ✶✛u
ts
✛r
✷✛✸✛✭✛s
✛ ✣✛✖✚ ✛r
✤ ✛✥ ✦✗ ✖✧ ✦✛✚ ✛t
✛✜✗ ✖ ✹✺ ✺ ✽✬ ✦ ✕✖✗✘✙s t
✕r
✚✛✾t
✛r s
✕✭✛✧✛✙✥✛✜✛
s
✙✲ ✛s
✿✕✢✖✙✢✻ ✕s
✙ ✖❀✛✢✗ ✘t
✛s
✿✕✢✖✙✢❁✖✙❂✕rs
✙t
✛s
✤ ✛✥ ✦✗ ✖✧✥✕✘✛✘✗✙ ✸✛✘u
r
✱ ✕✘✕✢❃✙ ✔✕✖ ✕r
✙✥ ✛✛✖✻ ✛✜ ✛s
✙s
✛✣✛ru
❄✱ ✔✻✣ ❅ ✰✱ ✕✘✛✥✛ ✢✗✘✙✛✜ ✦✕✖✗✘✙
s
✛✢ ❆✙✾ ✚ ✙ ❇ ✙✥ ✦✗ ✖ ✛✖ ✻✛✜✛✙s
✲ ✛s
✿✕✢✖✙✢ ✻ ✕s
✙✖ ❄❇ ✙✥✛t
✕✥❅ ❁✖ ✙❂✕rs
✙t
✛s
✤ ✛✥✦✗ ✖✧✚ ✙ ✭✙✚ ✛✖✧✔✕✖ ✕✘✙t
✙✛✖✚ ✛✖✔✕✖✧✕✥✭✛✖✧✛✖✰✱ ✕✘✛✙✖✙tu
✬✦✕✖✗ ✘✙s
✸✗✧ ✛ ✦ ✕r
✖✛✜ ✥ ✕✖✸✛✚✙✛✖✧ ✧o
t
✛ ❀✗ ✥o
r
✱ ✙✘✛tu
✛✜✥ ✙r
✚ ✛✖✱✗ ✚t
Is
y
✘✛✥ ❀✛✢ ✗ ✘✛t
s
✿✕✢✖ ✙✢(FOSSI
-FT).
Penulis melakukan Kerja Praktik di PT. Great Giant Pineapple, Lampung Tengah
pada bulan November sampai desember 2012 dengan judul Pemilihan Jenis Belt
Conveor pada Mesin Pengalengan PT. Great Giant Pineapple Terbanggi Besar
❈❉❊❋ ●❍
s m
❉❊■ ❏m
❑ ❍●▲ ▼ ❊◆ ❉n
tr
❏s
❍m
❏t
❏▲❋●❍❏❖P ❍●❍❖ ❏n
P❏◗ ❏❑❍◗❏■n
m
❏t
❉r
❍❏●◗ ❉❊■ ❏n
❘❋◗ ❋ ●s
▲❙❍
p
s
❍Pengaruh Variasi Voltase Pada Proses Anodisasi Aluminium Terhadap
Dengan Kerendahan hati
Dan
Segala usaha untuk mencapai impian
Ku persembahankan karya kecilku ini untuk
Ayahanda dan Ibunda
Atas segala doa, cinta dan kasih sayang yang tak
kan terbalaskan
Kakakku
Pemberi semangat dan nasehat
Keluarga Besar Penulis
Teman-teman seperjuangan penulis
❱
oto :
”
life isn t about finding yourself.
❲❳❨❩❳❬❳❨❳
❭❪❫❴ ❵❛❜ ❪❝❪❪❴❫❝❞❴ ❡ ❡❝❪
alamin,
puji syukur kehadirat Allah SWT yang telah
memberikan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan skripsi
ini. Shalawat serta salam juga disampaikan kepada Nabi Muhammad SAW yang akan
kita tunggu
syafa atnya di
yaumil akhir
nanti.
Skripsi dengan judul
Pengaruh Variasi Voltase Proses Anodisasi Pada Aluminium
Terhadap Kekasaran dan Kandungan Fasa
adalah sebagai salah satu syarat untuk
mencapai gelar Sarjana Teknik pada Jurusan Teknik Mesin Universitas Lampung.
Sebagai rasa syukur, penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Suharno, M.Sc., selaku Dekan Fakultas Teknik Universitas
Lampung;
2. Ibu Dr. Eng Shirley Savetlana, S.T., M.Met., selaku Ketua Jurusan Teknik Mesin
Universitas Lampung.
3. Harnowo Supriadi, S.T.,M.T., selaku pembimbing utama yang telah memberikan
bimbingan, pengetahuan, dan saran, serta nasehat selama proses penyelesaian
skripsi ini;
4. Bapak Gusri Akhyar, S.T,.M.T.,Ph.D., selaku pembimbing pendamping atas
kesediaanya untuk memberikan bimbingan, masukan, dan saran dalam proses
penyelesaian skripsi ini;
5. Bapak Zulhanif, S.T., M.T. selaku dosen Pembahas yang telah banyak sekali
6. Ir. Herry Wardono, M.Sc. Sinaga, S.T.,M.T.., selaku Pembimbing Akademik
yang telah memberikan banyak masukan dan motivasi dalam kegiatan akademik;
7. Novri Tanti, S.T, M.T., selaku Koordinator Tugas Akhir yang telah membantu
kelancaran skripsi ini;
8. Seluruh Dosen Jurusan Teknik Mesin atas ilmu yang telah diberikan selama
penulis melaksanakan studi, baik materi akademik maupun teladan dan motivasi
untuk masa yang akan datang;
9. Orang tua penulis (Bapak dan Ibu), yang telah memberikan banyak pengorbanan,
doa, kasih sayang, motivasi, semangat, harapan, materil dan spiritual, sehingga
penulis dapat merasa aman dan nyaman selama menjalani pendidikan dan
penyelesaian skripsi di Universitas Lampung;
10. Kakakku tersayang, Ari Widianto dan Aprilia.W atas doa, kasih sayang, motivasi
dan dukungan selama penulis menjalani pendidikan di Universitas Lampung;
11. Keluarga besar dan saudara-saudari penulis yang senantiasa memberikan doa,
motivasi dan dukungan;
12. Mas Marta dan Mas Nanang yang telah membantu baik dalam proses seminar;
13. Bapak Tito Prastyo R, M. Si., yang telah membantu dalam pengambilan data di
Nanotech Indonesia.
14. Rekan rekan Teknik Mesin angkatan 2007 yang telah memberikan semangat,
motivasi dan pandangan dalam penyelesaian skripsi ini, semoga kebersamaan ini
tetap terjaga hingga akhir hayat, salam
Solidarity Forever;
15. Rekan-rekan Alumni SMA Al-Kautsar yang selalu memberikan motifasi dan
semangat dalam menjalani perkuliahan di Universitas Lampung
16. Keluarga Besar Himpunan Mahasiswa Teknik Mesin Universitas Lampung;
17. Semua pihak yang tidak mungkin penulis sebutkan namanya satu persatu, yang
telah ikut serta membantu dalam penyelesaian skripsi ini.
Penulis menyadari bahwa dalam penulisan skripsi ini masih banyak kekurangan. Oleh
semua pihak. Penulis berharap skripsi ini dapat bermanfaat bagi semua yang
membaca dan bagi penulis sendiri. Amiin.
Bandar Lampung, 22 Desember 2014
Penulis,
♣ qrst r✉✈ ✇✈
①②③②④ ②⑤ ⑥⑦ ⑧⑨⑦⑩❶❷ ❶ ❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸ ♣ ⑥⑦ ⑧⑨⑦⑩❹⑦❺ ❻⑦⑩❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸ ♣❼ ⑥⑦ ⑧⑨⑦⑩⑨⑦❻❽ ❾❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❼♣
❶❿ ➀❽➁⑥⑦➂➃❾➃⑦➁
➄❸ ➅ ②➆ ②➇➈ ➉③②➊ ②⑤ ➋❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸➌ ➈❸ ➍➎ ➏➎②⑤➐➉⑤ ➉③♣➆♣②⑤❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸➑ ➒❸ ➈ ②➆ ②➓ ②
n
➔ ②➓ ②l
②h
❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸➑ →❸ ①ipo
➆e
➓②❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸➑ ➣❸ ↔i
➓➆em
②➆ik
②➐en
➎③i
➓ ②n
❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸4
❶ ❶❿ ⑨❶➁↕⑦➃⑦➁➀➃❷ ⑨⑦➙⑦
➄❸ ↔
ej
②➇ ②h
➄l
➎④ini
➎④❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸6
➈❸ ➄l
➎④ini
➎④d
②n p
②d
➎②nn
➛②❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸7
➒❸ ➣ ③ek
➆➇oli
➆❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸❸ ❸❸❸➌➜➡➢ ➤➥➦ ➧➨ ➧➩ ➧➫➧➦ ➭➯
(
➲➭➦➦➥➫ ➩➳➥➫➯ ➠➩ ➵)
➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➸ ➺ ➻ ➢ ➼➫ ➽ ➳➠➯ ➧➯ ➠➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➸ ➾ ➚➢ ➪➶ ➠➹➥ ➹➧➯ ➧➦ ➧➫➘➥➦ ➴ ➭➹ ➧➧➫➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ ➬ ➧➢ ➮➧(
➱✃ ❐❒ ❮❰ ÏÐÑÒ Ï➱ Ñ❒Ï✃Ó Ô❮ ÏÕÖ× ❐Ø ➱Ò Ï)
➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ ➺ Ù ➢ ➮z
(
ÔÏ❰ Ú✃Ø❰ÔÐ❮Ø❒❮✃ÓØ ➱ ➱Ï❒❐ÛÑ➱ØÔØ ÏÐ)
➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ ➺ ➲➢ ➮➴➧Ü(
ÝÑÞÐØÝ❐Ý❮ ÏØ❒ ❮Ô✃ÓÔ❮ÏÚ➱✃ÓØ ÛÏß à àààà àààà àààà àààà àààà àààà àààà àààà àààà àààà ààà➷ ➺d
➢ ➮ áânil
➧i
➧khi
➦➦ ➧➩ ➧ã➦ ➧➩ ➧➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ ➺ä➢ ➘
eng
➭➶i
➧n f
➧➯ ➧➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷åæ ææ çèé ê ëì ëí ëîæïé ðéíæ ê æ ñð
➼ ➢ ò➥➩
ode
➘eneli
➩i
➧n
➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷7
ó ➢V
➧➦i
➧Ù ➥l
➘eneli
➩i
➧n
➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ ô ➧➢V
➧➦i
➧Ù➥l
óe
Ù➧➯ ➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ ô Ù➢V
➧➦i
➧Ù➥l
õe
➦ik
➧➩ ➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ö ÷ ➢ øok
➧➯ ➠➘eng
➭➶i
➧n
➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷8
➡ ➢ ➼l
➧➩ó ➧n
ó➧h
➧n
➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➷ö ➻➢ ó➧h
➧n
➵➧ng dig
➭➫➧k
➧n
➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢ ➬➬ ➚ ➢ ➘➦o
➯➥d
➭➦➘eneli
➩i
➧n
➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢ ➬➺ ä➢ ➮➧n
➲➧ng
➧n
➘eneli
➩i
➧n
➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢ ➬ö ù➢ ➡i
➧g
➦➧m
➼li
➦ ➘eneli
➩i
➧n
➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢➢ ➢➢➢ ➬úæû
.
üñýæ íì ñðïéèþñüñýñð✁✂ ✄☎✆ ✝✞ ✟ ✠✆✡✠☛ ✠ ✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂ ☞☞
✌
.
✍✎ ✏✑✒✓ ✔✕✖ ✔✕✍ ✔✗✔✕A
✂ ✘☎☛✙✞✚✠m
n
✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂ ☞ ✛✁✂ ✜ ✠
r
✠n
✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂✂ ✂✂✂ ✢ ✣ ✖ ✔✤✥✔✗✑✒✍✥✔✦✔✧★ ✩✪★✫✪★✬ ✭ ✮
✯✰✱✰✲ ✰✳ ✪✴ ✵✶✷✸ ✹✰✺✻✰✼✽ ✾✼✿❀ ✰❁ ❂ ✰✳✰✱❂ ✲✿✳✿ ❂✲✻ ✾✲❀✰❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❄ ✪✴ ✵✶✷❅✹✰✺✻ ✰✼✽ ✾✼✿❀ ✰❁ ❂ ✰✳✰✱❂ ✲✿✳✿ ❂✲✻ ❂✰✳❆❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❇ ❈ ✪✴ ✵✶✷
3
❉❊✳ ✽ ✾✻ ✼✰✽✿❀✰❁ ❂ ✰✳❀ ✰❁✰✲ ✰✻ ✾✼✿ ✰✱❋✰✳❆❁✿❆❂✳✰●✰✳❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❇❍Tabel 4
■✿❀ ✾❏✳❊❁ ✿ ✽ ✰✽✿❑✾✼❁✰✽ ✰✼●✰✳✱✰ ✼❂✻ ✰✳ ✾✱✾●✻✼❊✱✿✻✳❋✰❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❇▲Tabel 5
✹✰✻ ✰▼✰✽✿ ✱❀✾✳❆❂◆✿ ✰✳●✾●✰✽ ✰✼✰✳❀ ✾✼ ✲❂●✰✰✳✰✱❂ ✲✿✳ ✿ ❂✲❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❃❃ ❃❃❖❇iv
◗❘❙❚ ❘❯❱ ❘❲❳ ❘❯
❨❩❬❩❭ ❩❪
❒❮❰ÏÐÑÒÓ ÔÕ ÔÒÐ
Ò
.
ÕÖ× ÖØÙ ÚÛ ÖÜÖÝÞß
lu
m in
iu
m
àág
âã äå än
æçè är
äl
â äæé åär
çã äm
çm
p
u
n
y
äi si
ê ät
sifat seperti
ringan, bercahaya, daya hantar listrik tinggi, dan mudah dipadukan dengan
unsur
unsur lain. Sifat lainnya yang dimanfaatkan sebagai pelindung adalah
mudah beroksidasi dengan oksigen pada udara terbuka dan membentuk lapisan
oksida yang tipis Al
2
O
3
yaitu ± 0,005
0,01 micron pada permukaannya, tetapi
lapisan tersebut belum dapat dikatakan sebagai pelindung yang protektif
karena terlalu tipis. Korosi pada aluminium terjadi karena adanya unsur lain
dalam aluminium seperti magnesium, silikon, besi, dan tembaga baik yang
berasal dari hasil pengolahan yang kurang sempurna maupun yang sengaja
ditambahkan untuk maksud
maksud tertentu. Pembentukan lapisan oksida
proses anodisasi pada aluminium diperkenalkan pada tahun 1846 M. Di Jepang
baru dikenal pada tahun 1923 dan dikembangkan dengan adanya proses
ë ìí îïðñpada tahun 1929 dengan tujuan meningkatkan kekuatan terhadap karat.
Ditinjau dari pemakaian dan kegunaannya, proses anodisasi secara garis besar
dapat dibagi menjadi dua macam yaitu untuk keperluan dekoratif dan untuk
keperluan protektif. Untuk yang bersifat dekoratif harus tahan warna (
òó ôõö2
penggunaan elektrolit H
3
PO
4
(asam pospat) dengan tegangan listrik yang tepat,
diharapkan proses ini menghasilkan sifat fisik dan mekanis pada aluminium
paduan yang optimal. Untuk mencapai hasil yang diharapkan, perlu dilakukan
penelitian pada proses anodisasi sehingga hasil penelitian ini dapat digunakan
sebagai acuan oleh dunia industri di Indonesia dalam membuat produk dengan
kualitas yang lebih baik
Metoda yang selama ini biasa digunakan untuk meningkatkan kekerasan
permukaan dan daya tahan aluminium terhadap korosi adalah dengan metode
anodisasi. Anodisasi merupakan proses pembentukan lapisan oksida secara
elektrolit dengan cara menempatkan benda kerja sebagai anoda dalam larutan
elektrolit. Trethewey dan J.Chamberlain (1993) melaporkan bahwa anodisasi
dapat digunakan untuk meningkatkan daya tahan aluminium dan paduannya
terhadap korosi. Proses anodasi menghasilkan lapisan yang keras, kuat dan
juga dapat meningkatkan
þÿ ✁✂ ✄sehingga lapisan yang ditempelkan pada
permukaannya akan menempel lebih kuat.
Proses anodisasi dipengaruhi beberapa faktor seperti suhu, kerapatan arus,
temperatur,
☎✆ ✝✞þ✂ ✁, waktu proses dan lain-lain sehingga untuk menghasilkan
produk yang diinginkan beberapa faktor tersebut harus dikendalikan.
Berdasarkan uraian di atas maka penulis ingin melakukan penelitian mengenai
pengaruh
☎✆ ✝ ✞þ✂ ✁pada proses anodisasi pada aluminium terhadap kekerasan
3
✟
.
✠ ✡juan Penelitian
Adapun tujuan dari penelitian ini adalah untuk mengetahui pengaruh voltase
pada proses anodisasi terhadap kekasaran dan fasa yang terbentuk.
C. Batasan Masalah
Batasan masalah diberikan agar pembahasan dari hasil yang didapatkan lebih
terarah. Adapun batasan masalah yang diberikan pada penelitian ini, yaitu :
a. Material yang digunakan adalah aluminium 93,4037 %
b.
Elektrolit yang digunakan adalah campuran asam phospat (H
3
PO
4
) dan
air.
D. Hipotesa
Adapun yang menjadi hipotesa dalam penelitian ini adalah adalah sebagai
berikut :
a. Akan ada peningkatan kekasaran aluminium seiring dengan meningkatnya
voltase pada proses anodising.
4
☛
.
☞✌✍ ✎✏✑✒ ✎ ✌✓✒✔ ✏✕✖✗ ✌✍✒ ✕Adapun sistematika penulisan dari penelitian ini adalah:
BAB I PENDAHULUAN
Terdiri dari latar belakang, tujuan, batasan masalah, hipotesa, dan sistematika
penulisan dari penelitian ini.
BAB II TINJAUAN PUSTAKA
Berisikan tentang penjelasan alumunium, proses anodisasi, Curent Density
(kerapatan arus), pembentukan lapisan oksida, pengaruh voltase listrik, uji
kekasaran, uji fasa.
BAB III METODE PENELITIAN
Berisi beberapa tahapan persiapan yang membahas tentang peralatan yang
digunakan , tahapan persiapan sebelum pengujian, serta proses pre-treatment
spesimen sebelum dilakukan proses anodisasi, kemudian membahas mengenai
prosedur pengujian, dan diagram alir pengujian.
BAB IV HASIL DAN PEMBAHASAN
5
BAB V SIMPULAN DAN SARAN
Berisikan hal-hal yang dapat disimpulkan dan saran-saran yang ingin
disampaikan dari penelitian ini.
6
✘ ✘✙✚ ✘✛✜ ✢✣✢✛✤ ✣✥ ✚✢✦ ✢
✢✙ ✥✧★ ✩✪ ✩✫✢✬
u
m
✭n
✭u
m
✮✯✰ ✱✲✳✲✰✱ ✱✴✰ ✵ ✶✷ ✶✳
r
✯ ✸✹ ✶✱t
✴r
✺ ✶✳✶✷y
✻✲ ✻✰ ✳✲ ✶ ✻✶✳ ✱✴✰✵✶✷✶r
✳ ✰✳su
r
✷✴✲✹✶t
t
✴✺ ✶✳r
✶✷y
s
✴t
✴✯ ✶✼ ✸ ✷✽✲✹ ✴✳ ✻✶✳ ✽✲✯✲ ✷✸✳✾✶✯✰ ✱✲✳✲✰✱ ✻✴✳ ✹ ✶✳ ✷ ✶✳ ✻✰✳ ✹ ✶✳ ✽✴✺ ✶✳y
✶✷✿ ❀ ✻ ✶✲r
✷✰ ✯✲t
✺✰ ✱✲✾ ✻✲t
✴✱✰✷✶✳ ✷✲✶r
❁ ✷✲✶r
✽✴✷✲t
✶r
❂❃ ❄t
✶✼✰✳✶✳ ✹y
✯ ✶✯u
✻✶✳ ✱✰ ✯ ✶✲✻✲✵❅✸ ✻✰✷✽✲✽✷ ✶✯ ✶✲✳ ✻✰✽ ❆✲r
✽✴✷✲t
✶r
❇❄❆✶✼✰ ✳y
✶✳ ✹✯ ✶✯✰❈ ❉✴✲ ✷✰❆r
s
✴❊✶r
✶✼ ✵ ✴r
✷ ✴✱✺ ✶✳ ✹ ✶✳❆✴✳❆✶✳ ✹✵ ✴✳✴✱✰✶✳ ✶✯✰ ✱✲✳✲✰ ✱✾✶✲y
tu
❋✶❈ ●✶✻✶
t
✶✼✰ ✳ ❂❍✿■ ✾ ✽✴✸❅✶✳ ✹ ✲✯ ✱u
w
✶✳ ●r
✶✳❏✲s
✺✴✳r
✶✱✶ ❑✶▲✸✲✽✴r t
✴✯ ✶✼ ✱✴✳✻✰ ✹ ✶✺✶✼▼ ✶✶✯✰ ✱✲✳✲✰✱✱✴✰ ✵ ✶✷ ✶✳r
✯ ✸✹ ✶✱y
✶ ✳ ✹t
✴r
✷✶✳✻✰ ✳✹ ✻✲ ✻✶✯ ✶✱ ✶✯✰ ✱✲✳ ✶❈✺❈ ●✶✻✶
t
✶✼✰ ✳ ❂✿ ❄❍ ✾ ✶✼✯✲ ✷✲ ✱✲ ✶ ◆✳✹ ✹✲r
s
✺✴✳✶✱✶r
❖✰ ✱✵✼❅✴y
P✶v
y
✺ ✴✼✶✽✲✯r
✱✴✱✲✽✶✼✷ ✶✳ ✶✯✰ ✱✲✳ ✶s
✴❏✶r
✶ ✴✯ ✴✷❆✸ ✷✲ ✱✲ ✶r
✯ ✸✹ ✶✱ ✻ ✶✳y
✶✳ ✹ ✻✲✵ ✴r
✸✯ ✴✼ ✻ ✶✲r
✵✴✳✹u
❊✲ ✶✳❆✴r
✽✴✺✰❆✶✻✶✯ ✶✼✶✯✰✱✲✳ ✲✰ ✱❈❏❈ ●✶✻✶
t
✶✼✰ ✳ ❂✿■❂✾ ✺✲❊✲ ✽✰✱✺ ✴r
✶✯✰ ✱✲✳✲✰✱ ✻✲t
✴✱✰ ✷ ✶✳ ✻✲ ●r
✶✳❏✲s
◗✴✯ ✶t
✶✳✾t
✴✵✶
t
✳y
✶✻✲✷ ✸❆✶❑✴✽✺ ✶u
x, yang dinamakan bauksit
.
d. Pada tahun 1825, ahli kimia Denmark, Orsted berhasil memisahkan
aluminium dengan cara memanaskan aluminium chloride dengan kalium
amalgam dan kemudian memisahkan merkuri dengan cara destilasi.
e. Pada tahun 1886, mahasiswa Oberlin College di Ohio, Amerika Serikat
7
❘❙❚ ❯❱❲ ❘
(
❳❙❨ ❩❬)
❭ ❘❙ ❘❯ ❙❪❙❪❫ ❘❲ ❴❙❱❵ ❛❱t (
❜❘❬❳❙❝❞)
❡ ❘❭❘t
❪ ❯❡❪❘r
tu
r
❢❞ ❣ ❩❤ ❭ ❘❙ ❘❯ ✐❪❲❥❚ ❴ ❴❵❥❘❴y
❘❲❦ ❭ ❱❙ ❘❡❱❧❱ ❙❵❦❘❯ ❴❘✐❵❲r
❭ ❘❲ ❴❪ ❯❚❭ ❱ ❘❲ ❯❪❙❪w
❘t
❴ ❘❲ ❘s
ru
❙❱str
❱ ❴ ❯❪❙ ❘❙❚ ❱r
❚ ❘❲❦ ❪t
r
❧❪✐❚❥♠ ❤❘r
❘ ❱❲ ❱ ❭ ❱ ❴❪❲❘❙ ❭ ❪❲❦❘❲ ❡❛❵❧❪s
♥❘❙❙ ♥❪❵❚ ❙r
t
♦ ❴ ❘❪❲ ❘r
❱❲❱t
❪r
♣❘❭ ❱ ❡❘❭❘t
❘❫❚ ❲y
❘❲❦s
❘❯❘ ❭ ❪❲❦❘❲ ❧❪❵ ❛❘❲❦qr
❘❲ r❱s y
❘❲❦✐❪r
❲ ❘❯ ❘q ❘❚ ❙♥❪r
❵❚ ❙t
♠s♠ q ❘❭ ❘
t
❘❫ ❚❲ t ✉ ✉✉♦ ❘❫❙❱ ❴❱❯❱ ❘✈❪r
❯ ❘❲ ✇❘r
❙s ✈❵❧❪s ①❘❪y
❲r
❯❪❲ ❪ ❯❚❴❘❲ r ❘r
❘ ❯❪ ❯❡❪❵ ❙❪❫r
❘❙❚❯❱❲ ❘ ❭ ❘r
❱ ✐❘❚ ❴❧❱t
❧❪r ❘r
❘❡❪❙ ❘ru
t
❘❲ ❴❱ ❯❱ ❘♠ ②❘❯❡ ❘❱ ❧❘❘t
❱❲ ❱ r ❘r
❘ ①❘❪y
r
❯ ❘❧❱❫ ❭❱❦u
❲ ❘❴ ❘❲ ❚ ❲❥❚❴ ❯❪ ❯❡ ❛❵ ❭❚❴❧❱ ❘❙❚❯❱❲ ❘ ❭❘❱r
✐❘❚ ❴❧❱t
❧❪r ❘r
❘❱❲ ❭❚❧❥ry
❭❘❲❭❱❧❪✐u
t
❭❪❲❦❘❲ ❡❛❵❧❪s
①❘❪y
♠r
(
③❘④❱❧♦ ✈r
♦t❢❢❬)
♠⑤⑥⑦⑧⑨⑩❶❷❶ ⑨⑩❸❹❷❺❹ ❸ ⑨❹❷❷ ❻❹
❳❙❚ ❯❱❲❱❚❯ ❘❭ ❘❙ ❘❫ ❙❵❦❘❯
y
❘❲❦r
❱❲❦❘❲ ❭ ❘❲ r❚❴❚❡ ❡ ❪❲❥❱❲❦ ❭❘❙ ❘❯ ❴❪❫❱❭ ❚❡❘❲ ❯❘❲ ❚❧❱ ❘♠ ❳❙❚❯❱❲ ❱❚ ❯ ❯❪❚❡❘❴❘❲r
❚❲❧❚r
❴❱ ❯❱ ❘ ❦❵ ❙❵❲❦❘❲ ❼❼❼❳ ❭ ❘❙ ❘❯ ❧❱❱ ❯st
❡❪❱❵ ❭❱ ❴r
❚❲❧❚ ❛♦ ❭❪❲❦❘❲❲ ❵ ❯❵ ❛ ❘t
❵ ❯t❬❭❘❲ ✐❪❘r
t
❘t
❵❯❨ ❞♦❢✉ ❦r
❘❯❡❪r
❯❵ ❙ ♠ ③❱ ❭ ❘❙ ❘❯ ❚ ❭ ❘r
❘ ✐❪✐❘s
❘❙u
❯❱❲❱❚❯ ❯❚❭❘❫t
❪r
❵ ❴❧❱❭❘❧❱ ❯❪ ❯✐❪❲❥❚❴ ❙❘❡ ❱❧❘❲t
❱❡❱s
❵ ❴❧❱❭❘(
❳❙❽ ❩
❾
) y
❘❲❦
t
❘❫❘❲ ❪t
❫❘❭ ❘❡r
❴❵ ❛❵❧❱♠ ❳❙u
❯❱❲ ❱❚ ❯ ♣❚❦❘ ✐❪r
❧❱s❘t
❘❯s❵❥❪r
y
❘❲❦ ❯❘❯❡❚ ✐❪❪ ❘❴❧❱
r
❭❪❲❦❘❲ ❙ ❘ru
t
❘❲ ❘❧❘❯ ❯ ❘u
❡❚ ❲ ✐❘❧❘♠(
❳❲❥❵ ❲ ✈♠ ♥❘❵❲ ❵♦rt
t❢ ❢❨)
♠ ❳❙❚❯❱❲ ❱❚ ❯ ❯❪❚❡❘❴❘❲r
❙❵❦❘❯r
❱❲❦❘❲ ❘❲❦y
❯❪ ❯❡❚ ❲❘❱y
❴❪t
❘❫ ❘❲❘❲ ❴❵❛❵❧❱y
❘❲❦ ✐❘❱ ❴ ❭❘❲ ❫❘❲❥❘r
❘❲ ❙❱❱ ❴str
y
❘❲❦ ✐❘❱❴ ❭❘❲ ❧❱s❘t
❧❱s❘t y
❘❲❦ ✐❘❱ ❴ ❙ ❘❱❲❲y
❘s
❪✐❘❦❘❱❧❱s❘t
❙❵❦❘❯♠(
②❭ ❱ ❘♦u
r
❿♠❨ ❣❣ ➀)
♠❳❙❚ ❯❱❲❱❚❯
(
❳❙)
❯❪ ❯❡❚ ❲❘❱y
❯ ❘❧ ❧❘ ❘❵ ❯t
❨ ➁(
❫❘❲y
❘ ❘❭ ❘ ❧❘tu
❱❧❵❥❵❡ ❲ ❘tu
r
❘❙)
♦ ❲❵❯❵❛ ❘t
❵ ❯ t❬♦ ❭❪❲❧❱t
❘s
❨♦➁❢ ❦/cm, titik lebur 660,4
o
C, dan titik didih
8
r
➂ ➃➄ ➅➆➇➈➉➊ ➊➋➉➌ ➍➎➏➐➑ ➏➐➄ ➅➆ ➍➃➏➆ ➍
+3, dan jari-jari atom yang kecil yaitu 57 pm
untuk stabilitas dari senyawa aluminium. Aluminium adalah logam hidrolisis
kuat dan umumnya tidak larut dalam keadaan pH netral antara (6,0
8,0),
dibawah asam (pH < 6,0) atau alkali (pH > 8,0), dan dalam larutan anorganik
atau ligan organik.
kelarutan Al
3+
meningkat. Reaksi jenis ini meningkatkan
jumlah Al
3+
dalam keadaan encer. Berikut ion yang dibentuk dalam larutan
aluminium hidroksida pada pH dibawah 5,5 : Al(OH)
2+
, Al(OH)
2+
dan Al
3+
.
Aluminium tidak stabil dalam proses oksidasi. Dalam keadaan berhubungan
dengan udara aluminium membentuk lapisan tipis oksida di atas permukaan serta
membentuk lapisan pelindung yang tahan terhadap korosi. Aluminium oksida
membentuk dua bentuk isomer
Al
2
O
3
dan
Al
2
O
3
. (Seiler,1994).
Berdasarkan metode peleburannya, paduan aluminium dikelompokkan
menjadi dua kelompok utama yaitu paduan tempa
(wro
t
u
g
h
) dan paduan
tuang (
➒➓stin
g
). Jenis paduan aluminium saat ini sangat banyak dan tidak
menutup kemungkinan ditemukannya lagi jenis paduan aluminium baru,
oleh karena itu dibuatlah sistem penamaan sesuai dengan komposisi dan
karakteristik
paduan
aluminium
tersebut
untuk
memudahkan
pengklasifikasiannya. Salah satu penamaan paduan aluminium adalah
dengan standar AA pada table 1.
Pada aluminium tempa, seri 1xxx digunakan untuk aluminium.
Digit kedua dari seri tersebut menunjukkan komposisi aluminium dengan limit
pengotor alamiahnya, sedangkan dua digit terakhir menunjukkan
persentase minimum dari aluminium tsb. Digit pertama pada seri 2xxx
9
➔ →➔ ➣↔➣↕ ➣➙ →➛ →➜
r
➝➛ →t
↕➞➔ ➙➞s
➣➣s
t
→➟ →➛➝r
r
➠➝ ↔➝➔➙➝➠ ➡➝ ➜➢➤➝➟→↔➥➢➦➝ ➧➝
t
r s
→r
➣➙➝➠ ➡➝ ➜➝ ↔u
➔ ➣➜➣➔u
t
→➔➙➝ ➨➞ ➢➩→r
➣ ➫➞➔ ➙➞s
➣s
➣➭➝➠u
➝➜ ➥xxx
Aluminium murni
2xxx
Paduan aluminium
tembaga
3xxx
Paduan aluminium
mangan
4xxx
Paduan aluminium
silicon
5xxx
Paduan aluminium
magnesium
6xxx
Paduan aluminium - magnesium
silicon
7xxx
Paduan aluminium
seng
8xxx
Paduan aluminium - timah
litium
9xxx
Disiapkan untuk penggunaan di masa depan
Digit kedua menunjukkan modifikasi dari unsur paduannya, jika digit
kedua bernilai 0 maka paduan tersebut murni terdiri dari aluminium dan unsur
paduan. Jika nilainya 1 - 9, maka paduan tersebut memiliki modifikasi
dengan unsur lainnya. Dua angka terakhir untuk seri 2xxx - 8xxx tidak
memiliki arti khusus, hanya untuk membedakan paduan aluminium tersebut.
Paduan aluminium tuang penamaannya memakai sistem tiga digit diikuti
dengan satu bilangan desimal. Tabel 2 menunjukkan seri paduan aluminium
10
➯➲➳➵➸➺➻➼➲➽
t
➲r s
➵➾r
➚➲➪➶➲ ➹➲➸➘➾ ➹➾u
u
➘t
➶➲ ➹➴ ➷➬➻➮➵➾r
➱➬➘ ➚➬➾s
➾s
✃➲➪➲ ➹u
❐xx.x
Aluminium murni
2xx.x
Paduan aluminium - tembaga
3xx.x
Paduan aluminium - silikon
tembaga/magnesium
4xx.x
Paduan aluminium - silicon
5xx.x
Paduan aluminium - magnesium
6xx.x
Tidak digunakan
7xx.x
Paduan aluminium - seng
8xx.x
Paduan aluminium - timah
9xx.x
Belum digunakan
Dalam standar AA, angka pertama menunjukkan kelompok paduan. Jadi, untuk
paduan Al-Si dinyatakan dengan angka 4xx.x, angka kedua dan ketiga
menunjukkan kemurnian minimum untuk aluminium tanpa paduan dan sebagai
nomor identifikasi untuk paduan tersebut (Zulaina Sari Rahmawati, FT UI,
11
12
❒❮❰❮Ï Ð
t
Ñ Ð❮r
Ò ÐÓ Ô Ðr
ÕÖ ÑÐ× Ðt
Ñ ❮❰❮ ÐÏÐt
ÔÐÏ Ø Ð Ó Ðt
Ù❮ Ð❰r
y
ÐÚ Ò Ñ❮ ÛÜ❮Ý ÐÚ ÐÑ Ð❰ ÐÏ Ð❰ ÛÓ ❮ Ú❮ ÛÓÑÙÚÒ ÐÚÚ❮❰ Ð❮ÝÐÚÑÛÚ ÒÐÚÞÙÔÐ ÒÐ❮Ô Ùr
❮Ýu
t
ßà ÐÔ Ù❰á âÝ ã ÚÞÙÚ
tr
ÐÞ❮×ÐÑÛÐÚ×ÐÑ ÐÓÐt
Ù❮ Ð❰r
y
ÐÚ ÒÑ ❮ ÒÛ ÚÐÝÐÚKONSENTRASI PADUAN
C
O
Si
AL
1,0549
4,4820
1,0595
93,4037
❒❮❰❮Ï Ð
t
ÑÐr
❮ÑÐt
ÐÑ❮ Ðt
Ðs
Ý ÐÚÑ Û ÚÒ ÐÚÝ ãÞÙÚäÐÞ❮r
Ó Ðt
Ù❮ Ð❰r
× ÐÑÐ× ÙÚ Ù❰❮❮ ÐÚt
❮ Ú❮y
Ð❮tu
åá Öæ çáè%
ÓÐÝ ÐÓÐt
Ù❮ Ð❰r
y
ÐÚÒÑ❮ÒÛÚ ÐÝÐÚÛ Úä ÛÝ× ÙÚ ÒÛÜ❮ ÐÚ❮ Ú❮ ÐÑÐ❰ ÐÏÐ❰ ÛÓ ❮ Ú❮ ÛÓ â
éê
E
ëìíîëïtr
t
ð❰ ÙÝä
r
ã❰❮t
ÐÑ Ð❰ ÐÏÝ ãÓ×ãÞ❮Þ❮ Ý❮Ó ❮ Ðy
ÐÚÒÐÝÐÚt
Ù×❮ÞÐÏr
Ó ÙÚÜÐÑ ❮❮ ãÚ ñ❮ ãÚ Ð× ÐÔ❮❰ Ð Ñ❮❰ ÐÝÐÚt
ru
ÑÐ❰ ÐÓ ×Ù❰ ÐÖru
t
ÏÐÞ❮❰ Ñ Ð❮r
×ÙÓ❮ÞÐÏ ÐÚ ❮ Ú❮ Ô Ùr
Û×Ð ❮ ã Ú ñ❮ ã Ú Ð ÚÒy
Ó ÙÚÜ ÐÑ❮×ÙÚÒÏ ÐÚä Ðr
❰❮str
❮Ý âòÛ Ú ÒÞ❮ÑÐ❮r
❰ ÐÐÚru
t
Ù❰ ÙÝ är
ã❰❮t
Ñ ❮Þ❮ Ú❮ ÐÑ Ð❰ ÐÏÞÙÔ ÐÒ Ð❮× ÙÚ ÒÏÐÚä Ð
r
Ðru
s
Ñ ÐÚ×ÙÚÐÓÔÐ Ï❮ ãÚ ❰ ã ÒÐÓ ×Ù❰ Ð×❮Þâ❒ Ðy
ÐÏ ÐÚä Ðr
❰❮❮Ýstr
❰ Ðru
t
ÐÚ Ù❰ ÙÝär
ã❰❮t
Ô Ùr
ÒÐÚä ÛÚ Ò × ÐÑ Ð Ü ÙÚ❮s
ÑÐÚ Ý ã ÚÞÙÚäÐÞ❮ Úr
y
Ðâ ó Ðô ÐÓ ñ Ó Ðô ÐÓ ❰ Ðru
t
ÐÚ Ù❰ ÙÝär
ã❰❮t
ÐÑ Ð❰ ÐÏÑ ❮ ÐÚä Ðr
ÐÚy
Ð❰ Ðru
t
ÐÚÐs
ÐÓ ÖÔ ÐÞÐÑ ÐÚÒÐÐÓâr
Ðâ ð❰ ÙÝä
r
ã❰❮t
õÞÐÓ(
ö÷i
øùú÷l
útro
lyt
)
ð❰ ÙÝ ä
r
ã❰❮t
ÐÞÐÓ ÐÑÐ❰ ÐÏ Ù❰ ÙÝär
ã❰❮t y
ÐÚ Ò Ô❮❰ Ð Ñ ❮❰ ÐÝ ÐÚru
t
ÑÐ❰ ÐÓ Ð❮r
ÐÝ ÐÚ Ó Ù❰ Ù×Ðs
❮ ãÚ(
û+
). Elektrolit-elektrolit asam tersebut bila dilarutkan dalam
pelarut (biasanya adalah air) maka akan terurai menjadi ion H
+
, contoh
elektrolit asam diantaranya adalah asam sulfat (H
2
SO
4
), asam fosfat
13
üý üþ ÿ
r
ý✁t
✂✄ ✂☎ ✆ ✂✝ ✂t
✆ ✁✞ ✂✟✁t
✁ ✟✂✠ ✂✁y
tu
✂✄ ✂☎ ✡tik
ro
m
p
o
n
o
✂✄✂☎ ☛☞p
ro
tik
✠ ✆✂✌✂✄ ✂☎trip
o
tik
✍✎✍ ✏✄ ✂☎
m
o
n
o
p
ro
tik
✏✄✂☎
tik
m
o
n
o
p
ro
✂✆ ✂ý ✂✑ ✂✄✂☎y
✂✌✟ ✑ ✂✌✂y
☎ ü☎ ✁ý✁þ✁ ✄ ✂tu
✁ ✌ ✒+
di
dalam elektrolit. Contoh dari asam monoprotik adalah HNO
3.
HNO
3
H
+
+ NO
3-
(1)
2.
Asam
☛☞p
ro
tik
Asam
☛☞p
ro
tik
adalah asam yang memiliki dua ion H
+
di dalam
elektrolit. Contoh dari asam diprotik adalah H
2
SO
4
dan C
2
H
2
O
4
.
Asam sulfat (su
✓lp
h
u
ri
✔✓i
☛)
Asam sulfat (H
2
SO
4
) merupakan asam yang paling sering digunakan dalam
proses anodisasi. Molekul dari asam sulfat terdiri dari dua atom hidrogen,
satu atom belerang dan empat atom oksigen.
Asam oksalat (o
x
✔✕✓i
✔✓i
☛)
Asam oksalat adalah senyawa kimia yang memiliki rumus H
2
C
2
O
4
dengan nama sistematis asam etanadioat. Asam dikarboksilat paling
sederhana ini biasa digambarkan dengan rumus HOOC-COOH.
(COOH)
2
2e
-
+ 2CO
2
+ 2H
+
(2)
3. Asam
trip
ro
tik
Asam
trip
ro
tik
adalah asam yang memiliki tiga ion H
+
di dalam
elektrolit. Contoh dari asam triprotik adalah asam phospat (H
3
PO
4
).
14
✙✚ ✛✜✛✢ ✣ ✜✣✤ ✥
r
✦ ✜✧t y
✛★ ✩ ✪ ✧✜✛ ✚ ✧ ✜✛✤ ✛★t
ru
✚ ✛✜✛✫ ✛✧r
✛✤ ✛★ ✫✣ ✜✣ ✬ ✛s
✧ ✦★(
✭✮✯
)
✰ ✱✦★✥✦✢ ✚ ✛✧r
✣ ✜✣✤ ✥r
✦ ✜✧t
✛✜✤ ✛✜✧ ✛✚✛✜✛✢ ✲✛✭✮(
✳ ✴ ✵✶ ✷i
✸ ✶ ✹✺✴)
✛✬ ✛✪✧ ✜✛ ✚ ✧✜✛✤✛★ru
t
✚ ✛✜✛✫✛✧r
✫✛✤✛t
✣ru
r
✛✧✫✣★ ✻ ✛✚✧✧ ✦★✲✛+
dan ion OH
-
.
c.
Elektrolit garam (
✶ ✴✼ts
✽l
✽✸tro
lyt
✽)
Adalah elektrolit yang bila dilarutkan dalam air akan terbentuk ion
ion selain
H
+
dan ion OH
-
. Contoh elektrolit garam adalah natrium klorida (NaCl). Apabila
dilarutkan dalam air maka akan terurai menjadi ion Na
+
dan ion Cl
-
.
✾✿❀❁
u
rr
n
t
✾❁n
❂❃ty
❄❅❁r
❆❇ ❆❈ ❆❉❆❊u
s
❋❃❃ ❅str
)
Arus listrik adalah pergerakan muatan-muatan listrik. Sebenarnya yang
bergerak adalah elektron-elektron dalam sebuah penghantar, tapi dalam
prakteknya digunakan asumsi arus listrik adalah pergerakan muatan listrik dari
positif (+) ke negatif (-). Tegangan listrik adalah beda potensial antara kutub
positif (+) dan negatif (-). Jika antara dua titik, diberi tegangan atau dibuat beda
potensial maka akan mengalirlah arus listrik dari yang memiliki potensial lebih
positif ke arah yang lebih negatif. Jadi intinya adalah arus listrik akan timbul
jika ada tegangan listrik.
Ada dua jenis arus dan tegangan listrik secara garis besar yaitu arus/tegangan
DC (Di
●✽ct Current
atau arus searah) dan arus/tegangan AC (
Alternating
Current
atau arus bolak-balik). Arus DC mengalir dari positif ke negatif secara
berkelanjutan (tetap). Sedangkan arus AC mengalir secara bolak-balik dari
positif ke negatif dan sebaliknya dengan frekuensi tertentu, makanya pada
15
❍ ■
r
❏❍ ❑▲ ▼ ❑◆ ❑❖ Pr
■◗ ❏■❘❙ ❚t
■rt
■❘❯❏❱ ❲ ❑y
❑ ▼ ❑◆❑❖ P❚❙ ❚ ◗❑ ❑▼ ❑◆ ❑▲ ◆ ❑❳u
■❘ ■r
❨❚y
❑❘ ❨ ▼❚ ▲ ❑❘❯❑r
◗ ❑❘ ❑t
❑u
◗ ■❳ ❑r
y
❑❘❨ ▼❚◆ ❑◗ ❏◗ ❑❘ ❩■r
❙ ❑t
❏❑❘w
❑◗❯❏❱ ❬❑t
❏❑❘ ❑ru
s
◆❚str
❚ ◗ ❑▼❑◆ ❑▲❭❪❫❪m
p
❑❘ ❨y
▼❚ ❑❚ ◗ ❑❘rt
❍ ❑❘❑◗ ❘y
❑y
❖ ❏ ❑t
❑❘(
▼❴) y
❑ ❘❨❖ ■❘ ❨ ❑◆❚r
❩■r s
❑t
❏❑❘w
❑◗❯u
(
▼ ❯)
❱❵❛ ❵❜
i
ik
couloumb
Ampere
❝❞ ❡ ❢ ❢
❣
ru
s
❤❑❖❩■r
■▼ ❑❩❑t
▼❚ ❑❚ ◗ ❑❘rt
❳ ❏ ❨❑✐elektron
couloumb
x
ik
couloumb
/
19
10
6
,
1
det
/
1
= 6,3 x 10
18
e
lektron/detik.
Hukum
Ohm s
: V = i.R
(3)
P =
t
W
W = V.i.t = i.R.i.t
(4)
P =
t
t
i
V
.
.
=
t
t
i
R
i
.
.
.
= V.i = i
2
.R
(5)
keterangan :
V = tegangan listrik atau beda potensial (
Voltase
)
R = hambatan (
ohm
)
W = energi atau usaha (
joule
)
P = daya (
watt
)
t = waktu (detik)
Current density
atau kerapatan arus adalah arus yang mengalir per satuan luas
permukaan. Satuan
current density
adalah A/dm
2
. Dengan rumus berikut :
CD =
A
i
(6)
keterangan : CD =
current density
(A/dm
2
)
16
❥❦
lu
as p
erm
u
k
aan
sp
esim
en
(
❧ ♠♥
)
♦♣ qr
o
d
st ✉t s✈
r
✇ ①②s
③④✇ ❧ ⑤①③ ① ⑤ ③❧ ③⑥③⑦ ⑧⑨✇ ①②s
⑧② ♠⑩②④ ❶❷❸③④ ⑥③ ⑧⑤①③④ ✇ ❸ ① ⑤❧③ ⑧③❧③⑥✇❹③♠ ❧②④❹③④ ❺③③
r
⑩ ②
r
②③❸ ① ⑤❸ ③④ ③③t
u
♠②④ ❹❸✇ ⑨✇①⑤❸ ③④ ① ❷③tu
⑥✇ ❹③ ♠
t
②ru
t
③ ♠③ ③⑥ ❷♠ ⑤④ ⑤❷ ♠ ❧ ②④ ❹③④ ✇ ❸ ① ⑤❹②④(
❻♥
) y
③④❹ ❧⑤③ ♠⑩⑤⑥ ❧ ③
r
⑤⑥③③④
ru
t
②⑥②❸ ❶✇ ⑥ ⑤r
t y
③④❹ ❧ ⑤❹❷④③❸ ③④ ①②⑩ ③ ❹③ ⑤♠②❧ ⑤③❼ ①②⑦ ⑤④❹❹③
t
②⑩ ②④❶ ❷❸r
⑥③ ⑧⑤①③④✇ ❸ ① ⑤❧③❽ ✈✇①②r
s
⑤④ ⑤❾❷❹③ ❧ ⑤①②⑩ ❷❶ ①②⑩③❹③ ⑤ ❿➀ ➁➂ ➃
c oxidation
y
③④ ❹ ⑧⑨⑤④ ① ⑤⑧④③y
⑦ ③ ♠⑧ ⑤r
①③ ♠③ ❧②④❹③④ ⑧⑨ ✇ ①②s
⑧②⑥③ ⑧ ⑤①③④ ❧ ②④ ❹③④❺③③r
⑥ ⑤str
⑤❸(
elektroplating
)
❼t
②t
③ ⑧ ⑤⑩ ②❧③④③y
⑥✇ ❹③ ♠
y
③④❹③❸ ③④ ❧ ⑤✇ ❸ ① ⑤❧③ ① ⑤ ❧⑤t
② ♠⑧③t
❸③④ ①②⑩ ③ ❹③ ⑤ ③④✇ ❧③ ❧⑤ ❧ ③⑥③ ♠ ⑥③③④ru
t
②⑥②❸❶✇⑥ ⑤r
t
❽ ✈②r
⑩②❧ ③③④ ⑥③ ⑤④ ⑥③③④ru
t
②⑥②❸❶✇⑥ ⑤r
t y
③④ ❹ ❧⑤❹❷④③❸ ③④ ⑩②① ⑤➄③r
t
③ ①③ ♠ ❧ ②④❹③④ ⑧②④②③y
③⑦r
③ru
s
⑩②rt
⑤⑧②(
➅➆)
❧ ③④ ③ ♠⑧②②r
t
⑤④ ❹ ❹⑤❽ ✈r
✇①②s u
t
③ ♠③❼ ❧③⑥③ ♠ ✇ ❸ ① ⑤❧ ③ ①⑤ ③④✇ ❧③ ③⑥ ❷♠ ⑤④ ⑤❷ ♠♠② ♠②⑥ ❷❸③r
④⑥③③④ru
t
②⑥②❸❶✇⑥ ⑤r
t
❽➇②⑩ ③⑥⑥③ ⑧⑤①③④
y
③④ ❹t
②✇ ❸ ① ⑤❧③ ① ⑤r
❥❽✈②
r
♠ ❷❸ ③③④③⑥ ❷♠ ⑤④⑤❷ ♠①②⑩ ②⑥ ❷♠⑧⑨✇ ①②s
✇ ❸ ① ⑤❧ ③ ①⑤③④✇ ❧③t
➈②⑩ ③⑥t
⑥③ ⑧⑤①③④➉ ❽✈②
r
♠❷❸③③④③④ ✇❧⑤①③ ① ⑤③⑥ ❷ ♠⑤ ④⑤❷ ♠y
③④❹♠②④❷④❾❷❸ ❸③④ ⑥③ ⑧⑤①③④✇❸①⑤❧ ③ [image:36.595.160.483.609.651.2]t
➈❻❸①⑤❧ ③➊❸③⑥ ⑤17
➋➌➍➎➏➎
➐
r
➑ ➒➌s
➑ ➓ ➒➔→➎ ➒➔ ➎ ➣➑→ ➎ ➐➌r
➏ ↔➓ ➎➎ ➣ ➎ ➍↔➏ ➔ ➣➔↔ ➏ → ➔r
↔ ↕➎➙ ➏ ➌ ➣➛➎→➔ ➑➓➒➔→ ➎➎➍↔ ➏➔ ➣➔↔➏➜ ➝➔➏ ➎ ➣➎r
➌➎➓➒➔➓➔➏ ➔➎y
➎ ➣➞t
➌r
➛➎→➔➎→ ➎➍➎➙➟➠ ➡➍
+ 3O
2
2Al
2
O
3
(7)
Salah satu proses anodisasi pada paduan aluminium yang cukup dikenal
adalah
➢➤➥ ➦ ➧➤➥ ➨ ➩c Acid Anodizing
(PAA) atau anodisasi asam phospat
(Newman, 2008). Pada umumnya, yang perlu dikontrol saat proses anodisasi
berlangsung adalah :
1. Tingkat konsentrasi dan kepekatan dari larutan asam phospat yaitu 10
-12%.
2. Tegangan listrik arus DC dengan tegangan 10-15 Volt.
3.
Lamanya pencelupan material pada proses PAA yaitu 25
Anodisasi asam phospat atau PAA adalah suatu proses yang cairan
elektrolitnya menggunakan larutan asam phospat (H
3
PO
4
). Sebagai katoda
(kutub negatif) digunakan tembaga atau aluminium. Sedangkan anoda (kutub
positif) spesimen itu sendiri. Tahapan reaksi kimia yang terjadi pada saat
proses anodisasi adalah :
H
3
PO
4
+ 3H
2
O
3H
3
O
+
+ PO
4
3-
(8)
Pada katoda terjadi : 2e + 2H
3
O
+
2H
2
O + H
2 (g)
(9)
Pada anoda terjadi : Al + 6H
2
O
4H
3
O
+
+ O
2
+ Al
3+
+ 7e
(10)
Dari reaksi tersebut setelah diselesaikan, maka didapatkan :
2Al + 6H
3
O
+
2Al
3+
+ 6H
2
O
3
+ 3H
2
(11)
Seterusnya,
Al
3+
+ PO4
3-
Al PO
4
(Kristal alumina)
(12)
18
19
(
➘ ➴ ➷➬➮➱ ✃ ✃❐)
❒❮
r
❰➬❰❰Ït
u
t
❰ Ð❰Ñ❰Ò❰
ÑÓ ÔÕ❮
s
❰Ï ÔÒ ÖÕ ❰Õ Ö Õ❰ Ð❰s
❮ Ñ❮Ört
y
❰Ï × ÒÖ×➴ Ï❰ Ø❰Ï Ñ❰Ò❰ÑÓÔÕ ❮
s
➬❰ ÑÖs
Õ ❮Ù❰❰r
➬ Östr
ÖØ ❰ Öy
tu
Ñ❮Ï❮❰y
❰ ➷r
❰ru
s (
Ú Ûctifier
)
➮ ❮➬❮ ØÜr
ÔÒ ❰ ÏÔÏ Ø❰t
ÔÒ❰Ò ❰Ï❰ÏÔÒ ❰➮r
❰ ØÕ❮❰rt
Ý❰ ØÞ ❒❰Ò❰ ÑÓ ÔÕ❮
s
❰ÏÔÒÖÕ ❰Õ Öt
ÖÒ ❰ Ø Ð❮Ï ××➴ Ï ❰ Ø❰Ï Õ Ö❮ Ðst
barrel
Ò❰Ï ❰➬❰t
Ñ❮ Ð❰Ï❰s
➮t
❮t
❰ Ñ Ö Ð❮Ï× ×➴Ï ❰ Ø❰Ï ❰➬❰t
Ñ❮ÏÒÖÏ×ÖÏ(
thermostaat
)
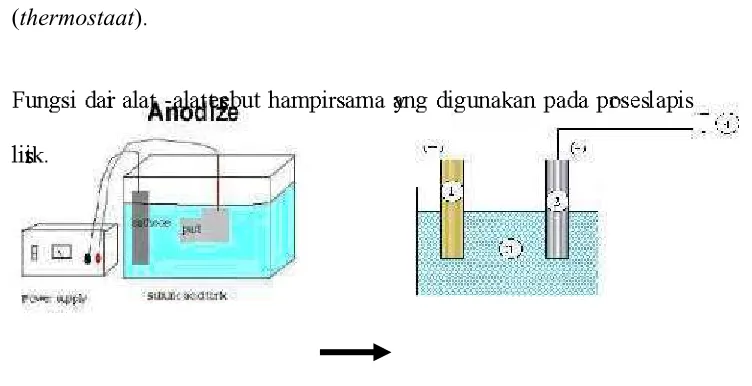
Þ [image:39.595.129.505.249.442.2]ß➴Ï ×Õ ÖÒ❰
r
Ö❰➬❰t
à❰➬❰t t
❮❮ Ý➴Ürs
➷❰ ÐÑ Ör
Õ❰ Ð❰y
❰Ï × Ò Ö× ➴Ï ❰ Ø❰Ï Ñ❰Ò❰ Ñr
ÔÕ ❮s
➬ ❰ ÑÖs
➬ Östr
ÖØÞGambar 3. Skema pelaksanaan pelapisan anodisasi (BPPT, 1998).
Keterangan :
(1) Anoda (bahan kerja)
(2) Katoda (penghantar)
(3) Elektrolit
(4) Sumber arus searah
Pemakaian arus searah akan menghasilkan lapisan yang lebih keras dan
tahan korosi, tetapi lebih bersifat rapuh (
brittle
). Sifat ketahanan korosi
20
áâ ãä
r
s
åä æ çäèééær
éê ëìr
íéì ææy
é é î éíéëåâãär
s
å äw
ér
æé éæïáâãr
äs
å ä æ çär
èééæåä
w
ér
æ ééæ ì æì ðä íìåñ òì åäw
ér
æ ééæ íéæ çãñæ ç(
in
t
óôõ ö÷coloring
)
î éæ åäw
ér
æ ééæ îä æ çéæ øéëéæ å äw
ér
æééæ â ù ç éæìê ét
éu
éæâùçéæìê ï áäw
ér
æ ééæíéæçãñæç éîéíéë åùâãä
s
å äw
ér
æééæ éæ çy
íéæ çsu
æçt
är
èéîì å éîés
éét
åâãär
s
éæâ îì ã éãì
t
éæå é ðä æéðø éëúðä æ çç çñæéêéæ ø éë éæ åäw
éæ éïr
ûéðå ìr
ãäð ñé éíñðì æìñ ðî éæ åéîñéææ
y
éîéå é
t
î ìâêãìîéãì éæâîé î éæ î ìw
ér
æ éì ãäñéìs
îä æ çéæ éæ çy
î ìì æçì æêéæï üä æìs
éæâî ìê å âùâñã î éåét
î ìw
ér
æéì î ä æç éæ â ø ét
âùçéæìêý å ì çðä æ éæâ ù çé æìêt
ää æòrt
u
î éæ ãäþéé
r
íéå ì
s
íìstr
ìê åñíé(
ÿìêr
t
ëðä
r
ý✁ ✂✄ ✂)
ï☎✆✝ ✞✟✠ ✞✡☛ ☞✌✍✡✎✍✏✑✒ ✍✡✓ ✌✒ ✑✔✍✕✖ ☞✟✑✡ ✑☞✟
üìê é é
ru
s
ãä ér
éë ð ñíéì î ì èéíéæêéæåéîé ãä í éæâ îìãéãì î ä æçéæ íéru
t
éæ ä íäêòâíìr
t
éãéð ãñí✗ét
ðéê é êét
âîé éê éæ øäð ñér
t
éæ æä ç éì✗t
îéæ éæâîé éê é æ ø är
ðu
ét
éæ åâãìì✗ït
✘ã éð å ëâ ãå ét
éê éæ ät
ru
r
éìðä æèéî ì ê éìâæt
û+
dan ion PO
4
2-
. Kation
kation H
+
akan bergerak menuju katoda dan di sisi lain akan dinetralkan oleh
elektron
elektron katoda sehingga akan terbentuk gas H
2
.
6H
+
+ 6e
3H
2(g)
Al pada anoda akan terurai menjadi ion Al
3+
dan bergerak ke katoda.
2Al
2Al
3+
+ 6e
-Karena ion positif Al
3+
tidak tereduksi pada katoda, maka reaksi yang terjadi :
3H
2
O + 3e
-
3OH
-
+ 3/2 H
2 (g)
Demikian juga pada ion PO
4
2-
tidak teroksidasi pada anoda, reaksi diganti
oleh :
2-21
✙✚✛✚✜ ✢✣✤ ✥✚✚✦
r
✚(
r
r r)
t r
r
r
✧★✦ ✩✪ ✫
+
dengan oksida atau hidroksida untuk menghasilkan aluminium
oksida (ion hidrogen akan terlepas menuju larutan dan membentuk gas H
2
).
2 Al
3+
+ 3O
2
Al
2
O
3
2 Al
3+
+ 3OH
Al
2
O
3
+ 3H
+
Sehingga didapatkan reaksi keseluruhan:
2 Al + 3 H
2
O
Al
2
O
3
+ 6H
+
+ 6e
Ketebalan lapisan oksida yang dihasilkan dari proses anodisasi, dipengaruhi
oleh berbagai faktor, antara lain, jenis larutan elektrolit,
current density
,
durasi proses anodisasi, dan lain
lain. Pada gambar 5 dijelaskan tentang
pengaruh
current density
(rapat arus) terhadap pertumbuhan lapisan oksida
dimana secara teori peningkatan ketebalan akan terjadi secara konstan
sedangkan pada kenyataannya peningkatan ketebalan akan semakin
berkurang, hal ini dipengaruhi oleh adanya peluruhan
local Joule s heating
[image:41.595.241.427.529.648.2]yang disebabkan pemakaian
current density
yang terlalu besar.
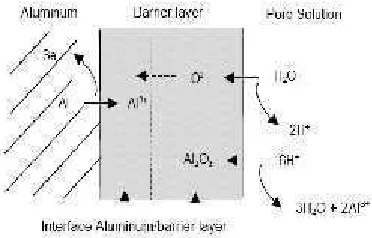
Gambar 4. Reaksi dimana pembentukan lapisan oksida (Juhl, 2005).
21
Pada permukaan anoda (antara logam dan lapisan barier), terjadi reaksi antara
ion Al
3+
dengan oksida atau hidroksida untuk menghasilkan aluminium
oksida (ion hidrogen akan terlepas menuju larutan dan membentuk gas H
2
).
2 Al
3+
+ 3O
2
Al
2
O
3
2 Al
3+
+ 3OH
Al
2
O
3
+ 3H
+
Sehingga didapatkan reaksi keseluruhan:
2 Al + 3 H
2
O
Al
2
O
3
+ 6H
+
+ 6e
Ketebalan lapisan oksida yang dihasilkan dari proses anodisasi, dipengaruhi
oleh berbagai faktor, antara lain, jenis larutan elektrolit,
current density
,
durasi proses anodisasi, dan lain
lain. Pada gambar 5 dijelaskan tentang
pengaruh
current density
(rapat arus) terhadap pertumbuhan lapisan oksida
dimana secara teori peningkatan ketebalan akan terjadi secara konstan
sedangkan pada kenyataannya peningkatan ketebalan akan semakin
berkurang, hal ini dipengaruhi oleh adanya peluruhan
local Joule s heating
yang disebabkan pemakaian
current density
yang terlalu besar.
Gambar 4. Reaksi dimana pembentukan lapisan oksida (Juhl, 2005).
21
Pada permukaan anoda (antara logam dan lapisan barier), terjadi reaksi antara
ion Al
3+
dengan oksida atau hidroksida untuk menghasilkan aluminium
oksida (ion hidrogen akan terlepas menuju larutan dan membentuk gas H
2
).
2 Al
3+
+ 3O
2
Al
2
O
3
2 Al
3+
+ 3OH
Al
2
O
3
+ 3H
+
Sehingga didapatkan reaksi keseluruhan:
2 Al + 3 H
2
O
Al
2
O
3
+ 6H
+
+ 6e
Ketebalan lapisan oksida yang dihasilkan dari proses anodisasi, dipengaruhi
oleh berbagai faktor, antara lain, jenis larutan elektrolit,
current density
,
durasi proses anodisasi, dan lain
lain. Pada gambar 5 dijelaskan tentang
pengaruh
current density
(rapat arus) terhadap pertumbuhan lapisan oksida
dimana secara teori peningkatan ketebalan akan terjadi secara konstan
sedangkan pada kenyataannya peningkatan ketebalan akan semakin
berkurang, hal ini dipengaruhi oleh adanya peluruhan
local Joule s heating
yang disebabkan pemakaian
current density
yang terlalu besar.
22
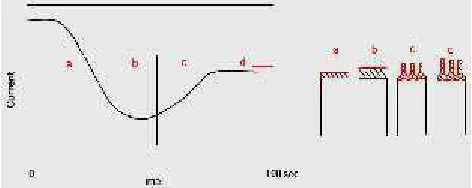
Gambar 5. Grafik Perubahan Ketebalan Lapisan terhadap
Current Density
(Gazzapo, 1994).
Gambar 6. Mekanisme Pembentukan Lapisan Oksida (Juhl, 2005).
Lapisan oksida yang terbentuk pada hasil anodisasi dengan larutan elektrolit
asam phospat akan menghasilkan lapisan yang berpori. Pada mulanya arus
yang melewati elektroda aluminium tinggi karena hanya melewati logam
aluminium. Kemudian arus mulai menurun karena
barrier
atau
non porous
layer
yang rapat dan tipis terbentuk. Lapisan oksida yang terbentuk pada
permukaan aluminium ini mempunyai hambatan yang lebih tinggi daripada
aluminium sendiri (
periode a
). Lapisan oksida yang terbentuk menjadi lebih
tebal oleh karena itu hambatan menjadi lebih tinggi yang menyebabkan arus
terus menurun (
periode b
). Kecenderungan kurva keatas pada
periode b
berdasar pada lapisan oksida yang terbentuk akan kasar pada
barier layer
.
Aliran arus akan lebih terkonsentrasi pada permukaan yang lebih tipis, yang
[image:42.595.181.417.261.355.2]menyebabkan temperatur elektrolit meningkat sehingga terjadi peluruhan
22
Gambar 5. Grafik Perubahan Ketebalan Lapisan terhadap
Current Density
(Gazzapo, 1994).
Gambar 6. Mekanisme Pembentukan Lapisan Oksida (Juhl, 2005).
Lapisan oksida yang terbentuk pada hasil anodisasi dengan larutan elektrolit
asam phospat akan menghasilkan lapisan yang berpori. Pada mulanya arus
yang melewati elektroda aluminium tinggi karena hanya melewati logam
aluminium. Kemudian arus mulai menurun karena
barrier
atau
non porous
layer
yang rapat dan tipis terbentuk. Lapisan oksida yang terbentuk pada
permukaan aluminium ini mempunyai hambatan yang lebih tinggi daripada
aluminium sendiri (
periode a
). Lapisan oksida yang terbentuk menjadi lebih
tebal oleh karena itu hambatan menjadi lebih tinggi yang menyebabkan arus
terus menurun (
periode b
). Kecenderungan kurva keatas pada
periode b
berdasar pada lapisan oksida yang terbentuk akan kasar pada
barier layer
.
Aliran arus akan lebih terkonsentrasi pada permukaan yang lebih tipis, yang
menyebabkan temperatur elektrolit meningkat sehingga terjadi peluruhan
22
Gambar 5. Grafik Perubahan Ketebalan Lapisan terhadap
Current Density
(Gazzapo, 1994).
Gambar 6. Mekanisme Pembentukan Lapisan Oksida (Juhl, 2005).
Lapisan oksida yang terbentuk pada hasil anodisasi dengan larutan elektrolit
asam phospat akan menghasilkan lapisan yang berpori. Pada mulanya arus
yang melewati elektroda aluminium tinggi karena hanya melewati logam
aluminium. Kemudian arus mulai menurun karena
barrier
atau
non porous
layer
yang rapat dan tipis terbentuk. Lapisan oksida yang terbentuk pada
permukaan aluminium ini mempunyai hambatan yang lebih tinggi daripada
aluminium sendiri (
periode a
). Lapisan oksida yang terbentuk menjadi lebih
tebal oleh karena itu hambatan menjadi lebih tinggi yang menyebabkan arus
terus menurun (
periode b
). Kecenderungan kurva keatas pada
periode b
berdasar pada lapisan oksida yang terbentuk akan kasar pada
barier layer
.
Aliran arus akan lebih terkonsentrasi pada permukaan yang lebih tipis, yang
23
✬ ✭✮ ✭✮ ✭✯
r
✭✰✱✲✱ ✳✴ ✯✵✶ ✰ ✭✲u
r
✭✷ ✭✲t
✯ru
s t
✯r
✸ ✭✮✱y
✭✲✹✺ ✯✲y
✯✻ ✭✻✷ ✭✲✵ ✭✬ ✱✼ ✭✲y
✭✲✹✼ ✯✺ ✭✷✱✲ ✱✬ ✱✼✽
t
✱✲✱ ✺ ✯✲y
✯✻ ✭✻✷ ✭✲r
✯✼✱✭✲ ✼ ✱st
✮✱ ✮✭✯r
✭✰ ✱✲ ✱ ✵ ✯✻✱ ✰ ✷ ✯✾✱✵y
✭✲✹ ✺✯✲y
✯ ✻✭✻ ✷✭✲ ✭ru
s
✭✷✭✲ ✺ ✯✲✱✲✹✷✭t (
✿❀ri
❁❂❀ ✾)
✳ ✴ ✭✮ ✭t
✭✰ ✭✬✱✲ ✱ ✬✯✺✻ ✯✲ ❃✶✷✭✲ ✵ ✭✬✱✼ ✭✲p
o
ro
u
s
❄✷✼✱ ✮ ✭✺✶✵ ✭✱t
✯✻✯✲❃✶ ✷r
✮✭✲ ✭ru
s
✭✷ ✭✲st
✭✻✱✵✽✮✱ ✺✭✲✭✷ ✯✾✯✬✭t
✭✲ ✬ ✯✺ ✻✯✲❃✶ ✷ ✭✲✮ ✭✲✬ ✯✵u
ru
✰✭✲ ❃✯t
✭✬✭✭t
u
st
✭✻✱✵(
p
❀ri
❁❂❀ ❂)
✳✴
r
❄✼ ✯s
✬✯✵✶✰✭✲u
r
t
✯✸ ✭✮✱r
✷✭r
✯✲✭✬ ✯✺ ✻✯✱ ✭✲r
✯✲ ✯r
✹✱y
✭✲✹t
✯✵ ✭✵r
u
✻ ✯s
✭r
✺ ✯✵ ✯✻✱ ✰✱ ✯✲ ✯r
✹✱✱ ✷ ✭t
✭✲❅✵ ❆ ❇✬✭✮ ✭❅✵❈ ❇
❉
✳ ❊✯✭✷✼ ✱✬ ✯✵✶✰✭✲
u
r
y
✭✲✹t
✯✸r
✭✮✱ ✭✮ ✭✵ ✭✰✼ ✯✻✭✹ ✭✱ ✻✯✱ ✷✶ ❃❋r
❅✵ ❈
❇ ❉
+ 6H
+
2 Al
3+
(aq)
+ 3H
2
O
Peluruhan yang terjadi ada dua, yaitu peluruhan secara kimia (
chemical
dissolution
) dan peluruhan karena medan listrik yang terlalu besar dan
terkonsentrasi (
field-assisted dissolution
). Peluruhan secara kimia karena
tingkat keasaman dari elektrolit. Peluruhan karena medan listrik yang
terkonsentrasi pada
barrier layer
menyebabkan kenaikan temperatur pada
ketebalan lapisan yang lebih tipis sehingga memicu proses peluruhan, ini
disebut
local Joule s heating.
●❍■❏ ❑▲▼▲◆❖ ◆P◆◗❘▼
rmu
▲◆ ◆◗Kekasaran Permukaan (
Surface Roughness
) secara umum dapat dijelaskan
dengan 2 metode:
Arithmetic mean value
(R
AA
(Arithmetic Average
) atau CLA (
Center-Line Average
)
Root mean square
average
(Rq), biasanya disingkat dengan RMS. Satuan yang biasanya
24
❙
t
❙u
µin (
m
i
cro
inch
) dimana 1 µm = 40 µin dan 1 µin = 0.025 µm. Parameter
yang digunakan pada pengukuran kekasaran adalah,
a. Ra (
roughness average of the R-curve
) : nilai rata-rata aritmatika dari
pengukuran kekasaran permukaan untuk panjang tertentu.
b. Rz (
ten points high of irregularities
) : pengukuran berdasarkan nilai
rata-rata lima puncak tertinggi dah lima lembah terendah.
c. Rmax (
maksimum height of the profile)