Oleh
EKAWATI DANIAL
Tesis
Sebagai Salah Satu Syarat untuk Mencapai Gelar MAGISTER SAINS
Pada
Program Studi Pascasarjana Magister Agronomi Fakultas Pertanian Universitas Lampung
PROGRAM PASCASARJANA MAGISTER AGRONOMI
UNIVERSITAS LAMPUNG
ABSTRACT
IN VITRO PROPAGATION OF BANANAS
CV. AMBON KUNING AND RAJA BULU
By
EKAWATI DANIAL
Banana is one of the most important fruits in Indonesia, since it contributes to food security for millions of people, a rich source of vitamins, minerals, and carbohydrates as well as important cash crop. Traditionally, banana is propagated by suckers, because almost all of edible banana are triploid and seed sterlie. Therefore, the availability of a large number of uniform and clean plant materials become a constraint for commercial banana cultivation. In vitro propagation has been widely used as an alternative for rapid clonal propagation of banana. Ambon Kuning and Raja Bulu are two of the most popular banana cultivars in Indonesia. This study, which was conducted at Plant Science Laboratory and Green House of Faculty of Agriculture the University of Lampung since February 2012 to May 2013, consisted of two experiment: i.e (1) effects of BA concentrations on shoot and propagule multiplication of banana cv. Ambon Kuning and Raja Bulu, and (2) effects of different acclimatization media and fertilizer on survival rates and planlet growth. Treatments in experiment I were arranged factorially in a completely randomized design with three replications. The first factor was BA concentrations (2,5 mg/l, 5,0 mg/l and 7,5 mg/l) and second factor was banana cultivars (Ambon Kuning and Raja Bulu). Each experimental unit consisted of three culture bottles each of which contained 1 explant. Subculture to the same medium was conducted every 4 weeks until 20 weeks of culture, when the number of shoots, propagules and length of shoots were recorded. Treatments in
data were subjected to analysis of variance, and further mean separation was done using least significant difference (LSD). Results of experiment I showed that both BA concentrations and cultivars as well as their interaction significantly affected shoot and propagule multiplication. The highest number of shoots and propagules per explant on both cultivars per explant were obtained on MS + 5 mg/l BA. Banana cv. Ambon Kuning produced significantly more shoots and propagules per explant compared to Raja Bulu. The highest number of shoots (25,6) and propagules (40,7) in cv. Ambon Kuning and in cv. Raja Bulu (i.e. 1,9 shoots and 12,3 propagules) per explant were obtained in MS + 5 mg/l BA. Results of experiment II showed that all treatments tested produced 100% planlet survival. Both media and fertilizer application significantly affected planlet growth. The best media for planlet growth was M3 (sand:compost, 1:1), with produced the highest plant height and fresh weights. Application of NPK solution on planlets increased plant growth, as shown by the increased of plant height, number of leaves, chlorophyll content (spad unit) and fresh weights. Most of the
acclimatized planlets were planted in the field and produced fruits of high quality.
ABSTRAK
PERBANYAKAN IN VITRO TANAMAN PISANG AMBON KUNING DAN RAJA BULU
Oleh
EKAWATI DANIAL
Pisang adalah buah yang sangat bergizi yang merupakan sumber vitamin, mineral dan juga karbohidrat. Pisang Ambon Kuning dan Raja Bulu merupakan dua kultivar pisang yang populer di Indonesia. Penyediaan bibit pisang biasanya dilakukan menggunakan tunas anakan atau belahan bonggol tetapi cara tersebut membutuhkan waktu yang lama. Teknik kultur jaringan merupakan teknik alternatif yang dapat digunakan untuk menyediakan bahan tanam dalam jumlah besar dan bermutu tinggi dan dalam waktu yang relatif singkat. Penelitian dilaksanakan di Laboratorium Kultur Jaringan Tanaman dan Rumah Kaca
diulang tiga kali. Setiap satuan percobaan terdiri dari sepuluh pot yang masing-masing berisi satu planlet. Keseragaman data diuji dengan Uji Barlett, jika asumsi terpenuhi dilakukan analisis ragam, kemudian dilanjutkan dengan uji beda nyata terkecil (BNT) pada taraf 5 % untuk pemisahan nilai tengahnya. Hasil percobaan I menunjukkan bahwa, baik konsentrasi BA, varietas pisang maupun interaksi antar keduanya berpengaruh terhadap pembentukan mata tunas, tunas dan propagul per eksplan. Jumlah tunas dan propagul per eksplan terbanyak pada kedua kultivar pisang tersebut didapatkan pada perlakuan BA 5 mg/l. Pisang Ambon Kuning menunjukkan daya regenerasi mata tunas, tunas dan propagul yang lebih tinggi daripada pisang Raja Bulu. Jumlah tunas dan propagul terbanyak pada pisang Ambon Kuning pada perlakuan BA 5 mg/l sebesar 25,6 tunas dan 40,7 propagul per eksplan, sedangkan pada pisang Raja Bulu adalah 1,9 tunas dan 12,3 propagul per eksplan. Pada percobaan II, semua perlakuan
campuran media aklimatisasi baik dengan pemupukan atau tanpa pemupukan menghasilkan 100% planlet pisang Ambon Kuning yang teraklimatisasi. Campuran media aklimatisasi dan pemupukan secara signifikan mempengaruhi pertumbuhan planlet. Media tanam yang terbaik bagi pertumbuhan planlet adalah media M3 (pasir : kompos, 1:1), yang menghasilkan tinggi tanaman dan bobot tanaman yang tertinggi. Pemupukan planlet dengan NPK (32:10:10) pada konsentrasi 2 g/l meningkatkan tinggi tanaman, jumlah daun, tingkat kehijauan daun dan bobot tanaman Ambon Kuning yang diaklimatisasi. Tidak terdapat interaksi antara campuran media dan pemupukan dalam pengaruhnya terhadap pertumbuhan planlet. Planlet-planlet yang berhasil diaklimatisasi, ditanam di kondisi lapangan dan menghasilkan buah yang bermutu baik.
DAFTAR ISI
Halaman
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN ... vii
I. PENDAHULUAN ... 1
1.1 Latar Belakang dan Masalah ... 1
1.2 Tujuan Penelitian ... 8
1.3 Kerangka pemikiran ... 8
1.4 Hipotesis ... 12
II.TINJAUAN PUSTAKA ... 13
2.1 Klasifikasi dan Morfologi Tanaman Pisang ... 13
2.2 Perbanyakan Tanaman Pisang Konvensional ... 16
2.3 Perbanyakan Tanaman Pisang Kultur Jaringan ... 18
2.4 Media Kultur ... 21
2.5 Zat Pengatur Pertumbuhan ... 23
III. METODE PENELITIAN ... 28
4.1.2 Pengaruh Campuran Media Tanam dan Pemupukan terhadap Keberhasilan Aklimatisasi dan Pertumbuhan
Bibit Pisang Ambon Kuning ... 42
4.1.2.1 Rata-rata Tinggi Tanaman ... 43
4.1.2.2 Rata-rata Jumlah Daun ... . 45
4.1.2.3 Rata-rata Tingkat Kehijauan Daun ... 46
4.1.2.4 Rata-rata Bobot Tanaman di Pembibitan ... 47
4.1.2.5 Rata-rata Tinggi Tanaman di Pembibitan ... 49
4.1.2.6 Rata-rata Jumlah Daun di Pembibitan ... 50
4.1.2.7 Rata-rata Bobot Tanaman di Pembibitan... 51
4.2 Pembahasan ... 56
V. KESIMPULAN DAN SARAN ... 65
5.1 Kesimpulan ... 65
5.2 Saran ... 66
DAFTAR PUSTAKA ... 67
1.1 Latar Belakang dan Masalah
Pisang sebagai bahan konsumsi adalah buah yang sangat bergizi yang merupakan sumber vitamin, mineral dan juga karbohidrat. Kandungan gizi pisang terdiri dari air, karbohidrat, protein, lemak dan vitamin A, B1, B2 dan C (Direktorat Hasil
dan Pemasaran Hortikultura, 2005).
Perkebunan pisang yang permanen (diusahakan terus menerus) dengan mudah dapat ditemukan di Meksiko, Jamaika, Amerika Tengah, Panama, Kolombia, Ekuador dan Filipina. Di negara tersebut, budidaya pisang sudah merupakan
suatu industri yang didukung oleh kultur teknis yang prima dan stasiun
pengepakan yang modern dan pengepakan yang memenuhi standard internasional. Hal tersebut menunjukkan bahwa pisang memang komoditas perdagangan yang
sangat tidak mungkin diabaikan (Pujaratno, 2010).
Di Indonesia ada 14 kultivar pisang yang dikembangkan , selain itu Indonesia memiliki keragaman plasma nutfah yang besar. Berdasarkan sifat ciri buahnya dapat dibagi menjadi beberapasubgroup, yaitu: Becici, Mas, Ambon, Cavendish,
Sentra produksi pisang terbesar di Indonesia adalah di Pulau Jawa, yaitu Jawa Barat, Jawa Tengah, dan Jawa Timur. Di luar pulau Jawa sentra produksi pisang di Sumatera Selatan dan Lampung, buah pisang yang dihasilkan dipasarkan ke
Jakarta dan sekitarnya (Satuhu dan Supriyadi, 2000).
Menurut catatan Direktorat Budidaya dan Pascapanen Buah (2011), wilayah andalan pengembangan kawasan pisang di Lampung adalahLampung Selatan,
Lampung Barat, Lampung Timur, dan Pesawaran.
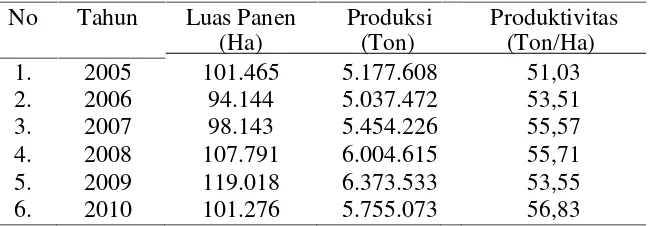
Tabel 1. Luas Panen, Produksi dan Produktivitas Pisang Tahun 2005-2010.
No Tahun Luas Panen Produksi Produktivitas
(Ha) (Ton) (Ton/Ha)
Sumber: Kementerian Pertanian, Direktorat Jenderal Hortikultura (2011).
Sentra produksi utama pisang Indonesia pada tahun 2012 antara lain berada pada Jawa Timur (1.362.881 ton), Jawa barat (1.192.861 ton), dan Lampung (817.606
ton) (Badan Pusat Statistik, 2013).
Meningkatnya produksi dan luas panen pisang tidak selalu diikuti dengan
produktivitas pisang yang meningkat. Hal ini dapat dilihat bahwa pada tahun
2007 produktivitas pisang sebesar 55,57 ton/ha dan meningkat pada tahun 2008 yaitu 55,71 ton/ha tetapi terjadi penurunan pada tahun 2009 menjadi 53,55 ton/ha
Secara konvensional penyediaan bibit pisang dilakukan dengan yaitu menggunakan tunas anakan maupun belahan bonggol. Tetapi dengan cara
tersebut dari jumlah anakan yang diperoleh relatif sedikit, yaitu 5—10 anakan per
rumpun per tahun. Menurut Yusnita dan Hapsoro (2012), jika ditanam secara monokultur maka untuk satu hektar lahan dibutuhkan sebanyak 1000—2500 bibit
pisang.
Musa paradisiacayang sangat digemari karena kandungan gizinya diantaranya adalah pisang Ambon Kuning dan Raja Bulu. Pada umumnya tanaman pisang ini diperbanyak dengan cara menggunakan bibit yang berasal dari anakan dan
belahan bonggol, sehingga sulit untuk mendapatkan bibit yang berkualitas dalam jumlah besar dan dalam waktu relatif singkat. Menurut Bhasole dkk. (2011),
untuk kepentingan komersial bahan tanam tersebut dapat diperoleh melalui teknik
kultur jaringan. Selain itu, menurut Roy dkk. (2010), teknik ini menghasilkan multiplikasi yang tinggi, secara genetik seragam, dan bahan tanamnya bebas hama dan penyakit. Selain itu, bibit pisang yang dihasilkan secarain vitrolebih cepat
tumbuh dan menghasilkan anakan lebih banyak.
Kultur jaringan tanaman merupakan teknik menumbuhkan dan mengembangkan
bagiaan tanaman yang berupa sel, jaringan atau organ dalam kondisi aseptik secarain vitroyang dicirikan oleh kondisi yang aseptik, penggunaan media kultur
Penggunaan teknik kultur jaringan umumnya dilakukan untuk perbanyakan tunas kemudian dilanjutkan dengan pengakaran dan aklimatisasi. Pada perbanyakanin vitrotanaman pisang, perbanyakan tunas umumnya dilakukan melalui
multiplikasi tunas aksilar.
Golongan zat pengatur pertumbuhan yang digunakan untuk penggandaan tunas adalah dari golongan sitokinin. Sitokinin merupakan ZPT yang penting dalam
pengaturan pembelahan sel dan morfogenesis.
Jenis sitokinin yang paling sering digunakan adalah benziladenin (BA), kinetin,
2-iP, dan thidiazuron. Namun dari keempat sitokinin tersebut, BA paling sering digunakan karena efektifitasnya tinggi dan harganya relatif murah (Yusnita,
2003). Pemberian sitokinin ke dalam media kultur dapat dilakukan secara tunggal atau dikombinasikan dengan jenis sitokinin yang lain, atau dikombinasikan
dengan auksin pada konsentrasi rendah untuk multiplikasi tunas.
Berdasarkan hasil penelitian Yusnita dkk. (1996) pada perbanyakan tunas pisang Ambon Kuning secarain vitro,dinyatakan bahwa semakin tinggi konsentrasi BA
yang digunakan antara 1—5 mg/l semakin banyak tunas yang dihasilkan tetapi
kualitas tunas yang dihasilkan umumnya semakin rendah. Penelitian Anegra (2008) menunjukkan bahwa tunas dan mata tunas pisang Ambon Kuning yang
berada pada media pemeliharaan yang mengandung 2 mg/l BA stabil
bermultiplikasi pada bulan kelima setelah tanan. Sedangkan hasil penelitian
Hirimburegama dan Gamage (1997) mengungkapkan bahwa respons jaringan tanaman pisang spesifik terhadap genotipe. Respons pisang bergenotipe AAA lebih baik daripada pisang bergenotipe AAB.
Akan tetapi pada penelitian Ismaryati (2010) pada eksplan pisang Tanduk yang
bergenotipe AAB jumlah mata tunas pada subkultur ke 5, 6, dan 7 masing-masing sebanyak 2,9; 5,3; dan 12,1 per eksplan. Sedangkan jumlah tunas yang dihasilkan
yaitu sebanyak 2,8; 4,1; dan 7,0 per eksplan. Jumlah mata tunas yang dihasilkan oleh pisang Tanduk ini lebih tinggi daripada jumlah mata tunas pada kultur pisang Ambon Kuning yang bergenotipe AAA yaitu 1,6; 2,7 dan 4,6 per eksplan.
Perbedaan tingkat multiplikasi tunas melalui respons terhadap konsentrasi BA tersebut menunjukkan bahwa topik ini masih perlu kajian lebih lanjut.
Setelah jumlah tunas dalam botol-botol sudah dianggap mencukupi kebutuhan akan jumlah bibit, tunas-tunas dapat dipindahkan ke botol kultur baru yang berisi
media untuk pemanjangan dan penagakaran. Setelah dikulturkan di media yang mengandung auksin ini, tunas-tunas pisang akan berakar dan menjadi siap untuk dikeluarkan dari botol sebagai tanaman lengkap dan siap diaklimatisasi.
Aklimatisasi adalah proses penyesuaian planlet dari kondisi mikro dalam botol yang terkendali ke kondisi lingkungan luar yang alami, sehingga tanaman
mempunyai perakaran yang lebih baik, pertumbuhan yang lebih baik dan lebih kokoh (Wulandari, 2006).
mula-mula tinggi dan diturunkan secara bertahap, sedangkan intensitas cahaya mula-mula rendah, lalu ditingkatkan secara bertahap. Hingga pada akhirnya bibit-bibit pisang tersebut dapat bertahan dan tumbuh dengan baik pada kondisi dengan
sinar matahari penuh dan dapat ditanam di lapangan (Hapsoro dan Yusnita, 2012).
Aklimatisasi memerlukan media tanam tertentu yang sifatnya porous, tidak mudah terdekomposisi, mempunyai kemampuan memegang air, mengandung hara cukup
tinggi, tidak menjadi sumber inokulum cendawan patogen, dan mudah diperoleh dalam jumlah yang dibutuhkan (Yusnita, 2010).
Pemilihan media tanam yang tepat merupakan salah satu faktor penentu keberhasilan dalam aklimatisasi, karena media berperan sebagi tempat tumbuh dan berkembangnya tanaman. Media yang memiliki kelembaban rendah dapat
menyebabkan planlet rusak dan bahkan mati dalam waktu yang relatif singkat. Menurut Satsijati (1991) dalam Ismaryati (2010), untuk memperoleh bibit pisang yang baik dan sehat dalam pertumbuhannya dibutuhkan media tanam yang tepat,
karena media tanam merupakan tempat penyimpanan atau sumber hara tanaman.
Secara umum, media tanam harus dapat menjaga kelembapan daerah sekitar akar,
menyediakan cukup udara, dan dapat menahan ketersediaan unsur hara (Rahmawan, 2010). Media tanam sekam bakar memiliki porositas tinggi dan
ringan, dapat mengurangi pengaruh penyakit akibat gulma dan bakteri. Sifat ini menguntungkan jika digunakan sebagai media tanam karena mendukung
perbaikan struktur tanah karena aerasi dan drainase menjadi lebih baik. Kompos
Pasir sering digunakan sebagai media tanam alternatif untuk menggantikan fungsi tanah. Sejauh ini, pasir dianggap memadai dan sesuai jika digunakan sebagai media untuk penyemaian benih, pertumbuhan bibit tanaman, dan perakaran setek
batang tanaman. Pasir malang dan pasir bangunan merupakan jenis pasir yang sering digunakan sebagai media tanam (Rahmawan, 2010).
Penambahan unsur hara perlu dilakukan untuk meningkatkan laju pertumbuhan
dan keberhasilan pada saat aklimatisasi planlet pisang. Penambahan unsur hara dapat dilakukan dengan pemupukan. Bibit pisang yang sudah diaklimatisasi biasanya dipupuk menggunakan larutan hara lengkap, yang berisi baik unsur hara
makro maupun mikro. Pupuk majemuk yang kandungan unsur N-nya lebih tinggi daripada P dan K-nya dapat digunakan untuk memacu pertumbuhan awal bibit (Yusnita, 2010).
Tersedianya campuran media tanam dengan komposisi yang tepat menentukan
keberhasilan aklimatisasi planlet. Jenis media tanam yang mampu mengikat air dan unsur hara dengan baik sesuai untuk aklimatisasi. Tanaman dapat menyerap unsur hara melalui akar atau melalui daun. Untuk dapat menyerap unsur hara
tanaman membutuhkan air. Penambahan unsur hara dalam media tanam yang tepat akan menghasilkan tanaman yang hidup dengan baik. Oleh karena itu,
Berdasarkan latar belakang masalah yang ada, dua percobaan dilakukan untuk menjawab masalah yang dirumuskan dalam pertanyaan-pertanyaaan sebagai berikut :
1. Bagaimanakah pengaruh konsentrasi BA dari 2,5 mg/l, 5 mg/l, 7,5 mg/l dan varietas pisang Ambon Kuning (AAA) dan Raja Bulu (AAB) terhadap perbanyakan mata tunas, tunas dan propagulin vitro?
2. Bagaimanakah pengaruh campuran media tanam dan pemupukan terhadap keberhasilan aklimatisasi dan pertumbuhan bibit pisang Ambon Kuning.
1.2 Tujuan Penelitian
Berdasarkan identifikasi dan perumusan masalah, tujuan penelitian dirumuskan sebagai berikut :
1. Mempelajari pengaruh konsentrasi BA (benziladenin) 2,5 mg/l; 5 mg/l; dan 7,5 mg/l terhadap perbanyakan mata tunas, tunas, propagul dan panjang tunasin vitropisang Ambon Kuning dan Raja Bulu.
2. Mengetahui pengaruh campuran media tanam dan pemupukan terhadap
keberhasilan aklimatisasi bibit pisang Ambon Kuning.
1.3 Kerangka Pemikiran
Teknik kultur jaringan tanaman memiliki prospek yang lebih baik daripada
beberapa keuntungan seperti klon yang banyak dapat dihasilkan dalam waktu singkat hanya dari sejumlah material kecil, dan teknik ini tidak tergantung musim.
Dua faktor terpenting yang menentukan keberhasilan teknik kultur jaringan adalah ZPT dan genotipe. ZPT yang sering digunakan pada perbanyakanin vitroadalah
sitokinin dan auksin (Yusnita, 2003).
Menurut Madhulatha (2004) dalam Bhosale (2011), sitokinin seperti
benzylaminopurine (BAP) diketahui dapat mengurangi dominansi tunas apikal dan menginduksi pembentukan tunas aksilar dan adventif dari jaringan meristem
pisang.
Genotipe tanaman asal eksplan juga merupakan faktor yang sangat mempengaruhi pertumbuhan dan morfogenesis eksplan dalam kulturin vitro. Pisang Grand
Naine dan Philipine Lakatan (AAA), serta Saba dan Pelipita (ABB) dapat dipacu
multiplikasi tunasnya dengan mengkulturkan eksplan mata tunas di media MS yang ditambah dengan 5 mg/l BA (Cronauer dan Krikorian, 1984).
Menurut Hirimburegama dan Gamage (1996), respons jaringan tanaman pisang
spesifik terhadap genotipe. Respons pisang bergenotipe AAA lebih baik daripada pisang bergenotipe AAB.
Pembiakanin vitrotanaman pisang dapat dibagi menjadi beberapa tahap, yaitu tahap 0: memilih dan menyiapkan tanaman induk untuk eksplan; tahap 1: inisiasi
Tanaman untuk sumber eksplan harus jelas jenisnya dan harus dalam kondisi sehat serta tidak terinfeksi patogen. Tahap 0 ini bertujuan agar semua sifat bibit diharapkan akan sesuai dengan sifat induknya.
Tahap inisiasi kultur bertujuan untuk mendapatkan kultur awal yang aseptik dan
aksenik. Bahan tanam yang biasa digunakan adalah tunas dari bonggol. Kultur pada tahap inisiasi ini dikatakan berhasil jika eksplan tetap hidup dan media
maupun eksplan tidak terkontaminasi mikroorganisme.
Tahap berikutnya adalah tahap multiplikasi tunas. Pada tahap ini eksplan
dirangsang untuk melakukan perbanyakan tunas dan diberikan zat pengatur tumbuh (ZPT) sitokinin dalam media kultur. Tahap selanjutnya adalah
memindahkan tunas yang dihasilkan dari tahap multiplikasi untuk pemanjangan dan pengakaran.
Tahap akhir dari perbanyakan tanaman dengan teknik kultur jaringan adalah aklimatisasi planlet. Aklimatisasi yaitu melatih tanaman yang sebelumnya
ditumbuhkan di dalam botol kultur dengan suplai media yang lengkap untuk dapat
hidup secara mandiri dan berfotosintesis pada kondisi eksternal. Aklimatisasi dilakukan dengan mengkondisikan planlet dalam media (Yusnita, 2003).
Planlet yang telah mengalami berbagai tahapan aseptik siap ditanam di media campuran pasir-arang sekam-kompos. Pada awal aklimatisasi dilakukan
pengurangan kelembaban udara dan penambahan intensitas cahaya secara
sehat serta tumbuh dengan baik pada kondisi sinar matahari penuh dan siap ditanam di lapangan.
Media campuran arang sekam, pasir malang dan kompos dengan perbandingan 1:1:1 menghasilkan persentase tanaman yang hidup sebesar 100% pada
aklimatisasi tanaman pisang Tanduk dan Ambon Kuning (Ismaryati, 2010).
Media arang sekam digunakan karena bersifat porous, dan menyimpan air, pasir malang memiliki rongga-rongga yang halus sehingga mampu memegang tanaman dengan baik, sedangkan kompos selain sebagai media juga berfungsi sebagai
pupuk (http ://www.emirgarden.com, 2008).
Masing-masing bahan campuran media tanam tersebut memiliki sifat fisik dan kandungan hara yang berbeda. Pencampuran dua jenis media atau lebih diharapkan dapat saling melengkapi kekurangan masing-masing media seperti kecepatan melapuk, penyediaan hara tanaman, dan kemampuan mempertahankan
kelembaban (Marlina dan Rusnandi, 2007).
Growmore adalah pupuk daun lengkap dalam bentuk kristal berwarna biru, sangat mudah larut dalam air, mengandung hara lengkap dengan konsentrasi yang berbeda sesuai dengan kebutuhan, dapat diserap dengan mudah oleh tanaman baik
itu melalui penyemprotan daun maupun disiram ke dalam tanah. Pupuk daun Growmore (32:10:10) mengandung persentase N yang lebih besar. Formula ini
1.4 Hipotesis
1. Semakin tinggi konsentrasibenziladenin(BA) dalam media kultur maka
semakin banyak tunas pisang Ambon Kuning dan Raja Bulu yang dihasilkan.
2. Kedua kultivar pisang yaitu Ambon Kuning dan Raja Bulu menghasilkan respons yang berbeda terhadap BA tertentu yang sama.
3. Campuran media tanam pasir malang : arang sekam : kompos (1:1:1) memberikan pertumbuhan yang terbaik.
2.1 Klasifikasi dan Morfologi Tanaman Pisang
Klasifikasi tanaman pisang menurut Jumari dan Pudjorianto (2000) adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae
Kelas : Monocotyledonae
Ordo : Scitaminae
Famili : Musaceae
Subfamili : Muscoidae
Genus : Musa
Species : Musa paradisiacaLinn
Jenis pisang dibagi menjadi tiga, yaitu: 1) Pisang yang dimakan buahnya tanpa
dimasak yaituM.paradisiacavarSapientum. Misalnya pisang Ambon, Susu, Raja, Cavendish, Barangan dan Mas, 2) Pisang yang dimakan setelah buahnya
seratnya misalnya pisang Manila (Abaca) (Pujaratno, 2010). Tanaman pisang diduga berasal dari Asia Selatan dan Asia Tenggara. Hingga saat ini, budidaya tanaman pisang tersebar luas hingga 107 negara beriklim tropis. Pusat keragaman
pisang (Musa paradisiaca) berada di daerah Asia Tenggara, Papua, dan Australia Tropika (Mudzakir, 2009).
Sunarjono (2002) dalam Nisa dan Rodinah (2005), mengungkapkan kelompok pisang yang terkenal ialah yang mempunyai susunan gen tripel (AAB dan AAA),
bersifat triploid, dan tidak berbiji (partenokarpi) (Sunarjono, 2002). Huruf besar
“A”dan“B”masing-masing menggambarkan banyaknya genom (kelompok
kromosom) yang berasal dari nenek moyang pisang diploidMusa acuminatadan Musa balbisiana. Pisang kepok mengandung genom BBB, pisang mauli
mengandung genom AA dan pisang raja mengandung genom AAB.
Beberapa jenisnya (Musa acuminata,M. balbisiana, danM. ×paradisiaca) menghasilkan buah konsumsi yang dinamakan sama. Buah ini tersusun dalam
tandan dengan kelompok-kelompok tersusun menjari, yang disebut sisir. Hampir semua buah pisang memiliki kulit berwarna kuning ketika matang, meskipun ada
beberapa yang berwarna jingga, merah, hijau, ungu, atau bahkan hampir hitam (http://id.wikipedia.org/wiki/Pisang, 2012).
Pisang termasuk dalam golongan terna monokotil tahunan berbentuk pohon yang
pada bonggol yang selanjutnya tumbuh menjadi tanaman pisang (Budiman, 2009). Daun penumpu bunga berjejal rapat dan tersusun secara spiral secara spiral. Daun pelindung berwarna merah tua, berlilin, dan mudah rontok dengan panjang
10—25 cm. Bunga tersusun dalam dua baris melintang. Lima daun tenda bunga melekat sampai tinggi dan panjangnya 6—7 cm. Setelah bunga keluar akan terbentuk sisir pertama, kemudian memanjang lagi dan membentuk sisir (Satuhu
dan Supriyadi 2000).
Pisang Ambon Kuning memiliki jumlah sisir tiap tandan 8—14. Jumlah buah tiap
sisir 14—20. Panjang buah 14—20 cm, tebal kulit 2,4—3,0 mm. Daging buah berwarna putih kekuningan, tekstur lunak dan halus, serta beraroma jelas dan khas
dan rasanya manis (Gardjito dan Saifudin, 2011).
Pisang Raja Bulu memiliki daging buah agak tebal, rasanya manis, dan aromanya kuat. Pada waktu matang, warna kulit buahnya kuning berbintik-bintik cokelat, sementara warna daging buahnya putih kemerahan. Pisang Raja bulu memiliki
jumlah sisir 6—7 tiap tandan. Setiap sisir berisi sekitar 10—15 buah. Panjang buahnya ± 25 cm dengan diameter 6—6,5 cm (Supriyadi dan Suyanti, 2010).
Pisang sebagai bahan konsumsi adalah buah yang sangat bergizi yang merupakan sumber vitamin, mineral dan juga karbohidrat. Pisang dijadikan buah meja, sale
pisang, pure pisang dan tepung pisang. Kulit pisang dapat dimanfaatkan untuk membuat cuka melalui proses fermentasi alkohol dan asam cuka. Daun pisang
ternak ruminansia (domba, kambing). Sedangkan, air umbi batang pisang kepok
dimanfaatkan sebagai obat disentri dan pendarahan usus besar sedangkan air batang pisang digunakan sebagai obat sakit kencing dan penawar racun
(Direktorat Pengolahan dan Pemasaran Hasil Hortikultura, 2005).
2.2 Perbanyakan Tanaman Pisang secara Konvensional
Pisang memiliki ciri khas berbatang semu. Batang tanaman yang sesungguhnya adalah bonggol yang berada di bawah tanah ini memiliki mata tunas sebagai titik
tumbuh. Mata tunas kemudian tumbuh menjadi tunas anakan yang dapat digunakan sebagai bahan tanam selanjutnya (Suyanti dan Supriyadi, 2010).
Bibit tanaman pisang pada umumnya diperbanyak secara vegetatif, yaitu dengan menggunakan anakan yang tumbuh dari bonggol induknya. Bibit tanaman pisang
juga dapat diperoleh dari bonggol tanaman pisang yang dibelah-belah yang terdapat pada bonggol tersebut. Bibit yang diperoleh dari bonggol pisang yang dibelah-belah itu dikenal dengan nama bibitbit, sedangkan bibit yang berupa
anakan disebutsucker(Cahyono, 2010).
Tanaman pisang membutuhkan jumlah unsur hara yang besar untuk mendapatkan
hasil yang tinggi. Nitrogen, kalsium dan fosfat adalah unsur pokok yang
dibutuhkan dalam jumlah yang besar. Hal ini dapat dipenuhi melalui penanaman
hara tanaman pisang. Pupuk yang berasal dari limbah pertanian dan pupuk
kandang sangat cocok untuk tanaman pisang. Pupuk organik mampu meningkatkan struktur tanah dan bertindak sebagai sumber unsur hara.
Mikroorganisme terdapat pada sebagian besar pupuk organik dan memberikan pengaruh yang menguntungkan dalam penyerapan unsur hara (Robinson, 2006).
Pemberian pupuk anorganik juga diperlukan oleh tanaman pisang. Kandungan unsur haranya sudah tertentu, dapat diberikan dalam bentuk yang dikehendaki dan
waktu yang sesuai dengan kebutuhan unsur hara tanaman. Serta memiliki kandungan unsur hara yang relatif lebih tinggi dibandingkan pupuk organik.
Pupuk yang diperlukan tanaman pisang untuk tumbuh dan berproduksi terdiri atas tiga unsur utama, yaitu nitrogen, fosfor dan kalium. Ketiga unsur tersebut sangat
sedikit tersedia dalam tanah. Oleh karena itu, pemberian pupuk , khususnya N, P, K sangat dianjurkan guna mencukupi kebutuhan tanaman. Tanaman pisang tumbuh di tanah yang pengaturan drainasenya baik dengan kisaran pH optimalnya
5—7. Pada saat tanam dapat diberikan pupuk organik dan dilanjutkan dengan
pemberian pupuk anorganik (Cahyono, 2009).
Pupuk organik merupakan pupuk dengan bahan dasar yang diambil dari alam
dengan jumlah dan jenis unsur hara yang terkandung secara alami. Sementara pupuk anorganik merupakan pupuk buatan pabrik dengan jenis dan kadar unsur
hara yang sengaja ditambahkan atau diatur dalam jumlah tertentu (Musnamar,
Salah satu tanaman yang diperbanyak secara komersial melalui teknik kultur jaringan adalah pisang. Keunggulan bibit pisang hasil kultur jaringan
dibandingkan dengan bibit dari anakan adalah bahwa perbanyakan melalui teknik
kultur jaringan dapat mengatasi masalah penyakit layu bakteri pada tanaman pisang yang selama ini masih sulit diatasi. Hal tersebut karena bibit asal kulturin
vitromerupakan bibit yang terbebas dari penyakit sehingga dapat mencegah penyebaran penyakit di pertanaman yang baru. Ukuran bibit yang kecil
memudahkan untuk transportasi. Ukuran dan umur bibit seragam sehingga waktu
panen dapat diatur untuk kepentingan ekspor.
Perbanyakan tanaman pisang melalui teknik kultur jaringan dari satu mata tunas pisang dapat dihasilkan 500 atau lebih bibit pisang dalam waktu kurang lebih satu tahun (Yusnita, 2003).
Pembiakan tanaman secara kultur jaringan menurut George (2008), dapat dibagi
menjadi 5 tahap yang berurutan sebagai berikut:
1. Tahap 0, memilih dan menyiapkan tanaman induk untuk eksplan 2. Tahap 1, inisiasi kultur (culture establishment).
3. Tahap 2, multiplikasi atau perbanyakan propagul (bahan tanaman yang
diperbanyak seperti tunas atau embrio).
4. Tahap 3, mempersiapkan untuk transfer propagul ke lingkungan eksternal yaitu pemanjangan tunas, induksi, dan perkembangan akar.
bahan tanam dan dipindahkan ke dalam medium buatan untuk pertumbuhan atau
pemeliharaan. Bahan tanam awal atau eksplan yang digunakan untuk memulai pengulturan merupakan merupakan salah satu faktor penting yang menentukan
keberhasilan perbanyakanin vitro. Beberapa aspek penting yang harus dipertimbangkan dalam pemilihan eksplan adalah dari bagian tanaman mana eksplan diambil, umur jaringan, kesehatan tanaman atau kebersihannya dari
infestasi mikroorganisme, ukuran eksplan dan cara sterilisasi eksplan (Yusnita,
2010).
Menurut Yusnita (2003), umumnya bagian tanaman yang digunakan sebagai eksplan adalah jaringan muda yang sedang tumbuh aktif karena jaringan tanaman
yang masih muda mempunyai daya regenerasi yang tinggi, sel-selnya masih aktif membelah diri, dan relatif bersih (mengandung lebih sedikit kontaminan).
Pemilihan eksplan didasarkan oleh beberapa faktor, yaitu organ yang digunakan, waktu pengambilan eksplan, ukuran eksplan, kualitas tanaman asal eksplan, dan
umur ontogeni, serta kualitas fisiologi tanaman sumber eksplan (Wattimena,
1998).
Sumber eksplan sebagai bahan tanam harus jelas jenis dan varietasnya, serta harus sehat dan bebas dari hama penyakit. Potongan daun, potongan akar, hipokotil,
potongan batang berbuku, meristem, dan lain-lain dapat digunakan sebagai
sumber eksplan. Eksplan untuk inisiasi kultur pisang ekplan yang digunakan berupa mata tunas aktif dan mata tunas yang berada pada bonggol. Tahap inisiasi
ditujukan untuk menggandakan propagul dan memeliharanya pada keadaan
tertentu, yang sewaktu-waktu bisa dilanjutkan untuk tahap berikutnya. Pada tahap ini biasanya dibutuhkan zat pengatur tumbuh (ZPT). Tunas-tunas dari tahap
multiplikasi selanjutnya menuju tahap pengakaran dan aklimatisasi. Aklimatisasi bertujuan agar planlet mampu beradaptasi dan tumbuh dengan baik pada
lingkunganex vitro. Aklimatisasi dilakukan dengan cara mengurangi kelembaban
dan menambah intensitas cahaya secara bertahap.
Prosedur pembiakan dengan kultur jaringan baru bisa dikatakan berhasil jika planlet dapat diaklimatisasi ke kondisi eksternal dengan keberhasilan tinggi. Planlet atau tunas mikro lebih bersifat heterotrofik karena sudah terbiasa tumbuh
dalam kondisi berkelembaban sangat tinggi, aseptik, serta suplai hara mineral dan sumber energi berkecukupan. Tanaman juga memperlihatkan beberapa gejala ketidaknormalan, seperti bersifat sukulen, lapisan kultikula tipis dan jaringan
vaskulernya tidak berkembang sempurna, morfologi daun abnormal dengan tidak berfungsinya stomata sebagaimana mestinya, struktur mesofil berubah, dan aktivitas fotosintesis sangat rendah. Planlet dengan karakteristik seperti itu
mudah layu atau kering jika dipindahkan kekondisi eksternal secara tiba-tiba.
21
Media kultur merupakan salah satu faktor penentu keberhasilan kultur. Beberapa karakteristik dari kultur jaringan antara lain pengulturan dilakukan secarain vitro,
dalam kondisi aseptik, lingkungan yang terkontrol, menggunakan media berisi hara lengkap, dan sering kali menggunakan zat pengatur pertumbuhan (Yusnita,
2010).
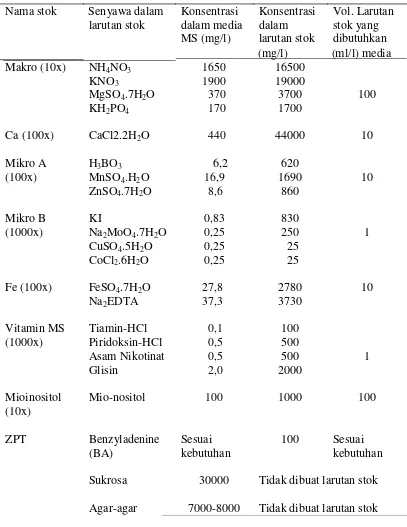
Terdapat beberapa jenis media kultur jaringan. Formulasi media yang digunakan
untuk pengulturan dalam menumbuhkan dan menggandakan tunas aksilar pisang adalah media Murashige dan Skoog (1962) yang komponennya terdiri dari
garam-garam mineral, gula, vitamin, zat pengatur tumbuh (ZPT), dan bahan pemadat media (Yusnita, 2003).
Nama stok Senyawa dalam
Ca (100x) CaCl2.2H2O 440 44000 10
Mikro A H3BO3 6,2 620
Sukrosa 30000 Tidak dibuat larutan stok Agar-agar 7000-8000 Tidak dibuat larutan stok
23
Zat pengatur tumbuh adalah senyawa organik bukan hara yang dalam konsentrasi rendah (< 1 mM) dapat mendorong, menghambat atau secara kualitatif mengubah
pertumbuhan dan perkembangan tanaman. Pengaruh sitokinin di dalamin vitro berhubungan dengan proses pembelahan sel, proliferasi tunas ketiak, dan
menghambat pertumbuhan akar tanaman, sedangkan peranan auksin dalam kultur in vitroterutama untuk pertumbuhan kalus, suspensi sel dan pertumbuhan akar (Widyastuti dan Donowati, 2008).
Strategi dalam kultur jaringan untuk perbanyakan adalah dengan mengulturkan eksplan pada media yang mengandung sitokinin (perangsang pembelahan sel)
untuk meransang pembentukan dan perbanyakan tunas, kemudian mengulturkan tunas pada media yang mengandung auksin untuk merangsang pembentukan akar (Yusnita, 2003).
Pemberian sitokinin ke dalam media kultur bisa secara tunggal, atau di kombinasi
dengan jenis sitokinin yang lain, atau dikombinasikan dengan auksin pada konsentrasi rendah. Contoh ZPT dari golongan sitokinin untuk mendorong perbanyakan tunas pisang adalahbenzyladenine(BA) dankinetin. Sedangkan
contoh ZPT golongan auksin untuk merangsang pengakaran pada tunas adalah indoleacetic acid (IAA),naphtleneacetic acid(NAA), dan indolebutyric acid
Aklimatisasi planlet dilakukan dengan menanam planlet di media campuran tanah-kompos-arang sekam atau yang sejenisnya, lalu mengatur agar kelembaban
mula-mula tinggi dan diturunkan secara bertahap, sedangkan intensitas cahaya mula-mula rendah, lalu ditingkatkan secara bertahap. Cara yang sering dilakukan
adalah menanam planlet di bak-bak atau polibag berisi media tumbuh yang diletakkan dalam bedengan bersungkup plastik, atau naungan paranet, lalu setelah beberapa hari sungkup plastik dibuka secara bertahap, atau dipindahkan ke
bedengan tanpa sungkup plastik tetapi masih bernaungan, hingga pada akhirnya bibit-bibit pisang tersebut dapat bertahan dan tumbuh dengan baik pada kondisi dengan sinar matahari penuh, dan dapat ditanam di lapangan (Hapsoro dan
Yusnita, 2012).
Ketika planlet-planlet telah berakar dengan baik, planlet-planlet tersebut harus diaklimatisasi ke lingkungan normal. Tanamanin vitroyang telah berakar ini dipindahkan dari botol-botol kultur dan dicuci dari media agar untuk
menghilangkan sumber potensial kontaminasi. Planlet kemudian
dipindahtanamkan ke media yang telah disterilisasi atau pada campuran tanah di
dalam pot-pot kecil. Pada awalnya bibit-bibit tanaman tersebut harus terhindar dari kekeringan dengan menggunakan naungan, dalam ruangan dengan
kelembaban tinggi atau disemprot dengan butiran air yang kecil. Setelah beberapa
hari akan terbentuk akar-akar yang berfungsi. Planlet-planlet secara bertahap
dapat diatasi (Hartmann, 2002).
Media tanam merupakan komponen utama dalam perbanyakan tanaman. Secara umum media tanam harus dapat menjaga kelembaban daerah sekitar akar, menyediakan cukup udara, dan dapat menahan ketersediaan unsur hara.
Planlet-planlet yang telah berakar dapat dipindahtanamkan ke dalam bedengan pipa yang berisi kompos dengan ruang udara yang cukup. Media tanam yang berasal dari kompos ini terlebih dahulu disterilisasi untuk menghilangkan infeksi
bakteri atau jamur (George, 1996). Menurut Boxus (1987) dalam George (1996), mengatakan bahwa pada campuran media tanam yang digunakan harus steril
karena infeksi jamur sering ditemukan tumbuh diatas permukaan media tanam. Hasil penelitian Sismanto (2010) pada planlet anthurium yang diaklimatisasi pada campuran media pasir malang dan arang sekam, campuran media arang sekam,
cocopeat dan kompos menghasilkan persentase tanaman hidup yang sangat tinggi yaitu 100 persen. Demikian juga pada hasil penelitian Ismaryati (2010),
keberhasilan aklimatisasi planlet pisang Tanduk dan pisang Ambon Kuning pada media tanam campuran arang sekam, pasir malang dan kompos umur 4 minggu dan 12 minggu setelah ditanam dengan menggunakan media tanah (top soil) yang
dicampur dengan media bahan organik juga sangat tinggi yaitu 100 persen.
Untuk mendapatkan media tanam yang baik dan sesuai, harus memiliki
pemahaman mengenai karakteristik media tanam yang berbeda-beda dari setiap
1. Kompos
Kompos merupakan media tanam organik yang bahan dasarnya berasal dari proses fermentasi tanaman atau limbah organik, seperti jerami, sekam, daun, rumpu, dan
sampah kota. Kelebihan dari penggunaan kompos sebagai media tanam adalah sifatnya yang mampu mengembalikan kesuburan tanah melalui perbaikan
sifat-sifat tanah, baik fisik, kimiawi, maupun biologis. Selain itu, kompos juga menjadi fasilitator dalam penyerapan unsur nitrogen (N) yang sangat dibutuhkan oleh tanaman. Kompos yang baik untuk digunakan sebagai media tanam yaitu yang
telah mengalami pelapukan secara sempurna, ditandai dengan perubahan warna dari bahan pembentuknya (hitam kecokelatan), tidak berbau, memiliki kadar air yang rendah, dan memiliki suhu ruang.
2. Sekam
Sekam adalah kulit biji padi (Oryza sativa) yang sudah digiling. Sekam padi yang biasa digunakan bisa berupa sekam bakar atau sekam mentah (tidak dibakar). Sekam bakar dan sekam mentah memiliki tingkat porositas yang sama. Sebagai
media tanam, keduanya berperan penting dalam perbaikan struktur tanah sehingga sistem aerasi dan drainase di media tanam menjadi lebih baik.
3. Pasir
Pasir sering digunakan sebagai media tanam alternatif untuk menggantikan fungsi
tanah. Sejauh ini, pasir dianggap memadai dan sesuai jika digunakan sebagai media untuk penyemaian benih, pertumbuhan bibit tanaman, dan perakaran setek
ke media lain. Sementara bobot pasir yang cukup berat akan mempermudah tegaknya batang. Selain itu, keunggulan media tanam pasir adalah kemudahan dalam penggunaan dan dapat meningkatkan sistem aerasi serta drainase media
tanam. Pasir memiliki pori-pori berukuran besar (pori-pori makro) maka pasir menjadi mudah basah dan cepat kering oleh proses penguapan. Kohesi dan
konsistensi pasir sangat kecil sehingga mudah terkikis oleh air. Dengan demikian media pasir lebih membutuhkan pengairan dan pemupukan yang lebih intensif. Hal tersebut yang menyebabkan pasir jarang digunakan sebagai media tanam
secara tunggal. Penggunaan pasir sebagai media tanam sering dikombinasikan dengan campuran bahan anorganik lain, seperti kerikil, batu-batuan, atau bahan
organik yang disesuaikan dengan jenis tanaman
Penelitian ini merupakan studi pembiakanin vitrotanaman pisang yang terdiri dari 2 percobaan yaitu:
1. Pengaruh konsentrasi BA dan varietas pisang (Ambon Kuning dan Raja Bulu) terhadap perbanyakan propagulin vitro.
2. Pengaruh campuran media tanam dan pemupukan terhadap keberhasilan
aklimatisasi dan pertumbuhan bibit pisang Ambon Kuning.
3.1 Percobaan I: Pengaruh Konsentrasi BA dan Varietas Pisang terhadap Perbanyakan Propagul in Vitro
3.1.1 Tempat dan Waktu
Penelitian dilaksanakan di laboratorium Kultur Jaringan Tanaman, Fakultas
Pertanian Universitas Lampung dari bulan Mei 2012 sampai dengan Mei 2013.
3.1.2 Eksplan dan Sterilisasi Eksplan
2,5 cm. Eksplan direndam dalam larutan 150 mg/l asam askorbat dan 50 mg/l asam sitrat selama 30 menit. Kemudian eksplan disterilkan dengan cara dimasukkan ke dalam larutan pemutihBayclin50% dan ditambah 1—2 tetes
larutan Tween 20 kemudian dikocok menggunakanshakerselama 30 menit. Eksplan lalu diperkecil ukurannya menjadi 1 cm x 1 cm x 1,5 cm. Selanjutnya
eksplan direndam sambil dikocok lagi dalam larutan 15%Bayclinselama 10 menit, lalu dibilas dengan air steril sebanyak minimal tiga kali.
3.1.3 Media Kultur
Media prekondisi dan media kultur yang digunakan adalah media MS (Murashige dan Skoog, 1962). Komponen media prekondisi adalah garam-garam MS, 30 g/l sukrosa, 0,1 mg/l tiamin-HCl, 0,5 mg/l piridoksin-HCl, 0,5 mg/l asam nikotinat, 2 mg/l glisin, dan 1 mg/l benziladenin (BA). Pemadat media digunakan 7 g/l
agar-agar .
Komponen media perlakuan sama dengan media prekondisi, kecuali bahwa konsentrasi BA yang digunakan adalah sesuai dengan perlakuan percobaan yaitu: MS + BA 2,5 mg/l, MS + BA 5 mg/l dan MS + BA 7,5 mg/l.
Tingkat keasaman media prekondisi dan media perlakuan diatur tingkat
keasamannya menjadi 5,8 menggunakan pH meter dengan penambahan KOH 1 N
Percobaan dilaksanakan dengan Rancangan Teracak Sempurna (RTS) dengan perlakuan yang disusun secara faktorial (3x2). Faktor pertama adalah berbagai konsentrasi benziladenin (BA) yaitu 2,5 mg/l; 5,0 mg/l; dan 7,5mg/l. Faktor kedua
adalah varietas pisang, yaitu Ambon Kuning dan Raja Bulu. Setiap perlakuan diulang tiga kali. Setiap satu unit percobaan terdiri dari 3 botol kultur yang
masing-masing berisi satu eksplan. Data yang diperoleh dianalisis ragam dan apabila hasil uji F nyata maka dilakukan uji lanjut dengan uji BNT 5%.
3.1.5 Penanaman Eksplan dan Subkultur
Penanaman eksplan steril dan subkultur dilakukan di dalamlaminar air flow
cabinet(LAFC) dengan kondisi aseptik. Setelah 10 hari di media prekondisi, eksplan kemudian dipindahkan ke media kultur sesuai dengan perlakuan pada masing-masing percobaan. Pencacahan mata tunas dilakukan agar mata tunas
terbelah dan menghasilkan lebih dari satu mata tunas serta menekan dominansi apikal.
Eksplan lalu disubkultur sesuai ke media perlakuan yang baru setiap 4 minggu. Eksplan yang telah memiliki tunas dipisahkan dan masing-masing ditanam pada botol yang terpisah agar mengalami multiplikasi.
Kultur diinkubasikan dalam ruang kultur pada suhu 26oC ± 2oC dengan
Pengamatan dilakukan terhadap jumlah mata tunas per eksplan dan jumlah tunas per eksplan yaitu pada minggu ke-20 setelah penanaman. Jumlah mata tunas per eksplan dihitung berdasarkan semua mata tunas yang terbentuk dari eksplan yang
memiliki ukuran panjang kurang dari 0,5 cm. Jumlah tunas per eksplan dihitung berdasarkan semua tunas yang terbentuk dari setiap eksplan. Pengamatan juga
dilakukan terhadap penampakan visual kultur pada umur 20 minggu setelah tanam.
3.2 Percobaan II. Pengaruh Campuran Media Tanam dan Pemupukan terhadap Keberhasilan Aklimatisasi dan Pertumbuhan Bibit Pisang Ambon Kuning
3.2.1 Tempat dan Waktu
Pelaksanaan percobaan ini dilakukan di Laboratorium Kultur Jaringan kemudian
dilanjutkan pelaksanaanya di rumah kaca Laboratorium Ilmu Tanaman Fakultas Pertanian Universitas Lampung dari bulan Pebruari 2012 sampai dengan Mei
2012.
3.2.2 Bahan Tanaman
Bahan tanaman yang digunakan adalah planlet pisang Ambon Kuning yang telah
Media aklimatisasi yang digunakan adalah campuran media arang sekam, pasir malang, kompos daun bambu dengan perbandingan 1:1:1 (M1), media arang sekam dan kompos dengan perbandingan 1:1 (M2) dan media pasir malang dan
kompos dengan perbandingan 1:1 (M3). Pupuk daun yang digunakan bermerek dagang Growmore biru, dengan perbandingan NPK (32:10:10) dengan dosis 2 g/l.
3.2.4 Cara Aklimatisasi
Bibit-bibit dalam botol yang sudah siap diaklimatisasi dikeluarkan dari ruang kultur kemudian diletakkan di ruang penguatan (hardening) selama 3 hari.
Tunas-tunas yang sudah berakar yang disebut planlet ini dikeluarkan dari botol dengan hati-hati agar akar dan daunnya tidak rusak.
Planlet-planlet dicuci hingga bersih di bawah air kran mengalir, terutama bagian akar dan leher akar agar bersih dari sisa-sisa media yang menempel, kemudian dicelupkan ke dalam larutan fungisida Dithane M-45 dengan konsentrasi 2 g/l.
Planlet yang sudah dicelupkan ke dalam larutan fungisida dikeringanginkan, ditanam dalam pot gelas plastik individu yang tetlah berisi media. Pot-pot
tersebut diletakkan di dalam ruangan dan dilakukan penyungkupan dengan
plastik. Sungkup plastik dibuka bertahap dimulai dengan waktu selama ± 3 jam, 6 jam, 9 jam hingga planlet tampak kuat dan kokoh. Penyiraman dilakukan satu
setelah berumur 10 hari. Lantai bak tanam ditutup dengan sekam yang telah dicuci bersih dan direndam Dithane M-45 dan ditaburi furadan.
Pemberian pupuk Growmore dilakukan pada saat bibit-bibit pisang berumur 2 minggu sebanyak 20 ml per tanaman sesuai dengan perlakuan. Bibit-bibit pisang
yang tidak mendapatkan perlakuan pupuk dilakukan penyiraman setara dengan yang memperoleh perlakuan pemupukan.
Pemberian perlakuan pemupukan dilakukan hingga minggu ke-7. Bibit-bibit pisang yang sudah teraklimatisasi tersebut kemudian dipindahkan ke polibeg
berukuran 3 kg dengan menggunakan media campuran tanah (top soil) dan media bahan organik kompos daun untuk pembesaran bibit dengan perbandingan 1:1.
Bibit-bibit pisang dalam polibeg yang tidak mendapat perlakuan pemupukan pada umur 2 bulan atau 8 minggu mendapat perlakuan yang sama dengan bibit-bibit
pisang yang diberikan perlakuan pemupukan Growmore hingga bibit berumur 1 bulan atau 4 minggu di pembibitan. Pengamatan dilakukan kembali setelah bibit-bibit tanaman pisang berumur 12 minggu sejak dikeluarkan dari botol.
3.2.5 Rancangan Percobaan
Percobaan II ini dilaksanakan dengan Rancangan Teracak Sempurna (RTS) dengan perlakuan secara faktorial (3x2). Faktor pertama adalah berbagai
perbandingan 1:1). Faktor kedua adalah pemupukan Growmore (32:10:10) yaitu: P0= Tanpa pemupukan dan P1= Dengan pemupukan.
Setiap perlakuan diulang tiga kali. Setiap satuan percobaan terdiri dari sepuluh pot yang masing-masing berisi satu planlet. Data yang diperoleh dianalisis ragam
dan apabila hasil uji F nyata maka dilakukan uji lanjut dengan uji BNT 5%.
3.2.6 Pengamatan
Pada saat bibit-bibit pisang berumur 8 minggu dan 12 minggu setelah tanam
dilakukan pengamatan sesuai dengan variabel pengamatan, yaitu persentase hidup, tinggi tanaman (cm), jumlah daun, tingkat kehijauan daun pisang, bobot
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil Percobaan I dan II dapat disimpulkan sebagai berikut:
1. Baik konsentrasi BA, varietas pisang maupun interaksi antar keduannya berpengaruh terhadap pembentukan mata tunas, tunas dan propagul per
eksplan. Jumlah tunas dan propagul per eksplan terbanyak didapatkan pada perlakuan BA 5 mg/l. Pisang ambon Kuning menunjukkan daya regenerasi
mata tunas, tunas dan propagul yang lebih tinggi daripada pisang Raja Bulu. Jumlah tunas dan propagul terbanyak pada pisang Ambon Kuning pada perlakuan BA 5 mg/l sebesar 25,6 tunas dan 40,7 propagul per eksplan,
sedangkan pada pisang Raja Bulu adalah 1,9 tunas dan 12,3 propagul per eksplan.
2. Semua perlakuan campuran media aklimatisasi baik dengan pemupukan atau tanpa pemupukan menghasilkan 100% planlet pisang Ambon Kuning yang teraklimatisasi. Campuran media aklimatisasi tanam berpengaruh terhadap
tinggi tanaman dan jumlah daun bibit pisang, namun tidak berpengaruh terhadap tingkat kehijauan daun, bobot tanaman dan panjang akar. Pemupukan planlet dengan NPK (32:10:10) pada konsentrasi 2 g/l
antara campuran media dan pemupukan dalam pengaruhnya terhadap pertumbuhan planlet.
5.2 Saran
Pemberian BA 5 mg/l pada media dasar MS dalam multiplikasi pisang Raja Bulu menghasilkan jumlah mata tunas terbanyak tetapi untuk menghasilkan jumlah
tunas yang tinggi membutuhkan waktu yang cukup lama. Oleh karena itu disarankan untuk mengkombinasikan dengan jenis sitokinin yang lainnya untuk
DAFTAR PUSTAKA
Al Amin, M.D. dan M.R Karim, M.R. Amin, S. Rahman dan N.M Mamun. 2009. in vitro micropropagation of banana (Musa spp). Bangladesh. Agril.Res. 34(4): 645-659
Anegra, R. 2008. Pengaruh Benziladenin (BA) dan Jenis Pemadat Media terhadap Perbanyakan Tunas Aksilar Pisang Ambon Kuning secara in vitro. Skripsi Sarjana Pertanian. Jurusan Budidaya Pertanian. Fakultas Pertanian. Universitas Lampung.
Badan Pusat Statistik. 2013. Produksi Buah-Buahan Menurut Provinsi (Ton) 2012. http://www.bps.go.id/tab sub/view.php?kat=3& tabel=1&1d subyek=55¬ab=1.
Bhasole, U.P, S.V. Dubhashi, N.S. Mail dan H.P. Rathod. 2011. In vitro shoot multiplication in different species of banana. Asian Journal of Plant Scienceand Research. 1(3): 23-27
Budiman, I. 2009. Pengembangan digital library biologi.
http://www.hortikultura.go.id//www.egiplikasi. Diakses tanggal 1 Maret 2012.
Cahyono, B. 2009. Pisang, Usaha Tani dan Penanganan Pascapanen. Penerbit Kanisius. Yogyakarta. 112 hlm.
Chikezie, U.N.Y. 2012. Effect of ascorbic acid on blackening and sprouting of Musa spp shoot tips. ISABB Journal of Biotechnology and Bioinformatics. 2(2): 11-17
Cronaeur, S.S. and A.D. Krikorian. 1984. Rapid multiplication of bananas and plaintains by in vitro shoot tip culture. Horticulture Science. 19: 234-235 Damayanti, F dan Samsurianto. 2010. Konservasi in vitro plasma nutfah untuk
aplikasi di bank gen.Bioprospek. 7(2):1-6
Direktorat Hasil dan Pemasaran Hortikultura. 2006. Road Map Pisang, Pasca Panen, Pengelolaan dan Pemasaran Hasil Pisang. 14 hlm.
Direktur Budidaya dan Pascapanen Buah. 2012. Pedoman Penanganan Pascapanen Pisang. Jakarta. 93 hlm.
Fatimah, S. N. 2008. Efektifitas Air Kelapa dan Leri terhadap Pertumbuhan Tanaman Hias Bromelia (Neoregelia carolinae) pada Berbagai Media yang Berbeda. Skripsi. UMS.
Gardjito, M dan Saifudin. 2011. PenangananPascapanen Buah-buahan Tropis. Penerbit Kanisius. Jakarta. 208 hlm.
George, E.F. 1996. Plant Propagation by Tissue Culture In Practice. 2nd edition. Edington, Wilts, England: Exegetics Ltd. 1361 hlm
George, E. F., Michael A. Hall, and Geert-Jan De Klerk. 2008. Plant Propagation by Tissue Culture. 3rd Edition. Volume 1. Springer. Dordrecht. 504 hlm.
Hartmann, H.T., D.E. Kester, F.T. Davies dan R.L. Geneve. 2002. Part IV Cell and Tissue Culture Propagation. In Plant Propagation Principle and Practices. 7th Edition. Upper Saddle River. New Jersey. hlm 708
Hirimburegama, K dan N. Gamage. 1997. Cultivar specificity with respect to in vitro micropropagation of Musa spp. (banana and plaintain). Horticultural Science. 75:205-211.
Http://agritekno.tripod.com/growmore.htm. Diakses tanggal 11 Pebruari 2013. Http://id.wikipedia.org/wiki/pisang. 2012. Diakses tanggal 11 Pebruari 2013
Http://kangtoo.wordpress.com/macam-macam-media-tanam/. Diakses 4 Desember 2013.
Hobir, Mariska, Kosmiatin dan Rusyadi. 1997. Pertumbuhan dan produksi serat tanaman abaka asal kultur jaringan.Jurnal Penelitian Tanaman Industri. III(3): 87-91
Ismaryati, T. 2010. Studi Multiplikasi Tunas, Pengakaran dan Aklimatisasi pada Perbanyakan in vitro Tanaman Pisang Raja Bulu, Tanduk, dan Ambon Kuning. Tesis Pascasarjana. Magister Agronomi. Universitas Lampung Jumari dan A. Pudjorianto. 2000. Kekerabatan Fenetik Kultivar Pisang di Jawa.
Kalimuthu, K., M. Saravanakumar, and R. Senthilkumar. 2007. In vitro micropropogation of Musa sapientum L. (Cavendish Dwarf). African Journal of Biotechnology 6 (9): 1106—9.
Komponen Media Tanam. 2008. http://www.emirgarden.com.
Kosky, R.G dan L.A. Barranco, B.C. Perez, D. Daniels, M. Reyez Vega, Manuel de Feria Silva. 2006. Trueness to-type and yield components of the banana hybrid cultivar FHIA-18 plants regenerated via somatis embryogenesis in a bioreactor.Euphytica. 150:63-68
Marlina, N dan D. Rusnandi. 2007. Teknik Alimatisasi Planlet Anthurium pada Beberapa Media Tanam. Buletin Teknik Pertanian. Vol 12(1): 38—40. Meydayanti, H.YS. Tanpa tahun. Tanggapan Beberapa Klon dan Media Tanam
terhadap Pertumbuhan dan Pembungaan Mawar Mini(Rosa hybrid L.) Skripsi Sarjana Pertanian. Fakultas Pertanian. Universitas Nasional. Mudzakir, Z. 2009. Kultur Jaringan (Tissue Culture): Perbanyakan Pisang
Cavendish Secara Kultur Jaringan. Dalam
http://zacky-zone89.blogspot.com/2009/06/perbanyakan-pisang-cavendish-secara.html
Muhammad, A dan Iqbal Hussain, S.M. Saqlan Naqvi, Hamid Rashid. 2004. Banana planlet production through tissue culture. Pak .J. Bot. 36(3):617-620.
Muharam, A dan I Djatnika, Yoyo Sulyo, H. Sunarjono. 1992. Pisang sebagai komoditas andalan, prospek dan kendalanya. Pusat Penelitian dan pengembangan Hortikultura Lembang. 5 hlm
Musnamar, E.I. 2004. Pupuk Organik. Penebar Swadaya. Jakarta. 72 hlm
Nisa, C. dan Rodinah. 2005. Kultur Jaringan Beberapa Kultivar Buah Pisang (Musa paradisiaca L.) dengan Pemberian Campuran NAA dan Kinetin. Bioscientiae 2(2): 23-6.
Nisyawati dan K. Kariyana. 2013. Effect of ascorbic acid, activated choarcoal and light duration on shoot regeneration of banana cultivar barangan (Musa acuminata) in vitro culture. IJRAS. 15(1):13-17
Pujaratno. 2010. Budidaya Pisang. http://bpp_kedamen.com/2010/10/budidaya pisang-html
Rahmawan, M. 2010. Pengaruh Media Tanam Tanah dan Pasir Terhadap Pertumbuhan Tanaman Jagung.
Robinson, J.C. 2006. Bananas and Plaintains. CABI Publishing. London. UK. 238 hlm.
Roy, O.S, Bantawa, P, Ghosh,S.K, da Silva, J.A.T, DebGhosh, P, Mondal, T.K. 2010. Micropropagation and field performance of ‘Malbhog’ (Musa paradisiaca, AAB group): a popular banana cultivar with high keeping quality of North East India. Tree and Forestry Science and Biotechnology. 4. 52-58.
Sari, E. P. 2012. Multiplikasi Tunas Pisang Ambon Kuning Sebagai Respons Terhadap Konsentrasi Benzyladenine dan Indole-3-Acetic Acid. Skripsi. Universitas Lampung. Bandar Lampung.
Satuhu, S dan A. Supriyadi. 2000. Pisang Budidaya. Pengolahan, dan Prospek Pasar. Penebar Swadaya. Jakarta. 124 hlm.
Sismanto, 2010. Studi Perbanyakan tanaman Anthurium Gelombang Cinta (Anthurium plowmanii) secara in Vitro. Tesis Pascasarjana Magister Agronomi. Universitas Lampung.
Supriyadi, A dan Suyanti. 2010. Pisang: Budidaya, Pengolahan, dan Prospek Pasar. Penebar Swadaya. Jakarta. 132 hlm.
Taiz, L dan E. Zeiger, 2010. Plant Physiology. Sinaner Associates Inc. Publisher. Sunderland. Massachusets. USA. 782 hlm.
Wattimena, G.A. 1988. Zat Pengatur Tumbuh Tanaman. Pusat Antar Universitas. Institut Pertanian Bogor. Bogor. 145 hlm.
Widyastuti, N dan Donowati. 2008. Peranan Beberapa Zat Pengatur Tumbuh (ZPT) Tanaman pada Kultur in vitro. Saint dan Teknologi BPPT. 3(5): 08.
Wulandari, R.A. 2006. Produksi Benih Hortikultura melalui Teknik Kultur Jaringan. Makalah yang disajikan dalam Seminar Perbenihan Hortikultura di Solo Jawa Tengah tanggal 24 April 2006. 11 hlm.
Yusnita, K. Mantja, dan D. Hapsoro. 1996. Pengaruh benziladenin, adenin, dan asam indolasetat terhadap Perbanyakan Tunas Pisang Ambon Kuningsecara in Vitro. Agrotropika 1(1): 29-32
Yusnita. 2003. Kultur Jaringan: Cara Memperbanyak Tanaman secara Efisien. Agromedia Pustaka. Jakarta. 105 hlm.
Yusnita dan D. Hapsoro. 2012. Eksplorasi, Karakterisasi, Seleksi, dan
Perbanyakan Klonal in vitro untuk Mendapatkan Genotipe-genotipe Unggul Pisang Komersial Lampung. Penelitian Unggulan Unila. 22 hlm.