ABSTRACT
EFFECT of KEPOK BANANA PEEL (Musa acuminata) to HEPATOCYTE of RAT (Rattus norvegicus) INDUCED by ASPIRIN
By
DESTI NURUL QOMARIYAH
Hepatotoxicity is liver damage caused disruption of physiological functions of the liver. The damage that occurs can be caused by an infectious agent and the use of drugs. One drug that can trigger hepatotoxicity is aspirin. Hepatotoxicity occurred along with an increase in the incidence of diseases that require long aspirin therapy. Liver damage can be overcome by using medicinal plants (herbal). Plants containing rich in antioxidants as a hepatoprotective agent is a kepok banana peel. The aim of this study was to determine the effect of kepok banana peel extract to hepatocyte of rat induced by aspirin. This study method is experimental with randomized controlled design with a pattern posttest control group design. The samples of this study were 25 white rats (Rattus norvegicus) Sprague Dawley strain and calculated based on the frederer’s formula. The result showed that the average damage of hepatocyte on rat induced by aspirin is 88%, whereas the effective dose kepok banana peel extract (100 mg/kg) got damage by 22%. The conclusion of this study was aspirin at toxic doses can cause liver damage and kepok banana peel extract is able to provide optimal improvement on liver damage induced by aspirin.
ABSTRAK
PENGARUH EKSTRAK KULIT PISANG KEPOK (Musa acuminata) TERHADAP HEPAR TIKUS (Rattus norvegicus) YANG DIINDUKSI ASPIRIN
Oleh
DESTI NURUL QOMARIYAH
Hepatotoksisitas adalah kerusakan pada hati yang menyebabkan terganggunya fungsi kerja hati secara fisiologis. Kerusakan yang terjadi dapat disebabkan oleh agen infeksius dan penggunaan
obat−obatan. Salah satu obat yang dapat mencetuskan terjadinya hepatotoksisitas adalah aspirin.
Hepatotoksisitas yang terjadi seiring dengan peningkatan angka kejadian penyakit yang membutuhkan terapi aspirin yang lama. Kerusakan hati ini dapat diatasi dengan menggunakan
tanaman−tanaman obat (herbal). Tanaman yang mengandung kaya antioksidan sebagai zat hepatoprotektor adalah kulit pisang kepok. Tujuan dari penelitian ini adalah untuk mengetahui pengaruh dari pemberian ekstrak kulit pisang kepok terhadap hepar tikus yang diinduksi aspirin. Metode penelitian ini adalah eksperimental dengan rancangan acak terkontrol dengan pola post test control group design. Sampel penelitian adalah tikus putih (Rattus norvegicus) galur Sprague dawley berjumlah 25 ekor yang dihitung berdasarkan rumus frederer. Dari hasil penelitian didapatkan bahwa rerata kerusakan hepar tikus yang diinduksi aspirin sebesar 88%, sedangkan pada pemberian dosis efektif ekstrak kulit pisang kepok (100 mg/kgBB) didapatkan kerusakan sebesar 22%. Kesimpulan dari penelitian ini adalah pemberian aspirin pada dosis toksik dapat menyebabkan kerusakan hepar dan ekstrak kulit pisang kepok mampu memberikan perbaikan yang optimal pada kerusakan hepar yang diinduksi aspirin.
PENGARUH EKSTRAK KULIT PISANG KEPOK (Musa acuminata) TERHADAP HEPAR TIKUS (Rattus norvegicus) YANG DIINDUKSI ASPIRIN
Oleh
DESTI NURUL QOMARIYAH
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA KEDOKTERAN
Pada
Program Studi Pendidikan Dokter Fakultas Kedokteran Universitas Lampung
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
PENGARUH EKSTRAK KULIT PISANG KEPOK (Musa acuminata)
TERHADAP HEPAR TIKUS (Rattus novergicus) YANG DIINDUKSI ASPIRIN
Skripsi
Oleh
Desti Nurul Qomariyah
FAKULTAS KEDOKTERAN
UNIVERSITAS LAMPUNG
BANDAR LAMPUNG
v DAFTAR GAMBAR
Gambar 1 Histologi hati normal ... ... ... ... ... ... ...9
Gambar 2 Lobulus Hati ... ... ... ... ... ... ... ...10
Gambar 3 Kerangka Teori... ... ... ... ... ... ... ...24
Gambar 4 Kerangka Konsep... ... ... ... ... ... ... ....24
Gambar 5 Diagram Alur Penelitian... ... ... ... ... ... ....36
Gambar 6 Sel hepar tikus putih kelompok K+...40
Gambar 7 Sel hepar tikus putih kelompok K−... ... ... ... ...41
Gambar 8 Sel hepar tikus putih kelompok K3... ... ... ... ...41
Gambar 9 Sel hepar tikus putih kelompok K4... ... ... ... ...42
Gambar 10 Sel hepar tikus putih kelompok K5... ... ... ... ...42
DAFTAR ISI
Halaman
DAFTAR ISI ... i
DAFTAR TABEL... iv
DAFTAR GAMBAR ... v
DAFTAR LAMPIRAN ... vi
BAB I PENDAHULUAN 1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 4
1.3Tujuan Penelitian ... 4
1.4Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA 2.1 Hati ... 6
2.1.1 Anatomi Hati ... 6
2.1.2 Fisiologi Hati ... 7
2.1.3 Histologi Hati ... 9
2.1.4 Histopatologi Hati ... 13
2.2 Pisang Kepok ... 16
2.2.1 Klasifikasi... 16
ii
2.2.3 Kandungan Kulit Pisang Kepok dan Fungsinya ... 17
2.3 Aspirin ... 18
2.4 Toksisitas Apsirin pada Hepar ... 20
2.5 Tikus Putih (Rattus norvegicus) galur Sprague dawley ... 21
2.5.1 Klasifikasi Tikus Putih ... 21
3.4.3.1 Alat dalam pembuatan preparat histopatologi 29 3.5 Prosedur Penelitian ... 29
iii
3.5.2 Prosedur pemberian ekstrak kulit pisang kepok ... 30
3.5.3 Prosedur perlakuan ... 31
3.6 Diagram Alur penelitian……… 36
3.7 Identifikasi Variabel dan Definisi Operasional Variabel .... 37
3.7.1 Identifikasi Variabel ... 37
3.7.1.1 Variabel Independen ... 37
3.7.1.2 Variabel Dependen……… 37
3.7.2 Definisi Operasional Variabel………. ... 37
3.8 Analisis Data ... 38
3.9 Ethical Clearance ... .. 38
BAB IV. HASIL DAN PEMBAHASAN 4.1Hasil Penelitian……… 39
4.2 Pembahasan……… 47
BAB V. KESIMPULAN DAN SARAN 5.1 Kesimpulan……… 52
5.2 Saran………... 52
vi DAFTAR SINGKATAN
ATP : Adenosin Tri Phospate
BPOM : Badan Pengawas Obat dan Makanan
COX : Cyclooxygenase
EtOH : Etanol
FMIPA : Fakultas Matematika dan Ilmu Pengetahuan Alam
GST : Glutation S−Transferase
HE : Hematoksilin
IACUC : Institusional Animal Care and Use Committee
IP : Intraperitoneal
iv DAFTAR TABEL
Tabel 1 Definisi Operasional Variabel... ... ... ... ... ...37
Tabel 2 Hasil persentase kerusakan hepar tikus putih... ... ... ...43
Tabel 3 Hasil rata rata gambaran histopatologi hepar... ... ... ...44
Tabel 4Hasil analisis Saphiro−Wilk... ... ... ... ... ... ...46
Bismillahirrahmannirrahim…
Kupersembahkan karya ini untuk kedua orang tuaku tercinta, kakak-kakak ku
terkasih dan semua sahabat-sahabat ku tersayang.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 29 Desember 1994, dari pasangan Ayahanda Purn.
Slamet Ali Yunus dan Ibunda Sri Murtiningsih dan merupakan anak ketiga dari tiga bersaudara
(Kakak Evi Febriani dan Dewintha Airene Novianti).
Pendidikan Taman Kanak-kanak (TK) diselesaikan di TK Sukatani Permai Depok pada tahun
2000, Sekolah Dasar (SD) diselesaikan di SDN Sindang Karsa I Depok pada tahun 2006,
Sekolah Menengah Pertama (SMP) diselesaikan di SMPN 11 Depok pada tahun 2009, dan
Sekolah Menengah Atas (SMA) diselesaikan di SMAN 1 Depok pada tahun 2012.
Tahun 2012, penulis terdaftar sebagai mahasiswa Fakultas Kedokteran Universitas Lampung.
Selama menjadi mahasiswa penulis pernah aktif pada organisasi PMPATD Pakis Rescue Team,
PTBMMKI (Perhimpunan Tim Bantuan Medis Mahasiswa Kedokteran Indonesia) dan Forum
SANWACANA
Puji syukur Penulis ucapkan kehadirat Allah SWT, karena atas rahmat dan
hidayah-Nya skripsi ini dapat diselesaikan. Shalawat serta salam semoga selalu
tercurahkan kepada Nabi Muhammad S.A.W, keluarga, sahabat dan kita para
pengikutnya yang setia hingga akhir zaman.
Skripsi Ini Berjudul “PENGARUH EKSTRAK KULIT PISANG KEPOK
(Musa acuminata) TERHADAP HEPAR TIKUS (Rattus norvegicus) YANG
DIINDUKSI ASPIRIN” adalah salah satu syarat untuk memperoleh gelar sarjana
Kedokteran di Universitas Lampung.
Dalam kesempatan ini, penulis mengucapkan terima kasih kepada:
1. Prof. Dr. Ir. Hasriadi Mat Akin M.P. selaku Rektor Universitas Lampung.
2. Dr. dr. Muhartono, M. Kes, Sp.PA selaku Dekan Fakultas Kedokteran
Universitas Lampung sekaligus Pembimbing Utama yang sudah bersedia
meluangkan waktu dan kesediaannya untuk memberikan bimbingan,
kritik, saran serta nasihat yang bermanfaat dalam proses penyelesaian
skripsi ini;
3. dr. Khairun Nisa Berawi, M. Kes, AIFO selaku Pembimbing Kedua yang
telah bersedia untuk meluangkan waktu, memberikan bimbingan, kritik,
saran, dan nasihat kepada saya untuk senantiasa menyempurnakan
4. Prof. Dr. dr. Efrida Warganegara, M. Kes, Sp.MK selaku Pembahas yang
telah bersedia meluangkan waktu, memberikan masukan, kritik, saran dan
nasihat bermanfaat dalam penyelesaian skripsi ini;
5. dr. Mukhlis Imanto, Sp.THT selaku Pembimbing Akademik atas waktu
dan bimbingannya selama proses pembelajaran di Fakultas Kedokteran
Universitas Lampung;
6. Seluruh Staf Dosen FK Unila atas ilmu yang telah diberikan kepada
penulis untuk menambah wawasan yang menjadi landasan untuk mencapai
cita-cita;
7. Seluruh staf pengajar program studi pendidikan dokter unila atas ilmu
yang telah diberikan kepada saya untuk menambah ilmu pengetahuan yang
menjadi landasan untuk mencapai cita-cita;
8. Seluruh Staf Tata usaha, administrasi, akademik, pegawai dan karyawan
FK Unila;
9. Ayahanda tercinta, Purn. Slamet Ali Yunus terima kasih atas doa, kasih
sayang, nasihat serta bimbingan yang telah diberikan untuku, serta selalu
mengingatkanku untuk selalu mengingat Allah SWT. Semoga Allah SWT
selalu melindungi dan menjadikannya ladang pahala;
10.Ibunda, Sri Murtiningsih, terima kasih atas doa, kasih sayang, nasihat serta
bimbingan yang telah diberikan untuku, setiap doa yang terlontar selalu
menjadi penguat untukku menjalani hari-hariku disini
11.Kakak-kakak saya, mbak Ani dan mbak Novi atas segala doa dan motivasi
12.Keluargaku di Lampung, Bukan Genk (Andika Yusuf, Fairuz
Rabbaniyyah, Farida Hakim, Ferina Nur Haqiqi, Gheavani Legowo, Hani
Zahiyyah, Hanifah Rahmania, Idzni Mardhiyah, Nico Aldrin, Nindriya
Kurniandari, Ratna Agustina) terimakasih atas segala keceriaan, pelajaran
hidup, semangat, canda tawa, tangis dan segala ilmu yang telah diberikan.
Uhibukifillah, till we meet again in……….Jannah.
13.Tim penelitian saya (Deborah Natasha dan Fauziah Paramitha) atas
kerjasamanya dalam melakukan penelitian ini selama 2 bulan penuh
walaupun lelah menghampiri namun tetap bersemangat untuk
menyelesaikan penelitian ini dengan baik dan maksimal;
14.Sahabat-sahabat saya GP (Adietya Bima, Alexander Dicky, Bobi Kurnia,
Fairuz Rabbaniyah, Ivani ridwan, Karina Nellova, Luqmanul Hakim, M.
Ridho Ansori, Nico Aldrin, Radian Pandhika) atas segala kegilaan dan
momen kebahagiaan yang dapat menghilangkan beban pikiran selama ini.
15.Sahabat-sahabat Pakis alias Idak Galau alias Cewetngets (Ade Marantika,
Ajeng Defri, Amri Yusuf, Debby Aprilia, Elly Rahmawati, Istigfariza,
Karina Nellova, Leon L. Gaya, M. Ridho Ansori, Martin Paskal, Ria Rizki
Jayanti, Septyne Rahayuni, Silvi Qiroatul, Singgih Suhan Nanto,
Zygawindi Nur Hayati) atas segala keceriaan, perjuangan MUNAS
JAMNAS 2015 yang tidak akan pernah terlupakan, tawa canda dan kabum
tinut tinut yang tiada hentinya.
16. Teman-teman sejawat angkatan 2012 yang tidak bisa disebutkan satu per
17.Kakak-kakak dan adik-adik tingkat (2002-2015) yang sudah memberikan
semangat kesatuan Fakultas Kedokteran UNILA.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kata sempurna.
Semoga penelitian yang sederhana ini dapat memberikan wawasan dan manfaat
bagi kita semua. Aamiin.
Bandar Lampung, Desember 2015
Penulis
BAB I PENDAHULUAN
1.1 Latar Belakang Masalah
Hepatotoksisitas merupakan kerusakan pada hati yang berkaitan dengan
gangguan fungsi kerja hati, yang dapat disebabkan oleh agen infeksius dan
penggunaan obat−obatan (Victor, 2006). Salah satu obat yang dapat
mengakibatkan hepatotoksisitas adalah aspirin (Katzung et al., 2009). Aspirin
termasuk golongan salisilat, salah satu jenis nonsteroidal anti−inflammatory
drugs atau NSAIDs yang banyak digunakan untuk pengobatan nyeri ringan
sampai sedang. Efek aspirin antara lain sebagai analgesik (melawan sakit dan
nyeri), anti piretik (menurunkan demam), anti inflamasi serta anti koagulan
(Nuraeni, 2007).
Dewasa ini terjadi peningkatan pemakaian aspirin yang berbanding lurus dengan
angka kejadian penyakit yang mebutuhkan terapi aspirin dalam kurun waktu
yang panjang. Salah satu contoh penyakit tersebut adalah penyakit
kardiovaskuler. Penyakit kardiovaskuler memiliki angka kejadian 57,9%, yang
2
Hepatotoksisitas akibat aspirin dapat terjadi akibat penggunaannya dalam kurun
waktu lama atau melebihi dosis (Katzung et al., 2009). Kerusakan hati yang
disebabkan oleh aspirin yaitu menghambat metabolisme aerob glukosa di hepar
sehingga terjadi gangguan fungsi hati dalam melakukan kinerjanya (Irvanda,
2007). Kerusakan hati ini dapat diatasi dengan menggunakan tanaman−tanaman
obat (Kemenkes, 2011).
Tanaman obat dilaporkan lebih aman dibandingkan dengan obat sintetik (Javed
et al., 2006). Indonesia yang beriklim tropis merupakan negara dengan
keanekaragaman hayati terbesar kedua di dunia setelah Brazil. Indonesia
memiliki 25.000−30.000 spesies tanaman yang merupakan 80% dari jenis
tanaman di dunia dan 90% dari jenis tanaman di Asia. Hasil inventarisasi yang
dilakukan PT Eisai pada 1986 terdapat sekitar tujuh ribu spesies tanaman di
Indonesia yang digunakan masyarakat sebagai obat khususnya oleh
pengembangan obat tradisonal Indonesia menjadi fitofarmaka industri jamu dan
didaftarkan ke Badan Pengawas Obat dan Makanan (BPOM) Republik Indonesia
sebanyak 283 spesies tanaman (Warintek, 2011).
Tanaman yang saat ini sedang dikembangkan penelitiannya adalah tanaman
pisang (Imam et al., 2011). Salah satu provinsi penghasil pisang terbanyak di
Indonesia adalah Lampung yang mencapai jumlah produksi sebanyak 5.037.472
3
Sepertiga bagian dari seluruh total produksi tersebut merupakan kulit pisang
(Hartono, 2013).
Pada penelitian yang dilakukan oleh Fatemeh dikemukakan bahwa secara in
vitro kulit pisang memiliki aktivitas antioksidan yang lebih tinggi dibandingkan
dengan bagian tanaman pisang lainnya. Aktivitas antioksidan pada kulit pisang
mencapai 94,25% pada konsentrasi 125 µ g/ml sedangkan pada bagian buah
pisang hanya sekitar 70% pada konsentrasi 50 mg/ml (Fatemeh et al., 2012;
Shodehindeet al., 2013). Antioksidan yang dimiliki oleh kulit pisang antara lain
flavonoid dan fenolik memiliki manfaat sebagai hepatoprotektor melalui
mekanisme detoksifikasi dengan jalan meningkatkan ekspresi enzim Glutation
S−Transferase(GST) yang mampu meningkatkan aktivitas antioksidan endogen
hati (Mahardikasari, 2013).
Peneliti melihat dengan adanya potensi dari provinsi Lampung ini sebagai
sumber kulit pisang dan adanya masalah hepatotoksisitas yang ditimbulkan oleh
aspirin. Berdasarkan hal tersebut maka peneliti mempunyai keinginan untuk
menguji ekstrak kulit pisang kepok pada gambaran histopatologi hepar tikus
4
1.2 Rumusan masalah
Berdasarkan latar belakang masalah yang sudah diuraikan di atas, maka pada
penelitian kali ini peneliti ingin mengetahui apakah ada pengaruh ekstrak kulit
pisang kepok terhadap perubahan histopatologi hepar tikus (Rattus norvegicus)
yang diinduksi aspirin.
1.3 Tujuan penelitian
1.3.1 Tujuan Umum
Untuk mengetahui pengaruh ekstrak kulit pisang kepok terhadap
histopatologi hepar tikus(Rattus norvegicus) yang diinduksi oleh aspirin.
1.3.2 Tujuan Khusus
1. Untuk melihat perubahan histopatologi hepar tikus (Rattus norvegicus)
yang diinduksi aspirin sebelum dan sesudah diberikan ekstrak kulit
pisang kepok.
2. Untuk mengetahui dosis efektif ekstrak kulit pisang kepok yang
berpengaruh terhadap perubahan histopatologi hepar tikus (Rattus
5
1.4 Manfaat penelitian
Adapun manfaat penelitian kali ini adalah :
1.4.1 Untuk Peneliti
Penelitian ini diharapkan dapat menambah khasanah dalam
mengembangkan bidang keilmuan sehingga dapat menjadi hal baru
sebagai referensi untuk penelitian selanjutnya.
1.4.2 Untuk masyarakat
Penelitian ini dapat memanfaatkan kandungan antioksidan yang dimiliki
kulit pisang kepok yang semula hanya dianggap limbah sehingga di sisi
lain dapat mengurangi limbah rumah tangga sehingga kesehatan
masyarakat menjadi lebih baik.
1.4.3 Untuk Pemerintah
Penelitian ini diharapkan dapat memajukan kawasan Lampung dengan
menonjolkan pisang kepok sebagai ciri khas dan senatiasa mendapat
6
BAB II
TINJAUAN PUSTAKA
2.1 Hati
2.1.1 Anatomi Hati
Hati adalah kelenjar terbesar yang terdapat dalam tubuh manusia dengan
berat kurang lebih 1,5 kg (Mescher, 2007). Hati merupakan organ viseral
terbesar yang terletak di bawah tulang rusuk (Sloane, 2004).
Hati mempunyai tekstur yang lunak, lentur, dan terletak di bagian atas
cavitas abdominalis tepat berada di bawah diaphragma. Sebagian besar hati
terletak di hemidiaphragma dextra dan profunda arcus costalis dextra
memisahkan hati dari pleura, pericardium, cor, dan pulmo (Snell, 2006).
Suplai darah pada hati (70%−80%) berasal dari vena porta yang berasal
dari lambung, usus, dan limpa, sisanya (20%−30%) disuplai oleh arteri
hepatica. Seluruh zat yang diserap melalui usus tiba di hati melalui vena
porta hepatica, kecuali lipid kompleks (kilomikron), yang diangkut melalui
7
menampung, mengubah dan mengumpulkan metabolit dari darah.
Pengeluaran ini terjadi dalam empedu, suatu sekret eksokrin dari hati yang
penting untuk pencernaan lipid di usus. Hati juga menghasilkan protein
plasma, seperti albumin, fibrinogen dan berbagai protein pembawa lainnya
(Mescher, 2007).
2.1.2 Fisiologi Hati
Hati adalah organ metabolik yang sangat penting dalam tubuh, organ ini
dilihat sebagai pabrik biokimia utama (Sherwood, 2012). Fungsi hati antara
lain:
1. Metabolisme karbohidrat
Fungsi hati dalam metabolisme karbohidrat adalah menyimpan glikogen
dalam jumlah besar, mengkonversi galaktosa dan fruktosa menjadi
glukosa, glukoneogenesis, dan membentuk banyak senyawa kimia yang
penting dari hasil perantara metabolisme karbohidrat (Guyton et al.,
2008).
2. Metabolisme lemak
Fungsi hati dalam metabolisme lemak adalah dengan mengsekresikan
garam empedu yang membantu pencernaan lemak melalui efek
deterjennya (emulsifikasi) sehingga mempermudah penyerapan lemak
8
3. Metabolisme protein
Fungsi hati dalam metabolisme protein adalah deaminasi asam amino,
pembentukan ureum untuk mengeluarkan amonia dari cairan tubuh, dan
interkonversi beragam asam amino dan membentuk senyawa lain dari
asam amino (Guytonet al.,2008).
4. Sintesis Protein Plasma
Hati memproduksi banyak protein. Kebanyakan protein tersebut
merupakan proten fase akut yaitu protein yang diproduksi dan di
sekresikan ke dalam plasma apabila terdapat rangsangan stress. Protein
lainnya yang diproduksi adalah protein yang mengangkut steroid dan
hormone lain dalam plasma serta faktor−faktor pembekuan. Protein
tersebut antara lain albumin, orosomukoid, antiproteaseɑ 1dan lain−lain
(Ganong, 2008).
5. Lain−lain
Fungsi hati yang lainnya adalah sebagai tempat penyimpanan vitamin,
dan menyimpan besi dalam bentuk ferritin. Hati membentuk zat−zat
yang digunakan untuk koagulasi darah dalam jumlah banyak dan
mengeluarkan atau mengekskresikan obat−obatan, hormon dan zat lain
9
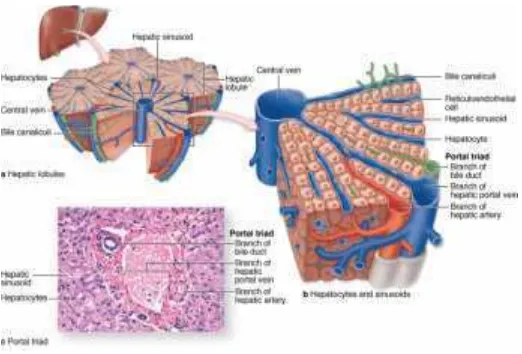
2.1.3 Histologi Hati
Sel−sel hati atau hepatosit menghasilkan sel epitel yang berkelompok
membentuk lempeng−lempeng yang saling berhubungan. Hepatosit tersusun
berupa ribuan lobulus hati kecil polihedral yang merupakan unti fungsional
dan struktural hati. Setiap lobulus memiliki tiga sampai enam area portal di
bagian perifernya dan suatu venula yang disebut vena sentral di bagian
pusatnya. Zona portal di sudut lobulus terdiri atas jaringan ikat dengan suatu
venula (cabang vena portal), arteriol (cabang arteri hepatica) dan duktus
epitel kuboid (cabang sistem duktus biliaris)−ketiga struktur yang disebut
trias porta (Mescher, 2007).
Gambar 1. Histologi hati normal (Sumber: Mescher, 2007)
Venula tersebut mengandung darah dari vena mesenterica superior dan
10
dari aorta abdominalis. Duktusnya membawa empedu yang dibuat oleh
sel−sel parenkim (hepatosit) dan akhirnya mencurahkan isinya ke dalam
duktus hepatikus. Area portal juga memiliki serabut saraf dan pembuluh
limfe. Pada beberapa hewan (misalnya babi) setiap lobulus terpisah dari
lobulus lain oleh selapis jaringan ikat sehingga lobulus dapat dikenali
dengan jelas. Pada manusia, lobulus berkontak erat hampir disetiap sisinya
dan lebih menentukan batas yang jelas antar berbagai lobulus (Mescher,
2007).
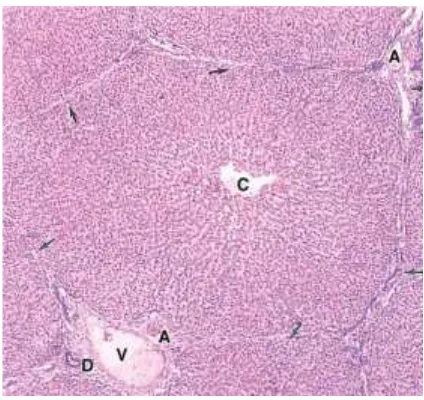
Gambar 2. Lobulus Hati. Arteriola (A), Venula (V), Duktus biliari (D), Venula sentralis (C) (Sumber: Mescher, 2007).
Hepatosit merupakan sel eksokrin dan endokrin dari lobulus hepatis.
Hepatosit membentuk suatu dinding tebal yang membatasi rongga
11
rongga sinusoidal. Komponen−komponen yang menyusun trias portal yang
terdapat pada jaringan ikat, dipisahkan oleh lapisan tipis yang
memisahkannya dengan lobul hepatis. Darah dari vena portal dan arteri
hepatis mengalir ke sinusoid dan bermuara di venula sentral. Hepatosit
mempunyai 2 bagian yaitu bagian basolateral dan bagian apikal. Bagian
basolateral mengandung banyak mikrovili dan bagian apikal membatasi
kanalikulus biliaris (Kierszenbaum & Tres, 2012).
Sinusoid lebar yang tidak teratur ini hanya terdiri atas lapisan diskontinu sel
endotel bertingkap. Sel−sel endotel terpisah dari hepatosit di bawahnya oleh
suatu lamina basal tipis yang tidak kontinu dan suatu celah perisinusoid
(celah Disse) yang sangat sempit. Mikrovili hepatosit menonjol ke dalam
celah tersebut demi terjadinya pertukaran antara sel tersebut dan plasma.
Pertukaran ini penting secara fisiologis bukan saja karena banyaknya
makromolekul (misalnya lipoprotein, albumin, fibrinogen) yang disekresi ke
dalam darah oleh hepatosit, tetapi juga karena hati mengambil dan
mengatabolisme sejumlah besar molekul besar ini (Mescher, 2007).
2.1.3.1 Hepatosit
Hepatosit merupakan sel polihedral besar, dengan enam atau lebih
permukaan, dan berdiameter 20−30 μ m. Pada sediaan yang dipulas
dengan hematosilin dan eosin (H dan E), sitoplasma hepatosit
12
berjumlah hingga 2000 per sel. Hepatosit memiliki inti sferis besar
dengan nukleolus. Sel−sel tersebut sering memiliki dua atau lebih
nukleolus dan sekitar 50% darinya bersifat polipoid, dengan dua,
empat, delapan atau melebihi jumlah kromosom diploid normal. Inti
polipoid ditandai dengan ukuran yang lebih besar, yang
proporsional dengan sifat ploid−nya (Mescher, 2007).
Hepatosit secara aktif mensintesis protein untuk kepentingan
metabolisme tubuh. oleh karena itu sel ini mempunyai banyak
sekali ribosom, retikulum endoplasma kasar dan badan golgi.
Karena kebutuhan hepatosit akan energi yang banyak, tiap−tiap sel
menandung 2000 mitokondria. Sel−sel yang terletak didekat vena
sentral mengandung dua kali lebih banyak mitokondira namun lebih
kecil dibandingkan dengan mitokondria pada hepatosit di area
periportal (Gartner & Hiatt, 2007).
Permukaan setiap hepatosit berkontak dengan dinding sinusoid,
melalui celah Disse, dan dengan permukaan hepatosit lain. Di
tempat dua hepatosit berkontak, terbentuk suatu celah tubular di
antara kedua sel ini yang disebut kanalikulus biliaris (Mescher,
13
Kanalikuli, bagian pertama sistem duktus biliaris, adalah celah
panjang berdiameter 1−2 μ m. Kanalikuli hanya dibatasi membran
plasma dari dua hepatosit, yang menjulurkan sedikit mikrovili di
bagian dalamnya. Membran sel di dekat kanalikuli ini diikat dengan
kuat oleh taut erat. Taut celah juga terdapat di antara hepatosit,
yang memungkinkan tempat komunikasi antar sel dan koordinasi
aktivitas sel−sel (Mescher, 2007).
2.1.4 Histopatologi Hati
2.1.4.1 Jejas reversibel
a. Pembengkakan Sel
Pembengkakan merupakan manifestasi pertama yang ada
hampir pada semua bentuk jejas sel, sebagai akibat pergeseran
air ekstraseluler ke dalam sel, akibat gangguan pengaturan ion
dan volume karena kehilangan Adenosin Tri Phospate (ATP)
(Chandrasoma & Taylor, 2005).
Bila air berlanjut tertimbun dalam sel, vakuol−vakuol kecil
jernih tampak dalam sitoplasma yang diduga merupakan
retikulum endoplasma yang melebar dan menonjol keluar atau
segmen pecahannya. Gambaran jejas nonletal ini
kadang−kadang disebut degenerasi hidropik atau degenerasi
14
tampak edematosa (degenerasi balon) dengan sitoplasma
ireguler bergumpal dan rongga−rongga jernih yang lebar
(Robbinset al., 2007).
b. Perlemakan Hati
Perlemakan hati merupakan akumulasi trigliserida dalam sel−sel
parenkim hati. Akumulasi timbul pada keadaan berikut:
1. Peningkatan mobilisasi lemak jaringan yang menyebabkan
peningkatan jumlah asam lemak yang sampai ke hati;
2. Peningkatan kecepatan konversi dari asam lemak menjadi
trigliserida di dalam hati karena aktivitas enzim yang terlibat
meningkat;
3. Penurunan oksidasi trigliserida menjadi asetil−koA dan
penurunan bahan keton;
4. Penurunan sintesis protein akseptor lipid (Chandrasoma &
Taylor, 2005).
2.1.4.2 Jejas Ireversibel
a. Nekrosis
Nekrosis sel dapat terjadi langsung atau dapat mengikuti
degenerasi sel (jejas reversibel). Gambaran mikroskopik dari
nekrosis dapat berupa gambaran piknosis, karioreksis, dan
15
yaitu nekrosis fokal, nekrosis zona, nekrosis submasif. Nekrosis
sel hati fokal adalah nekrosis yang terjadi secara acak pada satu
sel atau sekelompok kecil sel pada seluruh daerah
lobulus−lobulus hati. Nekrosis ini dikenali pada biopsi melalui
badan asidofilik (councilman) yang merupakan sel hati nekrotik
dengan inti piknotik atau lisis dan sitoplasma terkoagulasi
berwarna merah muda. Selain itu dapat dikenali juga pada
daerah lisis sel hati yang dikelilingi oleh kumpulan sel kupffer
dan sel radang (Chandrasoma & Taylor, 2005).
Nekrosis zona sel hati adalah nekrosis sel hati yang terjadi pada
regio−regio yang identik disemua lobulus hati, sedangkan
nekrosis submasif merupakan nekrosis sel hati yang meluas
melewati batas lobulus, sering menjembatani daerah portal
dengan vena sentralis (bridging necrosis) (Chandrasoma &
Taylor, 2005).
b. Fibrosis
Fibrosis merupakan akumulasi matriks ekstraseluler yang
merupakan respon dari cedera akut atau kronik pada hati. Pada
tahap awal, fibrosis mungkin terbentuk di dalam atau di sekitar
saluran porta atau vena sentralis atau mungkin mengendap
16
penyembuhan terhadap cedera. Cedera pada hepatosit akan
mengakibatkan pelepasan sitokin dan faktor solubel lainnya
oleh sel kupffer serta sel tipe lainnya pada hati. Faktor−faktor
ini akan mengaktivasi sel stelat yang akan mensintesis sejumlah
besar komponen matriks ekstraseluler (Robbinset al., 2007).
c. Sirosis
Berlanjutnya fibrosis dan cedera parenkim menyebabkan hepar
terbagi−bagi menjadi nodus hepatosit yang mengalami
regenerasi dan dikelilingi oleh jaringan parut. Jaringan parut ini
disebut sirosis (Robbinset al., 2007).
2.2 Pisang Kepok
Pisang merupakan buah terbanyak kedua di dunia. Sekitar 16% dari total jumlah
buah dunia merupakan pisang (FAO, 2009).
2.2.1 Klasifikasi
Klasifikasi botani tanaman pisang adalah sebagai berikut:
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Monocotyledonae
17
Genus : Musa
Spesies :Musa spp. (Warintek, 2011)
2.2.2 Jenis−jenis pisang
Jenis pisang dibagi menjadi empat:
a. Pisang yang dapat dimakan buahnya tanpa perlu diolah (dimasak)
yaitu M. paradisiaca var Sapientum, M. nana atau disebut juga M.
cavendishii, M. sinensis, misalnya pisang ambon, susu, raja,
cavendish, barangan dan mas.
b. Pisang yang dapat dimakan setelah buahnya diolah (dimasak) yaitu
M. paradisiaca forma typica atau disebut juga M. paradisiaca
normalis, misalnya pisang nangka, tanduk dan kepok.
c. Pisang berbiji yaitu M. brachycarpa yang di Indonesia dimanfaatkan
daunnya, misalnya pisang batu dan klutuk.
d. Pisang yang diambil seratnya misalnya pisang manila (abaca)
(Warintek, 2011).
2.2.3 Kandungan Kulit Pisang Kepok dan Fungsinya
Kulit pisang mempunyai kandungan flavonoid dan fenolik
(Venkatarangaiah et al., 2014). Flavonoid dan fenolik merupakan
antioksidan yang dapat berfungsi sebagai hepatoprotektor (Rahardianet
al., 2010). Kandungan antioksidan tersebut terkandung lebih banyak
18
Flavonoid merupakan senyawa polifenol yang bersifat polar sehingga
mudah larut di dalam air, etanol, methanol, butanol dan aseton.
Flavonoid mempunyai fungsi sebagai zat anti mikroba, anti inflamasi
serta anti oksidan. Melalui mekanisme penghambatan pada jalur
metabolisme asam arakhidonat, pembentukan prostaglandian dan
pelepasan histamin flavonoid berfungsi sebagai anti inflamasi atau
memperlambat proses peradangan (Mahardikasari, 2013).
Flavonoid juga memiliki manfaat sebagai hepatoprotektor (Pinzaru et
al., 2011). Cara kerja flavonoid sebagai hepatoprotektor adalah dengan
proses detoksifikasi dengan jalan meningkatkan ekspresi enzim
Gluthation S−Transferase (GST) yang merupakan antioksidan endogen
pada hati. Enzim GST berfungsi untuk detoksifikasi dengan mengubah
zat yang kurang polar menjadi lebih polar melalui pengikatan senyawa
elektron aktif yang tidak berpasangan pada zat toksik (Mahardikasari,
2013).
2.3 Aspirin
Aspirin merupakan obat yang efektif sebagai anti−inflmasi, meskipun aspirin
mungkin lebih efektif sebagai analgesik. Aspirin diabsorbsi begitu saja dan cepat
dihidrolisis menjadi asam asetat dan salisilat oleh esterase dalam jaringan dan
19
dapat menjadi jenuh sehingga fraksi yang tidak terikat meningkat seiring dengan
meningkatnya konsentrasi total. Di luar kandungan dalam tubuh total sebesar
600 mg, peningkatan dosis salisilat tersebut dapat waktu meningkatkan
konsentrasi salisilat secara tidak proporsional. Seiring meningkatnya dosis
aspirin, waktu paruh eliminasi salisilat meningkat dari 3−5 jam (untuk dosis 600
mg/hari) menjadi 12−16 jam (dosis >3,6 gr/hari). Alkalinisasi urine
meningkatkan laju ekskresi salisilat bebas dan konjugatnya yang larut dalam air
(Katzunget al., 2009).
Aspirin merupakan penghambat nonselektif untuk kedua isoform COX
(cyclooxygenase), tapi salisilat lebih tidak efektif dalam menghambat kedua
isoform tersebut. Salisilat non−terasetilasi dapat bekerja sebagai penangkap
radikal oksigen. Aspirin secara ireversibel menghambat COX dan menghambat
agregasi trombosit, sementara salisilat non−terasetilasi tidak. Hal ini disebabkan
aspirin secara ireversibel menghambat COX trombosit sehingga antitrombosit
aspirin bertahan selama 8−10 hari (sesuai masa hidup trombosit) (Katzunget al.,
2009).
Aspirin dapat menurunkan insidensi serangan iskemik transien, angina tak stabil,
trombosis arteri koronaria dengan infark miokard, dan trombosis pascagraft pirau
20
2.4 Toksisitas aspirin pada hepar
Golongan salisilat (termasuk aspirin) memproduksi efek toksik di hati dengan
dua cara. Proses pertama adalah hepatotoksisitas yang diinduksi oleh dosis
aspirin dan biasanya terjadi pada kadar plasma aspirin di atas 150 μ g/l. Efek
toksik di hati yang kedua sering terjadi pada pasien dengan abnormalitas jaringan
ikat. Hanya sekitar 5% dari populasi golongan kedua yang mempunyai gejala
seperti hepatomegali, anoreksia, nausea, danjaundice(Irvanda, 2007).
Pengaruh aspirin dalam penghambatan proses fosforilasi oksidatif serupa dengan
pengaruh yang ditimbulkan 2,4−dinitrofenol. Pada dosis toksik, aspirin dapat
menghambat metabolisme aerob dari beberapa enzim dehidrogenase di hepar dan
jaringan lainnya, dengan cara berkompetisi dengan koenzim nukleotida piridin
dan penghambatan beberapa enzim oksidase yang membutuhkan nukleotida
sebagai koenzim, seperti xanthin oksidase (Irvanda, 2007).
Efek serius lainnya yang dapat ditimbulkan aspirin di hepar mencakup
pengosongan simpanan glikogen di hepar. Dosis toksik aspirin mampu
mengurangi metabolisme aerob dari glukosa, meningkatkan kinerja enzim
glukosa−6−fosfatase serta sekresi glukokortikoid. Penting untuk disimak bahwa
meskipun insidens toksisitas aspirin rendah pada dosis kuratif, namun efeknya
pada dosis toksik amat berbahaya terhadap hepar. Terlebih aspirin termasuk
21
2.5 Tikus Putih (Rattus norvegicus)galur Sprague Dawley
2.5.1. Klasifikasi Tikus Putih
Klasifikasi tikus putih adalah:
Kingdom : Animalia
Filum : Chordata
Kelas : Mamalia
Ordo : Rodentia
Subordo : Odontoceti
Familia : Muridae
Genus : Rattus
Spesies :Rattus norvegicus(Narendra, 2007)
2.5.2 Jenis Tikus Putih
Tikus putih atau tikus albino galur outbred lebih sering digunakan untuk
penelitian di laboratorium dibandingkan galur inbred. Beberapa contoh
jenis tikus putih galur outbred adalah Wistar, Sprague dawley, dan Long
Evans. Sprague dawley merupakan galur yang lebih cepat tumbuh
dibandingkan tikus Wistar. SedangkanLong Evans merupakan galur yang
lebih kecil dibandingkan tikus Wistar atau Sprague dawley. Galur Fisher
344 danLewis adalah tikus putih galurinbredyang paling banyak dipakai
22
2.5.3 Biologi Tikus Putih
Tikus putih (Rattus norvegicus) sering dipakai menjadi hewan percobaan
karena tikus merupakan hewan yang mewakili kelas mamalia sehingga
keutuhan organ, kebutuhan nutrisi, metabolisme biokimia, sistem
reproduksi, pernafasan, peredaran darah, serta ekskresinya menyerupai
manusia. Tikus juga dapat secara alami menderita suatu penyakit, seperti
hipertensi dan diabetes, dan juga sering dipakai dalam studi nutrisi,
tingkah laku, kerja obat, dan toksikologi (Animal Care Program, 2011).
Tikus putih (Rattus norvegicus) galur Sprague dawley mempunyai
beberapa sifat yang menguntungkan, antara lain dapat berkembang biak
dalam waktu yang cepat, mudah dipelihara dalam jumlah banyak, lebih
tenang, dan ukurannya lebih besar daripada tikus lainnya. Tikus putih
galur Sprague dawley juga memiliki ciri−ciri lainnya seperti albino,
kepala kecil, ekor yang lebih panjang dibandingkan badannya,
temperamennya baik, kemampuan laktasi yang tinggi, dan tahan terhadap
perlakuan. Keuntungan utama tikus putih (Rattus norvegicus) galur
Sprague dawley adalah ketenangan dan kemudahan penanganannya
23
2.6 Kerangka Teori
Seperti yang telah dijelaskan sebelumnya bahwa kulit pisang memiliki
kandungan antioksidan yang dapat berfungsi sebagai hepatoprotektor antara lain
flavonoid dan fenolik (Rahardian et al., 2010). Mekanisme antioksidan tersebut
bekerja sebagai hepatoprotektor adalah dengan meningkatkan ekspresi enzim
GST yang merupakan antioksidan endogen pada hati yang dapat mencegah
ikatan zat−zat beracun ke DNA, RNA maupun bagian hepatosit lainnya
(Mahardikasari, 2013).
Mekanisme Aspirin yang dapat mengganggu fungsi hati adalah dengan cara
penghambatan proses fosforilasi oksidatif yaitu menghambat metabolisme aerob
dari beberapa enzim di hepar dan jaringan lainnya, dengan cara berkompetisi
dengan koenzim nukleotida piridin dan mmenghambat beberapa enzim oksidase
yang membutuhkan nukleotida sebagai koenzim, seperti xanthin oksidase.
Mekanisme lainnya yaitu berupa pengosongan simpanan glikogen di hepar.
Dosis toksik aspirin juga mampu mengurangi metabolisme aerob dari glukosa,
meningkatkan kinerja enzim glukosa−6−fosfatase serta sekresi glukokortikoid
(Irvanda, 2007).
Melihat uraian di atas berdasarkan mekanisme kerja antioksidan pada kulit
pisang dan peranan aspirin dalam membuat kerusakan pada hepar, diharapkan
24
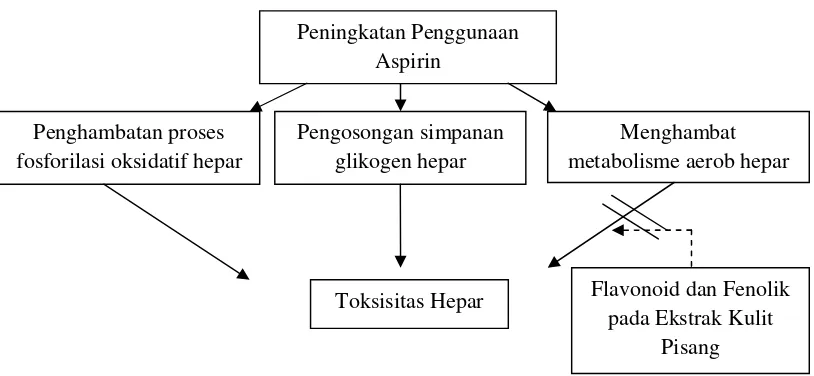
menghambat kerja toksik aspirin. Berdasarkan keterangan−keterangan tersebut
maka tersusunlah kerangka teori yang disajikan pada gambar 3.
Gambar 3.Kerangka teori pengaruh ekstrak kulit pisang kepok terhadap hepar tikus putih yang diinduksi aspirin.
2.7 Kerangka Konsep
Kerangka konsep pada penelitian kali ini tersaji pada gambar 4.
25
2.8 Hipotesis
Terdapat pengaruh pemberian ekstrak kulit pisang kepok terhadap gambaran
26
BAB III
METODE PENELITIAN
3.1 Desain Penelitian
Jenis penelitian ini adalah penelitian eksperimental dengan metode rancangan
acak terkontrol dengan pola post test control group design. Penelitian dilakukan
dengan cara membandingkan hasil observasi pada kelompok eksperimental dan
kontrol. Subjek penelitian yang akan digunakan adalah 25 ekor tikus putih (Rattus
norvegicus) jantan dewasa galur Sprague dawley, sehat, umur 3 sampai 4 bulan
dengan berat badan 100 sampai 200 gram yang dibeli dari Institut Pertanian
Bogor dan dikelompokkan secara randomisasi ke dalam 5 kelompok.
3.2 Waktu dan Tempat
Penelitian dilakukan selama empat bulan dengan tempat penelitian di Fakultas
Kedokteran Universitas Lampung, pembuatan ekstraksi di Fakultas Matematika
dan Ilmu Pengetahuan Alam (FMIPA) Universitas Lampung dan pembuatan
preparat histopatologi di laboratorium Patologi Anatomi Fakultas Kedokteran
27
3.3 Populasi dan Sampel
Populasi penelitian ini adalah tikus jantan galurSprague dawley, umur 3−4 bulan,
berat badan 100−200 gram yag diperoleh dari Fakultas Kedokteran Hewan
Institut Pertanian Bogor. Sampel penelitian sebanyak 25 ekor dipilih secara acak
dan dibagi ke dalam 5 kelompok perlakuan sesuai dengan rumus Frederer
(Bintari, 2014).
Rumus Frederer, rumus yang digunakan dalam penentuan besar sampel untuk uji
eksperimental yakni t(n−1) >15. Dimana t merupakan kelompok perlakuan dan n
adalah besar sampel setiap kelompok.
5(n−1) >15
5n−5 >15
5n >20
n>4
Jadi, sampel yang digunakan tiap kelompok percobaan sebanyak 5 ekor (n>4) dan
jumlah kelompok yang akan digunakan adalah 5 kelompok sehingga penelitian ini
akan menggunakan 25 ekor tikus putih dari populasi yang ada.
3.3.1 Kriteria Inklusi
1. Jantan
2. Berat Badan (BB) 100−200 gram
28
4. Sehat (rambut tidak kusam, rontok, botak, dan aktif)
3.3.2 Kriteria Ekslusi
1. Mati selama waktu penelitian dilakukan
2. Adanya penurunan Berat Badan (BB) lebih dari 10% selama masa
adaptasi di laboratorium
3. Sakit (penampakan rambut kusam, rontok atau botak dan aktivitas
kurang atau tidak aktif).
3.4 Bahan dan Alat Penelitian
3.4.1 Bahan Penelitian
Bahan yang digunakan yaitu aspirin dengan aspirin 90 mg, ekstrak kulit
pisang kepok dengan dosis 125 mg/kgBB, 250 mg/kgBB dan 500
mg/kgBB, aquadest, alkohol 96%, tikus putih jantan dewasa galur
Sprague dawley, pakan dan minum tikus (Nirmalaet al.,2012).
3.4.2 Bahan Kimia
Bahan yang digunakan untuk membuat preparat histologis dengan metode
paraffin meliputi: larutan formalin 10% untuk fiksasi, alkohol 70%,
alkohol 96%, alkohol absolut, etanol, xylol, pewarna Hematoksisilin dan
29
3.4.3 Alat Penelitian
1. Alat selama Perlakuan
Alat penelitian yang digunakan dalam penelitian adalah neraca analitik
metler toledo,dengan tingkat ketelitian 0,01 gram untuk menimbang
berat tikus, spuit oral 1cc dan 5cc, minor set untuk membedah perut
tikus (laparatomi), kandang tikus, botol minum tikus, mikroskop
cahaya, gelas ukur dan pengaduk, dan kamera digital.
2. Alat dalam Pembuatan Preparat Histopatologi
Alat pembuat preparat histopatologi yang digunakan adalah object
glass, deck glass, tissue cassette, rotary microtome, oven, waterbath,
platening table, autotechnicome processor, staining jar, staining rack,
kertas saring,histoplast, danparaffin dispenser.
3.5 Prosedur Penelitian
3.5.1 Prosedur Pemberian Aspirin
Penentuan dosis yang diberikan pada perlakuan terhadap tikus
berdasarkan hasil konversi dari manusia berat badan 70 kg ke tikus
dengan berat badan 200 gram. Angka konversi dari manusia ke tikus
adalah 0,018. Pada manusia, dosis aspirin pada manusia dewasa dengan
berat badan 70 kg adalah 5 g/hari. Pemakaian dosis harian aspirin sebesar
30
pertama pemakaian. Sehingga, dosis aspirin yang diberikan pada tikus
dengan berat 200 gram adalah 0,018x5.000=90 mg. Sediaan aspirin yang
digunakan adalah aspirin tablet 500 mg. Aspirin tersebut dihancurkan
dengan cara digerus dan dilarutkan dalam 5,5 ml aquadest. Jadi dalam 1
ml larutan terdapat 90 mg aspirin. Diberikan peroral satu kali sehari pada
pagi hari sebelum pemberian pakan standar.
3.5.2 Prosedur Pemberian Ekstrak Kulit Pisang Kepok
Dosis ekstrak kulit pisang yang efektif digunakan pada tikus adalah 250
mg/kgBB (Nirmala et al., 2012). Hasil penelitian inilah yang mendasari
penggunaan 3 dosis ekstrak kulit pisang yaitu 125 mg/kgBB, 250
mg/kgBB dan 500 mg/kgBB. Jadi perhitungan dosis untuk tikus dengan
berat 200 gram adalah
200 gr berat tikus = 0,2 kg
Dosis pertama : 125 mg/kgBB X 0,2 kg=25 mg
Dosis kedua : 250 mg/kgBB X 0,2 kg=50 mg
Dosisi ketiga : 500 mg/kgBB X 0,2 kg=100 mg.
Pembuatan ekstrak kulit pisang kepok menggunakan dua kilogram kulit
pisang kepok dipotong−potong lalu dikeringkan di dalam oven selama 24
jam. Kulit−kulit ini kemudian direndam dalam EtOH (etanol) selama 24
jam. Setelah itu rendaman diuapkan, hasilnya berupa ekstrak etanol
kasar. Dari dua kilogram kulit pisang diperoleh sekitar 150 ml ekstrak
31
pada kulit pisang matang, karena berdasarkan uji in vitro, ekstrak etanol
kasar dan kulit pisang matang memiliki aktivitas antioksidan yang
tertinggi.
3.5.3 Prosedur Perlakuan
1. Tikus sebanyak 25 ekor dikelompokkan dalam 5 kelompok. Kelompok
I sebagai kelompok kontrol normal, dimana hanya akan diberi
akuades. Kelompok II sebagai kontrol positif, dimana diberikan
aspirin dengan dosis 90 mg. Kelompok III adalah kelompok perlakuan
coba dengan pemberian ekstrak kulit pisang kepok dosis 25 mg,
kelompok IV diberikan ekstrak kulit pisang kepok dengan dosis 50
mg, dan kelompok V diberikan ekstrak kulit pisang kepok dengan
dosis 100 mg. Ekstrak kulit pisang kepok diberikan setelah 2 jam
induksi aspirin dosis 90 mg. Masing−masing diberikan secara per oral
selama 14 hari. Selama 1 minggu tiap−tiap kelompok tikus
diadaptasikan sebelum diberi perlakuan.
2. Ukur Berat Badan (BB) tikus sebelum perlakuan
3. Mencekoki tikus dengan aspirin dan ekstrak kulit pisang kepok selama
14 hari. Tikus tetap diberikan makanad libitum.
4. Setelah dihentikan, 5 tikus jantan dari masing-masing kelompok
dianastesi dengan Ketamine−xylazine 75−100 mg/kg+5−10 mg/kg
secara Intraperitoneal (IP) kemudian tikus di euthanasia berdasarkan
32
metode cervical dislocation dengan cara ibu jari dan jari telunjuk
ditempatkan dikedua sisi leher di dasar tengkorak atau batang ditekan
ke dasar tengkorak. Sedangkan posisi tangan lainnya, berada pada
pangkal ekor atau kaki belakang dengan cepat ditarik sehingga
menyebabkan pemisahan antara tulang leher dan tengkorak.
5. Setelah tikus dipastikan mati, dilakukan laparotomi, hati tikus diambil
untuk pembuatan sediaan mikroskopis. Pembuatan sediaan
mikroskopis menggunakan metode paraffin dan pewarnaan HE
(Hematoksilin).
6. Sampel hati difiksasi dengan formalin 10%
7. Teknik pembuatan preparat histopatologi, antara lain :
a.Fixation
Spesimen berupa potongan organ hepar yang telah dipotong
kemudian segera difiksasi dengan formalin 10% selama 24 jam,
kemudian potongan dicuci dengan air mengalir sebanyak 3‒5 kali.
b.Trimming
Potongan kelenjar yang telah terfiksasi dikecilkan hingga ukuran
±3 mm.
c. Dehidrasi
Dehidrasi bertujuan untuk mengeluarkan air yang terdapat di
dalam jaringan. Potongan organ hepar berturut‒turut direndam
dalam alkohol 70% selama 0,5 jam (2 kali), alkohol 96% selama
33
d.Clearing
Clearingbertujuan untuk membersihkan sisa alkohol yang terdapat
dalam jaringan. Tahap ini dilakukan dengan memasukan jaringan
kedalam larutan xylol I dan xylol II, masing‒ masing selama 1
jam.
e. Impregnasi
Impregnasi merupakan tahapan pmenuhi pori-pori atau celah-celah
yang berada pada hepatosit. Tahap ini dilakukan menggunakan
paraffin selama 1 jam dalam oven suhu 65°C sebanyak 2 kali.
f.Embedding
Sisa paraffin yang masih tersisa di dalam jaringan dibersihkan
dengan memanaskan beberapa saat di atas api dan diusap dengan
kapas. Paraffin cair disiapkan dengan memasukkan paraffin ke
dalam cangkir logam dan dimasukkan dalam oven dengan suhu
diatas 58°C. Kemudian paraffin cair dituangkan ke dalam base
mole. Jaringan yang telah diimpreg dipindahkan satu persatu dari
tissue cassette ke dasar base mole dengan mengatur jarak yang satu
dengan yang lainnya. Biarkan membeku kemudian lepaskan tissue
cassette dari base mole. Blok parafin telah siap dipotong dengan
mikrotom.
g.Cutting
Sebelum dipotong, blok didinginkan terlebih dahulu di lemari es.
34
halus dengan ketebalan 4−5 mikron. Pemotongan jaringan
dilakukan dengan menggunakan rotary microtome dengan
disposable knife. Kemudian dipilih lembaran potongan yang paling
baik, diapungkan pada air, dan dihilangkan kerutannya dengan
cara menekan salah satu sisi lembaran jaringan tersebut dengan
ujung jarum dan sisi yang lain ditarik menggunakan kuas runcing.
Lembaran jaringan dipindahkan ke dalam water bath pada suhu
60oC selama beberapa detik sampai mengembang sempurna.
Dengan gerakan menyendok, lembaran jaringan tersebut diambil
dengan slide bersih dan ditempatkan di tengah atau pada sepertiga
atas atau bawah. Slide yang berisi jaringan ditempatkan pada
inkubator (suhu 37oC) selama 24 jam sampai jaringan melekat
sempurna.
h. Staining(pewarnaan)
Setelah dipastikan jaringan melekat sempurna padaobject glass,
lalu dilakukan proses pewarnaan dengan prosedur sebagai berikut:
1. Lakukan deparafinisasi dalam larutan xylol I selama 3
menit, larutanxylol II selama 3 menit dan larutanxylol III
selama 3 menit.
2. Lakukan hidrasi pada alkohol 100% selama 2 menit,
alkohol 95% selama 2 menit, alkohol 80% selama 2 menit,
35
3. Pulasan inti menggunakan larutan meyer hematoksilin
selama 15 menit, lau dialiri air mengalir dan eosin selama
1 menit untuk pewarnaan sitoplasma.
4. Proses selanjutnya adalah dehidrasi dengan menggunakan
alkohol 70% sebanyak 3 celupan, alkohol 80% sebanyak 3
celupan, alkohol 95% sebanyak 3 celupan dan alkohol
100% sebanyak 3 celupan.
5. Setelah itu dilakukan penjernihan kembali dengan
menggunakan larutan xylol I selama 2 menit dan larutan
xylolII selama 2 menit.
i. Mounting
Dengan entelan dan tutup dengan deck glass Pemeriksaan
mikroskopis pada pewarnaan Hematoksilin‒ Eosin dilakukan
dengan mengamati degenerasi bengkak keruh yang merupakan
hasil efek kemopreventif ekstrak pada slide pada hepar. Degenarasi
bengkak keruh pada organ hepar tikus dilihat dengan melakukan
pengamatan sediaan histopatologi menggunakan mikroskop
dengan perbesaran 400x.
j. Pembacaan Slide
Dengan mikroskop Slide diperika dengan 5 lapang pandang
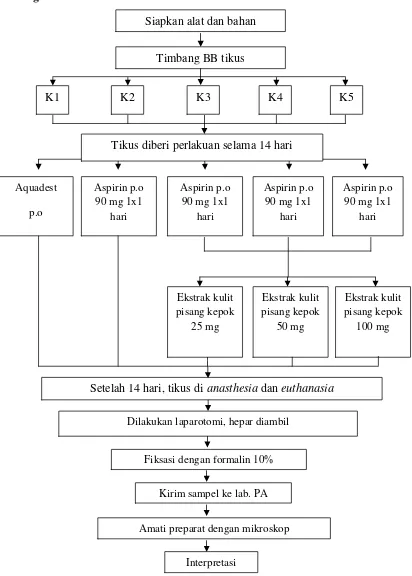
36
Setelah 14 hari, tikus dianasthesiadaneuthanasia
Dilakukan laparotomi, hepar diambil
37
3.7 Identifikasi Variabel dan Definisi Operasional Variabel
3.7.1 Identifikasi Variabel
1. Variabel Independen
a. Perlakuan coba: pemberian ekstrak kulit pisang kepok dan aspirin
b. Perlakuan kontrol negatif: pemberian aspirin tanpa ekstrak kulit pisang
kepok
2. Variabel Dependen
Variabel dependen adalah kerusakan hepar.
3.7.2 Definisi Operasional Variabel
Definisi operasional variabel adalah dosis ekstrak kulit pisang kepok dan
kerusakan hepar disajikan dalam tabel 1.
Tabel 1. Definisi Operasional Variabel.
Variabel Definisi Skala
Dosis ekstrak kulit pisang kepok
Ekstrak kulit pisang diberikan menggunakan sonde secara oral. Dosis efektif pada penelitian sebelumnya: 125 mg/kgBB, 250 mg/kgBB dan 500 mg/kgBB
Numerik Rasio
38
3.8 Analisis Data
Analisis data penelitian diproses dengan aplikasi pengolahan data. Dengan tingkat
signifikansi p=0,05. Hasil penelitian dianalisis secara statistik dengan uji
normalitas data (Saphiro−Wilk). Didapatkan data tidak berdistribusi normal maka
alternatifnya dipilih uji Kruskal−Wallis. Hipotesis dianggap bermakna dengan
p<0.05. Lalu dilanjutkan dengan analisis uji statisticMann Whitney.
3.9 Etik Penelitian
Penelitian ini telah disetujui oleh Komisi Etik Penelitian Kesehatan Fakultas
Kedokteran Universitas Lampung sesuai dengan surat persetujuan etik nomor
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Pemberian aspirin pada dosis 90 mg/kgBB dapat membuat kerusakan pada
hepar tikus putih (Rattus norvegicus).
2. Pemberian ekstrak kulit pisang kepok dapat memberikan perbaikan pada
hepar tikus putih (Rattus norvegicus) yang diinduksi aspirin.
3. Pemberian ekstrak kulit pisang kepok pada dosis 100 mg/kgBB memberikan
perbaikan yang optimal pada kerusakan hepar tikus putih (Rattus norvegicus)
yang diinduksi aspirin.
5.2 Saran
1. Diharapkan dapat di lanjutkan nya penelitian tentang manfaat ekstrak kulit
pisang kepok untuk organ tubuh lainnya dalam memperbaiki kerusakan.
2. Peneliti lain disarankan untuk menguji efek toksik dan efektifitas dari ekstrak
kulit pisang kepok.
3. Peneliti lain disarankan untuk menelaah lebih lanjut mengenai kandungan zat
53
Daftar Pustaka
Akbar B. 2010. Tumbuhan Dengan Kandungan Senyawa Aktif yang Berpotensi
Sebagai Bahan Antifertilitas. Jakarta: Adabia Press.
Animal care program. 2011. Guide For The Care and Use of Laboratory Animals.
Washington DC: The National Academies Press.
Bintari GS. 2014. Temulawak (Curcuma xanthorrhiza Roxb) as gastroprotector of
mucosal cell damage.Majority Unila. 3(5): 77−84.
Chandrasoma, Taylor. 2005. Ringkasan Patologi Anatomi. Jakarta: EGC.
Clarinta U, Muhartono, Fiana DN. 2014. The role of giving 40% ethanol of
mangosteen rind (Garcinia mangostana L.) against rifampicin−induced hepar
histopathology appearance in male rat. Majority Unila. 3(2): 164−72.
FAO. 2009. The State of Food and Agriculture: Livestock in balance. Roma:
54
Fatemeh SR, Saifullah R, Abbas FMA, Azhar ME. 2012. Total phenolics, flavonoids
and antioxidant activity of banana pulp and peel flours: influence of variety
and stage of ripenes. International Food Research Journal. 19(3): 1041−46.
Ganong WF. 2008. Review of Medical Physiology. New York: The McGraw−Hill
Companies.
Gartner PL, Hiatt JL. 2007. Color Textbook of Histology. China: Elsevier Saunders.
Guyton AC, Hall JE. 2008. Buku Ajar Fisiologi Kedokteran, Edisi ke−11. Jakarta:
EGC penerbit buku kedokteran.
Hartono D. 2013. Bioetanol dari kulit pisang kepok dengan proses fermentasi.
Skripsi. Banda Aceh: Universitas Malikussaleh.
Hendra J, Suprapto, Mulyanti N. 2008. Teknologi Budidaya Pisang. Bandar
Lampung:Balai Besar Pengkajian dan Pengembangan Teknologi Pertanian.
Imam MZ, Akter S, Mazumder EH, Rana S. 2011. Antioxidant activities of different
parts of Musa sapientum L. ssp. sylvestris fruit. Journal of Applied
Pharmaceutical Science. 1(10): 68−72.
Irvanda R. 2007. Pengaruh pemberian aspirin berbagai dosis per oral terhadap
gambaran histopatologi hepar. Artikel Karya Tulis Ilmiah. Semarang:
55
Jain N, Shrivastava R, Raghuwanshi AK, Shrivastava VK. 2012. Aspirin induced
changes in serum acp, alp, got, gpt, bilirubin, and creatinine in corelation with
histopatological changes in liver and kidney of female albino rat.
International Journal of Applied Pharmaceutics. 3(4): 9−11.
Javed I, Iqbal Z, Rahman ZU, Khan FH, Muhammad F, Aslam B. et al. 2006.
Antihyperlipidaemic efficacy of Trachyspermum ammi in albino rabbits.
Pakistan Vet. Journal. 26(1): 23−9.
Katzung BG, Masters SB, Trevor AJ. 2009. Katzung Basic & Clinical Pharmacology,
11th ed. United States of America: Lange.
Kemenkes. 2010. Riset Kesehatan Dasar. Jakarta: Badan Penelitian dan
Pengembangan Kesehatan Kementrian Kesehatan RI.
Kemenkes. 2011. Formularium Obat Herbal Asli Indonesia. Jakarta: Direktorat
Jendral Bina Gizi dan KIA.
Kierszenbaum AL, Tres LL. 2012. Histology and Cell Biology, 3rd ed. United States
of America: Elsevier Saunders.
Kumar S, Mishra CK, Ahuja A, Rani A, Nema RK. 2012. Phytoconstituents aand
pharmacological activities of Musa paradisiaca Linn. Asian Journal of
56
Mahardikasari LW. 2013. Uji toksisitas akut ekstrak batang pisang ambon (Musa
paradisiaca var. Sapientum) terhadap mencit (Mus musculus) dengan
parameter LD50. Skripsi. Surabaya: Universitas Airlangga.
Mescher AL. 2007. Junqueira’s Basic Histology Text & Atlas, 12th ed. United States:
Lange.
Narendra DW. 2007. Pengaruh dehidrasi dengan pemberian bisacodyl terhadap
gambaran hematokrit tikus putih jantan (Rattus Norvegicus). Skripsi. Bogor:
Institut pertanian Bogor.
Nirmala M, Girija K, Lakshman K, Divya T. 2012. Hepatoprotective activity of Musa
paradisiaca on experimental animal models. Asian Pac J Trop Biomed. 2(1):
11−5.
Nuraeni D. 2007. Pengaruh pemberian aspirin dosis toksik per oral terhadap
gambaran histopatologi gaster, duodenal dan jejunum tikus wistar. Artikel
karya tulis ilmiah. Semarang: Fakultas Kedokteran Universitas Diponegoro.
Pane ER. 2013. Uji aktivitas senyawa antioksidan dari ekstrak metanol kulit pisang
raja (Musa paradisiaca Sapientum). Tadris Biologi Fakultas Tarbiyah IAIN
Raden Fatah. 3(2): 76−81.
Pinzaru LA, Hadaruga DI, Hadaruga NG, Corpas L, Grozescu F, Peter F. 2011.
57
dsc−molecular modeling correlatio. Digest Journal of Nanomaterialsand
Biostructures. 6(4): 1605−17.
Rahardian MRR, Mulyadi, Nurkhasanah. 2010. Efek hepatoprotektor ekstrak etanol
kelopak bunga rosella (Hibiscus sabdariffa L.) pada tikus sprague dawley
yang diinduksi 7,12−dimetilbenzena(α)antrasen: kajian sgot, sgpt, alp dan
gambaran histopatologi hepar. Tesis. Yogyakarta: Fakultas Pascasarjana
Farmasi Universitas Ahmad Dahlan.
Robbins SL, Cotran RS, Kumar V. 2007. Buku Ajar Patologi Edisi ke−7. Jakarta:
EGC.
Sherwood L. 2012. Anatomi dan Fisiologi Manusia dari Sel ke Sistem. Jakarta: EGC.
Shodehinde SA, Oboh G. 2013. Antioxidant properties of aqueous extracts of unripe
Musa paradisiaca on sodium nitroprusside induced lipid peroxidation in rat
pancreas in vitro. Asian Pacific Journal Tropical Biomed. 3(6): 449−57.
Singh S, Prakash P. 2014. Evaluatin of antioxidant activity of banana peels (Musa
acuminata) extracts using different extraction methods. Chemical Science
Transactions. 4(1): 158−60.
Sloane E. 2004. Anatomi dan Fisiologi Untuk Pemula. Jakarta: EGC.
Snell RS. 2006. Anatomi Klinik Untuk Mahasiswa Kedokteran Edisi ke−6. Jakarta:
58
Venkatarangaiah K, Krishnappa P, Kumar S, Rajanna S, Haris M, Keriyappa V.
2014. Pharmacological properties of corm ethanol of Musa Paradisiaca (L.)
CV. Puttabale. World Journal Of Pharmacy And Pharmaceutical Sciences.
3(5): 1362−83.
Victor J, Navarro MD, John R, Senior MD. 2006. Drug−Related Hepatotoxicity. The
New England Journal of Medicine. 3(54): 731−9.
Warintek. 2011. Prospek dan arah pengembangan agribisnis pisang. [diakses pada
tanggal 20 Februari 2015]. Tersedia dari: