i
PENETAPAN KADAR HIDROGEN PEROKSIDA DALAM
SEDIAAN PEWARNA RAMBUT SECARA TITRASI REDOKS
MENGGUNAKAN ALAT AUTOTITRATOR
TUGAS AKHIR
OLEH:
FITRI ANDIKA HASAN
NIM 122410052
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ii
LEMBAR PENGESAHAN
PENETAPAN KADAR HIDROGEN PEROKSIDA DALAM
SEDIAAN PEWARNA RAMBUT SECARA TITRASI REDOKS
MENGGUNAKAN ALAT AUTOTITRATOR
TUGAS AKHIR
DiajukanUntukMemenuhiSalahSatuSyaratUntukMemperolehGelar AhliMadyaPadaProgram Diploma III AnalisFarmasidanMakananFakultas
Farmasi Universitas Sumatera Utara
Oleh:
FITRI ANDIKA HASAN
NIM 122410052
Medan, April 2015 DisetujuiOleh:
iii
KATA PENGANTAR
Assalamu’alaikum Wr. Wb.
Segala puji dan syukur bagi Allah SWT, Tuhan Yang Maha Esa pengayom segenap alam yang telah melimpahkan rahmat, karunia dan ridhoNya, sehingga penulis dapat mengerjakan dan menyelesaikan tugas akhir yang berjudul
“Penetapan Kadar Hidrogen Peroksida Dalam Sediaan Pewarna Rambut
Secara Titrasi Redoks Menggunakan Alat Autotitrator” tugas akhir ini diajukan sebagai salah satu syarat untuk memperoleh gelar ahlimadya pada Program Studi Diploma III Analis Farmasi dan Makanan pada Fakultas Farmasi Universitas Sumatera Utara.
Selama penulisan Tugas Akhir ini, penulis banyak mendapat bimbingan dan bantuan dari berbagai pihak, maka dengan segala ketulusan hati penulis menyampaikan terimakasih sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara.
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi USU.
iv
5. Ibu Dra. Djendakita Purba, M.Si., Apt., selaku Dosen Penasehat Akademik penulis selama melaksanakan pendidikan pada Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi USU.
6. Bapak dan Ibu dosen beserta seluruh staf di Fakultas Farmasi USU yang telah mendidik penulis selama masa perkuliahan.
7. Bapak Drs. M. Ali Bata Harahap, M.Kes., Apt., selaku Kepala Balai Besar Pengawas Obat dan Makanan di Medan yang telah memberi izin pelaksanaan Praktik Kerja Lapangan (PKL).
8. Ibu Lambok Oktavia SR, S.Si., M.Kes., Apt., selaku Koordinator Pembimbing Praktek Kerja Lapangan di Balai Besar Pengawas Obat dan Makanan di Medan.
9. Bapak dan Ibu seluruh staff diBalai Besar Pengawas Obat dan Makanan di Medan.
10. Teman-teman satu kelompok PKL yaitu, Lesti, Palupi, dan Tami memberikan motivasi, dukungan, dan semangat.
11. Teman-teman Analis Farmasi dan Makanan – 2012 yang selalu menyemangati dan memberikan bantuan serta seluruh kenangan terindah selama berada di bangku perkuliahan.
12. Serta semua pihak yang tak dapat penulis sebutkan satu persatu yang telah banyak membantu penulis dalam penyusunan tugas akhir ini.
v
do’a, kasih sayang serta dorongan moril maupun materil kepada penulis selama ini. Semoga kalian selalu dalam lindungan Allah SWT.
Penulis menyadari bahwa tulisan ini jauh dari sempurna, sehingga dibutuhkan saran dan kritik yang bersifat membangun demi perbaikan dan kesempurnaan tulisaan ini. Akhir kata penulis berharap semoga tulisan ini dapat memberikan kontribusi yang bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Wassalamu’alaikum Wr. Wb
Medan, April 2015 Penulis
vi
PENETAPAN KADAR HIDROGEN PEROKSIDA DALAM SEDIAAN PEWARNA RAMBUT SECARA TITRASI REDOKSMENGGUNAKAN ALAT AUTOTITRATOR
Abstrak
Hidrogen peroksida memiliki peranan pada saat melakukan pewarnaan rambut.Suatu kosmetika pewarna rambut memiliki kandungan hidrogen peroksida karena sifat senyawa hidrogen peroksida yang tidak berwarna, berbau keasaman, dan larut dengan baik dalam air. Tujuan penelitian ini adalah untuk menentukan kadar hidrogen peroksida di dalam sediaan pewarna rambut.
Penentuan kadar hidrogen peroksida dilakukan menurut metode titrasi redoks menggunakan alat autotitrator sesuai dengan prosedur di laboratorium Kosmetika dan Alat Kesehatan di Balai Besar Pengawas Obat dan Makanan Medan.
Dari hasil pengujian hidrogen peroksida dalam sediaan pewarna rambut secara titrasi permanganometri menggunakan alat autotitrator, diperoleh kadar hidrogen peroksida sebesar 6.0125 pada Garnier color naturals cream. Hasil pengujian menunjukkan bahwa pewarna rambut yang diperiksa mengandung kadar hidrogen peroksida yang memenuhi persyaratan menurut PerMenKes No. 1176/Menkes/Per/VIII/2010, yaitu ≤ 12%.
vii
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
BAB II TINJAUAN PUSTAKA... 3
2.1 Hidrogen Peroksida ... 3
2.1.1Hidrogen Peroksida Pada Pewarna Rambut ... 3
2.1.2 Efek Hidrogen Peroksida ... 4
2.1.3Penetapan Kadar Hidrogen Peroksida Pada Titrasi Redoks ... 4
2.2Pewarna Rambut ... 5
2.2.1 Zat Pewarna Rambut ... 5
2.2.2 Proses Pewarnaan ... 6
2.3 Titrasi Redoks ... 6
viii
2.4 Autotitrator ... 8
2.4.1 Cara Kerja Autotitrator ... 9
BAB III METODE PERCOBAAN... 11
3.1 Tempat Pengujian ... 11
3.5.1.2 Kalium Permanganat 0,1 N... 12
3.6 Pembakuan Kalium Permanganat ... 12
BAB V KESIMPULAN DAN SARAN... 16
5.1 Kesimpulan ... 16
5.2 Saran ... 16
DAFTAR PUSTAKA ... 17
ix
DAFTAR TABEL
x
DAFTAR LAMPIRAN
Halaman Lampiran 1 Pembakuan Kalium Permanganat 0,1 N ... 19 Lampiran 2 Perhitungan Penetapan Kadar Hidrogen Peroksida Dalam
vi
PENETAPAN KADAR HIDROGEN PEROKSIDA DALAM SEDIAAN PEWARNA RAMBUT SECARA TITRASI REDOKSMENGGUNAKAN ALAT AUTOTITRATOR
Abstrak
Hidrogen peroksida memiliki peranan pada saat melakukan pewarnaan rambut.Suatu kosmetika pewarna rambut memiliki kandungan hidrogen peroksida karena sifat senyawa hidrogen peroksida yang tidak berwarna, berbau keasaman, dan larut dengan baik dalam air. Tujuan penelitian ini adalah untuk menentukan kadar hidrogen peroksida di dalam sediaan pewarna rambut.
Penentuan kadar hidrogen peroksida dilakukan menurut metode titrasi redoks menggunakan alat autotitrator sesuai dengan prosedur di laboratorium Kosmetika dan Alat Kesehatan di Balai Besar Pengawas Obat dan Makanan Medan.
Dari hasil pengujian hidrogen peroksida dalam sediaan pewarna rambut secara titrasi permanganometri menggunakan alat autotitrator, diperoleh kadar hidrogen peroksida sebesar 6.0125 pada Garnier color naturals cream. Hasil pengujian menunjukkan bahwa pewarna rambut yang diperiksa mengandung kadar hidrogen peroksida yang memenuhi persyaratan menurut PerMenKes No. 1176/Menkes/Per/VIII/2010, yaitu ≤ 12%.
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Pewarna rambut mengandung Hidrogen peroksida (H2O2) dan pewarna. Untuk mengubah warna, peroksida harus dimasukkan ke dalam korteks rambut agar dapat mengubah susunan kimia pada pigmen rambut. Warna hitam pada rambut harus dipudarkan lebih dulu agar menjadi lebih terang, sehingga lebih mudah diubah menjadi warna lain. Semakin sering rambut dipudarkan, kutikula akan rusak dan membentuk sisik. Padahal, kutikula adalah pelindung rambut. Kerusakan pada kutikula dapat mengakibatkan rambut mudah kusut saat basah, bersisik dan kering (Chakim, 2006).
Apabila rambut sudah terkena kandungan H2O2 yang terkandung dalam kosmetik pewarnaan, maka batang rambut yang tidak kuat dalam menahan bahan kimia membuat rambut mudah rusak yang mengakibatkan batang rambut terbuka, sehingga rambut pecah-pecah, rontok, patah, dan kering (Purba, 2006).
Analisis hidrogen peroksida dalam sediaan pewarna rambut dapat dilakukan dengan metode titrasi redoks karena reagensia ini mudah diperoleh, murah, dan tak memerlukan indikator kecuali bila digunakan larutan yang sangat encer (Day dan Underwood, 1986).
2
bergantung pada kedua proses ini.Oksidasi didefinisikan sebagai hilangnya hidrogen, atau perolehan oksigen, atau hilangnya elektron.Reduksi didefinisikan sebagai perolehan hidrogen, atau hilangnya oksigen, atau perolehan elektron (Cairns, 2014).
1.2 Tujuan
Penelitian dilakukan untuk mengetahui kadar hidrogen peroksida dalam sediaan pewarna rambut secara titrasi redoks menggunakan alat autotitrator serta mengetahui pewarna rambut yang digunakan memenuhi persyaratan kadar hidrogen peroksida yang diizinkan oleh pemerintah Indonesia.
1.3 Manfaat
3
BABII
TINJAUAN PUSTAKA
2.1 Hidrogen Peroksida
Hidrogen peroksida dikenal sebagai dihidrogen dioksida, hidrogen dioksida, oksidol dan peroksida, dengan rumus kimia H2O2, pH 4.5, cairan bening, tidak berwarna dan tidak berbau, dan lebih kental dari air. Memiliki sifat oksidator yang sangat kuat dan digunakan sebagai bahan pemutih, juga sebagai desinfektan.Hidrogen peroksida mempunyai sifat-sifat sebagai berikut:
a. Bukan asam, tetapi dapat mengubah warna lakmus menjadi merah. b. Larutan pekat hidrogen peroksida dapat merusak kulit.
c. Memiliki daya desinfektan (Bariqina dan Ideawati, 2001).
2.1.1 Hidrogen Peroksida Pada Pewarna Rambut
Hidrogen peroksida sangat berguna dalam pembuatan kosmetika penataan rambut seperti yang tersebut berikut ini.
a) Sebagai bahan penambah dalam larutan pengeriting dan bahan cat rambut untuk memudahkan meresapnya bahan-bahan tersebut ke dalam korteks rambut.
4
pengeriting dengan memulihkan ikatan antara molekul-molekul tanduk (Bariqina dan Ideawati, 2001).
2.1.2 Efek Hidrogen Peroksida
Kelainan-kelainan pada batang rambut yang tidak sampai mempengaruhi akar rambut, misalnya batang rambut yang terbelah ujungnya, kekeringan dan kekusaman akibat berjemur disinar matahari, rapuh karena tindakan pengeringan dengan alat-alat yang panas (blow-dry), pengeritingan, pelurusan, pewarnaan dan sasakan. Sementara itu kelainan-kelainan rambut yang dapat sampai mempengaruhi akar rambut, misalnya rambut yang kusut sehingga waktu disisir banyak yang putus atau tercabut dengan akar rambutnya, infeksi karena jamur dan kuman serta keracunan bahan-bahan kimia atau cat rambut yang sampai ke akar rambut (Tranggono dan Latifah, 2007).
2.1.3 Penetapan Kadar Hidrogen Peroksida Pada Titrasi Redoks
Larutan baku kalium permanganat dapat dipakai untuk menentukan beberapa zat yang bersifat sebagai reduktor (Rivai, 2006). Menurut Farmakope Edisi IV (1995) Larutan baku kalium permanganat hanya digunakan untukmenetapkan kadar hidrogen peroksida dengan cara titrasi. Dimana tiap ml larutan kalium permanganat 0,1N setara dengan 1,701 mg hidrogen peroksida.
5
peroksida menggunakan kalium permanganat, reaksi yang terjadi adalah sebagai berikut:
5H2O2 + 2MnO-4 + 6H+ = 5O2↑ + 2Mn2+ + 8H2O (Rivai, 2006)
2.2 Pewarnaan Rambut
Sediaan pewarna rambut adalah sediaan kosmetika yang digunakan dalam tatarias rambut untuk mewarnai rambut, baik untuk mengembalikan warna rambut asalnya atau warna lain (Ditjen POM, 1985). Warna rambut manusia bermacam-macam, tergantung pada jenis pigmen yang terdapat di dalam korteks rambut. Ketika usia semakin lanjut maka warna rambut semakin memutih, karena mulai kehilangan pigmen yang disebabkan oleh menurunnya fungsi melanosit dan menurunnya aktivitas tirosin. Pemutihan rambut juga dapat terjadi karena faktor keturunan (Putro, 1998).
Zat warna mulai bekerja saat kontak dengan lapisan terluar dari rambut. Disini terjadi adsorpsi berupafenomena antarmuka padat-cair. Zat warna rambut melewati kompleks membran sel dan melalui kutikula masuk ke dalam korteks secara permeasi dan difusi (Mitsui, 1997).
2.2.1 Zat Pewarna Rambut
6
Zat warna alam yang lazim digunakan adalah zat warna yang diperoleh dari sumber alam berasal dari tumbuhan, baik sebagai simplisia, sediaan galenika seperti ekstrak dan rebusan, sari komponen warna, maupun zat semisintetik yang dibuat berdasarkan pola warna senyawa komponen warna yang terkandung dalam simplisianya (Ditjen POM, 1985).
2.2.2 Proses Pewarnaan
Berdasarkan proses sistem pewarnaan, pewarna rambut dibagi dalam 2 golongan:
1. Pewarnaan Rambut Langsung
Sediaan pewarnaan rambut lansung telah mengandung zat warna, sehingga dapat lansung digunakan dalam pewarna rambut, tanpa terlebih dahulu harus dibangkitkan dengan pembangkit warna (Ditjen POM, 1985).
2. Pewarnaan Rambut Tidak Langsung
Sediaan pewarnaan rambut tidak lansung disajikan dalam 2 kemasan, masing-masing berisi komponen zat warna dan komponen pembangkit warna. Jika hendak digunakan terlebih dahulu harus dicampur komponen satu dengan yang lainnya (Ditjen POM, 1985).
2.3 Titrasi Redoks
7
demikian, agar titrasi redoks ini berhasil dengan baik, maka persyaratan berikut harus dipenuhi:
1) Harus tersedia pasangan sistem redoks yang sesuai sehingga terjadi pertukaran elektron secara stoikiometris.
2) Reaksi redoks harus berjalan cukup cepat dan berlangsung secara terukur (kesempurnaan 99,9%).
3) Harus tersedia cara penentuan titik akhir yang sesuai.
Cara titrasi redoks untuk penentuan reduktor digolongkan sesuai dengan oksidator yang digunakan sebagai pentiter. Umumnya, KMnO4, K2Cr2O7, Ce(SO4), KbrO3 dan I2 digunakan sebagai pentiter. Karena itu, cara-cara titrasi redoks ini digolongkan sebagai titrasi permanganometri, titrasi bikromatometri, titrasi serimetri, titrasi bromatometri dan titrasi iodometri (Rivai, 2006).
2.3.1 Penggunaan Kalium Permanganat Pada Titrasi Redoks
8
Kalium permanganat (KMnO4) merupakan oksidator kuat dalam larutan yang bersifat asam. Paro-reaksinya sebagai berikut:
MnO-4 + 5e + 8H+→ Mn2+ + 4H2O E0 = + 1,51V
Reaksi ini tidak berbolak-balik, sedangkan potensial elektroda bakunya diukur secara tidak langsung. Potensial elektrodanya sangat tergantung pada pH. Karena itu titrasi harus dilakukan dalam larutan yang bersifat asam kuat (H2SO4 1N). Meskipun demikian kalium permanganat juga merupakan oksidator kuat dalam larutan yang bersifat asam lemah, netral atau basa lemah.
Larutan baku KMnO4 dibuat dengan melarutkan sejumlah kalium permanganat dalam air, mendidihkannya selama delapan jam atau lebih, kemudian saring endapan MnO2 yang terbentuk, lalu bakukan dengan zat baku utama. Zat baku utama yang lazim dipakai adalah natrium oksalat. Reaksi yang terjadi pada proses pembakuan tersebut adalah sebagai berikut:
5C2O2-4 + 2MnO-4 + 16H+→ 10CO2↑+ 2Mn2+ + 8H2O
Titik akhir titrasi ditandai dengan timbulnya warna merah muda yang disebabkan oleh kelebihan permanganat (Rivai, 2006)
2.4 Autotitrator
9
sebenarnya disebut kosong indikator. Titrasi dapat dikelompokkan berdasarkan jenis reaksi yang dapat asam-basa, oksidasi-reduksi (ORP), kompleksasi, atau curah hujan (Liptak, 1994).
Sebuah Titrator pada dasarnya terdiri dari buret listrik, sensor yang sinyal diperkuat dengan preamplifier dan komputer mikro. Selama titrasi, Titrator yang mengukur sinyal dari sensor dan menggunakan informasi ini untuk mengontrol penambahan titran dengan buret listrik. Setelah titik akhir tercapai, mikro menghitung volume titran ditambahkan dan mengkonversi nilai ini ke hasilnya (misalnya konsentrasi seperti konsentrasi garam meja dalam kecap) berdasarkan formula. Rumus yang dibutuhkan untuk perhitungan ini dapat diprogram dan tergantung pada jenis analisis (Anonim, 2014).
2.4.1 Cara Kerja Titrator
Bentuk kurva titrasi (volume titran vs sinyal dari sensor) tergantung pada jenis sampel yang dianalisa dan sensor yang digunakan.
• Jenis sampel: Kurva titrasi dapat memiliki satu atau beberapa titik akhir. Titrasi asam karbonat dengan natrium hidroksida menghasilkan dua titik akhir. Dalam banyak kasus, tidak semua titik akhir terdeteksi dalam titrasi yang menarik.
• Jenis sensor: pH dan logam elektroda biasanya menghasilkan kurva berbentuk S, sedangkan titrasi conductometric menghasilkan satu berbentuk V.
10
• Menghitung titik akhir dengan benar untuk berbagai bentuk kurva. • Menyaring titik akhir yang tidak menarik.
11
BAB III
METODOLOGI
3.1 Tempat Pengujian
Pengujian penetapan kadar hidrogen peroksida dalam sediaan pewarna rambut secara titrasi permanganometri dilakukan di Laboratorium Pengujian Kosmetika dan Alat Kesehatan, Balai Besar Pengawas Obat dan Makanan Medan, Jalan Willem Iskandar Pasar V Barat I No. 2 Medan.
3.2 Alat
Alat yang digunakan adalah Autotitrator, Beaker Glass, Buret 25 ml, Erlenmeyer 125 ml,Gelas Ukur 20 ml, Labu Ukur 1000 ml,Timbangan Analitik, dan Pipet Tetes.
3.3 Bahan
Bahan yang digunakan adalah Akuades, Asam Sulfat 2 N, Kalium Permanganat 0,1 N dan Natrium Oksalat.
3.4 Data Sampel
− Nama sampel : Garnier Color Naturals Cream
− No. Batch : G0824600
− No Reg : BPOM No. NA 17111001868
− Pabrik : LOREAL India pvt. Ltd.
12
− Komposisi :Water, Cetearyl Alcohol, Deceth-3, Propylene Glycol, Laureth-12, Ammonium hydroxide, Oleth-30, Lauric acid, Hexadimethrine chloride, Glycol distearate, 4-amino-2-hydroxytoluene, Ethanolamine, Polyquaterinium-22, Silica dimethyl silylate, Cl 77891, 2,4-Diaminophenoxyethanol Hcl, M-Aminophenol, Dimethicon, Pentasodium Pentetate, P-Penylenediamine, Carbomer, Resorcinol, Fragrance.
3.5 Prosedur
3.5.1 Pembuatan Pereaksi
3.5.1.1Asam Sulfat 2 N
Ditambahkan hati-hati dengan pengadukan 55,5 ml asam sulfat P pada lebih kurang 1000 ml air lalu dinginkan hingga suhu 25o.
3.5.1.2Kalium Permanganat 0,1 N
Dilarutkan lebih kurang 3,3 g kalium permanganat P dengan air dalam labu 1000 ml. Didihkan larutan selama lebih kurang 15 menit. Ditutup labu, biarkan selama tidak kurang dari 2 hari, lalu disaring.
3.6 Pembakuan Kalium Permanganat
13
aquadest lalu encerkan dengan7 ml H2SO4 p, tambahkan 2 tetes jingga metil dan panaskan hingga suhu lebih kurang 700c, kemudian tambahkan perlahan-lahan larutan KMnO4 0,1 N hingga warna merah muda yang tahan 15 detik.
3.7 Cara Pengujian
Ditimbang 0,5 g sampel dalam labu erlenmeyer, ditambahkan 20 ml
aquadest dan kocok hingga larut. Tambahkan 20 ml asam sulfat 2N dikocok
sampai homogen. Dihidupkan alat autotitrarator, letakkan sampel diatas alat autotitrator yang didalamnya telah dimasukkan magnetik bar.Dipilih metode pengujian redoks untuk menguji H2O2 pada sampel.Isi berat sampel yang telah ditimbang pada alat autotitrator, dan beri nama A dilakukan duplo beri nama B pada sampel selanjutnya. Pilih Menu start pada alat autotitrator.Sampel akan dititrasi dengan kalium permanganat 0,1N secara otomatis dan akan dihomogenkan dengan bantuan magnetik bar. Alat autotitrator akan berhenti bekerja jika sampel telah mencapai titik akhir titrasi.Di cetak hasil pengujian pada alat autotitrator.
3.8 Penetapan Kadar
Kadar H2O2 = V x N x 1,701
W x 0,1 x 100%
Keterangan :
1 ml KMnO4 0,1 N setara dengan 1,701 mg Hidrogen Peroksida
14
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Penetapan kadar hidrogen peroksida dalam sediaan pewarna rambut Garnier Color Naturals Cream.
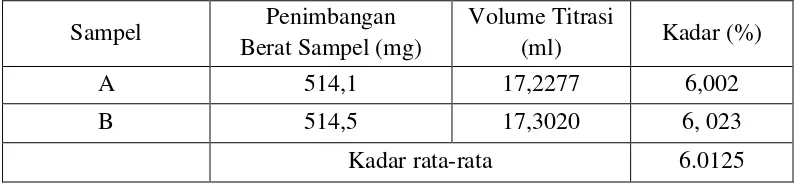
Tabel 4.1 Hasil Penetapan Kadar Hidrogen Peroksida
Sampel Penimbangan
Kadar rata-rata 6.0125
4.2 Pembahasan
15
sebagai pengasam sehingga H2SO4 tidak ikut bereaksi, maka keakuratan volume H2SO4 tidak mempengaruhi hasil titrasi.
Ketika titrasi dilakukan secara otomatis, sampel secara otomatis dikirim ke analyzer, pengiriman titran secara otomatis berakhir setelah mencapai titik akhir, dan hasilnya secara otomatis direkam atau dikirimkan untuk tujuan pengendalian. Autotitrator biasanya mampu menargetkan titik akhir dalam 0-14 pH atau 0-2000 kisaran mV. Mereka mendeteksi laju aliran titran yang diperlukan untuk membawa sampel (dengan laju alir konstan) ke titik akhir (Liptak, 1994).
16
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kadar Hidrogen Peroksida yang diperoleh sebesar 6,0125% pada Garnier Color Naturals Cream.Kadar hidrogen peroksida yang diperoleh dalam sampel memenuhi persyaratan yang diizinkan menurut PerMenKes No. 1176/Menkes/Per/VIII/2010, yaitu ≤ 12%.
5.2 Saran
17
DAFTAR PUSTAKA
Anonim, (2014). Autotitrator. From:
Bariqina, E., Dan Ideawati, Z., (2001). Perawatan Dan Penataan Rambut.
Yogyakarta: Adicita Karya Nusa. Hal. 3, 26-27.
Cairns, D. (2004). Intisari Kimia Farmasi. Jakarta: Buku Kedokteran EGC. Hal 139.
Chakim, T. (2006).Hubungan Antara Kandungan Hidrogen Peroksida Dalam
Pewarna Rambut Terhadap Kerusakan Rambut. Semarang: Program
Pendidikan Sarjana Universitas Diponegoro. Hal: 3-4.
Day, R.A, Dan Underwood A.L. (1986). Analisis Kimia Kuantitatif, Edisi Kelima. Jakarta: Penerbit Erlangga. Hal: 290-293.
Ditjen POM. (1985). Formularium Kosmetika Indonesia. Jakarta: Departemen Kesehatan R.I. Hal: 189.
Ditjen POM. (1993). Metode Analisa Pusat Pengujian Obat Dan Makanan
Nasional No.12/KO/05 Tentang Penetapan Kadar Hidrogen Peroksida.
Jakarta: Badan Pengawas Obat Dan Makanan R.I .
Ditjen POM. (1995). Farmakope Indonesia, Jilid IV. Jakarta: Departemen Kesehatan R.I. Hal: 1135, 1160.
Ham, M. (2006). Membuat Reagen Kimia Di Laboratorium. Jakarta: PT. Bumi Aksara. Hal: 151.
Khopkar, SM. (2003). Konsep Dasar Kimia Analitik. Jakarta: Penerbit Universitas Indonesia. Hal: 53.
Liptak, BG. (1994). Analytical Instrumentation. America: By Chilton Book Company. Hal: 460.
Mitsui, T. (1997). New Cosmetic Science. Amsterdam: Elsevier Book Company. Hal: 49, 431-432.
Peraturan Menteri Kesehatan Republik Indonesia. (2010). No. 1176/Menkes/Per/VIII/2010 Tentang Persyaratan Teknis Bahan Kosmetika.
18
Putro, D.S.(1998). Agar Awet Muda. Ungaran: Trubus Agriwidya. Hal: 12-15. Rivai, H. (2006). Asas Pemeriksaan Kimia. Jakarta: Penerbit UI Press. Hal:
346-364.
19
LAMPIRAN
Lampiran 1
Pembakuan Kalium Permanganat 0,1 N Pengamatan
1 ml KMnO4 0,1 N setara dengan 6,7 mg natrium oksalat
20
Lampiran 2
Perhitungan Penetapan Kadar Hidrogen Peroksida Dalam Sediaan Pewarna Rambut
Sampel Pengamatan Volume
Titrasi (ml) Wadah + Zat (g) Wadah + Sisa (g)
A 66,6151 66,1010 17,2277
B 63,8063 63,2918 17,3020
V1 = 17,2277 ml W1 = 514,1 mg V2 = 17,3020 ml W2 = 514,5 mg Normalitas KMnO4 = 0,1053 N
1 ml KMnO4 0,1 N setara dengan 1,701 mg Hidrogen Peroksida
21
Lampiran 3
22
Lampiran 4