IDENTIFIKASI ZAT WARNA PADA SAUS YANG BEREDAR
DI PASAR PANCUR BATU KABUPATEN DELI SERDANG
SECARA KROMATOGRAFI KERTAS
TUGAS AKHIR
OLEH:
ARSILIA PUJI ASTUTI
NIM 122410020
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
IDENTIFIKASI ZAT WARNA PADA SAUS YANG BEREDAR
DI PASAR PANCUR BATU KABUPATEN DELI SERDANG
SECARA KROMATOGRAFI KERTAS
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Untuk Memperoleh Gelar Ahli Madya Pada Program Diploma III Analis Farmasi dan Makanan
Fakultas Farmasi Universitas Sumatera Utara
Oleh:
ARSILIA PUJI ASTUTI
NIM 122410020
Medan, April 2015 Disetujui Oleh:
Dosen Pembimbing
Drs. Suryanto, M.Si., Apt. NIP 196106191991031001
Disahkan Oleh: Wakil Dekan I
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Esa, yang
telah memberikan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan
Tugas Akhir ini dengan judul “IDENTIFIKASI ZAT WARNA PADA SAUS YANG BEREDAR DI PASAR PANCUR BATU KABUPATEN DELI SERDANG”.
Tugas Akhir ini merupakan salah satu syarat untuk menyelesaikan
program pendidikan D-III Analis Farmasi dan Makanan (AFAMA) Fakultas
Farmasi Universitas Sumatera Utara.
Selama proses pengerjaan Tugas Akhir ini penulis banyak mendapatkan
pengarahan, bimbingan, dan bantuan dari berbagai pihak, maka pada kesempatan
ini penulis mengucapkan terimakasih kepada:
1. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Wakil Dekan I Fakultas
Farmasi Universitas Sumatera Utara.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi
Universitas Sumatera Utara.
3. Bapak Popi Patilaya, S.Si. M.Sc., Apt., selaku Sekretaris Program Studi
Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas
Sumatera Utara.
4. Bapak Drs. Suryanto. M.Si., Apt., selaku Dosen Pembimbing Tugas Akhir
yang telah banyak memberikan bimbingan dan pengarahan dengan penuh
5. Ibu Dra. Hj. Ernawati, Apt., selaku Koordinator Pembimbing Praktik Kerja
Lapangan di Balai Laboratorium Dinas Kesehatan Provinsi Sumatera Utara
yang telah memberikan kesempatan kepada penulis untuk melaksanakan
kegiatan PKL.
6. Rekan - rekan Mahasiswa Program Studi D – III Analisa Farmasi dan
Makanan angkatan 2012 Fakultas Farmasi Universitas Sumatera Utara
yang tidak dapat disebutkan satu persatu.
Terima kasih khususnya penulis ucapkan kepada Ayahanda tercinta Ilham
Riva’i dan Ibunda tercinta Gunawati Arsianingsih yang telah mendukung penulis
serta seluruh keluarga yang telah memberikan restu dan motivasi hingga Tugas
Akhir ini selesai.
Dalam penyusunan Tugas Akhir ini penulis menyadari sepenuhnya bahwa
tulisan ini masih jauh dari kata sempurna, baik dari susunan, bahasa maupun isi
yang terkandung didalamnya. Oleh karena itu, penulis sangat mengharapkan
masukan berupa saran dan kritikan yang bersifat membangun, guna untuk
kesempurnaan penulis pada masa yang akan datang.
Akhir kata penulis mengucapkan terima kasih kepada semua pihak yang
telah membantu dan mendukung penulis dalam penyusunan Tugas Akhir ini,
semoga Tugas Akhir ini bermanfaat bagi pembacanya.
Medan, Mei 2015
Penulis
DAFTAR ISI
Halaman
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR TABEL ... vii
ABSTRAK ... viii
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Tujuan ... 4
1.3 Manfaat ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Saus .. ... 5
2.2 Pewarna Makanan ... 5
2.2.1 Pembagian Zat Warna ... 7
2.2.2 Dampak Pewarna Makanan ... 10
2.3 Kromatografi ... 11
2.4 Kromatografi Kertas ... 12
2.4.1 Cara Kerja Secara Umum ... 13
2.4.2 Alat dan Teknik ... 14
2.4.3 Kertas ... 15
2.4.4 Pelarut-Pelarut ... 16
2.4.5 Cara Pembuatan Cuplikan pada Kertas ... 16
2.4.6 Identifikasi dari Senyawa-senyawa ... 17
3.1 Tempat ... 18
3.2 Sampel, Alat, dan Bahan ... 18
3.3 Prosedur Kerja ... 19
3.3.1 Bulu Domba Bebas Lemak ... 19
3.3.2 Penyediaan Fasa Diam ... 19
3.3.3 Penjenuhan Bejana Kromatografi ... 20
3.3.4 Pemeriksaan Zat Pewarna Pada Sampel Saus ... 20
BABIV HASIL DAN PEMBAHASAN ... 22
4.1 Hasil ... 22
4.1.1 Perhitungan ... 22
4.2 Pembahasan ... 23
BAB V KESIMPULAN DAN SARAN ... 25
5.1 Kesimpulan ... 25
5.2 Saran ... 25
DAFTAR TABEL
Tabel 2.1 Bahan Pewarna Sintetis yang Dilarang di Indonesia ... 9
Tabel 2.2 Bahan Pewarna Sintetis yang Diizinkan di Indonesia... 10
Tabel 2.3 Macam-Macam Kertas Kromatografi ... 15
Tabel 2.4 Pelarut-Pelarut untuk Kromatografi ... 16
Tabel 4.1 Hasil Pemeriksaan Zat warna Pada Saus yang Beredar di Pasar Pancur Batu Kabupaten Deli Serdang ... ... 23
IDENTIFIKASI ZAT PEWARNA PADA SAUS YANG BEREDAR DI PASAR PANCURBATU KABUPATEN DELI SERDANG
SECARA KROMATOGRAFI KERTAS
Abstrak
Saus cabe merupakan salah satu olahan produk pangan yang sangat popular karena digunakan sebagai pelengkap dalam pengolahan makanan. Umumnya pada proses pembuatan saus cabe ditambahkan zat pewarna agar menghasilkan warna yang lebih menarik. Pembuatannya dilakukan oleh pabrik dan ada juga industri rumah tangga sehingga peraturan penggunaan jenis dan kadar zat pewarna belum tetap. Tidak semua produk saus cabe yang dipasarkan khususnya di pasar tradisional mencantumkan jenis atau kode zat pewarna yang digunakan sehingga penting dilakukan penelitian untuk mengetahui jenis zat pewarna yang digunakan diperbolehkan atau tidak.
Identifikasi ini bertujuan untuk mengetahui zat pewarna apa yang terkandung dalam saus yang beredar di pasaran. Telah dilakukan pemeriksaan zat pewarna pada berbagai macam saus yang diperjualbelikan di Pasar Pancur Batu Kabupaten Deli Serdang, yang dilaksanakan di Balai Laboratorium Kesehatan Daerah Bagian Toksikologi, analisa dilakukan dengan menggunakan eksperimen laboratorium dengan metode Kromatografi Kertas. Secara umum tujuan pemeriksaan ini adalah untuk mengetahui adanya zat pewarna berbahaya yang terdapat dalam saus yang diperjualbelikan di Pasar Pancur Batu Kabupaten Deli Serdang.
Dari hasil pemeriksaan terhadap tiga sampel saus, terdapat dua sampel saus positif mengandung zat pewarna berbahaya yang dilarang seperti Orange RN dan Ponceau 3R, dengan ciri-ciri yang sama dengan standar baku Orange RN dan Ponceau 3R yang digunakan, yaitu dilihat dengan menghitung harga Rf pada bercak yang dihasilkan.
BAB I PENDAHULUAN 1.1 Latar Belakang
Makanan adalah salah satu kebutuhan dasar manusia. Dalam kehidupan
sehari-hari manusia tidak terlepas dari makanan. Sebagai kebutuhan dasar
makanan tersebut harus mengandung zat gizi untuk dapat memenuhi fungsinya
dan aman dikonsumsi karena makanan yang tidak aman dapat menimbulkan
gangguan kesehatan bahkan keracunan (Cahyadi, 2009).
Aneka makanan dan minuman yang berwarna-warni tampil semakin
menarik. Warna-warni pewarna membuat aneka produk makanan mampu
mengundang selera, walaupun demikian konsumen harus berhati-hati. Badan
Pengawas Obat dan Makanan (BPOM) sering menemukan produk makanan yang
menggunakan pewarna tekstil. Pada era modern ini, bahan pewarna tampaknya
sudah tidak bisa dipisahkan dari berbagai jenis makanan dan minuman olahan.
Produsen pun berlomba-lomba untuk menarik perhatian para konsumen dengan
menambahkan pewarna pada makanan dan minuman (Anonim, 2009).
Kasus penyalahgunaan bahan tambahan pangan yang biasa terjadi adalah
penggunaan bahan tambahan yang dilarang untuk bahan pangan dan penggunaan
bahan makanan melebihi batas yang ditentukan. Penyebab lain, produsen
berusaha memenuhi kebutuhan dengan mendapat keuntungan besar, tetapi harga
murah melalui penggunaan zat pewarna makanan yang digunakan untuk
mempertahankan makanan agar tetap menarik (Syah, 2005).
Pemerintah Indonesia melalui Menteri Kesehatan RI telah mengeluarkan
yang dilarang digunakan dalam makanan pada tanggal 1 Juni 1979
No.235/Menkes/Per/VI/79, kemudian disusul dengan Surat Keputusan Menteri
Kesehatan RI tanggal 1 Mei 1985 No.239/Menkes/Per/V/85, yang berisikan jenis
pewarna yang dilarang. Terakhir telah dikeluarkan pula Surat Keputusan
No.722/Menkes/Per/IX/88, yang mengatur batas maksimum penggunaan dan
pewarna yang diizinkan di Indonesia (Depkes RI, 2011).
Bahan pewarna yang sering digunakan dalam makanan olahan adalah
pewarna sintetis (buatan) dan pewarna natural (alami). Pewarna sintetis terbuat
dari bahan kimia seperti Tartrazin untuk warna kuning dan Alleura red untuk
warna merah, kadangkala pengusaha yang nakal menggunakan pewarna bukan
makanan untuk memberikan warna pada makanan. Agar mendapat keuntungan
besar produsen sering menggunakan pewarna tekstil untuk makanan padahal
pewarna tersebut dilarang keras digunakan pada makanan karena bisa
menyebabkan kanker dan penyakit lainnya. Pewarna sintetis yang boleh
digunakan untuk makanan pun harus dibatasi penggunaannya, karena pada
dasarnya, setiap senyawa sintetis yang masuk ke dalam tubuh akan menimbulkan
efek (Syah, 2005).
Pemakaian bahan pewarna sintetis ternyata dapat menimbulkan hal-hal
yang tidak diinginkan dan bahkan mungkin memberi dampak negatif terhadap
kesehatan manusia. Beberapa hal yang mungkin memberi dampak negatif tersebut
terjadi bila:
a. Bahan pewarna sintetis ini dimakan dalam jumlah kecil, namun berulang.
c. Kelompok masyarakat luas dengan daya tahan yang berbeda-beda, yaitu
tergantung pada umur, jenis kelamin, berat badan, mutu pangan
sehari-hari, dan keadaan fisik.
d. Berbagai lapisan masyarakat yang mungkin menggunakan bahan pewarna
sintetis secara berlebihan.
e. Penyimpanan bahan pewarna sintetis oleh pedagang bahan kimia yang
tidak memenuhi persyaratan (Cahyadi, 2009).
Berdasarkan hal di atas maka dipilihlah judul tentang ”Identifikasi zat
pewarna pada saus yang beredar di Pasar Pancur Batu Kabupaten Deli Serdang
secara kromatografi kertas” karena identifikasi tersebut sangat penting untuk
1.2 Tujuan dan Manfaat 1.2.1 Tujuan
Adapun tujuan penulisan tugas akhir ini adalah untuk mengetahui apakah
saus yang diperjualbelikan di Pasar Pancur Batu Kabupaten Deli Serdang
mengandung zat pewarna yang diperbolehkan atau tidak.
1.2.1 Manfaat
Adapun manfaat penulisan tugas akhir ini adalah:
1. Untuk memenuhi salah satu syarat penyelesaikan program pendidikan
di Akademi Analis Farmasi dan Makanan Fakultas Farmasi di
Univertas Sumatera Utara.
2. Untuk menambah wawasan dalam mengembangkan ilmu pengetahuan
serta memberikan pengalaman kepada penulis dalam melakukan riset.
3. Untuk menambah informasi serta wawasan kepada masyarakat terkait
adanya zat pewarna berbahaya yang terkandung di dalam saus yang
beredar di Pasar Pancur Batu Kabupaten Deli Serdang melalui dunia
pendidikan serta dampak yang ditimbulkan.
4. Memberikan informasi dan bahan masukan bagi Dinas Kesehatan,
BPOM, Perusahaan Daerah Pasar tentang pemakaian zat pewarna pada
BAB II
TINJAUAN PUSTAKA 2.1 Saus
Kata ”saus” berasal dari bahasa Perancis (sauce) yang diambil dari bahasa
latin salsus yang berarti “digarami”. Sedangkan saus dalam istilah dalam
masak-memasak berarti cairan kental yang digunakan sewaktu atau dihidangkan
bersama-sama makanan sebagai penyedap atau agar makanan kelihatan bagus.
Saus juga dapat diartikan sebagai cairan kental (pasta) yang terbuat dari bubur
buah berwarna menarik (biasanya merah), mempunyai aroma dan rasa yang
merangsang dengan atau tanpa rasa pedas.Saus merupakan salah satu produk
pangan yang sangat populer. Saus tidak saja hadir dalam sajian seperti mie bakso,
atau mie ayam, tetapi juga dijadikan bahan pelengkap nasi goreng, mie goreng
dan aneka makanan fast food (Anonim, 2009).
2.2 Pewarna Makanan
Penentuan mutu bahan makanan pada umumnya sangat bergantung pada
beberapa faktor diantaranya cita rasa, warna, tekstur, dan nilai gizinya. Disamping
itu ada faktor lain, misalnya sifat mikrobiologis. Tetapi sebelum faktor-faktor lain
dipertimbangkan, secara visual faktor warna tampil lebih dahulu dan
kadang-kadang sangat menentukan. Suatu bahan yang dinilai bergizi, enak, dan teksturnya
sangat baik tidak akan dimakan apabila memiliki warna yang tidak sedap
dipandang atau memberi kesan menyimpang dari warna yang seharusnya. Selain
sebagai faktor yang ikut menentukan mutu, warna juga dapat digunakan sebagai
pengolahan ditandai dengan adanya warna yang seragam dan merata (Winarno,
1995).
Pada tahun 1960 dikeluarkan peraturan mengenai penggunaan zat pewarna
yang disebut Color Additive Amandement yang dijadikan undang-undang. Dalam
undang-undang ini zat pewarna dibagi menjadi dua kelompok yaitu Certified
Color dan Uncertified Color.
1. Certified Color
Ada dua macam yang tergolong Certified Color yaitu Dye dan Lake.
Keduanya adalah zat pewarna buatan. Zat pewarna yang termasuk golongan dye
telah melalui prosedur sertifikasi yang ditetapkan FDA (Food and Drug
Administration). Sedangkan zat pewarna lake yang terdiri dari satu warna dasar,
tidak merupakan warna campuran, juga harus mendapat sertifikat.
a. Dye
Dye adalah zat pewarna yang pada umumnya bersifat larut dalam air dan
larutannya dapat mewarnai. Pelarut yang dapat digunakan selain air adalah
propilenglikol, gliserin atau alkohol. Dye terdapat dalam bentuk bubur, butiran,
pasta, maupun cairan yang penggunaannya tergantung kondisi bahan, kondisi
proses, dan zat pewarnanya sendiri.
b. Lake
Diizinkan pemakaiannya sejak tahun 1959, dan penggunaanya meluas dengan
cepat. Zat pewarna ini merupakan gabungan dari zat warna (dye) dengan radikal
bebas (Al atau Ca) yang dilapisi dengan hidrat alumina.
Lapisan alumina ini tidak larut dalam air, sehingga lake ini tidak larut pada
pewarna ini digunakan untuk produk-produk yang tidak terkena air. Lake sering
kali lebih baik digunakan untuk produk-produk yang mengandung lemak dan
minyak. Daya mewarnai lake adalah dengan membentuk dispersi yang menyebar
pada bahan yang diwarnai.
2. Uncertified Color Additive
Zat pewarna yang termasuk Uncertified Color Additive adalah zat pewarna
mineral, walaupun zat pewarna seperti kantaxantin yang telah dapat dibuat secara
sintetik. Untuk penggunaannya zat pewarna ini bebas dari prosedur sertifikasi dan
termasuk daftar yang telah tetap. Satu-satunya zat pewarna Uncertified Color
Additive yang penggunaanya masih bersifat sementara adalah carbon black
(Winarno, 1995).
2.2.1 Pembagian Zat Pewarna
1. Pewarna Alami
Pewarna alami merupakan yang berasal dari tumbuh-tumbuhan atau
hewan yang lebih aman untuk dikonsumsi. Contohnya karotenoid adalah
kelompok zat pewarna yang meliputi warna kuning, orange dan merah. Biasanya
terdapat pada tomat, wortel, cabai merah dan jeruk. Sedangkan dari hewan
terdapat dalam lobster (udang) dan kulit udang.
Berikut penjelasan untuk beberapa tumbuhan yang dapat dijadikan sebagai
pewarna makanan.
a. Buah Bit (pemberi warna pink atau merah keunguan)
Buah berwarna merah tua ini mengandung vitamin A (karotenoid), vitamin
penyakit hati empedu, penghancur sel kanker dan tumor, mencegah anemia,
menurunkan kolesterol dan membantu produksi sel darah merah.
b. Wortel (pemberi warna kuning/jingga)
Wortel bermanfaat dalam menurunkan kadar kolesterol dalam darah, serta
membantu pertahanan tubuh dari resiko, terutama kanker, paru-paru, kanker
larynk (tenggorokan), esophagus (kerongkongan), prostat, kandung kemih dan
leher rahim.
c. Kunyit (pemberi warna kuning)
Kunyit mengandung curcumin, suatu zat pewarna kuning. Jenis tanaman
obat ini berguna sebagai obat anti gatal dan anti kejang, mengurangi
pembengkakan dan menyembuhkan hidung tersumbat.
d. Daun Suji dan Daun Pandan (pemberi warna hijau)
Daun suji lebih sering dipakai sebagai pewarna pada kue jajan pasar dan
minuman. Daun pandan juga bisa memberikan warna pada masakan dengan cara
menumbuk dan memeras airnya, namun efek warnanya tidak sekuat daun suji
e. Sawi (pemberi warna hijau)
Sayuran ini kaya akan protein, lemak, karbohidrat, Ca, P, Fe, Vitamin A,
Vitamin B dan Vitamin C. Manfaatnya untuk mengurangi rasa gatal di
tenggorokan pada penderita batuk, penyembuh penyakit kepala, bahan pembersih
kepala, bahan pembersih darah, memperbaiki fungsi ginjal, serta memperbaiki dan
memperlancar pencernaan (Winarno, 1995).
2. Pewarna Sintetik
Pewarna sintetik/buatan adalah pewarna yang biasanya dibuat di
berbahaya apabila dicampurkan ke dalam makanan. Pewarna sintetik/buatan dapat
menyebabkan gangguan kesehatan terutama pada fungsi hati dalam tubuh kita.
Contoh-contoh zat pewarna sintetik yang digunakan antara lain indigoten, alleura
red, fast green dan tartrazine. Proses pembuatan zat pewarna sintetik biasanya
melalui perlakuan pemberian asam sulfat atau asam nitrat yang sering kali
dikontaminasi oleh arsen atau logam berat lainnya yang bersifat racun (Winarno,
1995).
Di Indonesia peraturan mengenai penggunaan zat pewarna yang diizinkan
dan dilarang untuk pangan diatur melalui SK Menteri Kesehatan RI Nomor
722/Menkes/Per/IX/8 (Cahyadi, 2009).
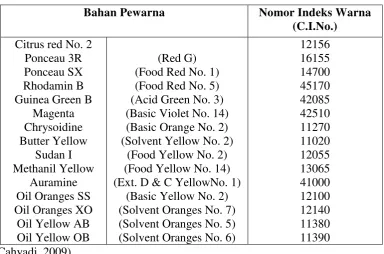
Tabel 2.1 Bahan Pewarna Sintetis yang Dilarang di Indonesia
Bahan Pewarna Nomor Indeks Warna
(C.I.No.)
Citrus red No. 2 Ponceau 3R Ponceau SX Rhodamin B Guinea Green B
Magenta Oil Oranges SS Oil Oranges XO
Oil Yellow AB (Basic Violet No. 14) (Basic Orange No. 2) (Solvent Yellow No. 2)
(Food Yellow No. 2) (Food Yellow No. 14) (Ext. D & C YellowNo. 1)
(Basic Yellow No. 2) (Solvent Oranges No. 7) (Solvent Oranges No. 5) (Solvent Oranges No. 6)
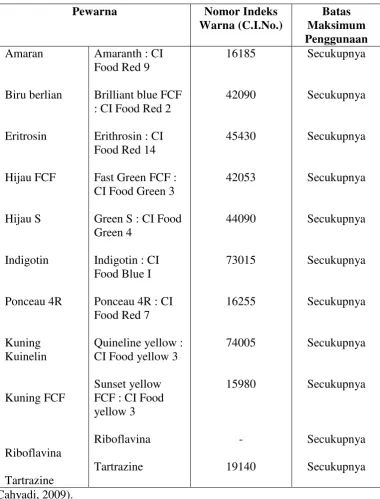
Tabel 2.2 Bahan Pewarna Sintetis yang Diizinkan di Indonesia
Pewarna Nomor Indeks
Warna (C.I.No.)
Brilliant blue FCF : CI Food Red 2
Erithrosin : CI Food Red 14
Quineline yellow : CI Food yellow 3
2.2.2 Dampak Pewarna Makanan
Pemakaian bahan pewarna sintetis ternyata dapat menimbulkan hal-hal
yang tidak diinginkan dan bahkan mungkin memberi dampak negatif terhadap
kesehatan manusia. Beberapa hal yang mungkin memberi dampak negatif tersebut
a. Bahan pewarna sintetis ini dimakan dalam jumlah kecil, namun berulang.
b. Bahan pewarna sintetis dimakan dalam jangka waktu lama.
c. Kelompok masyarakat luas dengan daya tahan yang berbeda-beda, yaitu
tergantung pada umur, jenis kelamin, berat badan, mutu pangan
sehari-hari, dan keadaan fisik.
d. Berbagai lapisan masyarakat yang mungkin menggunakan bahan pewarna
sintetis secara berlebihan.
e. Penyimpanan bahan pewarna sintetis oleh pedagang bahan kimia yang
tidak memenuhi persyaratan (Cahyadi, 2009).
2.3 Kromatografi
Kromatografi adalah suatu nama yang diberikan untuk teknik pemisahan
tertentu. Cara yang asli telah diketengahkan pada tahun 1903 oleh Tsweet, yang
telah menggunakannya untuk pemisahan senyawa-senyawa yang berwarna, dan
nama kromatografi diambil dari senyawa yang berwarna (Sastrohamidjojo, 1985).
Pada dasarnya semua cara kromatografi menggunakan dua fasa yaitu satu
fasa tetap (stationary) dan yang lain fasa bergerak (mobile). Fasa bergerak dapat
berupa zat cair atau gas maka semua ada empat macam sistem kromatografi.
Keempat macam sistem kromatografi tersebut adalah:
1). Fasa bergerak zat cair-fasa tetap padat:
Dikenal sebagai kromatografi serapan yang meliputi
- Kromatografi lapisan tipis
- Kromatografi penukar ion.
2). Fasa bergerak gas-fasa tetap padat:
3). Fasa bergerak zat cair-fasa tetap zat cair:
Dikenal sebagai kromatografi partisi
- Kromatografi kertas
4). Fasa bergerak gas-fasa tetap zat cair:
- Kromatografi gas-cair
- Kromatografi kolom kapiler (Sastrohamidjojo, 1985).
2.4 Kromatografi Kertas
Kromatografi kertas dikenal sebagai “analisa kapiler”. Metode-metode ini
sangat bersesuaian dengan kromatografi serapan dan sekarang kromatografi kertas
dipandang sebagai perkembangan dari sistem partisi. Salah satu zat padat dapat
digunakan untuk menyokong fasa tetap yaitu bubuk selulosa. Mula-mula telah
dilakukan pemisahan asam-asam amino dan peptida-peptida yang merupakan
hasil hidrolisa protein wool dengan suatu cara di mana kolom yang berisi bubuk
diganti dengan lembaran kertas dan kemudian diletakkan dalam bejana tertutup
yang berisi uap jenuh larutan. Ini adalah merupakan jenis dari sistem partisi di
mana fasa tetap adalah air, disokong oleh molekul-molekul selulose dari kertas,
dan fasa bergerak biasanya merupakan campuran dari satu atau lebih
pelarut-pelarut organik dan air. Hasil-hasil yang baik dapat diperoleh dengan peralatan
dan materi-materi yang sangat sederhana. Senyawa-senyawa yang terpisahkan
dapat dideteksi pada kertas dan dapat segera diidentifikasikan. Bahkan jika
dikehendaki, komponen-komponen yang terpisahkan dapat diambil dari kertas
dengan jalan memotong-motongnya dan kemudian dilarutkan secara terpisah
2.4.1 Cara Kerja Secara Umum
Setetes dari larutan yang mengandung campuran yang akan dipisahkan
diteteskan/diletakkan pada daerah yang diberi tanda di atas sepotong kertas saring
dimana ia akan meluas membentuk noda yang bulat. Bila noda telah kering kertas
dimasukkan dalam bejana tertutup yang sesuai dengan satu ujung, dimana tetesan
cuplikan ditempatkan, tercelup dalam pelarut yang dipilih sebagai fasa bergerak
(jangan sampai noda tercelup karena berarti senyawa yang akan dipisahkan akan
terlarut dari kertas). Pelarut bergerak melalui serat-serat dari kertas oleh gaya
kapiler dan menggerakkan komponen-komponen dari campuran cuplikan pada
perbedaan jarak dalam arah aliran pelarut. Bila permukaan pelarut telah bergerak
sampai jarak yang cukup jauhnya atau setelah waktu yang telah ditentukan, maka
kertas diambil dari bejana dan kedudukan dari permukaan pelarut diberi tanda dan
lembaran kertas dibiarkan kering. Jika senyawa-senyawa berwarna maka akan
terlihat sebagai pita-pita atau noda-noda yang terpisah (Sastrohamidjojo, 1985).
Metoda identifikasi yang paling mudah adalah berdasarkan pada
kedudukan dari noda relatif terhadap permukaan pelarut, menggunakan harga Rf.
Kadang-kadang, terutama pada gugus-gugus yang besar dari senyawa-senyawa
yang susunan kimianya mirip, seperti asam-asam amino, harga-harga Rf sangat
berdekatan satu sama lain. Bila akan melakukan pemisahan dengan kromatografi
kertas maka hal-hal berikut perlu mendapatkan perhatian:
1). Metoda (penaikkan, penurunan atau mendatar)
2). Macam dari kertas
3). Pemilihan dan pembuatan pelarut (fasa bergerak)
5). Pembuatan cuplikan
6). Waktu pengembangan
7). Metoda deteksi dan identifikasi (Sastrohamidjojo, 1985).
2.4.2 Alat dan Teknik
Metode penurunan. Alat yang pokok adalah berupa bejana yang terbuat
dari gelas, platina atau logam tahan karat yang di atasnya ditutup untuk mencegah
penguapan dari pelarut.
Metode penaikan. Bejana yang digunakan untuk kromatografi penaikan
sama seperti untuk kromatografi penurunan, tetapi pelarut diletakkan di bagian
bawah dari bejana, dan kertas dicelupkan di atasnya.
Metode mendatar. Dalam cara ini kertas dibentuk bulat di tengahnya
diberi lubang sebagai tempat untuk meletakkan sumbu yang terbuat baik dari
gulungan kertas atau dari benang dimana melalui ini pelarut dapat naik yang
kemudian membasahi kertas untuk kemudian mengembang melingkar membawa
senyawa yang dipisahkan (Sastrohamidjojo, 1985).
2.4.3 Kertas
Pekerjaan mula-mula dalam kromatografi kertas dilakukan dengan
menggunakan kertas saring Whatmann No. 1 dan hingga sekarang masih dipakai.
Kertas dalam pemisahan terutama mempunyai pengaruh pada kecepatan aliran
pelarut. Sedangkan fungsi dari kertas sendiri sangat kompleks. Efek-efek serapan
disebabkan oleh sifat polar dari gugus-gugus hidroksil di mana ini kemungkinan
sangat penting dan sejumlah kecil dari gugus karboksil dalam selulosa dapat
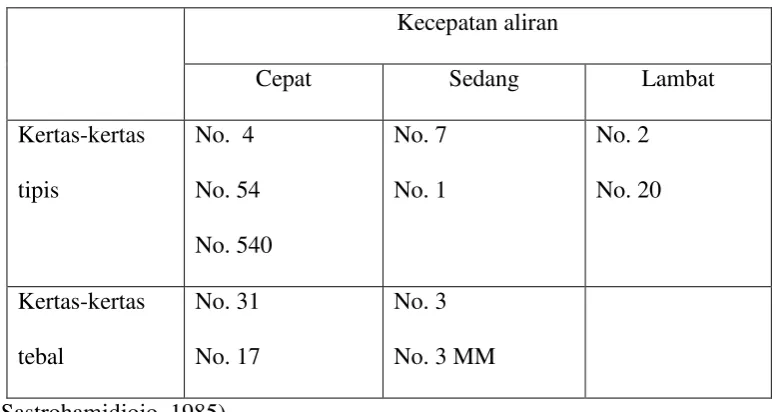
Tabel 2.3 Macam-macam Kertas Kromatografi
Kecepatan aliran
Cepat Sedang Lambat
Kertas-kertas
tipis
No. 4
No. 54
No. 540
No. 7
No. 1
No. 2
No. 20
Kertas-kertas
tebal
No. 31
No. 17
No. 3
No. 3 MM
(Sastrohamidjojo, 1985).
Kertas saring Whatman No.1 biasanya dipotong-potong menjadi beberapa
carik dan cuplikan ditotolkan pada salah satu ujung carik itu. Kromatogram dapat
dikembangkan dengan cara menaik atau menurun. Untuk cara menaik, kertas
digantungkan pada penggantung berbentuk kail yang dipasang pada penutup
bejana kromatografi. Pelarut berada di dasar bejana dan kertas dicelupkan ke
dalam pelarut di dalam wadah dan diberati dengan batang kaca supaya tetap pada
tempatnya. Lembaran kertas diangkat, dikeringkan, dan ditampakkan dengan cara
2.4.4 Pelarut-Pelarut
Beberapa campuran pelarut dapat dilihat dalam daftar berikut:
Tabel 2.4 Pelarut-pelarut untuk Kromatografi Kertas
Pemisahan Pelarut Perbandingan
Asam-asam amino Asam-asam lemak n-butanol/1,5 M NH3 Larutan jenuh
Fe, Cl, Br, I (garam-garam Na)
Piridin/air 90 : 10
Hg, Pb, Cd, Cu, Bi (klorida-klorida)
n-butanol/3 M HCl Larutan jenuh
(Sastrohamidjojo, 1985).
2.4.5 Cara Pembuatan Cuplikan Pada Kertas
Larutan campuran yang akan dipisahkan ditempatkan pada kertas yang
berupa noda. Biasanya dibiarkan untuk berkembang membentuk suatu bulatan.
Noda sebaiknya dibiarkan kering dalam udara, tetapi bila mungkin dapat
dikeringkan dengan menggunakan udara panas, terutama jika larutan bersifat
asam, karena ia dapat menyebabkan kertas menjadi hitam (Gritter, 1991).
Harus dicegah penempatan larutan terlalu banyak. Karena kelebihan setiap
komponen akan menyebabkan tidak akan tercapainya kesetimbangan partisi
selama bergerak, hingga akan mengakibatkan terjadinya kedudukan/lokasi yang
kabur. Ada beberapa cara pembuatan noda. Salah satu cara adalah dengan
menggunakan gelas kapiler dengan diameter yang sama, di mana cara ini yang
sering digunakan. Sedangkan cara yang lain dapat menggunakan alat penyuntik
2.4.6 Identifikasi dari Senyawa-senyawa
Dalam mengidentifikasi noda-noda dalam kertas sangat lazim
menggunakan harga Rf (retordation factor) yang didefinisikan sebagai:
Rf = jarak yang digerakkan oleh senyawa
jarak yang digerakkan oleh permukaan pelarut
Ada beberapa faktor yang mempengaruhi harga Rf yaitu:
- Pelarut
- Suhu
- Ukuran dari bejana
- Kertas
- Sifat dari campuran
Untuk mengukur Rf perlu melokalisir permukaan pelarut. Harga-harga Rf
biasanya dinyatakan sebagai fraksi/bagian. Perbedaan dalam harga-harga Rf untuk
dua senyawa yang dipisahkan tergantung pada besarnya noda-noda dan
panjangnya aliran pelarut. Cara yang paling mudah dalam mengukur Rf adalah
dengan menggunakan mistar (Sastrohamidjojo, 1985).
Cara lain untuk mengidentifikasi senyawa-senyawa yaitu dengan
reaksi-reaksi warna yang karakteristik. Reaksi kebanyakan sangat berguna dalam
pemisahan senyawa-senyawa anorganik, tetapi untuk senyawa organik sangat
kecil kejadian-kejadiannya, karena kebanyakan konstituen-konstituen dari
BAB III
METODE PENELITIAN 3.1 Tempat
Identifikasi zat pewarna pada saus yang beredar di Pasar Pancur Batu
Kabupaten Deli Serdang secara kromatografi kertas, dilakukan di Balai
Laboratorium Kesehatan Provinsi Sumatera Utara Jl. Williem Iskandar Pasar V
Barat I No.4 Medan-Estate.
3.2 Sampel, Alat, dan Bahan 3.2.1 Sampel
Sampel dari penelitian ini adalah sampel saus dengan merk yang berbeda
yang beredar di Pasar Pancur Batu Kabupaten Deli Serdang.
3.2.2 Alat-alat
Alat yang digunakan adalah batang pengaduk, beaker glass 250 ml, bulu
domba, chamber 10x20x20 cm, erlenmeyer 250 ml, gelas ukur 25 ml, kertas
timbang, kertas whatman No.1 20x20 cm, labu ukur 100 ml, neraca analitik,
pemanas listrik, penggaris besi 30 cm, pensil, pipet mikro.
3.2.3 Bahan-bahan
Bahan yang digunakan adalah Ammonia 10%, Asam Asetat 10%,
Aquadest, Metanol, Tri-Natrium Sitrat.
3.3 Prosedur Kerja
Fasadiam : Kertas saring Whatmann No.1
Baku pembanding :Timbang seksama lebih kurang 50 mg metanil yellow
dan brilliant blue, pindahkan ke dalam labu tentukur 25
ml. Tambahkan metanol secukupnya hingga garis
tanda. Aduk hingga homogen.
3.3.1 Bulu Domba Bebas Lemak
Cara kerja:
a. Bersihkan 10 g bulu domba dengan detergen, bilas dengan aquadest
hingga bersih.
b. Masukan ke dalam beaker glass 100 ml.
c. Tambahkan 25 ml eter, kocok dan ditutup dengan gelas arloji.
d. Rendam selama 12 jam.
e. Angkat bulu domba dan keringkan.
3.3.2 Penyediaan Fasa Diam
Cara kerja:
a. Digunakan kertas saring Whatman No.1 dengan susunan dan tebal
yang sesuai.
b. Diukur kertas saring dengan lebar 20 cm (lebar tidak kurang dari 2,5
cm dan tidak lebih dari panjang bejana) dan panjang 20 cm (panjang
lebih kurang sama dengan tinggi bejana).
c. Buat garis tipis dengan pensil melintang pada kertas saring dengan
jarak 2 cm dari ujung bawah kertas.
d. Tandai titik penotolan dengan jarak 2 cm.
3.3.3 Penjenuhan Bejana Kromatografi
Cara kerja:
a. Bersihkan bejana kromatografi.
b. Sediakan kertas sarinng dengan ukuran tinggi 18 cm (2 cm di bawah
tinggi bejana) dengan lebar sama dengan panjang bejana. Dapat juga
seluruh sisi bejana dilapisi dengan kertas saring.
c. Masukan lebih kurang 100 ml fasa gerak (campuran
tri-natriumsitrat-amoniak-aquadest) ke dalam bejana kromatografi.
d. Tinggi fasa gerak 0,5 cm sampai 1 cm dari dasar bejana. Kertas saring
harus selalu tercelup ke dalam fasa gerak pada dasar bejana.
e. Bejana ditutup kedap dan biarkan sistem mencapai keseimbangan.
f. Penjenuhan ditandai dengan kertas saring basah seluruhnya.
g. Catat waktu yang dibutuhkan untuk penjenuhan.
3.3.4 Pemeriksaan Zat Pewarna Pada Sampel Saus
Cara kerja:
a. 50 g sampel dimasukkan ke dalam beaker glass.
b. Tambahkan 10 ml asam asetat 10% dan beberapa helai bulu domba
bebas lemak.
c. Didihkan selama 10 menit.
d. Bulu domba diambil dicuci dengan aquadest.
e. Masukkan ke dalam ke cawan porselin yang bersih ditambah 25 ml
NH4OH 10% didihkan 10 menit.
f. Zat warna larut, masuk ke dalam larutan basa.
h. Larutan berwarna diuapkan di atas penangas air sampai kering.
i. Residu dilarutkan dalam sedikit metanol.
j. Totolkan pada kertas kromatografi sampai jenuh.
k. Dimasukkan kertas kromatografi ke dalam chamber yang berisi eluen:
5 ml NH4OH pekat, 2 g Tri-Natriumsitrat, 95ml aquades.
l. Tutup chamber dan biarkan kertas kromatografi mencapai batas
pengembang.
m. Biarkan sistem bergerak fasa gerak merambat 14 cm di atas titik
penotolan.
n. Angkat kertas kromatografi yang telah mencapai batas pengembang.
o. Keringkan kertas kromatografi.
p. Amati bercak.
q. Dihitung harga Rf.
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil
Setelah dilakukan pemeriksaan zat pewarna terhadap saus yang beredar di
Pasar Pancur Batu Kabupaten Deli Serdang maka dari tiga sampel yang diperiksa,
ketiga sampel tersebut mengandung zat pewarna berbahaya seperti Orange RN
dan Ponceau 3R setelah membandingkan harga Rf-nya dengan harga Rf baku
pembanding. Dalam pemeriksaan ini pelarut yang dipakai adalah pelarut tipe G
sesuai dengan peraturan Menteri Kesehatan RI No.239/Menkes/Per/V/85 tentang
warna yang dinyatakan sebagai bahan berbahaya.
4.1.1 Perhitungan
Rf = jarak titik pusat bercak dari titik penotolan (cm) jarak rambat fasa gerak dari titik penotolan (cm)
Sampel :
Saus A : Rf 1 = 1,3/12 = 0,10
Rf 2 = 3,8/12 = 0,31
Saus B : Rf 1 = 1,7/12 = 0,14
Rf 2 = 4,1/12 = 0,34
Saus C : Rf 1 = 3,4/12 = 0,28
Rf 2 = 4,9/12 = 0,40
Baku Pembanding
Orange RN : Rf = 0,28
Tabel 4.1 Hasil Pemeriksaan Zat Pewarna Pada Saus Yang Beredar Di Pasar Pancur Batu Kabupaten Deli Serdang
No. Sampel Rf 1 Rf 2 Keterangan
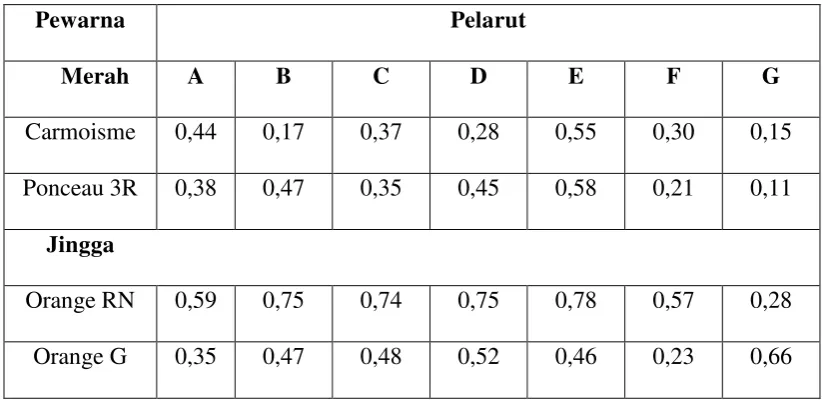
Tabel 4.2 Harga Rf Untuk Berbagai Macam Pelarut
Pewarna Pelarut
4.2 Pembahasan
Dari hasil identifikasi zat pewarna pada saus secara Kromatografi kertas
dengan menggunakan pelarut tipe G dapat dilihat dari harga Rf, maka dapat
disimpulkan bahwa Saus A dan Saus B mengandung Ponceau 3R dan Orange RN,
sedangkan Saus C hanya mengandung Orange RN yang merupakan pewarna
sintesis yang tidak diperbolehkan.
Orange RN merupakan pewarna orange yang pernah punya nomor indeks
15970 tapi karena jarang dipakai industri, produksinya dihentikan. Selain itu,
dalam percobaan terhadap babi, tikus, dan mencit, Orange RN menunjukkan
dampak yang parah terhadap sistem pembentukan sel darah dan hati. Sedangkan
Ponceau 3R adalah butiran atau serbuk merah hingga merah tua dan mempunyai
sifat tidak berbau. Selain itu, zat tersebut mudah larut dalam air, dalam gliserol P,
serta sukar larut dalam etanol P. Di pasar zat ini banyak dijumpai pada minuman
ringan bahkan beberapa produk sirup. Secara umum zat ini digunakan sebagai
penambah warna makanan seperti saus. Kelompok Ponceau yang dilarang sebagai
pewarna makanan dan minuman seperti Ponceau 3R yang biasa disebut Acid Red,
Ponceau SX (Food Red 1, FD dan C Red no. 4), dan Ponceau 6R. Zat-zat ini
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Hasil penelitian dari tiga sampel saus yang diuji dapat disimpulkan: bahwa
zat pewarna Bahan Tambahan Pangan yang digunakan untuk mewarnai saus
adalah zat pewarna sintetik (buatan) yang tidak diperbolehkan seperti Ponceau 3R
dan Orange RN.
5.2 Saran
1. Disarankan kepada masyarakat agar lebih berhati-hati dalam membeli dan
mengkonsumsi saus yang beredar di pasaran dengan warna yang mecolok
serta harga yang jauh lebih murah.
2. Disarankan kepada produsen agar memakai zat pewarna yang ditetapkan
oleh Pemerintah yang sesuai dengan SNI atau Permenkes RI
No.772/Menkes/Per/IX/1988 sehingga tidak merugikan kesehatan
konsumen.
3. Disarankan kepada pemerintah untuk melakukan pengawasan secara terus
menerus terhadap bahan makanan yang mengandung zat warna dan
melakukan penyuluhan terhadap industri-industri makanan yang memakai
DAFTAR PUSTAKA
Anonim. (2009). Mc Donald Say No to Tomat. Jakarta.www. kaskus.us. diaskes tanggal 11 Juni 2009.
Cahyadi, W. (2009). Analisis dan Aspek Kesehatan Bahan Tambahan Makanan.
Edisi ke-2. Bandung: Bumi Aksara. Halaman 25-36.
Cahyadi, W. (2009). Bahan Tambahan Pangan. Jakarta: Bumi Aksara. Halaman 63-74.
Depkes RI. (2011). Peraturan Menteri Kesehatan RI No.239/Menkes/Per/V/1985 Tentang Zat Warna Tertentu Yang Dinyatakan Sebagai Bahan Berbahaya.
Depkes RI, Jakarta.
Gritter, Roy J. (1991). Pengantar Kromatografi. Bandung: ITB. Halaman 157.
Sastrohamidjojo, H. (1985). Kromatografi. Yogyakarta: Liberty Yogyakarta. Halaman 1-24.
Syah, P. (2005). Manfaat dan Bahaya Bahan Tambahan Makanan. Jakarta. Balai Penerbit: FK UI. Halaman 37-43.
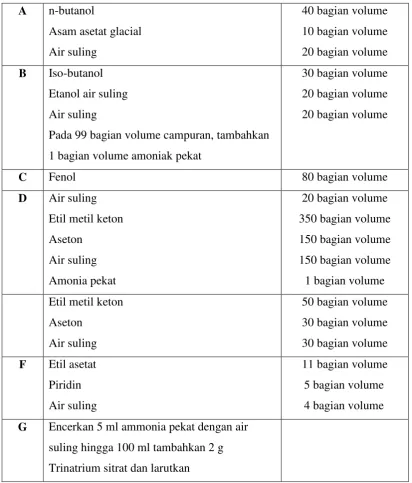
LAMPIRAN 1
TABEL PELARUT DALAM PERCOBAAN KROMATOGRAFI
A n-butanol
Asam asetat glacial Air suling
40 bagian volume 10 bagian volume 20 bagian volume
B Iso-butanol Etanol air suling Air suling
Pada 99 bagian volume campuran, tambahkan 1 bagian volume amoniak pekat
30 bagian volume 20 bagian volume 20 bagian volume
C Fenol 80 bagian volume
D Air suling Etil metil keton Aseton
Air suling Amonia pekat
20 bagian volume 350 bagian volume 150 bagian volume 150 bagian volume 1 bagian volume Etil metil keton
Aseton Air suling
50 bagian volume 30 bagian volume 30 bagian volume
F Etil asetat Piridin Air suling
11 bagian volume 5 bagian volume 4 bagian volume
G Encerkan 5 ml ammonia pekat dengan air suling hingga 100 ml tambahkan 2 g Trinatrium sitrat dan larutkan
LAMPIRAN 2
Gambar 1. Sampel A
Gambar 2. Sampel B
Gambar 4. Residu dalam metanol