STANDARDISASI EKSTRAK ETANOL TANAMAN
KATUMPANGAN AIR (
Peperomia pellucida
L. Kunth)
SKRIPSI
MUCHAMMAD IRSYAD
NIM. 109102000019
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
STANDARDISASI EKSTRAK ETANOL TANAMAN
KATUMPANGAN AIR (
Peperomia pellucida
L. Kunth)
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
MUCHAMMAD IRSYAD
NIM. 109102000019
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
Skripsi ini adalah hasil karya sendiri,
dan semua sumber yang dikutip maupun dirujuk
telah saya nyatakan dengan benar.
Nama : Muchammad Irsyad
NIM : 109102000019
Tanda Tangan :
Nama : Muchammad Irsyad Program Studi : Farmasi
Judul : Standardisasi Ekstrak Etanol Tanaman Katumpangan Air
(Peperomia pellucida L. Kunth)
Katumpangan air (Peperomia pellucida L. Kunth) merupakan salah satu tanaman obat potensial yang digunakan masyarakat untuk pengobatan asam urat, rematik, sakit kepala, maupun sakit perut. Kandungan kimia yang terkandung dalam tanaman ini adalah alkaloid, tanin, saponin, flavonoid, dan triterpenoid. Penelitian ini bertujuan untuk menetapkan beberapa parameter non spesifik maupun parameter spesifik dari ekstrak etanol tanaman katumpangan air. Standardisasi ekstrak tanaman obat perlu dilakukan untuk menjaga penggunaan obat alami yang tidak sesuai syarat mutu. Standardisasi dilakukan dengan menetapkan parameter spesifik dan non spesifik dari tiga tempat tumbuh yang berbeda yaitu Tangerang Selatan, Bogor, Yogyakarta. Hasil standardisasi untuk parameter spesifik menunjukkan organoleptik ekstrak (kental, warna coklat hijau kehitaman, rasa pahit dan berbau khas), dengan kandungan senyawa larut dalam air (7,39%±0,433
– 13,29%±3,311), larut dalam etanol (15,33%±0,635 – 16,68%±0,898), dan kadar total flavonoid (3,807%±0,007 – 4,244%±0,003). Hasil untuk parameter non spesifik menunjukkan kadar air (12,25%±0,372 – 16,34%±0,655), kadar abu total (1,21%±0,117 - 2,78%±0,458), kadar abu tidak larut asam (0,19%±0,030 – 1,62%±0,152), susut pengeringan (21,62%±2,257 – 24,98%±0,697), dan bobot jenis (1,00g/mL±0,000 – 1,00g/mL±0,002). Hasil pengujian cemaran mikroba (0,61 x 103 – 1,13 x 103 koloni/g) sedangkan pengujian cemaran kapang/khamir (0,1 x 102 – 1,7 x 102 koloni/g) serta hasil pengujian logam timbal (0,15 – 0,18 mg/kg), cadmium (0 – 0,11 mg/kg), dan arsen (< 0,005 µg/kg).
Nama : Muchammad Irsyad Program Studi : Pharmacy
Judul : Standardization of Extract Ethanol of Katumpangan Air (Peperomia pellucida L. Kunth)
Peperomia pellucida L. unth known as “ atumpangan ir” is one of the
potential medicinal plants that used for the treatment of the gout, rheumatism, headache, and abdominal pain. Chemical constituents contained in this plant are alkaloids, tannins, saponins, flavonoids, and triterpenoids. This study aims to establish some non-specific parameters and the specific parameters of the ethanol extract from katumpangan air. Standardization needs to be done to keep the use of natural medicines that do not fit the quality requirements. Standardization is done by determine the specific and non-specific parameters of three different growth places such as the South Tangerang, Bogor, and Yogyakarta. The results of standardization for specific parameters showed organoleptic extract (thick, blackish green brown color, bitter taste and characteristic odor), the content of water-soluble compounds (7,39%±0,433 – 13,29%±3,311), soluble in ethanol (15,33%±0,635 – 16,68%±0,898), and total flavonoid content (3,807%±0,007 – 4,244%±0,003). Results for non-specific parameter shows moisture content (12,25%±0,372 – 16,34%±0,655), total ash content (1,21%±0,117 – 2,78%±0,458), acid insoluble ash content (0,19%±0,030 – 1,62%±0,152), drying
shrinkage (21,62%±2,257 – 24,98%±0,697), and specific gravity
(1,00g/mL±0,000 – 1,00g/mL±0,002). Microbial contamination testing results (0,61x103– 1,13x103 coloni/g) while the contaminant testing mold/yeast (0,1x102
– 1,7x102 coloni/g) as well as test results lead metal (0,15 – 0,18 mg/kg), cadmium (0 – 0,11 mg/kg), and arsenic (<0.005µg/kg).
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah
melimpahkan nikmat dan karunia-Nya sehingga penulis dapat menyelesaikan
penelitian dan penyusunan skripsi ini.
Skripsi dengan judul “Standardisasi Ekstrak Etanol Tanaman Katumpangan Air (Peperomia pellucida L. Kunth)” ini disusun untuk memenuhi salah satu syarat menempuh ujian akhir guna mendapatkan gelar Sarjana Farmasi
pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas
Islam Negeri Syarif Hidayatullah Jakarta.
Dalam proses penelitian dan penyusunan skripsi ini penulis menyadari ada
beberapa pihak yang sangat memberikan kontribusi kepada penulis. Maka
perkenankanlah penulis menyampaikan rasa terima kasih yanng sebesar-besarnya
khususnya kepada :
1. Ibu Puteri Amelia, M. Farm., Apt. sebagai pembimbing I dan Ibu Marissa
Angelina, M. Farm., Apt. sebagai pembimbing II yang telah rela
meluangkan waktu, pikiran dan tenaganya untuk membimbing serta
memotivasi penulis selama penelitian.
2. Dr. Linar Zalinar Udin selaku Kepala Pusat Penelitian Kimia Lembaga
Ilmu Pengetahuan Indonesia beserta staff atas penggunaan segala fasilitas
dan bantuannya selama penelitian.
3. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp.And selaku Dekan Fakultas
Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Drs. Umar Mansur, M.Sc., Apt. selaku Ketua Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
5. Ayahanda ambang rif isworo dan Ibunda Noor Sa’diyah yang selalu
memberikan kasih sayang semangat dukungan dan do’a terbaik yang tak
terhingga di setiap langkah penulis.
6. Pakdhe Choiruzad, Budhe Tini, Om Aflah, Tante Dewi, yang telah
selama penelitian.
8. Bapak/Ibu Dosen yang telah membimbing penulis selama mengikuti
proses kuliah dan praktikum serta staff akademika di Program Studi
Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam
Negeri Syarif Hidayatullah Jakarta.
9. Pemberi semangat yang selalu mendoakan dan selalu sabar menghadapi
penulis dalam menyelesaikan penelitian ini, Pratiwi Ramelia.
10.Teman-teman dekat penulis, Muhammad Arif, Gian Pertela, Indah Fadlul
Maula, Nadya Zahrayny. Serta teman penelitian di LIPI Serpong Puslit
Kimia, Risda dan Neneng.
11.Teman-teman Farmasi angkatan 2009 atas dukungan, pertemanan dan
kerjasamanya.
12.Semua pihak yang telah membantu penulis selama ini yang tidak bisa
disebutkan satu persatu.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, namun
penulis berharap semoga hasil penelitian ini dapat bermanfaat bagi perkembangan
ilmu pengetahuan pada umumnya dan ilmu farmasi pada khususnya.
Jakarta, September 2013
Sebagai civitas akademik Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta, saya yang bertanda tangan dibawah ini :
Nama : Muchammad Irsyad
NIM : 10910200019
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan (FKIK)
Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya
ilmiah saya dengan judul
STANDARDISASI EKSTRAK ETANOL TANAMAN
KATUMPANGAN AIR (Peperomia pellucida L. Kunth)
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital
Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta
untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Dengan demikian persetujuan publikasi karya ilmiah ini saya buat dengan
sebenarnya.
Dibuat di : Ciputat
Pada Tanggal : 25 September 2013
Yang menyatakan
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN SKRIPSI ... v
ABSTRAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
DAFTAR ISI ... xi
1.3 Tujuan Penelitian... 3
1.4 Manfaat Penelitian... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Katumpangan Air (Peperomia pellucida L. Kunth)... 5
2.1.1 Klasifikasi Tanaman... 5
2.1.2 Nama Daerah ... 5
2.4.1 Standardisasi Menjamin Keseragaman Khasiat ... 15
2.4.2 Standardisasi untuk Uji Klinik ... 15
2.4.3 Standardisasi Menjamin Aspek Keamanan dan Stabilitas Ekstrak ... 15
2.4.4 Standardisasi Meningkatkan Nilai Ekonomi ... 16
2.5 Penentuan Mutu Ekstrak ... 16
2.6 Kromatografi ... 18
BAB III METODE PENELITIAN ... 27
3.1 Tempat dan Waktu Penelitian ... 27
3.2 Bahan dan Alat ... 27
3.3.4 Penentuan Parameter-parameter Standardisasi ... 29
3.3.4.1 Parameter Spesifik ... 29
a. Identitas ... 29
b. Penetapan Organoleptik Ekstrak ... 29
c. Penentuan Kadar Senyawa Terlarut dalam Pelarut Tertentu ... 29
d. Identifikasi Kandungan Kimia Ekstrak ... 30
e. Kadar Total Flavonoid... 32
3.3.4.2 Parameter Non Spesifik ... 33
a. Penetapan Susut Pengeringan ... 33
b. Penetapan Kadar Air ... 33
c. Penetapan Kadar Abu ... 34
d. Penentuan Bobot Jenis ... 35
e. Penentuan Cemaran Mikroba dan Kapang .. 35
f. Penentuan Cemaran Logam ... 36
BAB IV HASIL DAN PEMBAHASAN ... 37
4.1 Hasil Determinasi Tanaman ... 37
4.2 Hasil Ekstrak Etanol Katumpangan Air ... 37
4.3 Hasil Parameter-parameter Standardisasi... 38
4.3.1 Parameter Spesifik ... 38
4.3.2 Parameter Non Spesifik... 39
Gambar 2.1 Tanaman Katumpangan Air (Peperomia pellucida L. Kunth) ... 6
Gambar 2.2 Skema alat dan proses pemisahan KLT ... 20
Gambar 2.3 Diagram skematis Spektrofotometer UV-Vis ... 23
Gambar 2.4 Diagram skematis Spektrofotometer Serapan Atom ... 24
Gambar 4.1 Pola kromatogram KLT dengan fase gerak 40:60 ... 44
Gambar 4.2 Hasil uji cemaran mikroba P. pellucida Tangerang Selatan ... 48
Gambar 4.3 Hasil uji cemaran mikroba P. pellucida Bogor ... 49
Gambar 4.4 Hasil uji cemaran mikroba P. pellucida Yogyakarta ... 50
Gambar 4.5 Hasil uji cemaran kapang P. pellucida Tangerang Selatan ... 51
Gambar 4.6 Hasil uji cemaran kapang P. pellucida Bogor ... 52
Gambar 4.7 Hasil uji cemaran kapang P. pellucida Yogyakarta ... 53
Gambar L.1 Ekstrak etanol P. pellucida Tangerang Selatan ... 65
Gambar L.2 Ekstrak etanol P. pellucida Bogor ... 65
Gambar L.3 Ekstrak etanol P. pellucida Yogyakarta ... 65
Gambar L.4 Maserasi simplisia P. pellucida ... 65
Gambar L.5 Penghalusan simplisia P. pellucida ... 65
Gambar L.6 Pemekatan maserat dengan vacuum rotary evaporator ... 65
Gambar L.7 Furnace ... 66
Gambar L.8 Sperktrofotometer UV-Vis ... 66
Gambar L.9 Autoklaf ... 66
Gambar L.10 Bagan pembuatan masing-masing ekstrak P. pellucida ... 74
Gambar L.11 Kromatogram ekstrak etanol P. pellucida sebelum UV 254nm ... 92
Tabel 4.1 Hasil rendemen ekstrak etanol katumpangan air ... 37
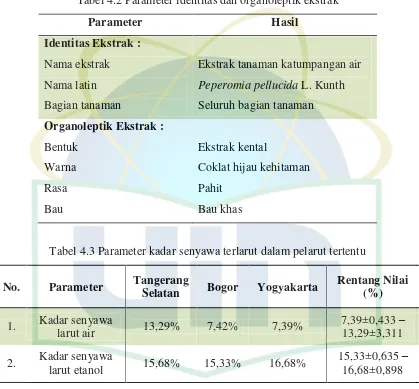
Tabel 4.2 Parameter identitas dan organoleptik ekstrak ... 38
Tabel 4.3 Parameter kadar senyawa terlarut dalam pelarut tertentu ... 38
Tabel 4.4 Identifikasi golongan kimia ekstrak ... 38
Tabel 4.5 Parameter non spesifik ekstrak katumpangan air ... 39
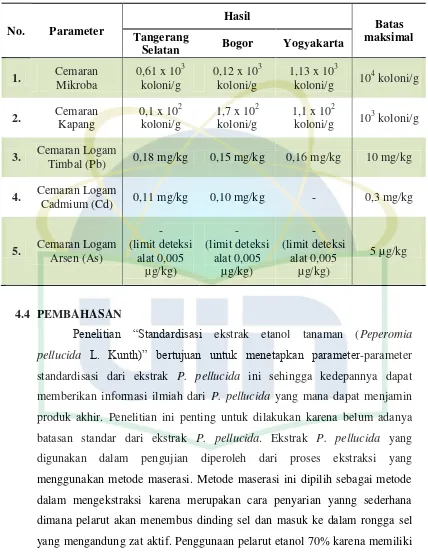
Tabel 4.6 Parameter non spesifik cemaran-cemaran... 40
Tabel 4.7 Nilai Rf dengan perbandingan fase gerak 40:60 ... 44
Tabel L.1 Senyawa terlarut dalam air ... 76
Tabel L.2 Senyawa terlarut etanol ... 78
Tabel L.3 Kadar air ... 80
Tabel L.4 Kadar abu total... 82
Tabel L.5 Kadar abu tidak larut asam ... 84
Tabel L.6 Susut pengeringan... 86
Tabel L.7 Bobot jenis ... 88
Tabel L.8 Cemaran mikroba ... 90
Tabel L.9 Cemaran kapang/khamir ... 91
Tabel L.10 Nilai Rf dengan fase gerak n-heksan : etil asetat ... 93
Tabel L.11 Cemaran logam ... 94
Lampiran 1 Alur Penelitian ... 63
Lampiran 2 Determinasi Tanaman Katumpangan Air ... 64
Lampiran 3 Bahan dan Alat Penelitian ... 65
Lampiran 4 Hasil Uji Cemaran Logam ... 67
Lampiran 5 Kurva Kalibrasi Standar Quersetin ... 71
Lampiran 6 Kurva Kalibrasi Standar Logam Pb+, Cd+, As+ ... 72
Lampiran 7 Skema Perolehan Ekstrak P. pellucida ... 74
Lampiran 8 Perhitungan Rendemen Ekstrak... 75
Lampiran 9 Perhitungan Senyawa Terlarut Air ... 76
Lampiran 10 Perhitungan Senyawa Terlarut Etanol ... 78
Lampiran 11 Perhitungan Kadar Air ... 80
Lampiran 12 Perhitungan Kadar Abu Total ... 82
Lampiran 13 Perhitungan Kadar Abu Tidak Larut Asam ... 84
Lampiran 14 Perhitungan Susut Pengeringan ... 86
Lampiran 15 Perhitungan Bobot Jenis ... 88
Lampiran 16 Perhitungan Cemaran Mikroba ... 90
Lampiran 17 Perhitungan Cemaran Kapang/Khamir ... 91
Lampiran 18 Pola Kromatogram KLT ... 92
Lampiran 19 Perhitungan Cemaran Logam ... 94
1.1 LATAR BELAKANG
Tanaman obat sudah sejak zaman dahulu dipergunakan untuk
meningkatkan kesehatan, memulihkan kesehatan, pencegahan penyakit dan
penyembuhan oleh masyarakat Indonesia. Indonesia memiliki berbagai
keaneka ragaman hayati sehingga Indonesia kaya akan sumber bahan obat
alam dan tradisional yang digunakan untuk ramuan obat tradisional secara
turun temurun (Saifudin, 2011). Dalam dasa warsa terakhir, perhatian dunia
terhadap obat-obatan dari bahan alam (obat tradisional) menunjukkan
peningkatan, baik di negara-negara berkembang maupun di negara-negara
maju. Badan Kesehatan Dunia (WHO) menyebutkan bahwa hingga 65%
dari penduduk negara-negara maju telah menggunakan pengobatan
tradisional (Depkes, 2007).
Pengembangan obat tradisional diusahakan agar dapat sejalan
dengan pengobatan modern. Berbagai penelitian dan pengembangan yang
memanfaatkan kemajuan teknologi juga dilakukan sebagai upaya
peningkatan mutu dan keamanan produk yang diharapkan dapat lebih
meningkatkan kepercayaan terhadap manfaat obat tradisional juga didukung
oleh Peraturan Menteri Kesehatan Republik Indonesia, tentang fitofarmaka,
yang berarti diperlukan adanya pengendalian mutu simplisia yang akan
digunakan untuk bahan baku obat atau sediaan galenik (BPOM, 2005).
Salah satu cara untuk mengendalikan mutu simplisia adalah dengan
melakukan standardisasi simplisia. Standardisasi diperlukan agar dapat
diperoleh bahan baku yang seragam yang akhirnya dapat menjamin efek
farmakologi tanaman tersebut (BPOM, 2005). Selain itu dilakukannya
standardisasi diperlukan untuk menjamin aspek keamanan dan stabilitas
ekstrak. Fakta menyebutkan bahwa obat berbasis tumbuhan telah melekat di
dalam kehidupan masyarakat dimana Indonesia merupakan negara terkaya
biodiversitasnya, kecenderungan masyarakat kembali ke alam meneguhkan
ekonomi tinggi. Pemikiran pemerintah yang menjadi isu besar adalah
bagaimana menjamin obat yang berbasis herbal di atas memiliki mutu yang
terukur, mampu mendukung derajat kesehatan dan terjamin keamanan
terbebas dari bahan dan mikroba berbahaya serta bagaimana menaikkan
nilai ekonomi sehingga menjadi negara produsen yang bermartabat
(Saifudin, 2011).
Pemerintah RI melalui Depkes-BPOM mulai mengintensifkan
pembuatan standar dan acuan standardisasi bahan obat alam. Namun,
ekstrak tanaman yang sudah dibakukan standardisasinya baru sedikit. Hal
ini jika dibandingkan dengan ribuan tanaman obat dan berpotensi obat
sangatlah penting untuk dilakukan standardisasi untuk tanaman lainnya.
Dengan demikian prospek dan pekerjaan standardisasi bahan obat alam
merupakan isu besar dan tantangan besar hingga tahun-tahun mendatang.
(Saifudin, 2011).
Tanaman katumpangan air (Peperomia pellucida L. Kunth)
merupakan tanaman yang berasal dari Amerika Selatan tetapi umumnya
ditemukan di Asia Tenggara (Purba, 2007). Tanaman ini biasa digunakan
masyarakat untuk pengobatan asam urat, rematik, sakit kepala maupun sakit
perut. Bagian tanaman yang sering digunakan masyarakat ini yaitu seluruh
dari tanaman ini, atau sering disebut herba. Bahkan di Filipina tanaman ini
yang disebut masyarakat sekitar disebut pansit-pansitan dapat dimanfaatkan
sebagai obat antara lain untuk menurunkan kadar asam urat dan untuk
mengobati masalah ginjal (Majumder, Pulak et al., 2011). Di Kalimantan
oleh penduduk lokal, banyak digunakan dengan cara direbus dan air
rebusannya diminum untuk mengatasi sakit reumatik karena asam urat
tinggi. Selain itu juga dimanfaatkan sebagai obat untuk mengatasi penyakit
ginjal, sakit perut, abses, bisul, jerawat, radang kulit, luka bakar, batuk,
diare, masuk angin serta hipertensi (Purba, 2007). Sedangkan di Amerika
Selatan masyarakatnya menggunakan rebusan daun dan batangnya untuk
pengobatan asam urat dan artritis (Majumder, Pulak, 2011).
Beberapa hasil penelitian yang telah dilakukan dapat menunjukkan
antiinflamasi (Wijaya dan Monica, 2004), memiliki efek antipiretik (Khan,
et al., 2008), antimikroba dan antikanker (Wei, et al., 2011) dan memiliki
efek analgetik (Mulyani, 2011). Selain itu juga di Indonesia juga sudah ada
produk berlabel jamu yang dipasarkan untuk pengobatan asam urat dengan
komposisi adanya campuran ekstrak P. pellucida. Dengan banyaknya
penggunaan masyarakat terhadap tanaman katumpangan air ini maka dirasa
perlu untuk dilakukan proses standardisasi sehingga dapat dibuat bahan
baku obat yang terjamin mutunya.
Pada penelitian ini dilakukan standardisasi terhadap ekstrak tanaman
katumpangan air yang berasal dari tiga tempat tumbuh daerah yang berbeda
yaitu Tangerang Selatan, Bogor, dan Yogyakarta dengan menetapkan
parameter standar umum ekstrak yaitu parameter non spesifik yang meliputi
susut pengeringan, bobot jenis, kadar air, kadar abu, cemaran mikroba dan
kapang, dan cemaran logam berat, serta parameter spesifik yang meliputi
identitas ekstrak, organoleptik ekstrak, senyawa terlarut dalam pelarut
tertentu, pola kromatogram, dan kandungan kimia ekstrak.
1.2 RUMUSAN MASALAH
Belum dilakukannya standardisasi tanaman katumpangan air
(P. pellucida L. Kunth).
1.3 TUJUAN PENELITIAN
1. Menetapkan parameter non spesifik yang meliputi susut pengeringan,
bobot jenis, kadar air, kadar abu, cemaran mikroba dan kapang, dan
cemaran logam berat pada ekstrak etanol tanaman katumpangan air
(P. pellucida L. Kunth).
2. Menetapkan parameter spesifik yang meliputi identitas ekstrak,
organoleptik ekstrak, senyawa terlarut dalam pelarut tertentu, pola
kromatogram, dan kandungan kimia ekstrak pada ekstrak etanol
1.4 MANFAAT PENELITIAN
Hasil penelitian ini diharapkan dapat memberikan informasi ilmiah
dari tanaman katumpangan air dalam upaya menjamin keamanan
2.1 KATUMPANGAN AIR (Peperomia pellucida L. Kunth)
2.1.1 Klasifikasi Tanaman
Adapun klasifikasi tumbuhan ini adalah sebagai berikut:
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivision : Spermatophyta
Division : Magnoliophyta
Class : Magnoliopsida (Dicotyledons)
Subclass : Magnoliidae
Order : Piperales
Family : Piperaceae
Genus : Peperomia
Species : Peperomia pellucida L. Kunth
(sumber: Majumder, Pulak et al, 2011)
2.1.2 Nama Daerah
Nama daerah dari tumbuhan ini adalah sladanan, rangu-rangu,
suruhan (Jawa), saladaan (Sunda), tumpangan air (Sumatera, Jakarta),
gofu goroho (Ternate), ulasiman bato (Filipina), cao hu jiao (Cina)
(Hariana, Arief., 2006)
2.1.3 Deskripsi
Katumpangan Air (Peperomia pellucida L. Kunth) merupakan
tumbuhan yang biasanya tumbuh liar di tempat-tempat yang lembab
dan bergerombol. Tumbuhan katumpangan air merupakan famili
Piperaceae (suku sirih-sirihan) dengan genus Peperomia. Tumbuhan ini
mudah dijumpai di kebun, halaman rumah, tepi jalan, di pinggiran
selokan, dan di tempat lain yang lembab atau berair. Tumbuhan ini
tropis dan subtropis. Tingginya sekitar 10-20 cm, dengan batang yang
tegak, bercabang, lunak dan berwarna hijau pucat dengan akar yang
serabut dangkal dan berwarna putih. Memiliki bunga majemuk
berbentuk bulir yang terdapat pada pangkal. Lebar daun katumpangan
air ini sekitar 0.5-2 cm berbentuk hati dan panjang sekitar 4 cm
(Hariana, Arief., 2006).
Gambar 2.1 Tanaman Katumpangan Air (sumber: koleksi pribadi, 2013)
2.1.4 Tempat Tumbuh
Tumbuhan ini tersebar luas di Amerika Selatan dan banyak
negara-negara Asia, tumbuh sekitar 400 m dpl (diatas permukaan laut)
sebagai gulma di sepanjang pinggir jalan, di perkebunan, di tanah
lembab dan di tempat teduh sekitar rumah yang biasanya
menggerombol. Sebagian besar tumbuhan ini banyak ditemukan di
daerah tropis (Majumder, Pulak et al., 2011). Peperomia pellucida
secara luas didistribusikan di banyak negara Amerika dan Asia Selatan
(Arrigoni-Blank, 2002).
2.1.5 Kandungan Kimia
Senyawa kimia yang terdapat dalam katumpangan air
2011), flavonoid (Majumder, Pulak et al, 2011), Selain itu menurut
Majumder Pulak (2011) juga memiliki aktivitas antijamur.
2.1.6 Khasiat
Katumpangan air (P. pellucida L. Kunth) sering digunakan
sebagai ramuan dalam pengobatan tradisional. Tumbuhan ini memiliki
manfaat dalam pengobatan sakit kepala, demam, sakit perut, abses,
bisul dan gangguan ginjal (Oloyede, 2011). Menurut penelitian Sio,
Susie O (2001) P. pellucida L. Kunth dapat digunakan sebagai alternatif
pengobatan asam urat. Berbagai penelitian sudah dilakukan dan
menunjukkan bahwa tanaman ini memiliki aktivitas analgesik,
antipiretik, antiinflamasi, hipoglikemik (Sheikh H., et al, 2013),
antibakteri (Xu Su, 2005), antijamur (Majumder, Pulak et al, 2007),
antimikroba dan antikanker (Wei et al, 2011).
P. pellucida mempunyai banyak khasiat sebagai obat, namun
karakterisasinya belum ada dan masih sedikit yang meneliti tentang
kandungan kimianya. Menurut Hembing (2006), P. pellucida berkhasiat
untuk mengatasi nyeri pada rematik, penyakit asam urat, radang kulit,
luka terpukul dan luka bakar ringan. Bagian yang digunakan adalah
herba. Menurut hasil penelitian Muhtadi (2004), tentang aktivitas
antidiabetes ekstrak etanol dari herba suruhan (Peperomia pellucida
H.B.&K.), hasil penapisan fitokimia dari ekstrak etanol menunjukkan
adanya golongan senyawa steroida.
2.2 EKSTRAKSI
2.2.1 Pengertian Ekstraksi
Pengambilan bahan aktif dari suatu tumbuhan, dapat dilakukan
dengan cara ekstraksi. Pengertian ekstraksi adalah kegiatan penarikan
kandungan kimia yang dapat larut sehingga terpisah dari bahan yang
tidak dapat larut. Pengetahuan mengenai golongan senyawa aktif yang
dikandung dalam simplisia akan mempermudah proses pemilihan
ekstraksi adalah melarutkan senyawa polar dalam pelarut polar dan
senyawa non polar dalam senyawa non polar. Metode ekstraksi dipilih
berdasarkan beberapa faktor seperti sifat dari bahan mentah obat, daya
penyesuaian dengan tiap macam metode ekstraksi, dan kepentingan
dalam memperoleh ekstrak yang sempurna atau mendekati sempurna
(Ansel, 1989).
2.2.2 Metode Ekstraksi
Beberapa metode ekstraksi dengan menggunakan pelarut
(Depkes, 2000) yaitu:
1). Cara dingin
a. Maserasi
Maserasi ialah proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau
pengadukan pada temperatur ruangan (kamar). Secara teknologi
termasuk ekstraksi dengan prinsip metode pencapaian
konsentrasi pada keseimbangan. Maserasi kinetik berarti
dilakukan pengadukan yang kontinyu (terus-menerus).
Remaserasi berarti dilakukan pengulangan penambahan pelarut
setelah dilakukan penyaringan maserat pertama, dan seterusnya.
b. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu
baru sampai sempurna (exhaustive extraction) yang umumnya
dilakukan pada temperatur ruangan. Proses ini terdiri dari
tahapan pengembangan bahan, tahap maserasi antara, tahap
perkolasi sebenarnya (penetesan/penampungan ekstrak), terus
menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya
2). Cara Panas
a. Refluks
Refluks merupakan ekstraksi dengan pelarut pada
temperatur titik didihnya, selama waktu tertentu dan jumlah
pelarut terbatas yang relatif konstan dengan adanya pendingin
balik. Umumnya dilakukan pengulangan proses pada residu
pertama sampai 3-5 kali sehingga dapat termasuk proses
ekstraksi sempurna.
b. Sokletasi
Sokletasi ialah ekstraksi dengan menggunakan pelarut
yang selalu baru yang umumnya dilakukan dengan alat khusus
sehingga terjadi ekstraksi kontinyu dengan jumlah pelarut relatif
konstan dengan adanya pendinginan balik.
c. Digesti
Digesti merupakan maserasi kinetik (dengan pengadukan
kontinyu) pada temperatur yang lebih tinggi dari temperatur
ruangan (kamar), yaitu secara umum dilakukan pada temperatur
40-50oC.
d. Infusa
Infusa adalah ekstraksi dengan pelarut air pada
temperatur penangas air mendidih, temperatur terukur 96oC -
98oC selama waktu tertentu (15-20 menit).
e. Dekok
Dekok adalah infus yang waktunya lebih lama (lebih dari
30 menit) dan temperatur sampai titik didih air.
2.3 EKSTRAK
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi
senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan
pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan
dan massa atau serbuk yang tersisa diperlakukan sedemikian hingga
ekstrak yakni: ekstrak cair, ekstrak kental dan ekstrak kering. Ekstrak cair
jika hasil ekstraksi masih bisa dituang, biasanya kadar air lebih dari 30%.
Ekstrak kental jika memiliki kadar air antara 5-30%. Ekstrak kering jika
mengandung kadar air kurang dari 5% (Voigt, 1994).
2.4 STANDARDISASI
Standardisasi dalam kefarmasian tidak lain adalah serangkaian
parameter, prosedur dan cara pengukuran yang hasilnya merupakan
unsur-unsur terkait paradigma mutu kefarmasian, mutu dalam artian memenuhi
syarat standard (kimia, biologi dan farmasi), termasuk jaminan (batas-batas)
stabilitas sebagai produk kefarmasian umumnya. Persyaratan mutu ekstrak
terdiri dari berbagai parameter standar umum dan parameter standar
spesifik. Pengertian standardisasi juga berarti proses menjamin bahwa
produk akhir obat (obat, ekstrak atau produk ekstrak) mempunyai nilai
parameter tertentu yang konstan (ajeg) dan ditetapkan terlebih dahulu
(Depkes, 2000).
Mengingat obat herbal dan berbagai tanaman memiliki peran penting
dalam bidang kesehatan bahkan bisa menjadi produk andalan Indonesia
maka perlu dilakukan upaya penetapan standar mutu dan keamanan ekstrak
tanaman obat (Saifudin, 2011).
Dalam standardisasi obat herbal dapat meliputi dua aspek: (Depkes,
2000)
1. Aspek parameter spesifik
Parameter spesifik adalah aspek kandungan kimia kualitatif dan
aspek kuantitatif kadar senyawa kimia yang bertanggung jawab langsung
terhadap aktivitas farmakologis tertentu.
1) Identitas (parameter identitas ekstrak) meliputi : deskripsi tata nama,
nama ekstrak (generik, dagang, paten), nama lain tumbuhan
(sistematika botani), bagian tumbuhan yang digunakan (rimpang,
2) Organoleptik
Parameter organoleptik ekstrak meliputi penggunaan panca indera
mendeskripsikan bentuk, warna, bau, rasa guna pengenalan awal
yang sederhana se-objektif mungkin.
3) Senyawa terlarut dalam pelarut tertentu
Yaitu melarutkan ekstrak dengan pelarut (alkohol/air) untuk
ditentukan jumlah larutan yang identik dengan jumlah senyawa
kandungan secara gravimetrik. Dalam hal tertentu dapat diukur
senyawa terlarut dalam pelarut lain misalnya heksana, diklorometan,
metanol. Tujuannya untuk memberikan gambaran awal jumlah
senyawa kandungan.
4) Uji kandungan kimia ekstrak
a) Pola kromatogram
Dilakukan sebagai analisis kromatografi sehingga memberikan
pola kromatogram yang khas. Bertujuan untuk memberikan
gambaran awal komposisi kandungan kimia berdasarkan pola
kromatogram (KLT/KCKT)
b) Kadar kandungan kimia tertentu
Suatu kandungan kimia yang berupa senyawa identitas atau
senyawa kimia utama ataupun kandungan kimia lainnya, maka
secara kromatografi instrumental dapat dilakukan penetapan
kadar kandungan kimia tersebut. Instrumen yang dapat digunakan
adalah densitometri, kromatografi gas, KCKT atau instrumen
yang sesuai. Tujuannya memberikan data kadar kandungan kimia
tertentu sebagai senyawa identitas atau senyawa yang diduga
bertanggung jawab pada efek farmakologi (Depkes, 2000).
2. Aspek parameter non spesifik
Parameter non spesifik adalah segala aspek yang tidak terkait
dengan aktivitas farmakologis secara langsung namun mempengaruhi
1) Susut pengeringan dan bobot jenis
a) Parameter susut pengeringan yaitu pengukuran sisa zat setelah
pengeringan pada temperatur 105°C selama 30 menit atau
sampai berat konstan yang dinyatakan sebagai nilai persen.
Dalam hal khusus (jika bahan tidak mengandung minyak
menguap/atsiri dan sisa pelarut organik menguap) identik
dengan kadar air, yaitu kandungan air karena berada di
atmosfer/lingkungan terbuka. Adapun tujuan menentukan susut
pengeringan untuk memberikan batasan maksimal (rentang)
tentang besarnya senyawa yang hilang pada proses pengeringan.
b) Parameter bobot jenis adalah masa per satuan volume pada suhu
kamar tertentu (25°C) yang ditentukan dengan alat khusus
piknometer atau alat lainnya. Adapun tujuan menentukan bobot
jenis ekstrak yaitu memberikan batasan tentang besarnya masa
per satuan volume yang merupakan parameter khusus ekstrak
cair sampai ekstrak pekat (kental) yang masih dapat dituang.
2) Kadar air
Yaitu pengukuran kandungan air yang berada di dalam bahan,
dilakukan dengan cara yang tepat diantara cara titrasi, destilasi atau
gravimetrik. Adapun tujuan menentukan kadar air untuk
memberikan batasan minimal atau rentang tentang besarnya
kandungan air di dalam bahan.
3) Sisa pelarut
Yaitu menentukan kandungan sisa pelarut tertentu (yang memang
ditambahkan). Untuk ekstrak cair berarti kandungan pelarutnya,
misalnya kadar alkohol. Adapun tujuan menentukan sisa pelarut
untuk memberikan jaminan bahwa selama proses tidak
meninggalkan sisa pelarut yang memang seharusnya tidk boleh ada.
Sedangkan untuk ekstrak cair menunjukkan jumlah pelarut (alkohol)
4) Cemaran logam berat
Yaitu menentukan kandungan logam berat secara spektroskopi
serapan atom yang lebih valid. Adapun tujuan uji cemaran logam
berat untuk memberikan jaminan bahwa ekstrak tidak mengandung
logam berat tertentu (As, Pb, Cd) melebihi nilai yang ditetapkan
karena berbahaya (toksik) bagi kesehatan.
5) Cemaran mikroba
Yaitu menentukan (identifikasi) adanya mikroba yang patogen
secara analisis mikrobiologis. Adapun tujuan dari uji cemaran
mikroba untuk memberikan jaminan bahwa ekstrak tidak boleh
mengandung mikroba patogen dan tidak mengandung mikroba non
patogen melebihi batas yang ditetapkan karena berpengaruh pada
stabilitas ekstrak dan berbahaya (toksik) bagi kesehatan.
6) Cemaran kapang/khamir
Yaitu menentukan adanya jamur secara mikrobiologis. Adapun uji
ini dilakukan untuk memberikan jaminan bahwa ekstrak tidak
mengandung semaran jamur melebihi batas yang ditetapkan karena
berpengaruh pada stabilitas ekstrak dan aflatoksin yang berbahaya
bagi kesehatan (Depkes, 2000).
Pemerintah melalui Departemen Kesehatan dan Badan POM
menetapkan standar dan parameter mutu dan keamanan bahan apapun
termasuk bahan obat herbal yang dikonsumsi oleh masyarakat. Standar
inilah yang digunakan oleh institusi yang memiliki kepentingan dengan obat
herbal dan mereka harus menepati mutu produk yang telah ditetapkan
(Saifudin, 2011).
Produsen, suplier, agen, pengimpor dan pengekspor berbahan baku
ekstrak wajib menaati ketentuan pengujian, parameter hasil dan metode
yang digunakan termasuk instrumentasi dan parameter keamanan. Untuk itu
harus melakkukan proses standardisasi ekstrak jika produk herbal beredar di
masyarakat sebagai obat herbal terstandard dan fitofarmaka (Saifudin,
Terdapat 3 kategori obat herbal yang beredar di Indonesia, yakni:
(Saifudin, 2011)
1. Jamu
Suatu bahan pengobatan tradisional namun sudah terdaftar di
institusi pemerintah yang tanpa dilakukan standardisasi yang belum
mengalami standardisasi dan belum diteliti khasiat atau farmakologinya
baik secara pra klinik maupun klinik.
2. Obat herbal terstandar
Suatu bahan baku telah distandardisasi dan telah diteliti serta
terbukti khasiatnya secara pra klinik pada hewan uji.
3. Fitofarmaka
Suatu bahan baku telah distandardisasi dan khasiatnya telah
dibuktikan secara klinik pada pasien manusia.
Idealnya ekstrak yang ditetapkan parameter mutu dan keamanannya
adalah ekstrak yang berasal dari tanaman yang telah diteliti dan ditetapkan
efek farmakologis dan toksisitas kliniknya, yakni telah teruji pada pasien
sehingga output yang dihasilkan adalah produk dengan nilai ekonomi dan
berdaya guna tinggi (Saifudin, 2011).
Masyarakat secara turun temurun atau mengikuti tren dalam
mengonsumsi obat herbal tertentu yang sebenarnya banyak diantaranya
belum mengalami penelitian farmakologi maupun toksikologinya. Demikian
pula jamu yang beredar di pasaran, hendaknya minimal bahan baku
ekstraknya telah ditetapkan aspek parameter non spesifiknya (Saifudin,
2011).
Sudah menjadi tugas pemerintah untuk menetapkan parameter mutu
dan menjaga keamanan masyarakat dalam penggunaan obat herbal sehingga
bahan obat herbal apapun yang telah dikonsumsi masyarakat tetap pada
batas aman meskipun bahan atau produk belum mengalami uji farmakologi
2.4.1 Standardisasi Menjamin Keseragaman Khasiat
Mayoritas penggunaan bahan obat berbasis herbal di Indonesia
masih bersifat tidak terukur baik kepastian tanaman, takaran, cara
penyiapan sehingga tidak menjamin konsistensi khasiat. Salah satu
tujuan dari standardisasi adalah menjaga konsistensi dan keseragaman
khasiat dari obat herbal. Standardisasi melibatkan pemastian kadar
senyawa aktif farmakologis melalui analisis kuantitatif metabolit
sekunder yang akan menjamin keseragaman khasiat.
Tercatat sekitar 997 industri obat tradisional di Indonesia dan 98
diantaranya adalah produsen dengan skala besar dan sedang. Produsen
dengan skala besar dan sedang telah mampu mengekspor produknya ke
negara lain. Selain itu juga banyak bahan mentah rempah dan obat
herbal diekspor ke luar negeri tanapa mengalami pengolahan. Problem
yang seringkali dihadapi adalah belum terstandardnya bahan baku yang
diperdagangkan bahkan dijumpainya kontaminan mikrobiologis pada
produk obat herbal.
2.4.2 Standardisasi untuk Uji Klinik
Uji Klinik adalah uji senyawa kimia obat, obat herbal, ekstrak
dan berbagai sediaan pada dosis tertentu dengan target biologis manusia
agar memberikan respon biologis berupa parameter-parameter klinik
perbaikan dari kondisi patologis yang terkait dengan penyakit tertentu.
Untuk itu semua aspek dituntut terdesain dan dikontrol dengan baik.
Respon uji klinik sangat ditentukan oleh konsistensi dosis. Jika jumlah
zat aktif yang diberikan tidak konsisten maka disini peran besar
standardisasi untuk menjaga senyawa-senyawa aktif selalu konsisten
terukur antarperlakuan.
2.4.3 Standardisasi Menjamin Aspek Keamanan dan Stabilitas Ekstrak
Tempat tumbuh tanaman, penanganan pasca panen, proses
ekstraksi, penyimpanan simplisia tanaman dan ekstrak juga
pestisida dalam tanah, udara dan air, jenis dan jumlah mikroorganisme
dan metabolit pencemar berbahaya. Keberadaan air di dalam suatu
ekstrak juga mempengaruhi stabilitas bahan baku bahkan bentuk
sediaan yang nantinya dihasilkan. Untuk itu dilakukan berbagai analisis
untuk menentukan batas minimal kadar air, zat dan jumlah mikroba
pencemar. Proses standardisasi yang meliputi aspek kimiawi metabolit
sekunder, jumlah cemaran mikroba minimal dan cemaran logam berat
sangatlah penting karena terkait dengan khasiat dan keamanan pada
konsumen.
2.4.4 Standardisasi Meningkatkan Nilai Ekonomi
Tanaman obat dan rempah Indonesia mempunyai potensi besar
sebagai produk unggulan. Belum tingginya upaya lintas sektoral dan
terpadu antara swasta-pemerintah-perguruan tinggi untuk mengangkat
secara sistematis natural product Indonesia mengakibatkan banyak
produk ekspor herbal yang berdaya tawar rendah. Standardisasi adalah
upaya penting untuk menaikkan nilai ekonomi produk alam Indonesia.
2.5 PENENTUAN MUTU EKSTRAK
Lingkungan tempat tumbuh tanaman obat sangat mempengaruhi
kualitas dan keamanan bahan baku ekstrak dan produk akhir yang
dihasilkan. Tanaman budidaya akan lebih bisa dikontrol untuk
meningkatkan mutu. Beberapa aspek yang mempengaruhi mutu ekstrak
adalah (Saifudin, 2011):
1. Kesahihan tanaman
Tanaman obat sangat banyak dan sangat mirip secara morfologi
sehingga secara fundamental perlu dihindari kesalahan dalam
pengambilan spesies.
2. Genetik
Tanaman budidaya cenderung mempunyai genetik yang lebih
seragam sehingga mudah mengontrol kandungan senyawanya. Namun,
kimianya yang kurang baik tetapi bisa ditanggulangi dengan
pembentukan ekstrak dan proses standardisasi.
3. Lingkungan tempat tumbuh
Kualitas tanah, mutu air, dan iklim akan mempengaruhi kualitas
serta kuantitas metabolit sekunder (senyawa alami). Adanya
pencemaran logam berat dan mikroorganisme asing akan
mempengaruhi keamanan pada konsumen karena logam berat akan
terakumulasi dan akan terbentuk metabolit baru jika terdapat
mikroorganisme asing.
4. Waktu panen
Pemanenan sebaiknya dilakukan pada saat tanaman
mengandung kadar metabolit tertinggi. Untuk itu perlu diperhatikan
musim panen, kematangan organ terpilih dan siklus biosintesis harian.
Semua berdasarkan penelitian ilmiah terkait.
5. Penanganan pasca panen
Teknologi pasca panen berupa penggunaan alat, pengeringan
yang aman dan baik, pengepakan dan penyimpanan mempengaruhi
ekstrak. Demikian juga dengan pengeringan sinar matahari langsung
harus dikontrol agar zat-zat penting tidak rusak.
6. Teknologi ekstraksi
Pemilihan metode ekstraksi disesuaikan dengan kemampuan
industri pembuat. Metode ekstraksi apapun yang terpenting harus
memenuhi standar tidak dipermasalahkan. Penggunaan pelarut dan
peralatan logam atau kaca untuk ekstraksi harus cermat.
7. Teknologi pengentalan dan pengeringan ekstrak
Umumnya standardisasi dilakukan terhadap ekstrak kental yakni
ekstrak yang cukup liat karena masih mengandung air. Pengentalan
umumnya menggunakan tangas air, vacuum oven, freeze bulk dryer.
8. Cara menyimpan ekstrak
Penyimpanan yang baik yaitu dengan menyimpan yang
menghindarkan dari kontaminasi dan menjaga stabilitas ekstrak serta
menyebabkan uap air terabsorpsi ke dalam ekstrak sehingga kadar air
meningkat. Sebaiknya penyimpanan dilakukan di dalam ruang
berpengatur udara.
2.6 KROMATOGRAFI
Kromatografi adalah suatu metode pemisahan berdasarkan
perbedaan perpindahan dari komponen-komponen senyawa diantara dua
fase yaitu fase diam, dapat berupa zat cair atau zat padat, dan fase gerak,
dapat berupa gas atau zat cair (Depkes, 1995; Stahl, 1985). Fase diam dapat
berupa bahan padat dalam bentuk molekul kecil, atau dalam bentuk cairan
yanng dilapiskan pada pendukung padat atau dilapiskan pada dinding
kolom. Fase gerak dapat berupa gas atau cairan. Jika gas digunakan sebagai
fase gerak, maka prosesnya dikenal sebagai kromatografi gas. Dalam
kromatografi cair dan juga kromatografi lapis tipis, fase gerak yang
digunakan selalu cair (Gandjar dan Rohman, 2007).
Kromatografi dapat dibedakan atas berbagai macam tergantung pada
pengelompokannya. Menurut Gandjar dan Rohman kromatografi dibedakan
berdasarkan mekanisme pemisahannya menjadi: kromatografi adsorbsi,
kromatografi partisi, kromatografi pasangan ion, kromatografi penukar ion,
kromatografi eksklusi ukuran, dan kromatografi afinitas.
Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi
atas: kromatografi kertas, kromatografi lapis tipis, kromatografi cair kinerja
tinggi, dan kromatografi gas (Gandjar dan Rohman, 2007).
Pemisahan dan pemurnian kandungan tumbuhan terutama dilakukan
dengan mengunakan salah satu atau gabungan dari beberapa teknik tersebut
dan dapat digunakan pada skala mikro maupun makro (Harborne, 1987).
Dalam penggunaan kromatografi untuk tujuan kualitatif dapat
mengungkapkan ada atau tidak adanya senyawa tertentu dalam cuplikan.
Sedangkan untuk tujuan kuantitatif dapat menunjukkan banyaknya
masing-masing komponen campuran. Selain penggunaan kualitatif dan kuantitatif,
memperoleh komponen campuran dalam jumlah memadai dalam keadaan
murni.
Selama pemisahan kromatografi, solut individual akan membentuk
profil konsentrasi yanng simetris atau dikenal juga dengan profil Gaussian
dalam arah aliran fase gerak. Profil dikenal juga dengan puncak atau pita,
secara perlahan-lahan akan melebar dan sering juga membentuk profil yang
asimetrik karena solut-solut melanjutkan migrasinya ke fase diam (Gandjar
dan Rohman, 2007).
2.6.1 Kromatografi Lapis Tipis
Kromatografi lapis tipis (KLT) merupakan salah satu metode
pilihan kromatografi secara fisikokimia. Kromatografi lapis tipis
merupakan bentuk kromatografi planar. Berbeda dengan kromatografi
kolom yang mana fase diamnya dikemas di dalamnya, pada
kromatografi lapis tipis fase diamnya berupa lapisan yang seragam pada
permukaan bidang datar yang didukung oleh lempeng kaca atau plat
aluminium. Kromatografi lapis tipis ini dapat dikatakan sebagai bentuk
terbuka dari kromatografi kolom (Gandjar dan Rohman, 2007).
Fase diam yang biasa digunakan dalam kromatografi lapis tipis
adalah silika dan serbuk selulosa. Lempeng KLT telah tersedia di
pasaran dan telah ditambah dengan reagen fluoresen untuk
memfasilitasi deteksi bercak solut. Selain itu lempeng KLT juga telah
ditambahkan dengan agen pengikat seperti kalsium sulfat. Sedangkan
fase gerak yang digunakan harus memiliki kemurnian yang sangat
tinggi. Hal ini dikarenakan kromatografi lapis tipis merupakan teknik
yang sensitif (Gandjar dan Rohman, 2007).
Fase gerak pada kromatografi lapis tipis dapat dipilih
menggunakan sistem yang paling sederhana ialah campuran 2 pelarut
organik karena daya elusi campuran kedua pelarut ini dapat sudah
diatur sehingga pemisahan dapat terjadi secara optimal (Gandjar dan
Pemisahan pada kromatografi lapis tipis akan optimal jika
sampel ditotolkan dengan ukuran bercak sekecil dan sesempit mungkin.
Penotolan sampel yang tidak tepat akan menyebabkan bercak yang
menyebar dan puncak ganda. Untuk memperoleh reprodusibilitas,
volume sampel yang ditotolkan paling sedikit 0,5 µL. Jika volume
sampel yang akan ditotolkan lebih besar dari 2-10 µL maka penotolan
harus dilakukan secara bertahap dengan dilakukan pengeringan antar
totolan. Setelah sampel ditotolkan pada lempeng KLT, tahap
selanjutnya adalah mengembangkan sampel tersebut dalam suatu bejana
kromatografi yang sebelumnya telah dijenuhkan dengan fase gerak
(Gandjar dan Rohman, 2007).
Selama proses pengembangan, bejana kromatografi harus
tertutup rapat. Jumlah volume fase gerak harus mampu mengelusi
lempeng sampai ketinggian lempeng yang telah ditentukan. Setelah
lempeng terelusi, dilakukan deteksi bercak. (Gandjar dan Rohman,
2007).
Gambar 2.2 Skema alat dan proses pemisahan KLT
Bercak pemisahan pada KLT umumnya merupakan bercak yang
tidak berwarna. Untuk penentuannya dapat dilakukan secara kimia,
fisika, maupun biologi. Cara kimia yang biasa digunakan adalah dengan
mereaksikan bercak dengan suatu pereaksi melalui cara penyemprotan
sehingga bercak menjadi jelas. Cara fisika yang dapat digunakan untuk
menampakkan bercak adalah dengan fluoresensi sinar ultraviolet.
Chamber
Plat KLT Spot sampel
Pelarut (Solvent) Garis pensil
Fluoresensi sinar ultraviolet terutama untuk senyawa yang dapat
berfluoresensi, membuat bercak akan terlihat jelas. Jika senyawa tidak
dapat berfluoresensi maka bahan penyerapnya akan diberi indikator
yang berfluoresensi, dengan demikian bercak akan kelihatan hitam
sedang latar belakangnya akan terlihat berfluoresensi (Gandjar dan
Rohman, 2007).
Kromatografi lapis tipis digunakan secara luas untuk analisis
solut-solut organik terutama dalam bidang biokimia, farmasi, klinis,
forensik, baik untuk analisis kualitatif atau untuk analisis kuantitatif.
Penggunaan umum kromatografi lapis tipis adalah untuk menentukan
banyaknya komponen dalam campuran, identifikasi senyawa,
memantau berjalannya suatu reaksi, menentukan efektifitas pemurnian,
menentukan kondisi yang sesuai untuk kromatografi kolom, serta untuk
memantau kromatografi kolom, melakukan screening sampel untuk
obat (Gandjar dan Rohman, 2007).
Harga Rf dihitung dengan menggunakan perbandingan
sebagaimana persamaan sebagai berikut:
Harga maksimum Rf adalah 1, sampel bermigrasi dengan kecepatan
sama dengan fase gerak. Harga minimum Rf adalah 0, dan ini teramati
jika sampel tertahan pada posisi titik awal di permukaan fase diam
(Gandjar dan Rohman, 2007).
2.7 SPEKTROFOTOMETRI
Spektrofotometri adalah ilmu yang mempelajari tentang penggunaan
spektrofotometer. Spektrofotometer adalah alat yang terdiri dari
spektrofotometer dan fotometer. Spektofotometer adalah alat yang
digunakan untuk mengukur energi secara relatif jika energi tersebut
ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi dari panjang
transmitans atau absorbans suatu sampel sebagai fungsi panjang gelombang,
pengukuran terhadap berbagai sampel pada suatu panjang gelombang
tunggal dapat pula dilakukan (Underwood and Day, 2002).
Spektrofotometer menghasilkan sinar dari spektrum dengan panjang
gelombang tertentu, dan fotometer adalah alat pengukur intensitas cahaya
yang ditransmisikan atau yang diabsorpsi.
2.7.1 Spektrofotometri UV-Vis
Spektrofotometri UV-Vis adalah alat yang digunakan untuk
mengukur serapan yang dihasilkan dari interaksi kimia antara radiasi
elektromagnetik dengan molekul atau atom dari suatu zat kimia pada
daerah ultraviolet (200-400 nm) dan sinar tampak (400-800 nm).
Spektrofotometri UV-Vis melibatkan energi elektronik yang cukup
besar pada molekul yang dianalisis, sehingga spektrofotometri UV-Vis
lebih banyak dipakai untuk analisis kuantitatif dibandingkan kualitatif.
Teknik spektroskopi pada daerah ultraviolet dan sinar tampak
biasa disebut spektroskopi UV-Vis. Dari spektrum absorpsi dapat
diketahui panjang gelombang dengan absorbans- maksimum dari suatu
unsur atau senyawa. Konsentrasi suatu unsur atau senyawa juga dengan
mudah dapat dihitung dari kurva standar yang diukur pada panjang
gelombang dengan absorbans maksimum.
Absorbsi cahaya UV-Vis mengakibatkan transisi elektronik,
yaitu promosi elektron-elektron dari orbital keadaan dasar yang
berenergi rendah ke orbital keadaan tereksitasi berenergi lebih tinggi.
Energi yang terserap kemudian terbuang sebagai cahaya atau
tersalurkan dalam reaksi kimia. Absorbsi cahaya tampak dan radiasi
ultraviolet meningkatkan energi elektronik sebuah molekul, artinya
energi yang disumbangkan oleh foton-foton memungkinkan
electron-electron itu mengatasi kekangan inti dan pindah keluar ke orbital baru
yag lebih tinggi energinya. Semua molekul dapat menyerap radiasi
maupun menyendiri, yang dapat dieksitasi ke tingkat energi yang lebih
tinggi (Underwood and Day, 2002).
Suatu pernyataan dalam suatu penetapan kadar atau pengujian
mengenai panjang gelombang serapan maksimum mengandung
implikasi bahwa maksimum tersebut tepat pada atau dalam batas 2 nm
dari panjang gelombang yang ditetapkan (Depkes, 1995).
Suatu spektrofotometri UV-Vis tersusun dari sumber spektrum
tampak yang kontinyu, monokromator, sel pengabsorbsi untuk larutan
sampel atau blanko dan suatu alat untuk mengukur perbedaan absorbsi
antara sampel dan blangko ataupun pembanding (Khopkar, 2003)
Gambar 2.3 Diagram skematis Spektrofotometer UV-Vis
(sumber: Underwood and Day, 2002)
2.7.2 Spektrofotometri Serapan Atom
Spektroskopi serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sedikit (trace) dan sangat sedikit
(ultratrace). Cara analisis ini memberikan kadar total unsur logam
dalam suatu sampel dan tidak tergantung pada bentuk molekul dari
logam dalam sampel tersebut. Cara ini cocok untuk analisis sedikit
logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang
dari 1 ppm), pelaksanaannya relatif sederhana. Spektroskopi serapan
atom didasarkan pada penyerapan energi sinar oleh atom-atom netral,
dan sinar diserap biasanya sinar tampak atau ultraviolet. Perbedaan
terletak pada bentuk spektrum, cara pengerjaan sampel dan
Metode spektroskopi serapan atom mendasarkan pada prinsip
absorbsi cahaya oleh atom. Atom-atom akan menyerap cahaya pada
panjang gelombang tertentu, tergantung pada sifat unsurnya. Cahaya
pada panjang gelombang tertentu mempunyai cukup energi untuk
mengubah tingkat elektronik suatu atom yang mana transisi elektronik
suatu atom bersifat spesifik. Dengan menyerap suatu energi, maka atom
akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat
ditingkatkan energinya ke tingkat eksitasi (Gandjar dan Rohman, 2007).
Keberhasilan analisis dengan spektroskopi serapan atom ini
tergantung pada proses eksitasi dan cara memperoleh garis resonansi
yang tepat serta temperatur nyala harus sangat tinggi (Gandjar dan
Rohman, 2007). Pengukuran dalam spektroskopi serapan atom ini
didasarkan pada radiasi yang diserap oleh atom yang tidak tereksitasi
dalam bentuk uap (Hermanto, 2009).
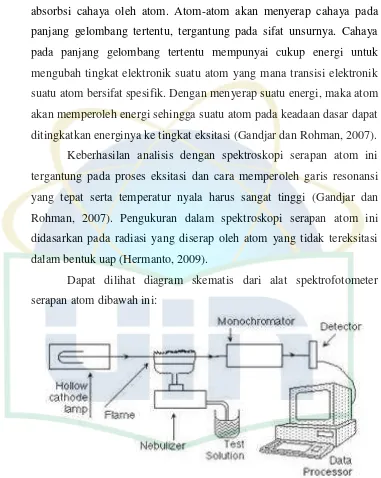
Dapat dilihat diagram skematis dari alat spektrofotometer
serapan atom dibawah ini:
Gambar 2.4 Diagram skematis Spektrofotometer Serapan Atom (sumber: Anshori, 2005)
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda
berongga (hollow cathode lamp). Lampu ini terdiri dari atas tabung
kaca tertutup yang mengandung suatu katoda dan anoda. Katoda
dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas
mulia (neon atau argon) dengan tekanan rendah (10-15 torr). Bila
antara anoda dan katoda diberi suatu selisih tegangan yang tinggi
(600 volt), maka katoda akan memancarkan berkas-berkas elektron
yang bergerak menuju anoda yang mana kecepatan dan energinya
sangat tinggi. Elektron-elektron dengan energi tinggi ini dalam
perjalanannya menuju anoda akan bertabrakan dengan gas-gas
mulia yang diisikan.
Akibat dari tabrakan-tabrakan ini membuat unsur-unsur gas
mulia akan kehilangan elektron dan menjadi ion bermuatan positif.
Ion-ion gas mulia yang bermuatan positif ini akan bergerak ke
katoda yang mana pada katoda ini terdapat unsur yang sesuai
dengan unsur yang akan dianalisis. Atom-atom unsur dari katoda
ini kemudian akan mengalami eksitasi ke tingkat energi-energi
elektron yang lebih tinggi dan akan memancarkan spektrum
pancaran dari unsur yang sama dengan unsur yang akan dianalisis.
2. Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa
padatan atau cairan menjadi bentuk uap atomnya, dan juga
berfungsi untuk atomisasi. Pada cara spektrofotometri serapan
atom, nyala ini berfungsi atom dari tingkat dasar ke tingkat yang
lebih tinggi. Sumber nyala yang paling banyak digunakan adalah
campuran asetilen sebagai bahan pembakar dan udara sebagai
pengoksidasi.
3. Monokromator
Pada spektrofotometer serapan atom, monokromator
dimaksudkan untuk memisahkan dan memilih panjang gelombang
yang digunakan dalam analisis. Di samping sistem optik, dalam
monokromator juga terdapat suatu alat yang digunakan untuk
memisahkan radiasi resonansi dan kontinyu yang disebut dengan
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang
melalui tempat pengatoman. Biasanya digunakan tabung
pengandaan foton (photomultiplier tube).
5. Readout
Readout merupakan suatu alat penunjuk atau dapat juga
diartikan sebagai sistem pencatatan hasil. Pencatatan hasil
dilakukan dengan suatu alat yang telah terkalibrasi untuk
pembacaan suatu transmisi atau absorbsi. Hasil pembacaan dapat
berupa angka atau berupa kurva dari suatu recorder yang
menggambarkan absorbansi atau intensitas emisi.
Untuk keperluan analisis kuantitatif dengan spektrofotometer
serapan atom, maka sampel harus dalam bentuk larutan. Ada beberapa
cara untuk melarutkan sampel, yaitu:
a) Langsung dilarutkan dengan pelarut yang sesuai
b) Sampel dilarutkan dalam suatu asam
c) Sampel dilarutkan dalam suatu basa atau dilebur dahulu dengan
basa kemudian hasil leburan dilarutkan dalam pelarut yang sesuai
Metode pelarutan apapun yang akan dipilih untuk dilakukan
analisis spektrofotometer serapan atom, yang terpenting adalah bahwa
larutan yang dihasilkan harus jernih, stabil, dan tidak mengganggu
3.1 TEMPAT DAN WAKTU PENELITIAN
Penelitian dilaksanakan mulai bulan Februari hingga Agustus 2013
di Laboratorium Bahan Alam, Pusat Penelitian Kimia – Lembaga Ilmu Pengetahuan Indonesia (LIPI), Pusat Penelitian Ilmu Pengetahuan dan
Teknologi (PUSPIPTEK), Serpong.
3.2 BAHAN DAN ALAT
3.2.1 Bahan Uji
Bahan uji yang digunakan adalah seluruh bagian tanaman
katumpangan air (Peperomia pellucida L. Kunth) dengan spesifikasi
batang yang tegak dan lunak dengan akar yang serabut dangkal dan
berwarna putih. Tanaman ini diperoleh dari 3 tempat tumbuh yang
berbeda, yaitu Tangerang Selatan (Jl. Raya Puspiptek, Kota Tangerang
Selatan), Bogor (Desa Tugu Jaya, Kecamatan Cigombong, Kabupaten
Bogor), dan Yogyakarta (Jl. Cangkringan, Kecamatan Tirtomartani,
Kabupaten Sleman).
3.2.2 Bahan Kimia
Bahan-bahan kimia yang digunakan dalam penelitian ini adalah
etanol 70%, kloroform LP, aquadest, etanol 95%, metanol, n-heksn, etil
asetat, H2SO4 2M, pereaksi Meyer, pereaksi Dragendorf, serbuk Mg,
HCl pekat, FeCl3 1%, NaOH 1N, eter, pereaksi Lieberman-Buchard,
HCl 4N, AlCl3 10%, Na asetat 1M, kuersetin, H2SO4 encer, HNO3
pekat, Nutrient Agar (NA), Potato Dextrose Agar (PDA), HNO3 pekat,
HClO4.
3.2.3 Alat
Alat-alat yang digunakan dalam penelitian ini adalah timbangan
cawan petri, kertas saring, tabung reaksi, pipet tetes, oven, krus, kertas
saring bebas abu, piknometer, labu ukur, cawan petri, inkubator, plat
KLT, hot plate, desikator, Spektrofotometer UV-Vis, Spektrofotometer
Serapan Atom
3.3 PROSEDUR KERJA
3.3.1 Determinasi Sampel
Determinasi terhadap P. pellucida dari ketiga tempat tumbuh
dilakukan di Herbarium Bogoriense, Pusat Penelitian Biologi-LIPI,
Bogor, Jawa Barat.
3.3.2 Penyiapan Simplisia
Simplisia yang berasal dari ketiga tempat tumbuh yang berbeda
dipisahkan terlebih dahulu dari masing-masing lokasi agar dalam
penyiapan simplisia tidak tercampur. Penyiapan simplisia tanaman
katumpangan air dilakukan dengan cara sortasi basah untuk
memisahkan kotoran atau bahan-bahan asing lainnya dari batang dan
daun. Kemudian dilakukan pencucian untuk menghilangkan tanah dan
pengotor lainnya yang masih menempel pada bahan yang sudah
disortasi basah. Tahap selanjutnya adalah proses pengeringan dalam
oven pada suhu 45°C (Depkes, 1985) selama 5 hari dan dilakukan
sortasi kering. Kemudian dilakukan penggilingan untuk mendapatkan
serbuk simplisia.
3.3.3 Pembuatan Ekstrak
Masing-masing ekstrak dibuat dengan memaserasi ±1kg
simplisia kering katumpangan air (Peperomia pellucida L. Kunth) yang
sudah dibuat serbuk dengan etanol 70%. Proses maserasi dilakukan
sampai hasil maserat mendekati tidak berwarna dan setiap 24 jam
dilakukan penyaringan. Maserat dikumpulkan lalu dikentalkan dengan
menggunakan vacuumrotary evaporator. Kemudian dihitung rendemen
3.3.4 Penentuan Parameter-parameter Standardisasi
3.3.4.1 Parameter spesifik
a) Identitas ekstrak (Depkes, 2000)
Deskripsi tata nama, nama lain tumbuhan, bagian tumbuhan yang
digunakan dan nama Indonesia tumbuhan.
b) Penetapan organoleptik ekstrak (Depkes, 2000)
Penetapan organoleptik ekstrak, meliputi bentuk, warna, bau, dan
rasa.
c) Penentuan kadar senyawa terlarut dalam pelarut tertentu (Depkes,
2000)
1. Kadar senyawa yang larut dalam air
Sejumlah 1 gram ekstrak dimaserasi selama 24 jam
dengan 20 mL air-kloroform LP (1:1) kemudian disaring.
Diuapkan 20 mL filtrat hingga kering dalam cawan penguap,
residu dipanaskan pada suhu 105ºC hingga bobot tetap.
Dihitung kadar dalam persen senyawa yang larut dalam air
terhadap berat ekstrak awal.
Ket : A1 = Bobot cawan + residu setelah pemanasan (g)
A0 = Bobot cawan kosong (g)
B = Bobot sampel awal (g)
2. Kadar senyawa yang larut dalam etanol
Sejumlah 1 gram ekstrak dimaserasi selama 24 jam
dengan 20 mL etanol 95%. Hasil maserasi disaring cepat
20 mL filtrat hingga kering dalam cawan penguap, residu
dipanaskan pada suhu 105ºC hingga bobot tetap. Dihitung
kadar dalam persen senyawa yang larut dalam etanol terhadap
berat ekstrak awal.
d) Identifikasi Kandungan Kimia Ekstrak
1. Penapisan golongan kimia ekstrak
a. Uji alkaloid
Sejumlah ekstrak ditambahkan 10 mL
kloroform-amoniak, lalu disaring ke dalam tabung reaksi. Filtrat
ditambahkan dengan beberapa tetes H2SO4 2M dan dikocok
sehingga terpisah dua lapisan. Lapisan asam yang terdapat
di bagian atas dipipet ke dalam dua tabung reaksi.
Masing-masing tabung reaksi ditambahkan pereaksi Meyer (5 g KI
dilarutkan dalam 90 mL air dan ditambahkan perlahan
HgCl2 sambil diaduk dan diencerkan hingga volume 100
mL) dan pereaksi Dragendorff (campuran Bi(NO3)2 5H2O
dalam asam nitrat dan larutan KI). Adanya alkaloid
ditunjukkan dengan terbentuknya endapan putih dengan
pereaksi Meyer dan endapan jingga sampai merah coklat
dengan pereaksi Dragendorff. (Atmoko, T., 2009).
b. Uji Flavonoid
Sejumlah ekstrak ditambah air secukupnya dan
dipanaskan selama 5 menit, kemudian disaring. Filtrat
ditambahkan sedikit serbuk Mg dan 1 mL HCl pekat,
kemudian larutan dikocok. Keberadaan flavonoid ditandai
dengan terbentuknya warna kuning, jingga atau merah.
c. Uji Saponin
Sejumlah ekstrak ditambah air secukupnya dan
dipanaskan selama 5 menit, setelah itu ditambahkan
beberapa tetes HCl pekat. Adanya saponin ditandai dengan
terbentuknya busa/buih yang stabil selama ± 15 menit
(Atmoko, T., 2009).
d. Uji Tanin
Sejumlah ekstrak dalam tabung reaksi ditambah air
secukupnya dan dipanaskan selama 5 menit, lalu disaring.
Filtrat ditambahkan FeCl3 1%. Adanya tanin ditandai
dengan terbentuknya warna hijau kebiruan (Atmoko, T.,
2009).
e. Uji Kuinon
Sejumlah ekstrak dalam tabung reaksi ditambah air,
dididihkan selama 5 menit, lalu disaring. Filtrat ditambah
NaOH 1N. Adanya kuinon ditandai dengan terbentuknya
warna merah (Ciulei, I.,1984).
f. Uji Steroid dan Triterpenoid
Sejumlah ekstrak diekstraksi dengan eter dan fraksi
yang larut dalam eter dipisahkan. Lapisan eter dipipet dan
diuji dengan pereaksi Lieberman Buchard (asam asetat
anhidrat : H2SO4 pekat = 3:1). Warna merah atau violet
menunjukkan adanya triterpenoid dan warna hijau atau biru
menunjukkan adanya steroid (Atmoko, T., 2009).
2. Pola kromatogram
a. Profil KLT ekstrak (Helmi A, 2006)
Ekstrak (5 mg) dilarutkan dengan metanol sebanyak
1 mL untuk memperoleh larutan uji. Larutan uji dari ketiga
tempat lokasi ditotolkan pada plat KLT dan dielusi dengan
80:20; 60:40; 40:60; 20:80; 0:100. Kemudian dihitung nilai
Rf-nya dan dibandingkan dari ketiga sampel tersebut.
e) Kadar Total Flavonoid (Chang, et al., 2002) Pembuatan larutan uji
Sebanyak 1 gram dari masing-masing ekstrak
ditimbang, kemudian dihidrolisis dengan HCl 4N selama 30
menit dan disaring. Ekstrak disari/dilarutkan dengan 15 mL
etil asetat sebanyak 3 kali. Kemudian fraksi etil asetat
dikumpulkan dan dipekatkan. Hasil ekstrak etil asetat
dimasukkan labu kemudian dilarutkan dengan metanol
hingga 25 mL.
Pengukuran Spektrofotometer UV
Larutan uji dipipet 0,5 mL yang kemudian dilarutkan
dengan metanol 1,5 mL pada tabung reaksi. Selanjutnya
larutan ditambahkan pereaksi dengan komposisi: 0,1 mL
AlCl3 10%, 0,1 mL Na asetat 1M, dan 2,8 mL aquadest.
Larutan dicampur hingga homogen dan diinkubasi pada suhu
kamar selama 30 menit. Larutan diukur serapannya pada
spektrofotometer UV dengan panjang gelombang 415 nm
dengan menggunakan larutan blangko tanpa AlCl3 namun
diganti dengan aquadest. Kadar flavonoid total dinyatakan
dengan kesetaraan pembanding kuersetin.
Pembuatan kurva kalibrasi dilakukan dengan pembanding
kuersetin
Sebanyak 25 mg kuersetin dilarutkan dengan metanol
dalam labu 100 mL dan diencerkan hingga batas, larutan ini
digunakan sebagai larutan induk. Kemudian dibuat 5
konsentrasi berbeda dengan diencerkan menggunakan
metanol. Tiap konsentrasi dipipet 0,5 mL kemudian
dilarutkan dengan 1,5 mL metanol. Setelah itu
0,1 mL AlCl3 10%, 0,1 mL Na asetat 1M, dan 2,8 mL
aquadest. Larutan dicampur homogen dan diinkubasi suhu
kamar selama 30 menit. Larutan diukur serapannya pada
spektrofotometer UV dengan panjang gelombang 415 nm
dengan blangko tanpa kuersetin.
3.3.4.2 Parameter Non Spesifik
a) Penetapan Susut Pengeringan (Depkes, 2000)
Sebanyak 1 gram ekstrak ditimbang dalam cawan yang
sebelumnya telah dipanaskan pada suhu 105ºC selama 30 menit
dan ditimbang. Ratakan dengan menggoyangkan hingga
merupakan lapisan setebal (5 mm-10 mm) dan dikeringkan pada
suhu penetapan hingga bobot tetap, buka tutupnya, biarkan cawan
dalam keadaan tertutup dan mendingin dalam desikator hingga
suhu kamar, kemudian dicatat bobot tetap yang diperoleh.
Ket : A = Bobot sampel sebelum dipanaskan (g)
B = Bobot sampel setelah dipanaskan (g)
(Selawa, W., 2013)
b) Penetapan Kadar Air (Metode gravimetri) (Depkes, 2000)
Sebanyak 1 gram ekstrak ditimbang dalam wadah yang
telah ditara. Dikeringkan pada suhu 105ºC selama 5 jam di dalam
oven dan setelah itu ditimbang. Kadar air dihitung dalam persen
terhadap berat sampel awal.
Ket : A = Bobot sampel sebelum dipanaskan (g) B = Bobot sampel setelah dipanaskan (g)