MEMBRAN KOMPOSIT POLISULFON TERSULFONASI-
TITANIUM DIOKSIDA UNTUK APLIKASI
DIRECT
METHANOL FUEL CELL
AHMAD HAWARI ASSUFI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Membran Komposit
Polisulfon Tersulfonasi-Titanium Dioksida untuk Aplikasi Direct Methanol Fuel
Cell adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, November 2014
Ahmad Hawari Assufi
ABSTRAK
AHMAD HAWARI ASSUFI. Membran Komposit Polisulfon Tersulfonasi–
Titanium Dioksida untuk Aplikasi Direct Methanol Fuel Cell. Dibimbing oleh
SRI MULIJANI dan ARMI WULANAWATI.
Penelitian ini menyintesis dan mencirikan membran polisulfon
tersulfonasi-titanium dioksida (sPSf-TiO2). Sulfonasi dilakukan pada suhu 40 °C selama 60
menit menggunakan oleum sebagai agen sulfonasi dan TiO2 ditambahkan untuk
meningkatkan kinerja membran. Derajat sulfonasi sebesar 47.5% dan morfologi
membran menunjukkan bahwa tambahan TiO2 membuat membran lebih rapat
dibandingkan tanpa tambahan TiO2. Membran yang dicirikan dengan
spektrofotometer inframerah transformasi fourier menunjukkan puncak gugus
sulfonat tertrisubtitusi 1,2,4- pada 1724 cm-1. Membran komposit diperoleh
dengan menambahkan polisulfon tersulfonasi dengan TiO2 dengan ragam
konsentrasi 3% dan 5%. Nilai konduktivitas dan beda potensial tertinggi
dihasilkan pada membran sPSf-TiO2 5% dengan nilai berturut turut 1.07 × 10-3
S/cm dan 422 mV. Berdasarkan ciri tersebut, membran komposit sPSf-TiO2 dapat
diaplikasikan untuk direct methanol fuel cell.
Kata kunci: membran komposit, polisulfon tersulfonasi, sel bahan bakar, titanium dioksida
ABSTRACT
AHMAD HAWARI ASSUFI. Composite of Sulfonated Polysulfone–Titanium
Dioxide Membrane for Application on Direct Methanol Fuel Cell. Supervised by SRI MULIJANI and ARMI WULANAWATI.
This experiment is to synthesize and to characterize sulfonated
polysulfone-titanium dioxide composite membranes (sPSf-TiO2). The sulfonation was done in
40 °C for 60 minutes using oleum as the sulfonation agent and TiO2 was added to
improve membrane performances. The degree of sulfonation through sulfonation process was 47.5% and the morphology of the membrane showed that the addition
of TiO2 made the membrane denser than that without TiO2. The infared spectra
showed there was 1,2,4- trisubstituted sulfonate group at 1724 cm-1. The
composite membrane was produced by adding sulfonated polysulfone and TiO2
with concentration of 3% and 5%. The composite membrane sPSf-TiO2 5% gave
the highest proton conductivity and voltage as of 1.07 × 10-3 S/cm and 422 mV,
respectively. Based on the result, the composite membrane sPSf-TiO2 can be
applied for direct methanol fuel cell system.
MEMBRAN KOMPOSIT POLISULFON TERSULFONASI-
TITANIUM DIOKSIDA UNTUK APLIKASI
DIRECT
METHANOL FUEL CELL
AHMAD HAWARI ASSUFI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi : Membran Komposit Polisulfon Tersulfonasi-Titanium Dioksida
untuk Aplikasi Direct Methanol Fuel Cell
Nama : Ahmad Hawari Assufi
NIM : G44100069
Disetujui oleh
Dr Sri Mulijani, MS Armi Wulanawati, MSi
Pembimbing 1 Pembimbing 2
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah yang berjudul “Membran Komposit Polisulfon
Tersulfonasi-Titanium dioksida untuk Aplikasi Direct Methanol Fuel Cell”
berhasil diselesaikan. Karya tulis ini disusun berdasarkan hasil penelitian yang dilakukan di Laboratorium Kimia Fisik Departemen Kimia, Institut Pertanian Bogor pada bulan Januari hingga Juni 2014.
Penulis mengucapkan terima kasih kepada pihak yang turut membantu dalam penyusunan karya ilmiah ini sehingga dapat terselesaikan dengan baik khususnya kepada Ibu Dr Sri Mulijani, MS selaku pembimbing utama, Ibu Armi Wulanawati, MSi selaku pembimbing kedua atas bimbingan, arahan, dan ilmu yang telah diberikan. Penulis juga berterima kasih kepada Ibu, Ayah, Kakak-kakak atas dukungan dan doanya, kepada Bapak Dr Jajang Juansah, Bapak Yani, Ibu Ai, Bapak Ismail, Bapak Didi, Ibu Aah, dan Umi atas bantuan serta masukkan selama penelitian berlangsung. Ucapan terima kasih juga penulis sampaikan kepada rekan kerja, yaitu Vallian Ghali, Ginna Ramadhini Putri, Dita Iryani, Eva NS, dan Suci Rahmadani untuk kebersamaan, dukungan, dan semangat yang diberikan. Selain itu, terima kasih kepada Amima Aqmarina, Nanda Andrian, Aji Kusomo Wibowo, dan Bachtiar Mustakim yang senantiasa memberikan masukan, dorongan, dan semangat kepada penulis.
Semoga karya ilmiah ini dapat bermanfaat.
Bogor, November 2014
1
DAFTAR ISI
DAFTAR GAMBAR xiv
DAFTAR LAMPIRAN xiv
PENDAHULUAN 1
BAHAN DAN METODE 2
Bahan dan Alat 2
Metode 2
Sintesis Polisulfon Tersulfonasi (sPSf) 2
Penentuan Derajat Sulfonasi 2
Preparasi Membran Polisulfon Tersulfonasi-Titanium Dioksida 3
Penentuan Densitas 3
Pengujian Water Uptake 3
Karakterisasi Membran 4
Pengukuran Konduktivitas Proton Membran 4
Pengukuran Permeabilitas Metanol 5
Uji Aplikasi Sistem DMFC 5
HASIL DAN PEMBAHASAN 6
Polisulfon Tersulfonasi (sPSf) 6
Membran Komposit Polisulfon Tersulfonasi-Titanium dioksida 8
Water Uptake dan Permeabilitas Metanol 8
Densitas Membran 10
Konduktivitas Proton Membran 10
FTIR Error! Bookmark not defined.
Morfologi Membran 13
Aplikasi Sistem DMFC 14
SIMPULAN DAN SARAN 17
Simpulan 17
Saran 17
DAFTAR PUSTAKA 17
2
DAFTAR GAMBAR
1 Perubahan warna sebelum dan sesudah sulfonasi 6
2 Reaksi polisulfon tersulfonasi 7
3 Proses transfer proton pada membran polisulfon tersulfonasi- TiO2 8
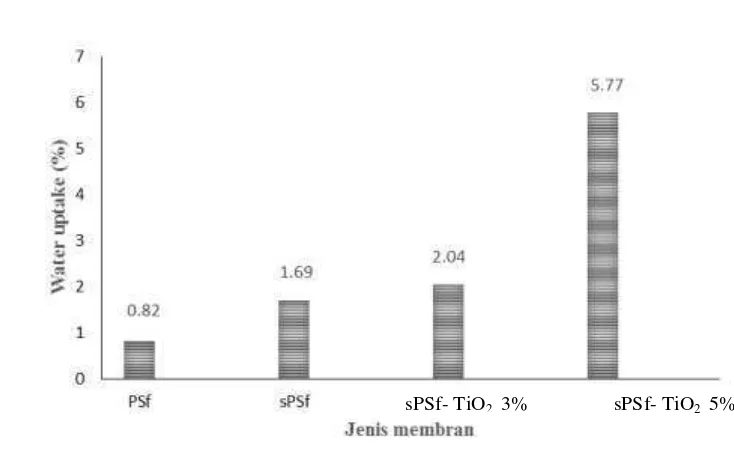
4 Nilai water uptake membran 9
5 Densitas jenis membran 10
6 Konduktivitas proton membran dengan elektrode nonaktivasi dan
aktivasi 11
7 Konduktivitas proton membran aktivasi 12
8 Spektrum inframerah PSf 13
9 Morfologi membran 14
10 Bejana pada sistem DMFC 15
11 Beda potensial membran aktivasi 16
12 Nilai arus yang dihasilkan membran 16
DAFTAR LAMPIRAN
1 Diagram alir penelitian 19
2 Penentuan derajat sulfonasi (DS) 20
3 Data penentuan water uptake 20
4 Data penentuan densitas 22
5 Data hasil FTIR 22
6 Data penentuan konduktivitas proton elektrode karbon-karbon 23
7 Data persentase peningkatan konduktivitas proton 24
8 Beda potensial yang dihasilkan pada setiap membran 24
1
PENDAHULUAN
Sel bahan bakar adalah suatu sistem elektrokimia yang mengubah energi kimia dari hidrogen dan oksigen langsung menjadi energi listrik (Hasan 2007)
tanpa menghasilkan emisi gas CO2 dan CO seperti bahan bakar fosil dan dapat
diperbaharui. Prinsip sel bahan bakar adalah menggunakan pembakaran listrik-kimiawi, sel akan memproduksi energi listrik arus searah (Suhada 2001). Sel bahan bakar terdiri dari anode dan katode dan dipisahkan oleh membran elektrolit yang hanya dapat menghantarkan ion saja sedangkan elektron tidak dapat
melewati membran elektrolit. Saat ini banyak penelitian mengenai Direct
Methanol Fuel Cell (DMFC) sebagai bagian dari Polymer Electrolyte Membrane Fuel Cell (PEMFC), yang memanfaatkan membran sebagai elektrolit. DMFC dengan metanol sebagai elektrolit biasanya beroperasi pada suhu kamar dengan kerapatan daya yang cukup tinggi (Irwan 2009). Sifat-sifat tersebut mempunyai peluang aplikasi dibidang transportasi, pembangkit listirk, dan perangkat elektronik portabel.
Membran yang sering digunakan sebagai elektrolit adalah membran nafion yang terbuat dari fluoro polimer dengan menambahkan rantai cabang gugus
sulfonat (Liu et al 2010). Kelebihan membran ini adalah memiliki konduktivitas
proton yang tinggi sebesar 0.086 S/cm pada suhu 30-32 °C (Smitha et al. 2005),
gugus sulfonat yang dimiliki mampu menghantarkan proton, ketahanan mekanik
yang baik, dan stabilitas kimia yang baik (Devrim et al 2009). Kekurangan dari
membran ini adalah memiliki permeabilitas metanol yang tinggi, mahal, dan
penurunan kinerja membran di atas suhu 80 °C karena adanya methanol
cross-over pada katode sebesar 4.9 × 10-6 cm2/s (Handayani et al. 2007)
Hal tersebut dapat diatasi dengan mengganti nafion dengan suatu poliaromatik seperti polibenzimidazol, polieter sulfon, polisulfon, polieter keton
(Handayani et al. 2007). Salah satu poliaromatik yang sedang dikembangkan
adalah polisulfon, yang mengandung gugus benzena, sehingga memungkinkan adanya penambahan gugus pada rantai polimer. Polisulfon adalah bahan polimer yang tahan terhadap panas, stabil antara pH 1.5-13, mempunyai kekuatan tarik yang baik, tidak larut atau rusak oleh asam encer atau alkali (Juniarzadinata 2011). Polisulfon adalah suatu produk polimer bersifat hidrofobik. Salah satu proses modifikasi yang sering dilakukan adalah sulfonasi yaitu penambahan
gugus sulfonat ( -SO3H) pada rantai polimer (Pramono et al. 2012).
Pada penelitian sebelumnya dilaporkan bahwa sulfonasi dapat menurunkan sifat ketahanan termal pada polistirena dan pada polisulfon tersulfonasi
(Pramono et al. 2012). Hal tersebut dapat diatasi dengan menambahkan suatu
komposit. Marita (2011) menyebutkan kelebihan menggunakan membran komposit adalah dapat memperoleh kinerja membran yang optimal sehubungan
dengan selektivitas, stabilitas kimia dan termal, dan laju permeasi. TiO2
merupakan bahan yang dapat dijadikan sebagai komposit. Menurut Luntraru et al.
(2013), TiO2 merupakan material anorganik yang dapat digunakan sebagai
fotokatalisator, pigmen dan membran komposit. Kombinasi TiO2 dengan ion ferri,
fero dan besi akan meningkatkan aktivitas fotokatalitik, sedangkan menurut
Mingliang et al. (2011) TiO2 memiliki stabilitas dan hidrofilisitas yang tinggi.
2
terhadap suhu tetapi dengan konsentrasi yang tinggi dapat menurunkan kelarutan dari komposit dan mengakibatkan membran rapuh.
Berdasarkan uraian tersebut maka pada penelitian ini dilakukan sintesis dan
karakterisasi membran polisulfon tersulfonasi TiO2 untuk aplikasi Direct
Methanol Fuel Cell pada suhu sulfonasi sebesar 40 °C serta mempelajari
pengaruh penambahan konsentrasi komposit TiO2 terhadap kinerja membran.
Membran polisulfon yang dihasilkan diharapkan memiliki sifat fisik yang kuat, biodegradabel, memiliki konduktivitas yang tinggi, ketahanan termal yang baik serta dapat menjadi sumber energi listrik yang ramah lingkungan, dapat diperbaharui, dan dapat mengurangi dampak negatif limbah di lingkungan.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah polisulfon (Sigma-Aldrich), titanium
dioksida (TiO2), asam sulfat berasap yang mengandung 65% SO3 (oleum),
kloroform, gas nitrogen, kloroform teknis, diklorometana, metanol, NaOH, HCl,
larutan K3Fe(CN)6, larutan Na2HPO4, fenolftalein, dan air deionisasi. Alat-alat
yang digunakan dalam penelitian ini adalah peralatan gelas, oven, labu leher tiga, piknometer, neraca analitik, SEM JEOL JSM 836 OLA, FTIR BRUCKER
TENSOR 27, impedance analyzer, dan alat DMFC.
Metode
Sintesis Polisulfon Tersulfonasi (sPSf) (Xing et al. 2004)
Polisulfon (PSf) sebanyak 10 g dilarutkan ke dalam kloroform sehingga diperoleh larutan PSf dengan konsentrasi 10% (b/v), selanjutnya oleum sebanyak 20 mL diteteskan secara bertahap dalam corong pisah yang dihubungkan dengan
labu leher tiga dengan dialiri gas nitrogen, gas SO3 dari oleum didorong oleh gas
nitrogen menuju larutan PSf, selanjutnya larutan tersebut dipanaskan pada suhu
40 °C lalu diaduk menggunakan pengaduk mekanik. Sintesis sPsf dilakukan
selama 60 menit di ruang asam.
Penentuan Derajat Sulfonasi (Martins et al. 2007)
3
DS = × 100% (1)
Keterangan:
Vawal = Volume HCl blangko (mL)
Vakhir = Volume HCl sampel (mL)
N = Normalitas HCl (N) BE = Bobot ekuivalen (g/ek)
Preparasi Membran Polisulfon Tersulfonasi-Titanium Dioksida(sPSf-TiO2) (Devrim et al. 2009)
Titanium dioksida masing-masing sebanyak 3% dan 5% dari bobot polisulfon ditambahkan ke dalam polisufon tersulfonasi (sPSf) yang telah kering dengan dilarutkan dalam diklorometana. Selanjutnya, campuran diaduk hingga
homogen, kemudian didiamkan sampai tidak ada gelembung. Larutan sPSf-TiO2
dituangkan ke dalam pelat kaca yang telah dilapisi selotip pada bagian tepi (1 lapis) dan membran siap dicetak.
Penentuan Densitas
Membran sPSf-TiO2 yang telah dicetak dipotong dengan ukuran yang
seragam, kemudian dimasukkan ke dalam piknometer yang telah diketahui bobot
kosongnya (w0). Bobot piknometer dan sampel ditimbang dan dicatat (w1).
Kemudian piknometer yang berisi potongan sampel ditambahkan akuades hingga
tidak terdapat gelembung udara dan ditimbang bobotnya (w2). Bobot piknometer
berisi air juga ditimbang dan bobotnya dicatat (w3). Bobot jenis sampel dihitung
menggunakan persamaan 2:
d = (2)
Keterangan:
d : bobot jenis sampel (g/mL)
dl: bobot jenis air (g/mL)
da : bobot jenis udara (g/mL)
Pengujian Water Uptake (Devrim et al. 2009)
Membran sPSf-TiO2 berukuran 1 × 1 cm2 dikeringkan dalam oven pada
suhu 120 °C selama 24 jam lalu ditimbang sebagai wkering. Setelah kering,
membran direndam dalam air deionisasi pada suhu ruang selama 24 jam. Selanjutnya, membran dikeluarkan dan dibersihkan dengan tisu lalu ditimbang
sebagai wbasah. Penimbangan dilakukan untuk mengetahui selisih bobot membran
4
Water uptake (%) =
(3)
Karakterisasi Membran
Gugus Fungsi
Membran diuji menggunakan spektrofotometer FTIR, dengan resolusi 4 dan
payar 32. Pengujian dengan FTIR dilakukan untuk sampel PSf, sPSf, sPSf-TiO2
5% dalam bentuk lapis tipis, dan titanium dioksida dalam bentuk serbuk.
Morfologi
Pengukuran morfologi membran yang terbentuk diuji menggunakan SEM berdasarkan penampang lintang dan bagian muka membran. Membran PSf, sPSf,
dan sPSf-TiO2 dibekukan dengan nitrogen cair selama 10 menit kemudian
dipatahkan dan ditempelkan pada cell holder. Membran dilapisi dengan emas lalu
dimasukkan ke dalam chamber, dan dipotret permukaan dan penampang lintang
membran.
Pengukuran Konduktivitas Proton Membran
Pengukuran konduktivitas dilakukan menggunakan alat LCR meter (Laboratorium Biofisika Membran, Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, IPB). Membran dipotong sesuai ukuran elektrode.
Membran diaktivasi dengan merendam setiap membran dalam H2O2 selama 1 jam
lalu direndam kembali dalam H2SO4 selama 1 jam, setelah itu membran dibilas
dengan air deionisasi. Elektrode yang digunakan ialah karbon dan logam (tembaga-besi). Elektrode juga diaktivasi dengan cara merendam ke dalam larutan HCl 1 N selama 1 hari, kemudian dengan NaOH 1 N selama 1 hari, setelah itu elektrode aktif dicuci dengan air deionisasi dan direndam hingga akan digunakan (Wisojodharmo dan Dewi 2008).
5
Nilai konduktansi (G) yang diperoleh, dikonversi menjadi nilai
konduktivitas per satuan jarak yang disebut dengan nilai konduktivitas proton (σ)
melalui persamaan 4:
σ = G (4)
Keterangan :
σ : konduktivitas proton (S/cm)
A : luas permukaan (cm2)
l : jarak antar kedua elektrode (cm) G : nilai konduktansi (S)
Pengukuran Permeabilitas Metanol (Shin et al. 2005)
Permeabilitas metanol diuji secara kualitatif untuk mengetahui metanol yang terdifusi melalui membran. Sebuah bejana yang terdiri atas 2 kompartemen disiapkan untuk mengapit membran. Kompartemen A diisi dengan 160 mL metanol 0.3 M. Sistem dibiarkan selama 30 menit untuk melihat metanol yang terdifusi melalui membran yang masuk ke kompartemen B.
Uji Aplikasi Sistem DMFC
Konduktivitas dalam sistem sel bahan bakar diukur menggunakan 2 sistem bejana, yaitu sistem anode dan katode. Bejana pertama sebagai sistem anode diisi dengan 160 mL larutan metanol 0.3 M, sedangkan bejana kedua sebagai sistem
katode diisi dengan 80 mL larutan K3Fe(CN)61 mM dan 80 mL larutan Na2HPO4.
6
HASIL DAN PEMBAHASAN
Polisulfon Tersulfonasi (sPSf)
Polisulfon tersulfonasi dapat diperoleh melalui reaksi polisulfon dengan agen sulfonasi seperti oleum. Sifat polisulfon yang hidrofobik menyebabkan berkurangnya kemampuan dalam proses transfer proton. Sifat hidrofobik dapat diubah menjadi hidrofilik dengan sulfonasi, yaitu proses memasukkan gugus sulfonat dalam kerangka polisulfon, sehingga menghasilkan suatu membran bermuatan positif yang berperan dalam meningkatkan sifat hidrofilisitas dan
konduktivitasnya (Piluharto et al. 2012). Proses sintesis polisulfon tersulfonasi
menggunakan kloroform sebagai pelarut dari polisulfon dengan prinsip like
dissolve like dan pelarut yang digunakan tidak boleh bereaksi dengan oleum dan polisulfon tersebut. Polisulfon tersulfonasi disintesis dengan bantuan gas nitrogen
yang berfungsi sebagai pendorong SO3H menuju ke larutan polisulfon. Sintesis ini
dilakukan pada suhu 40 °C selama 60 menit dalam ruang asam. Perubahan warna yang terjadi sebelum dan sesudah sulfonasi yaitu dari tidak berwarna (Gambar 1a) menjadi kuning kecoklatan (Gambar 1b)
(a) (b)
(a) (b)
Gambar 1 Perubahan warna sebelum (a) dan sesudah (b) proses sulfonasi
Agen sulfonasi yang dapat digunakan dalam sulfonasi antara lain asam sulfat (Dewi dan Handayani 2007), trimetil silil ester (Lufrano 2008), asam
klorosulfonat (Devrim et al. 2009), dan oleum. Penelitian ini menggunakan oleum
atau asam sulfat berasap sebagai agen sulfonasi. Pemilihan oleum ini didasarkan karena sulfonasi yang terjadi lebih cepat, lebih efesien, dan pereaksi yang digunakan sedikit. Adanya gugus sulfonat yang masuk ke larutan polisulfon
menyebabkan membran bersifat hidrofilik dan berhubungan dengan
7
Hasil penelitian Handayani dan Dewi (2007) pada membran elektrolit polieter eter keton tersulfonasi pada suhu sulfonasi 45 °C dan 60 °C diperoleh nilai DS berturut - turut sebesar 47% dan 68%. Berikut ini adalah reaksi yang terjadi pada proses sulfonasi (Gambar 2):
8
Membran Komposit Polisulfon Tersulfonasi-Titanium Dioksida
Membran komposit adalah membran yang terdiri dari dua lapisan, lapis aktif yang rapat dari material yang berbeda dan lapis pendukung yang berpori. Menurut Marita (2011) membran komposit dapat meningkatkan kinerja membran sehubungan dengan stabilitas kimia, selektivitas, dan laju permeasi. Membran ini dibuat dengan teknik inversi fase yaitu pembuatan membran fase cair menjadi fase padat. Membran komposit dibuat dengan mencampurkan polisulfon tersulfonasi
(sPSf) dengan komposit yaitu TiO2 dengan berbagai konsentrasi (3% dan 5%) dan
melarutkannya dengan diklorometana. Larutan membran yang sudah homogen lalu dicetak di atas pelat kaca dan dibiarkan menguap.
Penambahan TiO2 menyebabkan membran lebih hidrofilik karena sifat TiO2
yang memiliki hidrofilitas yang baik, selain itu fungsi TiO2 yaitu sebagai pengisi.
Adanya komposit tersebut membuat konduktivitas proton semakin tinggi, proses transfer proton dapat dilihat pada Gambar 3.
Gambar 3 Proses transfer proton pada membran polisulfon tersulfonasi- TiO2
Water Uptake dan Permeabilitas Metanol
Water uptake adalah kemampuan membran dalam menyerap air yang berguna sebagai media perpindahan proton yang berkaitan dengan konduktivitas
proton. Nilai water uptake menyatakan banyaknya air yang terserap ke dalam
membran. Perhitungan nilai water uptake dapat dilihat pada Lampiran 3.
Pengujian water uptake dilakukan pada membran PSf, sPSf, sPSf-TiO2 3%, dan
9
Gambar 4 Nilai water uptake membran
Berdasarkan hasil percobaan nilai water uptake pada polisulfon
tersulfonasi lebih besar daripada membran polisulfon tanpa sulfonasi. Hal ini diakibatkan oleh sulfonasi, dapat menyebabkan membran bersifat hidroflik
sehingga membran lebih baik menyerap air dan meningkatkan nilai water uptake
hingga 2x lebih besar dibanding tanpa sulfonasi.
Penambahan komposit juga dapat meningkatkan nilai water uptake. Shin
et al. (2004) telah melakukan penelitian pada polistirena dan politetrafloroetilena
tersulfonasi menyatakan membran komposit memiliki nilai water uptake yang
lebih tinggi dibanding dengan membran tanpa komposit. Mingliang et al. (2011)
menyatakan bahwa TiO2 memiliki stabilitas dan hidrofilisitas yang tinggi
sehingga penambahan komposit TiO2 meningkatkan nilai water uptake.
Penambahan komposit dengan konsentrasi masing-masing 3% dan 5% dapat
meningkatkan nilai water uptake berturut – turut sebesar 1.2× dan 3× dibanding
dengan polisullfon tersulfonasi tanpa komposit. Nilai ini menunjukkan semakin
tinggi konsentrasi komposit yang ditambahkan maka semakin tinggi nilai water
uptake yang dihasilkan. Hal ini berhubungan dengan perpindahan proton karena
nilai water uptake yang tinggi dapat meningkatkan kemampuan membran dalam
proses transfer proton sehingga meningkat juga nilai konduktivitas proton yang
dihasilkan. Namun, water uptake yang terlalu tinggi dapat menyebabkan air yang
terkandung dapat berikatan dengan metanol sehingga menyebabkan methanol
cross-over. Dewi dan Handayani (2009) menyatakan methanol cross-over dapat menyebabkan hilangnya sebagian bahan bakar yang digunakan dan menyebabkan laju reaksi di katode semakin lambat yang menurunkan kinerja voltase sel secara keseluruhan. Uji kualitatif permeabilitas metanol menunjukkan bahwa tidak adanya metanol yang melewati membran. Hal ini terlihat dari keringnya bagian sisi permukaan membran setelah dilewati membran, sehingga membran tersebut baik digunakan untuk aplikasi DMFC.
10
Densitas Membran
Penentuan densitas dilakukan untuk melihat pengaruh penambahan komposit dan sulfonasi terhadap kerapatan dan keteraturan membran. Data yang diperoleh (Gambar 5) menunjukkan proses sulfonasi dapat menaikkan nilai densitas, karena adanya gugus sulfonat dapat mengisi rongga pada membran. Penambahan gugus sulfonat dapat membuat struktur membran menjadi lebih rapat dan teratur, sehingga dapat menigkatkan nilai densitas sebesar 2.21% dibanding tanpa sulfonasi. Penambahan komposit juga memengaruhi nilai dari densitas.
Peningkatan nilai densitas seiring dengan kenaikkan konsentrasi komposit. TiO2
bersifat sebagai pengisi pada membran polisulfon tersulfonasi-titanium dioksida sehingga dapat mengisi rongga pada membran dan keteraturan dan kerapatan
membran dapat meningkat (Pramono et al. 2012). Penambahan komposit TiO2
dengan konsentrasi masing-masing 3% dan 5% juga meningkatkan nilai densitas berturut - tuut sebesar 0.68% dan 1.14%. Berikut nilai densitas yang diperoleh (Gambar 5) dan perhitungan lengkap densitas membran dapat dilihat pada Lampiran 4.
Gambar 5 Densitas jenis membran
Konduktivitas Proton Membran
Membran polimer elektrolit yang baik digunakan untuk aplikasi DMFC seharusnya memiliki permeabilitas metanol yang rendah dan memiliki
konduktivitas proton yang tinggi (Shin et al. 2004). Penentuan konduktivitas
proton menggunakan alat impedance analyzer LCR-meter dengan elektrode
karbon dan logam. Penentuan dilakukan pada membran PSf, sPSf, sPSf-TiO2 3%,
dan sPSf-TiO2 5% dengan membandingkan antara membran aktivasi dan
nonaktivasi (Lampiran 6). Hasil yang diperoleh ditunjukkan pada Gambar 6a dan 6b.
11
(a)
(b)
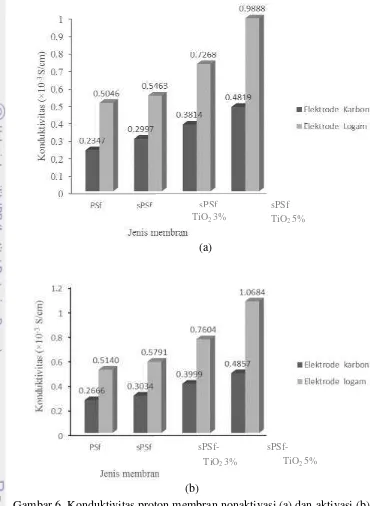
Gambar 6 Konduktivitas proton membran nonaktivasi (a) dan aktivasi (b)
Gambar (6a dan 6b) menunjukkan membran yang diaktivasi memiliki nilai konduktivitas proton yang lebih besar dibandingkan membran nonaktivasi baik elektode karbon maupun logam. Hal ini disebabkan oksidator kuat yang
digunakan pada proses aktivasi yaitu H2O2 dan H2SO4 dapat mengaktifkan
gugus-gugus penghantar proton pada membran sehingga meningkatkan nilai
konduktivitas. Selain itu, proses sulfonasi dan penambahan TiO2 dapat
meningkatkan nilai konduktivitas proton. Hal ini dikarenakan penambahan TiO2
dan adanya gugus sulfonat dapat meningkatkan sifat membran menjadi hidrofilik
(Devrim et al. 2009) dan meningkatkan nilai water uptake. Nilai water uptake
sPSf
-
sPSf-
TiO2 3%
TiO2 3%
sPSf
- TiO2 5%
sPSf-
12
yang semakin besar menyebabkan transfer proton pada membran semakin baik dan meningkatkan nilai konduktivitas proton. Perhitungan persentase peningkatan konduktivitas tercantum pada Lampiran 7.
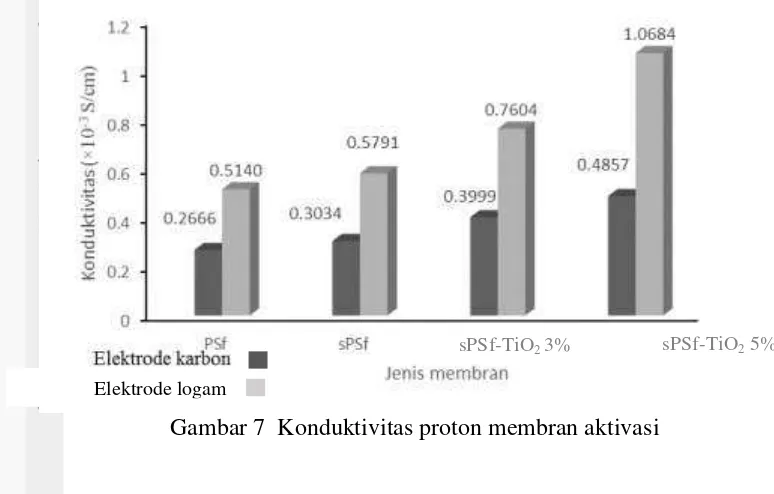
Selain itu, elektode logam menghasilkan nilai konduktivitas proton yang lebih tinggi dibanding dengan elektrode karbon (Gambar 7). Hal ini dikarenakan logam bersifat konduktor yang dapat menghantarkan arus listrik sedangkan
elektrode karbon bersifat inert. Hasil yang diperoleh untuk membran sPSf-TiO2
5% dengan elektrode karbon dan logam, berturut- turut sebesar 0.4857 × 10-3 dan
1.0684 × 10-3S/cm. Elektrode logam memberikan hasil 2× lebih besar daripada
elektrode karbon. Nilai tersebut masih lebih kecil dibanding konduktivitas
membran nafion yaitu sebesar 8.2 × 10-2 S/cm.
Gambar 7 Konduktivitas proton membran aktivasi
Karakterisasi Membran
Gugus Fungsi
Pengujian FTIR dilakukan pada membran PSf dan sPSf untuk melihat
adanya subtitusi gugus –SO3H pada cincin aromatik polisulfon sedangkan pada
membran sPSf-TiO2 5% untuk melihat adanya pengaruh penambahan TiO2
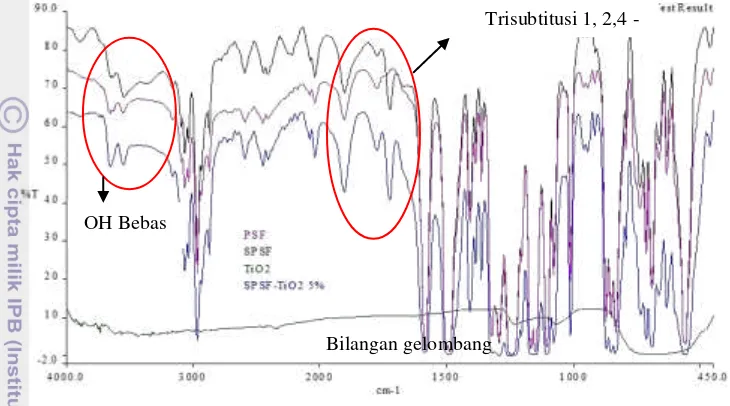
sebagai komposit. Keberhasilan sulfonasi ditunjukkan dengan munculnya pita
serapan gugus OH bebas dari –SO3H pada bilangan gelombang 3650-3600 cm-1
yang semakin melebar (Pavia et al. 2009). Spektrum inframerah dari gugus yang
ada pada membran (Lampiran 5). Perbedaan spektum PSf dan sPSf terlihat dengan munculnya pita serapan baru pada membran sPSf pada bilangan
gelombang 1724 cm-1. Menurut Pavia et al. (2009) pada bilangan gelombang
tersebut mengindikasikan adanya gugus yang tersubtitusi 1, 2, 4-. Pada gugus
tersebut diduga gugus –SO3H yang masuk pada cincin aromatik pada posisi orto
dari C-O-C dari struktur polisulfon. Tambahan TiO2 pada polisulfon tersulfonasi
tidak menunjukkan perbedaan atau munculnya serapan baru. Hal ini
mengindikasikan tidak ada pengaruh penambahan TiO2 terhadap pita serapan
Elektrode logam
13
baru, artinya tidak ada interaksi antara membran dengan TiO2, TiO2 hanya
berfungsi sebagai pengisi.
Gambar 8 Spektrum inframerah PSf ( ), sPSf ( ), dan sPSf-TiO2 5% ( )
Morfologi Membran
Morfologi permukaan membran PSf, sPSf, dan sPSf-kitosan 5% dianalisis
dengan menggunakan Scanning Electron Microscope dengan perbesaran 10000
kali. Hasil analisis morfologi membran dapat dilihat pada Gambar 9. Pada permukaan atas membran PSf (9a) lebih heterogen dibanding dengan membran
PSf (9b) dan sPSf-TiO2 (9c). Menurut Devrim et al. (2009) polimer polisulfon
merupakan polimer yang amorf dengan struktur polimer yang kaku, sedangkan polisulfon tersulfonasi merupakan polimer yang kristalin. Hal ini berhubungan dengan kehomogenan membran. Kehomogenan tersebut karena pengaruh adanya gugus sulfonat sehingga struktur membran menjadi lebih rapat (9b). Penambahan
TiO2 dapat meningkatkan kehomogenan (9c) dan berfungsi sebagai pengisi.
(a) (b) (c)
Bilangan gelombang
TiO2
OH Bebas
14
(d) (e) (f)
Gambar 9 Struktur permukaan atas membran PSf (9a), sPSf (9b), dan sPSf-TiO2
5% (9c) serta penampang lintang membran PSf (9d), sPSf (9e), dan
sPSf- TiO2 5% 98f) dengan perbesaran 10000х.
Berdasarkan hasil penampang lintang menunjukkan membran PSf (9d) lebih
berongga dibanding dengan sPSf (9e) dan sPSf-TiO2 5% (9f). Hal ini berkaitan
densitas yang dihasilkan, densitas berhubungan dengan keteraturan dan kerapatan
membran. Membran sPSf-TiO2 5% memiliki densitas lebih tinggi dibanding sPSf
dan PSf. Hal ini dikarenakan penambahan TiO2 dapat meningkatkan kerapatan
rongga pada membran (Pramono et al. 2012), rongga yang semakin rapat akan
menyebabkan membran lebih rapat.
Aplikasi Sistem DMFC
Membran elektrolit yang dihasilkan diuji pada sistem DMFC, uji ini dilakukan pada sebuah bejana yang terdiri atas 2 kompartemen. Kompartemen A (anode) berisi larutan metanol yang berfungsi sebagai bahan bakar sedangkan kompartemen B (katode) berisi larutan kalium ferisianida dalam buffer fosfat (Gambar 10).
15
Gambar 10 Bejana pada sistem DMFC
Beda potensial tertinggi yang dihasilkan dalam uji aplikasi ini terdapat pada
membran sPSf-TiO2 sebesar 422 mV dengan elektrode logam. Kenaikan
konsentrasi TiO2 dapat meningkatkan nilai beda potensial, penambahan TiO2 akan
meningkatkan transfer ion atau konduktivitas membran, konduktivitas berbanding
lurus dengan beda potensial (Pramono et al. 2012). Adanya TiO2 dan gugus
sulfonat dapat mempercepat transfer proton. Peningkatan presentase konduktivitas proton dapat dilihat pada Lampiran 7.
Dalam DMFC metanol langsung diubah menjadi energi listrik melalui proses kimia dengan menggunakan membran sebagai penghalang selektif (Marita
2011). Proses oksidasi metanol menghasilkan elektron, proton, dan gas CO2. Gas
CO2 dikeluarkan dari sistem sementara proton bergerak melewati membran
menuju katode kemudian bereaksi dengan O2 dan menghasilkan air, sedangkan
tumpukan elektron di anode akan mengalir ke katode dengan menghasilkan beda
potensial (Marita 2011). Fe3+ dari larutan K3Fe(CN)6 akan tereduksi menjadi Fe2+
oleh aliran elektron dari anode tersebut dengan ditandai timbulnya warna kuning kehijauan pada larutan. Berikut reaksi yang terjadi dalam sistem.
Reaksi 1:
Anoda : CH3OH (l) + H2O (l)CO2(g)+ 6H++ 6e
-Katoda : 3/2 O2(g) + 6H++ 6e-3H2O(l)
Reaksi keseluruhan : CH3OH(l) + 3/2 O2(g) CO2(g) + 2H2O(l)
(Kundu dan Sharma 2007)
Reaksi 2:
Reduksi : Fe3+ + e- Fe2+ E° = 0.77 V
Oksidasi : Fe Fe2+ + 2e- E° = 0.44 V
Beda potensial yang dihasilkan elektorode karbon lebih rendah daripada elektrode logam (Gambar 11). Hal ini disebabkan elektrode karbon bersifat inert sehingga tidak ada reaksi baik di katode maupun anode, sedangkan elektode logam merupakan elektrode aktif yang ikut bereaksi terutama di anodenya dapat
mengalami oksidasi, sehingga Fe akan teroksidasi menjadi Fe2+. Hal ini
16
Gambar 11 Beda potensial membran aktivasi
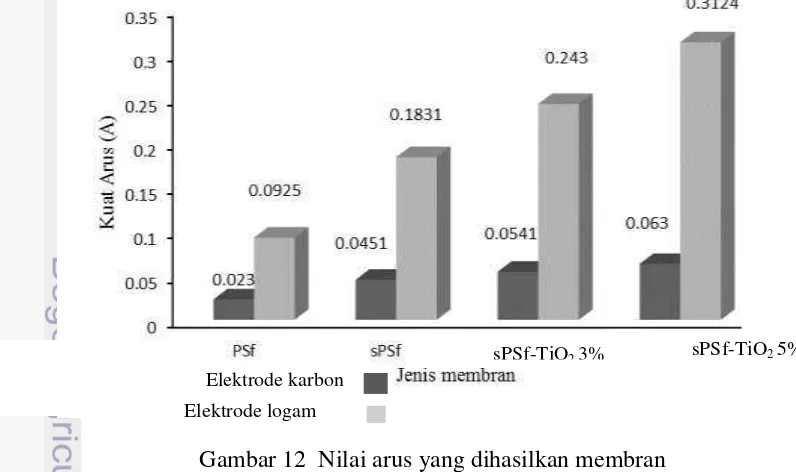
Arus yang dihasilkan dapat diperoleh dengan mengkonversi nilai beda potensialnya (Lampiran 9). Gambar 12 menunjukkan nilai arus yang dihasilkan pada sistem. Penambahan komposit dan gugus sulfonat dapat meningkatkan arus yang dihasilkan, hal ini dikarenakan arus berbanding lurus dengan beda potensial. Nilai arus yang dihasilkan menunjukkan banyaknya muatan listrik akibat pergerakan elektron pada sistem DMFC. Semakin banyak elektron yang bergerak maka nilai kuat arus yang dihasilkan akan semakin tinggi.
Gambar 12 Nilai arus yang dihasilkan membran Elektrode logam
Elektrode karbon Elektrode karbon
Elektrode logam
sPSf-TiO2 3% sPSf-TiO2 5%
17
SIMPULAN DAN SARAN
Simpulan
Pembuatan membran polisulfon tersulfonasi-TiO2 telah berhasil dilakukan
pada suhu 40 °C. Hal ini dibuktikan dengan hasil substitusi sulfonat yang masuk cincin aromatik dengan nilai derajat sulfonasi sebesar 47.52%. Selain itu dari hasil FTIR juga ditunjukkan adanya puncak gugus sulfonat 1,2,4- pada serapan 1724
cm-1. Keberadaan komposit TiO2 dengan konsentrasi 5% pada membran
meningkatkan nilai konduktivitas dan beda potensial yang dihasilkan
berturut-turut, yaitu sebesar 1.07 × 10-3 S/cm dan 422 mV dengan elektrode logam. Uji
kualitatif kemampuan menunjukkan tidak ada metanol yang terdifusi melewati membran ditandai dengan keringnya bagian sisi permukaan membran sehingga
hal ini dapat diaplikasikan pada sistem direct methanol fuel cell.
Saran
Perlu dilakukan penelitian lebih lanjut sintesis polisulfon tersulfonasi-Titanium dioksida dengan konsentrasi polisulfon yang lebih besar, penentuan
konsentrasi optimum dari TiO2 yang digunakan untuk melihat pengaruh beda
nyata dari penambahan TiO2 dan suhu sulfonasi optimum, serta uji analisis DSC
untuk mengetahui ketahanan termal dari membran, Uji XRD untuk melihat krisatalinitas membran. Serta dilakukan variasi suhu sistem DMFC untuk mengetahui sifat elektrokimia sistem sel bahan bakar terhadap pengaruh
kinetikanya. Lebih baik lagi jika dibuat membrane electrode assembly (MEA) dari
membran polisulfon tersulfonasi-TiO2 agar menghasilkan nilai konduktivitas
proton yang lebih besar.
DAFTAR PUSTAKA
Devrim Yilser, Erkan Sedar, Bac Nurcan, Eroglu Inci. 2009. Preapration and characterization of sulfonated polysulphone/titanium dioxide composite
membranes for proton exchange membrane fuel cells. J of Hydrogen
Energy. 34(2009):3467-3475.
Handayani S, Dewi EL. 2007. Pengaruh suhu operasi terhadap karakteristik
membran elektrolit polieter eter keton tersulfonasi. J Material Science. 8(2)
ISSN:1411-1098.
Handayani S. 2008. Membran elektrolit berbasis polieter-eter keton tersulfonasi
untuk direct methanol fuel cell suhu tinggi [disertasi]. Jakarta (ID):
Universitas Indonesia.
Hasan A. 2007. Aplikasi sistem fuel cell sebagai energi ramah lingkungan di
sektor transportasi dan pembangkit. J Environment Science Technology.
18
Juniarzadinata R. 2011. Kajian struktur dan uji fluks membran polisulfon dengan metode inversi fasa [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Kundu PP dan Sharma Vinay. 2007. Composites of proton- conducting polymer
electolyte membrane in direct methanol fuel cels. Critical Reviews in Solid
State and Materials Sciences. 32:51-66.
Liu L, Chakm A, & Feng X. 2004. Preparation of hollow fiber poly (ether block amide)/ polysulfone composite membrans for separation of carbon dioxide
from nitrogen. Chemical Engineering Journal. 105:43-51.
Lufrano F, Baglio V, Staiti P, Arico AS, Antonucci V. 2008. Polymer electrolytes
based on sulfonated polysulfone fordirect methanol fuel cells. J Power
Source. 179:34–41.
Luntraru VI, Vaireanu DI, Ghindeanu DL, Nechifor G. 2013. The synthesis and
characterization of a new composite material: polysulfone- Fe3O4/TiO2.
Sci.Bull. 75.
Marita IM. 2011. Pembuatan dan karakterisasi komposit membran PEEK silika/clay untuk aplikasi direct methanol fuel cell [tesis]. Semarang (ID): Universitas Diponegoro.
Martins CR, Hallwass F, Almeida YMB, Paoli MA. 2007. Solid-state 13C NMR
analysis of sulfonated polystyrene. Ann Magn Reson 6:46-55.
Mingliang Luo, Qingzhi W, Jialin Liu, Zilong JIA. 2011. Fabrication of
SPES/Nano-TiO2 composite ultrafiltration membrane and its anti-fouling
mechanism. Chinese Journal of Chemical Engineering. 19(1)45-51.
Pavia DL, Lampman GM, Kriz GS, Vyvyan JR 2009. Introduction to
Spectroscopy 4th Ed. Washington (US): Thomson Learning, Inc.
Piluharto B, Cynthia LR, Tanti H. 2012. Pengembangan membran penukar proton
berbasis polisulfon tersulfonasi untuk aplikasi direct methanol fuel cell
(DMFC) [laporan]. Jember (ID): Universitas Jember.
Pramono E, Wicaksono A, Priyadi, Wulansari J. 2012. Pengaruh derajat sulfonasi
terhadap degradasi termal polistirena tersulfonasi. J physics 2(2):157.
Pramono E, Radiman CL Loos KU. 2012.
Polysulphone/sulfonated-polysulphone/TiO2 composite membrane for fuel cell aplications. J of
Hydrogen Energy. 40(2012):45-51.
Shin JP, Chang BJ, Kim JH, Le SB, Suh DH. 2005. Sulfonated polystyrene/PTFE
composite membrane. J Membrane Science.251:247-254.
Smitha B, Anjali Devi D, Sridhar S. 2008. Proton-conducting composite
membranes of chitosan andsulfonated polysulfone for fuel cell application. J
Energy Fuel. 33:4138–4146.
Suhada H. 2001. Fuel cell sebagai penghasil energi abad 21. Jurnal Teknik Mesin.
3(2):92-100.
Suka I G, Rifan M, Pandiangan KD, Simanjuntak W, Dewi EL. 2009. Sulfonasi membran poliakrilonitril butadiena stirena (ABS) sebagai membran polimer
elektrolit direct metahnol fuel cell (DMFC). J Sains MIPA. 15(1):28-34.
19
Xing P, Gilles PR, Michael DG, Serguei DM, Keping W, Serge K. 2004. Synthesis and characterization of sulfonated poly(ether ether ketone) for
Proton Exchange Membranes. J Membrane Science. 229:95-106.
LAMPIRAN
Lampiran 1 Diagram alir penelitian
Penambahan Titanium Dioksida Penambahan oleum pada suhu
40 °C selama 60 menit.
Polisulfon (PSf)
Sintesis Polisulfon
Tersulfonasi (sPSf)
Penentuan
Derajat Sulfonasi
Membran Polisulfon Tersulfonasi-
Titanium Dioksida (sPSf-TiO2)
Pencirian Kinerja Membran Aplikasi pada
DMFC
1. FTIR
2. SEM 1. Pengukuran Bobot Jenis
2. Pengujian Water Uptake
3. Pengukuran Konduktivitas Membran
20
Lampiran 2 Penentuan derajat sulfonasi (DS)
Contoh perhitungan (ulangan 1): Diketahui:
Lampiran 3 Data penentuan water uptake
Jenis membran Ulangan Bobot membran (g) Water Uptake
Rerata
Contoh perhitungan (membran sPSf-TiO25% ulangan 1)
Water uptake (%) =
=
=5.77%
Ulangan Bobot sampel
22
Lampiran 4 Data penentuan densitas
Jenis membran Ulangan w (g) d (g/mL) d Rerata d (g/mL)
0 1 2 3 1 (g/mL)
PSf 1 20.2273 20.2314 44.4993 44.4986 0.99805 1.2033 1.2038
2 20.2273 20.2308 44.4992 44.4986 0.99805 1.2043
sPSf 1 20.2271 20.2292 44.5022 44.5018 0.99805 1.2326 1.2034
2 20.2271 20.2287 44.5021 44.5018 0.99805 1.2281
sPSf-TiO2 3% 1
20.2158 20.2194 44.4885 44.4878 0.99875 1.2395
1.2388
2 20.2158 20.222 44.489 44.4878 0.99875 1.2381
sPSf-TiO2 5%
1 20.2151 20.2196 44.4969 44.496 0.99875 1.2481
1.2444
2 20.2151 20.2192 44.4968 44.496 0.99875 1.2406
Contoh perhitungan (membran sPSf-TiO2 5% ulangan 1)
d=
=
d =1.2481 g/mL
Ket: w0,1,2,3 berturut-turut= bobot pikno kosong, bobot pikno+sampel, bobot pikno+sampe+akuades, bobot pikno+akuades
dl, da, dan d berturut-turut= densitas air, densitas udara (0.00125 g/mL), dan densitas sampel
22
Lampiran 5 Data hasil FTIR
Gugus fungsi Bilangan gelombang membran (cm
-1
)
PSf sPSf sPSf-TiO2 5%
Ikatan C=C pada cincin aromatik 1586.40-1488.71 1586.64-1488.57 1586.71-1491.96
Ikatan C-H pada cincin aromatik 3093.51-3067.57 3094.73-3067.58 3094.57-3067,61
Ikatan Hidrogen O-H - 3628.77 3653.36
Ikatan C-O pada eter 1250.01 1249.18 1252.60
Cincin aromatik tertrisubstitusi 1,2,4- - 1724.29 1725.04
Ikatan S=O asimetrik 1323.58 1323.53 1323.27
Ikatan S=O simetrik 1153.34 1151.66 1153.96
23
Lampiran 6 Data penentuan konduktivitas proton elektrode karbon
Jenis membran
Tebal Konduktans (×10-3 S) Resistansi (Ω) Konduktivitas (×10
-3
S/cm)
(cm) nonaktivasi aktivasi nonaktivasi aktivasi nonaktivasi aktivasi
PSf 0.008 155.77 176.95 6.4197 5.6513 0.2347 0.2666
Luas permukaan elektrode: 5.31 cm2
Jenis membran
Tebal (cm)
Konduktans (×10-3 S) Resistansi (Ω) Konduktivitas (×10
-3
S/cm)
nonaktivasi aktivasi nonaktivasi aktivasi nonaktivasi Aktivasi
PSf 0.008 297.73 303.25 3.3587 3.2976 0.5046 0.514
Luas permukaan elektrode: 4.72 cm2
Contoh perhitungan (membran sPSf-TiO2 3% elektrode karbon):
σ = G×
σ : konduktivitas proton (S/cm)
A : luas permukaan (cm2)
24
Lampiran 7 Data persentase peningkatan konduktivitas proton
Elektrode Jenis membran Konduktivitas (mS/cm) Peningkatan (%)
Aktivasi Nonaktivasi Aktivasi Nonaktivasi
Karbon
PSf 0.2666 0.2347 0 0
sPSf 0.3034 0.2997 13.80 27.69
sPSf-TiO2 3% 0.3999 0.3814 31.81 27.26
sPSf- TiO2 5% 0.4857 0.4819 21.46 26.35
Logam
PSf 0.5140 0.5046 0 0
sPSf 0.5791 0.5463 12.67 8.26
sPSf- TiO23% 0.7604 0.7286 31.31 33.37
sPSf- TiO25% 1.0684 0.9888 40.50 35.71
Contoh perhitungan peningkatan konduktivitas akibat penambahan gugus sulfonat
(elektrode karbon, membran aktivasi sPSf-TiO2 5%):
Peningkatan (%) =
Peningkatan (%) = = 21.46%
Lampiran 8 Beda potensial yang dihasilkan pada setiap membran
Jenis membran Beda potensial (mV)
Karbon Logam
PSf 130 305
sPSf 140 335
sPSf-TiO23% 153 410
sPSf-TiO2 5% 171 422
Lampiran 9 Nilai arus yang dihasilkan pada setiap membran
Membran G (S) V (Volt) I (Ampere)
Karbon Logam Karbon Logam Karbon Logam
PSf 0.1770 0.3033 0.130 0.305 0.0230 0.0925
sPSf 0.3222 0.5467 0.140 0.335 0.0451 0.1831
sPSf-TiO23% 0.3539 0.5928 0.153 0.410 0.0541 0.2430
sPSf- TiO25% 0.3685 0.7404 0.171 0.422 0.0630 0.3124
Contoh perhitungan (membran sPSf-TiO2 5%, elektrode karbon):
I = G × V
= 0.3685 Sх0.171
25
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta 23 Maret 1993. Penulis merupakan anak ke 8 dari pasangan H. Muhamad Hasan dan Hj. Siti Huriyah. Tahun 2010 penulis lulus dari Sekolah Menengah Atas Negeri 48 Jakarta dan melanjutkan pendidikan di Institut Pertanian Bogor dengan jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam melalui jalur undangan seleksi masuk IPB (USMI). Penulis merupakan penerima beasiswa peningkatan prestasi akademik.
Penulis aktif di kegiatan non-akademik, seperti menjadi anggota (2012) departemen Pengembangan Kimia dan Seni Ikatan Mahasiswa Kimia (Imasika) dan Wakil Ketua Umum Ikatan Mahasiswa Kimia (Imasika) (2013), (2012-2014) Anggota departemen kewirusahaan Ikatan Himpunan Mahasiswa Kimia Indonesia (Ikahimki), dan Anggota Komunitas Pecinta Alam departemen kimia IPB
(Akapela), (2012) menjadi Wakil Ketua Chemistry Challenge Pesta Sains
Nasional, dan aktif diberbagai kepanitian. Penulis juga aktif mengajar mata kuliah kimia di bimbingan belajar Primagama. Bulan Juli-Agustus 2014 penulis
melaksanakan Praktik Lapangan di Direktorat Pengolahan Resarch &
Development PT Pertamina (Persero) dengan judul laporan Kajian Kinerja
Surfaktan Alkil Poliglikosida dan Polimer Poliakrilamida untuk Enhanced Oil
Recovery.